Přehled zakončení názvů anorganických sloučenin a iontů
|
|
|
- Lukáš Konečný
- před 5 lety
- Počet zobrazení:
Transkript
1 Hodnota kladného oxidačního čísla Přehled zakončení názvů anorganických sloučenin a iontů Zakončení příd. jména binární sl. hydroxidu soli kationtu Zakončení přídavného jména kyseliny jejího aniontu Zakončení podstatného jména soli I -ný -ná -nanový -nan II -natý -natá -natanový -natan III -itý -itá -itanový -itan IV -ičitý -ičitá -ičitanový -ičitan V -ičný -ečný -ičná -ečná -ičnanový -ečnanový -ičnan -ečnan VI -ový -ová -anový -an VII -istý -istá -istanový -istan VIII -ičelý -ičelá -ičelanový -ičelan Příklad: Dusík - oxidační číslo V binární sloučenina: oxid dusičný N 2 O 5 kyselina: kyselina dusičná HNO 3 její aniont: dusičnanový aniont NO 3 sůl kyseliny: Ag - oxidační číslo I dusičnan stříbrný AgNO 3 Přehled jednoduchých číslovkových předpon 1 mono - 6 hexa - 11 undeka - 2 di - 7 hepta - 12 dodeka - 3 tri - 8 okta - : 4 tetra - 9 nona - 1/2 hemi - 5 penta - 10 deka - 3/2 seskvi - 1
2 Přehled běžných oxidačních čísel vybraných prvků ve sloučeninách Název a symbol prvku Oxid. číslo Název a symbol prvku Oxid. číslo Arsen As -3, 3, 5 Molybden Mo 4, 6 Antimon Sb 3, 5 Nikl Ni 2, 3 Baryum Ba 2 Olovo Pb 2, 4 Bor B -3, 3 Osmium Os 4, 8 Brom Br -1, 1, 5 Platina Pt 2, 4 Césium Cs 1 Rhenium Re 7 Cín Sn 2, 4 Rhodium Rh 3, 4 Draslík K 1 Rtuť Hg 1, 2 Dusík N -3, 1, 2, 3, 4, 5 Rubidium Rb 1 Fluor F -1 Ruthenium Ru 3, 4, 8 Fosfor P -3, 1, 3, 5 Síra S -2, 4, 6 Hliník Al 3 Sodík Na 1 Hořčík Mg 2 Stroncium Sr 2 Chlor Cl -1, 1, 3, 5, Stříbro Ag 1 7 Chrom Cr 2, 3, 6 Titan Ti 3, 4 Jód I -1, 1, 5, 7 Uhlík C -4, 2, 4 Kadmium Cd 2 Uran U 4, 6 Kobalt Co 2, 3 Vápník Ca 2 Křemík Si -4, 4 Vodík H -1, 1 Kyslík O -2 Zinek Zn 2 Lithium Li 1 Zirkonium Zr 4 Mangan Mn 2, 3, 4, 6, 7 Zlato Au 3 Měď Cu 1, 2 Železo Fe 2, 3 2
3 Názvosloví binárních sloučenin Sloučeniny, jejichž stavební částice (molekuly, ionty) jsou tvořeny atomy dvou různých chemických prvků. OM m Obecný vzorec: M X n OX M - prvek s kladným oxidačním číslem OM X - prvek se záporným oxidačním číslem OX m, n - indexy - přirozená čísla Musí platit: Součet oxidačních čísel všech atomů v molekule je roven nule. m.om + n. OX = 0 Pozn.1 - Indexy m, n rovné 1 se nepíší. Pozn.2 - Jsou -li oba indexy m, n dělitelné týmž číslem, indexy se vydělí. Obecný název podstatné jméno + přídavné jméno prvek se záporným oxid. číslem prvek s kladným oxid. číslem název prvku + -id název prvku + koncovka koncovka přídavného jména podle hodnoty oxid. čísla Příklady binárních sloučenin oxid X = O M m O n -II sulfid X = S M m S n -II kyanid X = CN M m CN n -I halogenidy - fluorid X = F M m F n -I - chlorid X = Cl M m Cl n -I - bromid X = Br M m Br n -I - jodid X = I M m I n -I 3
4 Názvosloví hydroxidů Vznikají reakcí zásadotvorného (hydroxidotvorného) oxidu s vodou. OM Obecný vzorec: M ( OH) I n M - zásadotvorný prvek s kladným oxid. číslem OM OH - hydroxidový aniont, oxidační číslo -I n - index - přirozené číslo - u hydroxidů n = OM ; obvykle = 1 4 Musí platit: Součet oxidačních čísel všech atomů v molekule je roven nule. Pozn.1 - Index n rovný 1 se nepíše. Obecný název hydroxid + přídavné jméno název prvku + koncovka prvek s kladným oxid. číslem koncovka přídavného jména podle hodnoty oxid. čísla Tvorba názvu, vzorce obdobně jako u binárních sloučenin. 4
5 Názvosloví bezkyslíkatých kyselin Molekuly bezkyslíkaté kyseliny obsahují vodík a neobsahují kyslík. Vznikají rozpouštěním některých plynných sloučenin vodíku ve vodě. Obecný vzorec: Vzorce bezkyslíkatých kyselin jsou totožné se vzorci původních sloučenin. Obecný název: kyselina + přídavné jméno název původní sloučeniny + - ová Příklady bezkyslíkatých kyselin sloučenina vzorec sl. kyselina vzorec kyseliny fluorovodík HF fluorovodíková HF chlorovodík HCl chlorovodíková HCl bromovodík HBr bromovodíková HBr jodovodík HI jodovodíková HI sirovodík H 2 S sirovodíková H 2 S kyanovodík HCN kyanovodíková HCN 5
6 Názvosloví kyslíkatých kyselin (oxokyselin) Molekuly obsahují vodík, kyslík, kyselinotvorný prvek (centrální atom). Vznikají reakcí kyselinotvorných oxidů s vodou. I m OX x Obecný vzorec: H X O II n H - atom vodíku, oxid. číslo I X - centrální atom ( kyselinotvorný prvek) O - atom kyslíku, oxid. číslo -II m, x, n - indexy - přirozená čísla Musí platit: Součet oxidačních čísel všech atomů v molekule je roven nule. m.i + x.ox + n.(-ii) = 0 Pozn.1 - Indexy m, x, n rovné 1 se nepíší. Pozn.2 - Jsou -li indexy m, x, n dělitelné týmž číslem, indexy se vydělí. Rozdělení oxokyselin: - jednoduché oxokyseliny - polykyseliny Jednoduché oxokyseliny Pouze jeden centrální atom X x = 1 I OX II m n Obecný vzorec: H X O 6
7 Obecný název: kyselina + přídavné jméno kyselinotvorný prvek název prvku + koncovka koncovka přídavného jména podle hodnoty oxid. čísla Počet vodíkových atomů - m - sudé oxid. číslo kyselin. prvku - 2 atomy vodíku ; m = 2 - liché oxid. číslo kyselin. prvku - 1 atom vodíku ; m = 1 Pozn. Prvek tvoří v témže oxidačním čísle více jednoduchých kyselin. - Název oxokyseliny se zpřesňuje pomocí číslovkových předpon. - Zpřesnění názvu číslovkovou předponou, které vyjádří: - počet vodíkových atomů v molekule ( - hydrogen- ). - počet kyslíkových atomů v molekule ( - oxo - ). příklad: fosfor - oxid. číslo V HPO 3 1 atom vodíku k. hydrogenfosforečná H 3 PO 4 3 atomy vodíku k. trihydrogenfosforečná nebo 3 atomy kyslíku k. trioxofosforečná nebo 4 atomy kyslíku k. tetraoxofosforečná Polykyseliny Více centrálních atomů než jeden. V názvu navíc uveden: - počet centrálních atomů. - počet vodíkových nebo kyslíkových atomů. Příklad: H 2 Cr 2 O 7 kyselinotv.prvek: Cr, oxid. číslo VI, - chromová kyselina dihydrogendichromová kyselina heptaoxodichromová 7
8 Názvosloví solí kyslíkatých kyselin (oxokyselin) Obecný vzorec: K m A n K - vzorec kationtu A - vzorec aniontu m, n - indexy - přirozená čísla Musí platit: Součet celkového náboje kationtů a celkového náboje aniontů je roven nule. Pozn.1 - Indexy m, n rovné 1 se nepíší. Pozn.2 - Jsou -li oba indexy m, n dělitelné týmž číslem, indexy se vydělí. Obecný název: podstatné jméno + přídavné jméno název aniontu + vypuštěná název kationtu koncovka - ový z názvu aniontu název prvku s klad. oxid. č. + + koncovka dle oxid. č. Soli jednoduchých kyslíkatých kyselin Příklad síran hlinitý - sůl kyseliny sírové kyselina sírová aniont síranový 2 H2SO4 (SO ) 4 hlinitý -itý ; oxid. číslo III ; vzorec kationtu Al 3+ (SO ) 2 4 zápis iontů v pořadí kationt - aniont Al 3+ vzorec Al ( SO )
9 Hydrogensoli Aniont obsahuje jeden nebo několik vodíkových atomů. Počet vodíkových atomů v aniontu se uvede v názvu aniontu číslovkovou předponou. Příklad 1 kyselina sírová H SO (SO ) 1 (HSO 4) aniont síranový aniont hydrogensíranový hydrogensíran vápenatý vápenatý -natý ; oxid. číslo II ; vzorec kationtu Ca 2+ (HSO 4) zápis iontů v pořadí kationt - aniont Ca 2+ 1 vzorec ( ) Ca HSO 4 2 Příklad 2 kyselina trihydrogenfosforečná kyselina vz. an. název aniontu název soli HPO (PO 3 4 fosforečný fosforečnan 3 4 ) 2 (HPO hydrogenfosforečný hydrogenfosforečnan 4) ( H PO 1 2 4) dihydrogenfosforečný dihydrogenfosforečnan 9
10 Soli polykyselin Obdobné zásady jako pro názvosloví solí jednoduchých oxokyselin. Číslovkovými předponami se uvede: - počet centrálních atomů, - počet kationtů, - počet atomů kyslíku v aniontu ( nepovinné ). Příklad 1 Na B O úplný název: heptaoxotetraboritan disodný zjednodušený název: tetraboritan disodný Příklad 2 KCrO úplný název: heptaoxodichroman didraselný zjednodušený název: dichroman didraselný Radek
Názvosloví kyslíkatých kyselin (oxokyselin) II n
 (oxokyselin) Molekuly obsahují vodík, kyslík, atom(y) kyselinotvorného prvku (centrální atom(y)). Vznikají reakcí kyselinotvorných oxidů s vodou. Obecný vzorec: H X O m x n H - atom vodíku, oxid. číslo
(oxokyselin) Molekuly obsahují vodík, kyslík, atom(y) kyselinotvorného prvku (centrální atom(y)). Vznikají reakcí kyselinotvorných oxidů s vodou. Obecný vzorec: H X O m x n H - atom vodíku, oxid. číslo
U Ústav procesní a zpracovatelské techniky FS ČVUT. Názvosloví solí kyslíkatých kyselin
 (oxokyselin) Obecný vzorec: K m A n K - vzorec kationtu A - vzorec aniontu m, n - indexy - počty iontů - přirozená čísla Pozn.1 - Indexy m, n rovné 1 se nepíší. Pozn.2 - Jsou -li oba indexy m, n dělitelné
(oxokyselin) Obecný vzorec: K m A n K - vzorec kationtu A - vzorec aniontu m, n - indexy - počty iontů - přirozená čísla Pozn.1 - Indexy m, n rovné 1 se nepíší. Pozn.2 - Jsou -li oba indexy m, n dělitelné
1) BEZKYSLÍKATÉ KYSELINY:
 KYSELINY Jsou to látky, které se ve vodě štěpí na kationty H + a anionty (radikály) kyseliny (např. Cl -, NO 3-, SO 4 2- ). 1) BEZKYSLÍKATÉ KYSELINY: (koncovka -vodíková) Kyselina fluorovod vodíková chlorovod
KYSELINY Jsou to látky, které se ve vodě štěpí na kationty H + a anionty (radikály) kyseliny (např. Cl -, NO 3-, SO 4 2- ). 1) BEZKYSLÍKATÉ KYSELINY: (koncovka -vodíková) Kyselina fluorovod vodíková chlorovod
Triviální Voda (H 2 O) Amoniak Soda. Systematické. Většina názvů se skládá ze 2 slov Výjimka: např. chlorovodík např. jodid draselný (KI)
 Názvosloví anorganických sloučenin České názvosloví je jednoznačné Názvosloví anorganických sloučenin Triviální Voda (H 2 O) Amoniak Soda Systematické Většina názvů se skládá ze 2 slov Výjimka: např. chlorovodík
Názvosloví anorganických sloučenin České názvosloví je jednoznačné Názvosloví anorganických sloučenin Triviální Voda (H 2 O) Amoniak Soda Systematické Většina názvů se skládá ze 2 slov Výjimka: např. chlorovodík
Seminář z chemie. RNDr. Jana Fauknerová Matějčková místnost: 617,
 Seminář z chemie RNDr. Jana Fauknerová Matějčková místnost: 617, 615 email: Jana.Matejckova@lf3.cuni.cz Semináře týden datum název semináře či praktika 1. 30.9. Názvosloví v anorganické chemii 2. 11.10.
Seminář z chemie RNDr. Jana Fauknerová Matějčková místnost: 617, 615 email: Jana.Matejckova@lf3.cuni.cz Semináře týden datum název semináře či praktika 1. 30.9. Názvosloví v anorganické chemii 2. 11.10.
Základy chemického názvosloví
 Základy chemického názvosloví Oxidační číslo O. č. je počet elementárních nábojů částice Elementární náboj je nejmenší možný Hodnota 1,602. 10-19 C e - má jeden záporný elementární náboj P + má jeden kladný
Základy chemického názvosloví Oxidační číslo O. č. je počet elementárních nábojů částice Elementární náboj je nejmenší možný Hodnota 1,602. 10-19 C e - má jeden záporný elementární náboj P + má jeden kladný
NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN
 NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN univerzální jazyk chemiků ( abeceda; chem. vzorce ; chem. rovnice ) české názvosloví je jedno z nejdokonalejších na světě (prof. Emil Votoček) OXIDAČNÍ ČÍSLO = náboj,
NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN univerzální jazyk chemiků ( abeceda; chem. vzorce ; chem. rovnice ) české názvosloví je jedno z nejdokonalejších na světě (prof. Emil Votoček) OXIDAČNÍ ČÍSLO = náboj,
Kuchyňská sůl = chlorid sodný. Modrá skalice = síran měďnatý SO 4. Potaš = uhličitan draselný K 2 CO 3
 SOLI Kuchyňská sůl Modrá skalice Potaš Kuchyňská sůl = chlorid sodný Na Cl Modrá skalice = síran měďnatý Cu SO 4 Potaš = uhličitan draselný K 2 CO 3 Chemické názvosloví solí Soli = sloučeniny odvozené
SOLI Kuchyňská sůl Modrá skalice Potaš Kuchyňská sůl = chlorid sodný Na Cl Modrá skalice = síran měďnatý Cu SO 4 Potaš = uhličitan draselný K 2 CO 3 Chemické názvosloví solí Soli = sloučeniny odvozené
U 218 - Ústav procesní a zpracovatelské techniky FS ČVUT
 Sloučeniny, jejichž stavební částice (molekuly, ionty) jsou tvořeny atomy dvou různých chemických prvků. Obecný vzorec: M m X n M - prvek s kladným oxidačním číslem OM X - prvek se záporným oxidačním číslem
Sloučeniny, jejichž stavební částice (molekuly, ionty) jsou tvořeny atomy dvou různých chemických prvků. Obecný vzorec: M m X n M - prvek s kladným oxidačním číslem OM X - prvek se záporným oxidačním číslem
II. Chemické názvosloví
 II. Chemické názvosloví 1. Oxidy jsou dvouprvkové sloučeniny kyslíku a jiného prvku. Názvy oxidů jsou dvouslovné. Tvoří je podstatné jméno oxid (postaru kysličník) a přídavné jméno utvořené od názvu prvku
II. Chemické názvosloví 1. Oxidy jsou dvouprvkové sloučeniny kyslíku a jiného prvku. Názvy oxidů jsou dvouslovné. Tvoří je podstatné jméno oxid (postaru kysličník) a přídavné jméno utvořené od názvu prvku
Anorganické názvosloví
 Anorganické názvosloví Obr. č. 1: Emil Votoček Chemické názvosloví je univerzálním "jazykem chemiků", umělý jazyk s cílem vytvořit každé sloučeniny pokud možný jednoduchý a jednoznačný název. Chemické
Anorganické názvosloví Obr. č. 1: Emil Votoček Chemické názvosloví je univerzálním "jazykem chemiků", umělý jazyk s cílem vytvořit každé sloučeniny pokud možný jednoduchý a jednoznačný název. Chemické
1H 1s. 8O 1s 2s 2p - - - - - - H O H
 OXIDAČNÍ ČÍSLO 1H 1s 8O 1s 2s 2p 1H 1s - - - - + - - + - - + - - H O H +I -II +I H O H - - - - Elektronegativita: Oxidační číslo vodíku: H +I Oxidační číslo kyslíku: O -II Platí téměř ve všech sloučeninách.
OXIDAČNÍ ČÍSLO 1H 1s 8O 1s 2s 2p 1H 1s - - - - + - - + - - + - - H O H +I -II +I H O H - - - - Elektronegativita: Oxidační číslo vodíku: H +I Oxidační číslo kyslíku: O -II Platí téměř ve všech sloučeninách.
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T3-11 Téma: Soli Střední škola ok: 2012 2013 Varianta: A Soli Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník SOLI sůl je sloučenina, která se skládá z iontu kovu a
DUM Základy přírodních věd DUM III/2-T3-11 Téma: Soli Střední škola ok: 2012 2013 Varianta: A Soli Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník SOLI sůl je sloučenina, která se skládá z iontu kovu a
Názvosloví anorganických sloučenin
 Názvosloví anorganických sloučenin Oxidační číslo udává náboj, kterým by byl atom prvku nabit, kdyby všechny elektrony vazeb v molekule patřily elektronegativnějším vazebným partnerům (atomům) udává náboj,
Názvosloví anorganických sloučenin Oxidační číslo udává náboj, kterým by byl atom prvku nabit, kdyby všechny elektrony vazeb v molekule patřily elektronegativnějším vazebným partnerům (atomům) udává náboj,
Oxidační číslo je rovno náboji, který by atom získal po p idělení všech vazebných elektronových párů atomům s větší elektronegativitou.
 NÁZVOSLOVÍ Oxidační číslo je rovno náboji, který by atom získal po p idělení všech vazebných elektronových párů atomům s větší elektronegativitou. -II +III -II +I O N O H Oxidační čísla se značí ímskými
NÁZVOSLOVÍ Oxidační číslo je rovno náboji, který by atom získal po p idělení všech vazebných elektronových párů atomům s větší elektronegativitou. -II +III -II +I O N O H Oxidační čísla se značí ímskými
Názvosloví. Názvosloví binárních sloučenin. Struktura prezentace: DOPORUČENÍ OXIDAČNÍ ČÍSLA. Při cvičení se vzorci a názvy si vždy pište
 Názvosloví Struktura prezentace: I. Názvosloví binárních sloučenin 4 Název sloučeniny 6 Vzorec 7 Názvy kationtů 9 Názvy aniontů 13 Vzorec z názvu 15 Název ze vzorce 18 II. Názvosloví hydroxidů, kyanidů
Názvosloví Struktura prezentace: I. Názvosloví binárních sloučenin 4 Název sloučeniny 6 Vzorec 7 Názvy kationtů 9 Názvy aniontů 13 Vzorec z názvu 15 Název ze vzorce 18 II. Názvosloví hydroxidů, kyanidů
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T30 Téma: Kyseliny Střední škola Rok: 2012 2013 Varianta: A Kyseliny Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník VÝKLAD jsou to sloučeniny KYSELINY ve vodných roztocích
DUM Základy přírodních věd DUM III/2-T30 Téma: Kyseliny Střední škola Rok: 2012 2013 Varianta: A Kyseliny Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník VÝKLAD jsou to sloučeniny KYSELINY ve vodných roztocích
Chemická nomenklatura
 Chemická nomenklatura racionální chemické názvy anorganických sloučenin jsou většinou dvouslovné, skládající se ze substantiva a adjektiva elektronegativní části (aniontu) se uvádí v názvu jako první ve
Chemická nomenklatura racionální chemické názvy anorganických sloučenin jsou většinou dvouslovné, skládající se ze substantiva a adjektiva elektronegativní části (aniontu) se uvádí v názvu jako první ve
Střední průmyslová škola strojnická Vsetín Číslo projektu. Druh učebního materiálu prezentace Pravidla pro tvorbu vzorců a názvů kyselin a solí
 Název školy Střední průmyslová škola strojnická Vsetín Číslo projektu CZ.1.07/1.5.00/34.0483 Autor RNDr. Miroslava Pospíšilíková Název šablony III/2 Název DUMu 10.3 Názvosloví kyselin a solí Tematická
Název školy Střední průmyslová škola strojnická Vsetín Číslo projektu CZ.1.07/1.5.00/34.0483 Autor RNDr. Miroslava Pospíšilíková Název šablony III/2 Název DUMu 10.3 Názvosloví kyselin a solí Tematická
název soli tvoří podstatné a přídavné jméno
 OPAKOVÁNÍ název soli tvoří podstatné a přídavné jméno podstatné jméno charakterizuje anion soli a jeho náboj: chlorid Cl - přídavné jméno charakterizuje kation soli a jeho oxidační číslo: sodný Na + podstatné
OPAKOVÁNÍ název soli tvoří podstatné a přídavné jméno podstatné jméno charakterizuje anion soli a jeho náboj: chlorid Cl - přídavné jméno charakterizuje kation soli a jeho oxidační číslo: sodný Na + podstatné
11. Anorganicke na zvoslovı
 11. Anorganicke na zvoslovı Základní veličinou, na níž je názvosloví anorganické chemie vybudováno, je oxidační číslo prvků. Jde o pojem formální a oxidační číslo velmi často neodpovídá skutečné elektronové
11. Anorganicke na zvoslovı Základní veličinou, na níž je názvosloví anorganické chemie vybudováno, je oxidační číslo prvků. Jde o pojem formální a oxidační číslo velmi často neodpovídá skutečné elektronové
Přílohy. Příloha 1. Mapa s výskytem dolů a pramenů s hladinami vod po r (Čadek et al. 1968) [Zadejte text.]
![Přílohy. Příloha 1. Mapa s výskytem dolů a pramenů s hladinami vod po r (Čadek et al. 1968) [Zadejte text.] Přílohy. Příloha 1. Mapa s výskytem dolů a pramenů s hladinami vod po r (Čadek et al. 1968) [Zadejte text.]](/thumbs/81/83251433.jpg) Přílohy Příloha 1 Mapa s výskytem dolů a pramenů s hladinami vod po r. 1895 (Čadek et al. 1968) Příloha 2 Komplexní rozbor vody z pramene Pravřídlo 2002 (Lázně Teplice) Chemické složení Kationty mg/l mmol/l
Přílohy Příloha 1 Mapa s výskytem dolů a pramenů s hladinami vod po r. 1895 (Čadek et al. 1968) Příloha 2 Komplexní rozbor vody z pramene Pravřídlo 2002 (Lázně Teplice) Chemické složení Kationty mg/l mmol/l
VY_52_INOVACE_08_II.1.7_SOLI SOLI. PROCVIČOVÁNÍ a) PRACOVNÍ LIST
 VY_52_INOVACE_08_II.1.7_SOLI SOLI PROCVIČOVÁNÍ a) PRACOVNÍ LIST PRACOVNÍ LIST 1. Pojmenuj kyselinu a odděl aniontovou skupinu. H 2 SO 4 HClO 3 H 2 SO 3 H 2 CO 3 H 2 SiO 4 HCl HNO 3 H 2 Se HClO H 2 WO 4
VY_52_INOVACE_08_II.1.7_SOLI SOLI PROCVIČOVÁNÍ a) PRACOVNÍ LIST PRACOVNÍ LIST 1. Pojmenuj kyselinu a odděl aniontovou skupinu. H 2 SO 4 HClO 3 H 2 SO 3 H 2 CO 3 H 2 SiO 4 HCl HNO 3 H 2 Se HClO H 2 WO 4
POKYNY TEORETICKÁ ČÁST
 POKYNY nejprve si prostuduj teoretickou část s uvedenými typovým příklady jakmile si budeš jist, že teoretickou část zvládáš, procvič si své dovednosti na příkladech k procvičování jako doplňující úlohu
POKYNY nejprve si prostuduj teoretickou část s uvedenými typovým příklady jakmile si budeš jist, že teoretickou část zvládáš, procvič si své dovednosti na příkladech k procvičování jako doplňující úlohu
Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 1 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 1 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Chemické názvosloví anorganických sloučenin 2
 Chemické názvosloví anorganických sloučenin 2 Tříprvkové sloučeniny Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je. Mgr. Vlastimil Vaněk. Dostupné z Metodického portálu www.rvp.cz, ISSN:
Chemické názvosloví anorganických sloučenin 2 Tříprvkové sloučeniny Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je. Mgr. Vlastimil Vaněk. Dostupné z Metodického portálu www.rvp.cz, ISSN:
MENDELU PŘÍPRAVNÝ KURZ. Chemie anorganická a analytická. Mgr. Jiří Vlček, Ph.D.
 MENDELU PŘÍPRAVNÝ KURZ Chemie anorganická a analytická Mgr. Jiří Vlček, Ph.D. Inovace předmětu probíhá v rámci projektu CZ.1.07/2.2.00/28.0302 Inovace studijních programů AF a ZF MENDELU směřující k vytvoření
MENDELU PŘÍPRAVNÝ KURZ Chemie anorganická a analytická Mgr. Jiří Vlček, Ph.D. Inovace předmětu probíhá v rámci projektu CZ.1.07/2.2.00/28.0302 Inovace studijních programů AF a ZF MENDELU směřující k vytvoření
TEORETICKÁ ČÁST (OH) +II
 POKYNY nejprve si prostuduj teoretickou část s uvedenými typovým příklady jakmile si budeš jist, že teoretickou část zvládáš, procvič si své dovednosti na příkladech k procvičování jako doplňující úlohu
POKYNY nejprve si prostuduj teoretickou část s uvedenými typovým příklady jakmile si budeš jist, že teoretickou část zvládáš, procvič si své dovednosti na příkladech k procvičování jako doplňující úlohu
Názvosloví anorganických sloučenin
 Chemické názvosloví Chemické prvky jsou látky složené z atomů o stejném protonovém čísle (počet protonů v jádře atomu. Každému prvku přísluší určitý mezinárodní název a od něho odvozený symbol (značka).
Chemické názvosloví Chemické prvky jsou látky složené z atomů o stejném protonovém čísle (počet protonů v jádře atomu. Každému prvku přísluší určitý mezinárodní název a od něho odvozený symbol (značka).
Didaktika chemického anorg. názvosloví
 Didaktika chemického anorg. názvosloví RNDr. Milan Šmídl, Ph.D. 1 Didaktické zpracování zopakovat základní pojmy týkající se tvorby a čtení chemického názvosloví a správných českých a latinských názvů
Didaktika chemického anorg. názvosloví RNDr. Milan Šmídl, Ph.D. 1 Didaktické zpracování zopakovat základní pojmy týkající se tvorby a čtení chemického názvosloví a správných českých a latinských názvů
Gymnázium, Brno, Elgartova 3
 Gymnázium, Brno, Elgartova 3 Šablona: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Název projektu: GE Vyšší kvalita výuky Číslo projektu: CZ.1.07/1.5.00/34.0925 Autor: Mgr. Petra Holzbecherová
Gymnázium, Brno, Elgartova 3 Šablona: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Název projektu: GE Vyšší kvalita výuky Číslo projektu: CZ.1.07/1.5.00/34.0925 Autor: Mgr. Petra Holzbecherová
Složení látek a chemická vazba Číslo variace: 1
 Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/
 Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT- PZC 2/9 Procvičování názvosloví v
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT- PZC 2/9 Procvičování názvosloví v
NÁZVOSLOVÍ SOLÍ. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 14. 5. 2013. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková NÁZVOSLOVÍ SOLÍ Datum (období) tvorby: 14. 5. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s názvoslovím
Autor: Mgr. Stanislava Bubíková NÁZVOSLOVÍ SOLÍ Datum (období) tvorby: 14. 5. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s názvoslovím
DUM VY_52_INOVACE_12CH01
 Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH01 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH01 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
1) Stechiometrický vzorec vyjadřuje stechiometrické složení látky (poměr atomů)
 Chemické vzorce Chemické vzorce 1) Stechiometrický vzorec vyjadřuje stechiometrické složení látky (poměr atomů) např. oxid fosforečný {P 2 O 5 }, oxid křemičitý {SiO 2 } 2) Molekulový vzorec vyjadřuje
Chemické vzorce Chemické vzorce 1) Stechiometrický vzorec vyjadřuje stechiometrické složení látky (poměr atomů) např. oxid fosforečný {P 2 O 5 }, oxid křemičitý {SiO 2 } 2) Molekulový vzorec vyjadřuje
Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 2 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 2 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
I. NÁZVOSLOVN ZVOSLOVÍ
 I. NÁZVOSLOVN ZVOSLOVÍ PRVKY: Název prvku tvoří 1 aža 2 písmenovp smenová zkratka, 2. písmeno p je malé. Názvy jsou v PSP (periodické soustavě prvků). Př.: kobalt je Co, ne CO Pozn.: PSP je nejdůle ležitější
I. NÁZVOSLOVN ZVOSLOVÍ PRVKY: Název prvku tvoří 1 aža 2 písmenovp smenová zkratka, 2. písmeno p je malé. Názvy jsou v PSP (periodické soustavě prvků). Př.: kobalt je Co, ne CO Pozn.: PSP je nejdůle ležitější
Autor: Rajsik www.nasprtej.cz Téma: Názvosloví anorganických sloučenin Ročník: 1. NÁZVOSLOVÍ Anorganických sloučenin
 n - založena na oxidačních číslech Oxidační číslo NÁZVOSLOVÍ Anorganických sloučenin - římskými číslicemi, pravý horní index - nesloučené prvky a molekuly jednoho prvku mají oxidační číslo 0 (např. O 3,S
n - založena na oxidačních číslech Oxidační číslo NÁZVOSLOVÍ Anorganických sloučenin - římskými číslicemi, pravý horní index - nesloučené prvky a molekuly jednoho prvku mají oxidační číslo 0 (např. O 3,S
Výukový materiál zpracován v rámci operačního projektu. EU peníze školám. Registrační číslo projektu: CZ.1.07/1.5.00/34.0512
 Výukový materiál zpracován v rámci operačního projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0512 Střední škola ekonomiky, obchodu a služeb SČMSD Benešov, s.r.o. CHEMIE Anorganická
Výukový materiál zpracován v rámci operačního projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0512 Střední škola ekonomiky, obchodu a služeb SČMSD Benešov, s.r.o. CHEMIE Anorganická
Periodická tabulka řádek = perioda sloupec = skupina
 Periodická tabulka řádek = perioda = počet vrstev v elektronovém obalu sloupec = skupina (nadepsáno nahoře) = počet valenčních elektronů Valenční elektrony jsou ty, které se podílejí na vzniku chemických
Periodická tabulka řádek = perioda = počet vrstev v elektronovém obalu sloupec = skupina (nadepsáno nahoře) = počet valenčních elektronů Valenční elektrony jsou ty, které se podílejí na vzniku chemických
Seminář z anorganické chemie
 Univerzita Jana Evangelisty Purkyně v Ústí nad Labem Přírodovědecká fakulta Studijní opora pro dvouoborové kombinované bakalářské studium Seminář z anorganické chemie Ing.Fišerová Cílem kurzu je seznámit
Univerzita Jana Evangelisty Purkyně v Ústí nad Labem Přírodovědecká fakulta Studijní opora pro dvouoborové kombinované bakalářské studium Seminář z anorganické chemie Ing.Fišerová Cílem kurzu je seznámit
OBSAH. 1) Směsi. 2) Voda, vzduch. 3) Chemické prvky (názvy, značky) atomy prvků, molekuly. 4) Chemické prvky (vlastnosti, použití)
 OBSAH 1) Směsi 2) Voda, vzduch 3) Chemické prvky (názvy, značky) atomy prvků, molekuly 4) Chemické prvky (vlastnosti, použití) 5) Názvosloví halogenidy 6) Názvosloví oxidy, sulfidy 7) Názvosloví kyseliny,
OBSAH 1) Směsi 2) Voda, vzduch 3) Chemické prvky (názvy, značky) atomy prvků, molekuly 4) Chemické prvky (vlastnosti, použití) 5) Názvosloví halogenidy 6) Názvosloví oxidy, sulfidy 7) Názvosloví kyseliny,
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T3-2-09 Téma: Oxidy Střední škola Rok: 2012 2013 Varianta: A Oxidy Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník VÝKLAD OXIDY zásadotvorné oxidy můžeme rozdělit například
DUM Základy přírodních věd DUM III/2-T3-2-09 Téma: Oxidy Střední škola Rok: 2012 2013 Varianta: A Oxidy Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník VÝKLAD OXIDY zásadotvorné oxidy můžeme rozdělit například
Základní stavební částice
 Základní stavební částice ATOMY Au O H Elektroneutrální 2 H 2 atomy vodíku 8 Fe Ř atom železa IONTY Na + Cl - H 3 O + P idávat nebo odebírat se mohou jenom elektrony Kationty Kladn nabité Odevzdání elektron
Základní stavební částice ATOMY Au O H Elektroneutrální 2 H 2 atomy vodíku 8 Fe Ř atom železa IONTY Na + Cl - H 3 O + P idávat nebo odebírat se mohou jenom elektrony Kationty Kladn nabité Odevzdání elektron
Sklářské a bižuterní materiály 2005/06, Cvičení 1
 Cvičení 1 1. Seznámení s podmínkami zápočtu 100% účast na cvičení případně omluva, úspěšné zvládnutí testu, aktivní účast na cvičení Podklady na stránce: www.ksr.tul.cz/studium-podklady.htm 2. Obecné vysvětlení
Cvičení 1 1. Seznámení s podmínkami zápočtu 100% účast na cvičení případně omluva, úspěšné zvládnutí testu, aktivní účast na cvičení Podklady na stránce: www.ksr.tul.cz/studium-podklady.htm 2. Obecné vysvětlení
DUM VY_52_INOVACE_12CH19
 Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH19 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH19 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Chemický seminář Periodická tabulka prvků Základní chemické pojmy Úvod do anorganického názvosloví
 Chemický seminář 26.9.2013 Periodická tabulka prvků Základní chemické pojmy Úvod do anorganického názvosloví Periodicka tabulka prvku Názvy skupin Alkalické kovy: Li, Na, K, Rb, Cs, Fr Kovy alkalických
Chemický seminář 26.9.2013 Periodická tabulka prvků Základní chemické pojmy Úvod do anorganického názvosloví Periodicka tabulka prvku Názvy skupin Alkalické kovy: Li, Na, K, Rb, Cs, Fr Kovy alkalických
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T3-2-20 Téma: Test obecná chemie Střední škola Rok: 2012 2013 Varianta: A Test obecná chemie Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Otázka 1 OsO 4 je
DUM Základy přírodních věd DUM III/2-T3-2-20 Téma: Test obecná chemie Střední škola Rok: 2012 2013 Varianta: A Test obecná chemie Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Otázka 1 OsO 4 je
Názvosloví kyselin a hydroxidů
 Názvosloví kyselin a hydroxidů Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. Kyseliny Kyseliny
Názvosloví kyselin a hydroxidů Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. Kyseliny Kyseliny
Obecná a anorganická chemie. Kyslíkaté kyseliny
 Šablona č. I, sada č. 2 Vzdělávací oblast Vzdělávací obor Tematický okruh Téma Člověk a příroda Chemie Obecná a anorganická chemie Kyslíkaté kyseliny Ročník 9. Anotace Aktivita slouží k upevnění učiva
Šablona č. I, sada č. 2 Vzdělávací oblast Vzdělávací obor Tematický okruh Téma Člověk a příroda Chemie Obecná a anorganická chemie Kyslíkaté kyseliny Ročník 9. Anotace Aktivita slouží k upevnění učiva
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_17_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_17_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_17_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
DUM VY_52_INOVACE_12CH04
 Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH04 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH04 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Příklady oxidy, soli, kyseliny
 DUM Základy přírodních věd DUM III/2-T3-2-13 Téma: Příklady oxidy, soli, kyseliny Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník Příklady oxidy, soli, kyseliny
DUM Základy přírodních věd DUM III/2-T3-2-13 Téma: Příklady oxidy, soli, kyseliny Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník Příklady oxidy, soli, kyseliny
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 03.04.2013 Číslo DUMu: VY_32_INOVACE_14_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 03.04.2013 Číslo DUMu: VY_32_INOVACE_14_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 03.04.2013 Číslo DUMu: VY_32_INOVACE_14_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Anorganické názvosloví
 Anorganické názvosloví BINÁRNÍ SLOUČENINY: OXIDY PEROXIDY BEZKYSLÍKATÉ KYSELINY A JEJICH SOLI HYDRIDY KYSLÍKATÉ KYSELINY A JEJICH SOLI (HYDROGEN SOLI, HYDRÁTY SOLÍ) THIOKYSELINY A JEJICH SOLI IZOPOLYKYSELINY
Anorganické názvosloví BINÁRNÍ SLOUČENINY: OXIDY PEROXIDY BEZKYSLÍKATÉ KYSELINY A JEJICH SOLI HYDRIDY KYSLÍKATÉ KYSELINY A JEJICH SOLI (HYDROGEN SOLI, HYDRÁTY SOLÍ) THIOKYSELINY A JEJICH SOLI IZOPOLYKYSELINY
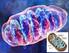
Zemská kůra. kyslík křemík hliník hořčík vápník sodík železo ostaní prvky
 Cvičení 1 1. Seznámení s podmínkami zápočtu 100% účast na laboratořích, odevzdání protokolů z laboratorních prací, odevzdání semestrální práce. Podklady na stránce: www.ksk.vslib.cz/studium-podklady.htm
Cvičení 1 1. Seznámení s podmínkami zápočtu 100% účast na laboratořích, odevzdání protokolů z laboratorních prací, odevzdání semestrální práce. Podklady na stránce: www.ksk.vslib.cz/studium-podklady.htm
DUM VY_52_INOVACE_12CH05
 Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH05 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH05 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.04.2013 Číslo DUMu: VY_32_INOVACE_16_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.04.2013 Číslo DUMu: VY_32_INOVACE_16_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.04.2013 Číslo DUMu: VY_32_INOVACE_16_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_15_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_15_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_15_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
-ičelý -natý -ičitý - ečný (-ičný) -istý -ný -itý -ový
 1 Halogenidy dvouprvkové sloučeniny halogenů s jinými prvky atomy halogenů mají v halogenidech oxidační číslo -I 1) Halogenidy - názvosloví Podstatné jméno názvu je zakončeno koncovkou.. Zakončení přídavného
1 Halogenidy dvouprvkové sloučeniny halogenů s jinými prvky atomy halogenů mají v halogenidech oxidační číslo -I 1) Halogenidy - názvosloví Podstatné jméno názvu je zakončeno koncovkou.. Zakončení přídavného
KYSELINY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 27. 3. 2013. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková KYSELINY Datum (období) tvorby: 27. 3. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základními anorganickými
Autor: Mgr. Stanislava Bubíková KYSELINY Datum (období) tvorby: 27. 3. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základními anorganickými
VY_32_INOVACE_148. Základní škola Luhačovice, příspěvková organizace. Mgr. Milena Švagerová. Člověk a příroda. Chemie. Opakování učiva chemie
 VY_32_INOVACE_148 Škola Základní škola Luhačovice, příspěvková organizace Jméno autora Mgr. Milena Švagerová Datum: 1.9.2012 Ročník: 9. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Tematický
VY_32_INOVACE_148 Škola Základní škola Luhačovice, příspěvková organizace Jméno autora Mgr. Milena Švagerová Datum: 1.9.2012 Ročník: 9. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Tematický
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost.
 Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Názvy slou enin. íslovkové p edpony
 Názvy slou enin Název slou eniny se skládá z podstatného a p ídavného jména. Podstatné jméno udává druh chemické slou eniny. Název je bu obecný (kyselina, hydroxid,...), nebo je odvozen od elektronegativní
Názvy slou enin Název slou eniny se skládá z podstatného a p ídavného jména. Podstatné jméno udává druh chemické slou eniny. Název je bu obecný (kyselina, hydroxid,...), nebo je odvozen od elektronegativní
Agrochemie - cvičení 01+02
 Agrochemie - cvičení 01+02 Za kým jít? Pavel Švehla KAVR, č. dv. 359 tel.: 224 38 27 31 e-mail: svehla@af af.czu.cz Za kým jít? Marek Neuberg Suterén 014B E-mail: euronymos666@seznam.cz Věskeré materiály
Agrochemie - cvičení 01+02 Za kým jít? Pavel Švehla KAVR, č. dv. 359 tel.: 224 38 27 31 e-mail: svehla@af af.czu.cz Za kým jít? Marek Neuberg Suterén 014B E-mail: euronymos666@seznam.cz Věskeré materiály
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 27.03.2013 Číslo DUMu: VY_32_INOVACE_18_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 27.03.2013 Číslo DUMu: VY_32_INOVACE_18_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 27.03.2013 Číslo DUMu: VY_32_INOVACE_18_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Prvky, kyseliny, soli, komplexní sloučeniny. 1 / 14
 Názvosloví Prvky, kyseliny, soli, komplexní sloučeniny http://z-moravec.net/ 25. října 2017 1 / 14 Prvky 2 / 14 Prvky Bohrium Bh Curium Cm Darmstadtium Ds Einsteinium Es Flerovium Fl Hassium Hs Kalifornium
Názvosloví Prvky, kyseliny, soli, komplexní sloučeniny http://z-moravec.net/ 25. října 2017 1 / 14 Prvky 2 / 14 Prvky Bohrium Bh Curium Cm Darmstadtium Ds Einsteinium Es Flerovium Fl Hassium Hs Kalifornium
NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV:VY_32_INOVACE_102_Soli AUTOR: Igor Dubovan ROČNÍK, DATUM: 9., 15. 9.
 NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV:VY_32_INOVACE_102_Soli AUTOR: Igor Dubovan ROČNÍK, DATUM: 9., 15. 9. 2011 VZDĚL. OBOR, TÉMA: Chemie, Soli ČÍSLO PROJEKTU: OPVK
NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV:VY_32_INOVACE_102_Soli AUTOR: Igor Dubovan ROČNÍK, DATUM: 9., 15. 9. 2011 VZDĚL. OBOR, TÉMA: Chemie, Soli ČÍSLO PROJEKTU: OPVK
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Mezipředmětové vazby matematika chemie. Aplikace matematiky v učivu chemie na základní škole.
 MASARYKOVA UNIVERZITA BRNO Pedagogická fakulta Katedra chemie Mezipředmětové vazby matematika chemie. Aplikace matematiky v učivu chemie na základní škole. Diplomová práce Brno 2008 Vedoucí: Mgr. Irena
MASARYKOVA UNIVERZITA BRNO Pedagogická fakulta Katedra chemie Mezipředmětové vazby matematika chemie. Aplikace matematiky v učivu chemie na základní škole. Diplomová práce Brno 2008 Vedoucí: Mgr. Irena
1 mol (ideálního) plynu, zaujímá za normálních podmínek objem 22,4 litru. , Cl 2 , O 2
 10.výpočty z rovnic praktické provádění výpočtů z rovnic K výpočtu chemických rovnic je důležité si shrnout tyto poznatky: Potřebujem znát vyjadřování koncentrací, objemový zlomek, molární zlomek, molární
10.výpočty z rovnic praktické provádění výpočtů z rovnic K výpočtu chemických rovnic je důležité si shrnout tyto poznatky: Potřebujem znát vyjadřování koncentrací, objemový zlomek, molární zlomek, molární
DUM VY_52_INOVACE_12CH06
 Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH06 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH06 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost.
 Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost.
 Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
SULFIDY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 14. 3. 2013. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková SULFIDY Datum (období) tvorby: 14. 3. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s dvouprvkovými
Autor: Mgr. Stanislava Bubíková SULFIDY Datum (období) tvorby: 14. 3. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s dvouprvkovými
Základy analýzy potravin Přednáška 1
 ANALÝZA POTRAVIN Význam a využití kontrola jakosti surovin, výrobků jakost výživová jakost technologická jakost hygienická autenticita, identita potravinářských materiálů hodnocení stravy (diety) Analytické
ANALÝZA POTRAVIN Význam a využití kontrola jakosti surovin, výrobků jakost výživová jakost technologická jakost hygienická autenticita, identita potravinářských materiálů hodnocení stravy (diety) Analytické
Názvosloví anorganických sloučenin
 Názvosloví anorganických sloučenin Názvy jsou tvořeny z podstatného a přídavného jména. Podstatné jméno určuje typ sloučeniny, například: oxid, kyselina, hydroxid apod. Přídavné jméno udává, od kterého
Názvosloví anorganických sloučenin Názvy jsou tvořeny z podstatného a přídavného jména. Podstatné jméno určuje typ sloučeniny, například: oxid, kyselina, hydroxid apod. Přídavné jméno udává, od kterého
Počet protonů a elektronů v atomu odpovídá jeho protonovému číslu (pořadovému číslu prvku v periodické tabulce).
 1. Atom Atom je chemicky nedělitelná částice s neutrálním elektrickým nábojem, která se skládá z jádra a obalu. V jádře (na obrázku označeno růžově) se nachází kladně nabité protony (značíme je "p", v
1. Atom Atom je chemicky nedělitelná částice s neutrálním elektrickým nábojem, která se skládá z jádra a obalu. V jádře (na obrázku označeno růžově) se nachází kladně nabité protony (značíme je "p", v
Soli. Názvosloví, vznik a použití solí, hydrogensoli a hydráty solí, hnojiva, použití solí ve stavebnictví
 Soli Názvosloví, vznik a použití solí, hydrogensoli a hydráty solí, hnojiva, použití solí ve stavebnictví Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu
Soli Názvosloví, vznik a použití solí, hydrogensoli a hydráty solí, hnojiva, použití solí ve stavebnictví Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu
Gymnázium, Brno, Elgartova 3
 Gymnázium, Brno, Elgartova 3 Šablona: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Název projektu: GE Vyšší kvalita výuky Číslo projektu: CZ.1.07/1.5.00/34.0925 Autor: Mgr. Petra Holzbecherová
Gymnázium, Brno, Elgartova 3 Šablona: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Název projektu: GE Vyšší kvalita výuky Číslo projektu: CZ.1.07/1.5.00/34.0925 Autor: Mgr. Petra Holzbecherová
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939. Název projektu: Investice do vzdělání - příslib do budoucnosti
 Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
- litina (radiátory, kotle) a ocel ( dráty, plechy, mosty,
 Rozdělení prvků podle skupenstvní a) plynné (označujeme g = gaseus) vodík, dusík, kyslík, fluor, chlor, helium, neon, argon, krypton, xenon, radon b) kapalné (l = liquidus) rtuť, brom c) pevné (s solidus)
Rozdělení prvků podle skupenstvní a) plynné (označujeme g = gaseus) vodík, dusík, kyslík, fluor, chlor, helium, neon, argon, krypton, xenon, radon b) kapalné (l = liquidus) rtuť, brom c) pevné (s solidus)
Obecná a anorganická chemie
 Šablona č. I, sada č. 2 Vzdělávací oblast Vzdělávací obor Tematický okruh Téma Člověk a příroda Chemie Obecná a anorganická chemie Oxidy Ročník 9. Anotace Aktivita slouží k upevnění učiva na téma oxidy,
Šablona č. I, sada č. 2 Vzdělávací oblast Vzdělávací obor Tematický okruh Téma Člověk a příroda Chemie Obecná a anorganická chemie Oxidy Ročník 9. Anotace Aktivita slouží k upevnění učiva na téma oxidy,
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939. Název projektu: Investice do vzdělání - příslib do budoucnosti
 Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
HALOGENIDY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 27. 2. 2013. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková HALOGENIDY Datum (období) tvorby: 27. 2. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s dvouprvkovými
Autor: Mgr. Stanislava Bubíková HALOGENIDY Datum (období) tvorby: 27. 2. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s dvouprvkovými
Vyberte z těchto částic Cu Cl 2 Fe 2+ Na + CO H 2 SO 4 Ag Cl - NaOH. atomy: Cu Ag molekuly: Cl 2 CO H 2 SO 4 NaOH kationty: Fe 2+ Na +
 OPAKOVÁNÍ Vyberte z těchto částic Cu Cl 2 Fe 2+ Na + CO H 2 SO 4 Ag Cl - NaOH atomy: Cu Ag molekuly: Cl 2 CO H 2 SO 4 NaOH kationty: Fe 2+ Na + Vyberte z těchto částic Cu Cl 2 Fe 2+ Na + CO H 2 SO 4 Ag
OPAKOVÁNÍ Vyberte z těchto částic Cu Cl 2 Fe 2+ Na + CO H 2 SO 4 Ag Cl - NaOH atomy: Cu Ag molekuly: Cl 2 CO H 2 SO 4 NaOH kationty: Fe 2+ Na + Vyberte z těchto částic Cu Cl 2 Fe 2+ Na + CO H 2 SO 4 Ag
Názvosloví anorganických sloučenin
 Názvosloví anorganických sloučenin CHEMICKÁ NOMENKLATURA Milan Haminger, BiGy Brno Chemické názvosloví Název chemické sloučeniny = slovní záznam chemického vzorce. Název anorganické sloučeniny: - podstatné
Názvosloví anorganických sloučenin CHEMICKÁ NOMENKLATURA Milan Haminger, BiGy Brno Chemické názvosloví Název chemické sloučeniny = slovní záznam chemického vzorce. Název anorganické sloučeniny: - podstatné
Příklad Sestavte rovnice následujících dějů: reakce hydroxidu sodného s kyselinou tetrahydrogendifosforečnou 4NaOH + H 4 P 2 O 7 Na 4 P 2 O 7
 Příklad 2.2.9. Sestavte rovnice následujících dějů: reakce hydroxidu sodného s kyselinou tetrahydrogendifosforečnou 4NaOH + H 4 P 2 O 7 Na 4 P 2 O 7 + 4H 2 O reakce dimerního oxidu antimonitého s kyselinou
Příklad 2.2.9. Sestavte rovnice následujících dějů: reakce hydroxidu sodného s kyselinou tetrahydrogendifosforečnou 4NaOH + H 4 P 2 O 7 Na 4 P 2 O 7 + 4H 2 O reakce dimerního oxidu antimonitého s kyselinou
Ch - Stavba atomu, chemická vazba
 Ch - Stavba atomu, chemická vazba Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl
Ch - Stavba atomu, chemická vazba Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl
Gymnázium, Brno, Elgartova 3
 Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Základy názvosloví Autor: Název: Mgr. Petra Holzbecherová Anorganické
Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Základy názvosloví Autor: Název: Mgr. Petra Holzbecherová Anorganické
KONTROLNÍ TEST ŠKOLNÍHO KOLA
 Ústřední komise Chemické olympiády 50. ročník 2013/2014 ŠKOLNÍ KOLO kategorie D KONTROLNÍ TEST ŠKOLNÍHO KOLA časová náročnost: 90 minut 1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16 17
Ústřední komise Chemické olympiády 50. ročník 2013/2014 ŠKOLNÍ KOLO kategorie D KONTROLNÍ TEST ŠKOLNÍHO KOLA časová náročnost: 90 minut 1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16 17
DUM č. 19 v sadě. 24. Ch-2 Anorganická chemie
 projekt GML Brno Docens DUM č. 19 v sadě 24. Ch-2 Anorganická chemie Autor: Aleš Mareček Datum: 26.09.2014 Ročník: 2A Anotace DUMu: Materiál je určen pro druhý ročník čtyřletého a šestý ročník víceletého
projekt GML Brno Docens DUM č. 19 v sadě 24. Ch-2 Anorganická chemie Autor: Aleš Mareček Datum: 26.09.2014 Ročník: 2A Anotace DUMu: Materiál je určen pro druhý ročník čtyřletého a šestý ročník víceletého
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T3-2-12 Téma: Kovy Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý VÝKLAD Kovy KOVY UMÍSTĚNÍ V PERIODICKÉ SOUSTAVĚ PRVKŮ přibližně tři čtvrtiny
DUM Základy přírodních věd DUM III/2-T3-2-12 Téma: Kovy Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý VÝKLAD Kovy KOVY UMÍSTĚNÍ V PERIODICKÉ SOUSTAVĚ PRVKŮ přibližně tři čtvrtiny
Předmět: CHEMIE Ročník: 8. ŠVP Základní škola Brno, Hroznová 1. Výstupy předmětu
 Chemie ukázka chemického skla Chemie přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce práce s dostupnými a běžně používanými látkami (směsmi). Na základě piktogramů žák posoudí nebezpečnost
Chemie ukázka chemického skla Chemie přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce práce s dostupnými a běžně používanými látkami (směsmi). Na základě piktogramů žák posoudí nebezpečnost
ANODA KATODA elektrolyt:
 Ukázky z pracovnívh listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Ukázky z pracovnívh listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
ZÁPADOČESKÁ UNIVERZITA V PLZNI
 ZÁPADOČESKÁ UNIVERZITA V PLZNI FAKULTA PEDAGOGICKÁ KATEDRA CHEMIE ANORGANICKÉ NÁZVOSLOVÍ A CHEMICKÉ VÝPOČTY VE VÝUCE CHEMIE NA ZÁKLADNÍ ŠKOLE DIPLOMOVÁ PRÁCE Bc. Lenka Trhlíková Učitelství pro základní
ZÁPADOČESKÁ UNIVERZITA V PLZNI FAKULTA PEDAGOGICKÁ KATEDRA CHEMIE ANORGANICKÉ NÁZVOSLOVÍ A CHEMICKÉ VÝPOČTY VE VÝUCE CHEMIE NA ZÁKLADNÍ ŠKOLE DIPLOMOVÁ PRÁCE Bc. Lenka Trhlíková Učitelství pro základní
4. CHEMICKÉ ROVNICE. A. Vyčíslování chemických rovnic
 4. CHEMICKÉ ROVNICE A. Vyčíslování chemických rovnic Klíčová slova kapitoly B: Zachování druhu atomu, zachování náboje, stechiometrický koeficient, rdoxní děj Čas potřebný k prostudování učiva kapitoly
4. CHEMICKÉ ROVNICE A. Vyčíslování chemických rovnic Klíčová slova kapitoly B: Zachování druhu atomu, zachování náboje, stechiometrický koeficient, rdoxní děj Čas potřebný k prostudování učiva kapitoly
Gymnázium, Brno, Elgartova 3
 Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Základy názvosloví Autor: Název: Mgr. Petra Holzbecherová Procvičování
Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Základy názvosloví Autor: Název: Mgr. Petra Holzbecherová Procvičování
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH ROVNIC VY_32_INOVACE_03_3_18_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH ROVNIC VY_32_INOVACE_03_3_18_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH
