Podmínky vzniku makromolekuly
|
|
|
- Antonie Horáčková
- před 5 lety
- Počet zobrazení:
Transkript
1 Podmínky vzniku makromolekuly
2 Vznik makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce nejméně dvoufunkční 2) termodynamická podmínka Změna Gibbsovy energie musí být menší nebo rovna nule 3) kinetická podmínka Molekula musí být snadno aktivovatelná rychlost polymerizace musí být daleko rychlejší než další reakce probíhající v systému Vhodně zvolený mechanismus
3 Vznik makromolekuly Podmínky vzniku makromolekuly o Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce nejméně dvoufunkční funkčnost = počet kovalentních vazeb, které může molekula vytvořit s jiným reaktantem za existujících reakčních podmínek Reagují-li dva monofunkční monomery vzniká produkt, který nemá již žádnou reaktivní skupinu reakce nemůže pokračovat! Reakcí dvou dvoufunkčních monomerů vzniká produkt, který má 2 reaktivní místa reakce může pokračovat
4 Vznik makromolekuly Podmínky vzniku makromolekuly o Přítomnost dvou a více fčních skupin v molekule např. -O, -O, -OO, -N 2, -S Kyselina adipová examethylendiamin O O O 2 O N 2 2 N 2 o Násobná vazba (adice) olefiny, konjug. Dieny, vinylové slč, trojná, =heteroatom 6 4 Ethylen 2 2 Kyselina akrylová 2 OO o yklická struktura (v průběhu rce se otevírá) heterocykly, cykloalkeny N 2 O 5 6-kaprolaktam
5 Vznik makromolekuly Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace Zieglerovy Nattovy katalyzátory metallocenové katalyzátory o Stupňovité polymerizace polykondenzace polyadice
6 Vznik makromolekuly princip řetězových polymerizací Opakovaná adice mol. monomeru na růstová centra (vysoce reaktivní meziprodukty radikály, ionty..) Iniciace molekula monomeru se aktivuje působením iniciátoru (E) I R* R* + M R-M* Propagace dochází k růstu řetězce makromolekuly (přesun R) R-M* + M R-M-M* + M P n * + M P n+1 * R-M-M* R-M-M-M* Terminace dochází k ukončení růstu řetězce makromolekuly P n * + P m * P n -P m rekombinace P n + P m disproporcionace P n * + X P n + X* přenos
7 Vznik makromolekuly Základní princip stupňovitých polymerizací - MM vznikají reakcí funkčních skupin dvojfunkčních monomerů a vzniklých oligomerů (polymerů) - Opakování jedné základní rce (stabilní meziprodukty) - Všechny funkční skupiny stejná reaktivita (velikost molekuly nehraje roli - Spojování molekul různé velikosti stejná rychlost, E a T, derivatizace fčních skupin (chloridy), katalyzátory (+) - Pomalý, plynulý nárůst Pn, (polyadice, polykondenzace) aaa + bbb aaa + bbb n aaa + n bbb aabb + ab + aaa + bbb aabb + aabab + aababb + ab + aaa + bbb a[ab] n b (2n -1) ab
8 Vznik makromolekuly Iniciace, propagace a terminace Stupňovité polyreakce Iniciace, propagace a terminace jsou z hlediska reakční rychlosti a mechanismu identické reakce. Řetězové polyreakce Iniciace, propagace a terminace jsou z hlediska reakční rychlosti a mechanismu podstatně odlišné reakce.
9 Vznik makromolekuly Aktivační energie Stupňovité polyreakce Aktivační energie je pro každý růstový krok stejná. Řetězové polyreakce Aktivační energie iniciace je odlišná od aktivační energie propagace.
10 Vznik makromolekuly Iniciace reakce Stupňovité polyreakce Katalyzátory vystupují z reakce nezměněny. Iniciace reakce probíhá i bez katalyzátoru, avšak podstatně pomaleji. Řetězové polyreakce Iniciace reakce se dosahuje sloučeninami, které se zabudovávají v makromolekulách jako koncové skupiny.
11 Vznik makromolekuly Ubývání monomeru Stupňovité polyreakce Monomer je schopný kombinace s jiným monomerem nebo s jinou rostoucí složkou systému, což vede k rychlému vymizení monomeru. Řetězové polyreakce Monomer je schopen reagovat pouze s aktivním koncem řetězce, což vede k plynulému ubývání monomeru v průběhu polyreakce.
12 Vznik makromolekuly Růst řetězce polymeru Stupňovité polyreakce Řetězové polyreakce Růst řetězce polymeru je pomalý. Polymery s velkou molekulovou hmotností nejsou na začátku vůbec přítomny. Pro dosažení velkých M je potřeba vysoká konverze. Růst každého iniciovaného polymerního řetězce je velmi rychlý. Již v prvních časových stádiích polymerizace jsou přítomny makromolekuly s velkou M, která se s časem výrazně nemění.
13 Vznik makromolekuly Reakční doba Stupňovité polyreakce Dlouhá reakční doba vede k velké molekulové hmotnosti polymeru. Řetězové polyreakce Dlouhá reakční doba vede k vysokému výtěžku.
14 Řetězové polymerizace
15 Řetězové polymerizace Základní princip řetězových polymerizací Iniciace molekula monomeru se aktivuje působením iniciátoru I R* R* + M R-M* Propagace dochází k růstu řetězce makromolekuly R-M* + M R-M-M* R-M-M* + M R-M-M-M* P n * + M P n+1 * Terminace dochází k ukončení růstu řetězce makromolekuly P n * + P m * P n -P m rekombinace P n + P m disproporcionace P n * + X P n + X* přenos
16 Řetězové polymerizace harakterické znaky řetězových polymerizací o Molekuly rostou opakovanou adicí na aktivní centrum. o Koncentrace monomeru se snižuje postupně v průběhu polymerizace. o Pro vznik vysokomolekulárního polymeru nejsou nutné dlouhé reakční časy. o Průměrný polymerační stupeň se mění s časem jen málo. o Koncentrace rostoucích molekul je malá (10-8 až 10-3 M). o Čas potřebný k vytvoření dlouhé makromolekuly je řádově několik sekund.
17 Řetězové polymerizace Kinetické podmínky polymerizovatelnosti o Dostatečná aktivace monomeru (reaktivní meziprodukt) o Většina řetězových reakcí je uskutečňována otevřením dvojné vazby mezi atomy uhlíku. R * + S R * S Způsob aktivace monomeru (rozštěpení dvojné vazby) závisí na typu substituentu S.
18 Řetězové polymerizace Kinetické podmínky polymerizovatelnosti Způsob aktivace monomeru (rozštěpení dvojné vazby) závisí na typu substituentu. Substituent ovlivňuje: - Rozložení elektronové hustoty na dvojné vazbě indukční efekt - Stabilizaci vznikajících růstových center rezonanční efekt 1) Elektrondonorní substituent - zvyšuje elektronovou hustotu na dvojné vazbě - S = alkyl-, alkenyl-, alkoxy-, fenyl- - mohou polymerizovat kationtově - růstové centrum je kation, iniciátor je kation R+ + R + S S
19 Řetězové polymerizace Kinetické podmínky polymerizovatelnosti Kationtová polymerizace alkylvinyletherů (alkoxy sk., podobně fenylové a vinylové substituenty styren, isopren) - Polymerizace účinkem kationtových iniciátorů Rozložení hustoty elektronového oblaku na dvojné vazbě indukční efekt R+ + RR + OS R O S R R+ + Stabilizace vznikajících růstových center rezonanční efekt R + O R R O + R
20 Řetězové polymerizace Kinetické podmínky polymerizovatelnosti 1) Elektrondonorní substituent - STABILIZAE Stabilizace vznikajících růstových center závisí na substituentu S. S = alkenyl-, alkoxy-, fenyl- delokalizace kladného náboje, růstové centrum je rezonančně stabilizováno mohou být kationtově polymerizovány za vzniku vysokomelukulárního polymeru. S = -, alkyl- malý indukční efekt, rostoucí centrum není rezonančně stabilizováno, kationtově lze připravit pouze polymery s malým polymeračním stupněm.
21 Řetězové polymerizace Kinetické podmínky polymerizovatelnosti 2) Elektronakceptorní substituent - snižuje elektronovou hustotu na dvojné vazbě - S = -NO 2, -O-R, -OOR, -N, - usnadňují atak záporně nabité částice na atom z nějž vychází dvojná vazba - mohou polymerizovat aniontově růstové centrum je anion R- + - R O O 3 O O 3
22 Řetězové polymerizace Kinetické podmínky polymerizovatelnosti Aniontová polymerizace vinylacetátu Rozložení hustoty elektronového oblaku na dvojné vazbě indukční efekt R- + - R O O 3 O O 3 Růstové centrum je rezonančně stabilizováno. R O - O 3 R O - O 3
23 Řetězové polymerizace Kinetické podmínky polymerizovatelnosti Radikálové polymerizace iniciace radikálem Radikálově polymerují: -Monomery substituované halogeny, kde se příliš neuplatňuje indukční efekt substituentu (vinylchlorid), - aniontově polymerizující monomery (S = -NO 2, -O-R, -OOR, -N) Radikálově zpravidla nepolymerují: - monomery se zvýšenou elektronovou hustotu na dvojné vazbě (polymerují kationtově- S = alkenyl-, alkoxy- ) Univerzální: -vinyl, -fenyl (buta-1,3-dien, styren) + R.. S S R
24 Řetězové polymerizace Kinetické podmínky polymerizovatelnosti Polymerizace polyethylenu - kationtově - pouze nízkomolekulární polymer - radikálově - polymerizace možná jen za vysokých tlaků a teplot Polymerizace polypropylenu - kationtově - pouze nízkomolekulární polymer důvod - nízká stabilizace růstového centra K přípravě vysokomolekulárního polymeru se využívají koordinační polymerizace
25 Řetězové polymerizace
26
27 Řetězové polymerizace Termodynamika řetězových polymerizací Při zvoleném konstantním tlaku platí: G mp mp T S mp Gibbsova energie při reakci monomer (m) polymer (p) Při rovnováze je rovna nule T c S mp mp entalpie je při naprosté většině polymerizací záporná polymerizace jsou exotermní reakce (polymerizační teplo) entropie je při naprosté většině polymerizací záporná (vzrůstá uspořádanost) Stropní teplota teplota, při které jsou si rovny rychlosti polymerizace a depolymerizace (nad T c nevznikají MM, ale OLIGA)
28 Řetězové polymerizace Termodynamika řetězových polymerizací Tab.7-3 str.66 Prokop Faktory ovlivňující entalpii polymerizace substituovaných alkenů: o rozdíly v rezonanční stabilizaci monomeru a polymeru o rozdíly ve stérickém napětí v monomeru a polymeru o rozdíly v nevazebných interakcích v monomeru a polymeru Entropie hodnota se příliš neliší
29 Radikálová polymerizace
30 radikálová polymerizace Monomery s dvojnou vazbou : olefiny, dieny, vinyly a vinylideny
31 radikálová polymerizace Radikálová polymerizace Výhody: -není velmi citlivá na přítomnost nečitsoty -není tolik citlivá na přítomnost stop kyslíku -lze ji provádět většinou při teplotách 20 až 80 a atmosférického tlaku -iniciátory jsou většinou netoxické -umožňuje přípravu velkého množství kopolymerů Nevýhody: -nejedná se o stereospecifickou polymerizaci
32 radikálová polymerizace iniciace o iniciace radikálem o aktivním centrem jsou volné radikály sloučeniny s nepárovým elektronem + R.. S S R
33 radikálová polymerizace iniciace Iniciace molekula monomeru se aktivuje působením iniciátoru I R + M R R-M Při iniciaci vznikají primární radikály, které reakcí s molekulou monomeru vytvářejí aktivní centrum. Primární radikál : - vysoce reaktivní radikály (rezonančně nestabilizované) mají krátkou střední dobu života, podílejí se nejen na reakci s monomerem, ale také na vedlejších reakcích polymerizace neprobíhá vůbec nebo vznikají jen polymery s nízkým P n. - málo reaktivní radikály (rezonančně stabilizované) málo reaktivní, působí jako inhibitory reakce (reagují jen s jinými radikály). Vlastnosti používaných iniciátorů jsou někde mezi těmito extrémy. Střední doba života desetiny až jednotky vteřin.
34 radikálová polymerizace Rozdělení iniciátorů Podle způsobu, jakým vznikají: - termické štěpení kovalentních vazeb - fotolytický rozklad kovalentních vazeb - oxidačně redukční reakce - štěpení kovalentních vazeb účinkem záření s vysokou energií - elektrochemicky
35 radikálová polymerizace Termický rozklad iniciátorů Zahřátím ( ) dochází k rozpadu iniciátoru a vzniku dvou primárních volných radikálů dibenzoylperoxid 2 benzoyloxy radikály str.70 Prokop Do této skupiny patří: peroxidy diacylperoxidy(i), dialkylperoxidy(ii), peroxyestery(iii), peroxydikarbonáty(iv), hydroperoxidy(v), anorganické peroxidy azosloučeniny 2,2 -azo-bis(isobutyronitril) (AIBN)
36 radikálová polymerizace Primární volný radikál se může účastnit těchto reakcí: - s monomerem za vzniku aktivního centra - dalšího rozkladu primárního radikálu - indukovaného rozkladu peroxidů - vzájemné reakce (rekombinace) dvou radikálů za vzniku stabilního produktu způsobuje pokles koncentrace radikálů tím snižuje účinnost iniciátoru klecový efekt. Počet primárních radikálů podílejících se na iniciační reakci elkový počet primárních radikálů vzniklých rozpadem iniciátoru
37 radikálová polymerizace Fotoiniciace o Vhodné fotoiniciátory jsou všechny sloučeniny, které absorbují světelnou energii nutnou pro disociaci vazby. o Nejčastěji se používají peroxidy a azosloučeniny. o Výhoda lze je provádět i při nízkých teplotách. o Rychlost iniciace je úměrná intenzitě absorbovaného světla Rozklad benzoinu
38 radikálová polymerizace Oxidačně redukční iniciace o Radikály vznikají chemickou reakcí peroxidu s redukčním činidlem. o Jako redukční činidla jsou používány soli kovů, terc. aminy, kyselina askorbová atd. o Aktivační energie redox reakce je nízká iniciace je možná i za nízkých teplot. kumylhydroperoxid Anorganické peroxidy 2 O 2
39 radikálová polymerizace PROPAGAE Propagace dochází k růstu řetězce makromolekuly R-M + M R-M-M + M P n + M R-M-M P n+1 R-M-M-M o Monomer reaguje s primárním radikálem tím ochotněji, čím je vznikající růstové centrum více rezonančně stabilizované. o Málo rezonančně stabilizovaná růstová centra vznikají při iniciaci obtížně. S S = -OR, -O 3, -N, -OOR, -= 2, - 2 R, -l, - 6 5, -OOR
40 radikálová polymerizace PROPAGAE Rezonanční stabilizace radikálových vinylových monomerů klesá v řadě: Tab str.75 Prokop
41 radikálová polymerizace PROPAGAE Koncentrace iniciátoru v polymerizujícím systému je nízká. Důvod: mol l -1 1) Více rostoucích aktivních center = více exotermních reakcí = problém s odvodem tepla 2) Více rostoucích aktivních center = větší pravděpodobnost rekombinace = snížení polymeračního stupně
42 radikálová polymerizace TERMINAE Terminace dochází k ukončení růstu řetězce makromolekuly P n + P m P n -P m rekombinace P n + P m disproporcionace Po době řádově několika sekund dochází k ukončení aktivního centra (makroradikálu). Rekombinace spojení dvou aktivních center, nízká aktivační energie Disproporcionace musí dojít k přesunu atomu vodíku, více energeticky náročná reakce, podíl disproporcionace na terminaci záleží na podmínkách reakce (teplota).
43 radikálová polymerizace TERMINAE Přenosové reakce Dochází k přenosu radikálu z aktivního centra rostoucího řetězce na jinou chemickou strukturu P n + X P n + X Přenosová rce je vždy spojena s výměnou atomu (, X) Přenašeč složky polymerizačního systému: - přenos monomerem - přenos polymerem - přenos rozpouštědlem - přenos iniciátorem - přenos regulátorem molárních hmotností
44 S S S S S S Přenos monomerem Uplatňuje se při vyšších polymerizačních teplotách Regulace průměrné molární hmotnosti pomocí teploty (polyvinylchlorid) Proč nelze radikálovou polymerizací získat vysokomolekulární polypropylen? radikálová polymerizace
45 radikálová polymerizace Přenos monomerem Při přenosu vzniká nejstabilnější radikál rezonančně stabilizován Zastavení růstu řetězce autoinhibice
46 radikálová polymerizace Přenos polymerem R 2 R 2 2 S S S R 2 S R o Zaniká růstové aktivní centrum na konci lineární makromolekuly o Vzniká růstové aktivní centrum uvnitř makromolekuly o Dochází k větvení o Délka větve je srovnatelná se délkou primární makromolekuly o Může dojít až k sesítění o Je možný také intramolekulární přenos radikálu
47 radikálová polymerizace Přenos rozpouštědlem o ílené snižování (regulace) molární hmotnosti polymerů o Využití látek s relativně vysokou přenosovou konstantou - regulátory o Často se s výhodou jako regulátory používají rozpouštědla (l 4, Br 4, disulfidy, thioly) o Telomery oligomery s definovanými koncovými skupinami. Vznikají při polymerizacích, kdy je použito velké množství přenašeče (rozpouštědlo)
48 Další možnosti zániku či snížení reaktivity aktivních center: - Reakce s primárním radikálem - Reakce s látkou za vzniku vysoce stabilizovaného radikálu neschopného adice další molekuly monomeru tyto látky zastaví polymerizaci inhibitory (chinony, alkylfenoly, thiokarbonáty). Zabránění samovolné polymerizace během skladování - Reakce s látkou za vzniku stabilizovaného radikálu, který aduje další molekulu monomeru s menší rychlostí ve srovnání s původním makroradikálem retardéry.
o Řetězové polymerizace o Stupňovité polymerizace Základní typy polymerizací
 vznik makromolekuly Vznik makromolekuly Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité
vznik makromolekuly Vznik makromolekuly Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité
Polymerizace. Polytransformace
 vznik makromolekuly Polymerizace Polytransformace Podmínky vzniku makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce
vznik makromolekuly Polymerizace Polytransformace Podmínky vzniku makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce
Řetězové polymerizace
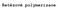 Řetězové polymerizace Polyethylen Polypropylen Polystyren Polyvinylchlorid Kaučuky PMMA PTFE Polyakryláty.. 2 Řetězová polymerizace Řetězové polymerizace 3 odlišné kroky iiciace Propagace Terminace Initiating
Řetězové polymerizace Polyethylen Polypropylen Polystyren Polyvinylchlorid Kaučuky PMMA PTFE Polyakryláty.. 2 Řetězová polymerizace Řetězové polymerizace 3 odlišné kroky iiciace Propagace Terminace Initiating
o Řetězové polymerizace o Stupňovité polymerizace Základní typy polymerizací
 Vznik makromolekuly Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité polymerizace polykondenzace
Vznik makromolekuly Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité polymerizace polykondenzace
Řetězová polymerizace
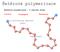 Řetězová polymerizace Řetězové polymerizace 3 odlišné kroky iiciace Propagace Terminace Initiating species Chain Step-Growth Iontové polymerizace aniontové, kationtové v závislosti na typu rostoucího aktivního
Řetězová polymerizace Řetězové polymerizace 3 odlišné kroky iiciace Propagace Terminace Initiating species Chain Step-Growth Iontové polymerizace aniontové, kationtové v závislosti na typu rostoucího aktivního
Kopolymerace polymerace dvou a více monomerů
 Kopolymerace polymerace dvou a více monomerů ( 1 monomer homopolymer; 2 monomery kopolymer; 3 monomery ternární kopolymer [ př ABS]) mezní případy kopolymerace: n A n B A A n B B n A B n Struktury vznikajících
Kopolymerace polymerace dvou a více monomerů ( 1 monomer homopolymer; 2 monomery kopolymer; 3 monomery ternární kopolymer [ př ABS]) mezní případy kopolymerace: n A n B A A n B B n A B n Struktury vznikajících
Úvod do studia organické chemie
 Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
MAKROMOLEKULÁRNÍ LÁTKY
 MAKROMOLEKULÁRNÍ LÁTKY 1. Základní pojmy - makromolekulární látky = molekulové systémy složené z velkého počtu atomů, které jsou vázány chemickou vazbou do dlouhých řetězců - řetězce jsou tvořeny stavebními
MAKROMOLEKULÁRNÍ LÁTKY 1. Základní pojmy - makromolekulární látky = molekulové systémy složené z velkého počtu atomů, které jsou vázány chemickou vazbou do dlouhých řetězců - řetězce jsou tvořeny stavebními
Iontové polymerizace
 Iontové polymerizace Vznik makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce nejméně dvoufunkční 2) termodynamická podmínka
Iontové polymerizace Vznik makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce nejméně dvoufunkční 2) termodynamická podmínka
Alkeny. Alkeny. Největšíprůmyslový význam majíethen (ethylen) a propen (propylen) jako suroviny pro další přeměny nebo pro polymerace
 Alkeny Dvojná vazba je tvořena jednou vazbou sigma a jednou vazbou pí. Dvojná vazba je kratší než vazba jednoduchá a všechny čtyři atomy vázané na dvojnou vazbu leží v jedné rovině. Fyzikální vlastnosti
Alkeny Dvojná vazba je tvořena jednou vazbou sigma a jednou vazbou pí. Dvojná vazba je kratší než vazba jednoduchá a všechny čtyři atomy vázané na dvojnou vazbu leží v jedné rovině. Fyzikální vlastnosti
Reakce alkanů 75. mechanismem), iniciované světlem nebo radikálovými iniciátory: Oxidace kyslíkem, hoření, tvorba hydroperoxidů.
 eakce alkanů 75 5. eakce alkanů Alkany poskytují především radikálové reakce (často probíhající řetězovým mechanismem), iniciované světlem nebo radikálovými iniciátory: alogenace pomocí X 2 ; bromaci lze
eakce alkanů 75 5. eakce alkanů Alkany poskytují především radikálové reakce (často probíhající řetězovým mechanismem), iniciované světlem nebo radikálovými iniciátory: alogenace pomocí X 2 ; bromaci lze
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/
 Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 LRR/CHPB2 Chemie pro biology 2 Reakce a reakční mechanismy v organické chemii Lucie Szüčová Osnova: homolytické a heterolytické
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 LRR/CHPB2 Chemie pro biology 2 Reakce a reakční mechanismy v organické chemii Lucie Szüčová Osnova: homolytické a heterolytické
VIII. 6.5 Polyadice. H. Schejbalová & I. Stibor, str. 179. I. Prokopová, str. 181. D. Lukáš 2013
 VIII. 6.5 Polyadice H. Schejbalová & I. Stibor, str. 179. I. Prokopová, str. 181. D. Lukáš 2013 1 Vzdělávací záměr 1. Polyadice obecný průběh polyadice, odlišnosti od polykondenzace. 2. Syntéza polyuretanů
VIII. 6.5 Polyadice H. Schejbalová & I. Stibor, str. 179. I. Prokopová, str. 181. D. Lukáš 2013 1 Vzdělávací záměr 1. Polyadice obecný průběh polyadice, odlišnosti od polykondenzace. 2. Syntéza polyuretanů
Vlastnosti. Pozor! H 3 C CH 3 H CH 3
 Alkeny Vlastnosti C n 2n obsahují dvojné vazby uhlíky v sp 2 hybridizaci násobná vazba vzniká překryvem 2p orbitalů obou atomů uhlíku nad a pod prostorem obsazeným vazbou aby k překryvu mohlo dojít, musí
Alkeny Vlastnosti C n 2n obsahují dvojné vazby uhlíky v sp 2 hybridizaci násobná vazba vzniká překryvem 2p orbitalů obou atomů uhlíku nad a pod prostorem obsazeným vazbou aby k překryvu mohlo dojít, musí
Názvosloví Konformace Isomerie. Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o )
 ALKANY 1 Názvosloví Konformace Isomerie Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o ) 2 Alkany (resp. cykloalkany) jsou nejzákladnější organické sloučeniny složené pouze z
ALKANY 1 Názvosloví Konformace Isomerie Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o ) 2 Alkany (resp. cykloalkany) jsou nejzákladnější organické sloučeniny složené pouze z
Radikály jsou zároveň velmi reaktivní - stabilních radikálů, které lze izolovat a skladovat, není příliš mnoho.
 Radikálové reakce se odlišují od reakcí, se kterými jsme se dosud setkali. Při zápisu mechanismů nebudeme přesunovat elektronové páry, ale pouze jeden elektron. To se mimojiné projeví na způsobu, jak takové
Radikálové reakce se odlišují od reakcí, se kterými jsme se dosud setkali. Při zápisu mechanismů nebudeme přesunovat elektronové páry, ale pouze jeden elektron. To se mimojiné projeví na způsobu, jak takové
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: Číslo DUMu: VY_32_INOVACE_10_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 12.02.2013 Číslo DUMu: VY_32_INOVACE_10_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 12.02.2013 Číslo DUMu: VY_32_INOVACE_10_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Obsah. Ú v o d Kinetické f a k to r y Stacionární Živé Nestacionární... 27
 Obsah 7 Ú v o d... 15 1 Polymerace... ^ 11 Podle druhu aktivních c e n t e r... 19 111 R adikálové... 19 112 Iontové... 19 1121 Kationtové... 20 1122 A niontové... 2^ 113 K o o rd in a č n í... 2(* 12
Obsah 7 Ú v o d... 15 1 Polymerace... ^ 11 Podle druhu aktivních c e n t e r... 19 111 R adikálové... 19 112 Iontové... 19 1121 Kationtové... 20 1122 A niontové... 2^ 113 K o o rd in a č n í... 2(* 12
Energie v chemických reakcích
 Energie v chemických reakcích Energetická bilance reakce CH 4 + Cl 2 = CH 3 Cl + HCl rozštěpení vazeb vznik nových vazeb V chemických reakcích dochází ke změně vazeb mezi atomy. Vazebná energie uvolnění
Energie v chemických reakcích Energetická bilance reakce CH 4 + Cl 2 = CH 3 Cl + HCl rozštěpení vazeb vznik nových vazeb V chemických reakcích dochází ke změně vazeb mezi atomy. Vazebná energie uvolnění
Polymery lze rozdělit podle několika kritérií. Podle původu rozlišujeme polymery přírodní a syntetické. Přírodní polymery jsou:
 MAKROMOLEKULÁRNÍ LÁTKY (POLYMERY) Makromolekuly jsou molekulové systémy složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců. Tyto řetězce tvoří pravidelně se opakující části,
MAKROMOLEKULÁRNÍ LÁTKY (POLYMERY) Makromolekuly jsou molekulové systémy složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců. Tyto řetězce tvoří pravidelně se opakující části,
MATERIÁLY A TECHNOLOGIE 1 PAVEL ČERNÝ
 MATERIÁLY A TECHNOLOGIE 1 PAVEL ČERNÝ Co vás napadne, když se řekne plast? Proč právě plasty? skupina syntetických materiálů slovo plast ze slova plastický, tvárný, formovatelný název plyne z chemické
MATERIÁLY A TECHNOLOGIE 1 PAVEL ČERNÝ Co vás napadne, když se řekne plast? Proč právě plasty? skupina syntetických materiálů slovo plast ze slova plastický, tvárný, formovatelný název plyne z chemické
Inovace studia molekulární a buněčné biologie
 Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
18. Reakce v organické chemii
 1) homolýza, heterolýza 2) substituce, adice, eliminace, přesmyk 3) popis mechanismů hlavních typů reakcí (S R, A E, A R ) 4) příklady 18. Reakce v organické chemii 1) Homolýza, heterolýza KLASIFIKACE
1) homolýza, heterolýza 2) substituce, adice, eliminace, přesmyk 3) popis mechanismů hlavních typů reakcí (S R, A E, A R ) 4) příklady 18. Reakce v organické chemii 1) Homolýza, heterolýza KLASIFIKACE
o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace
 Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité polymerizace polykondenzace polyadice Stupňovitá
Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité polymerizace polykondenzace polyadice Stupňovitá
H H C C C C C C H CH 3 H C C H H H H H H
 Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Chemická kinetika. Chemické změny probíhající na úrovni atomárně molekulové nazýváme reakční mechanismus.
 Chemická kinetika Chemická reakce: děj mezi jednotlivými atomy a molekulami, při kterých zanikají některé vazby v molekulách výchozích látek a jsou nahrazovány vazbami v molekulách nově vznikajících látek.
Chemická kinetika Chemická reakce: děj mezi jednotlivými atomy a molekulami, při kterých zanikají některé vazby v molekulách výchozích látek a jsou nahrazovány vazbami v molekulách nově vznikajících látek.
ALKENY NENASYCENÉ UHLOVODÍKY
 ALKENY NENASYCENÉ ULOVODÍKY 1 ALKENY - mají ve svých molekulách alespoň jednu dvojnou vazbu- C=C homologický vzorec : C n 2n názvy od alkanů zakončeny koncovkou en CYKLOALKENY - homologický vzorec : C
ALKENY NENASYCENÉ ULOVODÍKY 1 ALKENY - mají ve svých molekulách alespoň jednu dvojnou vazbu- C=C homologický vzorec : C n 2n názvy od alkanů zakončeny koncovkou en CYKLOALKENY - homologický vzorec : C
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Karboxylové kyseliny a jejich funkční deriváty
 Karboxylové kyseliny a jejich funkční deriváty Úvod Karboxylové kyseliny jsou nejdůležitější organické kyseliny. Jejich funkční skupina je karboxylová skupina a tento název je složen ze slov karbonyl a
Karboxylové kyseliny a jejich funkční deriváty Úvod Karboxylové kyseliny jsou nejdůležitější organické kyseliny. Jejich funkční skupina je karboxylová skupina a tento název je složen ze slov karbonyl a
2. Polarita vazeb, rezonance, indukční a mezomerní
 32 Polarita vazeb a reaktivita 2. Polarita vazeb, rezonance, indukční a mezomerní efekty ktetové pravidlo je užitečné pro prvky druhé periody (,, ) a halogeny. Formální náboj atomu určíme jako rozdíl počtu
32 Polarita vazeb a reaktivita 2. Polarita vazeb, rezonance, indukční a mezomerní efekty ktetové pravidlo je užitečné pro prvky druhé periody (,, ) a halogeny. Formální náboj atomu určíme jako rozdíl počtu
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 16, 566 01 Vysoké Mýto Alkeny Vlastnosti dvojné vazby Hybridizace uhlíku vázaného dvojnou vazbou je sp. Valenční úhel který svírají vazby na uhlíkovém atomu je přibližně
Gymnázium Vysoké Mýto nám. Vaňorného 16, 566 01 Vysoké Mýto Alkeny Vlastnosti dvojné vazby Hybridizace uhlíku vázaného dvojnou vazbou je sp. Valenční úhel který svírají vazby na uhlíkovém atomu je přibližně
Karbonylové sloučeniny
 Karbonylové sloučeniny více než 120 o 120 o C O C C d + d - C O C sp 2 C sp 2 R C O H R 1 C O R 2 1.aldehydy, ketony Nu E R C O R C O 2. karboxylové kyseliny a funkční deriváty O H 3. deriváty kys. uhličité
Karbonylové sloučeniny více než 120 o 120 o C O C C d + d - C O C sp 2 C sp 2 R C O H R 1 C O R 2 1.aldehydy, ketony Nu E R C O R C O 2. karboxylové kyseliny a funkční deriváty O H 3. deriváty kys. uhličité
VII.6.4 Polykondenzace Lineární polymery. H. Schejbalová & I. Stibor, str I. Prokopová, str D. Lukáš 2013
 VII.6.4 Polykondenzace Lineární polymery H. Schejbalová & I. Stibor, str. 172. I. Prokopová, str. 157. D. Lukáš 2013 1 Vzdělávací záměr 1. Polykondenzace uvést obecný průběh stupňovité reakce 2. Příklady
VII.6.4 Polykondenzace Lineární polymery H. Schejbalová & I. Stibor, str. 172. I. Prokopová, str. 157. D. Lukáš 2013 1 Vzdělávací záměr 1. Polykondenzace uvést obecný průběh stupňovité reakce 2. Příklady
Organická chemie (KATA) rychlý souhrn a opakování
 Organická chemie (KATA) rychlý souhrn a opakování Molekulové orbitaly hybridizace N a O Polarita vazby, induktivní efekt U kovalentní vazby mezi rozdílnými atomy, nebude elektronový pár oběma atomy sdílen
Organická chemie (KATA) rychlý souhrn a opakování Molekulové orbitaly hybridizace N a O Polarita vazby, induktivní efekt U kovalentní vazby mezi rozdílnými atomy, nebude elektronový pár oběma atomy sdílen
Pericycklické reakce
 Reakce, v nichž se tvoří nebo zanikají vazby na konci π-systému. Nejedná se o iontový ani radikálový mechanismus, intermediáty nejsou ani kationty ani anionty! Průběh reakce součinným procesem přes cyklický
Reakce, v nichž se tvoří nebo zanikají vazby na konci π-systému. Nejedná se o iontový ani radikálový mechanismus, intermediáty nejsou ani kationty ani anionty! Průběh reakce součinným procesem přes cyklický
HOŘENÍ A VÝBUCH. Ing. Hana Věžníková, Ph. D.
 HOŘENÍ A VÝBUCH Ing. Hana Věžníková, Ph. D. 1 HOŘENÍ A VÝBUCH Definice hoření Vysvětlení procesu hoření Základní podmínky pro hoření Co jsou hořlavé látky (hořlaviny) a jak je lze klasifikovat Chemické
HOŘENÍ A VÝBUCH Ing. Hana Věžníková, Ph. D. 1 HOŘENÍ A VÝBUCH Definice hoření Vysvětlení procesu hoření Základní podmínky pro hoření Co jsou hořlavé látky (hořlaviny) a jak je lze klasifikovat Chemické
Typy molekul, látek a jejich vazeb v organismech
 Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Makromolekulární látky
 Makromolekulární látky Učební texty k výuce chemie školní rok 2016/2017 Makromolekuly látky složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců látky s velkou relativní molekulovou
Makromolekulární látky Učební texty k výuce chemie školní rok 2016/2017 Makromolekuly látky složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců látky s velkou relativní molekulovou
Obsah. 2. Mechanismus a syntetické využití nejdůležitějších organických reakcí 31 2.1. Adiční reakce 31 2.1.1. Elektrofilní adice (A E
 Obsah 1. Typy reakcí, reakčních komponent a jejich roztřídění 6 1.1. Formální kritérium pro klasifikaci reakcí 6 1.2. Typy reakčních komponent a způsob jejich vzniku jako další kriterium pro klasifikaci
Obsah 1. Typy reakcí, reakčních komponent a jejich roztřídění 6 1.1. Formální kritérium pro klasifikaci reakcí 6 1.2. Typy reakčních komponent a způsob jejich vzniku jako další kriterium pro klasifikaci
Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4.
 Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Alkyny. C n H 2n-2 (obsahuje jednu trojnou vazbu) uhlíky v sp hybridizaci
 Alkyny C n H 2n-2 (obsahuje jednu trojnou vazbu) uhlíky v sp hybridizaci 1 Klasifikace 2 Alkyny - dvě π vazby; lineární uspořádání Pozor! 3 Vlastnosti -π elektrony jsou méně mobilní než u alkenů H CH 3
Alkyny C n H 2n-2 (obsahuje jednu trojnou vazbu) uhlíky v sp hybridizaci 1 Klasifikace 2 Alkyny - dvě π vazby; lineární uspořádání Pozor! 3 Vlastnosti -π elektrony jsou méně mobilní než u alkenů H CH 3
ORGANICKÁ CHEMIE I pro bakalářský stud. program (Varianta A) Jméno a příjmení... Datum... Kroužek/Fakulta.../... Vyučující na semináři...
 ORGANICKÁ CEMIE I pro bakalářský stud. program (Varianta A) Jméno a příjmení... Datum... Kroužek/Fakulta.../... Vyučující na semináři... Počet bodů v části A:... Počet bodů v části B:... Počet bodů celkem:...
ORGANICKÁ CEMIE I pro bakalářský stud. program (Varianta A) Jméno a příjmení... Datum... Kroužek/Fakulta.../... Vyučující na semináři... Počet bodů v části A:... Počet bodů v části B:... Počet bodů celkem:...
Izomerie Reakce organických sloučenin Názvosloví organické chemie. Tomáš Hauer 2.LF UK
 Izomerie Reakce organických sloučenin Názvosloví organické chemie Tomáš Hauer 2.LF UK Izomerie Izomerie izomerní sloučeniny stejný sumární vzorec, různá struktura prostorové uspořádání = izomery různé
Izomerie Reakce organických sloučenin Názvosloví organické chemie Tomáš Hauer 2.LF UK Izomerie Izomerie izomerní sloučeniny stejný sumární vzorec, různá struktura prostorové uspořádání = izomery různé
Vytvrzování reaktoplastických hybridních systémů. Bc. Vilém Galbavý
 Vytvrzování reaktoplastických hybridních systémů Bc. Vilém Galbavý Diplomová práce 2011 UTB ve Zlíně, Fakulta technologická 2 UTB ve Zlíně, Fakulta technologická 3 UTB ve Zlíně, Fakulta technologická 4
Vytvrzování reaktoplastických hybridních systémů Bc. Vilém Galbavý Diplomová práce 2011 UTB ve Zlíně, Fakulta technologická 2 UTB ve Zlíně, Fakulta technologická 3 UTB ve Zlíně, Fakulta technologická 4
Radiační odstraňování vybraných kontaminantů z podzemních a odpadních vod
 Radiační odstraňování vybraných kontaminantů z podzemních a odpadních vod Václav Čuba, Viliam Múčka, Milan Pospíšil, Rostislav Silber ČVUT v Praze Centrum pro radiochemii a radiační chemii Fakulta jaderná
Radiační odstraňování vybraných kontaminantů z podzemních a odpadních vod Václav Čuba, Viliam Múčka, Milan Pospíšil, Rostislav Silber ČVUT v Praze Centrum pro radiochemii a radiační chemii Fakulta jaderná
Dusíkové pravidlo. Počet dusíků m/z lichá m/z sudá 0, 2, 4,... (sudý) EE + OE +. 1, 3, 5,... (lichý) OE +. EE +
 Dusíkové pravidlo Základní formulace (platí pro M R a OE +. ): lichá M R = lichý počet dusíků v molekule sudá M R = sudý počet dusíků v molekule nebo nula Pro ionty EE + přesně naopak: lichá hodnota m/z
Dusíkové pravidlo Základní formulace (platí pro M R a OE +. ): lichá M R = lichý počet dusíků v molekule sudá M R = sudý počet dusíků v molekule nebo nula Pro ionty EE + přesně naopak: lichá hodnota m/z
Kyselost, bazicita, pka
 Kyselost, bazicita, pka Kyselost, bazicita, pk a Organické reakce často kysele nebo bazicky katalyzovány pk a nám říká, jak je (není) daný atom vodíku kyselý důležité pro předpovězení, kde bude daná látka
Kyselost, bazicita, pka Kyselost, bazicita, pk a Organické reakce často kysele nebo bazicky katalyzovány pk a nám říká, jak je (není) daný atom vodíku kyselý důležité pro předpovězení, kde bude daná látka
UHLOVODÍKY ALKANY (...)
 UHLOVODÍKY ALKANY (...) alifatické nasycené uhlovodíky nerozvětvené i rozvětvené mezi atomy uhlíku pouze jednoduché vazby (σ vazby), mezi nimi úhel 109 28 název: kmen + an obecný vzorec C n H 2n + 2 tvoří
UHLOVODÍKY ALKANY (...) alifatické nasycené uhlovodíky nerozvětvené i rozvětvené mezi atomy uhlíku pouze jednoduché vazby (σ vazby), mezi nimi úhel 109 28 název: kmen + an obecný vzorec C n H 2n + 2 tvoří
2.3.2012. Oxidace. Radikálová substituce alkanů. Elektrofilní adice. Dehydrogenace CH 3 CH 3 H 2 C=CH 2 + 2 H. Oxygenace (hoření)
 xidace alkanů Dehydrogenace Reaktivita alkanů xidace Radikálová substituce 3 3 2 = 2 2 xygenace (hoření) 4 2 2 2 2 2 2 4 3 2 2 4 2 Radikálová substituce alkanů Iniciace (vznik radikálu, homolytické štěpení
xidace alkanů Dehydrogenace Reaktivita alkanů xidace Radikálová substituce 3 3 2 = 2 2 xygenace (hoření) 4 2 2 2 2 2 2 4 3 2 2 4 2 Radikálová substituce alkanů Iniciace (vznik radikálu, homolytické štěpení
Autor: Tomáš Galbička Téma: Alkany a cykloalkany Ročník: 2.
 Alkany uhlovodíky s otevřeným řetězcem a pouze jednoduchými vazbami vazby sigma, největší výskyt elektronů na spojnici jader v názvu mají koncovku an Cykloalkany uhlovodíky s uzavřeným řetězcem a pouze
Alkany uhlovodíky s otevřeným řetězcem a pouze jednoduchými vazbami vazby sigma, největší výskyt elektronů na spojnici jader v názvu mají koncovku an Cykloalkany uhlovodíky s uzavřeným řetězcem a pouze
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
Chemická vazba. Molekula vodíku. Elektronová teorie. Oktetové pravidlo (Kossel, Lewis, 1916) Pevnost vazby vazebná energie.
 Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch
 Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch Atom, složení a struktura Chemické prvky-názvosloví, slučivost Chemické sloučeniny, molekuly Chemická vazba
Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch Atom, složení a struktura Chemické prvky-názvosloví, slučivost Chemické sloučeniny, molekuly Chemická vazba
5. CHEMICKÉ REAKCE. KLASIFIKACE CHEMICKÝCH REAKCÍ a) Podle vnějších změn Reakce skládání = SYNTÉZY z jednodušších -> složitější 2H 2 + O 2 -> 2H 2 O
 Na www.studijni-svet.cz zaslal(a): Kikusska94 5. CHEMICKÉ REAKCE Je děj při kterém v molekulách reagujících látek dochází k zániku některých vazeb a ke vzniku vazeb nových. Produkty rekce mají jiné chemické
Na www.studijni-svet.cz zaslal(a): Kikusska94 5. CHEMICKÉ REAKCE Je děj při kterém v molekulách reagujících látek dochází k zániku některých vazeb a ke vzniku vazeb nových. Produkty rekce mají jiné chemické
POLYMERY II MECHANISMY VZNIKU VÝROBNÍ POSTUPY
 PLYMERY II MEANISMY VZNIKU VÝRBNÍ PSTUPY čem budeme mluvit Typy polymeračních reakcí mechanismy Základní způsoby výroby polymerů PLYMERAČNÍ REAKE ADIČNÍ KNDENZAČNÍ ŘETĚZVÉ PSTUPNÉ KRDINAČNÍ (ZIEGLER-NATTA)
PLYMERY II MEANISMY VZNIKU VÝRBNÍ PSTUPY čem budeme mluvit Typy polymeračních reakcí mechanismy Základní způsoby výroby polymerů PLYMERAČNÍ REAKE ADIČNÍ KNDENZAČNÍ ŘETĚZVÉ PSTUPNÉ KRDINAČNÍ (ZIEGLER-NATTA)
Vytvrzování reaktoplastů pomocí UV záření. Bc. Petr Minář
 Vytvrzování reaktoplastů pomocí UV záření Bc. Petr Minář Diplomová práce 2013 Příjmení a jméno: Minář Petr Obor: Inženýrství polymerů P R O H L Á Š E N Í Prohlašuji, že beru na vědomí, že odevzdáním
Vytvrzování reaktoplastů pomocí UV záření Bc. Petr Minář Diplomová práce 2013 Příjmení a jméno: Minář Petr Obor: Inženýrství polymerů P R O H L Á Š E N Í Prohlašuji, že beru na vědomí, že odevzdáním
12. Elektrochemie základní pojmy
 Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
2.3 CHEMICKÁ VAZBA. Molekula bílého fosforu P 4 a kyseliny sírové H 2 SO 4. Předpona piko p je dílčí jednotkou a udává velikost m.
 2.3 CHEMICKÁ VAZBA Spojováním dvou a více atomů vznikají molekuly. Jestliže dochází ke spojování výhradně atomů téhož chemického prvku, pak se jedná o molekuly daného prvku (vodíku H 2, dusíku N 2, ozonu
2.3 CHEMICKÁ VAZBA Spojováním dvou a více atomů vznikají molekuly. Jestliže dochází ke spojování výhradně atomů téhož chemického prvku, pak se jedná o molekuly daného prvku (vodíku H 2, dusíku N 2, ozonu
Klasifikace chem. reakcí
 Chemické reakce Chemické reakce Chemická reakce spočívá ve vzájemné interakci základních stavebních částic výchozích látek (atomů, molekul, iontů), vedoucí ke spojování, oddělování či přeskupování atomových
Chemické reakce Chemické reakce Chemická reakce spočívá ve vzájemné interakci základních stavebních částic výchozích látek (atomů, molekul, iontů), vedoucí ke spojování, oddělování či přeskupování atomových
Plazmové metody. Základní vlastnosti a parametry plazmatu
 Plazmové metody Základní vlastnosti a parametry plazmatu Atom je základní částice běžné hmoty. Částice, kterou již chemickými prostředky dále nelze dělit a která definuje vlastnosti daného chemického prvku.
Plazmové metody Základní vlastnosti a parametry plazmatu Atom je základní částice běžné hmoty. Částice, kterou již chemickými prostředky dále nelze dělit a která definuje vlastnosti daného chemického prvku.
Charakteristika Teorie kyselin a zásad. Příprava kyselin Vlastnosti + typické reakce. Významné kyseliny. Arrheniova teorie Teorie Brönsted-Lowryho
 Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
Aminy a další dusíkaté deriváty
 Aminy a další dusíkaté deriváty Aminy jsou sloučeniny příbuzné amoniaku, u kterých jsou nahrazeny jeden, dva nebo všechny tři atomy vodíku alkylovými nebo arylovými skupinami. Aminy mají stejně jako amoniak,
Aminy a další dusíkaté deriváty Aminy jsou sloučeniny příbuzné amoniaku, u kterých jsou nahrazeny jeden, dva nebo všechny tři atomy vodíku alkylovými nebo arylovými skupinami. Aminy mají stejně jako amoniak,
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 KARBONYLOVÉ SLOUČENINY = látky, které obsahují karbonylovou skupinu Aldehydy mají skupinu C=O na konci řetězce, aldehydická skupina má potom tvar... Názvosloví aldehydů: V systematickém názvu je zakončení
KARBONYLOVÉ SLOUČENINY = látky, které obsahují karbonylovou skupinu Aldehydy mají skupinu C=O na konci řetězce, aldehydická skupina má potom tvar... Názvosloví aldehydů: V systematickém názvu je zakončení
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE doc. Ing. David MILDE, Ph.D. tel.: 585634443 E-mail: david.milde@upol.cz (c) -017 Doporučená literatura Černohorský T., Jandera P.: Atomová spektrometrie. Univerzita Pardubice 1997.
ATOMOVÁ SPEKTROMETRIE doc. Ing. David MILDE, Ph.D. tel.: 585634443 E-mail: david.milde@upol.cz (c) -017 Doporučená literatura Černohorský T., Jandera P.: Atomová spektrometrie. Univerzita Pardubice 1997.
Enzymy charakteristika a katalytický účinek
 Enzymy charakteristika a katalytický účinek Tematická oblast Datum vytvoření Ročník Stručný obsah Způsob využití Autor Kód Chemie přírodních látek enzymy 28.7.2012 3. ročník čtyřletého G Charakteristika
Enzymy charakteristika a katalytický účinek Tematická oblast Datum vytvoření Ročník Stručný obsah Způsob využití Autor Kód Chemie přírodních látek enzymy 28.7.2012 3. ročník čtyřletého G Charakteristika
1. PROCES A PODMÍNKY HOŘENÍ, HOŘLAVÉ LÁTKY
 1. PROCES A PODMÍNKY HOŘENÍ, HOŘLAVÉ LÁTKY V této kapitole se dozvíte: Jak lze definovat hoření? Jak lze vysvětlit proces hoření? Jaké jsou základní podmínky pro hoření? Co jsou hořlavé látky (hořlaviny)
1. PROCES A PODMÍNKY HOŘENÍ, HOŘLAVÉ LÁTKY V této kapitole se dozvíte: Jak lze definovat hoření? Jak lze vysvětlit proces hoření? Jaké jsou základní podmínky pro hoření? Co jsou hořlavé látky (hořlaviny)
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními prin
 Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
o Řetězové polymerizace o Stupňovité polymerizace Základní typy polymerizací
 Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité polymerizace polykondenzace polyadice Stupňovitá
Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité polymerizace polykondenzace polyadice Stupňovitá
Obsah Chemická reakce... 2 PL:
 Obsah Chemická reakce... 2 PL: Vyčíslení chemické rovnice - řešení... 3 Tepelný průběh chemické reakce... 4 Rychlost chemických reakcí... 4 Rozdělení chemických reakcí... 4 1 Chemická reakce děj, při němž
Obsah Chemická reakce... 2 PL: Vyčíslení chemické rovnice - řešení... 3 Tepelný průběh chemické reakce... 4 Rychlost chemických reakcí... 4 Rozdělení chemických reakcí... 4 1 Chemická reakce děj, při němž
Chemická vazba. Příčinou nestability atomů a jejich ochoty tvořit vazbu je jejich elektronový obal.
 Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
ATOMOVÁ SPEKTROMETRIE
 ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
ATOMOVÁ SPEKTROMETRIE Atomová spektrometrie valenčních e - 1. OES (AES). AAS 3. AFS 1 Atomová spektra čárová spektra Tok záření P - množství zářivé energie (Q E ) přenesené od zdroje za jednotku času.
Úvod do koroze. (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají)
 Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Valenční elektrony a chemická vazba
 Valenční elektrony a chemická vazba Ve vnější energetické hladině se nacházejí valenční elektrony, které se mohou podílet na tvorbě chemické vazby. Valenční elektrony často znázorňujeme pomocí teček kolem
Valenční elektrony a chemická vazba Ve vnější energetické hladině se nacházejí valenční elektrony, které se mohou podílet na tvorbě chemické vazby. Valenční elektrony často znázorňujeme pomocí teček kolem
Složení a struktura atomu Charakteristika elementárních částic. Modely atomu. Izotopy a nuklidy. Atomové jádro -
 MATURITNÍ OKRUHY Z CHEMIE Obecná chemie Složení a struktura atomu Charakteristika elementárních částic. Modely atomu. Izotopy a nuklidy. Atomové jádro - hmotnostní úbytek, vazebná energie jádra, jaderné
MATURITNÍ OKRUHY Z CHEMIE Obecná chemie Složení a struktura atomu Charakteristika elementárních částic. Modely atomu. Izotopy a nuklidy. Atomové jádro - hmotnostní úbytek, vazebná energie jádra, jaderné
Průvodka. CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Pořadí DUMu v sadě 07
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Reakční kinetika. Nauka zabývající se rychlostí chemických reakcí a ovlivněním rychlosti těchto reakcí
 Nauka zabývající se rychlostí chemických reakcí a ovlivněním rychlosti těchto reakcí Vymezení pojmů : chemická reakce je děj, při kterém zanikají výchozí látky a vznikají látky nové reakční mechanismus
Nauka zabývající se rychlostí chemických reakcí a ovlivněním rychlosti těchto reakcí Vymezení pojmů : chemická reakce je děj, při kterém zanikají výchozí látky a vznikají látky nové reakční mechanismus
 Chemická vazba Něco málo opakování Něco málo opakování Co je to atom? Něco málo opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího
Chemická vazba Něco málo opakování Něco málo opakování Co je to atom? Něco málo opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího
Dusíkové pravidlo. Počet dusíků m/z lichá m/z sudá 0, 2, 4,... (sudý) EE + OE +.
 Dusíkové pravidlo Základní formulace (platí pro M R a OE +. ): lichá M R = lichý počet dusíků v molekule sudá M R = sudý počet dusíků v molekule nebo nula Pro ionty EE + přesně naopak: lichá hodnota m/z
Dusíkové pravidlo Základní formulace (platí pro M R a OE +. ): lichá M R = lichý počet dusíků v molekule sudá M R = sudý počet dusíků v molekule nebo nula Pro ionty EE + přesně naopak: lichá hodnota m/z
CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT. Protolytické děje VY_32_INOVACE_18_15. Mgr. Věra Grimmerová. grimmerova@gymjev.
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Základní parametry 1 H NMR spekter
 LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
Organické látky. Organická geochemie a rozpuštěný organický uhlík
 Organická geochemie a rozpuštěný organický uhlík struktura, nomenklatura a funkční skupiny huminové látky a další přírodní OC reaktivita DOC/POC distribuce kyselost (acidita) Přírodní a znečišťující organické
Organická geochemie a rozpuštěný organický uhlík struktura, nomenklatura a funkční skupiny huminové látky a další přírodní OC reaktivita DOC/POC distribuce kyselost (acidita) Přírodní a znečišťující organické
Do této skupiny patří dusík, fosfor, arsen, antimon a bismut. Společnou vlastností těchto prvků je pět valenčních elektronů v orbitalech ns a np:
 PRVKY PÁTÉ SKUPINY Do této skupiny patří dusík, fosfor, arsen, antimon a bismut. Společnou vlastností těchto prvků je pět valenčních elektronů v orbitalech ns a np: Obecná konfigurace: ns np Nejvyšší kladné
PRVKY PÁTÉ SKUPINY Do této skupiny patří dusík, fosfor, arsen, antimon a bismut. Společnou vlastností těchto prvků je pět valenčních elektronů v orbitalech ns a np: Obecná konfigurace: ns np Nejvyšší kladné
VLASTNOSTI ALKANŮ 2. RADIKÁLOVÁ SUBSTITUCE 3. ELIMINAČNÍ REAKCE VÝZNAMNÉ ALKANY. Substituční reakce. Sulfochlorace alkanů. Termolýza.
 Kromě CO 2 vznikají i saze roste svítivost Substituční reakce vazby: C C C H jsou nepolární => jsou radikálové S R...radikálová substituce 3 fáze... VLASTNOSTI ALKANŮ tady něco chybí... 2. RADIKÁLOVÁ SUBSTITUCE
Kromě CO 2 vznikají i saze roste svítivost Substituční reakce vazby: C C C H jsou nepolární => jsou radikálové S R...radikálová substituce 3 fáze... VLASTNOSTI ALKANŮ tady něco chybí... 2. RADIKÁLOVÁ SUBSTITUCE
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
Celosvětová produkce plastů
 PRODUKCE PLASTŮ Zpracování plastů cvičení 1 TU v Liberci, FS Celosvětová produkce plastů Mil. tun Asie (bez Japonska) 16 % Střední a západní Evropa 21 % Společenství nezávislých států 3 % 235 mil. tun
PRODUKCE PLASTŮ Zpracování plastů cvičení 1 TU v Liberci, FS Celosvětová produkce plastů Mil. tun Asie (bez Japonska) 16 % Střední a západní Evropa 21 % Společenství nezávislých států 3 % 235 mil. tun
MATURITNÍ OTÁZKY Z CHEMIE
 MATURITNÍ OTÁZKY Z CHEMIE 1 Složení a struktura atomu Vývoj představ o složení a struktuře atomu, elektronový obal atomu, modely atomu, pojem orbital, typy orbitalů, jejich znázorňování a pravidla pro
MATURITNÍ OTÁZKY Z CHEMIE 1 Složení a struktura atomu Vývoj představ o složení a struktuře atomu, elektronový obal atomu, modely atomu, pojem orbital, typy orbitalů, jejich znázorňování a pravidla pro
Příklady k semináři z organické chemie OCH/SOCHA. Doc. RNDr. Jakub Stýskala, Ph.D.
 Příklady k semináři z organické chemie /SA Doc. RNDr. Jakub Stýskala, Ph.D. Příklady k procvičení 1. Které monochlorované deriváty vzniknou při radikálové chloraci následující sloučeniny. Který z nich
Příklady k semináři z organické chemie /SA Doc. RNDr. Jakub Stýskala, Ph.D. Příklady k procvičení 1. Které monochlorované deriváty vzniknou při radikálové chloraci následující sloučeniny. Který z nich
STEJNOSMĚRNÝ PROUD Nesamostatný výboj TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY.
 STEJNOSMĚRNÝ PROUD Nesamostatný výboj TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Plyny jsou tvořeny elektricky neutrálními molekulami. Proto jsou za
STEJNOSMĚRNÝ PROUD Nesamostatný výboj TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Plyny jsou tvořeny elektricky neutrálními molekulami. Proto jsou za
Oxidace a redukce. Hoření = slučování s kyslíkem = oxidace. 2 Mg + O 2 2 MgO S + O 2 SO 2. Redukce = odebrání kyslíku
 Oxidace a redukce Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe + 3 CO CuO + H 2 Cu + H 2 O 1 Oxidace a redukce Širší pojem oxidace
Oxidace a redukce Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe + 3 CO CuO + H 2 Cu + H 2 O 1 Oxidace a redukce Širší pojem oxidace
Průvodka. CZ.1.07/1.5.00/ Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
