STRUKTURA KAPALIN STRUKTURA KAPALIN
|
|
|
- Lukáš Vacek
- před 8 lety
- Počet zobrazení:
Transkript
1 Předmět: Ročník: Vytvořil: Datum: FYZIKA PRVNÍ MGR. JÜTTNEROVÁ Název zpracovaného celku: STRUKTURA KAPALIN STRUKTURA KAPALIN Struktura kapalin, povrchová vrstva kapaliny: Každá molekula kapaliny kmitá kolem své rovnovážné polohy velmi krátkou dobu, potom se přemístí a zaujme novou rovnovážnou polohu. Molekuly kapaliny neustále mění své rovnovážné polohy. Volný povrch kapaliny má podobné vlastnosti jako tenká pružná blána. Vysvětlení: Mezi molekulami jsou velmi malé vzdálenosti molekuly na sebe působí velkými přitažlivými silami. Každá molekula je přitahována jen nejbližšími molekulami ve svém okolí (tzv. sféra molekulového působení). Molekula je uvnitř kapaliny (viz obr. A) silové působení okolních molekul se vyruší. Molekula je v blízkosti povrchu kapaliny (viz obr. případy B a C) v tzv. povrchové vrstvě (vrstvě molekul, jejichž vzdálenost od volného povrchu kapaliny je menší než poloměr sféry molekulového působení) výslednice těchto sil směřuje dovnitř kapaliny a je kolmá k volnému povrchu kapaliny vzniká povrchové napětí a povrch kapaliny se chová jako pružná blána. B C A Zdroj obr: Povrchová vrstva je velmi tenká (tloušťka je řádově 10-7 m) a má jiné vlastnosti než mají vrstvy uvnitř kapaliny. 1
2 Povrchová energie, povrchové napětí, povrchová síla: Přechází-li částice z vnitřku kapaliny do povrchové vrstvy kapaliny, musí vykonat určitou práci molekuly v povrchové vrstvě mají větší potenciální energii než molekuly uvnitř kapaliny. Rozdíl potenciální energie molekul v povrchové vrstvě a potenciální energie, kterou by měly molekuly uvnitř kapaliny, se nazývá povrchová energie. Povrchová síla: má směr tečny k povrchu kapaliny pokus, který ukazuje na existenci povrchové síly: - drátěný rámeček s pohyblivou příčkou dáme do mýdlového roztoku nebo do roztoku jaru a vody - vytvoří se blána - blána se stahuje a táhne příčku silou F, kterou nazýváme povrchová síla Zdroj obr: Povrchové napětí: povrchové napětí je rovno podílu velikosti povrchové síly a délky okraje povrchové blány, na který povrchová síla působí: F σ = l charakterizuje vlastnost povrchové vrstvy kapaliny závisí na druhu kapaliny a na prostředí, které se nachází nad volným povrchem kapaliny závisí na teplotě, s rostoucí teplotou klesá hodnoty povrchového napětí pro některé kapaliny jsou uvedeny v MFCHT N σ = = N m newton na metr m jednotka: [ ] 1 Odkazy na video: 2
3 Úloha 1: a) Proč jsme v předchozím pokusu s rámečkem použili místo čisté vody mýdlovou vodu? b) Proč blána táhne pohyblivou příčku? c) Jakým způsobem můžeme určit experimentálně velikost povrchové síly? Vysvětlete podle obrázku. Zdroj obr: d) Působí povrchová síla i na ostatní části rámečku? e) Ovlivňuje velikost povrchové síly délka příčky? Pokud ano, jak? 3
4 Význam povrchového napětí: umožňuje pohyb drobného hmyzu (vodoměrky) po vodní hladině položíme-li na vodní hladinu například jehlu, žiletku nebo minci, povrch vody se prohne, ale předměty se nepotopí (i když jejich hustota je větší než hustota vody) Zdroje obr: tvar vodních kapek: kapalina nabývá takového tvaru, aby obsah povrchu byl co nejmenší (ze všech těles má při daném objemu nejmenší povrch koule) kapky mají kulový tvar (jejich protáhlý tvar způsobuje tíhová síla) Zdroje obr: využití v domácnosti (mytí, praní): studená voda má vysoké povrchové napětí a přidáním saponátu, prášku na praní nebo mýdla do vody snížíme povrchové napětí vody a nečistota se potom lépe odděluje 4
5 Úloha 2: Vysvětlete, jak se změní povrchová energie a teplota při slévání malých kapiček do jedné velké kapky. Příklad 1: Pohyblivá příčka délky 4 cm na rámečku s mýdlovou blánou ve svislé poloze je v rovnovážném stavu, jestliže je zatížena závažím o hmotnosti 320 mg. Hmotnost příčky zanedbejte. Vypočtěte: a) velikost povrchové síly, která působí na příčku b) povrchové napětí mýdlového roztoku ve vodě ve styku se vzduchem Příklad 2: Určete povrchovou energii volné hladiny vody, která je v nádrži tvaru kvádru. Rozměry dna jsou 4 m a 2,5 m. Voda sahá do výšky 180 cm. Povrchové napětí vody je 0,073 N/m. 5
6 Jevy na rozhraní pevného tělesa a kapaliny: Kapilární tlak Je způsobený pružností povrchové vrstvy. Vzniká pod zakřiveným povrchem kapaliny při stěnách nádoby, u kapek, bublin, v kapilárách. Je kolmý k povrchu kapaliny v každém místě. 2σ Pro kapku a kapiláru: = p k R σ povrchové napětí kapaliny R poloměr kulového povrchu Pro tenkou kulovou bublinu se dvěma povrchy (mýdlová bublina): σ povrchové napětí kapaliny R poloměr bubliny Čím menší je poloměr bubliny, tím větší je kapilární tlak v bublině. p k 4σ = R Odkaz na video: Zakřivení volného povrchu kapaliny Kapalina bývá ve styku se stěnami nádoby. Mohou nastat dva případy. 1) Kapalina smáčí stěny nádoby: Zdroj obr: voda ve skleněné nádobě líh ve skleněné nádobě rtuť v měděné nádobě kapalina vytváří dutý povrch, kapalina u stěny vystupuje výše 6
7 2) Kapalina nesmáčí stěny nádoby: Zdroj obr: rtuť ve skleněné nádobě kapalina vytváří vypuklý povrch Vysvětlení zakřivení povrchu částice kapaliny na sebe působí přitažlivými silami (síly soudržnosti) částice kapaliny a částice stěny nádoby na sebe působí silami (síly přilnavosti) pokud jsou síly soudržnosti malé ve srovnání se silami přilnavosti, povrch kapaliny je dutý (výslednice sil směřuje ven z kapaliny). pokud jsou síly soudržnosti větší než síly přilnavosti, je povrch kapaliny vypuklý (výslednice sil směřuje dovnitř kapaliny). Zakřivení je výrazné v kapilárách (úzké trubice, průměr řádově mm) Odkaz na video: Kapilární jevy Mezi základní kapilární jevy patří kapilární elevace a kapilární deprese. Skleněnou kapiláru (na obou koncích otevřenou) ponoříme svisle do vody v širší nádobě (viz obr.) v kapiláře pozorujeme duté zakřivení povrchu kapaliny v kapiláře je hladina vody výše než hladina vody v nádobě tento jev nazýváme kapilární elevace (vzestup) jev pozorujeme u kapalin, které smáčejí stěny kapiláry čím menší je průměr kapiláry, tím výše kapalina v kapiláře vystoupí Zdroj obr: 7
8 Skleněnou kapiláru (na obou koncích otevřenou) ponoříme svisle do rtuti v širší nádobě (viz obr.) v kapiláře pozorujeme vypuklé zakřivení povrchu kapaliny v kapiláře je hladina rtuti níže než volná hladina rtuti v nádobě tento jev nazýváme kapilární deprese (pokles) jev pozorujeme u kapalin, které nesmáčejí stěny kapiláry Zdroj obr: Výpočet výšky, do níž vystoupí kapalina v kapiláře při kapilární elevaci: hydrostatický tlak odpovídající výšce h je stejný jako kapilární tlak způsobený zakřivením volného povrchu kapaliny v kapiláře R poloměr kapiláry ρ hustota kapaliny 2σ hρg= R 2σ h = ρgr zvýšení volné hladiny v kapiláře je nepřímo-úměrné poloměru kapaliny při určitém poloměru kapiláry je výška tím větší, čím větší je povrchové napětí kapaliny Význam kapilárních jevů v praxi: kapilární elevací se kapalina nasává do knotů v půdě se kapilárami voda dostává z hloubky do horních vrstev půdy, v nichž jsou kořeny rostliny kapilární elevace umožňuje přenášení vody a živin z kořenů rostliny (rostlinné buňky tvoří tenké kapiláry) do nadzemních částí rostliny kapalina kapilárami vzlíná do stěn budov aby voda nevzlínala stěnami, musí se základy budov izolovat abychom zabránili pronikání různých materiálů stěnami, napouštíme je látkami, které ve styku s kapalinou vykazují kapilární depresi (impregnací tkanin zabraňujeme například prosakování vody stěnami stanu, obuvi, sportovního oblečení) 8
9 Změny skupenství látek: Přehled skupenských přeměn ukazuje následující obrázek: Zdroj obr: Tání a tuhnutí Tání: Je přeměna pevné látky v kapalinu. Tání krystalické látky: Při zahřívání krystalické látky (například ledu, kovu) se zvyšuje jejich teplota. Jakmile látka dosáhne teploty tání, změní se na kapalinu téže teploty říkáme, že látka taje. Od tohoto okamžiku se teplota soustavy pevná látka kapalina nemění do té doby, dokud všechna látka neroztaje. Pokud všechna látka roztaje a dále jí dodáváme teplo, začne se teplota vzniklé kapaliny zvyšovat. Teplota, při níž látka taje, se nazývá teplota tání. Různé krystalické látky mají různé teploty tání. Teplota tání závisí na tlaku. V MFCHT jsou uvedeny teploty tání za normálního atmosférického tlaku. Graf závislosti teploty krystalické látky na dodávaném teple Zdroj obr: 9
10 Tání amorfní látky: Amorfní látky (vosk, sklo, plasty) při zahřívání postupně měknou, než se přemění v kapalinu. Tají v určitém rozmezí teplot. Graf závislosti teploty amorfní látky na dodávaném teple: Zdroj obr: Skupenské teplo tání: Je teplo, které musí přijmout pevné těleso zahřáté na teplotu tání, aby se změnilo na kapalinu téže teploty. Pro různé látky je skupenské teplo tání různé. Značka: L t Jednotka: J joule Měrné skupenské teplo tání: Je množství tepla, které musí přijmout 1 kg pevné látky zahřáté na teplotu tání, aby se přeměnila na kapalinu téže teploty. l Lt m t= m hmotnost tělesa 1 Jednotka: J kg joule na kilogram Pro různé látky má různou hodnotu. Měrné skupenské teplo ledu je poměrně velké na jaře taje v přírodě led a sníh pomalu. 10
11 Tání krystalické látky z hlediska molekulové fyziky: Pokud se zvyšuje teplota látky (látka přijímá teplo), roste střední kinetická energie částic částice zvětšují své rozkmity a tím i vzdálenost mezi nimi. Jestliže je látky zahřátá na teplotu tání, rozkmity částic jsou tak velké, že je narušena vazba mezi částicemi částice se uvolňují ze svých rovnovážných poloh a začnou se pohybovat jako v kapalině (mřížka se rozpadá, látka taje). Vazebné síly mezi částicemi jsou v různých látkách různě velké různé látky tají při různých teplotách (za daného vnějšího tlaku). Jestliže látka dosáhne teploty tání a i nadále přijímá teplo, nemění se střední kinetická energie částic, a tím ani teplota látky. Zvětšuje se však střední potenciální energie částic. Pokud všechna látka roztála a dále přijímá teplo, opět se začne zvětšovat střední kinetická energie částic a teplota kapaliny se začne zvyšovat. Tuhnutí (krystalizace): Tuhnutí je přeměna kapaliny v pevnou látku. Tuhnutí probíhá za určité teploty, která se nazývá teplota tuhnutí. Jakmile kapalina dosáhne teploty tuhnutí, začnou se v kapalině vytvářet krystalizační jádra. K nim se připojují a pravidelně uspořádávají další částice látky. Vznikají krystalky, které při ztuhnutí látky vytvářejí zrna. Teplota tuhnutí závisí na tlaku. Skupenské teplo tuhnutí: Je teplo, které musí odevzdat kapalina ochlazená na teplotu tuhnutí svému okolí, aby se přeměnila na krystalickou látku téže teploty. Je teplo, které kapalina ochlazená na teplotu tuhnutí odevzdává svému okolí. Skupenské teplo tuhnutí je stejně velké jako skupenské teplo tání pevného tělesa z téže látky a stejné hmotnosti. Změna objemu tělesa při tání (tuhnutí): Většina látek svůj objem při táni zvětšuje a při tuhnutí zmenšuje. Výjimku tvoří například led, který při tání svůj objem zmenšuje a voda, která při tuhnutí svůj objem zvětšuje. Význam: - led má menší hustotu než voda plave na vodě a zamezuje zamrzání vody do větší hloubky - led způsobuje praskání zdiva a potrubí v zimě v puklinách hornin zmrzlá voda trhá horniny Závislost teploty tání na tlaku: Teplota tání se u většiny látek s rostoucím tlakem zvyšuje. Výjimkou je led s rostoucím tlakem se teplota tání snižuje. 11
12 Regelace ledu (znovuzamrznutí): tímto pokusem můžeme ověřit snížení teploty tání ledu, jestliže dojde ke zvětšení vnějšího tlaku. Zdroj obr: Látky, u nichž se teplota tání s rostoucí tlakem zvyšuje, zvětšují při tání svůj objem. Látky, u nichž se teplota tání s rostoucí tlakem snižuje, zmenšují při tání svůj objem (led). Vypařování, var a kondenzace Vypařování: Je přeměna kapaliny v páru. Kapalina se vypařuje na volném povrchu při jakékoli teplotě. Rychlost vypařování kapaliny závisí na: teplotě kapaliny na ploše povrchu kapaliny na druhu kapaliny odstraňujeme-li vzniklé páry nad kapalinou (foukáním, odsáváním, větrem), vypařování se urychlí Skupenské teplo vypařování: Je teplo, které musí přijmout kapalina zahřátá na teplotu vypařování, aby se přeměnila na páru téže teploty. L Značka: v Jednotka: J joule Měrné skupenské teplo vypařování: Je množství tepla, které musí přijmout 1 kg kapaliny zahřáté na teplotu vypařování, aby se přeměnila na páru téže teploty. l Lv m v= m hmotnost vypařené kapaliny 1 Jednotka: J kg joule na kilogram Klesá s rostoucí teplotou kapaliny. 12
13 Var: Při zahřívání kapaliny se při určité teplotě vytvářejí uvnitř kapaliny bubliny páry. Bubliny zvětšují svůj objem a vystupují k povrchu kapaliny. Jde o vypařování kapaliny nejen na povrchu, ale i uvnitř kapaliny. Teplota, při níž dochází k varu (za daného vnějšího tlaku), se nazývá teplota varu. Teplota varu při daném tlaku závisí na: vnějším tlaku s rostoucí tlakem se zvětšuje druhu kapaliny. Teploty varu některých látek za normálního tlaku jsou uvedeny v MFCHT. Využití varu při vyšším tlaku: tlakový (Papinův) hrnec sterilizace chirurgických nástrojů Využití varu při nižším tlaku: při nižším tlaku je teplota varu nižší výroba sirupů, kondenzovaného mléka, sušeného mléka, sirupů, léků Vypařování z hlediska molekulové fyziky: Při vypařování unikají nejrychlejší molekuly z kapaliny do prostoru nad kapalinou, některé z nich se vrátí do kapaliny (předpokládáme, že je kapalina v uzavřené nádobě a vyplňuje ji jen z části). Po určité době je počet molekul, které opustily kapalinu stejný jako počet molekul, které se do ní vrátily. V otevřené nádobě je počet molekul, které se vracejí do kapaliny, menší. Kapaliny ubývá, páry přibývá. Snižuje se teplota kapaliny, protože ji opouštějí ty nejrychlejší molekuly. SYTÁ PÁRA: vzniká při vypařování do uzavřeného prostoru (v uzavřené nádobě) sytá pára je pára, která je v rovnovážném stavu se svou kapalinou vzduch je nad povrchem vody párou nasycen tlak syté páry nezávisí při stálé teplotě na objemu páry neplatí pro ni stavová rovnice ideálního plynu Zdroj obr: 13
14 PŘEHŘÁTÁ PÁRA: zahříváme-li sytou páru bez přítomnosti kapaliny, vznikne přehřátá pára má nižší tlak a hustotu než sytá pára téže teploty svými vlastnostmi se podobá plynům; platí pro ni přibližně stavová rovnice ideálního plynu má nižší tlak a hustotu než sytá pára téže teploty Kondenzace (kapalnění): Je přeměna páry v kapalinu (snížením teploty nebo objemu). Pára odevzdává do svého okolí skupenské teplo kondenzační. Měrné skupenské teplo kondenzační = měrnému skupenskému teplu vypařování téže látky při stejné teplotě. Molekuly páry se spojují v drobné kapičky, které postupně rostou. V ovzduší kondenzuje vodní pára, přičemž vzniká rosa. Zdroje obr: Sublimace a desublimace: Sublimace: Je přeměna látky z pevného skupenství ve skupenství plynné. Látky, které sublimují za běžného atmosférického tlaku: led, sníh, suchý led (pevný oxid uhličitý), kafr, jod, všechny vonící nebo páchnoucí látky. Měrné skupenské teplo sublimace: Ls ls= m L skupenské teplo sublimace přijaté při sublimaci tělesem o hmotnosti m s 14
15 Desublimace: Je přeměna látky z plynného skupenství ve skupenství pevné. Desublimují jodové páry, přičemž vznikají krystalky jodu; z vodní páry se při teplotách menších než 0 C vytváří jinovatka. Jinovatka Zdroj obr: Látka svému okolí teplo odevzdává. 15
16 PRACOVNÍ LIST 1 ZMĚNY SKUPENSTVÍ Úloha 1: Nádobu s ledem o teplotě 0 C vložíme do vody o teplotě 0 C. Roztaje led? Odpověď zdůvodněte. Úloha 2: Proč taje sníh nejrychleji vlivem deště? Úloha 3: Ve sklenici s vodou je kostka ledu. Změní se výška volné hladiny vody ve sklenici, jestliže všechen led roztaje? Úloha 4: Jak se změní hustota ledu při přechodu z pevného skupenství do kapalného? 16
17 PRACOVNÍ LIST 2 ZMĚNY SKUPENSTVÍ Úloha 5: Vysvětlete, proč ve vysokých horách musíme vařit brambory delší dobu. Úloha 6: Vysvětlete, proč je nám zima, když vylezeme z vody. Proč je nám ještě větší zima, když vylezeme z vody a fouká vítr. Úloha 7: Vysvětlete, proč uschne prádlo rychleji, když fouká vítr. Úloha 8: Led při teplotě vzduchu menší než 0 C netaje, ale přesto ho postupně ubývá. Vysvětlete tento jev. Úloha 9: Vysvětlete princip a využití tlakového hrnce. 17
18 PRACOVNÍ LIST 3 ZMĚNY SKUPENSTVÍ Příklad 1: Určete množství tepla, které musí přijmout těleso z mědi o hmotnosti 500 g a teplotě 20 C, aby se roztavilo. Tepelné ztráty do okolí zanedbejte. Měrná tepelná kapacita mědi je 383 J kg -1 K -1, teplota tání mědi je 1083 C, měrné skupenské teplo tání mědi je J kg -1. Příklad 2: Určete změnu vnitřní energie železného tělesa o hmotnosti 2,3 kg zahřátého na teplotu tání, jestliže se přemění z pevného skupenství v kapalné téže teploty? Měrné skupenské teplo tání železa je 279 kj kg -1. Příklad 3: Určete změnu vnitřní energie roztavené mědi o hmotnosti 5 kg zahřáté na teplotu tání, jestliže se přemění z kapalného skupenství na pevné téže teploty? Měrné skupenské teplo tání mědi je 204 kj kg
19 PRACOVNÍ LIST 4 ZMĚNY SKUPENSTVÍ Příklad 4: Z 200 g vody o teplotě 20 C se mají udělat ledové kostky o teplotě 0 C. Kolik tepla je třeba vodě odebrat? Měrná tepelná kapacita vody je 4200 J kg -1 K -1 a měrné skupenské teplo tání ledu je 334 kj kg -1. Příklad 5: Jakou minimální rychlost musí mít olověná střela, aby se po nárazu na pancéřovou desku zcela roztavila? Předpokládáme, že při nárazu střela neodevzdá žádnou energii okolí. Počáteční teplota střely je 27 C, teplota tání olova je 327 C, měrná tepelná kapacita olova je 129 J kg -1 K -1 a měrné skupenské teplo tání olova je 23 kj kg -1. Příklad 6: Vypočtěte množství tepla, kterého je zapotřebí, aby se led o hmotnosti 1 kg a teplotě - 20 C přeměnil na páru o teplotě 100 C. Měrná tepelná kapacita ledu je 2100 J kg -1 K -1, měrná tepelná kapacita vody je 4200 J kg -1 K -1, měrné skupenské teplo vypařování vody při teplotě 100 C je 2,26 MJ kg -1, měrné skupenské teplo tání ledu je 334 J kg
20 PRACOVNÍ LIST 5 ZMĚNY SKUPENSTVÍ Příklad 7: Vypočtěte množství tepla, které musí přijmout voda o hmotnosti 200 g a teplotě 0 C, zvýší-li se její teplota na 70 C a při této teplotě se všechna přemění v páru téže teploty? Měrná tepelná kapacita vody je 4200 J kg -1 K -1, měrné skupenské teplo vypařování vody při teplotě 70 C je 2,32 MJ kg -1. Předpokládejte tepelně izolovanou nádobu a zanedbejte vypařování vody během zahřívání. Příklad 8: Voda o teplotě 10 C začala vařit na elektrickém vařiči za pět minut. Za jak dlouhou začátku varu se voda úplně vypařila? Měrná tepelná kapacita vody je 4200 J kg -1 K -1 a měrné skupenské teplo vypařování vody při teplotě 100 C je 2,26 MJ kg
21 Vlhkost vzduchu: Udává obsah vodní páry ve vzduchu (v důsledku vypařování vody z moří, řek, jezer, rybníků a vody obsažené v rostlinách, půdě; ze zemského povrchu při vodních srážkách). Absolutní vlhkost vzduchu: m Φ = V m hmotnost vodní páry obsažené ve vzduchu o objemu V kg Φ = 3 m = kg m 3 jednotka: [ ] je rovna hustotě vodní páry, která je obsažena ve vzduchu vodní pára je většinou párou přehřátou hodnoty uvedeny v MFCHT Relativní vlhkost vzduchu: udává, jak se stav vodní páry liší od stavu syté vodní páry Φ ϕ = 100% Φ max podíl absolutní vlhkosti vzduchu a vlhkosti, při níž je vzduch za dané teploty vodní parou nasycen vyjadřuje se v procentech suchý vzduch: ϕ = 0% (neobsahuje vodní páru a je jde o dokonale suchý vzduch) vzduch zcela nasycený vodní párou: ϕ =100% (vzduch je nasycen vodní párou) pro člověka nejvhodnější: ϕ = 50% 70% měří se vlhkoměrem vlasový vlhkoměr - je založen na principu prodlužování lidského vlasu zbaveného tuku se zvyšující se vlhkostí vzduchu Zdroj obr: rosný bod - teplota rosného bodu je teplota, při níž je vzduch vodními parami maximálně nasycen relativní vlhkost vzduchu dosáhne 100 % - pokud teplota klesne pod tento bod, nastává kondenzace - pokud teplota rosného bodu klesne pod 0 C, tvoří se jinovatka 21
22 Seznam použité literatury a internetových zdrojů E. SVOBODA, F. BARTÁK, M. ŠIROKÁ: Fyzika pro technické obory. SPN, O. LEPIL, M. BEDNAŘÍK, R. HÝBLOVÁ R: Fyzika I pro SŠ. Prometheus K. BARTŮŠKA K: Sbírka řešených úloh z fyziky II. Prometheus M. BEDNAŘÍK, E. SVOBODA, V. KUNZOVÁ: Fyzika II pro studijní obory SOU, SPN, 1988 K. LEPIL: Fyzika pro gymnázia Molekulová fyzika a termika. Prometheus
Digitální učební materiál
 Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
Vlastnosti kapalin. Povrchová vrstva kapaliny
 Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
LOGO. Struktura a vlastnosti kapalin
 Struktura a vlastnosti kapalin Povrchová vrstva kapaliny V přírodě velmi často pozorujeme, že se povrch kapaliny, např. vody, chová jako pružná blána, která unese např. hmyz Vysvětlení: Molekuly kapaliny
Struktura a vlastnosti kapalin Povrchová vrstva kapaliny V přírodě velmi často pozorujeme, že se povrch kapaliny, např. vody, chová jako pružná blána, která unese např. hmyz Vysvětlení: Molekuly kapaliny
KAPALINY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník
 KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Kapaliny Krátkodosahové uspořádání molekul. Molekuly kmitají okolo rovnovážných poloh. Při zvýšení teploty se zmenšuje doba setrvání v rovnovážné
KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Termika - 2. ročník Kapaliny Krátkodosahové uspořádání molekul. Molekuly kmitají okolo rovnovážných poloh. Při zvýšení teploty se zmenšuje doba setrvání v rovnovážné
Vnitřní energie pevné látky < Vnitřní energie kapaliny < Vnitřní energie plynu (nejmenší energie)
 Změny skupenství Při změně tělesa z pevné látky na kapalinu nebo z kapaliny na plyn se jeho vnitřní energie zvyšuje musíme dodávat teplo (zahřívat). Při změně tělesa z plynu na kapalinu, nebo z kapaliny
Změny skupenství Při změně tělesa z pevné látky na kapalinu nebo z kapaliny na plyn se jeho vnitřní energie zvyšuje musíme dodávat teplo (zahřívat). Při změně tělesa z plynu na kapalinu, nebo z kapaliny
ZMĚNY SKUPENSTVÍ LÁTEK
 ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
2 Jevy na rozhraní Kapilární tlak Kapilární jevy Objemová roztažnost kapalin 7
 Obsah Obsah 1 Povrchová vrstva 1 2 Jevy na rozhraní 3 2.1 Kapilární tlak........................... 4 2.2 Kapilární jevy........................... 5 3 Objemová roztažnost kapalin 7 1 Povrchová vrstva
Obsah Obsah 1 Povrchová vrstva 1 2 Jevy na rozhraní 3 2.1 Kapilární tlak........................... 4 2.2 Kapilární jevy........................... 5 3 Objemová roztažnost kapalin 7 1 Povrchová vrstva
Struktura a vlastnosti kapalin
 Struktura a vlastnosti kapalin (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Povrchová vrstva Jevy na rozhraní Kapilární tlak Kapilární jevy Objemová roztažnost
Struktura a vlastnosti kapalin (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Povrchová vrstva Jevy na rozhraní Kapilární tlak Kapilární jevy Objemová roztažnost
SKUPENSKÉ PŘEMĚNY POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D11_Z_OPAK_T_Skupenske_premeny_T Člověk a příroda Fyzika Skupenské přeměny Opakování
STRUKTURA A VLASTNOSTI KAPALIN
 STRUKTURA A VLASTNOSTI KAPALIN Struktura kapalin je něco mezi plynem a pevnou látkou Částice kmitají ale mohou se také přemísťovat Zvýšením teploty se a tím se zvýší tekutost kapaliny Malé vzdálenosti
STRUKTURA A VLASTNOSTI KAPALIN Struktura kapalin je něco mezi plynem a pevnou látkou Částice kmitají ale mohou se také přemísťovat Zvýšením teploty se a tím se zvýší tekutost kapaliny Malé vzdálenosti
LOGO. Změny skupenství
 Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
Změny skupenství Látka existuje ve třech skupenstvích Pevném Kapalném Plynném Látka může přecházet z jednoho skupenství do druhého. Existují tedy tyto změny skupenství: Změny skupenství plyn sublimace
F8 - Změny skupenství Číslo variace: 1
 F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
F8 - Změny skupenství Číslo variace: 1 1. K vypařování kapaliny dochází: při každé teplotě v celém jejím objemu pouze při teplotě 100 C v celém objemu kapaliny pouze při normální teplotě a normálním tlaku
F - Změny skupenství látek
 F - Změny skupenství látek Určeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn
F - Změny skupenství látek Určeno jako učební text pro studenty dálkového studia a jako shrnující text pro studenty denního studia. VARIACE 1 Tento dokument byl kompletně vytvořen, sestaven a vytištěn
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny
 Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
DUM č. 12 v sadě. 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia
 projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
projekt GML Brno Docens DUM č. 12 v sadě 10. Fy-1 Učební materiály do fyziky pro 2. ročník gymnázia Autor: Vojtěch Beneš Datum: 03.05.2014 Ročník: 1. ročník Anotace DUMu: Kapaliny, změny skupenství Materiály
(test version, not revised) 24. listopadu 2010
 Změny skupenství (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Tání Tuhnutí Sublimace a desublimace Vypařování a var. Kondenzace Sytá pára Fázový diagram Vodní
Změny skupenství (test version, not revised) Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Tání Tuhnutí Sublimace a desublimace Vypařování a var. Kondenzace Sytá pára Fázový diagram Vodní
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově
 Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_6_ Změny skupenství látek Ing. Jakub Ulmann 6 Změny skupenství látek 6.1 Tání 6.2 Tuhnutí 6.3 Změna
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_6_ Změny skupenství látek Ing. Jakub Ulmann 6 Změny skupenství látek 6.1 Tání 6.2 Tuhnutí 6.3 Změna
KAPALINY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Sekunda
 KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Sekunda Vlastnosti molekul kapalin V neustálém pohybu Ve stejných vzdálenostech, nejsou ale vázány Působí na sebe silami: odpudivé x přitažlivé Vlastnosti kapalin
KAPALINY Mgr. Jan Ptáčník - GJVJ - Fyzika - Sekunda Vlastnosti molekul kapalin V neustálém pohybu Ve stejných vzdálenostech, nejsou ale vázány Působí na sebe silami: odpudivé x přitažlivé Vlastnosti kapalin
Název DUM: Změny skupenství v příkladech
 Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Změny skupenství
Základní škola národního umělce Petra Bezruče, Frýdek-Místek, tř. T. G. Masaryka 454 Zpracováno v rámci OP VK - EU peníze školám Jednička ve vzdělávání CZ.1.07/1.4.00/21.2759 Název DUM: Změny skupenství
VÝUKOVÝ MATERIÁL. 0301 Ing. Yvona Bečičková Tematická oblast. Termika Číslo a název materiálu VY_32_INOVACE_0301_0215 Anotace
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
SKUPENSTVÍ LÁTEK Prima - Fyzika
 SKUPENSTVÍ LÁTEK Prima - Fyzika Skupenství látek Pevné skupenství Skupenství látek Skupenství látek Pevné skupenství Kapalné skupenství Skupenství látek Pevné skupenství Kapalné skupenství Plynné skupenství
SKUPENSTVÍ LÁTEK Prima - Fyzika Skupenství látek Pevné skupenství Skupenství látek Skupenství látek Pevné skupenství Kapalné skupenství Skupenství látek Pevné skupenství Kapalné skupenství Plynné skupenství
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově. 06_5_ Struktura a vlastnosti kapalin
 Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_5_ Struktura a vlastnosti kapalin Ing. Jakub Ulmann 5 Struktura a vlastnosti kapalin 5.1 Povrchové napětí
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 06_5_ Struktura a vlastnosti kapalin Ing. Jakub Ulmann 5 Struktura a vlastnosti kapalin 5.1 Povrchové napětí
JEVY NA ROZHRANÍ PEVNÉHO TĚLESA A KAPALINY
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Dagmar Horká MGV_F_SS_1S3_D17_Z_MOLFYZ_Jevy_na_rozhrani_pevneho_tel esa_a_kapaliny_pl Člověk a příroda Fyzika
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Dagmar Horká MGV_F_SS_1S3_D17_Z_MOLFYZ_Jevy_na_rozhrani_pevneho_tel esa_a_kapaliny_pl Člověk a příroda Fyzika
3.3 Částicová stavba látky
 3.3 Částicová stavba látky Malé (nejmenší) částice látky očekávali nejprve filozofové (atomisté) a nazvali je atomy (z řeckého atomos = nedělitelný) starověké Řecko a Řím. Mnohem později chemici zjistili,
3.3 Částicová stavba látky Malé (nejmenší) částice látky očekávali nejprve filozofové (atomisté) a nazvali je atomy (z řeckého atomos = nedělitelný) starověké Řecko a Řím. Mnohem později chemici zjistili,
TEPELNÉ JEVY. Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie
 TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
TEPELNÉ JEVY Mgr. Jan Ptáčník - GJVJ - Fyzika - Tercie Vnitřní energie tělesa Každé těleso se skládá z látek. Látky se skládají z částic. neustálý neuspořádaný pohyb kinetická energie vzájemné působení
1. Molekulová stavba kapalin
 1 Molekulová stavba kapalin 11 Vznik kapaliny kondenzací Plyn Vyjdeme z plynu Plyn je soustava molekul pohybujících se neuspořádaně všemi směry Pohybová energie molekul převládá nad energii polohovou Každá
1 Molekulová stavba kapalin 11 Vznik kapaliny kondenzací Plyn Vyjdeme z plynu Plyn je soustava molekul pohybujících se neuspořádaně všemi směry Pohybová energie molekul převládá nad energii polohovou Každá
23_ 2 24_ 2 25_ 2 26_ 4 27_ 5 28_ 5 29_ 5 30_ 7 31_
 Obsah 23_ Změny skupenství... 2 24_ Tání... 2 25_ Skupenské teplo tání... 2 26_ Anomálie vody... 4 27_ Vypařování... 5 28_ Var... 5 29_ Kapalnění... 5 30_ Jak určíš skupenství látky?... 7 31_ Tepelné motory:...
Obsah 23_ Změny skupenství... 2 24_ Tání... 2 25_ Skupenské teplo tání... 2 26_ Anomálie vody... 4 27_ Vypařování... 5 28_ Var... 5 29_ Kapalnění... 5 30_ Jak určíš skupenství látky?... 7 31_ Tepelné motory:...
Změna skupenství, Tání a tuhnutí, Sublimace a desublimace Vypařování a kapalnění Sytá pára, Fázový diagram, Vodní pára
 Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
Zěny skupenství átek Zěna skupenství, Tání a tuhnutí, Subiace a desubiace Vypařování a kapanění Sytá pára, Fázový diagra, Vodní pára Zěna skupenství = fyzikání děj, při které se ění skupenství átky Skupenství
1) Skupenství fáze, forma, stav. 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára)
 SKUPENSTVÍ 1) Skupenství fáze, forma, stav 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára) 3) Pevné látky nemění tvar, objem částice blízko sebe, pohybují se kolem urč.
SKUPENSTVÍ 1) Skupenství fáze, forma, stav 2) 3 druhy skupenství (1 látky): pevné (led) kapalné (voda) plynné (vodní pára) 3) Pevné látky nemění tvar, objem částice blízko sebe, pohybují se kolem urč.
VÝUKOVÝ MATERIÁL Ing. Yvona Bečičková Tematická oblast. Termika Číslo a název materiálu VY_32_INOVACE_0301_0220 Anotace
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
Termika. Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději.
 Termika Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději. 1. Vnitřní energie Brownův pohyb a difúze látek prokazují, že částice látek jsou v neustálém neuspořádaném pohybu. Proto mají kinetickou
Termika Nauka o teple se zabývá měřením teploty, tepla a tepelnými ději. 1. Vnitřní energie Brownův pohyb a difúze látek prokazují, že částice látek jsou v neustálém neuspořádaném pohybu. Proto mají kinetickou
Řešení: Fázový diagram vody
 Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
Řešení: 1) Menší hustota ledu v souladu s Archimédovým zákonem zapříčiňuje plování jedu ve vodě. Vodní nádrže a toky tudíž zamrzají shora (od hladiny). Kdyby hustota ledu byla větší než hustota vody, docházelo
ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, BYSTRÉ 9. ROČNÍK. Změny skupenství. Filip Skalský, David Řehůřek
 ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, 569 92 BYSTRÉ 9. ROČNÍK Změny skupenství Filip Skalský, David Řehůřek ŠKOLNÍ ROK 2011/2012 Prohlašujeme, že jsme absolventskou práci vypracovali samostatně
ABSOLVENTSKÁ PRÁCE ZÁKLADNÍ ŠKOLA, ŠKOLNÍ 24, 569 92 BYSTRÉ 9. ROČNÍK Změny skupenství Filip Skalský, David Řehůřek ŠKOLNÍ ROK 2011/2012 Prohlašujeme, že jsme absolventskou práci vypracovali samostatně
Molekulová fyzika a termika
 Molekulová fyzika a termika Fyzika 1. ročník Vzdělávání pro konkurenceschopnost Inovace výuky oboru Informační technologie MěSOŠ Klobouky u Brna Mgr. Petr Kučera 1 Obsah témat v kapitole Molekulová fyzika
Molekulová fyzika a termika Fyzika 1. ročník Vzdělávání pro konkurenceschopnost Inovace výuky oboru Informační technologie MěSOŠ Klobouky u Brna Mgr. Petr Kučera 1 Obsah témat v kapitole Molekulová fyzika
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Kalorimetrická rovnice, skupenské přeměny
 Základní škola Nový Bor, náměstí Míru 128, okres Česká Lípa, příspěvková organizace e mail: info@zsnamesti.cz; www.zsnamesti.cz; telefon: 487 722 010; fax: 487 722 378 Registrační číslo: CZ.1.07/1.4.00/21.3267
Základní škola Nový Bor, náměstí Míru 128, okres Česká Lípa, příspěvková organizace e mail: info@zsnamesti.cz; www.zsnamesti.cz; telefon: 487 722 010; fax: 487 722 378 Registrační číslo: CZ.1.07/1.4.00/21.3267
CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO.
 CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO. 01) Složení látek opakování učiva 6. ročníku: Všechny látky jsou složeny z částic nepatrných rozměrů (tj. atomy, molekuly,
CELKOVÉ OPAKOVÁNÍ UČIVA + ZÁPIS DO ŠKOLNÍHO SEŠITU část 03 VNITŘNÍ ENERGIE, TEPLO. 01) Složení látek opakování učiva 6. ročníku: Všechny látky jsou složeny z částic nepatrných rozměrů (tj. atomy, molekuly,
Měření měrného skupenského tepla tání ledu
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
Laboratorní práce č. 2: Určení povrchového napětí kapaliny
 Přírodní vědy moderně a interaktivně SEMINÁŘ FYZIKY Laboratorní práce č. 2: Určení povrchového napětí kapaliny G Gymnázium Hranice Přírodní vědy moderně a interaktivně SEMINÁŘ FYZIKY G Gymnázium Hranice
Přírodní vědy moderně a interaktivně SEMINÁŘ FYZIKY Laboratorní práce č. 2: Určení povrchového napětí kapaliny G Gymnázium Hranice Přírodní vědy moderně a interaktivně SEMINÁŘ FYZIKY G Gymnázium Hranice
STRUKTURA PEVNÝCH LÁTEK A KAPALIN
 STRUKTURA PEVNÝCH LÁTEK A KAPALIN 18. POVRCHOVÁ VRSTVA KAPALIN, KAPILÁRNÍ ELEVACE, DEPRESE Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. POVRCHOVÉ NAPĚTÍ - Povrchové napětí je efekt, při kterém
STRUKTURA PEVNÝCH LÁTEK A KAPALIN 18. POVRCHOVÁ VRSTVA KAPALIN, KAPILÁRNÍ ELEVACE, DEPRESE Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. POVRCHOVÉ NAPĚTÍ - Povrchové napětí je efekt, při kterém
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů
 ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Číslo materiálu Mgr. Vladimír Hradecký 8_F_1_13 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Číslo materiálu Mgr. Vladimír Hradecký 8_F_1_13 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH
 SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
VI. STRUKTRURA A VLASTNOSTI KAPALIN
 VI. STRUKTRURA A VLASTNOSTI KAPALIN KAPALINY z molekul konajících tepelný pohyb (potvrzuje difúze, Brownův pohyb) molekuly kmitají (f~10 12 Hz) kolem rovnovážných poloh, které se po velmi krátké době (~
VI. STRUKTRURA A VLASTNOSTI KAPALIN KAPALINY z molekul konajících tepelný pohyb (potvrzuje difúze, Brownův pohyb) molekuly kmitají (f~10 12 Hz) kolem rovnovážných poloh, které se po velmi krátké době (~
UČIVO. Termodynamická teplota. První termodynamický zákon Přenos vnitřní energie
 PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
3.2 Látka a její skupenství
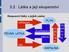 3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
4. Kolmou tlakovou sílu působící v kapalině na libovolně orientovanou plochu S vyjádříme jako
 1. Pojem tekutiny je A) synonymem pojmu kapaliny B) pojmem označujícím souhrnně kapaliny a plyny C) synonymem pojmu plyny D) označením kapalin se zanedbatelnou viskozitou 2. Příčinou rozdílné tekutosti
1. Pojem tekutiny je A) synonymem pojmu kapaliny B) pojmem označujícím souhrnně kapaliny a plyny C) synonymem pojmu plyny D) označením kapalin se zanedbatelnou viskozitou 2. Příčinou rozdílné tekutosti
Termodynamika 2. UJOP Hostivař 2014
 Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
Termodynamika 2 UJOP Hostivař 2014 Skupenské teplo tání/tuhnutí je (celkové) teplo, které přijme pevná látka při přechodu na kapalinu během tání nebo naopak Značka Veličina Lt J Nedochází při něm ke změně
FYZIKA 2. ROČNÍK. Změny skupenství látek. Tání a tuhnutí. Pevná látka. soustava velkého počtu částic. Plyn
 Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
Zěny skuenství látek Pevná látka Kaalina Plyn soustava velkého očtu částic Má-li soustava v rovnovážné stavu ve všech částech stejné fyzikální a cheické vlastnosti (stejnou hustotu, stejnou strukturu a
34_Mechanické vlastnosti kapalin... 2 Pascalův zákon _Tlak - příklady _Hydraulické stroje _PL: Hydraulické stroje - řešení...
 34_Mechanické vlastnosti kapalin... 2 Pascalův zákon... 2 35_Tlak - příklady... 2 36_Hydraulické stroje... 3 37_PL: Hydraulické stroje - řešení... 4 38_Účinky gravitační síly Země na kapalinu... 6 Hydrostatická
34_Mechanické vlastnosti kapalin... 2 Pascalův zákon... 2 35_Tlak - příklady... 2 36_Hydraulické stroje... 3 37_PL: Hydraulické stroje - řešení... 4 38_Účinky gravitační síly Země na kapalinu... 6 Hydrostatická
Vnitřní energie, práce a teplo
 Vnitřní energie, práce a teplo Míček upustíme z výšky na podlahu o Míček padá zvětšuje se, zmenšuje se. Celková mechanická energie se - o Míček se od země odrazí a stoupá vzhůru zvětšuje se, zmenšuje se.
Vnitřní energie, práce a teplo Míček upustíme z výšky na podlahu o Míček padá zvětšuje se, zmenšuje se. Celková mechanická energie se - o Míček se od země odrazí a stoupá vzhůru zvětšuje se, zmenšuje se.
Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
ÚVODNÍ POJMY, VNITŘNÍ ENERGIE, PRÁCE A TEPLO POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D08_Z_OPAK_T_Uvodni_pojmy_vnitrni_energie _prace_teplo_t Člověk a příroda Fyzika
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D08_Z_OPAK_T_Uvodni_pojmy_vnitrni_energie _prace_teplo_t Člověk a příroda Fyzika
VÝUKOVÝ MATERIÁL. 0301 Ing. Yvona Bečičková Tematická oblast. Termika Číslo a název materiálu VY_32_INOVACE_0301_0214 Anotace
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
POZNÁMKA: V USA se používá ještě Fahrenheitova teplotní stupnice. Převodní vztahy jsou vzhledem k volbě základních bodů složitější: 9 5
 TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
TEPLO, TEPLOTA Tepelný stav látek je charakterizován veličinou termodynamická teplota T Jednotkou je kelvin T K Mezi Celsiovou a Kelvinovou teplotní stupnicí existuje převodní vztah T 73,5C t POZNÁMKA:
Molekulová fyzika a termika:
 Molekulová fyzika a termika: 1. Měření teploty: 2. Délková roztažnost a Objemová roztažnost látek 3. Bimetal 4. Anomálie vody 5. Částicová stavba látek, vlastnosti látek 6. Atomová hmotnostní konstanta
Molekulová fyzika a termika: 1. Měření teploty: 2. Délková roztažnost a Objemová roztažnost látek 3. Bimetal 4. Anomálie vody 5. Částicová stavba látek, vlastnosti látek 6. Atomová hmotnostní konstanta
Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha
 Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha Názvosloví páry Pro správné pochopení funkce parních systémů musíme znát základní pojmy spojené s párou. Entalpie Celková energie, příslušná danému
Názvosloví Kvalita Výroba Kondenzace Teplosměnná plocha Názvosloví páry Pro správné pochopení funkce parních systémů musíme znát základní pojmy spojené s párou. Entalpie Celková energie, příslušná danému
Mezi krystalické látky nepatří: a) asfalt b) křemík c) pryskyřice d) polvinylchlorid
 Mezi krystalické látky nepatří: a) asfalt b) křemík c) pryskyřice d) polvinylchlorid Mezi krystalické látky patří: a) grafit b) diamant c) jantar d) modrá skalice Mezi krystalické látky patří: a) rubín
Mezi krystalické látky nepatří: a) asfalt b) křemík c) pryskyřice d) polvinylchlorid Mezi krystalické látky patří: a) grafit b) diamant c) jantar d) modrá skalice Mezi krystalické látky patří: a) rubín
STRUKTURA PEVNÝCH LÁTEK A KAPALIN
 STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
STRUKTURA PEVNÝCH LÁTEK A KAPALIN 19. ZMĚNY SKUPENSTVÍ, FÁZOVÝ DIAGRAM Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. SKUPENSTVÍ - Skupenství neboli stav je konkrétní forma látky, charakterizovaná
Molekulová fyzika a termika. Přehled základních pojmů
 Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
LOGO. Molekulová fyzika
 Molekulová fyzika Molekulová fyzika Molekulová fyzika vysvětluje fyzikální jevy na základě znalosti jejich částicové struktury. Jejím základem je kinetická teorie látek (KTL). KTL obsahuje tři tvrzení:
Molekulová fyzika Molekulová fyzika Molekulová fyzika vysvětluje fyzikální jevy na základě znalosti jejich částicové struktury. Jejím základem je kinetická teorie látek (KTL). KTL obsahuje tři tvrzení:
Struktura a vlastnosti kapalin
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 7 Struktura a vlastnosti kapalin
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 7 Struktura a vlastnosti kapalin
Fyzika - Sexta, 2. ročník
 - Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
- Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
7. MECHANIKA TEKUTIN - statika
 7. - statika 7.1. Základní vlastnosti tekutin Obecným pojem tekutiny jsou myšleny. a. Mají společné vlastnosti tekutost, částice jsou od sebe snadno oddělitelné, nemají vlastní stálý tvar apod. Reálné
7. - statika 7.1. Základní vlastnosti tekutin Obecným pojem tekutiny jsou myšleny. a. Mají společné vlastnosti tekutost, částice jsou od sebe snadno oddělitelné, nemají vlastní stálý tvar apod. Reálné
6. Jaký je výkon vařiče, který ohřeje 1 l vody o 40 C během 5 minut? Měrná tepelná kapacita vody je W)
 TEPLO 1. Na udržení stále teploty v místnosti se za hodinu spotřebuje 4,2 10 6 J tepla. olik vody proteče radiátorem ústředního topení za hodinu, jestliže má voda při vstupu do radiátoru teplotu 80 ºC
TEPLO 1. Na udržení stále teploty v místnosti se za hodinu spotřebuje 4,2 10 6 J tepla. olik vody proteče radiátorem ústředního topení za hodinu, jestliže má voda při vstupu do radiátoru teplotu 80 ºC
V izolované soustavě nedochází k výměně tepla s okolím. Dokonalá izolovaná soustava neexistuje, nejvíce se jí blíží kalorimetr nebo termoska.
 Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
Přehled otázek z fyziky pro 2.ročník
 Přehled otázek z fyziky pro 2.ročník 1. Z jakých základních poznatků vychází teorie látek + důkazy. a) Látka kteréhokoli skupenství se skládá z částic molekul, atomů, iontů. b) Částice se v látce pohybují,
Přehled otázek z fyziky pro 2.ročník 1. Z jakých základních poznatků vychází teorie látek + důkazy. a) Látka kteréhokoli skupenství se skládá z částic molekul, atomů, iontů. b) Částice se v látce pohybují,
V izolované soustavě nedochází k výměně tepla s okolím. Dokonalá izolovaná soustava neexistuje, nejvíce se jí blíží kalorimetr nebo termoska.
 Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
Teplo a vnitřní energie pracovní list Vnitřní energie Všechny tělesa se skládají z částic, které vykonávají neustálý a neuspořádaný pohyb a které na sebe navzájem silově působí. Částice uvnitř všech těles
Připravil: Roman Pavlačka, Markéta Sekaninová Hydrostatika
 Připravil: Roman Pavlačka, Markéta Sekaninová Hydrostatika OPVK CZ.1.07/2.2.00/28.0220, "Inovace studijních programů zahradnických oborů s důrazem na jazykové a odborné dovednosti a konkurenceschopnost
Připravil: Roman Pavlačka, Markéta Sekaninová Hydrostatika OPVK CZ.1.07/2.2.00/28.0220, "Inovace studijních programů zahradnických oborů s důrazem na jazykové a odborné dovednosti a konkurenceschopnost
ZMĚNY SKUPENSTVÍ LÁTEK ČÁST 01
 ZMĚNY SKUPENSTVÍ LÁTEK ČÁST 01 A) Výklad: Změny skupenství látky Látka se může vyskytovat ve třech různých skupenstvích PEVNÉM, KAPALNÉM nebo PLYNNÉM. Např. voda (H 2 O)- může se vyskytovat jako krystalický
ZMĚNY SKUPENSTVÍ LÁTEK ČÁST 01 A) Výklad: Změny skupenství látky Látka se může vyskytovat ve třech různých skupenstvích PEVNÉM, KAPALNÉM nebo PLYNNÉM. Např. voda (H 2 O)- může se vyskytovat jako krystalický
4IS09F8 změna skupenství.notebook. Registrační číslo projektu: CZ.1.07/1.4.00/21.3075. Šablona: III/2. Sada: VY_32_INOVACE_4IS Pořadové číslo: 09
 Registrační číslo projektu: CZ.1.07/1.4.00/21.3075 Šablona: III/2 Sada: VY_32_INOVACE_4IS Pořadové číslo: 09 Ověření ve výuce Třída: 8.A Datum: 20.2.2013 1 Změna skupenství Předmět: Fyzika Ročník: 8. ročník
Registrační číslo projektu: CZ.1.07/1.4.00/21.3075 Šablona: III/2 Sada: VY_32_INOVACE_4IS Pořadové číslo: 09 Ověření ve výuce Třída: 8.A Datum: 20.2.2013 1 Změna skupenství Předmět: Fyzika Ročník: 8. ročník
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Energie. Název sady DUM. Člověk a příroda. Vzdělávací oblast. Fyzika. Autor, datum vytvoření Mgr. Zbyněk Šostý, 2012. interaktivní tabule
 Název DUM: Skupenství látek Název sady DUM Číslo DUM Vzdělávací oblast Vzdělávací obor Energie VY_32_INOVACE_14_S1 12 Člověk a příroda Fyzika Ročník 8. Autor, datum vytvoření Mgr. Zbyněk Šostý, 2012 Doporučená
Název DUM: Skupenství látek Název sady DUM Číslo DUM Vzdělávací oblast Vzdělávací obor Energie VY_32_INOVACE_14_S1 12 Člověk a příroda Fyzika Ročník 8. Autor, datum vytvoření Mgr. Zbyněk Šostý, 2012 Doporučená
Látkové množství n poznámky 6.A GVN
 Látkové množství n poznámky 6.A GVN 10. září 2007 charakterizuje látky z hlediska počtu částic (molekul, atomů, iontů), které tato látka obsahuje je-li v tělese z homogenní látky N částic, pak látkové
Látkové množství n poznámky 6.A GVN 10. září 2007 charakterizuje látky z hlediska počtu částic (molekul, atomů, iontů), které tato látka obsahuje je-li v tělese z homogenní látky N částic, pak látkové
Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika v učebně fyziky, interaktivní tabule
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Vnitřní energie, práce a teplo
 Vnitřní energie, práce a teplo Zákon zachování mechanické energie V izolované soustavě těles je v každém okamžiku úhrnná mechanická energie stálá. Mění se navzájem jen potenciální energie E p a kinetická
Vnitřní energie, práce a teplo Zákon zachování mechanické energie V izolované soustavě těles je v každém okamžiku úhrnná mechanická energie stálá. Mění se navzájem jen potenciální energie E p a kinetická
Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika v učebně fyziky, interaktivní tabule a i-učebnice
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Na libovolnou plochu o obsahu S v atmosférickém vzduchu působí kolmo tlaková síla, kterou vypočítáme ze vztahu: F = pa. S
 MECHANICKÉ VLASTNOSTI PLYNŮ. Co už víme o plynech? Vlastnosti ply nů: 1) jsou snadno stlačitelné a rozpínavé 2) nemají vlastní tvar ani vlastní objem 3) jsou tekuté 4) jsou složeny z částic, které se neustále
MECHANICKÉ VLASTNOSTI PLYNŮ. Co už víme o plynech? Vlastnosti ply nů: 1) jsou snadno stlačitelné a rozpínavé 2) nemají vlastní tvar ani vlastní objem 3) jsou tekuté 4) jsou složeny z částic, které se neustále
13 otázek za 1 bod = 13 bodů Jméno a příjmení:
 13 otázek za 1 bod = 13 bodů Jméno a příjmení: 4 otázky za 2 body = 8 bodů Datum: 1 příklad za 3 body = 3 body Body: 1 příklad za 6 bodů = 6 bodů Celkem: 30 bodů příklady: 1) Sportovní vůz je schopný zrychlit
13 otázek za 1 bod = 13 bodů Jméno a příjmení: 4 otázky za 2 body = 8 bodů Datum: 1 příklad za 3 body = 3 body Body: 1 příklad za 6 bodů = 6 bodů Celkem: 30 bodů příklady: 1) Sportovní vůz je schopný zrychlit
Ch - Rozlišování látek
 Ch - Rozlišování látek Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl kompletně
Ch - Rozlišování látek Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl kompletně
Vnitřní energie. Teplo. Tepelná výměna.
 Vnitřní energie. Teplo. Tepelná výměna. A) Výklad: Vnitřní energie vnitřní energie označuje součet celkové kinetické energie částic (tj. rotační + vibrační + translační energie) a celkové polohové energie
Vnitřní energie. Teplo. Tepelná výměna. A) Výklad: Vnitřní energie vnitřní energie označuje součet celkové kinetické energie částic (tj. rotační + vibrační + translační energie) a celkové polohové energie
Pracovní list číslo 01
 Pracovní list číslo 01 Měření délky Jak se nazývá základní jednotka délky? Jaká délková měřidla používáme k měření rozměrů a) knihy b) okenní tabule c) třídy.. d) obvodu svého pasu.. Jaké díly a násobky
Pracovní list číslo 01 Měření délky Jak se nazývá základní jednotka délky? Jaká délková měřidla používáme k měření rozměrů a) knihy b) okenní tabule c) třídy.. d) obvodu svého pasu.. Jaké díly a násobky
Doprovodné otázky pro studenty, kvízy, úkoly aj.
 Doprovodné otázky pro studenty, kvízy, úkoly aj. Otázky: 1. Jak se projeví menší hustota ledu v porovnání s vodou při zamrzání vodních nádrží a toků? 2. Jaký jev se nazývá anomálie vody? 3. Vysvětlete
Doprovodné otázky pro studenty, kvízy, úkoly aj. Otázky: 1. Jak se projeví menší hustota ledu v porovnání s vodou při zamrzání vodních nádrží a toků? 2. Jaký jev se nazývá anomálie vody? 3. Vysvětlete
VÝUKOVÝ MATERIÁL. 0301 Ing. Yvona Bečičková Tematická oblast
 VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
VÝUKOVÝ MATERIÁL Identifikační údaje školy Vyšší odborná škola a Střední škola, Varnsdorf, příspěvková organizace Bratislavská 2166, 407 47 Varnsdorf, IČO: 18383874 www.vosassvdf.cz, tel. +420412372632
5.7 Vlhkost vzduchu 5.7.5 Absolutní vlhkost 5.7.6 Poměrná vlhkost 5.7.7 Rosný bod 5.7.8 Složení vzduchu 5.7.9 Měření vlhkosti vzduchu
 Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
STRUKTURA A VLASTNOSTI PLYNŮ POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D09_Z_OPAK_T_Plyny_T Člověk a příroda Fyzika Struktura a vlastnosti plynů Opakování
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D09_Z_OPAK_T_Plyny_T Člověk a příroda Fyzika Struktura a vlastnosti plynů Opakování
MOLEKULOVÁ FYZIKA KAPALIN
 MOLEKULOVÁ FYZIKA KAPALIN Struktura kapalin Povrchová vrstva kapaliny Povrchová energie, povrchová síla, povrchové napětí Kapilární tlak Kapilarita Prof. RNDr. Emanuel Svoboda, CSc. STRUKTURA KAPALIN Tvoří
MOLEKULOVÁ FYZIKA KAPALIN Struktura kapalin Povrchová vrstva kapaliny Povrchová energie, povrchová síla, povrchové napětí Kapilární tlak Kapilarita Prof. RNDr. Emanuel Svoboda, CSc. STRUKTURA KAPALIN Tvoří
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA
 MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
Měření teplotní roztažnosti
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření teplotní roztažnosti Úvod Zvyšování termodynamické teploty
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření teplotní roztažnosti Úvod Zvyšování termodynamické teploty
Mechanické vlastnosti kapalin a plynů. opakování
 Mechanické vlastnosti kapalin a plynů opakování 1 Jakým směrem se šíří tlak? 2 Chlapci si zhotovili model hydraulického lisu podle obrázku. Na písty ručních stříkaček působí stejnou silou. Který chlapec
Mechanické vlastnosti kapalin a plynů opakování 1 Jakým směrem se šíří tlak? 2 Chlapci si zhotovili model hydraulického lisu podle obrázku. Na písty ručních stříkaček působí stejnou silou. Který chlapec
Mechanika plynů. Vlastnosti plynů. Atmosféra Země. Atmosférický tlak. Měření tlaku
 Mechanika plynů Vlastnosti plynů Molekuly plynu jsou v neustálém pohybu, pronikají do všech míst nádoby plyn je rozpínavý. Vzdálenosti mezi molekulami jsou větší než např. v kapalině. Zvýšením tlaku je
Mechanika plynů Vlastnosti plynů Molekuly plynu jsou v neustálém pohybu, pronikají do všech míst nádoby plyn je rozpínavý. Vzdálenosti mezi molekulami jsou větší než např. v kapalině. Zvýšením tlaku je
MECHANIKA KAPALIN A PLYNŮ. Mgr. Jan Ptáčník - GJVJ - Fyzika - Mechanika - 1. ročník
 MECHANIKA KAPALIN A PLYNŮ Mgr. Jan Ptáčník - GJVJ - Fyzika - Mechanika - 1. ročník Mechanika kapalin a plynů Hydrostatika - studuje podmínky rovnováhy kapalin. Aerostatika - studuje podmínky rovnováhy
MECHANIKA KAPALIN A PLYNŮ Mgr. Jan Ptáčník - GJVJ - Fyzika - Mechanika - 1. ročník Mechanika kapalin a plynů Hydrostatika - studuje podmínky rovnováhy kapalin. Aerostatika - studuje podmínky rovnováhy
Mechanika kapalin a plynů
 Mechanika kapalin a plynů Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Tekutiny Tlak Tlak v kapalině vyvolaný vnější silou Tlak v kapalině vyvolaný tíhovou silou Tlak v kapalině vyvolaný
Mechanika kapalin a plynů Petr Pošta pposta@karlin.mff.cuni.cz 24. listopadu 2010 Obsah Tekutiny Tlak Tlak v kapalině vyvolaný vnější silou Tlak v kapalině vyvolaný tíhovou silou Tlak v kapalině vyvolaný
Mechanika tekutin. Tekutiny = plyny a kapaliny
 Mechanika tekutin Tekutiny = plyny a kapaliny Vlastnosti kapalin Kapaliny mění tvar, ale zachovávají objem jsou velmi málo stlačitelné Ideální kapalina: bez vnitřního tření je zcela nestlačitelná Viskozita
Mechanika tekutin Tekutiny = plyny a kapaliny Vlastnosti kapalin Kapaliny mění tvar, ale zachovávají objem jsou velmi málo stlačitelné Ideální kapalina: bez vnitřního tření je zcela nestlačitelná Viskozita
III. STRUKTURA A VLASTNOSTI PLYNŮ
 III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
III. STRUKTURA A VLASTNOSTI PLYNŮ 3.1 Ideální plyn a) ideální plyn model, předpoklady: 1. rozměry molekul malé (ve srovnání se střední vzdáleností molekul). molekuly na sebe navzálem silově nepůsobí (mimo
Základní poznatky. Teplota Vnitřní energie soustavy Teplo
 Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
VNITŘNÍ ENERGIE. Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika
 VNITŘNÍ ENERGIE Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika Zákon zachování energie Ze zákona zachování mechanické energie platí: Ek + Ep = konst. Ale: Vnitřní energie tělesa Každé těleso má
VNITŘNÍ ENERGIE Mgr. Jan Ptáčník - GJVJ - Fyzika - 2. ročník - Termika Zákon zachování energie Ze zákona zachování mechanické energie platí: Ek + Ep = konst. Ale: Vnitřní energie tělesa Každé těleso má
Měření povrchového napětí
 Měření povrchového napětí Úkol : 1. Změřte pomocí kapilární elevace povrchové napětí daných kapalin při dané teplotě. 2. Změřte pomocí kapkové metody povrchové napětí daných kapalin při dané teplotě. Pomůcky
Měření povrchového napětí Úkol : 1. Změřte pomocí kapilární elevace povrchové napětí daných kapalin při dané teplotě. 2. Změřte pomocí kapkové metody povrchové napětí daných kapalin při dané teplotě. Pomůcky
Pracovní list č. 3 téma: Povětrnostní a klimatičtí činitelé část 2
 Pracovní list č. 3 téma: Povětrnostní a klimatičtí činitelé část 2 Obsah tématu: 1) Vzdušný obal země 2) Složení vzduchu 3) Tlak vzduchu 4) Vítr 5) Voda 1) VZDUŠNÝ OBAL ZEMĚ Vzdušný obal Země.. je směs
Pracovní list č. 3 téma: Povětrnostní a klimatičtí činitelé část 2 Obsah tématu: 1) Vzdušný obal země 2) Složení vzduchu 3) Tlak vzduchu 4) Vítr 5) Voda 1) VZDUŠNÝ OBAL ZEMĚ Vzdušný obal Země.. je směs
