PÍLOHA I SOUHRN ÚDAJ O PÍPRAVKU
|
|
|
- Břetislav Bezucha
- před 8 lety
- Počet zobrazení:
Transkript
1 PÍLOHA I SOUHRN ÚDAJ O PÍPRAVKU 1
2 1. NÁZEV PÍPRAVKU Rotarix, prášek pro pípravu perorální suspenze s rozpouštdlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po rekonstituci obsahuje: Rotavirus RIX4414 humanum vivum attenuatum* ne mén než 10 6,0 CCID 50 *Pomnožený na Vero bukách Úplný seznam pomocných látek viz bod LÉKOVÁ FORMA Prášek pro pípravu perorální suspenze s rozpouštdlem. Prášek je bílý. Rozpouštdlo je zakalená tekutina s pomalu se usazujícím bílým sedimentem a bezbarvým supernatantem. 4. KLINICKÉ ÚDAJE 4.1 Terapeutické indikace Rotarix je uren k aktivní imunizaci dtí od 6 týdn vku za úelem prevence gastroenteritidy zpsobené rotavirovou infekcí (viz bod 4.2). V klinických zkouškách byla prokázána úinnost proti gastroenteritid zpsobené rotaviry typu G1P[8], G3P[8] a G9P[8] (viz body 4.4 a 5.1). Rotarix se má podávat podle oficiálních doporuení. 4.2 Dávkování a zpsob podání Dávkování Okovací schéma se skládá ze dvou dávek. První dávka se mže podávat od 6 týdn vku. Interval mezi dávkami by ml být nejmén 4 týdny. Ob dávky okování by se mly aplikovat pokud možno ped dosažením vku 16 týdn, ale okovací schéma musí být dokoneno do 24. týdne vku. V klinických zkouškách bylo vzácn pozorováno vyplivnutí nebo regurgitace vakcíny a v takových pípadech nebyla podána náhradní dávka. Pokud ale dojde k málo pravdpodobnému jevu, že dít vyplivne nebo vyzvrátí vtšinu podané dávky vakcíny, je možné podat pi stejné návštv jednu náhradní dávku. Doporuuje se, aby dti, které dostaly jako první dávku Rotarix, dokonily 2-dávkové schéma vakcínou Rotarix. Nejsou k dispozici žádné údaje o bezpenosti, imunogenicit nebo úinnosti okování, pokud byl Rotarix podán jako první dávka a jako druhá dávka byla podána jiná rotavirová vakcína i naopak. Zpsob podání 2
3 Rotarix je uren pouze k perorálnímu podání. ROTARIX SE ZA ŽÁDNÝCH OKOLNOSTÍ NESMÍ PODAT INJEKN. 4.3 Kontraindikace Hypersensitivita na léivou látku nebo na kteroukoli z pomocných látek. Hypersensitivita po pedchozím podání rotavirových vakcín. Intususcepce v anamnéze. Osoby s vrozenou malformací gastrointestinálního traktu, které by mohly být predisponovány ke vzniku intususcepce. Dti se známým nebo suspektním deficitem imunity. Neoekává se, že asymptomatická HIV infekce ovlivní bezpenost a úinnost Rotarixu. Podávání Rotarixu osobám s asymptomatickou HIV infekcí se však nedoporuuje, protože chybí dostatené množství údaj. Aplikace vakcíny Rotarix musí být odložena u osob trpících akutním vážným horenatým onemocnním. Pítomnost slabé infekce není kontraindikací imunizace. Aplikace vakcíny Rotarix musí být odložena u osob trpících prjmem a zvracením. 4.4 Zvláštní upozornní a opatení pro použití Podle správné klinické praxe by se ped zahájením okování mla sestavit anamnéza okovaného zejména s ohledem na kontraindikace a klinické vyšetení. Vakcína obsahuje jako pomocnou látku 9 mg sacharózy. Toto množství je píliš malé na to, aby zpsobilo nežádoucí úinky u pacient, kteí mají vzácné ddiné problémy s fruktózovou intolerancí, s glukózo-galaktózovou malabsorpcí nebo se sacharázo-isomaltázovou insuficiencí. Nejsou k dispozici údaje o bezpenosti a úinnosti Rotarixu u dtí trpících gastrointestinálními nemocemi nebo poruchou rstu. U takových dtí se má podání Rotarixu s opatrností zvážit, zvlášt pokud, podle názoru lékae, nepodání vakcíny znamená vyšší riziko. Je známo, že po vakcinaci dochází k vyluování viru z vakcíny stolicí, s maximem exkrece okolo 7. dne. ástice virového antigenu detekované testem ELISA byly nalezeny v 50 % stolic odebraných po první dávce a ve 4 % stolic odebraných po druhé dávce. Když byly tyto stolice testovány na pítomnost živého kmene vakcíny, bylo jich pozitivních jen 17 %. Byly pozorovány pípady penosu takto vyloueného viru z vakcíny na séronegativní osoby, které byly v kontaktu s okovanými jedinci, aniž by to vyvolalo njaké klinické symptomy. Rotarix by se ml podávat s opatrností u jedinc, kteí pícházejí do úzkého kontaktu s imunodeficitními osobami, jako jsou napíklad osoby s nádorovým onemocnním nebo jinak imunokomprimované osoby nebo jedinci, kteí dostávají imunosupresivní terapií. Osoby, které jsou v kontaktu s erstv okovanými jedinci, by mly dodržovat osobní hygienu ( nap. mytí rukou po výmn dtských plen). Omezené údaje získané od 140 pedasn narozených dtí naznaují, že Rotarix lze podat nedonošeným dtem, ale pak mže být pozorována nižší imunitní odpov a hladina klinické ochrany není známá. Protektivní imunitní odpovdi nemusí být dosaženo u všech okovaných (viz bod 5.1). 3
4 V klinických zkouškách byla prokázána úinnost proti gastroenteritid zpsobené rotaviry typu G1P[8], G3P[8] a G9P[8]. Dosud nejsou k dispozici dostatené údaje, aby se dalo urit, jestli Rotarix mže chránit proti infekci zpsobené ostatními G typy. Klinické studie, z nichž byly získány údaje o úinnosti, byly provádny ve Finsku a ve Stední a v Jižní Americe (viz bod 5.1). Rotarix nechrání proti gastroenteritid zpsobené jinými patogeny než jsou rotaviry. Data o použití Rotarixu k post-expoziní profylaxi nejsou k dispozici. ROTARIX SE ZA ŽÁDNÝCH OKOLNOSTÍ NESMÍ PODAT INJEKN. 4.5 Interakce s jinými léivými pípravky a jiné formy interakce Rotarix lze podat souasn s kteroukoliv z následujících monovalentních nebo kombinovaných vakcín [vetn hexavalentních vakcín (DTPa-HBV-IPV/Hib)]: vakcína proti difterii, tetanu, pertusi (celobunná) (DTPw), vakcína proti difterii, tetanu, pertusi (acelulární) (DTPa), vakcína proti Haemophilus influenzae typu b (Hib), inaktivovaná vakcína proti poliomyelitid (IPV), vakcína proti hepatitid B (HBV) a pneumokoková vakcína. Klinické studie prokázaly, že imunitní odpovdi a bezpenostní profily podaných vakcín nebyly ovlivnny. Souasné podání Rotarixu a perorální vakcíny proti poliomyelitid (OPV) neovlivuje imunitní odpov na polio antigeny. I když souasné podání OPV mže lehce snížit imunitní odpov na rotavirovou vakcínu, není v souasné dob prokázáno, že by mohla být ovlivnna klinická protekce proti vážné rotavirové gastroenteritid. Imunitní odpov na Rotarix není ovlivnna, pokud se OPV podá 2 týdny od podání Rotarixu. Nejsou žádná omezení týkající se konzumace potravy nebo tekutin, a to ped ani po okování dítte. 4.6 Thotenství a kojení Rotarix není uren k okování dosplých. Lidská data o použití bhem thotenství nebo kojení tudíž nejsou k dispozici a reprodukní studie na zvíatech nebyla provedena. Nejsou k dispozici údaje, které by naznaovaly, že se bhem kojení snižuje ochrana proti rotavirové gastroenteritid vyvolaná Rotarixem. V dob okování je tedy možné pokraovat v kojení. 4.7 Úinky na schopnost ídit a obsluhovat stroje Není relevantní. 4.8 Nežádoucí úinky Celkem v jedenácti placebem kontrolovaných klinických studiích dostalo pibližn dtí zhruba dávek Rotarixu. Ve dvou klinických studiích (Finsko) byt Rotarix podáván samotný (podání bžných dtských vakcín bylo asov upraveno). Výskyt prjmu, zvracení, ztráty chuti k jídlu, horeky a podráždnosti se pi srovnání skupiny dostávající Rotarix a skupiny dostávající placebo nelišil. Po podání druhé dávky nebylo pozorováno zvýšení výskytu nebo závažnosti tchto reakcí. Ve zbývajících devíti studiích (Finsko, eská republika, Kanada, USA, Brazílie, Mexiko, Venezuela, Panama, Kolumbie, Peru, Singapur, Jižní Afrika) byl Rotarix podáván souasn s bžnými dtskými vakcínami (viz bod 4.5). Profil nežádoucích úink pozorovaný u tchto okovaných byl podobný profilu nežádoucích úink pozorovaných u subjekt okovaných stejnými dtskými vakcínami a placebem. 4
5 Výskyt nežádoucích úink byl aktivn monitorován až 14 dní po vakcinaci. Nežádoucí úinky jsou seazeny podle systému orgánové klasifikace a frekvence výskytu. Frekvence jsou hlášeny jako: Velmi asté ( 1/10) asté ( 1/100, < 1/10) Mén asté ( 1/1 000, < 1/100) Vzácné ( 1/10 000, < 1/1 000) Infekní a parazitární onemocnní: Vzácné: infekce horních cest dýchacích. Psychiatrické poruchy: Velmi asté: podráždnost. Mén asté: plá, porucha spánku. Poruchy nervového systému: Mén asté: somnolence. Respiraní, hrudní a mediastinální poruchy: Vzácné: chrapot, vodnatý výtok z nosu. Gastrointestinální poruchy: Velmi asté: nechutenství. asté: prjem, zvracení, flatulence, bolest bicha, regurgitace. Mén asté: zácpa. Poruchy kže a podkoží: Vzácné: dermatitida, vyrážka. Poruchy pohybového systému a pojivové tkán: Vzácné: svalová ke. Celkové a jinde nezaazené poruchy a lokální reakce po podání: asté: horeka, únava. Riziko spojené se vznikem intususcepce bylo hodnoceno v rozsáhlé bezpenostní studii provádné v Latinské Americe a ve Finsku, do níž bylo zahrnuto subjekt. Tato studie poskytla dkaz, že ve skupin dostávající Rotarix nebylo oproti skupin dostávající placebo zvýšené riziko vzniku intususcepce, viz následující tabulka. Intususcepce bhem 31 dní po Rotarix Placebo Relativní riziko (95% IS) podání: N= N= První dávky 1 2 0,50 (0,07;3,80) Druhé dávky 5 5 0,99 (0,31;3,21) IS: interval spolehlivosti 4.9 Pedávkování Nebyl hlášen žádný pípad pedávkování. 5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti 5
6 Farmakoterapeutická skupina: virové vakcíny, ATC kód: J07BH01 Protektivní úinnost Ve Finsku a v Latinské Americe byly provedeny klinické studie, v nichž se hodnotila protektivní úinnost Rotarixu proti jakékoli a proti závažné rotavirové gastroenteritid. Klinická studie provedená ve Finsku hodnotila na pibližn 400 subjektech vakcínu obsahující nižší titr vir (10 5,3 CCID50/dávka) než obsahuje komerní vakcína. Závažnost gastroenteritidy byla definována podle Vesikariho 20 bodové škály, v níž se pi hodnocení plného klinického obrazu rotavirové gastroenteritidy bere v úvahu závažnost a trvání prjmu a zvracení, závažnost horeky a dehydratace stejn jako nutnost léby. Po dvou dávkách Rotarixu byla protektivní úinnost vakcíny proti závážné gastroenteritid (Vesikariho skóre 11) bhem prvního roku života 90% (95% IS: 10,3;99,8) a proti jakékoliv rotavirové gastroenteritid 73% (95% IS: 27,1;90,9). Protektivní úinnost Rotarixu proti závažné respektive jakékoliv gastroenteritid byla ve druhém roce života 83% (95% IS: 7,2;98,4) a 73% (95% IS: 19,9;91,8). Typov specifická úinnost vakcíny pozorovaná proti závážné gastroenteritid (Vesikariho skóre 11) zpsobené G1P[8] byla 87% (95% IS: 24,8;99,7) a proti jakékoliv gastroenteritid zpsobené G1P[8] byla 68% (95% IS: 9,8;89,5). Klinická studie provedená v Latinské Americe hodnotila na více než subjektech vakcínu o komerním složení (titr vir 10 6,5 CCID 50 /dávka). Pozorovaná úinnost vakcíny proti závážné rotavirové gastroenteritid vyžadující hospitalizaci a/nebo rehydrataní terapii v lékaském zaízení byla 84,7% (95% IS: 71,7;92,4). Typov specifická úinnost vakcíny pozorovaná proti vážné gastroenteritid byla 91,8% (95% IS: 74,1;98,4) pro G1P[8], 87,7% (95% IS: 8,3;99,7) pro G3P[8], 90,6% (95% IS: 61,7;98,9) pro G9P[8] a 90,9% (95% IS: 79,2;96,8) pro kmeny s genotypem P8. Spolená analýza výsledk ze tí studií úinnosti* ukázala bod odhadu 67 % (95% IS: 14,8;87,1) pro úinnost proti važné gastroenteritid (Vesikariho skóre 11) zpsobené rotavirem typu G2P[4], což svdí o úinnosti proti tomuto typu. * V tchto studiích byly body odhadu a intervaly spolehlivosti následující: 100 % (95% IS: -1858,0;100), 100 % (95% IS: 21,1;100) a 45,4 % (95% IS: -81,5;86,6). Imunitní odpov Imunologický mechanismus, kterým Rotarix chrání proti rotavirové gastroenteritid není zcela znám. Závislost mezi protilátkovou odpovdí na okování proti rotaviru a ochranou proti rotavirové gastroenteritid nebyla stanovena. V následující tabulce je ukázáno množství subjekt v procentech s titry sérových anti-rotavirových IgA protilátek 20 U/ml (podle ELISA) pozorovanými v rzných studiích po druhé dávce vakcíny nebo placeba. Zem studie Okovací schema Virový titr Vakcína Placebo Finsko 2, 4 msíce CCID50/dávka 83,6 % 1,7 % Finsko 3, 5 msíc CCID50/dávka 94,8 % 3,7 % eská republika 3, 4 msíce CCID50/dávka 84,5 % 2,0 % Latinská Amerika 2, 3 až 4 msíce CCID50/dávka 77,9 % 15,1 % Vakcína obsahující nižší titr vir než má komerní vakcína Komerní vakcína 5.2 Farmakokinetické vlastnosti Vyhodnocování farmakokinetických vlastností není u vakcín požadované. 5.3 Pedklinické údaje vztahující se k bezpenosti 6
7 Neklinické údaje získané na základ konvenních studií toxicity po opakovaném podávání neodhalily žádné zvláštní riziko pro lovka. 6. FARMACEUTICKÉ ÚDAJE 6.1 Seznam pomocných látek Prášek Sacharosa Dextran Sorbitol Aminokyseliny Dulbeccova modifikace Eaglova média (DMEM) Rozpouštdlo Uhliitan vápenatý Xanthanová klovatina Sterilisovaná voda 6.2 Inkompatibility Studie kompatibility nejsou k dispozici, a proto tento léivý pípravek nesmí být mísen s žádnými dalšími léivými pípravky. 6.3 Doba použitelnosti 3 roky. Po rekonstituci: Po rekonstituci by se vakcína obsažená ve stíkace mla okamžit aplikovat. V pípad pechodného uchovávání rekonstituované vakcíny mimo chladniku experimentální údaje prokázaly, že rekonstituovaná vakcína, pokud je uchovávána pi pokojové teplot (18-25 C), je stabilní po dobu 24 hodin. Tyto údaje nejsou doporuením pro uchovávání. Pokud rekonstituovaná vakcína není použita bhem 24 hodin, mla by být znehodnocena. 6.4 Zvláštní opatení pro uchovávání Uchovávejte v chladnice (2 C 8 C). Chrate ped mrazem. Uchovávejte v pvodním obalu, aby byl pípravek chránn ped svtlem. V pípad pechodného uchovávání prášku a rozpouštdla mimo chladniku bylo experimentálními údaji prokázáno, že prášek i rozpouštdlo, pokud jsou uchovávány pi teplotách do 37 C, jsou stabilní po dobu 1 týdne. Tyto údaje nejsou doporuením pro uchovávání. Podmínky uchovávání rekonstituovaného pípravku viz bod Druh obalu a velikost balení 1 dávka prášku v lahvice (sklo typu I) se zátkou (butylpryž). 1 ml rozpouštdla v v pedplnné stíkace (sklo typu I) s pístovou zátkou a ochranným uzávrem (butylpryž). 7
8 Pevodní adaptér na rekonstituci (1 na dávku) v následujících velikostech balení: - balení obsahující 1 lahviku s práškem a 1 pedplnnou stíkaku s rozpouštdlem - balení obsahující 5 lahviek s práškem a 5 pedplnných stíkaek s rozpouštdlem - balení obsahující 10 lahviek s práškem a 10 pedplnných stíkaek s rozpouštdlem - balení obsahující 25 lahviek s práškem a 25 pedplnných stíkaek s rozpouštdlem. Na trhu nemusí být všechny velikosti balení. 6.6 Zvláštní opatení pro likvidaci Ve stíkace obsahující rozpouštdlo lze pi uchovávání pozorovat bílý sediment a irý supernatant. Ped rekonstitucí by mlo být rozpouštdlo ped i po protepání vizuáln zkontrolováno, zda neobsahuje jakékoliv cizorodé ástice a/nebo zda není zmnn fyzikální vzhled. Rekonstituovaná vakcína je trochu více zakalená než rozpouštdlo a má mlén bílý vzhled. Také rekonstituovaná vakcína by mla být ped aplikací vizuáln zkontrolována, zda neobsahuje jakékoliv cizorodé ástice a/nebo zda není zmnn fyzikální vzhled. Pokud jsou pozorovány cizorodé ástice nebo zmna vzhledu, je teba vakcínu vyadit. Všechen nepoužitý pípravek nebo odpad musí být zlikvidován v souladu s místními požadavky. Návod na rekonstituci a aplikaci vakcíny: 1. Odstrate plastový kryt z lahviky obsahující prášek. 2. Nasate pevodní adaptér na lahviku a tlate smrem dol, dokud není pevodní adaptér správn a bezpen pipojen. 3. Stíkaku obsahující rozpouštdlo ádn protepejte. Protepaná suspenze se bude jevit jako zakalená tekutina s pomalu se oddlujícím bílým sedimentem. 4. Odstrate ochranný uzávr ze stíkaky. 5. Nasate stíkaku na pevodní adaptér a siln ji do nho zatlate. 6. Vstíknte plný obsah stíkaky do lahviky obsahující prášek. 7. Lahviku se stále pipojenou stíkakou protepejte a zkontrolujte, zda se prášek úpln rozpustil. Rekonstituovaná vakcína bude vypadat o trochu více zakalená než samotné rozpouštdlo. Tento vzhled je normální. 8. Natáhnte veškerou sms zpt do stíkaky. 9. Odstrate stíkaku od pevodního adaptéru. 10. Tato vakcína je urena pouze k perorálnímu podání. Dít by se mlo usadit do zaklonné polohy. Aplikujte plný obsah stíkaky PERORÁLN (podáním plného obsahu stíkaky na vnitní stranu tváe). Nepodávejte injekn. Pokud se má rekonstituovaná vakcína ped podáním doasn uchovávat, nasate znovu na stíkaku ochranný uzávr. Stíkaka obsahující rekonstituovanou vakcínu se má ped perorálním podáním znovu lehce protepat. Nepodávejte injekn. 8
9 Pevodní adaptér Lahvika Stíkaka Ochranná zátka 1. Odstrate plastový kryt z lahviky obsahující lyofilizovaný prášek. 2. Nasate pevodní adaptér na lahviku a tlate ho smrem dol, dokud adaptér není bezpen napojen na vršek lahviky. 3. Stíkaku obsahující suspenzi ádn protepejte. Protepaná suspenze se bude jevit jako zakalená tekutina s pomalu se oddlujícím bílým sedimentem. 4. Odstrate ze stíkaky ochranný uzávr. 5. Nasate stíkaku na pevodní adaptér a siln ji do nho zatlate. 6.Vstíknte plný obsah stíkaky do lahviky obsahující lyofilizovaný prášek. 7. Lahviku se stále nasazenou stíkakou protepejte a zkontrolujte, zda se prášek úpln rozpustil. Rekonstituovaná vakcína bude mít zakalený vzhled. Tento vzhled je normální. 8. Natáhnte veškerou sms zpt do stíkaky. 9. Odstrate stíkaku od pevodního adaptéru. 10. Plný obsah stíkaky aplikujte peroráln (na vnitní stranu tváe). Dít by se mlo posadit do zaklonné polohy. Nepodávejte injekn. 7. DRŽITEL ROZHODNUTÍ O REGISTRACI GlaxoSmithKline Biologicals s.a. Rue de l'institut 89 B-1330 Rixensart, Belgie 8. REGISTRANÍ ÍSLO(A) 9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE 9
10 10. DATUM REVIZE TEXTU 10
11 PÍLOHA II A. VÝROBCE/VÝROBCI BIOLOGICKÉ LÉIVÉ LÁTKY/LÁTEK A VÝROBCE ODPOVDNÝ/VÝROBCI ODPOVDNÍ ZA PROPOUŠTNÍ ŠARŽÍ B. PODMÍNKY REGISTRACE 11
12 A. VÝROBCE/VÝROBCI BIOLOGICKÉ LÉIVÉ LÁTKY/LÁTEK A VÝROBCE ODPOVDNÝ /VÝROBCI ODPOVDNÍ ZA PROPOUŠTNÍ ŠARŽÍ Název a adresa výrobce/výrobc biologické léivé látky/biologických léivých látek GlaxoSmithKline Biologicals s.a. Rue de l Institut 89, 1330 Rixensart Belgie Název a adresa výrobce odpovdného/výrobc odpovdných za propouštní šarží GlaxoSmithKline Biologicals s.a. Rue de l Institut 89, 1330 Rixensart Belgie B. PODMÍNKY REGISTRACE PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ, KLADENÉ NA DRŽITELE ROZHODNUTÍ O REGISTRACI Výdej léivého pípravku je vázán na lékaský pedpis. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPENÉ A ÚINNÉ POUŽÍVÁNÍ LÉIVÉHO PÍPRAVKU Neuplatuje se. DALŠÍ PODMÍNKY Úední propouštní šarží: podle lánku 114 smrnice 2001/83/ES ve znní pozdjších pedpis bude úední propouštní šarží provádt nkterá státní laborato nebo laborato k tomuto úelu urená. 12
13 PÍLOHA III OZNAENÍ NA OBALU A PÍBALOVÁ INFORMACE 13
14 A. OZNAENÍ NA OBALU 14
15 ÚDAJE UVÁDNÉ NA VNJŠÍM OBALU BALENÍ OBSAHUJÍCÍ 1 LAHVIKU S 1 STÍKAKOU A 1 ADAPTÉREM 1. NÁZEV LÉIVÉHO PÍPRAVKU Rotarix, prášek pro pípravu perorální suspenze s rozpouštdlem Živá rotavirová vakcína 2. OBSAH LÉIVÉ LÁTKY/LÉIVÝCH LÁTEK 1 dávka (1 ml) po rekonstituci obsahuje: Rotavirus RIX4414 humanum vivum attenuatum* ne mén než 10 6,0 CCID 50 *Pomnožený na Vero bukách 3. SEZNAM POMOCNÝCH LÁTEK Prášek: sacharosa, dextran, sorbitol, aminokyseliny, Dulbeccova modifikace Eaglova média (DMEM) Rozpouštdlo: uhliitan vápenatý, xanthanová klovatina, sterilisovaná ištná voda 4. LÉKOVÁ FORMA A VELIKOST BALENÍ Prášek pro pípravu perorální suspenze s rozpouštdlem lahvika: prášek stíkaka: rozpouštdlo pevodní adaptér 1 dávka (1 ml) 5. ZPSOB A CESTA /CESTY PODÁNÍ K perorálnímu podání. Nepodávejte injekn! Ped použitím protepat. Ped použitím si pette píbalovou informaci 6. ZVLÁŠTNÍ UPOZORNNÍ, ŽE LÉIVÝ PÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DTÍ Uchovávejte mimo dosah a dohled dtí. 7. DALŠÍ ZVLÁŠTNÍ UPOZORNNÍ, POKUD JE POTEBNÉ 8. POUŽITELNOST Použitelné do: {MM/YYYY} 15
16 9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ Uchovávejte v chladnice. Chrate ped mrazem. Uchovávejte v pvodním obalu aby byl pípravek chránn ped svtlem. 10. ZVLÁŠTNÍ OPATENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉIVÝCH PÍPRAVK NEBO ODPADU Z TAKOVÝCH LÉIVÝCH PÍPRAVK, POKUD JE TO VHODNÉ Likvidujte v souladu s místními pedpisy. 11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgie 12. REGISTRANÍ ÍSLO/ÍSLA EU/0/00/000/ ÍSLO ŠARŽE.š.: 14. KLASIFIKACE PRO VÝDEJ Výdej léivého pípravku vázán na lékaský pedpis. 15. NÁVOD K POUŽITÍ 16. INFORMACE V BRAILLOV PÍSMU 16
17 ÚDAJE UVÁDNÉ NA VNJŠÍM OBALU BALENÍ OBSAHUJÍCÍ 5 LAHVIEK S 5 STÍKAKAMI A 5 ADAPTÉRY 1. NÁZEV LÉIVÉHO PÍPRAVKU Rotarix, prášek pro pípravu perorální suspenze s rozpouštdlem Živá rotavirová vakcína 2. OBSAH LÉIVÉ LÁTKY/LÉIVÝCH LÁTEK 1 dávka (1 ml) po rekonstituci obsahuje: Rotavirus RIX4414 humanum vivum attenuatum* ne mén než 106,0 CCID50 *Pomnožený na Vero bukách 3. SEZNAM POMOCNÝCH LÁTEK Prášek: sacharosa, dextran, sorbitol, aminokyseliny, Dulbeccova modifikace Eaglova média (DMEM) Rozpouštdlo: uhliitan vápenatý, xanthanová klovatina, sterilisovaná ištná voda 4. LÉKOVÁ FORMA A VELIKOST BALENÍ Prášek pro pípravu perorální suspenze s rozpouštdlem lahvika: prášek stíkaka: rozpouštdlo pevodní adaptér 5 x 1 dávka 1 dávka (1 ml) 5. ZPSOB A CESTA /CESTY PODÁNÍ K perorálnímu podání. Nepodávejte injekn! Ped použitím protepat. Ped použitím si pette píbalovou informaci 6. ZVLÁŠTNÍ UPOZORNNÍ, ŽE LÉIVÝ PÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DTÍ Uchovávejte mimo dosah a dohled dtí. 7. DALŠÍ ZVLÁŠTNÍ UPOZORNNÍ, POKUD JE POTEBNÉ 8. POUŽITELNOST 17
18 Použitelné do: {MM/YYYY} 9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ Uchovávejte v chladnice. Chrate ped mrazem. Uchovávejte v pvodním obalu aby byl pípravek chránn ped svtlem. 10. ZVLÁŠTNÍ OPATENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉIVÝCH PÍPRAVK NEBO ODPADU Z TAKOVÝCH LÉIVÝCH PÍPRAVK, POKUD JE TO VHODNÉ Likvidujte v souladu s místními pedpisy. 11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgie 12. REGISTRANÍ ÍSLO/ÍSLA EU/0/00/000/ ÍSLO ŠARŽE.š.: 14. KLASIFIKACE PRO VÝDEJ Výdej léivého pípravku vázán na lékaský pedpis. 15. NÁVOD K POUŽITÍ 16. INFORMACE V BRAILLOV PÍSMU 18
19 ÚDAJE UVÁDNÉ NA VNJŠÍM OBALU BALENÍ OBSAHUJÍCÍ 10 LAHVIEK S 10 STÍKAKAMI A 10 ADAPTÉRY 1. NÁZEV LÉIVÉHO PÍPRAVKU Rotarix, prášek pro pípravu perorální suspenze s rozpouštdlem Živá rotavirová vakcína 2. OBSAH LÉIVÉ LÁTKY/LÉIVÝCH LÁTEK 1 dávka (1 ml) po rekonstituci obsahuje: Rotavirus RIX4414 humanum vivum attenuatum* ne mén než 106,0 CCID50 *Pomnožený na Vero bukách 3. SEZNAM POMOCNÝCH LÁTEK Prášek: sacharosa, dextran, sorbitol, aminokyseliny, Dulbeccova modifikace Eaglova média (DMEM) Rozpouštdlo: uhliitan vápenatý, xanthanová klovatina, sterilisovaná ištná voda 4. LÉKOVÁ FORMA A VELIKOST BALENÍ Prášek pro pípravu perorální suspenze s rozpouštdlem lahvika: prášek stíkaka: rozpouštdlo pevodní adaptér 10 x 1 dávka 1 dávka (1 ml) 5. ZPSOB A CESTA /CESTY PODÁNÍ K perorálnímu podání. Nepodávejte injekn! Ped použitím protepat. Ped použitím si pette píbalovou informaci 6. ZVLÁŠTNÍ UPOZORNNÍ, ŽE LÉIVÝ PÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DTÍ Uchovávejte mimo dosah a dohled dtí. 7. DALŠÍ ZVLÁŠTNÍ UPOZORNNÍ, POKUD JE POTEBNÉ 8. POUŽITELNOST 19
20 Použitelné do: {MM/YYYY} 9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ Uchovávejte v chladnice. Chrate ped mrazem. Uchovávejte v pvodním obalu aby byl pípravek chránn ped svtlem. 10. ZVLÁŠTNÍ OPATENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉIVÝCH PÍPRAVK NEBO ODPADU Z TAKOVÝCH LÉIVÝCH PÍPRAVK, POKUD JE TO VHODNÉ Likvidujte v souladu s místními pedpisy. 11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgie 12. REGISTRANÍ ÍSLO/ÍSLA EU/0/00/000/ ÍSLO ŠARŽE.š.: 14. KLASIFIKACE PRO VÝDEJ Výdej léivého pípravku vázán na lékaský pedpis. 15. NÁVOD K POUŽITÍ 16. INFORMACE V BRAILLOV PÍSMU 20
21 ÚDAJE UVÁDNÉ NA VNJŠÍM OBALU BALENÍ OBSAHUJÍCÍ 25 LAHVIEK S 25 STÍKAKAMI A 25 ADAPTÉRY 1. NÁZEV LÉIVÉHO PÍPRAVKU Rotarix, prášek pro pípravu perorální suspenze s rozpouštdlem Živá rotavirová vakcína 2. OBSAH LÉIVÉ LÁTKY/LÉIVÝCH LÁTEK 1 dávka (1 ml) po rekonstituci obsahuje: Rotavirus RIX4414 humanum vivum attenuatum* ne mén než 106,0 CCID50 *Pomnožený na Vero bukách 3. SEZNAM POMOCNÝCH LÁTEK Prášek: sacharosa, dextran, sorbitol, aminokyseliny, Dulbeccova modifikace Eaglova média (DMEM) Rozpouštdlo: uhliitan vápenatý, xanthanová klovatina, sterilisovaná ištná voda 4. LÉKOVÁ FORMA A VELIKOST BALENÍ Prášek pro pípravu perorální suspenze s rozpouštdlem lahvika: prášek stíkaka: rozpouštdlo pevodní adaptér 25 x 1 dávka 1 dávka (1 ml) 5. ZPSOB A CESTA /CESTY PODÁNÍ K perorálnímu podání. Nepodávejte injekn! Ped použitím protepat. Ped použitím si pette píbalovou informaci 6. ZVLÁŠTNÍ UPOZORNNÍ, ŽE LÉIVÝ PÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DTÍ Uchovávejte mimo dosah a dohled dtí. 7. DALŠÍ ZVLÁŠTNÍ UPOZORNNÍ, POKUD JE POTEBNÉ 8. POUŽITELNOST 21
22 Použitelné do: {MM/YYYY} 9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ Uchovávejte v chladnice. Chrate ped mrazem. Uchovávejte v pvodním obalu aby byl pípravek chránn ped svtlem. 10. ZVLÁŠTNÍ OPATENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉIVÝCH PÍPRAVK NEBO ODPADU Z TAKOVÝCH LÉIVÝCH PÍPRAVK, POKUD JE TO VHODNÉ Likvidujte v souladu s místními pedpisy. 11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart, Belgie 12. REGISTRANÍ ÍSLO/ÍSLA EU/0/00/000/ ÍSLO ŠARŽE.š.: 14. KLASIFIKACE PRO VÝDEJ Výdej léivého pípravku vázán na lékaský pedpis. 15. NÁVOD K POUŽITÍ 16. INFORMACE V BRAILLOV PÍSMU 22
23 MINIMÁLNÍ ÚDAJE UVÁDNÉ NA MALÉM VNITNÍM OBALU LAHVIKA S PRÁŠKEM URENÁ K REKONSTITUCI ROZPOUŠTDLEM 1. NÁZEV LÉIVÉHO PÍPRAVKU A CESTA/CESTY PODÁNÍ Rotarix Prášek pro pípravu perorální suspenze Živá rotavirová vakcína K perorálnímu podání 2. ZPSOB PODÁNÍ 3. POUŽITELNOST Použ. do: 4. ÍSLO ŠARŽE.š.: 5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POET 1 dávka 6. JINÉ 23
24 MINIMÁLNÍ ÚDAJE UVÁDNÉ NA MALÉM VNITNÍM OBALU STÍKAKA S ROZPOUŠTDLEM URENÁ K REKONSTITUCI PRÁŠKU 1. NÁZEV LÉIVÉHO PÍPRAVKU A CESTA/CESTY PODÁNÍ Rotarix Rozpouštdlo pro pípravu perorální suspenze Živá rotavirová vakcína K perorálnímu podání 2. ZPSOB PODÁNÍ 3. POUŽITELNOST Použ. do: 4. ÍSLO ŠARŽE.š.: 5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POET 1 dávka 6. JINÉ 24
25 B. PÍBALOVÁ INFORMACE 25
26 PÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Rotarix, prášek pro pípravu perorální suspenze s rozpouštdlem Živá rotavirová vakcína Pette si pozorn celou píbalovou informaci díve, než bude Vaše dít okováno. - Ponechte si tuto píbalovou informaci. Je možné, že si ji budete potebovat znovu peíst. - Máte-li jakékoli další otázky, zeptejte se svého lékae nebo lékárníka. - Tato vakcína byla pedepsána Vašemu dítti. Nedávejte ji nikomu jinému. - Pokud se kterýkoli z nežádoucích úink vyskytne v závažné míe, nebo pokud si všimnete jakýchkoli nežádoucích úink, které nejsou uvedeny v této píbalové informaci, prosím, sdlte to svému lékai nebo lékárníkovi. V píbalové informaci naleznete: 1. Co je Rotarix a k emu se používá 2. emu musíte vnovat pozornost, než bude Vaše dít okováno vakcínou Rotarix 3. Jak se Rotarix podává 4. Možné nežádoucí úinky 5 Jak Rotarix uchovávat 6. Další informace 1. CO JE ROTARIX A K EMU SE POUŽÍVÁ Farmakoterapeutická skupina: virové vakcíny, ATC kód: J07BH01. Rotarix je virová vakcína obsahující živé, oslabené lidské rotaviry, která pomáhá chránit Vaše dít ped gastroenteritidou (prjem a zvracení) zpsobenou rotavirovou infekcí. Rotavirová infekce je nejastjší píinou vážného prjmu u kojenc a malých dtí. Rotavirus se snadno penáší z ruky do úst pi kontaku se stolicí infikované osoby. Vtšina dtí s rotavirovým prjmem se uzdraví sama. Ale nkteré dti velmi onemocní a nemoc je doprovázena vážným zvracením, prjmem a život ohrožující ztrátou tekutin vyžadující hospitalizaci. Rotavirové infekce jsou každoron zodpovdné za statisíce úmrtí na celém svt, hlavn v rozvojových zemích, v nichž není optimální výživa a zdravotní pée. Když je jedinci podána vakcína, imunitní systém (pirozená obrana tla) si vytvoí protilátky proti nejastji se vyskytujícím typm rotavir. Tyto protilátky chrání proti nemoci zpsobené tmito typy rotaviru. Tak, jak je tomu u všech vakcín, ani Rotarix nemusí úpln chránit všechny okované osoby ped rotavirovými infekcemi, kterým má zabránit. 2. EMU MUSÍTE VNOVAT POZORNOST, NEŽ BUDE VAŠE DÍT OKOVÁNO VAKCÍNOU ROTARIX Nepoužívejte Rotarix: jestliže Vaše dít mlo v minulosti jakoukoli alergickou reakci na rotavirové vakcíny nebo na kteroukoli složku obsaženou v pípravku Rotarix. Léivé látky a ostatní pomocné látky obsažené v Rotarixu jsou uvedeny na konci této píbalové informace. Projevy alergické reakce mohou zahrnovat svdivé kožní vyrážky, dýchací potíže a otok tváe nebo jazyka. jestliže Vaše dít mlo v minulosti intususcepci (neprchodnost stev, pi níž se jedna ást steva vsune do sousední ásti). jestliže se Vaše dít narodilo s vrozenou vadou trávicího systému, jež by ho inila náchylným k intususcepci. 26
27 jestliže Vaše dít má jakoukoli nemoc, která snižuje jeho odolnost vi infekci. jestliže Vaše dít má závažnou infekci s vysokou horekou. Je možné, že bude nutné odložit okování, dokud se neuzdraví. Slabá infekce jako napíklad rýma, by nemla pedstavovat problém, ale eknte o tom nejdív Vašemu lékai. jestliže Vaše dít má prjem nebo zvrací. Je možné, že bude nutné odložit okování, dokud se neuzdraví. Pi použití pípravku Rotarix je zapotebí zvláštní opatrnosti Je známo, že po okování dochází k vyluování živého viru z vakcíny stolicí okovaných dtí, zvlášt pak okolo 7. dne. Osoby, které jsou v kontaktu s nedávno okovanými dtmi, by si mly po výmn dtských plen mýt ruce. Rotarix se má opatrn podávat dtem, které jsou v bízkém kontaktu s jedinci, kteí mají jakoukoli nemoc nebo kteí užívají jakýkoli lék, jenž mže snižovat jejich odolnost vi infekci. Pokud se Rotarix podá pedasn narozeným dtem, mže být pozorována nižší imunitní odpov (sníženou schopnost tla odpovdt na vakcínu). U dtí s onemocnním žaludku nebo stev nebo u dtí se zpomalením rstu se má Rotarix podávat s opatrností. Vzájemné psobení s dalšími vakcínami Prosím, informujte svého lékae o všech lécích, které Vaše dít užívá nebo v nedávné dob užívalo, vetn lék, které jsou dostupné bez lékaského pedpisu, nebo jestli v poslední dob dostalo njakou jinou vakcínu. Rotarix mže být Vašemu dítti podán souasn s dalšími bžn doporuovanými vakcínami, jako jsou vakcíny proti záškrtu, tetanu, pertusi (dávivému kašli), vakcína proti Haemophilus influenzae typu b, perorální nebo inaktivovaná vakcína proti dtské obrn, vakcína proti hepatitid B a pneumokoková vakcína. Používání pípravku Rotarix s jídlem a pitím Ped ani po okování nejsou žádná omezení týkající se konzumace jídla nebo tekutin. Kojení Nejsou k dispozici údaje, které by naznaovaly, že se bhem kojení snižuje ochrana proti rotavirové gastroenteritid vyvolaná Rotarixem. V dob okování je tedy možné pokraovat v kojení. Dležité informace o nkterých složkách pípravku Rotarix Pokud Vám léka sdlil, že okované dít nesnáší nkteré cukry, obrate se ped použitím této vakcíny na svého lékae. 3. JAK SE ROTARIX PODÁVÁ Doporuenou dávku Rotarixu podá Vašemu dítti léka nebo zdravotní sestra. Vakcína (1 ml tekutiny) bude podána peroráln. Tato vakcína nesmí být za žádných okolností podána injekn. Vaše dít dostane dv dávky vakcíny. Každá dávka bude podána samostatn ve vhodné dob s asovým odstupem nejmén 4 týdn mezi obma dávkami. První dávka se mže podávat od 6 týdn vku. Ob dávky vakcíny se musí podat do 24. týdne vku, mly by se však podat pokud možno ped dosažením vku 16 týdn. V pípad, že Vaše dít vyplivne nebo vyzvrátí vtšinu podané dávky vakcíny, je možné podat pi stejné návštv jednu náhradní dávku. Pokud je Vašemu dítti jako první dávka podán Rotarix, doporuuje se, aby Vaše dít jako druhou dávku dostalo také Rotarix a ne jinou rotavirovou vakcínu. 27
28 Je dležité, abyste se ve vci následných návštv ídili pokyny Vašeho lékae nebo zdravotní sestry. Pokud zapomenete pijít k lékai v naplánované dob, požádejte lékae o radu. 4. MOŽNÉ NEŽÁDOUCÍ ÚINKY Podobn jako všechny léky, mže i Rotarix zpsobit nežádoucí úinky, které se ale nemusí vyskytnout u každého. Nežádoucí úinky, které se vyskytly v prbhu klinických studií s Rotarixem, byly následující: Velmi asté (nežádoucí úinky, které se mohou vyskytnout u 1 nebo u více než 1 na 10 dávek vakcíny): ztráta chuti k jídlu podráždnost asté (nežádoucí úinky, které se mohou vyskytnout mén než u 1 na 10 ale u 1 nebo více než u 1 na 100 dávek vakcíny): horeka, únava prjem, zvracení, opakované zvracení potravy, nadýmání, bolest bicha Mén asté (nežádoucí úinky, které se mohou vyskytnout mén než u 1 na 100 ale u 1 nebo více než u 1 na 1000 dávek vakcíny): plá porucha spánku, ospalost zácpa Vzácné (nežádoucí úinky, které se mohou vyskytnout mén než u 1 na 1000 ale u 1 nebo více než u 1 na dávek vakcíny): infekce horních cest dýchacích, chrapot, vodnatá rýma dermatitida, vyrážka svalové kee Pokud se kterýkoli z nežádoucích úink vyskytne v závažné míe, nebo pokud si všimnete jakýchkoli nežádoucích úink, které nejsou uvedeny v této píbalové informaci, prosím, sdlte to svému lékai nebo lékárníkovi. 5. JAK ROTARIX UCHOVÁVAT Uchovávejte mimo dosah a dohled dtí. Nepoužívejte pípravek Rotarix po uplynutí doby použitelnosti, uvedené na krabice. Doba použitelnosti se vztahuje k poslednímu dni uvedeného msíce. Uchovávejte v chladnice. Chrate ped mrazem. Uchovávejte v pvodním obalu aby byl pípravek chránn ped svtlem. Po rekonstituci by se vakcína obsažená ve stíkace mla okamžit aplikovat. Pokud rekonstituovaná vakcína není použita bhem 24 hodin, mla by být znehodnocena. Léivé pípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak máte likvidovat pípravky, které již nepotebujete. Tato opatení pomáhají chránit životní prostedí. 28
29 6. DALŠÍ INFORMACE Co pípravek Rotarix obsahuje - Léivými látkami jsou: Rotavirus RIX4414 humanum vivum attenuatum* ne mén než 10 6,0 CCID 50 *Pomnožený na Vero bukách - Pomocnými látkami v Rotarixu jsou: Prášek: sacharosa, dextran, sorbitol, aminokyseliny, Dulbeccova modifikace Eaglova média (DMEM). Rozpouštdlo: uhliitan vápenatý, xanthanová klovatina, sterilisovaná ištná voda. Jak pípravek Rotarix vypadá a co obsahuje toto balení Prášek pro pípravu perorální suspenze s rozpouštdlem. Rotarix je dodáván ve form blavého prášku ve sklenné lahvice obsahující jednu dávku a se samostatnou pedplnnou stíkakou s rozpouštdlem, která obsahuje pomalu se usazující bílý sediment a bezbarvý supernatant. Dodává se s pevodním adaptérem, který umožuje snadné penesení rozpouštdla do lahviky s práškem a smísení rzných souástí vakcíny. Ped podáním vakcíny Vašemu dítti musí být ob souásti smíseny dohromady. Smísená vakcína bude vypadat o nco zakalenjší než samotné rozpouštdlo. Rotarix je dostupný v baleních po 1, 5, 10 a 25 dávkách. Na trhu nemusí být všechny velikosti balení. Držitel rozhodnutí o registraci a výrobce GlaxoSmithKline Biologicals s.a. Rue de l Institut 89 B-1330 Rixensart Belgie Další informace o tomto pípravku získáte u místního zástupce držitele rozhodnutí o registraci: België/Belgique/Belgien GlaxoSmithKline s.a./n.v. Tél/Tel: eská republika GlaxoSmithKline s.r.o. Tel: gsk.czmail@gsk.com Danmark GlaxoSmithKline Pharma A/S Tlf: info@glaxosmithkline.dk Deutschland Luxembourg/Luxemburg GlaxoSmithKline s.a./n.v. Tél/Tel: Magyarország GlaxoSmithKline Kft. Tel.: Malta GlaxoSmithKline Malta Tel: Nederland 29
30 GlaxoSmithKline GmbH & Co. KG Tel: + 49 (0) produkt.info@gsk.com Eesti GlaxoSmithKline Eesti OÜ Tel: estonia@gsk.com GlaxoSmithKline A.E.B.E T: España GlaxoSmithKline, S.A. Tel: es-ci@gsk.com France Laboratoire GlaxoSmithKline Tél: + 33 (0) diam@gsk.com GlaxoSmithKline BV Tel: + 31 (0) nlinfo@gsk.com Norge GlaxoSmithKline AS Tlf: firmapost@gsk.no Österreich GlaxoSmithKline Pharma GmbH. Tel: at.info@gsk.com Polska GSK Commercial Sp. z.o.o. Tel.: + 48 (22) Portugal Smith Kline & French Portuguesa, Produtos Farmacêuticos, Lda. Tel: FI.PT@gsk.com Ireland GlaxoSmithKline (Ireland) Ltd Tel: (0) Ísland GlaxoSmithKline ehf. Tel: Italia GlaxoSmithKline S.p.A. Tel: GlaxoSmithKline Cyprus Ltd : Latvija GlaxoSmithKline Latvia SIA Tel: lv-epasts@gsk.com Slovenija GlaxoSmithKline d.o.o. Tel: (0) medical.x.si@gsk.com Slovenská republika GlaxoSmithKline Slovakia s.r.o. Tel: (0) recepcia.sk@gsk.com Suomi/Finland GlaxoSmithKline Oy Puh/Tel: Finland.tuoteinfo@gsk.com Sverige GlaxoSmithKline AB Tel: + 46 (0) info.produkt@gsk.com United Kingdom GlaxoSmithKline UK Tel: + 44 (0) customercontactuk@gsk.com Lietuva GlaxoSmithKline Lietuva UAB Tel info.lt@gsk.com 30
31 Tato píbalová informace byla naposledy schválena Podrobné informace o tomto pípravku jsou uveejnny na webových stránkách Evropské lékové agentury (EMEA): Následující informace je urena pouze pro zdravotnické pracovníky: Ve stíkace obsahující rozpouštdlo lze pi uchovávání pozorovat bílý sediment a irý supernatant. Ped rekonstitucí by rozpouštdlo mlo být ped i po protepání vizuáln zkontrolováno, zda neobsahuje jakékoliv cizorodé ástice a/nebo zda není zmnn fyzikální vzhled. Rekonstituovaná vakcína je trochu více zakalená než rozpouštdlo a má mlén bílý vzhled. Také rekonstituovaná vakcína by mla být ped aplikací vizuáln zkontrolována, zda neobsahuje jakékoliv cizorodé ástice a/nebo zda není zmnn fyzikální vzhled. Pokud jsou pozorovány cizorodé ástice nebo zmna vzhledu, je teba vakcínu vyadit. Všechen nepoužitý pípravek nebo odpad musí být zlikvidován v souladu s místními požadavky. Návod na rekonstituci a aplikaci vakcíny: 1. Odstrate plastový kryt z lahviky obsahující prášek. 2. Nasate pevodní adaptér na lahviku a tlate smrem dol, dokud není pevodní adaptér správn a bezpen pipojen. 3. Stíkaku obsahující rozpouštdlo ádn protepejte. Protepaná suspenze se bude jevit jako zakalená tekutina s pomalu se oddlujícím bílým sedimentem. 4. Odstrate ochranný uzávr ze stíkaky. 5. Nasate stíkaku na pevodní adaptér a siln ji do nho zatlate. 6. Vstíknte plný obsah stíkaky do lahviky obsahující prášek. 7. Lahviku se stále pipojenou stíkakou protepejte a zkontrolujte, zda se prášek úpln rozpustil. Rekonstituovaná vakcína bude vypadat o trochu více zakalená než samotné rozpouštdlo. Tento vzhled je normální. 8. Natáhnte veškerou sms zpt do stíkaky. 9. Odstrate stíkaku od pevodního adaptéru. 10. Tato vakcína je urena pouze k perorálnímu podání. Dít by se mlo usadit do zaklonné polohy. Aplikujte plný obsah stíkaky PERORÁLN (podáním plného obsahu stíkaky na vnitní stranu tváe). Nepodávejte injekn. Pokud se má rekonstituovaná vakcína ped podáním doasn uchovávat, nasate znovu na stíkaku ochranný uzávr. Stíkaka obsahující rekonstituovanou vakcínu se má ped perorálním podáním znovu lehce protepat. Nepodávejte injekn. 31
32 Pevodní adaptér Lahvika Stíkaka Ochranná zátka 1. Odstrate plastový kryt z lahviky obsahující lyofilizovaný prášek. 2. Nasate pevodní adaptér na lahviku a tlate ho smrem dol, dokud adaptér není bezpen napojen na vršek lahviky. 3. Stíkaku obsahující suspenzi ádn protepejte. Protepaná suspenze se bude jevit jako zakalená tekutina s pomalu se oddlujícím bílým sedimentem. 4. Odstrate ze stíkaky ochranný uzávr. 5. Nasate stíkaku na pevodní adaptér a siln ji do nho zatlate. 6. Vstíknte plný obsah stíkaky do lahviky obsahující lyofilizovaný prášek. 7. Lahviku se stále nasazenou stíkakou protepejte a zkontrolujte, zda se prášek úpln rozpustil. Rekonstituovaná vakcína bude mít zakalený vzhled. Tento vzhled je normální. 8. Natáhnte veškerou sms zpt do stíkaky. 9. Odstrate stíkaku od pevodního adaptéru. 10. Plný obsah stíkaky aplikujte peroráln (na vnitní stranu tváe). Dít by se mlo posadit do zaklonné polohy. Nepodávejte injekn. 32
Rotarix perorální suspenze v Živá rotavirová vakcína
 INFORMACE PRO UŽIVATELE Rotarix perorální suspenze v Živá rotavirová vakcína Vaše dí - - Máte- - - Pokud s V : 1. Co je Rotarix a k 2. 3. Jak se Rotarix podává 4. 5 Jak Rotarix uchovávat 6. Další informace
INFORMACE PRO UŽIVATELE Rotarix perorální suspenze v Živá rotavirová vakcína Vaše dí - - Máte- - - Pokud s V : 1. Co je Rotarix a k 2. 3. Jak se Rotarix podává 4. 5 Jak Rotarix uchovávat 6. Další informace
MACE: INFORMACE PRO UŽIVATELE. Cervarix Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná)
![MACE: INFORMACE PRO UŽIVATELE. Cervarix Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná) MACE: INFORMACE PRO UŽIVATELE. Cervarix Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná)](/thumbs/33/16328816.jpg) MACE: INFORMACE PRO UŽIVATELE Cervarix Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná) dostanete tuto vakcínu. - vou informaci. - Máte-. -. - V : 1. Co je Cervarix
MACE: INFORMACE PRO UŽIVATELE Cervarix Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná) dostanete tuto vakcínu. - vou informaci. - Máte-. -. - V : 1. Co je Cervarix
Rotavirus RIX4414 humanum vivum attenuatum* ne mén než 10 6,0 CCID 50
 1. NÁZEV P ÍPRAVKU Rotarix perorální suspenze v p edpln ném perorálním aplikátoru Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1,5 ml) obsahuje: Rotavirus RIX4414 humanum vivum
1. NÁZEV P ÍPRAVKU Rotarix perorální suspenze v p edpln ném perorálním aplikátoru Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1,5 ml) obsahuje: Rotavirus RIX4414 humanum vivum
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 55 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cervarix injekční suspenze Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná) Přečtěte si
B. PŘÍBALOVÁ INFORMACE 55 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cervarix injekční suspenze Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná) Přečtěte si
Živá rotavirová vakcína
 uživatele Živá rotavirová vakcína bude, protože. - Ponechte si tuto znovu - Máte-li jakékoli další otáznebo lékárníka. - Tato vakcína byla a pouze V. Nedávejte ji. - Pokud se ebo v. Viz bod 4. Co naleznete
uživatele Živá rotavirová vakcína bude, protože. - Ponechte si tuto znovu - Máte-li jakékoli další otáznebo lékárníka. - Tato vakcína byla a pouze V. Nedávejte ji. - Pokud se ebo v. Viz bod 4. Co naleznete
Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná), které nejsou uvedeny v
 INFORMACE PRO UŽIVATELE Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) vakcínou. Máte-l, které nejsou uvedeny v V : 1. Co je vakcína Synflorix a k 2. nflorix. 3. Jak se vakcína Synflorix
INFORMACE PRO UŽIVATELE Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) vakcínou. Máte-l, které nejsou uvedeny v V : 1. Co je vakcína Synflorix a k 2. nflorix. 3. Jak se vakcína Synflorix
Příbalová informace: informace pro pacienta. Integrilin 0,75 mg/ml infuzní roztok eptifibatidum
 Příbalová informace: informace pro pacienta Integrilin 0,75 mg/ml infuzní roztok eptifibatidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro pacienta Integrilin 0,75 mg/ml infuzní roztok eptifibatidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje důležité
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje důležité
Příbalová informace: informace pro uživatele. Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína
 Příbalová informace: informace pro uživatele Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
Příbalová informace: informace pro uživatele Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
Souhrn údajů o přípravku
 Příloha č. 1 ke sdělení sp.zn.: sukls204427/2010 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU PRIORIX prášek pro přípravu injekčního roztoku s rozpouštědlem Živá atenuovaná vakcína proti spalničkám, příušnicím
Příloha č. 1 ke sdělení sp.zn.: sukls204427/2010 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU PRIORIX prášek pro přípravu injekčního roztoku s rozpouštědlem Živá atenuovaná vakcína proti spalničkám, příušnicím
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gardasil, injekční suspenze Vakcína proti lidskému papilomaviru [typy 6, 11, 16, 18] (rekombinantní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gardasil, injekční suspenze Vakcína proti lidskému papilomaviru [typy 6, 11, 16, 18] (rekombinantní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro pacienta. Azomyr 0,5 mg/ml perorální roztok desloratadinum
 Příbalová informace: informace pro pacienta Azomyr 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta Azomyr 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele CELVAPAN injekční suspenze Vakcína proti chřipce (H1N1)v (celý virion, namnožená na buňkách Vero, inaktivovaná) Přečtěte si pozorně
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele CELVAPAN injekční suspenze Vakcína proti chřipce (H1N1)v (celý virion, namnožená na buňkách Vero, inaktivovaná) Přečtěte si pozorně
Příbalová informace: informace pro uživatele
 sp. zn. sukls167840/2014 Příbalová informace: informace pro uživatele Priorix inj.stříkačka, prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce Živá atenuovaná vakcína proti spalničkám,
sp. zn. sukls167840/2014 Příbalová informace: informace pro uživatele Priorix inj.stříkačka, prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce Živá atenuovaná vakcína proti spalničkám,
Příbalová informace: informace pro uživatele. Rotarix perorální suspenze v předplněném perorálním aplikátoru Živá rotavirová vakcína
 Příbalová informace: informace pro uživatele Rotarix perorální suspenze v předplněném perorálním aplikátoru Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
Příbalová informace: informace pro uživatele Rotarix perorální suspenze v předplněném perorálním aplikátoru Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
Příbalová informace: informace pro pacienta. Zurampic 200 mg potahované tablety lesinuradum
 Příbalová informace: informace pro pacienta Zurampic 200 mg potahované tablety lesinuradum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro pacienta Zurampic 200 mg potahované tablety lesinuradum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Rotarix perorální suspenze v předplněném perorálním aplikátoru Živá rotavirová vakcína
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Rotarix perorální suspenze v předplněném perorálním aplikátoru Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Rotarix perorální suspenze v předplněném perorálním aplikátoru Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE ProQuad Prášek pro přípravu injekční suspenze s rozpouštědlem Vakcína proti spalničkám, příušnicím, zarděnkám a planým neštovicím (živá) Před očkováním Vašeho
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE ProQuad Prášek pro přípravu injekční suspenze s rozpouštědlem Vakcína proti spalničkám, příušnicím, zarděnkám a planým neštovicím (živá) Před očkováním Vašeho
Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124912/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124912/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124912/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls16744/2009
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls16744/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU INFANRIX Vakcína proti difterii, tetanu a pertusi (acelulární) Injekční suspenze 2.
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls16744/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU INFANRIX Vakcína proti difterii, tetanu a pertusi (acelulární) Injekční suspenze 2.
Příbalová informace: informace pro uživatele. Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína
 Příbalová informace: informace pro uživatele Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
Příbalová informace: informace pro uživatele Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: informace pro pacienta. TAGRISSO 40 mg potahované tablety TAGRISSO 80 mg potahované tablety osimertinibum
 Příbalová informace: informace pro pacienta TAGRISSO 40 mg potahované tablety TAGRISSO 80 mg potahované tablety osimertinibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro pacienta TAGRISSO 40 mg potahované tablety TAGRISSO 80 mg potahované tablety osimertinibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Gardasil 9 injekční suspenze v předplněné injekční stříkačce 9valentní očkovací látka proti lidskému papilomaviru (rekombinantní, adsorbovaná) Tento přípravek
Příbalová informace: informace pro uživatele Gardasil 9 injekční suspenze v předplněné injekční stříkačce 9valentní očkovací látka proti lidskému papilomaviru (rekombinantní, adsorbovaná) Tento přípravek
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci
B. PŘÍBALOVÁ INFORMACE 1 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bonviva 3 mg injekční roztok Acidum ibandronicum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bonviva 3 mg injekční roztok Acidum ibandronicum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bonviva 3 mg injekční roztok Acidum ibandronicum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
Příbalová informace: informace pro uživatele. Rotarix prášek a rozpouštědlo pro perorální suspenzi Živá rotavirová vakcína
 Příbalová informace: informace pro uživatele Rotarix prášek a rozpouštědlo pro perorální suspenzi Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno,
Příbalová informace: informace pro uživatele Rotarix prášek a rozpouštědlo pro perorální suspenzi Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno,
Tato vakcína může obsahovat stopy neomycinu použitého v průběhu výrobního procesu (viz bod 4.3).
 1. NÁZEV PŘÍPRAVKU Twinrix Paediatric, injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná) a proti hepatitidě B (rdna) (HAB), adsorbovaná. 2. KVALITATIVNÍ A KVANTITATIVNÍ
1. NÁZEV PŘÍPRAVKU Twinrix Paediatric, injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná) a proti hepatitidě B (rdna) (HAB), adsorbovaná. 2. KVALITATIVNÍ A KVANTITATIVNÍ
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 35 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Menveo prášek a roztok pro přípravu injekčního roztoku Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si
B. PŘÍBALOVÁ INFORMACE 35 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Menveo prášek a roztok pro přípravu injekčního roztoku Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si
pak pomáhají Nimenrix chrání pouze proti infekcím vyvolaným bakteriemi Neisseria meningitidis a Y.
 ampulce -135 a Y informaci. Máteuedeny Vzhledem k Co naleznete této 1. Co je Nimenrix a k 2. 3. Jak se Nimenrix podáá 4. 5 Jak Nimenrix uchoáat 6. Obsah balení a další informace 1. Co je Nimenrix a k Co
ampulce -135 a Y informaci. Máteuedeny Vzhledem k Co naleznete této 1. Co je Nimenrix a k 2. 3. Jak se Nimenrix podáá 4. 5 Jak Nimenrix uchoáat 6. Obsah balení a další informace 1. Co je Nimenrix a k Co
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Živá atenuovaná vakcína proti spalničkám, příušnicím a zarděnkám
 Příloha č. 2b) k rozhodnutí o změně registrace sp.zn. sukls199309/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Priorix, prášek a rozpouštědlo pro injekční roztok Živá atenuovaná vakcína proti spalničkám,
Příloha č. 2b) k rozhodnutí o změně registrace sp.zn. sukls199309/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Priorix, prášek a rozpouštědlo pro injekční roztok Živá atenuovaná vakcína proti spalničkám,
Příbalová informace: informace pro uživatele. Rotarix perorální suspenze v předplněném perorálním aplikátoru Živá rotavirová vakcína
 Příbalová informace: informace pro uživatele Rotarix perorální suspenze v předplněném perorálním aplikátoru Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
Příbalová informace: informace pro uživatele Rotarix perorální suspenze v předplněném perorálním aplikátoru Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Protopic 0,03% mast Tacrolimusum monohydricum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Protopic 0,03% mast Tacrolimusum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Protopic 0,03% mast Tacrolimusum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele ProQuad Prášek a rozpouštědlo pro injekční suspenzi Vakcína proti spalničkám, příušnicím, zarděnkám a planým neštovicím (živá) Před očkováním Vás nebo Vašeho
Příbalová informace: informace pro uživatele ProQuad Prášek a rozpouštědlo pro injekční suspenzi Vakcína proti spalničkám, příušnicím, zarděnkám a planým neštovicím (živá) Před očkováním Vás nebo Vašeho
PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE. OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas
 PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace Informace pro uživatele
 Příbalová informace Informace pro uživatele Trobalt 50 mg potahované tablety Trobalt 100 mg potahované tablety Trobalt 200 mg potahované tablety Trobalt 300 mg potahované tablety Trobalt 400 mg potahované
Příbalová informace Informace pro uživatele Trobalt 50 mg potahované tablety Trobalt 100 mg potahované tablety Trobalt 200 mg potahované tablety Trobalt 300 mg potahované tablety Trobalt 400 mg potahované
Příbalová informace: informace pro uživatele. Ferriprox 500 mg potahované tablety Deferipronum
 Příbalová informace: informace pro uživatele Ferriprox 500 mg potahované tablety Deferipronum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatele Ferriprox 500 mg potahované tablety Deferipronum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat, protože obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE. Galvus 50 mg tablety Vildagliptinum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE Galvus 50 mg tablety Vildagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, neţ začnete tento přípravek uţívat. - Ponechte si příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE Galvus 50 mg tablety Vildagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, neţ začnete tento přípravek uţívat. - Ponechte si příbalovou informaci
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Vakcína proti difterii, tetanu, pertusi (acelulární) a adsorbovaná konjugovaná vakcína proti
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls124915/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU INFANRIX Hib Vakcína proti difterii, tetanu, pertusi (acelulární) a adsorbovaná konjugovaná
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls124915/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU INFANRIX Hib Vakcína proti difterii, tetanu, pertusi (acelulární) a adsorbovaná konjugovaná
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE. TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum
 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Aerius 0,5 mg/ml perorální roztok desloratadinum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Aerius 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Aerius 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
EU/1/97/029/001-002 EU/1/97/029/006-010
 Příbalová informace - Rp. Informace pro použití, čtěte pozorně! J07BC20 TWINRIX PAEDIATRIC injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná) a proti hepatitidě
Příbalová informace - Rp. Informace pro použití, čtěte pozorně! J07BC20 TWINRIX PAEDIATRIC injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná) a proti hepatitidě
Příloha č. 2a) k rozhodnutí o změně registrace sp.zn. sukls102421/2010 a příloha k sp. zn. sukls102423/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2a) k rozhodnutí o změně registrace sp.zn. sukls102421/2010 a příloha k sp. zn. sukls102423/2010 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Boostrix Polio inj. stříkačka Boostrix Polio inj.
Příloha č. 2a) k rozhodnutí o změně registrace sp.zn. sukls102421/2010 a příloha k sp. zn. sukls102423/2010 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Boostrix Polio inj. stříkačka Boostrix Polio inj.
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Infanrix hexa, prášek a suspenze pro přípravu injekční suspenze v předplněné injekční stříkačce. Vakcína proti difterii (D), tetanu (T), pertusi
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Infanrix hexa, prášek a suspenze pro přípravu injekční suspenze v předplněné injekční stříkačce. Vakcína proti difterii (D), tetanu (T), pertusi
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Prepandrix, suspenze a emulze pro přípravu injekční emulze. Prepandemická vakcína proti chřipce (H5N1) (štěpený virion, inaktivovaná, obsahující
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Prepandrix, suspenze a emulze pro přípravu injekční emulze. Prepandemická vakcína proti chřipce (H5N1) (štěpený virion, inaktivovaná, obsahující
Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná)
 1. Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (0,5 ml) obsahuje : Pneumococcale polysaccharidum serotypus 1 1,2 Pneumococcale polysaccharidum
1. Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (0,5 ml) obsahuje : Pneumococcale polysaccharidum serotypus 1 1,2 Pneumococcale polysaccharidum
Příbalová informace: informace pro uživatele. Baraclude 0,05 mg/ml perorální roztok entecavirum
 Příbalová informace: informace pro uživatele Baraclude 0,05 mg/ml perorální roztok entecavirum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatele Baraclude 0,05 mg/ml perorální roztok entecavirum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatele. Rotarix perorální suspenze ve stlačitelné tubě Živá rotavirová vakcína
 Příbalová informace: informace pro uživatele Rotarix perorální suspenze ve stlačitelné tubě Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože
Příbalová informace: informace pro uživatele Rotarix perorální suspenze ve stlačitelné tubě Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože
Příbalová informace: informace pro uživatele. Rotarix perorální suspenze Živá rotavirová vakcína
 Příbalová informace: informace pro uživatele Rotarix perorální suspenze Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože obsahuje pro Vás
Příbalová informace: informace pro uživatele Rotarix perorální suspenze Živá rotavirová vakcína Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože obsahuje pro Vás
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp. zn. sukls73676/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fluarix, injekční suspenze v předplněné injekční stříkačce Vakcína proti chřipce (štěpený virion, inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
sp. zn. sukls73676/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fluarix, injekční suspenze v předplněné injekční stříkačce Vakcína proti chřipce (štěpený virion, inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příbalová informace: informace pro uživatele Engerix-B 20 µg. antigenum tegiminis hepatitidis B injekční suspenze
 sp.zn. sukls204563/2014 Příbalová informace: informace pro uživatele Engerix-B 10 µg Engerix-B 20 µg antigenum tegiminis hepatitidis B injekční suspenze Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls204563/2014 Příbalová informace: informace pro uživatele Engerix-B 10 µg Engerix-B 20 µg antigenum tegiminis hepatitidis B injekční suspenze Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. HBVAXPRO 5 mikrogramů, injekční suspenze Vakcína proti hepatitidě typu B (rdna)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HBVAXPRO 5 mikrogramů, injekční suspenze Vakcína proti hepatitidě typu B (rdna) Přečtěte si pozorně celou příbalovou informaci dříve, než necháte Vaše dítě
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HBVAXPRO 5 mikrogramů, injekční suspenze Vakcína proti hepatitidě typu B (rdna) Přečtěte si pozorně celou příbalovou informaci dříve, než necháte Vaše dítě
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro pacienta. Forxiga 5 mg potahované tablety Forxiga 10 mg potahované tablety dapagliflozinum
 Příbalová informace: informace pro pacienta Forxiga 5 mg potahované tablety Forxiga 10 mg potahované tablety dapagliflozinum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: informace pro pacienta Forxiga 5 mg potahované tablety Forxiga 10 mg potahované tablety dapagliflozinum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: informace pro pacienta. Ristaben 50 mg potahované tablety Sitagliptinum
 Příbalová informace: informace pro pacienta Ristaben 50 mg potahované tablety Sitagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta Ristaben 50 mg potahované tablety Sitagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
P ÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 PÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Infanrix Penta, injekní suspenze Adsorbovaná vakcína proti difterii (D), tetanu (T), pertusi (acelulární komponenta) (Pa), hepatitid B (rdna) (HBV) a poliomyelitid
PÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Infanrix Penta, injekní suspenze Adsorbovaná vakcína proti difterii (D), tetanu (T), pertusi (acelulární komponenta) (Pa), hepatitid B (rdna) (HBV) a poliomyelitid
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Tyverb 250 mg, potahované tablety. Lapatinibum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Tyverb 250 mg, potahované tablety Lapatinibum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Tyverb 250 mg, potahované tablety Lapatinibum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Bexsero injekční suspenze v předplněné injekční stříkačce Vakcína proti meningokokům skupiny B (rdna, komponentní, adsorbovaná) Tento přípravek podléhá dalšímu
Příbalová informace: informace pro uživatele Bexsero injekční suspenze v předplněné injekční stříkačce Vakcína proti meningokokům skupiny B (rdna, komponentní, adsorbovaná) Tento přípravek podléhá dalšímu
Příbalová informace: Informace pro pacienta
 Příbalová informace: Informace pro pacienta CONBRIZA 20 mg potahované tablety Bazedoxifenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: Informace pro pacienta CONBRIZA 20 mg potahované tablety Bazedoxifenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
NEREGISTROVANÝ PŘÍPRAVEK použití povoleno v rámci specifického léčebného programu SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU ADACEL POLIO, injekční suspenze v předplněné stříkačce Vakcína (adsorbovaná) proti diftérii (snížený obsah antigenu), tetanu, pertusi (acelulární komponenta)
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU ADACEL POLIO, injekční suspenze v předplněné stříkačce Vakcína (adsorbovaná) proti diftérii (snížený obsah antigenu), tetanu, pertusi (acelulární komponenta)
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Rotarix perorální suspenze ve více-jednodávkových (5 jednotlivých dávek) stlačitelných tubách spojených proužkem Živá rotavirová vakcína Přečtěte si pozorně
Příbalová informace: informace pro uživatele Rotarix perorální suspenze ve více-jednodávkových (5 jednotlivých dávek) stlačitelných tubách spojených proužkem Živá rotavirová vakcína Přečtěte si pozorně
Rotavirus RIX4414 humanum vivum attenuatum* ne méně než 10 6,0 CCID 50
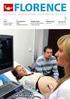 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro perorální suspenzi s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po rekonstituci obsahuje: Rotavirus RIX4414 humanum
1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro perorální suspenzi s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po rekonstituci obsahuje: Rotavirus RIX4414 humanum
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 51 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) Přečtěte
B. PŘÍBALOVÁ INFORMACE 51 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) Přečtěte
Příbalová informace: Informace pro pacienta. Neoclarityn 5 mg perorální lyofilizát desloratadinum
 Příbalová informace: Informace pro pacienta Neoclarityn 5 mg perorální lyofilizát desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: Informace pro pacienta Neoclarityn 5 mg perorální lyofilizát desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
o, protože., Máte- Vašemu d. lékárníkovi. v z bod 4.
 Infanrix hexa, prášek a i v Vakcína proti difterii (D), tetanu (T), pertus B (rdna) konjugovaná vakcína proti Haemophilus influenzae typu b (Hib), (adsorbovaná). o, protože., Máte- Vašemu d. Pokud se u
Infanrix hexa, prášek a i v Vakcína proti difterii (D), tetanu (T), pertus B (rdna) konjugovaná vakcína proti Haemophilus influenzae typu b (Hib), (adsorbovaná). o, protože., Máte- Vašemu d. Pokud se u
Příbalová informace: Informace pro uživatele. Ebixa 5 mg/dávka, perorální roztok Memantini hydrochloridum
 Příbalová informace: Informace pro uživatele Ebixa 5 mg/dávka, perorální roztok Memantini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: Informace pro uživatele Ebixa 5 mg/dávka, perorální roztok Memantini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
PŘÍBALOVÁ INFORMACE. EMADINE 0,5 mg/ml, Oční Kapky, roztok. Emedastinum
 PŘÍBALOVÁ INFORMACE EMADINE 0,5 mg/ml, Oční Kapky, roztok. Emedastinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou informaci.pro případ,
PŘÍBALOVÁ INFORMACE EMADINE 0,5 mg/ml, Oční Kapky, roztok. Emedastinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou informaci.pro případ,
Příbalová informace. GlaxoSmithKline Biologicals S.A., Rue de l Institut 89, 1330 Rixensart, Belgie
 Příbalová informace Informace pro použití, čtěte pozorně! INFANRIX Vakcína proti difterii, tetanu a pertusi (acelulární) (injekční suspenze) Výrobce GlaxoSmithKline Biologicals S.A., Rue de l Institut
Příbalová informace Informace pro použití, čtěte pozorně! INFANRIX Vakcína proti difterii, tetanu a pertusi (acelulární) (injekční suspenze) Výrobce GlaxoSmithKline Biologicals S.A., Rue de l Institut
sp.zn.: sukls244138/2011
 sp.zn.: sukls244138/2011 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE VAQTA Adult 50 U/ml injekční suspenze v předplněné injekční stříkačce Očkovací látka proti hepatitidě typu A, inaktivovaná, adsorbovaná
sp.zn.: sukls244138/2011 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE VAQTA Adult 50 U/ml injekční suspenze v předplněné injekční stříkačce Očkovací látka proti hepatitidě typu A, inaktivovaná, adsorbovaná
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE. Raloxifen Teva 60 mg potahované tablety Raloxifeni hydrochloridum
 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Raloxifen Teva 60 mg potahované tablety Raloxifeni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Raloxifen Teva 60 mg potahované tablety Raloxifeni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
Příbalová informace: informace pro pacienta
 Příbalová informace: informace pro pacienta Briviact 10 mg potahované tablety Briviact 25 mg potahované tablety Briviact 50 mg potahované tablety Briviact 75 mg potahované tablety Briviact 100 mg potahované
Příbalová informace: informace pro pacienta Briviact 10 mg potahované tablety Briviact 25 mg potahované tablety Briviact 50 mg potahované tablety Briviact 75 mg potahované tablety Briviact 100 mg potahované
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 58 Příbalová informace: informace pro pacienta Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) Přečtěte
B. PŘÍBALOVÁ INFORMACE 58 Příbalová informace: informace pro pacienta Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) Přečtěte
PANTOLOC Control 20 mg enterosolventní tablety Pantoprazolum
 PANTOLOC Control 20 mg enterosolventní tablety Pantoprazolum - - - Musíte se poradit s po 2 týdnech. - Bez porady s - V 1. Co je PANTOLOC Control a k 2. 3. Jak se PANTOLOC Control používá 4. Možné nežádoucí
PANTOLOC Control 20 mg enterosolventní tablety Pantoprazolum - - - Musíte se poradit s po 2 týdnech. - Bez porady s - V 1. Co je PANTOLOC Control a k 2. 3. Jak se PANTOLOC Control používá 4. Možné nežádoucí
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix prášek a rozpouštědlo pro perorální suspenzi Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po rekonstituci
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix prášek a rozpouštědlo pro perorální suspenzi Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po rekonstituci
Příloha č. 2a) k rozhodnutí o změně registrace sp.zn. sukls112037/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2a) k rozhodnutí o změně registrace sp.zn. sukls112037/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Boostrix inj. stříkačka, injekční suspenze v předplněné injekční stříkačce Adsorbovaná
Příloha č. 2a) k rozhodnutí o změně registrace sp.zn. sukls112037/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Boostrix inj. stříkačka, injekční suspenze v předplněné injekční stříkačce Adsorbovaná
P ÍLOHA I SOUHRN ÚDAJ O P ÍPRAVKU
 P ÍLOHA I SOUHRN ÚDAJ O P ÍPRAVKU 1 1. NÁZEV P ÍPRAVKU Rotarix, prášek pro p ípravu perorální suspenze s rozpoušt dlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
P ÍLOHA I SOUHRN ÚDAJ O P ÍPRAVKU 1 1. NÁZEV P ÍPRAVKU Rotarix, prášek pro p ípravu perorální suspenze s rozpoušt dlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
Cervarix, injekční suspenze Příbalové informace
 Cervarix, injekční suspenze Příbalové informace PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cervarix injekční suspenze Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná)
Cervarix, injekční suspenze Příbalové informace PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cervarix injekční suspenze Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná)
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp. zn. sukls122237/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Fluarix, injekční suspenze v předplněné injekční stříkačce Vakcína proti chřipce (štěpený virion, inaktivovaná) Přečtěte si pozorně
sp. zn. sukls122237/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Fluarix, injekční suspenze v předplněné injekční stříkačce Vakcína proti chřipce (štěpený virion, inaktivovaná) Přečtěte si pozorně
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele VAQTA Adult 50 U/ml injekční suspenze v předplněné injekční stříkačce Očkovací látka proti hepatitidě typu A, inaktivovaná, adsorbovaná Pro dospělé Přečtěte
Příbalová informace: informace pro uživatele VAQTA Adult 50 U/ml injekční suspenze v předplněné injekční stříkačce Očkovací látka proti hepatitidě typu A, inaktivovaná, adsorbovaná Pro dospělé Přečtěte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. JEVTANA 60 mg koncentrát pro přípravu infuzního roztoku s rozpouštědlem kabazitaxelum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE JEVTANA 60 mg koncentrát pro přípravu infuzního roztoku s rozpouštědlem kabazitaxelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE JEVTANA 60 mg koncentrát pro přípravu infuzního roztoku s rozpouštědlem kabazitaxelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Menveo prášek a roztok pro injekční roztok Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele Menveo prášek a roztok pro injekční roztok Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele INVANZ 1 g prášek pro přípravu koncentrátu pro přípravu infuzního roztoku ertapenemum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek
Příbalová informace: informace pro uživatele INVANZ 1 g prášek pro přípravu koncentrátu pro přípravu infuzního roztoku ertapenemum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek
Rotavirus RIX4414 humanum vivum attenuatum* ne méně než 10 6,0 CCID 50
 1. NÁZEV PŘÍPRAVKU Rotarix perorální suspenze Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1,5 ml) obsahuje: Rotavirus RIX4414 humanum vivum attenuatum* ne méně než 10 6,0 CCID
1. NÁZEV PŘÍPRAVKU Rotarix perorální suspenze Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1,5 ml) obsahuje: Rotavirus RIX4414 humanum vivum attenuatum* ne méně než 10 6,0 CCID
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Orlistat GSK 120 mg tvrdé tobolky 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka obsahuje orlistatum 120 mg Úplný seznam pomocných látek
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Orlistat GSK 120 mg tvrdé tobolky 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka obsahuje orlistatum 120 mg Úplný seznam pomocných látek
Příbalová informace: informace pro pacienta
 Příbalová informace: informace pro pacienta Nimenrix prášek pro přípravu injekčního roztoku s rozpouštědlem v předplněné injekční stříkačce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y
Příbalová informace: informace pro pacienta Nimenrix prášek pro přípravu injekčního roztoku s rozpouštědlem v předplněné injekční stříkačce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls167902/2010 a příloha k sp. zn. sukls16927/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls167902/2010 a příloha k sp. zn. sukls16927/2011 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Rhophylac 300 mikrogramů/2 ml, injekční roztok
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls167902/2010 a příloha k sp. zn. sukls16927/2011 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Rhophylac 300 mikrogramů/2 ml, injekční roztok
Jedna předplněná injekční stříkačka obsahuje immunoglobulinum humanum anti-d 1500 IU (300 mikrogramů).
 sp. zn. sukls262204/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Igamad 1500 IU, injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
sp. zn. sukls262204/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Igamad 1500 IU, injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Altargo 1% mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g obsahuje retapamulinum 10 mg (1 %). Úplný seznam pomocných látek viz bod 6.1. 3. LÉKOVÁ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Altargo 1% mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g obsahuje retapamulinum 10 mg (1 %). Úplný seznam pomocných látek viz bod 6.1. 3. LÉKOVÁ
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
P íbalová informace: informace pro uživatele
 P íbalová informace: informace pro uživatele Menveo prášek a roztok pro p ípravu injek ního roztoku Konjugovaná vakcína proti meningokokové skupin A, C, W135 a Y P e t te si pozorn tuto p íbalovou informaci
P íbalová informace: informace pro uživatele Menveo prášek a roztok pro p ípravu injek ního roztoku Konjugovaná vakcína proti meningokokové skupin A, C, W135 a Y P e t te si pozorn tuto p íbalovou informaci
ne méně 30 IU(25 Lf) Tetani anatoxinum 1
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU NEBO NA VNITŘNÍM OBALU LAHVIČKA + LAHVIČKA X 1 LAHVIČKA + LAHVIČKA X 10 LAHVIČKA + LAHVIČKA X 20 LAHVIČKA + LAHVIČKA X 25 LAHVIČKA + LAHVIČKA X 40 LAHVIČKA + LAHVIČKA X 50
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU NEBO NA VNITŘNÍM OBALU LAHVIČKA + LAHVIČKA X 1 LAHVIČKA + LAHVIČKA X 10 LAHVIČKA + LAHVIČKA X 20 LAHVIČKA + LAHVIČKA X 25 LAHVIČKA + LAHVIČKA X 40 LAHVIČKA + LAHVIČKA X 50
Zvláštní opatrnosti při použití KOGENATE Bayer 250 IU je zapotřebí
 Příbalová informace: informace pro uživatele KOGENATE Bayer 250 IU Prášek a rozpouštědlo pro injekční roztok Rekombinantní koagulační faktor VIII (octocogum alfa) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele KOGENATE Bayer 250 IU Prášek a rozpouštědlo pro injekční roztok Rekombinantní koagulační faktor VIII (octocogum alfa) Přečtěte si pozorně celou příbalovou informaci
