Jak připravit toxikologické souhrny v nástroji IUCLID a jak odvodit DNEL Praktický průvodce 14
|
|
|
- Bohuslav Matoušek
- před 7 lety
- Počet zobrazení:
Transkript
1 Jak připravit toxikologické souhrny v nástroji IUCLID a jak odvodit DNEL Praktický průvodce 14 Annankatu 18, P.O. Box 400, FI Helsinki, Finland Tel Fax echa.europa.eu
2
3 Praktický průvodce 14 3 PRÁVNÍ UPOZORNĚNÍ Tento dokument obsahuje pokyny k nařízení REACH, které vysvětlují povinnosti vyplývající z tohoto nařízení a způsob jejich plnění. Dovolujeme si nicméně uživatele upozornit, že jediným závazným právním textem je text nařízení REACH a že informace v tomto dokumentu nepředstavují právní poradenství. Evropská agentura pro chemické látky nenese odpovědnost za obsah tohoto dokumentu. Verze Změny Verze 1 První vydání červenec 2012 Praktický průvodce 14: Jak připravit toxikologické souhrny v nástroji IUCLID a jak odvodit DNEL Referenční číslo: ECHA-12-B-15-CS ISBN-13: ISSN: Datum vydání: červenec 2012 Jazyk: CS Evropská agentura pro chemické látky, 2012 Titulní strana Evropská agentura pro chemické látky Prohlášení o vyloucení odpovednosti a záruk: Toto je pracovní preklad dokumentu, který byl puvodne zverejnen v anglickém jazyce. Originální dokument je k dispozici na internetových stránkách agentury ECHA. Reprodukce je povolena pod podmínkou uvedení zdroje ve znění: Zdroj: Evropská agentura pro chemické látky, a za předpokladu, že tato skutečnost bude písemně oznámena oddělení pro komunikaci agentury ECHA (publications@echa.europa.eu). Tento dokument bude k dispozici v těchto 22 jazycích: angličtina, bulharština, čeština, dánština, estonština, finština, francouzština, italština, litevština, lotyština, maďarština, maltština, němčina, nizozemština, polština, portugalština, rumunština, řečtina, slovenština, slovinština, španělština a švédština Máte-li otázky nebo připomínky týkající se tohoto dokumentu, zašlete je prosím (s uvedením referenčního čísla a data vydání) prostřednictvím formuláře žádosti o informace. Tento formulář je k dispozici na webových stránkách agentury ECHA na adrese Evropská agentura pro chemické látky Poštovní adresa: PO Box 400, FI Helsinki, Finsko Adresa pro osobní návštěvu: Annankatu 18, Helsinki, Finsko
4 4 Praktický průvodce 14 Obsah 1. ÚVOD SOUHRN POŽADAVKŮ Z PŘÍLOHY 1 NAŘÍZENÍ REACH PRACOVNÍ POSTUP OD PODROBNÝCH SOUHRNŮ STUDIÍ K SOUHRNU SLEDOVANÝCH VLASTNOSTÍ Toxikokinetika, metabolismus a distribuce (7.1) Stručný popis klíčových informací Klíčové hodnoty pro posouzení chemické bezpečnosti Bioakumulační potenciál Míry absorpce Diskuze Akutní toxicita (7.2) Závěr o sledované vlastnosti Výběr sledovaných vlastností (výběr podrobného souhrnu studie) Zdůvodnění výběru Úroveň, při které dochází k účinkům Kvalita celé databáze Stručný popis klíčových informací Diskuze Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat Dráždivost/žíravost (7.3) Závěr o sledované vlastnosti Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Zdůvodnění výběru Úroveň, při které dochází k účinkům Stručný popis klíčových informací Diskuze Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat Senzibilizace (7.4) Závěr o sledované vlastnosti Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Zdůvodnění výběru Stručný popis klíčových informací Diskuze Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat Toxicita po opakovaných dávkách (7.5) Závěr o sledované vlastnosti Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Zdůvodnění výběru Úroveň, při které dochází k účinkům... 24
5 Praktický průvodce Typ zkoušky Druhy Kvalita celé databáze Cílový orgán Stručný popis klíčových informací Diskuze Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat Genetická toxicita (7.6) Závěr o sledované vlastnosti Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Zdůvodnění výběru Stručný popis klíčových informací Diskuze Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat Karcinogenita (7.7) Závěr o sledované vlastnosti Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Zdůvodnění výběru Úroveň, při které dochází k účinkům Typ zkoušky Druhy Kvalita celé databáze Cílový orgán Stručný popis klíčových informací Diskuze Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat Toxicita pro reprodukci (7.8) Závěr o sledované vlastnosti Výběr sledované vlastnosti Zdůvodnění výběru Úroveň, při které dochází k účinkům Druh zkoušky Druhy Kvalita celé databáze Stručný popis klíčových informací Diskuze Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat OD SOUHRNŮ SLEDOVANÝCH VLASTNOSTÍ K SOUHNRU TOXIKOLOGICKÝCH INFORMACÍ Nejcitlivější sledovaná vlastnost Odvození DNEL... 37
6 6 Praktický průvodce Sledované vlastnosti přispívající k odvození hodnot DNEL Přehled informací o DNEL, které mají být oznámeny prostřednictvím nástroje IUCLID Metoda odvození DNEL Výchozí bod deskriptoru dávky Oznámení hodnotících faktorů OD TOXIKOLOGICKÉHO SOUHRNU K POSOUZENÍ EXPOZICE A RIZIK Přehled typů posouzení chemické bezpečnosti Charakterizace rizika se nevyžaduje Kvantitativní charakterizace rizika Semikvantitativní charakterizace rizika Kvalitativní charakterizace rizika Seznam obrázků Obrázek 1: Pracovní postup pro toxikologické souhrny Obrázek 2: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro toxikokinetiku Obrázek 3: Seznam v nástroji IUCLID pro výběr závěru o bioakumulaci Obrázek 4: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro akutní toxicitu Obrázek 5: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro akutní toxicitu Obrázek 6: Seznam v nástroji ICULID pro výběr úrovně, při které dochází k účinkům, pro akutní toxicitu Obrázek 7: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro dráždivost Obrázek 8: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti Obrázek 9: Seznam v nástroji ICULID pro výběr úrovně, při níž dochází k účinkům, pro dráždivost/žíravost pro kůži/oči Obrázek 10: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro senzibilizaci kůže Obrázek 11: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro senzibilizaci Obrázek 12: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro toxicitu po opakovaných dávkách Obrázek 13: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro toxicitu po opakovaných dávkách Obrázek 14: Seznam v nástroji IUCLID pro výběr úrovně, při níž dochází k účinkům, pro toxicitu po opakovaných dávkách Obrázek 15: Seznam v nástroji IUCLID pro výběr druhu zkoušky pro toxicitu po opakovaných dávkách Obrázek 16: Seznam v nástroji IUCLID pro výběr druhu pro toxicitu po opakovaných dávkách Obrázek 17: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro genetickou toxicitu Obrázek 18: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro genetickou toxicitu Obrázek 19: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro karcinogenitu, není-li k dispozici žádná studie Obrázek 20: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro karcinogenitu Obrázek 21: Seznam v nástroji IUCLID pro výběr úrovně, při níž dochází k účinkům, pro karcinogenitu... 31
7 Praktický průvodce 14 7 Obrázek 22: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro toxicitu pro reprodukci Obrázek 23: Seznam v nástroji IUCLID pro výběr závěru z posouzení nebezpečnosti Obrázek 24: Seznam v nástroji IUCLID pro výběr nejcitlivější sledované vlastnosti Obrázek 25: Příklad z toxikologického souhrnu v nástroji IUCLID ( Toxikologické informace ) pro odvození DNEL... 40
8 8 Praktický průvodce ÚVOD Aby žadatelé o registraci prokázali bezpečné použití látek, musí splnit požadavky na informace, jak stanoví čl. 10 a 12 nařízení REACH č. 1907/2006/ES společně s přílohami I, VI, VII X a XI tohoto nařízení. Tento dokument podává informace o tom, jak vyplnit toxikologické souhrny v oddíle 7 nástroje IUCLID a jak odvodit hodnoty DNEL. DNEL (Derived No Effects Level odvozená úroveň, při které nedochází k nepříznivým účinkům) je mezní úroveň expozice látce, která by u člověka neměla být překročena. V nástroji IUCLID existují dvě úrovně toxikologických souhrnů: Souhrny jednotlivých sledovaných vlastností: souhrn sledované vlastnosti v nástroji IUCLID uvádí informace o jedné toxikologické sledované vlastnosti, které jsou zvoleny k přenesení do posouzení nebezpečnosti. Vychází z (podrobných) souhrnů studií oznámených k dané sledované vlastnosti (viz oddíly 7.1 až 7.12). Souhrn toxikologických informací: souhrn toxikologických informací (souhrn cílových vlastností Toxikologické informace v nástroji IUCLID) v oddíle 7 slučuje souhrny pro jednotlivé sledované vlastnosti a uvádí závěr vyplývající z posouzení nebezpečnosti pro každou cílovou skupinu (pracovníci, obecná populace), cestu expozice (orální, inhalací, dermální, oční) a druh účinku (dlouhodobý, krátkodobý, místní nebo systémový). Tento závěr lze vyjádřit jako kvantitativní prahovou hodnotu (např. DNEL nebo DMEL) nebo jako kvalitativní indikátor nebezpečnosti. Dále tento dokument vysvětluje, jaký dopad mají závěry posouzení nebezpečnosti na rozsah posouzení expozice a typ charakterizace rizika. Je třeba poznamenat, že tento praktický průvodce se nezabývá vypracováním podrobných souhrnů studií a souhrnů studií v nástroji IUCLID. Více informací naleznete v Praktickém průvodci 3: Jak oznamovat podrobné souhrny studií. Tento praktický průvodce nezahrnuje následující posouzení: odvození místních dermálních hodnot DNEL, odvození hodnot DMEL, oznamování údajů o účincích na člověka a jejich použití pro vyvození závěrů o sledovaných vlastnostech, souhrn sledovaných vlastností pro senzibilizaci dýchacích cest, odvození hodnot DNEL pro akutní systémovou toxicitu. Podrobnější pokyny k odvození hodnot DNEL naleznete v Pokynech k požadavkům na informace a posuzování chemické bezpečnosti, kapitole R.8: Charakterizace vztahu mezi dávkou [koncentrací] a odezvou, pokud jde o lidské zdraví.
9 Praktický průvodce SOUHRN POŽADAVKŮ Z PŘÍLOHY 1 NAŘÍZENÍ REACH Příloha I nařízení REACH vymezuje, jak by se mělo provádět posouzení nebezpečnosti pro lidské zdraví. To zahrnuje čtyři kroky: 1) vyhodnocení informací o účincích na jiné organismy než na člověka, 2) vyhodnocení informací o účincích na člověka, 3) klasifikace a označení a 4) odvození DNEL. Vyhodnocení informací o účincích na jiné organismy než na člověka obsahuje: určení nebezpečnosti pro daný účinek na základě všech informací o účincích na jiné organismy než na člověka, které jsou k dispozici, určení kvantitativního vztahu mezi dávkou (koncentrací) a odezvou (účinkem). Nelze-li stanovit kvantitativní vztah mezi dávkou (koncentrací) a odezvou (účinkem), mělo by být zahrnuto kvalitativní posouzení. Výběr studie a deskriptoru dávky k přenesení do posouzení nebezpečnosti by měl vycházet z následujících pravidel: Obvykle by se měla vybrat studie s nejnižším deskriptorem dávky. Je však třeba vzít v úvahu několik dalších faktorů, např. provedení studie, přiměřenost, relevantnost zkušebních biologických druhů, kvalita výsledků, platnost zkoušky. Pokud není vybrána studie s nejnižším deskriptorem dávky, měla by být tato skutečnost plně odůvodněna. Při určování hodnot DNEL by se měly vzít v úvahu následující skutečnosti: Hodnota DNEL by měla odrážet pravděpodobnou cestu (cesty), trvání a frekvenci expozice. U některých sledovaných vlastností (např. mutagenita) nemusí dostupné informace umožňovat odvození DNEL. Může být nutné v závislosti na určených použitích (a očekávané expozici) určit různé hodnoty DNEL pro každou příslušnou lidskou populaci. Při odvozování hodnot DNEL by se měly vzít v úvahu následující faktory: nejistota způsobená experimentálními údaji a vnitrodruhovou a mezidruhovou variabilitou, povaha a závažnost účinků, citlivost lidské populace, jíž se dané informace o expozici týkají. Nelze-li odvodit žádnou hodnotu DNEL, měla by se tato skutečnost jasně uvést a plně odůvodnit.
10 10 Praktický průvodce PRACOVNÍ POSTUP Obrázek 1 představuje hlavní pracovní postup od hlášení dostupných studií pro jednotlivé sledované vlastnosti až po odvození toxikologického souhrnu v nástroji IUCLID pro látky dosahující množství 10 tun či více za rok, který je poté přenesen do posouzení expozice a charakterizace rizika. Obrázek 1: Pracovní postup pro toxikologické souhrny Podrobný souhrn studie 1 Toxikokinetika, metabolismus a distribuce Toxikologický souhrn (Toxikologické informace) Rozsah posouzení expozice a typ charakterizace rizika Podrobný souhrn studie 2 Akutní toxicita Podrobný souhrn studie 3 Dráždivost / žíravost Senzibilizace 1. Postup začíná uvedením podrobných souhrnů studií v záznamech studií sledovaných vlastností v nástroji IUCLID. Tento krok je popsán v Praktickém průvodci 3: Jak oznamovat podrobné souhrny studií. 2. Poté se, je-li to možné, vybere jeden podrobný souhrn studie (tj. jeden záznam studie sledovaných vlastností v nástroji IUCLID), který se použije jako referenční v souhrnu sledovaných vlastností. Nicméně pokud je třeba, mohou se vzít v úvahu všechny podrobné souhrny studií pro konkrétní sledovanou vlastnost a lze na ně odkazovat v souhrnu sledovaných vlastností. Souhrn sledovaných vlastností by měl rovněž obsahovat vyhodnocení celé databáze, diskuzi o výsledcích a zdůvodnění klasifikace / rozhodnutí látku neklasifikovat.
11 Praktický průvodce Nakonec jsou informace ze všech souhrnů sledovaných vlastností sloučeny do (celkového) toxikologického souhrnu. Vyvodí se závěry týkající se nebezpečnosti, které zahrnují buď odvození DNEL či DMEL, nebo kvalitativní závěry ohledně nebezpečnosti. V závislosti na závěrech týkajících se nebezpečnosti je určen rozsah posouzení expozice a druh charakterizací rizika.
12 12 Praktický průvodce OD PODROBNÝCH SOUHRNŮ STUDIÍ K SOUHRNU SLEDOVANÝCH VLASTNOSTÍ V následujících oddílech nalezne žadatel o registraci pokyny, jak vyplnit pole související s každým souhrnem sledovaných toxikologických vlastností, který lze použít k vyvození závěrů ohledně nebezpečnosti. 4.1 Toxikokinetika, metabolismus a distribuce (7.1) Tento souhrn sledovaných vlastností v nástroji IUCLID obsahuje: volné textové pole k uvedení krátkého popisu dostupných klíčových informací, klíčové hodnoty na úrovni potenciální bioakumulace a klíčové hodnoty absorpce pro posouzení chemické bezpečnosti (CSA), diskuzní pole k dalšímu vysvětlení a odůvodnění výběru klíčových hodnot. Obrázek 2: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro toxikokinetiku Níže je uveden popis různých polí, která jsou k dispozici v souhrnu sledovaných vlastností: Toxikokinetika, metabolismus a distribuce: Stručný popis klíčových informací V tomto textovém poli by měly být popsány informace z hlavní studie týkající se absorpce, distribuce, metabolismu a exkrece nebo pozorování založená na fyzikálně-chemických vlastnostech Klíčové hodnoty pro posouzení chemické bezpečnosti V tomto oddíle by se měly uvést klíčové hodnoty týkající se míry bioakumulace a absorpce. Tyto informace se používají například v kontextu extrapolace mezi různými cestami expozice
13 Praktický průvodce nebo při diskuzi o potenciální vnitřní dávce v posouzení chemické bezpečnosti Bioakumulační potenciál Výběrem jedné možnosti z položek na seznamu lze vložit závěr ohledně bioakumulačního potenciálu (viz obrázek níže). Obrázek 3: Seznam v nástroji IUCLID pro výběr závěru o bioakumulaci Informace obvykle vycházejí z fyzikálně-chemických vlastností (log Ko/v, molekulová struktura a molekulová hmotnost) a metabolismu (jsou-li informace k dispozici). Zdůvodnění uvedené hodnoty lze vysvětlit v poli pro diskuzi níže Míry absorpce Informace obvykle vycházejí z fyzikálně-chemických vlastností (log Ko/v, molekulová struktura a molekulová hmotnost) Diskuze V tomto oddíle by měla být uvedena interpretace výsledků. To zahrnuje například: diskuzi o potenciálních chybějících údajích, relevantnost výsledků pro posouzení rizika, například rozsah, v jakém jsou výsledky ze studie na zvířatech relevantní pro lidské zdraví. 4.2 Akutní toxicita (7.2) Souhrn sledovaných vlastností v nástroji IUCLID obsahuje pro každou cestu expozice tyto prvky: seznam pro výběr závěru pro tuto sledovanou vlastnost, odkaz na vybrané záznamy studií (podrobné souhrny studií) podporující tento závěr, volné textové pole pro odůvodnění výběru této studie, druh deskriptoru dávky (výběr ze seznamu) a hodnota pro úroveň, při níž dochází k účinkům, zjištěná v dané studii, volné textové pole k charakterizaci kvality celé databáze pro tuto sledovanou vlastnost.
14 14 Praktický průvodce 14 Následující textová pole slouží k uvedení sloučených informací pro všechny tři cesty: volné textové pole k popisu klíčových informací získaných z podrobných souhrnů studií, volné textové pole k doplnění dalšího vysvětlení a argumentů týkajících se závěrů pro tuto sledovanou vlastnost (diskuze), volné textové pole k porovnání souhrnu sledovaných vlastností s kritérii pro klasifikaci a označení, a to za účelem odůvodnění klasifikace či rozhodnutí látku neklasifikovat. Obrázek 4: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro akutní toxicitu U všech tří sledovaných vlastností (orální, inhalační a dermální akutní toxicita) by měl být vybrán endpoint conclusion (závěr o sledované vlastnosti). Závěr o sledované vlastnosti by měl vycházet z mortality zvířat. Měla by se zvážit povaha a reverzibilita závažných účinků jiných než mortalita Závěr o sledované vlastnosti Seznam pro výběr závěru o sledované vlastnosti je:
15 Praktický průvodce Obrázek 5: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro akutní toxicitu Následující tabulka uvádí přehled různých možností dostupných v nástroji IUCLID. Možnosti závěrů o sledované vlastnosti Pozorovány nepříznivé účinky (Adverse effects observed) Kdy je tato možnost vhodná Jestliže byla v některé ze studií pozorována mortalita nebo závažné nepříznivé účinky. (Je třeba poznamenat, že zvířata, která jsou člověkem usmrcena kvůli utrpení a bolesti způsobenými sloučeninou, by se měla zaznamenat jako úmrtí související se sloučeninou.) Nepozorovány žádné nepříznivé účinky (No adverse effects observed Studie není k dispozici (No study available) Studie není k dispozici (nutné další informace) (No study available (further information necessary)) Jestliže je k dispozici studie a při mezní úrovni dávky nezemřela žádná zvířata ani nebyly pozorovány závažné účinky. Uveďte zdůvodnění. Není relevantní pro akutní toxicitu, neboť k provedení studií podle přílohy VII nebo VIII není nutný návrh zkoušek Výběr sledovaných vlastností (výběr podrobného souhrnu studie) Zde lze vybrat odkaz na podrobný souhrn studie, z nějž závěr o sledované vlastnosti vychází. Prostřednictvím tohoto odkazu lze dohledat původní zdroj informací pro následné kroky posouzení a podávání zpráv. Měla by být zvolena studie, která vzbuzuje nejvyšší obavy. V zásadě by se měly použít údaje o účincích na člověka, jsou-li k dispozici. Nicméně spolehlivý deskriptor dávky se na údajích o účincích na člověka zakládá jen zřídka. Při výběru podrobného souhrnu studie se musí vzít v úvahu mimo jiné následující faktory: 1) kvalita studie, např. Klimischovo skóre, 2) trvání studie, 3) zda je studie v souladu se správnou laboratorní praxí (GLP) nebo ne. Upřednostňují se dostupné epidemiologické údaje za předpokladu, že jsou spolehlivé a relevantní Zdůvodnění výběru Zdůvodnění výběru je nutné zejména tehdy, pokud nebyla vybrána studie (podrobný souhrn
16 16 Praktický průvodce 14 studie) s nejnižším deskriptorem dávky. Zdůvodnění může obsahovat například tvrzení, že studie s nejnižším deskriptorem dávky má nízkou kvalitu nebo že pozorovaný účinek není relevantní pro člověka. Jestliže není pro souhrn sledovaných vlastností vybrán žádný podrobný souhrn studie, mělo by se zdůvodnění uvést vždy Úroveň, při které dochází k účinkům Obrázek 6: Seznam v nástroji ICULID pro výběr úrovně, při které dochází k účinkům, pro akutní toxicitu Obvykle by se měla zvolit dávka LD50 (LC50 při inhalaci). Pokud nebyly pozorovány žádné nepříznivé účinky, rovná se úroveň, při níž dochází k účinkům, mezní dávce Kvalita celé databáze Je třeba zvážit následující faktory, neboť mohou mít vliv na posouzení nebezpečnosti: Do jaké míry splňují dostupné informace jako celek požadavek nařízení REACH na údaje, který se řídí tonáží (úplnost databáze)? Spolehlivost a konzistentnost různých studií: je třeba vzít v úvahu kvalitu zkušební metody, velikost a statistickou sílu návrhu studie, biologickou hodnověrnost, vztahy mezi dávkou a odezvou a statistické testy Stručný popis klíčových informací Zde by se měla uvést hlavní zjištění Diskuze V tomto oddíle by měla být uvedena interpretace výsledků. To zahrnuje například: diskuzi o potenciálních chybějících údajích, relevantnost výsledků pro posouzení rizika, například rozsah, v jakém jsou výsledky ze studie na zvířatech relevantní pro lidské zdraví.
17 Praktický průvodce Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat Souhrn sledovaných vlastností by se měl porovnat s kritérii klasifikace. Měly by být uvedeny důvody pro splnění či nesplnění kritérií klasifikace. Upozorňujeme, že klasifikace jako taková se oznamuje v oddíle 2 nástroje ICULID. 4.3 Dráždivost/žíravost (7.3) Souhrn sledovaných vlastností v nástroji IUCLID obsahuje pro každou cestu expozice tyto části: seznam pro výběr závěru pro tuto sledovanou vlastnost, seznam pro výběr možnosti označující úroveň, kdy dochází k účinku, kvalitativním způsobem. Pro dráždivost/žíravost pro kůži a oči jsou navíc k dispozici tyto části: odkaz na vybrané záznamy studií (podrobné souhrny studií) podporující tento závěr, volné textové pole pro odůvodnění výběru této studie. Následující textová pole slouží k uvedení sloučených informací pro všechny tři cesty: volné textové pole ke krátkému popisu klíčových informací získaných z podrobných souhrnů studií volné textové pole k doplnění dalšího vysvětlení a argumentů týkajících se závěrů pro tuto sledovanou vlastnost (diskuze), volné textové pole k porovnání souhrnu sledovaných vlastností s kritérii pro klasifikaci a označení, a to za účelem odůvodnění klasifikace či rozhodnutí látku neklasifikovat. Upozornění: dráždivost pro dýchací cesty není v tomto oddíle zahrnuta. Obrázek 7: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro dráždivost
18 18 Praktický průvodce Závěr o sledované vlastnosti Seznam pro výběr závěru o sledované vlastnosti je: Obrázek 8: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti Následující tabulka uvádí přehled různých dostupných možností. Možnosti závěrů o sledované vlastnosti Kdy je tato možnost vhodná Pozorovány nežádoucí účinky (Adverse effects observed) Nepozorovány žádné nepříznivé účinky (No adverse effects observed Studie není k dispozici (No study available) Studie není k dispozici (nutné další informace) (No study available (further information necessary)) Látka splňuje kritéria klasifikace pro dráždivost / žíravost / vážné poškození očí. Látka nesplňuje kritéria klasifikace pro příslušnou sledovanou vlastnost. Uveďte zdůvodnění. Není relevantní pro dráždivost/žíravost pro kůži/oči, neboť k provedení studií podle přílohy VII nebo VIII není nutný návrh zkoušek Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Zde lze vybrat odkaz na podrobný souhrn studie, z nějž vychází závěr o sledované vlastnosti. Prostřednictvím tohoto odkazu lze dohledat původní zdroj informací pro následné kroky posouzení a podávání zpráv. Měla by být vybrána studie, která vzbuzuje nejvyšší obavy. V zásadě by se měly použít údaje o účincích na člověka, jsou-li k dispozici. Nicméně spolehlivý deskriptor dávky se na údajích o účincích na člověka zakládá jen zřídka. Při výběru podrobného souhrnu studie se musí vzít v úvahu mimo jiné následující faktory: 1) kvalita studie, např. Klimischovo skóre, 2) trvání studie, 3) zda je studie v souladu se správnou laboratorní praxí (GLP) nebo ne. Upřednostňují se dostupné epidemiologické údaje za předpokladu, že jsou spolehlivé a relevantní Zdůvodnění výběru Zdůvodnění výběru je nutné zejména tehdy, pokud nebyla vybrána studie (podrobný souhrn studie) s nejnižším deskriptorem dávky. Zdůvodnění může obsahovat například tvrzení, že studie s nejnižším deskriptorem dávky má nízkou kvalitu nebo že pozorovaný účinek není relevantní pro člověka. Jestliže není pro souhrn sledovaných vlastností vybrán žádný podrobný
19 Praktický průvodce souhrn studie, mělo by se zdůvodnění uvést vždy Úroveň, při které dochází k účinkům Obrázek 9: Seznam v nástroji ICULID pro výběr úrovně, při níž dochází k účinkům, pro dráždivost/žíravost pro kůži/oči Úroveň, při níž dochází k účinkům, by se měla zvolit pouze tehdy, pokud látka splňuje kritéria klasifikace pro dráždivost/žíravost. Jestliže je látka určena ke klasifikaci v kategorii 1A, 1B nebo 1C pro kůži a kategorii 1 pro oči, měla by být zvolena úroveň účinku corrosive (žíravá). Jestliže je látka klasifikována v kategorii 2 (jak pro kůži, tak pro oči), měla by se zvolit úroveň účinku irritating (dráždivá) Stručný popis klíčových informací Zde by se měla uvést hlavní zjištění z vybraných studií Diskuze V tomto oddíle by měla být uvedena interpretace výsledků. To zahrnuje například: diskuzi o potenciálních chybějících údajích, relevantnost výsledků pro posouzení rizika, například rozsah, v jakém jsou výsledky ze studie na zvířatech relevantní pro lidské zdraví Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat Zde by se měl souhrn sledovaných vlastností porovnat s kritérii pro klasifikaci. Měly by být uvedeny důvody pro splnění či nesplnění kritérií. Upozorňujeme, že klasifikace jako taková se oznamuje v oddíle 2 nástroje ICULID. Rovněž upozorňujeme, že u sledované vlastnosti dráždivost/žíravost se závěry řídí klasifikací. V případě potřeby by měly být vysvětleny důvody, proč nepříznivé účinky hlášené v podrobných souhrnech studií nevedou ke klasifikaci látky (a tudíž k tvrzení no hazard identified (nebyla zjištěna žádná nebezpečnost)). 4.4 Senzibilizace (7.4) Souhrn sledovaných vlastností v nástroje IUCLID obsahuje pro každou cestu expozice tyto části:
20 20 Praktický průvodce 14 seznam pro výběr závěru pro tuto sledovanou vlastnost, odkaz na vybraný záznam studií (podrobný souhrn studií) podporující tento závěr, volné textové pole pro odůvodnění výběru této studie, volné textové pole ke krátkému popisu klíčových informací získaných z podrobných souhrnů studií, volné textové pole k doplnění dalšího vysvětlení a argumentů týkajících se závěrů pro tuto sledovanou vlastnost (diskuze). Následující textové pole slouží k uvedení sloučených informací pro tyto dvě cesty: volné textové pole k porovnání souhrnu sledovaných vlastností s kritérii pro klasifikaci a označení, a to za účelem odůvodnění klasifikace či rozhodnutí látku neklasifikovat. Upozornění: tento oddíl nezahrnuje senzibilizaci dýchacích cest Obrázek 10: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro senzibilizaci kůže Závěr o sledované vlastnosti Seznam pro výběr závěru o sledované vlastnosti je:
21 Praktický průvodce Obrázek 11: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro senzibilizaci Následující tabulka uvádí přehled různých dostupných možností. Možnosti závěrů o sledované vlastnosti Kdy je tato možnost vhodná Pozorovány nežádoucí účinky (Adverse effects Látka je klasifikována pro senzibilizaci. observed) Nepozorovány žádné nepříznivé účinky (No adverse Látka není klasifikována pro senzibilizaci. effects observed Studie není k dispozici (No study available) Uveďte zdůvodnění. Studie není k dispozici (nutné další informace) (No study available (further information necessary)) Není relevantní pro senzibilizaci, neboť k provedení studií podle přílohy VII nebo VIII není nutný návrh zkoušek Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Zde lze vybrat odkaz na podrobný souhrn studie, z nějž vychází závěr o sledované vlastnosti. Prostřednictvím tohoto odkazu lze dohledat původní zdroj informací pro následné kroky posouzení a podávání zpráv. Měla by se vybrat studie, která vzbuzuje nejvyšší obavy. V zásadě by se měly použít údaje o účincích na člověka, jsou-li k dispozici. Nicméně spolehlivý deskriptor dávky se na údajích o účincích na člověka zakládá jen zřídka. Při výběru podrobného souhrnu studie se musí vzít v úvahu mimo jiné následující faktory: 1) kvalita studie, např. Klimischovo skóre, 2) trvání studie, 3) zda je studie v souladu se správnou laboratorní praxí (GLP) nebo ne. Upřednostňují se dostupné epidemiologické údaje nebo jiné údaje o účincích na člověka za předpokladu, že jsou spolehlivé a relevantní Zdůvodnění výběru Zdůvodnění výběru je nutné zejména tehdy, pokud nebyla vybrána studie (podrobný souhrn studie) s nejnižším deskriptorem dávky. Zdůvodnění může obsahovat například tvrzení, že studie s nejnižším deskriptorem dávky má nízkou kvalitu nebo že pozorovaný účinek není relevantní pro člověka. Jestliže není pro souhrn sledovaných vlastností vybrán žádný podrobný souhrn studie, mělo by se zdůvodnění uvést vždy.
22 22 Praktický průvodce Stručný popis klíčových informací Zde by se měla uvést hlavní zjištění Diskuze V tomto oddíle by měla být uvedena interpretace výsledků. To zahrnuje například: diskuzi o potenciálních chybějících údajích, relevantnost výsledků pro posouzení rizika, například rozsah, v jakém jsou výsledky ze studie na zvířatech relevantní pro lidské zdraví Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat V tomto oddíle by se měl souhrn sledovaných vlastností porovnat s kritérii pro klasifikaci. Měly by být uvedeny důvody pro splnění či nesplnění kritérií. Upozorňujeme, že klasifikace jako taková se oznamuje v oddíle 2 nástroje ICULID. 4.5 Toxicita po opakovaných dávkách (7.5) Tento oddíl se týká sledovaných vlastností Neurotoxicita a Imunotoxicita. Souhrn sledovaných vlastností v nástroji IUCLID obsahuje pro každou cestu expozice tyto části: seznam pro výběr závěru pro tuto sledovanou vlastnost, odkaz na vybrané záznamy studií (podrobné souhrny studií) podporující tento závěr, volné textové pole pro odůvodnění výběru této studie, druh deskriptoru dávky (výběr ze seznamu) a hodnota pro úroveň, při níž dochází k účinkům, zjištěná v dané studii, seznam pro výběr druhu zkoušky a seznam pro výběr druhu v dané studii, volné textové pole k charakterizaci kvality celé databáze pro tuto sledovanou vlastnost, seznam pro výběr označení cílového orgánu, u nějž existují nejvyšší obavy. Následující textová pole slouží k uvedení sloučených informací pro všechny tři cesty (orální, dermální a inhalační): volné textové pole ke krátkému popisu klíčových informací získaných z podrobných souhrnů studií, volné textové pole k doplnění dalšího vysvětlení a argumentů týkajících se závěrů pro tuto sledovanou vlastnost (diskuze), volné textové pole k porovnání souhrnu sledovaných vlastností s kritérii pro klasifikaci a označení, a to za účelem odůvodnění klasifikace či rozhodnutí látku neklasifikovat.
23 Praktický průvodce Obrázek 12: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro toxicitu po opakovaných dávkách Závěr o sledované vlastnosti Seznam pro výběr závěru o sledované vlastnosti je: Obrázek 13: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro toxicitu po opakovaných dávkách
24 24 Praktický průvodce 14 Následující tabulka uvádí přehled různých dostupných možností. Možnosti závěrů o sledované vlastnosti Kdy je tato možnost vhodná Pozorovány nepříznivé účinky (Adverse effects observed) Nepozorovány žádné nepříznivé účinky (No adverse effects observed) Studie není k dispozici (No study available) Studie není k dispozici (nutné další informace) (No study available (further information necessary)) Pozorovány nepříznivé účinky při mezní nebo nižší dávce. Nebyly pozorovány žádné nepříznivé účinky při mezní nebo nižší dávce. Uveďte zdůvodnění. Dokumentace obsahuje návrh zkoušek pro toxicitu po opakovaných dávkách (90denní studie) Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Zde lze vybrat odkaz na podrobný souhrn studie, z nějž vychází závěr o sledované vlastnosti. Prostřednictvím tohoto odkazu lze dohledat původní zdroj informací pro následné kroky posouzení a podávání zpráv. Měla by být vybrána studie, která vzbuzuje nejvyšší obavy. V zásadě by se měly použít údaje o účincích na člověka, jsou-li k dispozici. Nicméně spolehlivý deskriptor dávky se na údajích o účincích na člověka zakládá jen zřídka. Při výběru podrobného souhrnu studie se musí vzít v úvahu mimo jiné následující faktory: 1) kvalita studie, např. Klimischovo skóre, 2) trvání studie, 3) zda je studie v souladu se správnou laboratorní praxí (GLP) nebo ne. Upřednostňují se dostupné epidemiologické údaje za předpokladu, že jsou spolehlivé a relevantní Zdůvodnění výběru Zvláštní zdůvodnění výběru je zapotřebí, jestliže se zvolí krátkodobá studie (např. 28denní studie) namísto studie dlouhodobé (např. 90denní studie), studie o nízké kvalitě namísto studie o kvalitě vysoké nebo studie, která není prováděna v souladu s GLP, namísto studie prováděné v souladu s GLP Úroveň, při které dochází k účinkům Obrázek 14: Seznam v nástroji IUCLID pro výběr úrovně, při níž dochází k účinkům, pro toxicitu po opakovaných dávkách Primárním deskriptorem dávky v tomto souhrnu sledovaných vlastností je NOAEL nebo NOAEC,
25 Praktický průvodce v některých studiích rovněž BMDL (benchmark dose level, úroveň referenční dávky). Hodnoty LOAEL nebo LOAEC by se měly používat pouze tehdy, pokud hodnoty NOAEL/NOAEC nejsou k dispozici. Je-li deskriptor dávky v podrobném souhrnu studie vyjádřen v ppm/ppb, měl by se nejprve převést na ng/m 3 nebo μg/m 3 nebo mg/m 3. U inhalační a dermální cesty existuje rovněž možnost oznámit výsledky týkající se místních účinků Typ zkoušky Obrázek 15: Seznam v nástroji IUCLID pro výběr druhu zkoušky pro toxicitu po opakovaných dávkách Druh zkoušky by měl být stejný jako ve vybraném podrobném souhrnu studie. Tyto informace se použijí k odvození DNEL Druhy Obrázek 16: Seznam v nástroji IUCLID pro výběr druhu pro toxicitu po opakovaných dávkách
26 26 Praktický průvodce 14 Vybraný druh by měl být stejný jako ve vybraném podrobném souhrnu studie Kvalita celé databáze Je třeba zvážit následující faktory, neboť mohou mít vliv na posouzení nebezpečnosti: Do jaké míry splňují dostupné informace jako celek požadavek nařízení REACH na údaje, který se řídí tonáží (úplnost databáze)? Spolehlivost a konzistentnost různých studií: zde je třeba vzít v úvahu kvalitu zkušební metody, velikost a statistickou sílu návrhu studie, biologickou hodnověrnost, vztahy mezi dávkou a odezvou a statistické testy Cílový orgán Existuje-li několik cílových orgánů, měl by se vybrat ten cílový orgán, u něhož nepříznivé účinky vedou k nejvyšším obavám, tj. orgán, který souvisí s deskriptorem dávky Stručný popis klíčových informací Zde by se měla uvést hlavní zjištění Diskuze V tomto oddíle by měla být uvedena interpretace výsledků. To zahrnuje například: diskuzi o potenciálních chybějících údajích, relevantnost výsledků pro posouzení rizika, například rozsah, v jakém jsou výsledky ze studie na zvířatech relevantní pro lidské zdraví Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat V tomto oddíle by se měl souhrn sledovaných vlastností porovnat s kritérii pro klasifikaci. Měly by být uvedeny důvody pro splnění či nesplnění kritérií. Upozorňujeme, že klasifikace jako taková se oznamuje v oddíle 2 nástroje ICULID. 4.6 Genetická toxicita (7.6) Tento souhrn sledovaných vlastností v nástroji IUCLID obsahuje následující části: seznam pro výběr závěru pro tuto sledovanou vlastnost, odkaz na vybrané záznamy studií (podrobné souhrny studií) podporující tento závěr, volné textové pole pro odůvodnění výběru této studie, volné textové pole ke krátkému popisu klíčových informací získaných z podrobných souhrnů studií, volné textové pole k doplnění dalšího vysvětlení a argumentů týkajících se závěrů pro tuto sledovanou vlastnost (diskuze), volné textové pole k porovnání souhrnu sledovaných vlastností s kritérii pro klasifikaci a označení, a to za účelem odůvodnění klasifikace či rozhodnutí látku neklasifikovat.
27 Praktický průvodce Obrázek 17: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro genetickou toxicitu Závěr o sledované vlastnosti Seznam pro výběr závěru o sledované vlastnosti je: Obrázek 18: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro genetickou toxicitu
28 28 Praktický průvodce 14 Následující tabulka uvádí přehled různých dostupných možností: Možnosti závěrů o sledované vlastnosti Pozorovány nepříznivé účinky (Adverse effects observed) Nepozorovány žádné nepříznivé účinky (No adverse effects observed) Studie není k dispozici (No study available) Studie není k dispozici (nutné další informace) (No study available (further information necessary)) Kdy je tato možnost vhodná Látka je mutagenní, např. pozitivní výsledek studie in vivo pro jakoukoli ze sledovaných vlastností (genová mutace / chromozomální aberace). Látka není mutagenní. Celkový závěr: látka není mutagenní. Uveďte zdůvodnění. Dokumentace obsahuje návrh zkoušky in vivo pro genotoxicitu Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Podrobný souhrn studie by měl být vybrán v situacích, kdy je k dispozici pouze jedna studie in vitro (látky v příloze VII) nebo obsahuje-li dokumentace pouze jednu pozitivní studii (in vitro nebo in vivo). Ve všech ostatních případech není třeba podrobný souhrn studie vybírat.
29 Praktický průvodce Zdůvodnění výběru Zdůvodnění výběru je zapotřebí, jestliže je vybrána krátkodobá studie namísto studie dlouhodobé, studie o nízké kvalitě namísto studie o kvalitě vysoké nebo studie, která není prováděna v souladu s GLP, namísto studie prováděné v souladu s GLP Stručný popis klíčových informací Zde by se měla uvést hlavní zjištění Diskuze V tomto oddíle by měla být uvedena interpretace výsledků. To zahrnuje například: diskuzi o potenciálních chybějících údajích, relevantnost výsledků pro posouzení rizika, například rozsah, v jakém jsou výsledky ze studie na zvířatech relevantní pro lidské zdraví Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat V tomto oddíle by se měl souhrn sledovaných vlastností porovnat s kritérii pro klasifikaci. Měly by být uvedeny důvody pro splnění či nesplnění kritérií. Upozorňujeme, že klasifikace jako taková by se měla uvést v oddíle 2 nástroje IUCLID. 4.7 Karcinogenita (7.7) Souhrn sledovaných vlastností v nástroje IUCLID obsahuje pro každou cestu expozice tyto části: seznam pro výběr závěru pro tuto sledovanou vlastnost, odkaz na vybrané záznamy studií (podrobné souhrny studií) podporující tento závěr, volné textové pole pro odůvodnění výběru této studie, druh deskriptoru dávky (výběr ze seznamu) a hodnota pro úroveň, při níž dochází k účinkům, zjištěná v dané studii, seznam pro výběr druhu zkoušky a seznam pro výběr druhu v dané studii, volné textové pole k charakterizaci kvality celé databáze pro tuto sledovanou vlastnost, seznam pro výběr označení cílového orgánu, u nějž existují nejvyšší obavy. Následující textová pole slouží k uvedení sloučených informací pro všechny tři cesty (orální, dermální a inhalační): volné textové pole k popisu klíčových informací získaných z podrobných souhrnů studií, volné textové pole k doplnění dalšího vysvětlení a argumentů týkajících se závěrů pro tuto sledovanou vlastnost (diskuze), volné textové pole k porovnání souhrnu sledovaných vlastností s kritérii pro klasifikaci a označení, a to za účelem odůvodnění klasifikace či rozhodnutí látku neklasifikovat.
30 30 Praktický průvodce 14 Obrázek 19: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro karcinogenitu, není-li k dispozici žádná studie Závěr o sledované vlastnosti Seznam pro výběr závěru o sledované vlastnosti je: Obrázek 20: Seznam v nástroji IUCLID pro výběr závěru o sledované vlastnosti pro karcinogenitu
31 Praktický průvodce Následující tabulka vysvětluje různé možnosti, které jsou k dispozici. Možnosti závěrů o sledované vlastnosti Kdy je tato možnost vhodná Pozorovány nepříznivé účinky (Adverse effects Látka je karcinogenní. observed) Nepozorovány žádné nepříznivé účinky (No adverse Látka nebyla shledána karcinogenní v dostupné effects observed) studii (dostupných studiích). Studie není k dispozici (No study available) Studie není k dispozici (nutné další informace) (No study available (further information necessary)) Uveďte zdůvodnění. Dokumentace obsahuje návrh zkoušek pro karcinogenitu Výběr sledované vlastnosti (výběr podrobného souhrnu studie) Zde lze vybrat odkaz na podrobný souhrn studie, z nějž vychází závěr o sledované vlastnosti. Prostřednictvím tohoto odkazu lze dohledat původní zdroj informací pro následné kroky posouzení a podávání zpráv. Měla by být vybrána studie, která vzbuzuje nejvyšší obavy. V zásadě by se měly použít údaje o účincích na člověka, jsou-li k dispozici. Nicméně spolehlivý deskriptor dávky se na údajích o účincích na člověka zakládá jen zřídka. Při výběru podrobného souhrnu studie se musí vzít v úvahu mimo jiné následující faktory: 1) kvalita studie, např. Klimischovo skóre, 2) trvání studie, 3) zda je studie v souladu se správnou laboratorní praxí (GLP) nebo ne. Upřednostňují se dostupné epidemiologické údaje za předpokladu, že jsou spolehlivé a relevantní Zdůvodnění výběru Zdůvodnění výběru je zapotřebí, jestliže je vybrána krátkodobá studie namísto studie dlouhodobé, studie o nízké kvalitě namísto studie o kvalitě vysoké nebo studie, která není prováděna v souladu s GLP, namísto studie prováděné v souladu s GLP Úroveň, při které dochází k účinkům Obrázek 21: Seznam v nástroji IUCLID pro výběr úrovně, při níž dochází k účinkům, pro karcinogenitu Výběr deskriptoru dávky by se měl vztahovat pouze ke karcinogenním účinkům. Ostatní účinky
32 32 Praktický průvodce 14 a deskriptory dávky by se měly uvádět v oddíle Stručný popis klíčových informací. Jestliže neexistuje žádná prahová hodnota pro karcinogenitu, měla by se zvolit hodnota T25. Pokud byla prahová hodnota pro karcinogenitu definována, měly by se zvolit jiné deskriptory dávky Typ zkoušky Většina studií karcinogenity in vivo jsou dlouhodobé studie Druhy Druhy by měly být stejné jako ty, které byly uvedeny ve vybraném podrobném souhrnu studie Kvalita celé databáze Je třeba zvážit následující faktory, neboť mohou mít vliv na posouzení nebezpečnosti: Do jaké míry splňují dostupné informace jako celek požadavek nařízení REACH na údaje, který se řídí tonáží (úplnost databáze)? Spolehlivost a konzistentnost různých studií: je třeba vzít v úvahu kvalitu zkušební metody, velikost a statistickou sílu návrhu studie, biologickou hodnověrnost, vztahy mezi dávkou a odezvou a statistické testy Cílový orgán Měl by se uvést orgán, u nějž byla pozorována rakovina. Pokud byla rakovina pozorována v několika orgánech, měl by být vybrán ten cílový orgán, u něhož nepříznivé účinky vedou k nejvyšším obavám, tj. orgán, který souvisí s deskriptorem dávky Stručný popis klíčových informací Zde by se měla uvést hlavní zjištění Diskuze V tomto oddíle by měla být uvedena interpretace výsledků. To zahrnuje například: diskuzi o potenciálních chybějících údajích, relevantnost výsledků pro posouzení rizika, například rozsah, v jakém jsou výsledky ze studie na zvířatech relevantní pro lidské zdraví Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat V tomto oddíle by se měl souhrn sledovaných vlastností porovnat s kritérii pro klasifikaci. Měly by se uvést důvody pro splnění či nesplnění kritérií klasifikace. Upozorňujeme, že klasifikace jako taková se oznamuje v oddíle 2 nástroje ICULID. 4.8 Toxicita pro reprodukci (7.8) Tento souhrn sledovaných vlastností v nástroji IUCLID zahrnuje následující části pro každou cestu expozice a zvlášť pro plodnost a vývojovou toxicitu: seznam pro výběr závěru pro tuto sledovanou vlastnost, odkaz na vybrané záznamy studií (podrobné souhrny studií) podporující tento závěr,
33 Praktický průvodce volné textové pole pro odůvodnění výběru této studie, druh deskriptoru dávky (výběr ze seznamu) a hodnota pro úroveň, při níž dochází k účinkům, zjištěná v dané studii, seznam pro výběr druhu zkoušky a seznam pro výběr druhu v dané studii, volné textové pole k charakterizaci kvality celé databáze pro tuto sledovanou vlastnost. Následující textová pole jsou k dispozici zvlášť pro plodnost a pro vývojovou toxicitu k uvedení sloučených informací pro všechny tři cesty: volné textové pole k popisu klíčových informací získaných z podrobných souhrnů studií, volné textové pole k doplnění dalšího vysvětlení a argumentů týkajících se závěrů pro tuto sledovanou vlastnost (diskuze), volné textové pole k porovnání souhrnu sledovaných vlastností s kritérii pro klasifikaci a označení, a to za účelem odůvodnění klasifikace či rozhodnutí látku neklasifikovat. Obrázek 22: Příklad ze souhrnu sledovaných vlastností v nástroji IUCLID pro toxicitu pro reprodukci Závěr o sledované vlastnosti Seznam pro výběr závěru o sledované vlastnosti je: Následující tabulka vysvětluje různé možnosti, které jsou k dispozici. Možnosti závěrů o sledované vlastnosti Pozorovány nepříznivé účinky (Adverse effects observed) Nepozorovány žádné nepříznivé účinky (No adverse effects observed) Studie není k dispozici (No study available) Kdy je tato možnost vhodná Pozorovány nepříznivé účinky na reprodukci při mezní nebo nižší dávce. Nebyly pozorovány žádné nepříznivé účinky na reprodukci při mezní nebo nižší dávce. Uveďte zdůvodnění.
34 34 Praktický průvodce 14 Studie není k dispozici (nutné další informace) (No study available (further information necessary)) Dokumentace obsahuje návrh zkoušek pro toxicitu pro reprodukci (pouze pro studie podle přílohy IX a X) Výběr sledované vlastnosti Zde lze vybrat odkaz na podrobný souhrn studie, z nějž vychází závěr o sledované vlastnosti. Prostřednictvím tohoto odkazu lze dohledat původní zdroj informací pro následné kroky posouzení a podávání zpráv. Měla by být vybrána studie, která vzbuzuje nejvyšší obavy. V zásadě by se měly použít údaje o účincích na člověka, jsou-li k dispozici. Nicméně spolehlivý deskriptor dávky se na údajích o účincích na člověka zakládá jen zřídka. Při výběru podrobného souhrnu studie se musí vzít v úvahu mimo jiné následující faktory: 1) kvalita studie, např. Klimischovo skóre, 2) trvání studie, 3) zda je studie v souladu se správnou laboratorní praxí (GLP) nebo ne. Upřednostňují se dostupné epidemiologické údaje za předpokladu, že jsou spolehlivé a relevantní Zdůvodnění výběru Zdůvodnění výběru je zapotřebí, jestliže je vybrána krátkodobá studie namísto studie dlouhodobé, studie o nízké kvalitě namísto studie o kvalitě vysoké nebo studie, která není prováděna v souladu s GLP, namísto studie prováděné v souladu s GLP Úroveň, při které dochází k účinkům Zde by se měl uvést deskriptor dávky pro specifický účinek na reprodukci. Deskriptor dávky pro ostatní účinky (např. toxicita pro matku) by měl být uveden v oddíle Stručný popis klíčových informací Druh zkoušky Dvougenerační studie (OECD 416) a prodloužená jednogenerační studie (OECD 443) se uvádějí jako subchronické studie. Studie prenatální vývojové toxicity a screeningová studie toxicity pro reprodukci (OECD 421/422) se uvádějí jako subakutní studie Druhy Druhy by měly být stejné jako ty, které byly uvedeny ve vybraném podrobném souhrnu studie Kvalita celé databáze Zde je třeba zvážit následující faktory, neboť mohou mít vliv na posouzení nebezpečnosti: Do jaké míry splňují dostupné informace jako celek požadavek nařízení REACH na údaje, který se řídí tonáží (úplnost databáze)? Spolehlivost a konzistentnost různých studií: je třeba vzít v úvahu kvalitu zkušební metody, velikost a statistickou sílu návrhu studie, biologickou hodnověrnost, vztahy mezi dávkou a odezvou a statistické testy Stručný popis klíčových informací Jelikož pro úroveň, při níž dochází k účinkům, nejsou k dispozici samostatná pole pro deskriptory dávky pro rodiče a pro potomky, měly by se oba deskriptory dávky uvést v tomto oddíle. Týká se to plodnosti i sledovaných vlastností souvisejících s vývojem.
35 Praktický průvodce Diskuze V tomto oddíle by měla být uvedena interpretace výsledků. To zahrnuje například: diskuzi o potenciálních chybějících údajích, relevantnost výsledků pro posouzení rizika, například rozsah, v jakém jsou výsledky ze studie na zvířatech relevantní pro lidské zdraví Zdůvodnění klasifikace či rozhodnutí látku neklasifikovat Zde by se měl souhrn sledovaných vlastností porovnat s kritérii pro klasifikaci. Měly by být uvedeny důvody pro splnění či nesplnění kritérií. Upozorňujeme, že klasifikace jako taková se oznamuje v oddíle 2.
Příručka pro předkládání údajů
 Příručka pro předkládání údajů Část 15 Zveřejňování informací: jak určit, které informace z registrační dokumentace budou zveřejněny na webových stránkách agentury ECHA Technická příloha pro oddíly 8,
Příručka pro předkládání údajů Část 15 Zveřejňování informací: jak určit, které informace z registrační dokumentace budou zveřejněny na webových stránkách agentury ECHA Technická příloha pro oddíly 8,
Praktický průvodce 8: Jak oznamovat změny totožnosti právnických osob
 Praktický průvodce 8: Jak oznamovat změny totožnosti právnických osob PRÁVNÍ UPOZORNĚNÍ Tento dokument obsahuje pokyny k nařízení REACH, které vysvětlují povinnosti vyplývající z tohoto nařízení a způsob
Praktický průvodce 8: Jak oznamovat změny totožnosti právnických osob PRÁVNÍ UPOZORNĚNÍ Tento dokument obsahuje pokyny k nařízení REACH, které vysvětlují povinnosti vyplývající z tohoto nařízení a způsob
Vědecký výzkum a vývoj, výzkum a vývoj zaměřený na výrobky a postupy (PPORD)
 POKYNY V KOSTCE Vědecký výzkum a vývoj, výzkum a vývoj zaměřený na výrobky a postupy (PPORD) Tento dokument si klade za cíl srozumitelným způsobem vysvětlit povinnosti, které mají žadatelé o výjimky dostupné
POKYNY V KOSTCE Vědecký výzkum a vývoj, výzkum a vývoj zaměřený na výrobky a postupy (PPORD) Tento dokument si klade za cíl srozumitelným způsobem vysvětlit povinnosti, které mají žadatelé o výjimky dostupné
Webinářpro hlavní žadatele o registraci CSA/CSR (I) 2. část nosti. 9. března George Fotakis, ECHA.
 Webinářpro hlavní žadatele o registraci CSA/CSR (I) 2. část Posouzení nebezpečnosti nosti Posouzení PBT 9. března 2010 George Fotakis, ECHA Rámec CSA Informace: k dispozici vyžadované/potřebné Posouzení
Webinářpro hlavní žadatele o registraci CSA/CSR (I) 2. část Posouzení nebezpečnosti nosti Posouzení PBT 9. března 2010 George Fotakis, ECHA Rámec CSA Informace: k dispozici vyžadované/potřebné Posouzení
Vědecký výzkum a vývoj, výzkum a vývoj zaměřený na výrobky a postupy (PPORD)
 P O K Y N Y V K O S T C E Vědecký výzkum a vývoj, výzkum a vývoj zaměřený na výrobky a postupy (PPORD) Tento dokument si klade za cíl srozumitelným způsobem vysvětlit povinnosti, které mají žadatelé o
P O K Y N Y V K O S T C E Vědecký výzkum a vývoj, výzkum a vývoj zaměřený na výrobky a postupy (PPORD) Tento dokument si klade za cíl srozumitelným způsobem vysvětlit povinnosti, které mají žadatelé o
HODNOCENÍ DLOUHODOBÉ TOXICITY ÚČINNÝCH LÁTEK A PŘÍPRAVKŮ. Petr Skácel Státní zdravotní ústav
 HODNOCENÍ DLOUHODOBÉ TOXICITY ÚČINNÝCH LÁTEK A PŘÍPRAVKŮ Petr Skácel Státní zdravotní ústav Toxikologické studie studie absorpce, distribuce, vylučování a metabolismu studie akutní toxicity, kožní a oční
HODNOCENÍ DLOUHODOBÉ TOXICITY ÚČINNÝCH LÁTEK A PŘÍPRAVKŮ Petr Skácel Státní zdravotní ústav Toxikologické studie studie absorpce, distribuce, vylučování a metabolismu studie akutní toxicity, kožní a oční
CO MŮŽE NAJÍT HYGIENIK V BEZPEČNOSTNÍCH LISTECH SMĚSÍ PRO VÝKON DOZORU
 CO MŮŽE NAJÍT HYGIENIK V BEZPEČNOSTNÍCH LISTECH SMĚSÍ PRO VÝKON DOZORU Alexandr Fuchs, SZÚ Praha 44. konzultační den SZÚ 10. listopadu 2011 OBSAH Osnova BL podle platného předpisu Klasifikace látek / komponent
CO MŮŽE NAJÍT HYGIENIK V BEZPEČNOSTNÍCH LISTECH SMĚSÍ PRO VÝKON DOZORU Alexandr Fuchs, SZÚ Praha 44. konzultační den SZÚ 10. listopadu 2011 OBSAH Osnova BL podle platného předpisu Klasifikace látek / komponent
24.4.2013. Co je ES, jak byl tvořen a k čemu slouží
 Co je ES, jak byl tvořen a k čemu slouží ES má být nástrojem k řízení rizika expozice nebezpečných chemických látek a směsí na člověka a životní prostředí. Zahrnuje kroky, které se týkají celého životního
Co je ES, jak byl tvořen a k čemu slouží ES má být nástrojem k řízení rizika expozice nebezpečných chemických látek a směsí na člověka a životní prostředí. Zahrnuje kroky, které se týkají celého životního
Jak použít údaje ze studií in vitro ke splně ní požadavků na informace dle nařízení REACH. Webinářo požadavcích na informace 30.
 Jak použít údaje ze studií in vitro ke splně ní požadavků na informace dle nařízení REACH Webinářo požadavcích na informace 30. listopadu 2009 Přehled Nařízení REACH a zkoušky in vitro Kritéria pro použití
Jak použít údaje ze studií in vitro ke splně ní požadavků na informace dle nařízení REACH Webinářo požadavcích na informace 30. listopadu 2009 Přehled Nařízení REACH a zkoušky in vitro Kritéria pro použití
Pokyny pro monomery a polymery
 POKYNY Pokyny pro monomery a polymery duben 2012 Verze 2.0 Pokyny pro provádění nařízení REACH Annankatu 18, P.O. Box 400, FI-00121 Helsinki, Finsko Tel. +358 9 686180 Fax +358 9 68618210 echa.europa.eu
POKYNY Pokyny pro monomery a polymery duben 2012 Verze 2.0 Pokyny pro provádění nařízení REACH Annankatu 18, P.O. Box 400, FI-00121 Helsinki, Finsko Tel. +358 9 686180 Fax +358 9 68618210 echa.europa.eu
Zjišťování toxicity látek
 Zjišťování toxicity látek 1. Úvod 2. Literární údaje 3. Testy in vitro 4. Testy na zvířatech in vivo 5. Epidemiologické studie 6. Zjišťování úrovně expozice Úvod Je známo 2 10 7 chemických látek. Prostudování
Zjišťování toxicity látek 1. Úvod 2. Literární údaje 3. Testy in vitro 4. Testy na zvířatech in vivo 5. Epidemiologické studie 6. Zjišťování úrovně expozice Úvod Je známo 2 10 7 chemických látek. Prostudování
Praktický průvodce 4: Jak oznamovat upuštění od požadavku na údaje
 Praktický průvodce 4: Jak oznamovat upuštění od požadavku na údaje PRÁVNÍ UPOZORNĚNÍ Informace uvedené v tomto praktickém průvodci nepředstavují právní poradenství a z právního hlediska nepředstavují nezbytně
Praktický průvodce 4: Jak oznamovat upuštění od požadavku na údaje PRÁVNÍ UPOZORNĚNÍ Informace uvedené v tomto praktickém průvodci nepředstavují právní poradenství a z právního hlediska nepředstavují nezbytně
Posouzení chemické bezpečnosti
 Pokyny v kostce Posouzení chemické bezpečnosti Cílem tohoto dokumentu je jednoduše vysvětlit požadavky podle nařízení REACH, které se týkají posouzení chemické bezpečnosti PRÁVNÍ OZNÁMENÍ Tento dokument
Pokyny v kostce Posouzení chemické bezpečnosti Cílem tohoto dokumentu je jednoduše vysvětlit požadavky podle nařízení REACH, které se týkají posouzení chemické bezpečnosti PRÁVNÍ OZNÁMENÍ Tento dokument
Úřední věstník Evropské unie L 69/7
 16.3.2011 Úřední věstník Evropské unie L 69/7 NAŘÍZENÍ KOMISE (EU) č. 253/2011 ze dne 15. března 2011, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 o registraci, hodnocení, povolování
16.3.2011 Úřední věstník Evropské unie L 69/7 NAŘÍZENÍ KOMISE (EU) č. 253/2011 ze dne 15. března 2011, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 o registraci, hodnocení, povolování
Aplikaci IUCLID vytvořila Evropská agentura pro chemické látky ve spolupráci s organizací OECD.
 Aplikaci IUCLID vytvořila Evropská agentura pro chemické látky ve spolupráci s organizací OECD. Právní upozornění Informace v tomto dokumentu nepředstavují právní poradenství. Za způsob využití těchto
Aplikaci IUCLID vytvořila Evropská agentura pro chemické látky ve spolupráci s organizací OECD. Právní upozornění Informace v tomto dokumentu nepředstavují právní poradenství. Za způsob využití těchto
(Nelegislativní akty) NAŘÍZENÍ
 17.11.2017 L 301/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) 2017/2100 ze dne 4. září 2017, kterým se stanoví vědecká kritéria pro určení vlastností vyvolávajících narušení
17.11.2017 L 301/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) 2017/2100 ze dne 4. září 2017, kterým se stanoví vědecká kritéria pro určení vlastností vyvolávajících narušení
Delegace naleznou v příloze dokument D033542/02 - ANNEX.
 Rada Evropské unie Brusel 14. července 2014 (OR. en) 11888/14 ADD 1 ENV 672 ENT 161 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 11. července 2014 Příjemce: Předmět: Generální sekretariát
Rada Evropské unie Brusel 14. července 2014 (OR. en) 11888/14 ADD 1 ENV 672 ENT 161 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 11. července 2014 Příjemce: Předmět: Generální sekretariát
Aktuální informace k REACH a GHS. Ing. Šárka Klimešová Výzkumný ústav maltovin Praha, s.r.o. Skalský Dvůr, 25. 27.5.2009
 Aktuální informace k REACH a GHS Ing. Šárka Klimešová Výzkumný ústav maltovin Praha, s.r.o. Skalský Dvůr, 25. 27.5.2009 REACH Nařízení (Regulation) Evropského parlamentu a Rady (ES) 1907/2006 ze dne 18.prosince
Aktuální informace k REACH a GHS Ing. Šárka Klimešová Výzkumný ústav maltovin Praha, s.r.o. Skalský Dvůr, 25. 27.5.2009 REACH Nařízení (Regulation) Evropského parlamentu a Rady (ES) 1907/2006 ze dne 18.prosince
Klasifikace směsí. Ing. Hana Krejsová. Tel.:
 Klasifikace směsí Ing. Hana Krejsová Tel.: 724278705 H.krejsova@seznam.cz Klasifikace akutní toxicity Akutní toxicita nepříznivé účinky k nimž dojde po aplikaci jedné dávky nebo vícenásobné dávky látky
Klasifikace směsí Ing. Hana Krejsová Tel.: 724278705 H.krejsova@seznam.cz Klasifikace akutní toxicity Akutní toxicita nepříznivé účinky k nimž dojde po aplikaci jedné dávky nebo vícenásobné dávky látky
CZ.1.07/1.5.00/34.0880. pracovní list. Hygiena a toxikologie. Experimentální toxikologie. Mgr. Alexandra Šlegrová
 Název školy Číslo projektu STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková organizace CZ.1.07/1.5.00/34.0880 Název projektu Klíčová aktivita Označení materiálu:
Název školy Číslo projektu STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková organizace CZ.1.07/1.5.00/34.0880 Název projektu Klíčová aktivita Označení materiálu:
Seminář Běžný podnik: povinnosti a bezpečnost práce při nakládání s chem. látkami. 11. 4. 2013 - Praha
 www.envigroup.cz www.ekonoviny.cz Aktuální semináře EKOnovin naleznete na internetu www.ekonoviny.cz Seminář Běžný podnik: povinnosti a bezpečnost práce při nakládání s chem. látkami Hlavní témata semináře:
www.envigroup.cz www.ekonoviny.cz Aktuální semináře EKOnovin naleznete na internetu www.ekonoviny.cz Seminář Běžný podnik: povinnosti a bezpečnost práce při nakládání s chem. látkami Hlavní témata semináře:
NAŘÍZENÍ KOMISE (EU) /... ze dne ,
 EVROPSKÁ KOMISE V Bruselu dne 3.12.2018 C(2018) 7942 final NAŘÍZENÍ KOMISE (EU) /... ze dne 3.12.2018, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 o registraci, hodnocení, povolování
EVROPSKÁ KOMISE V Bruselu dne 3.12.2018 C(2018) 7942 final NAŘÍZENÍ KOMISE (EU) /... ze dne 3.12.2018, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 o registraci, hodnocení, povolování
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: McFarlandův standard zákalu 1.3 Identifikace
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: McFarlandův standard zákalu 1.3 Identifikace
Příručka pro průmyslového uživatele nástroje REACH-IT
 Příručka pro průmyslového uživatele nástroje REACH-IT Část 09 Rozšířené vyhledávání Annankatu 18, P.O. Box 400, FI-00121 Helsinki, Finland Tel. +358 9 686180 Fax +358 9 68618210 echa.europa.eu 2 Příručka
Příručka pro průmyslového uživatele nástroje REACH-IT Část 09 Rozšířené vyhledávání Annankatu 18, P.O. Box 400, FI-00121 Helsinki, Finland Tel. +358 9 686180 Fax +358 9 68618210 echa.europa.eu 2 Příručka
Chesar Koncepce a celkový popis aplikace
 Chesar Koncepce a celkový popis aplikace 26. března 2010 Chesar - koncepce a celkový popis Zaměření a oblast použití aplikace Chesar Organizace a nástroje šest skupin funkcí Obecné pracovní postupy v aplikace
Chesar Koncepce a celkový popis aplikace 26. března 2010 Chesar - koncepce a celkový popis Zaměření a oblast použití aplikace Chesar Organizace a nástroje šest skupin funkcí Obecné pracovní postupy v aplikace
Identifikace a pojmenovávání látek podle nařízení REACH a CLP
 P O K Y N Y V K O S T C E Identifikace a pojmenovávání látek podle nařízení REACH a Dokument stručně vysvětluje hlavní principy identifikace a pojmenovávání látek Verze 2.0 duben 2017 2 Pokyny v kostce
P O K Y N Y V K O S T C E Identifikace a pojmenovávání látek podle nařízení REACH a Dokument stručně vysvětluje hlavní principy identifikace a pojmenovávání látek Verze 2.0 duben 2017 2 Pokyny v kostce
2006R1907 CS 05.06.2012 013.001 89. Obecné otázky
 2006R1907 CS 05.06.2012 013.001 89 HLAVA VIII OMEZENÍ VÝROBY, UVÁDĚNÍ NA TRH A POUŽÍVÁNÍ NĚKTERÝCH NEBEZPEČNÝCH LÁTEK, M3 SMĚSÍ A PŘEDMĚTŮ KAPITOLA 1 Obecné otázky Článek 67 Obecná ustanovení 1. Látka
2006R1907 CS 05.06.2012 013.001 89 HLAVA VIII OMEZENÍ VÝROBY, UVÁDĚNÍ NA TRH A POUŽÍVÁNÍ NĚKTERÝCH NEBEZPEČNÝCH LÁTEK, M3 SMĚSÍ A PŘEDMĚTŮ KAPITOLA 1 Obecné otázky Článek 67 Obecná ustanovení 1. Látka
Pokyny v kostce Identifikace a pojmenovávání látek podle nařízení REACH a CLP
 Pokyny v kostce Identifikace a pojmenovávání látek podle nařízení REACH a CLP Nejaktuálnější informace ohledně posouzení chemické bezpečnosti naleznete na internetových stránkách agentury ECHA. PRÁVNÍ
Pokyny v kostce Identifikace a pojmenovávání látek podle nařízení REACH a CLP Nejaktuálnější informace ohledně posouzení chemické bezpečnosti naleznete na internetových stránkách agentury ECHA. PRÁVNÍ
Cif Professional Window & Multi Surface Revize: Verze: 02.0
 Cif Professional Window & Multi Surface Revize: 20150109 Verze: 02.0 1.1 Identifikátor výrobku Obchodní název: Cif Professional Window & Multi Surface Diversey Europe Operations BV, Maarssenbroeksedijk
Cif Professional Window & Multi Surface Revize: 20150109 Verze: 02.0 1.1 Identifikátor výrobku Obchodní název: Cif Professional Window & Multi Surface Diversey Europe Operations BV, Maarssenbroeksedijk
Oznámení o zahájení nabídkového řízení pro výběr dopravce k uzavření smlouvy o veřejných službách v přepravě cestujících
 Metodické pokyny a validační pravidla pro vyplnění formuláře Oznámení o zahájení nabídkového řízení pro výběr dopravce k uzavření smlouvy o veřejných službách v přepravě cestujících Vydání Schváleno Ministerstvem
Metodické pokyny a validační pravidla pro vyplnění formuláře Oznámení o zahájení nabídkového řízení pro výběr dopravce k uzavření smlouvy o veřejných službách v přepravě cestujících Vydání Schváleno Ministerstvem
(Text s významem pro EHP)
 19.12.2014 L 365/89 NAŘÍZENÍ KOMISE (EU) č. 1357/2014 ze dne 18. prosince 2014, kterým se nahrazuje příloha III směrnice Evropského parlamentu a Rady 2008/98/ES o odpadech a o zrušení některých směrnic
19.12.2014 L 365/89 NAŘÍZENÍ KOMISE (EU) č. 1357/2014 ze dne 18. prosince 2014, kterým se nahrazuje příloha III směrnice Evropského parlamentu a Rady 2008/98/ES o odpadech a o zrušení některých směrnic
Příručka pro průmyslového uživatele nástroje REACH-IT
 Příručka pro průmyslového uživatele nástroje REACH- IT Část 10 Žádost o registrační číslo pro oznámenou látku Příručka pro průmyslového uživatele nástroje REACH-IT Část 10 Žádost o registrační číslo pro
Příručka pro průmyslového uživatele nástroje REACH- IT Část 10 Žádost o registrační číslo pro oznámenou látku Příručka pro průmyslového uživatele nástroje REACH-IT Část 10 Žádost o registrační číslo pro
Klasifikace látek a směsí
 Klasifikace látek a směsí Dle nařízení EP a Rady EU 1272/2008/EC (CLP) Ing. Hana Krejsová Výzkumný ústav organických syntéz a.s. Centrum ekologie, toxikologie a analytiky Rybitví č.p. 296, Rybitví 533
Klasifikace látek a směsí Dle nařízení EP a Rady EU 1272/2008/EC (CLP) Ing. Hana Krejsová Výzkumný ústav organických syntéz a.s. Centrum ekologie, toxikologie a analytiky Rybitví č.p. 296, Rybitví 533
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Hotová kultivační média ve zkumavkách. 1.3 Identifikace společnosti
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Hotová kultivační média ve zkumavkách. 1.3 Identifikace společnosti
Jak komunikovat s agenturou ECHA při hodnocení dokumentace. Praktický průvodce 12
 Jak komunikovat s agenturou ECHA při hodnocení dokumentace Praktický průvodce 12 2 Jak komunikovat s agenturou ECHA při hodnocení dokumentace PRÁVNÍ UPOZORNĚNÍ Tento dokument obsahuje pokyny týkající se
Jak komunikovat s agenturou ECHA při hodnocení dokumentace Praktický průvodce 12 2 Jak komunikovat s agenturou ECHA při hodnocení dokumentace PRÁVNÍ UPOZORNĚNÍ Tento dokument obsahuje pokyny týkající se
Suma Calc D5 Revize: Verze: 04.0
 Suma Calc D5 Revize: 2014-11-26 Verze: 04.0 1.1 Identifikátor výrobku Obchodní název: Suma Calc D5 Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands Kontaktní údaje
Suma Calc D5 Revize: 2014-11-26 Verze: 04.0 1.1 Identifikátor výrobku Obchodní název: Suma Calc D5 Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands Kontaktní údaje
Pokyny k požadavkům na informace a posouzení chemické bezpečnosti
 Pokyny k požadavkům na informace a posouzení chemické bezpečnosti Formát scénáře expozice v části D : Vypracování scénáře expozice v části F : Formát CSR Verze: 2.1 listopad 2012 PRÁVNÍ UPOZORNĚNÍ Tento
Pokyny k požadavkům na informace a posouzení chemické bezpečnosti Formát scénáře expozice v části D : Vypracování scénáře expozice v části F : Formát CSR Verze: 2.1 listopad 2012 PRÁVNÍ UPOZORNĚNÍ Tento
Datum vydání: Strana: 1 / 7 Datum revize: - nahrazuje revizi ze dne: - Název výrobku:
 Datum vydání: 1.12.2013 Strana: 1 / 7 BEZPEČNOSTNÍ LIST dle nařízení (ES) č. 1907/2006 ve znění nařízení (EU) č. 453/2010 1. IDENTIFIKACE LÁTKY NEBO SMĚSI A SPOLEČNOSTI NEBO PODNIKU 1.1 Identifikátor výrobku
Datum vydání: 1.12.2013 Strana: 1 / 7 BEZPEČNOSTNÍ LIST dle nařízení (ES) č. 1907/2006 ve znění nařízení (EU) č. 453/2010 1. IDENTIFIKACE LÁTKY NEBO SMĚSI A SPOLEČNOSTI NEBO PODNIKU 1.1 Identifikátor výrobku
VYHLÁŠKA č. 220/2004 Sb. ze dne 14. dubna 2004, kterou se stanoví náležitosti oznamování nebezpečných chemických látek a vedení jejich evidence
 VYHLÁŠKA č. 220/2004 Sb. ze dne 14. dubna 2004, kterou se stanoví náležitosti oznamování nebezpečných chemických látek a vedení jejich evidence Ministerstvo životního prostředí (dále jen "ministerstvo")
VYHLÁŠKA č. 220/2004 Sb. ze dne 14. dubna 2004, kterou se stanoví náležitosti oznamování nebezpečných chemických látek a vedení jejich evidence Ministerstvo životního prostředí (dále jen "ministerstvo")
Pokyny k požadavkům na informace a posuzování chemické bezpečnosti. Kapitola R.5: Přizpůsobení požadavků na informace
 Pokyny k požadavkům na informace a posuzování chemické bezpečnosti Kapitola R.5: Přizpůsobení požadavků na informace Verze: 2.1 Prosinec 2011 PRÁVNÍ UPOZORNĚNÍ Tento dokument obsahuje pokyny k nařízení
Pokyny k požadavkům na informace a posuzování chemické bezpečnosti Kapitola R.5: Přizpůsobení požadavků na informace Verze: 2.1 Prosinec 2011 PRÁVNÍ UPOZORNĚNÍ Tento dokument obsahuje pokyny k nařízení
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Pro vývoj atmosféry s nízkým obsahem
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Pro vývoj atmosféry s nízkým obsahem
Role zkoušek na zvířatech v rámci zajišťování bezpečného používání chemických látek
 REACH Informační list ECHA-12-FS-08-CS Role zkoušek na zvířatech v rámci zajišťování bezpečného používání chemických látek Cílem nařízení REACH je zajistit vysoký stupeň ochrany lidského zdraví a životního
REACH Informační list ECHA-12-FS-08-CS Role zkoušek na zvířatech v rámci zajišťování bezpečného používání chemických látek Cílem nařízení REACH je zajistit vysoký stupeň ochrany lidského zdraví a životního
Bezpečnostní list návod na úpravu
 Bezpečnostní list návod na úpravu Ing. Hana Krejsová Výzkumný ústav organických syntéz a.s. Bezpečnostní list návod Od 1.12.2012 musí být bezpečnostní listy na směsi v souladu s povinným formátem podle
Bezpečnostní list návod na úpravu Ing. Hana Krejsová Výzkumný ústav organických syntéz a.s. Bezpečnostní list návod Od 1.12.2012 musí být bezpečnostní listy na směsi v souladu s povinným formátem podle
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo K detekci cytochromoxidasy. 1.3 Identifikace společnosti
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo K detekci cytochromoxidasy. 1.3 Identifikace společnosti
Domestos Professional Pine Fresh Revize: Verze: 01.0
 Domestos Professional Pine Fresh Revize: 20150521 Verze: 01.0 1.1 Identifikátor výrobku Obchodní název: Domestos Professional Pine Fresh Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht,
Domestos Professional Pine Fresh Revize: 20150521 Verze: 01.0 1.1 Identifikátor výrobku Obchodní název: Domestos Professional Pine Fresh Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht,
Klasifikace alergenů z pohledu právních předpisů
 Klasifikace alergenů z pohledu právních předpisů M. Hornychová Státní zdravotní ústav mhornych@szu.cz 22. konzultační den CPL, 17. 4. 2008 Základní pojmy 2 zákona č. 356/2003 Sb. Klasifikace je postup
Klasifikace alergenů z pohledu právních předpisů M. Hornychová Státní zdravotní ústav mhornych@szu.cz 22. konzultační den CPL, 17. 4. 2008 Základní pojmy 2 zákona č. 356/2003 Sb. Klasifikace je postup
Jak oznamovat látky do seznamu klasifikací a označení
 Annankatu 18, P.O. Box 400, FI-00121 Helsinki, Finland Tel. +358 9 686180 Fax +358 9 68618210 echa.europa.eu Jak oznamovat látky do seznamu klasifikací a označení Praktický průvodce 7 červen 2012 Praktický
Annankatu 18, P.O. Box 400, FI-00121 Helsinki, Finland Tel. +358 9 686180 Fax +358 9 68618210 echa.europa.eu Jak oznamovat látky do seznamu klasifikací a označení Praktický průvodce 7 červen 2012 Praktický
Suma Inox Classic D7 Revize: Verze: 05.0
 Suma Inox Classic D7 Revize: 2015-05-25 Verze: 05.0 1.1 Identifikátor výrobku Obchodní název: Suma Inox Classic D7 Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands
Suma Inox Classic D7 Revize: 2015-05-25 Verze: 05.0 1.1 Identifikátor výrobku Obchodní název: Suma Inox Classic D7 Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands
PŘÍLOHA. 1. Příloha I nařízení (ES) č. 1907/2006 se mění takto:
 CS PŘÍLOHA 1. Příloha I nařízení (ES) č. 1907/2006 se mění takto: a) Pododdíl 0.1 se nahrazuje tímto: 0.1 Účelem této přílohy je stanovit, jak mají výrobci a dovozci posuzovat a prokazovat, že rizika plynoucí
CS PŘÍLOHA 1. Příloha I nařízení (ES) č. 1907/2006 se mění takto: a) Pododdíl 0.1 se nahrazuje tímto: 0.1 Účelem této přílohy je stanovit, jak mají výrobci a dovozci posuzovat a prokazovat, že rizika plynoucí
Revize: Verze: Identifikátor výrobku Obchodní název:
 Revize: 20150416 Verze: 01.0 1.1 Identifikátor výrobku Obchodní název: Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands Kontaktní údaje TEL: 296357111, FAX: 296357112
Revize: 20150416 Verze: 01.0 1.1 Identifikátor výrobku Obchodní název: Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands Kontaktní údaje TEL: 296357111, FAX: 296357112
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Selektivní suplement ke kultivačním
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Selektivní suplement ke kultivačním
Suma Special L4 Revize: 2014-11-11 Verze: 05.0
 Suma Special L4 Revize: 2014-11-11 Verze: 05.0 1.1 Identifikátor výrobku Obchodní název: Suma Special L4 Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands Kontaktní
Suma Special L4 Revize: 2014-11-11 Verze: 05.0 1.1 Identifikátor výrobku Obchodní název: Suma Special L4 Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands Kontaktní
Bezpečnost chemických výrob N Petr Zámostný místnost: A-72a tel.:
 Bezpečnost chemických výrob N1111 Petr Zámostný místnost: A-72a tel.: 4222 e-mail: petr.zamostny@vscht.cz Rizika spojená s toxickými látkami Toxicita látek Zákonné limity pro práci s toxickými látkami
Bezpečnost chemických výrob N1111 Petr Zámostný místnost: A-72a tel.: 4222 e-mail: petr.zamostny@vscht.cz Rizika spojená s toxickými látkami Toxicita látek Zákonné limity pro práci s toxickými látkami
Registrace chemických látek v rámci nařízení REACH
 Registrace chemických látek v rámci nařízení REACH Daniela Bittnerová ReachSpektrum, s.r.o., Dělnická 12, Praha 7 Daniela.Bittnerova@reachspektrum.eu tel.: 266 793 591 Nařízení REACH Nařízení Evropského
Registrace chemických látek v rámci nařízení REACH Daniela Bittnerová ReachSpektrum, s.r.o., Dělnická 12, Praha 7 Daniela.Bittnerova@reachspektrum.eu tel.: 266 793 591 Nařízení REACH Nařízení Evropského
Návrh vyhlášky o rozsahu informací poskytovaných o chemických směsích, které mají některé nebezpečné vlastnosti, a detergentech
 Návrh vyhlášky o rozsahu informací poskytovaných o chemických směsích, které mají některé nebezpečné vlastnosti, a detergentech CHLaP Ing. Hana Krejsová Tel.: 466 823 219 Mobil: 724 400 555 E-mail: hana.krejsova@vuos.com
Návrh vyhlášky o rozsahu informací poskytovaných o chemických směsích, které mají některé nebezpečné vlastnosti, a detergentech CHLaP Ing. Hana Krejsová Tel.: 466 823 219 Mobil: 724 400 555 E-mail: hana.krejsova@vuos.com
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Pro detekci koagulázy ve stafylokocích
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Pro detekci koagulázy ve stafylokocích
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006) Datum vydání: 23. 08.
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Vyvíječ anaerobní atmosféry, 3,5 l. 1.3 Identifikace společnosti
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Vyvíječ anaerobní atmosféry, 3,5 l. 1.3 Identifikace společnosti
Bezpečnostnílist DleNařízeníEvropskéhoparlamentuaRady(ES)č.1907/2006
 Bezpečnostnílist DleNařízeníEvropskéhoparlamentuaRady(ES)č.1907/2006 Suma Inox Classic D7 Revize: 2015-05-25 Verze: 05.0 ODDÍL1:Identifikacelátky/směsiaspolečnosti/podniku 1.1 Identifikátor výrobku Obchodní
Bezpečnostnílist DleNařízeníEvropskéhoparlamentuaRady(ES)č.1907/2006 Suma Inox Classic D7 Revize: 2015-05-25 Verze: 05.0 ODDÍL1:Identifikacelátky/směsiaspolečnosti/podniku 1.1 Identifikátor výrobku Obchodní
Rozšířený BL expoziční scénáře
 Rozšířený BL expoziční scénáře EXPOZIČNÍ SCÉNÁŘE HODNOCENÍ RIZIKA Ing. Hana Krejsová Tel: 724278705 H. Krejsova@seznam.cz Kdy se sestavuje bezpečnostní list? Pozor na směsi v obalu Látka je klasifikována
Rozšířený BL expoziční scénáře EXPOZIČNÍ SCÉNÁŘE HODNOCENÍ RIZIKA Ing. Hana Krejsová Tel: 724278705 H. Krejsova@seznam.cz Kdy se sestavuje bezpečnostní list? Pozor na směsi v obalu Látka je klasifikována
Forma elektronické podoby informací o nebezpečných směsích a detergentech a datovém rozhraní
 Příloha č. 2 k metodickému pokynu MZ k vyhlášce č. 61/2013 Sb. Forma elektronické podoby informací o nebezpečných směsích a detergentech a datovém rozhraní Tento dokument popisuje strukturu datového rozhraní
Příloha č. 2 k metodickému pokynu MZ k vyhlášce č. 61/2013 Sb. Forma elektronické podoby informací o nebezpečných směsích a detergentech a datovém rozhraní Tento dokument popisuje strukturu datového rozhraní
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Disky pro testování citlivosti na antibiotika.
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Disky pro testování citlivosti na antibiotika.
Pokyny k požadavkům na informace a posouzení chemické bezpečnosti Část B: Posouzení nebezpečnosti
 Pokyny k požadavkům na informace a posouzení chemické bezpečnosti Část B: Posouzení nebezpečnosti Verze 2.1 Prosinec 2011 1 PRÁVNÍ UPOZORNĚNÍ Tento dokument obsahuje pokyny k nařízení REACH, které vysvětlují
Pokyny k požadavkům na informace a posouzení chemické bezpečnosti Část B: Posouzení nebezpečnosti Verze 2.1 Prosinec 2011 1 PRÁVNÍ UPOZORNĚNÍ Tento dokument obsahuje pokyny k nařízení REACH, které vysvětlují
OBECNÉ POKYNY K TESTŮM, PŘEZKUMŮM NEBO VÝKONŮM, KTERÉ MOHOU VÉST K PODPŮRNÝM OPATŘENÍM EBA/GL/2014/ září 2014
 EBA/GL/2014/09 22. září 2014 Obecné pokyny k druhům testů, přezkumů nebo výkonů, které mohou vést k podpůrným opatřením podle čl. 32 odst. 4 písm. d) bodu iii) směrnice o ozdravných postupech a řešení
EBA/GL/2014/09 22. září 2014 Obecné pokyny k druhům testů, přezkumů nebo výkonů, které mohou vést k podpůrným opatřením podle čl. 32 odst. 4 písm. d) bodu iii) směrnice o ozdravných postupech a řešení
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Selektivní suplement ke kultivačním
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Selektivní suplement ke kultivačním
BEZPECNOSTNÍ LIST. (v souladu s narízením Komise (EU) c. 453/2010) ODDÍL 1: Identifikace látky/smesi a spolecnosti/podniku
 BEZPECNOSTNÍ LIST (v souladu s narízením Komise (EU) c. 453/2010) Identifikátor výrobku ODDÍL 1: Identifikace látky/smesi a spolecnosti/podniku Kód produktu 100034649 Název výrobku PLATE, C-MET SOLUBLE
BEZPECNOSTNÍ LIST (v souladu s narízením Komise (EU) c. 453/2010) Identifikátor výrobku ODDÍL 1: Identifikace látky/smesi a spolecnosti/podniku Kód produktu 100034649 Název výrobku PLATE, C-MET SOLUBLE
Sestavování bezpečnostních listů
 P O K Y N Y V K O S T C E Sestavování bezpečnostních listů Tento dokument si klade za cíl jednoduchou formou vysvětlit hlavní zásady a povinnosti týkající se sestavování a poskytování bezpečnostních listů
P O K Y N Y V K O S T C E Sestavování bezpečnostních listů Tento dokument si klade za cíl jednoduchou formou vysvětlit hlavní zásady a povinnosti týkající se sestavování a poskytování bezpečnostních listů
Informace od výrobce (dovozce) pro vypracování Zprávy o bezpečnosti kosmetického přípravku (ZBKP) dle Nařízení ES č. 1223/2009
 Informace od výrobce (dovozce) pro vypracování Zprávy o bezpečnosti kosmetického přípravku (ZBKP) dle Nařízení ES č. 1223/2009 Název hodnoceného výrobku: Odpovědná osoba (Název, adresa, IČ): 1. Kvantitativní
Informace od výrobce (dovozce) pro vypracování Zprávy o bezpečnosti kosmetického přípravku (ZBKP) dle Nařízení ES č. 1223/2009 Název hodnoceného výrobku: Odpovědná osoba (Název, adresa, IČ): 1. Kvantitativní
BEZPEČNOSTNÍ LIST. (podle nařízení (ES) č. 453/2010) AGRO CS a.s.
 Verze č.: 1.1 Vydaná: 19. 6. 2014 Nahrazuje verzi č.: 1.0 BEZPEČNOSTNÍ LIST (podle nařízení (ES) č. 453/2010) Oddíl 1: IDENTIFIKACE LÁTKY / SMĚSI A SPOLEČNOSTI / PODNIKU 1.1 Identifikátor výrobku: Chemický
Verze č.: 1.1 Vydaná: 19. 6. 2014 Nahrazuje verzi č.: 1.0 BEZPEČNOSTNÍ LIST (podle nařízení (ES) č. 453/2010) Oddíl 1: IDENTIFIKACE LÁTKY / SMĚSI A SPOLEČNOSTI / PODNIKU 1.1 Identifikátor výrobku: Chemický
Vybrané předpisy EU vztahující se k chemické bezpečnosti. Mirka Hornychová Státní zdravotní ústav
 Vybrané předpisy EU vztahující se k chemické bezpečnosti Mirka Hornychová Státní zdravotní ústav CHEMICKÉ LÁTKY TRH nařízen zení 1907/2006 REACH nařízen zení 1272/2008 CLP nařízen zení 689/2008 dovoz a
Vybrané předpisy EU vztahující se k chemické bezpečnosti Mirka Hornychová Státní zdravotní ústav CHEMICKÉ LÁTKY TRH nařízen zení 1907/2006 REACH nařízen zení 1272/2008 CLP nařízen zení 689/2008 dovoz a
Pronto Wood Polish Natural Revize: Verze: 03.0
 Pronto Wood Polish Natural Revize: 20150405 Verze: 03.0 1.1 Identifikátor výrobku Obchodní název: Pronto Wood Polish Natural Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands
Pronto Wood Polish Natural Revize: 20150405 Verze: 03.0 1.1 Identifikátor výrobku Obchodní název: Pronto Wood Polish Natural Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Selektivní suplement ke kultivačním
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Selektivní suplement ke kultivačním
: Prilocaine. Bezpečnostní list Bezpečnostní list podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0
 podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku Název látky : Látka : Prilocaine
podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku Název látky : Látka : Prilocaine
příslušné registraci prosinec Úvod Identifikace látky jedná se o polymer nebo ne?... 4
 1 (17) Název dokumentu Jak určit, zda je látka polymer Obsah 1. Úvod... 2 2. Identifikace látky jedná se o polymer nebo ne?... 4 2.1. Úvod výroba (případného) polymeru... 4 2.2. Co je to polymer?... 5
1 (17) Název dokumentu Jak určit, zda je látka polymer Obsah 1. Úvod... 2 2. Identifikace látky jedná se o polymer nebo ne?... 4 2.1. Úvod výroba (případného) polymeru... 4 2.2. Co je to polymer?... 5
OZNÁMENÍ O OTEVŘENÝCH VÝBĚROVÝCH ŘÍZENÍCH (2011/C 198 A/02)
 C 198 A/6 CS Úřední věstník Evropské unie 6.7.2011 OZNÁMENÍ O OTEVŘENÝCH VÝBĚROVÝCH ŘÍZENÍCH (2011/C 198 A/02) Máte zájem o profesní dráhu v orgánech a institucích EU? Splňuje váš profil naše kritéria?
C 198 A/6 CS Úřední věstník Evropské unie 6.7.2011 OZNÁMENÍ O OTEVŘENÝCH VÝBĚROVÝCH ŘÍZENÍCH (2011/C 198 A/02) Máte zájem o profesní dráhu v orgánech a institucích EU? Splňuje váš profil naše kritéria?
Bezpečnostní list Bezpečnostní list podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0
 Datum vydání: 31/05/2017 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku Název látky : Látka : Salmeterol Kód výrobku : 201600811 Synonyma Další
Datum vydání: 31/05/2017 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku Název látky : Látka : Salmeterol Kód výrobku : 201600811 Synonyma Další
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Hotová kultivační média na Petriho miskách. 1.3 Identifikace
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Hotová kultivační média na Petriho miskách. 1.3 Identifikace
Otázky a odpovědi. týkající se dotazování a identifikace látky
 Otázky a odpovědi 2 Otázky a odpovědi PRÁVNÍ UPOZORNĚNÍ Tento dokument otázek a odpovědí obsahuje informace o povinnostech vyplývajících z nařízení REACH (dále jen REACH nebo nařízení REACH) a vysvětluje,
Otázky a odpovědi 2 Otázky a odpovědi PRÁVNÍ UPOZORNĚNÍ Tento dokument otázek a odpovědí obsahuje informace o povinnostech vyplývajících z nařízení REACH (dále jen REACH nebo nařízení REACH) a vysvětluje,
č. 402/2011 Sb. VYHLÁŠKA o hodnocení nebezpečných vlastností chemických látek a chemických směsí a balení a označování nebezpečných chemických směsí
 č. 402/2011 Sb. VYHLÁŠKA ze dne 8. prosince 2011 o hodnocení nebezpečných vlastností chemických látek a chemických směsí a balení a označování nebezpečných chemických směsí Ministerstvo průmyslu a obchodu
č. 402/2011 Sb. VYHLÁŠKA ze dne 8. prosince 2011 o hodnocení nebezpečných vlastností chemických látek a chemických směsí a balení a označování nebezpečných chemických směsí Ministerstvo průmyslu a obchodu
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Selektivní suplement ke kultivačním
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Selektivní suplement ke kultivačním
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU * 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Vyvíječ atmosféry pro mikroaerofilní
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU * 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Vyvíječ atmosféry pro mikroaerofilní
Využití rozptylových studií pro hodnocení zdravotních rizik. MUDr.Helena Kazmarová Státní zdravotní ústav Praha
 Využití rozptylových studií pro hodnocení zdravotních rizik MUDr.Helena Kazmarová Státní zdravotní ústav Praha Obsah Hodnocení zdravotních rizik Expozice Popis imisní situace možnosti a problémy Rozptylové
Využití rozptylových studií pro hodnocení zdravotních rizik MUDr.Helena Kazmarová Státní zdravotní ústav Praha Obsah Hodnocení zdravotních rizik Expozice Popis imisní situace možnosti a problémy Rozptylové
Bezpečnost chemických výrob N111001
 8.11.21 Bezpečnost chemických výrob N1111 Petr Zámostný místnost: A-72a tel.: 4222 e-mail: petr.zamostny@vscht.cz Rizika spojená s toxickými látkami Toxicita látek Zákonné limity pro práci s toxickými
8.11.21 Bezpečnost chemických výrob N1111 Petr Zámostný místnost: A-72a tel.: 4222 e-mail: petr.zamostny@vscht.cz Rizika spojená s toxickými látkami Toxicita látek Zákonné limity pro práci s toxickými
Návrh ROZHODNUTÍ RADY. o uplatňování ustanovení schengenského acquis v oblasti Schengenského informačního systému v Chorvatské republice
 EVROPSKÁ KOMISE V Bruselu dne 18.1.2017 COM(2017) 17 final 2017/0011 (NLE) Návrh ROZHODNUTÍ RADY o uplatňování ustanovení schengenského acquis v oblasti Schengenského informačního systému v Chorvatské
EVROPSKÁ KOMISE V Bruselu dne 18.1.2017 COM(2017) 17 final 2017/0011 (NLE) Návrh ROZHODNUTÍ RADY o uplatňování ustanovení schengenského acquis v oblasti Schengenského informačního systému v Chorvatské
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Referenční kmeny pro kontrolu kvality
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo přípravku: Obchodní název: Další názvy látky: - 1.2 Použití látky nebo přípravku: Referenční kmeny pro kontrolu kvality
Bezpečnostní list Bezpečnostní list podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0
 podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku Název látky : Látka : Prednisolone
podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku Název látky : Látka : Prednisolone
DOKUMENTACE K ŽÁDOSTI
 1 KAPITOLA IV + PŘÍLOHA I DOKUMENTACE K ŽÁDOSTI MUDr. Alena Trunečková Oddělení klinického hodnocení 2 Článek 25 Údaje předložené v dokumentaci k žádosti Článek 26 Jazykové požadavky Příloha I Dokumentace
1 KAPITOLA IV + PŘÍLOHA I DOKUMENTACE K ŽÁDOSTI MUDr. Alena Trunečková Oddělení klinického hodnocení 2 Článek 25 Údaje předložené v dokumentaci k žádosti Článek 26 Jazykové požadavky Příloha I Dokumentace
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 2. IDENTIFIKACE NEBEZPEČNOSTI 3. SLOŽENÍ / INFORMACE O SLOŽKÁCH
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Kvalitativní přímý imunofluorescenční test pro stanovení
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Kvalitativní přímý imunofluorescenční test pro stanovení
: Fluoxetine. Bezpečnostní list Bezpečnostní list podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0
 podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku Název látky : Látka : Fluoxetine
podle Nařízení (ES) č. 1907/2006 (REACH) Datum vydání: 31/05/2017 Verze: 1.0 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Forma výrobku Název látky : Látka : Fluoxetine
Suma Grill D9 Revize: Verze: 05.0
 Suma Grill D9 Revize: 2014-08-12 Verze: 05.0 1.1 Identifikátor výrobku Obchodní název: Suma Grill D9 Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands Kontaktní údaje
Suma Grill D9 Revize: 2014-08-12 Verze: 05.0 1.1 Identifikátor výrobku Obchodní název: Suma Grill D9 Diversey Europe Operations BV, Maarssenbroeksedijk 2, 3542DN Utrecht, The Netherlands Kontaktní údaje
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Selektivní suplement ke kultivačním médiím. 1.3 Identifikace
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Selektivní suplement ke kultivačním médiím. 1.3 Identifikace
BEZPEČNOSTNÍ LIST (Podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006)
 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Selektivní suplement ke kultivačním médiím. 1.3 Identifikace
1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A SPOLEČNOSTI/PODNIKU 1.1 Identifikace látky nebo Obchodní název: Další názvy látky: - 1.2 Použití látky nebo Selektivní suplement ke kultivačním médiím. 1.3 Identifikace
Obecné pokyny. upřesňující podmínky pro vnitroskupinovou finanční podporu podle článku 23 směrnice 2014/59/EU EBA/GL/2015/
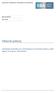 OBECNÉ POKYNY K PODMÍNKÁM PRO VNITROSKUPINOVOU FINANČNÍ PODPORU EBA/GL/2015/17 08.12.2015 Obecné pokyny upřesňující podmínky pro vnitroskupinovou finanční podporu podle článku 23 směrnice 2014/59/EU Obecné
OBECNÉ POKYNY K PODMÍNKÁM PRO VNITROSKUPINOVOU FINANČNÍ PODPORU EBA/GL/2015/17 08.12.2015 Obecné pokyny upřesňující podmínky pro vnitroskupinovou finanční podporu podle článku 23 směrnice 2014/59/EU Obecné
BEZPEČNOSTNÍ LIST podle Nařízení (ES) č. 1907/2006 (REACH) RELAVIT ACTIVE
 BEZPEČNOSTNÍ LIST podle Nařízení (ES) č. 1907/2006 (REACH) ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Název výrobku Číslo výrobku 500001270894, RAC/10, RAC/20 1.2.
BEZPEČNOSTNÍ LIST podle Nařízení (ES) č. 1907/2006 (REACH) ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Název výrobku Číslo výrobku 500001270894, RAC/10, RAC/20 1.2.
BEZPECNOSTNÍ LIST. (v souladu s narízením Komise (EU) c. 453/2010) ODDÍL 1: Identifikace látky/smesi a spolecnosti/podniku
 BEZPECNOSTNÍ LIST (v souladu s narízením Komise (EU) c. 453/2010) Identifikátor výrobku ODDÍL 1: Identifikace látky/smesi a spolecnosti/podniku Kód produktu Název výrobku Chemický název Registracní císlo
BEZPECNOSTNÍ LIST (v souladu s narízením Komise (EU) c. 453/2010) Identifikátor výrobku ODDÍL 1: Identifikace látky/smesi a spolecnosti/podniku Kód produktu Název výrobku Chemický název Registracní císlo
Příloha č. 1: Vstupní soubor dat pro země EU 1. část
 Příloha č. 1: Vstupní soubor dat pro země EU 1. část Reálný HDP na obyvatele v Eurech Belgie 27500 27700 27800 28600 29000 29500 30200 30200 29200 29600 29800 29009 Bulharsko 2300 2500 2600 2800 3000 3200
Příloha č. 1: Vstupní soubor dat pro země EU 1. část Reálný HDP na obyvatele v Eurech Belgie 27500 27700 27800 28600 29000 29500 30200 30200 29200 29600 29800 29009 Bulharsko 2300 2500 2600 2800 3000 3200
Obecné informace o nařízení o klasifikaci, označování a balení chemických látek (CLP)
 Obecné informace o nařízení o klasifikaci, označování a balení chemických látek (CLP) Webový seminář pro hlavní žadatele o registraci 9. dubna 2010 Gabriele Schöning Oddělen lení pro klasifikaci Evropská
Obecné informace o nařízení o klasifikaci, označování a balení chemických látek (CLP) Webový seminář pro hlavní žadatele o registraci 9. dubna 2010 Gabriele Schöning Oddělen lení pro klasifikaci Evropská
ití Posouzení expozice Charakterizace rizika Nástroje a pokyny
 Webinářpro hlavní žadatele o registraci CSA/CSR (I) 3. část Určen ená použit ití Posouzení expozice Charakterizace rizika Nástroje a pokyny 9. března 2010 Hélène Magaud, ECHA Přehled Právní kontext Použití
Webinářpro hlavní žadatele o registraci CSA/CSR (I) 3. část Určen ená použit ití Posouzení expozice Charakterizace rizika Nástroje a pokyny 9. března 2010 Hélène Magaud, ECHA Přehled Právní kontext Použití
Revize: Identifikátor výrobku Obchodní název:
 Revize: 20150212 01.0 1.1 Identifikátor výrobku Obchodní název: MCC Trading International GmbH, Schlüterstraße 5, D40235 Düsseldorf, www.horecaselect.info Kontaktníúdaje TEL: 296357111, FAX: 296357112
Revize: 20150212 01.0 1.1 Identifikátor výrobku Obchodní název: MCC Trading International GmbH, Schlüterstraße 5, D40235 Düsseldorf, www.horecaselect.info Kontaktníúdaje TEL: 296357111, FAX: 296357112
