Průvodce teorií měření ph
|
|
|
- Jozef Čech
- před 8 lety
- Počet zobrazení:
Transkript
1 Průvodce teorií měření ph Praktický popis postupu při měření ph Laboratorní prostředí Průvodce měřením ph teorie a praxe laboratorních ph aplikací
2
3 Obsah Obsah 1 Úvod do měření ph Kyselý nebo zásaditý? Proč se měří hodnota ph? Nástroje pro měření ph 7 a) ph elektroda 9 b) Referenční elektrody Praktický průvodce správným měřením ph 11 c) Kombinované elektrody 11 a) Příprava vzorku 11 b) Kalibrace 12 c) ph elektroda 14 d) Očekávaná správnost měření 15 Průvodce měřením ph krok za krokem 15 2 Výběr elektrody a manipulace s ní Diafragmy různých typů 18 a) Keramická diafragma 18 b) Objímková diafragma 19 c) Otevřená diafragma Referenční systémy a elektrolyty Typy a tvary skleněné membrány ph elektrody pro specifické aplikace 25 Snadné vzorky 25 Znečištěné vzorky 26 Emulze 26 Polopevné nebo pevné vzorky 27 Ploché a velmi malé vzorky 27 Malé vzorky a obtížné nádobky se vzorkem 27 InLab Power (Pro) Údržba elektrody Skladování elektrody 28 Krátkodobé skladování elektrody 28 Dlouhodobé skladování elektrody 29 Teplotní čidla Čištění elektrody 29 Zablokování sulfidem stříbrným (Ag 2S) 29 1
4 2 Obsah Zablokování chloridem stříbrným (AgCl) 29 Zablokování diafragmy bílkovinami 30 Zablokování diafragmy jinými látkami Regenerace elektrody a její životnost Další informace 30 3 Odstranění problémů při měření ph Kontrola přístroje a kabelu Kontrola teploty vzorku a aplikace Kontrola kalibračních roztoků a kalibrační procedury 32 Některé tipy pro použití kalibračních roztoků Kontrola elektrody 34 4 Kompletní teorie měření ph Definice hodnoty ph Korelace koncentrace a aktivity Kalibrační roztoky 40 Kapacita kalibračního roztoku (ß) 41 Hodnota ředění (ΔpH) 42 Teplotní vliv (ΔpH/ΔT) Měřící článek při měření ph 42 ph elektroda 44 Referenční elektroda Kalibrace/justování ph Vliv teploty na měření ph 48 Teplotní závislost elektrody 48 Izotermní průsečík 49 Další teplotní jevy 50 Teplotní závislost měřeného vzorku Jevy při měření speciálních roztoků 51 Alkalická chyba 51 Acidická chyba 52 Reakce s referenčním elektrolytem 52 Organická média 53 5 Přílohy Teplotní tabulky kalibračních roztoků METTLER TOLEDO 55
5 Tento průvodce se zaměřuje na jasný a praktický popis postupu při měření ph v laboratorním prostředí. V průvodci je uvedena celá řada různých tipů a praktických zkušeností při vlastním měření ph a v druhé části pak teoretický základ měření kyselosti a zásaditosti roztoků. Pozornost věnujeme také různým druhům ph elektrod a výběru správné ph elektrody pro specifický vzorek. 3
6 4Úvod do měření ph
7 1 Úvod do měření ph 1.1 Kyselý nebo zásaditý? Proč označujeme běžnou tekutinu, jako je třeba ocet, za kyselou? Důvodem je, že ocet obsahuje nadbytek hydroniových iontů (H 3O + ) a právě z tohoto důvodu je roztok kyselý. Na druhou stranu nadbytek hydroxylových iontů (OH ) vytváří roztok zásaditý. V čisté vodě jsou všechny hydroniové ionty neutralizovány hydroxylovými ionty a tento roztok má pak neutrální hodnotu ph. H 3O + + OH 2 H 2O Obrázek 1 Výsledkem reakce kyseliny a zásady je voda Pokud molekuly látky při disociaci uvolňují hydrogenové ionty nebo protony, nazýváme tuto látku jako kyselinu a výsledný roztok bude kyselý. Mezi nejznámější kyseliny patří kyselina chlorovodíková, kyselina sírová, kyselina octová nebo ocet. Rozklad octa znázorňuje následující rovnice: CH 3COOH + H 2O CH 3COO + H 3O + Obrázek 2 Disociace kyseliny octové Ne každá kyselina je stejně silná. Přesně řečeno označuje míru kyselosti celkový počet hydroniových iontů v roztoku. Hodnota ph je potom definovaná jako záporný logaritmus koncentrace hydroniových iontů. (Pro úplnou přesnost, hodnota ph je určena aktivitou vodíkových iontů. Další podrobnosti o aktivitě vodíkových iontů jsou uvedeny v kapitole 4.2). ph = log [H 3O + ] Obrázek 3 Rovnice pro výpočet hodnoty ph z koncentrace hydroniových iontů Kvantitativní rozdíl mezi kyselou a zásaditou látkou je možné stanovit na základě stanovení hodnoty ph. Na obrázku 4 je uvedeno několik příkladů hodnoty ph u některých běžných látek a chemikálií: 5
8 6Úvod do měření ph 1.2 Proč se měří hodnota ph? Potraviny a nápoje / domácí čisticí prostředky Obrázek 4 Hodnoty ph některých běžných látek a chemikálií Zásaditá část osy je hodnota ph mezi 7 a 14. Na konci osy je v nadbytku hydroxyl neboli aniont OH. Roztoky s těmito hodnotami ph jsou vytvářeny rozpuštěním zásaditých látek ve vodném roztoku. Zásaditá látka disociuje na hydroxylové ionty a vzniká tak zásaditý roztok. Mezi nejznámější zásady patří hydroxid sodný, čpavek nebo uhličitany. NH 3 + H 2O Obrázek Kyselina sírová 4,9% (1 M) Chemikálie Coca Cola Citronový džus Kys. chlorovodíková 0,37% (0,1 M) Pomerančový džus Pivo Kyselina octová 0,6% (0,1M) NH OH Reakce čpavku s vodou Sýr Mléko Voda Kyselina kyanovodíková 0,27% (0,1M) Vaječný bílek Antacid Mg(CH) 2 Celý rozsah hodnot ph ve vodných roztocích zahrnuje kyselé i zásadité hodnoty ph. Rozsah ph je od 0 do 14, přičemž ph 0 až 7 se nazývá kyselé a ph 7 až 14 se nazývá zásadité. Hodnota ph 7 je neutrální. Hodnotu ph měříme z různých důvodů: Pro výrobu produktů s definovanými vlastnostmi. Při výrobě je důležité kontrolovat hodnotu ph, jejíž přesná hodnota zaručuje, že hotové produkty mají požadované parametry. Různá hodnota ph může výrazně změnit vlastnosti hotových produktů, jako je například vzhled nebo chuť. Pro snížení výrobních nákladů. Tato závislost souvisí s výše uvedenými důvody. Pokud je výtěžnost daného výrobního procesu vyšší při určité hodnotě ph, budou výrobní náklady nižší pouze při této hodnotě ph. Borax Louh Uhličitan sodný (4%) vápenatý (nas.) Roztok čpavku 1,7% (1M) Roztok čpavku 0,017% (0,01M) Octan draselný 0,98% (0,1M) Jedlá soda 0,84% (0,1M)
9 Abychom zabránili poranění osob, znečištění životního prostředí nebo poškození vybavení. Některé látky mohou být při určité hodnotě ph nebezpečné. Musíme dbát na to, aby nedošlo k úniku těchto látek do prostředí, kde může dojít k poranění osob nebo ke zničení vybavení. Abychom určili případnou nebezpečnost takových látek, stanovíme nejprve jejich hodnotu ph. Abychom splnili právní požadavky. Z výše uvedeného je zřejmé, že některé látky nebo produkty mohou být nebezpečné. Vládní úřady proto zavádějí právní požadavky na ochranu osob před nebezpečnými látkami a materiály. Pro ochranu vybavení a technického zařízení. Výrobní zařízení přichází během výrobního procesu do styku s reakčními činidly. Pokud hodnota ph reakčních činidel neleží v určitých specifikovaných mezích, může dojít ke korozi výrobních zařízení. Koroze zkracuje životnost výrobní linky. Pro ochranu výrobní linky před nežádoucím poškozením je proto nutné monitorovat hodnoty ph. Pro výzkum a vývoj. Hodnota ph je rovněž důležitý parametr pro výzkumné účely, jako je studium biochemických procesů. Tyto příklady jasně popisují význam ph v celé řadě aplikací a důvody, proč se měření ph provádí tak často. 1.3 Nástroje pro měření ph Pro měření ph je potřeba měřicí zařízení citlivé na vodíkové ionty, které definují hodnotu ph. Princip měření spočívá v ponoření elektrody se skleněnou membránou citlivou na vodíkové ionty a sledováním reakce mezi ní a roztokem vzorku. Sledovaný potenciál ph elektrody sám o sobě ale neposkytuje dostatek informací a proto potřebujeme druhou elektrodu. Jedná se o elektrodu, která poskytuje referenční signál nebo potenciál pro ph elektrodu. Pro stanovení hodnoty ph měřeného roztoku je nezbytné používat diferenční potenciál obou elektrod najednou. Odezva ph elektrody závisí na koncentraci vodíkových iontů H + a poskytuje tak signál, který určuje kyselost/zásaditost roztoku. Referenční elektroda na druhou stranu neposkytuje odezvu na koncentraci vodíkových iontů H + v roztoku vzorku a je tak zdrojem konstantního potenciálu. K tomuto konstantnímu potenciálu se pak měří potenciál ph elektrody. 7
10 8Úvod Introduction do měření ph to ph 8 The potential between the two electrodes is therefore a measure of the number of hydrogen ions in the solution, which by definition gives one Potenciál the ph value mezi of dvěma the solution. elektrodami This je potential tedy počet is vodíkových a linear function iontů v of roztoku, the který hydrogen definuje concentration hodnotu ph in roztoku. the solution, Tento potenciál which allows je lineární quantitative funkcí koncentrace vodíku v to roztoku, be made. který The umožňuje formula provést for this kvantitativní function is měření. given below Rovnice in pro measurements figure tuto funkci 6: je uvedena na obrázku 6: E = E RT / nf = E 0 + 2,3RT / nf * log [H3O + ] * log [H 3O + ] E = measured potential = naměřený potenciál E0 = constant E 0 konstanta R = gas constant = plynová konstanta T = temperature in degrees Kelvin = teplota v K n = ionic charge = iontový náboj F = Faraday constant = Faradayova konstanta Figure 6. The relationship between the amount of acid in solution and the output potential of Obrázek 6 Vztah mezi množstvím kyseliny v roztoku a výstupním potenciálem ph elektrody a ph electrode. METTLER TOLEDO InLab Mono ph InLab Reference Pro Figure 7. The measurement assembly of ph and reference sensor. Obrázek 7 Sestava ph a referenční elektrody Na In figure obrázku 7 a 7 ph je uvedena measurement sestava setup pro měření with two ph s separate dvěma samostatnými sensors, a ph elektrodami. sensor and Jednou a reference pro stanovení sensor ph is a shown. druhou referenční. Nowadays, V a současnosti merger of se the obě two elektrody separate většinou sensors slučují into one do electrode jedné a toto is spojení very common referenční and a ph this elektrody combination of reference kombinovaná and elektroda. ph electrodes Každá is z called těchto tří the elektrod combined je jiná ph a electrode. má specific- se nazývá ké Each výhody of these a vlastnosti. three electrodes is different and has its own important features and properties.
11 a) ph elektroda ph elektroda slouží pro vlastní stanovení hodnoty ph v roztoku. Skládá se ze skleněného těla s tenkou skleněnou membránou na konci, která je citlivá na H + kationty. Na vnější straně této skleněné membrány se při kontaktu s vodným roztokem vytvoří gelová vrstva. Podobná gelová vrstva se vytvoří rovněž na vnitřní straně skleněné membrány, pokud je elektroda plněná vodným roztokem elektrolytu. Příklad gelové vrstvy je uvedený na obrázku dole: Vnitřní gelová vrstva Skleněná membrána LI Vnitřní pufr + SIO3 H internal + SIO3 = konstantní buffer LI + SIO3 LI + LI + SIO3 SIO3 SIO3 LI + LI + LI + SIO3 SIO3 SIO3 LI + LI + Kladný náboj Vnitřní pufr Záporný náboj SIO3 SIO3 Měřený roztok H + H + Vnější gelová vrstva H + H + Kyselý roztok Zásaditý roztok Skleněná membrána (0,2 0,5 mm) Gelová vrstva cca 1000 A (10 2 mm) Obrázek 8 Průřez skleněnou membránou Vodíkové kationty H + uvnitř a v okolí gelové vrstvy mohou buď difúzí procházet do nebo vycházet z této vrstvy v závislosti na hodnotě ph a tudíž na koncentraci vodíkových kationtů H + měřeného roztoku. Pokud je roztok zásaditý, odcházejí vodíkové kationty H + difúzí z této vrstvy a na vnější straně membrány se vytvoří záporný náboj. Jelikož je skleněná elektroda plněná vnitřním pufrem s konstantní hodnotou ph, potenciál na vnitřním povrchu membrány zůstává během měření konstantní. Potenciál ph elektrody představuje tudíž rozdíl mezi vnitřním a vnějším nábojem membrány. Schématické zobrazení standardní ph elektrody je uvedeno na obrázku 9. Platinový svod Vnitřní pufr Skleněná membrána Konektor S7 Obrázek 9 ph elektroda s membránou citlivou na ph 9
12 Úvod do měření ph b) Referenční elektrody Referenční elektroda slouží jako zdroj definovaného stabilního referenčního potenciálu vzhledem k potenciálu ph elektrody, která se používá pro měření. Referenční elektroda musí být pro tento účel vyrobena ze skla, které není citlivé na obsah vodíkových kationtů H + v roztoku. Elektroda musí být také otevřená vzhledem k prostředí vzorku, kam je ponořená. Proto je do těla referenční elektrody vytvořen otvor nebo diafragma, kterou může procházet vnitřní roztok nebo referenční elektrolyt do vzorku. Referenční elektroda a indikační ph cela musí být pro spránost měření ponořeny ve stejném roztoku. Obrázek typické referenční elektrody je uveden dále. Plnicí otvor Referenční systém Membrána Konektor S7 Referenční elektrolyt Obrázek 10 Referenční elektroda s referenčním elektrolytem, referenčním prvkem a diafragmou Konstrukce elektrody je navržena tak, že vnitřní referenční prvek je ponořen do definovaného referenčního pufru a přes diafragmu je v nepřímém kontaktu s roztokem vzorku. Tento kontakt je zárukou stabilního potenciálu. K dispozici je několik referenčních systémů, ale prakticky vždy se dnes používá systém stříbro/chlorid stříbrný. Potenciál tohoto referenčního systému je definován referenčním elektrolytem a referenčním prvkem stříbro/chlorid stříbrný. Je důležité, aby referenční elektrolyt měl vysokou koncentraci iontů, která poskytuje nízký elektrický odpor (další podrobnosti jsou uvedeny v kapitole 4.4). Jelikož referenční elektrolyt během měření proniká do roztoku vzorku, je třeba se vyvarovat chemické reakce mezi referenčním elektrolytem a roztokem vzorku, protože tato reakce může ovlivnit elektrodu a měření (další podrobnosti jsou uvedeny v kapitole 2.2). 10
13 c) Kombinované elektrody Kombinované elektrody (obrázek 11) nabízejí mnohem snazší manipulaci než dvě samostatné elektrody a dnes se používají ve většině případů. V kombinované elektrodě je skleněná ph elektroda rovnoměrně obklopena referenční elektrodou naplněnou referenčním elektrolytem. ph elektroda a referenční elektroda v kombinované elektrodě mají stejné vlastnosti jako samostatné elektrody. Jediným rozdílem je, že jsou spojeny do jedné kombinované elektrody pro snadnější použití. Pouze v případě, že se vzhledem k vlastnostem měřeného vzorku nechá očekávat, že životnost ph a referenční elektrody v kombinované elektrodě bude výrazně odlišná, doporučuje se místo kombinované elektrody používat pro měření samostatná ph elektroda a samostatná referenční elektroda. Pro další zjednodušení ph měření je možné do kombinované elektrody přidat také teplotní čidlo. Pak je možné provádět měření ph s teplotní kompenzací. Takové elektrody se také nazývají elektrody 3-v-1. Šroubovací víčko, hlava S7 nebo Multipin Referenční elektrolyt Lapač stříbrných iontů Keramická frita METTLER TOLEDO InLab Routine Otvor pro plnění, SafeLock Referenční systém ARGENTHAL Integrované teplotní čidlo Skleněná membrána citlivá na ph Obrázek 11 Typická kombinovaná ph elektroda s vnitřní ph elektrodou a vnější referenční elektrodou 1.4 Praktický průvodce správným měřením ph Nástroje nezbytné pro měření ph jsou relativné jednoduché, mají snadné použití a poskytují spolehlivé měření. Předpokladem ovšem je jejich správné použití. Při použití systémů pro měření ph je třeba dodržovat důležité pokyny, které jsou uvedeny dále. Na konci těchto pokynů je pak krok za krokem uveden postup pro získání správných výsledků měření ph. a) Příprava vzorku Při přípravě vzorku pro měření je třeba vzít v úvahu následující pravidla. Je velmi důležité provést buď měření teploty vzorku nebo zachovat konstantní teplotu vzorku na známé hodnotě. 11
14 Úvod do měření ph Důvodem je fakt, že hodnota ph vzorku závisí na teplotě a ph elektroda poskytuje výsledky měření v závislosti na teplotě. Tato teplotní závislost nepředstavuje problém v případě, že je teplota zaznamenávána a je prováděna její kompenzace. Před zahájením měření ph vždy promíchejte vzorek, abyste zajistili jeho homogenitu. Tak zajistíte, že naměřená hodnota je platná pro celý vzorek a nejen pro místo, kam je umístěna elektroda. V nádobce pak musí být také dostatečné množství vzorku tak, aby byla diafragma v referenční části plně ponořená do vzorku. To je nezbytné z toho důvodu, aby byl zajištěný kontakt mezi vnitřní a vnější částí referenční elektrody a aby elektrolyt mohl volně odtékat do vzorku. Samozřejmostí pak je dodržení základních pravidel pro správnou laboratorní praxi, jako je použití vhodného, čistého a označeného laboratorního skla pro vzorky a stanovení ph. b) Kalibrace Kalibraci ph elektrody je třeba provádět pravidelně. Kalibraci doporučujeme provádět alespoň jednou denně před zahájením měření. Při kalibraci se stanovuje strmost a offset elektrody. Teoretická hodnota strmosti a offsetu elektrody se vypočítá podle Nernstovy rovnice: E = E 0 + 2,3RT / nf * log [H 3O + ] + 2,3RT / nf * ph Strmost = 2,3RT / nf Offset = Při ph 7,00 by měla být 0 mv Obrázek 12 Strmost a odchylka pro ph elektrodu Kalibrace je nezbytná pro nastavení strmosti a offsetu elektrody na skutečné hodnoty pro použitý měřicí systém. Kalibrační křivka je pak použitá pro korelaci naměřených hodnot mv elektrody na hodnotu ph měřeného roztoku. 12
15 mv 7 ph Obrázek 13 Korelace mezi hodnotou mv naměřenou pomocí ph elektrody a hodnotou ph vzorku. Zobrazené křivky jsou teoretické pro chování s kompenzací odchylky a chování s kompenzací strmosti a offsetu. Jelikož je elektroda charakterizována pomocí nulového bodu a strmosti, doporučujeme provádět minimálně dvoubodovou kalibraci pro spolehlivé měření a lepší přesnost. Pokud jsou měření prováděna v celém rozsahu hodnoty ph, doporučujeme provádět tříbodovou kalibraci. Většina ph metrů umožňuje provést 3 5 bodovou kalibraci. Je třeba dodat, že měření vzorků by se mělo provádět pouze v oblasti, která byla kalibrována. Při kalibraci elektrody většina ph metrů vyžaduje zadání typu použitých kalibračních roztoků (pufrů). Existuje několik výrobců kalibračních roztoků a parametry nejčastěji používaných značek kalibračních roztoků jsou již uloženy v paměti ph metrů. Tyto tabulky pokrývají skupiny kalibračních roztoků pro široký teplotní rozsah. Tímto způsobem je možné ihned zvolit celou skupinu a umožnit použití kalibračních roztoků pro kalibraci s teplotní kompenzací. Tabulky pro skupiny kalibračních roztoků METTLER TOLEDO jsou uvedeny v příloze 5.1. Pokud se nepoužívá žádné teplotní čidlo nebo se používá externí teplotní čidlo, je třeba zajistit měření a kalibraci při stejné teplotě. V tomto případě je třeba ručně zadat teplotu, aby mohl ph metr provést korekci teploty kalibračních roztoků. Kalibrační roztoky použité pro kalibraci jsou velmi přesné roztoky s garantovanou hodnotou a přesností. Abyste zajistili co nejdelší použitelnost kalibračních roztoků i po jejich otevření, dodržujte následující pokyny: 13
16 Úvod do měření ph Na lahvičku s kalibračním roztokem poznamenejte datum prvního použití roztoku. Kalibrační roztoky vždy uchovávejte v těsně uzavřených lahvičkách a odlitý pufr ihned použijte. Použité kalibrační roztoky nikdy nevracejte do originálních lahviček nebo nesmíchávejte kalibrační roztoky různých výrobců. Zajistěte, aby se do lahvičky s kalibračním roztokem nedostal žádný kontaminant a lahvičku vždy těsně uzavřete. Kalibrační roztok vždy uložte při teplotě okolí. Lahvičky s roztokem pufru nevystavujte přímému slunečnímu záření. Před kalibrací elektrody vyčistěte a neprovádějte kalibraci přímo v lahvičce s originálním kalibračním roztokem. Nikdy nepoužívejte kalibrační roztok s prošlou dobou použitelnosti nebo roztok s podezřením na jeho kontaminaci. Po vypršení doby použitelnosti vyměňte kalibrační roztok za nový. Kalibraci opakujte vždy po vyčištění elektrody, její údržbě, regeneraci nebo při jejím dlouhodobém uložení, protože všechny tyto faktory mají vliv na potenciál ph elektrody. c) ph elektroda ph elektrody hrají důležitou roli při stanovení správné hodnoty ph. Pro dlouhou životnost ph elektrod a správné výsledky měření je proto velmi důležitá jejich údržba. Pokud nejsou elektrody po použití očištěny nebo se dlouhodobě nepoužívají, ztrácejí svou správnost a přesnost měření celého systému se snižuje. Postupné ztrácení přesnosti měření se projevuje jako stálý pokles strmosti elektrody. Jakmile strmost elektrody poklesne pod 50 mv na dekádu (85% teoretické strmosti) nebo ofset v nulovém bodě překročí ± 30 mv, je třeba provést intenzivní rekondicionování elektrody. Rekondicionování elektrody může zvýšit přesnost elektrody na požadovanou úroveň, ale někdy je nutné elektrodu zcela vyměnit. Na špatný výkon elektrody a její nízkou směrnici má vliv nejen špatná údržba, ale rovněž jiné faktory, jako je znečištění frity, ztráta elektrolytu, kontaminace skleněné baňky a použití nesprávných kalibračních pufrů. 14
17 Podrobnější postup při údržbě elektrody je uveden v kapitole 2. Pro elektrody je dalším důležitým faktorem teplota. Potenciál elektrody naměřený ve vzorku závisí částečně na teplotě vzorku. Jelikož se jedná o známou lineární závislost, je možné provést její kompenzaci. Problém ovšem vzniká v případě, pokud mezi elektrodou a vzorkem existuje gradient. Gradient způsobí drift měření ph až do okamžiku, kdy dojde k vyrovnání teploty vzorku a elektrody. Teprve pak bude měřená hodnota stabilní. Pokud budete ignorovat rozdíl teploty mezi elektrodou a vzorkem, bude měření nestabilní nebo uskutečníte chybné měření ph v nerovnovážném stavu. d) Očekávaná správnost měření Správnost vašeho měření je ovlivněna různými faktory, jako je správnost roztoků použitých pro kalibraci, použití nebo nepoužití teplotní kompenzace, správnost výběru elektrody pro konkrétní typ vzorku, poskytnutí dostatečně dlouhého času pro vytvoření rovnováhy a použití správného koncového bodu měření. To jsou pouze některé z faktorů, které mají na výsledek měření vliv. Pokud věnujete dostatečnou péči všem těmto faktorům, je možné dosáhnout správnosti měření ± 0,05 ph. Průvodce měřením ph krok za krokem Tento průvodce předpokládá použití kombinované ph elektrody. Pokud se používá samostatná ph a samostatná referenční elektroda, je třeba ověřit, že elektrody byly vloženy během měření do stejného roztoku. Dále zkontrolujte, že jsou obě elektrody připojeny k ph metru. Příprava 1) Zvolte správnou ph elektrodu pro váš typ vzorku (viz kapitola 2). 2) Připojte elektrodu a teplotní čidlo k ph metru. Kalibrace 3) Zapněte ph metr a zvolte správnou skupinu kalibračních roztoků nebo hodnoty kalibračních roztoků pro kalibraci. 4) Nastavte ph metr pro manuální korekci teploty v případě, že není připojeno teplotní čidlo. 15
18 Úvod do měření ph 5) Zvolte správnou teplotu pro kalibrační roztoky v případě, že se neprovádí automatická korekce teploty. 6) Připravte kalibrační roztoky určené pro kalibraci tak, že nalijete dostatečného množství kalibračních roztoků do čistých kádinek. 7) Ujistěte se, že kalibrační roztoky jsou pro kalibraci použity ve správném pořadí, pokud nemá ph metr funkci automatické identifikace kalibračního roztoku (Všechny ph metry METTLER TOLEDO mají funkci automatické identifikace kalibračního roztoku). 8) Vyjměte elektrodu z držáku a vizuálně zkontrolujte, zda nevykazuje elektroda nějaký zřetelný problém. Zkontrolujte, zda je otevřen plnicí otvor elektrolytu, aby nevznikal při doplňování elektrolytu podtlak a elektrolyt mohl pomalu protékat do vzorku. 9) Elektrodu opláchněte destilovanou nebo deionizovanou vodou. 10) Vezměte první kalibrační roztok, opatrně jej promíchejte a ponořte do něj elektrodu. 11) Stiskněte tlačítko pro kalibraci (nebo ekvivalentní) na ph metru. 12) Vyčkejte na ustálení měřené hodnoty. Přístroje METTLER TOLEDO mají integrován algoritmus pro automatické ukončení měření ph po ustálení měřené hodnoty. 13) Vytáhněte elektrodu z kalibračního roztoku a opláchněte ji. 14) Vezměte druhý kalibrační roztok, opatrně jej promíchejte a ponořte do něj elektrodu. 15) Stiskněte tlačítko pro kalibraci (nebo ekvivalentní) na ph metru. 16) Vyčkejte, dokud měření nedosáhne koncové hodnoty ph. 17) Vytáhněte elektrodu z kalibračního roztoku a opláchněte ji. 18) Pro třetí kalibrační bod opakujte kroky 8 až 11. Po dokončení kalibrace ukončete kalibrační proceduru na ph metru stiskem příslušného tlačítka. 19) Vytáhněte elektrodu z kalibračního roztoku, opláchněte ji a uložte do držáku. 20) Zkontrolujte výsledky kalibrace na ph metru. 21) Pokud jsou výsledky v pořádku, uložte je. Měření 1) Nalijte dostatek vzorku do měřicí nádobky tak, aby hladina vzorku byla nad diafragmou elektrody. 2) Zkontrolujte, zda je známá hodnota teploty vzorku nebo zda je teplota vzorku stanovena během měření ph pomocí interního nebo externího teplotního čidla. 16
19 3) Vzorek lehce promíchejte a ponořte ph elektrodu do roztoku. 4) Pokud se teplota vzorku a elektrody výrazně liší, zkontrolujte, zda se drift měření způsobený teplotním gradientem zastavil a teprve pak proveďte měření ph. 5) Stiskněte tlačítko pro měření na ph metru a vyčkejte, dokud nebude dosaženo stabilního koncového bodu. 6) Vytáhněte elektrodu z roztoku a opláchněte ji destilovanou nebo deionizovanou vodou. 7) Pro měření dalších vzorků opakujte kroky 1 až 6. 8) Po ukončení měření opláchněte elektrodu destilovanou nebo deionizovanou vodou a uložte ji do nádobky naplněné referenčním elektrolytem. 17
20 Výběr elektrody a manipulace s ní 2 Výběr elektrody a manipulace s ní Pro optimální měření ph je třeba vybrat správnou elektrodu. Nejdůležitější kritéria pro výběr elektrody jsou chemické složení vzorku, jeho homogenita, teplota, rozsah ph a velikost nádobky (omezení délky a šířky). Volba je obzvláště důležitá pro nevodné roztoky, roztoky s nízkou vodivostí, s vysokým obsahem bílkovin a vysokou viskozitou, u kterých jsou standardní skleněné elektrody pro obecné použití vystaveny různým zdrojům chyb. Doba odezvy a správnost měření pomocí elektrody závisí na celé řadě faktorů. Měření při extrémních hodnotách ph a teplotách nebo při nízké vodivosti může trvat delší dobu než měření vodných roztoků s neutrálním ph při pokojové teplotě. Význam různých typů vzorků je vysvětlen dále, přičemž se jako výchozí bod berou různé charakteristiky elektrody. Opět opakujeme, že v této kapitole jsou popisovány zejména kombinované ph elektrody. 2.1 Diafragmy různých typů a) Keramická diafragma Referenční část ph elektrody, která udržuje kontakt se vzorkem, může mít různou formu. Tyto formy se v minulosti vyvíjely na základě různých požadavků na měření ph různých typů vzorků. Standardní diafragma je nejjednodušší a je známá jako keramická frita. Skládá se z porézní keramiky, která je zatlačena do skleněného těla elektrody. Porézní keramický materiál poté umožňuje pomalý odtok elektrolytu z elektrody a zároveň zabraňuje jeho rychlému úniku. Tento druh diafragmy je vhodný pro standardní měření vodných roztoků. Příkladem takové elektrody je METTLER TOLEDO InLab Routine Pro. Schématické schéma principu této diafragmy je uvedeno na obrázku 14. Obrázek 14 Elektroda s keramickou fritou 18
21 Ačkoliv se jedná díky své jednoduchosti pro měření vodných roztoků pravděpodobně o nejpoužívanější typ diafragmy, má jednu velkou nevýhodu. Kvůli porézní struktuře diafragmy je relativně snadné, aby došlo k zablokování diafragmy vzorkem. To platí zejména v případě, pokud jde o viskózní vzorek nebo suspenzi. Vyšší opatrnosti je třeba dbát také u některých vodných roztoků s vysokou koncentrací bílkovin, jelikož bílkoviny se mohou na porézní diafragmě při kontaktu s referenčním elektrolytem (často jde o KCl) srážet. Srážlivá reakce způsobí zaplnění porézní struktury zbytky bílkovin a zablokování diafragmy, takže elektroda nemůže správně pracovat. Měření není možné v případě, pokud elektrolyt nemůže volně protékat, jelikož referenční potenciál není stabilní. Ke stejnému problému může dojít také kvůli reakci vnitřního elektrolytu s roztokem měřeného vzorku, které se setkávají v diafragmě. Při této reakci může dojít ke srážení a následnému zablokování diafragmy. To znamená, že pokud se používá KCl elektrolyt saturovaný AgCl se vzorky obsahujícími sulfidy, stříbro a sulfidy navzájem reagují a vzniká sulfid Ag 2S, který zablokuje keramickou fritu. b) Objímková diafragma Keramická frita má určitá omezení a není vhodná pro obtížnější vzorky, takže postupem času byly vyvinuty jiné diafragmy pro měření tohoto typu vzorků. Problémy, které má keramická frita s viskózními vzorky nebo suspenzemi, je možné vyřešit větší diafragmou, kterou nelze tak snadno zablokovat a kterou lze snadno čistit. Takovým typem diafragmy je objímková diafragma. Tato diafragma se skládá ze skleněné elektrody, na kterou lze navléknout plastovou nebo skleněnou objímku. Elektrolyt vytéká z elektrody skrz otvor, který je zakrytý skleněnou nebo plastovou objímkou. Objímku je možné vytáhnout více nebo méně bezpečně po skleněném těle elektrody pro regulaci odtoku elektrolytu z referenčního prvku. Schématické zobrazení skleněné diafragmy je uvedeno na obrázku 15. Společnost METTLER TOLEDO nabízí například elektrodu s objímkovou diafragmou InLab Science. Výhodou této diafragmy je, že jí elektrolyt protéká rychleji než u keramické frity. To je výhodné například pro vzorky s deficitem iontů. Čištění u této diafragmy je také velmi snadné, jelikož objímku je možné zcela vysunout a odstranit všechny 19
22 Výběr elektrody a manipulace s ní nečistoty z diafragmy pomocí deionizované vody nebo čisticího papíru (za předpokladu, že se nedotknete ph membrány!). Tento silnější průtok elektrolytu umožňuje také do určité míry samočištění diafragmy. Obrázek 15 Schématický nákres elektrody s objímkovou diafragmou Hlavní aplikace pro elektrody s objímkovou diafragmu jsou v oblastech, kde je pro přesné měření ph výhodou rychlý průtok elektrolytu a diafragma odolná proti zablokování. Rychlý průtok iontů je zvláště výhodný v kapalinách, které mají nízkou koncentraci iontů na úrovni několika mmol nebo nižší. Tyto kapaliny s iontovým deficitem mají velmi nízkou vodivost. Tyto vlastnosti zvyšují odpor na diafragmě a vedou k problémům s kontaktem mezi referenčním elektrolytem a měřeným roztokem a poskytují velmi nestabilní signál. Tento problém se řeší použitím skleněné zábrusové diafragmy, která vytváří optimální kontakt mezi referenčním elektrolytem a měřeným roztokem. Kapaliny s iontovým deficitem se obtížně měří, ale tento typ vzorků budeme popisovat později v této kapitole. Snadné čištění diafragmy a její větší odolnost k zablokování je velmi užitečná pro velmi viskózní vzorky jako olej, suspenze a emulze, jako například mléko. Elektroda má delší životnost a její čištění je snazší. Větší plocha diafragmy nabízí snadnější kontakt, což je výhodné pro olejové vzorky, které mají nízkou koncentraci iontů. 20
23 c) Otevřená diafragma Třetím typem diafragma je otevřená diafragma. Tato referenční elektroda je zcela otevřená okolnímu prostředí a má plný kontakt mezi referenčním elektrolytem a roztokem vzorku. To je možné pouze u referenčního elektrolytu z polymeru v pevném stavu. Schématické zobrazení diafragmy je uvedeno dole. Otevřená diafragma Obrázek 16 Příklad elektrody s otevřenou diafragmou Velkou výhodou této diafragmy je jednoduše fakt, že je zcela otevřená a tudíž dojde jen zřídka k jejímu zablokování. Otevřené diafragmy si dobře poradí s velmi znečištěnými vzorky a nabízejí dobré výsledky měření. Nevýhodou referenčního elektrolytu z polymeru v pevném stavu, který se používá pro otevřenou diafragmu, je delší odezva a nízký průtok elektrolytu. To znamená, že měřené vzorky musejí mít pro stabilní měření dostatečně vysokou koncentraci iontů. Bez ohledu na to jsou tyto elektrody vhodné pro většinu vzorků a jsou velmi robustní. 2.2 Referenční systémy a elektrolyty Ze všech možných referenčních systémů má pouze několik z nich praktický význam. Jedná se o referenční systém stříbro/chlorid stříbrný, jod/jodid a rtuť/ kalomel. Kalomelová referenční elektroda se nyní už ve větší míře nepoužívá. V tomto textu budeme probírat nejdůležitější referenční systém, kterým je systém stříbro/chlorid stříbrný. Potenciál referenčního systému elektrody je definován referenčním elektrolytem a referenčním prvkem (stříbro/chlorid stříbrný). Konvenční konstrukce tohoto referenčního systému představuje stříbrný drát potažený chloridem stříbrným. Pro tento typ referenčního systému stříbro/chlorid stříbrný je důležité, aby referenční elektrolyt měl velmi vysokou koncentraci AgCl (byl saturován), aby 21
24 Výběr elektrody a manipulace s ní nedošlo k rozpouštění povlaku AgCl ze stříbrného referenčního vodiče. Pokud by k tomu došlo, referenční prvek by přestal plnit svou funkci. U tohoto typu referenčního prvku došlo nedávno k uvedení nového referenčního prvku ARGENTHAL. Referenční prvek ARGENTHAL se skládá z malého zásobníku naplněného částicemi AgCl, který je zdrojem stříbrných iontů pro chemickou reakci na svodovém drátku. Zásobník obsahuje dostatek AgCl po celou dobu životnosti elektrody. Stříbrný drátek potažený AgCl Zásobník Ag/AgCl (ARGENTHAL ) Skleněná vlna Lapač stříbrných iontů Referenční elektrolyt bez Ag + Diafragma Obrázek 17 Schématický nákres referenčního systému ARGENTHAL To, který typ referenčního elektrolytu se používá v elektrodě, silně závisí na použitém referenčním systému a na typu vzorku. Referenční systém může být klasický stříbrný drátek nebo ARGENTHAL. Vzorek je možné rozdělit do dvou skupin na vodné a nevodné matrice. Pro vodné i nevodné roztoky je důležité, že referenční elektrolyt obsahuje velké množství iontů pro správnou funkci referenčního systému. Ideálně, soli použité jako zdroj těchto iontů v referenčním elektrolytu jsou dobře rozpustné v rozpouštědle, jsou ph neutrální (takže neovlivňují měření při jejich odtoku z elektrody) a nesrážejí se reakcí s jinými ionty přítomnými ve vzorku nebo pufru. KCl splňuje tyto požadavky nejlépe pro vodné roztoky a LiCl se nejlépe hodí pro nevodné roztoky. Konvenční referenční systém Ag/AgCl potřebuje přítomnost elektrolytu saturovaného AgCl, takže nedochází k rozpouštění AgCl, kterým je potažen stříbrný drátek. Jako referenční elektrolyt je tedy vhodné zvolit roztok 3 mol/l KCl saturovaný AgCl. Nevýhodou tohoto elektrolytu je, že stříbrné ionty reagují s vzorkem a vytvářejí nerozpustnou sraženinu a blokují diafragmu. 22
25 Referenční systém ARGENTHAL má zásobník s AgCl granulemi, které jsou nepřetržitým zdrojem AgCl. Tento zásobník obsahuje dostatek AgCl po celou dobu životnosti elektrody. Typicky systém ARGENTHAL je doplněn o lapač stříbrných iontů tak, aby neprocházely do elektrolytu. Výhodou referenčního systému ARGENTHAL je možnost použití standardního 3 mol/kcl jako referenčního elektrolytu místo 3 mol/l KCl saturovaného AgCl. Takže v kombinaci s lapačem stříbrných iontů nejsou v elektrolytu volné Ag + ionty, které by mohly způsobit srážecí reakci se vzorkem. Oddělení fází v kontaktní oblasti mezi elektrolytem a roztokem vzorku na diafragmě může způsobit nestabilní signál. Jako rozpouštědlo pro referenční elektrolyt ve vodných vzorcích se tedy používá deionizovaná voda. Pro nevodné systémy se používá jako rozpouštědlo etanol nebo kyselina octová. Dále uvádíme krátký přehled možné kombinace referenčního systému a elektrolytu: Elektrolyt pro vodné vzorky Elektrolyt pro nevodné vzorky ARGENTHAL Konvenční ARGENTHAL 3 mol/l KCl + H 2O 3 mol/l KCl + AgCl + H 2O LiCl + etanol / LiCl + kyselina octová Obrázek 18 Přehled použitých referenčních elektrolytů Kromě výše uvedených kapalných elektrolytů se používají rovněž gelové a pevné polymerové elektrolyty. Elektrody dodávané s těmito elektrolyty nelze doplňovat. Doba odezvy elektrody silně závisí na typu použitého elektrolytu. Elektrody s kapalným elektrolytem vykazují velmi krátkou dobu odezvy a poskytují výsledky s nejvyšší správností. Elektrody s gelovým a pevným polymerovým elektrolytem mají delší odezvu, ale vyžadují prakticky nulovou údržbu. 2.3 Typy a tvary skleněné membrány Skleněná membrána ph elektrody může mít různý tvar a vlastnosti v závislosti na aplikaci, pro kterou se elektroda používá. Kritériem pro výběr elektrody je konzistence vzorku, jeho objem a teplota, požadovaný rozsah měření a koncentrace iontů ve vzorku. 23
26 Výběr elektrody a manipulace s ní Jednou z hlavních vlastností elektrody je tvar membrány. Na obrázku 19 je pak uveden postup při výběru tvaru membrány včetně jejích vlastností a navrhované aplikace. Kulovitý Pro vzorky s nízkou teplotou: odolná proti smršťování Polokulovitý Pro vzorky s malým objemem: ph membrána pouze na spodní části Válcovitý Vysoce citlivá membrána: velká plocha povrchu, nižší odpor Špičatý Pro polopevné a pevné vzorky: snadno proniká do vzorku Plochý Pro povrchy a vzorky kapkovitého tvaru: velmi malá kontaktní plocha ph membrány Mikro Vzorky ve zkumavkách: velmi úzké tělo elektrody Obrázek 19 Různé tvary ph membrány Skleněná membrána je důležitá rovněž pro vlastnosti měření elektrody. V následující tabulce je uveden přehled různých typů skleněných ph membrán METTLER TOLEDO. 24
27 Typ skleněné membrány HA skleněná, silně zásadité LoT skleněná, nízká teplota A41 U univerzální skleněná HF skleněná, odolná kyselině fluorovodíkové Na skleněná, sodíková Vlastnosti/vzorky Pro vysoké teploty a vysoké hodnoty ph: mimořádně malá chyba při měření alkalických roztoků Pro nízké teploty a nízkou koncentraci iontů: sklo s nízkou odolností Pro vysoké teploty; odolná chemikáliím Pro standardní aplikace Pro vzorky s obsahem kyseliny fluorovodíkové (až do 1g/l) Používá se pouze pro elektrody pro detekci sodíku: sklo specifické pro sodík Elektroda se skleněnou HF membránou je v roztocích s kyselinou fluorovodíkovou robustnější než standardní ph elektrody. Kyselina fluorovodíková nad určitou koncentrací (> 1g/l) a pod ph 5 rozkládá sklo a zabraňuje vytvoření gelové vrstvy u standardní skleněné ph membrány. To opět vede k nestabilitě naměřených hodnot a snižuje životnost elektrody. Při vyšší koncentracích kyseliny fluorovodíkové je třeba použít antimonovou elektrodu, jako je například elektroda Sb850-SC 1 se speciální referenční elektrodou (tzn. DX202-SC 2 ). 2.4 ph elektrody pro specifické aplikace Po seznámení s různými typy diafragem, elektrolytů a membrán, které existují u ph elektrod, se podíváme na jejich význam pro měření ph v různých systémech. Snadné vzorky Pro rutinní měření vodných roztoků v chemické laboratoři postačují jednoduché ph elektrody. Výhodou jednoduché ph elektrody je velmi snadné použití a její robustnost. Obecně jsou tyto elektrody vyrobeny ze skla a mají keramickou fritu. ph elektrody jsou doplnitelné, takže je možné doplnit elektrolyt, vyčistit elektrodu a prodloužit tak její životnost. Vhodnou elektrodou pro jednoduchá laboratorní měření je InLab Routine s nebo bez teplotního čidla. 1 Elektroda METTLER TOLEDO Sb850-SC je antimonová elektroda s indikační elektrodou, Elektroda METTLER TOLEDO DX202-SC je plastová referenční elektroda,
28 Výběr elektrody a manipulace s ní Elektroda InLab Routine Pro má integrované teplotní čidlo pro automatické měření teploty a automatickou kompenzaci teploty během měření. Znečištěné vzorky Měření ph znečištěných vzorků může být obtížné, jelikož nečistoty ve vzorku mohou zkreslovat výsledky měření. Příkladem takových aplikací je měření kyselosti půdních vzorků, kontrola kvality v potravinářských produktech, jako jsou polévky a měření koloidní chemických systémů. Riziko zablokování diafragmy při použití ph elektrody s keramickou fritou je velmi vysoké. Proto je nejlepší použít ph elektrodu s otevřenou diafragmou, jako je elektroda InLab Expert s referenčním elektrolytem s pevným polymerem. Tělo elektrody má otvor pro přímý kontakt mezi elektrolytem a vzorkem. Pro teplotní kompenzaci během měření je možné použít elektrodu s vestavěným teplotním čidlem, jako je například elektroda InLab Expert Pro. Emulze Dalším typem vzorků, který vyžaduje při měření ph speciální péči, jsou emulze, například barvy, olej ve vodných disperzích, mléko a jiné potravinářské produkty. Takové vzorky mohou také zablokovat diafragmu ph elektrody, když disperzní fáze emulze zablokuje diafragmu. Částice emulzí, které mohou způsobit zablokování elektrody, jsou velmi malé. Proto není nutné provádět měření s otevřenou diafragmou. Jelikož elektrody s pevnými polymery mají relativně malou odezvu v porovnání s elektrodami s kapalným elektrolytem, je výhodné měřit emulze pomocí elektrod, které mají objímkovou diafragmu. Objímkovou diafragmu nelze snadno zablokovat a má velkou kontaktní plochu se vzorkem. Pokud dojde k zablokování diafragmy, je možné ji snadno vyčistit stáhnutím objímky z diafragmy. Pak je možné vyčistit celou elektrodu. Příkladem tohoto typu elektrody je InLab Science nebo InLab Science Pro, která má vestavěné teplotní čidlo. Elektrody s objímkovou diafragmou mají velkou kontaktní plochu mezi referenčním elektrolytem a roztokem vzorku a tudíž jsou vhodné pro vzorky, které vykazují nestabilní signál. 26
29 Polopevné nebo pevné vzorky Standardní ph elektrody nejsou obecně schopné vydržet tlak při zatlačování do pevných vzorků. Proto je pro pevné vzorky pro měření ph třeba použít speciální elektrodu, která umožňuje proniknout do vzorku. Tvar membrány je také důležitý, protože musí mít velkou plochu kontaktu se vzorkem i v případě, kdy je elektroda zatlačena do vzorku silou. Nejvhodnějšími elektrodami pro tento druh aplikací jsou elektrody METTLER TOLEDO InLab Solids nebo InLab Solids Pro. Elektrody mají špičatý konec, který umožňuje snadný průnik do vzorku a jejich membrána zaručuje správnost měření. Elektrody InLab Solids mají také otevřenou diafragmu, která zabraňuje zablokování pevným nebo polopevným vzorkem. Tato elektroda se typicky používá pro kontrolu kvality nebo kontrolu výrobního procesu sýra a masa. Ploché a velmi malé vzorky Někdy je potřeba provést stanovení ph vzorku, který je tak malý, že nepokrývá ani špičku ph elektrody. Pro tento typ měření existuje jediné řešení, kterým je plochá ph elektroda. Tato elektroda potřebuje pro měření ph pouze rovný povrch. Aplikace pro tento typ elektrody zahrnují stanovení ph kůže při kontrole zdravotního stavu a stanovení ph papíru při výrobě ručního papíru pro archiválie a důležité dokumenty. Existuje celá řada jiných aplikací, kde je k dispozici pouze malé množství vzorku, například stanovení ph vzorku krve. V tomto případě se plochá ph elektroda položí přímo na kapku krve, takže se vzorek krve rozprostře po celé ploše membrány. Mezi tento typ aplikací patří dále stanovení ph u velmi drahých biochemických vzorků, kterých je k dispozici pouze velmi malé množství. Nejvhodnější elektrodou METTLER TOLEDO pro tento typ měření je elektroda InLab Surface. Malé vzorky a obtížné nádobky se vzorkem U některých aplikací stanovení ph je k dispozici pouze malé množství vzorku nebo je třeba elektrodu zasunout do nádobek komplikovaného tvaru. Například se jedná o stanovení ph vzorku ve zkumavce, Eppendorfových zkumavkách nebo úzkých NMR zkumavkách. 27
30 Výběr elektrody a manipulace s ní Tyto nádobky s malým objemem vzorku obecně vyžadují malou a úzkou ph elektrodu, která umožňuje dosáhnout na vzorek a provést stanovení jeho ph. Dobrým příkladem elektrody s těmito vlastnostmi je elektroda InLab Micro (Pro). InLab Power (Pro) Elektroda InLab Micro (Pro) je relativně novým typem elektrody pro univerzální použití. Tato elektroda byla zkonstruována tak, že vnitřní elektrolyt je pod tlakem. Výhodou pak je, že vzorek se nemůže dostat do elektrody bez ohledu na parametry vzorku nebo aplikace. To znamená, že měření jsou spolehlivá a zároveň rychlá, protože průtok elektrolytu je vždy dostatečný pro stabilní měření. Tato elektroda je vhodná pro viskózní potravinářské produkty, jako jsou džemy nebo pro kosmetiku typu barvy na vlasy. 2.5 Údržba elektrody 2.6 Skladování elektrody Pro dlouhou životnost jakékoliv elektrody je velmi důležitá její pravidelná údržba. Elektrody s kapalným elektrolytem je třeba včas doplnit vždy, když dojde k poklesu hladiny elektrolytu pod hladinu roztoku. Tímto způsobem zabráníte zpětnému toku vzorku do elektrody. Referenční elektrolyt je třeba zcela vyměnit v pravidelném intervalu, tzn. jednou za měsíc. Díky tomu bude elektrolyt vždy čerstvý a bez krystalků vznikajících kvůli odpařování z otevřeného plnicího otvoru během měření. Dbejte na to, aby nedošlo uvnitř elektrody k vytvoření žádných bublin, speciálně ne blízko diafragmy. Pokud k tomu dojde, měření bude nestabilní. Abyste se zbavili bublinek, elektrodou mírně potřeste vertikálním pohybem stejným způsobem, jako tomu je například u lékařského teploměru. Elektrody je třeba vždy uložit do vodných roztoků nebo do roztoků bohatých na ionty. Díky tomu zůstane gelová vrstva vytvořená na skleněné membráně ph elektrody hydratovaná a bohatá na ionty. Tento způsob uložení ph elektrod je nezbytný pro to, aby ph membrána reagovala spolehlivě bez ohledu na hodnotu ph vzorku. Krátkodobé skladování elektrody Pokud nebudete elektrodu používat po kratší dobu nebo mezi dvěma měřeními je nejlepší umístit elektrodu do držáku, který obsahuje stejný elektrolyt jako elektroda (tzn. 3 mol/l KCl) nebo do kalibračního roztoku s ph 4 nebo ph 7. Zajistěte, že hladina roztoku v nádobce je pod hladinou plnicího roztoku v elektrodě. 28
31 Dlouhodobé skladování elektrody Při dlouhodobém skladování elektrody je třeba, aby byl kryt elektrody naplněn vnitřním roztokem elektrolytu, kalibračním roztokem ph 4 nebo roztokem 0,1 mol/l HCl. Zkontrolujte, že plnicí otvor pro referenční a kombinovanou elektrodu je uzavřený, aby nedocházelo k úbytku elektrolytu odpařováním, které by mohlo způsobit tvorbu krystalků uvnitř elektrody a diafragmy. Elektrodu nikdy neskladujte za sucha nebo ponořenou do destilované vody, protože by došlo k poškození skleněné membrány citlivé na ph a zkrácení životnosti elektrody. Ačkoliv regenerace elektrody může částečně obnovit parametry elektrody, která byla dobře skladována, dodržujte následující pokyny, které zajistí připravenost vaší elektrody pro okamžité použití. Teplotní čidla Po použití opláchněte teplotní čidla a uložte je v suchu v balicí krabičce, aby nedošlo k jejich poškození. 2.7 Čištění elektrody Pro vyčištění elektrody je opláchněte deionizovanou vodou po každém měření, ale nikdy ji neotírejte papírovým kapesníkem. Nerovný povrch papíru by poškrábal a poškodil skleněnou membránu citlivou na ph, odstranil gelovou vrstvu a vytvořil elektrostatický náboj na elektrodě. Elektrostatický náboj způsobí silnou nestabilitu měřicího signálu. Při kontaminaci určitých vzorků je třeba použít speciální čisticí procedury. Tyto procedury jsou popsány v dalším textu. Zablokování sulfidem stříbrným (Ag 2S) Pokud referenční elektrolyt obsahuje stříbrné ionty a měřený vzorek obsahuje sulfidy, dojde ke kontaminaci diafragmy a ke srážení sulfidu stříbrného. Pro vyčištění diaragmy použijte 8% roztok thiomočoviny v 0,1 mol/l HCl 3. Zablokování chloridem stříbrným (AgCl) Stříbrné ionty z referenčního elektrolytu mohou také reagovat se vzorkem, který obsahuje chloridové ionty, a vytvářet sraženinu AgCl. Sraženinu lze odstranit ponořením elektrody do koncentrovaného roztoku čpavku. 3 Tento roztok thiomočoviny je možné objednat u společnosti METTLER TOLEDO ( ) 29
32 Odstranění problémů při měření ph 2.8 Regenerace elektrody a její životnost Zablokování diafragmy bílkovinami Diafragmy kontaminované proteiny je možné často vyčistit ponořením elektrody do roztoku pepsin/hcl (5% pepsin v 0,1 mol/l HCl) na několik hodin 4. Zablokování diafragmy jinými látkami Pokud je diafragma zablokována jinými kontaminanty, pokuste se vyčistit elektrodu v ultrazvukové lázni vody nebo 0,1 mol/l HCl. I elektrody, u kterých byla pravidelně prováděna údržba a které byly správně skladovány, mohou začít po určité době vykazovat špatné výsledky. V takovém případě je možné regenerovat ph citlivou skleněnou membránu a obnovit výkon elektrody na předchozí úroveň v regeneračním roztoku bifluoridu amonného 5. Tento regenerační roztok je založen na silně zředěném roztoku kyseliny fluorovodíkové, která odstraní tenkou vrstvu ze skleněné membrány a ponechá volný povrch. Při použití regenerační směsi neponechávejte elektrodu v roztoku na dobu delší 1 2 minuty, protože dojde ke korozi ph citlivé membrány a elektroda bude nepoužitelná. Očekávaná životnost správně používané a udržované ph elektrody je kolem třech let. Faktory, které přispívají ke snížení životnosti elektrody, zahrnují vysokou teplotu a měření extrémních ph hodnot. 2.9 Další informace Další podrobnosti jsou uvedeny na internetových stránkách METTLER TOLEDO: Výběr elektrody a průvodce parametry: ph metry: 4 Pepsin lze objednat ze společnosti METTLER TOLEDO ( ). 5 Tento regenerační roztok je možné objednat METTLER TOLEDO pod objednávacím číslem
33 3 Odstranění problémů při měření ph Problémy, ke kterým může docházet během měření ph, mohou mít různé příčiny; vlastní ph metr, kabel a elektrodu, kalibrační roztoky, teplotu měření a typ vzorku (aplikaci). Zvláštní pozornost je třeba věnovat symptomům problémů, protože pomáhají identifikovat příčinu chyby. V následující tabulce je přehled symptomů a příčin problémů: Hodnota na displeji je příliš vysoká/ nízká nebo mimo rozsah měření --- Hodnota se nemění Dlouhá doba odezvy Vysoký offset po kalibraci Malá strmost po kalibraci Chyba kalibrace Drift měřených hodnot Zkontrolujte měřicí přístroj, kabel, elektrodu, kalibrační proceduru a teplotu vzorku Zkontrolujte měřicí přístroj, kabel, elektrodu Zkontrolujte elektrodu a vzorek/aplikaci Zkontrolujte elektrodu, kalibrační roztoky a kalibrační proceduru Zkontrolujte elektrodu, kalibrační roztoky a kalibrační proceduru Zkontrolujte měřicí přístroj, kabel, elektrodu, kalibrační roztoky a kalibrační proceduru Zkontrolujte elektrodu a vzorek/aplikaci 3.1 Kontrola přístroje a kabelu Symptomy, které jsou obvykle spojeny s problémem s ph metrem nebo kabelem, jsou hodnota měření mimo rozsah, žádná zobrazená hodnota nebo hodnota, která se neměnní. Pokud je třeba určit, zda je problém způsoben ph metrem nebo kabelem, postupujte podle následujících pokynů: Krok 1: Zkontrolujte, zda je možné zapnout ph metr. Pokud to není možné, vyměňte baterie nebo zkontrolujte zdroj napájení. Krok 2: Přepněte přístroj do režimu měření mv. Zkontrolujte potenciál pomocí zkratovací spojky: Hodnota na displeji by měla být 0 mv (± správnost měření přístroje). Pokud se nejedná o tento případ, zkontrolujte správné uzemnění přístroje a jeho zapojení do elektrické zásuvky. Krok 3: Použijte ph simulátor a zkontrolujte hodnotu mv při ph 4,01; 7,00 a 10,00. Na displeji by se měla zobrazit hodnota 0 mv nebo ±180 mv. Pokud se tyto hodnoty nezobrazí, je třeba provést opravu přístroje nebo změnit nastavení na výchozí z výrobního závodu. Krok 4: Zkontrolujte všechna připojení. Pokud má elektroda odpojitelný kabel, otestujte jej a vyměňte za stejný. 31
Princip měření ph. Seminář Mettler Toledo říjen 2010
 Princip měření ph Seminář Mettler Toledo říjen 2010 Agenda Co je ph? Definice ph Princip měření ph Konstrukce ph elektrody Kalibrace elektrody Teplotní kompenzace Skladování a čištění Měření ph elektrodami
Princip měření ph Seminář Mettler Toledo říjen 2010 Agenda Co je ph? Definice ph Princip měření ph Konstrukce ph elektrody Kalibrace elektrody Teplotní kompenzace Skladování a čištění Měření ph elektrodami
Pufrové roztoky S pufrovými roztoky TMS máte jistotu, že získáte přesné výsledky objemy: 100 ml, 250 ml, 1000 ml
 ph ELEKTRODY TMS Rozmanitost ph elektrod TMS Vám umožňuje vybrat si ten správný typ pro daný měřený vzorek, jeho objem a teplotu. Elektrody ve skleněném, nebo plastovém pouzdře skleněné pouzdro elektrody
ph ELEKTRODY TMS Rozmanitost ph elektrod TMS Vám umožňuje vybrat si ten správný typ pro daný měřený vzorek, jeho objem a teplotu. Elektrody ve skleněném, nebo plastovém pouzdře skleněné pouzdro elektrody
Měření ph nápojů a roztoků
 Měření ph nápojů a roztoků vzorová úloha (SŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Kyselý nebo zásaditý roztok? Proč je ocet považován za kyselý roztok? Ocet obsahuje nadbytek (oxoniových kationtů).
Měření ph nápojů a roztoků vzorová úloha (SŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Kyselý nebo zásaditý roztok? Proč je ocet považován za kyselý roztok? Ocet obsahuje nadbytek (oxoniových kationtů).
Měření ph nápojů a roztoků
 Měření ph nápojů a roztoků vzorová úloha (ZŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Kyselý nebo zásaditý roztok? Proč je ocet považován za kyselý roztok? Ocet obsahuje nadbytek (oxoniových kationtů).
Měření ph nápojů a roztoků vzorová úloha (ZŠ) Jméno Třída.. Datum.. 1 Teoretický úvod Kyselý nebo zásaditý roztok? Proč je ocet považován za kyselý roztok? Ocet obsahuje nadbytek (oxoniových kationtů).
PHB-209. Stolní ph/mv měřič
 PHB-209 Stolní ph/mv měřič PHB 209 ph METR PŘEDBĚŽNÉ VYZKOUŠENÍ... 2 VŠEOBECNÝ POPIS... 3 POPIS FUNKCE... 3 SPECIFIKACE... 3 PRŮVODCE NASTAVENÍM... 4 MĚŘENÍ ph... 4 MĚŘENÍ ORP (oxidačně redukční potenciál)...
PHB-209 Stolní ph/mv měřič PHB 209 ph METR PŘEDBĚŽNÉ VYZKOUŠENÍ... 2 VŠEOBECNÝ POPIS... 3 POPIS FUNKCE... 3 SPECIFIKACE... 3 PRŮVODCE NASTAVENÍM... 4 MĚŘENÍ ph... 4 MĚŘENÍ ORP (oxidačně redukční potenciál)...
ph-elektrody Testo Pokyn pro aplikaci
 ph-elektrody Testo Pokyn pro aplikaci cz 2 Obsah Obsah Popis elektrod...3 Pokyny pro aplikaci...4 Bezpečnostní pokyny...5 Příprava elektrod...6 Kalibrace a měření...7 Skladování elektrod...8 Čištění elektrod...9
ph-elektrody Testo Pokyn pro aplikaci cz 2 Obsah Obsah Popis elektrod...3 Pokyny pro aplikaci...4 Bezpečnostní pokyny...5 Příprava elektrod...6 Kalibrace a měření...7 Skladování elektrod...8 Čištění elektrod...9
PHH-720 Série. ph metr s vizuálním alarmem
 PHH-720 Série ph metr s vizuálním alarmem PHH 720 (M3866) Přímý, vodotěsný ph - metr se signalizací alarmu Přístroj je vyroben ve shodě s EN 50081 1 a 50082 1. Předběžné vyzkoušení přístroje Opatrně vybalte
PHH-720 Série ph metr s vizuálním alarmem PHH 720 (M3866) Přímý, vodotěsný ph - metr se signalizací alarmu Přístroj je vyroben ve shodě s EN 50081 1 a 50082 1. Předběžné vyzkoušení přístroje Opatrně vybalte
UŽIVATELSKÁ PŘÍRUČKA PRO ÚDRŽBU A USKLADNĚNÍ ELEKTROD
 UŽIVATELSKÁ PŘÍRUČKA PRO ÚDRŽBU A USKLADNĚNÍ ELEKTROD Děkujeme Vám, že jste si vybrali produkt od fi rmy Hanna Instruments. Před použitím elektrody si prosím pečlivě přečtěte tento instruktážní manuál.
UŽIVATELSKÁ PŘÍRUČKA PRO ÚDRŽBU A USKLADNĚNÍ ELEKTROD Děkujeme Vám, že jste si vybrali produkt od fi rmy Hanna Instruments. Před použitím elektrody si prosím pečlivě přečtěte tento instruktážní manuál.
PHH-222. ph metr. 4. Procedura kalibrace ph. 4-1 Důvod kalibrace
 PHH-222 ph metr 4. Procedura kalibrace ph 4-1 Důvod kalibrace Ideální ph elektroda generuje 0 mv při ph 7.00 (177.4 mv při ph 4), ph-208 je nakalibrováno na toto vstupní napětí (při 25 C okolní teploty).
PHH-222 ph metr 4. Procedura kalibrace ph 4-1 Důvod kalibrace Ideální ph elektroda generuje 0 mv při ph 7.00 (177.4 mv při ph 4), ph-208 je nakalibrováno na toto vstupní napětí (při 25 C okolní teploty).
Kvalita měření ph, teorie a praxe
 Kvalita měření ph, teorie a praxe Stanovení hodnoty ph patří vůbec k nejčastějším požadavkům v procesním, laboratorním i terénním měření v běžné praxi. Dále se zaměříme na exaktnější metody měření ph a
Kvalita měření ph, teorie a praxe Stanovení hodnoty ph patří vůbec k nejčastějším požadavkům v procesním, laboratorním i terénním měření v běžné praxi. Dále se zaměříme na exaktnější metody měření ph a
Laboratorní roztoky Laboratorní roztoky ph pufry Vodivostní standardy Roztoky pro ORP a DO Roztoky pro ISE Roztoky pro údržbu
 Laboratorní roztoky Laboratorní roztoky ph pufry Vodivostní standardy Roztoky pro ORP a DO Roztoky pro ISE Roztoky pro údržbu Roztoky pro kalibraci a údržbu Kompletní řada nezbytných doplňků Roztoky pro
Laboratorní roztoky Laboratorní roztoky ph pufry Vodivostní standardy Roztoky pro ORP a DO Roztoky pro ISE Roztoky pro údržbu Roztoky pro kalibraci a údržbu Kompletní řada nezbytných doplňků Roztoky pro
Stanovení izoelektrického bodu kaseinu
 Stanovení izoelektrického bodu kaseinu Shlukování koloidních částic do větších celků makroskopických rozměrů nazýváme koagulací. Ke koagulaci koloidních roztoků bílkovin dochází porušením solvatačního
Stanovení izoelektrického bodu kaseinu Shlukování koloidních částic do větších celků makroskopických rozměrů nazýváme koagulací. Ke koagulaci koloidních roztoků bílkovin dochází porušením solvatačního
Laboratorní ph elektrody kombinované - přehled
 Laboratorní ph elektrody kombinované - přehled 1. Způsob použití laboratorních ph elektrod kombinovaných Prostředí, ve kterém se měří ph Elektroda Kat. č. Poznámka Vodné roztoky obecně HC 113 12111 se
Laboratorní ph elektrody kombinované - přehled 1. Způsob použití laboratorních ph elektrod kombinovaných Prostředí, ve kterém se měří ph Elektroda Kat. č. Poznámka Vodné roztoky obecně HC 113 12111 se
Kombinované průmyslové tlakové ph elektrody typu SMH-xxx Elektrody se zvýšenou mechanickou odolností
 Kombinované průmyslové tlakové ph elektrody typu SMH-xxx Elektrody se zvýšenou mechanickou odolností Rozsah ph 0 až 13 Rozsah pracovních teplot 0 až 50 C Nulový bod ph=7 Odpor membrány max.150 M při 25
Kombinované průmyslové tlakové ph elektrody typu SMH-xxx Elektrody se zvýšenou mechanickou odolností Rozsah ph 0 až 13 Rozsah pracovních teplot 0 až 50 C Nulový bod ph=7 Odpor membrány max.150 M při 25
Kombinované průmyslové tlakové redoxní elektrody typu SORC-xxx
 Kombinované průmyslové tlakové redoxní elektrody typu SORC-xxx Rozsah pracovních teplot -10 až 70 C Max.přetlak 8 Barů Měrná část Pt elektroda Ø4mm označení popis použití SORC-233 běžné použití, tlak do
Kombinované průmyslové tlakové redoxní elektrody typu SORC-xxx Rozsah pracovních teplot -10 až 70 C Max.přetlak 8 Barů Měrná část Pt elektroda Ø4mm označení popis použití SORC-233 běžné použití, tlak do
VÚVeL Brno Kontrola hygieny prostředí a bezpečnosti výrobků v mlékárenských provozech
 13. 6. 2019 VÚVeL Brno Kontrola hygieny prostředí a bezpečnosti výrobků v mlékárenských provozech Proč kontrolovat čistící roztoky, oplachové a odpadní vody? Při čištění dochází k postupné kontaminaci
13. 6. 2019 VÚVeL Brno Kontrola hygieny prostředí a bezpečnosti výrobků v mlékárenských provozech Proč kontrolovat čistící roztoky, oplachové a odpadní vody? Při čištění dochází k postupné kontaminaci
Panelový měřič vodivosti model CDCN 201
 Panelový měřič vodivosti model Prvotní prohlídka Opatrně vyjměte přístroj z krabice a zjistěte, zda nedošlo k mechanickému poškození. Pokud zjistíte jakékoliv poškození, ihned kontaktujte servisní středisko
Panelový měřič vodivosti model Prvotní prohlídka Opatrně vyjměte přístroj z krabice a zjistěte, zda nedošlo k mechanickému poškození. Pokud zjistíte jakékoliv poškození, ihned kontaktujte servisní středisko
STANOVENÍ CHLORIDŮ. Odměrné argentometrické stanovení chloridů podle Mohra
 STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
STANOVENÍ CHLORIDŮ Odměrné argentometrické stanovení chloridů podle Mohra Cíl práce Stanovte titr odměrného standardního roztoku dusičnanu stříbrného titrací 5 ml standardního srovnávacího roztoku chloridu
APLIKAČNÍ LIST PRO PRÁCI S ph metrem - ionometrem
 APLIKAČNÍ LIST PRO PRÁCI S ph metrem - ionometrem 1 POPIS TLAČÍTEK zapnout/ vypnout přepínání modu měření (zmáčknutí delší 5s SETUP) přepíná do kalibračního modu ukládá hodnoty do paměti, hodnoty při kalibraci
APLIKAČNÍ LIST PRO PRÁCI S ph metrem - ionometrem 1 POPIS TLAČÍTEK zapnout/ vypnout přepínání modu měření (zmáčknutí delší 5s SETUP) přepíná do kalibračního modu ukládá hodnoty do paměti, hodnoty při kalibraci
Titrační senzory. Titrační senzory ph Argentometrie a redox Vodivost Tenzidy Reference Fotometrie. Inteligentní senzory pro všechny titrační aplikace
 Titrační senzory Titrační senzory ph Argentometrie a redox Vodivost Tenzidy Reference Fotometrie Inteligentní senzory pro všechny titrační aplikace Zkušenosti a inovace Dlouhodobé zkušenosti s moderními
Titrační senzory Titrační senzory ph Argentometrie a redox Vodivost Tenzidy Reference Fotometrie Inteligentní senzory pro všechny titrační aplikace Zkušenosti a inovace Dlouhodobé zkušenosti s moderními
Návod k obsluze. Konduktometr COND51
 Návod k obsluze Konduktometr COND51 1. ÚVOD: Děkujeme Vám, že jste si zakoupili laboratorní konduktometr COND51. Před jeho použitím si pečlivě přečtěte tento návod. Na základě neustálého vylepšování přístroje
Návod k obsluze Konduktometr COND51 1. ÚVOD: Děkujeme Vám, že jste si zakoupili laboratorní konduktometr COND51. Před jeho použitím si pečlivě přečtěte tento návod. Na základě neustálého vylepšování přístroje
4 STANOVENÍ KINEMATICKÉ A DYNAMICKÉ VISKOZITY OVOCNÉHO DŽUSU
 Laboratorní cvičení z předmětu Reologie potravin a kosmetických prostředků 4 STANOVENÍ KINEMATICKÉ A DYNAMICKÉ VISKOZITY OVOCNÉHO DŽUSU (KAPILÁRNÍ VISKOZIMETR UBBELOHDE) 1. TEORIE: Ve všech kapalných látkách
Laboratorní cvičení z předmětu Reologie potravin a kosmetických prostředků 4 STANOVENÍ KINEMATICKÉ A DYNAMICKÉ VISKOZITY OVOCNÉHO DŽUSU (KAPILÁRNÍ VISKOZIMETR UBBELOHDE) 1. TEORIE: Ve všech kapalných látkách
4. Doplňkové vybavení měřícího přístroje na zvláštní objednávku...4. 5. Bezpečnostní předpisy...4. 6. Vysvětlení pojmu ph hodnota...
 Obsah Strana Kombinovaný měřič elektrické vodivosti HI9811-5 (ph / C / EC / TDS) 1. Úvod...1 2. Základní popis a účel použití měřícího přístroje...3 3. Rozsah dodávky...3 4. Doplňkové vybavení měřícího
Obsah Strana Kombinovaný měřič elektrické vodivosti HI9811-5 (ph / C / EC / TDS) 1. Úvod...1 2. Základní popis a účel použití měřícího přístroje...3 3. Rozsah dodávky...3 4. Doplňkové vybavení měřícího
Nejistoty kalibrací a měření ph
 Nejistoty kalibrací a měření ph metru Ing. Alena Vospělová Český metrologický institut Okružní 31 638 00 Brno 1 DEFINICE ph ph patří mezi nejčastěji měřené veličiny v chemických laboratořích. Svým charakterem
Nejistoty kalibrací a měření ph metru Ing. Alena Vospělová Český metrologický institut Okružní 31 638 00 Brno 1 DEFINICE ph ph patří mezi nejčastěji měřené veličiny v chemických laboratořích. Svým charakterem
Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje.
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2018/19
Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje.
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
Bazénové elektrody a příslušenství pro rok 2014
 Bazénové elektrody a příslušenství pro rok 2014 1. ph elektrody kombinované vhodné pro bazény s gelovým elektrolytem 22111 ph kombinovaná HC 233 1.680,- pro běžné využití do 1 baru, samočistící, záruka
Bazénové elektrody a příslušenství pro rok 2014 1. ph elektrody kombinované vhodné pro bazény s gelovým elektrolytem 22111 ph kombinovaná HC 233 1.680,- pro běžné využití do 1 baru, samočistící, záruka
Thermo Scientific ORION ph elektrody
 ThermoScientific ORION nabízí pro měření ph nejen řadu přístrojů, ale hlavně široké spektrum elektrod různého provedení a pro různé účely. Rozsah a kvalita této nabídky je bezkonkurenční a zde naleznete
ThermoScientific ORION nabízí pro měření ph nejen řadu přístrojů, ale hlavně široké spektrum elektrod různého provedení a pro různé účely. Rozsah a kvalita této nabídky je bezkonkurenční a zde naleznete
Kyselost a zásaditost vodných roztoků
 Kyselost a zásaditost vodných roztoků Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je. Mgr. Vlastimil Vaněk. Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z
Kyselost a zásaditost vodných roztoků Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je. Mgr. Vlastimil Vaněk. Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z
Stanovení silných kyselin potenciometrickou titrací
 Úloha č. Stanovení silných kyselin potenciometrickou titrací Princip Potenciometrické titrace jsou jednou z nejrozšířenějších elektrochemických metod kvantitativního stanovení látek. V potenciometrické
Úloha č. Stanovení silných kyselin potenciometrickou titrací Princip Potenciometrické titrace jsou jednou z nejrozšířenějších elektrochemických metod kvantitativního stanovení látek. V potenciometrické
Potenciometrické stanovení disociační konstanty
 Potenciometrické stanovení disociační konstanty TEORIE Elektrolytická disociace kyseliny HA ve vodě vede k ustavení disociační rovnováhy: HA + H 2O A - + H 3O +, kterou lze charakterizovat disociační konstantou
Potenciometrické stanovení disociační konstanty TEORIE Elektrolytická disociace kyseliny HA ve vodě vede k ustavení disociační rovnováhy: HA + H 2O A - + H 3O +, kterou lze charakterizovat disociační konstantou
Průvodce měřením ph. v laboratořích. aby ph nebylo záhadou.
 Průvodce měřením ph v laboratořích aby ph nebylo záhadou www.chromservis.eu ph SONDA základní pojmy Kombinovaná ph sonda Běžná ph sonda, obsahující měrnou a referentní část (elektrodu). Propojíme-li měrnou
Průvodce měřením ph v laboratořích aby ph nebylo záhadou www.chromservis.eu ph SONDA základní pojmy Kombinovaná ph sonda Běžná ph sonda, obsahující měrnou a referentní část (elektrodu). Propojíme-li měrnou
Acidobazické děje - maturitní otázka z chemie
 Otázka: Acidobazické děje Předmět: Chemie Přidal(a): Žaneta Teorie kyselin a zásad: Arrhemiova teorie (1887) Kyseliny jsou látky, které odštěpují ve vodném roztoku proton vodíku H+ HA -> H+ + A- Zásady
Otázka: Acidobazické děje Předmět: Chemie Přidal(a): Žaneta Teorie kyselin a zásad: Arrhemiova teorie (1887) Kyseliny jsou látky, které odštěpují ve vodném roztoku proton vodíku H+ HA -> H+ + A- Zásady
Neutralizace, měření senzorem ph Vernier Laboratorní práce
 Neutralizace, měření senzorem ph Vernier Laboratorní práce VY_52_INOVACE_209 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Neutralizace, měření senzorem ph Vernier Laboratorní
Neutralizace, měření senzorem ph Vernier Laboratorní práce VY_52_INOVACE_209 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie Ročník: 8.,9. Neutralizace, měření senzorem ph Vernier Laboratorní
Volný chlór: - Měří se pomocí TDS testeru - základní test vody pro zjištění celkového množství rozpuštěných látek (minerály, soli, kovy)
 Poradíme Vám, jak na čistý bazén! - je to jednoduché, stačí vědět v jakém stavu je aktuálně bazénová voda. - pro udržení čisté nezávadné vody je nutné udržovat čistotu vody, PH, volný chlór a v případě
Poradíme Vám, jak na čistý bazén! - je to jednoduché, stačí vědět v jakém stavu je aktuálně bazénová voda. - pro udržení čisté nezávadné vody je nutné udržovat čistotu vody, PH, volný chlór a v případě
Chemické výpočty II. Vladimíra Kvasnicová
 Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
Chemické výpočty II Vladimíra Kvasnicová Převod jednotek pmol/l nmol/l µmol/l mmol/l mol/l 10-12 10-9 10-6 10-3 mol/l µg mg g 10-6 10-3 g µl ml dl L 10-6 10-3 10-1 L Cvičení 12) cholesterol (MW=386,7g/mol):
Víme, co vám nabízíme
 PDF vygenerováno: 19.12.2017 19:28:19 Katalog / Laboratorní přístroje / Konduktometry HANNA Univerzální přenosný multimetr pro měření ph, vodivosti a koncentrace rozpuštěného kyslíku Lehký a mimořádně
PDF vygenerováno: 19.12.2017 19:28:19 Katalog / Laboratorní přístroje / Konduktometry HANNA Univerzální přenosný multimetr pro měření ph, vodivosti a koncentrace rozpuštěného kyslíku Lehký a mimořádně
Finnpipette Stepper. Návod k použití
 Finnpipette Stepper Návod k použití Autorizovaný prodejce: DYNEX TECHNOLOGIES, spol. s r.o. Lidická 977 273 43 Buštěhrad Tel.: +420 220 303 600 Fax: +420 224 320 133 office@dynex.cz www.dynex.cz 1 2 OBSAH
Finnpipette Stepper Návod k použití Autorizovaný prodejce: DYNEX TECHNOLOGIES, spol. s r.o. Lidická 977 273 43 Buštěhrad Tel.: +420 220 303 600 Fax: +420 224 320 133 office@dynex.cz www.dynex.cz 1 2 OBSAH
Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 12. 4. 2013. Ročník: osmý
 ph Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 4. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základní vlastností
ph Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 4. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základní vlastností
Stolní ph metr ph50. Návod k obsluze
 Stolní ph metr ph50 Návod k obsluze Verze 20121015 Chromservis s.r.o., Jakobiho 327, 109 00 Praha 10 Petrovice tel.: +420 274 021 211, fax.: +420 274 021 220 www.chromservis.cz, e-mail: prodej@chromservis.cz
Stolní ph metr ph50 Návod k obsluze Verze 20121015 Chromservis s.r.o., Jakobiho 327, 109 00 Praha 10 Petrovice tel.: +420 274 021 211, fax.: +420 274 021 220 www.chromservis.cz, e-mail: prodej@chromservis.cz
UŽIVATELSKÁ PŘÍRUČKA (překlad původního návodu k použití) SB 52 Tužkový měřič ph/orp/ C/ F
 UŽIVATELSKÁ PŘÍRUČKA (překlad původního návodu k použití) SB 52 Tužkový měřič ph/orp/ C/ F SUBOTA Indikátor automatické kompenzace teploty Indikátor nestability Měřící jednotka na hlavním LCD Hlavní LCD
UŽIVATELSKÁ PŘÍRUČKA (překlad původního návodu k použití) SB 52 Tužkový měřič ph/orp/ C/ F SUBOTA Indikátor automatické kompenzace teploty Indikátor nestability Měřící jednotka na hlavním LCD Hlavní LCD
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
 OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
Orbisint CPS11 a CPS11D
 Technická informace Orbisint CPS11 a CPS11D ph elektrody, analogová a digitální s technologií Memosens. Pro standardní aplikace v procesu a oblasti životního prostředí, s PTFE membránou odpuzující nečistoty,
Technická informace Orbisint CPS11 a CPS11D ph elektrody, analogová a digitální s technologií Memosens. Pro standardní aplikace v procesu a oblasti životního prostředí, s PTFE membránou odpuzující nečistoty,
3 Acidobazické reakce
 3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
3 Acidobazické reakce Brønstedova teorie 1. Uveďte explicitní definice podle Brønstedovy teorie. Kyselina je... Báze je... Konjugovaný pár je... 2. Doplňte tabulku a pojmenujte všechny sloučeniny. Kyselina
Úvod do koroze. (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají)
 Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
ÚPRAVA VODY V ENERGETICE. Ing. Jiří Tomčala
 ÚPRAVA VODY V ENERGETICE Ing. Jiří Tomčala Úvod Voda je v elektrárnách po palivu nejdůležitější surovinou Její množství v provozních systémech elektráren je mnohonásobně větší než množství spotřebovaného
ÚPRAVA VODY V ENERGETICE Ing. Jiří Tomčala Úvod Voda je v elektrárnách po palivu nejdůležitější surovinou Její množství v provozních systémech elektráren je mnohonásobně větší než množství spotřebovaného
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY
 ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
ZÁKLADNÍ CHEMICKÉ POJMY A ZÁKONY Klíčová slova: relativní atomová hmotnost (A r ), relativní molekulová hmotnost (M r ), Avogadrova konstanta (N A ), látkové množství (n, mol), molární hmotnost (M, g/mol),
Elektrody pro snímání biologických potenciálů. X31ZLE Základy lékařské elektroniky Jan Havlík Katedra teorie obvodů
 Elektrody pro snímání biologických potenciálů X31ZLE Základy lékařské elektroniky Jan Havlík Katedra teorie obvodů xhavlikj@fel.cvut.cz Spojení elektroda elektrolyt organismus vodič 2. třídy (ionty) přívodní
Elektrody pro snímání biologických potenciálů X31ZLE Základy lékařské elektroniky Jan Havlík Katedra teorie obvodů xhavlikj@fel.cvut.cz Spojení elektroda elektrolyt organismus vodič 2. třídy (ionty) přívodní
Inhibitory koroze kovů
 Inhibitory koroze kovů Úvod Korozní rychlost kovových materiálů lze ovlivnit úpravou prostředí, ve kterém korozní děj probíhá. Mezi tyto úpravy patří i použití inhibitorů koroze kovů. Inhibitor je látka,
Inhibitory koroze kovů Úvod Korozní rychlost kovových materiálů lze ovlivnit úpravou prostředí, ve kterém korozní děj probíhá. Mezi tyto úpravy patří i použití inhibitorů koroze kovů. Inhibitor je látka,
PHH-860. Ruční měřící přístroj ph/mv/teploty s komunikačním rozhraním RS-232
 PHH-860 Ruční měřící přístroj ph/mv/teploty s komunikačním rozhraním RS-232 Uživatelská příručka PHH-860 Ruční Měřící Přístroj ph/mv/teploty Se Schopností Komunikace Prostřednictvím Rozhraní RS-232 www.omegaeng.cz
PHH-860 Ruční měřící přístroj ph/mv/teploty s komunikačním rozhraním RS-232 Uživatelská příručka PHH-860 Ruční Měřící Přístroj ph/mv/teploty Se Schopností Komunikace Prostřednictvím Rozhraní RS-232 www.omegaeng.cz
Studium kyselosti a zásaditosti roztoků kolem nás
 Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Studium kyselosti a zásaditosti roztoků kolem nás (laboratorní práce) Označení: EU-Inovace-Ch-8-10 Předmět: Chemie Cílová
Zvyšování kvality výuky v přírodních a technických oblastech CZ.1.07/1.1.28/02.0055 Studium kyselosti a zásaditosti roztoků kolem nás (laboratorní práce) Označení: EU-Inovace-Ch-8-10 Předmět: Chemie Cílová
Laboratorní práce č. 8: Elektrochemické metody stanovení korozní rychlosti
 Laboratorní práce č. 8: Elektrochemické metody stanovení korozní rychlosti Cíl práce: Cílem laboratorní úlohy Elektrochemické metody stanovení korozní rychlosti je stanovení korozní rychlosti oceli v prostředí
Laboratorní práce č. 8: Elektrochemické metody stanovení korozní rychlosti Cíl práce: Cílem laboratorní úlohy Elektrochemické metody stanovení korozní rychlosti je stanovení korozní rychlosti oceli v prostředí
Návod k obsluze HI 993310 Přenosný konduktometr pro půdu
 Návod k obsluze HI 993310 Přenosný konduktometr pro půdu www.hanna-instruments.cz 1 Vážený zákazníku, děkujeme Vám, že jste si vybral produkt od firmy Hanna Instruments. Před použitím přístroje si prosím
Návod k obsluze HI 993310 Přenosný konduktometr pro půdu www.hanna-instruments.cz 1 Vážený zákazníku, děkujeme Vám, že jste si vybral produkt od firmy Hanna Instruments. Před použitím přístroje si prosím
chemie Měření ph elektrolytů, hydrolýza solí Cíle Podrobnější rozbor cílů Zařazení do výuky Časová náročnost Zadání úlohy Návaznost experimentů
 Měření ph elektrolytů, hydrolýza solí pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 07 úloha číslo Cíle Cílem tohoto laboratorního cvičení je měření ph silných a slabých
Měření ph elektrolytů, hydrolýza solí pracovní návod s metodickým komentářem pro učitele připravil M. Škavrada chemie 07 úloha číslo Cíle Cílem tohoto laboratorního cvičení je měření ph silných a slabých
ZKOUŠEČKA NAPĚTÍ AX-T903. Návod k obsluze
 ZKOUŠEČKA NAPĚTÍ AX-T903 Návod k obsluze Bezpečnost Mezinárodní bezpečnostní symboly Varování před potencionálním nebezpečím. Přečtěte si návod k obsluze. Upozornění!Nebezpečné napětí! Riziko úrazu elektrickým
ZKOUŠEČKA NAPĚTÍ AX-T903 Návod k obsluze Bezpečnost Mezinárodní bezpečnostní symboly Varování před potencionálním nebezpečím. Přečtěte si návod k obsluze. Upozornění!Nebezpečné napětí! Riziko úrazu elektrickým
Inovace bakalářského studijního oboru Aplikovaná chemie CZ.1.07/2.2.00/ Výpočty z chemických vzorců
 Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
Výpočty z chemických vzorců 1. Hmotnost kyslíku je 80 g. Vypočítejte : a) počet atomů kyslíku ( 3,011 10 atomů) b) počet molů kyslíku (2,5 mol) c) počet molekul kyslíku (1,505 10 24 molekul) d) objem (dm
Stanovení kritické micelární koncentrace
 Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Stanovení kritické micelární koncentrace TEORIE KONDUKTOMETRIE Měrná elektrická vodivost neboli konduktivita je fyzikální veličinou, která popisuje schopnost látek vést elektrický proud. Látky snadno vedoucí
Úloha č. 8 POTENCIOMETRICKÁ TITRACE. Stanovení silných kyselin alkalimetrickou titrací s potenciometrickou indikací bodu ekvivalence
 1 Princip Úloha č. 8 POTENCIOMETRICKÁ TITRACE Stanovení silných kyselin alkalimetrickou titrací s potenciometrickou indikací bodu ekvivalence Nepřímá potenciometrie potenciometrická titrace se využívá
1 Princip Úloha č. 8 POTENCIOMETRICKÁ TITRACE Stanovení silných kyselin alkalimetrickou titrací s potenciometrickou indikací bodu ekvivalence Nepřímá potenciometrie potenciometrická titrace se využívá
Děkuji moc za výběr tohoto produktu. Teploměr změří během několika vteřin tělesnou teplotu a to buď na čele a nebo v uchu.. To má následující výhody:
 Přehled Děkuji moc za výběr tohoto produktu. Teploměr změří během několika vteřin tělesnou teplotu a to buď na čele a nebo v uchu.. To má následující výhody: 1) provedení 4-v-1 Měří teplotu okolí a tělesnou
Přehled Děkuji moc za výběr tohoto produktu. Teploměr změří během několika vteřin tělesnou teplotu a to buď na čele a nebo v uchu.. To má následující výhody: 1) provedení 4-v-1 Měří teplotu okolí a tělesnou
Ústřední komise Chemické olympiády. 56. ročník 2019/2020 ŠKOLNÍ KOLO. Kategorie A. Praktická část Zadání 40 bodů
 Ústřední komise Chemické olympiády 56. ročník 2019/2020 ŠKOLNÍ KOLO Kategorie A Praktická část Zadání 40 bodů PRAKTICKÁ ČÁST 40 BODŮ Autor Doc. Ing. Petr Exnar, CSc. Technická univerzita v Liberci Recenze
Ústřední komise Chemické olympiády 56. ročník 2019/2020 ŠKOLNÍ KOLO Kategorie A Praktická část Zadání 40 bodů PRAKTICKÁ ČÁST 40 BODŮ Autor Doc. Ing. Petr Exnar, CSc. Technická univerzita v Liberci Recenze
Laboratorní cvičení z kinetiky chemických reakcí
 Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU KOBALTU METODOU ICP-MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KOBALTU METODOU ICP-MS 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení celkového obsahu kobaltu v krmivech metodou hmotnostní spektrometrie
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KOBALTU METODOU ICP-MS 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení celkového obsahu kobaltu v krmivech metodou hmotnostní spektrometrie
5b MĚŘENÍ VISKOZITY KAPALIN POMOCÍ PADAJÍCÍ KULIČKY
 Laboratorní cvičení z předmětu Reologie potravin a kosmetických prostředků 5b MĚŘENÍ VISKOZITY KAPALIN POMOCÍ PADAJÍCÍ KULIČKY 1. TEORIE: Měření viskozity pomocí padající kuličky patří k nejstarším metodám
Laboratorní cvičení z předmětu Reologie potravin a kosmetických prostředků 5b MĚŘENÍ VISKOZITY KAPALIN POMOCÍ PADAJÍCÍ KULIČKY 1. TEORIE: Měření viskozity pomocí padající kuličky patří k nejstarším metodám
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MĚDI, ŽELEZA, MANGANU A ZINKU METODOU FAAS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MĚDI, ŽELEZA, MANGANU A ZINKU METODOU FAAS 1 Účel a rozsah Tato metoda specifikuje podmínky pro stanovení obsahu mědi, manganu, zinku a železa ve
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MĚDI, ŽELEZA, MANGANU A ZINKU METODOU FAAS 1 Účel a rozsah Tato metoda specifikuje podmínky pro stanovení obsahu mědi, manganu, zinku a železa ve
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
Dávkovací stanice VA PRO SALT
 Dávkovací stanice VA PRO SALT Překlad původního návodu k použití 1 Obsah 1. VŠEOBECNÝ ÚVOD... 2 2. OBSAH BALENÍ... 3 3. TECHNICKÉ ÚDAJE... 3 4. POKYNY K MONTÁŽI... 3 5. ELEKTRICKÉ ZAPOJENÍ... 4 6. NASTAVENÍ
Dávkovací stanice VA PRO SALT Překlad původního návodu k použití 1 Obsah 1. VŠEOBECNÝ ÚVOD... 2 2. OBSAH BALENÍ... 3 3. TECHNICKÉ ÚDAJE... 3 4. POKYNY K MONTÁŽI... 3 5. ELEKTRICKÉ ZAPOJENÍ... 4 6. NASTAVENÍ
2. PROTOLYTICKÉ REAKCE
 2. PROTOLYTICKÉ REAKCE Protolytické reakce představují všechny reakce spojené s výměnou protonů a jsou označovány jako reakce acidobazické. Teorie Arrheniova (1884): kyseliny disociují ve vodě na vodíkový
2. PROTOLYTICKÉ REAKCE Protolytické reakce představují všechny reakce spojené s výměnou protonů a jsou označovány jako reakce acidobazické. Teorie Arrheniova (1884): kyseliny disociují ve vodě na vodíkový
Jana Fauknerová Matějčková
 Jana Fauknerová Matějčková převody jednotek výpočet ph ph vodných roztoků ph silných kyselin a zásad ph slabých kyselin a zásad, disociační konstanta, pk ph pufrů koncentace 1000mg př. g/dl mg/l = = *10000
Jana Fauknerová Matějčková převody jednotek výpočet ph ph vodných roztoků ph silných kyselin a zásad ph slabých kyselin a zásad, disociační konstanta, pk ph pufrů koncentace 1000mg př. g/dl mg/l = = *10000
CDE681 - Snímač vodivosti a měrného odporu. Uživatelská příručka
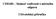 CDE681 - Snímač vodivosti a měrného odporu Uživatelská příručka Obsah: Omega.com První část Úvod Oddíl č.1: - Základní údaje - 1.1 Popis: Výhody rozšířeného výkonnějšího modelu...5 Charakteristiky snímače....5
CDE681 - Snímač vodivosti a měrného odporu Uživatelská příručka Obsah: Omega.com První část Úvod Oddíl č.1: - Základní údaje - 1.1 Popis: Výhody rozšířeného výkonnějšího modelu...5 Charakteristiky snímače....5
Teorie kyselin a zásad poznámky 5.A GVN
 Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
Teorie kyselin a zásad poznámky 5A GVN 13 června 2007 Arrheniova teorie platná pouze pro vodní roztoky kyseliny jsou látky schopné ve vodném roztoku odštěpit vodíkový kation H + HCl H + + Cl - CH 3 COOH
Metodika stanovení kyselinové neutralizační kapacity v pevných odpadech
 Metodika stanovení kyselinové neutralizační kapacity v pevných odpadech 1 Princip Principem zkoušky je stanovení vodného výluhu při různých přídavcích kyseliny dusičné nebo hydroxidu sodného a následné
Metodika stanovení kyselinové neutralizační kapacity v pevných odpadech 1 Princip Principem zkoušky je stanovení vodného výluhu při různých přídavcích kyseliny dusičné nebo hydroxidu sodného a následné
PHH-60MS/PHH-60TDS PHH-80MS/PHH-80TDS
 PHH-60MS/PHH-60TDS PHH-80MS/PHH-80TDS Měřič ph a vodivosti v provedení Pocket Pal Návod k použití Příprava přístroje Instalace baterií (obr. 2) Opatrně vyjměte přístroj z přenosného obalu. Neztraťte malý
PHH-60MS/PHH-60TDS PHH-80MS/PHH-80TDS Měřič ph a vodivosti v provedení Pocket Pal Návod k použití Příprava přístroje Instalace baterií (obr. 2) Opatrně vyjměte přístroj z přenosného obalu. Neztraťte malý
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253
 Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 16 Iontová chromatografie Iontová chromatografie je speciální technika vyvinutá pro separaci anorganických iontů a organických
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 16 Iontová chromatografie Iontová chromatografie je speciální technika vyvinutá pro separaci anorganických iontů a organických
Ústřední komise Chemické olympiády. 42. ročník. KRAJSKÉ KOLO Kategorie D. SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut
 Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Ústřední komise Chemické olympiády 42. ročník 2005 2006 KRAJSKÉ KOLO Kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Časová náročnost: 60 minut Institut dětí a mládeže Ministerstva školství, mládeže a tělovýchovy
Analyzátor sodíku. Easy Na Jednoduchost Přesnost Specifičnost. Specifické stanovení obsahu sodíku Snadné a přesné
 Analyzátor sodíku Easy Na Jednoduchost Přesnost Specifičnost Specifické stanovení obsahu sodíku Snadné a přesné Úvod Analyzátor sodíku pro jednoduchou a přesnou analýzu Nový analyzátor sodíku stanovuje
Analyzátor sodíku Easy Na Jednoduchost Přesnost Specifičnost Specifické stanovení obsahu sodíku Snadné a přesné Úvod Analyzátor sodíku pro jednoduchou a přesnou analýzu Nový analyzátor sodíku stanovuje
Praktické ukázky analytických metod ve vinařství
 Praktické ukázky analytických metod ve vinařství Ing. Mojmír Baroň Stanovení v moštu Stanovení ph a veškerých titrovatelných kyselin Stanovení ph Princip: Hodnota ph je záporný dekadický logaritmus aktivity
Praktické ukázky analytických metod ve vinařství Ing. Mojmír Baroň Stanovení v moštu Stanovení ph a veškerých titrovatelných kyselin Stanovení ph Princip: Hodnota ph je záporný dekadický logaritmus aktivity
Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory
 Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory Titrace je spolehlivý a celkem nenáročný postup, jak zjistit koncentraci analytu, její
Automatická potenciometrická titrace Klinická a toxikologická analýza Chemie životního prostředí Geologické obory Titrace je spolehlivý a celkem nenáročný postup, jak zjistit koncentraci analytu, její
Stanovení celkové kyselosti nápojů potenciometrickou titrací
 Stanovení celkové kyselosti nápojů potenciometrickou titrací Princip metody U acidobazických titrací se využívají dva druhy indikace bodu ekvivalence - vizuální a instrumentální. K vizuální indikaci bodu
Stanovení celkové kyselosti nápojů potenciometrickou titrací Princip metody U acidobazických titrací se využívají dva druhy indikace bodu ekvivalence - vizuální a instrumentální. K vizuální indikaci bodu
Chemický průmysl. Školní pokusy. Stanovení indexu lomu. Brožura s tipy a triky. škola hrou. pro stanovení indexu lomu
 Chemický průmysl Školní pokusy Stanovení indexu lomu Brožura s tipy a triky Vyzkoušejte přírodní 10 tipů zákony a v praxi triků škola hrou pro stanovení indexu lomu Vážený čtenáři, především Vám děkujeme
Chemický průmysl Školní pokusy Stanovení indexu lomu Brožura s tipy a triky Vyzkoušejte přírodní 10 tipů zákony a v praxi triků škola hrou pro stanovení indexu lomu Vážený čtenáři, především Vám děkujeme
PHH-7011. Uživatelská příručka. ph/mv/teplota - vodotěsný tester. tel: 596 311 899 fax: 596 311 114 web: www.jakar.cz e-mail: kontakt@jakar.
 PHH-7011 Uživatelská příručka ph/mv/teplota - vodotěsný tester Obsah Úvod 3 Vlastnosti 3 Specifikace. 3 Popis přístroje... 4 Popis displeje 5 Funkce klávesnice 5 Pokyny k obsluze. 6 Kalibrace. 6 Měření.
PHH-7011 Uživatelská příručka ph/mv/teplota - vodotěsný tester Obsah Úvod 3 Vlastnosti 3 Specifikace. 3 Popis přístroje... 4 Popis displeje 5 Funkce klávesnice 5 Pokyny k obsluze. 6 Kalibrace. 6 Měření.
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC
 Strana 1 STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Postup specifikuje podmínky pro stanovení obsahu semduramicinu v krmivech metodou vysokoúčinné kapalinové chromatografie (HPLC) v koncentračním
Strana 1 STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Postup specifikuje podmínky pro stanovení obsahu semduramicinu v krmivech metodou vysokoúčinné kapalinové chromatografie (HPLC) v koncentračním
CHEMIE. Pracovní list č. 7 - žákovská verze Téma: ph. Mgr. Lenka Horutová. Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.
 www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
www.projektsako.cz CHEMIE Pracovní list č. 7 - žákovská verze Téma: ph Lektor: Mgr. Lenka Horutová Projekt: Student a konkurenceschopnost Reg. číslo: CZ.1.07/1.1.07/03.0075 Teorie: Pro snadnější výpočet
Galvanický článek. Li Rb K Na Be Sr Ca Mg Al Be Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi As CU Hg Ag Pt Au
 Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
Na www.studijni-svet.cz zaslal(a): Téra2507. Elektrochemické metody
 Na www.studijni-svet.cz zaslal(a): Téra2507 Elektrochemické metody Elektrolýza Do roztoku elektrolytu ponoříme dvě elektrody a vložíme na ně dostatečně velké vnější stejnosměrné napětí. Roztok elektrolytu
Na www.studijni-svet.cz zaslal(a): Téra2507 Elektrochemické metody Elektrolýza Do roztoku elektrolytu ponoříme dvě elektrody a vložíme na ně dostatečně velké vnější stejnosměrné napětí. Roztok elektrolytu
Charlesův zákon (pt závislost)
 Charlesův zákon (pt závislost) V této úloze pomocí čidla tlaku plynu GPS-BTA a teploměru TMP-BTA (nebo čidla Go!Temp) objevíme součást stavové rovnice ideálního plynu Charlesův zákon popisující izochorický
Charlesův zákon (pt závislost) V této úloze pomocí čidla tlaku plynu GPS-BTA a teploměru TMP-BTA (nebo čidla Go!Temp) objevíme součást stavové rovnice ideálního plynu Charlesův zákon popisující izochorický
PRAKTIKUM II. Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK. Název: Elektrická vodivost elektrolytů. stud. skup.
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM II. Úloha č. 26 Název: Elektrická vodivost elektrolytů Pracoval: Lukáš Vejmelka stud. skup. FMUZV 73) dne 12.12.2013 Odevzdal
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM II. Úloha č. 26 Název: Elektrická vodivost elektrolytů Pracoval: Lukáš Vejmelka stud. skup. FMUZV 73) dne 12.12.2013 Odevzdal
ČIDLO PRO MĚŘENÍ KONCENTRACE CHLORU TYP CSCT 43
 ČIDLO PRO MĚŘENÍ KONCENTRACE CHLORU TYP CSCT 43 Návod k používání a údržbě! OBSAH 1. Rozsah použití... strana 2 2. Rozsah dodávky... strana 3 3. Uvedení do provozu... strana 3 4. Měření... strana 4 5.
ČIDLO PRO MĚŘENÍ KONCENTRACE CHLORU TYP CSCT 43 Návod k používání a údržbě! OBSAH 1. Rozsah použití... strana 2 2. Rozsah dodávky... strana 3 3. Uvedení do provozu... strana 3 4. Měření... strana 4 5.
Teploměr MS6501 R242C
 Teploměr MS6501 R242C Návod k použití Obsah 1. Přehled... 3 2. Popis teploměru... 3 3. Použití... 4 4. Specifikace... 5 5. Přesnost... 6 5.1 C...6 5.2 F...6 6. Údržba... 6 7. Výměna baterie... 7 1 Symbol
Teploměr MS6501 R242C Návod k použití Obsah 1. Přehled... 3 2. Popis teploměru... 3 3. Použití... 4 4. Specifikace... 5 5. Přesnost... 6 5.1 C...6 5.2 F...6 6. Údržba... 6 7. Výměna baterie... 7 1 Symbol
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Střední odborná škola a Střední odborné učiliště, Hustopeče, Masarykovo nám. 1
 Číslo projektu Číslo materiálu Název školy CZ.1.07/1.5.00/34.0394 VY_32_INOVACE_15_OC_1.01 Střední odborná škola a Střední odborné učiliště, Hustopeče, Masarykovo nám. 1 Autor Tématický celek Ing. Zdenka
Číslo projektu Číslo materiálu Název školy CZ.1.07/1.5.00/34.0394 VY_32_INOVACE_15_OC_1.01 Střední odborná škola a Střední odborné učiliště, Hustopeče, Masarykovo nám. 1 Autor Tématický celek Ing. Zdenka
ČISTICÍ PROSTŘEDEK A VAŠE RUCE
 ČISTICÍ PROSTŘEDEK A VAŠE RUCE Úvod Marta žije v městě, které má tvrdou vodu - obsahuje velké množství minerálních látek. 1 Jedním z problémů při používání tvrdé vody je, že v místech, kde voda stojí,
ČISTICÍ PROSTŘEDEK A VAŠE RUCE Úvod Marta žije v městě, které má tvrdou vodu - obsahuje velké množství minerálních látek. 1 Jedním z problémů při používání tvrdé vody je, že v místech, kde voda stojí,
DOPLŇKOVÝ STUDIJNÍ MATERIÁL CHEMICKÉ VÝPOČTY. Zuzana Špalková. Věra Vyskočilová
 DOPLŇKOVÝ STUDIJNÍ MATERIÁL CHEMICKÉ VÝPOČTY Zuzana Špalková Věra Vyskočilová BRNO 2014 Doplňkový studijní materiál zaměřený na Chemické výpočty byl vytvořen v rámci projektu Interní vzdělávací agentury
DOPLŇKOVÝ STUDIJNÍ MATERIÁL CHEMICKÉ VÝPOČTY Zuzana Špalková Věra Vyskočilová BRNO 2014 Doplňkový studijní materiál zaměřený na Chemické výpočty byl vytvořen v rámci projektu Interní vzdělávací agentury
ZÁKLADNÍ MODELY TOKU PORÉZNÍ MEMBRÁNOU
 ZÁKLADNÍ MODELY TOKU PORÉZNÍ MEMBRÁNOU Znázornění odporů způsobujících snižování průtoku permeátu nástřik porézní membrána Druhy odporů R p blokování pórů R p R a R m R a R m R g R cp adsorbce membrána
ZÁKLADNÍ MODELY TOKU PORÉZNÍ MEMBRÁNOU Znázornění odporů způsobujících snižování průtoku permeátu nástřik porézní membrána Druhy odporů R p blokování pórů R p R a R m R a R m R g R cp adsorbce membrána
