SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
|
|
|
- Ivana Vaňková
- před 7 lety
- Počet zobrazení:
Transkript
1 Príloha č. 1 k notifikácii o zmene, ev.č. 2013/05607 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU PICOPREP prášok na perorálny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedno vrecko obsahuje nasledujúce liečivá: Dinátriumpikosulfát Oxid horečnatý, ľahký Kyselina citrónová, bezvodá 10,0 mg 3,5 g 12,0 g Jedno vrecko ďalej obsahuje: Hydrogenuhličitan draselný 0,5 g [ekvivalentné 5 mmol (195 mg) draslíka] Laktóza (ako súčasť chuťovej prísady) Úplný zoznam pomocných látok, pozri časť LIEKOVÁ FORMA Prášok na perorálny roztok vo vrecku. Biely kryštalický prášok. 4. KLINICKÉ ÚDAJE 4.1 Terapeutické indikácie Vyčistenie čreva pred rádiologickým alebo endoskopickým vyšetrením. Vyčistenie čreva pred chirurgickým výkonom, keď je to klinicky nevyhnutné (pozri časť 4.4 otvorená kolorektálna operácia). 4.2 Dávkovanie a spôsob podávania Spôsob podávania: perorálne Deň pred nemocničným vyšetrením sa odporúča bezzvyšková diéta. Na zabránenie dehydratácie počas liečby liekom PICOPREP sa odporúča vypiť za hodinu približne 250 ml vody alebo inej čírej tekutiny, pokiaľ pretrváva účinok lieku. Pokyny na rozpúšťanie: Obsah jedného vrecka sa rozpustí v pohári vody (približne 150 ml). Po premiešaní 2 3 minúty vznikne belavý zakalený roztok so slabou pomarančovou vôňou. Pripravený roztok sa vypije. Ak je horúci, treba počkať, kým nevychladne na prijateľnú teplotu. Dospelí (vrátane starších pacientov):
2 Jedno vrecko sa rozpustí vo vode, ako je uvedené vyššie a užije sa ráno pred 8. hodinou deň pred vyšetrením. Druhé vrecko treba užiť o 6 až 8 hodín neskôr. Pediatrická populácia: K lieku je priložená odmerná lyžička. Odporúča sa zarovnať povrch naplnenej lyžičky pomocou plochej hrany, napr. tupou hranou noža, a odstrániť tak prebytok prášku. Takto sa odmeria jednou lyžičkou ¼ vrecka (4 g prášku). 1 2 roky: 1 lyžička ráno, 1 lyžička popoludní 2 4 roky: 2 lyžičky ráno, 2 lyžičky popoludní 4 9 rokov: 1 vrecko ráno, 2 lyžičky popoludní 9 a viac rokov: dávka ako pre dospelých Požadované množstvo prášku sa rozpustí v pohári, ktorý obsahuje približne 50 ml vody na 1 lyžičku prášku. Po premiešaní 2 3 minúty vznikne belavý zakalený roztok so slabou pomarančovou vôňou. Pripravený roztok sa vypije. Ak je horúci, treba počkať, kým nevychladne na prijateľnú teplotu. Nespotrebovaný obsah vrecka sa má zlikvidovať. Pokyny na rozpustenie celého vrecka pre deti vo veku 4 9 rokov sú uvedené v pokynoch na rozpúšťanie pre dospelých. 4.3 Kontraindikácie - Precitlivenosť na ktorúkoľvek zložku lieku - Kongestívne zlyhanie srdca - Retencia žalúdočného obsahu - Gastrointestinálne vredy - Toxická kolitída - Toxický megakólon - Ileus - Nauzea a vracanie - Akútne brušné stavy vyžadujúce chirurgický zákrok, napr. akútna apendicitída - Známa alebo suspektná obštrukcia čreva alebo perforácia - Závažná dehydratácia - Rabdomyolýza - Hypermagneziémia - Akútne črevné zápalové ochorenie - U pacientov so závažným poškodením funkcie obličiek môže dôjsť k hromadeniu horčíka v plazme. V týchto prípadoch je potrebné použiť iný liek. 4.4 Osobitné upozornenia a opatrenia pri používaní Pretože sa nedokázal klinicky významný prínos prečistenia čriev pred plánovanou otvorenou kolorektálnou operáciou, látky na prečistenie čriev sa majú podať pred operáciou na črevách len vtedy, ak je to nevyhnutné. Riziká liečby je treba dôkladne zvážiť oproti možným prínosom a potrebám zvoleného operačného postupu. V nedávnej minulosti vykonaný chirurgický výkon v tráviacom trakte. Pozornosť treba tiež venovať pacientom s poškodením funkcie obličiek, chorobou srdca alebo zápalovým črevným ochorením. Opatrnosť je potrebná u pacientov užívajúcich lieky, ktoré môžu ovplyvniť rovnováhu vody a/alebo elektrolytov, napr. diuretiká, kortikosteroidy, lítium (pozri časť 4.5). 2
3 PICOPREP môže ovplyvniť absorpciu pravidelne predpisovaných perorálnych liekov a má sa používať s opatrnosťou, napr. boli hlásené ojedinelé prípady kŕčov u pacientov užívajúcich antiepileptiká, u ktorých bola predtým epilepsia pod kontrolou (pozri časti 4.5 a 4.8). Nedostatočný perorálny príjem vody a elektrolytov môže spôsobiť klinicky významnú deficienciu predovšetkým u menej odolných pacientov. Vzhľadom k tomu je potrebné venovať zvýšenú pozornosť deťom, starším a oslabeným jedincom a pacientom s rizikom hypokaliémie. U pacientov s príznakmi a znakmi hyponatriémie je potrebné urýchlene obnoviť rovnováhu tekutín/elektrolytov. Doba prečisťovania čriev nemá byť dlhšia ako 24 hodín, pretože dlhšia príprava môže zvýšiť riziko nerovnováhy vody a elektrolytov. Liek obsahuje 5 mmol (alebo 195 mg) draslíka v jednom vrecku. Je potrebné to vziať do úvahy u pacientov so zníženou funkciou obličiek alebo u pacientov s diétou kontrolovanou na obsah draslíka. Tento liek obsahuje laktózu ako zložku chuťovej prísady. Liek sa nemá podávať pacientom so zriedkavými dedičnými poruchami: intoleranciou galaktózy, deficienciou laktázy alebo s poruchou absorpcie glukózy a galaktózy. PICOPREP sa nemá používať ako bežné laxatívum. 4.5 Liekové a iné interakcie PICOPREP je preháňadlo, a teda zrýchľuje tranzit tráviacim traktom. Absorpcia iných perorálne užívaných liekov (napr. antiepileptiká, kontraceptíva, antidiabetiká, antibiotiká) môže byť preto počas liečby zmenená (pozri časť 4.4). Tetracyklínové a fluorochinolónové antibiotiká, železo, digoxín, chlórpromazín a penicilamín sa majú užiť najmenej 2 hodiny pred podaním lieku PICOPREP a nie menej ako 6 hodín po jeho podaní, aby sa zabránilo chelácii s horčíkom. Účinok lieku PICOPREP znižujú laxatíva zväčšujúce objem stolice. Pozornosť sa vyžaduje u pacientov užívajúcich lieky, ktoré môžu spôsobovať hypokaliémiu (ako sú diuretiká alebo kortikosteroidy alebo lieky, u ktorých je hlavným rizikom hypokaliémia, napr. srdcové glykozidy). Pozornosť sa má tiež venovať pacientom, ktorí užívajú PICOPREP súčasne s NSAID alebo liekmi indukujúcimi SIADH, napr. tricyklické antidepresíva, inhibítory spätného vychytávania serotonínu, antipsychotiká a karbamazepín, pretože tieto lieky môžu zvyšovať riziko retencie vody a/alebo elektrolytickej nerovnováhy. 4.6 Gravidita a laktácia Nie sú k dispozícii klinické údaje o účinku lieku PICOPREP počas gravidity. Štúdie na zvieratách preukázali reprodukčnú toxicitu (pozri časť 5.3). Nakoľko PICOPREP je stimulačné laxatívum, kvôli bezpečnosti sa neodporúča jeho užívanie počas gravidity. Nie sú skúsenosti s užívaním lieku PICOPREP u dojčiacich matiek. No vzhľadom na farmakokinetické vlastnosti liečiv možno u dojčiacich matiek zvážiť liečbu s liekom PICOPREP. 4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje Netýka sa. 4.8 Nežiaduce účinky Trieda orgánových systémov podľa MedDRA Poruchy imunitného Časté ( 1/100 až < 1/10) Menej časté ( 1/1 000 až < 1/100) Anafylaktická reakcia, Neznáme (z dostupných údajov) 3
4 systému Poruchy metabolizmu a výživy Poruchy nervového systému Poruchy gastrointestinálneho traktu Bolesť hlavy Nauzea a proktalgia hypersenzitivita Hyponatriémia a hypokaliémia Epilepsia, tonickoklonické záchvaty (grand mal), kŕče, zmätenosť Vracanie, abdominálna bolesť, aftoidné vredy v ileu* Hnačka, fekálna inkontinencia Poruchy kože Vyrážka (vrátane a podkožného tkaniva erytematóznej a makulopapulóznej vyrážky, žihľavka, purpura) *Hlásené boli ojedinelé prípady mierne závažných reverzibilných aftoidných vredov v ileu. Frekvencia nežiaducich účinkov sa uvádza na základe skúseností po uvedení lieku na trh. Hnačka a fekálna inkontinencia patria k primárnym klinickým účinkom lieku PICOPREP. Po uvedení lieku na trh boli hlásené ojedinelé prípady závažnej hnačky. Hlásená bola hyponatriémia sprevádzaná kŕčmi alebo bez nich. U epileptických pacientov boli hlásené ojedinelé prípady záchvatov/grand mal kŕče, ktoré nesúviseli s hyponatriémiou. Hlásené boli ojedinelé prípady anafylaktoidnej reakcie. 4.9 Predávkovanie Predávkovanie môže viesť k silným hnačkám. Liečba je vo všeobecnosti podporná a dôležité je dodržiavať príjem tekutín. 5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti Farmakoterapeutická skupina: kontaktné laxatíva ATC kód: A06AB58 Liečivá v lieku PICOPREP sú dinátriumpikosulfát a citrát horečnatý. Dinátriumpikosulfát je lokálne pôsobiace stimulačné preháňadlo. V hrubom čreve sa bakteriálne štiepi na aktívnu laxatívnu zlúčeninu, bis-(p-hydroxyfenyl)-pyridyl-2-metán (BHPM), ktorá stimuluje sliznicu hrubého čreva aj konečníka. Citrát horečnatý pôsobí ako osmotické laxatívum, teda udržiava vlhkosť stolice v hrubom čreve. Celkový účinok týchto dvoch látok pozostáva z "vymývania" v kombinácii so stimuláciou peristaltiky, čo zabezpečuje vyčistenie čreva. Liek nie je určený na použitie ako bežné laxatívum. 5.2 Farmakokinetické vlastnosti Obidve liečivá pôsobia lokálne v hrubom čreve a ani jedno z nich sa neabsorbuje v detekovateľnom množstve. 4
5 5.3 Predklinické údaje o bezpečnosti Štúdie o vývoji v prenatálnom období na potkanoch a králikoch nepreukázali žiaden teratogénny účinok po perorálnom užití dinátriumpikosulfátu, no embryotoxicita sa pozorovala u potkanov v dávke a mg/kg/deň a u králikov v dávke mg/kg/deň. Zodpovedajúce hranice bezpečnosti boli až krát vyššie ako predpokladaná dávka u ľudí. U potkanov denná dávka 10 mg/kg v neskorom štádiu gestácie (vývoja plodu) a počas laktácie spôsobila zníženie hmotnosti a prežívania potomstva. Fertilita potkaních samcov a samičiek nebola ovplyvnená perorálnymi dávkami dinátriumpikosulfátu do dávky 100 mg/kg. 6. FARMACEUTICKÉ INFORMÁCIE 6.1 Zoznam pomocných látok Hydrogenuhličitan draselný Sacharín sodný Prírodná sprejovo sušená pomarančová príchuť, ktorá obsahuje arabskú gumu, laktózu, kyselinu askorbovú a butylovaný hydroxyanizol 6.2 Inkompatibility Neaplikovateľné. 6.3 Čas použiteľnosti 3 roky Po otvorení vrecko ihneď použite a zvyšok prášku alebo roztoku zlikvidujte. 6.4 Špeciálne upozornenia na uchovávanie Uchovávajte v pôvodnom obale na ochranu pred vlhkosťou. 6.5 Druh obalu a obsah balenia Vrecko: 4 vrstvy: papier polyetylén nízkej hustoty alumínium termoplastická živica Páry vreciek sa môžu od seba oddeliť odtrhnutím pozdĺž perforácie. Hmotnosť 1 vrecka: 16,1 g Balenie obsahuje odmernú lyžičku na dávkovanie pre deti. PICOPREP sa dodáva v balení s 2 vreckami, 100 vreckami (50 balení s 2 vreckami) alebo 300 vreckami (150 balení s 2 vreckami). Na trh nemusia byť uvedené všetky veľkosti balenia. 6.6 Špeciálne opatrenia na likvidáciu Žiadne zvláštne požiadavky. 5
6 7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII Ferring-Léčiva, a.s. K Rybníku Jesenice u Prahy Česká republika 8. REGISTRAČNÉ ČÍSLO 61/0393/10-S 9. DÁTUM PRVEJ REGISTRÁCIE/PREDĹŽENIA REGISTRÁCIE Dátum prvej registrácie: Dátum posledného predĺženia registrácie: 10. DÁTUM REVÍZIE TEXTU Jún
Jeden sáček rovněž obsahuje: Hydrogenuhličitan draselný 0,5g (ekvivalentní 5 mmol (195 mg) draslíku) Laktosa (součást aroma)
 Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls115288/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PICOPREP prášek pro přípravu perorálního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls115288/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PICOPREP prášek pro přípravu perorálního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
PRÍLOHA III DODATKY K SÚHRNU CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU A PÍSOMNEJ INFORMÁCII PRE POUŽÍVATEĽOV
 PRÍLOHA III DODATKY K SÚHRNU CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU A PÍSOMNEJ INFORMÁCII PRE POUŽÍVATEĽOV Tieto zmeny v SPC a písomnej informácii pre používateľov sú platné v čase Rozhodnutia Komisie. Po
PRÍLOHA III DODATKY K SÚHRNU CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU A PÍSOMNEJ INFORMÁCII PRE POUŽÍVATEĽOV Tieto zmeny v SPC a písomnej informácii pre používateľov sú platné v čase Rozhodnutia Komisie. Po
Jeden sáček rovněž obsahuje: Hydrogenuhličitan draselný 0,5g (ekvivalentní 5 mmol (195 mg) draslíku) Laktosa (součást aroma)
 Sp.zn.sukls152030/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PICOPREP prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující léčivé látky: Natrii picosulfas
Sp.zn.sukls152030/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PICOPREP prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující léčivé látky: Natrii picosulfas
Jeden sáček rovněž obsahuje: Hydrogenuhličitan draselný 0,5g (ekvivalentní 5 mmol (195 mg) draslíku) Laktosa (součást aroma)
 Sp.zn.sukls258690/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PICOPREP prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující léčivé látky: Natrii picosulfas
Sp.zn.sukls258690/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PICOPREP prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující léčivé látky: Natrii picosulfas
Príloha III. Úpravy súhrnu charakteristických vlastností lieku, označenie na obale a písomná informácia je výsledkom postupu preskúmania.
 Príloha III Úprava príslušným častí súhrnu charakteristických vlastností lieku a písomnej informácii pre používateľa Poznámka: Úpravy súhrnu charakteristických vlastností lieku, označenie na obale a písomná
Príloha III Úprava príslušným častí súhrnu charakteristických vlastností lieku a písomnej informácii pre používateľa Poznámka: Úpravy súhrnu charakteristických vlastností lieku, označenie na obale a písomná
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls196661/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PICOPREP prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující léčivé látky: Natrii picosulfas
Sp.zn.sukls196661/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PICOPREP prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující léčivé látky: Natrii picosulfas
Biologické aktivity magnézia (2) Zastúpenie magnézia v organizme (2) Štvrtý najčastejší katión v ľudskom organizme
 Biologické aktivity magnézia (2) Štvrtý najčastejší katión v ľudskom organizme Druhý najčastejší katión v intracelulárnom priestore Podieľa sa na metabolizme enzýmov, elektrolytov a energetickom metabolizme
Biologické aktivity magnézia (2) Štvrtý najčastejší katión v ľudskom organizme Druhý najčastejší katión v intracelulárnom priestore Podieľa sa na metabolizme enzýmov, elektrolytov a energetickom metabolizme
MAGNOSOLV V TEHOTENSTVE
 V TEHOTENSTVE Tehotenstvo predstavuje stav nedostatku horčíka v organizme hladina horčíka v sére klesá asi o 10% (1) Dôsledkom manifestného nedostatku horčíka môže byť zvýšené riziko potratu - predčasný
V TEHOTENSTVE Tehotenstvo predstavuje stav nedostatku horčíka v organizme hladina horčíka v sére klesá asi o 10% (1) Dôsledkom manifestného nedostatku horčíka môže byť zvýšené riziko potratu - predčasný
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha k sp. zn. sukls224939/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Molaxole prášek pro přípravu perorálního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující
Příloha k sp. zn. sukls224939/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Molaxole prášek pro přípravu perorálního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující
NÁZOV, FARMACEUTICKÁ FORMA, MNOŽSTVO ÚČINNÝCH LÁTOK V LIEKU, SPÔSOB PODÁVANIA, UCHÁDZAČ, DRŽITEĽ ROZHODNUTIA O REGISTRÁCII V ČLENSKÝCH ŠTÁTOCH
 PRÍLOHA I NÁZOV, FARMACEUTICKÁ FORMA, MNOŽSTVO ÚČINNÝCH LÁTOK V LIEKU, SPÔSOB PODÁVANIA, UCHÁDZAČ, DRŽITEĽ ROZHODNUTIA O REGISTRÁCII V ČLENSKÝCH ŠTÁTOCH 1 LIEKY OBSAHUJÚCE JÓDKAZEÍN/TIAMÍN S UDELENÝM POVOLENÍM
PRÍLOHA I NÁZOV, FARMACEUTICKÁ FORMA, MNOŽSTVO ÚČINNÝCH LÁTOK V LIEKU, SPÔSOB PODÁVANIA, UCHÁDZAČ, DRŽITEĽ ROZHODNUTIA O REGISTRÁCII V ČLENSKÝCH ŠTÁTOCH 1 LIEKY OBSAHUJÚCE JÓDKAZEÍN/TIAMÍN S UDELENÝM POVOLENÍM
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls23403/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Citrafleet prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček (15,08 g) obsahuje následující léčivé
Sp.zn.sukls23403/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Citrafleet prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček (15,08 g) obsahuje následující léčivé
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUTTALAX 7,5 mg, perorální kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml (= 15 kapek) roztoku obsahuje natrii picosulfas monohydricus 7,5 mg Pomocná
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUTTALAX 7,5 mg, perorální kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml (= 15 kapek) roztoku obsahuje natrii picosulfas monohydricus 7,5 mg Pomocná
Lieky a pacienti s bolesťou
 Dozadu Na začiatok Ďalej Lieky a pacienti s bolesťou Kúpite si občas v lekárni lieky na bolesť alebo vám ich pravidelne predpisuje lekár? Čítajte ďalej a zistite, či pri liečbe občasnej alebo chronickej
Dozadu Na začiatok Ďalej Lieky a pacienti s bolesťou Kúpite si občas v lekárni lieky na bolesť alebo vám ich pravidelne predpisuje lekár? Čítajte ďalej a zistite, či pri liečbe občasnej alebo chronickej
ANNEX III ZMENY V SÚHRNE CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU A PÍSOMNÝCH INFORMÁCIÁCH PRE POUŽÍVATEĽOV
 ANNEX III ZMENY V SÚHRNE CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU A PÍSOMNÝCH INFORMÁCIÁCH PRE POUŽÍVATEĽOV 25 PRÍLOHY K DOPLNENIU RELEVANTNÝCH SEKCII SÚHRNU CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU LIEKOV OBSAHUJÚCICH
ANNEX III ZMENY V SÚHRNE CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU A PÍSOMNÝCH INFORMÁCIÁCH PRE POUŽÍVATEĽOV 25 PRÍLOHY K DOPLNENIU RELEVANTNÝCH SEKCII SÚHRNU CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU LIEKOV OBSAHUJÚCICH
Príloha III. Úprava relevantných častí Súhrnu charakteristických vlastností lieku a Písomnej informácie pre používateľa
 Príloha III Úprava relevantných častí Súhrnu charakteristických vlastností lieku a Písomnej informácie pre používateľa Poznámka: Tento súhrn charakteristických vlastností lieku, označenia obalov a písomnej
Príloha III Úprava relevantných častí Súhrnu charakteristických vlastností lieku a Písomnej informácie pre používateľa Poznámka: Tento súhrn charakteristických vlastností lieku, označenia obalov a písomnej
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls147367/2013 a sp.zn. sukls83349/2015, sukls83357/2015, sukls151866/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Duphalac se švestkovou příchutí, 667 mg/ml, perorální roztok 2. KVALITATIVNÍ
Sp.zn.sukls147367/2013 a sp.zn. sukls83349/2015, sukls83357/2015, sukls151866/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Duphalac se švestkovou příchutí, 667 mg/ml, perorální roztok 2. KVALITATIVNÍ
(tolkapón) tablety DENNÍK PACIENTA. Pomôže vám dodržiavať pravidelné vyšetrenia funkcie pečene počas prvého roku užívania
 (tolkapón) tablety DENNÍK PACIENTA Pomôže vám dodržiavať pravidelné vyšetrenia funkcie pečene po prvého roku užívania INFORMÁCIE O PACIENTOVI 03 PRED UŽITÍM TASMARU SI, PROSÍM, PREČÍTAJTE NASLEDOVNÉ INFORMÁCIE
(tolkapón) tablety DENNÍK PACIENTA Pomôže vám dodržiavať pravidelné vyšetrenia funkcie pečene po prvého roku užívania INFORMÁCIE O PACIENTOVI 03 PRED UŽITÍM TASMARU SI, PROSÍM, PREČÍTAJTE NASLEDOVNÉ INFORMÁCIE
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls53327/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Laevolac 10 g/15 ml perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls53327/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Laevolac 10 g/15 ml perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček
sp.zn. sukls119361/2010
 sp.zn. sukls119361/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LAXYGAL perorální kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku (1 ml = 18 kapek) obsahuje natrii picosulfas
sp.zn. sukls119361/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LAXYGAL perorální kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku (1 ml = 18 kapek) obsahuje natrii picosulfas
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Príloha č. 2 k notifikácii o zmene, ev. č.: 2017/01968-Z1B Schválený text k rozhodnutiu o prevode, ev. č.: 2017/01969-TR 1. NÁZOV LIEKU Capsagamma 53 mg/100 g krém SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
Príloha č. 2 k notifikácii o zmene, ev. č.: 2017/01968-Z1B Schválený text k rozhodnutiu o prevode, ev. č.: 2017/01969-TR 1. NÁZOV LIEKU Capsagamma 53 mg/100 g krém SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
2. Kvalitatívne a kvantitatívne zloženie lieku Triprolidini hydrochloridum 25,0 mg, Pseudoephedrini hydrochloridum 600,0 mg v 100 ml sirupu.
 1 Súhrn charakteristických vlastností lieku (SPC) 1. Názov lieku TRIFED sirup 2. Kvalitatívne a kvantitatívne zloženie lieku Triprolidini hydrochloridum 25,0 mg, Pseudoephedrini hydrochloridum 600,0 mg
1 Súhrn charakteristických vlastností lieku (SPC) 1. Názov lieku TRIFED sirup 2. Kvalitatívne a kvantitatívne zloženie lieku Triprolidini hydrochloridum 25,0 mg, Pseudoephedrini hydrochloridum 600,0 mg
Choďte menej v noci, užívajte si viac cez deň
 Novinka pre pacientov s LUTS/BPH Choďte menej v noci, užívajte si viac cez deň Novinka v liečbe LUTS/BPH Negatívne vplyvy noktúrie Lekári považujú noktúriu za jeden z najviac obťažujúcich symptómov LUTS/BPH.
Novinka pre pacientov s LUTS/BPH Choďte menej v noci, užívajte si viac cez deň Novinka v liečbe LUTS/BPH Negatívne vplyvy noktúrie Lekári považujú noktúriu za jeden z najviac obťažujúcich symptómov LUTS/BPH.
Vyšetrenie trvá 2 3 hodiny, počas ktorých pacient opakovane vydýchne do prístroja. Lek ár by mal byť informovaný:
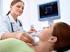 Dychový test na SIBO pokyny pre pacienta je bezbolestný dychový test, ktorým možno diagnostikovať bakteriálne prerastanie v tenk om čreve na základe stanovenia koncentrácie v odíka vo vydychovanom vzduchu.
Dychový test na SIBO pokyny pre pacienta je bezbolestný dychový test, ktorým možno diagnostikovať bakteriálne prerastanie v tenk om čreve na základe stanovenia koncentrácie v odíka vo vydychovanom vzduchu.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vistaprep prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje: Macrogolum 3350 Natrii chloridum Natrii hydrogencarbonas
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vistaprep prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje: Macrogolum 3350 Natrii chloridum Natrii hydrogencarbonas
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 1. NÁZOV LIEKU Vermox 100 mg, tablety SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE LIEKU Liečivo: mebendazol 100 mg v jednej tablete. Pomocná látka so známym účinkom:
1. NÁZOV LIEKU Vermox 100 mg, tablety SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE LIEKU Liečivo: mebendazol 100 mg v jednej tablete. Pomocná látka so známym účinkom:
(REF: ARV-HA-3 / REF: ARV-HA-1)
 Hyaluronát sodný 2% (REF: ARV-HA-3 / REF: ARV-HA-1) OBSAH, ref. ARV-HA-3 OBSAH, ref. ARV-HA-1 3 ArthroVisc injekčné striekačky 1 ArthroVisc injekčná striekačka 3 zarážky prsta 1 zarážka prsta Ver.4.X /
Hyaluronát sodný 2% (REF: ARV-HA-3 / REF: ARV-HA-1) OBSAH, ref. ARV-HA-3 OBSAH, ref. ARV-HA-1 3 ArthroVisc injekčné striekačky 1 ArthroVisc injekčná striekačka 3 zarážky prsta 1 zarážka prsta Ver.4.X /
Informácie o liečbe Gilenyou (fingolimod), ktoré je dôležité si pamätať
 Informácie o liečbe Gilenyou (fingolimod), ktoré je dôležité si pamätať Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Môžete prispieť tým, že
Informácie o liečbe Gilenyou (fingolimod), ktoré je dôležité si pamätať Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Môžete prispieť tým, že
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls90149/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUTTALAX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 tableta obsahuje Natrii picosulfas 5 mg Pomocná látka se známým účinkem: monohydrát
sp.zn.sukls90149/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUTTALAX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 tableta obsahuje Natrii picosulfas 5 mg Pomocná látka se známým účinkem: monohydrát
Písomná informácia pre používateľa. BISACODYL-K 5 mg obalené tablety. bisakodyl
 Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/07420-ZIB Písomná informácia pre používateľa BISACODYL-K 5 mg obalené tablety bisakodyl Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete
Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/07420-ZIB Písomná informácia pre používateľa BISACODYL-K 5 mg obalené tablety bisakodyl Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Príloha č. 1 k notifikácii o zmene, ev. č.: 2014/00763-Z1A SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Gyno-Pevaryl 50 vaginálne guľôčky Gyno-Pevaryl 150 vaginálne guľôčky Gyno-Pevaryl 150
Príloha č. 1 k notifikácii o zmene, ev. č.: 2014/00763-Z1A SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Gyno-Pevaryl 50 vaginálne guľôčky Gyno-Pevaryl 150 vaginálne guľôčky Gyno-Pevaryl 150
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. Název přípravku E-Z-HD 2. Kvalitativní a kvantitativní složení Léčivá látka: Barii sulfas (síran barnatý)
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. Název přípravku E-Z-HD 2. Kvalitativní a kvantitativní složení Léčivá látka: Barii sulfas (síran barnatý)
Pomocné látky se známým účinkem: Jedna obalená tableta obsahuje glukosu, 51,8 mg monohydrátu laktosy a 14,1mg sacharosy..
 sp.zn. sukls252727/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU STADALAX 5 mg, obalené tablety 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ Jedna obalená tableta obsahuje bisacodylum 5 mg. Pomocné látky
sp.zn. sukls252727/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU STADALAX 5 mg, obalené tablety 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ Jedna obalená tableta obsahuje bisacodylum 5 mg. Pomocné látky
Lisovaná pastilka Hnědá lisovaná kostka s ovocnou vůní.
 sp.zn. sukls185038/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU REGULAX pikosulfát kostky 10 mg lisované pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna lisovaná pastilka obsahuje natrii picosulfas
sp.zn. sukls185038/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU REGULAX pikosulfát kostky 10 mg lisované pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna lisovaná pastilka obsahuje natrii picosulfas
Pomocné látky se známým účinkem: prostý sirup 67%, usušená tekutá glukosa.
 sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls175187/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Duphalac 667 g/l, perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: lactulosum 667 g v 1000 ml perorálního roztoku
sp.zn.sukls175187/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Duphalac 667 g/l, perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: lactulosum 667 g v 1000 ml perorálního roztoku
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls180301/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ROBITUSSIN EXPECTORANS na odkašlávání 100 mg/5 ml, sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 5 ml sirupu obsahuje guaifenesinum 100
sp.zn.sukls180301/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ROBITUSSIN EXPECTORANS na odkašlávání 100 mg/5 ml, sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 5 ml sirupu obsahuje guaifenesinum 100
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU. Každá tableta obsahuje 157,36 mg dihydrátu zinkumorotátu (zodpovedá 25 mg zinku).
 Schválený text k rozhodnutiu o prevode, ev.č. 2012/07128 Príloha č. 2 k notifikácii zmeny v registrácii lieku, ev.č. 2012/07129 1. NÁZOV LIEKU Zinkorot tablety SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
Schválený text k rozhodnutiu o prevode, ev.č. 2012/07128 Príloha č. 2 k notifikácii zmeny v registrácii lieku, ev.č. 2012/07129 1. NÁZOV LIEKU Zinkorot tablety SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Schválený text k rozhodnutiu o zmene v registrácii lieku, ev. č.: 2012/03190 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Kombi-Kalz 500 mg/800 IU filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE
Schválený text k rozhodnutiu o zmene v registrácii lieku, ev. č.: 2012/03190 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Kombi-Kalz 500 mg/800 IU filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE
Prášek pro perorální roztok v sáčku. Téměř bílý prášek s vůní a chutí po pomerančích a grapefruitech.
 Sp.zn.sukls96899/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FORLAX 4 g, prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje: Makrogolum 4000... 4,00 g
Sp.zn.sukls96899/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FORLAX 4 g, prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje: Makrogolum 4000... 4,00 g
VETERINÁRNA AMBULANCIA
 VETERINÁRNA AMBULANCIA ŽDIARSKA 21, KOŠICE, 04012 www.veterinar-jazero.sk Vakcinácia spoločenských zvierat MVDr. René Mandelík, PhD. MVDr. Michal Moško Vakcinácia spoločenských zvierat (psy, mačky, králiky,
VETERINÁRNA AMBULANCIA ŽDIARSKA 21, KOŠICE, 04012 www.veterinar-jazero.sk Vakcinácia spoločenských zvierat MVDr. René Mandelík, PhD. MVDr. Michal Moško Vakcinácia spoločenských zvierat (psy, mačky, králiky,
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Príloha č. 2 k notifikácii o zmene, ev.č.: 2016/01047-Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Magnerot tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá tableta obsahuje 500 mg
Príloha č. 2 k notifikácii o zmene, ev.č.: 2016/01047-Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Magnerot tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá tableta obsahuje 500 mg
PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA. Zinkorot tablety Liečivo: dihydrát zinkumorotátu
 Schválený text k rozhodnutiu o prevode, ev.č. 2012/07128 Príloha č. 3 k notifikácii zmeny v registrácii lieku, ev.č. 2012/07129 PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA Zinkorot tablety Liečivo: dihydrát zinkumorotátu
Schválený text k rozhodnutiu o prevode, ev.č. 2012/07128 Príloha č. 3 k notifikácii zmeny v registrácii lieku, ev.č. 2012/07129 PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA Zinkorot tablety Liečivo: dihydrát zinkumorotátu
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. PICOPREP prášek pro perorální roztok
 Sp.zn.sukls152030/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PICOPREP prášek pro perorální roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
Sp.zn.sukls152030/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PICOPREP prášek pro perorální roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
Autizmus, tráviace funkcie a vplyv probiotík
 Autizmus, tráviace funkcie a vplyv probiotík K. Babinská, S. Lakatošová, A. Tomova, V. Husárová, A. Pivovarčiová, J. Bakoš, A. Harinek, L. Slobodníková, V. Piačková, A. Gvozdjáková, M. Bucová, A. Čorejová,
Autizmus, tráviace funkcie a vplyv probiotík K. Babinská, S. Lakatošová, A. Tomova, V. Husárová, A. Pivovarčiová, J. Bakoš, A. Harinek, L. Slobodníková, V. Piačková, A. Gvozdjáková, M. Bucová, A. Čorejová,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. PICOPREP prášek pro přípravu perorálního roztoku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls115288/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PICOPREP prášek pro přípravu perorálního roztoku Přečtěte si pozorně celou příbalovou informaci
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls115288/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PICOPREP prášek pro přípravu perorálního roztoku Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k opravě rozhodnutí o prodloužení registrace sp.zn. sukls209263/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 1 k opravě rozhodnutí o prodloužení registrace sp.zn. sukls209263/2009 1. NÁZEV PŘÍPRAVKU FORLAX 10 g SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje Macrogolum
Příloha č. 1 k opravě rozhodnutí o prodloužení registrace sp.zn. sukls209263/2009 1. NÁZEV PŘÍPRAVKU FORLAX 10 g SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje Macrogolum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls96899/2013 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU FORLAX 10 g, prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje: Macrogolum 4000 10,00 g
sp.zn.sukls96899/2013 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU FORLAX 10 g, prášek pro perorální roztok v sáčku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje: Macrogolum 4000 10,00 g
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/01589 - Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU ERDOMED 225 mg prášok na perorálny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/01589 - Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU ERDOMED 225 mg prášok na perorálny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Podpora kognitívnych funkcií v rámci asistovaného samoliečenia
 Podpora kognitívnych funkcií v rámci asistovaného samoliečenia Peter Stanko ADC Solutions, spol. s r. o. Prezentácia bola pripravená v spolupráci so spoločnosťou EGIS SLOVAKIA Dispenzačná starostlivosť
Podpora kognitívnych funkcií v rámci asistovaného samoliečenia Peter Stanko ADC Solutions, spol. s r. o. Prezentácia bola pripravená v spolupráci so spoločnosťou EGIS SLOVAKIA Dispenzačná starostlivosť
Písomná informácia pre používateľa. STADATUSSIN perorálny roztok 1,35 mg/ml. pentoxyverín
 Schválený text k rozhodnutiu o registrácii, ev. č.: 2015/04605-REG Písomná informácia pre používateľa STADATUSSIN perorálny roztok 1,35 mg/ml pentoxyverín Pozorne si prečítajte celú písomnú informáciu
Schválený text k rozhodnutiu o registrácii, ev. č.: 2015/04605-REG Písomná informácia pre používateľa STADATUSSIN perorálny roztok 1,35 mg/ml pentoxyverín Pozorne si prečítajte celú písomnú informáciu
Sirup Popis přípravku: čirá, nažloutlá až žlutá, sirupovitá kapalina sladké chuti, bez zápachu
 sp. zn. sukls5925/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LACTULOSA BIOMEDICA sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml sirupu obsahuje lactulosum 66,7 g (což odpovídá lactulosi solutio
sp. zn. sukls5925/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LACTULOSA BIOMEDICA sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml sirupu obsahuje lactulosum 66,7 g (což odpovídá lactulosi solutio
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls248152/2017 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Clensia, prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Clensia je k dispozici ve formě prášku ve dvou oddělených
Sp.zn.sukls248152/2017 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Clensia, prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Clensia je k dispozici ve formě prášku ve dvou oddělených
Souhrn údajů o přípravku
 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
INTOXIKÁCIE U PEDIATRICKÉHO PACIENTA. II. KPAIM DFNsP Banská Bystrica Nikola Chovanová, Oliver Petrík
 INTOXIKÁCIE U PEDIATRICKÉHO PACIENTA II. KPAIM DFNsP Banská Bystrica Nikola Chovanová, Oliver Petrík Malé deti: náhodné intoxikácie Adolescenti: suicidálne pokusy demoštratívne pokusy prvé kontakty s alkoholom,
INTOXIKÁCIE U PEDIATRICKÉHO PACIENTA II. KPAIM DFNsP Banská Bystrica Nikola Chovanová, Oliver Petrík Malé deti: náhodné intoxikácie Adolescenti: suicidálne pokusy demoštratívne pokusy prvé kontakty s alkoholom,
Všeobecne záväzné nariadenie Mesta Trenčianske Teplice č. x/2016 o používaní pyrotechnických výrobkov na území mesta Trenčianske Teplice
 Dôvodová správa S účinnosťou k 2.12.2015 došlo k zmene zákona č. 58/2014 Z. z. o výbušninách, výbušných predmetoch a munícii a o zmene a doplnení niektorých zákonov v znení neskorších predpisov, ktorý
Dôvodová správa S účinnosťou k 2.12.2015 došlo k zmene zákona č. 58/2014 Z. z. o výbušninách, výbušných predmetoch a munícii a o zmene a doplnení niektorých zákonov v znení neskorších predpisov, ktorý
Složky přípravku MOVIPREP jsou obsaženy ve dvou oddělených sáčcích. Koncentrace iontů po rozpuštění obou sáčků v jednom litru vody:
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls11346/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU MOVIPREP, prášek pro přípravu perorálního roztoku 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls11346/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU MOVIPREP, prášek pro přípravu perorálního roztoku 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp. zn. sukls76878/2017 1. NÁZEV PŘÍPRAVKU SMECTA 3 g prášek pro perorální suspenzi SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje diosmectitum 3 g. Pomocné látky
sp. zn. sukls76878/2017 1. NÁZEV PŘÍPRAVKU SMECTA 3 g prášek pro perorální suspenzi SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje diosmectitum 3 g. Pomocné látky
Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls7306/2012
 Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls7306/2012 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU ORENZYM 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 200 m.j. (36,60 mg)
Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls7306/2012 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU ORENZYM 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 200 m.j. (36,60 mg)
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jeden sáček obsahuje macrogolum 4000 4 g (LaxBalance jablko) nebo 10 g (LaxBalance grapefruit, LaxBalance citrón).
 Sp.zn.sukls85836/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LaxBalance jablko 4 g LaxBalance grapefruit 10 g LaxBalance citrόn 10 g prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Sp.zn.sukls85836/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LaxBalance jablko 4 g LaxBalance grapefruit 10 g LaxBalance citrόn 10 g prášek pro perorální roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Výprava do kosti: Najčastejším ochorením kostí na svete je osteoporóza.
 Výprava do kosti: Kosť je živé tkanivo. Ako mnohé ďalšie tkanivá v tele, aj kostra sa počas života potrebuje neustále obnovovať. Celá kostra dospelého človeka sa kompletne obnoví v priebehu 7 10 rokov.
Výprava do kosti: Kosť je živé tkanivo. Ako mnohé ďalšie tkanivá v tele, aj kostra sa počas života potrebuje neustále obnovovať. Celá kostra dospelého človeka sa kompletne obnoví v priebehu 7 10 rokov.
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls25933/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPACOL 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ a) Bisacodyl 5 mg v 1 tabletě b) Disodium monohydrogen phosphate dodecahydrate 7,217
sp.zn. sukls25933/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPACOL 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ a) Bisacodyl 5 mg v 1 tabletě b) Disodium monohydrogen phosphate dodecahydrate 7,217
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU. Jedna obalená tableta obsahuje 12,5 mg sodnej soli tianeptínu (čo zodpovedá 11,87 mg tianeptínu).
 Príloha č. 1 k notifikácii o zmene, ev.č.: 2015/02247-Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU COAXIL obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna obalená tableta
Príloha č. 1 k notifikácii o zmene, ev.č.: 2015/02247-Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU COAXIL obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna obalená tableta
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls163404/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FENOLAX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna enterosolventní tableta obsahuje bisacodylum 5 mg. Pomocné látky: laktóza, sacharóza,
sp.zn. sukls163404/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FENOLAX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna enterosolventní tableta obsahuje bisacodylum 5 mg. Pomocné látky: laktóza, sacharóza,
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp. zn. sukls179223/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NEO-ANGIN BEZ CUKRU 1,2 mg/0,6 mg/5,72 mg Pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje: alcohol dichlorbenzylicus
sp. zn. sukls179223/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NEO-ANGIN BEZ CUKRU 1,2 mg/0,6 mg/5,72 mg Pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje: alcohol dichlorbenzylicus
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU DULCOLAX Příloha č. 2 k rozhodnutí o registraci sp.zn.sukls112181/09 SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 enterosolventní tableta obsahuje: Bisacodylum
1. NÁZEV PŘÍPRAVKU DULCOLAX Příloha č. 2 k rozhodnutí o registraci sp.zn.sukls112181/09 SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 enterosolventní tableta obsahuje: Bisacodylum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls18973/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Bisacodyl-K 5 mg, obalené tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje bisacodylum 5 mg. Pomocné látky
sp.zn. sukls18973/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Bisacodyl-K 5 mg, obalené tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje bisacodylum 5 mg. Pomocné látky
Externé zariadenia Používateľská príručka
 Externé zariadenia Používateľská príručka Copyright 2009 Hewlett-Packard Development Company, L.P. Informácie obsiahnuté v tomto dokumente sa môžu zmeniť bez predchádzajúceho upozornenia. Jediné záruky
Externé zariadenia Používateľská príručka Copyright 2009 Hewlett-Packard Development Company, L.P. Informácie obsiahnuté v tomto dokumente sa môžu zmeniť bez predchádzajúceho upozornenia. Jediné záruky
Činnosť dermatovenerologických ambulancií v SR 2015
 Štatistické prehľady Činnosť dermatovenerologických ambulancií v SR 2015 Prehľad informuje o výsledkoch štatistického zisťovania na základe ročného výkazu o činnosti dermatovenerologickej ambulancie A
Štatistické prehľady Činnosť dermatovenerologických ambulancií v SR 2015 Prehľad informuje o výsledkoch štatistického zisťovania na základe ročného výkazu o činnosti dermatovenerologickej ambulancie A
Aktivita 1.5: Zdravotná výchova 80 hodín
 Aktivita 1.5: Zdravotná výchova 80 hodín Obsahové zameranie vzdelávacieho programu: 1. hodina Zopakovanie si predchádzajúcej hodiny Zdravotná starostlivosť Zdravotná dokumentácia 2. hodina Zopakovanie
Aktivita 1.5: Zdravotná výchova 80 hodín Obsahové zameranie vzdelávacieho programu: 1. hodina Zopakovanie si predchádzajúcej hodiny Zdravotná starostlivosť Zdravotná dokumentácia 2. hodina Zopakovanie
PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽOV. Hidrasec pre deti 30 mg granulát na perorálnu suspenziu. Racekadotril
 PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽOV Hidrasec pre deti 30 mg granulát na perorálnu suspenziu Racekadotril Pozorne si prečítajte celú písomnú informáciu predtým, než začnete užívať tento liek, pretože obsahuje
PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽOV Hidrasec pre deti 30 mg granulát na perorálnu suspenziu Racekadotril Pozorne si prečítajte celú písomnú informáciu predtým, než začnete užívať tento liek, pretože obsahuje
Enterálna a parenterálna výživa u pacienta na OAIM. Bc. Elexová Katarína kolektív OAIM
 Enterálna a parenterálna výživa u pacienta na OAIM. Bc. Elexová Katarína kolektív OAIM Leonardo da Vinci Ľudské telo umiera a život si vyžaduje jeho nepretržitú OBNOVU Malnutrícia u pacientov v nemocnici
Enterálna a parenterálna výživa u pacienta na OAIM. Bc. Elexová Katarína kolektív OAIM Leonardo da Vinci Ľudské telo umiera a život si vyžaduje jeho nepretržitú OBNOVU Malnutrícia u pacientov v nemocnici
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
Expozičný scenár a karta bezpečnostných údajov- povinnosti, možnosti a termíny
 Expozičný scenár a karta bezpečnostných údajov- povinnosti, možnosti a termíny Komunikácia v rámci dodávateľského reťazca registrované látky informácie o chemickej bezpečnosti boli zosumarizované registrujúcimi
Expozičný scenár a karta bezpečnostných údajov- povinnosti, možnosti a termíny Komunikácia v rámci dodávateľského reťazca registrované látky informácie o chemickej bezpečnosti boli zosumarizované registrujúcimi
Protokol o začatí, kontrole a zmene liečby psoriatickej artritídy
 Zdravotná poisťovňa: Všeobecná zdravotná poisťovňa Kód zdravotnej poisťovne: 25 Protokol o začatí, kontrole a zmene liečby psoriatickej artritídy Liečba: začatie liečby pokračovanie liečby zmena biologickej
Zdravotná poisťovňa: Všeobecná zdravotná poisťovňa Kód zdravotnej poisťovne: 25 Protokol o začatí, kontrole a zmene liečby psoriatickej artritídy Liečba: začatie liečby pokračovanie liečby zmena biologickej
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/01588 - Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU ERDOMED 300 mg tvrdé kapsuly 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá kapsula
Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/01588 - Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU ERDOMED 300 mg tvrdé kapsuly 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá kapsula
Příloha č. 1 k opravě rozhodnutí o prodloužení registrace sp.zn. sukls209250/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 1 k opravě rozhodnutí o prodloužení registrace sp.zn. sukls209250/2009 1. NÁZEV PŘÍPRAVKU FORLAX 4 g SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje Macrogolum
Příloha č. 1 k opravě rozhodnutí o prodloužení registrace sp.zn. sukls209250/2009 1. NÁZEV PŘÍPRAVKU FORLAX 4 g SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje Macrogolum
Úplný seznam pomocných látek viz bod 6.1. Čirý žluto-hnědý sirup s charakteristickou příchutí medu a citronu.
 Sp.zn.sukls121997/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU OlynMuco s příchutí medu a citronu 20 mg/ml 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Tento přípravek obsahuje guaifenesinum 20 mg v 1 ml.
Sp.zn.sukls121997/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU OlynMuco s příchutí medu a citronu 20 mg/ml 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Tento přípravek obsahuje guaifenesinum 20 mg v 1 ml.
Analýza rizík a kontrolné opatrenia
 Analýza rizík a kontrolné opatrenia Monika Karácsonyová Karol Munka 2. workshop k projektu SK0135 30.3.2011 VÚVH Bratislava Analýza rizík systematický proces využívania dostupných informácií na identifikovanie
Analýza rizík a kontrolné opatrenia Monika Karácsonyová Karol Munka 2. workshop k projektu SK0135 30.3.2011 VÚVH Bratislava Analýza rizík systematický proces využívania dostupných informácií na identifikovanie
Dusičnany v pitnej vode
 Dusičnany v pitnej vode Povolenú hodnotu dusičnanov v pitnej vode stanovuje NV SR č. 354/2006 Z.z. (platné znenie) a určuje medznú hodnotu pre ukazovateľ dusičnany najviac 50 mg.l -1. Prípustnú hodnotu
Dusičnany v pitnej vode Povolenú hodnotu dusičnanov v pitnej vode stanovuje NV SR č. 354/2006 Z.z. (platné znenie) a určuje medznú hodnotu pre ukazovateľ dusičnany najviac 50 mg.l -1. Prípustnú hodnotu
POWLI Fig. A Copyright 2014 VARO
 POWLI421 1 7 6 2 3 4 5 Fig. A Copyright 2014 VARO www.varo.com POWLI421 Fig 1 Copyright 2014 VARO www.varo.com LED BATERKA 1,5 W POWLI421 POWLI421 SK 1 POPIS (OBR. A) 1. Otočná hlava 2. Hlavný vypínač
POWLI421 1 7 6 2 3 4 5 Fig. A Copyright 2014 VARO www.varo.com POWLI421 Fig 1 Copyright 2014 VARO www.varo.com LED BATERKA 1,5 W POWLI421 POWLI421 SK 1 POPIS (OBR. A) 1. Otočná hlava 2. Hlavný vypínač
Zácpa: k úpravě fyziologického rytmu tlustého střeva.
 sp.zn. sukls199268/2012 a sp.zn. sukls192494/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Lactulose AL sirup 66,7 g / 100 ml 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml sirupu obsahuje lactulosum
sp.zn. sukls199268/2012 a sp.zn. sukls192494/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Lactulose AL sirup 66,7 g / 100 ml 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml sirupu obsahuje lactulosum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Světle modré, kulaté, bikonvexní obalené tablety, průměr přibližně 12,4 mm, výška přibližně 7,5 mm.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Baldriparan obalené tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje Valerianae extractum siccum 6,0 7,4 : 1, extrahováno ethanolem
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Baldriparan obalené tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje Valerianae extractum siccum 6,0 7,4 : 1, extrahováno ethanolem
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/01587 - Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU ERDOMED 3,5 % prášok na perorálnu suspenziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/01587 - Z1B SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU ERDOMED 3,5 % prášok na perorálnu suspenziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Příbalová informace: informace pro pacienta PICOPREP prášek pro perorální roztok. Natrii picosulfas/ Magnesii oxidum leve/ Acidum citricum anhydricum
 Sp.zn.sukls196661/2015 Příbalová informace: informace pro pacienta PICOPREP prášek pro perorální roztok Natrii picosulfas/ Magnesii oxidum leve/ Acidum citricum anhydricum Přečtěte si pozorně celou příbalovou
Sp.zn.sukls196661/2015 Příbalová informace: informace pro pacienta PICOPREP prášek pro perorální roztok Natrii picosulfas/ Magnesii oxidum leve/ Acidum citricum anhydricum Přečtěte si pozorně celou příbalovou
PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA INFUSIO GLUCOSI 5 IMUNA. Infúzny intravenózny roztok.
 Príloha č. 2a k notifikácii zmeny, ev. č. 2106/6944 PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA INFUSIO GLUCOSI 5 IMUNA Infúzny intravenózny roztok. Držiteľ rozhodnutia o registrácii Imuna Pharm, a.s. Jarková 17
Príloha č. 2a k notifikácii zmeny, ev. č. 2106/6944 PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA INFUSIO GLUCOSI 5 IMUNA Infúzny intravenózny roztok. Držiteľ rozhodnutia o registrácii Imuna Pharm, a.s. Jarková 17
EDUKÁCIA PRIMÁRNYCH OPATROVATEĽOV PACIENTOV V PALIATÍVNEJ STAROSTLIVOSTI
 EDUKÁCIA PRIMÁRNYCH OPATROVATEĽOV PACIENTOV V PALIATÍVNEJ STAROSTLIVOSTI Radka Šerfelová, Martina Lepiešová Centrum paliatívnej starostlivosti Bjørnstjerne Bjørnsona Ústav ošetrovateľstva JLF UK v Martine
EDUKÁCIA PRIMÁRNYCH OPATROVATEĽOV PACIENTOV V PALIATÍVNEJ STAROSTLIVOSTI Radka Šerfelová, Martina Lepiešová Centrum paliatívnej starostlivosti Bjørnstjerne Bjørnsona Ústav ošetrovateľstva JLF UK v Martine
Žiadateľ bude musieť zabezpečiť súlad s príslušnou monografiou európskeho liekopisu pre anastrozol, ktorá sa v súčasnosti reviduje.
 Príloha II Vedecké závery a odôvodnenie zmien a doplnení v súhrne charakteristických vlastností lieku, označení obalu a písomnej informácii pre používateľov predložené Európskou agentúrou pre lieky 7 Vedecké
Príloha II Vedecké závery a odôvodnenie zmien a doplnení v súhrne charakteristických vlastností lieku, označení obalu a písomnej informácii pre používateľov predložené Európskou agentúrou pre lieky 7 Vedecké
Souhrn údajů o přípravku
 sp. zn. sukls127840/2015 1. Název přípravku IBEROGAST Perorální kapky, roztok. Souhrn údajů o přípravku 2. Kvalitativní a kvantitativní složení 100 ml přípravku obsahuje: Iberidis amarae herbae recentis
sp. zn. sukls127840/2015 1. Název přípravku IBEROGAST Perorální kapky, roztok. Souhrn údajů o přípravku 2. Kvalitativní a kvantitativní složení 100 ml přípravku obsahuje: Iberidis amarae herbae recentis
TIENS CHITOSAN rokov čínskej múdrosti v kombinácii s najmodernejšou západnou technológiou. Udržiavanie hmotnosti Kontrola cholesterolu
 . 5000 rokov čínskej múdrosti v kombinácii s najmodernejšou západnou technológiou Udržiavanie hmotnosti Kontrola cholesterolu Zloženie TIENS Chitosanu účinne podporuje chudnutie. Na jednej strane znižuje
. 5000 rokov čínskej múdrosti v kombinácii s najmodernejšou západnou technológiou Udržiavanie hmotnosti Kontrola cholesterolu Zloženie TIENS Chitosanu účinne podporuje chudnutie. Na jednej strane znižuje
Súhrn charakteristických vlastností lieku
 PRÍLOHA Č. 1 K ROZHODNUTIU O PREDĹŽENÍ REGISTRÁCIE LIEKU EV. Ć.: 1994/2002 PRÍLOHA Č. 2 K ROZHODNUTIU O PREVODE REGISTRÁCIE LIEKU EV. Ć.: 2106/5889 Súhrn charakteristických vlastností lieku 1. NÁZOV LIEKU
PRÍLOHA Č. 1 K ROZHODNUTIU O PREDĹŽENÍ REGISTRÁCIE LIEKU EV. Ć.: 1994/2002 PRÍLOHA Č. 2 K ROZHODNUTIU O PREVODE REGISTRÁCIE LIEKU EV. Ć.: 2106/5889 Súhrn charakteristických vlastností lieku 1. NÁZOV LIEKU
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 Schválený text k rozhodnutiu o zmene, ev.č.: 2013/07585-ZME 1. NÁZOV LIEKU Igantibe 200 IU/ml, injekčný roztok SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Liečivo:
Schválený text k rozhodnutiu o zmene, ev.č.: 2013/07585-ZME 1. NÁZOV LIEKU Igantibe 200 IU/ml, injekčný roztok SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Liečivo:
Osoba podľa 8 zákona finančné limity, pravidlá a postupy platné od
 A. Právny rámec Osoba podľa 8 zákona finančné limity, pravidlá a postupy platné od 18. 4. 2016 Podľa 8 ods. 1 zákona č. 343/2015 Z. z. o verejnom obstarávaní a o zmene a doplnení niektorých zákonov v znení
A. Právny rámec Osoba podľa 8 zákona finančné limity, pravidlá a postupy platné od 18. 4. 2016 Podľa 8 ods. 1 zákona č. 343/2015 Z. z. o verejnom obstarávaní a o zmene a doplnení niektorých zákonov v znení
Zoznam povinných merateľných ukazovateľov národného projektu Zelená domácnostiam
 Príloha č. 5 vyzvania Zoznam povinných merateľných ukazovateľov projektu, vrátane ukazovateľov relevantných k HP Zoznam povinných merateľných ukazovateľov národného projektu Zelená domácnostiam Operačný
Príloha č. 5 vyzvania Zoznam povinných merateľných ukazovateľov projektu, vrátane ukazovateľov relevantných k HP Zoznam povinných merateľných ukazovateľov národného projektu Zelená domácnostiam Operačný
VZOR OZNÁMENIE O ZARADENÍ PODNIKU PODĽA 5 ZÁKONA
 VZOR OZNÁMENIE O ZARADENÍ PODNIKU PODĽA 5 ZÁKONA 1. Dôvod vypracovania oznámenia Označiť dôvod/zmenu x Nové oznámenie Nový podnik 3 ods. 5 písm. a) zákona Aktualizácia oznámenia Možnosť výberu z viacerých
VZOR OZNÁMENIE O ZARADENÍ PODNIKU PODĽA 5 ZÁKONA 1. Dôvod vypracovania oznámenia Označiť dôvod/zmenu x Nové oznámenie Nový podnik 3 ods. 5 písm. a) zákona Aktualizácia oznámenia Možnosť výberu z viacerých
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU HUMAN ALBUMIN GRIFOLS 5%, infúzny roztok. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE LIEKU Human Albumin Grifols 5% je roztok, ktorý obsahuje 50 g/l
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU HUMAN ALBUMIN GRIFOLS 5%, infúzny roztok. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE LIEKU Human Albumin Grifols 5% je roztok, ktorý obsahuje 50 g/l
