AIA-PACK TPOAb. Rev. 04/09 POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SOUHRN A VYSVĚTLENÍ PRINCIP STANOVENÍ DODÁVANÝ MATERIÁL
|
|
|
- Naděžda Zemanová
- před 7 lety
- Počet zobrazení:
Transkript
1 Rev. 04/09 Pozor: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ AIA-PACK TPOAb AIA-PACK TPOAb je určen pouze pro diagnostické použití in vitro ke kvantitativnímu měření protilátek proti thyroideální peroxidáze (TPOAb) v lidském séru nebo v heparinizované plazmě na analyzátorech systému Tosoh AIA. SOUHRN A VYSVĚTLENÍ Protilátky proti štítné žláze, zejména antimikrosomální a antithyreoglobulinové protilátky, jsou ukazatelem souvisejícím s autoimunitními onemocněními štítné žlázy, jako například Gravesova a Hashimotova choroba. K detekci antimikrosomálních protilátek jsou dostupné některé metody založené na buňkách nebo částicích potažených thyroideální mikrosomální frakcí. V současnosti byla jako hlavní součást antigenu, která je rozpoznávána antimikrosomálními protilátkami, identifikována thyroideální peroxidáza (TPO) (1 2). Nálezy vedly k některým senzitivním a specifickým testům pro antimikrosomální protilátky, které jsou protilátkami anti-tpo (TPOAb) využívající TPO antigen (3 8). AIA-PACK TPOAb je činidlo enzymové imunoanalýzy k měření koncentrací TPOAb v lidském séru nebo heparinizované plazmě pomocí zrn potažených TPO antigenem a myší protilátkou proti lidskému IgG označenou alkalickou fosfatázou. PRINCIP STANOVENÍ ST AIA-PACK TPOAb je dvoumístná imunoenzymometrická analýza, která je celá prováděná v testovací miskách AIA-PACK TPOAb. TPOAb přítomný v testovaném vzorku se váže na TPO antigen imobilizovaný na magnetických zrnech AIA-PACK TPOAb. Zrna jsou promývána, aby se odstranil jakýkoli nenavázaný materiál, a poté jsou inkubována s enzymem značenou myší monoklonální protilátkou proti lidské IgG protilátce. Magnetická zrna jsou promytím zbavena nenavázaných, enzymem značených monoklonálních protilátek a jsou pak inkubována s fluorogenním substrátem, 4-methylumbeliferylfosfátem (4MUP). Množství enzymem značených monoklonálních protilátek, které se vážou na zrna, je přímo úměrné koncentraci TPOAb v testovaném vzorku. Je vynesena standardní křivka a neznámé koncentrace vzorků jsou vypočítány pomocí této křivky. DODÁVANÝ MATERIÁL Katalogové č zásobníků x 20 testovacích kelímků AIA-PACK TPOAb CUP 5 ampulí x 5 ml AIA-PACK TPOAb CONJUGATE Plastové testovací kelímky obsahují dvanáct lyofylizovaných magnetických zrn potažených TPO antigenem (AIA-PACK TPOAb CUP) a lahvičky obsahující tekutou myší monoklonální protilátku proti lidské IgG konjugovanou s hovězí alkalickou fosfatázou s azidem sodným jako konzervační látkou (AIA-PACK TPOAb CONJUGATE). POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY Následující materiály jsou požadovány pro provedení analýzy TPO pomocí AIA-PACK TPOAb (kat. č ) na analyzátorech systému TOSOH AIA. Následující materiály společnost Tosoh dodává samostatně. Materiály Kat. č. AIA-1200 XL AIA AIA Nex IA nebo AIA AIA Nex IA nebo AIA-21 LA AIA-1800 ST AIA-1800 LA AIA-2000 ST AIA-2000 LA AIA-600 II AIA-600 II BCR AIA-PACK SUBSTRATE SET (pouze pro řady AIA-1200 nebo AIA-600) AIA-PACK SUBSTRATE REAGENT / AIA-PACK SUBSTRATE RECONSTITUENT AIA-PACK SUBSTRATE SET II (pro analyzátory systému TOSOH AIA s výjimkou řad AIA-1200 a AIA-600) AIA-PACK SUBSTRATE REAGENT II / AIA-PACK SUBSTRATE RECONSTITUENT II AIA-PACK TPOAb CONJUGATE AIA-PACK TPOAb CALIBRATOR SET CALIBRATOR (1) 0 IU/ml CALIBRATOR (2) 0,5 IU/ml (přibližně) CALIBRATOR (3) 2 IU/ml (přibližně) CALIBRATOR (4) 4 IU/ml (přibližně) CALIBRATOR (5) 10 IU/ml (přibližně) CALIBRATOR (6) 23 IU/ml (přibližně) AIA-PACK TPOAb CONTROL SET CONTROL LEVEL 1 2 IU/ml (přibližně) CONTROL LEVEL 2 10 IU/ml (přibližně) AIA-PACK TPOAb/TgAb SAMPLE DILUTING SOLUTION AIA-PACK WASH CONCENTRATE AIA-PACK DILUENT CONCENTRATE AIA-PACK DETECTOR STANDARDIZATION TEST CUP Další požadavky pouze pro řady AIA-1200: AIA-1200 PIPETTE TIPS AIA-PACK AIA-1200 DETECTOR STANDARDIZATION SOLUTION Další požadavky pouze pro AIA-600: KELÍMKY NA VZORKY Další požadavky pro AIA Nex IA / AIA-21, AIA-600 II, AIA-1800 a AIA-2000: KELÍMKY NA VZORKY AIA-PACK SAMPLE TREATMENT CUP Další požadavky pouze pro AIA Nex IA/AIA-21: PIPETOVACÍ ŠPIČKY PŘEDEM VLOŽENÉ ŠPIČKY PRO PIPETU
2 Další požadavky pouze pro AIA-600 II, AIA-1800 a AIA-2000: PIPETOVACÍ ŠPIČKY STOJAN NA PIPETY PŘEDEM VLOŽENÉ ŠPIČKY PRO PIPETU Používejte pouze materiály dodané společností Tosoh. Nepoužívejte náhradní materiály získané z jiných zdrojů, protože výkonnost testu je charakterizována přísně na základě materiálů společnosti Tosoh. VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ 1. AIA-PACK TPOAb je určen pouze pro diagnostické použití in vitro. 2. V rámci jednoho zásobníku nemíchejte testovací kelímky různých šarží nebo různých testů. 3. Různé šarže AIA-PACK TPOAb CONJUGATE nesmí být smíchány. Test AIA-PACK TPOAb musí být prováděn s použitím konjugátu a testových kelímků stejné šarže a ne s testovými kelímky jiné šarže. 4. AIA-PACK TPOAb obsahuje azid sodný, který může reagovat s olověným nebo měděným potrubím za vzniku potenciálně výbušných azidů kovu. Při likvidaci těchto činidel do kanalizace je vždy spláchněte velkým množstvím vody, aby nedocházelo k hromadění azidu. 5. Lidské biologické materiály užívané při přípravě tohoto produktu byly testovány metodami schválenými FDA s negativními výsledky pro přítomnost HBsAg, protilátek proti HIV-1 a HCV. Protože žádná testovací metoda neposkytuje absolutní jistotu, že produkty z lidské krve nemohou přenášet infekční agens, je doporučené zacházet s tímto produktem se stejnými bezpečnostními opatřeními jako se vzorky pacientů. 6. AIA-PACK TPOAb CONJUGATE se skládá z myší monoklonální protilátky proti lidské IgG označené alkalickou fosfatázou, která způsobuje nižší aktivitu protilátky při kontaktu s lidským sérem nebo plazmou. 7. Nepoužívejte po uplynutí data exspirace. SKLADOVÁNÍ A STABILITA Veškeré materiály jsou stabilní do data exspirace uvedeného na štítku, jsou-li uchovávány při specifikované teplotě. Materiály Kat. č. 2 8 C: AIA-PACK TPOAb (CUP a CONJUGATE) AIA-PACK TPOAb CONJUGATE AIA-PACK TPOAb CALIBRATOR SET AIA-PACK TPOAb CONTROL SET AIA-PACK TPOAb/TgAb SAMPLE DILUTING SOLUTION AIA-PACK SUBSTRATE SET AIA-PACK SUBSTRATE SET II AIA-PACK WASH CONCENTRATE AIA-PACK DILUENT CONCENTRATE C: AIA-PACK DETECTOR STANDARDIZATION TEST CUP AIA-PACK SAMPLE TREATMENT CUP Testovací kelímky AIA-PACK TPOAb mohou být skladovány až 1 den při teplotě C. - Po otevření zůstává AIA-PACK TPOAb CONJUGATE stabilní po dobu 7 dnů při teplotě 2 8 C. - Materiály kalibračních roztoků by měly být spotřebovány do 1 dne od otevření, za předpokladu, že jsou lahvičky těsně uzavřeny a uloženy v chladu při teplotě 2 8 C Po otevření bude SAMPLE DILUTING SOLUTION stabilní po dobu až 30 dnů, pokud je zchlazený na teplotu 2 8 C. - Materiály kontrolních roztoků by měly být spotřebovány do 7 dnů od otevření, za předpokladu, že jsou lahvičky těsně uzavřeny a uloženy v chladu při teplotě 2 8 C. - Rekonstituovaný roztok substrátu je stabilní 3 dny při C nebo 7 dnů při teplotě 2 8 C. - Pracovní ředicí roztok a promývací roztoky jsou stabilní po dobu 30 dnů při C. Jestliže se činidla zakalí nebo změní barvu, nepoužívejte je. ODBĚR VZORKŮ A MANIPULACE S NIMI 1. Pro stanovení je nutno použít sérum nebo heparinizovanou plazmu. NESMÍ BÝT POUŽITA EDTA nebo citrátová plazma. 2. Používá-li se sérum, vzorek žilní krve se odebírá asepticky bez konzervačních látek. Uchovávejte při teplotě C než se vytvoří sraženina (obvykle minut), pak odstředěním získejte vzorek séra pro test. 3. Používá-li se heparinizovaná plazma, vzorek žilní krve se odebírá asepticky s určeným aditivem. Co nejdříve odstřeďte a oddělte plazmu od sedimentovaných buněk. 4. Během sériového sledování jednotlivého pacienta nestřídejte druhy vzorků. U určitých pacientů se mohou koncentrace naměřené v různých druzích vzorků poněkud lišit. 5. Před provedením analýzy mohou být vzorky uloženy při teplotě 2 8 C po dobu maximálně 24 hodin. Nelze-li analýzu provést do 24 hodin, musí být vzorek uchováván zmražený při teplotě -20 C nebo nižší po dobu maximálně 60 dnů. 6. Zabraňte opakovanému zmrazování a rozmrazování vzorků. Zakalené vzorky séra nebo vzorky, které obsahují částice hmoty, musí být před analýzou odstředěny. Před analýzou pomalu ponechte vzorky dosáhnout teploty C a jemně je promíchejte. 7. Všechny vzorky pacientů před analýzou vyžadují ředění. Vzorky ředěné 51-krát AIA-PACK TPOAb/TgAb SAMPLE DILUTING SOLUTION. AIA Nex IA / AIA-21, AIA-600, AIA-1800 a AIA-2000 provedou automaticky ředění a vypočítají výsledky. ˇ5edění vzorků je prováděno ručně před analýzou pro AIA-1200 XL a AIA-600. Další informace týkající se provozu přístroje naleznete ve specifickém uživatelském manuálu systému TOSOH AIA. Materiály AIA-PACK TPOAb CALIBRATOR a CONTROL nevyžadují před analýzou ředění. 8. Naředěný vzorek musí být spotřebován do 24 hodin a nesmí být skladován. 9. Naředěný vzorek potřebný pro analýzu je 10 µl. POSTUP Podrobné pokyny pro AIA Nex IA/AIA-21, AIA-600 II, AIA-1800, AIA-2000 a AIA-360 naleznete v uživatelském manuálu. I. Příprava činidla A. Substrátový roztok Před přípravou pracovního činidla ponechte všechna činidla, aby dosáhla teploty C. Pro AIA-1200 XL a AIA-600 přidejte celý obsah AIA-PACK SUBSTRATE RECONSTITUENT (100 ml) do lyofilizovaného AIA-PACK SUBSTRATE REAGENT a důkladně promíchejte, aby se pevný materiál rozpustil. U AIA Nex IA/AIA-21, AIA600, AIA-1800 nebo AIA-2000 přidejte celý obsah AIA-PACK SUBSTRATE RECONSTITUENT II (100 ml) k AIA-PACK SUBSTRATE REAGENT II (lyofilizovanému), důkladně promíchejte, aby se pevný materiál rozpustil. B. Promývací roztok Přidejte celý obsah AIA-PACK WASH CONCENTRATE (100 ml) k přibližně 2,0 l vody reagenční čistoty třídy I CAP nebo typu I NCCLS, dobře promíchejte a upravte konečný objem na 2,5 l. 4-11
3 C. Ředicí roztok Přidejte celý obsah AIA-PACK DILUENT CONCENTRATE (100 ml) k přibližně 4,0 l vody reagenční čistoty třídy I CAP nebo typu I NCCLS, dobře promíchejte a upravte konečný objem na 5,0 l. D. TPOAb konjugát AIA-PACK TPOAb CONJUGATE je dodáván připravený k použití. E. Roztok pro ředění vzorků AIA-PACK TPOAb/TgAb SAMPLE DILUTING SOLUTION je dodávaný připravený k použití. II. Postup kalibrace A. Kalibrační křivka Kalibrační roztoky k použití s AIA-PACK TPOAb jsou uvedeny v normě NIBSC (kód 66/387) Kalibrační křivka pro ST AIA-PACK TPOAb bude stabilní až 90 dnů. Stabilita kalibrace je sledována prováděním kontroly kvality a závisí na správné manipulaci s činidlem a na řádné údržbě systému Tosoh AIA podle pokynů výrobce. Opětovná kalibrace může být nutná častěji, když jsou kontroly mimo nastavené rozmezí pro tento test nebo když jsou prováděny určité servisní postupy (např. nastavení teploty, změny mechanismu odběru vzorků, údržba promývací sondy nebo nastavení či výměna žárovky detektoru). Kalibrační křivka vzorku z AIA-1800 sleduje a znázorňuje algoritmus použitý při výpočtu výsledků. Rozsah koncentrací kalibrační křivky je zobrazen v 1/51 rozsahu testu vzorků pacienta. Koncentrace vzorků pacienta jsou vypočítány vynásobením koncentrací získaných z kalibrační křivky a faktorem ředění. AIA Nex IA /AIA-21, AIA-600 II, AIA-1800 a AIA-2000 automaticky vypočítají koncentrace vzorků pacienta pomocí faktoru ředění a ohlásí výsledky. B. Postup kalibrace 1. Pokyny postupu viz příslušný uživatelský manuál systému Tosoh AIA. 2. Ověřte, že jsou obě šarže AIA-PACK TPOAb CUP a AIA-PACK TPOAb CONJUGATE stejné. 3. Ověřte, že kalibrační šarže a čísla koncentrací byly správně zadány do softwaru Kalibrační roztoky pro ST AI-PACK TPOAb jsou dodávány připraveny k použití. Společnost Tosoh doporučuje, aby všechny kalibrační roztoky byly spuštěny trojmo. C. Kritéria přijatelnosti kalibrace 1. Průměrná rychlost pro CALIBRATOR (1) má být < 1,0 nmol/(l s). 2. Vzhledem k tomu, že existuje přímý vztah mezi koncentrací a rychlostí, musí rychlost vzrůstat s narůstající koncentrací. 3. Opakující se hodnoty musí být v rozmezí 10 %. D. Kontrola kalibrace a přijetí 1. Pečlivě zkontrolujte křivku kalibrace a použijte výše uvedená kritéria. 2. Je-li to nutné, editujte kalibraci a potom kalibraci akceptujte. Další informace o kalibraci naleznete v uživatelském manuálu systému Tosoh AIA. III. Postup kontroly kvality A. Komerčně dostupné kontroly Komerčně dostupné kontroly by měly být spuštěny nejméně jednou denně. Doporučuje se, aby byly použity nejméně dva stupně kontrol, normální a abnormální. Metoda laboratoře pro tento určitý test specifikuje následující: Kontrolní materiál: Frekvenci: Číslo šarže kontrolního materiálu, přijatelné limity a nápravná opatření v případě, že kontroly nesplní laboratorní kritéria, můžete nalézt ve zvláštním dokumentu o kontrole kvality, který je v laboratoři. B. Postup kontroly kvality 1. Kontrolní vzorky se mají použít ke kontrole kvality. Další informace o pokynech postupu kontroly kvality naleznete v příslušném uživatelském manuálu systému Tosoh AIA. 2. Materiál kontroly kvality, který má projít tímto testem, je specifikovaný individuální metodou laboratoře. IV. Zpracování vzorků A. Příprava Všechny vzorky pacientů vyžadují před analýzou ředění a jsou naředěny 51-krát pomocí AIA-PACK TPOAb/TgAb SAMPLE DILUTING SOLUTION. Naředěné nebo nenaředěné vzorky pacientů jsou umístěny na příslušné pozice analyzátorů systému Tosoh AIA. Další informace o přípravě vzorků a provozu přístroje naleznete v kapitole ODBĚR A MANIPULACE SE VZORKY a konzultujte specifický uživatelský manuál systému TOSOH AIA. Primární zkumavky a také kelímky na vzorky jsou kódovány čárovým kódem a můžou být použité v AIA Nex IA/AIA-21, AIA-600 II, AIA-1800 a AIA B. Postup analýzy 1. Poskytněte dostatečné množství testovacích kelímků AIA-PACK TPOAb a CONJUGATE pro počet vzorků, které mají být analyzovány. 2. Vložte vzorky pacienta podle pokynů v uživatelském manuálu a pokračujte v analýze. Poznámka: AIA-PACK SAMPLE TREATMENT CUP bude v případě použití vestavěných ředění vyžadován systémem AIA Nex IA/AIA-21, AIA-600 II, AIA-1800 a AIA POZNÁMKY K POSTUPU 1) Lyofilizovaný substrát musí být zcela rozpuštěn. 2) Ligandové analýzy prováděné analyzátory systému Tosoh AIA vyžadují, aby laboratoř používala vodu označenou Společností amerických patologů třídou I nebo podle NCCLS typem I. Voda musí být 6-11
4 testována nejméně jednou měsíčně a neměla by osahovat částicovou hmotu včetně bakterií. ph vody by mělo být také pravidelně testováno. Další informace naleznete v dokumentu NCCLS Příprava a testování reagenční vody v klinické laboratoři, dokument NCCLS C3-A3, svazek 11, č. 13, původně odsouhlaseném jako směrnice NCCLS v říjnu ) Vyskytne-li se vzorek obsahující koncentraci TPOAb vyšší než IU/ml, musíte tento vzorek naředit AIA-PACK TPOAb/TgAb SAMPLE DILUTING SOLUTION a provést analýzu znovu podle postupu analýzy. Doporučené ředění pro vzorky obsahující koncentraci větší než IU/ml je 1:10. Je žádoucí takové ředění, aby byl odečet naředěného vzorku mezi 3,0 a IU/ml. Pokud se nepoužívá funkce automatické ředění, musí být provedeno 51-násobné ředění. Další informace o ředění vzorků naleznete ve specifickém uživatelském manuálu systému Tosoh AIA. 4) V analyzátorech systémů Tosoh AIA (s výjimkou AIA-600) mohou být současně uloženy dvě různé kalibrační křivky pro každý analyt. Proto mohou být v rámci téhož cyklu použity dvě různé šarže testovacích kelímků a konjugátu. AIA-600 může použít jednu kalibrační křivku pro každý analyt, protože do AIA-600 lze vložit pouze jednu šarži konjugátu. 5) Nejsou-li pro tento test specifikace analýzy připraveny v softwaru systému, musí být specifikace zadány pod kódem testu 047. VÝPOČET VÝSLEDKŮ Analyzátory systémů Tosoh AIA provádějí všechny operace manipulace se vzorky a činidly automaticky. Analyzátory systémů Tosoh AIA odečítají míru fluorescence generovanou reakcí a automaticky ji převádějí na míru koncentrace TPOAb v IU/ml. U vzorků vyžadujících ředění provedou systémy AIA Nex IA/AIA-21, AIA-600 II, AIA-1800 a AIA-2000 automaticky ředění a vypočtou výsledky, pokud byly faktory ředění zadány do softwaru. Faktory ředění mohou být zadány při programování vzorků na monitoru testu. Ruční ředění vzorku je vyžadováno pro AIA-1200 XL a AIA-600. Podrobné informace o programování ředění naleznete v příslušném uživatelském manuálu. VYHODNOCENÍ VÝSLEDKŮ Kontrola kvality Za účelem sledování a vyhodnocení přesnosti analytické výkonnosti se doporučuje v souladu s místními nařízeními analyzovat komerčně dostupné kontrolní vzorky. Minimální doporučená frekvence zpracování interního kontrolního materiálu je: Po kalibraci je spuštěna třístupňová analýza interních kontrolních vzorků, aby byla akceptována kalibrační křivka. Tři stupně kontrol jsou opakovány, když jsou provedeny určité servisní postupy (např. nastavení teploty, změna mechanismu pro odběr vzorků, údržba promývací sondy nebo nastavení či výměna žárovky detektoru). K ověření celkového výkonu analyzátorů systému Tosoh AIA by měl být po denní údržbě provedený nejméně dva stupně kontroly. Je-li jedna nebo více hodnot kontrolního vzorku(ů) mimo přípustné rozmezí, bude před ohlášením výsledků pacientů nutné prošetřit validitu kalibrační křivky. Je nutno dodržovat standardní laboratorní postupy podle přísného zákonného orgánu, který na provoz laboratoře dohlíží. OMEZENÍ Pro diagnostické účely je nutné využívat výsledky tohoto testu společně s dalšími údaji (např. symptomy, výsledky dalších testů, klinickými dojmy, léčbou atd.). Pomocí AIA-PACK TPOAb je nejvyšší koncentrace TPOAb měřitelná po 51-násobném ředění s AIA-PACK TPOAb/TgAb SAMPLE DILUTING SOLUTION 20 IU/ml, což odpovídá IU/ml ve vzorcích a nejnižší měřitelná koncentrace je 0,05 IU/ml (senzitivita testu), což odpovídá 3,0 IU/ml ve vzorcích. Přestože přibližná hodnota nejvyššího kalibračního roztoku je 23 IU/ml, přesná koncentrace se může poněkud lišit. Specifikaci testu ASSAY RANGE HIGH (VYSOKÝ ROZSAH TESTU) je nutno definovat jako horní hranici rozsahu testu, a to 20 IU/ml, která odpovídá přibližně IU/ml v původních vzorcích. Přestože hemolýza nemá významný vliv na test, mohou hemolyzované vzorky poukazovat na špatné zacházení se vzorkem před analýzou a výsledky je nutno interpretovat opatrně. Lipémie má na test nevýznamný vliv, kromě případu silné lipémie, kdy může dojít k prostorové interferenci. Vzorky pacientů, kteří užívají léky a/nebo u kterých probíhá léčba, mohou vykazovat chybné výsledky. Vzorky pacienta mohou obsahovat lidské protilátky proti myším (HAMA) buď v důsledku přirozené tvorby protilátek, anebo tvorby protilátek jako odpovědi na léčebné režimy. HAMA mohou způsobovat falešně pozitivní výsledky testů užívajících myší monoklonální protilátky. Jiné heterofilní protilátky jsou také známé svou interferencí s testy tohoto typu. AIA-PACK TPOAb byl vytvořen k minimalizaci účinků HAMA a heterofilních protilátek, ale interference způsobená vysokými titry protilátek nemůže být vyloučena. Pro úplnější pochopení omezeních tohoto postupu, si laskavě přečtěte oddíly ODBĚR A MANIPULACE SE VZORKY, VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ, SKLADOVÁNÍ A STABILITA a POZNÁMKY K POSTUPU této příbalové informace. PŘEDPOKLÁDANÉ HODNOTY Každá laboratoř by měla stanovit referenční interval, který odpovídá charakteristikám testované populace. Podobně jako u všech diagnostických postupů musí být klinické výsledky interpretovány s ohledem na současně podávané léky. Referenční rozmezí Ve skupině sérových vzorků od 200 relativně zdravých Asiatů bylo 97,5% hodnot menších než 3,2 IU/ml. VÝKONNOSTNÍ CHARAKTERISTIKY PŘESNOST a. Výtěžnost: Tři vzorky byly označeny třemi rozdílnými hladinami TPOAb a testovány před a po označení. Vzorek Původní TPOAb Předpokládaná Naměřená Procento hodnota přidaný hodnota hodnota výtěžnosti (IU/ml) (IU/ml) (IU/ml) (IU/ml) (%) Vzorek A1 3,89 2,51 6,41 6,71 104,7 3,89 5,03 8,92 9,58 107,4 3,89 10,05 13,95 14,33 102,8 Vzorek B1 5,82 2,50 8,32 8,39 100,8 5,82 5,00 10,82 11,00 101,7 5,82 10,00 15,82 15,84 100,1 Vzorek C1 4,47 2,48 6,95 7,10 102,1 4,47 4,96 9,44 9,41 99,7 4,47 9,92 14,40 13,33 92,
5 b. Ředění: Tři vzorky naředěné 51 x byly sériově naředěny pomocí AIA-PACK TPOAb/TgAb SAMPLE DILUTING SOLUTION a analyzovány. Vzorek Faktor Předpokládaná Naměřená Procento hodnota hodnota výtěžnosti (IU/ml) (IU/ml) (%) Vzorek A2 žádný 9,86 9,86 100,0 7,5/10 7,39 7,47 101,0 5,0/10 4,93 4,90 99,5 2,5/10 2,46 2,36 95,9 1,0/10 0,99 0,92 92,8 Vzorek B2 žádný 5,34 5,34 100,0 7,5/10 4,01 3,95 98,5 5,0/10 2,67 2,56 96,0 2,5/10 1,34 1,29 96,8 1,0/10 0,53 0,49 91,9 Vzorek C2 žádný 7,06 7,06 100,0 7,5/10 5,30 5,37 101,3 5,0/10 3,53 3,56 100,8 2,5/10 1,77 1,72 97,2 1,0/10 0,71 0,66 93,6 PŘESNOST a. Variační koeficient metody byl hodnocen ve třech vzorcích 10 opakovanými měřeními. Vzorek Počet Průměr Standardní Koeficient opakování odchylka variace (IU/ml) (IU/ml) (%) Vzorek L 10 1,91 0,068 3,6 Vzorek M 10 10,30 0,333 3,2 Vzorek H 10 17,10 0,753 4,4 b. Variační koeficient metody byl hodnocen ve dvou odlišných koncentracích analýzou vzorků ve 20 oddělených cyklech. Vzorek Počet Průměr Standardní Koeficient opakování odchylka variace (IU/ml) (IU/ml) (%) Vzorek L 20 1,90 0,049 2,6 Vzorek H 20 15,82 0,402 2,5 KORELACE Korelace mezi sérem (x) a heparinizovanou plazmou (y) v AIA-PACK TPOAb byla provedena s použitím 78 pacientských vzorků. Směrnice 0,991 Průsečík s osou y 0,111 Korelační koeficient 0,997 Rozmezí vzorků 2,74-903,79 Počet vzorků 78 SENZITIVITA Minimální detekovatelné koncentrace (MDC) lidské TPOAb je odhadnuta na 0,05 IU/ml, což odpovídá 3 IU/ml v původních vzorcích (faktor ředění 51). Nejnižší detekovatelná koncentrace (MDC) je definována jako taková koncentrace lidské TPOAb, která odpovídá míře fluorescence, jež je dvě směrodatné odchylky od střední hodnoty míry fluorescence dvaceti opakovaných stanovení kalibračním roztokem (1). INTERFERENCE Interference je pro účely této studie definovaná jako výtěžnost přesahující 10 % známé průměrné hodnoty koncentrace vzorku po přidání následujících látek k vzorkům pacienta. Hemoglobin (až do 410 mg/dl), volný bilirubin (do 13 mg/dl) a konjugovaný bilirubin (do 18 mg/dl) neinterferují se stanovením. Lipémie indikovaná koncentrací triglyceridů (do 290 mg/dl) neinterferuje s testem. Protein indikovaný koncentrace albuminu (do 5,0 mg/dl) neinterferuje se stanovením. Kyselina askorbová (do 20 mg/dl) neinterferuje s testem. Heparin (do 100 U/ml) neinterferuje s testem. Výsledky jsou získané přidáním interferujících látek do ředěných vzorků. REFERENCE 1. Portmann L., Hamada N., Heinrich G. and DeGroot L. J.: Anti-thyroid peroxidase antibody in patients with autoimmune thyroid disease: possible identity with anti-microsomal antibody. J. Clin. Endocrinol. Metab. 61, (1985). 2. Kotani T., Umeki K., Matsunaga S., Kato E. and Ohtaki S.: Detection of autoantibodies to thyroid peroxidase in autoimmune thyroid disease by micro-elisa and immunoblotting. J. Clin. Endocrinol. Metab. 62, (1986). 3. Beever K., Bradbury J., Phillips D., McLachlan S. M., Pegg C., Goral A. Overbeck W., Feifel G. and Rees Smith B.: Highly Sensitive Assays of Autoantibodies to Thyroglobulin and to Thyroid peroxidase. Clin. Chem. 35, (1989). 4. Kaufman K. D., Filetti S., Seto P. and Rapoport B.: Recombinant Human Thyroid Peroxidase Generated in Eukaryotic Cells: A Source of Specific Antigen for the Immunological Assay of Antimicrosomal Antibodies in the Sera of Patients with Autoimmune Thyroid Disease. J. Clin. Endocrinol. Metab. 70, (1990). 5. Mariotti S, Caturegli P, Piccolo P, Barbesino G and Pinchera A: Antithyroid peroxidase autoantibodies in thyroid diseases. J. Clin. Endocrinol. Metab. 71, (1990). 6. Kendler D. L., Martin A., Magnusson R. P. and Davies T. F.: Detection of autoantibodies to recombinant human thyroid peroxidase by sensitive enzyme immunoassay. Clin. Endocrinol. 33, (1990). 7. Roti E., Gardini E., Minelli R., Bianconi L. and Braverman L. E.: Prevalence of anti-thyroid peroxidase antibodies in serum in the elderly: comparison with other tests for anti-thyroid antibodies. Clin. Chem. 38, (1992). 8. Engler H., Riesen W. F. and Keller B.: Anti-thyroid peroxidase (anti-tpo) antibodies in thyroid diseases, non-thyroidal illness and controls. Clinical validity of a new commercial method for detection of anti-tpo (thyroid microsomal) autoantibodies. Clin. Chim. Acta 225, (1994)
6 TOSOH CORPORATION 3-8-2, Shiba, Minato-ku TOKYO (JAPONSKO) Tel.: +81 (0) Fax: +81 (0) TOSOH EUROPE N.V. Transportstraat 4 B-3980 TESSENDERLO (BELGIE) Tel.: +32 (0) Fax: +32 (0) TOSOH BIOSCIENCE, INC Shoreline Court, Suite 101 South San Francisco, CA 94080, USA Telefon: Objem netto (po rekonstituci pro lyofilizovaný materiál) 11-11
AIA-PACK TgAb. Rev. 04/09 POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SOUHRN A VYSVĚTLENÍ PRINCIP STANOVENÍ DODÁVANÝ MATERIÁL
 Rev. 04/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ AIA-PACK TgAb AIA-PACK TgAb je určen pouze pro
Rev. 04/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ AIA-PACK TgAb AIA-PACK TgAb je určen pouze pro
ST AIA-PACK OVCA ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ DODÁVANÝ MATERIÁL
 EU rev. OVCA-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK OVCA ST AIA-PACK OVCA je určen
EU rev. OVCA-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK OVCA ST AIA-PACK OVCA je určen
ST AIA-PACK C-Peptide
 EU rev. CPEP-010311 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK C-Peptide ST AIA-PACK C-Peptide
EU rev. CPEP-010311 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK C-Peptide ST AIA-PACK C-Peptide
AIA-PACK B12 POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SOUHRN A VYSVĚTLENÍ PRINCIP STANOVENÍ DODÁVANÝ MATERIÁL
 EU rev. B12-010410 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ AIA-PACK B12 AIA-PACK B12 je určen pro
EU rev. B12-010410 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ AIA-PACK B12 AIA-PACK B12 je určen pro
ST AIA-PACK PAP ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ DODÁVANÝ MATERIÁL
 EU rev. PAP-011011 Pozor: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK PAP ST AIA-PACK PAP je určen pouze
EU rev. PAP-011011 Pozor: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK PAP ST AIA-PACK PAP je určen pouze
ST AIA-PACK 27.29 POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SOUHRN A VYSVĚTLENÍ PRINCIP STANOVENÍ PŘÍPRAVA ANALÝZY
 EU rev. 27.29-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. Pro zákazníky z členských států Evropské Unie: přečtěte
EU rev. 27.29-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. Pro zákazníky z členských států Evropské Unie: přečtěte
ST AIA-PACK Intact PTH
 Rev. 04/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK Intact PTH ST AIA-PACK Intact PTH je
Rev. 04/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK Intact PTH ST AIA-PACK Intact PTH je
ST AIA-PACK SLA ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ DODÁVANÝ MATERIÁL
 EU rev. SLA-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ST AIA-PACK SLa Určeno pro kvantitativní stanovení karbohydrátového
EU rev. SLA-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ST AIA-PACK SLa Určeno pro kvantitativní stanovení karbohydrátového
AIA-PACK FOLATE POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SOUHRN A VYSVĚTLENÍ PRINCIP STANOVENÍ DODÁVANÝ MATERIÁL
 EU rev. FOL-010710 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ AIA-PACK FOLATE AIA-PACK FOLATE je určen
EU rev. FOL-010710 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ AIA-PACK FOLATE AIA-PACK FOLATE je určen
ST AIA-PACK CK-MB DODÁVANÝ MATERIÁL ÚČEL POUŽITÍ POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY SOUHRN A VYSVĚTLENÍ PRINCIP STANOVENÍ
 EU rev. CKMB-010212 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK CK-MB ST AIA-PACK CK-MB je
EU rev. CKMB-010212 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK CK-MB ST AIA-PACK CK-MB je
ST AIA-PACK IgE II. Rev. 05/09 ÚČEL POUŽITÍ SOUHRN A VYSVĚTLENÍ PRINCIP STANOVENÍ VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ DODÁVANÝ MATERIÁL
 Rev. 05/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK IgE II ST AIA-PACK IgE II je určen
Rev. 05/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK IgE II ST AIA-PACK IgE II je určen
ST AIA-PACK PRL. Rev. 09/09 POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ
 Rev. 09/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. Pro zákazníky z členských států Evropské Unie: přečtěte si prosím
Rev. 09/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. Pro zákazníky z členských států Evropské Unie: přečtěte si prosím
ST AIA-PACK BMG. Rev. 07/09 POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ
 Rev. 07/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK BMG ST AIA-PACK BMG je určen pouze
Rev. 07/09 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK BMG ST AIA-PACK BMG je určen pouze
ST AIA-PACK CEA POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ
 EU rev. CEA-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK CEA ST AIA-PACK CEA je určen
EU rev. CEA-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK CEA ST AIA-PACK CEA je určen
AIA-PACK RBC FOLATE DODÁVANÝ MATERIÁL MATERIÁL POTŘEBNÝ, NEDODÁVANÝ NÁZEV A ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ
 EU rev. RBC-010510 Pozor: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. AIA-PACK RBC FOLATE Pro kvantitativní měření folát v červených
EU rev. RBC-010510 Pozor: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. AIA-PACK RBC FOLATE Pro kvantitativní měření folát v červených
ST AIA-PACK Testosterone
 EU rev. TES-010310 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK Testosterone ST AIA-PACK Testosterone
EU rev. TES-010310 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK Testosterone ST AIA-PACK Testosterone
ST AIA-PACK HCG ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ VAROVÁNÍ A BEZPEČNOSTNÍ OPATŘENÍ DODÁVANÝ MATERIÁL
 EU rev. HCG-010712 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. Pro zákazníky z členských států Evropské Unie: Přečtěte
EU rev. HCG-010712 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. Pro zákazníky z členských států Evropské Unie: Přečtěte
ST AIA-PACK ucpsaii POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ DODÁVANÝ MATERIÁL
 EU rev. UCPA-010211 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK ucpsaii ST AIA-PACK ucpsaii
EU rev. UCPA-010211 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK ucpsaii ST AIA-PACK ucpsaii
ST AIA PACK ctni 2nd-Gen
 ST AIA PACK ctni 2nd-Gen CERTIFIKÁT ISO 9001:2000 NÁZEV A POUŽITÍ AIA-PACK ctni 2-nd-Gen je určen pouze pro diagnostické užití in vitro ke kvantitativnímu měření srdečního troponinu I (ctni) v lidském
ST AIA PACK ctni 2nd-Gen CERTIFIKÁT ISO 9001:2000 NÁZEV A POUŽITÍ AIA-PACK ctni 2-nd-Gen je určen pouze pro diagnostické užití in vitro ke kvantitativnímu měření srdečního troponinu I (ctni) v lidském
ST AIA-PACK AFP POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ
 EU rev. AFP-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK AFP ST AIA-PACK AFP je určen
EU rev. AFP-011011 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. ÚČEL POUŽITÍ ST AIA-PACK AFP ST AIA-PACK AFP je určen
HbA1c. Axis - Shield. Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299
 Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
CHORUS a-tpo (36 testů)
 CHORUS a-tpo 86074 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
CHORUS a-tpo 86074 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
Validace sérologických testů výrobcem. Vidia spol. s r.o. Ing. František Konečný IV/2012
 Validace sérologických testů výrobcem Vidia spol. s r.o. Ing. František Konečný IV/2012 Legislativa Zákon č. 123/2000 Sb. o zdravotnických prostředcích ve znění pozdějších předpisů Nařízení vlády č. 453/2004
Validace sérologických testů výrobcem Vidia spol. s r.o. Ing. František Konečný IV/2012 Legislativa Zákon č. 123/2000 Sb. o zdravotnických prostředcích ve znění pozdějších předpisů Nařízení vlády č. 453/2004
ST AIA-PACK PSAII POTŘEBNÉ MATERIÁLY, KTERÉ NEJSOU SOUČÁSTÍ DODÁVKY ÚČEL POUŽITÍ SHRNUTÍ A VYSVĚTLENÍ TESTU PRINCIP STANOVENÍ DODÁVANÝ MATERIÁL
 EU rev. PSA-020312 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. Pro zákazníky z členských států Evropské Unie: Přečtěte
EU rev. PSA-020312 Upozornění: Tento návod k použití je v souladu se směrnicí IVD 98/79/ES a je určen pro zákazníky z členských států Evropské unie. Pro zákazníky z členských států Evropské Unie: Přečtěte
Hemolyzační promývací roztok 80 H
 NÁVOD K POUŽITÍ Hemolyzační promývací roztok 80 H KATALOGOVÉ ČÍSLO P 213.01 POUŽITÍ Hemolyzační promývací roztok 80 H se používá jako hemolyzační roztok pro automatické analyzátory glykovaného hemoglobinu
NÁVOD K POUŽITÍ Hemolyzační promývací roztok 80 H KATALOGOVÉ ČÍSLO P 213.01 POUŽITÍ Hemolyzační promývací roztok 80 H se používá jako hemolyzační roztok pro automatické analyzátory glykovaného hemoglobinu
Objednací číslo Určení Třída IgG Substrát Formát EI G Parainfluenza viry typu 1. Ag-potažené mikrotitrační jamky
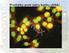 Protilátky proti virům parainfluenzy 1 (IgG) Návod na použití ELISA testu Objednací číslo Určení Třída IgG Substrát Formát EI 2721-9601 G Parainfluenza viry typu 1 IgG Ag-potažené mikrotitrační jamky 96
Protilátky proti virům parainfluenzy 1 (IgG) Návod na použití ELISA testu Objednací číslo Určení Třída IgG Substrát Formát EI 2721-9601 G Parainfluenza viry typu 1 IgG Ag-potažené mikrotitrační jamky 96
CHORUS MUMPS IgG (36 testů)
 CHORUS MUMPS IgG 81075 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné
CHORUS MUMPS IgG 81075 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné
laboratorní technologie
 Evaluace imunoanalytického systému Olympus AU3000i Firma OLYMPUS uvedla na trh imunoanalytický systém AU3000i. Přístroj pracuje na principu heterogenní imunoanalýzy s technologií paramagnetických mikročástic
Evaluace imunoanalytického systému Olympus AU3000i Firma OLYMPUS uvedla na trh imunoanalytický systém AU3000i. Přístroj pracuje na principu heterogenní imunoanalýzy s technologií paramagnetických mikročástic
CA15-3 IRMA Souprava CA15-3 IRMA umožňuje přímé in-vitro kvantitativní stanovení s tumorem asociovaného antigenu CA15-3 v lidském séru
 Informace o výrobku Informace o ostatních produktech jsou dostupné na www.demeditec.com Návod k použití CA15-3 IRMA Souprava CA15-3 IRMA umožňuje přímé in-vitro kvantitativní stanovení s tumorem asociovaného
Informace o výrobku Informace o ostatních produktech jsou dostupné na www.demeditec.com Návod k použití CA15-3 IRMA Souprava CA15-3 IRMA umožňuje přímé in-vitro kvantitativní stanovení s tumorem asociovaného
Hemolyzační promývací roztok 60 H
 NÁVOD K POUŽITÍ Hemolyzační promývací roztok 60 H KATALOGOVÉ ČÍSLO P 113.01 POUŽITÍ Hemolyzační promývací roztok 60 H se používá jako hemolyzační roztok pro automatické analyzátory glykovaného hemoglobinu
NÁVOD K POUŽITÍ Hemolyzační promývací roztok 60 H KATALOGOVÉ ČÍSLO P 113.01 POUŽITÍ Hemolyzační promývací roztok 60 H se používá jako hemolyzační roztok pro automatické analyzátory glykovaného hemoglobinu
Instructions for use. PeliClass human IgG subclass Plus kit PeliClass sheep anti human IgG2 Plus. PeliClass latex sheep anti human IgG4 Plus
 Instructions for use Sanquin Reagents B.V. Plesmanlaan 125 1066 CX Amsterdam The Netherlands PeliClass human IgG subclass Plus kit PeliClass sheep anti human IgG1 Plus PeliClass sheep anti human IgG2 Plus
Instructions for use Sanquin Reagents B.V. Plesmanlaan 125 1066 CX Amsterdam The Netherlands PeliClass human IgG subclass Plus kit PeliClass sheep anti human IgG1 Plus PeliClass sheep anti human IgG2 Plus
Parametry metod automatické fotometrické analýzy
 Parametry metod automatické fotometrické analýzy Každá metoda prováděná automatickým biochemickým analyzátorem má v softwaru řídícího počítače nadefinované parametry: číslo (aplikační kód) metody název
Parametry metod automatické fotometrické analýzy Každá metoda prováděná automatickým biochemickým analyzátorem má v softwaru řídícího počítače nadefinované parametry: číslo (aplikační kód) metody název
JAK MOHOU VÝROBCI IVD POMÁHAT LABORATOŘÍM PŘI AKREDITACI
 Referenční laboratoř MZ ČR pro klinickou biochemii při Ústavu klinické biochemie a laboratorní diagnostiky VFN a 1. LF UK JAK MOHOU VÝROBCI IVD POMÁHAT LABORATOŘÍM PŘI AKREDITACI IVD MD A INFORMACE POSKYTOVANÉ
Referenční laboratoř MZ ČR pro klinickou biochemii při Ústavu klinické biochemie a laboratorní diagnostiky VFN a 1. LF UK JAK MOHOU VÝROBCI IVD POMÁHAT LABORATOŘÍM PŘI AKREDITACI IVD MD A INFORMACE POSKYTOVANÉ
PŘÍPRAVA REAGENCIÍ A STABILITA:
 REF 816A 10 lahviček z nichž každá obsahuje 0,5ml LAtrol Abnormální kontroly REF 816N 10 lahviček z nichž každá obsahuje 1,0ml LAtrol Normální kontroly UŽITÍ: LAtrol Abnormální kontrolní plazma (REF 816A)
REF 816A 10 lahviček z nichž každá obsahuje 0,5ml LAtrol Abnormální kontroly REF 816N 10 lahviček z nichž každá obsahuje 1,0ml LAtrol Normální kontroly UŽITÍ: LAtrol Abnormální kontrolní plazma (REF 816A)
CRP. Axis - Shield. SINGLE TESTS CRP kvantitativní stanovení pomocí přístroje NycoCard Reader II
 Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Lékařská technika a speciální zdravotní materiál Společnost je zapsána v obchodním rejstříku Městského soudu v Praze, odd. C vložka 1299 Obchodní 110, 251 70 Praha Čestlice Tel. +420 296 328 300 Fax. +420
Validační protokol LT CRP HS II (ADVIA 1800)
 Validační protokol LT CRP HS II (ADVIA 1800) Datum vydání: 9.5.2011 Zpracoval: Ing. Luděk Šprongl Pracoviště: Centrální laboratoř, Šumperská nemocnice a.s. Validační protokol LT CRP HS II 1. CÍL, PŘEDMĚT
Validační protokol LT CRP HS II (ADVIA 1800) Datum vydání: 9.5.2011 Zpracoval: Ing. Luděk Šprongl Pracoviště: Centrální laboratoř, Šumperská nemocnice a.s. Validační protokol LT CRP HS II 1. CÍL, PŘEDMĚT
MagPurix Viral Nucleic Acid Extraction Kit
 MagPurix Viral Nucleic Acid Extraction Kit Kat. č. ZP02003 Doba zpracování: 40-55 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Viral Nucleic Acid Extraction Kit je určena
MagPurix Viral Nucleic Acid Extraction Kit Kat. č. ZP02003 Doba zpracování: 40-55 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Viral Nucleic Acid Extraction Kit je určena
CHORUS INSULIN (36 testů)
 CHORUS INSULIN 86086 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
CHORUS INSULIN 86086 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
CHORUS. CHLAMYDOPHILA PNEUMONIAE IgA
 CHORUS CHLAMYDOPHILA PNEUMONIAE IgA 81252 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy...
CHORUS CHLAMYDOPHILA PNEUMONIAE IgA 81252 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy...
NÁVOD K POUŽITÍ. VITROS Chemistry Products Performance Verifier I and II. Účel použití. Reagencie. Varování a bezpečnostní upozornění.
 NÁVOD K POUŽITÍ VITROS Chemistry Products Performance Verifier I and II Performance Verifier I and II 806 7324 823 1474 Účel použití Pouze pro diagnostické použití in vitro. VITROS Chemistry Products Performance
NÁVOD K POUŽITÍ VITROS Chemistry Products Performance Verifier I and II Performance Verifier I and II 806 7324 823 1474 Účel použití Pouze pro diagnostické použití in vitro. VITROS Chemistry Products Performance
CHORUS HSV 1 SCREEN (36 testů)
 CHORUS HSV 1 SCREEN 81018 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné
CHORUS HSV 1 SCREEN 81018 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné
Návod k použití Informace o produktech jsou dostupné na internetových stránkách: www.demeditec.com
 Návod k použití Informace o produktech jsou dostupné na internetových stránkách: www.demeditec.com TPA IRMA Radioimunoanalýza pro kvantitativní stanovení cytokeratinu 8 a 18 v séru Prosím používejte pouze
Návod k použití Informace o produktech jsou dostupné na internetových stránkách: www.demeditec.com TPA IRMA Radioimunoanalýza pro kvantitativní stanovení cytokeratinu 8 a 18 v séru Prosím používejte pouze
G7 HSi Elution Buffer No. 1 (S) No. 2 (S) No. 3 (S)
 1/13 2/13 Automated Glycohemoglobin Analyzer HLC-723G7 EU rev. G7S-01010 Bezpečnostní opatření K vaší ochraně anebo k ochraně vašeho majetku před možným poškozením a k zajištění osobní bezpečnosti si před
1/13 2/13 Automated Glycohemoglobin Analyzer HLC-723G7 EU rev. G7S-01010 Bezpečnostní opatření K vaší ochraně anebo k ochraně vašeho majetku před možným poškozením a k zajištění osobní bezpečnosti si před
Metody testování humorální imunity
 Metody testování humorální imunity Co je to humorální imunita? Humorální = látková Buněčné produkty Nespecifická imunita příklady:» Lysozym v slinách, slzách» Sérové proteiny (proteiny akutní fáze)» Komplementový
Metody testování humorální imunity Co je to humorální imunita? Humorální = látková Buněčné produkty Nespecifická imunita příklady:» Lysozym v slinách, slzách» Sérové proteiny (proteiny akutní fáze)» Komplementový
Verifikace sérologických testů v imunologických laboratořích ISO 15189 5.5 Postupy vyšetření
 Verifikace sérologických testů v imunologických laboratořích ISO 15189 5.5 Postupy vyšetření Andrea Vinciková Centrum imunologie a mikrobiologie Zdravotní ústav se sídlem v Ústí nad Labem Validace Ověřování,
Verifikace sérologických testů v imunologických laboratořích ISO 15189 5.5 Postupy vyšetření Andrea Vinciková Centrum imunologie a mikrobiologie Zdravotní ústav se sídlem v Ústí nad Labem Validace Ověřování,
Bezpečnostní opatření
 Bezpečnostní opatření 181344, Rev. A říjen 212 ADVIA Centaur CP Souprava Ferritin změna analytické citlivosti a upravení hodnot kalibrátoru C Dle našich záznamů jste obdrželi ADVIA Centaur kalibrátor C
Bezpečnostní opatření 181344, Rev. A říjen 212 ADVIA Centaur CP Souprava Ferritin změna analytické citlivosti a upravení hodnot kalibrátoru C Dle našich záznamů jste obdrželi ADVIA Centaur kalibrátor C
Nová doporučení o interní kontrole kvality koagulačních vyšetření. RNDr. Ingrid V. Hrachovinová, Ph.D. Laboratoř pro poruchy hemostázy, ÚHKT Praha
 Nová doporučení o interní kontrole kvality koagulačních vyšetření RNDr. Ingrid V. Hrachovinová, Ph.D. Laboratoř pro poruchy hemostázy, ÚHKT Praha Proč vnitřní kontrola kvality (VKK) ve vyšetření hemostázy?
Nová doporučení o interní kontrole kvality koagulačních vyšetření RNDr. Ingrid V. Hrachovinová, Ph.D. Laboratoř pro poruchy hemostázy, ÚHKT Praha Proč vnitřní kontrola kvality (VKK) ve vyšetření hemostázy?
Rapid-VIDITEST. Rota-Adeno Card. (Jednokrokový kazetový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy
 Rapid-VIDITEST Rota-Adeno Card (Jednokrokový kazetový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II č. 365, Vestec, 252 42 Jesenice
Rapid-VIDITEST Rota-Adeno Card (Jednokrokový kazetový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II č. 365, Vestec, 252 42 Jesenice
DIAQUICK Mononukleóza kazeta z plné krve, séra nebo plazmy
 DIAQUICK Mononukleóza kazeta z plné krve, séra nebo plazmy REF CONT Z06620CE 30 testů individuálně balených 30 jednorázových pipet 1 lahvička s pufrem (pro 30 testů) 2 kontroly (pozitivní a negativní)
DIAQUICK Mononukleóza kazeta z plné krve, séra nebo plazmy REF CONT Z06620CE 30 testů individuálně balených 30 jednorázových pipet 1 lahvička s pufrem (pro 30 testů) 2 kontroly (pozitivní a negativní)
Protilátky proti ovariu ELISA
 Návod k použití Protilátky proti ovariu ELISA Kat.č.: BS-40-20 Počet testů: 96 Skladování: 2 C 8 C (36 F 46 F) Na enzymy vázané imunosorbentní stanovení (ELISA) ke zjištění protilátek působících proti
Návod k použití Protilátky proti ovariu ELISA Kat.č.: BS-40-20 Počet testů: 96 Skladování: 2 C 8 C (36 F 46 F) Na enzymy vázané imunosorbentní stanovení (ELISA) ke zjištění protilátek působících proti
CHORUS. MYCOPLASMA PNEUMONIAE IgA
 CHORUS MYCOPLASMA PNEUMONIAE IgA 81033 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 4 3 Složení soupravy... 4
CHORUS MYCOPLASMA PNEUMONIAE IgA 81033 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 4 3 Složení soupravy... 4
CHORUS SS-A (36 testů)
 CHORUS SS-A 86018 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
CHORUS SS-A 86018 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
Metody testování humorální imunity
 Metody testování humorální imunity Co je to humorální imunita? Humorální = látková Buněčné produkty Nespecifická imunita příklady:» Lysozym v slinách, slzách» Sérové proteiny (proteiny akutní fáze)» Komplementový
Metody testování humorální imunity Co je to humorální imunita? Humorální = látková Buněčné produkty Nespecifická imunita příklady:» Lysozym v slinách, slzách» Sérové proteiny (proteiny akutní fáze)» Komplementový
Sérologický kardiolipinový a netreponemový test určený pro rychlou detekci Syphilisu KATALOGOVÉ ČÍSLO: RPRL-0100 (100 testů)
 RPRL VDRL Carbon Sérologický kardiolipinový a netreponemový test určený pro rychlou detekci Syphilisu KATALOGOVÉ ČÍSLO: RPRL-0100 (100 testů) (1, 2) KLINICKÝ VÝZNAM Syfilis je venerické onemocnění způsobené
RPRL VDRL Carbon Sérologický kardiolipinový a netreponemový test určený pro rychlou detekci Syphilisu KATALOGOVÉ ČÍSLO: RPRL-0100 (100 testů) (1, 2) KLINICKÝ VÝZNAM Syfilis je venerické onemocnění způsobené
IMMUVIEW L. PNEUMOPHILA AND L. LONGBEACHE URINARY ANTIGEN TEST
 Dodává: GALI spol. s r.o., Ke Stadionu 179, Semily 513 01 tel. 481 689 050 fax. 481 689 051 info@gali.cz www.gali.cz IMMUVIEW L. PNEUMOPHILA AND L. LONGBEACHE URINARY ANTIGEN TEST 1 IMMUVIEW L. PNEUMOPHILA
Dodává: GALI spol. s r.o., Ke Stadionu 179, Semily 513 01 tel. 481 689 050 fax. 481 689 051 info@gali.cz www.gali.cz IMMUVIEW L. PNEUMOPHILA AND L. LONGBEACHE URINARY ANTIGEN TEST 1 IMMUVIEW L. PNEUMOPHILA
Základy fotometrie, využití v klinické biochemii
 Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
Základy fotometrie, využití v klinické biochemii Základní vztahy ve fotometrii transmitance (propustnost): T = I / I 0 absorbance: A = log (I 0 / I) = log (1 / T) = log T Lambertův-Beerův zákon A l = e
Revmatoidní faktor (RF)
 Siemens Healthcare Diagnostics Inc. Návod k použití 2011-09 Revmatoidní faktor (RF) Systém ADVIA 1200 Nové informace Výchozí verze této metody Výchozí verze této metody Výchozí verze této metody Přehled
Siemens Healthcare Diagnostics Inc. Návod k použití 2011-09 Revmatoidní faktor (RF) Systém ADVIA 1200 Nové informace Výchozí verze této metody Výchozí verze této metody Výchozí verze této metody Přehled
DEMEDITEC Bordetella pertussis IgA ELISA
 DEMEDITEC Bordetella pertussis IgA ELISA Kat. č. DEBPT02 Návod k použití soupravy VÝROBCE: Demeditec Diagnostics GmbH Lise-Meitner-Straße 2 D-24145 Kiel (Germany), tel: +49 (0)431/71922-0, fax. +49 (0)431/71922-55,
DEMEDITEC Bordetella pertussis IgA ELISA Kat. č. DEBPT02 Návod k použití soupravy VÝROBCE: Demeditec Diagnostics GmbH Lise-Meitner-Straße 2 D-24145 Kiel (Germany), tel: +49 (0)431/71922-0, fax. +49 (0)431/71922-55,
CHORUS dsdna-g (36 testů)
 CHORUS dsdna-g 86032 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
CHORUS dsdna-g 86032 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
STANOVENÍ ANTIOXIDAČNÍ KAPACITY METODOU FOTOCHEMILUMINISCENCE NA PŘÍSTROJI PHOTOCHEM
 STANOVENÍ ANTIOXIDAČNÍ KAPACITY METODOU FOTOCHEMILUMINISCENCE NA PŘÍSTROJI PHOTOCHEM ANTIOXIDAČNÍ KAPACITA RŮZNÝCH DRUHŮ MASA (drůbeží, rybí) Princip metodiky: Analyzátor Photochem je určen pro stanovení
STANOVENÍ ANTIOXIDAČNÍ KAPACITY METODOU FOTOCHEMILUMINISCENCE NA PŘÍSTROJI PHOTOCHEM ANTIOXIDAČNÍ KAPACITA RŮZNÝCH DRUHŮ MASA (drůbeží, rybí) Princip metodiky: Analyzátor Photochem je určen pro stanovení
Rapid-VIDITEST RSV. (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů)
 Rapid-VIDITEST RSV (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad
Rapid-VIDITEST RSV (Jednokrokový kazetový test pro in vitro diagnostiku Respiračního syncytiálního viru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad
STANOVENÍ ANTIOXIDAČNÍ KAPACITY METODOU FOTOCHEMILUMINISCENCE NA PŘÍSTROJI PHOTOCHEM
 STANOVENÍ ANTIOXIDAČNÍ KAPACITY METODOU FOTOCHEMILUMINISCENCE NA PŘÍSTROJI PHOTOCHEM ANTIOXIDAČNÍ KAPACITA ČAJŮ Princip metodiky: Analyzátor Photochem je určen pro stanovení antioxidační kapacity vybraných
STANOVENÍ ANTIOXIDAČNÍ KAPACITY METODOU FOTOCHEMILUMINISCENCE NA PŘÍSTROJI PHOTOCHEM ANTIOXIDAČNÍ KAPACITA ČAJŮ Princip metodiky: Analyzátor Photochem je určen pro stanovení antioxidační kapacity vybraných
CA125 IRMA Souprava CA125 IRMA umožňuje přímé in-vitro kvantitativní stanovení s tumorem asociovaného antigenu CA125 v lidském séru
 Informace o výrobku Informace o ostatních produktech jsou dostupné na www.demeditec.com Návod k použití CA125 IRMA Souprava CA125 IRMA umožňuje přímé in-vitro kvantitativní stanovení s tumorem asociovaného
Informace o výrobku Informace o ostatních produktech jsou dostupné na www.demeditec.com Návod k použití CA125 IRMA Souprava CA125 IRMA umožňuje přímé in-vitro kvantitativní stanovení s tumorem asociovaného
Analytické znaky laboratorní metody Interní kontrola kvality Externí kontrola kvality
 Analytické znaky laboratorní metody Interní kontrola kvality Externí kontrola kvality RNDr. Alena Mikušková FN Brno Pracoviště dětské medicíny, OKB amikuskova@fnbrno.cz Analytické znaky laboratorní metody
Analytické znaky laboratorní metody Interní kontrola kvality Externí kontrola kvality RNDr. Alena Mikušková FN Brno Pracoviště dětské medicíny, OKB amikuskova@fnbrno.cz Analytické znaky laboratorní metody
AESKULISA. Objednací kód: 3402. BioVendor - Laboratorní medicína a.s. Tel: +49-6734-9627-0 Fax: +49-6734-9627-27 Tel: +420549124111
 AESKULISA Tg Objednací kód: 3402 Aesku.Diagnostics BioVendor - Laboratorní medicína a.s. Mikroforum Ring 2, D-55234 Wendelsheim, Germany Karásek 1767/1, 621 00 Brno Tel: +49-6734-9627-0 Fax: +49-6734-9627-27
AESKULISA Tg Objednací kód: 3402 Aesku.Diagnostics BioVendor - Laboratorní medicína a.s. Mikroforum Ring 2, D-55234 Wendelsheim, Germany Karásek 1767/1, 621 00 Brno Tel: +49-6734-9627-0 Fax: +49-6734-9627-27
CHORUS COPROCOLLECT. Výrobce: DIESSE Diagnostica Senese Via delle Rose Monteriggioni (Siena) Itálie
 CHORUS COPROCOLLECT 86602 Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 3 4 Další potřebné vybavení
CHORUS COPROCOLLECT 86602 Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 3 4 Další potřebné vybavení
Objednací číslo Protilátky proti Třída Ig Substrát Formát EI 2691-9601 G Chřipka A IgG Ag-potažené mikrotitrační jamky
 Protilátky třídy IgG proti chřipce typu A Návod na použití ELISA testu Objednací číslo Protilátky proti Třída Ig Substrát Formát EI 2691-9601 G Chřipka A IgG Ag-potažené mikrotitrační jamky 96 x 01 (96).
Protilátky třídy IgG proti chřipce typu A Návod na použití ELISA testu Objednací číslo Protilátky proti Třída Ig Substrát Formát EI 2691-9601 G Chřipka A IgG Ag-potažené mikrotitrační jamky 96 x 01 (96).
AESKULISA. Objednací kód: 3601
 AESKULISA Insulin Objednací kód: 3601 Aesku.Diagnostics BioVendor - Laboratorní medicína a.s. Mikroforum Ring 2, D-55234 Wendelsheim, Germany Karásek 1767/1, 621 00 Brno Tel: +49-6734-9627-0 Fax: +49-6734-9627-27
AESKULISA Insulin Objednací kód: 3601 Aesku.Diagnostics BioVendor - Laboratorní medicína a.s. Mikroforum Ring 2, D-55234 Wendelsheim, Germany Karásek 1767/1, 621 00 Brno Tel: +49-6734-9627-0 Fax: +49-6734-9627-27
CHORUS DEAMINATED GLIADIN-A
 CHORUS DEAMINATED GLIADIN-A 86098 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další
CHORUS DEAMINATED GLIADIN-A 86098 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další
Rapid-VIDITEST Adenovirus Resp.
 Rapid-VIDITEST Adenovirus Resp. (Jednokrokový kazetový test pro in vitro diagnostiku Adenoviru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II
Rapid-VIDITEST Adenovirus Resp. (Jednokrokový kazetový test pro in vitro diagnostiku Adenoviru z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II
CHORUS AMA-M (36 testů)
 CHORUS AMA-M2 86084 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
CHORUS AMA-M2 86084 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
Kalibrace analytických metod. Miroslava Beňovská s využitím přednášky Dr. Breineka
 Kalibrace analytických metod Miroslava Beňovská s využitím přednášky Dr. Breineka Měřící zařízení (zjednodušeně přístroje) pro měření fyzikálních veličin musí být výrobci kalibrovaná Objem: pipety Teplota
Kalibrace analytických metod Miroslava Beňovská s využitím přednášky Dr. Breineka Měřící zařízení (zjednodušeně přístroje) pro měření fyzikálních veličin musí být výrobci kalibrovaná Objem: pipety Teplota
Objednací číslo Určení Ig-třída Substrát Formát EI M CMV (Cytomegalovirus)
 Protilátky proti CMV (IgM) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2570-9601 M CMV (Cytomegalovirus) IgM Ag-potažené mikrotitrační jamky 96 x 01 (96) Princip testu:
Protilátky proti CMV (IgM) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2570-9601 M CMV (Cytomegalovirus) IgM Ag-potažené mikrotitrační jamky 96 x 01 (96) Princip testu:
CHORUS. MYCOPLASMA PNEUMONIAE IgM
 CHORUS MYCOPLASMA PNEUMONIAE IgM 81035 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4
CHORUS MYCOPLASMA PNEUMONIAE IgM 81035 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4
MASTAZYME TM Cardiolipin
 MASTAZYME TM Cardiolipin Enzymatická imunoesej pro detekci autoprotilátek třídy IgG a IgM proti kardiolipinu v séru a plasmě Návod k použití Pouze pro in vitro diagnostiku Test Kód Kit pro MASTAZYME TM
MASTAZYME TM Cardiolipin Enzymatická imunoesej pro detekci autoprotilátek třídy IgG a IgM proti kardiolipinu v séru a plasmě Návod k použití Pouze pro in vitro diagnostiku Test Kód Kit pro MASTAZYME TM
Rapid-VIDITEST. H. pylori. (Jednokrokový kazetový test pro in vitro diagnostiku Helicobacter pylori ve stolici ) Návod k použití soupravy
 Rapid-VIDITEST H. pylori (Jednokrokový kazetový test pro in vitro diagnostiku Helicobacter pylori ve stolici ) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice
Rapid-VIDITEST H. pylori (Jednokrokový kazetový test pro in vitro diagnostiku Helicobacter pylori ve stolici ) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II 365, Vestec, 252 42 Jesenice
TSKgel G7 HSi. Návod k použití. Bezpečnostní opatření. [Upozornění použitá v textu]
![TSKgel G7 HSi. Návod k použití. Bezpečnostní opatření. [Upozornění použitá v textu] TSKgel G7 HSi. Návod k použití. Bezpečnostní opatření. [Upozornění použitá v textu]](/thumbs/26/8489490.jpg) 1/13 2/13 Automated Glycohemoglobin Analyzer HLC-723G7 EU rev. G7S-01010 Bezpečnostní opatření K vaší ochraně anebo k ochraně vašeho majetku před možným poškozením a k zajištění osobní bezpečnosti si před
1/13 2/13 Automated Glycohemoglobin Analyzer HLC-723G7 EU rev. G7S-01010 Bezpečnostní opatření K vaší ochraně anebo k ochraně vašeho majetku před možným poškozením a k zajištění osobní bezpečnosti si před
BEZPEČNOSTNÍ LIST NYCOCARD D-DIMER WASHING SOLUTION. 1. POPIS PRODUKTU A VÝROBCE Název produktu: NycoCard D-Dimer Washing Solution Aplikace:
 BEZPEČNOSTNÍ LIST NYCOCARD D-DIMER WASHING SOLUTION 1. POPIS PRODUKTU A VÝROBCE Název produktu: NycoCard D-Dimer Washing Solution Aplikace: Určeno k užití s sety NycoCard D-Dimer. NycoCard D-Dimer Single
BEZPEČNOSTNÍ LIST NYCOCARD D-DIMER WASHING SOLUTION 1. POPIS PRODUKTU A VÝROBCE Název produktu: NycoCard D-Dimer Washing Solution Aplikace: Určeno k užití s sety NycoCard D-Dimer. NycoCard D-Dimer Single
KATALOG DIAGNOSTICKÝCH SETŮ S K A L A B 2018
 KATALOG DIAGNOSTICKÝCH SETŮ S K A L A B 2018 set Princip Objem Cena Hořčík 600 A (Mg 600 A) 104 Hořečnaté ionty reagují v prostředí trisového pufru při ph = 8,8 s arsenazem III za vzniku stabilního modrého
KATALOG DIAGNOSTICKÝCH SETŮ S K A L A B 2018 set Princip Objem Cena Hořčík 600 A (Mg 600 A) 104 Hořečnaté ionty reagují v prostředí trisového pufru při ph = 8,8 s arsenazem III za vzniku stabilního modrého
GanglioCombi. se směsí enzymů značených IgG a IgM. anti-ganglioside protilátky ELISA (GA1, GM1, GM2, GD1a, GD1b a GQ1b)
 GanglioCombi se směsí enzymů značených IgG a IgM anti-ganglioside protilátky ELISA (GA1, GM1, GM2, GD1a, GD1b a GQ1b) EK-GCO-GM 2 x 96 testů (12 profilů pacientů, IgG & IgM) Datum revize: 11.8.2010 1 /
GanglioCombi se směsí enzymů značených IgG a IgM anti-ganglioside protilátky ELISA (GA1, GM1, GM2, GD1a, GD1b a GQ1b) EK-GCO-GM 2 x 96 testů (12 profilů pacientů, IgG & IgM) Datum revize: 11.8.2010 1 /
Rapid-VIDITEST Influenza A+B
 Rapid-VIDITEST Influenza A+B (Jednokrokový blisterový test pro in vitro diagnostiku viru Influenzy typu A a B z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o.,
Rapid-VIDITEST Influenza A+B (Jednokrokový blisterový test pro in vitro diagnostiku viru Influenzy typu A a B z nosních výtěrů, výplachů a aspirátů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o.,
Protokol o srovnání POCT EUROLyser CRP s akreditovanou metodou stanovení CRP imunoturbidimetricky na analyzátoru Unicel DxC 800
 Protokol o zkoušce č.j. 3/2016, počet stran 8, strana číslo 1 Referenční laboratoř pro klinickou biochemii při Ústavu lékařské biochemie a laboratorní diagnostiky VFN Karlovo nám. 32, 121 11 Praha 2, tel.:
Protokol o zkoušce č.j. 3/2016, počet stran 8, strana číslo 1 Referenční laboratoř pro klinickou biochemii při Ústavu lékařské biochemie a laboratorní diagnostiky VFN Karlovo nám. 32, 121 11 Praha 2, tel.:
CHORUS ANA-Screen (36 testů)
 CHORUS ANA-Screen 86014 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 4 3 Složení soupravy... 4 4 Další potřebné
CHORUS ANA-Screen 86014 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 4 3 Složení soupravy... 4 4 Další potřebné
CHORUS BETA 2-GLYCOPROTEIN-M
 CHORUS BETA 2-GLYCOPROTEIN-M 86052 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další
CHORUS BETA 2-GLYCOPROTEIN-M 86052 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další
CHORUS (36 testů)
 CHORUS Sm 86016 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
CHORUS Sm 86016 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
Objednací číslo Protilátky proti Třída Ig Substrát Formát EI M Chřipka A IgM Ag-potažené mikrotitrační jamky
 Protilátky třídy IgM proti chřipce typu A Návod na použití ELISA testu Objednací číslo Protilátky proti Třída Ig Substrát Formát EI 2691-9601 M Chřipka A IgM Ag-potažené mikrotitrační jamky 96 x 01 (96).
Protilátky třídy IgM proti chřipce typu A Návod na použití ELISA testu Objednací číslo Protilátky proti Třída Ig Substrát Formát EI 2691-9601 M Chřipka A IgM Ag-potažené mikrotitrační jamky 96 x 01 (96).
IMUNOENZYMATICKÉ SOUPRAVY K DIAGNOSTICE CYTOMEGALOVIROVÉ INFEKCE
 INFEKČNÍ SÉROLOGIE Virologie IMUNOENZYMATICKÉ SOUPRAVY K DIAGNOSTICE CYTOMEGALOVIROVÉ INFEKCE Cytomegalovirus ELISA soupravy jsou určeny ke stanovení specifických protilátek třídy IgA, IgG a IgM v lidském
INFEKČNÍ SÉROLOGIE Virologie IMUNOENZYMATICKÉ SOUPRAVY K DIAGNOSTICE CYTOMEGALOVIROVÉ INFEKCE Cytomegalovirus ELISA soupravy jsou určeny ke stanovení specifických protilátek třídy IgA, IgG a IgM v lidském
Rapid-VIDITEST. Rota-Adeno Blister. (Jednokrokový blisterový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy
 Rapid-VIDITEST Rota-Adeno Blister (Jednokrokový blisterový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II č. 365, Vestec, 252 42
Rapid-VIDITEST Rota-Adeno Blister (Jednokrokový blisterový test pro in vitro diagnostiku rotavirů a adenovirů) Návod k použití soupravy Výrobce: VIDIA spol. s r.o., Nad Safinou II č. 365, Vestec, 252 42
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I
 1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
1. Příloha 1 Návod úlohy pro Pokročilé praktikum z biochemie I Vazba bromfenolové modři na sérový albumin Princip úlohy Albumin má unikátní vlastnost vázat menší molekuly mnoha typů. Díky struktuře, tvořené
AESKULISA. Crohn s-check. Objednací kód: 3509
 AESKULISA Crohn s-check Objednací kód: 3509 Aesku.Diagnostics BioVendor - Laboratorní medicína a.s. Mikroforum Ring 2, D-55234 Wendelsheim, Germany Karásek 1767/1, 621 00 Brno Tel: +49-6734-9627-0 Fax:
AESKULISA Crohn s-check Objednací kód: 3509 Aesku.Diagnostics BioVendor - Laboratorní medicína a.s. Mikroforum Ring 2, D-55234 Wendelsheim, Germany Karásek 1767/1, 621 00 Brno Tel: +49-6734-9627-0 Fax:
Protilátky proti Helicobacter pylori (IgG) Návod na použití ELISA testu
 Protilátky proti Helicobacter pylori (IgG) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2080-9601 G Helicobacter pylori IgG Ag-potažené mikrotitrační jamky 96 x 01 (96)
Protilátky proti Helicobacter pylori (IgG) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2080-9601 G Helicobacter pylori IgG Ag-potažené mikrotitrační jamky 96 x 01 (96)
CHORUS. MYCOPLASMA PNEUMONIAE IgG
 CHORUS MYCOPLASMA PNEUMONIAE IgG 81034 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4
CHORUS MYCOPLASMA PNEUMONIAE IgG 81034 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4
MONO - Rychlý test na mononukleózu (plná krev/sérum/plazma) Příbalová informace
 C 35 MONO - Rychlý test na mononukleózu (plná krev/sérum/plazma) Příbalová informace Rychlý test pro diagnostiku infekční mononukleózy (IM), kvalitativní detekce heterofilních protilátek IM v plné krvi,
C 35 MONO - Rychlý test na mononukleózu (plná krev/sérum/plazma) Příbalová informace Rychlý test pro diagnostiku infekční mononukleózy (IM), kvalitativní detekce heterofilních protilátek IM v plné krvi,
CHORUS ASCA-A (36 testů)
 CHORUS ASCA-A 86062 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
CHORUS ASCA-A 86062 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 3 3 Složení soupravy... 4 4 Další potřebné vybavení
CHORUS GLIADIN-G (36 testů)
 CHORUS GLIADIN-G 86058 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 4 3 Složení soupravy... 4 4 Další potřebné
CHORUS GLIADIN-G 86058 (36 testů) Výrobce: DIESSE Diagnostica Senese Via delle Rose 10 53035 Monteriggioni (Siena) Itálie OBSAH 1 Úvod... 3 2 Princip testu... 4 3 Složení soupravy... 4 4 Další potřebné
Objednací číslo Určení Ig-třída Substrát Formát EI 2192-9601 M Chlamydia pneumoniae IgM Ag-potažené mikrotitrační jamky
 Protilátky proti Chlamydia pneumoniae (IgM) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2192-9601 M Chlamydia pneumoniae IgM Ag-potažené mikrotitrační jamky 96 x 01
Protilátky proti Chlamydia pneumoniae (IgM) Návod na použití ELISA testu Objednací číslo Určení Ig-třída Substrát Formát EI 2192-9601 M Chlamydia pneumoniae IgM Ag-potažené mikrotitrační jamky 96 x 01
Aspartátaminotransferáza (AST)
 1 Aspartátaminotransferáza (AST) AST je buněčný enzym přítomný v řadě tkání, jako jsou srdce, kosterní svaly, ledviny, mozek, játra, pankreas či erytrocyty. Vyskytuje se ve dvou izoformách, cytoplazmatické
1 Aspartátaminotransferáza (AST) AST je buněčný enzym přítomný v řadě tkání, jako jsou srdce, kosterní svaly, ledviny, mozek, játra, pankreas či erytrocyty. Vyskytuje se ve dvou izoformách, cytoplazmatické
IL-6. Laterální imunodifuze pro semikvantitativní měření lidského interleukinu 6 (IL- 6)
 IL-6 Laterální imunodifuze pro semikvantitativní měření lidského interleukinu 6 (IL- 6) Lateralní průtokový imunologický test pro kvantitativní stanovení lidského interleukinu-6 (IL-6), vyhodnocení pomocí
IL-6 Laterální imunodifuze pro semikvantitativní měření lidského interleukinu 6 (IL- 6) Lateralní průtokový imunologický test pro kvantitativní stanovení lidského interleukinu-6 (IL-6), vyhodnocení pomocí
Protokol o zkoušce č.j. 1/2016, počet stran 12, strana číslo 1. V Praze dne Č.j. 1/2016
 Protokol o zkoušce č.j. 1/2016, počet stran 12, strana číslo 1 Referenční laboratoř pro klinickou biochemii při Ústavu lékařské biochemie a laboratorní diagnostiky VFN Karlovo nám. 32, 121 11 Praha 2,
Protokol o zkoušce č.j. 1/2016, počet stran 12, strana číslo 1 Referenční laboratoř pro klinickou biochemii při Ústavu lékařské biochemie a laboratorní diagnostiky VFN Karlovo nám. 32, 121 11 Praha 2,
TSKgel G8 Variant HSi
 TSKgel G8 Variant HSi 1/14 TSKgel G8 Variant HSi 2/14 Tosoh Automated Glycohemoglobin Analyzer HLC-723G8 Rev. DC012030 Bezpečnostní opatření K vaší ochraně anebo k ochraně vašeho majetku před možným poškozením
TSKgel G8 Variant HSi 1/14 TSKgel G8 Variant HSi 2/14 Tosoh Automated Glycohemoglobin Analyzer HLC-723G8 Rev. DC012030 Bezpečnostní opatření K vaší ochraně anebo k ochraně vašeho majetku před možným poškozením
