Obsah. Ú v o d Kinetické f a k to r y Stacionární Živé Nestacionární... 27
|
|
|
- Alexandra Růžena Zemanová
- před 7 lety
- Počet zobrazení:
Transkript
1 Obsah 7 Ú v o d Polymerace... ^ 11 Podle druhu aktivních c e n t e r R adikálové Iontové Kationtové A niontové... 2^ 113 K o o rd in a č n í... 2(* 12 Podle reaktivity aktivních c e n te r... 2l) 121 Retézové polymerace Postupné polyadice Podle počtu monomerů v polymerujícím systém u H om opolym erace... 2' 132 Kopolymerace Statistické Alternujici B lokové Roubovací Podle počtu fází na počátku a v průbčhu r e a k c e Hom ogenní Homogenní, přecházející v heterogenní ; srážecí Heterogenní Polymerace v kapalné fázi V b l o k u V roztoku V su sp e n z i.../ V e m u lz i Podle uspořádáni vznikajících řetězců... 2(> 161 S neřízenou p ro p a g a c í Stcreospccifické Kinetické f a k to r y Stacionární Živé Nestacionární Dílčí d ě je Separace dílčích d ě jů Fyzikální vlivy: teplota, tlak, viskozita Výběr in ic iá to ru... 29
2 Čistota p ro stře lil In ic iá to r M onomery Třidění m onom erů Organickochemická klasifikace Vinylové a vinylidenové m o n o m ery l i l A lk e n y Vinylové a vinylidenové monomery s polárními substituenty D ieny Konjugované d ie n y Nekonjugované dieny s izolovanými vazbam i Sloučeniny s kumulovanými dvojnými v azb am i Alkiny Cyklické m onom ery Cykloalkany Cyklické alkeny, nekonjugované i konjugované cyklické dieny Aromatické sloučeniny H eterocykly Jiné m onom ery Vztah mezi strukturou monomeru a způsobem jeho polymerace Donor akceptorové vlastnosti m onom erů Monomery jako donory elektronů Monomery jako akceptory elektronů Vlastnosti polymerujících m onom erů Fyzikální vlastnosti monomerů Chemické vlastnosti m o n o m e rů Reaktivita m o n o m e rů Monomer a ostatní složky systém u... 6! 241 Fyzikální vztahy... ^ 242 Chemické in te ra k c e Komplexy m onom erů Dvojice (trojice...) m onom erů Monomery spolu nekom plexují Z monomerů vznikají donor-akceptorové k o m p le x y Modely monomerů Zdroje m onom erů Toxicita m o n o m e rů In ic ia c e... ** 31 Vznik primárních r a d ik á lů Termická (spontánni) in ic ia c e Iniciátory Peroxidy, jejich rozpad Redox in iciace... 87
3 Azoiniciátory, jejich r o z p a d Fotoiniciace Senzibilace Iniciace transferem energie Fotosenzibilace transferem e le k tro n u Iniciace fragmentací Iniciace produkty rozpadu donor-akceptorových komplexů Iniciátory vznikající in s í t u Vliv k y s lík u Jiné způsoby vzniku r a d ik á lů Netypické in iciáto ry Multifunkční in ic iá to ry Polymerni iniciátory Chováni primárnich ra d ik á lů Klečový efekt Účinnost iniciace Reakce radikálu s nenasycenou molekulou ! Iniciace radikálové polym erace Vznik iniciace schopného a n io n t u Vlastnosti vazby kov u h lik Iniciace alkylkovovými sloučeninami Vlastnosti vazby kov kyslík a kov d u s í k Iniciace alk o h o lá ty Transfer elektronu z donoru na m onom er Iniciace alkalickými k o v y Iniciace radikál-anionty Jiné způsoby vzniku iniciujících aniontů Reakce aniontu s monom erem Iniciace aniontové poly m erace Aktivátory aniontové polym erace Vznik iniciace schopného k a tio n tu Iniciátory kationtových polymeraci Brönstedot у ky s e lin y Lewisovy kyseliny Koiniciace Multifunkční iniciátory Reakce kationtu s m o n o m erem Vznik komplexů, iniciujících koordinační polym erace Zieglerovy-Naltovy katalyzátory Katalyzátory z přechodových kovů působících v nepřítomnosti a lk y lk o v ů Iniciující donor-akceptorové kom plexy Vznik radikál-iontů a jejich reakce s m o n o m e ry Polymerace iniciované termicky aktivovanými donor akceptorovými komplexy Polykombinace am fiio n tů... Monomery jako iontové páry (monomerní soli) Jiné druhy iniciace Elektroiniciace Mechanochemická in ic ia c e lil '
4 Iniciace v plazmě Iniciace nepolymerujícich sloučenin Kinetika iniciace Aktivní centra polymeraci Aktivní centra radikálových polym eraci Reaktivita radikálů Reaktivita radikálových center v průbčhu polymerace Horké" ra d ik á ly Zásah do struktury center Některé radikály zvláštního význam u Iontová aktivní c e n t r a Ionty, iontové páry a jejich asociáty Centra kationtových polym eraci K arbokationty Karboxoniová c e n t r a Oxoniová c e n t r a Kationty jiných prvků než uhlíku a kyslíku Centra aniontových p o ly m eraci K arbanionty Jiné a n io n ty Amfiionty Radikál jio n ty Koordinační centra Koordinační centra Zieglerových- Nattových polymeraci Pevné Zieglerovy-Nattovy k ataly záto ry Rozpustné Zieglerovy-Nattovy kataly záto ry Nosičové katalyzátory Vlastnosti koordinačních center Zicglerových Nattových polymeraci Jiná koordinační centra Transformace c e n te r Živá a spící c e n tr a Propagace Teoretické podmínky propagace Termodynamické podm ínky Mezní polymeračni teplota. \ ' Reakční teplo a změna entropie při propagaci Vliv tlaku na p ro p a g a c i Chemické v li v y Přítomnost n ečisto t Propagace a polykondenzace Kinetické v l i v y Stacionární poly m erace Živé polymerace s rychlou iniciací Nestacionární polym erace
5 5133 Teplota polymerace Okolí aktivního centra (vnčjši vlivy) P rostředí Důsledky vzniku p o ly m e ru Vzrůst viskozity Vznik pevné l a z e Aktivní centra a polymer Matriční e f e k t Obecné rysy propagace Konverze Odvod polymeračního te p la Objemová kontrakce polymerujícího s y s té m u Rizená p ro p ag ace Stereospecifický r ů s t Konfigurace řetězců a statistika stereochemie p ro p ag ace Obecné faktory určující způsob řízené adice Růst na volném centru Růst na vázaném c e n tr u Stereoelektivni a stereoselektivní polym erace Propagace na vazbě přechodový kov u h l í k Stereochemická kontrola propagace 1-alkenů Stereochemická kontrola propagace konjugovaných a nekonjugovaných d ie n ů Izomeračni polymerace Cyklopolym e r a c e Propagace anhydridů N-karboxy-a-aminokyselin Polymerace v micelách (emulzní polymerace) Iniciace ve vodní f á z i Smithova-Ewartova te o rie Novější t e o r i e Polymerace v emulzi, iniciovaná nerozpustným iniciátorem Iontové emulzni polym erace Kopolymerace Kopolymerační rovnice Kopolymerační parametry Experimentální stanovení kopolymeračních param etrů Teorie kopolymeračních p a ra m e trů Distribuce monomerních jednotek v k o p o ly m e ru Iontová kopolym erace Koordinační kopolym erace Multisložková kopolym erace Vliv předposledního č le n u Kopolymerace s monomery a jejich komplexy Ternární kopolymerace a kopolymerace vice než tří m o n o m erů Termodynamika kopolym erace Kopolymerace při teplotě nad 7), b jednoho z m o n o m erů Kinetika kopolymerace Zvláštní druhy kopolym erace
6 Alternující kopolymerace Kombinace am fiiontů Blokové k o p o ly m ery Roubované kopolym ery Mechanismus p ro p a g a c e A d i c e Inzerce Koordinační inzerce Polymerace otevíráním c y k l ů Vznik makrocyklů při polymeraci cyklických m onom erů Polymerace na aktivujících lig a n d e c h Vétvení, síťováni D epropagace Kinetika p ro p a g a c e Propagace v živých systém ech Určení rychlosti propagace na volných iontech a iontových párech u živých polym eraci Propagace heterocyklů. Periodické změny reaktivity rostoucího c e n tr a Rychlostní konstanta p ro p a g a c e Term inace Zánik aktivity rad ik álů... 3!1 611 Kombinace, disproporcionace ra d ik á lů Vliv tlaku na terminaci Vliv koncentrace polymeru a délky jeho řetězců Terminace primárnich radikálů s primárními ra d ik á ly Systémy s brzděnou term in aci G e l-e fe k t Zakotvené ra d ik á ly Inhibice, inhibitory A utoinhibice Nestacionárni stavy radikálových p o ly m e ra c i Pre-efekt radikálové polymerace se vzájemnou terminaci ra d ik á lů Vyhasínáni radikálové polymerace vzájemnou terminaci ra d ik á lů Rotujici sektory Prostorově přerušovaná polym erace Končení iontových polymeraci Končeni za účasti párového i o n t u Posun rovnováh mezi ionty, iontovými páry a estery Výměny párových io n t ů Kombinace io n tů Terminace nestabilním párovým io n te m Přeměna aktivního centra na neaktivní částici nebo málo aktivní ion Agregace center Polymeračně neaktivní komplexy iontů Autoinhibice (autoterminace) Terminace nesprávnou adicí m o n o m e ru
7 6225 Terminace nečistotami Kombinace makroiontů Končeni koordinačních polymeraci Končení d o n o ry Končení přerušením vazby kov polymer v aktivním c e n tr u Končení dezaktivací organokovu Spontánní" term inace Využili te rm in a c e M akrom ery Dezaktivace center Stanovení počtu center Kinetika terminace Přenos Obecná charakteristika přenosových r e a k c í Retardace Degradativní přenos Větveni (siťování) přenosem Větveni nesprávnou" adicí monomeru nebo iniciátoru Multifunkční přen ašeče Přenos p o ly m erem Přenosy u radikálových polymeraci Mechanismus některých přenosů Přenosy u aniontových polym eraci Přenosy H0,H Přenosy u kationtových polymeraci Přenos při polymeraci uhlovodíkových monomerů a monomerů s heteroatomy v pobočném řetězci Přenosy při polymeraci monomerů s heteroatomy v c y k lu Přenosy u koordinačních polym eraci Přenosy organokovy Přenosy molekulárním H Ostatní přenosy koordinačních polymeraci Molekulové hmotnosti produktů polymeraci Kopolymerujici přenašeče Využití p ře n o sů Regulace molekulových hm otnosti Roubování přenosem Vznik makromerů přenosem Kinetika... 3g3 81 Polymeračni rychlost Rychlost iniciace... З Radikálová polymerace
8 Celková reakční rychlost ideálních polymeraci Reakce různě dlouhých r a d ik á lů Neideální radikálová polym erace Příklad : Kinetická analýza polymerace vinylchloridu Iontové p o ly m erace Živé polymerace s pomalou in ic ia c i Nestacionární polym erace Přiklad: Polymerace 3,3-bis(chlormethylJ-oxetanu Koordinační polym erace Model kinetiky Zieglerových-Nattových polym eraci Přiklad : Polymerace ethylenu Polymeračni stupeň p ro d u k tu Distribuce molekulových hmotnosti p ro d u k tu Střední polymeračni stupeň číselný a h m o tn o s tn í Rychlost živých polymeraci a distribuční křivky molekulových hmotnosti jejich produktů Distribuce molekulových hmotností produktů radikálových polymeraci Příklad: Kinetika změn distribuce molekulových hmotnosti v průběhu polymerace heterocyklů Technika zkoumání polym eraci Sumární průběh polymerace. příklady konkrétně používaných m e to d D ila to m e trie K alo rim etrie Chromatografické metody Spektrální m eto d y Základni d ě je Vznik aktivních c e n te r Reakce aktivních center během polym erace Analýza polym eru Stanovení molekulových hmotností a jejich ro zd ělen i Takticita polym erů Rozvětvení makromolekul Chemická analýza polym erů Potlačení kontaminace polymerujících systém ů Otevřené s y s té m y Vysokovakuové s y s té m y Zpracováni výsledků Kinetická a n a lý z a Využiti výsledků Publikace a přihlášky vy n álezů Návrh většího zařízeni Seznam sy m b o lů R ejstřík...465
Kopolymerace polymerace dvou a více monomerů
 Kopolymerace polymerace dvou a více monomerů ( 1 monomer homopolymer; 2 monomery kopolymer; 3 monomery ternární kopolymer [ př ABS]) mezní případy kopolymerace: n A n B A A n B B n A B n Struktury vznikajících
Kopolymerace polymerace dvou a více monomerů ( 1 monomer homopolymer; 2 monomery kopolymer; 3 monomery ternární kopolymer [ př ABS]) mezní případy kopolymerace: n A n B A A n B B n A B n Struktury vznikajících
Polymerizace. Polytransformace
 vznik makromolekuly Polymerizace Polytransformace Podmínky vzniku makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce
vznik makromolekuly Polymerizace Polytransformace Podmínky vzniku makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce
Podmínky vzniku makromolekuly
 Podmínky vzniku makromolekuly Vznik makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce nejméně dvoufunkční 2) termodynamická
Podmínky vzniku makromolekuly Vznik makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce nejméně dvoufunkční 2) termodynamická
Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch
 Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch Atom, složení a struktura Chemické prvky-názvosloví, slučivost Chemické sloučeniny, molekuly Chemická vazba
Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch Atom, složení a struktura Chemické prvky-názvosloví, slučivost Chemické sloučeniny, molekuly Chemická vazba
H H C C C C C C H CH 3 H C C H H H H H H
 Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
o Řetězové polymerizace o Stupňovité polymerizace Základní typy polymerizací
 vznik makromolekuly Vznik makromolekuly Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité
vznik makromolekuly Vznik makromolekuly Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité
Obsah. 2. Mechanismus a syntetické využití nejdůležitějších organických reakcí 31 2.1. Adiční reakce 31 2.1.1. Elektrofilní adice (A E
 Obsah 1. Typy reakcí, reakčních komponent a jejich roztřídění 6 1.1. Formální kritérium pro klasifikaci reakcí 6 1.2. Typy reakčních komponent a způsob jejich vzniku jako další kriterium pro klasifikaci
Obsah 1. Typy reakcí, reakčních komponent a jejich roztřídění 6 1.1. Formální kritérium pro klasifikaci reakcí 6 1.2. Typy reakčních komponent a způsob jejich vzniku jako další kriterium pro klasifikaci
Úvod do studia organické chemie
 Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
kopolymerace kopolymery
 kopolymerace kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické
kopolymerace kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické
MAKROMOLEKULÁRNÍ LÁTKY
 MAKROMOLEKULÁRNÍ LÁTKY 1. Základní pojmy - makromolekulární látky = molekulové systémy složené z velkého počtu atomů, které jsou vázány chemickou vazbou do dlouhých řetězců - řetězce jsou tvořeny stavebními
MAKROMOLEKULÁRNÍ LÁTKY 1. Základní pojmy - makromolekulární látky = molekulové systémy složené z velkého počtu atomů, které jsou vázány chemickou vazbou do dlouhých řetězců - řetězce jsou tvořeny stavebními
Přírodní proteiny, nukleové kyseliny (NA)
 kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické akrylonitril-butadien-styrenový
kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické akrylonitril-butadien-styrenový
1. ročník Počet hodin
 SOUSTAVY LÁTEK A JEJICH SLOŽENÍ rozdělení přírodních látek a vlastnosti chemických látek soustavy látek a jejich složení STAVBA ATOMU historie pohledu na atom složení a struktura atomu stavba atomu VELIČINY
SOUSTAVY LÁTEK A JEJICH SLOŽENÍ rozdělení přírodních látek a vlastnosti chemických látek soustavy látek a jejich složení STAVBA ATOMU historie pohledu na atom složení a struktura atomu stavba atomu VELIČINY
4 Term ika. D ůsledky zavedení tep lo ty a tep la Stavová r o v n i c e Stavová rovnice termická a kalorická
 Obsah Předm luva И 1 Výchozí představy term odynam iky 13 1.1 Předmět zkoumání termodynamiky... 13 1.1.1 Celkový r á m e c... 13 1.1.2 Teplo, teplota, e n tr o p ie... 14 1.1.3 Vymezení term o d y n am
Obsah Předm luva И 1 Výchozí představy term odynam iky 13 1.1 Předmět zkoumání termodynamiky... 13 1.1.1 Celkový r á m e c... 13 1.1.2 Teplo, teplota, e n tr o p ie... 14 1.1.3 Vymezení term o d y n am
Chemická kinetika. Chemické změny probíhající na úrovni atomárně molekulové nazýváme reakční mechanismus.
 Chemická kinetika Chemická reakce: děj mezi jednotlivými atomy a molekulami, při kterých zanikají některé vazby v molekulách výchozích látek a jsou nahrazovány vazbami v molekulách nově vznikajících látek.
Chemická kinetika Chemická reakce: děj mezi jednotlivými atomy a molekulami, při kterých zanikají některé vazby v molekulách výchozích látek a jsou nahrazovány vazbami v molekulách nově vznikajících látek.
MATURITNÍ OTÁZKY Z CHEMIE
 MATURITNÍ OTÁZKY Z CHEMIE 1 Složení a struktura atomu Vývoj představ o složení a struktuře atomu, elektronový obal atomu, modely atomu, pojem orbital, typy orbitalů, jejich znázorňování a pravidla pro
MATURITNÍ OTÁZKY Z CHEMIE 1 Složení a struktura atomu Vývoj představ o složení a struktuře atomu, elektronový obal atomu, modely atomu, pojem orbital, typy orbitalů, jejich znázorňování a pravidla pro
ENZYMY. RNDr. Lucie Koláčná, Ph.D.
 ENZYMY RNDr. Lucie Koláčná, Ph.D. Enzymy: katalyzátory živé buňky jednoduché nebo složené proteiny Apoenzym: proteinová část Kofaktor: nízkomolekulová neaminokyselinová struktura nezbytně nutná pro funkci
ENZYMY RNDr. Lucie Koláčná, Ph.D. Enzymy: katalyzátory živé buňky jednoduché nebo složené proteiny Apoenzym: proteinová část Kofaktor: nízkomolekulová neaminokyselinová struktura nezbytně nutná pro funkci
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Otázky ke zkoušce z obecné chemie (Prof. RNDr. Karel Procházka, DrSc.)
 Otázky ke zkoušce z obecné chemie (Prof. RNDr. Karel Procházka, DrSc.) Na ústní zkoušku se může přihlásit student, který má zápočet ze cvičení a úspěšně složenou zkouškovou písemku. Na ústní zkoušku se
Otázky ke zkoušce z obecné chemie (Prof. RNDr. Karel Procházka, DrSc.) Na ústní zkoušku se může přihlásit student, který má zápočet ze cvičení a úspěšně složenou zkouškovou písemku. Na ústní zkoušku se
Pericycklické reakce
 Reakce, v nichž se tvoří nebo zanikají vazby na konci π-systému. Nejedná se o iontový ani radikálový mechanismus, intermediáty nejsou ani kationty ani anionty! Průběh reakce součinným procesem přes cyklický
Reakce, v nichž se tvoří nebo zanikají vazby na konci π-systému. Nejedná se o iontový ani radikálový mechanismus, intermediáty nejsou ani kationty ani anionty! Průběh reakce součinným procesem přes cyklický
Složení a struktura atomu Charakteristika elementárních částic. Modely atomu. Izotopy a nuklidy. Atomové jádro -
 MATURITNÍ OKRUHY Z CHEMIE Obecná chemie Složení a struktura atomu Charakteristika elementárních částic. Modely atomu. Izotopy a nuklidy. Atomové jádro - hmotnostní úbytek, vazebná energie jádra, jaderné
MATURITNÍ OKRUHY Z CHEMIE Obecná chemie Složení a struktura atomu Charakteristika elementárních částic. Modely atomu. Izotopy a nuklidy. Atomové jádro - hmotnostní úbytek, vazebná energie jádra, jaderné
Reakční kinetika. Nauka zabývající se rychlostí chemických reakcí a ovlivněním rychlosti těchto reakcí
 Nauka zabývající se rychlostí chemických reakcí a ovlivněním rychlosti těchto reakcí Vymezení pojmů : chemická reakce je děj, při kterém zanikají výchozí látky a vznikají látky nové reakční mechanismus
Nauka zabývající se rychlostí chemických reakcí a ovlivněním rychlosti těchto reakcí Vymezení pojmů : chemická reakce je děj, při kterém zanikají výchozí látky a vznikají látky nové reakční mechanismus
Polymery lze rozdělit podle několika kritérií. Podle původu rozlišujeme polymery přírodní a syntetické. Přírodní polymery jsou:
 MAKROMOLEKULÁRNÍ LÁTKY (POLYMERY) Makromolekuly jsou molekulové systémy složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců. Tyto řetězce tvoří pravidelně se opakující části,
MAKROMOLEKULÁRNÍ LÁTKY (POLYMERY) Makromolekuly jsou molekulové systémy složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců. Tyto řetězce tvoří pravidelně se opakující části,
Iontové polymerizace
 Iontové polymerizace Vznik makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce nejméně dvoufunkční 2) termodynamická podmínka
Iontové polymerizace Vznik makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce nejméně dvoufunkční 2) termodynamická podmínka
Chemická kinetika. Chemická kinetika studuje Rychlost chemických reakcí Mechanismus reakcí (reakční kroky)
 Chemická kinetika Chemická kinetika studuje Rychlost chemických reakcí Mechanismus reakcí (reakční kroky) Rychlé reakce výbuch, neutralizace H + +OH Pomalé reakce rezivění železa Časová závislost průběhu
Chemická kinetika Chemická kinetika studuje Rychlost chemických reakcí Mechanismus reakcí (reakční kroky) Rychlé reakce výbuch, neutralizace H + +OH Pomalé reakce rezivění železa Časová závislost průběhu
Seminář z chemie. Charakteristika vyučovacího předmětu
 Seminář z chemie Časová dotace: 2 hodiny ve 3. ročníku, 4 hodiny ve 4. Ročníku Charakteristika vyučovacího předmětu Seminář je zaměřený na přípravu ke školní maturitě z chemie a k přijímacím zkouškám na
Seminář z chemie Časová dotace: 2 hodiny ve 3. ročníku, 4 hodiny ve 4. Ročníku Charakteristika vyučovacího předmětu Seminář je zaměřený na přípravu ke školní maturitě z chemie a k přijímacím zkouškám na
Ú v o d... 11. 1 Úvod d o c h iru rg ic k é h o o š e tř o v a te ls tv í (R enáta Z eleníková)... 13
 Obsah Ú v o d... 11 1 Úvod d o c h iru rg ic k é h o o š e tř o v a te ls tv í (R enáta Z eleníková)... 13 1.1 C h arak te ristik a ch iru rg ic k éh o o š e tř o v a te ls tv í... 13 1.1.1 Č in n o sti
Obsah Ú v o d... 11 1 Úvod d o c h iru rg ic k é h o o š e tř o v a te ls tv í (R enáta Z eleníková)... 13 1.1 C h arak te ristik a ch iru rg ic k éh o o š e tř o v a te ls tv í... 13 1.1.1 Č in n o sti
Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4.
 Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Vlastnosti. Pozor! H 3 C CH 3 H CH 3
 Alkeny Vlastnosti C n 2n obsahují dvojné vazby uhlíky v sp 2 hybridizaci násobná vazba vzniká překryvem 2p orbitalů obou atomů uhlíku nad a pod prostorem obsazeným vazbou aby k překryvu mohlo dojít, musí
Alkeny Vlastnosti C n 2n obsahují dvojné vazby uhlíky v sp 2 hybridizaci násobná vazba vzniká překryvem 2p orbitalů obou atomů uhlíku nad a pod prostorem obsazeným vazbou aby k překryvu mohlo dojít, musí
Alkeny. Alkeny. Největšíprůmyslový význam majíethen (ethylen) a propen (propylen) jako suroviny pro další přeměny nebo pro polymerace
 Alkeny Dvojná vazba je tvořena jednou vazbou sigma a jednou vazbou pí. Dvojná vazba je kratší než vazba jednoduchá a všechny čtyři atomy vázané na dvojnou vazbu leží v jedné rovině. Fyzikální vlastnosti
Alkeny Dvojná vazba je tvořena jednou vazbou sigma a jednou vazbou pí. Dvojná vazba je kratší než vazba jednoduchá a všechny čtyři atomy vázané na dvojnou vazbu leží v jedné rovině. Fyzikální vlastnosti
Charakteristika Teorie kyselin a zásad. Příprava kyselin Vlastnosti + typické reakce. Významné kyseliny. Arrheniova teorie Teorie Brönsted-Lowryho
 Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
Energie v chemických reakcích
 Energie v chemických reakcích Energetická bilance reakce CH 4 + Cl 2 = CH 3 Cl + HCl rozštěpení vazeb vznik nových vazeb V chemických reakcích dochází ke změně vazeb mezi atomy. Vazebná energie uvolnění
Energie v chemických reakcích Energetická bilance reakce CH 4 + Cl 2 = CH 3 Cl + HCl rozštěpení vazeb vznik nových vazeb V chemických reakcích dochází ke změně vazeb mezi atomy. Vazebná energie uvolnění
Přírodní proteiny, nukleové kyseliny (NA)
 kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické akrylonitril-butadien-styrenový
kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické akrylonitril-butadien-styrenový
9. Chemické reakce Kinetika
 Základní pojmy Kinetické rovnice pro celistvé řády Katalýza Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti reakční mechanismus elementární reakce a molekularita reakce reakční rychlost
Základní pojmy Kinetické rovnice pro celistvé řády Katalýza Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti reakční mechanismus elementární reakce a molekularita reakce reakční rychlost
ALKENY NENASYCENÉ UHLOVODÍKY
 ALKENY NENASYCENÉ ULOVODÍKY 1 ALKENY - mají ve svých molekulách alespoň jednu dvojnou vazbu- C=C homologický vzorec : C n 2n názvy od alkanů zakončeny koncovkou en CYKLOALKENY - homologický vzorec : C
ALKENY NENASYCENÉ ULOVODÍKY 1 ALKENY - mají ve svých molekulách alespoň jednu dvojnou vazbu- C=C homologický vzorec : C n 2n názvy od alkanů zakončeny koncovkou en CYKLOALKENY - homologický vzorec : C
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
Předmět: Seminář chemie (SCH) Náplň: Obecná chemie, anorganická chemie, chemické výpočty, základy analytické chemie Třída: 3. ročník a septima Počet hodin: 2 hodiny týdně Pomůcky: Vybavení odborné učebny,
PODĚKOVÁNI K DRUHÉMU VYDÁNÍ...7 PŘEDMLUVA К PRVNÍMU VYDÁNI... 8 FARMAKOTERAPIE V OBDOBÍ TĚHOTENSTVÍ
 PODĚKOVÁNI K DRUHÉMU VYDÁNÍ...7 PŘEDMLUVA К PRVNÍMU VYDÁNI... 8 FARMAKOTERAPIE V OBDOBÍ TĚHOTENSTVÍ 1 OBECNÁ Č Á S T...16 1.1 Ú v o d...16 1.2 P rin c ip y te r a to lo g ie...17 1.3 F a rm a k o k in
PODĚKOVÁNI K DRUHÉMU VYDÁNÍ...7 PŘEDMLUVA К PRVNÍMU VYDÁNI... 8 FARMAKOTERAPIE V OBDOBÍ TĚHOTENSTVÍ 1 OBECNÁ Č Á S T...16 1.1 Ú v o d...16 1.2 P rin c ip y te r a to lo g ie...17 1.3 F a rm a k o k in
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
2.5.2 N ěm ecko 95 Z áv ěr k ap ito ly 96
 Obsah Seznam zkratek 13 Ú vod 15 1. T e o re tic k á a m e to d o lo g ic k á v ý c h o d is k a 19 1.1 Pojm y válka a m ír a je jic h v z á je m n ý d y a d ic k ý v z ta h 19 1.1.1 C o je d y a d ic
Obsah Seznam zkratek 13 Ú vod 15 1. T e o re tic k á a m e to d o lo g ic k á v ý c h o d is k a 19 1.1 Pojm y válka a m ír a je jic h v z á je m n ý d y a d ic k ý v z ta h 19 1.1.1 C o je d y a d ic
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 16, 566 01 Vysoké Mýto Alkeny Vlastnosti dvojné vazby Hybridizace uhlíku vázaného dvojnou vazbou je sp. Valenční úhel který svírají vazby na uhlíkovém atomu je přibližně
Gymnázium Vysoké Mýto nám. Vaňorného 16, 566 01 Vysoké Mýto Alkeny Vlastnosti dvojné vazby Hybridizace uhlíku vázaného dvojnou vazbou je sp. Valenční úhel který svírají vazby na uhlíkovém atomu je přibližně
Chemická vazba. Molekula vodíku. Elektronová teorie. Oktetové pravidlo (Kossel, Lewis, 1916) Pevnost vazby vazebná energie.
 Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Řetězová polymerizace
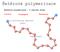 Řetězová polymerizace Řetězové polymerizace 3 odlišné kroky iiciace Propagace Terminace Initiating species Chain Step-Growth Iontové polymerizace aniontové, kationtové v závislosti na typu rostoucího aktivního
Řetězová polymerizace Řetězové polymerizace 3 odlišné kroky iiciace Propagace Terminace Initiating species Chain Step-Growth Iontové polymerizace aniontové, kationtové v závislosti na typu rostoucího aktivního
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: Číslo DUMu: VY_32_INOVACE_10_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 12.02.2013 Číslo DUMu: VY_32_INOVACE_10_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 12.02.2013 Číslo DUMu: VY_32_INOVACE_10_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Průvodka. CZ.1.07/1.5.00/ Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
POLYMERY II MECHANISMY VZNIKU VÝROBNÍ POSTUPY
 PLYMERY II MEANISMY VZNIKU VÝRBNÍ PSTUPY čem budeme mluvit Typy polymeračních reakcí mechanismy Základní způsoby výroby polymerů PLYMERAČNÍ REAKE ADIČNÍ KNDENZAČNÍ ŘETĚZVÉ PSTUPNÉ KRDINAČNÍ (ZIEGLER-NATTA)
PLYMERY II MEANISMY VZNIKU VÝRBNÍ PSTUPY čem budeme mluvit Typy polymeračních reakcí mechanismy Základní způsoby výroby polymerů PLYMERAČNÍ REAKE ADIČNÍ KNDENZAČNÍ ŘETĚZVÉ PSTUPNÉ KRDINAČNÍ (ZIEGLER-NATTA)
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace
 Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Ú vod... I 7. In te rd is c ip lin á rn í p řís tu p k p ro b le m a tic e u m ír á n í a s m r t i...19 T h a n a to lo g ie...19
 11 OBSAH Ú vod... I 7 In te rd is c ip lin á rn í p řís tu p k p ro b le m a tic e u m ír á n í a s m r t i...19 T h a n a to lo g ie...19 T h a n a to p s y c h o lo g ie...20 T hanatosociologie... 22
11 OBSAH Ú vod... I 7 In te rd is c ip lin á rn í p řís tu p k p ro b le m a tic e u m ír á n í a s m r t i...19 T h a n a to lo g ie...19 T h a n a to p s y c h o lo g ie...20 T hanatosociologie... 22
2.2.2 Ú m y sln á u b lížen í n a zd rav í a d alší n á siln é tre stn é čin y N ásiln o sti - les v io le n c e s...
 1. K rim in o lo g ic k á č á s t... 13 1.1 V y m ezen í n á siln é k rim in a lity a so u v isejících p o jm ů... 13 1.1.1 N ásilí a n á siln á k r im in a lita... 14 1.1.2 A grese, k rim in á ln í a
1. K rim in o lo g ic k á č á s t... 13 1.1 V y m ezen í n á siln é k rim in a lity a so u v isejících p o jm ů... 13 1.1.1 N ásilí a n á siln á k r im in a lita... 14 1.1.2 A grese, k rim in á ln í a
Názvosloví Konformace Isomerie. Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o )
 ALKANY 1 Názvosloví Konformace Isomerie Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o ) 2 Alkany (resp. cykloalkany) jsou nejzákladnější organické sloučeniny složené pouze z
ALKANY 1 Názvosloví Konformace Isomerie Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o ) 2 Alkany (resp. cykloalkany) jsou nejzákladnější organické sloučeniny složené pouze z
2.4 Stavové chování směsí plynů Ideální směs Ideální směs reálných plynů Stavové rovnice pro plynné směsi
 1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
Gymnázium Zikmunda Wintra Rakovník. Schéma témat profilové části maturitní zkoušky z předmětu CHEMIE
 Gymnázium Zikmunda Wintra Rakovník Schéma témat profilové části maturitní zkoušky z předmětu CHEMIE Součástí každého tématu jsou úlohy z názvosloví chemických sloučenin a chemických výpočtů. 1. Stavba
Gymnázium Zikmunda Wintra Rakovník Schéma témat profilové části maturitní zkoušky z předmětu CHEMIE Součástí každého tématu jsou úlohy z názvosloví chemických sloučenin a chemických výpočtů. 1. Stavba
Základní chemické pojmy
 MZ CHEMIE 2015 MO 1 Základní chemické pojmy Atom, molekula, prvek, protonové číslo. Sloučenina, chemicky čistá látka, směs, dělení směsí. Relativní atomová hmotnost, molekulová hmotnost, atomová hmotnostní
MZ CHEMIE 2015 MO 1 Základní chemické pojmy Atom, molekula, prvek, protonové číslo. Sloučenina, chemicky čistá látka, směs, dělení směsí. Relativní atomová hmotnost, molekulová hmotnost, atomová hmotnostní
ZAKLADY FYZIKALNI CHEMIE HORENí, VÝBUCHU A HAŠENí
 r SDRUŽENí POŽÁRNíHO A BEZPEČNOSTNíHO INžENÝRSTVí. JAROSLAV K,\LOUSEK,.,.,. ZAKLADY FYZIKALNI CHEMIE HORENí, VÝBUCHU A HAŠENí EDICESPBI SPEKTRUM OBSAH. strana 1. FyzikálnÍ chemie v požární ochranč a bezpečnosti
r SDRUŽENí POŽÁRNíHO A BEZPEČNOSTNíHO INžENÝRSTVí. JAROSLAV K,\LOUSEK,.,.,. ZAKLADY FYZIKALNI CHEMIE HORENí, VÝBUCHU A HAŠENí EDICESPBI SPEKTRUM OBSAH. strana 1. FyzikálnÍ chemie v požární ochranč a bezpečnosti
Karbonylové sloučeniny
 Karbonylové sloučeniny více než 120 o 120 o C O C C d + d - C O C sp 2 C sp 2 R C O H R 1 C O R 2 1.aldehydy, ketony Nu E R C O R C O 2. karboxylové kyseliny a funkční deriváty O H 3. deriváty kys. uhličité
Karbonylové sloučeniny více než 120 o 120 o C O C C d + d - C O C sp 2 C sp 2 R C O H R 1 C O R 2 1.aldehydy, ketony Nu E R C O R C O 2. karboxylové kyseliny a funkční deriváty O H 3. deriváty kys. uhličité
Vybrané kapitoly z chemie a technologie polymerů II N112041
 Studijní opory pro studenty VŠCHT registrované na předmět: Vybrané kapitoly z chemie a technologie polymerů II N112041 Vyučující: Jan Merna, Ústav polymerů, VŠCHT Praha Živé / Řízené polymerace Knowing
Studijní opory pro studenty VŠCHT registrované na předmět: Vybrané kapitoly z chemie a technologie polymerů II N112041 Vyučující: Jan Merna, Ústav polymerů, VŠCHT Praha Živé / Řízené polymerace Knowing
UHLOVODÍKY ALKANY (...)
 UHLOVODÍKY ALKANY (...) alifatické nasycené uhlovodíky nerozvětvené i rozvětvené mezi atomy uhlíku pouze jednoduché vazby (σ vazby), mezi nimi úhel 109 28 název: kmen + an obecný vzorec C n H 2n + 2 tvoří
UHLOVODÍKY ALKANY (...) alifatické nasycené uhlovodíky nerozvětvené i rozvětvené mezi atomy uhlíku pouze jednoduché vazby (σ vazby), mezi nimi úhel 109 28 název: kmen + an obecný vzorec C n H 2n + 2 tvoří
Obsah O A U T O R O V I...12 Ú V O D... 13
 Obsah O BSAH strana O A U T O R O V I...12 Ú V O D... 13 I. V la s tn o s ti p ly n ů a p ly n n ý c h paliv 1.1 Fyzikální vlastnosti plynů Tlak p ly n u...15 Teplota plynu...16 Normální stavy plynu...17
Obsah O BSAH strana O A U T O R O V I...12 Ú V O D... 13 I. V la s tn o s ti p ly n ů a p ly n n ý c h paliv 1.1 Fyzikální vlastnosti plynů Tlak p ly n u...15 Teplota plynu...16 Normální stavy plynu...17
Název školy: SPŠ Ústí nad Labem, středisko Resslova
 Název školy: SPŠ Ústí nad Labem, středisko Resslova Číslo projektu: CZ.1.07/1.5.00/34.10.1036 Klíčová aktivita: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Digitální učební materiály Autor:
Název školy: SPŠ Ústí nad Labem, středisko Resslova Číslo projektu: CZ.1.07/1.5.00/34.10.1036 Klíčová aktivita: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Digitální učební materiály Autor:
VIII. 6.5 Polyadice. H. Schejbalová & I. Stibor, str. 179. I. Prokopová, str. 181. D. Lukáš 2013
 VIII. 6.5 Polyadice H. Schejbalová & I. Stibor, str. 179. I. Prokopová, str. 181. D. Lukáš 2013 1 Vzdělávací záměr 1. Polyadice obecný průběh polyadice, odlišnosti od polykondenzace. 2. Syntéza polyuretanů
VIII. 6.5 Polyadice H. Schejbalová & I. Stibor, str. 179. I. Prokopová, str. 181. D. Lukáš 2013 1 Vzdělávací záměr 1. Polyadice obecný průběh polyadice, odlišnosti od polykondenzace. 2. Syntéza polyuretanů
Hmotnost atomů a molekul 6 Látkové množství 11. Rozdělení směsí 16 Separační metody 20. Hustota, hmotnostní a objemový zlomek 25.
 Obsah Obecná chemie II. 1. Látkové množství Hmotnost atomů a molekul 6 Látkové množství 11 2. Směsi Rozdělení směsí 16 Separační metody 20 3. Chemické výpočty Hustota, hmotnostní a objemový zlomek 25 Koncentrace
Obsah Obecná chemie II. 1. Látkové množství Hmotnost atomů a molekul 6 Látkové množství 11 2. Směsi Rozdělení směsí 16 Separační metody 20 3. Chemické výpočty Hustota, hmotnostní a objemový zlomek 25 Koncentrace
E K O G Y M N Á Z I U M B R N O o.p.s. přidružená škola UNESCO
 Seznam výukových materiálů III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast: Předmět: Vytvořil: Obecná chemie Chemie Mgr. Soňa Krampolová 01 - Látkové množství, molární hmotnost VY_32_INOVACE_01.pdf
Seznam výukových materiálů III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast: Předmět: Vytvořil: Obecná chemie Chemie Mgr. Soňa Krampolová 01 - Látkové množství, molární hmotnost VY_32_INOVACE_01.pdf
Ú V O D 3. 2 D O P R A V N Í S L U Ž B Y S lu žby železničn í d o p ra v y 20
 OBSAH Ú V O D 3 1 S L U Ž B Y C E S T O V N ÍH O R U C H U 5 3.1 P o d s ta ta a z v lá štn o sti slu ž eb cestovního ru c h u 6 1.2 K lasifik ace a c h a ra k te ris tik a slu ž eb cesto v n íh o r u
OBSAH Ú V O D 3 1 S L U Ž B Y C E S T O V N ÍH O R U C H U 5 3.1 P o d s ta ta a z v lá štn o sti slu ž eb cestovního ru c h u 6 1.2 K lasifik ace a c h a ra k te ris tik a slu ž eb cesto v n íh o r u
Inovace studia molekulární a buněčné biologie
 Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
INTERPRETACE HMOTNOSTNÍCH SPEKTER
 INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/
 Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 LRR/CHPB2 Chemie pro biology 2 Reakce a reakční mechanismy v organické chemii Lucie Szüčová Osnova: homolytické a heterolytické
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 LRR/CHPB2 Chemie pro biology 2 Reakce a reakční mechanismy v organické chemii Lucie Szüčová Osnova: homolytické a heterolytické
Nultá věta termodynamická
 TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
TEST + ŘEŠENÍ. PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKOUŠKY Z CHEMIE bakalářský studijní obor Bioorganická chemie 2010
 30 otázek maximum: 60 bodů TEST + ŘEŠEÍ PÍSEMÁ ČÁST PŘIJÍMACÍ ZKUŠKY Z CEMIE bakalářský studijní obor Bioorganická chemie 2010 1. apište názvy anorganických sloučenin: (4 body) 4 BaCr 4 kyselina peroxodusičná
30 otázek maximum: 60 bodů TEST + ŘEŠEÍ PÍSEMÁ ČÁST PŘIJÍMACÍ ZKUŠKY Z CEMIE bakalářský studijní obor Bioorganická chemie 2010 1. apište názvy anorganických sloučenin: (4 body) 4 BaCr 4 kyselina peroxodusičná
Dilatometrické sledování kinetiky radikálové polymerizace 1
 Dilatometrické sledování kinetiky radikálové polymerizace 1 1. Úvod Radikálovou polymerizací se průmyslově vyrábí asi 50 % syntetických polymerů. Detailní znalost vlivu reakčních parametrů na rychlost
Dilatometrické sledování kinetiky radikálové polymerizace 1 1. Úvod Radikálovou polymerizací se průmyslově vyrábí asi 50 % syntetických polymerů. Detailní znalost vlivu reakčních parametrů na rychlost
CHEMIE - Úvod do organické chemie
 Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Tabulace učebního plánu. Obecná chemie. Vzdělávací obsah pro vyučovací předmět : Ročník: 1.ročník a kvinta
 Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
Chemie - Sexta, 2. ročník
 - Sexta, 2. ročník Chemie Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
- Sexta, 2. ročník Chemie Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
Obsah A R IT M E T IK A...
 Obsah з A R IT M E T IK A... P řiro zená čísla a číslo n u la... Zápis přirozených č ís e l... Řím ské č íslice... Arabské číslice a desítková soustava... Šedesátková soustava... Porovnávání přirozených
Obsah з A R IT M E T IK A... P řiro zená čísla a číslo n u la... Zápis přirozených č ís e l... Řím ské č íslice... Arabské číslice a desítková soustava... Šedesátková soustava... Porovnávání přirozených
Polymerační způsoby. Bloková polymerace: monomer + iniciátor (0,1%) + (event. regulátor)
 Polymerační způsoby Technika provedení radikálové polymerace: Polymerace homogenní: a) bloková b) roztoková Polymerace heterogenní: a) srážecí b) suspenzní c) emulzní d) ostatní polymerace Bloková polymerace:
Polymerační způsoby Technika provedení radikálové polymerace: Polymerace homogenní: a) bloková b) roztoková Polymerace heterogenní: a) srážecí b) suspenzní c) emulzní d) ostatní polymerace Bloková polymerace:
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Autor: Tomáš Galbička Téma: Alkany a cykloalkany Ročník: 2.
 Alkany uhlovodíky s otevřeným řetězcem a pouze jednoduchými vazbami vazby sigma, největší výskyt elektronů na spojnici jader v názvu mají koncovku an Cykloalkany uhlovodíky s uzavřeným řetězcem a pouze
Alkany uhlovodíky s otevřeným řetězcem a pouze jednoduchými vazbami vazby sigma, největší výskyt elektronů na spojnici jader v názvu mají koncovku an Cykloalkany uhlovodíky s uzavřeným řetězcem a pouze
PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKOUŠKY Z CHEMIE bakalářský studijní obor Bioorganická chemie 2011
 Kód uchazeče:... Datum:... PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKUŠKY Z CHEMIE bakalářský studijní obor Bioorganická chemie 2011 30 otázek maximum: 60 bodů čas: 60 minut 1. Napište názvy anorganických sloučenin: (4
Kód uchazeče:... Datum:... PÍSEMNÁ ČÁST PŘIJÍMACÍ ZKUŠKY Z CHEMIE bakalářský studijní obor Bioorganická chemie 2011 30 otázek maximum: 60 bodů čas: 60 minut 1. Napište názvy anorganických sloučenin: (4
EU peníze středním školám digitální učební materiál
 EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními prin
 Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Chemie - 3. ročník. přesahy, vazby, mezipředmětové vztahy průřezová témata. očekávané výstupy RVP. témata / učivo. očekávané výstupy ŠVP.
 očekávané výstupy RVP témata / učivo Chemie - 3. ročník Žák: očekávané výstupy ŠVP přesahy, vazby, mezipředmětové vztahy průřezová témata 1.1., 1.2., 1.3., 1.4., 2.1. 1. Látky přírodní nebo syntetické
očekávané výstupy RVP témata / učivo Chemie - 3. ročník Žák: očekávané výstupy ŠVP přesahy, vazby, mezipředmětové vztahy průřezová témata 1.1., 1.2., 1.3., 1.4., 2.1. 1. Látky přírodní nebo syntetické
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie 2. ročník a sexta 2 hodiny týdně Školní tabule, interaktivní tabule, tyčinkové a kalotové modely molekul, zpětný
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie 2. ročník a sexta 2 hodiny týdně Školní tabule, interaktivní tabule, tyčinkové a kalotové modely molekul, zpětný
Rychlost chemické reakce A B. time. rychlost = - [A] t. [B] t. rychlost = Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C;
![Rychlost chemické reakce A B. time. rychlost = - [A] t. [B] t. rychlost = Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C; Rychlost chemické reakce A B. time. rychlost = - [A] t. [B] t. rychlost = Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C;](/thumbs/56/39180690.jpg) Rychlost chemické reakce A B time rychlost = - [A] t rychlost = [B] t Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C; 1 1 R A = RB = R 2 3 C Př.: Určete rychlost rozkladu HI v následující
Rychlost chemické reakce A B time rychlost = - [A] t rychlost = [B] t Reakční rychlost a stechiometrie A + B C; R C = R A = R B A + 2B 3C; 1 1 R A = RB = R 2 3 C Př.: Určete rychlost rozkladu HI v následující
18. Reakce v organické chemii
 1) homolýza, heterolýza 2) substituce, adice, eliminace, přesmyk 3) popis mechanismů hlavních typů reakcí (S R, A E, A R ) 4) příklady 18. Reakce v organické chemii 1) Homolýza, heterolýza KLASIFIKACE
1) homolýza, heterolýza 2) substituce, adice, eliminace, přesmyk 3) popis mechanismů hlavních typů reakcí (S R, A E, A R ) 4) příklady 18. Reakce v organické chemii 1) Homolýza, heterolýza KLASIFIKACE
Obsah. Slovo úvodem T o m á š T y l i...11. O becné poznám ky. V la d im ír B e n e š s t... 15. H istorick é rem in isce n c e
 Obsah Slovo úvodem T o m á š T y l i...11 O becné poznám ky V la d im ír B e n e š m l... 12 H istorick é rem in isce n c e V la d im ír B e n e š s t... 15 1 Vybrané k ap itoly z a n a to m ie a fy zio
Obsah Slovo úvodem T o m á š T y l i...11 O becné poznám ky V la d im ír B e n e š m l... 12 H istorick é rem in isce n c e V la d im ír B e n e š s t... 15 1 Vybrané k ap itoly z a n a to m ie a fy zio
Fyzikální chemie. ochrana životního prostředí analytická chemie chemická technologie denní. Platnost: od 1. 9. 2009 do 31. 8. 2013
 Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
Celosvětová produkce plastů
 PRODUKCE PLASTŮ Zpracování plastů cvičení 1 TU v Liberci, FS Celosvětová produkce plastů Mil. tun Asie (bez Japonska) 16 % Střední a západní Evropa 21 % Společenství nezávislých států 3 % 235 mil. tun
PRODUKCE PLASTŮ Zpracování plastů cvičení 1 TU v Liberci, FS Celosvětová produkce plastů Mil. tun Asie (bez Japonska) 16 % Střední a západní Evropa 21 % Společenství nezávislých států 3 % 235 mil. tun
Ú v o d K o m u je u rč e n a t a t o k n ih a C o n a le z n e te v t é t o k n iz e T y p o g ra fic k é k o n v e n c e...
 Ú v o d...1 1 K o m u je u rč e n a t a t o k n ih a... 1 2 C o n a le z n e te v t é t o k n iz e... 1 2 T y p o g ra fic k é k o n v e n c e... 1 3 1. S e z n á m e n í s d a ta b á z e m i...1 5 1.1
Ú v o d...1 1 K o m u je u rč e n a t a t o k n ih a... 1 2 C o n a le z n e te v t é t o k n iz e... 1 2 T y p o g ra fic k é k o n v e n c e... 1 3 1. S e z n á m e n í s d a ta b á z e m i...1 5 1.1
Chemie 2018 CAUS strana 1 (celkem 5)
 Chemie 2018 CAUS strana 1 (celkem 5) 1. Vápník má atomové číslo 20, hmotnostní 40. Kolik elektronů obsahuje kationt Ca 2+? a) 18 b) 20 c) 40 d) 60 2. Kolik elektronů ve valenční sféře má atom Al? a) 1
Chemie 2018 CAUS strana 1 (celkem 5) 1. Vápník má atomové číslo 20, hmotnostní 40. Kolik elektronů obsahuje kationt Ca 2+? a) 18 b) 20 c) 40 d) 60 2. Kolik elektronů ve valenční sféře má atom Al? a) 1
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
Netkané textilie. Materiály 2
 Materiály 2 1 Pojiva pro výrobu netkaných textilií Pojivo je jednou ze dvou základních složek pojených textilií. Forma pojiva a jeho vlastnosti předurčují technologii a podmínky procesu pojení způsob rozmístění
Materiály 2 1 Pojiva pro výrobu netkaných textilií Pojivo je jednou ze dvou základních složek pojených textilií. Forma pojiva a jeho vlastnosti předurčují technologii a podmínky procesu pojení způsob rozmístění
HOŘENÍ A VÝBUCH. Ing. Hana Věžníková, Ph. D.
 HOŘENÍ A VÝBUCH Ing. Hana Věžníková, Ph. D. 1 HOŘENÍ A VÝBUCH Definice hoření Vysvětlení procesu hoření Základní podmínky pro hoření Co jsou hořlavé látky (hořlaviny) a jak je lze klasifikovat Chemické
HOŘENÍ A VÝBUCH Ing. Hana Věžníková, Ph. D. 1 HOŘENÍ A VÝBUCH Definice hoření Vysvětlení procesu hoření Základní podmínky pro hoření Co jsou hořlavé látky (hořlaviny) a jak je lze klasifikovat Chemické
Klasifikace chem. reakcí
 Chemické reakce Chemické reakce Chemická reakce spočívá ve vzájemné interakci základních stavebních částic výchozích látek (atomů, molekul, iontů), vedoucí ke spojování, oddělování či přeskupování atomových
Chemické reakce Chemické reakce Chemická reakce spočívá ve vzájemné interakci základních stavebních částic výchozích látek (atomů, molekul, iontů), vedoucí ke spojování, oddělování či přeskupování atomových
Vyučovací předmět: chemie. Ročník: 1. ročník + kvinta
 Vyučovací předmět: chemie Ročník: 1. ročník + kvinta Očekávaný výstup žák Školní výstup žák Učivo OBECNÁ CHEMIE využívá odbornou terminologii při popisu látek a vysvětlování chemických dějů provádí chemické
Vyučovací předmět: chemie Ročník: 1. ročník + kvinta Očekávaný výstup žák Školní výstup žák Učivo OBECNÁ CHEMIE využívá odbornou terminologii při popisu látek a vysvětlování chemických dějů provádí chemické
o Řetězové polymerizace o Stupňovité polymerizace Základní typy polymerizací
 Vznik makromolekuly Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité polymerizace polykondenzace
Vznik makromolekuly Základní typy polymerizací o Řetězové polymerizace radikálové iontové: aniontové, kationtové polymerizace za otevření kruhu koordinační polymerizace o Stupňovité polymerizace polykondenzace
Reakce alkanů 75. mechanismem), iniciované světlem nebo radikálovými iniciátory: Oxidace kyslíkem, hoření, tvorba hydroperoxidů.
 eakce alkanů 75 5. eakce alkanů Alkany poskytují především radikálové reakce (často probíhající řetězovým mechanismem), iniciované světlem nebo radikálovými iniciátory: alogenace pomocí X 2 ; bromaci lze
eakce alkanů 75 5. eakce alkanů Alkany poskytují především radikálové reakce (často probíhající řetězovým mechanismem), iniciované světlem nebo radikálovými iniciátory: alogenace pomocí X 2 ; bromaci lze
2.3 VÝPOČHT SVĚTLOSTI POTRUBÍ Tlakové ztráty při proudění vzduchu potrubím a míslními odpory PtTimčr ootľubi...
 O BSA H OBSAH... 1 SEZNAM ZÁKLADNÍHO POUŽITÉHO OZNAČENÍ VF.LIĆ1N... 6 PŘ ED M LU V A...9 1. ÚVOD... 11 2. FYZIKÁLNÍ VLASTNOSTI VZDUŠIN. VEDENÍ V Z D U ŠIN...14 2.1 F y z i k á l n í v l a s t n o s t i
O BSA H OBSAH... 1 SEZNAM ZÁKLADNÍHO POUŽITÉHO OZNAČENÍ VF.LIĆ1N... 6 PŘ ED M LU V A...9 1. ÚVOD... 11 2. FYZIKÁLNÍ VLASTNOSTI VZDUŠIN. VEDENÍ V Z D U ŠIN...14 2.1 F y z i k á l n í v l a s t n o s t i
Vytvrzování reaktoplastických hybridních systémů. Bc. Vilém Galbavý
 Vytvrzování reaktoplastických hybridních systémů Bc. Vilém Galbavý Diplomová práce 2011 UTB ve Zlíně, Fakulta technologická 2 UTB ve Zlíně, Fakulta technologická 3 UTB ve Zlíně, Fakulta technologická 4
Vytvrzování reaktoplastických hybridních systémů Bc. Vilém Galbavý Diplomová práce 2011 UTB ve Zlíně, Fakulta technologická 2 UTB ve Zlíně, Fakulta technologická 3 UTB ve Zlíně, Fakulta technologická 4
16.IZOMERIE a UHLOVODÍKY 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem liší?
 16.IZOMERIE a UHLOVODÍKY 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem liší? 4) Urči typy konstituční izomerie. 5) Co je tautomerie
16.IZOMERIE a UHLOVODÍKY 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem liší? 4) Urči typy konstituční izomerie. 5) Co je tautomerie
Úvod do koroze. (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají)
 Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Třídění látek. Chemie 1.KŠPA
 Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
