INSPEKCE ODBĚRU TKÁNÍ A BUNĚK A TKÁŇOVÝCH ZAŘÍZENÍ. Operační příručka pro příslušné orgány. Verze 1.0
|
|
|
- Alois Janda
- před 8 lety
- Počet zobrazení:
Transkript
1 EVROPSKÁ KOMISE GENERÁLNÍ ŘEDITELSTVÍ PRO ZDRAVÍ A OCHRANU SPOTŘEBITELE Veřejné zdraví a posouzení rizik Právní předpis v oblasti zdraví a mezinárodní INSPEKCE ODBĚRU TKÁNÍ A BUNĚK A TKÁŇOVÝCH ZAŘÍZENÍ Operační příručka pro příslušné orgány Verze 1.0 Tato operační příručka pro příslušné orgány byla vypracována pouze pro informační účely. Tato příručka nebyla přijata ani schválena Evropskou komisí. Není právně závazná. OBSAH
2 Strana 1.0 Úvod 2.0 Povinnosti inspektorů 3.0 Kvalifikace a školení 3.1 Vzdělání a zkušenost 3.2 Osobní předpoklady 3.3 Vstupní školení 3.4 Odborné školení 3.5 Odborná příprava při zaměstnání 3.6 Oprávnění 4.0 Druhy inspekcí 5.0 Plánování inspekcí 5.1 Stanovení priorit rutinních inspekcí 5.2 Neohlášené inspekce 6.0 Inspekční postupy 6.1 Inspekční postupy před zahájením inspekce 6.2 Inspekční postupy během inspekce Zahajovací schůze Inspekce zařízení Přezkum dokumentace Závěrečná schůze Inspekční poznámky 6.3 Inspekční postupy po ukončení inspekce Zpráva o inspekci a nápravná opatření Akreditace a jmenování tkáňových zařízení a udělení příslušného oprávnění nebo povolení 7.0 Systém inspektorátu zaměřený na řízení jakosti 2
3 7.1 Výkon systému 7.2 Výkon inspektora 7.3 Kvalifikace inspektora Příloha 1 Příloha 2 Příloha 3 Příloha 4 Příloha 5 Příloha 6 Odběr a vyšetření dárce Příjem, zpracování, skladování a distribuce Posouzení postupů přípravy Hodnocení zpráv o posouzení rizik Dovoz/vývoz ověřování technických požadavků Navrhovaný společný formát dokumentace tkáňových zařízení (TED) Příloha 7 Příloha 8 Příloha 9 Navrhovaný formát formuláře pro záznam zjištění inspekcí Navrhovaný společný formát zprávy o inspekci tkáňových zařízení Navrhovaný společný formát dokumentace týkající se postupu přípravy (PPD) Příloha 10 Příloha 11 Příloha 12 Navrhovaný společný formát osvědčení o udělení oprávnění Dokumenty použité při vypracování těchto pokynů Zkratky a glosář 3
4 1.0 Úvod Článek 7 směrnice 2004/23/EC 1 stanoví potřebu provádění inspekcí a kontrolních opatření. Odstavec 5 stanoví, že Aby se dosáhlo jednotné úrovně odborné způsobilosti a plnění povinností, postupem vyjednávání ve výborech se stanoví pokyny o podmínkách inspekce a kontrolních opatření a pokyny pro školení a kvalifikaci úředníků účastnících se těchto činností. Cílem této operační příručky je podpořit členské státy při provádění řady regulačních povinností za účelem dosažení souladu se směrnicemi 2004/23/ES, 2006/17/ES 2 a 2006/86/ES 3. Předmětem příručky jsou následující činnosti: inspekce, akreditace a jmenování tkáňových zařízení a udělení příslušného oprávnění nebo povolení inspekce a schvalování podmínek odběru tkání a buněk; inspekce a udělování příslušného oprávnění pro postupy přípravy tkání a buněk; a inspekce a udělování oprávnění pro dovoz a vývoz. Cílem operační příručky je podpořit členské státy, které zavádějí takové regulační systémy poprvé. Dále je jejím cílem podpora normalizace regulačních systémů, které jsou již osvědčené v Evropské unii. Působnost této operační příručky zahrnuje tři související směrnice o jakosti a bezpečnosti lidských tkání a buněk používaných při transplantaci nebo v rámci asistovaného početí. Jednotlivé části této příručky pojednávají o lidských tkáních a buňkách používaných například jako výchozí materiál pro výrobu léčivých přípravků pro moderní terapii (ATMP) (tj. přípravků pro genovou terapii, přípravků pro somatobuněčnou terapii nebo Směrnice Evropského parlamentu a Rady 2004/23/ES ze dne 31. března 2004 o stanovení jakostních a bezpečnostních norem pro darování, odběr, vyšetřování, zpracování, konzervaci, skladování a distribuci lidských tkání a buněk (Úř. věst L 102, , s. 48). Směrnice Komise 2006/17/ES ze dne 8. února 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o určité technické požadavky na darování, opatřování a vyšetřování lidských tkání a buněk (Úř. věst. L 38, , s. 40). Směrnice Komise ze dne 24. října 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o požadavky na sledovatelnost, oznamování závažných nežádoucích reakcí a účinků a některé technické požadavky na kódování, zpracování, konzervaci, skladování a distribuci lidských tkání a buněk (Úř. věst. L 294, , s. 32). 4
5 přípravků tkáňového inženýrství). V těchto případech se uplatní regulační požadavky stanovené výše uvedenými směrnicemi o darování, odběru a vyšetřování. Nařízení 1394/2007 o léčivých přípravcích pro moderní terapii 4 se použije ode dne 30. prosince Členským státům se doporučuje, aby připravily integrovaný systém za účelem řízení svých regulačních povinností na rozhraní mezi odvětvím tkání/buněk a odvětvím léčiv (např. status místa, postupy při inspekci, postup akreditace a jmenování a udělování příslušného oprávnění nebo povolení, systém sledovatelnosti materiálů a systém kódování). 2.0 Povinnosti inspektorů Inspektoři musí od příslušných orgánů obdržet jasný mandát v písemné podobě k provedení konkrétního úkolu a musí jim být vydány oficiální prostředky identifikace. Inspektoři by měli shromáždit podrobné informace, které budou poskytnuty příslušnému orgánu společně se zvláštním mandátem k provádění inspekce. Inspekce se provádí namátkově, neboť inspektoři nemohou přezkoumat všechny oblasti a dokumentaci během jediné inspekce. Inspektoři nejsou odpovědní za případné nedostatky, které nemohly být zjištěny během inspekce z důvodu omezené časové kapacity nebo omezené oblasti působnosti nebo z toho důvodu, že během inspekce nebylo možné pozorovat některé postupy. 3.0 Kvalifikace a školení 3.1 Vzdělání a zkušenost Inspektoři by měli minimálně: (a) vlastnit diplom, osvědčení nebo jiný doklad formální způsobilosti v oblasti lékařských nebo biologických věd udělený při ukončení vysokoškolského studia nebo studia uznaného dotyčným členským státem za rovnocenné; a (b) mít praktickou zkušenost v příslušných oblastech v rámci tkáňového, buněčného či krevního zařízení. Další předchozí zkušenosti mohou rovněž být považovány za relevantní. Ve výjimečných případech mohou příslušné orgány rozhodnout, že významná zkušenost určité osoby může být důvodem pro její osvobození od požadavku a). 4 Nařízení Evropského parlamentu a Rady (ES) č. 1394/2007 ze dne 13. listopadu 2007 o léčivých přípravcích pro moderní terapii a o změně směrnice 2001/83/ES a nařízení (ES) č. 726/2004 (Úř. věst. L 324, , s. 121). 5
6 Inspektoři by měli mít praktickou zkušenost po ukončení vysokoškolského vzdělání v příslušných oblastech v rámci tkáňového, buněčného či krevního zařízení. Mezi další předchozí zkušenosti, jež lze rovněž považovat za relevantní, patří: příslušná zkušenost ve farmaceutickém průmyslu; zkušenost v oblasti zdravotnictví; nebo regulační pracovní zkušenost v rámci příslušného orgánu, který provádí inspekce krevních zařízení nebo nemocničních krevních bank, tkáňových a buněčných zařízení nebo léčiv. 3.2 Osobní předpoklady Inspektoři by měli mít dobré schopnosti v oblasti mezilidských vztahů. Dále by měli mít dobré komunikační schopnosti, měli by být s to vést efektivní diskuse, rychle chápat složité problémy a jednat asertivně, a zároveň mít odpovídající takt a profesionální přístup. Inspektoři by měli mít vysokou míru osobní bezúhonnosti a vyspělosti, měli by být otevřeni jiným názorům, chápat složité problémy, mít schopnost správného úsudku, jednat asertivně a mít analytické dovednosti, houževnatost a měli by být schopni realistického vnímání situace. 3.3 Vstupní školení Aby mohli noví inspektoři získat pracovní místo na inspektorátu, musí prokázat, že mají kvalifikaci a/nebo zkušenost, která je nezbytná k výkonu jejich funkce. Kromě toho musí být uznáno, že dovednosti vyžadované pro výkon funkce inspektora jsou odborné. Inspektorát proto zajistí vstupní školení, bez ohledu na kvalifikaci či předchozí zkušenost. Vstupní školení by se mělo týkat alespoň následujících témat: činnost tkáňových zařízení (darování, odběr, vyšetřování, zpracování, konzervaci, skladování a distribuci); akreditace a jmenování a udílení příslušného oprávnění nebo povolení v členských státech; směrnice EU o tkáních a buňkách; inspekční techniky a postupy, včetně praktických cvičení; mezinárodní systémy řízení jakosti (ISO a EN); vnitrostátní zdravotní systémy a tkáňové a buněčné organizace v členských státech; vnitrostátní právní předpisy platné v členských státech; organizace vnitrostátních regulačních orgánů; mezinárodní inspekční nástroje a další příslušné orgány. Inspektoři by se měli účastnit průběžné odborné přípravy zaměřené na výše uvedená témata, aby byli informováni o případných změnách technických a právních předpisů. 3.4 Odborné školení Jak je uvedeno výše, inspektoři by obecně měli mít celou řadu dovedností získaných ve vzdělávacích institucích, na odborných školeních, v rámci předchozí pracovní zkušenosti a/nebo během další odborné přípravy. Není nicméně pravděpodobné, že by inspektoři měli stejnou úroveň znalostí ve všech oblastech týkajících se tkání a buněk. Měl by být zaveden postup provádění analýzy školicích potřeb pro nové zaměstnance a stávající 6
7 pracovníky, aby se zajistilo, že inspektoři budou provádět inspekce v souladu se standardními požadavky. Mezi důležitá témata, u nichž mohou inspektoři vyžadovat odborné školení, patří: obecné zásady transplantace tkání a buněk; základní znalost postupů a vybavení používaných v tkáňových zařízeních; základní zásady lékařsky asistovaných reprodukčních technologií (MART); základní znalost nařízení o zdravotnických prostředcích; základní znalost farmaceutických právních předpisů (zejména nařízení o ATMP); řešení, validace a údržba kritického prostředí a zařízení; systém zpracování a ochrany údajů; Efektivní komunikace, včetně řízení konfliktů; obecná hygiena; identifikace nezákonné či podvodné činnosti a následná akce za účelem jejího potření; laboratorní techniky, diagnostické testy in vitro (screeningové testy a techniky amplifikace nukleových kyselin); řízení rizik; konkrétní vnitrostátní pokyny/požadavky; přenosná onemocnění; péče a dohled. Inspektoři by se měli účastnit průběžné odborné přípravy zaměřené na výše uvedená témata, aby byli informováni o případných změnách technických a právních předpisů. 3.5 Odborná příprava při zaměstnání Program odborné přípravy při zaměstnání by měl zahrnovat určitý počet (stanovený inspektorátem) inspekcí za účasti svědků. Inspektoři uchazeči o odbornou přípravu musí nejdříve doprovázet schváleného inspektora na několika inspekcích, poté musí provést řadu inspekcí sami a nakonec musí provést několik inspekcí pod dohledem schváleného inspektora. 3.6 Oprávnění Dříve než je uchazečům o odbornou přípravu uděleno oprávnění k provádění inspekcí jejich schopnosti musí být potvrzeny a zdokumentovány CA. Výkon a schopnosti inspektorů by měly být pravidelně ověřovány ve světle požadavků systému jakosti používaného příslušným orgánem/inspektorátem. 4.0 Druhy inspekcí V závislosti na činnosti tkáňových zařízení a zúčastněných třetích stran lze provádět různé druhy inspekcí. Inspekce mohou být na místě nebo administrativní. Mohou se vztahovat na celý systém nebo mohou být zaměřeny na jedno či několik specifických témat (systémy jakosti, zpracování specifických tkání či buněk, specifický postup přípravy nebo zvláštní problém atd.). 7
8 Všeobecné inspekce zaměřené na systém by měly být prováděny na místě a měly by se vztahovat na všechny postupy a činnosti, včetně organizační struktury, politik, povinností, řízení jakosti, pracovníků, dokumentace, zařízení, vybavení, smluv, stížností, stažení z distribuce, auditů atd. Inspekce by měly být prováděny alespoň jednou za čtyři roky činnosti. Inspekce by měly být prováděny dříve než je tkáňové zařízení akreditováno, jmenováno nebo obdrželo oprávnění nebo povolení. (Nicméně akreditace/jmenování/oprávnění/povolení mohou být případně založeny na přezkumu dokumentu.) Tyto inspekce mohou být nezbytné v případě jakýchkoli výraznějších odchylek od původní akreditace, jmenování, oprávnění nebo povolení (např. změna činnosti nebo postupu přípravy). Provedení těchto inspekcí může být rovněž zapotřebí v případě existence historie nedostatků (např. závažných nežádoucích účinků (SAE) a závažných nežádoucích reakcí (SAR)). Tematické inspekce by měly být prováděny na místě a vztahují se na jedno či několik specifických témat, jako jsou systémy řízení jakosti, zpracování specifických tkání či buněk, specifické postupy přípravy atd. Jsou prováděny: v době průběžného hodnocení mezi dvěma všeobecnými inspekcemi zaměřenými na systém; pokud jsou postupy přípravy v rámci tkáňového zařízení nové, složité, inovační či jedinečné; kdykoli je u některého ze specifických témat nahlášena významná změna; eventuálně v případě existence (historie) specifických nedostatků (např. SAE or SAR). Administrativní přezkumy nejsou prováděny na místě, ale na odlehlém místě. Mohou se vztahovat na všechny postupy a činnosti nebo být zaměřeny na jedno či několik specifických témat. Budou založeny na aktuální dokumentaci tkáňového zařízení (TED). Lze je využívat v následujících situacích: k provedení počátečního hodnocení činností tkáňových zařízení; v rámci přípravy na inspekce na místě; v době průběžného hodnocení mezi dvěma všeobecnými inspekcemi zaměřenými na systém, pokud nedošlo k žádným významným změnám. Opětovné inspekce mohou být nezbytné k provádění průběžného hodnocení nebo opětovného posouzení za účelem monitorování nápravných opatření, jejichž přijetí bylo požadováno na základě předchozí inspekce. Lze rovněž provádět další specifické inspekce: Inspekce laboratoří provádějících vyšetření dárců: Součástí těchto inspekcí je obvykle hodnocení dodržování správné laboratorní praxe týkající se kontroly jakosti. 8
9 Inspekce mohu být prováděny příslušným orgánem jiným než příslušný orgán odpovědný za provádění inspekce tkáňových zařízení, v závislosti na situaci v každém členském státě. Mohly by být nicméně součástí všeobecné inspekce zaměřené na systém nebo tematické inspekce v případě, že je zkušební laboratoř součástí tkáňového zařízení. Inspekce třetích stran: Příslušné orgány by měly provádět inspekce na místě u třetích stran zejména v případě, kdy posouzení rizik svědčí o tom, že je to vhodné. Možnost provedení inspekce třetích stran by měla být zvážena například v následujících situacích: v případě, že třetí strany jednají jako dodavatelé kritických služeb významnému počtu tkáňových zařízení, např. obchodní zařízení zabývající se zpracováním tkání, centralizované organizace provádějící výběr dárce tkáně a/nebo organizace provádějící odběr nebo smluvní sterilizační společnosti. v případě, že třetí strany jednají jako dodavatelé kritických služeb jedinému tkáňovému zařízení, avšak toto zařízení dodává velký počet tkání či buněk. v případě, že je v rámci inspekce tkáňových zařízení odhalena vysoká míra neplnění písemné dohody třetí stranou. Společné inspekce: Zvláštní okolnosti, včetně omezených zdrojů či odborných znalostí, mohou vést členský stát ke zvážení možnosti požádat příslušný orgán jiného členského státu EU o provedení společných inspekcí na svém území ve spolupráci s úředníky žádajícího členského státu. 5.0 Plánování inspekcí Příslušné orgány by měly plánovat sled inspekcí předem. Měly by navrhnout program a zajistit, aby frekvence inspekcí jednotlivých tkáňových zařízení byla dodržena podle plánu. Měly by být k dispozici dostatečné zdroje, které umožní provedení stanoveného programu inspekcí náležitým způsobem. Směrnice 2004/23/ES stanoví, že inspekce v tkáňových zařízeních budou prováděny alespoň každé dva roky. Obsahuje doporučení, aby všeobecná inspekce zaměřená na systém, která zahrnuje všechny oblasti činnosti, byla prováděna alespoň jednou za čtyři roky. V době mezi dvěma všeobecnými inspekcemi zaměřenými na systém lze provést tematickou inspekci, která je zaměřena na konkrétní téma nebo postup (týkající se například dříve nahlášených nedostatků nebo nových činností). Kromě toho lze provést administrativní přezkum, pokud od poslední inspekce na místě nedošlo k žádným významným změnám. 5.1 Stanovení priorit inspekcí Inspekce by měly být naplánovány v souladu s dokumentovanými kritérii založenými na posouzení rizik. U rutinních inspekcí by kritéria plánování měla být vázána na následující ukazatele: 9
10 složitost operací v daném místě; dodržování platných nařízení (jak je uvedeno ve vyplněné dokumentaci tkáňových zařízení); prokázání dosavadních výsledků (např. počet nedostatků odhalených v rámci předchozí inspekce); počet nahlášených případů závažných nežádoucích účinků/reakcí nebo případů nařízeného stažení z distribuce; rozsah činnosti, včetně významných změn. 5.2 Neohlášené inspekce Inspekce mohou být prováděny bez předchozího předběžného oznámení tkáňovému zařízení, jestliže existuje důkaz nebo informace odůvodňující takový krok. Kritéria pro provádění takových neohlášených inspekcí by mohla zahrnovat podezření z nezákonné či podvodné činnosti, závažná porušení zákonných požadavků, jež mohou vystavit dárce nebo příjemce riziku, závažná nežádoucí reakce, která má za následek smrt pacienta nebo závažné případy stažení produktu atd. 6.0 Inspekční postupy Tato část obsahuje obecné pokyny týkající se postupů u všech druhů inspekcí. Příloha 1 až 5 obsahuje technické pokyny týkající se způsobu ověřování plnění specifických technických požadavků, pokud jde o: odběr tkání a buněk a vyšetřování dárců (příloha 1); příjem, zpracování, skladování a distribuce (příloha 2); posouzení postupů přípravy (příloha 3); hodnocení zpráv o posouzení rizik (příloha 4) a dovoz/vývoz (příloha 5). 6.1 Inspekční postupy před zahájením inspekce Mělo by být přijato rozhodnutí o členství týmu, přičemž je třeba vzít v úvahu druh inspekce. Inspekce mohou být prováděny jediným inspektorem, pokud z posouzení rizik provedených příslušnými orgány před zahájením inspekce vyplývá, že je vhodné provést v dotčeném tkáňovém zařízení inspekci jedinou osobou. Nicméně obecně platí, že inspekce jedinou osobou by neměly být prováděny. Pokud to finanční prostředky umožňují, tým by měl být složen ze členů s různými odbornými znalostmi. Alespoň jeden z inspektorů by měl mít úroveň způsobilosti a stupeň vzdělání požadovaný článkem 17 směrnice 2004/23/ES u osoby odpovědné za tkáňové zařízení nebo mít odpovídající vzdělání a ukončené školení, aby byl schopen provádět inspekce. Pokud je to třeba, inspektoři mohou požádat o pomoc technického odborníka (např. v oblasti technologie kmenových buněk nebo lékařsky asistované reprodukční technologie) nebo další odborníky (např. v oblasti práva či lékařství) za účelem provedení zvláštní inspekce. Odborníci by měli mít odborné znalosti v oblasti, která je předmětem inspekce. Úloha odborníků nespočívá v provádění inspekce, ale v poskytování poradenství inspektorům ohledně technických záležitostí. Úlohu odborníků v týmu je třeba jasně stanovit v oficiálních dokumentech, dohodě o důvěrnosti opatřené podpisy odborníků a jejich prohlášení o neexistenci střetu zájmů. Odborníci by měli být informováni o politice inspektorátu týkající se provádění inspekcí. 10
11 Před zahájením inspekce by se tým měl seznámit s organizací, která bude předmětem inspekce. Tento proces by měl zahrnovat alespoň: přezkum dokumentace tkáňového zařízení (TED) za účelem ověření současného stavu s ohledem na směrnice EU o tkáních a buňkách a veškeré další relevantní vnitrostátní předpisy; přezkum dokumentace týkající se postupu přípravy (PPD); přezkum případných zpráv předchozích inspekcí; přezkum případných rozdílů (změn) s ohledem na udělení povolení tkáňovému zařízení; případné zvláštní požadavky na oděvy/vakcinaci, jejichž splnění je třeba ke vstupu do tkáňového zařízení; přezkum případných následných opatření přijatých v reakci na předchozí inspekce; přezkum případů stažení tkání či buněk zahájených po ukončení předchozí inspekce, existují-li; přezkum relevantních závažných nežádoucích účinků (SAE) nebo závažných nežádoucích reakcí (SAR) oznámených po skončení předchozí inspekce, existujíli; přezkum veškerých vnitrostátních norem či pokynů vztahujících se na místo, které má být předmětem inspekce; rozsah činnosti, včetně významných změn. Plán inspekce může být vypracován výslovně pro účely inspekce, která má být provedena. Měl by obsahovat veškeré záležitosti zkoumané v rámci předběžné inspekce, které vyžadují provedení zvláštního šetření během inspekce, a upozornit na všechny relevantní záležitosti zaznamenané v rámci přezkumu TED, aby bylo zajištěno, že budou předmětem diskuse a posouzení během inspekce. Doporučenou praxí je informovat předem organizaci, v níž bude prováděna inspekce, o: cílech a rozsahu inspekce ve světle předchozích inspekcí, včetně inspekce zařízení provádějících odběr v odůvodněných případech. osobách, jejichž přítomnost je vyžadována během inspekce; v případech, kdy jsou předmětem inspekce konkrétní postupy, by měly být přítomny osoby za ně přímo odpovědné. totožnosti členů inspekčního týmu a jejich konkrétní úloha; době a místě inspekce (datum, čas a místo); organizačních jednotkách, v nichž bude prováděna inspekce; odhadovaném času a trvání u každé významnější inspekční činnosti (prostory, postupy atd.); přehledu hlavní dokumentace, která by měla být k dispozici pro přezkum během inspekce; časovém harmonogramu zahajovací a závěrečné schůze; přibližném harmonogramu předání písemné zprávy o inspekci; možnosti sdílení výsledků inspekce s dalšími regulačními orgány v tomtéž nebo jiném příslušném orgánu, pokud je to důležité. 6.2 Inspekční postupy během inspekce 11
12 Inspektoři by měli usilovat o vytvoření konstruktivní atmosféry během inspekce. Měli by si být vědomi svého vlivu na rozhodovací procesy. Měli by odpovědět na dotazy, avšak neměli by na sebe brát úlohu konzultanta. Úloha inspektorů nicméně není omezena výhradně na odhalování chyb, nedostatků a nesrovnalostí; jejich úkolem je rovněž doprovázet případné nálezy poučnými a motivačními připomínkami. Inspekce mohou narušit obvyklé rozvržení práce v kontrolované organizaci. Inspektoři by proto měli dbát na to, aby nevystavili tkáně či buňky riziku, a měli by svou činnost provádět pečlivě a plánovitě. Inspektoři budou mít přístup k důvěrným informacím. S těmito informacemi musí nakládat způsobem, jenž zajistí zachování jejich integrity a soulad se zákonnými požadavky na ochranu důvěrnosti a zveřejnění s ohledem na ochranu veřejného zdraví. V některých případech si inspektoři mohou vyžádat kopie dokumentů, které mohou být užitečné pro vypracování zprávy o počáteční inspekci nebo jako důkaz konkrétních nálezů. V některých členských státech je inspektorům povoleno pořizovat fotografie nebo videozáznamy pro účely zajištění důkazů z kontrolovaných míst, pokud se tím nenaruší inspekční postup nebo jakost a bezpečnost tkání a buněk Zahajovací schůze Inspekce by měly být zahájeny zahajovací schůzí, na níž by se obvykle inspekční tým měl setkat s vedoucími pracovníky a klíčovými zaměstnanci organizace, včetně odpovědné osoby. Účelem této schůze je seznámení s týmem a případnými úředníky či odborníky, kteří tento tým doprovázejí, a prodiskutovat plán inspekce (v němž mohou být provedeny neohlášené změny). Během zahajovací schůze by inspekční tým měl: nastínit účel a rozsah inspekce; přezkoumat strukturu řízení organizace (organizační schéma); určit dokumenty, které mohou být vyžadovány během inspekce v závislosti na činnostech/oblastech, na něž se inspektoři zaměřují, ačkoli by v této fázi měly být k dispozici veškeré dokumenty; potvrdit, že veškeré informace budou považovány za důvěrné; vysvětlit, zda nedostatky budou oznámeny, jakmile jsou odhaleny, nebo na schůzích na konci každého dne, kde se oznámí souhrnné výsledky, nebo až na poslední závěrečné schůzi. Tkáňové zařízení by mělo být na požádaní s to: popsat systém řízení jakosti; vysvětlit organizační strukturu a pracovní postupy; vysvětlit každý jednotlivý krok od odběru po zpracování a distribuci; vysvětlit významné změny týkající se zařízení, vybavení, postupů a zaměstnanců, k nimž došlo od provedení poslední inspekce; vysvětlit, jak byly napraveny nedostatky, pokud tato informace již nebyla poskytnuta příslušnému orgánu; určit osoby, které budou doprovázet inspekční tým během inspekce; přidělit inspektorům místnost, je-li to třeba; pokud je inspekce prováděna týmem, bude zapotřebí samostatná místnost pro účely zasedání týmu. 12
13 Krátká návštěva místa bezprostředně po zahajovací schůzi by mohla být užitečná pro získání přehledu o místě a případných významných změnách, ke kterým došlo od předchozí inspekce. Tato návštěva by neměla nahrazovat důkladnou návštěvu zařízení uskutečněnou později v rámci inspekce. V některých případech může být v této fázi nezbytné sledovat určité činnosti, které v době provádění inspekce na daném místě nebudou vykonávány Inspekce zařízení V rámci inspekce by měla být provedena krátká návštěva za účelem zjištění, zda je konstrukce zařízení a vybavení vyhovující a v souladu s popisem v dokumentaci tkáňového zařízení a zda jsou využívány způsobem, jenž odpovídá zamýšleným operacím. Měly by být přezkoumány veškeré změny, k nimž došlo od poslední inspekce. Inspektoři obvykle sledují tok činností, pro jejichž provádění je (či bude) tkáňovému zařízení uděleno povolení, přičemž se zohlední podrobná ustanovení směrnic 2004/23/ES, 2006/17/ES a 2006/86/ES. Někdy je vhodné soustředit se na jediný útvar v rámci organizace, pokud jsou zde zvláštní problémy nebo požadavky. Předmětem pozornosti by měly být příslušné obslužné prostory, např. vodní, parní či větrací systémy a podpora inženýrství. Během návštěvy zařízení by inspektoři měli aktivně diskutovat o pozorovaných aspektech s klíčovými zaměstnanci, odpovědnými pracovníky a provozovateli za účelem zjištění skutečností, vymezení problematických oblastí a posouzení znalostí zaměstnanců Přehled dokumentace Měl by být zkontrolován systém dokumentace, včetně specifikací, pokyny týkající se přípravných postupů, přepravy a balení, postupy a záznamy týkající se různých procesů, kontroly jakosti a distribuce, a to na základě přezkumu vybraných vzorků jak ve fázi používání, tak ve fázi, kdy se staly součástí úplných záznamů. Všeobecná inspekce zaměřená na systém bude obvykle zahrnovat přezkum dokumentovaného systému řízení jakosti u činností, pro něž bylo oprávnění buď již uděleno, nebo je požadováno, včetně následujícího orientačního seznamu: popis práce, organizační schéma, úloha odpovědné osoby a určeného lékaře 5 ; školení zaměstnanců, včetně základního/vstupního školení, rekvalifikační plány a posouzení odborné způsobilosti; kontrola dokumentů včetně zachování (např. kontrola změn) standardních pracovních postupů (SOP); validace (postupy) a kvalifikace (vybavení a zařízení); preventivní programy údržby (vybavení a zařízení); sledování podmínek kontroly sterility a kvality vzduchu; kritéria výběru dodavatelů, pokud existují; uzavírání smluv mezi třetí stranou a dodavatelem; systém vnitřního auditu, vnitřní inspekce a preventivní a nápravná opatření; 5 Každé tkáňové zařízení musí mít přístup k určenému lékaři, jenž mu bude poskytovat poradenství a dohlížet na jeho lékařské činnosti, jako je výběr dárců, přezkoumání klinických výstupů použitých tkání a buněk nebo podle potřeby interakce s klinickými uživateli. 13
14 řízení procesu vyřazení, skladování a zničení materiálu dárce v případech, že není vhodný pro použití u člověka; správa stížností, nesoulad, závažné nežádoucí reakce (SAR), závažné nežádoucí účinky (SAE), plány stažení a pohotovostní plány pro ukončení činností; sledovatelnost, nakládání s údaji a důvěrnost; dovoz/vývoz; vedení záznamů: výroční zpráva o činnostech a výroční zpráva o vigilanci. S odpovědnou osobou by měl být veden pohovor a měl by být vypracováno kritické hodnocení její funkce. Měly by být jasně vymezeny smluvní činnosti a povinnosti různých účastníků. Měl by být přezkoumán soulad smluv s vnitrostátními předpisy, které provádějí směrnice 2004/23/ES, 2006/17/ES a 2006/86/ES. Během inspekce by měl být přezkoumán postup zaznamenávání a přezkumu SAE a SAR a systém pro stažení tkání a buněk z distribuce v členských státech i mimo ně. Je třeba přezkoumat a projednat všechny zprávy o SAR a SAE. Měl by být přezkoumán systém provádění vnitřních inspekcí v organizaci. Ačkoli se nepředpokládá, že inspektoři budou běžně číst samotné zprávy, přezkum harmonogramu auditů/vnitřních inspekcí uskutečněných v minulém roce může být užitečný pro potvrzení uspokojivého provedení auditů. Poté může následovat kontrola záznamů o preventivních a nápravných opatřeních vypracovaných v době, kdy byly provedeny audity/vnitřní inspekce za účelem zajištění toho, že byla přijata vhodná opatření. Měly by být přezkoumány postupy kontroly dovozu či vývozu tkání a buněk (v relevantních případech) a zkontrolována dokumentace týkající se jednotlivých případů. Technické pokyny týkající se inspekce dovozu a vývozu jsou uvedeny v příloze 5. Tematické inspekce budou zahrnovat přezkum dokumentace související s dotyčným tématem. Inspekce zaměřené na postupy budou zahrnovat přezkum specifické dokumentace související s jedním či několika ukončenými či neukončenými postupy přípravy specifických tkání či buněk, včetně: souladu s dokumentací týkající se postupu přípravy (viz příloha 9); sledovatelnosti (včetně zavedeného dárcovského a tkáňového/buněčného systému kódování); postupu validace; zpracování instrukcí a záznamů; postupů pro vydávání údajů; specifikací a údajů týkajících se kontroly jakosti u výchozích materiálů, meziproduktů a hotových tkání a buněk, dalších materiálů, činidel a technických zařízení; balení a označování; distribuce. 14
15 6.2.4 Závěrečná schůze Po ukončení inspekce by inspektoři měli vypracovat seznam zjištění během závěrečné schůze se zástupci organizace obvykle se jedná o odpovědnou osobu, osobu pověřenou správou systému řízení jakosti (v relevantních případech) a případné zaměstnance přizvané odpovědnou osobou. Závěrečná schůze představuje významnou součást inspekce. Nedostatky pozorované během inspekce by měly být jasně popsány a jestliže to vyžadují standardní pracovní postupy příslušného orgánu písemně oznámeny organizaci. Navrhovaný standardní formát je uveden v příloze 7. Mělo by být provedeno ústní hodnocení závažnosti zaznamenaných nedostatků. Během této schůze by měly být uvedeny skutečnosti a objektivní důkazy, které podporují učiněná pozorování, zejména pokud jde o hlavní či kritická zjištění. Organizace může případně projednat první návrhy týkající se nápravných opatření. Na této schůzi by měla být pokud možno nahlášena veškerá relevantní zjištění, aby dotyčná organizace mohla co nejdříve přijmout potřebná nápravná opatření. Nedostatky by měly být hlášeny se zřetelem na vnitrostátní právní předpisy, které provádí tři směrnice EU o tkáních a buňkách. V případě kritických nedostatků, které představují riziko pro zdraví a bezpečnost dárců a příjemců tkání a buněk, inspektorát deleguje své pravomoci na inspektory, kteří požádají o okamžitou karanténu a/nebo zastavení dodávek a je-li to třeba stažení lidských tkání či buněk z distribuce. V takových zvláštních případech musí být dodržovány standardní pracovní postupy příslušného orgánu Inspekční poznámky Zprávy o inspekci by měly být založeny na poznámkách učiněných během inspekce. S těmito poznámkami by mělo být nakládáno v souladu s postupy stanovenými příslušným orgánem. Formulář, který by mohl sloužit k zaznamenávání zjištění učiněných v rámci inspekce, je obsažen v příloze Inspekční postupy po ukončení inspekce Zpráva o inspekci a nápravná opatření Písemná zpráva o inspekci by měla obsahovat obecné informace o tkáňovém zařízení, popis inspekce a pozorování a závěry z nich vyplývající. Zpráva by rovněž měla obsahovat odkaz na dokumentaci tkáňového zařízení (TED) společně s případnými opravami TED zaznamenanými během inspekce. Navrhovaný standardní formát zprávy je uveden v příloze 8. Její součástí je standardní klasifikace nedostatků. Zjištění učiněná během inspekce mohou být z této zprávy vyňata a zaslána tkáňovému zařízení dopisem, nebo lze tkáňovému zařízení zaslat celou zprávu, v závislosti na vnitřních postupech příslušného orgánu. Závěry zprávy by měly jasně identifikovat nedostatky a klasifikovat je jako kritické, hlavní a jiné (na základě definic uvedených v příloze 8). To se obvykle provádí na inspektorátu za účelem zajištění souladu s dalšími inspekcemi. Mělo by být stanoveno datum, dokdy musí tkáňové zařízení předložit návrhy a harmonogram, pokud jde o nápravu nedostatků uvedených ve zprávě (akční plán). Inspektoři by měli navrhovaný akční plán zhodnotit a na jeho základě podat příslušnému schvalujícímu orgánu doporučení v souladu se zvláštním mandátem inspekce, přičemž jasně uvedou, zda je tkáňové zařízení v souladu s vnitrostátními právními předpisy, které provádí směrnice 2004/23/ES, 2006/17/ES a 2006/86/ES, či nikoli. Tkáňové zařízení by mělo být písemně informováno o přijatém rozhodnutí. 15
16 V některých případech inspekční tým může považovat za nezbytné vykonání návštěvy druhého místa (opětovná inspekce) nebo si může před vydáním doporučení vyžádat doplňující informace o nápravných opatřeních. Opatření přijatá příslušným orgánem budou záviset na povaze a rozsahu nedostatků a přiměřenosti nápravného akčního plánu ve světle směrnic EU a značných znalostí příslušného orgánu o postupech existujících ve všech druzích tkáňových zařízení Akreditace a jmenování tkáňových zařízení a udělení příslušného oprávnění nebo povolení Článek 6 směrnice 2004/23/ES stanoví, že tkáňová zařízení musí být akreditována, jmenována nebo obdržet oprávnění nebo povolení od příslušného orgánu pro činnosti, které provádějí. Návrh formátu osvědčení o autorizaci založeného na ustanoveních směrnic 2004/23/ES, 2006/17/ES a 2006/86/ES je obsažen v příloze 10. Tento formát by mohl usnadnit zavedení veřejného registru příslušného orgánu pro tkáňová zařízení podle směrnice 2004/23/ES (článek 10) a sítě propojující národní registry tkáňových zařízení, jak stanoví čl. 10 odst. 3. Navrhovaný formát zahrnuje pouze základní informace, které musí být vždy obsaženy v osvědčení a registru příslušného orgánu schválených tkáňových zařízení. Lze doplnit další informace v závislosti na vlastních požadavcích příslušného orgánu. Tyto informace nebudou uveřejněny ve veřejném registru, ale budou součástí národního registru spravovaného příslušným orgánem. Tento formát lze použít bez ohledu na to, zda příslušný orgán využívá pro účely první akreditace, jmenování, oprávnění nebo povolení inspekce na místě, či nikoli. Jakýkoli příslušný orgán by měl na žádost jiného příslušného orgánu poskytnout kopii osvědčení o autorizaci uděleného tkáňovému zařízení. 16
17 Obrázek 1: Inspekční postupy Zahájení inspekce jmenování vedoucího inspekčního týmu stanovení cílů, rozsahu a kritérií inspekce stanovení proveditelnosti inspekce volba inspekčního týmu vyrozumění zařízení, které má být předmětem inspekce Provádění přezkumu dokumentů přezkum dokumentace tkáňového zařízení (TED) určení přiměřenosti s ohledem na inspekční kritéria příprava plánu inspekce svěření úkolů inspekčnímu týmu příprava pracovních dokumentů Příprava inspekce na místě Provádění inspekce na místě průběh zahajovací schůze komunikace během inspekce přijímání rozhodnutí o úkolech a povinnostech průvodců a pozorovatelů shromažďování a ověřování informací zjišťování v rámci inspekce příprava závěrů inspekce průběh závěrečné schůze Příprava, schvalování a distribuce zprávy o inspekci příprava zprávy o inspekci schvalování a distribuce zprávy o inspekci s klasifikovanými nedostatky navržení akčního plánu (kontrolovaným zařízením) hodnocení akčního plánu podávání doporučení příslušnému orgánu, pokud jde o udělování oprávnění, povolení a akreditaci Kroky navazující na inspekci 17
18 7.0 Systém inspektorátu zaměřený na řízení jakosti Všechny příslušné orgány by měly mít zavedený systém řízení jakosti zahrnující odpovídající standardní pracovní postupy a příslušný systém vnitřního auditu. Tyto orgány by měly provádět pravidelné hodnocení svých inspekčních systémů ve světle stanovených postupů. Seznam informací, které mohou být užitečné pro vývoj systému řízení jakosti, je uveden níže. 7.1 Výkon systému Každý příslušný orgán vyhotoví svůj vlastní orientační seznam. Pravidelné hodnocení by mělo být prováděno minimálně u následujících ukazatelů výkonu; počet inspekcí za rok; počet středisek, která jsou každoročně akreditována, pověřena nebo jimž je uděleno oprávnění nebo povolení; průměrná doba od provedení inspekce do vydání závěrečné zprávy; počet zhodnocených postupů za rok; počet schválených postupů za rok; průměrná doba od podání žádosti o udělení oprávnění pro postup do vydání závěrečné zprávy; srovnání výsledků následných inspekcí. 7.2 Výkon inspektora Inspektoři a odborníci je-li využito jejich služeb by měli být podrobeni každoročnímu přezkumu výkonu, který by měl zahrnovat určení školicích potřeb. Příkladem lze uvést následující klíčové ukazatele výkonu, které by měly být pravidelně přezkoumávány: počet inspekcí provedených každoročně každým inspektorem; počet středisek, která jsou každoročně akreditována, pověřena nebo jimž je uděleno oprávnění nebo povolení každým inspektorem (v relevantních případech); průměrná doba, kterou každý z inspektorů potřebuje od vykonání inspekce do vydání závěrečné zprávy; počet postupů každoročně zhodnocených (v relevantních případech) každým inspektorem; počet postupů každoročně schválených (v relevantních případech) každým inspektorem; 7.3 Dovednosti inspektora Systém by měl zahrnovat pravidelné hodnocení, např. vedoucími či odbornými inspektory, kteří jsou pozorovateli inspekcí, za účelem posouzení dovedností inspektora v následujících oblastech: rozsah a důkladnost inspekce; schopnost rozpoznat nedostatky; posouzení závažnosti nedostatků; doporučená opatření; 18
19 účinnost akce, o jejímž provádění bylo rozhodnuto. Poznámka: Tyto ukazatele by měly být přizpůsobeny druhu, velikosti a složitosti kontrolovaného tkáňového zařízení. 19
20 Příloha 1: Odběr a vyšetření dárce Odběr Inspektoři musí zkontrolovat, zda organizace provádějící odběr splňuje požadavky uvedené ve směrnici 2006/17/ES a prováděcí opatření členského státu. Postupy darování a odběru lze ověřit: buď nepřímo provedením auditu těchto služeb v tkáňových zařízeních; nebo přímo prostřednictvím zvláštní inspekce na místě v organizaci, kde jsou tyto činnosti vykonávány. Pro ověření plnění těchto požadavků se doporučuje použití těchto metod: Přezkum dokumentů Organizační schéma popis práce, kvalifikace a způsobilost určeného lékaře a kvalifikace a školení zaměstnanců; schvalování a akreditace podmínek odběru (pokud autorizací není pověřen příslušný orgán); záznamy o dárcích: SOP a záznamy; postup odběru: SOP a záznamy; SOP pro ověřování totožnosti dárce; SOP pro posuzování kritérií výběru u zemřelých dárců (s fungujícím i nefungujícím srdcem) a žijících dárců; SOP pro získání vzorků krve za účelem sérologického vyšetřování dárců a/nebo vyšetřování dárců za pomoci NAT, identifikace vzorků a zacházení s nimi a validace a posouzení laboratorních testů. v relevantních případech SOP související s balením, označováním a přepravou; systém sledovatelnosti (např. kódování odebraných tkání a buněk); průvodní dokumenty ke tkáním či buňkám určených pro tkáňová zařízení; SOP pro řízení SAE a SAR. Pohovory se zaměstnanci Účelem pohovorů s vybranými zaměstnanci je posoudit jejich znalosti a povědomí o postupech a přiměřenost zajišťovaného školení. Pozorování a šetření Inspektoři by měli zkontrolovat, zda výběr a posouzení dárců byly provedeny vyškolenými zaměstnanci v souladu s SOP a podrobně popsány v záznamech. Mělo by se přezkoumat, zda je výběr dárců a screeningové záznamy v souladu s požadavky na totožnosti dárce, souhlas, poskytnuté informace, chorobopis, 20
21 posouzení kritérií výběru a rizika chování, důkladné lékařské vyšetření a výsledky laboratorních testů. Inspektoři by měli ověřit, zda jsou v případě žijících dárců prováděny osobní pohovory v souladu s přílohou I směrnice 2006/17/ES. Inspektoři by měli zkontrolovat, zda jsou v případě zemřelých dárců vedeny záznamy o příčině, době a okolnostech smrti. Měli by rovněž potvrdit, že zahájení odběru tkáně předcházelo splnění vnitrostátních a místních požadavků týkající se potvrzení smrti. Inspektoři by měli náhodně vybrat několik záznamů o dárcích s cílem ověřit, zda tkáňové zařízení splňuje kritéria vyloučení dárce stanovená v příloze I směrnice 2006/17/ES. Tento přezkum by měl potvrdit, že anamnéza chování dárce (důležitá s ohledem na zvýšené riziko přenosu nemocí) byla zkontrolována. Zvláštní pozornost by měla být věnována nádorům, infekcím a rizikovým faktorům u přenosných nemocí. Inspektoři by měli ověřit, zda všechna povinná biologická vyšetření byla provedena v souladu s použitelnými právními předpisy. V případě zemřelých dárců by měly být krevní vzorky odebrány předtím, než nastala smrt, nebo, pokud to není možné, do 24 hodin po smrti. V případě žijících dárců musí být krevní vzorky odebrány v době darování nebo, pokud to není možné, do 7 dnů po darování. Inspektoři by měli zkontrolovat, zda krevní vzorky používané pro vyšetření nejsou zředěny předchozími transfúzemi či infúzemi, které by mohly znehodnotit výsledky vyšetření. Podmínky odběru: Inspektoři by měli přezkoumat, zda je odběr tkání a buněk prováděn ve vhodných místnostech školenými zaměstnanci a zda je používáno kvalifikované vybavení a metody, které jsou podrobně popsány v SOP. Zařízení by mělo disponovat vyhrazeným prostorem pro zemřelé dárce. Inspektoři by měli zkontrolovat, zda jsou dodržovány příslušné postupy a aseptické techniky při dekontaminaci a čištění, jejichž účelem je vyhnout se křížové kontaminaci či zvýšené míře kontaminace. Kdykoli je to možné, je třeba používat nástroje na jednorázové použití. Vybavení a nástroje musí být kvalifikované a mezi jednotlivými odběry je třeba provádět jejich sterilizaci v souladu s validovanou metodou. V případě žijících dárců odběr musí být prováděn v prostředí, které zajišťuje ochranu jejich zdraví, bezpečnost a soukromí. Přeprava: Inspektoři by měli přezkoumat vhodnost prostor, v nichž jsou dočasně skladovány tkáně či buňky, než jsou zaslány a přepraveny do tkáňového zařízení (včetně kontroly teploty). měly by zkontrolovat několik obalových nádob a jejich štítků a posoudit jejich vhodnost. Měli by přezkoumat sterilitu primárního obalu v době používání a zkontrolovat, zda jsou dodržovány podmínky týkající se celistvosti a skladování a/nebo přepravy tkání či buněk. Jestliže inspekce tkáňového zařízení, v němž jsou zpracovávány a distribuovány tkáně a buňky, proběhla před provedením inspekce zařízení/organizace provádějících odběr, mohou inspektoři uskutečnit náhodnou křížovou kontrolu klinických a biologických a jakýchkoli dalších příslušných údajů o dárcích s cílem ověřit soulad se záznamy o dárcích vedenými v tkáňovém zařízení. Záznamy o dárcích: U každého dárce musí být veden záznam s následujícími údaji: 21
22 a) jméno, příjmení a datum narození dárce; pokud se darování týká matky a dítěte (např. pupečníková krev či placenta), uvede se jak jméno a datum narození matky, tak i jméno, pokud je známo, a datum narození dítěte; b) věk, pohlaví, lékařskou anamnézu a anamnézu chování (shromážděné informace musí být dostačující, aby v případě potřeby umožnily použití kritérií pro vyloučení); c) výsledek tělesného vyšetření, kde to je vhodné; d) vzorec hemodiluce, kde to je vhodné; e) formulář souhlasu/oprávnění, kde to je vhodné; f) klinické údaje, výsledky laboratorních vyšetření a výsledky jiných provedených vyšetření; g) pokud byla na zemřelém dárci provedena pitva, musí být výsledky zařazeny do dokumentace (u tkání a buněk, které nelze skladovat delší dobu, musí být zaznamenána předběžná ústní zpráva o pitvě); h) v případě dárců krvetvorných progenitorových buněk musí být doložena vhodnost dárce pro zvoleného příjemce. U nepříbuzenských darování, kde má organizace odpovědná za odběr omezený přístup k údajům příjemce, musí být organizaci provádějící transplantaci poskytnuty údaje o dárci důležité pro potvrzení jeho vhodnosti; i) v případě nepartnerských darování gamet musí být provedena genetická screeningová vyšetření na autosomálně recesivní geny, o kterých je podle mezinárodních vědeckých důkazů známo, že se vyskytují v etnickém prostředí dárce. Rovněž musí být hodnoceno riziko přenosu dědičných předpokladů, o kterých je známo, že se vyskytují v rodině. Dárce musí ke všem vyšetřením dát souhlas; j) v případě žijících dárců je třeba provést posouzení veškerých zdravotních rizik pro ně samotné (např. způsobilost dárce kostní dřeně k obecné anesteziologii, superovulace, podání sedativ nebo rizika spojená s postupem odběru vajíček u dárce vajíček). Záznamy musí být v souladu s právními předpisy o ochraně údajů a musí být čitelné a nesmazatelné. Musí být zavedena opatření k zajištění ochrany údajů a důvěrnosti v souladu s článkem 14 směrnice 2004/23/ES. Zpráva o odběru v případě každého opatření tkání či buněk musí být tkáňovému zařízení předána zpráva o odběru. Tato zpráva musí obsahovat alespoň následující údaje: a) název a adresu tkáňového zařízení, které má přijmout buňky nebo tkáně; b) údaje pro identifikaci dárce (včetně toho, jak a kdo dárce identifikoval) v souladu s použitelnými právními předpisy o ochraně údajů; 22
23 c) popis a identifikaci opatřených tkání a buněk (včetně vzorků k vyšetření, je-li to třeba); d) totožnost osoby, která je odpovědná za provedení odběru, včetně jejího podpisu; e) datum, čas (případně začátek a konec), místo odběru a použité postupy (SOP) včetně veškerých událostí, ke kterým došlo; podmínky prostředí v zařízení pro odběr (popis fyzického prostoru, kde došlo k odběru), pokud je to relevantní; f) datum, čas a jméno osoby, která získala vzorky pro biologická vyšetření; g) u zemřelých dárců podmínky uchování za chladu (ano, či ne) a čas začátku a konce uchování za chladu; h) identifikační čísla/čísla šarže použitých činidel a přepravních roztoků (v relevantních případech); i) v případě zemřelých dárců musí zpráva obsahovat rovněž datum a čas smrti. Pokud je sperma odebráno doma, musí být tato skutečnost uvedena ve zprávě o odběru a zpráva obsahuje pouze: a) název a adresu tkáňového zařízení, které má přijmout buňky/tkáně; b) identifikaci dárce (je-li to třeba); c) podpis dárce potvrzující, že sperma je jeho. Vyšetřování dárců Soulad s požadavky na vyšetřování stanovenými ve směrnici 2006/17/ES by měl být ověřen buď prostřednictvím: inspekcí laboratoří provádějících vyšetření dárců: V případě, že je vyšetřování prováděno mimo tkáňové zařízení nebo organizaci provádějící odběr a příslušný orgán nemá pro provádění inspekce takové laboratoře pravomoc, inspektoři by si měli během všeobecné inspekce zaměřené na systém vyžádat důkaz o tom, že externí laboratoř byla akreditována, jmenována nebo obdržela oprávnění nebo povolení od příslušného orgánu či orgánů k provádění takových vyšetření. Inspektoři provádějící inspekci tkáňových zařízení by měli: o vyžadovat kopii osvědčení o povolení nebo ověřit u ostatních příslušných orgánů, zda bylo vydáno příslušné oprávnění pro provádění screeningových vyšetření dárců tkání a buněk; o požadovat, aby tkáňová zařízení doložila, jakým způsobem kontrolují soulad zkušebních laboratoří se stanovenými požadavky; 23
24 o požadovat, aby tkáňová zařízení doložila, jakým způsobem kontrolují trvalé plnění stanovených požadavků. Během inspekce tkáňových zařízení by měly být přezkoumány prostředky použité k doložení. nebo v rámci všeobecných inspekcí zaměřených na systém, které jsou prováděny v tkáňovém zařízení nebo v organizaci provádějící odběr: Pokud je laboratoř součástí tkáňového zařízení, inspektor by měl: o zkontrolovat, zda je vyšetřování popsané v postupech v souladu s požadavky vnitrostátních předpisů, které provádějí směrnici 2006/17/ES; o přezkoumat, jak je vyšetřování prováděno v praxi, a nahlédnout do reprezentativního počtu záznamů za účelem ověření jejich souladu s vnitrostátními předpisy, které provádějí směrnici 2006/17/ES; o přezkoumat SOP. 24
25 Příloha 2: Příjem, zpracování, skladování a distribuce Příjem: Ověřování kontrol přijímaných tkání a buněk Inspektoři musí zkontrolovat, zda tkáňové zařízení ověřuje, zda jsou přijímané tkáně a buňky v souladu s požadavky uvedenými ve směrnici 2006/17/ES a prováděcími opatřeními členského státu. Systém by měl být přezkoumán v plném rozsahu, přičemž zvláštní pozornost by měla být věnována aspektům uvedeným níže: Pro ověření plnění těchto požadavků se doporučuje použití těchto metod: Přezkum dokumentů souhlas nebo dárce/rodiny; dokumentace o lékařské anamnéze a anamnéze chování dárce; vyšetřování dárců; identifikace dárce a tělesná prohlídka; přezkum anamnézy dárce a propuštění/vyřazení; dokumentace o odběru; označování, balení a přeprava opatřených tkání či buněk; postup odběru tkání a buněk; postup posouzení potencionálních dárců; systém pro zajištění sledovatelnosti při zajištění důvěrnosti; Pohovory se zaměstnanci S osobou odpovědnou za výběr dárce by měl být uskutečněn pohovor. Pokud tato osoba není určeným registrovaným lékařem, měl by být v ideálním případě registrovaný lékař rovněž přítomen. V případě existence samostatné organizace, která hraje významnou úlohu (např. transplantační koordinační úřad), by taková organizace měla rovněž být přizvána k pohovoru. Pozorování a šetření V některých případech může být pro inspektory užitečné uskutečnit křížovou kontrolu informací o odběru shromážděných během inspekce v tkáňovém zařízení prostřednictvím inspekce na místě v zařízení provádějícím odběr. Zpracování Inspektoři musí zkontrolovat, zda tkáňové zařízení splňuje požadavky uvedené ve směrnici 2006/86/ES a prováděcí opatření členského státu. 25
26 Inspektoři musí zkontrolovat, zda jsou informace poskytnuté v TED a PPD přesné a zda jsou používané postupy slučitelné s vybavením a zařízením používaným tkáňovým zařízením. Pro ověření plnění těchto požadavků se doporučuje použití těchto metod: Přezkum dokumentů SOP; záznamy o zpracování; výsledky klasifikace prostor určených pro zpracování (včetně přezkumu listinného důkazu, který podporuje oznamovanou klasifikaci); postupy zajišťující a údaje dokazující trvalý soulad s klasifikací (včetně počítání částic, odběru environmentálních mikrobiálních vzorků a postupů pro vstup do prostoru, včetně postupů oblékání); postupy, které zabraňují vzniku křížové kontaminace; postupy zajišťující omezený přístup a ochranu důvěrných údajů; postupy nahlašování SAE/SAR. Pohovory se zaměstnanci Účelem pohovorů s vybranými zaměstnanci je posoudit jejich znalosti a povědomí o postupech. Pozorování a šetření Inspekce (kontrolovaného) prostoru pro zpracování. Zvláštní pozornost by měla být věnována: o toku zaměstnanců, přijímaným tkáním a buňkám, konečným produktům a odpadu, které se nacházejí v prostoru; o uspořádání, velikost a fungování šaten nacházejících se mezi klasifikovanými prostory; o postupy převlékání, oblékání, mytí rukou atd.; o přiměřenost povrchů, vybavení atd.; pozorování procesu zpracování, je-li to možné; přezkum případných zpráv o závažných nežádoucích účincích či závažných nežádoucích reakcích souvisejících se zpracováním a příslušná nápravná opatření. Skladování a distribuce Inspektoři by měli zkontrolovat, zda tkáňové zařízení splňuje požadavky uvedené ve směrnici 2006/86/ES a prováděcí opatření členského státu. Inspektoři musí zkontrolovat, zda jsou informace uvedené v TED přesné. Pro ověření plnění těchto požadavků se doporučuje použití těchto metod: Přezkum dokumentů SOP pro skladování; 26
KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY
 Požadavky na vstupní materiál lidské tkáně a buňky 1 KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY MUDr. Ivana Koblihová Inspektor lidských tkání a buněk Požadavky na vstupní
Požadavky na vstupní materiál lidské tkáně a buňky 1 KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY MUDr. Ivana Koblihová Inspektor lidských tkání a buněk Požadavky na vstupní
2017 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 2 NOVELA ZÁKONA A VYHLÁŠKY DOVOZ TKÁNÍ A BUNĚK ZE TŘETÍCH ZEMÍ Mgr. Eva Tomková, Ph.D. 3 Obsah Písemná smlouva mezi dovážejícím tkáňovým zařízením a dodavatelem ze třetí země Žádost o povolení dovážejícího
2 NOVELA ZÁKONA A VYHLÁŠKY DOVOZ TKÁNÍ A BUNĚK ZE TŘETÍCH ZEMÍ Mgr. Eva Tomková, Ph.D. 3 Obsah Písemná smlouva mezi dovážejícím tkáňovým zařízením a dodavatelem ze třetí země Žádost o povolení dovážejícího
Zdravotnické laboratoře. MUDr. Marcela Šimečková
 Zdravotnické laboratoře MUDr. Marcela Šimečková Český institut pro akreditaci o.p.s. 14.2.2006 Obsah sdělení Zásady uvedené v ISO/TR 22869- připravené technickou komisí ISO/TC 212 Procesní uspořádání normy
Zdravotnické laboratoře MUDr. Marcela Šimečková Český institut pro akreditaci o.p.s. 14.2.2006 Obsah sdělení Zásady uvedené v ISO/TR 22869- připravené technickou komisí ISO/TC 212 Procesní uspořádání normy
c) příjemcem osoba, která obdržela transfuzi krve nebo krevních
 L 256/32 Úřední věstník Evropské unie 1.10.2005 SMĚRNICE KOMISE 2005/61/ES ze dne 30. září 2005, kterou se provádí směrnice Evropského parlamentu a Rady 2002/98/ES, pokud jde o požadavky na sledovatelnost
L 256/32 Úřední věstník Evropské unie 1.10.2005 SMĚRNICE KOMISE 2005/61/ES ze dne 30. září 2005, kterou se provádí směrnice Evropského parlamentu a Rady 2002/98/ES, pokud jde o požadavky na sledovatelnost
SMĚRNICE. (Text s významem pro EHP)
 L 238/44 SMĚRNICE SMĚRNICE KOMISE (EU) 2017/1572 ze dne 15. září 2017, kterou se doplňuje směrnice Evropského parlamentu a Rady 2001/83/ES, pokud jde o zásady a pokyny pro správnou výrobní praxi pro humánní
L 238/44 SMĚRNICE SMĚRNICE KOMISE (EU) 2017/1572 ze dne 15. září 2017, kterou se doplňuje směrnice Evropského parlamentu a Rady 2001/83/ES, pokud jde o zásady a pokyny pro správnou výrobní praxi pro humánní
Kontrola u žadatele. Mgr. Jana Sikorová, CSc. Státní ústav pro kontrolu léčiv inspekční odbor. Obsah přednášky
 [ 1 ] Kontrola u žadatele Mgr. Jana Sikorová, CSc. Státní ústav pro kontrolu léčiv inspekční odbor Obsah přednášky [ 2 ] Provedení kontroly u žadatele (dále kontrola ). Předmět kontroly. Kontrola systému
[ 1 ] Kontrola u žadatele Mgr. Jana Sikorová, CSc. Státní ústav pro kontrolu léčiv inspekční odbor Obsah přednášky [ 2 ] Provedení kontroly u žadatele (dále kontrola ). Předmět kontroly. Kontrola systému
Zákon o lidských tkáních a buňkách
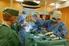 [ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Zákon o lidských tkáních a buňkách 296/2008 Sb. o zajištění jakosti a bezpečnosti lidských tkání a buněk určených k použití u člověka a o změně souvisejících
[ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Zákon o lidských tkáních a buňkách 296/2008 Sb. o zajištění jakosti a bezpečnosti lidských tkání a buněk určených k použití u člověka a o změně souvisejících
KOMISE Úřední věstník Evropské unie L 278/15. (Akty, jejichž zveřejnění není povinné)
 10.10.2006 Úřední věstník Evropské unie L 278/15 II (Akty, jejichž zveřejnění není povinné) KOMISE ROZHODNUTÍ KOMISE ze dne 29. září 2006 o vydání pokynů, kterými se stanoví kritéria pro provádění auditů
10.10.2006 Úřední věstník Evropské unie L 278/15 II (Akty, jejichž zveřejnění není povinné) KOMISE ROZHODNUTÍ KOMISE ze dne 29. září 2006 o vydání pokynů, kterými se stanoví kritéria pro provádění auditů
L 320/8 Úřední věstník Evropské unie 17.11.2012
 L 320/8 Úřední věstník Evropské unie 17.11.2012 NAŘÍZENÍ KOMISE (EU) č. 1078/2012 ze dne 16. listopadu 2012 o společné bezpečnostní metodě sledování, kterou mají používat železniční podniky, provozovatelé
L 320/8 Úřední věstník Evropské unie 17.11.2012 NAŘÍZENÍ KOMISE (EU) č. 1078/2012 ze dne 16. listopadu 2012 o společné bezpečnostní metodě sledování, kterou mají používat železniční podniky, provozovatelé
KOORDINAČNÍ STŘEDISKO TRANSPLANTACÍ Ruská 85, Praha 10
 Stanovisko KST Věc: Souhlas s darováním tkání od zemřelých dárců Vydáno: 5. března 2014 Klíčová slova: tkáně, darování, vyjádření souhlasu, zemřelý dárce Obecným a základním zdrojem právní úpravy transplantací
Stanovisko KST Věc: Souhlas s darováním tkání od zemřelých dárců Vydáno: 5. března 2014 Klíčová slova: tkáně, darování, vyjádření souhlasu, zemřelý dárce Obecným a základním zdrojem právní úpravy transplantací
OBECNÉ ZÁSADY EVROPSKÉ CENTRÁLNÍ BANKY (EU)
 L 306/32 OBECNÉ ZÁSADY OBECNÉ ZÁSADY EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2016/1993 ze dne 4. listopadu 2016, kterými se stanoví zásady pro koordinaci hodnocení podle nařízení Evropského parlamentu a Rady (EU)
L 306/32 OBECNÉ ZÁSADY OBECNÉ ZÁSADY EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2016/1993 ze dne 4. listopadu 2016, kterými se stanoví zásady pro koordinaci hodnocení podle nařízení Evropského parlamentu a Rady (EU)
Návrh. VYHLÁŠKA ze dne 2016 o požadavcích na systém řízení
 Návrh II. VYHLÁŠKA ze dne 2016 o požadavcích na systém řízení Státní úřad pro jadernou bezpečnost stanoví podle 236 zákona č..../... Sb., atomový zákon, k provedení 24 odst. 7, 29 odst. 7 a 30 odst. 9:
Návrh II. VYHLÁŠKA ze dne 2016 o požadavcích na systém řízení Státní úřad pro jadernou bezpečnost stanoví podle 236 zákona č..../... Sb., atomový zákon, k provedení 24 odst. 7, 29 odst. 7 a 30 odst. 9:
[ 1 ] Ing. František Chuchma, CSc. Seminář SVP/SDP, Státní ústav kontrolu léčiv
![[ 1 ] Ing. František Chuchma, CSc. Seminář SVP/SDP, Státní ústav kontrolu léčiv [ 1 ] Ing. František Chuchma, CSc. Seminář SVP/SDP, Státní ústav kontrolu léčiv](/thumbs/49/25341073.jpg) [ 1 ] [ 2 ] VYR-32 verze 4 kapitola 1 Farmaceutický systém jakosti The Rules Governing Medicinal Products in EU, EU Guidelines to GMP, Chapter 1 Platnost od 31.1.2013 Právní základ: čl.47 Směrnice Evropského
[ 1 ] [ 2 ] VYR-32 verze 4 kapitola 1 Farmaceutický systém jakosti The Rules Governing Medicinal Products in EU, EU Guidelines to GMP, Chapter 1 Platnost od 31.1.2013 Právní základ: čl.47 Směrnice Evropského
(Text s významem pro EHP)
 25.3.2017 L 80/7 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2017/556 ze dne 24. března 2017 o podrobných pravidlech pro provádění inspekčních postupů správné klinické praxe podle nařízení Evropského parlamentu a Rady
25.3.2017 L 80/7 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2017/556 ze dne 24. března 2017 o podrobných pravidlech pro provádění inspekčních postupů správné klinické praxe podle nařízení Evropského parlamentu a Rady
Nemocniční výjimka pokyn UST-37
 1 Nemocniční výjimka pokyn UST-37 2 Právní rámec Zákon č. 378/2007 Sb., o léčivech a změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Vyhláška č. 228/2008 Sb., o
1 Nemocniční výjimka pokyn UST-37 2 Právní rámec Zákon č. 378/2007 Sb., o léčivech a změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Vyhláška č. 228/2008 Sb., o
Nařízení vlády č. 208/2015 Sb. Nařízení vlády o technických požadavcích na pyrotechnické výrobky a jejich uvádění na trh
 Nařízení vlády č. 208/2015 Sb. Nařízení vlády o technických požadavcích na pyrotechnické výrobky a jejich uvádění na trh Částka 84/2015 Platnost od 20.08.2015 Účinnost od 04.09.2015 Aktuální znění 04.09.2015
Nařízení vlády č. 208/2015 Sb. Nařízení vlády o technických požadavcích na pyrotechnické výrobky a jejich uvádění na trh Částka 84/2015 Platnost od 20.08.2015 Účinnost od 04.09.2015 Aktuální znění 04.09.2015
PŘÍLOHA NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) /...
 EVROPSKÁ KOMISE V Bruselu dne 13.7.2018 C(2018) 4426 final ANNEX 1 PŘÍLOHA NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) /... kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) 2016/1011, pokud
EVROPSKÁ KOMISE V Bruselu dne 13.7.2018 C(2018) 4426 final ANNEX 1 PŘÍLOHA NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) /... kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) 2016/1011, pokud
DOPORUČENÍ. DOPORUČENÍ KOMISE ze dne 24. září 2013 o auditech a posouzeních prováděných oznámenými subjekty v oblasti zdravotnických prostředků
 25.9.2013 Úřední věstník Evropské unie L 253/27 DOPORUČENÍ DOPORUČENÍ KOMISE ze dne 24. září 2013 o auditech a posouzeních prováděných oznámenými subjekty v oblasti zdravotnických prostředků (Text s významem
25.9.2013 Úřední věstník Evropské unie L 253/27 DOPORUČENÍ DOPORUČENÍ KOMISE ze dne 24. září 2013 o auditech a posouzeních prováděných oznámenými subjekty v oblasti zdravotnických prostředků (Text s významem
SMĚRNICE KOMISE 2006/86/ES
 L 294/32 Úřední věstník Evropské unie 25.10.2006 SMĚRNICE KOMISE 2006/86/ES ze dne 24. října 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o požadavky na sledovatelnost,
L 294/32 Úřední věstník Evropské unie 25.10.2006 SMĚRNICE KOMISE 2006/86/ES ze dne 24. října 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o požadavky na sledovatelnost,
Technik pro kontrolu kvality a bezpečnosti potravin v masném průmyslu (kód: M)
 Technik pro kontrolu kvality a bezpečnosti v masném průmyslu (kód: 29-077-M) Autorizující orgán: Ministerstvo zemědělství Skupina oborů: Potravinářství a ářská chemie (kód: 29) Týká se povolání: Technik
Technik pro kontrolu kvality a bezpečnosti v masném průmyslu (kód: 29-077-M) Autorizující orgán: Ministerstvo zemědělství Skupina oborů: Potravinářství a ářská chemie (kód: 29) Týká se povolání: Technik
ČÁST TŘETÍ POŽADAVKY NA SUBSYSTÉMY. 6 Ověřování subsystému
 V. Vybrané části nařízení vlády č. 133/2005 Sb., o technických požadavcích na provozní a technickou propojenost evropského železničního systému, ve znění nařízení vlády č. 371/2007 Sb., nařízení vlády
V. Vybrané části nařízení vlády č. 133/2005 Sb., o technických požadavcích na provozní a technickou propojenost evropského železničního systému, ve znění nařízení vlády č. 371/2007 Sb., nařízení vlády
Formuláře zprávy a kontrolního seznamu korporátního auditu IQPP Verze 10 Realizováno 1. července 2019
 Formuláře zprávy a kontrolního seznamu korporátního auditu IQPP Realizováno 1. července 2019 Jedná se o překlad anglického originálního textu. V případě rozporu mezi anglickým originálem a českým překladem
Formuláře zprávy a kontrolního seznamu korporátního auditu IQPP Realizováno 1. července 2019 Jedná se o překlad anglického originálního textu. V případě rozporu mezi anglickým originálem a českým překladem
Systémy řízení jakosti pro realizaci výzkumu a vývoje
 Systémy řízení jakosti pro realizaci výzkumu a vývoje Aplikování systémů řízení jakosti pro výrobu a používání technologií a materiálů a vedení experimentů Blažena Jedličková 25.5.2011 Co? Dle čeho? (systém)
Systémy řízení jakosti pro realizaci výzkumu a vývoje Aplikování systémů řízení jakosti pro výrobu a používání technologií a materiálů a vedení experimentů Blažena Jedličková 25.5.2011 Co? Dle čeho? (systém)
AUDITOR KVALITY PŘEHLED POŽADOVANÝCH ZNALOSTÍ K HODNOCENÍ ZPŮSOBILOSTI CO 4.5/2007
 Gradua-CEGOS, s.r.o., Certifikační orgán pro certifikaci osob č. 3005 akreditovaný Českým institutem pro akreditaci, o.p.s. podle ČSN EN ISO/IEC 17024 AUDITOR KVALITY PŘEHLED POŽADOVANÝCH ZNALOSTÍ K HODNOCENÍ
Gradua-CEGOS, s.r.o., Certifikační orgán pro certifikaci osob č. 3005 akreditovaný Českým institutem pro akreditaci, o.p.s. podle ČSN EN ISO/IEC 17024 AUDITOR KVALITY PŘEHLED POŽADOVANÝCH ZNALOSTÍ K HODNOCENÍ
(Text s významem pro EHP) (6) Tyto pracovní postupy by měly zohlednit právní předpisy
 L 129/10 Úřední věstník Evropské unie 17.5.2006 NAŘÍZENÍ KOMISE (ES) č. 736/2006 ze dne 16. května 2006 o pracovních postupech Evropské agentury pro bezpečnost letectví pro provádění normalizačních inspekcí
L 129/10 Úřední věstník Evropské unie 17.5.2006 NAŘÍZENÍ KOMISE (ES) č. 736/2006 ze dne 16. května 2006 o pracovních postupech Evropské agentury pro bezpečnost letectví pro provádění normalizačních inspekcí
NAŘÍZENÍ VLÁDY ze dne 12. prosince o podmínkách akreditace a provádění zkoušek z odborné způsobilosti
 NAŘÍZENÍ VLÁDY ze dne 12. prosince 2006 o podmínkách akreditace a provádění zkoušek z odborné způsobilosti Vláda nařizuje podle 21 písm. b) zákona č. 309/2006 Sb., kterým se upravují další požadavky bezpečnosti
NAŘÍZENÍ VLÁDY ze dne 12. prosince 2006 o podmínkách akreditace a provádění zkoušek z odborné způsobilosti Vláda nařizuje podle 21 písm. b) zákona č. 309/2006 Sb., kterým se upravují další požadavky bezpečnosti
PŘÍLOHY NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU)
 EVROPSKÁ KOMISE V Bruselu dne 13.7.2018 C(2018) 4438 final ANNEXES 1 to 2 PŘÍLOHY NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) 2016/1011, pokud
EVROPSKÁ KOMISE V Bruselu dne 13.7.2018 C(2018) 4438 final ANNEXES 1 to 2 PŘÍLOHY NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) 2016/1011, pokud
10/01/2012 ESMA/2011/188
 Obecné pokyny a doporučení Spolupráce zahrnující přenesení úkolů mezi Evropským orgánem pro cenné papíry a trhy, příslušnými orgány a odvětvovými příslušnými orgány podle nařízení (EU) č. 513/2011 o ratingových
Obecné pokyny a doporučení Spolupráce zahrnující přenesení úkolů mezi Evropským orgánem pro cenné papíry a trhy, příslušnými orgány a odvětvovými příslušnými orgány podle nařízení (EU) č. 513/2011 o ratingových
ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne ,
 EVROPSKÁ KOMISE V Bruselu dne 14.3.2019 C(2019) 2029 final ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne 14.3.2019, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 305/2011, pokud
EVROPSKÁ KOMISE V Bruselu dne 14.3.2019 C(2019) 2029 final ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne 14.3.2019, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 305/2011, pokud
SBÍRKA PŘEDPISŮ ČESKÉ REPUBLIKY
 Ročník 2006 SBÍRKA PŘEDPISŮ ČESKÉ REPUBLIKY PROFIL PŘEDPISU: Titul předpisu: Nařízení vlády o podmínkách akreditace a provádění zkoušek z odborné způsobilosti Citace: 592/2006 Sb. Částka: 188/2006 Sb.
Ročník 2006 SBÍRKA PŘEDPISŮ ČESKÉ REPUBLIKY PROFIL PŘEDPISU: Titul předpisu: Nařízení vlády o podmínkách akreditace a provádění zkoušek z odborné způsobilosti Citace: 592/2006 Sb. Částka: 188/2006 Sb.
Audity ISŘ. Je-li tento dokument vytištěn, stává se neřízeným. MERO ČR, a. s. Veltruská 748, Kralupy nad Vltavou SJ-GŘ Lenka Šloserová v. r.
 MERO ČR, a. s. Veltruská 748, Kralupy nad Vltavou SJ-GŘ-22 A Audity ISŘ 13. Lenka Šloserová v. r. 19. listopadu 2015 Hana Fuxová v. r. Ing. Stanislav Bruna v. r. - Organizační změny - Implementace ISO
MERO ČR, a. s. Veltruská 748, Kralupy nad Vltavou SJ-GŘ-22 A Audity ISŘ 13. Lenka Šloserová v. r. 19. listopadu 2015 Hana Fuxová v. r. Ing. Stanislav Bruna v. r. - Organizační změny - Implementace ISO
(Oznámení) SPRÁVNÍ ŘÍZENÍ ÚČETNÍ DVŮR OZNÁMENÍ O VOLNÉM PRACOVNÍM MÍSTĚ ECA/2018/1. Jedno (1) pracovní místo ředitele audit
 6.3.2018 CS Úřední věstník Evropské unie C 84 A/1 V (Oznámení) SPRÁVNÍ ŘÍZENÍ ÚČETNÍ DVŮR OZNÁMENÍ O VOLNÉM PRACOVNÍM MÍSTĚ ECA/2018/1 Jedno (1) pracovní místo ředitele audit (funkční skupina AD, platová
6.3.2018 CS Úřední věstník Evropské unie C 84 A/1 V (Oznámení) SPRÁVNÍ ŘÍZENÍ ÚČETNÍ DVŮR OZNÁMENÍ O VOLNÉM PRACOVNÍM MÍSTĚ ECA/2018/1 Jedno (1) pracovní místo ředitele audit (funkční skupina AD, platová
1. ÚČEL ROZSAH PLATNOSTI POJMY A ZKRATKY POPIS... 3
 Obsah: 1. ÚČEL... 3 2. ROZSAH PLATNOSTI... 3 3. POJMY A ZKRATKY... 3 3.1 Audit SMK... 3 3.2 Vedoucí auditor/auditor... 3 3.3 Zpráva z auditu kvality... 3 3.4 Zkratky... 3 4. POPIS... 3 4.1 Plánování auditu...
Obsah: 1. ÚČEL... 3 2. ROZSAH PLATNOSTI... 3 3. POJMY A ZKRATKY... 3 3.1 Audit SMK... 3 3.2 Vedoucí auditor/auditor... 3 3.3 Zpráva z auditu kvality... 3 3.4 Zkratky... 3 4. POPIS... 3 4.1 Plánování auditu...
ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY (EU)
 1.6.2017 L 141/21 ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2017/935 ze dne 16. listopadu 2016 o přenesení pravomoci přijímat rozhodnutí o způsobilosti a bezúhonnosti a o hodnocení splnění požadavků na
1.6.2017 L 141/21 ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2017/935 ze dne 16. listopadu 2016 o přenesení pravomoci přijímat rozhodnutí o způsobilosti a bezúhonnosti a o hodnocení splnění požadavků na
Obecné pokyny k vyřizování stížností pojišťovnami
 EIOPA-BoS-12/069 CS Obecné pokyny k vyřizování stížností pojišťovnami 1/7 1. Obecné pokyny Úvod 1. Podle článku 16 nařízení o orgánu EIOPA (European Insurance and Occupational Pensions Authority, Evropského
EIOPA-BoS-12/069 CS Obecné pokyny k vyřizování stížností pojišťovnami 1/7 1. Obecné pokyny Úvod 1. Podle článku 16 nařízení o orgánu EIOPA (European Insurance and Occupational Pensions Authority, Evropského
2006R2023 CS
 2006R2023 CS 17.04.2008 001.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ KOMISE (ES) č. 2023/2006 ze dne 22. prosince
2006R2023 CS 17.04.2008 001.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ KOMISE (ES) č. 2023/2006 ze dne 22. prosince
Konference na téma Systém CEN v oboru stavebnictví dubna Pondělí, 25. dubna h.
 Konference na téma Systém CEN v oboru stavebnictví 2005 25. 26. dubna 2005 Pondělí, 25. dubna 2005 16.00 h. Úloha evropských norem v oblasti podpory Směrnice o veřejných zakázkách RA Ulrich Paetzold Generální
Konference na téma Systém CEN v oboru stavebnictví 2005 25. 26. dubna 2005 Pondělí, 25. dubna 2005 16.00 h. Úloha evropských norem v oblasti podpory Směrnice o veřejných zakázkách RA Ulrich Paetzold Generální
DOKUMENTACE K ŽÁDOSTI
 1 KAPITOLA IV + PŘÍLOHA I DOKUMENTACE K ŽÁDOSTI MUDr. Alena Trunečková Oddělení klinického hodnocení 2 Článek 25 Údaje předložené v dokumentaci k žádosti Článek 26 Jazykové požadavky Příloha I Dokumentace
1 KAPITOLA IV + PŘÍLOHA I DOKUMENTACE K ŽÁDOSTI MUDr. Alena Trunečková Oddělení klinického hodnocení 2 Článek 25 Údaje předložené v dokumentaci k žádosti Článek 26 Jazykové požadavky Příloha I Dokumentace
PROHLÁŠENÍ O OCHRANĚ OSOBNÍCH ÚDAJŮ. Oddělení R1 Registrace a transparentnost, GŘ pro hospodářskou soutěž
 PROHLÁŠENÍ O OCHRANĚ OSOBNÍCH ÚDAJŮ Toto prohlášení se týká zpracování osobních údajů v rámci šetření týkajících se státní podpory a souvisejících úkolů ve společném zájmu, které provádí Komise. Údaje,
PROHLÁŠENÍ O OCHRANĚ OSOBNÍCH ÚDAJŮ Toto prohlášení se týká zpracování osobních údajů v rámci šetření týkajících se státní podpory a souvisejících úkolů ve společném zájmu, které provádí Komise. Údaje,
ISA 610 POSUZOVÁNÍ PRÁCE INTERNÍHO AUDITU. (Platí pro audity účetních závěrek sestavených za období počínající 15.prosince 2004 nebo po tomto datu)
 POSUZOVÁNÍ PRÁCE INTERNÍHO AUDITU (Platí pro audity účetních závěrek sestavených za období počínající 15.prosince 2004 nebo po tomto datu) O B S A H Odstavec Úvod... 1-4 Rozsah a cíle interního auditu..
POSUZOVÁNÍ PRÁCE INTERNÍHO AUDITU (Platí pro audity účetních závěrek sestavených za období počínající 15.prosince 2004 nebo po tomto datu) O B S A H Odstavec Úvod... 1-4 Rozsah a cíle interního auditu..
Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah
 2007R1394 CS 02.07.2012 001.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY (ES) č. 1394/2007
2007R1394 CS 02.07.2012 001.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY (ES) č. 1394/2007
Informace pro žadatele
 F001/2018-2 Strana 1 z 6 Informace pro žadatele o posouzení odborné způsobilosti k výkonu metrologické funkce 2 Průběh certifikace 2.1 Základní rozsah certifikace Rozsah certifikace pro všechny funkce
F001/2018-2 Strana 1 z 6 Informace pro žadatele o posouzení odborné způsobilosti k výkonu metrologické funkce 2 Průběh certifikace 2.1 Základní rozsah certifikace Rozsah certifikace pro všechny funkce
Systém managementu jakosti ISO 9001
 Systém managementu jakosti ISO 9001 Požadavky na QMS Organizace potřebují prokázat: schopnost trvale poskytovat produkt produkt splňuje požadavky zákazníka a příslušné předpisy zvyšování spokojenosti zákazníka
Systém managementu jakosti ISO 9001 Požadavky na QMS Organizace potřebují prokázat: schopnost trvale poskytovat produkt produkt splňuje požadavky zákazníka a příslušné předpisy zvyšování spokojenosti zákazníka
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne
 EVROPSKÁ KOMISE V Bruselu dne 12.2.2019 C(2019) 873 final PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne 12.2.2019 o vzorech ES prohlášení a certifikátů pro železniční prvky interoperability a subsystémy,
EVROPSKÁ KOMISE V Bruselu dne 12.2.2019 C(2019) 873 final PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne 12.2.2019 o vzorech ES prohlášení a certifikátů pro železniční prvky interoperability a subsystémy,
EIOPA(BoS(13/164 CS. Obecné pokyny k vyřizování stížností zprostředkovateli pojištění
 EIOPA(BoS(13/164 CS Obecné pokyny k vyřizování stížností zprostředkovateli pojištění EIOPA WesthafenTower Westhafenplatz 1 60327 Frankfurt Germany Phone: +49 69 951119(20 Fax: +49 69 951119(19 info@eiopa.europa.eu
EIOPA(BoS(13/164 CS Obecné pokyny k vyřizování stížností zprostředkovateli pojištění EIOPA WesthafenTower Westhafenplatz 1 60327 Frankfurt Germany Phone: +49 69 951119(20 Fax: +49 69 951119(19 info@eiopa.europa.eu
SPRÁVNÁ LABORATORNÍ PRAXE V BIOCHEMICKÉ LABORATOŘI
 SPRÁVNÁ LABORATORNÍ PRAXE V BIOCHEMICKÉ LABORATOŘI ZÁSADY SPRÁVNÉ LABORATORNÍ PRAXE Správná laboratorní praxe soubor opatření, které je nutné dodržovat pojišťuje kvalitu získaných analytických dat obor
SPRÁVNÁ LABORATORNÍ PRAXE V BIOCHEMICKÉ LABORATOŘI ZÁSADY SPRÁVNÉ LABORATORNÍ PRAXE Správná laboratorní praxe soubor opatření, které je nutné dodržovat pojišťuje kvalitu získaných analytických dat obor
Systémy řízení EMS/QMS/SMS
 Systémy řízení EMS/QMS/SMS Ústí nad Labem 10/2014 Ing. Jaromír Vachta Systém řízení EMS Systém environmentálního managementu Systém řízení podle ČSN EN ISO 14001:2004 Podstata EMS - detailní informace
Systémy řízení EMS/QMS/SMS Ústí nad Labem 10/2014 Ing. Jaromír Vachta Systém řízení EMS Systém environmentálního managementu Systém řízení podle ČSN EN ISO 14001:2004 Podstata EMS - detailní informace
NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU)
 19.6.2014 L 179/17 NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 664/2014 ze dne 18. prosince 2013, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 1151/2012, pokud jde o stanovení symbolů
19.6.2014 L 179/17 NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 664/2014 ze dne 18. prosince 2013, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 1151/2012, pokud jde o stanovení symbolů
(2014/434/EU) (2) Úzká spolupráce bude navázána rozhodnutím přijatým ECB, pokud jsou splněny podmínky vymezené v článku 7 nařízení (EU) č. 1024/2013.
 5.7.2014 L 198/7 ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY ze dne 31. ledna 2014 o úzké spolupráci s vnitrostátními příslušnými orgány zúčastněných členských států, jejichž měnou není euro (ECB/2014/5) (2014/434/EU)
5.7.2014 L 198/7 ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY ze dne 31. ledna 2014 o úzké spolupráci s vnitrostátními příslušnými orgány zúčastněných členských států, jejichž měnou není euro (ECB/2014/5) (2014/434/EU)
SYSTÉM FINANČNÍ KONTROLY OBCE
 SYSTÉM FINANČNÍ KONTROLY OBCE Obec: Brnířov Adresa: Brnířov 41, 345 06 Kdyně Identifikační číslo obce: 00572608 1) Předmět úpravy a právní rámec Tento vnitřní předpis vymezuje v souladu se zákonem č. 320/2001
SYSTÉM FINANČNÍ KONTROLY OBCE Obec: Brnířov Adresa: Brnířov 41, 345 06 Kdyně Identifikační číslo obce: 00572608 1) Předmět úpravy a právní rámec Tento vnitřní předpis vymezuje v souladu se zákonem č. 320/2001
ROZHODNUTÍ KOMISE (EU)
 12.12.2018 L 315/35 ROZHODNUTÍ KOMISE (EU) 2018/1961 ze dne 11. prosince 2018, kterým se stanoví vnitřní pravidla týkající se poskytování informací subjektům údajů a omezení některých jejich práv v souvislosti
12.12.2018 L 315/35 ROZHODNUTÍ KOMISE (EU) 2018/1961 ze dne 11. prosince 2018, kterým se stanoví vnitřní pravidla týkající se poskytování informací subjektům údajů a omezení některých jejich práv v souvislosti
2012 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 1 2 VÝCHOZÍ SUROVINY VE VÝROBĚ HUMÁNNÍCH LÉČIVÝCH PŘÍPRAVKŮ Ing. Eva Niklíčková Státní ústav pro kontrolu léčiv, Praha 3 Původní text kapitoly 5 Nákup výchozích látek je důležitá činnost, jež vyžaduje,
1 2 VÝCHOZÍ SUROVINY VE VÝROBĚ HUMÁNNÍCH LÉČIVÝCH PŘÍPRAVKŮ Ing. Eva Niklíčková Státní ústav pro kontrolu léčiv, Praha 3 Původní text kapitoly 5 Nákup výchozích látek je důležitá činnost, jež vyžaduje,
POŽADAVKY PLYNOUCÍ ZE SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2014/30/EU
 POŽADAVKY PLYNOUCÍ ZE SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2014/30/EU (revize textu k 1. 5. 2014) Dodávání na trh a uvádění do provozu (článek 4 směrnice) Členské státy přijmou veškerá vhodná opatření,
POŽADAVKY PLYNOUCÍ ZE SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2014/30/EU (revize textu k 1. 5. 2014) Dodávání na trh a uvádění do provozu (článek 4 směrnice) Členské státy přijmou veškerá vhodná opatření,
592/2006 Sb. NAŘÍZENÍ VLÁDY. ze dne 12. prosince 2006
 592/2006 Sb. NAŘÍZENÍ VLÁDY ze dne 12. prosince 2006 o podmínkách akreditace a provádění zkoušek z odborné způsobilosti Vláda nařizuje podle 21 písm. b) zákona č. 309/2006 Sb., kterým se upravují další
592/2006 Sb. NAŘÍZENÍ VLÁDY ze dne 12. prosince 2006 o podmínkách akreditace a provádění zkoušek z odborné způsobilosti Vláda nařizuje podle 21 písm. b) zákona č. 309/2006 Sb., kterým se upravují další
ČINNOSTI DOZORU NAD TRHEM ORGANIZACE A STRUKTURA
 ČINNOSTI DOZORU NAD TRHEM ORGANIZACE A STRUKTURA Strategie dozoru nad trhem Způsob, jakým je prováděn dozor nad trhem, je velmi ovlivněn souborem základních předpokladů a principů pokud jde o jeho postavení,
ČINNOSTI DOZORU NAD TRHEM ORGANIZACE A STRUKTURA Strategie dozoru nad trhem Způsob, jakým je prováděn dozor nad trhem, je velmi ovlivněn souborem základních předpokladů a principů pokud jde o jeho postavení,
2/6. 1 Úř. věst. L 158, , s Úř. věst. L 335, , s Úř. věst. L 331, , s
 EIOPA16/858 CS Obecné pokyny k usnadnění efektivního dialogu mezi příslušnými orgány vykonávajícími dohled nad pojišťovnami a statutárním auditorem či auditory a auditorskou společností či společnostmi,
EIOPA16/858 CS Obecné pokyny k usnadnění efektivního dialogu mezi příslušnými orgány vykonávajícími dohled nad pojišťovnami a statutárním auditorem či auditory a auditorskou společností či společnostmi,
Příručka pro žadatele
 Příručka pro žadatele Registrace organizace producentů v odvětví ovoce a zeleniny 18. dubna 2016 IČ: 48133981 DIČ: CZ48133981 Strana 1/5 OBSAH 1. Legislativa 2. Definice 3. Registrace organizace producentů
Příručka pro žadatele Registrace organizace producentů v odvětví ovoce a zeleniny 18. dubna 2016 IČ: 48133981 DIČ: CZ48133981 Strana 1/5 OBSAH 1. Legislativa 2. Definice 3. Registrace organizace producentů
11.11.2010 Úřední věstník Evropské unie L 293/15
 11.11.2010 Úřední věstník Evropské unie L 293/15 NAŘÍZENÍ KOMISE (EU) č. 1014/2010 ze dne 10. listopadu 2010 o sledování a hlášení údajů o registraci nových osobních automobilů podle nařízení Evropského
11.11.2010 Úřední věstník Evropské unie L 293/15 NAŘÍZENÍ KOMISE (EU) č. 1014/2010 ze dne 10. listopadu 2010 o sledování a hlášení údajů o registraci nových osobních automobilů podle nařízení Evropského
FV systémy a jejich QM Základní dokument FV systému
 Státní ústav pro kontrolu léčiv [ 1 ] FV systémy a jejich QM Základní dokument FV systému Oddělení farmakovigilance Státní ústav pro kontrolu léčiv [ 2 ] Co v dnešní prezentaci? Stručné představení modulů
Státní ústav pro kontrolu léčiv [ 1 ] FV systémy a jejich QM Základní dokument FV systému Oddělení farmakovigilance Státní ústav pro kontrolu léčiv [ 2 ] Co v dnešní prezentaci? Stručné představení modulů
Prováděcí nařízení Komise (EU) č. 607/2012 ze dne 6. července 2012 o prováděcích pravidlech pro systém náležité péče a pro četnost
 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 607/2012 ze dne 6. července 2012 o prováděcích pravidlech pro systém náležité péče a pro četnost a povahu kontrol kontrolních organizací podle nařízení Evropského parlamentu
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 607/2012 ze dne 6. července 2012 o prováděcích pravidlech pro systém náležité péče a pro četnost a povahu kontrol kontrolních organizací podle nařízení Evropského parlamentu
2012 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 2 KONTROLA JAKOSTI A AKTUALIZACE POKYNU VYR-32, KAPITOLA 6 Jan Tille, 03.02.2015 SÚKL 3 Legislativní vymezení Legislativní zdroje a zkratky: zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících
2 KONTROLA JAKOSTI A AKTUALIZACE POKYNU VYR-32, KAPITOLA 6 Jan Tille, 03.02.2015 SÚKL 3 Legislativní vymezení Legislativní zdroje a zkratky: zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících
PŘÍLOHY PROVÁDĚCÍHO NAŘÍZENÍ KOMISE,
 EVROPSKÁ KOMISE V Bruselu dne 4.4.2018 C(2018) 1866 final ANNEES 1 to 3 PŘÍLOHY PROVÁDĚCÍHO NAŘÍZENÍ KOMISE, kterým se stanoví praktická pravidla pro postup povolování železničních vozidel a železničních
EVROPSKÁ KOMISE V Bruselu dne 4.4.2018 C(2018) 1866 final ANNEES 1 to 3 PŘÍLOHY PROVÁDĚCÍHO NAŘÍZENÍ KOMISE, kterým se stanoví praktická pravidla pro postup povolování železničních vozidel a železničních
MANAŽER KVALITY PŘEHLED POŽADOVANÝCH ZNALOSTÍ K HODNOCENÍ ZPŮSOBILOSTI CO 4.4/2007
 Gradua-CEGOS, s.r.o., Certifikační orgán pro certifikaci osob č. 3005 akreditovaný Českým institutem pro akreditaci, o.p.s. podle ČSN EN ISO/IEC 17024 MANAŽER KVALITY PŘEHLED POŽADOVANÝCH ZNALOSTÍ K HODNOCENÍ
Gradua-CEGOS, s.r.o., Certifikační orgán pro certifikaci osob č. 3005 akreditovaný Českým institutem pro akreditaci, o.p.s. podle ČSN EN ISO/IEC 17024 MANAŽER KVALITY PŘEHLED POŽADOVANÝCH ZNALOSTÍ K HODNOCENÍ
Příloha č. 1 vyhlášky MZ ČR č. 385/2006, Sb., o zdravotnické dokumentaci aktuální znění
 Příloha č. 1 vyhlášky MZ ČR č. 385/2006, Sb., o zdravotnické dokumentaci aktuální znění MINIMÁLNÍ OBSAH SAMOSTATNÝCH ČÁSTÍ ZDRAVOTNICKÉ DOKUMENTACE 1. INFORMACE ZE ZDRAVOTNICKÉ DOKUMENTACE VEDENÉ LÉKAŘEM
Příloha č. 1 vyhlášky MZ ČR č. 385/2006, Sb., o zdravotnické dokumentaci aktuální znění MINIMÁLNÍ OBSAH SAMOSTATNÝCH ČÁSTÍ ZDRAVOTNICKÉ DOKUMENTACE 1. INFORMACE ZE ZDRAVOTNICKÉ DOKUMENTACE VEDENÉ LÉKAŘEM
(Text s významem pro EHP)
 13.2.2019 L 42/9 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2019/250 ze dne 12. února 2019 o vzorech ES prohlášení a certifikátů pro železniční prvky interoperability a subsystémy, o vzoru prohlášení o shodě s povoleným
13.2.2019 L 42/9 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2019/250 ze dne 12. února 2019 o vzorech ES prohlášení a certifikátů pro železniční prvky interoperability a subsystémy, o vzoru prohlášení o shodě s povoleným
s ohledem na Smlouvu o fungování Evropské unie, a zejména na čl. 127 odst. 6 a článek 132 této smlouvy,
 L 314/66 1.12.2015 ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2015/2218 ze dne 20. listopadu 2015 o postupu při vyloučení předpokladu, že zaměstnanci mají podstatný vliv na rizikový profil dohlížené úvěrové
L 314/66 1.12.2015 ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2015/2218 ze dne 20. listopadu 2015 o postupu při vyloučení předpokladu, že zaměstnanci mají podstatný vliv na rizikový profil dohlížené úvěrové
PŘÍLOHY. k návrhu. nařízení Evropského parlamentu a Rady,
 EVROPSKÁ KOMISE V Bruselu dne 7.9.2016 COM(2016) 491 final ANNEXES 1 to 7 PŘÍLOHY k návrhu nařízení Evropského parlamentu a Rady, kterým se zavádí certifikační systém Unie pro detekční zařízení pro zajištění
EVROPSKÁ KOMISE V Bruselu dne 7.9.2016 COM(2016) 491 final ANNEXES 1 to 7 PŘÍLOHY k návrhu nařízení Evropského parlamentu a Rady, kterým se zavádí certifikační systém Unie pro detekční zařízení pro zajištění
PROVÁDĚCÍ ROZHODNUTÍ KOMISE (EU) / ze dne
 EVROPSKÁ KOMISE V Bruselu dne 2.2.2018 C(2018) 533 final PROVÁDĚCÍ ROZHODNUTÍ KOMISE (EU) / ze dne 2.2.2018 o jednotných podrobných specifikacích pro shromažďování a analýzu údajů ke sledování a hodnocení
EVROPSKÁ KOMISE V Bruselu dne 2.2.2018 C(2018) 533 final PROVÁDĚCÍ ROZHODNUTÍ KOMISE (EU) / ze dne 2.2.2018 o jednotných podrobných specifikacích pro shromažďování a analýzu údajů ke sledování a hodnocení
SMĚRNICE Č. 001, O OCHRANĚ OSOBNÍCH ÚDAJŮ 1. ÚČEL 2. PŮSOBNOST 3. TERMÍNY, DEFINICE A ZKRATKY
 SMĚRNICE Č. 001, O OCHRANĚ OSOBNÍCH ÚDAJŮ 1. ÚČEL 1.1. Účelem této směrnice je stanovit základní pravidla zpracování osobních údajů ve Společnosti. Tato směrnice je jedním z organizačních opatření ochrany
SMĚRNICE Č. 001, O OCHRANĚ OSOBNÍCH ÚDAJŮ 1. ÚČEL 1.1. Účelem této směrnice je stanovit základní pravidla zpracování osobních údajů ve Společnosti. Tato směrnice je jedním z organizačních opatření ochrany
ZP-22 Metodika kontrol distributorů a dovozců zdravotnických prostředků
 ZP-22 Metodika kontrol distributorů a dovozců zdravotnických prostředků Tento pokyn je platný od 11. 03. 2019. ÚVOD Tato metodika obsahuje informace určené zejména pro dovozce a distributory zdravotnických
ZP-22 Metodika kontrol distributorů a dovozců zdravotnických prostředků Tento pokyn je platný od 11. 03. 2019. ÚVOD Tato metodika obsahuje informace určené zejména pro dovozce a distributory zdravotnických
SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2004/23/ES. ze dne 31. března 2004
 SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2004/23/ES ze dne 31. března 2004 o stanovení jakostních a bezpečnostních norem pro darování, odběr, vyšetřování, zpracování, konzervaci, skladování a distribuci lidských
SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2004/23/ES ze dne 31. března 2004 o stanovení jakostních a bezpečnostních norem pro darování, odběr, vyšetřování, zpracování, konzervaci, skladování a distribuci lidských
Technik pro kontrolu kvality a bezpečnosti potravin v konzervárenství (kód: M)
 Technik pro kontrolu kvality a bezpečnosti potravin v konzervárenství (kód: 29-093-M) Autorizující orgán: Ministerstvo zemědělství Skupina oborů: Potravinářství a potravinářská chemie (kód: 29) Týká se
Technik pro kontrolu kvality a bezpečnosti potravin v konzervárenství (kód: 29-093-M) Autorizující orgán: Ministerstvo zemědělství Skupina oborů: Potravinářství a potravinářská chemie (kód: 29) Týká se
CS Jednotná v rozmanitosti CS A8-0206/864. Pozměňovací návrh
 22.3.2019 A8-0206/864 864 Článek 2 d (nový) Článek 2d Inteligentní prosazování 1. Aniž je dotčena směrnice 2014/67/EU, členské státy v zájmu důslednějšího prosazování povinností uvedených v článku 2 této
22.3.2019 A8-0206/864 864 Článek 2 d (nový) Článek 2d Inteligentní prosazování 1. Aniž je dotčena směrnice 2014/67/EU, členské státy v zájmu důslednějšího prosazování povinností uvedených v článku 2 této
POŽADAVKY PLYNOUCÍ ZE SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2014/35/EU
 POŽADAVKY PLYNOUCÍ ZE SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2014/35/EU (revize textu k 1. 5. 2014) Dodávání na trh a bezpečnostní zásady (článek 3 směrnice) Elektrická zařízení mohou být dodávána na trh
POŽADAVKY PLYNOUCÍ ZE SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2014/35/EU (revize textu k 1. 5. 2014) Dodávání na trh a bezpečnostní zásady (článek 3 směrnice) Elektrická zařízení mohou být dodávána na trh
EVROPSKÁ KOMISE GENERÁLNÍ ŘEDITELSTVÍ PRO MOBILITU A DOPRAVU
 EVROPSKÁ KOMISE GENERÁLNÍ ŘEDITELSTVÍ PRO MOBILITU A DOPRAVU Brusel 10. července 2018 Zrušuje a nahrazuje oznámení ze dne 27. února 2018 OZNÁMENÍ ZÚČASTNĚNÝM STRANÁM VYSTOUPENÍ SPOJENÉHO KRÁLOVSTVÍ Z EU
EVROPSKÁ KOMISE GENERÁLNÍ ŘEDITELSTVÍ PRO MOBILITU A DOPRAVU Brusel 10. července 2018 Zrušuje a nahrazuje oznámení ze dne 27. února 2018 OZNÁMENÍ ZÚČASTNĚNÝM STRANÁM VYSTOUPENÍ SPOJENÉHO KRÁLOVSTVÍ Z EU
Přehled legislativy. Přehled legislativy týkající se farmakovigilančního (FV) auditu a inspekce. 30. listopadu
 Přehled legislativy týkající se farmakovigilančního (FV) auditu a inspekce 30. listopadu 2017 Přehled legislativy Evropská aktuální legislativa - Nařízení Evropského Parlamentu a Rady (EU) 1235/2010 -
Přehled legislativy týkající se farmakovigilančního (FV) auditu a inspekce 30. listopadu 2017 Přehled legislativy Evropská aktuální legislativa - Nařízení Evropského Parlamentu a Rady (EU) 1235/2010 -
ODŮVODNĚNÉ STANOVISKO VNITROSTÁTNÍHO PARLAMENTU K SUBSIDIARITĚ
 Evropský parlament 2014-2019 Výbor pro právní záležitosti 20.3.2017 ODŮVODNĚNÉ STANOVISKO VNITROSTÁTNÍHO PARLAMENTU K SUBSIDIARITĚ Věc: Odůvodněné stanovisko francouzského Senátu k návrhu nařízení Evropského
Evropský parlament 2014-2019 Výbor pro právní záležitosti 20.3.2017 ODŮVODNĚNÉ STANOVISKO VNITROSTÁTNÍHO PARLAMENTU K SUBSIDIARITĚ Věc: Odůvodněné stanovisko francouzského Senátu k návrhu nařízení Evropského
Pro účely této směrnice se: a) reprodukčními buňkami rozumí všechny tkáně a buňky určené k účelům asistované reprodukce;
 L 38/40 CS Úřední věstník Evropské unie 9.2.2006 SMĚRNICE KOMISE 2006/17/ES ze dne 8. února 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o určité technické požadavky
L 38/40 CS Úřední věstník Evropské unie 9.2.2006 SMĚRNICE KOMISE 2006/17/ES ze dne 8. února 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o určité technické požadavky
Návod k požadavkům ISO 9001:2015 na dokumentované informace
 International Organization for Standardization BIBC II, Chemin de Blandonnet 8, CP 401, 1214 Vernier, Geneva, Switzerland Tel: +41 22 749 01 11, Web: www.iso.org Návod k požadavkům ISO 9001:2015 na dokumentované
International Organization for Standardization BIBC II, Chemin de Blandonnet 8, CP 401, 1214 Vernier, Geneva, Switzerland Tel: +41 22 749 01 11, Web: www.iso.org Návod k požadavkům ISO 9001:2015 na dokumentované
Úřední věstník C 164 A. Evropské unie. Informace a oznámení. Oznámení. Ročník května České vydání. Obsah SPRÁVNÍ ŘÍZENÍ.
 Úřední věstník Evropské unie C 164 A České vydání Informace a oznámení Ročník 60 24. května 2017 Obsah V Oznámení SPRÁVNÍ ŘÍZENÍ Účetní dvůr 2017/C 164 A/01 Oznámení o volném pracovním místě ECA/2017/7
Úřední věstník Evropské unie C 164 A České vydání Informace a oznámení Ročník 60 24. května 2017 Obsah V Oznámení SPRÁVNÍ ŘÍZENÍ Účetní dvůr 2017/C 164 A/01 Oznámení o volném pracovním místě ECA/2017/7
STANOVISKO KOMISE. ze dne 30.11.2012
 EVROPSKÁ KOMISE V Bruselu dne 30.11.2012 C(2012) 8867 final STANOVISKO KOMISE ze dne 30.11.2012 podle čl. 3 odst. 1 nařízení (ES) č. 715/2009 a čl. 10 odst. 6 směrnice 2009/73/ES Česká republika Certifikace
EVROPSKÁ KOMISE V Bruselu dne 30.11.2012 C(2012) 8867 final STANOVISKO KOMISE ze dne 30.11.2012 podle čl. 3 odst. 1 nařízení (ES) č. 715/2009 a čl. 10 odst. 6 směrnice 2009/73/ES Česká republika Certifikace
2017 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 Seminář k novelizaci zákona a vyhlášky - program 2 Novela zákona-dovozy ze třetích zemí Novela vyhlášky-dovozy ze třetích zemí Přestávka-občerstvení Novela zákona-kódování Novela vyhlášky-kódování Přestávka-občerstvení
Seminář k novelizaci zákona a vyhlášky - program 2 Novela zákona-dovozy ze třetích zemí Novela vyhlášky-dovozy ze třetích zemí Přestávka-občerstvení Novela zákona-kódování Novela vyhlášky-kódování Přestávka-občerstvení
1993R0315 CS
 1993R0315 CS 07.08.2009 002.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ RADY (EHS) č. 315/93 ze dne 8. února 1993, kterým
1993R0315 CS 07.08.2009 002.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ RADY (EHS) č. 315/93 ze dne 8. února 1993, kterým
Žádosti členských států o aktualizaci seznamu Společenství
 L 84/8 Úřední věstník Evropské unie 23.3.2006 NAŘÍZENÍ KOMISE (ES) č. 473/2006 ze dne 22. března 2006, kterým se stanoví prováděcí pravidla pro seznam Společenství uvádějící letecké dopravce, kteří podléhají
L 84/8 Úřední věstník Evropské unie 23.3.2006 NAŘÍZENÍ KOMISE (ES) č. 473/2006 ze dne 22. března 2006, kterým se stanoví prováděcí pravidla pro seznam Společenství uvádějící letecké dopravce, kteří podléhají
SMĚRNICE Č. 1/2018, O OCHRANĚ OSOBNÍCH ÚDAJŮ
 SMĚRNICE Č. 1/2018, O OCHRANĚ OSOBNÍCH ÚDAJŮ 1. ÚČEL 1. Účelem této směrnice je stanovit základní pravidla zpracování osobních údajů ve Společnosti. Tato směrnice je jedním z organizačních opatření ochrany
SMĚRNICE Č. 1/2018, O OCHRANĚ OSOBNÍCH ÚDAJŮ 1. ÚČEL 1. Účelem této směrnice je stanovit základní pravidla zpracování osobních údajů ve Společnosti. Tato směrnice je jedním z organizačních opatření ochrany
Pravidla procesu hodnocení místních radiologických standardů a jejich souladu s národními radiologickými standardy
 1. Úvod Externí klinický audit (dále jen EKA) je způsob hodnocení kvality a bezpečí poskytovaných zdravotních služeb, jejichž součástí je lékařské ozáření, který definuje zákon č. 373/2011 Sb., o specifických
1. Úvod Externí klinický audit (dále jen EKA) je způsob hodnocení kvality a bezpečí poskytovaných zdravotních služeb, jejichž součástí je lékařské ozáření, který definuje zákon č. 373/2011 Sb., o specifických
AUTORIZAČNÍ NÁVOD AN 13/03 Požadavky na systém managementu jakosti laboratoře a zajišťování kvality výsledků
 AUTORIZAČNÍ NÁVOD AN 13/03 Požadavky na systém managementu jakosti laboratoře a zajišťování kvality výsledků Jakost = kvalita Požadavek Znak (charakteristika) Znak (charakteristika) jakosti Management
AUTORIZAČNÍ NÁVOD AN 13/03 Požadavky na systém managementu jakosti laboratoře a zajišťování kvality výsledků Jakost = kvalita Požadavek Znak (charakteristika) Znak (charakteristika) jakosti Management
Příloha č. 1 Kontrolní seznam o připravenosti na nařízení GDPR Checklist
 Příloha č. 1 Kontrolní seznam o připravenosti na nařízení GDPR Checklist Kategorie osobních údajů a subjektů údajů Prvky osobních údajů obsažené v každé kategorii dat Zdroj osobních údajů Účely, pro které
Příloha č. 1 Kontrolní seznam o připravenosti na nařízení GDPR Checklist Kategorie osobních údajů a subjektů údajů Prvky osobních údajů obsažené v každé kategorii dat Zdroj osobních údajů Účely, pro které
b) obsah návrhu na prodloužení platnosti pověření
 Strana 1832 Sbírka zákonů č. 94 / 2016 Částka 38 94 VYHLÁŠKA ze dne 23. března 2016 o hodnocení nebezpečných vlastností odpadů Ministerstvo životního prostředí a Ministerstvo zdravotnictví stanoví podle
Strana 1832 Sbírka zákonů č. 94 / 2016 Částka 38 94 VYHLÁŠKA ze dne 23. března 2016 o hodnocení nebezpečných vlastností odpadů Ministerstvo životního prostředí a Ministerstvo zdravotnictví stanoví podle
SDĚLENÍ KOMISE RADĚ, EVROPSKÉMU PARLAMENTU, EVROPSKÉMU HOSPODÁŘSKÉMU A SOCIÁLNÍMU VÝBORU A VÝBORU REGIONŮ
 EVROPSKÁ KOMISE V Bruselu dne 19.1.2010 KOM(2010)3 v konečném znění SDĚLENÍ KOMISE RADĚ, EVROPSKÉMU PARLAMENTU, EVROPSKÉMU HOSPODÁŘSKÉMU A SOCIÁLNÍMU VÝBORU A VÝBORU REGIONŮ o provádění směrnice 2002/98/ES,
EVROPSKÁ KOMISE V Bruselu dne 19.1.2010 KOM(2010)3 v konečném znění SDĚLENÍ KOMISE RADĚ, EVROPSKÉMU PARLAMENTU, EVROPSKÉMU HOSPODÁŘSKÉMU A SOCIÁLNÍMU VÝBORU A VÝBORU REGIONŮ o provádění směrnice 2002/98/ES,
EVROPSKÁ UNIE EVROPSKÝ PARLAMENT
 EVROPSKÁ UNIE EVROPSKÝ PARLAMENT RADA Štrasburk 11. března 2008 (OR. en) 2005/0191 (COD) LEX 888 PE-CONS 3601/x/08 REV x AVIATION 9 CODEC 30 NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY O SPOLEČNÝCH PRAVIDLECH
EVROPSKÁ UNIE EVROPSKÝ PARLAMENT RADA Štrasburk 11. března 2008 (OR. en) 2005/0191 (COD) LEX 888 PE-CONS 3601/x/08 REV x AVIATION 9 CODEC 30 NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY O SPOLEČNÝCH PRAVIDLECH
Výtisk č. : Platnost od: Schválil: Podpis:
 SM-05 INTERNÍ AUDITY Výtisk č. : Platnost od: Schválil: Podpis: 1 OBSAH Číslo kapitola strana 1 OBSAH... 2 2 PŘEHLED ZMĚN A REVIZÍ... 2 3 ÚČEL... 2 3.1 ROZSAH PLATNOSTI... 3 3.2 DEFINICE... 3 3.3 POUŽITÉ
SM-05 INTERNÍ AUDITY Výtisk č. : Platnost od: Schválil: Podpis: 1 OBSAH Číslo kapitola strana 1 OBSAH... 2 2 PŘEHLED ZMĚN A REVIZÍ... 2 3 ÚČEL... 2 3.1 ROZSAH PLATNOSTI... 3 3.2 DEFINICE... 3 3.3 POUŽITÉ
Pro účely této směrnice se: a) reprodukčními buňkami rozumí všechny tkáně a buňky určené k účelům asistované reprodukce;
 L 38/40 Úřední věstník Evropské unie 9.2.2006 SMĚRNICE KOMISE 2006/17/ES ze dne 8. února 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o určité technické požadavky
L 38/40 Úřední věstník Evropské unie 9.2.2006 SMĚRNICE KOMISE 2006/17/ES ze dne 8. února 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o určité technické požadavky
ZPRÁVA. o ověření roční účetní závěrky Evropského monitorovacího centra pro drogy a drogovou závislost za rozpočtový rok 2016, spolu s odpovědí centra
 C 417/150 CS Úřední věstník Evropské unie 6.12.2017 ZPRÁVA o ověření roční účetní závěrky Evropského monitorovacího centra pro drogy a drogovou závislost za rozpočtový rok 2016, spolu s odpovědí centra
C 417/150 CS Úřední věstník Evropské unie 6.12.2017 ZPRÁVA o ověření roční účetní závěrky Evropského monitorovacího centra pro drogy a drogovou závislost za rozpočtový rok 2016, spolu s odpovědí centra
Systémy řízení QMS, EMS, SMS, SLP
 Systémy řízení QMS, EMS, SMS, SLP Ústí nad Labem 11/2013 Ing. Jaromír Vachta Systém řízení QMS Systém managementu kvality Systém řízení podle ČSN EN ISO 9001:2009 - stanovení, pochopení a zajištění plnění
Systémy řízení QMS, EMS, SMS, SLP Ústí nad Labem 11/2013 Ing. Jaromír Vachta Systém řízení QMS Systém managementu kvality Systém řízení podle ČSN EN ISO 9001:2009 - stanovení, pochopení a zajištění plnění
INSPEKCE POSKYTOVÁNÍ SOCIÁLNÍCH SLUŽEB. Základní informace
 INSPEKCE POSKYTOVÁNÍ SOCIÁLNÍCH SLUŽEB Základní informace Právní zakotvení inspekcí Zákon č. 108/2006 Sb. o sociálních službách Vyhláška č. 505/2006 Sb., kterou se provádějí některá ustanovení zákona o
INSPEKCE POSKYTOVÁNÍ SOCIÁLNÍCH SLUŽEB Základní informace Právní zakotvení inspekcí Zákon č. 108/2006 Sb. o sociálních službách Vyhláška č. 505/2006 Sb., kterou se provádějí některá ustanovení zákona o
MEZINÁRODNÍ STANDARDY PRO PROFESNÍ PRAXI INTERNÍHO AUDITU
 MEZINÁRODNÍ STANDARDY PRO PROFESNÍ PRAXI INTERNÍHO AUDITU Základní standardy 1000 Účel, pravomoci a odpovědnosti Účel, pravomoci a odpovědnosti interního auditu musí být formálně stanoveny ve statutu interního
MEZINÁRODNÍ STANDARDY PRO PROFESNÍ PRAXI INTERNÍHO AUDITU Základní standardy 1000 Účel, pravomoci a odpovědnosti Účel, pravomoci a odpovědnosti interního auditu musí být formálně stanoveny ve statutu interního
ZPRÁVA. o ověření roční účetní závěrky Evropského policejního úřadu za rozpočtový rok 2016, spolu s odpovědí úřadu (2017/C 417/36)
 6.12.2017 CS Úřední věstník Evropské unie C 417/223 ZPRÁVA o ověření roční účetní závěrky Evropského policejního úřadu za rozpočtový rok 2016, spolu s odpovědí úřadu (2017/C 417/36) ÚVOD 1. Evropský policejní
6.12.2017 CS Úřední věstník Evropské unie C 417/223 ZPRÁVA o ověření roční účetní závěrky Evropského policejního úřadu za rozpočtový rok 2016, spolu s odpovědí úřadu (2017/C 417/36) ÚVOD 1. Evropský policejní
ANNEX PŘÍLOHA NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI,
 EVROPSKÁ KOMISE V Bruselu dne 16.5.2018 C(2018) 2857 final ANNEX PŘÍLOHA NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI, kterým se mění nařízení Komise v přenesené pravomoci (EU) č. 1042/2014 ze dne 25. července
EVROPSKÁ KOMISE V Bruselu dne 16.5.2018 C(2018) 2857 final ANNEX PŘÍLOHA NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI, kterým se mění nařízení Komise v přenesené pravomoci (EU) č. 1042/2014 ze dne 25. července
