Virové hemoragické horečky ve světě
|
|
|
- Radomír Pospíšil
- před 7 lety
- Počet zobrazení:
Transkript
1 Masarykova univerzita v Brně Přírodovědecká fakulta Ústav experimentální biologie Oddělení mikrobiologie Virové hemoragické horečky ve světě (Bakalářská práce studijního programu Biologie oboru Obecná biologie směr Mikrobiologie) Eva Slaninková Brno 2009
2 Prohlašuji tímto, ţe jsem bakalářskou práci na téma Virové hemoragické horečky ve světě vypracovala sama, pouze s pouţitím literatury a pramenů v práci uvedených. V Brně dne 10. května 2009
3 Ráda bych touto cestou poděkovala svému vedoucímu bakalářské práce, RNDr. Ivo Rudolfovi, Ph.D., a konzultantovi prof. RNDr. Zdeňku Hubálkovi, DrSc. za odbornou pomoc a připomínky při zpracování daného tématu.
4 Obsah Obsah... 1 Seznam pouţitých zkratek Úvod Cíl práce Hemoragické horečky Obecná charakteristika VHF jako zoonózy Léčba a prevence Čeleď Togaviridae Virus Chikungunya Virus O nyong nyong Čeleď Flaviviridae Virus ţluté zimnice Virus Dengue Virus omské hemoragické horečky Čeleď Bunyaviridae Virus krymsko-konţské hemoragické horečky Virus horečky Rift Valley Hantaviry Čeleď Arenaviridae Virus Junin Virus Machupo Virus Lassa Čeleď Filoviridae Virus Ebola Virus Marburg Čeleď Paramyxoviridae Virus Nipah Virus Hendra Diskuze Závěr Seznam pouţité literatury
5 Seznam pouţitých zkratek Ae. komár rodu Aedes AHF Argentine haemorrhagic fever (Argentinská hemoragická horečka) An. komár rodu Anopheles BHF Bolivian haemorrhagic fever (Bolivijská hemoragická horečka) CCHF Crimean-Congo haemorrhagic fever (Krymsko-konţská hemoragická horečka) CDC Centres for Disease Control and Prevention (Centrum pro kontrolu nemocí a prevenci) CNS centrální nervová soustava ELISA enzyme-linked immunosorbent assay (imunoenzymatický test) EN epidemická nefropatie GIT gastrointestinální trakt HF haemorrhagic fever (hemoragická horečka) HFRS HF with renal syndrome (hemoragická horečka s renálním syndromem) HPS hantavirus pulmonary syndrome (hantavirový plicní syndrom) CHIK chikungunya fever (horečka chikungunya) OHF Omsk haemorrhagic fever (Omská hemoragická horečka) ONN o nyong nyong fever (horečka o nyong nyong) P. kaloň rodu Pteropus PCR polymerase chain reaction (polymerázová řetězová reakce) RT-PCR reverse transcriptase PCR (PCR se zpětnou transkriptázou) RVF Rift Valley fever (horečka údolí Rift) +ssrna pozitivně orientovaná jednořetězcová RNA -ssrna negativně orientovaná jednořetězcová RNA VHF viral haemorrhagic fever (virová hemoragická horečka) WHO World Health Organization (Světová zdravotnická organizace) YF yellow fever (ţlutá zimnice) - 2 -
6 1. Úvod Skupina patogenů, způsobujících virové hemoragické horečky, je navzdory dnešním technologiím a znalostem stále ne příliš probádanou oblastí. Jde o vysoce infekční a často smrtelná onemocnění, dosud u nich není (aţ na výjimky) známa ţádná specifická léčba ani vakcína, rovněţ terapie běţnými antivirotiky je neúčinná. Asi polovinu těchto onemocnění způsobují arboviry, čímţ je přenos na člověka i pohyb virů v prostředí výrazně usnadněn. Díky rostoucí popularitě cestování do exotických krajin, kde je výskyt VHF nákaz frekventovanější, dochází k zavlečení chorob i do vyspělých zemí. Spolu se zvětšující se lidskou populací, masivní urbanizací, sociálními a teplotními změnami v rámci celé planety a vysokou adaptabilitou viru dochází k častějšímu kontaktu člověka s virem. Nezanedbatelné je také rostoucí riziko teroristických útoků. Viry způsobující VHF byly zařazeny mezi potenciální biologické zbraně právě pro jejich vysokou infekčnost, letalitu a neléčitelnost. Tyto všechny faktory vyvolávají stále větší zájem o zkoumanou problematiku nejen u mě, ale i ve vědeckých kruzích a u laické společnosti
7 2. Cíl práce Cílem práce je kompilační studie, která má za úkol podat formou literární rešerše komplexní přehled o výskytu nejvýznamnějších hemoragických virových nákaz ve světě. Důraz bude kladen na taxonomii virů, jejich biologické vlastnosti, molekulární charakteristiky, přirozené hostitele a na onemocnění, která způsobují, společně s diagnostikou, léčbou a prevencí těchto nákaz. Součástí práce bude přesné geografické rozšíření původců nákaz včetně dokumentace proběhlých epidemií a systému surveillance
8 3. Hemoragické horečky 3.1. Obecná charakteristika Termín virová hemoragická horečka (VHF = viral haemorrhagic fever) je pouţíván pro popis závaţného horečnatého multisystémového onemocnění, které je provázeno krvácivými projevy hemoragií a moţným selháním ţivotně důleţitých orgánů. Hemoragii můţe způsobit zvýšená permeabilita cév, poškození a porušení funkcí krevních cév, krevních destiček nebo krevních bílkovin zodpovědných za sráţení krve. Velká hemoragie ohroţuje pacienta vykrvácením a vznikem šoku, opakovaná drobná krvácení vedou k anemii a nedostatku ţeleza (Vokurka a kol. 2002). Přesto hemoragie sama o sobě je zřídka ţivot ohroţující. Závaţnější bývají spíše multiorgánová selhání hemoragií způsobená (Khan a kol. 1997). Koncept virových hemoragických horeček jako infekčních agens, včetně některých jejich klinických, epidemiologických a geografických rozdílů, byl sestaven díky izolaci a charakterizaci asi tuctu virů způsobujících hemoragickou horečku (Kenyon a kol. 1994). Tyto viry rozdělujeme do několika různých čeledí, viz Tab. 1. Všechny patří mezi obalené, +ss nebo ss RNA viry, tedy do IV. nebo V. třídy (Khan a kol. 1997). Čeleď, třída Virus Onemocnění Rozšíření Togaviridae IV. třída (+ssrna) Flaviviridae IV. třída (+ssrna) Bunyaviridae V. třída (-ssrna) Arenaviridae V. třída (-ssrna) Filoviridae V. třída (-ssrna) Paramyxoviridae V. třída (-ssrna) Chikungunya Vzácně HF Afrika, Asie O nyong nyong Vzácně HF Afrika Ţlutá zimnice Vzácně HF Afrika, jiţní Amerika Dengue Dengue HF Asie, střední a jiţní Amerika, Afrika, Austrálie Omská hemoragická horečka Omská HF Jiţní Sibiř, Rusko Krymsko-konţská Asie, Afrika, jiţní a CCHF hemoragická horečka východní Evropa Rift Valley Někdy HF Afrika Skupina Hantavirů HFRS, HPS, EN Asie, Evropa, Amerika Junin Argentinská HF Argentina Machupo Bolivijská HF Bolívie Lassa Lassa HF Západní Afrika Marburg Marburg HF Střední Afrika Ebola Ebola HF Střední Afrika Nipah HF Malajsie Hendra HF Austrálie Tab. 1 Přehled virů způsobujících VHF. Upraveno podle Hubálek 2000, Khan a kol. 1997, Rajčáni a Čiampor
9 3.2. VHF jako zoonózy Všechny viry VHF jsou zoonózy, tedy nemoci přenosné z ţivočichů na člověka. Pravé zoonózy zpravidla nejsou přenosné z jednoho člověka na druhého, avšak právě VHF viry tvoří výjimku (např. ţlutá zimnice, Ebola, Lassa ). Přenos nákazy ze zvířete na člověka probíhá přímo (kontaktem, aerosolem i alimentárně), nebo prostřednictvím vektora, kterým bývají většinou krev-sající druhy členovců, Arthropoda (nejčastěji komár nebo klíště). Virům, které jsou přenášeny pomocí členovců, se říká arboviry (arthropod-borne viruses). Zdrojem nákazy je však většinou zvířecí nebo lidský organismus, který v období nakaţlivosti z těla vylučuje infekční agens. V případě VHF to jsou převáţně hlodavci, netopýři a kaloni, různí kopytníci, opice i člověk. V meziepizootickém období (kdy nedochází k výskytu ţádných epidemií) agens přeţívá ve svém přírodním rezervoáru, kterým jsou nejčastěji hlodavci, opice a kaloni (Hubálek 2000). Ekologické a geografické rozšíření je tedy jasně spjato s vektory a hostiteli virů. V nich viry překonávají velké vzdálenosti a snadno dosáhnou nových biotopů, kde vznikají nová ohniska nákazy (Hubálek 2000). Jak je vidět v Tab. 1, původci VHF se nevyhýbají ţádnému kontinentu, snad kromě Antarktidy, kde prozatím neproběhl dostatek výzkumů na toto téma (Khan a kol. 1997) Léčba a prevence VHF se objevují převáţně v oblastech, kde je lékařská péče a diagnostická infrastruktura roztříštěná, či úplně chybí. Sporadický výskyt jednotlivých případů onemocnění ţádný velký vědecký pokrok nepřináší, proto je pouze při epidemiích příleţitost ke zkoumání původců nákaz a populace, kterou napadají (Khan a kol.1997). To jsou důvody, proč tyto nemoci stále budí respekt a je tak obtíţné se s nimi vypořádat. V případě nákaz organismy způsobujícími tak závaţná onemocnění jako VHF je nejdůleţitější včasná diagnostika a izolace pacienta. Proti většině virů nejsou známy ţádné účinné vakcíny ani ţádná specifická léčba, pouze na některé viry (CCHF, Lassa ) zabírá ribavirin (a to často jen v brzkých stádiích nemoci) (Handy 2004). V některých případech pomáhá pasivní podávání protilátek získané ze séra rekonvalescentů, zdaleka ale ne u všech VHF (Rajčáni a Čiampor 2006). Proto obecně jedinou pomocí pro pacienty zůstává podpůrná a symptomatická léčba (Handy 2004)
10 Podpůrná terapie spočívá v udrţování dostatečného mnoţství tekutin v těle, protišokové léčbě, zabránění hemokoagulace a podpoře jater, ledvin, plic a srdce. Výběr dodávané tekutiny je třeba pečlivě zváţit, aby nedošlo k zhoršení pulmonárního či periferních edémů. Koagulopatie bývala léčena heparinem (jeho účinky ale byly sporné), dnes se spíše uţívají velké dávky acylpyrinu (Handy 2004, Rajčáni a Čiampor 2006). Dialýza je vyţadována při selhání ledvin a umělá plicní ventilace při plicní hemoragii či plicním edému (Handy 2004). Třemi základními kroky v boji proti zoonotickým nákazám jsou prevence, kontrola a eradikace. Prevence ochraňuje člověka před případným onemocněním (pomocí např. repelentů, očkování ). Kontrola má za cíl potlačit výskyt a incidenci nemoci (pomocí karantény, léčby ). Eradikace znamená úplné vymýcení patogena z oblasti (Hubálek 2000). Zoonotické nákazy vyţadují odlišný přístup k prevenci a jejich kontrole neţ běţná onemocnění. Je to způsobeno jejich přenosností ze zvířat na člověka a vzápětí také mezilidským přenosem (Murphy 2008). Tkáně a tělní tekutiny nakaţených mohou obsahovat velké mnoţství infekčních agens, proto je jakýkoliv kontakt s pacienty velice přísně monitorován. Ošetřující personál pak ohroţuje riziko nozokomiálních nákaz. Tyto důvody způsobily zavedení doporučeného postupu při kontaktu a léčbě VHF pacientů. Základní kroky postupu obsahují (Handy 2004): Okamţitě informovat hygienickou a epidemiologickou stanici. Izolovat pacienta a zajistit přísná protiinfekční preventivní opatření. Minimalizovat kontakt s veškerými pacientovými tělními tekutinami. Kontaktovat specializovanou laboratoř a odeslat jim vzorky. Zajistit vyšetření pacienta na malárii v místní laboratoři. Opakovaně pouţitelný materiál dezinfikovat pouţitím 0,5% roztoku chlornanu sodného nebo 0,5% fenolem, pokud je moţné, tak autoklávovat, převařit nebo spálit (VHF viry naštěstí nejsou vysoce chemicky a teplotně rezistentní). Před příchodem výsledků ze specializované laboratoře je nutná symptomatická léčba, při nejasné diagnóze podávat ribavirin (zvlášť v rané fázi nemoci). Cílem péče o pacienty trpící VHF tedy není pouze záchrana jejich ţivota (vyléčení nemoci a obrana před sekundárními bakteriálními a houbovými infekcemi), ale také ochrana ošetřujícího personálu a zabránění dalšímu šíření viru v prostředí
11 4. Čeleď Togaviridae 4.1. Virus Chikungunya Obecná charakteristika Chikungunya je virové onemocnění způsobené arbovirem Chikungunya z rodu Alphavirus a čeledě Togaviridae, antigenní komplex Semliki Forest (Ligon 2006). Genom je tvořen lineární +ssrna, průměrná velikost kapsidu je nm a virion má fosfolipidový obal (Pialoux a kol. 2007). Kompletní genom má délku nukleotidů (Ligon 2006, Sudeep a Parashar 2008). CHIK virus se vyskytuje ve třech různých liniích odlišujících se genotypovými i antigenními charakteristikami: Západoafrický, Východo-středo-jihoafrický a Asijský druh (Ligon 2006, Pialoux a kol. 2007, Sudeep a Parashar 2008). Název CHIK viru pochází z afrického dialektu Swahili nebo Makonde, ve kterém sloveso kungunyala znamená ohnutý, shrbený. To je způsobeno artralgií, která je typickým příznakem nemoci (Pialoux a kol. 2007, Sudeep a Parashar 2008). Onemocnění Virus CHIK způsobuje onemocnění s charakteristickými klinickými příznaky. Po 2 4 dnech klidu náhle přichází vysoké horečky, bolest hlavy a svalů, artralgie a artritida. Zhruba u 50% případů se objevují také koţní problémy jako makulopapulární vyráţka, otok obličeje, petechie a zejména u dětí odlupující se puchýřkovitá vyráţka (Pialoux a kol. 2007). Méně časté bývá zvracení, nevolnosti a fotofobie (Ligon 2006). U závaţných případů mohou vzácně nastat neurologické problémy (meningoencefalitida) a hemoragické projevy (od krvácení z nosu a dásní aţ po krvácení v GIT, melanémii, leukopénii a trombocytopénii), které mohou vést k šoku a poté ke smrti (Sudeep a Parashar 2008). Většina příznaků je závislých na daném kmeni viru, kterým pacient onemocněl (Pialoux a kol. 2007). Bolesti kloubů (artralgie) a artritida jsou nejvýznamnějšími znaky pacientů s CHIK, přestoţe u dětí se objevují vzácně. Krutými a vracejícími se bolestmi trpí především kolena, kotníky, zápěstí a malé klouby na rukou, nejvíce po ránu. I po vyléčení mohou bolesti přetrvávat, a to od několika měsíců aţ po několik let od uzdravení, coţ můţe pacienta silně vyčerpávat (Pialoux a kol. 2007, Sudeep a Parashar 2008). Průběh nemoci je překvapivě dobrý. Pokud nedojde ke komplikacím, dochází u pacienta po několika dnech ke spontánní úlevě (Rajčáni a Čiampor 2006). Po prodělání nemoci je člověk proti infekci dlouhodobě imunní (Ligon 2006). CHIK tedy není povaţována - 8 -
12 za smrtelné onemocnění, přesto v posledních letech vzrostl počet úmrtí. Ohroţenou skupinou jsou především staří lidé, malé děti a novorozenci, u kterých je průběh nemoci závaţnější. Nově byl dokonce zaznamenán přenos viru z matky na dítě v průběhu těhotenství, novorozeně pak přišlo na svět s vrozeným onemocněním. Případné jiné vlivy na plod však ještě nebyly prozkoumány (Bodenmann a Genton 2006, Pialoux a kol. 2007). Diagnostika onemocnění CHIK je zaloţena na klinických příznacích a na laboratorních metodách. Nejvyuţívanějšími metodami jsou RT-PCR a serologie (ELISA, komplement fixační reakce, imunofluorescence, inhibice hemaglutinace). RT-PCR lze vyuţít jiţ od prvního dne infekce, klasické serologické metody jsou ale jednodušší (Pialoux a kol. 2007). Dalšími metodami vyuţívanými především ve výzkumu jsou izolace viru, sekvencování a fylogenetické analýzy, produkce imunního séra a virus neutralizační testy (Powers a kol. 2000). Ekologie Virus má dva odlišné ţivotní cykly sylvatický, který probíhá mezi opicemi a stromovými komáry, a urbánní, který zahrnuje člověka a synantropní komáry (Hubálek 2000). V Asii převaţuje urbánní cyklus a v Africe sylvatický, v průběhu kterého jsou nakaţeni nehumánní primáti a další lesní zvířata (Sudeep a Parashar 2008). Vektorem jsou komáři podčeledě Culicinae, hlavně z rodu Aedes, Mansonia a Culex. V urbánním cyklu jsou nejvýznamnějšími vektory Ae. albopitctus (Obr. 1) a Ae. aegypti (Obr. 2), v sylvatickém cyklu jde především o komáry Ae. africanus, Ae. furcifer a Ae. taylori (Hubálek 2000, Sudeep a Parashar 2008). Přírodním rezervoárem viru jsou hlavně opice, hlodavci, ptáci a další obratlovci (Pialoux a kol. 2007). Obr. 1 Samička komára Ae. albopictus. Obr. 2 Samička komára Ae. Aegypti Převzato z Pialoux a kol Převzato z Pialoux a kol
13 Většina epidemií probíhá v období dešťů, při povodních nebo v oblastech s velkými otevřenými vodními plochami, kde je zvýšený výskyt komárů. V období sucha je pak výskyt niţší (Yoosuf a kol. 2009). První výskyt CHIK viru byl zaznamenán na plošině Makonde na hranicích mezi Tanzánií a Mosambikem v letech Virus se poté z východní Afriky rozšířil téměř do celé Afriky a jihovýchodní Asie, kde se stal endemickým, jak je vidět na Obr. 3. Další rozšíření především do Evropy je zprostředkováno nakaţenými turisty vracejícími se z dovolené v tropech domů (Sudeep a Parashar 2008). Obr. 3 Geografické rozšíření CHIK viru. Upraveno podle Sudeep a Parashar Region výskytu CHIK infekce je místo, kde se pravidelně vyskytuje i horečka dengue. Díky podobným klinickým příznakům se tak často usuzuje, ţe v mnoha případech mohlo dojít k mylné diagnostice viru dengue. Proto předpokládáme, ţe výskyt CHIK viru je mnohem vyšší, neţ jsou oficiálně udávaná čísla (Powers a kol. 2000). Epidemie : epidemie v jihovýchodní Africe při níţ byl virus poprvé popsán
14 1958: první výskyt viru v Asii Bangkok, následován dalšími případy v Kambodţi, Malajsii, Vietnamu a na Taiwanu. 1963: první výskyt v Indii epidemie v Kalkatě a západním Bengálsku si vyţádala téměř 200 ţivotů, hlavně dětí (Sudeep a Parashar 2008) : první epidemie v Indonésii, která se rozšíříla na většinu ostrovů : 24 samostatných epidemií bylo zaznamenáno v Indonésii, CHIK se zde vyskytla po téměř 20 letech (Ligon 2006). Od 2005: propuknutí epidemie na ostrovech Indického oceánu, která trvá dodnes. Významný výskyt byl na ostrovech Reúnion, Madagaskar, Mauricius, Mayotte, na Maledivách, Seychellách, v Malajsii s dosahem aţ do Hong Kongu a Indie (Ligon 2006, Yoosuf a kol. 2009). Byly zaznamenány případy importované infekce u turistů z Francie, Německa, Švýcarska, Norska, Číny a Francouzské Guyany (Bodenmann a Genton 2006, Ligon 2006). Byl popsán také první případ introdukce CHIK viru u české turistky, která se nakazila při pobytě na ostrově Mauricius. Byla však vyléčena bez následků (Zelená a kol. 2006). Celá tato epidemie je významná především svou velikostí, novými dosud nepopsanými symptomy a častými úmrtími (Sudeep a Parashar 2008). 2007: první epidemie horečky CHIK v Evropě propukla v Itálii v oblasti Ravenna. Laboratorně bylo potvrzeno přes 200 případů Východo-středo-jihoafrického kmene CHIK viru, pouze jeden byl smrtelný (Rezza a kol. 2007). Léčba a prevence Dosud nebyla nalezena ţádná účinná specifická léčba, proto je vyuţívána pouze podpůrná terapie potlačující symptomy onemocnění. Podávány jsou analgetika bez kyseliny salicylové, antipyretika a protizánětlivé léky neobsahující steroidy (Ligon 2006, Pialoux a kol. 2007). Při bolestech jsou pouţívána mírná sedativa. Hydratace pacienta je udrţována intravenózně (pokud je to nutné), v případě hemoragie je zásadní zabránit cévní nestabilitě (Ligon 2006). V dnešní době není k dispozici ţádná komerčně dostupná vakcína. V minulosti jiţ byly některé vakcíny testovány na lidech, definitivní verze je ale stále ve fázi příprav (Pialoux a kol. 2007). Jedinou účinnou ochranou před CHIK infekcí je chránit se před komářím štípnutím a kontrolovat výskyt vektorů. Individuální ochrana zahrnuje pouţívání moskytiér, repelentů,
15 udrţování malých kouřících ohníčků k odplašení komárů a nošení oblečení s dlouhými rukávy (Ligon 2006). Před cestováním do tropických oblastí by se měli turisté informovat o epidemiologickém riziku a zvlášť opatrné by měli být těhotné ţeny, lidé starší 70 let a malé děti (Bodenmann a Genton 2006) Virus O nyong nyong Obecná charakteristika O nyong nyong je virové onemocnění způsobené arbovirem O nyong nyong rodu Alphavirus z čeledě Togaviridae, seroskupina Semliki Forest. Virion má průměr nm a je obalen lipidovou membránou s transmembránovými glykoproteiny. Genom je tvořen lineární +ssrna obsahující přibliţně bazí. Dle dřívějších výzkumů (sekvencování nukleových kyselin, zkříţená neutralizace a mapování monoklonálních protilátek) se ukázalo, ţe ONN virus je velice blízce příbuzný CHIK viru, geneticky jsou však odlišné (Lanciotti a kol. 1998). Onemocnění Po maximálně 10 denní inkubační době přichází horečnaté onemocnění, pro které jsou charakteristické bolesti hlavy, kloubů (symetrická polyartralgie), nízká horečka, lymfadenopatie a papulární nebo makulopapulární vyráţka (Vanlandingham a kol. 2005). Méně často se přidruţuje hemoragie z nosu, úst nebo GIT (Rajčáni a Čiampor 2006). Letalita je velmi nízká (Hubálek 2000). Diagnostika ONN viru je zaloţena na klinických příznacích a především na laboratorních metodách. Nejvíce vyuţívanými metodami jsou RT-PCR, ELISA a izolace viru z krve (Lanciotti a kol. 1998, Rajčáni a Čiampor 2006). Ekologie Vektorem ONN viru jsou komáři podčeledě Anophelinae, rodu Anopheles, především An. funestus a An. gambiae (Brault a kol. 2004, Hubálek 2000, Lanciotti a kol. 1998). Přírodní rezervoár viru dosud není znám, ale předpokládá se, ţe člověk je z řady obratlovců jediným přirozeným hostitelem viru (Lanciotti a kol. 1998, Powers a kol. 2000). Poprvé se ONN virus objevil a byl diagnostikován roku 1959 v Gulu, v severní Ugandě. Odtud se v následujících letech rozšířil po celé střední a východní Africe, která je
16 jediným místem výskytu ONN (Lanciotti a kol. 1998). Virus se vyskytuje sporadicky, ale jím způsobené epidemie jsou pak velmi rozsáhlé (Vanlandingham a kol. 2005). Epidemie : první epidemie ONN viru v severní Ugandě, která se rozšířila do sousední Keni, Tanzanie, Zairu, Malawi, Mosambiku a Senegalu. Byly nakaţeny 2 miliony lidí, nebyl však evidován ţádný smrtelný případ (Brault a kol. 2004, Lanciotti a kol. 1998). 1996: návrat epidemie v jiţní Ugandě po 35 letech v oblastech Rakai, Masaka a Mbarara, evidovány stovky případů (Hubálek 2000, Lanciotti a kol. 1998). 2002: epidemie ve střední Ugandě v blízkosti jezera Wamala v oblasti Mubende (Vanlandingham a kol. 2005). Léčba a prevence Není známa ţádná specifická léčba proti ONN viru, nadále je tedy uţívána základní symptomatická a podpůrná terapie. Při bolestech kloubů jsou podávána příslušná analgetika a nesteroidní antirevmatika. Vakcína proti ONN viru dosud nebyla vyvinuta (Rajčáni a Čiampor 2006). Důleţitou součástí ochrany před infekcí způsobenou arboviry je především individuální boj s komáry, který spočívá v častém pouţívání repelentů a moskytiér. Nedílnou součástí prevence je také informovanost o epidemiologické situaci v rizikové oblasti (Rajčáni a Čiampor 2006)
17 5. Čeleď Flaviviridae 5.1. Virus ţluté zimnice Obecná charakteristika Závaţné onemocnění způsobující virus ţluté zimnice řadíme do čeledě Flaviviridae, rodu Flavivirus a seroskupiny virů ţluté zimnice (Pacca a kol. 2009, Rajčáni a Čiampor 2006). Genom je tvořen lineární +ssrna a obsahuje nukleotidů (Pisano a kol. 1997). Velikost oválného virionu je průměrně nm (Ţemla a kol. 1998). Molekulární epidemiologická data naznačují existenci 7 genotypů viru YF, které jsou různě geograficky rozšířené a tím jsou i jednotlivé epidemie vţdy spojeny s jedním genotypem (Barrett a Higgs 2007). Virus byl poprvé vyizolován roku 1927 z nakaţeného muţe v Ghaně a stal se prototypovým kmenem jménem Asibi (Staples a Monath 2008, Wilson a kol. 2004). Onemocnění Po inkubační době trvající 3 6 dnů přichází náhle horečka, zimnice, bolesti svalů, hlavy, v bedrech a kříţi, virémie a neutropenie. Během několika dnů aţ týdne se přidává celková tělesná slabost, nevolnosti, zvracení, bolesti v podbřišku a ţloutenka (Monath 2008). Při těţkém průběhu nemoci můţe dojít k multiorgánovému selhání, které je způsobeno váţným poškozením jater a jejich kolapsem, selháním ledvin, nestabilitou krevního oběhu a syndromem šoku, často s hemoragií (krvácení především z nosu a dásní, tmavé zvratky s krví) (Heraud a kol. 1999). Tento stav pak vede často ke smrti. Právě poškození jater je hlavní znak odlišující YF od ostatních HF. Mortalita pacientů YF se pohybuje mezi % (Monath 2008). Diagnostika onemocnění je zaloţena na klinických příznacích a laboratorních testech. Nejvyuţívanějšími metodami jsou RT-PCR a ELISA (Herauld a kol. 1999, Onyango a kol. 2004). Ekologie Virus YF je schopen dvou různých cyklů přenosu. Primární sylvatický cyklus zahrnuje nehumánní primáty a stromové komáry, zatímco urbánní cyklus je zaměřen na člověka a synantropní komáry. Vektorem jsou nejčastěji samičky komárů čeledě Culicidae (Onyango a kol. 2004). V urbánním cyklu je nejvýznamnější komár Ae. aegypti, v sylvatickém pak různí
18 zástupci rodu Haemagogus (v Jiţní Americe) a Aedes (v Africe) (Heraud a kol. 1999, Hubálek 2000, Onyango a kol. 2004). Člověk se nakazí v sylvatickém cyklu pouze náhodně, např. při práci v lese poštípáním stromovými komáry. Z takto nakaţeného jedince se ale uţ urbánním cyklem šíří nákaza dále (Ţemla a kol. 1998). Přírodním rezervoárem viru v obratlovcích jsou opice, tropičtí lesní savci a vačice, v urbánním cyklu je hostitelem člověk (Heraud a kol. 1999, Hubálek 2000). Virus YF je geograficky rozšířen v tropických státech Afriky (viz Obr. 4) a Střední a Jiţní Ameriky (viz Obr. 5). Původně nejspíš virus pochází z Afriky a do Ameriky byl přenesen aţ po jejím objevení (Pacca a kol. 2009, Pisano a kol. 1997). První výskyt YF v Novém Světě byl popsán roku 1648 v Májských rukopisech, avšak v Africe se virus vyvinul z jiných arbovirů asi před 3000 lety. Od té doby proběhlo mnoho významných i menších epidemií (Pacca a kol. 2009). Obr. 4 Výskyt YF v Africe k Obr. 5 Výskyt YF v Jiţní Americe k Upraveno podle Wilson a kol Upraveno podle Wilson a kol Epidemie 18. a 19. století: častý výskyt epidemií v amerických tropech, pobřeţních městech Severní Ameriky a v Evropě (Staples a Monath 2008)
19 1900: epidemie na Kubě v průběhu války se Španělskem, kdy mnohem více vojáků zemřelo na YF neţ v bitvě. Do dvou let se podařilo epidemii eliminovat (Hubálek 2000, Staples a Monath 2008). Od roku 1940: pravidelná propuknutí epidemií YF ve východní Africe : největší dosud proběhlá epidemie, v Etiopii bylo zaznamenáno případů (Onyango a kol. 2004, Sanders a kol. 1996). 1978: epidemie v Gambii s 1600 smrtelných případů z celkového počtu : výskyt v Nigérii z 1450 případů bylo 565 smrtelných (Hubálek 2000) : epidemie v Keni s 30% úmrtností (Sanders a kol. 1996). 2007: výskyt YF v Bolívii, Brazílii, Kolumbii, Peru, Burkina Faso, Kamerunu, Mali, Senegalu a Togo (WHO 2009a). Léčba a prevence V současnosti není ţádný specifický lék, který by na YF s jistotou působil. Vyuţívá se tedy intenzivní podpůrná a symptomatická léčba. Byly také prováděny testy s ribavirinem, který by mohl být účinný při podání v brzké fázi onemocnění (Monath 2008). Jako jedinou spolehlivou ochranou před YF se ukázala vakcinace. Dnes pouţívanou vakcínou je atenuovaný (oslabený) kmen 17D, který je efektivní proti všem sedmi známým genotypům YF. Vakcína je komerčně dostupná a dosud s ní bylo očkováno více neţ 400 milionů lidí (Wilson a kol. 2004). V ojedinělých případech se můţe oslabený virus dostat do nervového systému a způsobit meningoencefalitidu. Proto by se neměly očkovat děti mladší 6 měsíců, důchodci a imunodeficientní osoby (Monath 2008). Některé vlády v endemických oblastech vyţadují povinné očkování i pro turisty vstupující do země, jiné alespoň očkování doporučují. Důvodem je riziko nakaţení se YF a poté přenesení infekce do jiných oblastí a také poměrně vysoká úmrtnost infikovaných neočkovaných turistů (Wilson a kol. 2004) Virus Dengue Obecná charakteristika Horečku dengue nebo hemoragickou horečku dengue způsobuje arbovirus Dengue rodu Flavivirus z čeledě Flaviviridae, který má čtyři serotypy: DEN-1, DEN-2, DEN-3 a DEN-4 (Edelman 2005, Gubler 1998). Genom viru je tvořen lineární +ssrna o délce
20 přibliţně nukleotidů (Guzmán a Kourí 2004). Sférický virion je relativně malý (40 50 nm) a má lipidový obal (Gubler 1998). Onemocnění Dengue je v dnešní době nejrozšířenějším a nejzávaţnějším arbovirovým onemocněním, které známe (Wilder-Smith a kol. 2009). Nemoc můţe probíhat asymptomaticky, jako mírné horečnaté onemocnění (nejčastěji u dětí), klasická horečka dengue nebo ţivot ohroţující hemoragická horečka se syndromem šoku (Edelman 2005, Gubler 1998, Guzmán a Kourí 2004). Klasická horečka dengue je onemocnění především starších dětí a dospělých. Inkubační doba po štípnutí infikovaným komárem je 4 aţ 7 dnů, poté následuje nečekaný nárůst teploty (38 41 C), bolest hlavy, svalů, kloubů, slabost, nevolnost, zvracení, fotofobie a zánět spojivek (Bulugahapitiya a kol. 2007, Gubler 1998, Rajčáni a Čiampor 2006). Vysoká horečka přetrvává 3 7 dnů a často je dvoufázová po poklesu se do 24 hodin zase vrátí (Gubler 1998). Koţní projevy se objevují u více neţ poloviny pacientů a mohou být také dvoufázové. Poprvé se objevuje zarudnutí kůţe ještě před nástupem horečky a podruhé (častěji) makulární nebo makulopapulární vyráţka na 2. aţ 6. den nemoci, která trvá další 2 3 dny. V některých případech se mohou objevit petechie, méně běţné je krvácení z nosu, dásní a GIT (Bulugahapitiya a kol. 2007, Gubler 1998). Průběh onemocnění provází nedostatek trombocytů a bílých krvinek. Akutní fáze nemoci trvá většinou do 7 dnů, rekonvalescence se ale můţe protáhnout i na několik týdnů. Fatální případy jsou u klasické horečky dengue zřídkavé (Gubler 1998). Hemoragická horečka dengue s šokovým syndromem je v první fázi nemoci těţko rozeznatelná od klasické horečky dengue či jiných HF. Nejpozdějí do 24 hodin od poklesu teploty však přichází kritická fáze, která uţ je snadno diagnostikovatelná. Nejčastějším projevem jsou petechie, potom také purpura (tečkovité krvácení do kůţe, sliznic a vnitřních orgánů), podlitiny, krvácení z nosu a dásní. Pokoţka pacienta je studená a oteklá, puls zrychlený a slabý, objevuje se trombocytopenie a leukopenie (Gubler 1998, Rajčáni a Čiampor 2006). Ve velmi závaţných případech trpí pacient rozsáhlým krvácením do GIT, s čímţ je také spojeno zvracení sraţené krve podobné kávové sedlině (Gubler 1998). Bez včasné diagnózy a odborné péče se můţe u pacienta rozvinout šok. Ten je způsoben především nedostatkem plasmy, která kvůli zvýšené permeabilitě cév přechází do mimocévních prostor (Bulugahapitiya a kol. 2007, Gubler 1998). Trvání šoku bývá krátké: buď pacient do 24 hodin podlehne anebo je vyléčen díky intenzivní protišokové terapii
21 Období rekonvalescence pak probíhá rychle, obvykle 2 3 dny. Úmrtnost pacientů s šokem dosahuje aţ 20%, při včasné léčbě je však menší neţ 1% (Gubler 1998). Včasná diagnostika původce nemoci je pro přeţití pacienta rozhodující. Kromě klinických, geografických a epidemiologických dat je důleţitá laboratorní diagnostika. V rutinní praxi jsou nejvíce vyuţívány serologické metody (hlavně ELISA), pak také izolace viru, PCR a RT-PCR (Guzmán a Kourí 2004). Ekologie Virus Dengue se přenáší sylvatickým cyklem spojeným s opicemi a komárem druhu Ae. niveus (Hubálek 2000) a urbánním cyklem spojeným s člověkem a jinými komáry rodu Aedes (podčeleď Culicinae). Nejvýznamnějším vektorem je Ae. aegypti, dalšími pak např. Ae. albopictus a Ae. polynesiensis. Samičky těchto komárů sají nejraději v uzavřených prostorách 2 3 hodiny po úsvitu a 2 3 hodiny před soumrakem (Gubler 1998). Virus se můţe přenášet transovariálním i sexuálním přenosem a také krevní transfuzí (Hubálek 2000, Wilder-Smith a kol. 2009). Hlavním přírodním rezervoárem viru je člověk, ačkoli nehumánní primáti v Africe a Asii mohou být také nakaţeni (Bulugahapitiya a kol. 2007). Geografické rozšíření viru Dengue je spjato s jeho hlavním vektorem Ae. aegypti, postiţenou oblastí jsou tedy tropy a subtropy na celém světě, viz Obr. 6. Infekce byla zaznamenána ve více neţ 100 státech světa (Wilder-Smith a kol. 2009), především v jiţní a jihovýchodní Asii, střední Africe a Střední a Jiţní Americe (Rajčáni a Čiampor 2006). Obr. 6 Celosvětová distribuce viru Dengue v roce Upraveno podle Bulugahapitiya a kol
22 Do celosvětových tropů se virus i vektor rozšířili v průběhu 18. a 19. století díky expandující lodní i suchozemské dopravě. Dynamika přenosu a vzniku epidemií se významně zvýšila po 2. světové válce v jihovýchodní Asii (Gubler 2002). Zde se virus do 20 let rozšířil takovým způsobem, ţe způsobil pandemii tropů (Hubálek 2000). Epidemie : epidemie v Austrálii. 1928: výskyt dengue v Evropě v Řecku (Hubálek 2000) : první známá epidemie HF dengue proběhla na Filipínách v Manile (Gubler 2002). 60. a 70. léta 20. století: v Americe je sporadický výskyt epidemií dengue díky programu eradikace komára Ae. aegypti v celé oblasti Střední a Jiţní Ameriky. V 70. letech byl program úspěšně ukončen a tak se Ae. aegypti opět vrátil a s ním postupně i výskyt dengue v celé oblasti (Gubler 1998) : opět vysoký počet případů v Americe, např. na Kubě za rok 1981 zaznamenáno případů (Hubálek 2000). 1997: první případy dengue v Argentině od roku Eradikace po tak douhou dobu byla pouze dočasná díky návratu Ae. aegypti (Avilés a kol. 1999). 1998: pandemie horečky dengue a HF dengue v 56 zemích s více neţ 1,2 milionu případů. Jen v Indonésii bylo zaznamenáno případů, z toho 1414 smrtelných (WHO 2004). 2008: výskyt viru DEN-3 v Africe v Pobřeţí slonoviny. Do té doby v Africe kolovaly především serotypy DEN-1 a DEN-2. Od 80. let 20. století byl zaznamenán zvýšený výskyt epidemií a i v Africe začíná HF dengue nabývat na významu (WHO 2009b). Léčba a prevence Dosud nebyla nalezena ţádná specifická léčba proti viru Dengue, proto je vyuţívána podpůrná symptomatická terapie. Podávána jsou antipyretika, plasma či krevní transfuze a zavedena jsou veškerá protišoková opatření. Důleţitá je včasná diagnostika onemocnění, jinak pacientovy šance na přeţití rychle klesají (Bulugahapitiya a kol. 2007). Vakcína proti viru Dengue je stále ve výzkumu, zatím ale nebyla nalezena ţádná spolehlivá očkovací látka. Pacient, který úspěšně překonal infekci virem Dengue má v těle trvale vytvořeny protilátky, nemůţe se tedy znovu stejným serotypem nakazit. Bohuţel
23 protilátky nepůsobí na ostatní serotypy, jeden člověk tedy můţe překonat aţ čtyři horečky dengue za ţivot (Edelman 2005, Gubler 1998). Opakovaná infekce však zvyšuje riziko vzniku syndromu HF a šoku, budoucí vakcína by tedy měla navodit imunitu proti všem 4 serotypům najednou (Rajčáni a Čiampor 2006). Úspěšná prevence je základem ochrany před rozšířením viru dengue do dalších oblastí jako je Evropa a Severní Amerika. V boji s komáry lze vyuţít insekticidy působící na dospělé jedince, účinnější je ale redukce počtu larev komárů. Toho lze dosáhnout vysoušením kaluţí a čistěním nádrţí na stojatou vodu nebo jejich úplným odstraněním, čímţ bude zničeno prostředí pro vývoj larev. Pouţívání repelentů, ochranného oblečení a moskytiér je samozřejmostí, pobyt v klimatizovaných místnostech můţe také sníţit riziko přítomnosti komárů. V endemických oblastech je nutný funkční systém surveillance zaloţený na spolupráci veškerého zdravotnického a odborného personálu (Gubler 1998) Virus omské hemoragické horečky Obecná charakteristika Omská hemoragická horečka je způsobena virem omské hemoragické horečky, který řadíme do čeledě Flaviviridae, rodu Flavivirus a serologické skupiny klíšťové encefalitidy (Li a kol. 2004). OHF virus je jedním ze tří virů této seroskupiny, které způsobují hemoragii, a jako jediný způsobuje minimální nebo ţádné neurologické komplikace (Lin a kol. 2003, Volk a kol. 2006). Genom je tvořen lineární +ssrna obsahující přibliţně nukleotidů (Gritsun a kol. 1993). Velikost virionu je do 50 nm a je obalen lipidovou membránou, do které jsou vnořeny proteiny a glykoproteiny (Rajčáni a Čiampor 2006, Volk a kol. 2006). OHF virus má dva antigenní podtypy: kmen Kubrin (podtyp I) a kmen Bogoluvovska (podtyp II) (Li a kol. 2004). Onemocnění Po inkubační době 2 aţ 10 dnů propuká dvoufázové horečnaté onemocnění. První nástup horečky trvá 5 12 dnů a s ním přichází bolesti hlavy, svalů, kašel, dehydratace, zánět spojivek, papulovezikulární vyráţka na měkkém patře, podlitiny, překrvený obličej a trup, lymfadenopatie a zvětšení sleziny (Borio a kol. 2009, Holbrook a kol. 2005, Lin a kol. 2003). Druhé horečnaté období se projevuje dnů po infekci. Často se objevuje hemoragický syndrom provázený krvácením z nosu, dásní, dělohy a plic (Holbrook a kol. 2005). Ve
24 výjimečných případech se můţe rozvinout pneumonie nebo neurologické obtíţe (Borio a kol. 2009). Úmrtnost na OHF je relativně nízká, pohybuje se mezi 0,5 aţ 3 % (Li a kol. 2004, Lin a kol. 2003). Laboratorní diagnostika je zaloţena na serologických metodách (ELISA) a na izolaci viru (Rajčáni a Čiampor 2006). Ekologie OHF virus je přenášen jeho hlavním vektorem klíštětem Dermacentor reticulatus a také druhem Dermacentor marginatus z čeledě Ixodidae. Přenos viru klíšťaty rodu Ixodes se povaţuje za nepravděpodobný (Holbrook a kol. 2005, Li a kol. 2004). Přírodním rezervoárem viru ve zvířatech jsou hlodavci jako ondatra a hryzec vodní, virus byl ale izolován i z různých savců, obojţivelníků a plazů ţijících v endemické oblasti (Holbrook a kol. 2005). Transovariální přenos pravděpodobně nehraje ţádnou roli v přenosu viru, protoţe virus dlouhodobě přeţívá v dospělých jedincích klíšťat a transstadiální přenos byl také zaznamenán. Člověk můţe být nakaţen téţ poţitím mléka infikovaných zvířat a stykem s jejich mrtvými těly (Lin a kol. 2003). Virus byl izolován i z vody a infikovaných vodních ţivočichů, kteří v ní ţili. Proto se předpokládá, ţe virus je v prostředí velmi stabilní (Holbrook a kol. 2005). Přenos z člověka na člověka nebyl zaznamenán (Borio a kol. 2009). Virus OHF je endemický v malé oblasti ve střední Sibiři, konkrétně v Omské a Novosibirské oblasti (Li a kol. 2004, Lin a kol. 2003). Epidemie 1928: zavlečení ondater do místní biocenózy. Od té doby se objevují sporadické případy onemocnění spojené s přenosem z ondater na člověka (Gritsun a kol. 1993). 1947: první izolace OHF viru z muţe na Sibiři, který trpěl hemoragií, v průběhu epidemie v Omské oblasti (Gritsun a kol. 1993, Li a kol. 2004). 1998: za celý rok zaznamenáno pouze 7 případů v Novosibirské oblasti, z toho byly 3 závaţné a 1 smrtelný (Netesov a Conrad 2001). Léčba a prevence Specifická léčba dosud nebyla vyvinuta. Nejdůleţitější je tedy podpůrná a symptomatická terapie, která zahrnuje především doplňování tekutin v těle. Účinná vakcína přímo proti OHF taktéţ není dostupná. Vysoce ohroţeným skupinám však můţe být podána
25 vakcína proti klíšťové encefalitidě, která také navozuje imunitu proti OHF viru (Borio a kol. 2009, Hubálek 2000). Ohroţenou skupinou jsou lovci ondater, kteří jsou často od infikované zvěře nakaţeni, proto je nutné bránit se styku s uhynulými zvířaty. Běţnější je však přenos od klíštěte, proto je důleţitější kontrola výskytu a ochrana před těmito členovci. V endemických oblastech by lidé měli pouţívat repelenty a ochranné oblečení (Li a kol. 2004, Lin a kol. 2003). OHF virus je zařazen do kategorie biologické ochrany biohazard 4 (Lin a kol. 2003)
26 6. Čeleď Bunyaviridae 6.1. Virus krymsko-konţské hemoragické horečky Obecná charakteristika Krymsko-konţská hemoragická horečka je onemocnění způsobené virem CCHF z čeledě Buynaviridae a rodu Nairovirus patřící do seroskupiny viru krymsko-konţské hemoragické horečky (Ergönül 2006, Whitehouse 2004). Genom je tvořen třemi segmenty lineární ssrna (Ergönül 2006, Weber a Mirazimi 2008). Virion má v průměru 100 nm a je obalen lipidovou membránou 5 7 nm silnou, kterou prostupují dva glykoproteiny vytvářející na povrchu nenápadné výběţky (Whitehouse 2004). Antigenní struktury CCHF virů vyskytujících se v různých geografických oblastech se vyznačují velkou genetickou diverzitou. V Africe kolují viry ze tří vývojových větví, v Asii také ze tří a v Evropě ze dvou vzájemně málo příbuzných kmeny objevující se na Balkáně, v Rusku a Turecku se významně odlišují od kmenu izolovaného v Řecku (Ergönül 2006). V průběhu 2. světové války byli vojáci na Krymu nakaţeni Krymskou hemoragickou horečkou. O několik let později se ukázalo, ţe virus je identický s virem Kongo, který byl izolován v Belgickém Kongu a Ugandě. Od té doby je virus nazýván virem krymsko-konţské hemoragické horečky (Ergönül 2006, Whitehouse 2004). Onemocnění CCHF je druhým nejrozšířenějším arbovirovým onemocněním, hned po viru horečky dengue (Weber a Mirazimi 2008). Průběh nemoci se vyznačuje čtyřmi fázemi: inkubace, prehemoragie, hemoragie a rekonvalescence, které jsou znázorněny na Grafu 1 (Ergönül 2006, Whitehouse 2004). Inkubační fáze, která následuje po kousnutí klíštětem, po styku s krví nebo tkáněmi nakaţeného zvířete nebo s infikovaným člověkem, je obvykle krátká trvá 3 7 dnů (Ergönül 2006). Přesná délka nejpravděpodobněji závisí na způsobu přenosu infekce a na mnoţství inokula (Weber a Mirazimi 2008). Prehemoragická fáze je charakterizována náhlým nástupem vysoké horečky (39 41 C), která přetrvává 4 12 dnů. Přidává se bolest hlavy, svalů, břicha a zad, zimnice, závrať a fotofobie. Dalšími méně častými příznaky jsou nevolnosti, zvracení a ztráta apetitu (Ergönül 2006, Whitehouse 2004), běţněji se vyskytuje překrvení obličeje, krku, hrudi, očního bělma a zánět spojivek. Celá fáze trvá průměrně 3 dny (Ergönül 2006)
27 3 6 dnů od počátku onemocnění nastává hemoragická fáze, která trvá 2 3 dny. Rozsah hemoragie je od petechií po velké podlitiny vyskytující se na kůţi a mukózních membránách. Často se vyskytuje krvácení z nosu, dásní, GIT, urogenitálního a dýchacího traktu, ve váţných případech také krvácení do mozku (Ergönül 2006, Whitehouse 2004). Charakteristické jsou tmavé zvratky podobné kávové sedlině (Whitehouse 2004). Zhruba u 30% případů se objevuje zvětšení sleziny nebo jater (Weber a Mirazimi 2008). Fáze rekonvalescence začíná dní po nástupu nemoci a často vyţaduje setrvání v nemocnici. Obecně je charakterizována slabostí, nevolností, labilním pulzem, polyneuritidou, dočasným vypadáním všech vlasů, dýchacími problémy, oslabením zraku, ztrátou sluchu a paměti (Ergönül 2006, Whitehouse 2004). Tyto problémy jsou zřídka trvalé, mohou ale přetrvávat po dobu jednoho i více let (Whitehouse 2004). Graf 1 Klinický a laboratorní vývoj CCHF. Upraveno podle Ergönül Míra úmrtnosti CCHF je velmi variabilní a liší se od místa epidemie i způsobu přenosu. Průměrně se pohybuje kolem 30%. Byly ale zaznamenány i epidemie s aţ 80% mortalitou. U nozokomiálních nákaz je úmrtnost průměrně také vyšší, neţ kdyţ dojde k přímému přenosu z klíštěte. Přesný důvod však není dosud znám. U pacientů, u kterých došlo k úmrtí, se většinou na infekci nevytvořila ţádná imunitní odpověď (Whitehouse 2004). Diagnostika je zaloţena na klinických příznacích, anamnéze a laboratorních testech. Nejvyuţívanějšími jsou RT-PCR, ELISA a izolace viru (Ergönül 2006)
28 Ekologie Vektorem CCHF viru jsou klíšťata podčeledě Ambylomminae, především druhy Hyalomma marginatum, Hyalomma anatolicum a Dermacentor marginatus (Ergönül 2006, Hubálek 2000). Virus byl laboratorně izolován z mnoha různých rodů, jako např. Hyalomma, Dermacentor, Rhipicephalus, Ornithodoros, Boophilus a Ixodes, to však nemusí znamenat, ţe všechny zmíněné rody fungují běţně jako vektory. To by muselo být potvrzeno také výskytem při nějaké epidemii. Zvýšený výskyt klíšťat a tím i CCHF bývá často zaznamenán, kdyţ je v dubnu a květnu neobvykle teplo (Ergönül 2006). Cirkulace viru v prostředí je charakterizována endemickým cyklem klíště obratlovec klíště. Přenos infekce však probíhá i bez vektora, tedy ze zvířete na člověka a pak z jednoho člověka na druhého. Nejčastějším zdrojem viru v obratlovcích (u kterých byly nalezeny protilátky) jsou koně, osli, kozy, ovce, skot, zajíci a jeţci. U zvířat však CCHF virus nezpůsobuje ţádné onemocnění (Ergönül 2006, Whitehouse 2004). Z virů přenášených klíšťaty má CCHF největší geografické rozšíření. Výskyt byl zaznamenán ve více jak 30 zemích Afriky, Asie, jihovýchodní Evropy a Středního Východu, jak je znázorněno na Obr. 7 (Whitehouse 2004). Obr. 7 Celosvětová distribuce CCHF viru. Upraveno podle Ergönül Epidemie 12. století: v oblasti dnešního Tádţikistánu výskyt hemoragického syndromu, který bychom dnes popsali jako CCHF (Whitehouse 2004) : první novodobá epidemie na poloostrově Krym v průběhu 2. světové války, kdy bylo nakaţeno asi 200 sovětských vojáků
29 1956: epidemie CCHF v Belgickém Kongu (dnešní Demokratická republika Kongo) a Ugandě (Ergönül 2006, Whitehouse 2004). 1965: epidemie v Číně, v průběhu které dosáhl počet fatálních případů 80% (Ergönül 2006). 1990: první případy CCHF v Saudské Arábii v okolí Mekky. K onemocnění člověka došlo ve všech případech přenosem ze zvířete a ne kousnutím klíštěte (El-Azazy a Scrimgeour 1997) : epidemie ve Spojených Arabských Emirátech s mortalitou téměř 73% (Whitehouse 2004). 1995, 2001, 2004: výskyt CCHF v Kosovu, dohromady bylo serologicky prokázáno 186 případů, z toho 27 % bylo fatálních (Ahmeti a Raka 2006, Papa a kol. 2002) : první výskyt CCHF v Turecku s mortalitou přibliţně 5 % a s více neţ 1000 zaznamenaných případů (Elaldi a kol. 2009, Ergönül 2008). Léčba a prevence K léčbě CCHF se jako u jiných HF vyuţívá symptomatická a podpůrná terapie. Ta spočívá v podávání látek ovlivňujících koagulaci a nesteroidních protizánětlivých léků. Nutná je také kontrola trombocytů a erytrocytů a podávání čerstvé mraţené plasmy. Někdy je vyţadována substituční terapie doplňující chybějící látky v krvi. Uţ delší dobu je také vyuţíván ribavirin (inhibuje replikaci RNA), který je nejvíce uţitečný v brzkých fázích onemocnění, jako profylaxe při nozokomiálních nákazách a pro zdravotnický personál. Jeho účinky se nadále prověřují, v názorech na léčbu ribavirinem se totiţ odborníci liší. Úspěšné byly také pokusy s podáním imunního séra od vyléčených dárců pacienti ve váţném stavu byli zcela uzdraveni (Ergönül 2008). Vakcína proti CCHF viru byla vyvinuta roku 1974 a byla zkoušena na dobrovolnících v Bulharsku, u kterých vyvolala tvorbu protilátek. Nebyl však proveden dostatek pokusů na efektivitu vakcíny a její výroba a produkce je sloţitá, její běţné uţívání je tedy nepravděpodobné (Ergönül 2006, Ergönül 2008, Whitehouse 2004). Základem prevence v endemických oblastech je ochrana před klíšťaty pomocí oblečení a repelentů. Zvlášť ohroţeni jsou pak pracovníci na farmách a jatkách a zdravotnický personál, který můţe přijít do styku s krví a tkáněmi infikovaných jedinců. Jmenovaní musí pouţívat rukavice, roušky, brýle a ochranný oděv (Ergönül 2006). Kvůli vysoké nakaţlivosti
30 viru a schopnosti přenášet se aerosolem nebo kapénkovou infekcí byl CCHF virus zařazen do kategorie biologické ochrany biohazard 4 (Whitehouse 2004) Virus horečky Rift Valley Obecná charakteristika Horečka Rift Valley je zoonotické onemocnění způsobené arbovirem Rift Valley z čeledě Bunyaviridae a rodu Phlebovirus. Genom viru je tvořen třemi segmenty lineární ssrna (Aradaib a kol. 2008, Sherman a kol. 2009). Sférický virion o velikosti nm (Rajčáni a Čiampor 2006) je obalen lipidovou membránou obsahující dva druhy transmembránových glykoproteinů (Sherman a kol. 2009). Název onemocnění vznikl roku 1930, kdy byl popsán první prokázaný případ RVF. Epidemie proběhla na farmě v oblasti Great Rift Valley v Keni a byla nakaţena jak zvířata, tak i lidé (Balkhy a Memish 2003). Onemocnění Většina případů infekce u člověka je asymptomatická a v případě onemocnění jde většinou o mírnou formu nemoci. Nákaza probíhá přenosem z vektora nebo kontaktem s nakaţenými zvířaty i jejich krví a tkáněmi. Po krátké 2 5 denní inkubační době nastává u pacienta nízká horečka, únava, bolest hlavy, svalů a kloubů. Přidruţenými symptomy mohou být i fotofobie, makulopapulární vyráţka a zvracení. Tyto příznaky trvají zhruba týden a pak dojde ke spontánnímu uzdravení (Balkhy a Memish 2003, WHO 2008). Přibliţně u 5 % pacientů ale dochází ke komplikacím trojího druhu. Oční forma způsobuje zhoršení vidění nebo dočasnou slepotu, pouze zřídka je poškození očí trvalé. V 1 % případů dochází k meningoencefalitidě, která je provázena bolestí hlavy, halucinacemi, závratí, ztrátou paměti a můţe vyústit v závaţné neurologické problémy. Nejzávaţnější a nejméně častá je hemoragická forma, která začíná ţloutenkou a dále se projevuje zvracením krve, krví ve stolici, podlitinami, krvácením z nosu, dásní a z míst vpichu jehly. Nástup hemoragie je rychlý a úmrtnost těchto pacientů je průměrně 50 %. Celkem však na RVF umírá méně neţ 1 % pacientů (WHO 2008). Diagnostika nemoci je zaloţená na klinických projevech a laboratorních testech. Nejspolehlivějšími testy jsou RT-PCR a izolace viru, serologie nemusí infekci v počáteční fázi identifikovat (Aradaib a kol. 2008)
31 Ekologie Přenos RVF je uskutečňován několika vektory z řad komárů, coţ z ní dělá významné zoonotické onemocnění. Významným faktorem je také transovariální přenos, díky kterému se virus přenáší ve vektorech z generace na generaci. K úspěšnému rozmnoţování komárů přispívají časté deště a stavba velkých přehrad (Balkhy a Memish 2003). Nejvýznamnějšími vektory jsou komáři čeledě Culucidae, především podčeledě Culicinae, rodu Aedes. Jde např. o druhy Ae. circumluteeolus, Ae. micintoshi, Ae. vexans, Ae. ochraceus, Ae. dalzieli, Ae. caballus, Ae. lineatopennis, ale také Culex theileri, Culex pipiensis (Balkhy a Memish 2003, Hubálek 2000). Méně významný je pak přenos pakomáry rodu Culicoides (čeleď Ceratopogonidae), flebotomy (čeleď Psychodidae) a jiným bodavým hmyzem (Hubálek 2000). Experimentálně se podařil také přenos komáry rodu Anopheles (Balkhy a Memish 2003). Přenos z člověka na člověka nebyl zaznamenán (WHO 2008). Zdrojem RVF viru v obratlovcích jsou především ovce, skot, kozy, velbloudi a hlodavci (Hubálek 2000, WHO 2008). U zvířat virus způsobuje závaţné onemocnění, jehoţ důsledkem mohou být velké ekonomické ztráty (WHO 2008). Virus RVF je rozšířen po téměř celé Africe a přilehlých ostrovech a v oblasti Arabského poloostrova v Asii (viz Obr. 8). Je otázkou, zda se virus bude šířit dále do Asie a Evropy, nebo se na Arabském poloostrovu zastaví (Balkhy a Memish 2003). Země s endemickým a hojným výskytem RVF: Země se zaznamenanými případy, pravidelnou izolací viru nebo serologickým průkazem RVF: Gambie, Senegal, Mauritánie, Namibie, Jihoafrická republika, Mosambik, Zimbabwe, Zambie, Keňa, Súdán, Egypt, Madagaskar, Saudská Arábie, Jemen Botswana, Angola, Democratická republika Kongo, Kongo, Gabon, Kamerun, Nigérie, Středoafrická republika, Čad, Niger, Burkina Faso, Mali, Guinea, Tanzanie, Malawi, Uganda, Etiopie, Somálsko Obr. 8 Celosvětová distribuce RVF viru. Upraveno podle URL
32 Epidemie 1930: první prokázaný výskyt RVF v oblasti Great Rift Valley v Keni (Balkhy a Memish 2003). 1977: rozsáhlá epidemie v Egyptě, která si vyţádala na 600 obětí (Siam a kol. 1980) : velká epidemie v Keni, Somálsku a Tanzanii (WHO 2008). 2000: první epidemie mimo africký kontinent v Saudské Arábii a Jemenu (Miller a kol. 2002) : další velký výskyt RVF v Keni, Somálsku, Tanzanii, Súdánu a později na ostrovech východní Afriky (Komory, Mayotte) (Sissoko a kol. 2009, WHO 2008). Léčba a prevence Dosud není známa ţádná specifická léčba proti RVF. V mírných případech však není specifická léčba vyţadována, protoţe zpravidla dochází k spontánnímu uzdravení. U závaţných případů s meningoencefalitidou nebo hemoragií je pro přeţití pacientů nutná podpůrná léčba zahrnující umělou plicní ventilaci a krevní transfuze (Balkhy a Memish 2003). Bylo jiţ vyvinuto několik účinných vakcín pro zvířata, vakcína pro člověka je však stále ve fázi výzkumu. Inaktivovaná vakcína byla testována na vysoce ohroţeném veterinárním a laboratorním personálu, avšak komerčně dostupná v dohledné době nejspíš nebude (Wallace a kol. 2006, WHO 2008). Ohroţenou skupinou jsou lidé pracující se zvířaty, na jatkách, řezníci a také laboranti, protoţe virus se můţe přenášet i aerosolem. Součástí prevence před nákazou je tedy kromě zabránění kontaktu s infikovanými zvířaty také kontrola výskytu vektorů a onemocnění u zvířat (WHO 2008) Hantaviry Obecná charakteristika Rod Hantavirus patří do čeledě Bunyaviridae a obsahuje mnoţství zástupců způsobujících závaţná onemocnění. Jde např. o viry Hantaan, Dobrava/ Belgrade, Seoul, Puumala, Tobetsu, Bat, Topografov, Thottapalyam, Thailand, Tula a Khabarovsk ze Starého světa, které většinou způsobují hemoragickou horečku s renálním syndromem nebo epidemickou nefropatii. Viry z Nového světa, jako např. Prospect Hill, Bloodland Lake, Isla
33 Vista, Leaky, Sin Nombre, Monongahela, New York, Blue River, Rio Mamore, Andes, El Moro Canyon, Rio Segundo, Bayou, Black Creek Canal, Mule Shoe, Cano Delgadito, Laguna Negra a Juquitiba, zpravidla způsobují hantavirový plicní syndrom. U některých z těchto virů ještě není jasné, zda jsou na člověka přenosné nebo zda u něj způsobují nějaké onemocnění (Hart a Bennett 1999). Např. virus Tula je pro člověka prakticky nepatogenní (Hubálek 2000). Nejvýznamnější patogenní druhy z této skupiny jsou uvedeny v Tab. 2 (Hart a Bennett 1999). Genom hantavirů je tvořen třemi segmenty lineární ssrna o velikostech přibliţně 6550, 3680 a 1830 bazí. Sférický virion má v průměru nm a na povrchu je obalen lipidovou membránou (Hart a Bennett 1999, Terajima a kol. 2004). Název rodu Hantavirus pochází od řeky Hantaan v Jiţní Korei, kde byl roku 1976 poprvé izolován prototypový virus Hantaan (Bryan a kol. 1997). Virus Přírodní rezervoár Geografické rozšíření Onemocnění Hantaan Apodemus agrarius Střední Evropa, Balkán, Kavkaz, východní Asie HFRS Dobrava/ Belgrade Apodemus flavicolis Balkán, Rusko, Estonsko HFRS Seoul Rattus norvegicus Celosvětově HFRS Puumala Myodes glareolus Severní Evropa, Rusko HFRS, EN Sin Nombre Peromyscus maniculatus USA, Mexiko HPS New York Peromyscus leucopus USA, Kanada, Mexiko HPS Andes Oligoryzomys longicaudatus Chile, Argentina HPS Black Creek Canal Sigmodon hispidus Střední Amerika HPS Tab. 2 Charakteristika nejvýznamnějších hantavirů. Upraveno podle Hart a Bennett Onemocnění Hemoragická horečka s renálním syndromem má pět fází: horečnatou, hypotenzní, oligurickou, polyurickou a fázi rekonvalescence. Obecně nejčastějšími příznaky jsou horečka, bolest hlavy, břicha a zad (Rusnak a kol. 2009), vyskytnout se můţe také bolest svalů, zimnice, kašel, zvracení a modročervené vidění. Výraznějšími znaky jsou ledvinová nedostatečnost a mírná hemoragie z nosu, vaginy a GIT (Pal a kol. 2005). Téměř polovina pacientů můţe mít nízký krevní tlak a aţ 60 % jich trpí oligurií (vylučování méně neţ 400 ml moče za den, zpravidla trvá 3 7 dní). V závaţnějších případech hrozí edém plic a ledvinové selhání v oligurické či polyurické fázi, které můţe vést k nutné dialýze (Rusnak a kol. 2009). Závaţnost onemocnění závisí na druhu viru i na vlastnostech infikovaného organismu. U virů Hantaan a Dobrava/ Belgrade je úmrtnost 5 35 %, u viru Seoul pouze 1 % (Hart a Bennett 1999)
34 Epidemická nefropatie bývá způsobena virem Puumala a jde o mírnou formu HFRS bez významných hemoragií (Pal a kol. 2005). Charakterizována je vysokou horečkou, bolestí hlavy, zad, břicha a drobným krvácením. Infekce však můţe vyústit i v selhání ledvin a šok. Úmrtnost na EN je zřídkavá, menší neţ 1 % (Terajima a kol. 2004). Hantavirový plicní syndrom se ze začátku infekce projevuje jako nespecifická nemoc s horečkou, bolestí svalů a hlavy, nevolností, zvracením a kašlem. Neproduktivní kašel se však stupňuje v dýchavičnost a závaţné dýchací problémy (Khan a kol. 1996). Po 2 aţ 4 dnech se dají radiologicky rozeznat příznaky zhrubnutí mezialveolových přepáţek a také hrozící edém plic, který je způsoben zvýšenou permeabilitou cév (Khan a kol. 1996, Rajčáni a Čiampor 2006). V závaţných případech hrozí také šok se selháním pravé poloviny srdce kvůli vysokému tlaku v plicním řečišti. Proto chtějí někteří odborníci změnit název nemoci z HPS na hantavirus cardiopulmonary syndrome (Rajčáni a Čiampor 2006). Mortalita nakaţených se pohybuje mezi %, byl však zaznamenán také asymptomatický průběh infekce nebo její mírná forma bez závaţných problémů (Hart a Bennett 1999). Selhání ledvin stejně jako hemoragie provází HPS výjimečně (Khan a kol. 1996). Laboratorní diagnostika je zaloţena na serologických metodách (ELISA, imunofluorescence), izolaci viru a RT-PCR, která je vysoce citlivá a specifická (Hart a Bennett 1999, Chandy a kol. 2009). Ekologie Hantaviry, na rozdíl od většiny rodů v čeledi Bunyaviridae, nepatří mezi arboviry, ale jsou přenášeny hlodavci (Hart a Bennett 1999). Kaţdý virus má svého specifického přenašeče, coţ je pravděpodobně také důvodem, proč se HPS viry nerozšířily ve Starém světě (americké druhy hlodavců u nás neţijí). Všichni tito hlodavci patří do řádu Rodentia a podřádu Sciurognathi, jednotlivé druhy přenášející významné viry jsou uvedeny výše v Tab. 2 (Khan a kol. 1996). Hlodavci jsou zároveň i přírodním rezervoárem hantavirů (Hubálek 2000). Přenos infekce na člověka probíhá kontaktem s nakaţenými zvířaty, jejich močí, výkaly a slinami a především inhalací aerosolu obsahujícího tyto částečky (Bayard a kol. 2004, Bryan a kol. 1997). Také byl zaznamenán přenos po pokousání hlodavcem (Hart a Bennett 1999). V Argentině a Chile byl prokázán přenos onemocnění (virus Andes) z člověka na člověka (Bayard a kol. 2004, Figueiredo a kol. 2009), nozokomiální nákazy se však neobjevily (Hart a Bennett 1999). HFRS je rozšířena ve Starém světě: virus Hantaan najdeme především v Korei, Číně, Japonsku a asijském Rusku, viry Dobrava/ Belgrade na Balkáně, v Německu, Estonsku
35 a Rusku a virus Seoul je rozšířen celosvětově (Hart a Bennett 1999). Virus Puumala způsobující EN se vyskytuje v severní a severozápadní Evropě, jeho výskyt však byl zaznamenán i na Balkáně (Pal a kol. 2005). HPS je zaznamenáván pouze z Nového světa: viry Sin Nombre a New York působí v Severní a Střední Americe (především USA, Kanada a Mexiko), Andes a další se vyskytují v Jiţní Americe (Argentina, Chile, Uruguay, Paraguay, Bolívie, Venezuela a Brazílie) a Black Creek Canal je rozšířen v okolí Střední Ameriky (Figueiredo 2009, Hart a Bennett 1999). Epidemie 1931: první výskyt tehdy ještě neznámé HFRS na severovýchodě Číny. Dnes je rozšířena na 90 % území Číny a do roku 1997 si vyţádala přes obětí (Yan a kol. 2007) : epidemie HFRS v průběhu korejské války, kdy vojáci trpěli horečkou s krvácením a selháním ledvin, si vyţádala několik stovek obětí (Rajčáni a Čiampor 2006). 1976: první izolace hantavirů v Jiţní Korei byl z hlodavce vyizolován virus Hantaan (Bryan a kol. 1997) : první výskyt hantavirů ve střední Evropě v Německu a bývalém Československu. První případ onemocnění v ČR byl roku 1992 (Pejčoch a Kříţ 2003). 1993: první výskyt HPS v průběhu epidemie na jihozápadě USA v oblasti Four Corners, původcem byl Sin Nombre virus (Bayard a kol. 2004, Kitsutani a kol. 1999) : výskyt HPS v Brazílii, zaznamenáno 877 případů způsobených virem Juquitiba a dalšími, z toho bylo 39 % smrtelných (Figueiredo a kol. 2009). 2002: epidemie mírné HFRS v Srbsku a Černé Hoře způsobená viry Dobrava a Puumala. Laboratorně bylo prokázáno 128 případů, z toho 2 byly smrtelné (Schmidt- Chanasit a kol. 2008). Při epidemii v Chorvatsku bylo prokázáno 186 případů, z toho 161 způsobených virem Puumala (Pal a kol. 2005). Léčba a prevence Léčba HFRS spočívá především v podpůrné terapii zaměřené na dostatek tekutin v organismu, kontrolu krevního tlaku a dialýzu, je-li to nutné. V brzké fázi onemocnění můţe být nasazen ribavirin, který zkracuje délku léčby a sniţuje úmrtnost (Rusnak a kol. 2009), v pozdějších fázích nemoci je nejdůleţitější prevence šoku a kolapsu oběhové soustavy
36 (Rajčáni a Čiampor 2006). Léčba HPS je taktéţ pouze podpůrná s nutnou umělou plicní ventilací, protišokovými opatřeními a kontrolou oběhové soustavy. Zkoušky s léčbou ribavirinem byly dosud neúspěšné, uvaţuje se tedy o pasivní imunizaci pacientů (Jonsson a kol. 2008, Khan a kol. 1996). Inaktivovaná vakcína proti HFRS byla vyvinuta v Číně a Korei, je tam komerčně dostupná a ukazuje se být účinná. Na přípravě vakcíny vyhovující evropské legislativě se stále pracuje (Rajčáni a Čiampor 2006). Účinná vakcína proti HPS dosud nebyla vyvinuta (Jonsson a kol. 2008). Ohroţenou skupinou jsou pracovníci v zemědělství, vojáci v terénu, lidé na venkově a obecně lidé, kteří přichází častěji do styku s hlodavci. Účinným preventivním opatřením především ve městech je deratizace (Rajčáni a Čiampor 2006) a všichni lidé by se měli bránit kontaktu s divokými hlodavci a jejich exkrety (Hart a Bennett 1999)
37 7. Čeleď Arenaviridae 7.1. Virus Junin Obecná charakteristika Virus Junin, etiologické agens argentinské hemoragické horečky (AHF), řadíme do čeledě Arenaviridae a jejího jediného rodu Arenavirus (Ţemla a kol. 1998). Fylogeneticky a geograficky patří do tzv. skupiny virů z Nového světa. Genom je tvořen dvěma segmenty lineární ssrna o velikostech 7300 a 3500 nukleotidů, přičemţ čtecí rámce segmentů jsou ambivalentní (mají pozitivní i negativní polaritu) (Rojek a kol. 2008, Ure a kol. 2008). Virion obsahující ribozomy je obalen lipidovou membránou a má v průměru nm, membrána má v sobě zanořené dva druhy glykoproteinů (Rajčáni a Čiampor 2006). Onemocnění Po inkubační době dlouhé obvykle 6 aţ 14 dnů propuká AHF vyznačující se třemi fázemi: prodromalickou, neurologicko-hemoragickou a fází rekonvalescence (Enria a kol. 2008). Týden trvající prodromalická fáze se projevuje nízkou horečkou, zimnicí, bolestí hlavy a svalů, často také nevolností a zvracením, fotofobií, bolestí v nadbřišku, zácpou nebo průjmem. Výraznějšími projevy jsou pak zčervenání nebo petechie kůţe na obličeji, krku a hrudi, zánět spojivek a periorbitální edém a krvácení z dásní (Enria a kol. 2008, Rajčáni a Čiampor 2006). Na konci fáze můţe pacient trpět třesem rukou a jazyka, letargií, špatnou koordinací pohybů a napětím ve svalech (Enria a kol. 2008). Přibliţně % pacientů AHF vstupuje do neurologicko-hemoragické fáze, která je charakterizována závaţnými hemoragickými a neurologickými projevy, šokem a bakteriálními infekcemi. Vykašlávání krve, podlitiny, krev v moči a stolici, tzv. nekonečné menstruace, krvácení z GIT to jsou jenom některé hemoragické příznaky. S poškozením CNS nastupuje zmatenost, problémy s koordinací pohybů, třes, delirium, křeče, v těţkých případech koma a šok (Enria a kol. 2008, Rajčáni a Čiampor 2006). Sekundární bakteriální infekce mohou pacientovi ještě přitíţit (Enria a kol. 2008). Období rekonvalescence přichází u mírných případů spontánně a trvá 2 3 týdny (Rajčáni a Čiampor 2006), u těţších případů trvá 1 3 měsíce a bývá provázeno tělesnou slabostí, dočasnou ztrátou paměti a vlasů (Enria a kol. 2008). Úmrtnost na AHF se pohybuje do 30 % (Goñi a kol. 2006)
38 Rutinní laboratorní diagnostika je zaloţena především na serologické metodě ELISA, moţná je také přímá izolace viru (Ure a kol. 2008). RT-PCR bude moţné pouţít, aţ budou zavedeny standardizované a spolehlivé primery vylučující falešně pozitivní výsledky (Rajčáni a Čiampor 2006). Ekologie Přenašečem a zároveň přírodním rezervoárem viru jsou hlodavci, především Calomys musculinus řádu Rodentia, podřádu Sciurognathi, čeledě Muridae. Největší výskyt těchto hlodavců a tím i AHF bývá zaznamenán kaţdoročně po velkých ţních (Polop a kol. 2008). Přenos infekce na člověka probíhá především inhalací prachu kontaminovaného močí, výkaly, slinami a krví nakaţených hlodavců, také ale poraněním na kůţi, do kterého se tyto částice mohou dostat (Goñi a kol. 2006, Ure a kol. 2008). AHF a virus Junin se vskytují v pampách severní a střední Argentiny, coţ souvisí s výskytem Calomys musculinus, který je v této oblasti endemický (Polop a kol. 2008, Ure a kol. 2008). Epidemie 50. léta 20. století: poprvé se objevila AHF, od té doby se vyskytuje pravidelně bez přerušení kaţdý rok při sezónních pracích (Enria a kol. 2008, Ure a kol. 2008). 1958: izolace viru Junin (URL 2). Graf 2 Počet oznámených a potvrzených případů AHF v letech Upraveno podle Enria a kol
39 Léčba a prevence Léčba AHF probíhá jiţ od konce 50. let pomocí imunního séra od rekonvalescentů s uspokojivými výsledky. Je potřeba ho však podávat do osmého dne od počátku onemocnění. U 10 % pacientů hrozí pozdní neurologický syndrom, který nastává po odeznění všech symptomů nemoci a je charakterizován horečkou, příznaky poškození mozečku, třesem a ztrátou některých smyslů. U pacientů neléčených specifickou terapií tento syndrom zaznamenán nebyl. Léčba ribavirinem zlepšuje stav pacientů, významné sníţení úmrtnosti však nebylo prokázáno (Enria a kol. 2008). Podpůrná léčba zahrnující doplňování tekutin a zabránění syndromu hemokoagulace je stále nutnou součástí terapie (Rajčáni a Čiampor 2006). Proti viru Junin byla zavedena ţivá oslabená vakcína, díky které se daří permanentně sniţovat počty nakaţených, jak naznačuje výše uvedený Graf 2 (Enria a kol. 2008). Nejvíce ohroţenou skupinou jsou argentinští farmáři, kteří přichází do styku s infikovanými hlodavci a jimi zamořeným prostředím. Nejlepší prevencí je tedy vakcinace a bránit se úzkému kontaktu s hlodavci (Ţemla a kol. 1998). Kvůli mimořádnému riziku laboratorní nákazy aerosolem byl virus zařazen do kategorie biologické ochrany biohazard 4 (Hubálek 2000) Virus Machupo Obecná charakteristika Virus Machupo řazený do čeledě Arenaviridae a rodu Arenavirus je etiologickým agens bolivijské hemoragické horečky (BHF) (Cajimat a kol. 2009). Je řazen do serologického komplexu Tacaribe, neboli skupiny arenavirů z Nového světa. Genom je tvořen dvěma segmenty ambivalentní lineární ssrna o velikostech zhruba 7100 a 3400 nukleotidů (Archer a Rico-Hesse 2002). Sférický nebo pleomorfní virion měří v průměru nm a je obalen lipidovou membránou. Ribozomy uvnitř virionu přinesly název arenavirům, protoţe při pozorování v elektronovém mikroskopu se jeví jako zrníčka písku (latinsky písek = arena) (Charrel a de Lamballerie 2003). Onemocnění Průběh BHF je velice podobný nákaze virem Junin a ostatními jihoamerickými hemoragickými horečkami. Po inkubační době 7 14 dnů přichází nečekaný nástup horečky, bolesti hlavy, zad, svalů a kloubů, malátnost a necitlivost kůţe. Obvykle se po 7 dnech těchto
40 nespecifických symptomů objevují hemoragické a neurologické problémy. Z hemoragických příznaků jsou to nejčastěji petechie na kůţi, otok obličeje, krvácení z nosu, dásní, vaginy a GIT, v závaţných případech můţe nastat cévní nedostatečnost a hypovolemický klinický šok (Charrel a de Lamballerie 2003, Kilgore a kol. 1995). Nejvýznamnějšími neurologickými symptomy jsou třes rukou a jazyka (způsobující aţ neschopnost mluvit), křeče a koma. Smrt obvykle přichází den od nástupu choroby. Období rekonvalescence vede k úplnému vyléčení, v průběhu však často dochází k vypadání vlasů a nadměrné únavě. Zhruba 20 % případů bývá smrtelných (Charrel a de Lamballerie 2003). Diagnostika onemocnění je zaloţena na anamnéze a laboratorních testech. Nejspolehlivějšími a nejuţívanějšími metodami jsou izolace viru z Vero buněk, RT-PCR a ELISA (Charrel a de Lamballerie 2003, Rajčáni a Čiampor 2006). Ekologie Přenašečem a zároveň přírodním rezervoárem viru jsou hlodavci rodu Calomys, především Calomys callosus (Kilgore a kol. 1995). Tito hlodavci patří do řádu Rodentia, podřádu Sciurognathi a čeledě Muridae (Charrel a de Lamballerie 2003). Přenos infekce na člověka probíhá inhalací aerosolu kontaminovaného močí, výkaly, slinami nebo krví hlodavců, pozřením kontaminovaných potravin nebo přímým kontaktem poraněné kůţe či sliznice s exkrety hlodavců. Byl také zaznamenán přenos BHF z člověka na člověka (Charrel a de Lamballerie 2003, Kilgore a kol. 1995). Virus Machupo a s ním BHF se vyskytuje v Bolívii, nejčastěji v oblasti Beni na severovýchodě země (Cajimat a kol. 2009). Epidemie 1959: první případ BHF a rozpoznání jejích klinických příznaků na severovýchodě Bolívie u města San Joaquín v oblasti Beni : epidemie BHF v okolí města San Joaquín se sporadickými případy po celé severovýchodní Bolívii a jednou nemocniční epidemií. V průběhu epidemie byl roku 1963 virus poprvé izolován (Cajimat a kol. 2009) : díky efektivní kontrole populace hlodavců nebyl zaznamenán jediný případ BHF. 1994: šest smrtelných případů ve městě Magdalena, kde se nakazili členové jedné rodiny přenosem z člověka na člověka (Kilgore a kol. 1995)
41 Léčba a prevence Specifická terapie imunním sérem rekonvalescentů se ukázala být účinná, avšak kvůli malému mnoţství případů a neexistenci banky na tuto plasmu, je málo vyuţívaná. Nespecifická léčba je zaloţena na udrţování dostatku tekutin v těle a podávání ribavirinu, jehoţ účinky ještě nebyly statisticky potvrzeny (Charrel a de Lamballerie 2003). Vakcína proti BHF dosud nebyla vytvořena, k ochraně vysoce rizikové skupiny lidí lze však pouţít vakcínu proti AHF (Kilgore a kol. 1995). Prevence před BHF spočívá především v zabránění styku s infikovanými hlodavci a jejich sekrety a exkrety. Vysoce ohroţenou skupinou jsou tedy pracovníci v zemědělství, kteří mohou tomuto styku těţko zabránit. První moţností je vakcinace látkou proti viru Junin. Druhou a jiţ ověřenou metodou je systematická likvidace přenašečů onemocnění jak ve městách, tak na venkově. Díky efektivnímu programu kontroly výskytu hlodavců se po dvacet let neobjevil jediný případ BHF (Charrel a de Lamballerie 2003, Kilgore a kol. 1995). Kvůli vysokému riziku přenosu infekce z člověka na člověka aerosolem byl virus Machupo zařazen do kategorie biologické ochrany biohazard 4 (Cajimat a kol. 2009) Virus Lassa Obecná charakteristika Hemoragická horečka Lassa je způsobena virem Lassa z čeledě Arenaviridae a jejího jediného rodu Arenavirus. Virus Lassa je řazen do serokomplexu Lassa-lymfocytární choriomeningitidy mezi další viry ze Starého světa (Charrel a kol. 2008). Genom je tvořen dvěma segmenty ambivalentní lineární ssrna o velikostech zhruba 7200 a 3400 nukleotidů. Stejně jako u ostatních arenavirů je virion obalen lipidovou membránou, v průměru má nm a obsahuje ribozomy (Moshkoff a kol. 2007, Rajčáni a Čiampor 2006). Jméno Lassa získal virus díky stejnojmenné vesničce v Nigérii, kde epidemie HF poprvé propukla (Curtis 2006). Onemocnění Průběh nákazy virem Lassa se můţe různit od asymptomatické infekce přes mírnou formu onemocnění aţ po závaţné multiorgánové selhání končící smrtí. Nemoc se nevyhýbá ţádné rase, věku ani pohlaví (Khan a kol. 2008). Po inkubační době trvající 5 21 dnů propuká onemocnění trvající jeden aţ čtyři týdny (Curtis 2006). Nespecifické příznaky na
42 začátku nemoci jako vysoká horečka, bolest hlavy, svalů a kloubů, zánět hrtanu a kašel, jsou provázeny bolestí břicha, zvracením a průjmem, často také zánětem spojivek (Curtis 2006, Khan a kol. 2008). Na hrudi, rukou a obličeji se můţe objevit makulopapulární vyráţka nebo petechie. Pouze u 20 % pacientů nemoc přechází do závaţnější formy projevující se otokem krku a obličeje, nízkým krevním tlakem, krvácením z nosu, dásní a rekta a šokem. Hlavními příznaky poškození CNS jsou zmatenost, koktání, ztráta orientace a rovnováhy, za konečné stadium se dá povaţovat koma (Khan a kol. 2008). Nemoc můţe provázet i encefalitida nebo meningitida (Curtis 2006). Smrt se objevuje nejčastěji mezi dnem choroby. Indikuje ji především šok, závaţné krvácení, neurologické příznaky a vysoká virémie (Khan a kol. 2008). V průběhu rekonvalescence můţe dojít k jednostrannému či oboustrannému poškození senzorických nervů, které je u jedné třetiny pacientů trvalé (Curtis 2006). Velké obtíţe vyvolává Lassa těhotným ţenám ve třetím trimestru. Infekce způsobuje vaginální krvácení a spontánní potrat se 100 % mortalitou plodu a 30 % u matek. Předčasný porod pak zvyšuje ţeně šanci na přeţití (Curtis 2006, Khan a kol. 2008). Úmrtnost hospitalizovaných pacientů se pohybuje mezi %, při epidemiích můţe dosáhnout aţ 50 %. Díky asymptomatickým nebo mírným infekcím je však celková úmrtnost na HF Lassa pouze 1 % (Curtis 2006). Mezi nejspolehlivější diagnostické metody patří RT-PCR, ELISA a izolace viru (Curtis 2006, Omilabu a kol. 2005). Ekologie Přenašečem viru jsou hlodavci rodu Mastomys, nejběţněji Mastomys natalensis, řádu Rodentia a čeledě Muridae (Denys a kol. 2005). Krysa mnohobradavková (Hubálek 2000) ţije ve velké části západní a střední Afriky a často v blízkosti lidských obydlí (Denys a kol. 2005). Zde zanechává své výkaly, moč a sliny, jejichţ infekční částice se dostávají do ovzduší a vdechnutím se člověk nejčastěji nakazí. Dalšími cestami je také kontakt poraněné kůţe s kontaminovanými předměty nebo pozření kontaminované potravy (Fleischer a kol. 2000) či celého hlodavce, který je v mnoha zemích západní Afriky povaţován za pochoutku (Curtis 2006). Přenos z člověka na člověka je uskutečňován přímým kontaktem s krví, tkáněmi, sekrety a exkrety infikovaných a také zraněním kontaminovanou jehlou (Curtis 2006, Hubálek 2000). Přírodní rezervoár viru dosud není znám (Denys a kol. 2005). Virus Lassa a s ním spojená HF Lassa je endemická v západní a střední Africe. Největší výskyt epidemií je zaznamenán v Guinei, Sierra Leone, Libérii, Nigérii a Středoafrické republice (Curtis 2006, Günther a kol. 2000), přestoţe serologické studie
43 prokázaly výskyt viru také v Senegalu, Mali a Kongu. Nejhojněji epidemie probíhají v období sucha mezi lednem a dubnem (Curtis 2006). Epidemie 1969: první epidemie HF Lassa propukla ve vesnici Lassa v severní Nigérii. Prvními nakaţenými byly dvě misionářské sestry (Curtis 2006, Fleischer a kol. 2000) : výskyt onemocnění v celé endemické oblasti (Hubálek 2000), na který reagovala CDC zavedením laboratorního, výzkumného a kontrolního programu k omezení epidemií VHF Lassa. Centrum výzkumu bylo umístěno ve středu endemické oblasti v Sierra Leone (Khan a kol. 2008). 2000: importovaný případ HF Lassa v Německu, kdy byl popsán nový kmen viru. Studentka se z cest po západní Africe vrátila s vysokou horečkou a dalšími nespecifickými příznaky. V důsledku pozdní diagnózy se u ní rozvinul šok a nakonec podlehla multiorgánovému selhání. Nikdo další nebyl nakaţen (Fleischer a kol. 2000, Günther a kol. 2000) : epidemie HF Lassa v Nigérii ve státě Edo, z 60 podezřelých bylo laboratorně potvrzeno 18 případů (Omilabu a kol. 2005). Léčba a prevence Při léčbě HF Lassa je nanejvýš důleţitá intenzivní symptomatická léčba zahrnující doplňování tekutin a protišokovou léčbu (Rajčáni a Čiampor 2006). Léčba ribavirinem ukázala také velice pozitivní výsledky (sníţení úmrtnosti u těţkých případů z 55 na 5 %), musí však být podán do šestého dne od počátku nemoci (Khan a kol. 2008). Pasivní podávání protilátek získaných ze séra rekonvalescentů se nesetkalo s úspěchem (Curtis 2006). Nyní je hlavním cílem výzkumů vyvinout účinnou vakcínu proti viru Lassa, která by byla spolehlivou prevencí před VHF Lassa v endemické oblasti (Günther a kol. 2000). Při prevenci před tímto zákeřným onemocněním je nutná především osvěta mezi místním obyvatelstvem. Lidé se pak sami budou bránit kontatku s hlodavci, nestrpí je v blízkosti svých obydlí, ani je nebudou pojídat (Curtis 2006, Rajčáni a Čiampor 2006). Neméně důleţitá je také ochrana před přenosem z člověka na člověka, která vyţaduje dodrţování základních hygienických návyků. Při vypuknutí epidemie je nevyhnutné řídit se pokyny zdravotníků (Curtis 2006). Virus Lassa byl zařazen do kategorie biologické ochrany biohazard 4 (Charrel a kol. 2008)
44 8. Čeleď Filoviridae 8.1. Virus Ebola Obecná charakteristika Ebolavirus je rodem čeledě Filoviridae, který obsahuje 4 druhy: Zaire ebolavirus, Sudan ebolavirus, Reston ebolavirus a Côte d Ivoire ebolavirus (Groseth a kol. 2009). Všechny čeledě řádu Mononegavirales, do které čeleď Filoviridae patří, jsou obalené viry s genomem tvořeným lineární ssrna (Ascenzi a kol. 2008). Délka genomu viru Ebola je přibliţně nukleotidů (Bray a Paragas 2002). V elektronovém mikroskopu se virus jeví jako dlouhé vlákno tvaru písmene U nebo čísla 6. Vlákno virionu měří na délku aţ 1400 nm, zatímco v průměru má pouhých 80 nm. Od tvaru je odvozen také název filovirů: filum znamená latinsky nit nebo vlákno (Ascenzi a kol. 2008). Virus Ebola je pojmenován podle řeky Ebola protékající Demokratickou republikou Kongo (dříve Zair), kde se poprvé onemocnění objevilo (Curtis 2006). Onemocnění Po inkubační době 3 21 dnů rychle nastupuje horečka, bolesti hlavy, svalů, břicha, nevolnosti, zvracení a vodnatý nebo krvavý průjem (Ascenzi a kol. 2008). U zhruba 50 % pacientů se na hrudi a ramenou tvoří makulopapulární vyráţka (Groseth a kol. 2007). Na začátku druhého týdne nemoci se postupně začnou projevovat cévní potíţe, koagulopatie, hemoragie (v rozsahu od drobných krvácení přes krvácení z nosu a dásní po rozsáhlou hemoragii především v GIT), dehydratace, šok a multiorgánové selhání. V této fázi pacient buď umírá nebo přechází do zdlouhavé rekonvalescence (Ascenzi a kol. 2008). Úmrtnost pacientů závisí od druhu ebolaviru, kterým je pacient nakaţen. U Eboly Zaire je mortalita %, zatímco u Eboly Sudan % (Bausch a kol. 2008). Ebolou Côte d Ivoire dosud onemocněl pouze jeden pacient, který byl plně uzdraven (Ascenzi a kol. 2009), a Ebola Reston u člověka zatím nezpůsobila ţádné onemocnění (Curtis 2006). Běţně uţívanými metodami laboratorní diagnostiky jsou ELISA, RT-PCR, izolace viru a histopatologie provedená na uhynulých zvířatech (URL 3). Ekologie Přenos infekce na člověka probíhá úzkým kontaktem s krví, sekrety nebo tkáněmi nakaţených osob nebo zvířat (často gorily a šimpanzi), v mnoha případech je původ
45 onemocnění neznámý (Groseth a kol. 2007). Nozokomiální nákazy, stejně jako onemocnění po poranění se jehlou, nejsou výjimkou (Bray a Paragas 2002, Curtis 2006). V přírodě se virus aerosolem nešíří a v průběhu inkubační doby také ne (Curtis 2006). Přírodní rezervoár viru není dosud znám, ale předpokládá se, ţe by to mohly být některé druhy netopýrů a kaloňů. Nad způsobem přenosu a přeţívání viru v přírodě visí stále otazník (Groseth a kol. 2007). Ebola je primárně rozšířena v tropické Africe zaznamenána byla ve státech Demokratická republika Kongo, Súdán, Gabon, Jihoafrická republika, Kongo, Pobřeţí slonoviny, Uganda a v Asii se vyskytla na Filipínách Ebola Reston. Sekundární infekce způsobené transportem nakaţených opic se objevily v Evropě i Americe (Bausch a kol. 2008). Epidemie 1976: první souběţná epidemie HF Ebola proběhla v Yambuku v Zairu, kde měla mortalitu 88 %, a v Nzara v Súdánu, kde byla mortalita 53 % (Ascenzi a kol. 2008). 1989: Ebola-Reston virus byl poprvé posán v Restonu ve Virginii v USA, kde byly zkoumány dovezené opice z Filipín. Čtyři vědci byli infikováni, ale ani jeden neonemocněl (Curtis 2006). 1994: jediná infekce Ebolou Côte d Ivoire v Pobřeţí slonoviny, kde se nakazil vědecký pracovník při pitvě šimpanze. Po mírném průběhu nemoci a léčbě ve Švýcarsku byl zcela uzdraven (Ascenzi a kol. 2008) : epidemie pravděpodobně nového kmene Bundibugyo ebolaviru v Ugandě. Ze 149 případů bylo 37 smrtelných (Towner a kol. 2008). 2008: prokázána infekce Ebolou Reston u prasat na Filipínách, vzápětí se objevily i protilátky v krvi farmářů, kteří se o prasata starali. Ţádné klinické příznaky onemocnění se však neprojevily (Morris 2009, URL 3). Léčba a prevence Doposud nebyl vyvinut ţádný účinný lék proti infekci virem Ebola. Zkoušky s imunním sérem rekonvalescentů ani ribavirinem nevedly ke zlepšení stavu pacientů (Bausch a kol. 2008), jedinou moţnou léčbou tedy zůstává podpůrná a symptomatická terapie (Bray a Paragas 2002). Na vývoji účinné vakcíny se stále pracuje (Ascenzi a kol. 2008). Prevence před HF Ebola je kvůli vysoké infekčnosti a neznámému přírodnímu rezervoáru velice obtíţná (Handy 2004). Nejlepší ochranou je brzká izolace případů
46 podezřelých z VHF, zabránit nebezpečnému kontaktu zdravotnického a laboratorního personálu s infikovanými osobami a uţívání ochranného oblečení, rukavic a brýlí při styku s pacienty. Při epidemiích je důleţitá osvěta mezi místním ohroţeným obyvatelstvem (Ascenzi a kol. 2008). Ebola je zařazena do kategorie biologické ochrany biohazard 4 (Groseth a kol. 2007) Virus Marburg Obecná charakteristika Rod Marburgvirus je řazen do čeledě Filoviridae, řádu Mononegavirales a obsahuje jediný druh Lake Victoria marburgvirus. V obaleném virionu je uzavřena jedna molekula -ssrna (Ascenzi a kol. 2008), která vytváří genom viru o velikosti přibliţně nukleotidů. Vláknitý virion má na délku nm a na šířku pouhých 80 nm (Bray a Paragas 2002). Virus Marburg je pojmenován podle města Marburg v Německu, kde byl virus poprvé popsán (Curtis 2006). Onemocnění Po inkubační době dlouhé 3 9 dnů nastupují nespecifické symptomy jako horečka, bolest hlavy, svalů a břicha, zimnice, nevolnosti, průjem, zvracení a makulopapulární vyráţka. Často se pacienti propadají do hluboké letargie, můţe se objevit také kašel, zánět spojivek či fotofobie. Asi u 45 % pacientů se rozvíjí hemoragické příznaky (Curtis 2006), nejčastěji krvácení z GIT, často ale také z nosu, dásní, vaginy, petechie a purpura. Smrt bývá predikována šokem, závaţným krvácením a vysokou virémií. Úmrtnost pacientů se pohybuje mezi % (Bausch a kol. 2008). Z laboratorních diagnostických metod je hojně uţívaná izolace viru, protoţe protilátky bývají v krvi detekovatelné aţ těsně před smrtí pacienta. Přesto ELISA dosahuje uspokojivých výsledků a PCR je tradičně úspěšná metoda. U neafrických pacientů je hlavním diagnostickým bodem anamnéza (Ligon 2005). Ekologie Virus Marburg je na člověka přenášen kontaktem s krví, sekrety a orgány infikované osoby nebo kontaktem či pozřením infikovaného zvířete (nejčastěji opice). Přenos viru
47 aerosolem nebyl v přírodě prokázán (Curtis 2006). Sekundární infekce způsobené přenosem viru z člověka na člověka, nozokomiální a laboratorní nákazy nejsou neobvyklé a často jsou příčinou většího počtu úmrtí, neţ primární infekce. Přírodní rezervoár viru není znám, podle současných výzkumů jsou jím nejpravděpodobněji některé druhy kaloňů (Bausch a kol. 2008). HF Marburg se vyskytuje v tropické Africe ve státech Zimbabwe, Jihoafrická republika, Keňa, Demokratická republika Kongo, Angola a Uganda. Případy zavlečené infekce proběhly v Německu, Srbsku a nově i v USA a Nizozemí (Bausch a kol. 2008, URL 4). Epidemie 1967: první výskyt viru Marburg proběhl souběţně v Marburgu, Franfurktu a Bělehradě, kde se od opic dovezených z Ugandy nakazilo 31 laboratorních pracovníků a vědců, z nichţ 7 zemřelo (Curtis 2006) : výskyt pouze 7 případů HF Marburg: 3 případy u turistů, 3 sekundární nákazy a 1 laboratorní infekce v Rusku (Ascenzi a kol. 2008) : epidemie v Angole v provincii Uige. Z 422 případů bylo 356 smrtelných (Ligon 2005). Léčba a prevence Ţádná vakcína nebo specifická léčba proti HF Marburg nebyla dosud úspěšně vyvinuta. Podpůrná terapie zahrnuje doplňování chybějících tekutin, v případě potřeby podporu dýchání a krevní transfuze. Můţe být podáván heparin pro zředění krve, názor na tuto léčbu je ale kontroverzní (Ligon 2005). Ribavirin také neprokázal dostatečnou účinnost (Handy 2004). Cílem pro dnešní vědce není pouze najít vhodnou léčbu pro pacienty trpící HF, ale i látku zajišťující profylaxi laboratorním a zdravotnickým pracovníkům, kteří bývají vystavováni působení viru při své práci (Bray a Paragas 2002). Prevence je u viru Marburg zaloţena stejně jako u viru Ebola na informovanosti místního obyatelstva, vyvarování se styku s nakaţenými osobami a zvířaty a pouţívání ochranných pomůcek při kontaktu s pacienty (Ascenzi a kol. 2008). Při úmrtí na nákazu VHF by mělo být tělo zemřelého spáleno, stejně jako oblečení, povlečení a všechny věci, se kterými přišel v době nemoci do úzkého kontaktu (Curtis 2006). Díky nebezpečnosti a infekčnosti byl virus Marburg zařazen do kategorie biologické ochrany biohazard 4 (Bray a Paragas 2002)
48 9. Čeleď Paramyxoviridae 9.1. Virus Nipah Obecná charakteristika Virus Nipah řadíme do čeledě Paramyxoviridae a do jejího nově vzniklého rodu Henipavirus. Do tohoto rodu patří také virus Hendra, se kterým má Nipah z % homologní genom (Wild 2009). Genom je tvořen lineární ssrna (Mungall a kol. 2008). Virion je obalen lipidovou membránou, do které jsou vnořeny dva glykoproteiny slouţící při vstupu viru do buňky (Diederich a kol. 2008). Charakter onemocnění i způsob přenosu se liší v závislosti na tom, zda jde o Malajský nebo Bangladéšský typ viru (Chong a kol. 2008). Čeleď Paramyxoviridae je zařazena do řádu Mononegavirales (Ascenzi a kol. 2008). Onemocnění Inkubační doba trvá od 4 dnů aţ do 2 měsíců (u Bangladéšského typu zpravidla do 10 dnů) a poté nastupuje horečka, bolesti hlavy, zvracení, závrať a ztráty vědomí. Výraznějšími znaky jsou tachykardie, vysoký krevní tlak, hypotonie, křečovité záškuby svalstva a vymizení reflexů. Nejzávaţnějším symptomem je encefalitida, která je často také příčinou úmrtí. U 70 % Bangladéšských pacientů byla zaznamenána také plicní nedostatečnost, zatímco v Malajsii se objevovala jen výjimečně (Lo a Rota 2008). V CNS a dalších orgánech byly detekovány mikroinfarkty způsobené trombózou, záněty cév, nedostatečné prokrvení orgánů a nekrózy (Wild 2009). Po překonání nemoci je moţný relaps encefalitidy, i pokud se dříve v průběhu choroby neobjevila (Lo a Rota 2008). Počet úmrtí způsobených virem Nipah se pohybuje kolem 40 %, ačkoli některé epidemie v Bangladéši dosáhly 100 % mortality (Chong a kol. 2008). Z laboratorních metod je pro diagnostiku onemocnění nejčastěji uţívaná serologická metoda ELISA a RT-PCR (Chadha a kol. 2006). Ekologie Za přírodní rezervoár viru jsou povaţováni kaloni rodu Pteropus, nejčastěji P. hypomelanus a P. vampyrus (Wild 2009). Kaloni jsou řazeni do řádu Chiroptera a podřádu Megachiroptera (Hubálek 2000). Avšak zdrojem viru jsou také prasata a další domácí zvířata jako koně, kočky a psi (Lo a Rota 2008), ve kterých se virus amplifikuje. Přenos na člověka pak můţe být uskutečňován jak kontaktem s kaloni, tak např. s infikovanými prasaty. Byl také
49 zaznamenán častý přenos nemoci konzumací potravin kontaminovaných výkaly a slinami kaloňů. Přenos viru z člověka na člověka nebo nozokomiální nákazy nejsou výjimečné (Chong a kol. 2008). Virus Nipah je rozšířen ve státech jihovýchodní Asie, coţ je znázorněno na Obr. 9 (Mungall a kol. 2008). Epidemie : v Malajsii severně od Kuala Lumpur nemoc poprvé propukla u prasat i lidí. Nakaţeno bylo 258 lidí, z nichţ bylo 105 případů smrtelných, preventivně musel být utracen milion kusů prasat. O několik měsíců později se epidemie rozšířila i na jih aţ do Singapuru (CDC 1999, Wild 2009). 2001: první epidemie v Indii v Západním Bengálsku. Všech 66 pacientů bylo starších 15 let, mortalita dosáhla 75 % a bylo zaznamenáno mnoho případů nozokomiální nákazy (Chadha a kol. 2006). 2001, 2003, 2004, 2005, 2007, 2008: epidemie v Bangladéši s průměrnou mortalitou 70 % (Lo a Rota 2008), kdy šlo většinou o přímou nákazu od kaloňů nebo jejich sekretů a exkretů (Chong a kol. 2008). Ačkoli jde o onemocnění převáţně dospělých, roku 2004 byly často nakaţeny děti do 15 let (11 z 12 nakaţených) (Montgomery a kol. 2008). 2007: malá epidemie v Indii v blízkosti hranic s Bangladéší (Lo a Rota 2008). Léčba a prevence Základem léčby je podpůrná a symptomatická terapie, která je aplikována také preventivně na osoby ohroţené a podezřelé z infekce (Wild 2009). V průběhu epidemie v Malajsii byla ověřena účinnost ribavirinu, který pomohl sníţit úmrtnost pacientů (Lo a Rota 2008). Dokonce byl pacienty dobře snášen, přestoţe bývá často spojován s nepříjemnými vedlejšími účinky. Dosud však neexistuje ţádná vakcína nebo specifická antivirová léčba přímo proti viru Nipah (Mungall a kol. 2008). Nejlepší prevencí před virem Nipah je vyhnout se styku s kaloni a jejich sekrety a exkrety. Nutné je tedy i pečlivé omývání ovoce ze stromů osídlených kaloni a dalších potravin, které jimi mohou být kontaminovány (Montgomery a kol. 2008). Ochrana před infikovaným dobytkem, domácími zvířaty a lidmi je naprostou samozřejmostí, jde totiţ o jedinou cestu zabránění šíření nákazy mezi lidmi (Wild 2009). Kaloni rodu Pteropus jsou
50 endemičtí také v Indii, Číně a Austrálii, proto je velice důleţitým cílem zabránit nebo eliminovat zavlečení viru do těchto zemí (Montgomery a kol. 2008). Virus Nipah byl díky vysoké infekčnosti zařazen do kategorie biologické ochrany biohazard 4 (Diederich a kol. 2008) Virus Hendra Obecná charakteristika Virus Hendra řadíme do čeledě Paramyxoviridae a do nového rodu Henipavirus vzniklého teprve roku 2002 (Ludlow a kol. 2008). Původně byl virus Hendra spolu s virem Nipah zařazen do rodu Morbillivirus (Mackenzie 1999), ve kterém byl nejpříbuznější viru psinky (Hubálek 2000). Genom je tvořen lineární ssrna (Ludlow a kol. 2008) a virion je obalený jemnou dvojitou membránou (Rajčáni a Čiampor 2006). Pojmenování viru je odvozeno od názvu předměstí Brisbane, které se také nazývá Hendra (Lane 1996). Onemocnění Onemocnění způsobené virem Hendra ještě nebylo dostatečně prozkoumáno kvůli nízkému počtu případů (Wild 2009). Nejčastěji je však charakterizováno těţkou akutní encefalitidou a respiratorními problémy (Ludlow a kol. 2008). Hemoragie a edém plic spojené se zánětem alveol, stejně jako encefalitida, byly zaznamenány u prvního pacienta, který infekci nepřeţil. U druhého pacienta se rozvinul relaps encefalitidy spolu s meningitidou, nekrózami a zápaly v různých částech mozku. Z celkového počtu 6 známých případů onemocnění u člověka, byly 3 případy smrtelné (Guillaume a kol. 2009). Laboratorní diagnostika je zaloţena na RT-PCR, ELISA a izolaci viru na Vero buňkách (Aljofan a kol. 2009, Guillaume a kol. 2009). Ekologie Přírodním rezervoárem viru jsou kaloni rodu Pteropus, řádu Chiroptera, podřádu Megachiroptera. Protilátky byly serologicky prokázány u mnoha druhů kaloňů, nejčastěji u P. alecto, P. poliocephalus, P. scapulatus a P. conspicillatus. Přenos viru na člověka byl však dosud zprostředkován pouze nákazou od koně (Mackenzie 1999). Způsob přenosu infekce z kaloňů na koně není zcela znám předpokládá se pozření trávy nebo ovoce infikovaného
51 močí, slinami, či jinými tekutinami kaloňů (Fogarty a kol. 2008). Přenos viru na člověka probíhá kontaktem s tekutinami nebo těly nakaţených či mrtvých zvířat. Dosud nebyl zaznamenán přenos infekce z člověka na člověka (Lane 1996). Onemocnění způsobené virem Hendra, jak je patrné na Obr. 9, bylo prokázáno pouze v Austrálii ve státě Queensland (Wild 2009). Obr. 9 Rozšíření virů Nipah a Hendra. Modrými hvězdičkami jsou vyznačeny proběhlé epidemie viru Nipah, červenými viru Hendra. Barevná plocha vyznačuje rozšíření kaloňů rodu Pteropus. Upraveno podle Wild Epidemie 1994: první výskyt onemocnění způsobeného virem Hendra na předměstí Brisbane v Austrálii. Infikovány byly dvě osoby a 20 závodních koní, z toho jeden trenér onemocnění podlehl a 13 koní zemřelo nebo bylo utraceno (Mackenzie 1999). Propuknutí nemoci v Hendra předpověděla smrt 2 koní na farmě v Mackay, kde se nakazil také farmář a po roce od kontaktu s koňmi podlehl relapsu encefalitidy (Lane 1996). 2004: onemocnění koní v Queenslandu v Austrálii, jediný nakaţený pacient infekci přeţil (Ludlow a kol. 2008, Wild 2009). 2006, 2007: další výskyt viru Hendra v Austrálii (Wild 2009). 2008: zatím poslední případ onemocnění způsobeného virem Hendra se odehrál v červenci 2008 a vyţádal si smrt jednoho veterináře (Guillaume a kol. 2009)
KRAJSKÁ HYGIENICKÁ STANICE MORAVSKOSLEZSKÉHO KRAJE SE SÍDLEM V OSTRAVĚ
 KRAJSKÁ HYGIENICKÁ STANICE MORAVSKOSLEZSKÉHO KRAJE SE SÍDLEM V OSTRAVĚ Nákazy přenášené různými přenašeči Tato skupina infekcí se vyznačuje tím, že zdrojem a rezervoárem nákazy obvykle bývají zvířata,
KRAJSKÁ HYGIENICKÁ STANICE MORAVSKOSLEZSKÉHO KRAJE SE SÍDLEM V OSTRAVĚ Nákazy přenášené různými přenašeči Tato skupina infekcí se vyznačuje tím, že zdrojem a rezervoárem nákazy obvykle bývají zvířata,
Krvácivá horečka (Ebola)
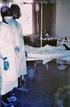 Krvácivá horečka (Ebola) Autor: Petra Grénarová Výskyt Virus Ebola je pojmenován podle řeky Ebola v jižním Súdánu, v jejíž blízkosti byl tento virus roku 1976 poprvé zaznamenán. Ve stejném roce se objevil
Krvácivá horečka (Ebola) Autor: Petra Grénarová Výskyt Virus Ebola je pojmenován podle řeky Ebola v jižním Súdánu, v jejíž blízkosti byl tento virus roku 1976 poprvé zaznamenán. Ve stejném roce se objevil
Strašák EBOLA TÝKÁ SE TAKÉ NÁS EVROPANY? Bc. Helena Marcinková
 Strašák EBOLA TÝKÁ SE TAKÉ NÁS EVROPANY? Bc. Helena Marcinková Ebola a Česká republika máme se bát? Jaké je riziko, že se Ebola dostane do České republiky a začne se tu šířit? Riziko pro turisty nebo obchodní
Strašák EBOLA TÝKÁ SE TAKÉ NÁS EVROPANY? Bc. Helena Marcinková Ebola a Česká republika máme se bát? Jaké je riziko, že se Ebola dostane do České republiky a začne se tu šířit? Riziko pro turisty nebo obchodní
Očkování cestovatelů. 1. infekční klinika 2. lékařská fakulta, Univerzita Karlova v Praze
 Očkování cestovatelů Milan Trojánek 1. infekční klinika 2. lékařská fakulta, Univerzita Karlova v Praze Klinika infekčních, parazitárních a tropických nemocí Nemocnice Na Bulovce, Praha Cestovní a
Očkování cestovatelů Milan Trojánek 1. infekční klinika 2. lékařská fakulta, Univerzita Karlova v Praze Klinika infekčních, parazitárních a tropických nemocí Nemocnice Na Bulovce, Praha Cestovní a
Klíšťová encefalitida
 Klíšťová encefalitida Autor: Michaela Měkýšová Výskyt Česká republika patří každoročně mezi státy s vysokým výskytem klíšťové encefalitidy. Za posledních 10 let připadá přibližně 7 nakažených osob na 100
Klíšťová encefalitida Autor: Michaela Měkýšová Výskyt Česká republika patří každoročně mezi státy s vysokým výskytem klíšťové encefalitidy. Za posledních 10 let připadá přibližně 7 nakažených osob na 100
Epidemiologie nákaz vyvolaných hantaviry přenášených z volně žijících hlodavců na člověka - rizika při pobytu v přírodě
 Epidemiologie nákaz vyvolaných hantaviry přenášených z volně žijících hlodavců na člověka - rizika při pobytu v přírodě RNDr. Marie Vacková, CSc. Katedra epidemiologie Fakulta vojenského zdravotnictví
Epidemiologie nákaz vyvolaných hantaviry přenášených z volně žijících hlodavců na člověka - rizika při pobytu v přírodě RNDr. Marie Vacková, CSc. Katedra epidemiologie Fakulta vojenského zdravotnictví
KOTVA CZ.1.07/1.4.00/21.3537
 KOTVA CZ.1.07/1.4.00/21.3537 Identifikátor materiálu EU: PRIR - 60 Anotace Autor Jazyk Vzdělávací oblast Vzdělávací obor PRIR = Oblast/Předmět Očekávaný výstup Speciální vzdělávací potřeby Prezentace žáka
KOTVA CZ.1.07/1.4.00/21.3537 Identifikátor materiálu EU: PRIR - 60 Anotace Autor Jazyk Vzdělávací oblast Vzdělávací obor PRIR = Oblast/Předmět Očekávaný výstup Speciální vzdělávací potřeby Prezentace žáka
KLÍŠŤOVÁ ENCEFALITIDA pohledem epidemiologa
 KLÍŠŤOVÁ ENCEFALITIDA pohledem epidemiologa MUDr. Renata Vaverková Krajská hygienická stanice Jihomoravského kraje se sídlem v Brně HVD - Hradec Králové 4. 10. 2013 KLÍŠŤOVÁ ENCEFALITIDA je nákazou s přírodní
KLÍŠŤOVÁ ENCEFALITIDA pohledem epidemiologa MUDr. Renata Vaverková Krajská hygienická stanice Jihomoravského kraje se sídlem v Brně HVD - Hradec Králové 4. 10. 2013 KLÍŠŤOVÁ ENCEFALITIDA je nákazou s přírodní
Epidemiologie. MUDr. Miroslava Zavřelová Ústav ochrany a podpory zdraví LF MU
 Epidemiologie MUDr. Miroslava Zavřelová Ústav ochrany a podpory zdraví LF MU Epidemiologie Studium hromadně se vyskytujících jevů Stanovení opatření intervence Analýza efektivity intervence Epidemiologie
Epidemiologie MUDr. Miroslava Zavřelová Ústav ochrany a podpory zdraví LF MU Epidemiologie Studium hromadně se vyskytujících jevů Stanovení opatření intervence Analýza efektivity intervence Epidemiologie
Importované arbovirové infekce v intenzivní péči
 Importované arbovirové infekce v intenzivní péči MUDr. Milan Trojánek, Ph.D. Klinika infekčních nemocí 2. lékařská fakulta, Univerzita Karlova, Praha Katedra infekčních nemocí Institut postgraduálního
Importované arbovirové infekce v intenzivní péči MUDr. Milan Trojánek, Ph.D. Klinika infekčních nemocí 2. lékařská fakulta, Univerzita Karlova, Praha Katedra infekčních nemocí Institut postgraduálního
Obecná epidemiologie. MUDr. Miroslava Zavřelová Ústav preventivního lékařství, odd. epidemiologie infekčních chorob
 Obecná epidemiologie MUDr. Miroslava Zavřelová Ústav preventivního lékařství, odd. epidemiologie infekčních chorob Epidemiologie Studium hromadně se vyskytujících jevů Stanovení opatření intervence Analýza
Obecná epidemiologie MUDr. Miroslava Zavřelová Ústav preventivního lékařství, odd. epidemiologie infekčních chorob Epidemiologie Studium hromadně se vyskytujících jevů Stanovení opatření intervence Analýza
Světový týden očkování
 Světový týden očkování 24. 4. 30. 4. 2019 Protected Together #VaccinesWork Vakcíny jsou bezpečné a účinné Každá vakcína s licencí je před schválením pro použití přísně kontrolována Trvale jsou monitorovány
Světový týden očkování 24. 4. 30. 4. 2019 Protected Together #VaccinesWork Vakcíny jsou bezpečné a účinné Každá vakcína s licencí je před schválením pro použití přísně kontrolována Trvale jsou monitorovány
specifickou léčbu, 8. záškrt, 9. spalničky, 10. zarděnky.
 ODHAD RIZIKA A TYPOVÉ SITUACE PŘI PODEZŘENÍ NA VÝSKYT INFEKČNÍHO ONEMOCNĚNÍ NA PALUBĚ LETADLA PRO POTŘEBU SOUČINNOSTI SE SLOŽKAMI INTEGROVANÉHO ZÁCHRANNÉHO SYSTÉMU Přehled typových situací při podezření
ODHAD RIZIKA A TYPOVÉ SITUACE PŘI PODEZŘENÍ NA VÝSKYT INFEKČNÍHO ONEMOCNĚNÍ NA PALUBĚ LETADLA PRO POTŘEBU SOUČINNOSTI SE SLOŽKAMI INTEGROVANÉHO ZÁCHRANNÉHO SYSTÉMU Přehled typových situací při podezření
NEBUNĚČNÁ ŽIVÁ HMOTA VIRY
 NEBUNĚČNÁ ŽIVÁ HMOTA VIRY Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje 11.3.2011 Mgr.Petra Siřínková Rozdělení živé přírody 1.nadříše.PROKARYOTA 1.říše:Nebuněční
NEBUNĚČNÁ ŽIVÁ HMOTA VIRY Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje 11.3.2011 Mgr.Petra Siřínková Rozdělení živé přírody 1.nadříše.PROKARYOTA 1.říše:Nebuněční
Očkujete se před cestou do zahraničí?
 Očkujete se před cestou do zahraničí? Rozšiřuje se spektrum cestovatelských oblastí Měli byste! Rozšiřuje se spektrum infekčních onemocnění Rozšiřuje se spektrum doporučených očkování Některé státy při
Očkujete se před cestou do zahraničí? Rozšiřuje se spektrum cestovatelských oblastí Měli byste! Rozšiřuje se spektrum infekčních onemocnění Rozšiřuje se spektrum doporučených očkování Některé státy při
STŘEDNÍ ZDRAVOTNICKÁ ŠKOLA A VYŠŠÍ ODBORNÁ ŠKOLA ZDRAVOTNICKÁ ŽĎÁR NAD SÁZAVOU OBECNÁ EPIDEMIOLOGIE MGR. IVA COUFALOVÁ
 STŘEDNÍ ZDRAVOTNICKÁ ŠKOLA A VYŠŠÍ ODBORNÁ ŠKOLA ZDRAVOTNICKÁ ŽĎÁR NAD SÁZAVOU OBECNÁ EPIDEMIOLOGIE MGR. IVA COUFALOVÁ EPIDEMIOLOGIE je obor, který zkoumá rozložení infekčních chorob v populaci, sleduje
STŘEDNÍ ZDRAVOTNICKÁ ŠKOLA A VYŠŠÍ ODBORNÁ ŠKOLA ZDRAVOTNICKÁ ŽĎÁR NAD SÁZAVOU OBECNÁ EPIDEMIOLOGIE MGR. IVA COUFALOVÁ EPIDEMIOLOGIE je obor, který zkoumá rozložení infekčních chorob v populaci, sleduje
Současné trendy v klinice a epidemiologii tropických virových infekcí. XX. hradecké virologické dny - Současný svět a virové infekce
 Současné trendy v klinice a epidemiologii tropických virových infekcí XX. hradecké virologické dny - Současný svět a virové infekce Hradec Králové, 12. října 2016 František Stejskal Klinika infekčních
Současné trendy v klinice a epidemiologii tropických virových infekcí XX. hradecké virologické dny - Současný svět a virové infekce Hradec Králové, 12. října 2016 František Stejskal Klinika infekčních
Vývoj vakcín proti horečkám dengue, chikungunya a Zika
 Vývoj vakcín proti horečkám dengue, chikungunya a Zika MUDr. Milan Trojánek, Ph.D. Klinika infekčních nemocí 2. lékařská fakulta, Univerzita Karlova v Praze Katedra infekčních nemocí Institut postgraduálního
Vývoj vakcín proti horečkám dengue, chikungunya a Zika MUDr. Milan Trojánek, Ph.D. Klinika infekčních nemocí 2. lékařská fakulta, Univerzita Karlova v Praze Katedra infekčních nemocí Institut postgraduálního
PNEUMOKOKOVÉ INFEKCE A MOŽNOSTI PREVENCE aneb CO MŮŽE ZPŮSOBIT PNEUMOKOK
 PNEUMOKOKOVÉ INFEKCE A MOŽNOSTI PREVENCE aneb CO MŮŽE ZPŮSOBIT PNEUMOKOK Očkování! Nejvýznamnější možnost prevence infekčních chorob! Lepší infekční chorobě předcházet než ji léčit! Významný objev v medicíně,
PNEUMOKOKOVÉ INFEKCE A MOŽNOSTI PREVENCE aneb CO MŮŽE ZPŮSOBIT PNEUMOKOK Očkování! Nejvýznamnější možnost prevence infekčních chorob! Lepší infekční chorobě předcházet než ji léčit! Významný objev v medicíně,
Epidemie Q horečky v Nizozemí a situace v ČR
 Epidemie Q horečky v Nizozemí a situace v ČR Kateřina Fabiánová, Čestmír Beneš SZÚ Praha 24. Pečenkovy epidemiologické dny, 15. 17. 9.2010 České Budějovice Epidemiologické charakteristiky Původce: Coxiella
Epidemie Q horečky v Nizozemí a situace v ČR Kateřina Fabiánová, Čestmír Beneš SZÚ Praha 24. Pečenkovy epidemiologické dny, 15. 17. 9.2010 České Budějovice Epidemiologické charakteristiky Původce: Coxiella
SANCO/1468/200 Datum poslední aktualizace CZ verze : 29/12/2009
 SANCO/1468/200 poslední aktualizace CZ verze : 29/12/2009 PŘECHODNÁ USTANOVENÍ Seznam členských států, poţadujících přechodné podmínky stanovené v článku 9a nařízení Komise č. 1266/2007 z 26 října 2007,
SANCO/1468/200 poslední aktualizace CZ verze : 29/12/2009 PŘECHODNÁ USTANOVENÍ Seznam členských států, poţadujících přechodné podmínky stanovené v článku 9a nařízení Komise č. 1266/2007 z 26 října 2007,
Martina Havlíčková Helena Jiřincová. NRL pro chřipku, Státní zdravotní ústav
 Pandemic H1N1 2009 Martina Havlíčková Helena Jiřincová NRL pro chřipku, Státní zdravotní ústav Z historie H1N1 1916-1917 pravděpodobná cirkulace viru, malá ohniska, lokální epidemie ve vojenských táborech,
Pandemic H1N1 2009 Martina Havlíčková Helena Jiřincová NRL pro chřipku, Státní zdravotní ústav Z historie H1N1 1916-1917 pravděpodobná cirkulace viru, malá ohniska, lokální epidemie ve vojenských táborech,
Autochtonní přenos horečky chikungunya ve Francii a v Itálii, srpen-září 2017
 Autochtonní přenos horečky chikungunya ve Francii a v Itálii, srpen-září 2017 - souhrn rychlého hodnocení rizika Evropského centra pro kontrolu a prevenci nemocí (ECDC), ke dni 13.9.2017 Souhrn: Aktuálně
Autochtonní přenos horečky chikungunya ve Francii a v Itálii, srpen-září 2017 - souhrn rychlého hodnocení rizika Evropského centra pro kontrolu a prevenci nemocí (ECDC), ke dni 13.9.2017 Souhrn: Aktuálně
Přílohy. Příloha č. 1: Přehled rozvojových cílů tisíciletí
 Přílohy Příloha č. 1: Přehled rozvojových cílů tisíciletí 1. Název cíle Odstranit extrémní chudobu a hlad popis cíle -snížit na polovinu počet extrémně chudých lidí (ti, kteří mají méně než 1 dolar na
Přílohy Příloha č. 1: Přehled rozvojových cílů tisíciletí 1. Název cíle Odstranit extrémní chudobu a hlad popis cíle -snížit na polovinu počet extrémně chudých lidí (ti, kteří mají méně než 1 dolar na
Flavivirové nákazy preventabilní očkováním u cestovatelů
 Flavivirové nákazy preventabilní očkováním u cestovatelů Milan Trojánek Klinika infekčních nemocí 2. lékařská fakulta, Univerzita Karlova v Praze Klinika infekčních, parazitárních a tropických nemocí Nemocnice
Flavivirové nákazy preventabilní očkováním u cestovatelů Milan Trojánek Klinika infekčních nemocí 2. lékařská fakulta, Univerzita Karlova v Praze Klinika infekčních, parazitárních a tropických nemocí Nemocnice
Klinické formy sezónn. M.Havlíčková, H.Jiřincová, J.Kynčl
 Klinické formy sezónn nní, aviárn rní a nové chřipky u člověka M.Havlíčková, H.Jiřincová, J.Kynčl Ptačí chřipka - byla, je i bude, rezervoár nových subtypů, u člověka často velmi těžký průběh Sezónní chřipka
Klinické formy sezónn nní, aviárn rní a nové chřipky u člověka M.Havlíčková, H.Jiřincová, J.Kynčl Ptačí chřipka - byla, je i bude, rezervoár nových subtypů, u člověka často velmi těžký průběh Sezónní chřipka
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/
 I n v e s t i c e d o r o z v o j e v z d ě l á v á n í Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Tento projekt je spolufinancován Evropským sociálním fondem a státním
I n v e s t i c e d o r o z v o j e v z d ě l á v á n í Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Tento projekt je spolufinancován Evropským sociálním fondem a státním
Fatální forma influenzy drůbeţe v chovu krůt
 Fatální forma influenzy drůbeţe v chovu krůt Doc. MVDr. Petr Lány, Ph.D. Mgr. Kateřina Rosenbergová Ústav infekčních chorob a epizootologie MVDr. Miša Škorič, Ph.D. Ústav patologické morfologie Fakulta
Fatální forma influenzy drůbeţe v chovu krůt Doc. MVDr. Petr Lány, Ph.D. Mgr. Kateřina Rosenbergová Ústav infekčních chorob a epizootologie MVDr. Miša Škorič, Ph.D. Ústav patologické morfologie Fakulta
Mgr. Stanislav Zlámal osmý
 Jméno Mgr. Stanislav Zlámal Datum 11. 9. 2013 Ročník osmý Vzdělávací oblast Člověk a příroda Vzdělávací obor Zeměpis Tematický okruh Obyvatelstvo Téma klíčová slova HIV/AIDS Anotace Pracovní list žákům
Jméno Mgr. Stanislav Zlámal Datum 11. 9. 2013 Ročník osmý Vzdělávací oblast Člověk a příroda Vzdělávací obor Zeměpis Tematický okruh Obyvatelstvo Téma klíčová slova HIV/AIDS Anotace Pracovní list žákům
SAMOSTATNÁ PRÁCE 2012 jmeno a prijmeni
 ZÁPADOČESKÁ UNIVERZITA V PLZNI SAMOSTATNÁ PRÁCE 2012 jmeno a prijmeni ZÁPADOČESKÁ UNIVERZITA V PLZNI Příušnice Samostatná práce Informatika a výpočetní technika KIV/IFYER jmeno a prijmeni Obsah 1 Příušnice
ZÁPADOČESKÁ UNIVERZITA V PLZNI SAMOSTATNÁ PRÁCE 2012 jmeno a prijmeni ZÁPADOČESKÁ UNIVERZITA V PLZNI Příušnice Samostatná práce Informatika a výpočetní technika KIV/IFYER jmeno a prijmeni Obsah 1 Příušnice
Virové hepatitidy. MUDr. Jana Bednářová, PhD. OKM FN Brno
 Virové hepatitidy MUDr. Jana Bednářová, PhD. OKM FN Brno Hepatitida A Taxonomie: Picornaviridae, Hepatovirus Morfologie: neobalený ssrna-virus pozitivní polarity, nesegmentovaný, 27 32 nm Stabilita: termostabilní
Virové hepatitidy MUDr. Jana Bednářová, PhD. OKM FN Brno Hepatitida A Taxonomie: Picornaviridae, Hepatovirus Morfologie: neobalený ssrna-virus pozitivní polarity, nesegmentovaný, 27 32 nm Stabilita: termostabilní
Změna klimatu a lidské zdraví. Brno, 4. května 2010
 Změna klimatu a lidské zdraví Brno, 4. května 2010 odborný konzultant v oblasti zdravotních a ekologických rizik e-mail: miroslav.suta (at) centrum.cz Světový den zdraví 2008 Globální hrozba pro zdraví
Změna klimatu a lidské zdraví Brno, 4. května 2010 odborný konzultant v oblasti zdravotních a ekologických rizik e-mail: miroslav.suta (at) centrum.cz Světový den zdraví 2008 Globální hrozba pro zdraví
Hrozba epidemie, pandemie chřipka, HIV
 Inovace a zkvalitnění výuky v oblasti přírodních věd Člověk a příroda 8.ročník červenec 2012 Hrozba epidemie, pandemie chřipka, HIV Anotace: Kód: VY_52_INOVACE_ Čap-Z 8.,9.26 Vzdělávací oblast: Autor:
Inovace a zkvalitnění výuky v oblasti přírodních věd Člověk a příroda 8.ročník červenec 2012 Hrozba epidemie, pandemie chřipka, HIV Anotace: Kód: VY_52_INOVACE_ Čap-Z 8.,9.26 Vzdělávací oblast: Autor:
CZ.1.07/1.5.00/34.0527
 Projekt: Příjemce: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Projekt: Příjemce: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Spalničky v Moravskoslezském kraji MUDr. Irena Martinková, MUDr.Šárka Matlerová, MMO,
 Spalničky v Moravskoslezském kraji MUDr. Irena Martinková, MUDr.Šárka Matlerová, MMO, 18.5.2017 Krajská hygienická stanice Moravskoslezského kraje se sídlem v Ostravě Na Bělidle 7, 702 00 Ostrava, podatelna@khsova.cz,
Spalničky v Moravskoslezském kraji MUDr. Irena Martinková, MUDr.Šárka Matlerová, MMO, 18.5.2017 Krajská hygienická stanice Moravskoslezského kraje se sídlem v Ostravě Na Bělidle 7, 702 00 Ostrava, podatelna@khsova.cz,
Prasečí chřipka (mexická, Swine Flu, Novel Flu H1N1) MUDr. František BEŇA
 Prasečí chřipka (mexická, Swine Flu, Novel Flu H1N1) MUDr. František BEŇA Charakteristika Respirační onemocnění způsobené virem chřipky typu A u prasat s lehkými symptomy, vysokou morbiditou a nízkou mortalitou
Prasečí chřipka (mexická, Swine Flu, Novel Flu H1N1) MUDr. František BEŇA Charakteristika Respirační onemocnění způsobené virem chřipky typu A u prasat s lehkými symptomy, vysokou morbiditou a nízkou mortalitou
Zkušenosti s laboratorní diagnostikou infekcí virem Zika. Hana Zelená NRL pro arboviry Zdravotní ústav se sídlem v Ostravě
 Zkušenosti s laboratorní diagnostikou infekcí virem Zika Hana Zelená NRL pro arboviry Zdravotní ústav se sídlem v Ostravě Základní charakteristika viru Zika Čeleď Flaviviridae, rod Flavivirus obalený RNA
Zkušenosti s laboratorní diagnostikou infekcí virem Zika Hana Zelená NRL pro arboviry Zdravotní ústav se sídlem v Ostravě Základní charakteristika viru Zika Čeleď Flaviviridae, rod Flavivirus obalený RNA
DIFERENCIÁLNÍ DIAGNOSTIKA HOREČKY PO NÁVRATU Z TROPŮ
 DIFERENCIÁLNÍ DIAGNOSTIKA HOREČKY PO NÁVRATU Z TROPŮ Interaktivní prezentace Prof. MUDr. Jiří Beran, CSc. Centrum očkování a cestovní medicíny Hradec Králové JAKÁ JSOU RIZIKA PRO CESTOVATELE V ZAHRANIČÍ?
DIFERENCIÁLNÍ DIAGNOSTIKA HOREČKY PO NÁVRATU Z TROPŮ Interaktivní prezentace Prof. MUDr. Jiří Beran, CSc. Centrum očkování a cestovní medicíny Hradec Králové JAKÁ JSOU RIZIKA PRO CESTOVATELE V ZAHRANIČÍ?
Hepatitida E nejen akutní onemocnění. Petr Husa Klinika infekčních chorob, LF MU a FN Brno Hepatitida B v roce 2012, Praha, 28.4.
 Hepatitida E nejen akutní onemocnění Petr Husa Klinika infekčních chorob, LF MU a FN Brno Hepatitida B v roce 2012, Praha, 28.4.2012 Rozdělení virových hepatitid 1. Enterálně přenosné VH A chronicita dosud
Hepatitida E nejen akutní onemocnění Petr Husa Klinika infekčních chorob, LF MU a FN Brno Hepatitida B v roce 2012, Praha, 28.4.2012 Rozdělení virových hepatitid 1. Enterálně přenosné VH A chronicita dosud
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354
 I n v e s t i c e d o r o z v o j e v z d ě l á v á n í Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Tento projekt je spolufinancován Evropským sociálním fondem a státním
I n v e s t i c e d o r o z v o j e v z d ě l á v á n í Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Tento projekt je spolufinancován Evropským sociálním fondem a státním
Proč právě datum 12. 5.?
 Proč právě datum 12. 5.? Na počest narození britské reformátorky lékařské péče Florence Nightingaleové (1820-1910) osvícené, odvážné a neúnavné ženy, která byla ve druhé polovině svého života upoutána
Proč právě datum 12. 5.? Na počest narození britské reformátorky lékařské péče Florence Nightingaleové (1820-1910) osvícené, odvážné a neúnavné ženy, která byla ve druhé polovině svého života upoutána
Základní sazby zahraničního stravného pro rok 20092010
 Základní sazby zahraničního stravného pro rok 20092010 Země Měnový kód Měna Základní sazby stravného Afghánistán EUR euro 35 Albánie EUR euro 35 Alžírsko EUR euro 35 Andorra EUR euro 40 Angola USD americký
Základní sazby zahraničního stravného pro rok 20092010 Země Měnový kód Měna Základní sazby stravného Afghánistán EUR euro 35 Albánie EUR euro 35 Alžírsko EUR euro 35 Andorra EUR euro 40 Angola USD americký
MODUL č. III. Epidemiologie a Hygiena
 MODUL č. III Epidemiologie a Hygiena Definice epidemiologie a rozdělení Definice: Epidemiologie je nauka o teoretických a praktických otázkách ochrany před chorobami (infekčními i neinfekčními). Rozdělení
MODUL č. III Epidemiologie a Hygiena Definice epidemiologie a rozdělení Definice: Epidemiologie je nauka o teoretických a praktických otázkách ochrany před chorobami (infekčními i neinfekčními). Rozdělení
Zásah Lékařů bez hranic při epidemii eboly
 Zásah Lékařů bez hranic při epidemii eboly MUDr. Irena Janoušková Medicína Katastrof Brno 2015 Lékaři bez hranic - založeno ve Francii: Médecins sans Frontières (MsF) - nezávislá mezinárodní humanitární
Zásah Lékařů bez hranic při epidemii eboly MUDr. Irena Janoušková Medicína Katastrof Brno 2015 Lékaři bez hranic - založeno ve Francii: Médecins sans Frontières (MsF) - nezávislá mezinárodní humanitární
KRAJSKÁ HYGIENICKÁ STANICE MORAVSKOSLEZSKÉHO KRAJE SE SÍDLEM V OSTRAVĚ
 KRAJSKÁ HYGIENICKÁ STANICE MORAVSKOSLEZSKÉHO KRAJE SE SÍDLEM V OSTRAVĚ Vzdušné nákazy např. plané neštovice, spalničky, ARI (akutní respirační infekce) a další Akutní respirační infekce (ARI), včetně chřipky,
KRAJSKÁ HYGIENICKÁ STANICE MORAVSKOSLEZSKÉHO KRAJE SE SÍDLEM V OSTRAVĚ Vzdušné nákazy např. plané neštovice, spalničky, ARI (akutní respirační infekce) a další Akutní respirační infekce (ARI), včetně chřipky,
VNL. Onemocnění bílé krevní řady
 VNL Onemocnění bílé krevní řady Změny leukocytů V počtu leukocytů Ve vzájemném zastoupení morfologických typů leukocytů Ve funkci leukocytů Reaktivní změny leukocytů Leukocytóza: při bakteriální infekci
VNL Onemocnění bílé krevní řady Změny leukocytů V počtu leukocytů Ve vzájemném zastoupení morfologických typů leukocytů Ve funkci leukocytů Reaktivní změny leukocytů Leukocytóza: při bakteriální infekci
Chlíbek Roman. Katedra epidemiologie Fakulta vojenského zdravotnictví UO Hradec Králov. lové
 MÁME ME SE BÁT B T PTAČÍ CHŘIPKY? Chlíbek Roman Katedra epidemiologie Fakulta vojenského zdravotnictví UO Hradec Králov lové CHŘIPKA Chřipka typy A, B, C Subtyp A 2 povrchové proteiny: HA, NA Hemaglutitin
MÁME ME SE BÁT B T PTAČÍ CHŘIPKY? Chlíbek Roman Katedra epidemiologie Fakulta vojenského zdravotnictví UO Hradec Králov lové CHŘIPKA Chřipka typy A, B, C Subtyp A 2 povrchové proteiny: HA, NA Hemaglutitin
Epidemiologie spály. MUDr. František BEŇA
 Epidemiologie spály MUDr. František BEŇA Klinický obraz a diagnostika infekce Charakteristickým příznakem - exantém, pokud streptokok skupiny A produkuje pyrogenní exotoxin (erytrogenní toxin). Dif.dg.
Epidemiologie spály MUDr. František BEŇA Klinický obraz a diagnostika infekce Charakteristickým příznakem - exantém, pokud streptokok skupiny A produkuje pyrogenní exotoxin (erytrogenní toxin). Dif.dg.
Lymeská borrelióza epidemiologická data za rok 2014
 Lymeská borrelióza epidemiologická data za rok 2014 Mapy a grafy incidencí lymeské borreliózy v České republice. Maps and graphs of lyme borreliosis (Lyme disease) in the Czech Republic. 15.září 2015 Doc.MUDr.Bohumír
Lymeská borrelióza epidemiologická data za rok 2014 Mapy a grafy incidencí lymeské borreliózy v České republice. Maps and graphs of lyme borreliosis (Lyme disease) in the Czech Republic. 15.září 2015 Doc.MUDr.Bohumír
Nákazy s přírodní ohniskovostí. MUDr. Miroslava Zavřelová ÚPL LF MU
 Nákazy s přírodní ohniskovostí MUDr. Miroslava Zavřelová ÚPL LF MU Přírodní ohnisko nákazy oblast s jedním biotopem (konkrétními přírodními podmínkami) přítomnost zdrojů nákazy (rezervoárových zvířat)
Nákazy s přírodní ohniskovostí MUDr. Miroslava Zavřelová ÚPL LF MU Přírodní ohnisko nákazy oblast s jedním biotopem (konkrétními přírodními podmínkami) přítomnost zdrojů nákazy (rezervoárových zvířat)
Výskyt rotavirových onemocnění v České republice v letech , EpiDat Michaela Špačková, Martin Gašpárek
 Výskyt rotavirových onemocnění v České republice v letech 1997-2017, EpiDat Michaela Špačková, Martin Gašpárek Oddělení epidemiologie infekčních nemocí, Národní referenční centrum pro analýzu epidemiologických
Výskyt rotavirových onemocnění v České republice v letech 1997-2017, EpiDat Michaela Špačková, Martin Gašpárek Oddělení epidemiologie infekčních nemocí, Národní referenční centrum pro analýzu epidemiologických
Hantavirové onemocnění s úmrtím. Mgr. Monika Kurucová - ÚP Kladno
 Hantavirové onemocnění s úmrtím Mgr. Monika Kurucová - ÚP Kladno Co jsou to hantaviry? řadí se dočeledi Bunyaviridae obalené RNA viry hantavirové infekce jsou zoonózy, jejich rezervoárem jsou běžní drobní
Hantavirové onemocnění s úmrtím Mgr. Monika Kurucová - ÚP Kladno Co jsou to hantaviry? řadí se dočeledi Bunyaviridae obalené RNA viry hantavirové infekce jsou zoonózy, jejich rezervoárem jsou běžní drobní
Plasmodium Babesia. přenos: krevsajícím hmyzem infekce: červených krvinek
 Plasmodium Babesia přenos: krevsajícím hmyzem infekce: červených krvinek Plasmodium falciparum - genom Plasmodium vivax Plasmodium ovale Plasmodium malariae Plasmodium knowlesi krevní apicomplexa intracelulární
Plasmodium Babesia přenos: krevsajícím hmyzem infekce: červených krvinek Plasmodium falciparum - genom Plasmodium vivax Plasmodium ovale Plasmodium malariae Plasmodium knowlesi krevní apicomplexa intracelulární
West Nile Virus, aneb je třeba být připraven
 West Nile Virus, aneb je třeba být připraven RNDr. Eva Křížová, Ph.D Transfuzní a tkáňové oddělení Fakultní nemocnice Brno Taxonomické zařazení a charakteristika WNV Rod: Flavivirus Charakteristika: RNA
West Nile Virus, aneb je třeba být připraven RNDr. Eva Křížová, Ph.D Transfuzní a tkáňové oddělení Fakultní nemocnice Brno Taxonomické zařazení a charakteristika WNV Rod: Flavivirus Charakteristika: RNA
Varicella v těhotenství. K.Roubalová Vidia s.r.o.
 Varicella v těhotenství K.Roubalová Vidia s.r.o. Infekce VZV 90% v dětství (3-5 let), 10% v dospělosti (horší průběh) Většina primárních infekcí symptomatická - Varicella Vždy virémie Infekčnost: vysoká:
Varicella v těhotenství K.Roubalová Vidia s.r.o. Infekce VZV 90% v dětství (3-5 let), 10% v dospělosti (horší průběh) Většina primárních infekcí symptomatická - Varicella Vždy virémie Infekčnost: vysoká:
Výskyt a význam infekce Borna disease virem u pacientů léčených
 Výskyt a význam infekce Borna disease virem u pacientů léčených pro závislost Sylva Racková Psychiatrická klinika LF UK v Plzni AT konference 28.04. 2010, Špindlerův Mlýn Borna Disease virus (BDV) charakteristika
Výskyt a význam infekce Borna disease virem u pacientů léčených pro závislost Sylva Racková Psychiatrická klinika LF UK v Plzni AT konference 28.04. 2010, Špindlerův Mlýn Borna Disease virus (BDV) charakteristika
Vzdělávací materiál projektu Zlepšení podmínek výuky v ZŠ Sloup
 Kód: Vzdělávací materiál projektu Zlepšení podmínek výuky v ZŠ Sloup Název vzdělávacího materiálu Imunita a infekční nemoci Anotace Pracovní list seznamuje žáka s druhy infekčních chorob a se způsoby jejich
Kód: Vzdělávací materiál projektu Zlepšení podmínek výuky v ZŠ Sloup Název vzdělávacího materiálu Imunita a infekční nemoci Anotace Pracovní list seznamuje žáka s druhy infekčních chorob a se způsoby jejich
Co víme nového o borelióze a klíšťové meningoencefalitidě?
 Co víme nového o borelióze a klíšťové meningoencefalitidě? Schánilec P. Hájek I. Agudelo C. F. Tato prezentace je spolufinancována Evropským sociálním fondem a státním rozpočtem České republiky. Rozšíření
Co víme nového o borelióze a klíšťové meningoencefalitidě? Schánilec P. Hájek I. Agudelo C. F. Tato prezentace je spolufinancována Evropským sociálním fondem a státním rozpočtem České republiky. Rozšíření
Virus lidského imunodeficitu. MUDr. Jana Bednářová, PhD. OKM FN Brno
 Virus lidského imunodeficitu MUDr. Jana Bednářová, PhD. OKM FN Brno HIV Human Immunodeficiency Virus AIDS Acquired Immunodeficiency Syndrome SIDA Syndrome d immuno-déficience acquise Historie původně opičí
Virus lidského imunodeficitu MUDr. Jana Bednářová, PhD. OKM FN Brno HIV Human Immunodeficiency Virus AIDS Acquired Immunodeficiency Syndrome SIDA Syndrome d immuno-déficience acquise Historie původně opičí
Chřipka podceňované onemocnění
 Chřipka podceňované onemocnění Tisková konference MZ, 21. prosince 2017, Praha Chlíbek Roman Katedra epidemiologie Fakulta vojenského zdravotnictví UO Česká vakcinologická společnost ČLS JEP Hradec Králové
Chřipka podceňované onemocnění Tisková konference MZ, 21. prosince 2017, Praha Chlíbek Roman Katedra epidemiologie Fakulta vojenského zdravotnictví UO Česká vakcinologická společnost ČLS JEP Hradec Králové
Arbovirové infekce v transfuzní medicíně riziko přenosu arbovirů Zika, WNV, dengue, chikungunya
 Arbovirové infekce v transfuzní medicíně riziko přenosu arbovirů Zika, WNV, dengue, chikungunya Odborný seminář firmy DiaSorin pro Zařízení transfuzní služby Zámek Berchtold, 25. května 2016 František
Arbovirové infekce v transfuzní medicíně riziko přenosu arbovirů Zika, WNV, dengue, chikungunya Odborný seminář firmy DiaSorin pro Zařízení transfuzní služby Zámek Berchtold, 25. května 2016 František
Co je prasečí chřipka?
 Co je prasečí chřipka? Prasečí chřipka je respirační onemocnění u prasat způsobené virem chřipky typu A, které u nich často propuká. Lidé za normálních okolností touto nemocí neonemocní, ale k nakažení
Co je prasečí chřipka? Prasečí chřipka je respirační onemocnění u prasat způsobené virem chřipky typu A, které u nich často propuká. Lidé za normálních okolností touto nemocí neonemocní, ale k nakažení
 www.printo.it/pediatric-rheumatology/cz/intro Lymeská artritida Verze č 2016 1. CO JE LYMESKÁ ARTRITIDA? 1.1. Co to je? Lymeská artritida je jednou z nemocí vyvolaných bakterií Borrelia burgdorferi (lymeská
www.printo.it/pediatric-rheumatology/cz/intro Lymeská artritida Verze č 2016 1. CO JE LYMESKÁ ARTRITIDA? 1.1. Co to je? Lymeská artritida je jednou z nemocí vyvolaných bakterií Borrelia burgdorferi (lymeská
HEMOFILIE - DIAGNOSTIKA A LÉČBA V SOUČASNOSTI
 HEMOFILIE - DIAGNOSTIKA A LÉČBA V SOUČASNOSTI Patofyziologie hemofilie Deficit koagulačního faktoru VIII (hemofilie A) nebo IX (hemofilie B), jeho dysfunkce nebo přítomnost jeho inhibitorů vede k poruše
HEMOFILIE - DIAGNOSTIKA A LÉČBA V SOUČASNOSTI Patofyziologie hemofilie Deficit koagulačního faktoru VIII (hemofilie A) nebo IX (hemofilie B), jeho dysfunkce nebo přítomnost jeho inhibitorů vede k poruše
Pertussis - Dávivý (černý) kašel. MUDr. František BEŇA
 Pertussis - Dávivý (černý) kašel MUDr. František BEŇA Původce - agens Bordetella pertussis, kokobacil citlivý na sluneční záření, teplo, vyschnutí a běžné dezinfekční prostředky. Výskyt ve čtyřech antigenních
Pertussis - Dávivý (černý) kašel MUDr. František BEŇA Původce - agens Bordetella pertussis, kokobacil citlivý na sluneční záření, teplo, vyschnutí a běžné dezinfekční prostředky. Výskyt ve čtyřech antigenních
Respirační viry. MUDr. Jana Bednářová, Ph.D. OKM FN Brno
 Respirační viry MUDr. Jana Bednářová, Ph.D. OKM FN Brno Respirační viry Viry chřipky A, B, C Adenoviry Respirační syncyciální virus Viry parainfluenzy Rhinoviry Koronaviry Vyjímečně: virus herpes simplex,
Respirační viry MUDr. Jana Bednářová, Ph.D. OKM FN Brno Respirační viry Viry chřipky A, B, C Adenoviry Respirační syncyciální virus Viry parainfluenzy Rhinoviry Koronaviry Vyjímečně: virus herpes simplex,
EPIDEMIE HOREČKY CHIKUNGUNYA
 EPIDEMIE HOREČKY CHIKUNGUNYA Tropické nemoci, 1. LF UK Praha MUDr. RNDr. František Stejskal, PhD Oddělení tropické medicíny III. klinika infekčních a tropických nemocí 1.LF UK a FN Bulovka tel. 2 2496
EPIDEMIE HOREČKY CHIKUNGUNYA Tropické nemoci, 1. LF UK Praha MUDr. RNDr. František Stejskal, PhD Oddělení tropické medicíny III. klinika infekčních a tropických nemocí 1.LF UK a FN Bulovka tel. 2 2496
Co nového přinesl chřipkový kongres Toronto VI.2007
 Co nového přinesl chřipkový kongres Toronto 17.-23.VI.2007 Havlík J 1, Havlíčková M 2, Kynčl J 2 Infekční klinika, FN Na Bulovce, Praha 1 Státní Zdravotní Ústav Praha 2 Options for the Control of Influenza
Co nového přinesl chřipkový kongres Toronto 17.-23.VI.2007 Havlík J 1, Havlíčková M 2, Kynčl J 2 Infekční klinika, FN Na Bulovce, Praha 1 Státní Zdravotní Ústav Praha 2 Options for the Control of Influenza
FN Hradec Králové JIP GMK. Vypracovala: Monika Uhlířová Dis.
 Nozokomiální nákazy FN Hradec Králové JIP GMK Vypracovala: Monika Uhlířová Dis. Definice: Vznikají v souvislosti s hospitalizací. Máme-li infekci označit za nozokomiální, musí být zřejmé, že nebyla přítomna
Nozokomiální nákazy FN Hradec Králové JIP GMK Vypracovala: Monika Uhlířová Dis. Definice: Vznikají v souvislosti s hospitalizací. Máme-li infekci označit za nozokomiální, musí být zřejmé, že nebyla přítomna
V roce 1981 byly v USA poprvé popsány příznaky nového onemocnění, které později dostalo jméno AIDS /Acquired Immune Deficiency Syndrome/ neboli
 Lenka Klimešová V roce 1981 byly v USA poprvé popsány příznaky nového onemocnění, které později dostalo jméno AIDS /Acquired Immune Deficiency Syndrome/ neboli Syndrom získaného imunodeficitu. V roce 1983
Lenka Klimešová V roce 1981 byly v USA poprvé popsány příznaky nového onemocnění, které později dostalo jméno AIDS /Acquired Immune Deficiency Syndrome/ neboli Syndrom získaného imunodeficitu. V roce 1983
Akutní a chronické hepatitidy
 Akutní a chronické hepatitidy MUDr. Jana Bednářová, PhD. Oddělení klinické mikrobiologie FN Brno Hepatitida zánět a poškození jater různými etiologickými agens zahrnujícími neinfekční příčiny i různá infekční
Akutní a chronické hepatitidy MUDr. Jana Bednářová, PhD. Oddělení klinické mikrobiologie FN Brno Hepatitida zánět a poškození jater různými etiologickými agens zahrnujícími neinfekční příčiny i různá infekční
Laboratorní diagnostika spalniček. A. Vinciková, E. Jílková Zdravotní ústav se sídlem v Ústí nad Labem
 Laboratorní diagnostika spalniček A. Vinciková, E. Jílková Zdravotní ústav se sídlem v Ústí nad Labem Spalničky Morbilli (lat.), osýpky (slovensky), measles (anglicky) původcem je Morbillivirus z čeledi
Laboratorní diagnostika spalniček A. Vinciková, E. Jílková Zdravotní ústav se sídlem v Ústí nad Labem Spalničky Morbilli (lat.), osýpky (slovensky), measles (anglicky) původcem je Morbillivirus z čeledi
Epidemie žluté zimnice v Brazílii aktualizace k 22. březnu 2018
 Epidemie žluté zimnice v Brazílii 2017-2018 aktualizace k 22. březnu 2018 Případy onemocnění žlutou zimnicí u lidí v Brazílii Od července 2017 do 11. kalendářního týdne 2018 bylo v Brazílii hlášeno 1098
Epidemie žluté zimnice v Brazílii 2017-2018 aktualizace k 22. březnu 2018 Případy onemocnění žlutou zimnicí u lidí v Brazílii Od července 2017 do 11. kalendářního týdne 2018 bylo v Brazílii hlášeno 1098
ZÁNĚTLIVÁ ONEMOCNĚNÍ CNS. Markéta Vojtová VOŠZ a SZŠ Hradec Králové
 ZÁNĚTLIVÁ ONEMOCNĚNÍ CNS Markéta Vojtová VOŠZ a SZŠ Hradec Králové Neuroinfekce 1 Dle toho, co postihují: Meningitidy Encefalitidy Myelitidy Kombinovaná postižení Meningoencefalitidy Encefalomyelitidy
ZÁNĚTLIVÁ ONEMOCNĚNÍ CNS Markéta Vojtová VOŠZ a SZŠ Hradec Králové Neuroinfekce 1 Dle toho, co postihují: Meningitidy Encefalitidy Myelitidy Kombinovaná postižení Meningoencefalitidy Encefalomyelitidy
CZ.1.07/1.5.00/34.0527
 Projekt: Příjemce: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Projekt: Příjemce: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
VY_32_INOVACE_07_B_18.notebook. July 08, 2013
 1 Škola Autor Název Téma SOŠ a SOU Milevsko Mgr. Jaroslava Neumannová VY_32_INOVACE_07_B_18_ZDR Vzdušné nákazy Datum tvorby 6.5.2013 Číslo projektu CZ.1.07/1.5.00/34.0557III/2 Inovace a zkvalitněnívýuky
1 Škola Autor Název Téma SOŠ a SOU Milevsko Mgr. Jaroslava Neumannová VY_32_INOVACE_07_B_18_ZDR Vzdušné nákazy Datum tvorby 6.5.2013 Číslo projektu CZ.1.07/1.5.00/34.0557III/2 Inovace a zkvalitněnívýuky
Leishmaniáza staronová hrozba
 Leishmaniáza staronová hrozba Dlhý J., KřížK B., Beneš Č. 24. Pečenkovy epidemiologické dny 15. 17. září 2010, České Budějovice Výskyt leishmaniázy ve světě prevalence = 12 milionů osob incidence = 1,5
Leishmaniáza staronová hrozba Dlhý J., KřížK B., Beneš Č. 24. Pečenkovy epidemiologické dny 15. 17. září 2010, České Budějovice Výskyt leishmaniázy ve světě prevalence = 12 milionů osob incidence = 1,5
RNDr K.Roubalová CSc.
 Cytomegalovirus RNDr K.Roubalová CSc. www.vidia.cz kroubalova@vidia.cz Lidský cytomegalovirus Β-herpesviridae, p největší HV (240 nm), cca 160 genů Příbuzné viry: myší, krysí, opičí, morčecí Kosmopolitní
Cytomegalovirus RNDr K.Roubalová CSc. www.vidia.cz kroubalova@vidia.cz Lidský cytomegalovirus Β-herpesviridae, p největší HV (240 nm), cca 160 genů Příbuzné viry: myší, krysí, opičí, morčecí Kosmopolitní
Seminář GPS IV. ročník NEMOCI A EPIDEMIE referát
 Gymnázium Dr. J. Pekaře Mladá Boleslav Seminář GPS IV. ročník NEMOCI A EPIDEMIE referát Jméno a příjmení: Matěj CHUMLEN Třída: 4. A Datum: 2. 11. 2014 Nemoci a epidemie 1. Základní informace I přes progresivně
Gymnázium Dr. J. Pekaře Mladá Boleslav Seminář GPS IV. ročník NEMOCI A EPIDEMIE referát Jméno a příjmení: Matěj CHUMLEN Třída: 4. A Datum: 2. 11. 2014 Nemoci a epidemie 1. Základní informace I přes progresivně
Anaplasma phagocytophilum - další z patogenů přenášených klíšťaty (kazuistika)
 Anaplasma phagocytophilum - další z patogenů přenášených klíšťaty (kazuistika) Ivana Stiborová1, Vlastimil Král1, Jana Pazderková2, Jitka Pohořská1, Josef Richter1 1 Centrum imunologie a mikrobiologie,
Anaplasma phagocytophilum - další z patogenů přenášených klíšťaty (kazuistika) Ivana Stiborová1, Vlastimil Král1, Jana Pazderková2, Jitka Pohořská1, Josef Richter1 1 Centrum imunologie a mikrobiologie,
Klíšťová encefalitida
 Klíšťová encefalitida MUDr. Tomáš Simota 12.5. 2012 Šafránkův pavilon, Plzeň Klinika pracovního lékařství LF UK a FN v Plzni Projekt Pracovní lékařství pro lékaře všech odborností Registrační číslo projektu
Klíšťová encefalitida MUDr. Tomáš Simota 12.5. 2012 Šafránkův pavilon, Plzeň Klinika pracovního lékařství LF UK a FN v Plzni Projekt Pracovní lékařství pro lékaře všech odborností Registrační číslo projektu
Očkování proti sezónní chřipce - Otázky a odpovědi
 Očkování proti sezónní chřipce - Otázky a odpovědi Co je chřipka. Jak se chřipka šíří. Kdo je chřipkou nejvíce ohrožen. Jak se chřipka léčí. Jak se proti chřipce bránit. Co je to chřipková vakcína. Kdy
Očkování proti sezónní chřipce - Otázky a odpovědi Co je chřipka. Jak se chřipka šíří. Kdo je chřipkou nejvíce ohrožen. Jak se chřipka léčí. Jak se proti chřipce bránit. Co je to chřipková vakcína. Kdy
Příloha č. 1. Kódovací kniha Jednotka měření: pořad
 Příloha č. 1 Kódovací kniha Jednotka měření: pořad 1 Země původu kód 2 Kontinent kód 1 Alžírsko 1 Afrika 2 Angola 1 Afrika 3 Benin 1 Afrika 4 Botswana 1 Afrika 5 Burundi 1 Afrika 6 Burkina Faso 1 Afrika
Příloha č. 1 Kódovací kniha Jednotka měření: pořad 1 Země původu kód 2 Kontinent kód 1 Alžírsko 1 Afrika 2 Angola 1 Afrika 3 Benin 1 Afrika 4 Botswana 1 Afrika 5 Burundi 1 Afrika 6 Burkina Faso 1 Afrika
Familiární středomořská (Mediterranean) horečka (Fever)
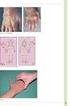 www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
Obsah. IMUNOLOGIE... 57 1 Imunitní systém... 57 Anatomický a fyziologický základ imunitní odezvy... 57
 Obsah Předmluva... 13 Nejdůležitější pojmy používané v textu publikace... 14 MIKROBIOLOGIE... 23 Mikroorganismy a lidský organismus... 24 Třídy patogenních mikroorganismů... 25 A. Viry... 25 B. Bakterie...
Obsah Předmluva... 13 Nejdůležitější pojmy používané v textu publikace... 14 MIKROBIOLOGIE... 23 Mikroorganismy a lidský organismus... 24 Třídy patogenních mikroorganismů... 25 A. Viry... 25 B. Bakterie...
EBOLA pokyny při výskytu onemocnění. pro potřeby ambulantních specialistů SAOF
 EBOLA pokyny při výskytu onemocnění! pro potřeby ambulantních specialistů SAOF virus eboly řadí se mezi filoviry (RNA viry) známe 5 typů ebola viru : Zaire, Bundibugyo, Sudan, Reston, Taï Forest. dnešní
EBOLA pokyny při výskytu onemocnění! pro potřeby ambulantních specialistů SAOF virus eboly řadí se mezi filoviry (RNA viry) známe 5 typů ebola viru : Zaire, Bundibugyo, Sudan, Reston, Taï Forest. dnešní
po přisátí klíštěte virus prokazován kůže virémie buňky RES (slezina, játra, kostní dřeň) mechanismus invaze do CNS nejasný, HEB při virémii
 Středoevropská klíšťová meningoencefalitida klinický obraz MUDr. Dita Smíšková, PhD Doc.MUDr.Vilma Marešová, CSc. MEK patogeneze po přisátí klíštěte virus prokazován nejprve v Langerhansových h buňkách
Středoevropská klíšťová meningoencefalitida klinický obraz MUDr. Dita Smíšková, PhD Doc.MUDr.Vilma Marešová, CSc. MEK patogeneze po přisátí klíštěte virus prokazován nejprve v Langerhansových h buňkách
Vrozený zarděnkový syndrom - kazuistika. MUDr. Martina Marešová HS hl.m. Prahy
 Vrozený zarděnkový syndrom - kazuistika MUDr. Martina Marešová HS hl.m. Prahy Zarděnky - historie zarděnky byly poprvé popsány ve 2. pol. 18. stol. v roce 1866 nazvány rubella v roce 1941 australský oftalmolog
Vrozený zarděnkový syndrom - kazuistika MUDr. Martina Marešová HS hl.m. Prahy Zarděnky - historie zarděnky byly poprvé popsány ve 2. pol. 18. stol. v roce 1866 nazvány rubella v roce 1941 australský oftalmolog
ROTAVIRUS ROTAVIRUS. Nyní mimořádný příspěvek VZP výše 1500 Kč. až do výše 1500 Kč. Je rozšířený, nakažlivý a může být nebezpečný. vašeho dítěte.
 ROTAVIRUS ROTAVIRUS Nyní mimořádný příspěvek VZP až domimořádný výše 1500 Kč. Nyní příspěvek VZP až do výše 1500 Kč. Je rozšířený, nakažlivý a může být nebezpečný. Je rozšířený, nakažlivý Přečtěte si o
ROTAVIRUS ROTAVIRUS Nyní mimořádný příspěvek VZP až domimořádný výše 1500 Kč. Nyní příspěvek VZP až do výše 1500 Kč. Je rozšířený, nakažlivý a může být nebezpečný. Je rozšířený, nakažlivý Přečtěte si o
Legionelóza, Legionářská nemoc (Leccos)
 Legionelóza, Legionářská nemoc (Leccos) Autor: Alena Kohoutková Výskyt Legionelóza je infekční onemocnění, které je rozšířeno po celém světě. Svůj název dostala podle členů americké legie, kteří se jí
Legionelóza, Legionářská nemoc (Leccos) Autor: Alena Kohoutková Výskyt Legionelóza je infekční onemocnění, které je rozšířeno po celém světě. Svůj název dostala podle členů americké legie, kteří se jí
EBOLA CO MOŽNÁ NEVÍTE
 EBOLA CO MOŽNÁ NEVÍTE MUDr. Jana Vidunová ZZS Plzeňského kraje HISTORIE poprvé popsána již v roce 1976 název podle říčky Ebola nacházející na území dnešní Demokratické republiky Kongo od roku 1976 asi
EBOLA CO MOŽNÁ NEVÍTE MUDr. Jana Vidunová ZZS Plzeňského kraje HISTORIE poprvé popsána již v roce 1976 název podle říčky Ebola nacházející na území dnešní Demokratické republiky Kongo od roku 1976 asi
PŘÍPRAVA ZDRAVOTNICKÉHO ZAŘÍZENÍ NA PANDEMII CHŘIPKY
 PŘÍPRAVA ZDRAVOTNICKÉHO ZAŘÍZENÍ NA PANDEMII CHŘIPKY TEORIE A PRAXE MUDr. Jarmila Kohoutová Oddělení nemocniční hygieny FNOL V.celostátní konference Medicína katastrof, traumatologické plánování a příprava,
PŘÍPRAVA ZDRAVOTNICKÉHO ZAŘÍZENÍ NA PANDEMII CHŘIPKY TEORIE A PRAXE MUDr. Jarmila Kohoutová Oddělení nemocniční hygieny FNOL V.celostátní konference Medicína katastrof, traumatologické plánování a příprava,
CZ.1.07/1.5.00/34.0527
 Projekt: Příjemce: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
Projekt: Příjemce: Digitální učební materiály ve škole, registrační číslo projektu CZ.1.07/1.5.00/34.0527 Střední zdravotnická škola a Vyšší odborná škola zdravotnická, Husova 3, 371 60 České Budějovice
PROBLEMATIKA SENIORŮ V OŠETŘOVATELSTVÍ
 Vysoká škola zdravotnická, o. p. s. PROBLEMATIKA SENIORŮ V OŠETŘOVATELSTVÍ 1 4. M E Z I N Á R O D N Í V Ě D E C K Á K O N F E R E N C E Očkování seniorů Lidmila Hamplová 16. DUBEN 2019 Očkování seniorů
Vysoká škola zdravotnická, o. p. s. PROBLEMATIKA SENIORŮ V OŠETŘOVATELSTVÍ 1 4. M E Z I N Á R O D N Í V Ě D E C K Á K O N F E R E N C E Očkování seniorů Lidmila Hamplová 16. DUBEN 2019 Očkování seniorů
N A Ř Í Z E N Í č. 4 /2007
 N A Ř Í Z E N Í č. 4 /2007 Č.j. 191/07-EPI-2397/2007 Krajské veterinární správy pro Liberecký kraj ze dne 30. listopadu 2007 Krajská veterinární správa pro Liberecký kraj, jako místně a věcně příslušný
N A Ř Í Z E N Í č. 4 /2007 Č.j. 191/07-EPI-2397/2007 Krajské veterinární správy pro Liberecký kraj ze dne 30. listopadu 2007 Krajská veterinární správa pro Liberecký kraj, jako místně a věcně příslušný
Globální prevalence nadváhy a obezity u dospělých podle oblastí
 Globál prevalence nadváhy a obezity u dospělých podle oblastí Evropská oblast Albánie 2008-9 Národ 10302 15-49 44.8 8.5 29.6 9.7 DHS Arménie 2005 Národ 6016 15-49 26.9 15.5 DHS Rakousko 2005/6 Národ 1054
Globál prevalence nadváhy a obezity u dospělých podle oblastí Evropská oblast Albánie 2008-9 Národ 10302 15-49 44.8 8.5 29.6 9.7 DHS Arménie 2005 Národ 6016 15-49 26.9 15.5 DHS Rakousko 2005/6 Národ 1054
Výskyt tohoto onemocn ní v Evrop má pokra ování v pr hu m síce srpna roku 2007
 Zprávy CEM (SZÚ, Praha) 2007; 16(9): 407 409. Aktuálně k výskytu onemocnění Chikungunya Latest news on Chikungunya Michaela Kubínyiová, Jan Kynčl Virová horečka Chikungunya patří mezi tzv. nově se objevující
Zprávy CEM (SZÚ, Praha) 2007; 16(9): 407 409. Aktuálně k výskytu onemocnění Chikungunya Latest news on Chikungunya Michaela Kubínyiová, Jan Kynčl Virová horečka Chikungunya patří mezi tzv. nově se objevující
HIV / AIDS MUDr. Miroslava Zavřelová Ústav preventivního lékařství LF MU
 HIV / AIDS MUDr. Miroslava Zavřelová Ústav preventivního lékařství LF MU e-mail: mizavrel@med.muni.cz I.E.S. Brno, 14. 10. 2014 Historie nákazy 1981 San Francisko, New York mladí pacienti s neobvyklými
HIV / AIDS MUDr. Miroslava Zavřelová Ústav preventivního lékařství LF MU e-mail: mizavrel@med.muni.cz I.E.S. Brno, 14. 10. 2014 Historie nákazy 1981 San Francisko, New York mladí pacienti s neobvyklými
Laboratorní di agnostik HBV HCV a Vratislav Němeček Státní zdravotní stav ústav
 Laboratorní diagnostika HBV a HCV Vratislav Němeček Státní zdravotní ústav Rozdílná role sexuálního 30 přenosu HBV a HCV 25 Rozdíly v četnosti virové nálože 20 15 10 HCV RNA HBV DNA HBV 5 hlavní způsoby
Laboratorní diagnostika HBV a HCV Vratislav Němeček Státní zdravotní ústav Rozdílná role sexuálního 30 přenosu HBV a HCV 25 Rozdíly v četnosti virové nálože 20 15 10 HCV RNA HBV DNA HBV 5 hlavní způsoby
AKTUÁLNE TRENDY V CESTOVNEJ MEDICÍNE A NOVINKY V OČKOVANÍ
 AKTUÁLNE TRENDY V CESTOVNEJ MEDICÍNE A NOVINKY V OČKOVANÍ Doc. MUDr. Rastislav Maďar, Ph.D., MBA, FFTM RCPS (Glasg.) Slovenský vakcinologický kongres 2017 Prednáška je podporená spoločnosťou Sanofi Pasteur
AKTUÁLNE TRENDY V CESTOVNEJ MEDICÍNE A NOVINKY V OČKOVANÍ Doc. MUDr. Rastislav Maďar, Ph.D., MBA, FFTM RCPS (Glasg.) Slovenský vakcinologický kongres 2017 Prednáška je podporená spoločnosťou Sanofi Pasteur
