Optimalizace podmínek derivatizace vybraných aminokyselin pomocí FMOC-Cl
|
|
|
- Simona Dostálová
- před 7 lety
- Počet zobrazení:
Transkript
1 UNIVERZITA KARLOVA V PRAZE P ř í r o d o v ě d e c k á f a k u l t a Studijní program: Chemie Studijní obor: Chemie v přírodních vědách Marie Chytrová Optimalizace podmínek derivatizace vybraných aminokyselin pomocí FMOC-Cl Optimization of derivatization conditions of selected amino acids with FMOC-Cl Bakalářská práce Vedoucí bakalářské práce: Doc. RNDr. Zuzana Bosáková Praha, 2012
2 Tato bakalářská práce vznikla v souvislosti s řešením výzkumného záměru MSM a grantu GA AV IAAX Prohlášení: Prohlašuji, že jsem závěrečnou práci zpracovala samostatně a že jsem uvedla všechny použité informační zdroje a literaturu. Tato práce ani její podstatná část nebyla předložena k získání jiného nebo stejného akademického titulu. V Praze dne.. podpis 2
3 Ráda bych touto cestou poděkovala své školitelce Doc. RNDr. Zuzaně Bosákové, CSc. za odborné vedení, ochotu, cenné rady a trpělivost, s níž se mi věnovala a za pomoc při zpracování výsledků této bakalářské práce. Dále děkuji kolektivu v laboratoři za vytvoření přátelského pracovního prostředí a své rodině, která mě po celou dobu studia podporovala. 3
4 ABSTRAKT Chirální HPLC metoda (mobilní fáze methanol/0,5% triethylamoniumoctanový pufr, ph 6,0 40/60 (v/v), teikoplaninová chirální stacionární fáze, fluorescenční detekce - ex 254 nm, em 314 nm) byla použita pro sledování výtěžnosti derivatizační reakce pro D/L-alanin, D/L-valin, D/L-leucin a D/L-isoleucin. Pro derivatizaci byl použit 9-fluorenylmethylchlormravenčan (FMOC-Cl). Byl sledován vliv ph 0,2 M vodného roztoku NaHCO 3 (8,0 9,5) a teploty derivatizace (22, 40 a 60 C) na výtěžnost derivatizace, která byla sledována velikostí plochy píku D-enantiomeru jednotlivých aminokyselin. Bylo zjištěno, že optimální hodnota ph je 8,5 a teplota 40 C. Vypracovaná metoda byla aplikována na reálný vzorek, výživový doplněk BCAA Extreme Pure obsahující L-isoleucin, L-leucin a L-valin. Bylo zjištěno, že preparát neobsahuje žádný balastní D-enantiomer Klíčová slova: chirální HPLC, teikoplanin, aminokyseliny, derivatizace, 9-fluorenyl- methylchlormravenčan (FMOC-Cl). 4
5 ABSTRACT Chiral HPLC method (mobile phase methanol/0.5% triethylammonium acetate buffer, ph /60 (v/v), teicoplanin based chiral stationary phase, fluorescence detection - - ex 254 nm, em 314 nm) was used for studying a recovery of derivatization procedure for D/L-alanin, D/L-valin, D/L-leucin and D/L-isoleucin. 9-Fluorenylmethyl chloroformate (FMOC-Cl) was used as a derivatization agent. The influence of derivatization temperature (22, 40 and 60 C) and ph value of 0.2 M NaHCO 3 ( ) on derivatization recovery was monitored in terms of D-enantiomer peak areas for the individual amino acid. The optimal derivatization conditions were found to be ph 8.5 and temperature 40 C. The developed method was applied to analysis of the real sample, food supplement BCCA Extreme Pure, containing L-isoleucin, L-leucin and L-valin. The sample was D-enantiomers free. Key words: chiral HPLC, teicoplanin, amino acids, derivatization, 9-fluorenylmethyl chloroformate (FMOC-Cl). 5
6 OBSAH 1. ÚVOD TEORETICKÁ ČÁST 2.1 Enantiomery Chirální separace v HPLC Makrocyklická antibiotika Aminokyseliny Derivatizace Vysokoúčinná kapalinová chromatografie EXPERIMENTÁLNÍ ČÁST 3.1 Chemikálie Přístroje a pomůcky Mobilní fáze a podmínky měření Příprava vzorků a činidel VÝSLEDKY A DISKUSE 4.1 Porovnání separace aminokyselin v nativním stavu a derivatizované formě Derivatizace Porovnání standardů derivatizovaných aminokyselin s derivatizovanými aminokyselinami Optimalizace průběhu derivatizace použitím hydrogenuhličitanu sodného o různé hodnotě ph Vliv teploty na průběh derivatizace Analýza reálného vzorku ZÁVĚR POUŽITÁ LITERATURA
7 SEZNAM ZKRATEK A SYMBOLŮ α A ACN BCAA D/L-Ala D/L-Ile D/L-Leu D/L-Val FMOC-Cl H HILIC h n HPLC k L LOD LOQ λ m MeOH n ot/min R RP-HPLC TEAA pufr t M t R v/v w w 1/2 selektivita plocha píku acetonitril aminokyseliny s rozvětveným řetězcem D/L-alanin D/L-isoleucin D/L-leucin D/L-valin 9-fluorenylmethylchlormravenčan výškový ekvivalent teoretického patra hydrofilní interakční chromatografie šum základní linie vysokoúčinná kapalinová chromatografie retenční faktor délka kolony mez detekce mez stanovitelnosti vlnová délka směrnice kalibrační křivky methanol účinnost počet otáček za 1 minutu rozlišení vysokoúčinná kapalinová chromatografie s obrácenými fázemi triethylamoniumoctanový pufr mrtvý čas kolony retenční čas objem/objem (objemový poměr složek mobilní fáze) šířka píku při základně šířka píku v polovině výšky 7
8 1. ÚVOD V současné době je věnována velká pozornost sledování stereoselektivního chování přírodních i uměle připravených sloučenin, jejichž enantiomery mohou mít odlišné biologické i fyziologické vlastnosti. Významná část přírodních látek vykazuje chiralitu a vyskytují se ve formě enantiomerů, případně diastereoizomerů. Plní nejen funkci základních stavebních jednotek živých organismů, ale jsou i důležitým prekurzorem pro syntézu řady léčiv a v poslední době se staly i populárními výživovými doplňky užívanými zejména sportovci. Velmi důležitými chirálními složkami potravin jsou aminokyseliny s nutričně využitelnými L-enantiomery. Vlivem nevhodného zpracování potraviny může docházet k racemizaci jednotlivých složek. Ke změně poměru enantiomerů dochází také při nesprávném skladování, např. v důsledku bakteriální kontaminace, či přídavkem syntetické příměsi. Např. D-aminokyseliny by neměly být přítomné v nekvašených, nijak nezpracovaných potravinách. Proto mohou sloužit jako významný ukazatel podmínek zpracování a kvality potravin. Z toho vyplývá, že určování enantiomerního zastoupení v potravinách a nápojích má velkou vypovídající hodnotu a je důležitou součástí potravinářské analýzy. 1 Vysokoúčinná kapalinová chromatografije (HPLC) patří mezi vhodné metody používané k enantioseparacím aminokyselim. Absence chromoforů v molekulách některých aminokyselin vede k nízké citlivosti detekce v UV oblasti, proto je nutné aminokyseliny derivatizovat vhodným činidlem a tím zvýšit citlivost detekce použité metody. Tato práce je zaměřena na optimalizaci RP-HPLC metody pro enantioseparaci D,L- -alaninu, D,L-isoleucinu, D,L-leucinu a D,L-valinu v derivatizované formě s důrazem na enantioseparaci D-isomerů za využití chirální stacionární fáze na bázi teikoplaninu. Derivatizace je realizována fluorescenčním derivatizačním činidlem 9- -fluorenylmethylchlormravenčanem (FMOC-Cl) a je sledován vliv různé hodnoty ph hydrogenuhličitanu sodného, který slouží jako rozpouštědlo pro studované aminokyseliny a teploty derivatizace na její výtěžnost. 8
9 2. TEORETICKÁ ČÁST 2.1 Enantiomery Isomery jsou sloučeniny se stejným molekulovým vzorcem, ale různým strukturním vzorcem nebo rozdílným prostorovým uspořádáním. 2 Prostorové uspořádání molekul se nazývá stereoizomerie. Dvě molekuly, které jsou zrcadlovým obrazem jedna druhé, nazýváme enantiomery. Stereoisomery, které nejsou enantiomery, nazýváme diastereoizomery. Diastereoizomery mohou být chirální i achirální. 3 Chiralita je odvozena od řeckého chiros ruka a je zpravidla zapříčiněna přítomností tzv. stereogenního centra, kterým je nejčastěji atom uhlíku se čtyřmi různými substituenty, ale mohou to být i jiné atomy, např. křemík, síra, dusík či fosfor. 2,4 Enantiomery rozlišujeme v názvu sloučeniny afixem (+) nebo (-), vztahujícím se ke směru stáčení roviny polarizovaného světla definované vlnové délky, nejčastěji při čáře sodíku. Enantiomery se strukturně vzájemně liší absolutní konfigurací. Ve spojení s názvem sloučeniny používáme symboliku R a S uváděnou před názvem sloučeniny a známou jako konvence R/S. Pokud molekula obsahuje více než jedno centrum chirality, aplikuje se tento postup na každé centrum chirality a konfigurace molekuly se vyjadřuje souborem R a S afixů. Afixy D a L, vyjadřující absolutní konfiguraci, používáme u cukrů, aminokyselin a peptidů. Každou látku, bez ohledu na její skupenství, obsahující ekvimolární množství enantiomerních molekul, nazýváme racemát. 3 Tato směs je opticky neaktivní, neboť se optické otáčivosti jednotlivých enantiomerů navzájem vyruší. 2 Chiralita je základní vlastnost přírody. Proteiny, enzymy a uhlohydráty jsou chirální. Např. proteiny jsou tvořeny L-aminokyselinami, uhlohydráty jsou tvořeny přírodními cukry s D-isomerií atd. Živé organismy představují chirální prostředí, které je schopno rozlišit jednotlivé enantiomery. Ačkoliv enantiomery vykazují stejné fyzikální vlastnosti, jako je molekulová hmotnost, teplota tání, teplota varu, pka aj. a liší se pouze směrem stáčení roviny polarizovaného světla, mohou mít zcela rozdílné biologické účinky, vzhledem k vysokým stereospecifickým interakcím s receptorovým povrchem. Např. u racemátu thalidomidu, který byl v 60. letech podáván těhotným ženám proti ranní nevolnosti, se prokázalo, že R-enantiomer má sice požadované účinky, ale jeho S- 9
10 -analog je silně teratogenní. Navíc, jestliže je podán pouze R- -thalidomid, dochází k racemizaci in vivo a vzniká opačný enantiomer. Bohužel stále je mnoho chirálních léčiv produkováno jako racemát nejen z důvodů obtížné nebo finančně nákladné enantioseparace, ale také z důvodů, že farmakologické a toxikologické studie byly provedeny pouze pro racemát, nebo z důvodů nestability enantiomerů a jejich opětovné racemizaci. 5,6 2.2 Chirální separace v HPLC Separace enantiomerů je označována jako chirální separace. Od objevu prvních optických isomerů L. Pasteurem, má význam chirality s ohledem na biologickou aktivitou nezanedbatelný význam. Fyziologické prostředí uvnitř živého organismu je chirální a biologická aktivita enantiomerních forem molekul se může dramaticky lišit. S výjimkou glycinu má všech 20 α-aminokyselin chirální atom uhlíku, sousedící s karboxylovou skupinou. Toto chirální centrum umožňuje existenci dvojic enantiomerů. Některé z geneticky zakódovaných aminokyselin tvoří stavební kameny bílkovin, což jsou nejdůležitější složky všech živých systémů. Mnohobuněčné organismy jsou obvykle založeny na L-aminokyselinách. Je dobře známo, že L-formy a D-formy peptidů se mohou výrazně lišit s ohledem na stabilitu a biologickou aktivitou. 7 Příprava enantiomerně čistých substituovaných analogů aminokyselin je náročný úkol, který vyžaduje přesné analytické metody, s nimiž je možno zjistit enantiomerní profil při syntézách. 7 V současné době je hledání nových, efektivních a dostupných chirálních selektorů předmětem mnoha výzkumů. Byly vyvinuty různé separační metody, včetně plynové chromatografie, kapilární elektroforézy, micelární elektrokinetické chromatografie, superkritické fluidní chromatografie a vyskoúčinné kapalinové chromatografie, které mohou být použity jako separační techniky pro analýzu chirálních látek. 8 Chirální HPLC separaci lze uskutečnit dvěma způsoby, a to buď přímým, či nepřímým způsobem. Přímá metoda spočívá v zavedení vhodné opticky aktivní látky, tzv. chirálního selektoru do separačního prostředí. Při interakci chirálního sekektoru s enantiomery vznikají přechodné diastereoizomerní komplexy o různých konstantách stability. Pokud jsou tyto konstanty dostatečně odlišné, může docházet k rozdílnému 10
11 zadržování jednoho z dvojice enantiomerů na koloně a tím i k jejich vzájemnému rozdělení. Chirální selektor může být chemicky vázaný na pevném inertním nosiči, se kterým tvoří tzv. chirální stacionární fázi, nebo může být přidaný jako aditivum do mobilní fáze. Obě zmíněné metody mají své výhody i nevýhody. Např. k výhodám přídavku chirálního selektoru do mobilní fáze patří možnost širokého výběru chirálního selektoru a jeho snadná výměna a možnost využití nechirální stacionární fáze, která je oproti chirální stacionární fázi levnější. Nevýhodou je velká spotřeba drahého chirálního selektoru a v některých případech i snížení citlivosti detekce. 8,9 V metodě nepřímé se používá nechirální stacionární fáze a vlastní separaci předchází derivatizační reakce mezi racemickým analytem a opticky čistým činidlem. Nevýhodou nepřímé metody je, že vzniká stabilní diastereoizomerní pár a tento způsob je nevýhodný např. pro izolaci jednotlivých enantiomerů Makrocyklická antibiotika Hledání účinných chirálních selektorů, které jsou schopny separovat širokou škálu enantiomernách sloučenin, je stále otevřený proces. Makrocyklická antibiotika se ukázala jako mimořádně užitečná třída chirálních selektorů, používaných pro biologické a farmakologické enantioseparace v HPLC, tenkovrstvé chromatografii a elektroforéze. K nejvýznamnější skupině makrocyklických antibiotik patři glykopeptidy. Do skupiny glykopeptidů patří avoparcin, teikoplanin, ristocetin A a vankomycin, které jsou v HPLC nejčastěji využívány ve formě chirálních stacionárních fází, tedy chirální selektor navázaný na nosiči. S úspěchem byly využity i pro enantioseparaci nativních a derivatizovaných forem aminokyselin. 11 Makrocyklická antibiotika mají molekulovou hmotnost větší než 600, ale menší než 2000 a mají mnoho funkčních skupin a podle prostředí mohou vykazovat kyselý, bazický, nebo neutrální charakter. Interakční mechanismus zahrnuje hydrofobní, dipól- -dipól nebo π-π interakce, vodíkové vazby a sterické repulze. Kromě hydrofobních částí mají tyto molekuly i hydrofilní a ionizovatelné skupiny, což jim zaručuje dobrou rozpustnost ve vodných roztocích. Jsou aktivní proti anaerobním i aerobním grampozitivním patogenním bakteriím. Svou specifickou vazbou na karboxylový konec D-alanyl-D-alaninu, přítomného v bakteriální buněčné stěně, zamezují polymerizaci 11
12 peptidoglykanu a tím vyvolávají inhibici syntézy buněčné stěny bakterií. 11,12,13 Jelikož v této práci byla používána chirální stacionární fáze s navázaným teikoplaninem, bude následující odstavec zaměřen na něj. Teikoplanin, jehož struktura je znázorněna na obr. 1, je fermentačním produktem bakterie Actinoplanes teichomyceticus. V molekule teikoplaninu je sedm aromatických jader, čtyři z nich jsou fenolické zbytky a další dva kruhy jsou substituované chlorem. 11 Teikoplanin je jediný mezi glykopeptidy, který má hydrofobní acylový postranní řetězec spojený s 2-amino-2-deoxy-β-glukopyranosylovou skupinou. Tento hydrofobní acylový postranní řetězec je zodpovědný za agregační schopnosti teikoplaninu. 12 Obr. 1 Strukturní vzorec teikoplaninu
13 2.4 Aminokyseliny Fyziologické prostředí uvnitř živého organismu je chirální a biologické aktivity enantiomerních forem molekul se mohou dramaticky lišit. Jak již bylo uvedeno, s výjimkou glycinu, mají všechny α-aminokyseliny chirální atom uhlíku sousedící s karboxylovou a aminovou skupinou. Toto chirální centrum umožňuje existenci dvojice enantiomerů. 7 Vedle základních funkčních skupin (karboxylové a aminové) má každá aminokyselina charakteristický postranní alifatický nebo aromatický zbytek, jímž se jednotlivé aminokyseliny liší a který rozhoduje o interakcích a funkcích peptidů a proteinů z nich složených. Některé geneticky zakódované aminokyseliny tvoří stavební kameny bílkovin. Mnohobuněčné organismy jsou obvykle založeny na L-aminokyselinách. 7 Příčinou této homochirality může být skutečnost, že L-aminokyseliny jsou stabilnější, než D-formy. 1 Racemizace opticky aktivních aminokyselin v metabolicky stabilních bílkovinách živých systémů se může uskutečnit jak ve zředěných kyselinách a bázích, tak i při neutrálním ph. Příprava enantiomerně čistých substituovaných analogů aminokyselin je náročný úkol, který vyžaduje přesné analytické metody, s nimiž je možno zjistit případné nedostatky asymetrických syntéz. Je dobře známo, že L- a D-formy peptidů se mohou výrazně lišit s ohledem na stabilitu a biologickou aktivitou. 7 L-enantiomery aminokyselin a hlavně aminokyselin s rozvětveným postraním hydrofobním řetězcem jsou součástí mnoha potravinových doplňků. Např. L-valin, L- -leucin a L-isoleucin jsou hojně užívané lidmi s nadměrnou fyzickou zátěží (např. sportovci). 1 Tyto aminokyseliny bývají označovány jako BCAA (z anglického brached chain amino acids kyseliny s rozvětveným řetězcem) a patří do skupiny esenciálních aminokyselin. Jsou katabolyzovány hlavně ve svalech, oxidace je provázena uvolňováním energie, při syntéze jiných aminokyselin slouží jako dárci dusíku, regulují syntézu a degradaci bílkovin. 16 Také pomáhají snižovat únavu v důsledku zvyšování hladiny serotoninu. Proto je nesmírně důležité kontrolovat enantiomerní čistotu těchto výrobků, aby nedocházelo k výživovým ztrátám z důvodu vzniku nemetabolisovatelných a biologicky nevyužitelných D-forem těchto aminokyselin. 1 Na obr. 2 jsou uvedeny strukturní vzorce L-enantiomerů studovaných aminokyselin. 13
14 Obr. 2 Strukturní vzorce a názvy studovaných aminokyselin. 2.5 Derivatizace Derivatizační techniky jsou používané v hmotnostní spektroskopii, jaderné magnetické rezonanci, UV-VIS a fluorescenční spektroskopii roztoků, v elektrochemických a radiochemických metodách, v separačních metodách atd. 17 Derivatizací se mění fyzikálně-chemické vlastnosti analytů. Hlavní důvody pro převedení analytů na deriváty jsou zlepšení detekovatelnosti, zlepšení chromatografických vlastností (např. změna polarity), zlepšení stability analytů, umožnění chirální separace, změna matrice pro lepší separaci. V HPLC je hlavním důvodem pro derivatizace zvýšení citlivosti detekce. Do molekuly analytu se zavádí 18, 19 chromofor (pro UV detekci) nebo fluorofor (pro fluorescenční detekci). Derivatizační reakce můžeme dělit podle různých kritérií: v závislosti na experimentálním uspořádání je dělíme na derivatizace před kolonou a za kolonou. V závislosti na použité technice máme derivatizace pro kapalinovou a plynovou chromatografii, případně dělení podle typu reaktivní skupiny derivatizačního činidla. Mezi funkční skupiny analytů, na kterých probíhá nejčastěji derivatizace, patří aminoskupiny a karboxylové či hydroxylové skupiny. 19 Hlavní nevýhodou derivatizace je zavedení operace navíc, která zvyšuje komplexnost analýzy, její chybu i celkovou dobu trvání. Proto je důležitá automatizace 14
15 derivatizačního kroku minimalizující tyto nevýhody. Derivatizační reakce by měla být rychlá, kvantitativní a s minimem vedlejších produktů. 18,19 Protože aminokyseliny nemají ve své struktuře konjugované dvojné vazby, je jejich UV detekce i při nízkých vlnových délkách obtížná a málo citlivá. Vzhledem k tomu, že aminokyseliny jsou snadno derivatizovatelné pomocí mnoha derivatizačních činidel za vzniku produktů absorbujících v UV oblasti či poskytující fluorescenci, jsou předkolonové derivatizační techniky často používanými metodami při stanovení aminokyselin. Mezi používaná derivatizační činidla patří např. o-ftalaldehyd (OPA), 9-fluorenylmethylchlormravenčan (FMOC-Cl), OPA/FMOC-Cl nebo 2,4- -dinitrofluorobenzen (DNFB). 20 Literatura uvádí desítky dalších derivatizačních činidel, s ohledem na zaměření této bakalářské práce bude dále uvedeno pouze používané derivatizační činidlo FMOC-Cl (obr. 3). Činidlo 9-fluorenylmethylchlormravenčan (FMOC-Cl) reaguje s primárními a sekundárními aminy za vzniku velmi stabilních derivátů vykazujících fluorescenci. Je používán pro derivatizaci a analýzu různých typů aminů, včetně biogenních aminů a polyaminů, alifatických aminů s krátkým řetězcem či neurotransmiterů. Díky zavedení chromoforů do struktury studovaných látek dochází ke zvýšení citlivosti detekce FMOC-derivátů oproti původním nederivatizovaným látkám o více než 3 řády. I tato derivatizace má své nevýhody. Jednou z nich je, že mnoho endogenních komponent v biologických matricích je reaktivních vůči derivatizačnímu činidlu. Proto je často nezbytné vzorek před analýzou přečistit. Další nevýhodou je přítomnost 9- -fluorenylmethoxykarboxylové kyseliny (FMOC-OH) v produktech derivatizace, vznikající hydrolýzou nezreagovaného FMOC-Cl. 21 Obr. 3 Schéma reakce FMOC-Cl s aminokyselinou. 15
16 2.6 Vysokoúčinná kapalinová chromatografie Vysokoúčinná kapalinová chromatografie je jednou z nejpoužívanějších separačních technik v analytické chemii, jelikož umožňuje analyzovat i velmi složité směsi látek o nízkých koncentracích. 22 Separace sloučenin na základě rozdílného rozdělení mezi dvě navzájem nemísitelné kapalné fáze je základem rozdělovací chromatografie. Separační systém se skládá z chemicky vázané stacionární fáze a nemísitelné mobilní fáze. Chromatografické separace jsou založeny na rozdílném rovnovážném rozdělení vzorku mezi tyto dvě fáze. Pro detekci je nejčastěji využíván UV/VIS spektrofotometrický detektor, který v některých případech poskytuje malou citlivost detekce. K podstatně citlivějším patří fluorimetrická detekce nebo hmotnostní, popřípadě tandemová hmotnostní detekce. 17 K základním retenčním charakteristikám sloužícím k popisu průběhu separace patří retenční faktor, rozlišení, separační faktor, výškový ekvivalent teoretického patra, mez stanovitelnosti a mez detekce. Retenční faktor k vyjadřuje míru zadržení a tedy zpožďování analytu v koloně. Je dán vztahem: k ( t t ) / t, (1) R kde t je retenční (tedy celkový) čas, který analyt stráví v separační koloně a R t je M mrtvý čas kolony, tedy celkový čas složky vzorku, která není na koloně zadržována a pohybuje se stejnou rychlostí, jako mobilní fáze. R Rozlišení R udává míru vzájemného překrývání dvou sousedních píků. Pokud je 1, 2 1,2 1,5, jsou píky rozděleny až na základní linii. Rozlišení je dáno vztahem: R M 1,2 2 R2 R1 1 w2 M ( t t ) /( w ), (2) kde t a R1 t jsou retenční časy dříve a později eluujícího analytu a R2 w a 1 w jsou 2 příslušné šířky píků při základně. Pro porovnání kolon různých délek slouží výškový ekvivalent teoretického patra H, který udává separační účinnost kolony: H L / n, (3) kde L udává délku kolony a n počet teoretických pater, který získáme výpočtem ze vztahu n 5,545 ( t / w, (4) R 2 1 / 2 ) 16
17 kde w značí šířku píku v polovině jeho výšky. 1/ 2 Mez stanovitelnosti LOQ a mez detekce LOD udávají hodnotu koncentrace, kterou jsme za daných experimentálních podmínek schopni s určitou spolehlivostí stanovit, respektive detekovat. Jdou dány vztahy: LOQ 10 hn / m (5) LOD 3 h / n m, (6) h vyjadřuje šum základní linie a m směrnici kalibrační křivky. n Kritériem pro separační schopnosti chromatografického systému je selektivita, která je pro látky 1 a 2 definovaná podle vztahu:, (7) 1 / 2 k2 / k1 kde k 1 a k 2 jsou retenční faktory dříve a později eluujícího analytu. Systém je tím selektivnější, čím je hodnota 1/ 2 vyšší. Pokud je 1/ 2 1, analyty se vzájemně neseparují. 17,18,22 17
18 3. EXPERIMENTÁLNÍ ČÁST 3.1 Chemikálie acetonitril R CHROMASOLV pro HPLC (Sigma-Aldrich, St. Louis, MO, USA) triethylamin, čistota 99% (Sigma-Aldrich, St. Louis, MO, USA) methanol CHROMASOLV pro HPLC (Sigma-Aldrich, St. Louis, MO, USA) hydrogenuhličitan sodný, NaHCO 3, čistota p.a. (Lach-Ner, Neratovice, ČR) hydroxid sodný, čistota p.a. (Lach-Ner, Neratovice, ČR) octová kyselina 99,8%, čistota p.a. (Lach-Ner, Neratovice, ČR) deionizovaná voda filtrovaná Milli-Q filtrovacím systémem (Millipore, Miliford, MA, USA) BCAA Extreme Pure (Aminostar s.r.o., Loukov u Mnichova Hradiště, ČR) 9-fluorenylmethylchloromravenčan (FMOC-Cl), čistota 99% (Sigma-Aldrich, St. Louis, MO, USA) standardy: o D/L-alanin (D/L-Ala), čistota 99%, o D/L-leucin (D/L-Leu), čistota 99% o D-isoleucin (D-Ile), čistota 99%; L-isoleucin (L-Ile), čistota 99% o D/L-valin (D/L-Val), čistota 99% o FMOC-D-alanin (FMOC-D-Ala-OH), čistota 99%, FMOC-L-alanin (FMOC-L- -Ala-OH), čistota 99% o FMOC-D-leucin (FMOC-D-Leu-OH), čistota 99%, FMOC-L-leucin (FMOC- -L-Leu-OH), čistota 99% o FMOC-D-valin (FMOC-D-Val-OH), čistota 99%, FMOC-L-valin (FMOC-L- -Val-OH), čistota 99% Veškeré standardy byly zakoupeny od firmy Sigma-Aldrich (Sigma-Aldrich, St. Louis, MO, USA). 18
19 3.2 Přístroje a pomůcky kapalinový chromatograf, jehož součástí byla vysokotlaká gradientová pumpa model Crystal 200, membránový vakuový odplyňovač CSI6150 (Cambridge Scientific Instruments, UK), UV/VIS detektor typu UV PU 4020 (Pye Unicam, Cambridge, UK), fluorescenční detektor FL 2000 (Spectra System, USA), dávkovací ventil Rheodyne (Cotati, CA, USA) se smyčkou o objemu 5 μl a ke sběru dat program Clarity verze (DataApex, Praha, ČR) kovová separační kolona Chirobiotic T (ASTEC Advanced Separation Technologies, Whipanny, NJ, USA) o rozměrech 250 mm x 4,6 mm I. D. naplněná teikoplaninem vázaným na silikagelový nosič o velikosti zrnění 5 μm analytické váhy APX-100 (Denver Instrument, USA) skleněná stříkačka Hamilton (Reno, Nevada, USA) o objemu 10 μl ph-metr model 4330 (Jenway, UK) ultrazvuk Ultrasonic LC30H (Elma, Německo) mikrocentrifuga (Denver Instrument, USA) bloková lázeň Grant model QBD2 (Cambridge Instruments, UK), program Origin 7.0 (OriginLab Corporation, USA) nylonový membránový filtr 0,45 μm (Whatman International Ltd, Maidstone, UK) 3.3 Mobilní fáze a podmínky měření Mobilní fáze pro separaci nativních aminokyselin byla složena z MeOH a deionizované vody v různých objemových poměrech. Pro chirální separaci derivatizovaných FMOC-aminokyselin byla použita mobilní fáze složená z MeOH v kombinaci s 0,5% vodným roztokem triethylamoniumoctanového pufru (TEAA) o ph 6,0 v poměru MeOH/TEAA pufr 40/60 (v/v). Příprava 0,5% TEAA pufru byla provedena odměřením 5 ml triethylaminu a přidáním tohoto množství do cca 800 ml deionizované vody. Přídavkem ledové kyseliny octové bylo upraveno ph na hodnotu 6,0. Vzniklý roztok byl doplněn na celkový objem 1 litr. UV detekce nativních aminokyselin byla měřena při 205 nm. 19
20 Fluorescenční detekce derivatizovaných analytů byla měřena při 254 nm pro excitaci a 314 nm pro emisi záření. Průtoková rychlost mobilní fáze byla pro nativní formy aminokyselin 0,5 ml/min, pro derivatizované aminokyseliny 0,7 ml/min. Separace probíhaly během celého experimentu za laboratorní teploty 22 ± 2 C. 3.4 Příprava vzorků a činidel Studované aminokyseliny alanin, leucin a valin byly dostupné ve formě racemátů, pro analýzu D/L-isoleucinu byly smíchány jeho D- a L-enantiomery v poměru 1:1. Pro analýzu derivatizovaných standardů FMOC-D/L-Ala, FMOC-D/L-Leu a FMOC- -D/L-Val byly smíchány jejich FMOC-D- a FMOC-L-enantiomery v poměru 1:1. Standard FMOC-D/L-Ile nebyl k dispozici. Standardní zásobní roztoky pro separaci nederivatizovaných aminokyselin byly připraveny navážením 1 mg vzorku (racemátu) a jeho rozpuštěním v 1 ml solventu tvořeného směsí MeOH/H 2 O v objemovém poměru 50/50 (v/v). Pro separaci derivatizovaných aminokyselin byly zásobní roztoky připraveny navážením 1 mg racemátu aminokyseliny a rozpuštěním v 1 ml 0,2 M NaHCO 3 o různém ph. Pro zkrácení doby rozpouštění byly vzorky ponechány po dobu 5 minut v ultrazvuku. Zásobní roztoky byly dále ředěny pomocí 0,2 M NaHCO 3 na požadované koncentrace. Zásobní roztok NaHCO 3 o koncentraci 0,2 M byl připraven rozpuštěním 4,20 g v přibližně 200 ml deionizované vody. Pomocí 1 M NaOH byla nastavena požadovaná hodnota ph a poté byl roztok doplněn na konečný objem 250 ml. Zásobní roztok 1 M NaOH byl připraven rozpuštěním 4,0 g vzorku ve 100 ml deionizované vody. Pro přípravu zásobního roztoku derivatizačního činidla byl 1 mg FMOC-Cl rozpuštěn v 1 ml acetonitrilu. Dalším ředěním pomocí acetonitrilu bylo dosaženo požadované koncentrace. Derivatizace aminokyselin byla provedena pomocí derivatizačního činidla FMOC- -Cl. Bylo smícháno 500 μl racemátu aminokyseliny o koncentraci 2 μg/ml s 500 μl FMOC-Cl o koncentraci 20 μg/ml. Směs byla intenzivně protřepávána po dobu 20
21 2 minut, centrifugována při 500 ot/min po dobu pěti minut a pro analýzu byla použita vrchní část vzorku. Zásobní roztoky byly skladovány v temnu při teplotě 5 C. Před analýzou byly ponechány 30 minut stát při laboratorní teplotě pro jejich temperaci. 21
22 4. VÝSLEDKY A DISKUSE 4.1 Porovnání separace aminokyselin v nativním stavu a derivatizované formě Tato bakalářská práce navazuje na výsledky diplomové práce Mgr. Pavla Repka, který vyvíjel a následně optimalizoval enantiomerní HPLC metodu s UV a fluorimetrickou detekcí pro chirální separaci racemických směsí alaninu, valinu, leucinu a isoleucinu v nativních a derivatizovaných formách s použitím různých stacionárních fází na bázi teikoplaninu a teikoplanin aglykonu v různých mobilních fázích. Z hlediska derivatizace byl sledován vliv objemového poměru D/L- -aminokyselina/derivatizační činidlo na výtěžnost derivatizační reakce. Závěrem práce byla volba objemového poměru 1/1 D/L-aminokyselina/derivatizační činidlo s desetinásobně vyšší koncentrací derivatizačního činidla pro derivatizaci racemátů aminokyselin. Separace nativních i derivatizovaných enantiomerů aminokyselin byla nejúčinnější na koloně Chrobiotic T. 23 Na začátku této práce byla otestována chirální kolona Chirobiotic T pro separaci nativních i FMOC-derivatizovaných aminokyselin za podmínek nalezených v práci P. Repka. 23 Pro porovnání průběhu enantioseparace D/L-aminokyselin v nativní a derivatizované formě bylo provedeno porovnávací měření s D/L-alaninem. Výsledky separace nativní a derivatizované aminokyseliny jsou uvedeny na obr. 4 a 5. Na základě již publikovaných výsledků byla pro analýzu nativní formy D/L-alaninu zvolena mobilní fáze MeOH/H 2 O s obsahem organického modifikátoru 50, 60 a 70 objemových procent. Průtok mobilní fáze byl nastaven na 0,5 ml/min. Pro měření byla zvolena UV detekce při 205 nm. Ze získaných chromatografických dat vyplývá, že s rostoucím objemovým zastoupením organického modifikátoru v mobilní fázi docházelo k nárůstu retenčního času, a tím prodloužení doby analýzy. Toto chování odpovídá tzv. HILIC (hydrofilní interakční chromatografie) módu a v tomto typu separačního systému se především uplatňují dipólové interakce a vodíková vazba. Nárůst retenčních charakteristik při zvyšování objemového zastoupení MeOH v mobilní fázi dokumentuje obr
23 Obr. 4 Enantioseparace nativního D/L-Ala v mobilních fázích MeOH/H 2 O A) 70/30 (v/v) B) 60/40 (v/v) C) 50/50 (v/v), D/L Ala o koncentraci 1 mg/ml v MeOH/H 2 O 50/50 (v/v), kolona Chirobiotic T, UV detekce při 205 nm, průtoková rychlost 0,5 ml/min, označení: 1: L-Ala, 2: D-Ala. Enantiomery FMOC-D/L-Ala byly separovány v mobilní fázi MeOH/0,5% TEAA pufr, ph 6,0 40/60 (v/v), která byla v práci P. Repka nalezena jako optimální. Derivatizace D/L-Ala probíhala v objemovém poměru racemát/derivatizační činidlo 1:1 s desetinásobně vyšší koncentrací derivatizačního činidla při laboratorní teplotě 22 ± 2 C a D/L-Ala byl rozpuštěn v 0,2 M NaHCO 3 o ph = 9,0. Příslušný chromatogram je uveden na obr
24 Obr. 5 Průběh separace FMOC-D/L-Ala, koncentrace D/L-Ala 1 μg/ml v 0,2 M NaHCO 3 o ph = 9,0, kolona Chirobiotic T, fluorescenční detekce při vlnové délce excitace 254 nm a vlnové délce emise 314 nm, průtoková rychlost 0,7 ml/min, mobilní : D-Ala, fáze MeOH/0,5% TEAA pufr, ph 6,0 40/60 (v/v), označení: 1: L-Ala, 2: derivatizační činidlo. Při porovnání obr. 4 s obr. 5 je patrné, že derivatizace aminokyseliny umožnila dobře detekovat i koncentrace o několik řádů nižší, než byla původní koncentrace nederivatizované aminokyseliny. Tento nárůst detekce dokládají i LOQ a LOD pro derivatizované aminokyseliny, jejichž limity se pohybují řádově v jednotkách ng/ml Derivatizace Hlavní náplní této práce bylo blíže prozkoumat podmínky deprivatizace s cílem dosáhnout co nejlepšího výtěžku derivatizace. Jak již bylo uvedeno výše, práce navazuje na výsledky P. Repka, ve kterých bylo zjištěno že za použití derivatizačního 24
25 činidla 9-fluorenylmethylchloromravenčanu (FMOC-Cl) je výhodné při derivatizaci studovaných aminokyselin postupovat tak, že aminokyseliny by měly být rozpouštěny v 0,2 M NaHCO 3 (testované ph bylo 9), objemový poměr D/L-aminokyselina/FMOC- -Cl by měl být 1:1, kdy koncentrace derivatizačního činidla je oproti koncentraci aminokyseliny desetkrát vyšší. 23 Takto připravená směs byla intenzivně protřepávána po dobu 2 minut. Protože filtrace směsi na odstranění případných nečistot, které by mohly narušit reprodukovatelnost separace, se projevila jako nevhodná, vzhledem k ulpívání podstatné části vzorku na filtračním médiu, bylo vhodné použít centrifugaci při 500 ot/min po dobu pěti minut a poté svrchní část vzorku odebrat k analýze. Analýza derivatizovaných aminokyselin probíhala v mobilní fázi MeOH/0,5% TEAA pufr 40/60 (v/v) při průtoku mobilní fáze 0,7 ml/min. Protože deriváty vykazují fluorescenci, mohla být k analýze derivatizovaných aminokyselin použita fluorescenční detekce při 254 nm pro excitaci a 314 nm pro emisi záření. 23 Pro zvolené aminokyseliny D/L-alanin, D/L-isoleucin, D/L-leucin a D/L-valin bylo v této práci hledáno vhodné ph roztoku NaHCO 3, ve kterém byly standardy aminokyselin rozpouštěny a vhodná teplota derivatizace aminokyselin pro optimalizaci derivatizačního postupu. 4.3 Porovnání standardů derivatizovaných aminokyselin s derivatizovanými aminokyselinami Pro porovnání výtěžnosti derivatizace FMOC-Cl derivatizačním činidlem byly zakoupeny standardy FMOC-D/L-Ala, FMOC-D/L-Leu a FMOC-D/L-Val. Ty byly nejprve rozpouštěny v ACN, zředěny na požadovanou koncentraci (1 μg/ml racemátu nativní aminokyseliny) a byly separovány za stejných podmínek jako laboratorně připravené FMOC-D/L-aminokyseliny a byly sledovány plochy píku D-enantiomerů. Acetonitril se však projevil jako nevhodné rozpouštědlo, vzhledem k velkému množství vznikajících vedlejších produktů při derivatizaci, které následně rušily enantioseparaci. Proto byl pro rozpouštění standardů FMOC-D/L-aminokyselin acetonitril nahrazen 0,2 M NaHCO 3 o ph 9. Analýza standardů derivatizovaných aminokyselin probíhala v mobilní fázi MeOH/0,5% TEAA pufr 40/60 (v/v) při průtoku mobilní fáze 0,7 ml/min. Byla použita 25
26 fluorescenční detekce při 254 nm pro excitaci a 314 nm pro emisi záření. Při stejných podmínkách proběhla i analýza derivatizovaných aminokyselin. V tab. 1 jsou porovnány plochy píků standardů FMOC-D-aminokyselin s derivatizovanými FMOC- -D-aminokyselinami. Z tabulky 1 je patrné, že plochy odpovídající standardům jsou vyšší než plochy laboratorně derivatizovaných aminokyselin, takže výtěžnost derivatizace byla menší než 100 %. Tabulka 1. Porovnání hodnot ploch píků (A) FMOC-D-enantiomerů aminokyselin pro zakoupené FMOC-derivatizované standardy a zderivatizované FMOC-D/L- -aminokyseliny. Experimentální podmínky: kolona Chirobiotic T, mobilní fáze MeOH/0,5% TEAA pufr 40/60 (v/v), průtoková rychlost 0,7 ml/min, fluorescenční detekce při vlnové délce excitace 254 nm a vlnové délce emise 314 nm, teplota = 22 C, ph = 9,0, koncentrace racemátů aminokyselin 1μg/ml, n = 3. FMOC-D-aminokyselina Ala Leu Val A A A mv. s mv. s mv. s Standard Deriv. vzorek Optimalizace průběhu derivatizace použitím hydrogenuhličitanu sodného o různé hodnotě ph Jak už bylo uvedeno výše, standardy aminokyselin byly rozpouštěny v 0,2 M roztoku NaHCO 3 a tímto roztokem byly i dále ředěny. Cílem této práce bylo najít vhodnou hodnotu ph roztoku NaHCO 3, při které bude následná derivatizace vzorku probíhat s co nejvyšší účinností. Byly sledovány hodnoty ph roztoku NaHCO 3 v rozmezí 8,0 9,5 po velikosti kroku 0,5. Hodnoty ph nižší než 8,0 nebyly používány z důvodu špatné rozpustnosti standardů nativních aminokyselin. Vzhledem k pracovní oblasti kolony nebyly používány ani hodnoty ph vyšší než 9,5. 26
27 Při jednotlivých hodnotách ph byl sledován vliv hodnoty ph na výtěžnost derivatizace FMOC-derivatizovaných racemátů aminokyselin. Naměřené hodnoty jsou uvedeny v tab. 2. Ze získaných údajů je patrné, že výtěžnost derivatizace, která byla pro jednotlivé aminokyseliny vyjádřena pomocí ploch píků D-enantiomerů, se změnou ph z 8,0 na 8,5 vzrůstá a s dalším zvyšováním ph opět klesá. Proto bylo ph 8,5 zvoleno jako nejvhodnější a bylo použito pro další měření. V racemické směsi FMOC-D/L-Ala, FMOC-D/L-Leu a FMOC-D/L-Val dochází k separaci D-enantiomerů na základní linii při všech testovaných hodnotách ph NaHCO 3 s výjimkou ph 9,5, kdy dochází ke koeluci FMOC-D- -Val s derivatizačním činidlem. Průběh enantioseparace směsi FMOC-D/L-Ala, FMOC- -D/L-Leu a FMOC-D/L-Val je zachycen na obr. 6. FMOC-D/L-isoleucin nebyl na přípravu směsi použit, protože při zvolených podmínkách separace nedocházelo k rozdělení FMOC-D-isoleucinu a FMOC-D-alaninu až na základní linii. Ze získaných výsledků je patrné, že při použití NaHCO 3 o ph 8,5 bylo dosahováno nejvyšších výtěžků derivatizace pro všechny D-enantiomery, naopak při ph 9,5 bylo dosaženo nejnižší výtěžnosti. Tabulka 2. Vliv ph 0,2 M roztoku NaHCO 3 používaného k rozpouštění a následnému ředění standardů nativních aminokyselin v derivatizační reakci na hodnoty plochy píků (A) D-enantiomerů aminokyselin. Experimentální podmínky: kolona Chirobiotic T, mobilní fáze MeOH/0,5% TEAA pufr 40/60 (v/v), průtoková rychlost 0,7 ml/min, fluorescenční detekce při vlnové délce exitace 254 nm a vlnové délce emise 314 nm, teplota = 22 C, koncentrace racemátů aminokyselin 1μg/ml, n = 3. FMOC-D/L-aminokyselina Ala Ile Leu Val A A A A ph mv. s mv. s mv. s mv. s 8, , , ,
28 Obr. 6: Enantioseparace racemické směsi FMOC-D/L-Ala, FMOC-D/L-Leu a FMOC- -D/L-Val, koncentrace jednotlivých racemátů 1 μg/ml ve směsi v 0,2 M NaHCO 3 o ph = 8,5, kolona Chirobiotic T, fluorescenční detekce při vlnové délce exitace 254 nm a vlnové délce emise 314 nm, průtoková rychlost 0,7 ml/min, mobilní fáze MeOH/0,5% TEAA pufr, ph 6,0 40/60 (v/v), označení: 1: FMOC-L-Ala, FMOC-L-Leu, FMOC-L- -Val, 2: FMOC-D-Val, 3: FMOC-D-Ala, 4: FMOC-D-Leu, : derivatizační činidlo. 4.5 Vliv teploty na průběh derivatizace Pro posouzení, zda má teplota při derivatizaci vliv na výtěžnost derivatizace, bylo postupováno následovně: Standardní roztoky byly postupně zahřívány v blokové lázni na teploty 22, 40 a 60 C a při těchto teplotách probíhala derivatizace. Aby nedocházelo k úniku nebo naopak k dodávání tepla do studovaného systému během derivatizace, bylo třeba zkumavky se vzorky izolovat od vnějšího prostředí. K tomu posloužil 28
29 polystyrénový kvádr o rozměrech 5 x 5 x 5 cm, který byl rozříznut na dvě nestejně velké části. Uvnitř vetší poloviny bylo vytvořeno místo na mikrozkumavku, menší polovina posloužila jako vrchní víko. V takto připraveném boxu byly vzorky po celou dobu derivatizace, poté byly ponechány při laboratorní teplotě 20 minut temperovat. Nakonec byla provedena centrifugace pro případné odstranění nečistot a vrchní část vzorku byla použita při analýze. Vliv teploty reakční směsi na účinnost derivatizace je uveden v tab. 3. Ze získaných údajů je patrné, že derivatizace neprobíhala výrazně ve prospěch konkrétní teploty, ale ani se naměřené hodnoty pro jednotlivé teploty od sebe výrazně nelišily. Pro další měření byla jako kompromis zvolena teplota 40 C. Tabulka 3. Vliv teploty roztoků D/L-aminokyselin a FMOC-derivatizačního činidla v derivatizační reakci na hodnoty plochy píků (A) D-enantiomerů aminokyselin. Experimentální podmínky: kolona Chirobiotic T, mobilní fáze MeOH/0,5% TEAA pufr 40/60 (v/v), průtoková rychlost 0,7 ml/min, fluorescenční detekce při vlnové délce exitace 254 nm a vlnové délce emise 314 nm, 0,2 M NaHCO 3 o ph = 8,5, D/L- -aminokyselina o koncentraci 1 μg/ml, n = 3. FMOC-D/L-aminokyselina Ala Ile Leu Val T A A A A C mv. s mv. s mv. s mv. s Analýza reálného vzorku Jako reálný vzorek byl použit přípravek BCAA Extreme Pure od společnosti Aminostar s.r.o., jehož složení je uvedeno v tab. 4. Tento přípravek je určen pro aktivní sportovce a jeho úkolem je zvýšení svalové syntézy proteinů, snížení katabolických procesů ve svalech a tím ochrana svalové hmoty
30 Tabulka 4. Složení přípravku BCAA Exteme Pure od společnosti Aminostar: L-leucin, L-isoleucin, L-valin, želatinová kapsle (želatina, barviva: oxid titaničitý, oxidy a hydroxidy železa), látky protispékavé: stearát hořečnatý a oxid křemičitý. 24 Aminokyselina mg/1 kapsle g/100 g L-Leu ,2 L-Ile L-Val Optimalizovaná metoda derivatizace a enantioselektivní HPLC byla použita pro zjištění, zda výše uvedený přípravek skutečně neobsahuje i D-analogy zmíněných aminokyselin. Vzorek ve formě kapslí byl zbaven vnějšího želatinového obalu a vnitřní sypký obsah byl za stálého míchání a následné sonifikace rozpuštěn ve 100 ml 0,2 M roztoku NaHCO 3 o ph 8,5. Protože kapsle neobsahovala jen samotné aminokyseliny, ale i další pomocné látky, zejména pak oxidy, vznikl bíle zakalený roztok, který bylo potřeba před další úpravou zfiltrovat. Roztok byl přefiltrován přes nylonový membránový filtr s velikostí pórů 0,45 μm. Z roztoku bylo odebráno 120 μl, ke kterým byl přidán 0,2 M NaHCO 3 na doplnění do objemu 1 ml. Takto vzniklý roztok byl dále ředěn až na konečnou koncentraci 2 μg/ml L-Ile a L-Val. V blokové lázni byl roztok zahřát na 40 C a derivatizován pomocí FMOC-Cl, též zahřátým na 40 C. Derivatizovaný vzorek byl centrifugován a vrchní část byla použita k analýze, jejíž výsledek je uveden na obr. 7, ze kterého je zřejmé, že chromatogram neobsahoval žádný pík příslušející D- -enantiomerům. 30
31 Obr. 7 Enantioseparace směsi FMOC-L-Ile, FMOC-L-Leu, FMOC-L-Val o koncentracích 1 μg/ml pro L-Ile, L-Val a koncentraci 4 μg/ml pro L-Leu. Experimentální podmínky: kolona Chirobiotic T, fluorescenční detekce při vlnové délce exitace 254 nm a vlnové délce emise 314 nm, průtoková rychlost 0,7 ml/min, mobilní fáze MeOH/0,5% TEAA pufr, ph 6,0 40/60 (v/v), ph NaHCO 3 8,5, teplota derivatizace 40 C, označení: 1: L-Ile, Leu, Val, 2: D-Ile, : derivatizační činidlo. 31
32 5. ZÁVĚR Cílem této bakalářské práce byla aplikace již vyvinuté enantioselektivní HPLC metody pro sledování enantioseparace aminokyselin alaninu, isoleucinu, leucinu a valinu s důrazem na D-formy v derivatizované podobě, realizované fluorescenčním derivatizačním činidlem 9-fluorenylmethylchlormravenčanem (FMOC-Cl) za využití chirální stacionární fáze na bázi teikoplaninu. Byl studován vliv hodnot ph 0,2 M NaHCO 3, používaného při rozpouštění studovaných racemátů aminokyselin i reálného vzorku, a vliv teploty roztoků studovaných látek a derivatizačního činidla na výtěžnost derivatizace, která byla sledována velikostí plochy píku D-enantiomeru jednotlivých aminokyselin. Na koloně Chirobiotic byly nejprve provedeny separace FMOC-derivatizovaných aminokyselin, kdy bylo k rozpuštění a následnému ředění standardů aminokyselin použito 0,2 M vodného roztoku NaHCO 3 při ph v rozmezí 8,0 9,5. Nejvyšší výtěžnosti derivatizace vyjádřené plochou píků příslušející D-enantiomerům, bylo dosaženo při ph 8,5. Pro optimalizaci metody při různé teplotě byly použity zahřáté zásobní roztoky aminokyselin a derivatizačního činidla. Jako zkoumané teploty byly zvoleny teploty 22, 40 a 60 C. Výtěžnost derivatizace neprobíhala výrazně ve prospěch konkrétní teploty, Jako kompromis pro další měření byla zvolena teplota 40 C. Analýza reálného vzorku výživového doplňku BCAA Extreme Pure od společnosti Aminostar s.r.o. obsahující L-isoleucin, L-leucin a L-valin neprokázala přítomnost D- -enantiomerů studovaných aminokyselin. 32
33 POUŽITÁ LITERATURA 1. Strkalová, S.; Kalíková, K.; Tesařová, E.: Výskyt a význam enantiomerů v potravinách. Chem. Listy 102, (2008). 2. Smith, S.W.: Chiral Toxicology: It's the Same Thing Only Different. Toxicol. Sci. 110, 4-30 (2009). 3. Červinka, O.: Chiralita a pojmy s ní související. Chem. Listy 93, (1999). 4. Loukotová, L.; Rambousková, M.; Bosáková, Z.; Tesařová, E.: Cellulose tris(3,5- -dimethylphenylcarbamate)-based chiral stationary phases as effective tools for enantioselective HPLC separation of structurally different disubstituted binaphthyls. Chirality 20, (2008). 5. Nerkar, A.G.; Lade, K.S.; Gadhave, N.A.; Sawant, S.D.: Chiral switches: A review. J. Pharm. Res. 4, (2011). 6. Kasprzyk-Hordern, B.: Pharmacologically active compounds in the environment and their chirality. Chem. Soc. Rev. 39, (2010). 7. Ilisz I., Berkecz R., Péter A.: Application of chiral derivatizing agents in the high- -performance liquid chromatographic separation of amino acid enantiomers: A review. J. Pharm. Biomed. Anal. 47, 1-15 (2008) 8. Ye, J.; Wu, J.; Liu, W.: Enantioselective separation and analysis of chiral pesticides by high-performance liquid chromatography. TrAC, Trends Anal. Chem. 28, (2009). 9. Armstrong, D.W.: Optical isomer separation by liquid chromatography. Anal. Chem. 59, 84A-88A, 90A-91A (1987). 10. Nuggehally, R.S.: Evaluation of experimental strategies for the development of chiral chromatographic methods based on diastereomer formation. Biomed. Chromatogr. 18, (2004). 11. Ilisz I., Berkecz R., Péter A.: HPLC separation of amino acid enantiomers and small peptides on macrocyclic antibiotic-based chiral stationary phases: A review. J. Sep. Sci. 29, (2006). 12. Ward, T. J., Farris III., A.B.: Chiral separations using the macrocyclic antibiotics: A review. J. Chromatogr. A 906, (2001). 33
34 13. Somma, S.; Gastaldo, L.; Corti, A.: Teicoplanin, a new antibiotic from Actinoplanes teichomyceticus nov. sp. Antimicrob. Agents Chemother. 26, (1984). 14. Desiderio C.; Fanali S.: Chiral analysis by capillary electrophoresis using antibiotics as chiral selector. J. Chromatogr. A 807, (1993). 15. Sajdok, J.; Kozak, A.; Zídková, J.; Kotrba, P.; Pilin, A.; Káš, J.: Modifikace proteinů v průběhu stárnutí organismů. Chem. Listy 95, (2001). 16. Chiarla, C.; Giovannini, I.; Boldrini, G.; Castagneto, M.: The branched- -chain amino acids, Minerva Gastroenterol. Dietol. 43, 189 (1997); anglický abstrakt; ID Lawrence, J.F.; Frei, R.W.: Journal of Chromatography Library Volume 7: Chemical Derivatization in Liquid Chromatography, Amsterdam, Elsevier Scientific Publishing Company, Štulík K.; Bosáková, Z.; Coufal, P.; Jelínek, I.; Pacáková, E.; Ševčík, J.: Analytické separační metody, Univerzita Karlova, Karolinum, Praha Deyl, Z.; Mikšík, I.; Tagliaro, F.; Tesařová, E.: Advanced Chromatographic and Electromigration Methods in Biosciences (Deyl, Z.; ed.), kap. 4., Elsevier, Amsterdam, Zhou, W.; Zhang, X.-Y.; Duan, G.-L.: Liquid-chromatography quantitative analysis of 20 amino acids after derivatization with FMOC-Cl and its application to different origin Radix isatidis, J. Chin. Chem. Soc. 58, (2011). 21. Molnár-Perl, I.: Quantitation of Amino Acids and Amines by Chromatography - - Methods and Protocols (Molnár-Perl, I.; ed.), kap. 2., Elsevier, Amsterdam Pacáková V.; Štulík K.: Vysokoúčinná kapalinová chromatografie, 1. vydání, Praha Univerzita Karlova, Státní pedagogické nakladatelství, Repko, P.: Využití chirálních stacionárních fází na bázi teikoplaninu a teikoplanin aglykonu pro enantioseparaci FMOC-derivatizovaných aminokyselin. Diplomová práce, Univerzita Karlova v Praze, Přírodovědecká fakulta, Praha
Chirální separace pomocí vysokoúčinné kapalinové chromatografie
 Chirální separace pomocí vysokoúčinné kapalinové chromatografie Zadání úlohy: a) Skupinové zadání Porovnejte vliv složení mobilní fáze na chirální separace jednotlivých β-blokátorů na vankomycinové koloně
Chirální separace pomocí vysokoúčinné kapalinové chromatografie Zadání úlohy: a) Skupinové zadání Porovnejte vliv složení mobilní fáze na chirální separace jednotlivých β-blokátorů na vankomycinové koloně
Přístupy k analýze opticky aktivních látek metodou HPLC
 Přístupy k analýze opticky aktivních látek metodou HPLC Karel Lemr Katedra analytické chemie, Přírodovědecká fakulta Univerzity Palackého tř. Svobody 8, 771 46 Olomouc lemr@prfnw.upol.cz Zentiva, Praha,
Přístupy k analýze opticky aktivních látek metodou HPLC Karel Lemr Katedra analytické chemie, Přírodovědecká fakulta Univerzity Palackého tř. Svobody 8, 771 46 Olomouc lemr@prfnw.upol.cz Zentiva, Praha,
Analýza kofeinu v kávě pomocí kapalinové chromatografie
 Analýza kofeinu v kávě pomocí kapalinové chromatografie Kofein (obr.1) se jako přírodní alkaloid vyskytuje v mnoha rostlinách (např. fazolích, kakaových bobech, černém čaji apod.) avšak nejvíce je spojován
Analýza kofeinu v kávě pomocí kapalinové chromatografie Kofein (obr.1) se jako přírodní alkaloid vyskytuje v mnoha rostlinách (např. fazolích, kakaových bobech, černém čaji apod.) avšak nejvíce je spojován
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC
 Strana 1 STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Postup specifikuje podmínky pro stanovení obsahu semduramicinu v krmivech metodou vysokoúčinné kapalinové chromatografie (HPLC) v koncentračním
Strana 1 STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Postup specifikuje podmínky pro stanovení obsahu semduramicinu v krmivech metodou vysokoúčinné kapalinové chromatografie (HPLC) v koncentračním
Chirální separace v CE
 Chirální separace v CE Chiralitu vykazují jak organické sloučeniny tak anorganické sloučeniny. Projevuje se existencí dvou konstitučně identických molekul (enantiomerů), které se liší pouze ve vzájemném
Chirální separace v CE Chiralitu vykazují jak organické sloučeniny tak anorganické sloučeniny. Projevuje se existencí dvou konstitučně identických molekul (enantiomerů), které se liší pouze ve vzájemném
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
VYUŽITÍ BEZKONTAKTNÍ VODIVOSTNÍ DETEKCE PRO HPLC SEPARACI POLYKARBOXYLÁTOVÝCH DERIVÁTŮ CYKLENU. Anna Hamplová
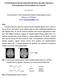 VYUŽITÍ BEZKOTAKTÍ VODIVOSTÍ DETEKCE PRO HPLC SEPARACI POLYKARBOXYLÁTOVÝCH DERIVÁTŮ CYKLEU Anna Hamplová Univerzita Karlova v Praze, Přírodovědecká fakulta, Katedra analytické chemie Albertov 6, 128 43
VYUŽITÍ BEZKOTAKTÍ VODIVOSTÍ DETEKCE PRO HPLC SEPARACI POLYKARBOXYLÁTOVÝCH DERIVÁTŮ CYKLEU Anna Hamplová Univerzita Karlova v Praze, Přírodovědecká fakulta, Katedra analytické chemie Albertov 6, 128 43
Separace chirálních látek. Zuzana Bosáková
 Separace chirálních látek Zuzana Bosáková Enantiomery opticky aktivní R-enantiomer S-enantiomer nechirální prostředí chirální prostředí živé organismy - chirální environmentální prostředí (proteiny L-aminokyselin)
Separace chirálních látek Zuzana Bosáková Enantiomery opticky aktivní R-enantiomer S-enantiomer nechirální prostředí chirální prostředí živé organismy - chirální environmentální prostředí (proteiny L-aminokyselin)
Stereochemie 7. Přednáška 7
 Stereochemie 7 Přednáška 7 1 ptická čistota p = [ ]poz [ ]max x 100 = ee = [R] - [S] [R] + [S] x 100 p optická čistota [R], [S] molární frakce R a S enantiomerů ee + 100 %R = ee + %S = ee + 100 - %R =
Stereochemie 7 Přednáška 7 1 ptická čistota p = [ ]poz [ ]max x 100 = ee = [R] - [S] [R] + [S] x 100 p optická čistota [R], [S] molární frakce R a S enantiomerů ee + 100 %R = ee + %S = ee + 100 - %R =
L 54/116 CS Úřední věstník Evropské unie
 L 54/116 CS Úřední věstník Evropské unie 26.2.2009 8. Výsledky kruhových testů V rámci ES byly provedeny kruhové testy, při nichž až 13 laboratoří zkoušelo čtyři vzorky krmiva pro selata, včetně jednoho
L 54/116 CS Úřední věstník Evropské unie 26.2.2009 8. Výsledky kruhových testů V rámci ES byly provedeny kruhové testy, při nichž až 13 laboratoří zkoušelo čtyři vzorky krmiva pro selata, včetně jednoho
Chirální separace v kapalinové chromatografii
 Pražské analytické centrum inovací Projekt CZ.04.3.07/4.2.01.1/0002 spolufinancovaný ESF a Státním rozpočtem ČR Chirální separace v kapalinové chromatografii Zuzana Bosáková PřF UK Praha Enantiomery R
Pražské analytické centrum inovací Projekt CZ.04.3.07/4.2.01.1/0002 spolufinancovaný ESF a Státním rozpočtem ČR Chirální separace v kapalinové chromatografii Zuzana Bosáková PřF UK Praha Enantiomery R
Vysokoúčinná kapalinová chromatografie
 Vysokoúčinná kapalinová chromatografie HPLC High Performance Liquid Chromatography Vysokoúčinná...X... Vysoceúčinná kapalinová chromatografie RRLC Rapid Resolution Liquid Chromatography Rychle rozlišovací
Vysokoúčinná kapalinová chromatografie HPLC High Performance Liquid Chromatography Vysokoúčinná...X... Vysoceúčinná kapalinová chromatografie RRLC Rapid Resolution Liquid Chromatography Rychle rozlišovací
ENANTIOSEPARACE A DERIVATIZACE VYBRANÉ AMINOKYSELINY
 UNIVERZITA KARLOVA V PRAZE Přírodovědecká fakulta Katedra analytické chemie ENANTIOSEPARACE A DERIVATIZACE VYBRANÉ AMINOKYSELINY ENANTIOSEPARATION AND DERIVATIZATION OF SELECTED AMINO ACID Bakalářská práce
UNIVERZITA KARLOVA V PRAZE Přírodovědecká fakulta Katedra analytické chemie ENANTIOSEPARACE A DERIVATIZACE VYBRANÉ AMINOKYSELINY ENANTIOSEPARATION AND DERIVATIZATION OF SELECTED AMINO ACID Bakalářská práce
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MELAMINU A KYSELINY KYANUROVÉ METODOU LC-MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MELAMINU A KYSELINY KYANUROVÉ METODOU LC-MS 1 Rozsah a účel Postup je určen pro stanovení obsahu melaminu a kyseliny kyanurové v krmivech. 2 Princip
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MELAMINU A KYSELINY KYANUROVÉ METODOU LC-MS 1 Rozsah a účel Postup je určen pro stanovení obsahu melaminu a kyseliny kyanurové v krmivech. 2 Princip
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto SUBSTITUČNÍ DERIVÁTY KARBOXYLOVÝCH O KYSELIN R C O X karboxylových kyselin - substituce na vedlejším uhlovodíkovém řetězci aminokyseliny - hydroxykyseliny
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto SUBSTITUČNÍ DERIVÁTY KARBOXYLOVÝCH O KYSELIN R C O X karboxylových kyselin - substituce na vedlejším uhlovodíkovém řetězci aminokyseliny - hydroxykyseliny
Bc. Gabriela Kučerová CHIRÁLNÍ SEPARACE NOVĚ SYNTETIZOVANÝCH AMINOKYSELIN METODOU HPLC. Chiral HPLC separation of newly synthesized amino acids
 U N I V E R Z I T A K A R L O V A V P R A Z E P ř í r o d o v ě d e c k á f a k u l t a Studijní program: Klinická a toxikologická analýza Bc. Gabriela Kučerová CHIRÁLNÍ SEPARACE NOVĚ SYNTETIZOVANÝCH AMINOKYSELIN
U N I V E R Z I T A K A R L O V A V P R A Z E P ř í r o d o v ě d e c k á f a k u l t a Studijní program: Klinická a toxikologická analýza Bc. Gabriela Kučerová CHIRÁLNÍ SEPARACE NOVĚ SYNTETIZOVANÝCH AMINOKYSELIN
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU HPLC - OCHRATOXIN A
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU HPLC - OCHRATOXIN A 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení ochratoxinu A v krmivech. 1 Ochratoxin A patří mezi
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU HPLC - OCHRATOXIN A 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení ochratoxinu A v krmivech. 1 Ochratoxin A patří mezi
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/
 Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 LRR/CHPB2 Chemie pro biology 2 Stereochemie organických molekul a izomerie Lucie Szüčová Osnova: stereochemie organických sloučenin
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 LRR/CHPB2 Chemie pro biology 2 Stereochemie organických molekul a izomerie Lucie Szüčová Osnova: stereochemie organických sloučenin
Stereochemie. Přednáška 6
 Stereochemie Přednáška 6 Stereoheterotopické ligandy a NMR spektroskopie Stereoheterotopické ligandy a NMR spektroskopie NMR může rozlišit atomy v odlišném okolí stíněny jinou měrou rozdíl v chemických
Stereochemie Přednáška 6 Stereoheterotopické ligandy a NMR spektroskopie Stereoheterotopické ligandy a NMR spektroskopie NMR může rozlišit atomy v odlišném okolí stíněny jinou měrou rozdíl v chemických
Vysokoúčinná kapalinová chromatografie. Petr Kozlík Katedra analytické chemie
 Vysokoúčinná kapalinová chromatografie Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz 1 Sylabus přednášky: Praxe v HPLC Mobilní fáze Chromatografická kolona Spoje v HPLC Vývoj chromatografické
Vysokoúčinná kapalinová chromatografie Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz 1 Sylabus přednášky: Praxe v HPLC Mobilní fáze Chromatografická kolona Spoje v HPLC Vývoj chromatografické
Studijní materiál HMF_1 1. Hydroxymethylfurfural a jeho stanovení v potravinách 2. Kapalinová chromatografie (HPLC, UPLC)
 Studijní materiál HMF_1 1. Hydroxymethylfurfural a jeho stanovení v potravinách 2. Kapalinová chromatografie (HPLC, UPLC) V Brně dne 20. 11. 2011 Vypracoval: RNDr. Ivana Borkovcová, Ph.D. 1. Hydroxymethylfurfural
Studijní materiál HMF_1 1. Hydroxymethylfurfural a jeho stanovení v potravinách 2. Kapalinová chromatografie (HPLC, UPLC) V Brně dne 20. 11. 2011 Vypracoval: RNDr. Ivana Borkovcová, Ph.D. 1. Hydroxymethylfurfural
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253
 Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 16 Iontová chromatografie Iontová chromatografie je speciální technika vyvinutá pro separaci anorganických iontů a organických
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 16 Iontová chromatografie Iontová chromatografie je speciální technika vyvinutá pro separaci anorganických iontů a organických
CS Úřední věstník Evropské unie L 54/89
 26.2.2009 CS Úřední věstník Evropské unie L 54/89 c) při vlnové délce mezi 230 a 320 nm se nesmí spektrum vzestupné části, vrcholu a sestupné části píku zkoušeného vzorku lišit od ostatních částí spektra
26.2.2009 CS Úřední věstník Evropské unie L 54/89 c) při vlnové délce mezi 230 a 320 nm se nesmí spektrum vzestupné části, vrcholu a sestupné části píku zkoušeného vzorku lišit od ostatních částí spektra
Aplikace elektromigračních technik
 Aplikace elektromigračních technik Capillary electrophoresis D.L.Barker High Performance Capillary electrophoresis M.G. Khaledi Analysis and detection by capillary electrophoresis M.L.Marina (ed.) Electrophoresis
Aplikace elektromigračních technik Capillary electrophoresis D.L.Barker High Performance Capillary electrophoresis M.G. Khaledi Analysis and detection by capillary electrophoresis M.L.Marina (ed.) Electrophoresis
HPLC - Detektory A.Braithwaite and F.J.Smith; Chromatographic Methods, Fifth edition, Blackie Academic & Professional 1996 Colin F. Poole and Salwa K.
 Vysokoúčinná kapalinová chromatografie - Detektory - I Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 HPLC - Detektory A.Braithwaite and F.J.Smith; Chromatographic Methods, Fifth
Vysokoúčinná kapalinová chromatografie - Detektory - I Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 HPLC - Detektory A.Braithwaite and F.J.Smith; Chromatographic Methods, Fifth
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU NEPOVOLENÝCH DOPLŇKOVÝCH LÁTEK METODOU LC-MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU NEPOVOLENÝCH DOPLŇKOVÝCH LÁTEK METODOU LC-MS 1 Účel a rozsah Tato metoda specifikuje podmínky pro stanovení nepovolených doplňkových látek Zn-bacitracinu,
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU NEPOVOLENÝCH DOPLŇKOVÝCH LÁTEK METODOU LC-MS 1 Účel a rozsah Tato metoda specifikuje podmínky pro stanovení nepovolených doplňkových látek Zn-bacitracinu,
STANOVENÍ AZOBARVIV VE SMĚSI METODOU RP-HPLC SE SPEKTROFOTOMETRICKOU DETEKCÍ
 STANOVENÍ AZOBARVIV VE SMĚSI METODOU RP-HPLC SE SPEKTROFOTOMETRICKOU DETEKCÍ 1 Úkol Separovat a metodou kalibrační křivky stanovit azobarviva (methyloranž - MO, dimethylová žluť - DMŽ) ve směsi metodou
STANOVENÍ AZOBARVIV VE SMĚSI METODOU RP-HPLC SE SPEKTROFOTOMETRICKOU DETEKCÍ 1 Úkol Separovat a metodou kalibrační křivky stanovit azobarviva (methyloranž - MO, dimethylová žluť - DMŽ) ve směsi metodou
Příloha 1. Návod pro laboratorní úlohu
 Příloha 1. Návod pro laboratorní úlohu VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE ÚSTAV CHEMIE A ANALÝZY POTRAVIN Technická 5, 166 28 Praha 6 tel./fax.: + 420 224 353 185; jana.hajslova@vscht.cz Analýza
Příloha 1. Návod pro laboratorní úlohu VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE ÚSTAV CHEMIE A ANALÝZY POTRAVIN Technická 5, 166 28 Praha 6 tel./fax.: + 420 224 353 185; jana.hajslova@vscht.cz Analýza
Vysokoúčinná kapalinová chromatografie. Petr Kozlík Katedra analytické chemie
 Vysokoúčinná kapalinová chromatografie Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz http://web.natur.cuni.cz/~kozlik/ 1 Vysokoúčinná kapalinová chromatografie Teorie HPLC Praktické
Vysokoúčinná kapalinová chromatografie Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz http://web.natur.cuni.cz/~kozlik/ 1 Vysokoúčinná kapalinová chromatografie Teorie HPLC Praktické
VYSOKOÚČINNÁ KAPALINOVÁ CHROMATOGRAFIE ZADÁNÍ ÚLOHY
 VYSOKOÚČINNÁ KAPALINOVÁ CHOMATOGAFIE ZADÁNÍ ÚLOHY Metodou vysokoúčinné kapalinové chromatografie separujte směs s-triazinových herbicidů, sledujte vliv složení mobilní fáze na separaci. Proveďte kvalitativní
VYSOKOÚČINNÁ KAPALINOVÁ CHOMATOGAFIE ZADÁNÍ ÚLOHY Metodou vysokoúčinné kapalinové chromatografie separujte směs s-triazinových herbicidů, sledujte vliv složení mobilní fáze na separaci. Proveďte kvalitativní
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MADURAMICINU A SEMDURAMICINU METODOU HPLC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MADURAMICINU A SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení maduramicinu a semduramicinu v krmivech a premixech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MADURAMICINU A SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení maduramicinu a semduramicinu v krmivech a premixech.
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - aflatoxin B1, B2, G1 a G2
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - aflatoxin B1, B2, G1 a G2 1 Rozsah a účel Metoda je vhodná pro stanovení aflatoxinů B1, B2, G1 a G2 v krmivech. 2 Princip
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - aflatoxin B1, B2, G1 a G2 1 Rozsah a účel Metoda je vhodná pro stanovení aflatoxinů B1, B2, G1 a G2 v krmivech. 2 Princip
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
STANOVENÍ ENANTIOMERŮ VYBRANÝCH LÉČIV POMOCÍ HPLC. Determination of enantiomers of selected drugs by HPLC
 U N I V E R Z I T A K A R L O V A V P R A Z E P ř ír o d o v ě d e c k á f a k u lt a Katedra fyzikální a makromolekulární chemie STANOVENÍ ENANTIOMERŮ VYBRANÝCH LÉČIV POMOCÍ HPLC Determination of enantiomers
U N I V E R Z I T A K A R L O V A V P R A Z E P ř ír o d o v ě d e c k á f a k u lt a Katedra fyzikální a makromolekulární chemie STANOVENÍ ENANTIOMERŮ VYBRANÝCH LÉČIV POMOCÍ HPLC Determination of enantiomers
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253
 Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 19 Chirální separace Enantiomery jsou molekuly, které nejsou ztotožnitelné se svými zrcadlovými obrazy. Obě zrcadlové formy
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 19 Chirální separace Enantiomery jsou molekuly, které nejsou ztotožnitelné se svými zrcadlovými obrazy. Obě zrcadlové formy
Stanovení koncentrace (kvantifikace) proteinů
 Stanovení koncentrace (kvantifikace) proteinů Bioanalytické metody Prof. RNDr. Pavel Peč, CSc. Úvod Kritéria výběru metod stanovení koncentrace proteinů jsou založena na možnostech pro vlastní analýzu,
Stanovení koncentrace (kvantifikace) proteinů Bioanalytické metody Prof. RNDr. Pavel Peč, CSc. Úvod Kritéria výběru metod stanovení koncentrace proteinů jsou založena na možnostech pro vlastní analýzu,
Organická chemie 3.ročník studijního oboru - kosmetické služby.
 Organická chemie 3.ročník studijního oboru - kosmetické služby. T-7 Funkční a substituční deriváty karboxylových kyselin Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu:
Organická chemie 3.ročník studijního oboru - kosmetické služby. T-7 Funkční a substituční deriváty karboxylových kyselin Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu:
Vysoká škola chemicko-technologická v Praze. Ústav organické technologie. Václav Matoušek
 Vysoká škola chemicko-technologická v Praze Ústav organické technologie VŠCHT PRAHA SVOČ 2005 Václav Matoušek Školitel : Ing. Petr Kačer, PhD. Prof. Ing. Libor Červený, DrSc. Proč asymetrická hydrogenace?
Vysoká škola chemicko-technologická v Praze Ústav organické technologie VŠCHT PRAHA SVOČ 2005 Václav Matoušek Školitel : Ing. Petr Kačer, PhD. Prof. Ing. Libor Červený, DrSc. Proč asymetrická hydrogenace?
LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ
 LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ STANOVENÍ SACHARIDŮ METODOU VYSOKOÚČINNÉ CHROMATOGRAFIE VE SPOJENÍ S DETEKTOREM EVAPORATIVE LIGHT SCATTERING (HPLC-ELSD) 1 Základní požadované znalosti
LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ STANOVENÍ SACHARIDŮ METODOU VYSOKOÚČINNÉ CHROMATOGRAFIE VE SPOJENÍ S DETEKTOREM EVAPORATIVE LIGHT SCATTERING (HPLC-ELSD) 1 Základní požadované znalosti
Vysokoúčinná kapalinová chromatografie. Petr Kozlík Katedra analytické chemie
 Vysokoúčinná kapalinová chromatografie Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz 1 Aplikace HPLC Analýza složek životního prostředí Toxikologie Potravinářská analýza Farmaceutická
Vysokoúčinná kapalinová chromatografie Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz 1 Aplikace HPLC Analýza složek životního prostředí Toxikologie Potravinářská analýza Farmaceutická
SPE je metoda vhodná pro rychlou přípravu vzorků, která užívá
 Extrakce na pevné fázi (SPE) Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Extrakce na pevné fázi (SPE) (Solid Phase Extraction) SPE je metoda vhodná pro rychlou přípravu vzorků,
Extrakce na pevné fázi (SPE) Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Extrakce na pevné fázi (SPE) (Solid Phase Extraction) SPE je metoda vhodná pro rychlou přípravu vzorků,
Stanovení sacharidů ve vybraných přírodních matricích pomocí kapalinové chromatografie s odpařovacím detektorem rozptylu světla (HPLC-ELSD)
 Stanovení sacharidů ve vybraných přírodních matricích pomocí kapalinové chromatografie s odpařovacím detektorem rozptylu světla (HPLC-ELSD) A) Ultrazvuková extrakce Ultrazvuková extrakce je významnou extrakční
Stanovení sacharidů ve vybraných přírodních matricích pomocí kapalinové chromatografie s odpařovacím detektorem rozptylu světla (HPLC-ELSD) A) Ultrazvuková extrakce Ultrazvuková extrakce je významnou extrakční
Principy chromatografie v analýze potravin
 Principy chromatografie v analýze potravin živočišného původu p Ivana Borkovcová Ústav hygieny a technologie mléka FVHE VFU Brno, borkovcovai@vfu.cz Úvod, základní pojmy chromatografické systémy dělení
Principy chromatografie v analýze potravin živočišného původu p Ivana Borkovcová Ústav hygieny a technologie mléka FVHE VFU Brno, borkovcovai@vfu.cz Úvod, základní pojmy chromatografické systémy dělení
Stanovení kreatininu v mase pomocí kapilární izotachoforézy
 Stanovení kreatininu v mase pomocí kapilární izotachoforézy Úkol: Pomocí kapilární izotachoforézy určete, zda je v předloženém reálném vzorku (vařená šunka) obsažen kreatinin. 1. Teoretická část 1.1.Kreatinin
Stanovení kreatininu v mase pomocí kapilární izotachoforézy Úkol: Pomocí kapilární izotachoforézy určete, zda je v předloženém reálném vzorku (vařená šunka) obsažen kreatinin. 1. Teoretická část 1.1.Kreatinin
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) Použití GC-MS spektrometrie
 LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) C Použití GC-MS spektrometrie Vedoucí práce: Doc. Ing. Petr Kačer, Ph.D., Ing. Kamila Syslová Umístění práce: laboratoř 79 Použití GC-MS spektrometrie
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) C Použití GC-MS spektrometrie Vedoucí práce: Doc. Ing. Petr Kačer, Ph.D., Ing. Kamila Syslová Umístění práce: laboratoř 79 Použití GC-MS spektrometrie
K a t e d r a f y z i k á l n í a m a k r o m o l e k u l á r n í c h e m i e
 U N I V E R Z I T A K A R L O V A V P R A Z E Přírodovědecká fakulta K a t e d r a f y z i k á l n í a m a k r o m o l e k u l á r n í c h e m i e STANOVENÍ ENANTIOMERŮ AMINOKYSELIN METODOU HPLC B a k
U N I V E R Z I T A K A R L O V A V P R A Z E Přírodovědecká fakulta K a t e d r a f y z i k á l n í a m a k r o m o l e k u l á r n í c h e m i e STANOVENÍ ENANTIOMERŮ AMINOKYSELIN METODOU HPLC B a k
Izomerie a stereochemie
 Izomerie a stereochemie 1 2 Izomery mají stejný sumární vzorec, ale liší se uspořádáním atomů v prostoru. Konstituční izomery jednotlivé atomy v molekule jsou spojeny různým způsobem Stereoizomery jednotlivé
Izomerie a stereochemie 1 2 Izomery mají stejný sumární vzorec, ale liší se uspořádáním atomů v prostoru. Konstituční izomery jednotlivé atomy v molekule jsou spojeny různým způsobem Stereoizomery jednotlivé
Separační metody Historie: Rozvoj separačních metod od minulého století Postavení separačních metod v rámci analytické chemie Význam chromatografie a
 Úvod do separačních metod pro analýzu léčiv Příprava předmětu byla podpořena projektem OPP č. CZ..7/3..00/3353 Separační metody Historie: Rozvoj separačních metod od minulého století Postavení separačních
Úvod do separačních metod pro analýzu léčiv Příprava předmětu byla podpořena projektem OPP č. CZ..7/3..00/3353 Separační metody Historie: Rozvoj separačních metod od minulého století Postavení separačních
DERIVATIZACE AMINOKYSELIN, PEPTIDŮ A PROTEINŮ PRO LASEREM INDUKOVANOU FLUORESCENČNÍ DETEKCI V KAPILÁRNÍ ELEKTRO-
 DERIVATIZACE AMINOKYSELIN, PEPTIDŮ A PROTEINŮ PRO LASEREM INDUKOVANOU FLUORESCENČNÍ DETEKCI V KAPILÁRNÍ ELEKTRO- FORÉZE MARKÉTA RYVOLOVÁ*, PETR TÁBORSKÝ, PATRIK VRÁBEL, JOSEF HAVEL a JAN PREISLER Katedra
DERIVATIZACE AMINOKYSELIN, PEPTIDŮ A PROTEINŮ PRO LASEREM INDUKOVANOU FLUORESCENČNÍ DETEKCI V KAPILÁRNÍ ELEKTRO- FORÉZE MARKÉTA RYVOLOVÁ*, PETR TÁBORSKÝ, PATRIK VRÁBEL, JOSEF HAVEL a JAN PREISLER Katedra
Analýza aniontových tenzidů v čisticích prostředcích kapilární elektroforézou
 Analýza aniontových tenzidů v čisticích prostředcích kapilární elektroforézou Úkol: Pomocí kapilární elektroforézy v nevodném prostředí semikvantitativně stanovte vybrané aniontové tenzidy v čisticím prostředku.
Analýza aniontových tenzidů v čisticích prostředcích kapilární elektroforézou Úkol: Pomocí kapilární elektroforézy v nevodném prostředí semikvantitativně stanovte vybrané aniontové tenzidy v čisticím prostředku.
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Příloha 2. Návod pro laboratorní úlohu
 Příloha 2. Návod pro laboratorní úlohu VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE ÚSTAV CHEMIE A ANALÝZY POTRAVIN Technická 5, 166 28 Praha 6 tel./fax.: + 42 224 353 185; jana.hajslova@vscht.cz Analýza
Příloha 2. Návod pro laboratorní úlohu VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE ÚSTAV CHEMIE A ANALÝZY POTRAVIN Technická 5, 166 28 Praha 6 tel./fax.: + 42 224 353 185; jana.hajslova@vscht.cz Analýza
Trendy v moderní HPLC
 Trendy v moderní HPLC Josef Cvačka, 5.1.2011 CHROMATOGRAFIE NA ČIPECH Miniaturizace separačních systémů Mikrofluidní čipy Mikrofabrikace Chromatografické mikrofluidní čipy s MS detekcí Praktické využití
Trendy v moderní HPLC Josef Cvačka, 5.1.2011 CHROMATOGRAFIE NA ČIPECH Miniaturizace separačních systémů Mikrofluidní čipy Mikrofabrikace Chromatografické mikrofluidní čipy s MS detekcí Praktické využití
Superkritická fluidní extrakce (SFE) Superkritická fluidní extrakce
 Superkritická fluidní extrakce (zkráceně SFE, z angl. Supercritical Fluid Extraction) = extrakce, kde extrakčním činidlem je tekutina v superkritickém stavu, tzv. superkritická (nadkritická) tekutina (zkráceně
Superkritická fluidní extrakce (zkráceně SFE, z angl. Supercritical Fluid Extraction) = extrakce, kde extrakčním činidlem je tekutina v superkritickém stavu, tzv. superkritická (nadkritická) tekutina (zkráceně
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách
 Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
Určení koncentrace proteinu fluorescenční metodou v mikrotitračních destičkách Teorie Stanovení celkových proteinů Celkové množství proteinů lze stanovit pomocí několika metod; například: Hartree-Lowryho
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU VITAMÍNU D METODOU LC/MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VITAMÍNU D METODOU LC/MS 1 Účel a rozsah Tento postup specifikuje podmínky pro stanovení vitamínu D3 v krmivech metodou LC/MS. 2 Princip Zkušební
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VITAMÍNU D METODOU LC/MS 1 Účel a rozsah Tento postup specifikuje podmínky pro stanovení vitamínu D3 v krmivech metodou LC/MS. 2 Princip Zkušební
Asymetrická transfer hydrogenace při syntéze prekurzorů farmaceutických substancí
 Laboratoř oboru Výroba léčiv (N111049) Asymetrická transfer hydrogenace při syntéze prekurzorů farmaceutických substancí O Vedoucí práce: Ing. Jiří Vavřík Ing. Jakub Januščák Studijní program: Studijní
Laboratoř oboru Výroba léčiv (N111049) Asymetrická transfer hydrogenace při syntéze prekurzorů farmaceutických substancí O Vedoucí práce: Ing. Jiří Vavřík Ing. Jakub Januščák Studijní program: Studijní
ÚSTAV CHEMIE A ANALÝZY POTRAVIN
 VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE ÚSTAV CHEMIE A ANALÝZY POTRAVIN Technická 5, 166 28 Praha 6 tel./fax.: + 420 220 443 185; jana.hajslova@vscht.cz LABORATOŘ Z ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ
VYSOKÁ ŠKOLA CHEMICKO-TECHNOLOGICKÁ V PRAZE ÚSTAV CHEMIE A ANALÝZY POTRAVIN Technická 5, 166 28 Praha 6 tel./fax.: + 420 220 443 185; jana.hajslova@vscht.cz LABORATOŘ Z ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ
Aplikační rozsah chromatografie
 Chromatografické metody II. Aplikační rozsah chromatografie Chromatografie Kapalinová chromatografie rozdělení Nízkotlaká (atmosferický tlak) LPC Střednětlaká (4 Mpa) FPLC Vysokotlaká (40 Mpa) HPLC Ultravysokotlaká
Chromatografické metody II. Aplikační rozsah chromatografie Chromatografie Kapalinová chromatografie rozdělení Nízkotlaká (atmosferický tlak) LPC Střednětlaká (4 Mpa) FPLC Vysokotlaká (40 Mpa) HPLC Ultravysokotlaká
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU VITAMÍNU A A VITAMÍNU E METODOU HPLC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VITAMÍNU A A VITAMÍNU E METODOU HPLC 1 Účel a rozsah Postup specifikuje podmínky pro stanovení vitamínu A a vitamínu E v krmivech a premixech. 2 Princip
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU VITAMÍNU A A VITAMÍNU E METODOU HPLC 1 Účel a rozsah Postup specifikuje podmínky pro stanovení vitamínu A a vitamínu E v krmivech a premixech. 2 Princip
Bílkoviny - proteiny
 Bílkoviny - proteiny Proteiny jsou složeny z 20 kódovaných aminokyselin L-enantiomery Chemická struktura aminokyselin R představuje jeden z 20 různých typů postranních řetězců R Hlavní řetězec je neměnný
Bílkoviny - proteiny Proteiny jsou složeny z 20 kódovaných aminokyselin L-enantiomery Chemická struktura aminokyselin R představuje jeden z 20 různých typů postranních řetězců R Hlavní řetězec je neměnný
STANOVENÍ ENANTIOMERŮ THEANINU POMOCÍ HPLC, POROVNÁNÍ METOD DETEKCE. TEREZA ŠLECHTOVÁ, KVĚTA KALÍKOVÁ a EVA TESAŘOVÁ. Úvod. Experimentální část
 Chem. isty 07, 8 3 (03) aboratorní přístroje a postupy STNOVENÍ ENNTIOMERŮ THENINU POMOCÍ HPC, POROVNÁNÍ METO ETEKCE TEREZ ŠECHTOVÁ, KVĚT KÍKOVÁ a EV TESŘOVÁ Katedra fyzikální a makromolekulární chemie,
Chem. isty 07, 8 3 (03) aboratorní přístroje a postupy STNOVENÍ ENNTIOMERŮ THENINU POMOCÍ HPC, POROVNÁNÍ METO ETEKCE TEREZ ŠECHTOVÁ, KVĚT KÍKOVÁ a EV TESŘOVÁ Katedra fyzikální a makromolekulární chemie,
Stanovení cholesterolu ve vaječném žloutku a mléce kapilární elektroforézou
 Stanovení cholesterolu ve vaječném žloutku a mléce kapilární elektroforézou Úkol Stanovte obsah cholesterolu ve vaječném žloutku a mléce pomocí kapilární elektroforézy. Teoretická část Cholesterol je steroidní
Stanovení cholesterolu ve vaječném žloutku a mléce kapilární elektroforézou Úkol Stanovte obsah cholesterolu ve vaječném žloutku a mléce pomocí kapilární elektroforézy. Teoretická část Cholesterol je steroidní
UNIVERZITA PARDUBICE FAKULTA CHEMICKO-TECHNOLOGICKÁ DISERTAČNÍ PRÁCE
 UNIVERZITA PARDUBICE FAKULTA CHEMICKO-TECHNOLOGICKÁ DISERTAČNÍ PRÁCE 2009 Ing. David Kahoun UNIVERZITA PARDUBICE FAKULTA CHEMICKO-TECHNOLOGICKÁ ANALÝZA BIOLOGICKY AKTIVNÍCH LÁTEK V MEDOVINÁCH METODOU HPLC
UNIVERZITA PARDUBICE FAKULTA CHEMICKO-TECHNOLOGICKÁ DISERTAČNÍ PRÁCE 2009 Ing. David Kahoun UNIVERZITA PARDUBICE FAKULTA CHEMICKO-TECHNOLOGICKÁ ANALÝZA BIOLOGICKY AKTIVNÍCH LÁTEK V MEDOVINÁCH METODOU HPLC
Jednotné pracovní postupy zkoušení krmiv Vydání 1 STANOVENÍ OBSAHU KOKCIDIOSTATIK METODOU LC-MS
 Strana 1 STANOVENÍ OBSAHU KOKCIDIOSTATIK METODOU LC-MS 1 Účel a rozsah Postup specifikuje podmínky pro stanovení diclazurilu, halofuginonu, lasalocidu, maduramicinu, monensinu, narasinu, nikarbazinu, robenidinu,
Strana 1 STANOVENÍ OBSAHU KOKCIDIOSTATIK METODOU LC-MS 1 Účel a rozsah Postup specifikuje podmínky pro stanovení diclazurilu, halofuginonu, lasalocidu, maduramicinu, monensinu, narasinu, nikarbazinu, robenidinu,
Jednotné pracovní postupy zkoušení krmiv Stanovení obsahu celkového a volného tryptofanu metodou HPLC
 Strana 1 STANOVENÍ OBSAHU CELKOVÉHO A VOLNÉHO TRYPTOFANU METODOU HPLC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení obsahu celkového a volného tryptofanu v krmivech metodou vysokoúčinné kapalinové
Strana 1 STANOVENÍ OBSAHU CELKOVÉHO A VOLNÉHO TRYPTOFANU METODOU HPLC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení obsahu celkového a volného tryptofanu v krmivech metodou vysokoúčinné kapalinové
STANOVENÍ AMINOKYSELINOVÉHO SLOŽENÍ BÍLKOVIN. Postup stanovení aminokyselinového složení
 STANVENÍ AMINKYSELINVÉH SLŽENÍ BÍLKVIN Důvody pro stanovení AK složení určení nutriční hodnoty potraviny, suroviny (esenciální vs. neesenciální AK) charakterizace určité bílkovinné frakce nebo konkrétní
STANVENÍ AMINKYSELINVÉH SLŽENÍ BÍLKVIN Důvody pro stanovení AK složení určení nutriční hodnoty potraviny, suroviny (esenciální vs. neesenciální AK) charakterizace určité bílkovinné frakce nebo konkrétní
OPTIMALIZACE METODY ANODICKÉ ROZPOUŠTĚCÍ VOLTAMETRIE PRO ANALÝZU BIOLOGICKÝCH VZORKŮ S OBSAHEM RTUTI
 Středoškolská technika 212 Setkání a prezentace prací středoškolských studentů na ČVUT OPTIMALIZACE METODY ANODICKÉ ROZPOUŠTĚCÍ VOLTAMETRIE PRO ANALÝZU BIOLOGICKÝCH VZORKŮ S OBSAHEM RTUTI Eliška Marková
Středoškolská technika 212 Setkání a prezentace prací středoškolských studentů na ČVUT OPTIMALIZACE METODY ANODICKÉ ROZPOUŠTĚCÍ VOLTAMETRIE PRO ANALÝZU BIOLOGICKÝCH VZORKŮ S OBSAHEM RTUTI Eliška Marková
isolace analytu oddělení analytu od matrice (přečištění) zakoncentrování analytu stanovení analytu (analytů) ve vícesložkové směsi
 SEPARAČNÍ METODY Využití separačních metod isolace analytu oddělení analytu od matrice (přečištění) zakoncentrování analytu stanovení analytu (analytů) ve vícesložkové směsi Druhy separačních metod Srážení
SEPARAČNÍ METODY Využití separačních metod isolace analytu oddělení analytu od matrice (přečištění) zakoncentrování analytu stanovení analytu (analytů) ve vícesložkové směsi Druhy separačních metod Srážení
 Vysokoúčinná kapalinová chromatografie High-Performance Liquid Chromatography (HPLC) Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Kapalinová chromatografie (LC) 1.1. Teorie kapalinové
Vysokoúčinná kapalinová chromatografie High-Performance Liquid Chromatography (HPLC) Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Kapalinová chromatografie (LC) 1.1. Teorie kapalinové
HYDROXYDERIVÁTY. Alkoholy Fenoly Bc. Miroslava Wilczková
 HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
Odměrná analýza, volumetrie
 Odměrná analýza, volumetrie metoda založená na měření objemu metoda absolutní: stanovení analytu ze změřeného objemu roztoku činidla o přesně známé koncentraci, který je zapotřebí k úplné a stechiometricky
Odměrná analýza, volumetrie metoda založená na měření objemu metoda absolutní: stanovení analytu ze změřeného objemu roztoku činidla o přesně známé koncentraci, který je zapotřebí k úplné a stechiometricky
Průtokové metody (Kontinuální měření v proudu kapaliny)
 Průtokové metody (Kontinuální měření v proudu kapaliny) 1. Přímé měření: analyzovaná kapalina většinou odvětvena + vhodný detektor 2. Kapalinová chromatografie (HPLC) Stanovení po předchozí separaci 3.
Průtokové metody (Kontinuální měření v proudu kapaliny) 1. Přímé měření: analyzovaná kapalina většinou odvětvena + vhodný detektor 2. Kapalinová chromatografie (HPLC) Stanovení po předchozí separaci 3.
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení vinylthiooxazolidonu (dále VOT) v krmivech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU 5-VINYL - 2-THIOOXAZOLIDONU (GOITRINU) METODOU GC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení vinylthiooxazolidonu (dále VOT) v krmivech.
Aminokyseliny, peptidy a bílkoviny
 Aminokyseliny, peptidy a bílkoviny Dělení aminokyselin Z hlediska obsahu v živé hmotě Z hlediska významu ve výživě Z chemického hlediska Z hlediska rozpustnosti Dělení aminokyselin Z hlediska obsahu v
Aminokyseliny, peptidy a bílkoviny Dělení aminokyselin Z hlediska obsahu v živé hmotě Z hlediska významu ve výživě Z chemického hlediska Z hlediska rozpustnosti Dělení aminokyselin Z hlediska obsahu v
Stanovení složení mastných kyselin
 LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ Stanovení složení mastných kyselin (metoda: plynová chromatografie s plamenovým ionizačním detektorem) Garant úlohy: Ing. Jana Kohoutková, Ph.D. 1 Obsah
LABORATOŘ ANALÝZY POTRAVIN A PŘÍRODNÍCH PRODUKTŮ Stanovení složení mastných kyselin (metoda: plynová chromatografie s plamenovým ionizačním detektorem) Garant úlohy: Ing. Jana Kohoutková, Ph.D. 1 Obsah
Chromatofokusace. separace proteinů na základě jejich pi vysoké rozlišení. není potřeba připravovat ph gradient zaostřovací efekt jednoduchost
 Chromatofokusace separace proteinů na základě jejich pi vysoké rozlišení není potřeba připravovat ph gradient zaostřovací efekt jednoduchost Polypufry - amfolyty Stacionární fáze Polybuffer 96 - ph 9-6
Chromatofokusace separace proteinů na základě jejich pi vysoké rozlišení není potřeba připravovat ph gradient zaostřovací efekt jednoduchost Polypufry - amfolyty Stacionární fáze Polybuffer 96 - ph 9-6
CS Úřední věstník Evropské unie L 54/85
 26.2.2009 CS Úřední věstník Evropské unie L 54/85 F. STANOVENÍ DICLAZURILU 2,6-dichlor-alfa-(4-chlorofenyl)-4-(4,5-dihydro-3,5-dioxo-1,2,4-triazin-2-(3-H)yl)benzenacetonitril 1. Účel a rozsah Tato metoda
26.2.2009 CS Úřední věstník Evropské unie L 54/85 F. STANOVENÍ DICLAZURILU 2,6-dichlor-alfa-(4-chlorofenyl)-4-(4,5-dihydro-3,5-dioxo-1,2,4-triazin-2-(3-H)yl)benzenacetonitril 1. Účel a rozsah Tato metoda
UNIVERZITA PARDUBICE Fakulta chemicko-technologická Katedra analytické chemie. Nám. Čs. Legií 565, Pardubice.
 UNIVERZITA PARDUBICE Fakulta chemicko-technologická Katedra analytické chemie Nám. Čs. Legií 565, 532 10 Pardubice 15. licenční studium INTERAKTIVNÍ STATISTICKÁ ANALÝZA DAT Semestrální práce VYUŽITÍ TABULKOVÉHO
UNIVERZITA PARDUBICE Fakulta chemicko-technologická Katedra analytické chemie Nám. Čs. Legií 565, 532 10 Pardubice 15. licenční studium INTERAKTIVNÍ STATISTICKÁ ANALÝZA DAT Semestrální práce VYUŽITÍ TABULKOVÉHO
Jednotné pracovní postupy zkoušení krmiv Vydání 1 STANOVENÍ OBSAHU KOKCIDIOSTATIK METODOU LC-MS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KOKCIDIOSTATIK METODOU LC-MS 1 Účel a rozsah Postup specifikuje podmínky pro stanovení diclazurilu, halofuginonu, lasalocidu, maduramicinu, monensinu,
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KOKCIDIOSTATIK METODOU LC-MS 1 Účel a rozsah Postup specifikuje podmínky pro stanovení diclazurilu, halofuginonu, lasalocidu, maduramicinu, monensinu,
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti ELEKTROMIGRAČNÍ METODY
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti ELEKTROMIGRAČNÍ METODY ELEKTROFORÉZA K čemu to je? kritérium čistoty preparátu stanovení molekulové hmotnosti makromolekul stanovení izoelektrického
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti ELEKTROMIGRAČNÍ METODY ELEKTROFORÉZA K čemu to je? kritérium čistoty preparátu stanovení molekulové hmotnosti makromolekul stanovení izoelektrického
Chromatografické testování a porovnání reverzních HPLC kolon
 U N I V E R Z I T A K A R L O V A V P R A Z E P ř í r o d o v ě d e c k á f a k u l t a K a t e d r a an alytické ch e mi e Chromatografické testování a porovnání reverzních HPLC kolon B a k a l á ř s
U N I V E R Z I T A K A R L O V A V P R A Z E P ř í r o d o v ě d e c k á f a k u l t a K a t e d r a an alytické ch e mi e Chromatografické testování a porovnání reverzních HPLC kolon B a k a l á ř s
EXTRAKČNÍ METODY. Studijní materiál. 1. Obecná charakteristika extrakce. 2. Extrakce kapalina/kapalina LLE. 3. Alkalická hydrolýza
 Studijní materiál EXTRAKČNÍ METODY 1. Obecná charakteristika extrakce 2. Extrakce kapalina/kapalina LLE 3. Alkalická hydrolýza 4. Soxhletova extrakce 5. Extrakce za zvýšené teploty a tlaku PLE, ASE, PSE
Studijní materiál EXTRAKČNÍ METODY 1. Obecná charakteristika extrakce 2. Extrakce kapalina/kapalina LLE 3. Alkalická hydrolýza 4. Soxhletova extrakce 5. Extrakce za zvýšené teploty a tlaku PLE, ASE, PSE
MINIATURIZACE PRŮTOKOVÝCH ELEKTROCHEMICKÝCH CEL PRO GENEROVÁNÍ TĚKAVÝCH SLOUČENIN. Jakub Hraníček
 MINIATURIZACE PRŮTOKOVÝCH ELEKTROCHEMICKÝCH CEL PRO GENEROVÁNÍ TĚKAVÝCH SLOUČENIN Jakub Hraníček Katedra analytické chemie, Přírodovědecká fakulta, Univerzita Karlova, Albertov 6, 128 43 Praha 2 E-mail:
MINIATURIZACE PRŮTOKOVÝCH ELEKTROCHEMICKÝCH CEL PRO GENEROVÁNÍ TĚKAVÝCH SLOUČENIN Jakub Hraníček Katedra analytické chemie, Přírodovědecká fakulta, Univerzita Karlova, Albertov 6, 128 43 Praha 2 E-mail:
IZOLACE, SEPARACE A DETEKCE PROTEINŮ I. Vlasta Němcová, Michael Jelínek, Jan Šrámek
 IZOLACE, SEPARACE A DETEKCE PROTEINŮ I Vlasta Němcová, Michael Jelínek, Jan Šrámek Studium aktinu, mikrofilamentární složky cytoskeletu pomocí dvou metod: detekce přímo v buňkách - fluorescenční barvení
IZOLACE, SEPARACE A DETEKCE PROTEINŮ I Vlasta Němcová, Michael Jelínek, Jan Šrámek Studium aktinu, mikrofilamentární složky cytoskeletu pomocí dvou metod: detekce přímo v buňkách - fluorescenční barvení
Zajištění správnosti výsledků analýzy kotininu a kreatininu
 Zajištění správnosti výsledků analýzy kotininu a kreatininu Š.Dušková, I.Šperlingová, L. Dabrowská, M. Tvrdíková, M. Šubrtová duskova@szu.cz sperling@szu.cz Oddělení pro hodnocení expozice chemickým látkám
Zajištění správnosti výsledků analýzy kotininu a kreatininu Š.Dušková, I.Šperlingová, L. Dabrowská, M. Tvrdíková, M. Šubrtová duskova@szu.cz sperling@szu.cz Oddělení pro hodnocení expozice chemickým látkám
Úvod k biochemickému. mu praktiku. Vladimíra Kvasnicová
 Úvod k biochemickému mu praktiku Vladimíra Kvasnicová organizace praktik pravidla bezpečné práce v laboratoři laboratorní vybavení práce s automatickou pipetou návody: viz. aplikace Výuka automatická pipeta
Úvod k biochemickému mu praktiku Vladimíra Kvasnicová organizace praktik pravidla bezpečné práce v laboratoři laboratorní vybavení práce s automatickou pipetou návody: viz. aplikace Výuka automatická pipeta
Víme, co vám nabízíme
 PDF vygenerováno: 30.12.2016 5:20: Katalog / Laboratorní pomůcky / ace / Nástavce a filtrační špičky na injekční stříkačky Nástavec filtrační na injekční stříkačky MACHEREY-NAGEL Jednoúčelové nástavce
PDF vygenerováno: 30.12.2016 5:20: Katalog / Laboratorní pomůcky / ace / Nástavce a filtrační špičky na injekční stříkačky Nástavec filtrační na injekční stříkačky MACHEREY-NAGEL Jednoúčelové nástavce
CHEMIE - Úvod do organické chemie
 Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Problémy v kapalinové chromatografii. Troubleshooting
 Problémy v kapalinové chromatografii Troubleshooting Problémy v HPLC Většinu problémů, které se vyskytují při separaci látek na chromatografické koloně můžeme vyčíst již z pouhého průběhu základní linie,
Problémy v kapalinové chromatografii Troubleshooting Problémy v HPLC Většinu problémů, které se vyskytují při separaci látek na chromatografické koloně můžeme vyčíst již z pouhého průběhu základní linie,
VYUŽITÍ TEPELNÉHO ZMLŽOVAČE V AAS
 1 VYUŽITÍ TEPELNÉHO ZMLŽOVAČE V AAS JAN KNÁPEK Katedra analytické chemie, Přírodovědecká fakulta MU, Kotlářská 2, Brno 611 37 Obsah 1. Úvod 2. Tepelný zmlžovač 2.1 Princip 2.2 Konstrukce 2.3 Optimalizace
1 VYUŽITÍ TEPELNÉHO ZMLŽOVAČE V AAS JAN KNÁPEK Katedra analytické chemie, Přírodovědecká fakulta MU, Kotlářská 2, Brno 611 37 Obsah 1. Úvod 2. Tepelný zmlžovač 2.1 Princip 2.2 Konstrukce 2.3 Optimalizace
POROVNÁNÍ ÚČINNOSTI SRÁŽENÍ REAKTIVNÍCH AZOBARVIV POUŽITÍM IONTOVÉ KAPALINY A NÁSLEDNÁ FLOKULACE AZOBARVIV S Al 2 (SO 4 ) 3.18H 2 O S ÚPRAVOU ph
 POROVNÁNÍ ÚČINNOSTI SRÁŽENÍ REAKTIVNÍCH AZOBARVIV POUŽITÍM IONTOVÉ KAPALINY A NÁSLEDNÁ FLOKULACE AZOBARVIV S Al 2 (SO 4 ) 3.18H 2 O S ÚPRAVOU ph Ing. Jana Martinková Ing. Tomáš Weidlich, Ph.D. prof. Ing.
POROVNÁNÍ ÚČINNOSTI SRÁŽENÍ REAKTIVNÍCH AZOBARVIV POUŽITÍM IONTOVÉ KAPALINY A NÁSLEDNÁ FLOKULACE AZOBARVIV S Al 2 (SO 4 ) 3.18H 2 O S ÚPRAVOU ph Ing. Jana Martinková Ing. Tomáš Weidlich, Ph.D. prof. Ing.
Metody separace. přírodních látek
 Metody separace přírodních látek (5) Chromatografie; základní definice a klasifikace ruzných metod; kapalinová chromatografie, plynová chromatografie, přístrojová technika. Chromatografie «F(+)d» 1897
Metody separace přírodních látek (5) Chromatografie; základní definice a klasifikace ruzných metod; kapalinová chromatografie, plynová chromatografie, přístrojová technika. Chromatografie «F(+)d» 1897
Izolace nukleových kyselin
 Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
Gelová permeační chromatografie
 Gelová permeační chromatografie (Gel Permeation Chromatography - GPC) - separační a čisticí metoda - umožňuje separaci skupin sloučenin s podobnou molekulovou hmotností (frakcionace) - analyty jsou po
Gelová permeační chromatografie (Gel Permeation Chromatography - GPC) - separační a čisticí metoda - umožňuje separaci skupin sloučenin s podobnou molekulovou hmotností (frakcionace) - analyty jsou po
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253
 Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 23 Preparativní chromatografie je používána pro separaci látek, které jsou určeny pro další zpracování. Množství získávané
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 23 Preparativní chromatografie je používána pro separaci látek, které jsou určeny pro další zpracování. Množství získávané
