MENDELU PŘÍPRAVNÝ KURZ. Chemie anorganická a analytická. Mgr. Jiří Vlček, Ph.D.
|
|
|
- Radomír Štěpánek
- před 8 lety
- Počet zobrazení:
Transkript
1 MENDELU PŘÍPRAVNÝ KURZ Chemie anorganická a analytická Mgr. Jiří Vlček, Ph.D. Inovace předmětu probíhá v rámci projektu CZ.1.07/2.2.00/ Inovace studijních programů AF a ZF MENDELU směřující k vytvoření mezioborové integrace. Projekt je spolufinancován z Evropského sociálního fondu a státního rozpočtu České republiky
2 Obsah 1. Základní pojmy o atomu Atom Částice v atomu Atomové jádro Obal atomu Prvek Periodická soustava prvků Názvosloví Oxidační číslo Název sloučeniny Vzorec sloučeniny Tvorba vzorců a názvů sloučenin Sloučeniny teoreticky odvozené od sloučenin vodíku a nekovu Veličiny a jednotky SI, násobky jednotek Látkové množství, molární hmotnost Rovnice, vyrovnání rovnic
3 1. Základní pojmy o atomu 1.1. Atom - nejmenší částice prvku - chemickými procesy nelze dále dělit - vykazuje všechny chemické vlastnosti prvku - v základním stavu elektroneutrální - velikost atomu 1 H m 112 Cn m - hmotnost atomu 1 H 1, kg 112 Cn 4, kg - dvě základní části jádro obal - tvořen třemi částicemi proton neutron elektron Obrázek 1: Znázornění velikosti atomu 3
4 Částice v atomu Proton Neutron Elektron - klidová hmotnost 1, kg - kladný náboj + 1, C - značí se 1 1p nebo p + - klidová hmotnost 1, kg - bez elektrického náboje - značí se 1 0n nebo n 0 - klidová hmotnost 9, kg - záporný náboj - 1, C - značí se e - Obrázek 2: Srovnání hmotnosti protonu a elektronu Elementární náboj = 1, C - náboj elektronu a náboj protonu jsou velikostně stejné, liší se pouze znaménkem - každý větší náboj je celistvým násobkem elementárního náboje 4
5 Atomové jádro - kladně nabité - tvořeno protony a neutrony - protony a neutrony se souhrnně nazývají nukleony - prostorově zabírá velice malou část atomu průměr krát menší než průměr atomu - soustřeďuje téměř veškerou hmotnost atomu = obrovská hustota - protony a neutrony poutány silnými jadernými silami - druh atomu je určen počtem protonů v jádře protonové (atomové) číslo určuje pořadí prvku v periodické tabulce Obrázek 3: Porovnání velikosti atomu (Koloseum) a jeho jádra (hořčičné semínko) foto: Google maps 5
6 Obal atomu - záporně nabitý - tvořen elektrony - zabírá takřka celý prostor atomu - hmotnost obalu je ve srovnání s hmotností jádra zanedbatelná - v základním stavu atomu je záporný náboj obalu velikostně stejný jako kladný náboj jádra = stejný počet elektronů a protonů - nejvyšší vrstva (nejdále od jádra) obsahuje elektrony podílející se na vzniku chemické vazby = valenční elektrony - struktura valenční vrstvy určuje chemické vlastnosti prvku 1.2. Prvek - látka skládající se z atomů se stejným počtem protonů v jádře - každý prvek má český a latinský název - pro zkrácený zápis se používá značka prvku Protonové ( atomové ) číslo Z - počet protonů v jádře atomu - počet elektronů v obalu vzhledem k celkové elektroneutralitě atomu - totožné s pořadovým číslem prvku v periodické soustavě Neutronové číslo N - počet neutronů v jádře Nukleonové číslo A -součet počtu neutronů a protonů v jádře A = N + Z 6
7 2. Periodická soustava prvků Periodický zákon: Definice: Vlastnosti prvků a jejich sloučenin jsou periodickou funkcí jejich atomových hmotností. (D. I. Mendělejev; 1869) - nyní se prvky řadí do tabulky podle narůstajícího atomového čísla - periodicita ve výstavbě valenčních elektronových vrstev Obrázek 4: Dlouhá Periodická tabulka prvků - svislé řady se nazývají skupiny - ve skupině zákonité změny vlastností, ne jen jejich prosté opakování = možnost předpovědi vlastností zatím neznámých prvků - vodorovné řady jsou periody - nejčastěji se z praktických důvodů používá zkrácená tabulka, kdy jsou řady f prvků vyjmuty pod tabulku Obrázek 5: Krátká Periodická tabulka prvků 7
8 3. Názvosloví - v českém názvosloví chemických sloučenin se využívá tvorby názvů sloučenin pomocí předpon a koncovek - základním parametrem, na kterém je založeno anorganické názvosloví, je oxidační číslo 3.1. Oxidační číslo = elektrický náboj, který by byl na atomu prvku přítomen, kdyby elektrony každé vazby z prvku vycházející, byly přiděleny elektronegativnějšímu z obou vazebných partnerů - jde o formální pojem, oxidační číslo nemusí odpovídat skutečnému uspořádání elektronů v molekule - oxidační čísla se zapisují římskými číslicemi vpravo nahoře u značky prvku - kladná oxidační čísla nabývají hodnot I až VIII, pro jednotlivé prvky je jeho maximální hodnota shodná s číslem skupiny (IUPAC 1970) ve které se nacházejí - při označení skupin 1-18, je ve skupinách 8,9,10 maximální oxidační číslo VIII, u skupin 11 až 18 se pro zjištění maximálního oxidačního čísla musí od čísla skupiny odečíst 10 - vodík má ve většině sloučenin oxidační číslo I - kyslík je nejčastěji ve sloučeninách s oxidačním číslem -II - záporné oxidační číslo se pohybuje v rozmezí od -I do -IV - atomy, atomy v molekulách prvků mají oxidační číslo 0 - součet všech oxidačních čísel všech atomů v elektroneutrální molekule je roven nule, u iontu odpovídá jeho náboji - kladným oxidačním číslům je v anorganickém názvosloví přiřazena koncovka 3.2. Název sloučeniny - název sloučeniny se skládá z podstatného a přídavného jména - podstatné jméno se týká elektronegativnější části molekuly a udává druh sloučeniny (oxid, uhličitan) - přídavné jméno popisuje elektropozitivní část molekuly, obsahuje název prvku od kterého je sloučenina odvozena 8
9 Tabulka 1: Oxidační čísla a jejich koncovky oxidační číslo koncovka kationtu kyselin aniontů I -ný -ná -nan II -natý -natá -natan III -itý -itá -itan IV -ičitý -ičitá -ičitan V -ečný, -ičný -ečná, -ičná -ečnan, -ičnan VI -ový -ová -an VII -istý -istá -istan VIII -ičelý -ičelá -ičelan 3.3. Vzorec sloučeniny - jednoduše a názorně charakterizuje sloučeninu - využitím značek prvků je uveden počet a druh atomů tvořících molekulu látky - vzorce se využívají hlavně v zápisu chemických dějů pomocí rovnic - jako první se do vzorce zapisuje elektropozitivní část, pak část elektronegativní 3.4. Tvorba vzorců a názvů sloučenin Sloučeniny teoreticky odvozené od sloučenin vodíku a nekovu voda H 2 O sulfan (sirovodík) H 2 S halogenovodíky HF, HCl, HBr, HI - koncovka -id - oxidační číslo nekovu ve sloučeninách je záporné = snaha o dosažení ideální elektronové konfigurace v periodické tabulce nejbližšího vzácného plynu 9
10 Oxidy - oxidační číslo kyslíku v oxidech má hodnotu -II - sloučeniny teoreticky odvozené od vody náhradou vodíků jiným prvkem Obrázek 6: Oxidační číslo oxidů - název se skládá z podstatného jména oxid a přídavného jména, vytvořeného z názvu prvku s kyslíkem sloučeného a koncovky pro dané oxidační číslo Tvorba vzorce z názvu: Př 1. oxid hlinitý - zapíšeme značky sloučených prvků v opačném pořadí než v názvu, první kationt Al O - doplníme oxidační čísla Al III O -II - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučeny dva atomy hliníku s třemi atomy kyslíku 2. III + 3. (-II) = 0 - doplníme počty atomů do vzorce Al 2 O 3 - lze použít i křížového pravidla 10
11 Př 2. oxid sodný - zapíšeme značky sloučených prvků Na O - doplníme oxidační čísla Na I O -II - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučeny dva atomy sodíku s jedním atomem kyslíku 2. I + 1. (-II) = 0 - jedničku do vzorce nepíšeme - doplníme počty atomů do vzorce Na 2 O Př 3. oxid siřičitý - zapíšeme značky sloučených prvků S O - doplníme oxidační čísla S IV O -II - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučen jeden atom síry s dvěma atomy kyslíku 1. IV + 2. (-II) = 0 - jedničku do vzorce nepíšeme - doplníme počty atomů do vzorce SO 2 Tvorba názvu ze vzorce: Z -II Př 1. P 2 O 5 P 2 O 5 - za pomoci pravidla nulového součtu oxidačních čísel určíme oxidační číslo elektropozitivního prvku 2. Z + 5. (-II) = 0 Z = V - přiřadíme koncovku oxidačního čísla k názvu prvku oxid fosforečný Př 2. CaO Ca Z O -II - za pomoci pravidla nulového součtu oxidačních čísel určíme oxidační číslo elektropozitivního prvku 1. Z + 1. (-II) = 0 Z = II - přiřadíme koncovku oxidačního čísla k názvu prvku oxid vápenatý 11
12 Hydroxidy - obsahují skupinu OH -I - sloučeniny teoreticky odvozené od vody, náhradou jednoho vodíku jiným atomem - OH skupinu bereme při vyčíslování jako celek s oxidačním číslem -I, nemůžeme měnit počet kyslíků nebo vodíků samostatně - název se skládá z podstatného jména hydroxid a přídavného jména, vytvořeného z názvu prvku s OH skupinou sloučeného a koncovky pro dané oxidační číslo Tvorba vzorce z názvu: Př 1. hydroxid vápenatý - zapíšeme značky sloučených prvků Ca OH - doplníme oxidační čísla Ca II OH -I - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučen jeden atom vápníku se dvěma OH skupinami 1. II + 2. (-I) = 0 - jedničku do vzorce nepíšeme - pokud je v molekule více OH skupin, ve vzorci se tato skupina napíše do závorky - doplníme počty atomů do vzorce Ca(OH) 2 Př 2. hydroxid draselný - zapíšeme značky sloučených prvků K OH - doplníme oxidační čísla K I OH -I - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučen jeden atom draslíku s jednou OH skupinou 1. I + 1. (-I) = 0 - jedničku do vzorce nepíšeme - doplníme počty atomů do vzorce KOH Tvorba názvu ze vzorce: Př 1. Al(OH) 3 Al Z (OH) 3 -I - za pomoci pravidla nulového součtu oxidačních čísel určíme oxidační číslo elektropozitivního prvku 1. Z + 3. (-I) = 0 Z = III - přiřadíme koncovku oxidačního čísla k názvu prvku hydroxid hlinitý 12
13 Př 2. Ba(OH) 2 Ba Z (OH) 2 -I - za pomoci pravidla nulového součtu oxidačních čísel určíme oxidační číslo elektropozitivního prvku 1. Z + 2. (-I) = 0 Z = II - přiřadíme koncovku oxidačního čísla k názvu prvku hydroxid barnatý Sulfidy - oxidační číslo síry v sulfidech má hodnotu -II - sloučeniny teoreticky odvozené od sulfanu (sirovodíku) náhradou vodíků jiným prvkem Obrázek 7: Oxidační číslo sulfidů - název se skládá z podstatného jména sulfid a přídavného jména, vytvořeného z názvu prvku se sírou sloučeného a koncovky pro dané oxidační číslo - tvorba vzorců a názvů je analogická s tvorbou názvů a vzorců oxidů, ve vzorcích je místo značky kyslíku značka síry, v názvech je pojem oxid nahrazen pojmem sulfid Hydrogensulfidy - obsahují skupinu HS -I - sloučeniny teoreticky odvozené od sulfanu náhradou jednoho vodíku jiným atomem - HS skupinu bereme při vyčíslování jako celek s oxidačním číslem -I, nemůžeme měnit počet atomů síry nebo vodíku samostatně 13
14 - název se skládá z podstatného jména hydrogensulfid a přídavného jména, vytvořeného z názvu prvku s SH skupinou sloučeného a koncovky pro dané oxidační číslo - tvorba vzorců a názvů je analogická s tvorbou názvů a vzorců hydroxidů, ve vzorcích je místo značky kyslíku značka síry, v názvech je pojem hydroxid nahrazen pojmem hydrogensulfid Halogenidy - oxidační číslo halogenů v halogenidech má hodnotu -I - sloučeniny teoreticky odvozené od jednotlivých halogenovodíků, náhradou vodíků jiným prvkem nebo skupinou Obrázek 8: Oxidační číslo halogenidů - název se skládá z podstatného jména fluorid, chlorid, bromid nebo jodid a přídavného jména, vytvořeného z názvu kovu s daným halogenidem sloučeného a koncovky pro dané oxidační číslo Tvorba vzorce z názvu: Př 1. chlorid železitý - zapíšeme značky sloučených prvků Fe Cl - doplníme oxidační čísla Fe III Cl -I - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučen jeden atom železa s třemi atomy chloru 1. III + 3. (-I) = 0 - doplníme počty atomů do vzorce FeCl 3 14
15 Př 2. bromid lithný - zapíšeme značky sloučených prvků Li Br - doplníme oxidační čísla Li I Br -I - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučen jeden atom lithia s jedním atomem kyslíku 1. I + 1. (-I) = 0 - jedničku do vzorce nepíšeme - doplníme počty atomů do vzorce LiBr Tvorba názvu ze vzorce: Př 1. ZnI 2 Zn Z I 2 -I - za pomoci pravidla nulového součtu oxidačních čísel, určíme oxidační číslo elektropozitivního prvku 1. Z + 2. (-I) = 0 Z = II - přiřadíme koncovku oxidačního čísla k názvu prvku jodid zinečnatý Kyseliny - obsahují vždy vodík s oxidačním číslem I - počet odštěpitelných vodíků určuje sytnost kyseliny - kyseliny dělíme na dvě skupiny bezkyslíkaté kyslíkaté Bezkyslíkaté kyseliny - binární sloučeniny složené z vodíku a nekovového prvku - název tvoří podstatné jméno kyselina a přídavné jméno, složené z názvu rozpuštěného plynu a koncovky -ová HF kyselina fluorovodíková HCl kyselina chlorovodíková HBr kyselina bromovodíková HI kyselina jodovodíková H 2 S kyselina sulfanová (sirovodíková) Kyslíkaté kyseliny (oxokyseliny) - mimo vodíku s oxidačním číslem I, obsahuje molekula kyslík s oxidačním číslem -II a centrální atom s různým oxidačním číslem - teoreticky vznikají reakcí oxidu centrálního atomu s vodou - vodík je na centrální atom připojen vazbou přes kyslík 15
16 - název tvoří podstatné jméno kyselina a přídavné jméno, charakterizující centrální atom a jeho oxidační číslo - pro jednoznačné definování kyseliny je někdy nutné použít předponu určující počet vodíků v molekule a předponu hydrogen- - předpona mono se v názvu většinou neuvádí Tabulka 2: Předpony násobků počet předpona mono di tri tetra penta hexa hepta okta nona deka - sumární vzorec kyslíkaté kyseliny tvoří značky prvků v pořadí vodík, centrální atom a kyslík Př. - název: kyselina trihydrogenfosforečná - sumární vzorec: H 3 PO 4 - strukturní vzorec: Tvorba vzorce z názvu: Př 1. kyselina chloristá - zapíšeme značky sloučených prvků H Cl O - doplníme oxidační čísla H I Cl VII O X -II - v molekulách oxokyselin kladné oxidační číslo vodíku a centrálního atomu vyvažuje kyslík s oxidačním číslem -II, součet kladných oxidačních čísel musí být proto sudé číslo - tato podmínka je splněna I + VII = VIII - počet kyslíkových atomů v molekule určíme za pomoci pravidla nulového součtu oxidačních čísel I + VII + X. (-II) = 0 - doplníme počty atomů do vzorce HClO 4 Př 2. kyselina uhličitá - zapíšeme značky sloučených prvků H C O - doplníme oxidační čísla H I C IV O X -II - podmínka sudého součtu kladných oxidačních čísel není splněna - v tomto případě přidáme do vzorce kyseliny jeden vodík H 2 I C IV O X -II 16
17 - součet kladných oxidačních čísel je nyní sudý (2. I) + IV = VI - počet kyslíkových atomů v molekule určíme za pomoci pravidla nulového součtu oxidačních čísel 2. I + IV + X. (-II) = 0 - doplníme počty atomů do vzorce H 2 CO 3 Př 3. kyselina trihydrogenboritá - zapíšeme značky sloučených prvků H B O - doplníme oxidační čísla H I B III O -II - předpona udává počet vodíků v molekule H I 3 B III O -II - součet kladných oxidačních čísel je sudý (3. I) + III = VI - počet kyslíkových atomů v molekule určíme za pomoci pravidla nulového součtu oxidačních čísel 3. I + VII + X. (-II) = 0 - doplníme počty atomů do vzorce H 3 BO 3 Tvorba názvu ze vzorce: Př 1. H 2 SO 4 H I 2 S Z -II O 4 - za pomoci pravidla nulového součtu oxidačních čísel určíme oxidační číslo elektropozitivního prvku 2. I + Z + 4. (-II) = 0 Z = VI - přiřadíme koncovku oxidačního čísla k názvu centrálního prvku kyselina sírová Př 2. HNO 2 H I N Z -II O 2 - za pomoci pravidla nulového součtu oxidačních čísel určíme oxidační číslo elektropozitivního prvku 1. I + Z + 2. (-II) = 0 Z = III - přiřadíme koncovku oxidačního čísla k názvu centrálního prvku kyselina dusitá 17
18 Soli oxokyselin - vznikají odštěpením jednoho nebo více vodíkových kationtů od molekuly kyseliny a jeho (jejich) náhradou kationtem kovu, nebo amonným kationtem - název tvoří podstatné jméno odvozené z názvu kyseliny, ze které sůl vznikla a koncovky oxidačního čísla jejího centrálního atomu a přídavné jméno, charakterizující kationt a jeho oxidační číslo - v případě že, se neodštěpily všechny vodíky, obsahuje název aniontu předponu určující počet neodštěpených vodíků a předponu hydrogen- - skupinu aniontu bereme jako celek s oxidačním číslem, které je shodné s počten odtržených vodíků, při vyčíslování nemůžeme měnit počet kteréhokoliv z prvků Př. - sůl kyseliny trihydrogenfosforečné - odštěpení vodíkového kationtu - nahrazení vodíku atomem draslíku s oxidačním číslem I = draselný - jeden vodík byl nahrazen, dva zůstávají v molekule = předpona dihydrogen- - sůl kyseliny fosforečné = fosforečnan Tvorba vzorce z názvu: dihydrogenfosforečnan draselný Př 1. siřičitan sodný - jedná se o sůl kyseliny siřičité - podle postupu v předcházející kapitole odvodíme vzorec kyseliny H 2 SO 3 18
19 - název aniontu siřičitan neobsahuje předponu hydrogen-, to znamená že byly odštěpeny oba vodíky = aniont má oxidační číslo -II SO 3 -II - vodík byl nahrazen sodíkem s oxidačním číslem I Na I SO 3 -II - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučeny dva atomy sodíku s jedním siřičitanovým aniontem 2. I + 1. (-II) = 0 - jedničku do vzorce nepíšeme - doplníme počty do vzorce Na 2 SO 3 Př 2. dusičnan měďnatý - jedná se o sůl kyseliny dusičné - podle postupu v předcházející kapitole odvodíme vzorec kyseliny HNO 3 - název aniontu dusičnan neobsahuje předponu hydrogen-, to znamená byly odštěpeny všechny vodíky = aniont má oxidační číslo -I NO 3 -I - vodík byl nahrazen mědí s oxidačním číslem II Cu II NO 3 -I - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučen jeden atom mědi s dvěma dusičnanovými anionty 1. II + 2. (-I) = 0 - jedničku do vzorce nepíšeme - skupina aniontu se napíše do závorky - doplníme počty do vzorce Cu(NO 3 ) 2 Př 3. hydrogenfosforečnan železitý - jedná se o sůl kyseliny trihydrogenfosforečné - podle postupu v předcházející kapitole odvodíme vzorec kyseliny H 3 PO 4 - název aniontu obsahuje předponu hydrogen-, to znamená byly odštěpeny dva ze tří vodíků = aniont má oxidační číslo -II HPO 4 -II - vodíky byly nahrazeny železem s oxidačním číslem III Fe III HPO 4 -II 19
20 - pro splnění nulového celkového součtu oxidačních čísel, musí být sloučeny dva atomy železa s třemi hydrogenfosforečnanovými anionty 2. III + 3. (-II) = 0 - skupina aniontu se napíše do závorky - doplníme počty do vzorce Fe 2 (HPO 4 ) 3 Tvorba názvu ze vzorce: Př 1. K 2 CO 3 K 2 Z CO 3 - jedná se o sůl kyseliny uhličité H 2 CO 3 = uhličitan - byly odtrženy dva vodíky, oxidační číslo skupiny je -II - za pomoci pravidla nulového součtu oxidačních čísel určíme oxidační číslo elektropozitivního prvku 2. Z + 1. (-II) = 0 Z = I - přiřadíme koncovku oxidačního čísla k názvu centrálního prvku uhličitan draselný 20
21 4. Veličiny a jednotky SI, násobky jednotek Tabulka 3: Základní veličiny a jednotky SI veličina jednotka název značka název značka délka l metr m hmotnost m kilogram kg čas t sekunda s elektrický proud I ampér A teplota T kelvin K svítivost I kandela cd látkové množství n mol mol Tabulka 4: Násobky jednotek předpona značka násobek exa E peta P tera T giga G 10 9 mega M 10 6 kilo k 10 3 hekto h 10 2 deka da 10 1 deci d 10-1 centi c 10-2 mili m 10-3 mikro µ 10-6 nano n 10-9 piko p femto f atto a Objem - v chemii často používanou veličinou, značka V - patří mezi odvozené veličiny SI - hlavní jednotka je m 3, ta je ale pro použití v chemii příliš velká - používá se nejčastěji litr(l) nebo mililitr (ml) - 1 l = 1 dm 3 ; 1 ml = 1cm 3 1 l = 1000 ml 21
22 5. Látkové množství, molární hmotnost Látkové množství - základní veličina soustavy SI - značíme n - jednotka je mol Definice : Mol je takové látkové množství, které obsahuje tolik základních částic, kolik atomů obsahuje 12 g uhlíku 12 C. - počet atomů ve 12 g uhlíku 12 C vyjadřuje Avogadrova konstanta N A = 6, mol -1 - odpočítáme - li tento počet atomů nebo molekul, máme daného prvku nebo látky právě jeden mol - pokud bychom toto množství atomů nebo molekul zvážili, získali bychom atomovou nebo molekulovou molární hmotnost. - molární hmotnost molekuly, získáme jako součet atomových hmotností atomů tvořících molekulu - jednotkou molární hmotnosti je g.mol -1 M(B) = m B / n(b) [g.mol -1 ] 22
23 6. Rovnice, vyrovnání rovnic - stručná, jasná charakteristika chemické reakce pomocí chemických vzorců látek a stechiometrických koeficientů - popis chemické reakce kvantitativní i kvalitativní - na levou stranu se zapisují výchozí látky reakce (reaktanty), na pravou produkty - obě strany rovnice se spojují šipkou ve směru od výchozích látek k produktům - rovnovážná reakce je spojena dvěma šipkami opačného směru nad sebou - zákon zachování hmotnosti se v rovnici projeví stejným počtem atomů jednoho druhu na obou stranách rovnice - u redoxních rovnic musí souhlasit i počet vyměňovaných elektronů na obou stranách rovnice - v rovnicích iontových je součet náboje na levé a pravé straně stejný - rovnosti počtu atomů, vyměňovaných elektronů a sumy náboje na obou stranách rovnice dosáhneme přidělením správných stechiometrických koeficientů k jednotlivým vzorcům reagujících látek = vyrovnání rovnice - nikdy neupravujeme počty atomů v jednotlivých vzorcích reagujících látek - poměr stechiometrických koeficientů vyjadřuje poměr látkových množství, v jakém dané látky vzájemně reagují - stechiometrický koeficient 1 se do rovnice nezapisuje - vyrovnávání začínáme některým z kationtů, nebo centrálním atomem složitého iontu, atomy kyslíku a vodíku dopočítáváme jako poslední Jednoduché reakce, při kterých dochází k výměně kationtů, nebo vytěsnění kationtu prvkem (snadné určení produktů) Př. 1 reakce chloridu vápenatého s dusičnanem stříbrným - reakcí si látky vymění své kationty, produkty reakce budou dusičnan vápenatý a chlorid stříbrný - do rovnice zapíšeme vzorce reaktantů a produktů CaCl 2 + AgNO 3 Ca(NO 3 ) 2 + AgCl - dusík je na pravé straně dvakrát, proto před vzorec AgNO 3 doplníme stechiometrický koeficient 2 CaCl AgNO 3 Ca(NO 3 ) 2 + AgCl 23
24 - nyní nesouhlasí atomy stříbra, před AgCl doplníme stechiometrický koeficient 2 CaCl AgNO 3 Ca(NO 3 ) AgCl - porovnáme počet všech ostatních atomů (Ca - 1, Cl - 2 a O -6) na obou stranách rovnice - souhlasí, rovnice je vyrovnána Př. 2 reakce kyseliny sírové s hydroxidem hlinitým - reakcí si látky vymění své kationty, produkty reakce budou síran hlinitý a voda - do rovnice zapíšeme vzorce reaktantů a produktů H 2 SO 4 + Al(OH) 3 Al 2 (SO 4 ) 3 + H 2 O - síra je na pravé straně třikrát, proto před vzorec H 2 SO 4 doplníme stechiometrický koeficient 3 3 H 2 SO 4 + Al(OH) 3 Al 2 (SO 4 ) 3 + H 2 O - nesouhlasí také atomy hliníku, před Al(OH) 3 doplníme stechiometrický koeficient 2 3 H 2 SO Al(OH) 3 Al 2 (SO 4 ) 3 + H 2 O - dále porovnáme počet vodíků, vlevo 12, vpravo 2, před H 2 O napíšeme 6 3 H 2 SO Al(OH) 3 Al 2 (SO 4 ) H 2 O - počet kyslíků je nyní na obou stranách 18 - rovnice je vyrovnána Př. 3 reakce kyseliny chlorovodíkové se zinkem - reakcí je z kyseliny vytěsněn plynný vodík a vzniká chlorid zinečnatý - do rovnice zapíšeme vzorce reaktantů a produktů HCl + Zn ZnCl 2 + H 2 - chlor je na pravé straně dvakrát, proto před vzorec HCl doplníme stechiometrický koeficient 2 2 HCl + Zn ZnCl 2 + H 2 - porovnáme počet vodíků, vlevo i vpravo 2 - rovnice je vyrovnána 24
25 Složité reakce vyžadují větší zkušenosti k určení produktů reakce, proto se dále zaměříme jen na jejich vyrovnání Př. 1 oxidačně redukční reakce manganistanu s železnatým kationtem v kyselém prostředí - MnO 4 + Fe 2+ + H + Mn 2+ + Fe 3+ + H 2 O - mimo počtu atomů musíme u této rovnici sledovat počet vyměňovaných elektronů a náboj jednotlivých látek - doplníme oxidační čísla všech prvků a zjistíme, u kterých došlo reakcí ke změně Mn VII O -II Fe 2+ + H + Mn 2+ + Fe 3+ + H I 2O -II - zapíšeme poloreakce oxidace a redukce Mn VII + 5 e - Mn 2+ Fe 2+ - e - Fe 3+ - počet vyměňovaných elektronů nesouhlasí, pro redukci jednoho atomu Mn je potřeba pět atomů Fe Mn VII + 5 e - Mn 2+ 5 Fe e - 5 Fe 3+ - doplníme zjištěné stechiometrické koeficienty do rovnice - MnO Fe 2+ + H + Mn Fe 3+ + H 2 O - kyslíky jsou na levé straně čtyři a vpravo jeden, proto před vzorec H 2 O doplníme stechiometrický koeficient 4 - MnO Fe 2+ + H + Mn Fe H 2 O - upravíme počet vodíků, doplněním stechiometrického koeficientu 8 k H + - MnO Fe H + Mn Fe H 2 O - provedeme kontrolu velikosti náboje, vlevo (1-) + 5 x (2+) + 8 x (1+) = (17+) a vpravo (2+) + 5 x (3+) = (17+) - souhlasí, rovnice je vyrovnána 25
Triviální Voda (H 2 O) Amoniak Soda. Systematické. Většina názvů se skládá ze 2 slov Výjimka: např. chlorovodík např. jodid draselný (KI)
 Názvosloví anorganických sloučenin České názvosloví je jednoznačné Názvosloví anorganických sloučenin Triviální Voda (H 2 O) Amoniak Soda Systematické Většina názvů se skládá ze 2 slov Výjimka: např. chlorovodík
Názvosloví anorganických sloučenin České názvosloví je jednoznačné Názvosloví anorganických sloučenin Triviální Voda (H 2 O) Amoniak Soda Systematické Většina názvů se skládá ze 2 slov Výjimka: např. chlorovodík
Základy chemického názvosloví
 Základy chemického názvosloví Oxidační číslo O. č. je počet elementárních nábojů částice Elementární náboj je nejmenší možný Hodnota 1,602. 10-19 C e - má jeden záporný elementární náboj P + má jeden kladný
Základy chemického názvosloví Oxidační číslo O. č. je počet elementárních nábojů částice Elementární náboj je nejmenší možný Hodnota 1,602. 10-19 C e - má jeden záporný elementární náboj P + má jeden kladný
Přehled zakončení názvů anorganických sloučenin a iontů
 Hodnota kladného oxidačního čísla Přehled zakončení názvů anorganických sloučenin a iontů Zakončení příd. jména binární sl. hydroxidu soli kationtu Zakončení přídavného jména kyseliny jejího aniontu Zakončení
Hodnota kladného oxidačního čísla Přehled zakončení názvů anorganických sloučenin a iontů Zakončení příd. jména binární sl. hydroxidu soli kationtu Zakončení přídavného jména kyseliny jejího aniontu Zakončení
NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN
 NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN univerzální jazyk chemiků ( abeceda; chem. vzorce ; chem. rovnice ) české názvosloví je jedno z nejdokonalejších na světě (prof. Emil Votoček) OXIDAČNÍ ČÍSLO = náboj,
NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN univerzální jazyk chemiků ( abeceda; chem. vzorce ; chem. rovnice ) české názvosloví je jedno z nejdokonalejších na světě (prof. Emil Votoček) OXIDAČNÍ ČÍSLO = náboj,
Kuchyňská sůl = chlorid sodný. Modrá skalice = síran měďnatý SO 4. Potaš = uhličitan draselný K 2 CO 3
 SOLI Kuchyňská sůl Modrá skalice Potaš Kuchyňská sůl = chlorid sodný Na Cl Modrá skalice = síran měďnatý Cu SO 4 Potaš = uhličitan draselný K 2 CO 3 Chemické názvosloví solí Soli = sloučeniny odvozené
SOLI Kuchyňská sůl Modrá skalice Potaš Kuchyňská sůl = chlorid sodný Na Cl Modrá skalice = síran měďnatý Cu SO 4 Potaš = uhličitan draselný K 2 CO 3 Chemické názvosloví solí Soli = sloučeniny odvozené
Oxidační číslo je rovno náboji, který by atom získal po p idělení všech vazebných elektronových párů atomům s větší elektronegativitou.
 NÁZVOSLOVÍ Oxidační číslo je rovno náboji, který by atom získal po p idělení všech vazebných elektronových párů atomům s větší elektronegativitou. -II +III -II +I O N O H Oxidační čísla se značí ímskými
NÁZVOSLOVÍ Oxidační číslo je rovno náboji, který by atom získal po p idělení všech vazebných elektronových párů atomům s větší elektronegativitou. -II +III -II +I O N O H Oxidační čísla se značí ímskými
II. Chemické názvosloví
 II. Chemické názvosloví 1. Oxidy jsou dvouprvkové sloučeniny kyslíku a jiného prvku. Názvy oxidů jsou dvouslovné. Tvoří je podstatné jméno oxid (postaru kysličník) a přídavné jméno utvořené od názvu prvku
II. Chemické názvosloví 1. Oxidy jsou dvouprvkové sloučeniny kyslíku a jiného prvku. Názvy oxidů jsou dvouslovné. Tvoří je podstatné jméno oxid (postaru kysličník) a přídavné jméno utvořené od názvu prvku
1) BEZKYSLÍKATÉ KYSELINY:
 KYSELINY Jsou to látky, které se ve vodě štěpí na kationty H + a anionty (radikály) kyseliny (např. Cl -, NO 3-, SO 4 2- ). 1) BEZKYSLÍKATÉ KYSELINY: (koncovka -vodíková) Kyselina fluorovod vodíková chlorovod
KYSELINY Jsou to látky, které se ve vodě štěpí na kationty H + a anionty (radikály) kyseliny (např. Cl -, NO 3-, SO 4 2- ). 1) BEZKYSLÍKATÉ KYSELINY: (koncovka -vodíková) Kyselina fluorovod vodíková chlorovod
Názvosloví anorganických sloučenin
 Názvosloví anorganických sloučenin Oxidační číslo udává náboj, kterým by byl atom prvku nabit, kdyby všechny elektrony vazeb v molekule patřily elektronegativnějším vazebným partnerům (atomům) udává náboj,
Názvosloví anorganických sloučenin Oxidační číslo udává náboj, kterým by byl atom prvku nabit, kdyby všechny elektrony vazeb v molekule patřily elektronegativnějším vazebným partnerům (atomům) udává náboj,
Chemické názvosloví anorganických sloučenin 2
 Chemické názvosloví anorganických sloučenin 2 Tříprvkové sloučeniny Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je. Mgr. Vlastimil Vaněk. Dostupné z Metodického portálu www.rvp.cz, ISSN:
Chemické názvosloví anorganických sloučenin 2 Tříprvkové sloučeniny Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je. Mgr. Vlastimil Vaněk. Dostupné z Metodického portálu www.rvp.cz, ISSN:
11. Anorganicke na zvoslovı
 11. Anorganicke na zvoslovı Základní veličinou, na níž je názvosloví anorganické chemie vybudováno, je oxidační číslo prvků. Jde o pojem formální a oxidační číslo velmi často neodpovídá skutečné elektronové
11. Anorganicke na zvoslovı Základní veličinou, na níž je názvosloví anorganické chemie vybudováno, je oxidační číslo prvků. Jde o pojem formální a oxidační číslo velmi často neodpovídá skutečné elektronové
Názvosloví. Názvosloví binárních sloučenin. Struktura prezentace: DOPORUČENÍ OXIDAČNÍ ČÍSLA. Při cvičení se vzorci a názvy si vždy pište
 Názvosloví Struktura prezentace: I. Názvosloví binárních sloučenin 4 Název sloučeniny 6 Vzorec 7 Názvy kationtů 9 Názvy aniontů 13 Vzorec z názvu 15 Název ze vzorce 18 II. Názvosloví hydroxidů, kyanidů
Názvosloví Struktura prezentace: I. Názvosloví binárních sloučenin 4 Název sloučeniny 6 Vzorec 7 Názvy kationtů 9 Názvy aniontů 13 Vzorec z názvu 15 Název ze vzorce 18 II. Názvosloví hydroxidů, kyanidů
Seminář z chemie. RNDr. Jana Fauknerová Matějčková místnost: 617,
 Seminář z chemie RNDr. Jana Fauknerová Matějčková místnost: 617, 615 email: Jana.Matejckova@lf3.cuni.cz Semináře týden datum název semináře či praktika 1. 30.9. Názvosloví v anorganické chemii 2. 11.10.
Seminář z chemie RNDr. Jana Fauknerová Matějčková místnost: 617, 615 email: Jana.Matejckova@lf3.cuni.cz Semináře týden datum název semináře či praktika 1. 30.9. Názvosloví v anorganické chemii 2. 11.10.
Střední průmyslová škola strojnická Vsetín Číslo projektu. Druh učebního materiálu prezentace Pravidla pro tvorbu vzorců a názvů kyselin a solí
 Název školy Střední průmyslová škola strojnická Vsetín Číslo projektu CZ.1.07/1.5.00/34.0483 Autor RNDr. Miroslava Pospíšilíková Název šablony III/2 Název DUMu 10.3 Názvosloví kyselin a solí Tematická
Název školy Střední průmyslová škola strojnická Vsetín Číslo projektu CZ.1.07/1.5.00/34.0483 Autor RNDr. Miroslava Pospíšilíková Název šablony III/2 Název DUMu 10.3 Názvosloví kyselin a solí Tematická
Anorganické názvosloví
 Anorganické názvosloví Obr. č. 1: Emil Votoček Chemické názvosloví je univerzálním "jazykem chemiků", umělý jazyk s cílem vytvořit každé sloučeniny pokud možný jednoduchý a jednoznačný název. Chemické
Anorganické názvosloví Obr. č. 1: Emil Votoček Chemické názvosloví je univerzálním "jazykem chemiků", umělý jazyk s cílem vytvořit každé sloučeniny pokud možný jednoduchý a jednoznačný název. Chemické
název soli tvoří podstatné a přídavné jméno
 OPAKOVÁNÍ název soli tvoří podstatné a přídavné jméno podstatné jméno charakterizuje anion soli a jeho náboj: chlorid Cl - přídavné jméno charakterizuje kation soli a jeho oxidační číslo: sodný Na + podstatné
OPAKOVÁNÍ název soli tvoří podstatné a přídavné jméno podstatné jméno charakterizuje anion soli a jeho náboj: chlorid Cl - přídavné jméno charakterizuje kation soli a jeho oxidační číslo: sodný Na + podstatné
VY_52_INOVACE_08_II.1.7_SOLI SOLI. PROCVIČOVÁNÍ a) PRACOVNÍ LIST
 VY_52_INOVACE_08_II.1.7_SOLI SOLI PROCVIČOVÁNÍ a) PRACOVNÍ LIST PRACOVNÍ LIST 1. Pojmenuj kyselinu a odděl aniontovou skupinu. H 2 SO 4 HClO 3 H 2 SO 3 H 2 CO 3 H 2 SiO 4 HCl HNO 3 H 2 Se HClO H 2 WO 4
VY_52_INOVACE_08_II.1.7_SOLI SOLI PROCVIČOVÁNÍ a) PRACOVNÍ LIST PRACOVNÍ LIST 1. Pojmenuj kyselinu a odděl aniontovou skupinu. H 2 SO 4 HClO 3 H 2 SO 3 H 2 CO 3 H 2 SiO 4 HCl HNO 3 H 2 Se HClO H 2 WO 4
Názvosloví anorganických sloučenin
 Chemické názvosloví Chemické prvky jsou látky složené z atomů o stejném protonovém čísle (počet protonů v jádře atomu. Každému prvku přísluší určitý mezinárodní název a od něho odvozený symbol (značka).
Chemické názvosloví Chemické prvky jsou látky složené z atomů o stejném protonovém čísle (počet protonů v jádře atomu. Každému prvku přísluší určitý mezinárodní název a od něho odvozený symbol (značka).
1H 1s. 8O 1s 2s 2p - - - - - - H O H
 OXIDAČNÍ ČÍSLO 1H 1s 8O 1s 2s 2p 1H 1s - - - - + - - + - - + - - H O H +I -II +I H O H - - - - Elektronegativita: Oxidační číslo vodíku: H +I Oxidační číslo kyslíku: O -II Platí téměř ve všech sloučeninách.
OXIDAČNÍ ČÍSLO 1H 1s 8O 1s 2s 2p 1H 1s - - - - + - - + - - + - - H O H +I -II +I H O H - - - - Elektronegativita: Oxidační číslo vodíku: H +I Oxidační číslo kyslíku: O -II Platí téměř ve všech sloučeninách.
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T3-11 Téma: Soli Střední škola ok: 2012 2013 Varianta: A Soli Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník SOLI sůl je sloučenina, která se skládá z iontu kovu a
DUM Základy přírodních věd DUM III/2-T3-11 Téma: Soli Střední škola ok: 2012 2013 Varianta: A Soli Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník SOLI sůl je sloučenina, která se skládá z iontu kovu a
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/
 Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT- PZC 2/9 Procvičování názvosloví v
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT- PZC 2/9 Procvičování názvosloví v
U Ústav procesní a zpracovatelské techniky FS ČVUT. Názvosloví solí kyslíkatých kyselin
 (oxokyselin) Obecný vzorec: K m A n K - vzorec kationtu A - vzorec aniontu m, n - indexy - počty iontů - přirozená čísla Pozn.1 - Indexy m, n rovné 1 se nepíší. Pozn.2 - Jsou -li oba indexy m, n dělitelné
(oxokyselin) Obecný vzorec: K m A n K - vzorec kationtu A - vzorec aniontu m, n - indexy - počty iontů - přirozená čísla Pozn.1 - Indexy m, n rovné 1 se nepíší. Pozn.2 - Jsou -li oba indexy m, n dělitelné
I. NÁZVOSLOVN ZVOSLOVÍ
 I. NÁZVOSLOVN ZVOSLOVÍ PRVKY: Název prvku tvoří 1 aža 2 písmenovp smenová zkratka, 2. písmeno p je malé. Názvy jsou v PSP (periodické soustavě prvků). Př.: kobalt je Co, ne CO Pozn.: PSP je nejdůle ležitější
I. NÁZVOSLOVN ZVOSLOVÍ PRVKY: Název prvku tvoří 1 aža 2 písmenovp smenová zkratka, 2. písmeno p je malé. Názvy jsou v PSP (periodické soustavě prvků). Př.: kobalt je Co, ne CO Pozn.: PSP je nejdůle ležitější
POKYNY TEORETICKÁ ČÁST
 POKYNY nejprve si prostuduj teoretickou část s uvedenými typovým příklady jakmile si budeš jist, že teoretickou část zvládáš, procvič si své dovednosti na příkladech k procvičování jako doplňující úlohu
POKYNY nejprve si prostuduj teoretickou část s uvedenými typovým příklady jakmile si budeš jist, že teoretickou část zvládáš, procvič si své dovednosti na příkladech k procvičování jako doplňující úlohu
Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 1 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 1 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Chemická nomenklatura
 Chemická nomenklatura racionální chemické názvy anorganických sloučenin jsou většinou dvouslovné, skládající se ze substantiva a adjektiva elektronegativní části (aniontu) se uvádí v názvu jako první ve
Chemická nomenklatura racionální chemické názvy anorganických sloučenin jsou většinou dvouslovné, skládající se ze substantiva a adjektiva elektronegativní části (aniontu) se uvádí v názvu jako první ve
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T30 Téma: Kyseliny Střední škola Rok: 2012 2013 Varianta: A Kyseliny Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník VÝKLAD jsou to sloučeniny KYSELINY ve vodných roztocích
DUM Základy přírodních věd DUM III/2-T30 Téma: Kyseliny Střední škola Rok: 2012 2013 Varianta: A Kyseliny Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník VÝKLAD jsou to sloučeniny KYSELINY ve vodných roztocích
1 mol (ideálního) plynu, zaujímá za normálních podmínek objem 22,4 litru. , Cl 2 , O 2
 10.výpočty z rovnic praktické provádění výpočtů z rovnic K výpočtu chemických rovnic je důležité si shrnout tyto poznatky: Potřebujem znát vyjadřování koncentrací, objemový zlomek, molární zlomek, molární
10.výpočty z rovnic praktické provádění výpočtů z rovnic K výpočtu chemických rovnic je důležité si shrnout tyto poznatky: Potřebujem znát vyjadřování koncentrací, objemový zlomek, molární zlomek, molární
Úpravy chemických rovnic
 Úpravy chemických rovnic Chemické rovnice kvantitativně i kvalitativně popisují chemickou reakci. Na levou stranu se v chemické rovnici zapisují výchozí látky (reaktanty), na pravou produkty. Obě strany
Úpravy chemických rovnic Chemické rovnice kvantitativně i kvalitativně popisují chemickou reakci. Na levou stranu se v chemické rovnici zapisují výchozí látky (reaktanty), na pravou produkty. Obě strany
Výukový materiál zpracován v rámci operačního projektu. EU peníze školám. Registrační číslo projektu: CZ.1.07/1.5.00/34.0512
 Výukový materiál zpracován v rámci operačního projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0512 Střední škola ekonomiky, obchodu a služeb SČMSD Benešov, s.r.o. CHEMIE Anorganická
Výukový materiál zpracován v rámci operačního projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.5.00/34.0512 Střední škola ekonomiky, obchodu a služeb SČMSD Benešov, s.r.o. CHEMIE Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 03.04.2013 Číslo DUMu: VY_32_INOVACE_14_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 03.04.2013 Číslo DUMu: VY_32_INOVACE_14_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 03.04.2013 Číslo DUMu: VY_32_INOVACE_14_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
DUM VY_52_INOVACE_12CH19
 Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH19 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH19 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Periodická tabulka řádek = perioda sloupec = skupina
 Periodická tabulka řádek = perioda = počet vrstev v elektronovém obalu sloupec = skupina (nadepsáno nahoře) = počet valenčních elektronů Valenční elektrony jsou ty, které se podílejí na vzniku chemických
Periodická tabulka řádek = perioda = počet vrstev v elektronovém obalu sloupec = skupina (nadepsáno nahoře) = počet valenčních elektronů Valenční elektrony jsou ty, které se podílejí na vzniku chemických
CHO cvičení, FSv, ČVUT v Praze
 2. Chemické rovnice Chemická rovnice je schématický zápis chemického děje (reakce), který nás informuje o reaktantech (výchozích látkách), produktech, dále o stechiometrii reakce tzn. o vzájemném poměru
2. Chemické rovnice Chemická rovnice je schématický zápis chemického děje (reakce), který nás informuje o reaktantech (výchozích látkách), produktech, dále o stechiometrii reakce tzn. o vzájemném poměru
Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 2 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
Gymnázium a Střední odbornáškola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: 2 Název materiálu: Ročník: Identifikace materiálu: Jméno autora: Předmět: Tématický celek:
DUM VY_52_INOVACE_12CH01
 Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH01 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH01 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH ROVNIC VY_32_INOVACE_03_3_18_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH ROVNIC VY_32_INOVACE_03_3_18_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_15_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_15_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_15_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
1) Stechiometrický vzorec vyjadřuje stechiometrické složení látky (poměr atomů)
 Chemické vzorce Chemické vzorce 1) Stechiometrický vzorec vyjadřuje stechiometrické složení látky (poměr atomů) např. oxid fosforečný {P 2 O 5 }, oxid křemičitý {SiO 2 } 2) Molekulový vzorec vyjadřuje
Chemické vzorce Chemické vzorce 1) Stechiometrický vzorec vyjadřuje stechiometrické složení látky (poměr atomů) např. oxid fosforečný {P 2 O 5 }, oxid křemičitý {SiO 2 } 2) Molekulový vzorec vyjadřuje
U 218 - Ústav procesní a zpracovatelské techniky FS ČVUT
 Sloučeniny, jejichž stavební částice (molekuly, ionty) jsou tvořeny atomy dvou různých chemických prvků. Obecný vzorec: M m X n M - prvek s kladným oxidačním číslem OM X - prvek se záporným oxidačním číslem
Sloučeniny, jejichž stavební částice (molekuly, ionty) jsou tvořeny atomy dvou různých chemických prvků. Obecný vzorec: M m X n M - prvek s kladným oxidačním číslem OM X - prvek se záporným oxidačním číslem
Složení látek a chemická vazba Číslo variace: 1
 Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T3-2-20 Téma: Test obecná chemie Střední škola Rok: 2012 2013 Varianta: A Test obecná chemie Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Otázka 1 OsO 4 je
DUM Základy přírodních věd DUM III/2-T3-2-20 Téma: Test obecná chemie Střední škola Rok: 2012 2013 Varianta: A Test obecná chemie Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Otázka 1 OsO 4 je
NÁZVOSLOVÍ SOLÍ. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 14. 5. 2013. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková NÁZVOSLOVÍ SOLÍ Datum (období) tvorby: 14. 5. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s názvoslovím
Autor: Mgr. Stanislava Bubíková NÁZVOSLOVÍ SOLÍ Datum (období) tvorby: 14. 5. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s názvoslovím
TEORETICKÁ ČÁST (OH) +II
 POKYNY nejprve si prostuduj teoretickou část s uvedenými typovým příklady jakmile si budeš jist, že teoretickou část zvládáš, procvič si své dovednosti na příkladech k procvičování jako doplňující úlohu
POKYNY nejprve si prostuduj teoretickou část s uvedenými typovým příklady jakmile si budeš jist, že teoretickou část zvládáš, procvič si své dovednosti na příkladech k procvičování jako doplňující úlohu
Gymnázium, Brno, Elgartova 3
 Gymnázium, Brno, Elgartova 3 Šablona: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Název projektu: GE Vyšší kvalita výuky Číslo projektu: CZ.1.07/1.5.00/34.0925 Autor: Mgr. Petra Holzbecherová
Gymnázium, Brno, Elgartova 3 Šablona: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Název projektu: GE Vyšší kvalita výuky Číslo projektu: CZ.1.07/1.5.00/34.0925 Autor: Mgr. Petra Holzbecherová
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost.
 Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Didaktika chemického anorg. názvosloví
 Didaktika chemického anorg. názvosloví RNDr. Milan Šmídl, Ph.D. 1 Didaktické zpracování zopakovat základní pojmy týkající se tvorby a čtení chemického názvosloví a správných českých a latinských názvů
Didaktika chemického anorg. názvosloví RNDr. Milan Šmídl, Ph.D. 1 Didaktické zpracování zopakovat základní pojmy týkající se tvorby a čtení chemického názvosloví a správných českých a latinských názvů
CHEMICKÉ REAKCE A HMOTNOSTI A OBJEMY REAGUJÍCÍCH LÁTEK
 CHEMICKÉ REAKCE A HMOTNOSTI A OBJEMY REAGUJÍCÍCH LÁTEK Význam stechiometrických koeficientů 2 H 2 (g) + O 2 (g) 2 H 2 O(l) Počet reagujících částic 2 molekuly vodíku reagují s 1 molekulou kyslíku za vzniku
CHEMICKÉ REAKCE A HMOTNOSTI A OBJEMY REAGUJÍCÍCH LÁTEK Význam stechiometrických koeficientů 2 H 2 (g) + O 2 (g) 2 H 2 O(l) Počet reagujících částic 2 molekuly vodíku reagují s 1 molekulou kyslíku za vzniku
Chemické repetitorium. Václav Pelouch
 ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Chemické repetitorium Václav Pelouch kapitola ve skriptech - 1 Anorganická a obecná chemie Stavba atomu Atom je nejmenší částice hmoty, která obsahuje jádro (složené
ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Chemické repetitorium Václav Pelouch kapitola ve skriptech - 1 Anorganická a obecná chemie Stavba atomu Atom je nejmenší částice hmoty, která obsahuje jádro (složené
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/
 Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT-PZC_2_6 Test obecná chemie Střední
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT-PZC_2_6 Test obecná chemie Střední
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_17_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_17_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.03.2013 Číslo DUMu: VY_32_INOVACE_17_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Chemické veličiny, vztahy mezi nimi a chemické výpočty
 SBÍRKA ŘEŠENÝCH PŘÍKLADŮ PRO PROJEKT PŘÍRODNÍ VĚDY AKTIVNĚ A INTERAKTIVNĚ CZ.1.07/1.1.24/01.0040 Chemické veličiny, vztahy mezi nimi a chemické výpočty Mgr. Jana Žůrková, 2013, 20 stran Obsah 1. Veličiny
SBÍRKA ŘEŠENÝCH PŘÍKLADŮ PRO PROJEKT PŘÍRODNÍ VĚDY AKTIVNĚ A INTERAKTIVNĚ CZ.1.07/1.1.24/01.0040 Chemické veličiny, vztahy mezi nimi a chemické výpočty Mgr. Jana Žůrková, 2013, 20 stran Obsah 1. Veličiny
Názvosloví kyslíkatých kyselin (oxokyselin) II n
 (oxokyselin) Molekuly obsahují vodík, kyslík, atom(y) kyselinotvorného prvku (centrální atom(y)). Vznikají reakcí kyselinotvorných oxidů s vodou. Obecný vzorec: H X O m x n H - atom vodíku, oxid. číslo
(oxokyselin) Molekuly obsahují vodík, kyslík, atom(y) kyselinotvorného prvku (centrální atom(y)). Vznikají reakcí kyselinotvorných oxidů s vodou. Obecný vzorec: H X O m x n H - atom vodíku, oxid. číslo
-ičelý -natý -ičitý - ečný (-ičný) -istý -ný -itý -ový
 1 Halogenidy dvouprvkové sloučeniny halogenů s jinými prvky atomy halogenů mají v halogenidech oxidační číslo -I 1) Halogenidy - názvosloví Podstatné jméno názvu je zakončeno koncovkou.. Zakončení přídavného
1 Halogenidy dvouprvkové sloučeniny halogenů s jinými prvky atomy halogenů mají v halogenidech oxidační číslo -I 1) Halogenidy - názvosloví Podstatné jméno názvu je zakončeno koncovkou.. Zakončení přídavného
DUM VY_52_INOVACE_12CH04
 Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH04 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH04 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Názvosloví kyselin a hydroxidů
 Názvosloví kyselin a hydroxidů Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. Kyseliny Kyseliny
Názvosloví kyselin a hydroxidů Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. Kyseliny Kyseliny
ZÁKLADNÍ CHEMICKÉ VÝPOČTY
 ZÁKLADNÍ CHEMICKÉ VÝPOČTY Látkové množství - vyjadřování množství: jablka pivo chleba uhlí - (téměř každá míra má svojí jednotku) v chemii existuje univerzální veličina pro vyjádření množství látky LÁTKOVÉ
ZÁKLADNÍ CHEMICKÉ VÝPOČTY Látkové množství - vyjadřování množství: jablka pivo chleba uhlí - (téměř každá míra má svojí jednotku) v chemii existuje univerzální veličina pro vyjádření množství látky LÁTKOVÉ
Vyšší odborná škola, Obchodní akademie a Střední odborná škola EKONOM, o. p. s. Litoměřice, Palackého 730/1
 DUM Základy přírodních věd DUM III/2-T3-2-09 Téma: Oxidy Střední škola Rok: 2012 2013 Varianta: A Oxidy Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník VÝKLAD OXIDY zásadotvorné oxidy můžeme rozdělit například
DUM Základy přírodních věd DUM III/2-T3-2-09 Téma: Oxidy Střední škola Rok: 2012 2013 Varianta: A Oxidy Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník VÝKLAD OXIDY zásadotvorné oxidy můžeme rozdělit například
Mezipředmětové vazby matematika chemie. Aplikace matematiky v učivu chemie na základní škole.
 MASARYKOVA UNIVERZITA BRNO Pedagogická fakulta Katedra chemie Mezipředmětové vazby matematika chemie. Aplikace matematiky v učivu chemie na základní škole. Diplomová práce Brno 2008 Vedoucí: Mgr. Irena
MASARYKOVA UNIVERZITA BRNO Pedagogická fakulta Katedra chemie Mezipředmětové vazby matematika chemie. Aplikace matematiky v učivu chemie na základní škole. Diplomová práce Brno 2008 Vedoucí: Mgr. Irena
Chemický seminář Periodická tabulka prvků Základní chemické pojmy Úvod do anorganického názvosloví
 Chemický seminář 26.9.2013 Periodická tabulka prvků Základní chemické pojmy Úvod do anorganického názvosloví Periodicka tabulka prvku Názvy skupin Alkalické kovy: Li, Na, K, Rb, Cs, Fr Kovy alkalických
Chemický seminář 26.9.2013 Periodická tabulka prvků Základní chemické pojmy Úvod do anorganického názvosloví Periodicka tabulka prvku Názvy skupin Alkalické kovy: Li, Na, K, Rb, Cs, Fr Kovy alkalických
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.04.2013 Číslo DUMu: VY_32_INOVACE_16_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.04.2013 Číslo DUMu: VY_32_INOVACE_16_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 18.04.2013 Číslo DUMu: VY_32_INOVACE_16_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Sklářské a bižuterní materiály 2005/06, Cvičení 1
 Cvičení 1 1. Seznámení s podmínkami zápočtu 100% účast na cvičení případně omluva, úspěšné zvládnutí testu, aktivní účast na cvičení Podklady na stránce: www.ksr.tul.cz/studium-podklady.htm 2. Obecné vysvětlení
Cvičení 1 1. Seznámení s podmínkami zápočtu 100% účast na cvičení případně omluva, úspěšné zvládnutí testu, aktivní účast na cvičení Podklady na stránce: www.ksr.tul.cz/studium-podklady.htm 2. Obecné vysvětlení
Příklad Sestavte rovnice následujících dějů: reakce hydroxidu sodného s kyselinou tetrahydrogendifosforečnou 4NaOH + H 4 P 2 O 7 Na 4 P 2 O 7
 Příklad 2.2.9. Sestavte rovnice následujících dějů: reakce hydroxidu sodného s kyselinou tetrahydrogendifosforečnou 4NaOH + H 4 P 2 O 7 Na 4 P 2 O 7 + 4H 2 O reakce dimerního oxidu antimonitého s kyselinou
Příklad 2.2.9. Sestavte rovnice následujících dějů: reakce hydroxidu sodného s kyselinou tetrahydrogendifosforečnou 4NaOH + H 4 P 2 O 7 Na 4 P 2 O 7 + 4H 2 O reakce dimerního oxidu antimonitého s kyselinou
Názvosloví anorganických sloučenin
 Názvosloví anorganických sloučenin CHEMICKÁ NOMENKLATURA Milan Haminger, BiGy Brno Chemické názvosloví Název chemické sloučeniny = slovní záznam chemického vzorce. Název anorganické sloučeniny: - podstatné
Názvosloví anorganických sloučenin CHEMICKÁ NOMENKLATURA Milan Haminger, BiGy Brno Chemické názvosloví Název chemické sloučeniny = slovní záznam chemického vzorce. Název anorganické sloučeniny: - podstatné
Složení soustav (roztoky, koncentrace látkového množství)
 VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
VZOROVÉ PŘÍKLADY Z CHEMIE A DOPORUČENÁ LITERATURA pro přípravu k přijímací zkoušce studijnímu oboru Nanotechnologie na VŠB TU Ostrava Doporučená literatura z chemie: Prakticky jakákoliv celostátní učebnice
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939. Název projektu: Investice do vzdělání - příslib do budoucnosti
 Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV:VY_32_INOVACE_102_Soli AUTOR: Igor Dubovan ROČNÍK, DATUM: 9., 15. 9.
 NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV:VY_32_INOVACE_102_Soli AUTOR: Igor Dubovan ROČNÍK, DATUM: 9., 15. 9. 2011 VZDĚL. OBOR, TÉMA: Chemie, Soli ČÍSLO PROJEKTU: OPVK
NÁZEV ŠKOLY: Základní škola Javorník, okres Jeseník REDIZO: 600 150 585 NÁZEV:VY_32_INOVACE_102_Soli AUTOR: Igor Dubovan ROČNÍK, DATUM: 9., 15. 9. 2011 VZDĚL. OBOR, TÉMA: Chemie, Soli ČÍSLO PROJEKTU: OPVK
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL.
 CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
Obecná a anorganická chemie. Kyslíkaté kyseliny
 Šablona č. I, sada č. 2 Vzdělávací oblast Vzdělávací obor Tematický okruh Téma Člověk a příroda Chemie Obecná a anorganická chemie Kyslíkaté kyseliny Ročník 9. Anotace Aktivita slouží k upevnění učiva
Šablona č. I, sada č. 2 Vzdělávací oblast Vzdělávací obor Tematický okruh Téma Člověk a příroda Chemie Obecná a anorganická chemie Kyslíkaté kyseliny Ročník 9. Anotace Aktivita slouží k upevnění učiva
Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9.
 Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9. Školní rok 0/03, 03/04 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup) Počet hodin pro kapitolu Úvod
Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9. Školní rok 0/03, 03/04 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup) Počet hodin pro kapitolu Úvod
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace
 Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Gymnázium, Brno, Elgartova 3
 Gymnázium, Brno, Elgartova 3 Šablona: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Název projektu: GE Vyšší kvalita výuky Číslo projektu: CZ.1.07/1.5.00/34.0925 Autor: Mgr. Petra Holzbecherová
Gymnázium, Brno, Elgartova 3 Šablona: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Název projektu: GE Vyšší kvalita výuky Číslo projektu: CZ.1.07/1.5.00/34.0925 Autor: Mgr. Petra Holzbecherová
Chemické rovnice. Úprava koeficientů oxidoredukčních rovnic
 Úprava koeficientů oxidoredukčních rovnic Má-li být zápis chemické rovnice úplný (a použitelný například pro výpočty), musejí být počty molekul látek v chemické rovnici vyjádřeny takovými stechiometrickými
Úprava koeficientů oxidoredukčních rovnic Má-li být zápis chemické rovnice úplný (a použitelný například pro výpočty), musejí být počty molekul látek v chemické rovnici vyjádřeny takovými stechiometrickými
ANODA KATODA elektrolyt:
 Ukázky z pracovnívh listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Ukázky z pracovnívh listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
N A = 6,023 10 23 mol -1
 Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
zadání příkladů 10. výsledky příkladů 7. 3,543 litru kyslíku
 zadání Jaký bude objem vodíku při tlaku 105 kpa a teplotě 15 stupňů Celsia, který vznikne reakcí 8 gramů zinku s nadbytkem kyseliny trihydrogenfosforečné? Jaký bude objem vodíku při tlaku 97 kpa a teplotě
zadání Jaký bude objem vodíku při tlaku 105 kpa a teplotě 15 stupňů Celsia, který vznikne reakcí 8 gramů zinku s nadbytkem kyseliny trihydrogenfosforečné? Jaký bude objem vodíku při tlaku 97 kpa a teplotě
DUSÍK NITROGENIUM 14,0067 3,1. Doplňte:
 Doplňte: Protonové číslo: Relativní atomová hmotnost: Elektronegativita: Značka prvku: Latinský název prvku: Český název prvku: Nukleonové číslo: Prvek je chemická látka tvořena z atomů o stejném... čísle.
Doplňte: Protonové číslo: Relativní atomová hmotnost: Elektronegativita: Značka prvku: Latinský název prvku: Český název prvku: Nukleonové číslo: Prvek je chemická látka tvořena z atomů o stejném... čísle.
Gymnázium, Brno, Elgartova 3
 Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Základy názvosloví Autor: Název: Mgr. Petra Holzbecherová Anorganické
Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Základy názvosloví Autor: Název: Mgr. Petra Holzbecherová Anorganické
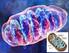
Zemská kůra. kyslík křemík hliník hořčík vápník sodík železo ostaní prvky
 Cvičení 1 1. Seznámení s podmínkami zápočtu 100% účast na laboratořích, odevzdání protokolů z laboratorních prací, odevzdání semestrální práce. Podklady na stránce: www.ksk.vslib.cz/studium-podklady.htm
Cvičení 1 1. Seznámení s podmínkami zápočtu 100% účast na laboratořích, odevzdání protokolů z laboratorních prací, odevzdání semestrální práce. Podklady na stránce: www.ksk.vslib.cz/studium-podklady.htm
CHEMICKÉ VÝPOČTY MOLÁRNÍ HMOTNOST LÁTKOVÉ MNOŽSTVÍ PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST
 CHEMICKÉ VÝPOČTY MOLÁRNÍ HMOTNOST LÁTKOVÉ MNOŽSTVÍ PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST AMEDEO AVOGADRO AVOGADROVA KONSTANTA 2 N 2 MOLY ATOMŮ DUSÍKU 2 ATOMY DUSÍKU
CHEMICKÉ VÝPOČTY MOLÁRNÍ HMOTNOST LÁTKOVÉ MNOŽSTVÍ PROJEKT EU PENÍZE ŠKOLÁM OPERAČNÍ PROGRAM VZDĚLÁVÁNÍ PRO KONKURENCESCHOPNOST AMEDEO AVOGADRO AVOGADROVA KONSTANTA 2 N 2 MOLY ATOMŮ DUSÍKU 2 ATOMY DUSÍKU
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
ANODA KATODA elektrolyt:
 Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Anorganické názvosloví
 Anorganické názvosloví BINÁRNÍ SLOUČENINY: OXIDY PEROXIDY BEZKYSLÍKATÉ KYSELINY A JEJICH SOLI HYDRIDY KYSLÍKATÉ KYSELINY A JEJICH SOLI (HYDROGEN SOLI, HYDRÁTY SOLÍ) THIOKYSELINY A JEJICH SOLI IZOPOLYKYSELINY
Anorganické názvosloví BINÁRNÍ SLOUČENINY: OXIDY PEROXIDY BEZKYSLÍKATÉ KYSELINY A JEJICH SOLI HYDRIDY KYSLÍKATÉ KYSELINY A JEJICH SOLI (HYDROGEN SOLI, HYDRÁTY SOLÍ) THIOKYSELINY A JEJICH SOLI IZOPOLYKYSELINY
DOUČOVÁNÍ KVINTA CHEMIE
 1. ÚVOD DO STUDIA CHEMIE 1) Co studuje chemie? 2) Rozděl chemii na tři důležité obory. DOUČOVÁNÍ KVINTA CHEMIE 2. NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN 1) Pojmenuj: BaO, N 2 0, P 4 O 10, H 2 SO 4, HMnO 4,
1. ÚVOD DO STUDIA CHEMIE 1) Co studuje chemie? 2) Rozděl chemii na tři důležité obory. DOUČOVÁNÍ KVINTA CHEMIE 2. NÁZVOSLOVÍ ANORGANICKÝCH SLOUČENIN 1) Pojmenuj: BaO, N 2 0, P 4 O 10, H 2 SO 4, HMnO 4,
ZÁPADOČESKÁ UNIVERZITA V PLZNI
 ZÁPADOČESKÁ UNIVERZITA V PLZNI FAKULTA PEDAGOGICKÁ KATEDRA CHEMIE ANORGANICKÉ NÁZVOSLOVÍ A CHEMICKÉ VÝPOČTY VE VÝUCE CHEMIE NA ZÁKLADNÍ ŠKOLE DIPLOMOVÁ PRÁCE Bc. Lenka Trhlíková Učitelství pro základní
ZÁPADOČESKÁ UNIVERZITA V PLZNI FAKULTA PEDAGOGICKÁ KATEDRA CHEMIE ANORGANICKÉ NÁZVOSLOVÍ A CHEMICKÉ VÝPOČTY VE VÝUCE CHEMIE NA ZÁKLADNÍ ŠKOLE DIPLOMOVÁ PRÁCE Bc. Lenka Trhlíková Učitelství pro základní
HALOGENIDY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 27. 2. 2013. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková HALOGENIDY Datum (období) tvorby: 27. 2. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s dvouprvkovými
Autor: Mgr. Stanislava Bubíková HALOGENIDY Datum (období) tvorby: 27. 2. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí s dvouprvkovými
KONTROLNÍ TEST ŠKOLNÍHO KOLA (70 BODŮ)
 KONTROLNÍ TEST ŠKOLNÍHO KOLA (70 BODŮ) Úloha 1 Ic), IIa), IIId), IVb) za každé správné přiřazení po 1 bodu; celkem Úloha 2 8 bodů 1. Sodík reaguje s vodou za vzniku hydroxidu sodného a dalšího produktu.
KONTROLNÍ TEST ŠKOLNÍHO KOLA (70 BODŮ) Úloha 1 Ic), IIa), IIId), IVb) za každé správné přiřazení po 1 bodu; celkem Úloha 2 8 bodů 1. Sodík reaguje s vodou za vzniku hydroxidu sodného a dalšího produktu.
KYSELINY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 27. 3. 2013. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková KYSELINY Datum (období) tvorby: 27. 3. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základními anorganickými
Autor: Mgr. Stanislava Bubíková KYSELINY Datum (období) tvorby: 27. 3. 2013 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Anorganické sloučeniny 1 Anotace: Žáci se seznámí se základními anorganickými
DUM VY_52_INOVACE_12CH05
 Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH05 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Základní škola Kaplice, Školní 226 DUM VY_52_INOVACE_12CH05 autor: Kristýna Anna Rolníková období vytvoření: říjen 2011 duben 2012 ročník, pro který je vytvořen: 8. a 9. vzdělávací oblast: vzdělávací obor:
Hydrochemie koncentrace látek (výpočty)
 1 Atomová hmotnostní konstanta/jednotka m u Relativní atomová hmotnost Relativní molekulová hmotnost Látkové množství (mol) 1 mol je takové množství látky, které obsahuje tolik částic, kolik je atomů ve
1 Atomová hmotnostní konstanta/jednotka m u Relativní atomová hmotnost Relativní molekulová hmotnost Látkové množství (mol) 1 mol je takové množství látky, které obsahuje tolik částic, kolik je atomů ve
Předmět: CHEMIE Ročník: 8. ŠVP Základní škola Brno, Hroznová 1. Výstupy předmětu
 Chemie ukázka chemického skla Chemie přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce práce s dostupnými a běžně používanými látkami (směsmi). Na základě piktogramů žák posoudí nebezpečnost
Chemie ukázka chemického skla Chemie přírodní věda, poznat chemické sklo a pomůcky, zásady bezpečné práce práce s dostupnými a běžně používanými látkami (směsmi). Na základě piktogramů žák posoudí nebezpečnost
Očekávané ročníkové výstupy z chemie 8. ročník
 Očekávané ročníkové výstupy z chemie 8. ročník Pomůcky: kalkulačka, tabulky, periodická tabulka prvků Témata ke srovnávací písemné práci z chemie (otázky jsou pouze orientační, v testu může být zadání
Očekávané ročníkové výstupy z chemie 8. ročník Pomůcky: kalkulačka, tabulky, periodická tabulka prvků Témata ke srovnávací písemné práci z chemie (otázky jsou pouze orientační, v testu může být zadání
Gymnázium Jana Pivečky a Střední odborná škola Slavičín. III/2 Inovace a zkvalitnění výuky prostřednictvím ITC
 Název projektu Číslo projektu Název školy Autor Název šablony Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748 Gymnázium Jana Pivečky a Střední odborná škola Slavičín Mgr. Veronika Prchlíková
Název projektu Číslo projektu Název školy Autor Název šablony Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748 Gymnázium Jana Pivečky a Střední odborná škola Slavičín Mgr. Veronika Prchlíková
chartakterizuje přírodní vědy,charakterizuje chemii, orientuje se v možných využití chemie v běžníém životě
 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup). Úvod do chemie Charakteristika chemie a její význam Charakteristika přírodních věd charakteristika chemie Chemie kolem nás chartakterizuje přírodní
Kapitola Téma (Učivo) Znalosti a dovednosti (výstup). Úvod do chemie Charakteristika chemie a její význam Charakteristika přírodních věd charakteristika chemie Chemie kolem nás chartakterizuje přírodní
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939. Název projektu: Investice do vzdělání - příslib do budoucnosti
 Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
SHRNUTÍ A ZÁKLADNÍ POJMY chemie 8.ročník ZŠ
 SHRNUTÍ A ZÁKLADNÍ POJMY chemie 8.ročník ZŠ 1. ČÍM SE ZABÝVÁ CHEMIE VLASTNOSTI LÁTEK, POKUSY - chemie přírodní věda, která studuje vlastnosti a přeměny látek pomocí pozorování, měření a pokusu - látka
SHRNUTÍ A ZÁKLADNÍ POJMY chemie 8.ročník ZŠ 1. ČÍM SE ZABÝVÁ CHEMIE VLASTNOSTI LÁTEK, POKUSY - chemie přírodní věda, která studuje vlastnosti a přeměny látek pomocí pozorování, měření a pokusu - látka
SMĚSI. 3. a) Napiš 2 typy pevné směsi:... b) Napiš 2 typy kapalné směsi:... c) Napiš 2 typy plynné směsi:... krev
 1 SMĚSI 1. Zakroužkuj stejnorodé směsi: destilovaná voda slaná voda polévka med krev sirup 2. a) Směs kapaliny a pevné látky se nazývá:... b) Směs dvou nemísitelných kapalin se nazývá:... c) Směs kapaliny
1 SMĚSI 1. Zakroužkuj stejnorodé směsi: destilovaná voda slaná voda polévka med krev sirup 2. a) Směs kapaliny a pevné látky se nazývá:... b) Směs dvou nemísitelných kapalin se nazývá:... c) Směs kapaliny
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost.
 Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Tento materiál byl vytvořen v rámci projektu Operačního programu Vzdělávání pro konkurenceschopnost. Projekt MŠMT ČR Číslo projektu Název projektu školy Klíčová aktivita III/2 EU PENÍZE ŠKOLÁM CZ.1.07/1.4.00/21.2146
Stavba atomu. Created with novapdf Printer (www.novapdf.com). Please register to remove this message.
 Stavba atomu Atom je v chemii základní stavební částice, jeho průměr je přibližně 10-10 m. Je složen z jádra a obalu. Atomové jádro obsahuje protony p + (kladný náboj) a neutrony n 0 (neutrální částice).
Stavba atomu Atom je v chemii základní stavební částice, jeho průměr je přibližně 10-10 m. Je složen z jádra a obalu. Atomové jádro obsahuje protony p + (kladný náboj) a neutrony n 0 (neutrální částice).
