PŘÍBALOVÁ INFORMACE. Informace pro použití, čtěte pozorně! LINDYNETTE 30 obalené tablety k vnitřnímu užití
|
|
|
- Ivana Kubíčková
- před 8 lety
- Počet zobrazení:
Transkript
1 PŘÍBALOVÁ INFORMACE Informace pro použití, čtěte pozorně! LINDYNETTE 30 obalené tablety k vnitřnímu užití Držitel rozhodnutí o registraci/výrobce Gedeon Richter Plc., Budapešť, Maďarsko Složení Léčivé látky: Ethinylestradiolum 0,030 mg, Gestodenum 0,075 mg v 1 obalené tabletě. Pomocné látky: Natrium-kalcium-edetát, magnesium-sterát, koloidní bezvodý oxid křemičitý, povidon, kukuřičný škrob, monohydrát laktosy, chinolinová žluť, oxid titaničitý, makrogol 6000, mastek, uhličitan vápenatý, sacharosa. Indikační skupina Hormonální kontraceptivum pro celkové použití. Charakteristika Jak funguje ženský reprodukční systém? Jednou měsíčně opouští vaječníky jedno vajíčko a prochází vejcovodem do dělohy. Oplodnění (spojení s mužskou spermií) probíhá obvykle již ve vejcovodu. Oplodněné vajíčko se samo uhnízdí ve stěně dělohy, která je speciálně uzpůsobená jej přijmout a vajíčko začíná růst. Jestliže nedojde k oplodnění, vajíčko je z organismu vyloučeno při nejbližší menstruaci. Jak LINDYNETTE 30 účinkuje? Všechny potahované tablety LINDYNETTE 30 obsahují stejná množství stejné kombinace hormonů. Takovým přípravkům se říká monofázická orální kontraceptiva. Obsahují dva rozdílné ženské pohlavní hormony, gestoden (ze skupiny progestogenů) a ethinylestradiol (ze skupiny estrogenů). Tyto hormony zabraňují uvolňování vajíčka z vaječníků, které probíhá každý měsíc, zahušťují hlen v děložním hrdle a ztěžují tím spermiím možnost spojit se s vajíčkem. Ovlivňují také děložní výstelku tak, že uhnízdění oplodněného vajíčka je obtížnější. Orální kontraceptiva jsou přípravky, které se polykají, aby se zabránilo otěhotnění. Pokud se užívají správně, představují účinnou a reverzibilní (tj. vratnou) formu antikoncepce. - Menstruační krvácení může být mírnější a také ztráta železa pro organismus může být menší. Proto se také méně často vyskytuje chudokrevnost v důsledku ztráty železa. Indikace Proč se LINDYNETTE 30 užívá? 1/8
2 LINDYNETTE 30 je určeno k ochraně před otěhotněním. Kontraindikace Kdy se nesmí LINDYNETTE 30 užívat? LINDYNETTE 30 se nesmí podávat, pokud je žena těhotná nebo pokud má podezření na těhotenství a v období kojení. LINDYNETTE 30 nesmí být užíváno, pokud žena má nebo v minulosti měla následující stavy: - Tvorba krevní sraženiny v povrchových cévách dolních končetin (trombofletitida) nebo v očních cévách. - Tvorba krevní sraženiny v hlubokých žílách dolních končetin, v plicních cévách (plicní embolie). - Srdeční záchvat nebo mozková příhoda. - Rakovina prsu nebo podezření na ni. - Rakovina pohlavních orgánů (dělohy, děložní výstelky, děložního čípku) nebo podezření na ni. - Jaterní nádor (benigní nebo maligní) nebo podezření na něj. - Porucha metabolismu tuků. Podávání nesmí být zahájeno nebo musí být přerušeno při následujících stavech: - Pocit bolesti na prsou (angina pectoris). - Blíže neobjasněné krvácení z rodidel (až do doby stanovení diagnózy lékařem). - Přecitlivělost na některou ze složek přípravku LINDYNETTE 30. Dále pokud měla následující stavy v průběhu těhotenství: - Těhotenská žloutenka nebo žloutenka po předchozím podávání orálních kontraceptiv. Ženy, které mají nebo měly některý z výše uvedených stavů, by měly požádat lékaře o doporučení jiné alternativní účinné metody zabránění početí. Nežádoucí účinky Jaké nežádoucí účinky můžete zažít při užívání orálních kontraceptiv? Následující nežádoucí účinky byly pozorovány ženami, které užívaly orální antikoncepci. Tyto účinky však nemusí být důsledkem užívání orální antikoncepce. Nežádoucí účinky se mohou vyskytnout v prvních měsících užívání orální antikoncepce a obvykle časem samy ustoupí. - Bolesti hlavy. - Otok (nahromadění přebytečného množství tekutiny v buňkách, tkáních nebo v dutinách). - Nevolnost, zvracení. - Žaludeční křeče, změny chuti. - Změny tělesné hmotnosti. - Porfyrie (skupina poruch biosyntézy krevního barviva - hemu). - Depresivní nálady, nervozita, závratě, změny pohlavního pudu. - Vyrážka, nodosní erytém (záněty podkožní tukové tkáně), akné, hnědé skvrny na tváři a po těle, podobné těhotenské pigmentaci, hirsutismus (nadměrné ochlupení), vypadávání vlasů. - Nesnášenlivost kontaktních čoček, zánět zrakového nervu, závažná oční onemocnění. 2/8
3 - Přerušované krvácení, špinění, menstruační změny, amenorea (vynechání menstruace), změny děložního čípku a děložní sekrece, poševní zánět. - Změny prsou: bolestivost, zvětšení, sekrece. - Zvýšení hladiny tuků v krvi, zhoršení glukózové tolerance (cukrovky). - Riziko vzniku krevních sraženin (trombů) Trombóza je charakterizována jako vznik krevní sraženiny, která může ucpat krevní cévy. Trombóza někdy vznikne v hlubokých žilách dolních končetin (trombóza hlubokých žil). Jestliže se trombus uvolní, může se krevním řečištěm dostat do plicní tepny a způsobit plicní embolii (ucpání plicní tepny). K trombóze hlubokých žil dochází vzácně a bez závislosti na užívání orální antikoncepce. Může k ní také dojít v průběhu těhotenství. V průběhu užívání orální antikoncepce je riziko vzniku trombózy vyšší, ale ne tak vysoké, jako je v průběhu těhotenství. Krevní trombus se může také dostat velmi vzácně do cév, zásobujících krví srdce (a může způsobit srdeční záchvat) nebo mozek (a vyvolat mrtvici). Velmi vzácně se může dostat do jater, střev, ledvin nebo do očí. Trombóza může v některých případech způsobit vážnou trvalou neschopnost nebo může dokonce skončit smrtí. Ke zvýšenému riziku trombózy dochází, jestliže užíváte orální antikoncepci a musíte podstoupit chirurgický zákrok, jste-li kvůli chorobě dlouhodobě připoutána na lůžko nebo těsně po porodu. Proto je třeba poradit se s lékařem, kdy je možno zahájit podávání orální antikoncepce po porodu nebo po přerušení těhotenství v druhém trimestru (viz. také Podávání v průběhu kojení). - Srdeční záchvat a mrtvice Orální antikoncepce může zvýšit tendenci vzniku mozkové mrtvice (blokáda nebo prasknutí cévy zásobující krví mozek) nebo srdečního záchvatu (ucpání cévy, zásobující krví srdce). Každá taková příhoda může končit smrtelně nebo může mít za následek vážnou neschopnost. Kouření podstatně zvyšuje možnost vzniku srdečního záchvatu nebo mozkové mrtvice a tedy i pravděpodobnost vzniku a úmrtí na srdeční onemocnění. - Zvýšený krevní tlak U žen užívajících orální antikoncepci bylo pozorováno zvýšení krevního tlaku a bylo pravděpodobnější u starších žen, užívajících orální antikoncepci dlouhodobě. - Onemocnění žlučníku U uživatelek orální antikoncepce je pravděpodobně vyšší riziko vzniku onemocnění žlučníku než u žen, které neužívají orální antikoncepci, i když toto riziko je vztahováno k orálním kontraceptivům s vyšším obsahem účinných látek - estrogenů. - Jaterní nádory Ve vzácných případech mohou orální kontraceptiva vyvolat vznik nezhoubných nádorů, které mohou prasknout a ohrozit život vnitřním krvácením. Kromě toho při podávání orální antikoncepce byl pozorován vznik rakoviny jater; přímá souvislost její incidence (výskytu) s podáváním orální antikoncepce však nebyla prokázána. I tak rakovina jater byla pozorována velmi vzácně, takže riziko rozvoje rakoviny jater po podávání orální antikoncepce je velmi nízké. - Rakovina rozmnožovacích orgánů U žen užívajících orální antikoncepci byla o něco častěji diagnostikována rakovina prsu, než u žen stejného věku, které neužívají orální antikoncepci. Tento velmi nízký rozdíl postupně mizí v průběhu 10 let po ukončení užívání orální antikoncepce. Není známo, zda rozdíl je způsoben orální antikoncepcí. Bývá vysvětlován také tím, že ženy užívající orální antikoncepci jsou vyšetřovány častěji, takže je u nich větší pravděpodobnost odhalení nádoru v ranném stádiu. 3/8
4 Některé studie svědčí o zvýšení rizika rakoviny děložního čípku u žen užívajících orální antikoncepci. Tato zjištění však mohou mít i jinou souvislost než jen s užíváním orální antikoncepce. O každém nežádoucím účinku by měl být informován lékař, zvláště, je-li nežádoucí účinek závažný nebo přetrvávající nebo jestliže došlo ke změně celkového zdravotního stavu a mohlo to být zapříčiněno orální antikoncepcí. Varovné signály Informujte ihned svého lékaře, jestliže budete mít následující pocity: - Ostrá bolest na hrudi, vykašlávání krve nebo náhlé ztížené dýchání (indikující možné ucpání plicní cévy krevní sraženinou). - Bolest v lýtku (možné ucpání žíly dolní končetiny). - Tíživá bolest hrudníku nebo tíha na hrudi (možný srdeční záchvat). - Náhlé silné bolesti hlavy nebo zvracení, závratě nebo mdloby, poruchy vidění nebo řeči, slabost nebo znecitlivění a brnění horních či dolních končetin (možná mozková mrtvice). - Náhlá částečná nebo úplná ztráta vidění (možné ucpání cévy, která zásobuje oko krví). - Hmatatelné uzlíky v prsou (možný zhoubný nebo nezhoubný nádor prsu). - Velké bolesti břicha nebo bolest břicha na pohmat (možné prasknutí jaterního nádoru). - Problémy se spánkem, slabost, ztráta energie, únava, náhlé změny nálady (možná závažná deprese). - Žloutenka nebo zežloutnutí kůže nebo oční koule, provázené často horečkou, únavou, ztrátou chuti k jídlu, tmavým zbarvením moči nebo světlým zbarvením stolice (možné jaterní onemocnění). - Začátek nebo nové vzplanutí migrény. Užívání orální antikoncepce má kromě svého hlavního účinku i další výhody: - Může zlepšit pravidelnost menstruačního cyklu. - Menstruační krvácení může být mírnější a také ztráta železa pro organismus může být menší. Proto se také méně často vyskytuje chudokrevnost v důsledku ztráty železa. - Méně častý může být také vznik dutin ve vaječníku (cyst). - Méně často dochází k mimoděložnímu těhotenství. - Méně častý může být výskyt nezhoubných nádorů prsu. - Méně často může dojít k akutnímu zánětu pánevních orgánů. - Orální kontraceptiva mohou poskytovat částečnou ochranu proti vzniku dvou druhů rakoviny, a to rakoviny vaječníků a rakoviny výstelky dělohy. - Může zlepšit akné (trudovitost kůže). Interakce Některá léčiva, jako např. rifampicin, léčiva k léčbě epilepsie, léčiva navozující spánek (např. fenobarbital ze skupiny barbiturátů), fenytoin, protizánětlivý lék fenylbutazon a některá antibiotika (jako griseofulvin, ampicilin a tetracyklin) mohou snižovat antikoncepční účinnost orální antikoncepce a zvyšovat krvácení mimo cyklus. Po dobu podávání výše uvedených léčiv a po dalších 7 dnů se doporučuje používat ještě jiný způsob antikoncepce. V případě nejasností je lépe se poradit s lékařem. Laboratorní vyšetření: orální kontraceptiva mohou ovlivnit výsledky laboratorních vyšetření. Proto je třeba před provedením laboratorních vyšetření informovat lékaře o užívání orální antikoncepce. 4/8
5 Váš lékař by měl vědět o všech lécích, které v současné době užíváte, nebo které začnete užívat, a to na lékařský předpis i bez něj. Než začnete současně s užíváním přípravku LINDYNETTE 30 užívat nějaký volně prodejný lék, poraďte se se svým ošetřujícím lékařem. Dávkování a způsob použití Kdy a jak užívat LINDYNETTE 30? Každý blistr obsahuje 21 potahovaných tablet. K dosažení maximální antikoncepční účinnosti je třeba tablety užívat přesně podle návodu jednou denně přibližně ve stejnou denní dobu a zapít tekutinou podle potřeby. Tablety se užívají po 21 po sobě následujících dní tak, že se berou postupně podle šipek a návodu na blistru. Užívání z nového balení začíná vždy po sedmidenní přestávce, během které se dostaví krvácení z hormonálního spádu. To obvykle začíná druhý až třetí den po užití poslední potahované tablety a nemusí být ukončeno v době zahájení užívání z nového balení. To znamená, že užívání z nového balení začíná vždy ve stejný den v týdnu a že krvácení probíhá také pravidelně ve stejné dny v týdnu každý měsíc. Pokud bylo předchozích 21 tablet užíváno správně, není třeba po dobu sedmidenní přestávky používat žádný doplňkový způsob antikoncepce. Ihned po skončení sedmidenní přestávky je nutno zahájit podávání z nového balení. - Zahájení užívání Jestliže v předchozím měsíci nebyla podávána žádná hormonální antikoncepce: užívání se zahájí první den menstruačního cyklu (první den menstruačního krvácení) užitím tablety označené na blistru příslušným dnem v týdnu Každý následující den se užije jedna tableta, přičemž se postupuje podle šipek na obalu do té doby, dokud není obal prázdný. Je možno zahájit podávání také den menstruačního cyklu, ale v tomto případě se doporučuje po dobu prvních 7 dní užívání tablet použít ještě další doplňkovou nehormonální antikoncepční metodu (jako např. kondom nebo spermicidy). Toto platí pouze pro první balení. - Přechod na LINDYNETTE 30 z jiné kombinované orální antikoncepce První potahovaná tableta přípravku LINDYNETTE 30 by měla být podána nejlépe následující den po užití poslední tablety s účinnou látkou předchozího antikoncepčního přípravku, ale nejpozději v den následující po pravidelném období přestávky v užívání kombinované orální antikoncepce (nebo po užití poslední tablety bez účinné látky předchozího antikoncepčního přípravku). - Přechod z čistě progestinové antikoncepce (mikropilule) Původní antikoncepci je možno změnit na podávání přípravku LINDYNETTE 30 kterýkoli den cyklu. Podávání potahovaných tablet LINDYNETTE 30 musí být zahájeno následující den po podání poslední mikropilule, ve stejnou denní dobu. Vždy je třeba použít ještě doplňkovou nehormonální metodu antikoncepce po dobu prvních 7 dní podávání tablet LINDYNETTE Přechod z antikoncepce ve formě injekce nebo implantátu První tableta LINDYNETTE 30 má být podána v den, kdy měla být podána injekce nebo kdy byl odstraněn implantát. V tomto případě je třeba použít ještě doplňkovou nehormonální metodu antikoncepce po dobu prvních 7 dní podávání přípravku LINDYNETTE 30. V případě nejasností je lépe se poradit s lékařem. - Po porodu Se zahájením užívání se obvykle čeká, než se dostaví první menstruační krvácení. Někdy, podle doporučení lékaře, je možné začít s užíváním dříve. Kojící ženy se před zahájením užívání musí poradit s lékařem. - Po vyvolaném nebo spontánním potratu Vždy je třeba se poradit s lékařem. Co dělat, když se zapomene užít LINDYNETTE 30? 5/8
6 Antikoncepční spolehlivost může být snížena, jestliže dojde k opomenutí užití tablet. Jestliže opoždění podání tablety LINDYNETTE 30 činí méně než 12 hodin, není důvod k obavám. Pacientka by měla užít zapomenutou potahovanou tabletu co nejdříve, jakmile si uvědomí opoždění. Následující tableta se pak užije v obvyklou dobu. Jestliže nedojde k užití opomenuté potahované tablety do 12 hodin od obvyklé doby podávání, může dojít ke snížení antikoncepční účinnosti. V tomto případě je třeba užít zapomenutou poslední tabletu ihned, jakmile si to pacientka uvědomí a následující tabletu užít v obvyklou dobu, takže může dojít k podání 2 potahovaných tablet v jednom dni. Další tablety se pak už podávají v obvyklou dobu. Po následujících 7 dnů je však třeba použít ještě doplňkovou metodu nehormonální antikoncepce jako např. kondom. Jestliže těchto 7 dnů skončí až po využívání všech potahovaných tablet z jednoho balení, ihned (bez přestávky v užívání) se začíná s podáváním tablet z nového balení. Až do využívání tohoto druhého balení pravděpodobně nedojde ke krvácení ze spádu, ale může se vyskytnout špinění nebo přerušované krvácení. Jestliže se nedostaví krvácení ze spádu po využívání druhého balení, je třeba nejprve se poradit s lékařem, aby vyloučil těhotenství, a teprve poté pokračovat v užívání z dalšího balení. Jestliže bylo opomenuto užití tablet a došlo-li týden předtím k pohlavnímu styku, je možné uvažovat o těhotenství. Je třeba neprodleně informovat lékaře a zahájit používání doplňkové metody antikoncepce. Co dělat, když dojde ke zvracení? Dojde-li ke zvracení do 3 4 hodin po podání potahované tablety, nemusí dojít k úplnému vstřebání účinných látek. To je podobný případ, jako když se zapomene užít tableta a proto se postupuje stejně, jak je výše uvedeno. Předávkování Po akutním užití velkých dávek přípravku malými dětmi nedošlo k žádnému závažnému účinku. Předávkování může vyvolat nevolnost a u žen krvácení z hormonálního spádu. V případě předávkování se poraďte s lékařem. Upozornění Předtím, než začnete užívat LINDYNETTE 30: je třeba se podrobit celkové lékařské prohlídce a vyhodnocení onemocnění v rodině. V průběhu dlouhodobého užívání se budete muset podrobit pravidelné kontrole zdravotního stavu, vždy nejméně jedenkrát za rok. Jestliže se u vás nebo ve vaší rodině v minulosti vyskytlo některé z následujících onemocnění, informujte o tom svého lékaře: - Rakovina prsu, uzlíky prsu, vazivové uzlíky prsu, neobvyklé nálezy při rentgenologickém nebo mamografickém vyšetření prsů. - Cukrovka (diabetes). - Zvýšené hladiny tuků (cholesterolu nebo triglyceridů). - Vysoký krevní tlak. - Migréna, jiné bolesti hlavy nebo epilepsie. - Psychická deprese. - Žlučníkové, srdeční nebo ledvinové onemocnění. Kombinovaná orální kontraceptiva musí být předepisována s opatrností u pacientek, které mají sklony k zadržování tekutin v organismu. Uživatelky orální antikoncepce s výše uvedenými stavy musí být vyšetřovány častěji. Lékař by měl být také informován v případě, že žena kouří nebo užívá další léky. Kouření cigaret zvyšuje riziko závažných nežádoucích účinků na srdce a krevní oběh. Toto riziko se zvyšuje s věkem a počtem vykouřených cigaret (15 a více cigaret denně) a je zcela zřetelné u žen nad 35 let věku. Ženy užívající orální antikoncepci nemají kouřit. 6/8
7 Vynechání krvácení a podávání před otěhotněním nebo v ranném těhotenství. V průběhu užívání může dojít k situacím, kdy se nedostaví krvácení z hormonálního spádu po využívání celého balení orálního kontraceptiva. Jestliže tablety byly užívány správně podle návodu a jednou se nedostaví krvácení z hormonálního spádu, pokračujte v užívání z nového balení a pro jistotu informujte lékaře. Jestliže jste neužívala přípravek tak, jak uvádí příbalový leták a nedostala jste menstruační krvácení, nebo se nedostavilo krvácení již dvakrát za sebou, můžete být těhotná. V takovém případě je třeba ihned informovat lékaře a přestat užívat orální antikoncepci, dokud se nevyloučí těhotenství. V mezidobí je třeba používat jinou metodu nehormonální antikoncepce jako např. kondom se spermicidem. Není prokázáno, že by podávání orální antikoncepce v ranném těhotenství vedlo ke zvýšení incidence novorozeneckých vad. Přesto Vám lékař nepředepíše orální kontraceptiva ani žádné další léky v průběhu těhotenství kromě případů, kdy je to zcela nezbytné. Míra rizika užívání v tomto případě musí být pečlivě zvážena lékařem před zahájením užívání. Těhotenství po ukončení užívání orální antikoncepce Je možné, že mezi ukončením užívání orální antikoncepce a skutečným otěhotněním dojde k určité časové prodlevě, zvláště u žen, které měly nepravidelný cyklus před zahájením podávání orální antikoncepce. Při žádoucím otěhotnění může být prospěšné počkat s početím do doby, až se po ukončení užívání orální antikoncepce obnoví pravidelný menstruační cyklus. Nebylo prokázáno zvýšení incidence novorozeneckých defektů v případě otěhotnění brzy po ukončení užívání orální antikoncepce. Podávání v průběhu kojení Protože některá léčiva mohou přecházet do mateřského mléka, je třeba se o možnosti začít užívat orální antikoncepci v průběhu kojení poradit nejdříve s lékařem. Bylo pozorováno několik nežádoucích účinků u kojených dětí, včetně zežloutnutí kůže (žloutenka) a zvětšení prsů. Kromě toho orální kontraceptiva mohou snížit množství a kvalitu mateřského mléka, proto by orální antikoncepce neměla být podávána po dobu kojení. Po dobu kojení by měla být používána jiná antikoncepční metoda, protože kojení představuje pouze částečnou ochranu proti otěhotnění a tato částečná ochrana se ještě snižuje v průběhu dlouhodobého kojení. O zahájení užívání orální antikoncepce se má uvažovat až po úplném odstavení dítěte. Zvláštní upozornění Tento přípravek (tak jako všechna orální kontraceptiva) zabraňuje otěhotnění. Nechrání proti infekci HIV (AIDS) ani proti jiným nemocem, přenášeným pohlavním stykem. Každá žena, která zvažuje užívání orální antikoncepce by měla znát výhody a rizika používání tohoto způsobu řízení otěhotnění. Příbalový leták poskytuje řadu informací k takovému rozhodnutí a pomůže také stanovit míru rizika rozvoje nežádoucích účinků spojených s užíváním. Podává informace, jak přesně přípravek užívat, aby byl maximálně účinný. Nemůže však nahradit pozorný rozhovor mezi pacientkou a lékařem. Informace podané v tomto příbalovém letáku mají být předmětem diskuse lékaře s pacientkou vždy před zahájením užívání a v průběhu každé další návštěvy u lékaře. Rady lékaře, které vyplývají z této diskuse je třeba dodržovat. Toto léčivo nesmí být podáváno k žádnému jinému účelu, než pro který bylo předepsáno. Pacientka je také nesmí poskytnout žádné jiné osobě k prevenci otěhotnění. Uchovávání Uchovávejte při teplotě do 30 0 C. Varování 7/8
8 Přípravek nesmí být používán po uplynutí doby použitelnosti vyznačené na obalu a při zřetelném poškození jako je např. změna barvy nebo mechanické poškození potahovaných tablet. Přípravek musí být uchováván mimo dosah a dohled dětí. Balení 1 x 21 a 3 x 21 obalených tablet Datum poslední revize: /8
PŘÍBALOVÁ INFORMACE. Informace pro použití, čtěte pozorně! LINDYNETTE 20 obalené tablety k vnitřnímu užití
 PŘÍBALOVÁ INFORMACE Informace pro použití, čtěte pozorně! LINDYNETTE 20 obalené tablety k vnitřnímu užití Výrobce a držitel registračního rozhodnutí Chemical Works of Gedeon Richter Ltd. Budapešť, Maďarsko
PŘÍBALOVÁ INFORMACE Informace pro použití, čtěte pozorně! LINDYNETTE 20 obalené tablety k vnitřnímu užití Výrobce a držitel registračního rozhodnutí Chemical Works of Gedeon Richter Ltd. Budapešť, Maďarsko
RADA A POUČENÍ LÉKAŘE
 RADA A POUČENÍ LÉKAŘE Obsah: Uživatelky kombinované hormonální antikoncepce Léčebné účinky kombinované hormonální antikoncepce Kontraindikace kombinované hormonální antikoncepce Vysvětlivky: COC = z anglického
RADA A POUČENÍ LÉKAŘE Obsah: Uživatelky kombinované hormonální antikoncepce Léčebné účinky kombinované hormonální antikoncepce Kontraindikace kombinované hormonální antikoncepce Vysvětlivky: COC = z anglického
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. DAISENETTE 75 MCG potahované tablety. desogestrelum
 Příloha č. 2 k rozhodnutí o registraci sp.zn.sukls122999/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DAISENETTE 75 MCG potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 2 k rozhodnutí o registraci sp.zn.sukls122999/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DAISENETTE 75 MCG potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci
RADA A POUČENÍ LÉKAŘE
 RADA A POUČENÍ LÉKAŘE KOMBINOVANÁ HORMONÁLNÍ ANTIKONCEPCE (MOŽNÉ UŽITÍ K YUZPEHO METODĚ) Obsah: a. Uživatelky kombinované hormonální antikoncepce b. Léčebné účinky kombinované hormonální antikoncepce c.
RADA A POUČENÍ LÉKAŘE KOMBINOVANÁ HORMONÁLNÍ ANTIKONCEPCE (MOŽNÉ UŽITÍ K YUZPEHO METODĚ) Obsah: a. Uživatelky kombinované hormonální antikoncepce b. Léčebné účinky kombinované hormonální antikoncepce c.
Příloha č. 2 k rozhodnutí o registraci sp. zn.:sukls107262/2011
 Příloha č. 2 k rozhodnutí o registraci sp. zn.:sukls107262/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE LAMYA 0,075 mg desogestrelum tablety Přečtěte si pozorně celou příbalovou informaci dříve, než
Příloha č. 2 k rozhodnutí o registraci sp. zn.:sukls107262/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE LAMYA 0,075 mg desogestrelum tablety Přečtěte si pozorně celou příbalovou informaci dříve, než
Příbalová informace: Informace pro uživatele. Zarelle 75 mikrogramů potahované tablety. desogestrelum
 Sp.zn.sukls59895/2013 Příbalová informace: Informace pro uživatele Zarelle 75 mikrogramů potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp.zn.sukls59895/2013 Příbalová informace: Informace pro uživatele Zarelle 75 mikrogramů potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE TRI-MINULET obalené tablety Ethinylestradiolum 0,030 mg, Gestodenum 0,050 mg
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE TRI-MINULET obalené tablety Ethinylestradiolum 0,030 mg, Gestodenum 0,050 mg - Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE TRI-MINULET obalené tablety Ethinylestradiolum 0,030 mg, Gestodenum 0,050 mg - Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls176965/2010 a příloha k sp.zn. sukls175819/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls176965/2010 a příloha k sp.zn. sukls175819/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CILEST, tablety norgestimatum/ethinylestradiolum Přečtěte
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls176965/2010 a příloha k sp.zn. sukls175819/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CILEST, tablety norgestimatum/ethinylestradiolum Přečtěte
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE. TRI-MINULET obalené tablety ethinylestradiolum/gestodenum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE TRI-MINULET obalené tablety ethinylestradiolum/gestodenum - Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. - Máte-li
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE TRI-MINULET obalené tablety ethinylestradiolum/gestodenum - Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. - Máte-li
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls143589/2012 a příloha ke sp.zn.sukls114150/2010, sukls226808/2012
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls143589/2012 a příloha ke sp.zn.sukls114150/2010, sukls226808/2012 Příbalová informace: informace pro uživatele Maitalon 3 mg/0,03 mg potahované
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls143589/2012 a příloha ke sp.zn.sukls114150/2010, sukls226808/2012 Příbalová informace: informace pro uživatele Maitalon 3 mg/0,03 mg potahované
PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta. UTROGESTAN 100 mg, měkké tobolky progesteronum
 sp.zn. sukls125023/2011 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta UTROGESTAN 100 mg, měkké tobolky progesteronum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls125023/2011 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta UTROGESTAN 100 mg, měkké tobolky progesteronum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
PROVERA 5 mg tablety (medroxyprogesteroni acetas)
 Příbalová informace: Informace pro uživatele PROVERA 5 mg tablety (medroxyprogesteroni acetas) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: Informace pro uživatele PROVERA 5 mg tablety (medroxyprogesteroni acetas) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls266850/2011
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls266850/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELKY Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls266850/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELKY Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat
Příloha č. 1 ke sdělení sp. zn. sukls161430/2011 a příloha ke sp. zn. sukls161393/2011
 Příloha č. 1 ke sdělení sp. zn. sukls161430/2011 a příloha ke sp. zn. sukls161393/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DUPHASTON, 10 mg, potahované tablety dydrogesteronum Přečtěte si pozorně
Příloha č. 1 ke sdělení sp. zn. sukls161430/2011 a příloha ke sp. zn. sukls161393/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DUPHASTON, 10 mg, potahované tablety dydrogesteronum Přečtěte si pozorně
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. VELAVEL 0,075 MG potahované tablety. Desogestrelum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VELAVEL 0,075 MG potahované tablety Desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VELAVEL 0,075 MG potahované tablety Desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
Příbalová informace: informace pro uživatele. DAISENETTE 75 MCG potahované tablety. desogestrelum
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls224251/2012 a příloha k sp.zn. sukls162703/2012 Příbalová informace: informace pro uživatele DAISENETTE 75 MCG potahované tablety desogestrelum
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls224251/2012 a příloha k sp.zn. sukls162703/2012 Příbalová informace: informace pro uživatele DAISENETTE 75 MCG potahované tablety desogestrelum
Livial tablety tibolonum
 Livial tablety tibolonum Příbalová informace - RP Informace pro použití, čtěte pozorně! Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou
Livial tablety tibolonum Příbalová informace - RP Informace pro použití, čtěte pozorně! Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou
Příloha č. 1 ke sdělení sp.zn. sukls9943/2012
 Příloha č. 1 ke sdělení sp.zn. sukls9943/2012 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE HARMONET obalené tablety Ethinylestradiolum, Gestodenum Přečtěte si pozorně celou příbalovou informaci dříve, než
Příloha č. 1 ke sdělení sp.zn. sukls9943/2012 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE HARMONET obalené tablety Ethinylestradiolum, Gestodenum Přečtěte si pozorně celou příbalovou informaci dříve, než
Příbalová informace: informace pro uživatelku. POSTINOR mikrogramů tablety levonorgestrelum
 Příbalová informace: informace pro uživatelku POSTINOR-2 750 mikrogramů tablety levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatelku POSTINOR-2 750 mikrogramů tablety levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls112215/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls112215/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE POSTINOR- 2 tablety levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci, protože
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls112215/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE POSTINOR- 2 tablety levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci, protože
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls55068/2009
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls55068/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AGOFOLLIN Injekční roztok (Estradioli dipropionas) Přečtěte si pozorně celou příbalovou
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls55068/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AGOFOLLIN Injekční roztok (Estradioli dipropionas) Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele. FLORETTE 0,075 MG potahované tablety. Desogestrelum
 sp.zn. sukls214464/2014 Příbalová informace: informace pro uživatele FLORETTE 0,075 MG potahované tablety Desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls214464/2014 Příbalová informace: informace pro uživatele FLORETTE 0,075 MG potahované tablety Desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
20 mikrogramů/24 hodin, intrauterinní inzert
 sp.zn.sukls206879/2010 Příbalová informace: informace pro uživatele 20 mikrogramů/24 hodin, intrauterinní inzert (levonorgestrelum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.sukls206879/2010 Příbalová informace: informace pro uživatele 20 mikrogramů/24 hodin, intrauterinní inzert (levonorgestrelum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatelku. POSTINOR- 2 750 mikrogramů tablety levonorgestrelum
 Příbalová informace: informace pro uživatelku POSTINOR- 2 750 mikrogramů tablety levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatelku POSTINOR- 2 750 mikrogramů tablety levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
zpět na stránku produktu zpět na obdobná léčiva
 sp.zn.sukls114756/2013 Příbalová informace: informace pro uživatele www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva Escapelle, 1500 mikrogramů, tableta Levonorgestrelum Přečtěte si
sp.zn.sukls114756/2013 Příbalová informace: informace pro uživatele www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva Escapelle, 1500 mikrogramů, tableta Levonorgestrelum Přečtěte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. GRACIAL tablety k perorálnímu podání (desogestrelum, ethinylestradiolum)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE GRACIAL tablety k perorálnímu podání (desogestrelum, ethinylestradiolum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE GRACIAL tablety k perorálnímu podání (desogestrelum, ethinylestradiolum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
TRINOVUM tablety ethinylestradiolum, norethisteronum
 Příbalová informace: informace pro uživatele TRINOVUM tablety ethinylestradiolum, norethisteronum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele TRINOVUM tablety ethinylestradiolum, norethisteronum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls117542/2010 PŘÍBALOVÁ INFORMACE
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls117542/2010 PŘÍBALOVÁ INFORMACE Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls117542/2010 PŘÍBALOVÁ INFORMACE Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
Příloha č. 1 k rozhodnutí o registraci sp. zn.:sukls120495/2011
 Příloha č. 1 k rozhodnutí o registraci sp. zn.:sukls120495/2011 Příbalová informace: informace pro uživatele Evellien 0,075 mg (desogestrelum) Potahované tablety Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp. zn.:sukls120495/2011 Příbalová informace: informace pro uživatele Evellien 0,075 mg (desogestrelum) Potahované tablety Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Mistra 2 mg/0,03 mg potahované tablety Dienogestum a ethinylestradiolum
 Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls59932/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Mistra 2 mg/0,03 mg potahované tablety Dienogestum a ethinylestradiolum Přečtěte si pozorně celou
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls59932/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Mistra 2 mg/0,03 mg potahované tablety Dienogestum a ethinylestradiolum Přečtěte si pozorně celou
Příbalová informace: informace pro uživatelky. Zafrilla 2 mg tablety dienogestum
 Příbalová informace: informace pro uživatelky Zafrilla 2 mg tablety dienogestum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité
Příbalová informace: informace pro uživatelky Zafrilla 2 mg tablety dienogestum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité
PŘÍBALOVÁ INFORMACE. Informace pro použití, čtěte pozorně! TRIAKLIM. Výrobce a držitel registračního rozhodnutí. Složení.
 PŘÍBALOVÁ INFORMACE Informace pro použití, čtěte pozorně! TRIAKLIM Potahované tablety k vnitřnímu užití. Výrobce a držitel registračního rozhodnutí Chemical Works of Gedeon Richter Ltd. Gyömröi út 19-21,
PŘÍBALOVÁ INFORMACE Informace pro použití, čtěte pozorně! TRIAKLIM Potahované tablety k vnitřnímu užití. Výrobce a držitel registračního rozhodnutí Chemical Works of Gedeon Richter Ltd. Gyömröi út 19-21,
Příbalová informace: Informace pro uživatele. Ramonna 1500 mikrogramů, tableta Levonorgestrelum
 Příbalová informace: Informace pro uživatele 1500 mikrogramů, tableta Levonorgestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás
Příbalová informace: Informace pro uživatele 1500 mikrogramů, tableta Levonorgestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás
PŘÍBALOVÁ INFORMACE. MINESSE potahované tablety gestodenum/ ethinylestradiolum
 sp.zn. sukls86673/2013 PŘÍBALOVÁ INFORMACE MINESSE potahované tablety gestodenum/ ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
sp.zn. sukls86673/2013 PŘÍBALOVÁ INFORMACE MINESSE potahované tablety gestodenum/ ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
Příbalová informace: Informace pro uživatele. Loette potahované tablety 100 mikrogramů / 20 mikrogramů levonorgestrelum, ethinylestradiolum,
 Příbalová informace: Informace pro uživatele Loette potahované tablety 100 mikrogramů / 20 mikrogramů levonorgestrelum, ethinylestradiolum, Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příbalová informace: Informace pro uživatele Loette potahované tablety 100 mikrogramů / 20 mikrogramů levonorgestrelum, ethinylestradiolum, Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příloha č. 1 ke sdělení sp.zn.sukls270387/2012 a sukls270395/2012
 Příloha č. 1 ke sdělení sp.zn.sukls270387/2012 a sukls270395/2012 Příbalová informace: informace pro uživatele Tamoxifen Ebewe 10 mg Tamoxifen Ebewe 20 mg tablety tamoxifeni citras Přečtěte si pozorně
Příloha č. 1 ke sdělení sp.zn.sukls270387/2012 a sukls270395/2012 Příbalová informace: informace pro uživatele Tamoxifen Ebewe 10 mg Tamoxifen Ebewe 20 mg tablety tamoxifeni citras Přečtěte si pozorně
Příbalová informace: informace pro uživatelku. Escapelle, 1500 mikrogramů, tableta Levonorgestrelum
 Sp.zn.sukls170715/2014 A sp.zn.sukls238446/2012, sukls41514/2013 Příbalová informace: informace pro uživatelku Escapelle, 1500 mikrogramů, tableta Levonorgestrelum Přečtěte si pozorně celou příbalovou
Sp.zn.sukls170715/2014 A sp.zn.sukls238446/2012, sukls41514/2013 Příbalová informace: informace pro uživatelku Escapelle, 1500 mikrogramů, tableta Levonorgestrelum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatelku. Escapelle 1500 mikrogramů, tableta Levonorgestrelum
 Příbalová informace: informace pro uživatelku Escapelle 1500 mikrogramů, tableta Levonorgestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatelku Escapelle 1500 mikrogramů, tableta Levonorgestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatele. Mertenil 40 mg potahované tablety. rosuvastatinum
 Sp.zn.sukls55651/2013 Příbalová informace: informace pro uživatele Mertenil 10 mg potahované tablety Mertenil 20 mg potahované tablety Mertenil 40 mg potahované tablety rosuvastatinum Přečtěte si pozorně
Sp.zn.sukls55651/2013 Příbalová informace: informace pro uživatele Mertenil 10 mg potahované tablety Mertenil 20 mg potahované tablety Mertenil 40 mg potahované tablety rosuvastatinum Přečtěte si pozorně
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Escapelle, tablety Levonorgestrelum
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls112213/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Escapelle, tablety Levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci, protože
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls112213/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Escapelle, tablety Levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci, protože
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CERAZETTE 75 mikrogramů tablety k perorálnímu podání (desogestrelum)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CERAZETTE 75 mikrogramů tablety k perorálnímu podání (desogestrelum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CERAZETTE 75 mikrogramů tablety k perorálnímu podání (desogestrelum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
Azalia 75 mikrogramů potahované tablety desogestrelum
 Příbalová informace: informace pro uživatelku Azalia 75 mikrogramů potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatelku Azalia 75 mikrogramů potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. AZALIA 75 mikrogramů potahované tablety desogestrelum
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls252226/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AZALIA 75 mikrogramů potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls252226/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AZALIA 75 mikrogramů potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatelku Evellien 0,075 mg (desogestrelum) Potahované tablety
 sp.zn. sukls55279/2015 Příbalová informace: informace pro uživatelku Evellien 0,075 mg (desogestrelum) Potahované tablety Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls55279/2015 Příbalová informace: informace pro uživatelku Evellien 0,075 mg (desogestrelum) Potahované tablety Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Důležité informace o užívání přípravku TASIGNA
 Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Příbalová informace: informace pro uživatelku. CERAZETTE 0,075 mg, potahované tablety desogestrelum
 Příbalová informace: informace pro uživatelku CERAZETTE 0,075 mg, potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatelku CERAZETTE 0,075 mg, potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Daylette 3 mg / 0,02 mg potahované tablety drospirenonum / ethinylestradiolum
 Sp.zn.sukls110452/2013 Příbalová informace - informace pro uživatele 3 mg / 0,02 mg potahované tablety drospirenonum / ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Sp.zn.sukls110452/2013 Příbalová informace - informace pro uživatele 3 mg / 0,02 mg potahované tablety drospirenonum / ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Klimonorm estradioli valeras, levonorgestrelum obalené tablety
 Sp.zn.:sukls252551/2011 Příbalová informace: informace pro pacienta Klimonorm estradioli valeras, levonorgestrelum obalené tablety Pečlivě si přečtěte celou příbalovou informaci dříve, než začnete tento
Sp.zn.:sukls252551/2011 Příbalová informace: informace pro pacienta Klimonorm estradioli valeras, levonorgestrelum obalené tablety Pečlivě si přečtěte celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. PRAMINO PRAMINO 28 tablety norgestimatum/ethinylestradiolum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PRAMINO PRAMINO 28 tablety norgestimatum/ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PRAMINO PRAMINO 28 tablety norgestimatum/ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. DESOGESTREL STADA 0,075 mg tablety desogestrelum
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls29622/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DESOGESTREL STADA 0,075 mg tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls29622/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DESOGESTREL STADA 0,075 mg tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE. Daylla 3 mg / 0,02 mg potahované tablety drospirenonum / ethinylestradiolum
 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Daylla 3 mg / 0,02 mg potahované tablety drospirenonum / ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Daylla 3 mg / 0,02 mg potahované tablety drospirenonum / ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Gravistat 125 Obalené tablety (ethinylestradiolum, levonorgestrelum)
 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELKY Gravistat 125 Obalené tablety (ethinylestradiolum, levonorgestrelum) Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELKY Gravistat 125 Obalené tablety (ethinylestradiolum, levonorgestrelum) Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat
2. Čemu musíte věnovat pozornost, než začnete APO-DONEPEZIL užívat
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls122778/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-DONEPEZIL 5 mg potahované tablety APO-DONEPEZIL 10 mg potahované tablety Přečtěte si
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls122778/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-DONEPEZIL 5 mg potahované tablety APO-DONEPEZIL 10 mg potahované tablety Přečtěte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE. MINULET obalené tablety ethinylestradiolum, gestodenum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE MINULET obalené tablety ethinylestradiolum, gestodenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat - Ponechte si
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE MINULET obalené tablety ethinylestradiolum, gestodenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat - Ponechte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Crinone 8 % (Progesteronum) vaginální gel
 sp. zn. sukls223332/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Crinone 8 % (Progesteronum) vaginální gel Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat
sp. zn. sukls223332/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Crinone 8 % (Progesteronum) vaginální gel Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat
Pečlivě si přečtěte celou příbalovou informaci dříve, než začnete tento přípravek užívat.
 sp. zn. sukls57616/2013 Informace pro použití, čtěte pozorně Pečlivě si přečtěte celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci pro případ, že si
sp. zn. sukls57616/2013 Informace pro použití, čtěte pozorně Pečlivě si přečtěte celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci pro případ, že si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE- VP
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn.: sukls237631/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE- VP ZODAC potahované tablety (cetirizini dihydrochloridum) Přečtěte si pozorně tuto příbalovou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.: sukls237631/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE- VP ZODAC potahované tablety (cetirizini dihydrochloridum) Přečtěte si pozorně tuto příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Agnucaston potahované tablety Agni casti fructus extractum siccum
 sp.zn.sukls289285/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Agnucaston potahované tablety Agni casti fructus extractum siccum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn.sukls289285/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Agnucaston potahované tablety Agni casti fructus extractum siccum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE. HARMONET obalené tablety ethinylestradiolum, gestodenum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE HARMONET obalené tablety ethinylestradiolum, gestodenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat - Ponechte si
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE HARMONET obalené tablety ethinylestradiolum, gestodenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat - Ponechte si
Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls145359/2011 a příloha k sp. zn. sukls178993/2011. Příbalová informace
 Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls145359/2011 a příloha k sp. zn. sukls178993/2011 Příbalová informace Vreya potahované tablety Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls145359/2011 a příloha k sp. zn. sukls178993/2011 Příbalová informace Vreya potahované tablety Přečtěte si pozorně celou příbalovou informaci dříve,
Paralen Grip chřipka a kašel potahované tablety (paracetamolum, dextromethorphani hydrobromidum monohydricum, phenylephrini hydrochloridum)
 Příloha č. 2 ke sdělení sp.zn.sukls96119/2011 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Paralen Grip chřipka a kašel potahované tablety (paracetamolum, dextromethorphani hydrobromidum monohydricum, phenylephrini
Příloha č. 2 ke sdělení sp.zn.sukls96119/2011 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Paralen Grip chřipka a kašel potahované tablety (paracetamolum, dextromethorphani hydrobromidum monohydricum, phenylephrini
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE. NEOFOLLIN Injekční roztok Estradioli valeras
 sp. zn. sukls75049/2013 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE NEOFOLLIN Injekční roztok Estradioli valeras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp. zn. sukls75049/2013 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE NEOFOLLIN Injekční roztok Estradioli valeras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bromhexin 8 Berlin-Chemie 8 mg, obalené tablety (Léčivá látka: bromhexini hydrochloridum)
 sp.zn. sukls162249/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bromhexin 8 Berlin-Chemie 8 mg, obalené tablety (Léčivá látka: bromhexini hydrochloridum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls162249/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bromhexin 8 Berlin-Chemie 8 mg, obalené tablety (Léčivá látka: bromhexini hydrochloridum) Přečtěte si pozorně tuto příbalovou informaci
EXESTEA 25 mg Potahované tablety Exemestanum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE EXESTEA 25 mg Potahované tablety Exemestanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE EXESTEA 25 mg Potahované tablety Exemestanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
Příloha č. 1 k rozhodnutí o registraci sp.zn.sukls94253/2011
 Příloha č. 1 k rozhodnutí o registraci sp.zn.sukls94253/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Yosefinne 0,02 mg/3mg potahované tablety Ethinylestradiolum/ Drospirenonum Přečtěte si pozorně
Příloha č. 1 k rozhodnutí o registraci sp.zn.sukls94253/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Yosefinne 0,02 mg/3mg potahované tablety Ethinylestradiolum/ Drospirenonum Přečtěte si pozorně
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CYSAXAL 100 mg tablety. Léčivá látka: Cyproteroni acetas
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CYSAXAL 100 mg tablety Léčivá látka: Cyproteroni acetas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CYSAXAL 100 mg tablety Léčivá látka: Cyproteroni acetas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
Příbalová informace: informace pro uživatele Binabic 150 mg, potahované tablety Bicalutamidum
 Sp.zn. sukls91007/2014 Příbalová informace: informace pro uživatele Binabic 150 mg, potahované tablety Bicalutamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Sp.zn. sukls91007/2014 Příbalová informace: informace pro uživatele Binabic 150 mg, potahované tablety Bicalutamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Quetiapin Reg Europe 25 mg Quetiapin Reg Europe 100 mg Quetiapin Reg Europe 150 mg Quetiapin Reg Europe 200 mg Quetiapin Reg Europe 300 mg
 Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls95277/2009, sukls95278/2009, sukls95279/2009, sukls95280/2009, sukls95281/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Quetiapin Reg Europe 25 mg
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls95277/2009, sukls95278/2009, sukls95279/2009, sukls95280/2009, sukls95281/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Quetiapin Reg Europe 25 mg
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge
 Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge Erivedge může způsobit závažné vrozené vady Může vést
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge Erivedge může způsobit závažné vrozené vady Může vést
Levonorgestrel Zentiva 1,5 mg tableta levonorgestrelum
 Sp.zn.sukls160838/2016 Příbalová informace: informace pro uživatele Levonorgestrel Zentiva 1,5 mg tableta levonorgestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp.zn.sukls160838/2016 Příbalová informace: informace pro uživatele Levonorgestrel Zentiva 1,5 mg tableta levonorgestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Biologie člověka Uspořádání pohlavních orgánů Vnitřní pohlavní orgány ženy Ve vaječnících dozrávají vajíčka (největší buňka lidského těla, obsahuje 23
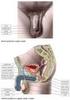 Výchova ke zdraví, sexuální výchova Lekce 3 Obsah: 1) krátké zopakování minulé lekce (anatomické uspořádání pohlavních orgánů a jejich funkce, menstruační cyklus, početí a vývoj plodu, těhotenství ) 2)
Výchova ke zdraví, sexuální výchova Lekce 3 Obsah: 1) krátké zopakování minulé lekce (anatomické uspořádání pohlavních orgánů a jejich funkce, menstruační cyklus, početí a vývoj plodu, těhotenství ) 2)
Příbalová informace: informace pro uživatele
 Sp.zn.sukls7954/2014 Příbalová informace: informace pro uživatele TORRI 0,075 mg tablety Desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Sp.zn.sukls7954/2014 Příbalová informace: informace pro uživatele TORRI 0,075 mg tablety Desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Sp.zn. sukls190258/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Astexana 25 mg Potahované tablety Exemestanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Sp.zn. sukls190258/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Astexana 25 mg Potahované tablety Exemestanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příloha č. 1 k opravě rozhodnutí o prodloužení sp. zn.: sukls23177/2007
 Příloha č. 1 k opravě rozhodnutí o prodloužení sp. zn.: sukls23177/2007 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE METFORMIN 850 MG ZENTIVA potahované tablety metformini hydrochloridum Přečtěte si pozorně
Příloha č. 1 k opravě rozhodnutí o prodloužení sp. zn.: sukls23177/2007 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE METFORMIN 850 MG ZENTIVA potahované tablety metformini hydrochloridum Přečtěte si pozorně
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
 Příloha č. 2 k rozhodnutí o nové registraci sp.zn.sukls208329/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sylviane 0,03 mg/3 mg potahované tablety Ethinylestradiolum / drospirenonum Přečtěte si pozorně
Příloha č. 2 k rozhodnutí o nové registraci sp.zn.sukls208329/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sylviane 0,03 mg/3 mg potahované tablety Ethinylestradiolum / drospirenonum Přečtěte si pozorně
Příbalová informace: informace pro uživatele AESCIN-TEVA. 20 mg, enterosolventní tablety. escinum alfa
 sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
MINULET obalené tablety ethinylestradiolum, gestodenum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE MINULET obalené tablety ethinylestradiolum, gestodenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat - Ponechte si
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE MINULET obalené tablety ethinylestradiolum, gestodenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat - Ponechte si
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls19853/2007
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls19853/2007 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HALOPERIDOL-RICHTER injekční roztok 5x1ml/5mg haloperidolum Přečtěte si pozorně celou
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls19853/2007 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HALOPERIDOL-RICHTER injekční roztok 5x1ml/5mg haloperidolum Přečtěte si pozorně celou
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE. Tessyron 75 mg potahované tablety clopidogrelum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Tessyron 75 mg potahované tablety clopidogrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Tessyron 75 mg potahované tablety clopidogrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou
Příbalová informace: Informace pro uživatele. Bromhexin 8 Berlin-Chemie 8 mg, obalené tablety bromhexini hydrochloridum
 sp.zn.sukls34096/2016 Příbalová informace: Informace pro uživatele Bromhexin 8 Berlin-Chemie 8 mg, obalené tablety bromhexini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
sp.zn.sukls34096/2016 Příbalová informace: Informace pro uživatele Bromhexin 8 Berlin-Chemie 8 mg, obalené tablety bromhexini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls197996/2010
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls197996/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Anaprex 1 mg potahované tablety anastrozolum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls197996/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Anaprex 1 mg potahované tablety anastrozolum Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro pacienta. XYNIA 0,075 mg potahované tablety. desogestrelum
 sp.zn.sukls236797/2015 Příbalová informace: informace pro pacienta XYNIA 0,075 mg potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn.sukls236797/2015 Příbalová informace: informace pro pacienta XYNIA 0,075 mg potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE!1 Příbalová informace: informace pro uživatele Esmya 5 mg tablety Ulipristali acetas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
B. PŘÍBALOVÁ INFORMACE!1 Příbalová informace: informace pro uživatele Esmya 5 mg tablety Ulipristali acetas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro uživatele. Protevasc 35 mg tablety s prodlouženým uvolňováním trimetazidini dihydrochloridum
 Příbalová informace: informace pro uživatele Protevasc 3 mg tablety s prodlouženým uvolňováním trimetazidini dihydrochloridum % Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro uživatele Protevasc 3 mg tablety s prodlouženým uvolňováním trimetazidini dihydrochloridum % Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Vyberte si správnou antikoncepci
 Vyberte si správnou antikoncepci Ženy mají v dnešní době úžasnou možnost rozhodnout nejen o tom, kolik budou mít dětí, ale také o načasování těhotenství. To už není pro ženu nutnou povinností, ale svobodnou
Vyberte si správnou antikoncepci Ženy mají v dnešní době úžasnou možnost rozhodnout nejen o tom, kolik budou mít dětí, ale také o načasování těhotenství. To už není pro ženu nutnou povinností, ale svobodnou
Příbalová informace: informace pro pacienta. Cerseii 0,02 mg/3 mg potahované tablety Ethinylestradiolum/Drospirenonum
 Sp. zn. sukls277320/2012 Příbalová informace: informace pro pacienta Cerseii 0,02 mg/3 mg potahované tablety Ethinylestradiolum/Drospirenonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Sp. zn. sukls277320/2012 Příbalová informace: informace pro pacienta Cerseii 0,02 mg/3 mg potahované tablety Ethinylestradiolum/Drospirenonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn.: sukls256710/2012
 sp.zn.: sukls256710/2012 Příbalová informace - informace pro uživatelky Lindynette 20 75 mikrogramů + 20 mikrogramů obalené tablety Gestodenum/ Ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci
sp.zn.: sukls256710/2012 Příbalová informace - informace pro uživatelky Lindynette 20 75 mikrogramů + 20 mikrogramů obalené tablety Gestodenum/ Ethinylestradiolum Přečtěte si pozorně celou příbalovou informaci
Magnesii lactici 0,5 tbl. Medicamenta tablety Magnesii lactas dihydricus
 sp.zn. sukls53238/2016 Příbalová informace: informace pro uživatele Magnesii lactici 0,5 tbl. Medicamenta tablety Magnesii lactas dihydricus Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
sp.zn. sukls53238/2016 Příbalová informace: informace pro uživatele Magnesii lactici 0,5 tbl. Medicamenta tablety Magnesii lactas dihydricus Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
Příloha č. 2 ke sdělení sp. zn. sukls227595/2011. Příbalová informace - Rp Informace pro použití, čtěte pozorně
 Příloha č. 2 ke sdělení sp. zn. sukls227595/2011 Příbalová informace - Rp Informace pro použití, čtěte pozorně Přečtěte si pozorně celou příbalovou informaci dříve, než začnete užívat Femoden. Ponechte
Příloha č. 2 ke sdělení sp. zn. sukls227595/2011 Příbalová informace - Rp Informace pro použití, čtěte pozorně Přečtěte si pozorně celou příbalovou informaci dříve, než začnete užívat Femoden. Ponechte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Rhonya 3 mg/ 30 µg potahované tablety drospirenonum/ethinylestradiolum
 Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls187238/2011 a příloha k sp.zn.sukls265272/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Rhonya 3 mg/ 30 µg potahované tablety drospirenonum/ethinylestradiolum
Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls187238/2011 a příloha k sp.zn.sukls265272/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Rhonya 3 mg/ 30 µg potahované tablety drospirenonum/ethinylestradiolum
Příbalová informace: informace pro uživatelku. Tri-Regol, obalené tablety (levonorgestrelum, ethinylestradiolum)
 Příbalová informace: informace pro uživatelku Tri-Regol, obalené tablety (levonorgestrelum, ethinylestradiolum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: informace pro uživatelku Tri-Regol, obalené tablety (levonorgestrelum, ethinylestradiolum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: Informace pro uživatele. Bromhexin Berlin-Chemie 8 mg obalené tablety bromhexini hydrochloridum
 sp. zn. sukls212749/2018 Příbalová informace: Informace pro uživatele Bromhexin Berlin-Chemie 8 mg obalené tablety bromhexini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
sp. zn. sukls212749/2018 Příbalová informace: Informace pro uživatele Bromhexin Berlin-Chemie 8 mg obalené tablety bromhexini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls248891/2010
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls248891/2010 PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE Mertenil 5 mg potahované tablety Mertenil 10 mg potahované tablety Mertenil 20 mg potahované
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls248891/2010 PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE Mertenil 5 mg potahované tablety Mertenil 10 mg potahované tablety Mertenil 20 mg potahované
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 1. NÁZEV PŘÍPRAVKU Ramonna 1500 mikrogramů, tableta
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ramonna 1500 mikrogramů, tableta 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje levonorgestrelum1500 mikrogramů. Pomocné látky se známým účinkem:
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Ramonna 1500 mikrogramů, tableta 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje levonorgestrelum1500 mikrogramů. Pomocné látky se známým účinkem:
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. TORVACARD 10 TORVACARD 20 TORVACARD 40 potahované tablety Atorvastatinum
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls96605/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE TORVACARD 10 TORVACARD 20 TORVACARD 40 potahované tablety Atorvastatinum Přečtěte si pozorně
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls96605/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE TORVACARD 10 TORVACARD 20 TORVACARD 40 potahované tablety Atorvastatinum Přečtěte si pozorně
BIKALARD 50 mg potahované tablety (bicalutamidum)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BIKALARD 50 mg potahované tablety (bicalutamidum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechejte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BIKALARD 50 mg potahované tablety (bicalutamidum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechejte si
Příbalová informace: informace pro pacienta. Norethisteron Zentiva 5 mg, tablety norethisteroni acetas
 sp. zn. sukls127842/2015 Příbalová informace: informace pro pacienta Norethisteron Zentiva 5 mg, tablety norethisteroni acetas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp. zn. sukls127842/2015 Příbalová informace: informace pro pacienta Norethisteron Zentiva 5 mg, tablety norethisteroni acetas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
