RotaTeq je určen k aktivní imunizaci kojenců ve věku od 6 týdnů za účelem prevence gastroenteritidy způsobené rotavirovou infekcí (viz bod 4.2).
|
|
|
- Antonín Esterka
- před 8 lety
- Počet zobrazení:
Transkript
1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům (živá, perorální) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna 2ml dávka obsahuje: Rotavirus sérotypus* G1 ne méně než 2, IU 1, 2 Rotavirus sérotypus* G2 ne méně než 2, IU 1, 2 Rotavirus sérotypus* G3 ne méně než 2, IU 1, 2 Rotavirus sérotypus* G4 ne méně než 2, IU 1, 2 Rotavirus sérotypus* P1[8] ne méně než 2, IU 1, 2 * humánní-bovinní rotavirové reasortanty (živé), vyrobené ve Vero buňkách. 1 infekční jednotky 2 jako spodní mez spolehlivosti (p = 0,95) Pomocné látky: Tato očkovací látka obsahuje mg sacharosy (viz bod 4.4). Úplný seznam pomocných látek viz bod LÉKOVÁ FORMA Perorální roztok Světle žlutá čirá tekutina, která může být až narůžovělá. 4. KLINICKÉ ÚDAJE 4.1 Terapeutické indikace RotaTeq je určen k aktivní imunizaci kojenců ve věku od 6 týdnů za účelem prevence gastroenteritidy způsobené rotavirovou infekcí (viz bod 4.2). V klinických studiích byla prokázána účinnost proti gastroenteritidě způsobené rotaviry sérotypů G1P1[8], G2P[4], G3P1[8], G4P1[8] a G9P1[8]. Viz body 4.4 a 5.1. RotaTeq by se měl podávat v souladu s oficiálními doporučeními. 4.2 Dávkování a způsob podání Dávkování Je nutno podat tři dávky očkovací látky RotaTeq. První dávku lze podat od věku šesti týdnů a ne později než ve věku 12. týdnů. 2
2 RotaTeq může být podáván předčasně narozeným dětem, jejichž gestační věk byl nejméně 25 týdnů. První dávka očkovací látky RotaTeq může být těmto dětem podána ve věku (nejméně) od 6. týdne po narození. Viz body 4.4.a 5.1. Mezi dávkami musí být intervaly nejméně 4 týdny. Je výhodnější, pokud jsou všechny tři dávky podány ve věku do týdnů. Všechny tři dávky by měly být podány do věku 26 týdnů. Protože nejsou k dispozici údaje o zaměnitelnosti vakcíny RotaTeq s jinými očkovací látkami proti rotaviru, doporučuje se, aby kojenci, jimž se jako první podá k imunizaci proti rotaviru očkovací látka RotaTeq, dostali další dávky téže vakcíny. Pokud je zřejmé nebo silně podezřelé, že nebyla polknuta úplná dávka (např. kojenec očkovací látku vyplivl nebo vyzvrátil), ze podat jednu náhradní dávku na stejné očkovací návštěvě, nicméně v klinických studiích nebyla tato možnost zkoušena. Pokud problém přetrvává, další náhradní dávky nesmí být podány. Po dokončení série 3 dávek se nedoporučuje podávat žádné další dávky (viz body 4.4 a 5.1 ohledně dostupných informací o přetrvávání ochrany). Způsob podání Pouze k perorálnímu podání. RotaTeq SE NESMÍ ZA ŽÁDNÝCH OKOLNOSTÍ APLIKOVAT INJEKČNĚ. RotaTeq lze podávat bez ohledu na konzumaci jídla, nápojů nebo mateřského mléka. Pokyny pro podání viz bod Kontraindikace Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku. Hypersenzitivita po předchozím podání vakcíny proti rotaviru. Předchozí anamnéza intususcepce. Jedinci s vrozenými malformacemi gastrointestinálního traktu, které by mohly predisponovat k intususcepci. Kojenci se známým deficitem imunity nebo s podezřením na něj. Neočekává se, že by asymptomatická infekce HIV ovlivnila bezpečnost nebo účinnost očkovací látky RotaTeq. Protože však neexistují dostatečné údaje, nedoporučuje se podávat RotaTeq kojencům s asymptomatickou infekcí HIV. U kojenců s akutním závažným horečnatým onemocněním je třeba podání očkovací látky RotaTeq odložit. Přítomnost lehké infekce není kontraindikací pro imunizaci. U kojenců s akutním průjmem nebo zvracením je třeba podání očkovací látky RotaTeq odložit. 3
3 4.4 Zvláštní upozornění a opatření pro použití K dispozici nejsou žádné údaje z klinických studií ohledně bezpečnosti ani účinnosti podávání očkovací látky RotaTeq kojencům se sníženou imunitou, kojencům infikovaným virem HIV nebo kojencům, u nichž byla v době od 42 dnů před podáním do 42 dnů po podání dávky očkovací látky RotaTeq provedena transfuze krve nebo jim byly podány imunoglobuliny. Případy gastroenteritidy v souvislosti s virem vakcíny byly hlášeny po uvedení přípravku na trh u kojenců s těžkou kombinovanou imunodeficiencí (combined immunodeficiency, SCID). Ve studiích se očkovací látka RotaTeq vylučovala stolicí u 8,9 % příjemců vakcíny téměř výhradně v týdnu po dávce 1 a pouze u jednoho příjemce vakcíny (0,3 %) po dávce 3. Vrchol exkrece nastal během 7 dní po dávce. Teoreticky je možné, že by se virus z vakcíny mohl přenést na séronegativní jedince. RotaTeq musí být podáván s opatrností jedincům, kteří jsou v úzkém kontaktu s osobami se sníženou imunitou (např. jedinci s malignitami nebo s jinak sníženou imunitou nebo jedinci dostávající imunosupresivní léčbu). Také osoby pečující o nedávno očkované by měly dodržovat přísnou hygienu zejména při manipulaci s exkrety. V klinických studiích byla očkovací látka Rotateq podávána přibližně dětem, které se narodily od 25. týdne do 36. týdne těhotenství. První očkovací dávka byla podána od 6. týdne po narození. Bezpečnost a účinnost očkovací látky Rotateq byla srovnatelná mezi touto podskupinou dětí a dětmi narozenými v termínu. Nicméně 19 z přibližně dětí se narodilo v 25. až 28. týdnu těhotenství, 55 se narodilo v 29. až 31. týdnu a zbytek se narodil ve 32. až 36. týdnu těhotenství. Viz body 4.2. a 5.1. Údaje o bezpečnosti a účinnosti u kojenců s aktivním onemocněním trávicího ústrojí (včetně chronického průjmu) nebo zpomaleným růstem nejsou k dispozici. Podávání očkovací látky RotaTeq je třeba zvážit u kojenců, u nichž by podle názoru lékaře mohlo nepodání vakcíny znamenat větší riziko. Úroveň ochrany poskytované očkovací látkou RotaTeq je založena na podání všech 3 dávek. Podobně jako u jiných vakcín nemusí vakcinace očkovací látkou RotaTeq zajistit úplnou ochranu všem příjemcům. Vakcína RotaTeq nechrání proti gastroenteritidám způsobeným jinými patogeny než rotaviry. Klinické studie účinnosti proti rotavirové gastroenteritidě byly provedeny v Evropě, USA, Latinské Americe a v Asii. V průběhu těchto studií byl nejčastějším sérotypem rotaviru v krevním oběhu G1P1[8]; zatímco rotaviry sérotypů G2P[4], G3P1[8], G4P1[8] a G9P1[8] byly zjišťovány méně často. Rozsah ochrany, který by mohl RotaTeq zajistit vůči jiným sérotypům rotavirů a v jiných populacích, není znám. K dispozici nejsou žádné klinické údaje ohledně použití očkovací látky RotaTeq k profylaxi po expozici infekci. Vakcína RotaTeq obsahuje sacharosu. Pacientům se vzácnými dědičnými problémy, jakými je intolerance fruktosy, malabsorpce glukosy a galaktosy nebo sacharoso-izomaltázová nedostatečnost, se nesmí tato očkovací látka podat. Možné riziko apnoe a nutnost monitorování dýchání po dobu hodin by se měly zvážit, když se podávají dávky základního očkování velmi předčasně narozeným dětem (narozené v 28. týdnu těhotenství) a zvláště těm, v jejichž předchozí anamnéze byla respirační nezralost. Protože prospěch očkování je u této skupiny dětí vysoký, neměla by se vakcinace odmítat ani oddalovat. 4
4 4.5 Interakce s jinými léčivými přípravky a jiné formy interakce Současné podávání očkovací látky RotaTeq s vakcínami obsahujícími jeden nebo více následujících antigenů ve věku přibližně 2, 4 a 6 měsíců prokázalo, že nedošlo k ovlivnění imunitních odpovědí a bezpečnostních profilů podávaných vakcín: - očkovací látka proti diftérii-tetanu-acelulární pertusi (DTaP) - očkovací látka proti Haemophilus influenzae typu b (Hib) - inaktivovaná očkovací látka proti poliomyelitidě (IPV) - očkovací látka proti hepatitidě B (HBV) - konjugovaná pneumokoková očkovací látka (PCV). Současné podávání očkovací látky RotaTeq s vakcínou proti DTaP-IPV-HBV-Hib (Infanrix hexa) ve věku přibližně 2, 3 a 4 měsíce prokázalo, že v porovnání se samostatnými podáními nedošlo k ovlivnění imunitních odpovědí a bezpečnostních profilů současně podávaných vakcín. Současné podávání očkovací látky RotaTeq s konjugovanou očkovací látkou proti meningokoku skupiny C (MenCC, hodnocenou vakcínou byl konjugovaný tetanový toxoid) ve věku 3 a 5 měsíců (a většinou ve stejnou dobu jako vakcína proti DTaP-IPV-Hib), následované třetí dávkou očkovací látky RotaTeq ve věku přibližně 6 měsíců, prokázalo, že imunitní odpovědi na vakcíny RotaTeq a MenCC nebyly ovlivněny. Současné podání vedlo k přijatelnému bezpečnostnímu profilu. Současné podávání očkovací látky RotaTeq a perorální vakcíny proti poliomyelitidě (OPV) neovlivnilo imunitní odpověď na antigeny polioviru. I když současné podávání OPV mírně snižovalo imunitní odpověď na očkovací látku proti rotaviru, současně není prokázáno, že může být ovlivněna klinická ochrana proti těžké rotavirové gastroenteritidě. Imunitní odpověď na RotaTeq nebyla ovlivněna, pokud byla OPV podána dva týdny po podání očkovací látky Rotateq. Proto lze přípravek RotaTeq podávat současně s monovalentními nebo kombinovanými dětskými vakcínami obsahujícími jeden nebo více z následujících antigenů: DTaP, Hib, IPV nebo OPV, HBV, PCV a MenCC. 4.6 Těhotenství a kojení RotaTeq je určen pouze pro použití u dětí. Údaje o použití v těhotenství nebo při kojení nejsou tudíž dostupné a reprodukční studie na zvířatech nebyly provedeny. 4.7 Účinky na schopnost řídit a obsluhovat stroje Není relevantní. 4.8 Nežádoucí účinky V podskupině kojenců ze 3 placebem kontrolovaných klinických studií (n = příjemců očkovací látky RotaTeq a příjemců placeba) byl RotaTeq hodnocen z hlediska všech nežádoucích účinků v době 42 dnů od vakcinace bez současného podání jiných pediatrických vakcín nebo s nimi. Nežádoucí účinky se vyskytly celkem u 47,0 % kojenců dostávajících RotaTeq ve srovnání s 45,8 % kojenců dostávajících placebo. Nejčastěji uváděné nežádoucí účinky, které se vyskytly častěji při podávání vakcíny než při podávání placeba, byly pyrexie (20,9 %), průjem (17,6 %) a zvracení (10,1 %). Nežádoucí účinky častější u očkované skupiny jsou uvedeny níže podle tříd orgánových systémů a četnosti výskytu. Na základě souhrnných údajů ze 3 klinických studií, ve kterých dostalo kojenců RotaTeq a kojenců placebo, se uvedené nežádoucí účinky vyskytly u příjemců očkovací látky RotaTeq s rozdílem incidencí mezi 0,2 % a 2,5 % ve srovnání s příjemci placeba. Četnosti výskytu byly hlášeny jako: 5
5 Velmi časté ( 1/10); časté ( 1/100, < 1/10); méně časté ( 1/1 000, < 1/100); vzácné ( 1/10 000, < 1/1 000) Infekce a infestace Časté: infekce horních cest dýchacích Méně časté: nazofaryngitida Gastrointestinální poruchy Velmi časté: průjem, zvracení Méně časté: bolest horní poloviny břicha Poruchy kůže a podkožní tkáně Méně časté: vyrážka Celkové poruchy a reakce v místě aplikace Velmi časté: pyrexie Závažné nežádoucí účinky byly hodnoceny u všech účastníků ( příjemců očkovací látky RotaTeq a příjemců placeba) 3 klinických studií až do 42 dnů po každé dávce. Celkový výskyt těchto závažných nežádoucích účinků dosáhl 0,1 % u příjemců očkovací látky RotaTeq a 0,2 % u příjemců placeba. Kawasakiho nemoc byla hlášena u 5 z příjemců vakcíny (< 0,1 %) a u 1 z příjemců placeba (< 0,1 %) s relativním rizikem (RR) 4,9 [95% CI; 0,6 239,1] (není statisticky významné). U dětí, kterým byla podávána očkovací látka RotaTeq ve velké neintervenční poregistrační studii bezpečnosti, žádné zvýšení rizika Kawasakiho nemoci nebylo pozorováno (viz bod 5.1). Otitis media a bronchospazmus byly uváděny u významně více příjemců vakcíny než u příjemců placeba; v případech, které podle hodnotícího lékaře souvisely s podáním vakcíny, však byla incidence otitis media (0,3 %) a bronchospazmu (< 0,1 %) stejná u příjemců vakcíny i placeba. Hematochezie byla hlášena jako nežádoucí účinek u 0,6 % (39/6, 130) příjemců vakcíny a u 0,6 % (34/5, 560) příjemců placeba do 42 dnů po každé dávce (rozdíly nebyly statisticky významné). Intususcepce Riziko intususcepce bylo posuzováno u kojenců v placebem kontrolované studii. V kombinovaných 42denních obdobích po každé dávce se vyskytlo 6 případů intususcepce u příjemců očkovací látky RotaTeq ve srovnání s 5 případy u příjemců placeba. 95 % CI pro relativní riziko byly 0,4, 6,4. V žádném období po žádné z dávek přitom nedocházelo k hromadění případů u příjemců očkovací látky RotaTeq. U dětí, kterým byla podávána očkovací látka RotaTeq ve velké neintervenční poregistrační studii bezpečnosti, žádné zvýšení rizika intususcepce nebylo pozorováno (viz bod 5.1) Hlášení po uvedení vakcíny na trh Následující nežádoucí účinky byly hlášeny spontánně u příjemců vakcíny Rotateq. Gastrointestinální poruchy: hematochezie Poruchy kůže a podkožní tkáně: kopřivka Další informace pro zvláštní populaci Apnoe u velmi předčasně narozených dětí ( 28. týden těhotenství) (viz bod 4.4). 4.9 Předávkování 6
6 K dispozici nejsou žádné údaje ohledně předávkování. 5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti Farmakoterapeutická skupina: virové vakcíny Kód ATC: J07BH02. Projektivní účinnost Účinnost očkovací látky RotaTeq byla hodnocena dvěma způsoby v placebem kontrolované studii REST (Rotavirus Efficacy and Safety Trial). 1. U očkovaných kojenců (2 834 ve skupině s očkovací látkou) se hodnotila účinnost ochrany jako snížení výskytu rotavirové (RV) gastroenteritidy vyvolané sérotypy proti nimž je očkovací látka zaměřena (G1-G4), která se vyskytla minimálně 14 dní po třetí dávce vakcíny během celé první rotavirové sezóny po vakcinaci. 2. U očkovaných kojenců ( ve skupině s očkovací látkou) se hodnotila účinnost ochrany jako pokles častosti hospitalizace a návštěv oddělení akutních příjmů v důsledku RV gastroenteritidy v době od 14 dnů po třetí dávce. Výsledky těchto analýz jsou uvedeny v následující tabulce. Snížení incidence RV gastroenteritidy po celou sezónu po vakcinaci (RotaTeq n = 2 834) % [95 % CI] Sérotyp Závažné onemocnění* (G1 G4) Stupeň závažnosti (G1 G4) 98,0 % 74,0 % 74,9 % [88,3 100,0] [66,8 79,9] G1 G2 G3 G4 G9 [67,3 80,9] [2,6 88,2] [< 0 99,6] [< 0 91,6] [< 0 99,3] 63,4 % 82,7 % 48,1 % 65,4 % * Závažná choroba je definována jako skóre >16/24 při použití validovaného klinického skórovacího systému založeného na intenzitě a trvání symptomů (horečka, zvracení, průjem a změny chování) Statisticky významné Snížení případů hospitalizace/vyšetření na oddělení akutních příjmů pro RV gastroenteritidy po dobu až 2 roky po vakcinaci (RotaTeq n = ) % [95 % CI] G1 G4 G1 G2 G3 G4 G9 94,5 % [91,2 96,6] 95,1 % [91,6 97,1] 87,6 % [< 0 98,5] 93,4 % [49,4 99,1] 89,1 % [52,0 97,5] 100 % [69,6 100] Statisticky významné Snížení incidence RV gastroenteritidy vyvolané G1 G4 v druhé rotavirové sezóně po vakcinaci dosáhlo 88,0 % [95% CI 49,4; 98,7] u závažného onemocnění a 62,6 % [95% CI 44,3; 75,4] u onemocnění bez ohledu na jeho závažnost. Účinnost proti rotavirům typů G2P[4], G3P1[8], G4P1[8] a G9P1[8] byla založena na menším počtu případů než účinnost proti typům G1. Účinnost pozorovaná proti typu G2P[4] byla s největší pravděpodobností odvozena ze složky G2 vakcíny. Pouze ve Finsku byla provedena prodloužená část studie REST. Tato Finnish Extension Study (FES) zahrnovala podsoubor subjektů hodnocení, které byly předtím zařazeny do studie REST. Děti do jednoho roku věku byly ve studii FES sledovány po dobu až 3 let po vakcinaci. 7
7 Ve studii REST bylo zdravotníky u populace hodnocené podle protokolu zaznamenáno 403 případů (20 ve vakcinované skupině a 383 v placebové skupině) souvisejících s rotavirovou gastroenteritidou G1 G4 a G9. Dodatečné údaje ze studie FES zvýšily počet o 136 zaznamenaných případů celkem, včetně 9 ve vakcinované skupině a 127 v placebové skupině. Celkem se během studie FES v příslušných skupinách vyskytlo 31 %, respektive 25 % případů. Na základě kombinovaných údajů ze studií REST a FES bylo za dobu až 3 let po vakcinaci snížení počtu hospitalizací a návštěv pohotovosti kvůli rotavirové gastroenteritidě 94,4 % (95% interval spolehlivosti: 91,6 96,2) pro sérotypy G1 G4, 95,5 % (95% interval spolehlivosti: 92,8 97,2) pro sérotyp G1, 81,9 % (95% interval spolehlivosti: 16,1 98,0) pro sérotyp G2, 89,0 % (95% interval spolehlivosti: 53,3 98,7) pro sérotyp G3, 83,4 % (95% interval spolehlivosti: 51,2 95,8) pro sérotyp G4 a 94,2 % (95% interval spolehlivosti: 62,2 99,9) pro sérotyp G9. V průběhu 3. roku nebyl ve vakcinované skupině (n = 3 112) žádný kontakt se zdravotní péčí kvůli rotavirové gastroenteritidě a v placebové skupině (n = 3 126) byl kontakt jeden (nebylo možno určit typ). K dosažení úrovně a trvání ochrany proti rotavirové gastroenteritidě pozorované v klinických hodnoceních je potřeba podat úplnou sérii 3 vakcinačních dávek očkovací látky RotaTeq (viz bod 4.2). Post hoc analýzy však ukázaly, že s pomocí očkovací látky RotaTeq bylo před podáním všech 3 dávek (tj. v době přibližně 14 dní po podání první dávky dál) dosaženo jistého snížení počtu případů rotavirové gastroenteritidy se závažností vyžadující hospitalizaci nebo návštěvu pohotovosti. Účinnost u nedonošenců Ve studii REST byl podán Rotateq přibližně dětem narozeným v 25. až 36. týdnu těhotenství. Účinnost očkovací látky Rotateq byla srovnávána mezi touto podskupinou dětí a dětmi narozenými v termínu. Poregistrační neintervenční studie bezpečnosti Ve velké, prospektivní, neintervenční poregistrační studii byla na dětech, kterým byla podána jedna nebo více dávek přípravku RotaTeq ( osobo-roků období sledování) analyzována rizika intususcepce a Kawasakiho nemoci. Během období sledování 0. až 30. den po očkování nebyly ve výskytu intususcepce ani Kawasakiho nemoci zjištěny žádné statisticky významné rozdíly v porovnání s očekávanými dosavadními rozdíly. Dále pak během období sledování 0. až 30. den nedošlo k žádnému statisticky významnému zvýšení rizika nežádoucích účinků v porovnání se souběžnou kontrolní skupinou kojenců, kterým byla podána vakcína DTaP, nikoli však vakcína RotaTeq (n=62 617, osobo-roků období sledování ). Intususcepce byla zaznamenaná v 6 potvrzených případech u kojenců očkovaných vakcínourotateq v porovnání s 5 případy u kojenců v souběžných kontrolních skupinách očkovaných vakcínou DTaP (relativní riziko = 0,8, 95% interval spolehlivosti: 0,22-3,52). Kawasakiho nemoc byla zaznamenaná ve zdravotní dokumentaci v 1 potvrzeném případu u kojenců očkovaných vakcínou RotaTeq v porovnání s 1 potvrzeným případem ve zdravotní dokumentaci pacienta v souběžných kontrolních skupinách očkovaných vakcínou DTaP (relativní riziko = 0,7, 95% interval spolehlivosti: 0,01-55,56). Celkové analýzy bezpečnosti neprokázaly žádná specifickábezpečnostní rizika. Imunogenita Imunologický mechanismus, kterým RotaTeq chrání před rotavirovou gastroenteritidou, zatím není přesně znám. Imunologický korelát ochrany vakcín proti rotaviru zatím nebyl zjištěn. Ve studiích fáze III bylo po aplikaci tří dávek dosaženo u 92,5 % až 100 % jedinců očkovaných přípravkem RotaTeq statisticky významného zvýšení protilátek IgA proti rotaviru v séru. Očkovací látka indukuje imunitní odpověď (tzn. výskyt neutralizující protilátky v séru) vůči pěti proteinům lidského rotaviru exprimovaným na reasortantu (G1, G2, G3, G4 a P1[8]). 5.2 Farmakokinetické vlastnosti U vakcín se hodnocení farmakokinetických vlastností nepožaduje. 8
8 5.3 Předklinické údaje vztahující se k bezpečnosti Studie perorální toxicity po jednorázovém a opakovaném podání dávky myším neukazuje žádné zvláštní nebezpečí pro člověka. Dávka podávaná myším byla přibližně 2, infekčních jednotek na kg (přibližně 14násobek předpokládané dávky pro kojence). Nepředpokládá se, že by RotaTeq znamenal nebezpečí pro životní prostředí. Viz bod FARMACEUTICKÉ ÚDAJE 6.1 Seznam pomocných látek Sacharosa Citronan sodný Monohydrát dihydrogenfosforečnanu sodného Hydroxid sodný Polysorbát 80 Živné půdy (s obsahem anorganických solí, aminokyselin a vitaminů) Čištěná voda 6.2 Inkompatibility Očkovací látka se nesmí mísit s jinými léčivými přípravky. 6.3 Doba použitelnosti 2 roky RotaTeq se musí podat ihned po vyjmutí z chladničky. 6.4 Zvláštní opatření pro uchovávání Uchovávejte v chladničce (2 C 8 C). Uchovávejte dávkovací tubu v krabičce, aby byl přípravek chráněn před světlem. 6.5 Druh obalu a velikost balení 2 ml roztoku v předplněné stlačitelné tubě (LDPE) s twist-off víčkem (HDPE) v ochranném sáčku, ve velikosti balení po 1 a 10 kusech. Na trhu nemusí být všechny velikosti balení. 6.6 Zvláštní opatření pro likvidaci přípravku Očkovací látku je třeba podávat perorálně bez mísení s jinými očkovací látkami nebo roztoky. Neředit. 9
9 Podávání vakcíny: Roztržením otevřete ochranný sáček a vyjměte dávkovací tubu. Podržte dávkovací tubu ve svislé poloze a poklepejte na twist-off víčko, aby se aplikátor vyprázdnil. Otevřete dávkovací tubu 2 jednoduchými pohyby: 1. Aplikátor propíchněte otáčením víčka ve směru hodinových ručiček až na doraz. 2. Víčko sejměte otáčením proti směru hodinových ručiček. Dávku vakcíny aplikujte jemným vymačkáváním tekutiny do úst kojence na vnitřní stranu tváře, dokud se dávkovací tuba nevyprázdní. (Ve špičce aplikátoru tuby může zůstat zbytková kapka.) Prázdnou tubu a víčko vyhoďte do předepsaných nádob na biologický odpad podle místních předpisů. Všechen nepoužitý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky. 7. DRŽITEL ROZHODNUTÍ O REGISTRACI Sanofi Pasteur MSD, SNC 8, rue Jonas Salk F LYON Francie 8. REGISTRAČNÍ ČÍSLO(A) EU/1/06/348/001 EU/1/06/348/002 10
10 9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE 27/06/ DATUM REVIZE TEXTU: DD/MMM/YYYY 11
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
Bezpečnost a účinnost přípravku RotaTeq u jedinců od narození do 6 týdnů věku nebyla stanovena.
 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus* G1 ne méně než 2,2 x 10 6 IU 1, 2
1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus* G1 ne méně než 2,2 x 10 6 IU 1, 2
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Vakcína proti rotavirům (živá, perorální) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna 2ml dávka obsahuje: Rotavirus sérotypus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Vakcína proti rotavirům (živá, perorální) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna 2ml dávka obsahuje: Rotavirus sérotypus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
SOUHRN ÚDAJŮ O PŘÍPRAVKU. PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová
 sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno. - Ponechte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno. - Ponechte
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína
Popis přípravku : Prášek: bílý lyofilizát. Rozpouštědlo: čirá bezbarvá tekutina
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (0,5 ml) rozpuštěné
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (0,5 ml) rozpuštěné
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. RotaTeq, perorální roztok Očkovací látka proti rotavirům (živá, perorální)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE RotaTeq, perorální roztok Očkovací látka proti rotavirům (živá, perorální) Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE RotaTeq, perorální roztok Očkovací látka proti rotavirům (živá, perorální) Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno.
Příbalová informace: informace pro uživatele. RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá
 Příbalová informace: informace pro uživatele RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože obsahuje
Příbalová informace: informace pro uživatele RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
sp.zn.: sukls130790/2012
 sp.zn.: sukls130790/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Po rekonstituci 1 dávka (0,5 ml) obsahuje:
sp.zn.: sukls130790/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Po rekonstituci 1 dávka (0,5 ml) obsahuje:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (0,5
1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (0,5
Pomocné látky se známým účinkem: prostý sirup 67%, usušená tekutá glukosa.
 sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Haemophilus influenzae typus b polysaccharidum konjugovaný s tetanickým toxoidem jako bílkovinným nosičem
 sp.zn.sukls200515/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b Prášek a rozpouštědlo pro injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp.zn.sukls200515/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b Prášek a rozpouštědlo pro injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Očkování proti rotavirům
 Očkování proti rotavirům MUDr. Hana Cabrnochová MUDr. Dana Vurmová Hradecké vakcinologické dny 2.11.2007 1 Rotavirové infekce Nejčast astější příčina hospitalizací pro vážnév gastroenteritidy 1 95% dětí
Očkování proti rotavirům MUDr. Hana Cabrnochová MUDr. Dana Vurmová Hradecké vakcinologické dny 2.11.2007 1 Rotavirové infekce Nejčast astější příčina hospitalizací pro vážnév gastroenteritidy 1 95% dětí
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.:sukls59594/25009, a příloha k sp.zn.: sukls230271/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.:sukls59594/25009, a příloha k sp.zn.: sukls230271/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. RotaTeq, perorální roztok Vakcína proti rotavirům (živá, perorální)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE RotaTeq, perorální roztok Vakcína proti rotavirům (živá, perorální) Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno. - Ponechte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE RotaTeq, perorální roztok Vakcína proti rotavirům (živá, perorální) Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno. - Ponechte
Souhrn údajů o přípravku. Typhoidi capsulae Vi polysaccharidum purificatum (stirpe Ty 2)
 sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Haemophilus influenzae type b polysaccharide
 sp. zn. sukls37951/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Po rekonstituci jedna dávka (0,5 ml) obsahuje:
sp. zn. sukls37951/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Po rekonstituci jedna dávka (0,5 ml) obsahuje:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.sukls158765/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.sukls158765/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls316718/2017 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
sp.zn. sukls316718/2017 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 1 dávka - 0,5 ml obsahuje: Typhoidi capsulae Vi polysaccharidum purificatum (stirpe Ty2)..25 mikrogramů
 sp. zn. sukls183609/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti břišnímu tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ
sp. zn. sukls183609/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti břišnímu tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ
1 dávka - 0,5 ml obsahuje: Typhoidi capsulae Vi polysaccharidum purificatum (stirpe Ty2)..25 mikrogramů
 sp.zn. sukls120097/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti břišnímu tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ
sp.zn. sukls120097/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti břišnímu tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příbalová informace: informace pro uživatele. RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá
 Příbalová informace: informace pro uživatele RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože obsahuje
Příbalová informace: informace pro uživatele RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls59573/2009
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls59573/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TETAVAX, injekční suspenze v předplněné injekční stříkačce Vakcína proti tetanu (adsorbovaná)
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls59573/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TETAVAX, injekční suspenze v předplněné injekční stříkačce Vakcína proti tetanu (adsorbovaná)
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
sp.zn.: sukls7967/2011
 sp.zn.: sukls7967/2011 Souhrn údajů o přípravku. 1. NÁZEV PŘÍPRAVKU sáčky 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ Jedna tobolka obsahuje léčivou látku: Lysatum bacteriale OM 85 cryodesicatum, odpovídá
sp.zn.: sukls7967/2011 Souhrn údajů o přípravku. 1. NÁZEV PŘÍPRAVKU sáčky 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ Jedna tobolka obsahuje léčivou látku: Lysatum bacteriale OM 85 cryodesicatum, odpovídá
Souhrn údajů o přípravku
 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro přípravu perorální suspenze s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Haemophilus influenzae typus b polysaccharidum konjugovaný s tetanickým toxoidem jako bílkovinným nosičem
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b Prášek a rozpouštědlo pro injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Po rekonstituci 1 dávka
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b Prášek a rozpouštědlo pro injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Po rekonstituci 1 dávka
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Feligen CRP Lyofilizát pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizovaná složka Léčivé
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Feligen CRP Lyofilizát pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizovaná složka Léčivé
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.: sukls265484/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AVAXIM 160 U, injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná, adsorbovaná) 2. KVALITATIVNÍ
sp.zn.: sukls265484/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AVAXIM 160 U, injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná, adsorbovaná) 2. KVALITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix prášek a rozpouštědlo pro perorální suspenzi Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po rekonstituci
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rotarix prášek a rozpouštědlo pro perorální suspenzi Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po rekonstituci
Pediatrická populace 1/5. sp.zn. sukls316718/2017 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU
 sp.zn. sukls316718/2017 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TETAVAX, injekční suspenze v předplněné injekční stříkačce Vakcína proti tetanu (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp.zn. sukls316718/2017 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TETAVAX, injekční suspenze v předplněné injekční stříkačce Vakcína proti tetanu (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
(DTPa-HBV- Lyofilizovaná složka vakcíny proti Haemophilus influenzae typ b (Hib) je bílý prášek.
 1 AVKU 1.. Vakcína proti difterii (D), tetanu (T), pertusi (acelulární komponenta) (Pa), (rdna) (HBV) (inaktivovaná) (IPV) a konjugovaná vakcína proti Haemophilus influenzae typu b (Hib), (adsorbovaná).
1 AVKU 1.. Vakcína proti difterii (D), tetanu (T), pertusi (acelulární komponenta) (Pa), (rdna) (HBV) (inaktivovaná) (IPV) a konjugovaná vakcína proti Haemophilus influenzae typu b (Hib), (adsorbovaná).
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus serotypus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus serotypus*
NEREGISTROVANÝ PŘÍPRAVEK použití povoleno v rámci specifického léčebného programu SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU ADACEL POLIO, injekční suspenze v předplněné stříkačce Vakcína (adsorbovaná) proti diftérii (snížený obsah antigenu), tetanu, pertusi (acelulární komponenta)
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU ADACEL POLIO, injekční suspenze v předplněné stříkačce Vakcína (adsorbovaná) proti diftérii (snížený obsah antigenu), tetanu, pertusi (acelulární komponenta)
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje: Rotavirus typus*
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011. Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Synflorix injekční suspenze v předplněné injekční stříkačce Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Menveo prášek a roztok pro injekční roztok. Konjugovaná vakcína proti meningokokům skupin A, C, W135 a Y 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Menveo prášek a roztok pro injekční roztok. Konjugovaná vakcína proti meningokokům skupin A, C, W135 a Y 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Rotavirus RIX4414 humanum vivum attenuatum* ne méně než 10 6,0 CCID 50
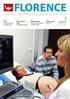 1. NÁZEV PŘÍPRAVKU Rotarix perorální suspenze Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1,5 ml) obsahuje: Rotavirus RIX4414 humanum vivum attenuatum* ne méně než 10 6,0 CCID
1. NÁZEV PŘÍPRAVKU Rotarix perorální suspenze Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1,5 ml) obsahuje: Rotavirus RIX4414 humanum vivum attenuatum* ne méně než 10 6,0 CCID
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU ROTATEQ (česky) 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje:
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU ROTATEQ (česky) 1 1. NÁZEV PŘÍPRAVKU RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (2 ml) obsahuje:
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Tetanol pur Injekční suspenze, adsorbovaná vakcína proti tetanu, bez konzervačních prosředků 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Tetanol pur Injekční suspenze, adsorbovaná vakcína proti tetanu, bez konzervačních prosředků 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Canigen Puppy 2b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Složení v dávce 1 ml Léčivá látka: Parvovirus enteritidis canis attenuatum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Canigen Puppy 2b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Složení v dávce 1 ml Léčivá látka: Parvovirus enteritidis canis attenuatum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.: sukls196586/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SMECTA prášek pro perorální suspenzi 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 sáček obsahuje: Léčivá látka: Diosmectitum 3,000 g Pomocné
sp.zn.: sukls196586/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SMECTA prášek pro perorální suspenzi 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 sáček obsahuje: Léčivá látka: Diosmectitum 3,000 g Pomocné
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp. zn. sukls76878/2017 1. NÁZEV PŘÍPRAVKU SMECTA 3 g prášek pro perorální suspenzi SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje diosmectitum 3 g. Pomocné látky
sp. zn. sukls76878/2017 1. NÁZEV PŘÍPRAVKU SMECTA 3 g prášek pro perorální suspenzi SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje diosmectitum 3 g. Pomocné látky
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls223527/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VACTETA 40 mezinárodních jednotek/0,5ml injekční suspenze Vakcína proti tetanu (adsorbovaná) 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ 1
sp.zn.sukls223527/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VACTETA 40 mezinárodních jednotek/0,5ml injekční suspenze Vakcína proti tetanu (adsorbovaná) 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ 1
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. Název přípravku E-Z-HD 2. Kvalitativní a kvantitativní složení Léčivá látka: Barii sulfas (síran barnatý)
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. Název přípravku E-Z-HD 2. Kvalitativní a kvantitativní složení Léčivá látka: Barii sulfas (síran barnatý)
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha k sp. zn. sukls224939/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Molaxole prášek pro přípravu perorálního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující
Příloha k sp. zn. sukls224939/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Molaxole prášek pro přípravu perorálního roztoku 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje následující
Souhrn údajů o přípravku
 sp. zn. sukls208148/2014 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Povrchové
sp. zn. sukls208148/2014 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Povrchové
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls71941/2012 a sukls103573/2013, sukls103568/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucidin Mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Natrii fusidas 20,0 mg v 1 g masti.
sp.zn. sukls71941/2012 a sukls103573/2013, sukls103568/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucidin Mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Natrii fusidas 20,0 mg v 1 g masti.
Rotavirus RIX4414 humanum vivum attenuatum* ne méně než 10 6,0 CCID 50
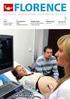 1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro perorální suspenzi s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po rekonstituci obsahuje: Rotavirus RIX4414 humanum
1. NÁZEV PŘÍPRAVKU Rotarix, prášek pro perorální suspenzi s rozpouštědlem Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1 ml) po rekonstituci obsahuje: Rotavirus RIX4414 humanum
AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Vakcína proti Haemophilus influenzae b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Act-HIB Vaccine, prášek pro přípravu inj. roztoku s rozpouštědlem Vakcína proti Haemophilus influenzae b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka:
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Act-HIB Vaccine, prášek pro přípravu inj. roztoku s rozpouštědlem Vakcína proti Haemophilus influenzae b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka:
Souhrn údajů o přípravku
 Sp.zn. sukls120620/2013 1. NÁZEV PŘÍPRAVKU Souhrn údajů o přípravku Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna 2013/2014 2. KVALITATIVNÍ A KVANTITATIVNÍ
Sp.zn. sukls120620/2013 1. NÁZEV PŘÍPRAVKU Souhrn údajů o přípravku Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna 2013/2014 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ. Po rekonstituci 1 dávka (0,5 ml) obsahuje:
 AVKU 1 1. -135 a Y 2. KVALITATIVÍ A KVATITATIVÍ SLOŽEÍ Po rekonstituci 1 dávka (0,5 ml) obsahuje: eisseria meningitidis A polysacharidum 1 eisseria meningitidis C polysacharidum 1 eisseria meningitidis
AVKU 1 1. -135 a Y 2. KVALITATIVÍ A KVATITATIVÍ SLOŽEÍ Po rekonstituci 1 dávka (0,5 ml) obsahuje: eisseria meningitidis A polysacharidum 1 eisseria meningitidis C polysacharidum 1 eisseria meningitidis
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
Rotavirus RIX4414 humanum vivum attenuatum* ne méně než 10 6,0 CCID 50
 1. NÁZEV PŘÍPRAVKU Rotarix perorální suspenze v předplněném perorálním aplikátoru Rotarix perorální suspenze ve stlačitelné tubě Rotarix perorální suspenze ve více-jednodávkových (5 jednotlivých dávek)
1. NÁZEV PŘÍPRAVKU Rotarix perorální suspenze v předplněném perorálním aplikátoru Rotarix perorální suspenze ve stlačitelné tubě Rotarix perorální suspenze ve více-jednodávkových (5 jednotlivých dávek)
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls16744/2009
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls16744/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU INFANRIX Vakcína proti difterii, tetanu a pertusi (acelulární) Injekční suspenze 2.
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls16744/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU INFANRIX Vakcína proti difterii, tetanu a pertusi (acelulární) Injekční suspenze 2.
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Canigen DHA 2 PPi/LR Lyofilizát pro přípravu injekční suspenze s rozpouštědlem. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky:
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Canigen DHA 2 PPi/LR Lyofilizát pro přípravu injekční suspenze s rozpouštědlem. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky:
Vakcína proti difterii, tetanu, pertusi (acelulární), poliomyelitidě (inaktivovaná) a konjugovaná vakcína proti hemofilu typu b (adsorbovaná)
 Sp.zn.sukls219304/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU PEDIACEL, injekční suspenze v předplněné injekční stříkačce Vakcína proti difterii, tetanu, pertusi (acelulární), poliomyelitidě (inaktivovaná)
Sp.zn.sukls219304/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU PEDIACEL, injekční suspenze v předplněné injekční stříkačce Vakcína proti difterii, tetanu, pertusi (acelulární), poliomyelitidě (inaktivovaná)
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124912/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124912/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124912/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Hiberix Vakcína proti Haemophilus influenzae typu b 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Vanguard R injekční suspenze pro psy, kočky, skot, prasata, ovce, kozy, koně a fretky
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Vanguard R injekční suspenze pro psy, kočky, skot, prasata, ovce, kozy, koně a fretky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Vanguard R injekční suspenze pro psy, kočky, skot, prasata, ovce, kozy, koně a fretky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka
* adsorbováno na hydroxid hlinitý (množství odpovídá 0,3 mg hliníku) ** obsah antigenu je vyjádřen v porovnání na vlastní referenční přípravek
 sp.zn. sukls96465/2017 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AVAXIM 160 U injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná, adsorbovaná) 2. KVALITATIVNÍ
sp.zn. sukls96465/2017 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AVAXIM 160 U injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná, adsorbovaná) 2. KVALITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Menveo prášek a roztok pro přípravu injekčního roztoku. Konjugovaná vakcína proti meningokokům skupin A, C, W135 a Y 2. KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Menveo prášek a roztok pro přípravu injekčního roztoku. Konjugovaná vakcína proti meningokokům skupin A, C, W135 a Y 2. KVALITATIVNÍ A KVANTITATIVNÍ
sp.zn.: sukls132182/2010 a sp.zn.: sukls82396/2014
 sp.zn.: sukls132182/2010 a sp.zn.: sukls82396/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MYTELASE tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ambenonii chloridum 10 mg v 1 tabletě. Pomocné látky
sp.zn.: sukls132182/2010 a sp.zn.: sukls82396/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MYTELASE tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ambenonii chloridum 10 mg v 1 tabletě. Pomocné látky
* adsorbováno na hydroxid hlinitý (množství odpovídá 0,3 mg hliníku) ** obsah antigenu je vyjádřen v porovnání na vlastní referenční přípravek
 sp.zn. sukls120097/2014 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU AVAXIM 160 U, injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná, adsorbovaná) 2. KVALITATIVNÍ
sp.zn. sukls120097/2014 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU AVAXIM 160 U, injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná, adsorbovaná) 2. KVALITATIVNÍ
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Locatim perorální roztok pro novorozená telata mladší než 12 hodin 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Bovinní
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Locatim perorální roztok pro novorozená telata mladší než 12 hodin 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Bovinní
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls221497/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucicort Krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Acidum fusidicum 20,0 mg (jako acidum fusidicum hemihydricum) Betamethasonum
sp.zn. sukls221497/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucicort Krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Acidum fusidicum 20,0 mg (jako acidum fusidicum hemihydricum) Betamethasonum
3. LÉKOVÁ FORMA Injekční suspenze vpředplněné injekční stříkačce; bezbarvá průhledná tekutina, v jednodávkových inj. stříkačkách (sklo, typu I).
 Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls97832/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna
Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls97832/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna
Souhrn údajů o přípravku
 Příloha č. 1 ke sdělení sp.zn.: sukls204427/2010 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU PRIORIX prášek pro přípravu injekčního roztoku s rozpouštědlem Živá atenuovaná vakcína proti spalničkám, příušnicím
Příloha č. 1 ke sdělení sp.zn.: sukls204427/2010 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU PRIORIX prášek pro přípravu injekčního roztoku s rozpouštědlem Živá atenuovaná vakcína proti spalničkám, příušnicím
Přecitlivělost na léčivé látky nebo na kteroukoliv z pomocných látek uvedených v bodě 6.1.
 sp.zn.: sukls50035/2010, sukls106419/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H rektální mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 g Selachiorum
sp.zn.: sukls50035/2010, sukls106419/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H rektální mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 g Selachiorum
Příbalová informace: informace pro uživatele. RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá
 Příbalová informace: informace pro uživatele RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože obsahuje
Příbalová informace: informace pro uživatele RotaTeq, perorální roztok Očkovací látka proti rotavirům, živá Přečtěte si pozorně celou příbalovou informaci dříve, než bude Vaše dítě očkováno, protože obsahuje
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.sukls79980/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.sukls79980/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.sukls79980/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls123741/2010
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls123741/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VAXIGRIP, injekční suspenze v předplněné injekční stříkačce. Vakcína proti chřipce (inaktivovaná,
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls123741/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VAXIGRIP, injekční suspenze v předplněné injekční stříkačce. Vakcína proti chřipce (inaktivovaná,
Rotavirus RIX4414 humanum vivum attenuatum* ne mén než 10 6,0 CCID 50
 1. NÁZEV P ÍPRAVKU Rotarix perorální suspenze v p edpln ném perorálním aplikátoru Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1,5 ml) obsahuje: Rotavirus RIX4414 humanum vivum
1. NÁZEV P ÍPRAVKU Rotarix perorální suspenze v p edpln ném perorálním aplikátoru Živá rotavirová vakcína 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (1,5 ml) obsahuje: Rotavirus RIX4414 humanum vivum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.: sukls243839/2011 a sp.zn.: sukls113646/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum 10,0 mg (odpovídá
sp.zn.: sukls243839/2011 a sp.zn.: sukls113646/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum 10,0 mg (odpovídá
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU APIGUARD gel (25% Thymolum) pro podání ve včelím úlu Vyhrazený veterinární léčivý přípravek 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU APIGUARD gel (25% Thymolum) pro podání ve včelím úlu Vyhrazený veterinární léčivý přípravek 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Tato vakcína může obsahovat stopy neomycinu použitého v průběhu výrobního procesu (viz bod 4.3).
 1. NÁZEV PŘÍPRAVKU Twinrix Paediatric, injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná) a proti hepatitidě B (rdna) (HAB), adsorbovaná. 2. KVALITATIVNÍ A KVANTITATIVNÍ
1. NÁZEV PŘÍPRAVKU Twinrix Paediatric, injekční suspenze v předplněné injekční stříkačce Vakcína proti hepatitidě A (inaktivovaná) a proti hepatitidě B (rdna) (HAB), adsorbovaná. 2. KVALITATIVNÍ A KVANTITATIVNÍ
ne méně 30 IU(25 Lf) Tetani anatoxinum 1
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU NEBO NA VNITŘNÍM OBALU LAHVIČKA + LAHVIČKA X 1 LAHVIČKA + LAHVIČKA X 10 LAHVIČKA + LAHVIČKA X 20 LAHVIČKA + LAHVIČKA X 25 LAHVIČKA + LAHVIČKA X 40 LAHVIČKA + LAHVIČKA X 50
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU NEBO NA VNITŘNÍM OBALU LAHVIČKA + LAHVIČKA X 1 LAHVIČKA + LAHVIČKA X 10 LAHVIČKA + LAHVIČKA X 20 LAHVIČKA + LAHVIČKA X 25 LAHVIČKA + LAHVIČKA X 40 LAHVIČKA + LAHVIČKA X 50
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná).
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná). 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná). 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka
Gynekologie: Metroragie, primární menoragie nebo menoragie související s nitroděložním tělískem bez prokazatelné organické příčiny.
 Sp.zn.sukls81671/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Cyclonamine 500 mg Tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje etamsylatum 500 mg. Léčivý přípravek obsahuje
Sp.zn.sukls81671/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Cyclonamine 500 mg Tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje etamsylatum 500 mg. Léčivý přípravek obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79120/2012 1. NÁZEV PŘÍPRAVKU NIZORAL krém SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ketoconazolum 20,0 mg v 1 g krému Pomocné
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79120/2012 1. NÁZEV PŘÍPRAVKU NIZORAL krém SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ketoconazolum 20,0 mg v 1 g krému Pomocné
