6. Produkce biotechnologických látek a downstream procesy
|
|
|
- Vladimíra Matějková
- před 8 lety
- Počet zobrazení:
Transkript
1 6. Produkce biotechnologických látek a downstream procesy Produkce terapeutických proteinů je složitý proces, který zahrnuje jak jejich vlastní expresi, tak také purifikační postupy a charakterizaci produktů. Systémy pro expresi byly podrobně charakterizovány v kapitole 4, bioreaktory v kapitole 5. V této kapitole se zaměříme na charakteristiku vlastních biotechnologických produktů vznikajících v bioreaktorech. Biotechnologické produkty pro terapeutické použití musí být přesně specifikovány, zvláště když jsou určeny k parenterální aplikaci Kultivační médium Pro dosažení optimálních růstových podmínek v bioreaktoru je třeba zabezpečit vhodné složení živného média. Média používaná ke kultivaci buněk jsou komplexní a sestávají ze směsi různých složek, a to cukrů, aminokyselin, elektrolytů, vitamínů a směsi peptonů, růstových faktorů, hormonů a dalších proteinů. Většina těchto látek je dostupná jako komerční preparáty, které stačí jen rozpustit ve vodě a sterilizovat. V případě savčích buněk tvoří významnou složku média fetální telecí sérum. Některé složky, jako např. právě fetální telecí sérum, obsahují významný podíl proteinů, které jsou kontaminujícími položkami, které interferují s purifikačními procesy. Kromě toho je složení takového séra značně proměnlivé; liší se individuálně zvíře od zvířete, ročního období, zpracování u dodavatele, apod. Sérum také může obsahovat různý nechtěný materiál, např. viry, mykoplazmata, bakterie nebo houby; může tak dojít ke kontaminaci kultury. Hrozbou mohou být i priony, které vyvolávají přenosnou spongiformní encefalitidu a to zejména tehdy, když je použit materiál z krav, koz nebo ovcí. Řada míněných problémů spojených s použitím séra vedla experimentátory k vytvoření médií, která sérum neobsahují, tzv. sérum-free médií. A obecným trendem je vytvářet média taková, která neobsahují složité nedefinované složky. Především při průmyslových aplikacích, např. při výrobě monoklonálních protilátek, se chemicky definovaná média a média bez sérové složky ukázala velmi úspěšná Kontaminující složky Kvalita se obvykle vyjadřuje v termínech čistoty a reprodukovatelnosti. Čistota farmaceutických přípravků je většinou vyšší než 99%, pokud jsou podávány parenterálně. To platí i pro proteinová terapeutika, u kterých je výsledná čistota velmi závislá na procesu purifikace. Přehled potenciálních kontaminujících složek proteinových farmaceutik je uveden v Tabulce Nyní si popíšeme vlastnosti některých z nich Viry Viry jsou potenciálními kontaminantami především pro živočišné buněčné kultury. Jejich koncentrace ve výsledném produktu jsou velmi nízké a je nesnadné je detekovat. Dají se detekovat elektronovým mikroskopem, citlivé testy in vitro nejsou k dispozici. U některých virů (např. hepatitidy) 1
2 jsou rizika dobře známá, u jiných ale nejsou k dispozici experimentální údaje. Například parvoviry mají dlouhou dobu latence, než se projeví jejich klinický účinek. Dlouhodobé účinky u pacientů léčených rekombinantními proteiny, které jsou kontaminovány takovými viry, samozřejmě nelze zanedbat. Viry mohou být zaneseny do kultivačních médií přímo ze surovin nebo z infikované buněčné linie. Nejčastějším zdrojem je výše zmíněné živočišné sérum. Sérem mohou být zaneseny také bakterie, mykoplazmata, priony, houby a endotoxiny. K detekci virů ve vstupním materiálu musí být používány certifikované metody, bez jejich použití nemůže být terapeutikum licencováno. Viry lze inaktivovat fyzikálními nebo chemickými metodami, např. teplem, zářením, sonikací, extrémními hodnotami ph, detergenty, rozpouštědly a určitými dezinfekčními prostředky. Tyto postupy mohou mít ale také destruktivní vliv na produkt, a proto musí být velmi opatrně vyzkoušeny a validovány. Elegantním a efektivním postupem pro odstranění virů je nanofiltrace. Tento postup je podrobně popsán v PDA technical report 41 z roku 2005 (revize v roce 2008). PDA = Parenteral Drug Association. Tabulka 6.1: Potenciálně kontaminující složky proteinových farmaceutik Původ Hostitelský organismus Kontaminující složka Viry Proteiny a DNA hostitele Glykosylační varianty Variantní N a C konce Endotoxiny (u gram-negativních hostitelů) Produkt Substituce a delece aminokyselin Denaturovaný protein Konformační izomery Dimery a agregáty Varianty disulfidických můstků Deaminované varianty Fragmenty proteinů Proces Komponenty růstového média Purifikační reagencie Kovy Materiály purifikačních kolon Nanofiltrace spočívá ve filtraci přes 15 nm membrány, kterými lze zachytit i ty nejmenší známé neobalené viry typu bovinního parvoviru. 2
3 Příklady metod, kterými lze redukovat, nebo inaktivovat viry jsou uvedeny v Tabulce 6.2. Tabulka 6.2: Metody redukce nebo inaktivace virů Kategorie Způsoby Příklad Inaktivace viru Teplo Pasterizace Záření Dehydratace Kroslinkující látky, denaturační a rozkladná činidla Neutralizace UV světlo Lyofilizace Β-propionolakton, formaldehyd, NaOH, organická rozpouštědla (např. chloroform), detergenty (např. Na-cholát) Specifické, neutralizující protilátky Odstranění viru Chromatografie Iontoměničová, imunoafinitní Filtrace Precipitace Nanofiltrace Cyroprecipitace Bakterie Bakterie mohou kontaminovat buněčné kultury, ale je snadné je odstranit filtrací. Nejjednodušším způsobem, jak zabránit kontaminaci média bakteriemi, je sterilizace všech vstupních materiálů a práce v aseptických podmínkách. Výroba by měla probíhat v tzv. čistých prostorech, kde je sterilita prostředí zajišťována např. filtrací vzduchu. V některých případech se do média přidávají antibiotika, což ale komplikuje následné purifikační kroky. Použití beta-laktamázových antibiotik je dokonce zakázáno, protože někteří lidé jsou k těmto antibiotikům zvýšeně citliví. Obecně lze zbytky antibiotik z média odstranit velmi těžko, proto se preferují technologie bez jejich použití. Bakterie mohou produkovat nebezpečné pyrogeny, ke kterým jsou někteří lidé citliví i ve velmi nízkých koncentracích (pikogramy/ml). Pyrogeny mohou vyvolat silnou horečku až s fatálními následky. Filtrací nelze pyrogeny odstranit. Odstranění pyrogenů je komplikováno také jejich různou velikostí a rozmanitou chemickou strukturou. Na druhou stranu jsou ale k dispozici komerční sety, které umožňují detekovat a kvantifikovat i malá množství pyrogenů. Při purifikaci se zpravidla alespoň v jednom kroku používá iontoměničová chromatografie, která by měla zaručit odstranění alespoň negativně nabitých endotoxinů. Skleněné nástroje, které se při purifikacích také používají, jsou před použitím depyrogenovány horkovzdušnou sterilizací při 180 C. Buněčné kultury jsou často kontaminovány mykoplasmaty druhu M. orale, M. laidlawaii, M. arginii nebo M. hyorhinis. Odborná literatura uvádí, že podíl mykoplasmaty kontaminovaných kultur dosahuje až 30% (v závislosti na laboratoři od 5% do 85%). Přítomnost mykoplasmat nezpůsobuje nějakou viditelnou změnu v makroskopických vlastnostech buněk ani ve vlastnostech média. Může ale změnit charakteristiky metabolismu, růst, životnost buněk, apod. Indikátory 3
4 přítomnosti mykoplasmat v buněčné kultuře mohou být Neschopnost buněk adherovat na povrch kultivační nádoby Snížená růstová rychlost buněčné kultury Shlukování kultivovaných buněk Hlavními zdroji kontaminace mykoplasmaty jsou samotné buňky experimentátor sérum, médium a aditiva tekutý dusík Mykoplasmata lze z buněčné kultury odstranit nejlépe antibiotiky gentamycinem nebo ciprofloxacinem Buněčná DNA Když se k produkci terapeutických proteinů použijí savčí buňky, můžou se ve finálních produktech objevit fragmenty DNA. Proto je třeba během purifikace nasadit krok, při kterém jsou molekuly DNA a RNA odstraněny až na bezpečnou úroveň. Kontrolu purifikace lze zabezpečit např. tím, že se buněčná linie inkubuje s radioaktivně značenými nukleotidy, jejichž obsah lze pak ve výsledných produktech snadno změřit. Jsou-li zbytky DNA stále přítomny, měl by být zařazen dodatečný purifikační krok. Otázka týkající se bezpečného množství kontaminující DNA zůstává ale předmětem spekulací. Transformace nahou DNA je velmi obtížná, úspěch je podmíněn spíše vysokou koncentrací DNA. Přesto Evropský lékopis doporučuje, aby množství DNA v konečném preparátu terapeutického proteinu nepřesáhlo 100 pg až 10 ng denní dávky podle druhu kultivačního systému Kontaminace proteiny V biotechnologických produktech se mohou objevovat také zbytky cizích proteinů. Tyto kontaminanty mohou být zdraví nebezpečné, protože mohou být rozpoznány jako antigeny a při opakovaném použití vyvolat imunitní odpověď. A přestože samotný rekombinantní protein žádnou takovou reakci vyvolat nemusí, interpretace může být opačná! Při hodnocení výsledného preparátu je tedy třeba posuzovat opatrně, která složka se na případné imunitní reakci podílí. Zdrojem kontaminujících proteinů mohou být jak hostitelské buňky, tak i růstové médium. Mezi kontaminujícími proteiny mohou být i varianty rekombinantních proteinů produkované hostitelskou buňkou. Takové proteiny mají s rekombinantním proteinem velmi podobnou strukturu a budou s ním velmi snadno kopurifikovány. Příkladem takového proteinu je urokináza nebo cytokiny hybridomů. Detekce kontaminujících proteinů se provádí citlivými imunologickými testy. 4
5 6.3. Downstream processing Jednou z kritických fází výroby biotechnologických produktů je izolace biologických produktů ze supernatantu buněčné kultury; purifikační procedury jsou obvykle finančně náročnější než procesy samotné výroby rekombinantního produkčního organismu. Např. cena za pryskyřice s proteinem A, která se používá k izolaci monoklonálních protilátek, tvoří jen 10% částky použité na výrobu monoklonální protilátky, kdežto cena za filtraci viru představuje asi 40% nákladů. Rekombinantní produkty získáváme zpravidla ve velmi zředěné formě, kolem mg/l (maximálně mg/l); cílem jsou koncentrace kolem 5-10 g/l. Zředěné roztoky je třeba zkoncentrovat předtím, než budou produkty purifikovány, protože se jinak pracuje s velkými objemy materiálu. Celý proces purifikace probíhá zhruba ve třech stupních v prvním je produkt zachycen a primárně purifikován, v dalším kroku je odstraněna hlavní část kontaminant a ve třetím jsou odstraněny zbývající kontaminující látky a variantní formy molekul. Někdy je z ekonomického důvodu vhodná obrácená strategie, kdy jsou nejprve zachyceny hlavní kontaminující složky a produkty jsou purifikovány až v následujících krocích. Tento postup se používá u vnitrobuněčných proteinů nesecernovaných do vnějšího prostředí. Je-li podíl produktu na celkovém proteinu malý, kolem 1 až 5%, pak je lepší první z popsaných postupů, protože velké množství nespecifických proteinů by mohlo zahltit specifické purifikační nástroje a celý proces zhatit. Po odstranění hlavní části kontaminant se purifikace provádí na co do velikosti malých a tedy levných chromatografických kolonách. Po purifikaci probíhají další kroky, formulace a sterilizace, což jsou procesy popsané v kapitole 8. V průběhu vytváření purifikačního protokolu by měly být posouzeny také možnosti a úskalí případných kroků vedoucích ke zvýšení objemu výroby. Proces fungující v malých množstvích není často vhodný pro množství velká ať už s ohledem na technické možnosti nebo ekonomiku procesu. Vývoj downstream procesů má dvě stádia formulace (design) a zvýšení objemu (scale-up). Separace nečistot z výsledného proteinu vyžaduje sérii purifikačních kroků (tzv. process design ), přičemž v každém kroku dochází k odstranění některých nečistot a produkt se přibližuje finální specifikaci. Z obecného pohledu obsahuje výchozí produkt buněčné zbytky anebo celé buňky, které je nezbytné odstranit. Vytvoření správného purifikačního postupu je usnadněno, když se podaří definovat hlavní kontaminující složky. Tato definice musí obsahovat detailní informaci o zdroji materiálu (jedná se o bakteriální kulturu nebo kulturu savčích buněk?) a hlavních kontaminujících složkách (např. albumin nebo analoga výsledného produktu). Kromě toho má také popisovat fyzikální charakteristiky produktu a jejich porovnání s vlastnostmi kontaminant (teplotní stabilita, izoelektrický bod, molekulová hmotnost, hydrofobicita, denzita, specifické vazebné vlastnosti), protože ty významně určují proces purifikace. Procesy určené k produkci terapeutik musí být reprodukovatelné a spolehlivé. Procesy purifikace mohou vystavit proteiny velkému fyzikálnímu stresu (např. vysoké teplotě nebo extrémním hodnotám ph), který může změnit vlastnosti proteinu vedoucí až ke ztrátě biologické aktivity. Jakákoli substance, která se aplikuje injekčně, musí být sterilní a prostá pyrogenních látek, respektive pyrogenní látky musí být přítomny v podlimitních množstvích, která jsou definována podle typu produktu. V Evropském lékopisu jsou udávány hodnoty pod 0,2mg/kg tělní hmotnosti. Produkce musí probíhat aseptickými technikami a v prostředí s čistým vzduchem a pod mikrobiologickou kontrolou všech materiálů a zařízení. Během validace purifikačního procesu musí být také prokázáno, že jsou odstraněny potenciální virové kontaminanty. Purifikační matrice musí být sanitovatelné nebo, 5
6 je-li to možné, sterilizovatelné přehřátými parami. Aby bylo možné odstranit pyrogeny, musí purifikační materiály vydržet buďto dlouhodobou sterilizaci v suchém vzduchu při 180 C nebo působení 1-2M hydroxidu sodného. Jestliže nějaký materiál, který je v kontaktu s produktem uvolňuje nějaké komponenty, musí být tyto látky analyzovány a v průběhu validace musí být prokázáno, že je možné je odstranit. V posledních letech se pro výroby používají umělohmotné materiály a výše zmíněné požadavky se proto staly ještě důležitější. Uvolňování nechtěných složek v průběhu purifikace je velkou překážkou pro afinitní chromatografii. V laboratorním měřítku je afinitní chromatografie užitečným nástrojem purifikace, ale pro přímé použití terapeutických proteinů u lidí je nutné naprosto nezvratně prokázat, že je možné odstranit jakékoli z chromatografie uvolněné látky. Termín scale-up se používá k popisu procesů konverze laboratorní procedury do ekonomického, průmyslového postupu. Během této fáze se proces posouvá z laboratorních podmínek do poloprovozu a konečně do plnoprovozu. Cílem procesu scale-up je výroba produktu vysoké kvality za kompetitivní cenu. Protože cena downstream procesů představuje 50 až 80% celkových nákladů, je třeba zvolit praktické a ekonomické způsoby purifikace. Kvalita metod purifikace proteinů je klíčem pro silnou pozici na trhu. Základní činnosti při purifikaci makromolekul z biologických zdrojů jsou zachyceny na obr Jak bylo zmíněno už výše, je formulace procesů purifikace produktů vysoce závislá na druhu produktu. Každý produkt je purifikován specifickým vícekrokovým postupem. Základní schéma uvedené na obrázku 6. 1 je komplexní. Typický příklad činností při purifikaci je zachycen na obr Je zde uveden proces purifikace glykosylovaného rekombinantního interferonu (velikost kolem 28 kda) produkovaného v savčích buňkách. Jakmile jsou objem a koncentrace produktu definovány, může začít purifikace. K separaci proteinů na základě širokého spektra různých fyzikálně-chemických kritérií (velikost, náboj, hydrofobicita, rozpustnost) existuje celá řada dostupných metod. Obr. 6.1: Základní činnosti při purifikaci biofarmaceutických makromolekul Odstranění částic Koncentrace Zachycení/Prvotní purifikace Průběžná purifikace 6
7 Konečná purifikace Sterilizace/Formulace Filtrace/centrifugace Produkty biotechnologického průmyslu jsou separovány z biologických systémů, které obsahují suspendovaný částicový materiál (a to celé buňky), lyzované buňky (a fragmenty rozbitých buněk), které vznikají poté, co jsou buňky degradovány, aby se z nich uvolnil vnitrobuněčný protein. Většina purifikačních procesů proto počítá s alespoň jedním krokem, ve kterém jsou takové částice odstraněny nebo koncentrovány. Nejčastější metodou je centrifugace nebo filtrace (ultrafiltrace, diafiltrace a mikrofiltrace). Cena a efektivita takových metod je vysoce závislá na fyzikální povaze částicového materiálu a produktu. Filtrace. Filtrací lze zkoncentrovat biomasu před její další purifikací. Pro účely oddělení buněk od média bylo vyvinuto několik filtračních systémů, z nichž nejúspěšnější je tangenciální průtokový systém. Při něm je tvorbě nánosů na membráně, tvorbě gelové vrstvy a polarizaci zabráněno vysokými střižnými silami. Při ultrafiltraci je směs molekul různých molekulových separována protlačováním dispergovaného materiálu přes membrány s póry definované velikosti. V principu je ale ultrafiltrací možno dosáhnout jen nízkého stupně purifikace, používá se spíš ke koncentraci makromolekul nebo k výměně vodné fáze, ve které jsou částice dispergovány nebo molekuly rozpuštěny v médiu, které je vhodnější pro další purifikační kroky. Centrifugace. Subbuněčné částice nebo organely suspendované ve viskózní tekutině je nesnadné separovat v jednom kroku centrifugace nebo filtrací. Ale je možné je použít centrifugace při různých rychlostech. Jádra buněk lze například získat centrifugací při 400 g po dobu 20 minut, vezikuly plasmatické membrány je třeba oddělit při vyšších otáčkách a za delší dobu centrifugace. Izopyknická centrifugace do rovnováhy je velmi účinným separačním nástrojem. V laboratorních podmínkách se využívá jak kontinuálního, tak i diskontinuálního hustotního gradientu. V průmyslových aplikacích se využívá diskontinuálních gradientů k získání precipitovaných proteinů nebo naopak kontaminujících složek Precipitace Rozpustnost proteinů závisí na fyzikálně-chemických vlastnostech prostředí, např. ph, složení a iontové síle roztoku. Když budeme pomalu zvyšovat iontovou sílu roztoku se směsí proteinů, dojde k selektivní precipitaci jednotlivých proteinů. Tento fenomén se označuje jako vysolování. Existuje 7
8 řada látek, které mají odlišný vysolovací potenciál. Dvě série látek s rostoucí vysolovací schopností jsou uvedeny níže, jedna pro negativně (I) a druhá pro pozitivně (II) nabité molekuly: (I) SCN -, I -, CLO - 4, NO - 3, Br -, Cl -, CH 3 COO -, PO , SO 4 (II) Ba 2+, Ca 2+, Mg 2+, Li +, Cs +, Na +, K +, Rb + +, NH 4 Velmi často se pro vysolování proteinů používá síran amonný. Dalším způsobem, jak precipitovat proteiny je použití organických rozpouštědel mísitelných s vodou. V tomto případě dochází ke změně dielektrické konstanty. Příkladem takových látek je polyethylenglykol a kyselina trichloroctová. Za určitých podmínek precipitují také chitosany a neiontové polyoxyethylenové detergenty. Precipitace je jednoduchá a relativně ekonomická technika, kterou lze snadno převádět z malých do velkých objemů. Používají se často k izolaci proteinů ze supernatantu buněčných kultur. Precipitace ale není pro účely purifikace dostačující, protože se spolu s požadovanou látkou sráží i látky kontaminující. S velkým množstvím precipitátu se rovněž často nesnadno manipuluje. Precipitace je přesto často používaná metoda, zvláště u některých aplikací. 8
9 Obr. 6.2: Proces purifikace glykosylovaného rekombinantního interferonu A = adsorpce, DF = diafiltrace, F = filtrace, TFF = tangenciální průtoková filtrace, UF = ultrafiltrace Buněčná kultura TFF/centrifugace Odstranění buněk, buněčných zbytků a částic (virů) UF Odstranění precipitátů a virů ultrafiltrací UF/DF Zkoncentrování kultury bez buněk, kapaliny a diafiltrátu Chromatografie - hydrofobní Odstranění zbývajících kontaminujících proteinů Chromatografie anionty Odstranění proteinů, lipidů, DNA a virů UF/DF Zkoncentrování: nastavení fyzikálních parametrů F Odstranění virů filtrací přes 40 nm filtr Chromatografie gelová filtrace Formulace: oddělení od agregátů UF/DF Zkoncentrování: nastavení fyzikálních parametrů F Sterilizace filtrací Chromatografie - kationty Odstranění BSA a transferinu Plnění Značení Farmaceutická výroba A Inaktivace viru Finální dávkování Chromatografické metody Biologicky aktivní látky tvoří rozsáhlou skupinu sloučenin se speciálními funkcemi, které jsou v podmínkách in vivo řízeny převážně malými změnami v jejich okolí. Proto mohou mít změny ph, iontové síly, koncentrace kovových iontů, kofaktorů atp. následek velké ovlivnění izolovaných biologicky aktivních molekul. Aby během izolace nedocházelo ke ztrátám jejich biologické aktivity, je nutné použít pokud možno co nejmírnější separační metody. Vývoj účinných izolačních metod, jako jsou gelová, ionexová, (bio)afinitní aj. chromatografie a nejrůznější typy elektroforéz, umožnil vývoj celé řady nových odvětví chemie. Bez rozvoje těchto metod by nebyl možný např. současný rozvoj chemie proteinů a nukleových kyselin se všemi významnými důsledky pro molekulární biologii, genové inženýrství, imunochemii aj. odvětví. Jejich další rozvoj není možný bez dostatečného 9
10 množství enzymů, transportních a regulačních proteinů, kofaktorů a jiných přírodních biologicky aktivních sloučenin. Při preparativní chromatografii jsou molekuly separovány na základě rozdílů v distribuci mezi dvěma fázemi, z nichž jedna je stacionární (většinou pevná fáze) a druhá mobilní. Mobilní fáze může být buď kapalina, nebo plyn. V současnosti jsou téměř všechny pevné fáze umístěny v koloně a mobilní fáze procházejí skrz pevnou fázi pomocí tlaku. Procesy purifikace využívají povětšinou dva až tři chromatografické postupy. V tabulce 6.3 je přehled chromatografických metod využívaných při purifikaci biotechnologických produktů. Koncentrace biologicky aktivních látek ve výchozím materiálu bývá obvykle nízká, navíc ve směsi s velkým počtem podobných látek. S výhodou se proto jako první purifikační stupeň izolace volí adsorpce. Je-li k dispozici specifický sorbent, schopný vyvazovat izolovanou biologicky aktivní látku na základě jejího biospecifického komplexu, s výhodou volíme jako první stupeň (a někdy i jako jediný, to v závislosti na účinnosti procesu purifikace) biospecifickou afinitní chromatografii. Protože při fyziologických hodnotách ph je většina proteinů nabitá negativně, využívá se pro jejich izolaci sorpce na anex. Dalším stupněm potom může být gelová chromatografie dělící na základě rozdílů v molekulové hmotnosti nebo některá z elektroforetických metod využívající rozdílu v elektrickém náboji. Izolaci čisté biologicky aktivní látky dosahujeme nejčastěji kombinací několika separačních metod. Při volbě purifikačního schématu bychom měli dbát na to, aby se neopakovaly metody založené na stejném dělícím principu. Stacionární fáze při chromatografii. Chromatografické postupy jsou u purifikačních postupů často oním rychlost-limitujícím krokem. Důležitým primárním faktorem, který má vliv na rychlost procesu, je transport dělených částic do pórů materiálu stacionární fáze. Jako adsorbenty slouží anorganické materiály typu silikagelu, skleněných kuliček, hydroxyapatitu, různých oxidů kovů (oxid hlinitý) a organických polymerů (dextrany, celulóza, agaróza). Separace probíhá na základě diferenciální interakce jednotlivých složek vzorku s chromatografickým médiem. Na interakci se podílí iontové skupiny (např. aminy nebo karboxyskupiny), dipolární skupiny (karbonylová skupina) a skupiny poskytující vodíkové vazby a skupiny akceptorové. Stacionární fáze užívané pro chromatografickou separaci velkých objemů se v posledních desetiletích velmi rozvinuly. Kromě konvenčních systémů se objevila technika tzv. perfúzní chromatografie, při které mobilní fáze protéká skrz velké póry uvnitř solidní fáze (obr. 6.3). Perfúzní chromatografie je rychlejší a i při vyšší rychlosti mobilní fáze si zachovává stejnou rozlišovací schopnost a vazebnou kapacitu. Dalším vývojem v tomto směru jsou spirálně stočené kolony s vysokým průtokem, velkou kapacitou a dobrou efektivitou zachycování částic. Ideální stacionární fáze musí mít řadu charakteristik, např. vysokou mechanickou odolnost, vysokou porozitu, žádné nespecifické interakce mezi proteinem a podpůrnou fází, vysokou kapacitu, biokompatibilitu a vysokou stabilitu matrice v různých rozpouštědlech. Především stabilita matrice v různých rozpouštědlech je nezbytná u těch kolon, které se používají k přípravě klinických materiálů a musí být v pravidelných intervalech čištěny, zbavovány pyrogenních látek, dezinfikovány a sterilizovány. Mnoho z uvedených kritérií splňuje vysokotlaká kapalinová chromatografie (HPLC). 10
11 Tabulka 6.3: Často používané separační postupy a jejich fyzikální principy Separační technika Model/princip Parametr separace Membránová separace Mikrofiltrace Velikost Ultrafiltrace Dialýza Velikost Velikost Centrifugace Izopyknická Denzita Izokineticá Denzita Extrakce Fluidní extrakce Rozpustnost Extrakce tekutina/tekutina Fázové rozhraní, změna rozpustnosti Precipitace Frakční precipitace Změna v rozpustnosti Chromatografie Iontoměničová Náboj Gelová filtrace Afinitní Hydrofobní interakce Adsorpce Velikost Specifické interakce ligandsubstrát Hydrofobicita Vazba kovalentní/nekovalentní Mobilní fáze musí být volena tak, aby docházelo k co nejmenším ztrátám biologické aktivity purifikovaného proteinu. Při HPLC se využívají stacionární fáze s malými póry. Tyto částice jsou malé, pevné a mají přesnou velikost, která zajišťuje velký celkový povrch; ani vysoký tlak tyto částice nedeformuje. Mobilní fáze je protlačována kolonou za vysokého tlaku. Reverzní HPLC systémy využívají méně polární stacionární fáze než je fáze mobilní, jsou používány při velkoobjemových purifikacích a mohou být využity jak k purifikaci, tak i ke koncentrování produktu. HPLC je relativně drahá a není tudíž vhodná pro velkoobjemové separace. Plastové kolony musí být používány jen při nízkém tlaku. Na druhou stranu jsou takové kolony rezistentní vůči všem pufrům na rozdíl o vysokotlakých kolon sestrojených z nerezavějících kovových materiálů. Plastové kolony jsou komerčně dostupné a umožňují purifikaci proteinu v jediném kroku, výsledků lze dosáhnout rychle a s vysokým rozlišením. 11
12 Obr. 6.3: Struktura konvenčních chromatografických částic a částic využívaných při perfúzní chromatografii Konvenční chromatografie Perfúzní chromatografie Adsorpční chromatografie. Adsorpční chromatografie se označuje také jako chromatografie na normální fázi. Při tomto typu chromatografie je stacionární fáze polárnější než fáze mobilní. Proteiny se selektivně váží ke statické matrix za jedněch podmínek a uvolňují za jiných podmínek. Při adsorpční chromatografii je možné nanášet na stacionární fázi velké objemy vzorku. V principu je tato metoda převoditelná na velká množství při nízkých nákladech. Iontoměničová (ionexová) chromatografie. Jejím základem je vratná výměna iontů mezi mobilní kapalnou a stacionární fází ionexů. Nerozpustná matrice obsahuje kovalentně vázané nabité částice, které přitahují opačně nabité částice mobilní fáze. Tyto opačně nabité ionty se mohou reverzibilně vyměňovat s jinými ionty stejného náboje. Jestliže matrice obsahuje pozitivně nabité skupiny, pak se na ni adsorbují negativně nabité ionty a tento ionex se nazývá anex (anion exchanger). V opačném případě obsahuje matrice záporně nabité skupiny, vážou se na ni kationy a ionex se označuje jako katex (cation exchanger). Jako materiál pro ionexy se tradičně používá různě modifikovaná celulóza (CM-celulóza: karboxymethyl OCH 2 COO -, SE-celulóza: -OCH 2 -CH 2 -SO 3 -, P-celulóza: -O-PO 3 -, DEAEcelulóza: diethylaminoethyl O-CH 2 -CH 2 -N + -(C 2 H 5 ) 2, QAE-celulóza: kvarterní arylaminoethyl O-CH 2 - CH 2 -N + -(C 2 H 5 ) 3, a jiné). Pro průmyslové použití jsou tyto materiály vhodné pouze pro vsádkové procesy, neboť je komplikovaná regenerace kolony do původního stavu. Používají se i matrice založené na Sephadexu, také pro vsádkové procesy. Vhodné je i použití ionexů odvozených od agarózy (Trisacryl, Fractogel ). Používají se i ionexy založené na bázi křemičitanů a syntetických polymerů, např. polyakrylátů. Při iontoměničové chromatografii je možné použít také tzv. negativního modu, tedy postupu, při kterém se na kolonu váží kontaminující složky, kdežto protein jí naopak protéká. Ionexová chromatografie patří mezi nejrozšířenější metody, které byly a jsou požívány pro izolace nejrůznějších biologicky aktivních látek (enzymy, nukleové kyseliny, antibiotika, vitamíny, nukleosidy a 12
13 nukleotidy, lipidy, aj.). Objemy při iontoměničové chromatografii lze snadno navýšit. Je také možné, aby mobilní fáze protékala kolonou jako postupný nebo skokový gradient roztoku solí nebo jako roztok s měnící se hodnotou ph. Např. glykosylované proteiny jsou eluovány v relativně širokém spektru hodnot ph a to až do dvou jednotek ph. Při purifikaci proteinů lze s výhodou využít řízenou mutagenezi a vložit do proteinu dodatečné aminokyseliny, které změní jeho eluční vlastnosti. Vhodně se k tomuto účelu používají molekuly argininu, které zajistí rekombinantnímu proteinu schopnost vázat se na katex za úplně jiných podmínek než ostatní proteiny. Afinitní (bioafinitní, imunoafinitní) chromatografie je založena na výjimečné vlastnosti biologicky aktivních látek tvořit pevné specifické reverzibilní komplexy s jinými komplexotvornými sloučeninami, tzv. afinitními ligandy. Principem izolační metody je interakce izolovaného proteinu s ligandem vázaným na pevný nosič. Pro purifikaci proteinů je to velmi účinná metoda. Jako ligand může být použita každá sloučenina, která s danou izolovanou látkou tvoří biospecifický reverzibilní komplex musí obsahovat funkční skupinu, kterou se kovalentně váže na pevný nosič a musí mít dostatečnou afinitu k izolované látce. Ligandy mohou být skupinově specifické nebo obecné. Příkladem tvorby komplexů mohou být dvojice enzym substrát, kofaktor efektor, protilátka antigen, hormon receptor apod. Pro účely separace se při afinitní chromatografii nejčastěji používají imobilizované pyridinové nebo adeninové nukleotidy nebo barviva s antrachinonovou strukturou (Procion Blue, Brown, Red, Green, Cibacron Blue, ) především pro separaci dehydrogenáz a kináz, imobilizovaný hemoglobin nebo kasein pro proteolytické enzymy, organortuťné deriváty pro izolace merkaptosloučenin, imobilizované lektiny pro izolace glykoproteinů, povrchových buněčných receptorů nebo celých buněk, imobilizované kovové ionty, např. Zn 2+ nebo Ni 2+, pro separaci proteinů. Jako pevný nosič se používá Sephadex nebo Trisacryl. Proteiny se k afinitním kolonám váží převážně za fyziologických podmínek. Kontaminanty jsou odstraněny intenzívním promýváním matrice a čistý protein je získáván poté, co se do mobilní fáze přidá činidlo kompetující s ligandem o vazebná místa na pevné fázi nebo po změně fyzikálních podmínek (např. ph eluentu), které vedou ke změně vazebných schopností proteinu. Příklady afinitní chromatografie aplikované na proteiny Vazba glykoproteinů na imobilizované lektiny (eluentem může být cukr) Vazba serinových proteáz na imobilizovaný lyzin (eluentem může být lyzin samotný) Protilátka a imobilizovaný protein A, který se váže na Fc fragment protilátky Protilátka a imobilizovaný protein G, který se taky váže na Fc fragment protilátky Hormony a růstové faktory a jejich imobilizované receptory nebo krátké peptidy tyto 13
14 receptory napodobující Některé proteiny mají vysoce selektivní vazebné schopnosti na komerčně dostupné látky. Při výrobě farmaceutických přípravků je třeba zajistit, aby tyto látky nebyly karcinogenní a aby se během chromatografie neuvolňovaly do mobilní fáze. Tzv. fúzní rekombinantní proteiny jsou exprimovány s partnerským haptenem, prostřednictvím kterého se jakýkoli protein může afinitně vázat ke specifickému ligandu. Po vyčištění je fúzní partner odštěpen specifickou proteázou a hapten je pak odstraněn jinou metodou. Tzv. imunoafinitní chromatografie využívá schopnosti protilátky vázat se ke svému specifickému epitopu. Metoda je použitelná k purifikaci protilátky nebo i antigenu, záleží na tom, co připojíme k pevné fázi. K výhodám imunoafinitní chromatografie patří vysoká specifičnost a spojení zkoncentrování a purifikace do jednoho kroku. Nevýhodou je někdy velmi silná vazba protilátky k antigenu. K imunoafinitní chromatografii je zapotřebí mít specifický receptor, což může činit problémy při přechodu na větší purifikační objemy a komercionalizaci. Imunoafinitní chromatografie byla využita k purifikaci např. interferonů, urokinázy, faktoru VIII:C, erytropoetinu, interleukinu 2, lidského faktoru X a rekombinantního aktivátoru tkáňového plasminogenu. Jako nová metoda, využívaná zatím převážně v laboratorním měřítku se používá vysokoúčinná bioafinitní chromatografie (HPLAC) plně automatizovaný systém pracující za zvýšeného tlaku. Při této metodě je možno mimo jiné dosáhnout lepšího rozlišení než při klasickém způsobu. Hydrofobní chromatografie. Principem této metody je dělení na normální fázi, rozpouštědlem je tedy voda. Za fyziologických podmínek je většina hydrofobních aminokyselin zanořena uvnitř proteinové globule a jen malá část je jich vystrčena na povrch. Naopak hydrofilní aminokyseliny se velmi ochotně spojují s okolními molekulami vody. Vysoké koncentrace solí snižují hydrataci proteinu a na jejich povrchu se objevuje více zbytků hydrofobních aminokyselin. Hydrofobní chromatografie je založena na nekovalentních a ne-elektrostatických interakcích mezi proteiny a stacionární fází. Hydrofobní charakteristiky rozpouštědla lze modulovat koncentracemi anorganických solí. Často se používá síran amonný nebo chlorid sodný. Pokud je koncentrace solí vysoká (až několika molární), jsou proteiny k hydrofobnímu povrchu matrix přitahovány. S klesající koncentrací solí afinita proteinu k pevné fázi klesá a proteiny jsou postupně vymývány. Metoda sice nemá tak vysokou rozlišovací schopnost jako RF-HPLC, ale použité chemikálie jsou vůči děleným proteinům mnohem méně agresívní, umožňuje obvykle získat vysoké výtěžky nepoškozených správně sbalených proteinů. Je ideální ji v purifikačním schématu zařadit za iontoměničovou chromatografii, při které je protein obvykle eluován v prostředí s vysokou iontovou silou. Gelová chromatografie. Dělení je při této metodě založeno na rozdílné velikosti a tvaru jednotlivých látek (obr. 6.4). Označuje se jako GPC (gelová permeační chromatografie) nebo SEC (Size exclusion chromatography nebo Steric exclusion chromatography) nebo taky jako gelová filtrace. Stacionární fáze je tvořena porézním materiálem, pro biologicky aktivní látky nejčastěji gelem, jehož inertní zesítěná polymerní matrice je nasycena kapalinou, nejčastěji vodou. Stejná kapalina pak může 14
15 být použita i jako mobilní fáze. Při průchodu směsi látek touto porézní stacionární fázi dochází k tomu, že malé molekuly jsou schopny difundovat dovnitř pórů matrice a jejich pohyb je tedy zpomalen, zatímco velké molekuly se nezachytí a prochází matricí rychleji čím větší molekula, tím rychleji prochází ven z kolony. Postupným promývání mobilní fází se ven z kolony vymyjí i malé molekuly. Důležité je, aby mezi děleným roztokem a matricí nedocházelo k žádným vazbám nebo k denaturaci děleného materiálu. Jako materiál na gelovou filtraci se tradičně používá zesíťovaný dextran (Sephadex) nebo polyakrylamid (BioGel P), které jsou vhodné pro laboratorní měřítko, ale pro výrobní potřeby jsou příliš měkké v průmyslu se používají rigidnější gely, např. Sephadex G25 nebo G5O, Sephacryl (dextran + PAD), Superdex (dextran + agaróza), Ultrogel AcA (agarosa + PAD) Superosa (zesíťovaná agaróza), Cellufin (celulóza) aj. Někdy se používají i materiály založené na silikagelu nebo porézním skle, ale ty nejsou většinou příliš vhodné pro biologické izolace jejich povrch je hydrofobní, proto nezřídka dochází k ireverzibilní vazbě proteinů na povrch matrice a uvolnění z matrice může probíhat pouze za podmínek hrozících denaturací. Řešením je modifikace tohoto materiálu hydrofilním polymerem, který může být dále derivatizován vhodnými skupinami. Pro průmyslové využití je metoda obvykle nepoužitelná, protože je při ní na malý vzorek zapotřebí velké kolony. Používá se v pozdějších fázích purifikace, kdy je už protein dostupný ve velmi koncentrovaném stavu. Jako konečný krok purifikace se hodí proto, že je při ní protein převeden do vhodného pufru, který se používá před finální preparací produktu. V této fází už neovlivní konečnou čistotu proteinu. Obr. 6.4: Schématické znázornění principu gelové filtrace Zesíťované částice gelu Malé molekuly mohou vstoupit dovnitř Velké molekuly nemohou vstoupit dovnitř 15
16 Vysokotlaká kapalinová chromatografie v reverzní fázi. Tato metoda (reversed-phase high performance liquid chromatography, RP-HPLC) využívá hydrofobních vlastností proteinů. Funkční skupiny na pevné fázi obsahují jeden až osmnáct atomů uhlíku na uhlovodíkovém řetězci. Čím delší řetězec je, tím hydrofobnější pevná fáze je. Proteiny vázané na matrix jsou z ní uvolněny použitím mobilní fáze s ještě větší hydrofobicitou. Většinou se používá acetonitril nebo etanol. Technika je velmi citlivá, dokáže odlišit molekuly s jediným atomem kyslíku navíc, když například dojde k oxidaci jediného zbytku methioninu nebo když dojde k hydrolýze aminoskupiny na glutaminu nebo asparaginu. Hydrofobicitu proteinu mění taky vytvoření disulfidické vazby. Metodu je tedy kromě studia homogenity proteinového izolátu využít taky ke sledování degradace přípravku např. při dlouhodobém skladování. Vysokoúčinná kapalinová chromatografie pracuje v plně automatizovaných zařízeních, které využívají k pohybu mobilní fáze zvýšeného tlaku, což vede k lepšímu rozlišení než při klasickém způsobu chromatografie. Kolony s rozšířeným filtrem. Jak už bylo řečeno dříve, jsou purifikační schémata založena na několika za sebou seřazených protokolech. To ovšem jednak zvyšuje cenu za purifikaci, ale navíc zvyšuje ztráty, protože v každém purifikačním kroku se část produkce ztratí. Proto se stále vyvíjejí postupy, které mají celou purifikaci zjednodušit. Konvenčním formátem adsorpční chromatografie jsou tzv. packed columns neboli kolony s pevným filtrem. V těchto typech kolon ale zůstává část materiálu uchycena ve vstupní části filtru a doslova ho ucpává. Tomu lze zabránit použitím pre-filtru s póry o průměru 0,2 μm. Dalším řešením je použití tzv. expanded columns neboli kolon s rozšířeným nebo taky tzv. fluidním filtrem (obr. 6.5). Rozšířený filtr nemá částice upěchované ve vrstvách, ale volně se vznášející v proudící mobilní fázi. Mobilní fáze působí proti gravitační síle, která normálně strhává částice dolů. A pokud je rychlost průtoku mobilní fáze správně vybalancovaná s ohledem na velikost částic, jejich viskozitu a hustotu mobilní fáze, pak se částice v koloně neusazují, ale permanentně se vznášejí. Velké částice (např. buňky) proudí kolonou ven a neucpávají ji. Purifikované molekuly jsou naopak selektivně zachycovány na adsorpčních částicích. Na takovou kolonu je možno aplikovat vzorek bez jeho předchozího pročištění např. centrifugací nebo filtrací, což zkracuje proces purifikace a snižuje cenu. V principu lze použitím rozšířeného filtru dosáhnout pročištění vzorku, jeho zkoncentrování a purifikace v jediném kroku. Z technologického hlediska je možno použít stejné kolony jako u aplikací s pevným filtrem. Co se separačního principu týče, je nejčastěji využívaná iontoměničová chromatografie. Technika našla uplatnění i v průmyslových aplikacích, při purifikacích antibiotik, např. streptomycinu a novobiocinu. 16
17 Obr. 6.5: Srovnání mezi kolonou s fixním (A) a rozšířeným (B) filtrem A B Buňky prostupují filtrem bez překážek Částice pevné fáze Zátka vytvořená z buněk Mobilní fáze obsahující nerozbité částice 17
18 6.4. Další otázky spojené s produkcí a purifikací proteinů Heterogenita N- a C-konců Hlavním problémem spojeným s expresí rekombinantních proteinů je jejich N-konec, který v případě produkce v E. coli začíná formylmetioninem. Pokud exprese proteinu neprobíhá správně, vznikají metionylované varianty polypeptidových řetězců nebo na N-konci chybí jedna nebo i více aminokyselin. Tomuto jevu se říká heterogenita N-konců. Tento fenomén je častý u rekombinantních proteinů citlivých k proteázám, které jsou buďto secernovány hostitelem nebo vneseny do média jako součást séra. Tyto proteázy odstřihují aminokyseliny od C- nebo N-konce a vytváří C- nebo N-koncovou heterogenitu. C- nebo N-koncová heterogenita je jevem nežádoucím, protože může způsobit problémy při purifikaci a charakterizaci proteinů. Přítomnost nadbytečných metioninů na N-konci mění sekundární a terciární strukturu proteinů. To může vést ke změně biologické aktivity a stability a zvyšovat imunogennost proteinu. Kromě toho je N-koncový metionin, ale i metionin uvnitř řetězce citlivý k oxidaci Chemická modifikace/konformační změny Ačkoli jsou savčí buňky schopny produkovat proteiny strukturálně shodné s proteiny endogenními, je třeba vždy postupovat obezřetně. Transkripty, které obsahují kódující sekvence genů pro příslušné proteiny, mohou být matricí pro konformační izomery těchto proteinů, protože neobvyklé sekundární struktury takových transkriptů mohou ovlivnit translaci. Dalším faktorem, který je třeba mít v patrnosti, je možná existence ekvilibria mezi požadovanou přirozenou formou proteinu a formami jinými, např. dimery. Pro biologickou aktivitu proteinů je esenciální jejich správné sbalení. Proto je důležité stanovit, jestli jsou všechny molekuly rekombinantního proteinu produkované v savčích buňkách opravdu sbaleny do správné struktury. Někdy se nesprávně sbalené proteiny stanoví snadno, jindy je to obtížné. Kromě konformačních změn mohou být proteiny v průběhu purifikace modifikovány proteolýzou, deaminací, hydroxylací nebo oxidací sulfhydrylových skupin. Tyto modifikace mohou vést k alespoň částečné denaturaci. A na druhou stranu může denaturace proteinů vést k chemickým modifikacím Glykosylace Mnoho terapeutických proteinů produkovaných metodami genového inženýrství jsou glykoproteiny. Přítomnost a povaha postranních řetězců oligosacharidů ovlivňuje řadu důležitých charakteristik, např. poločas proteinu v séru, rozpustnost, stabilitu a někdy i farmakologický účinek. Např. darboetin, geneticky modifikovaný erytropoetin 2. generace, obsahuje 80% uhlovodíků, zatímco přirozený glykoprotein jen 40%. To vede k prodloužení poločasu po intravenózní aplikaci u darboetinu z 8 na 24 hodin. Glykosylace proteinu není závislá na sekvenci DNA, je to enzymatická modifikace polypeptidového řetězce po translaci a může být závislá na prostředí uvnitř buňky. Savčí buňky obecně glykosylační mechanismy mají, ale stejně není možné kontrolovat celý proces glykosylace. Heterogenita glykosylace se projeví na délce postranních řetězců, typu oligosacharidu a vlastní 18
19 sekvenci uhlovodíku. Příkladem heterogenity glykosylace u rekombinantních proteinů jsou interleukin-4, gonádotropin, erytropoetin a tkáňový plasminogenový aktivátor. Struktura oligosacharidů a jejich složení se pochopitelně u různých expresních systémů liší. U hmyzích buněk jsou sekvence zpravidla kratší, než je tomu u savčích buněk. Rozdíly jsou ale také mezi jednotlivými druhy buněk savčích Proteolýza Proteázy hrají důležitou roli při úpravách rekombinantních proteinů, při jejich maturaci, modifikaci a taky při izolaci. Proteázy savčích buněk se podílejí na sekreci rekombinantních proteinů do kultivačního média. Dochází-li k sekreci kotranslačně, pak vnitrobuněčný proteolytický systém nebezpečný není. Proteázy se ale vylijí z buněk, když tyto zahynou nebo jsou poškozeny a lyzují. Je proto nezbytné zajistit, aby k poškozování buněk během purifikace nedocházelo. Dalším zdrojem proteolýzy jsou složky média, ve kterém buňky rostou. Sérum obsahuje řadu proteáz a zymogenů, které mohou ovlivnit secernované rekombinantní proteiny. Činnost proteáz lze omezit působením inhibitorů. Je vhodné kontrolovat integritu rekombinantního proteinu v každém kroku purifikace. Proteiny jsou mnohem citlivější k působení proteáz za zvýšené teploty. Purifikace se proto zpravidla provádějí při 4 C. Protože řada proteáz využívá jako kofaktor Ca 2+, přidávají se do purifikačních složek chelatační činidla, která Ca 2+ vychytávají Tvorba inkluzních tělísek V cytoplasmě bakterií vytvářejí proteiny husté, zrnité inkluze, tzv. inkluzní tělíska. Inkluzní tělíska se často tvoří v bakteriálních buňkách, které exprimují velká množství rekombinantního proteinu. V elektronovém mikroskopu lze inkluzní tělíska pozorovat jako velké husté útvary často přes celý průměr buněk. Inkluzní tělíska jsou amorfní proteinové agregáty držené pohromadě kovalentními i nekovalentními vazbami. Množství proteinů uložených v inkluzních tělískách nelze změřit přímo, takže není možno ani přesně změřit množství vytěženého proteinu. Inkluzní tělíska jsou nerozpustné komplexy, což může při velkoobjemových výrobách být fatální. Existují ale postupy, kterými je možno z inkluzních tělísek získat plně funkční struktury proteinů. Nejprve je nutné rozbít buňky a inkluzní tělíska uvolnit. Poté následuje rozpuštění inkluzí, což je ale většinou spojeno s velkým navýšením objemu izolátu. Zpravidla se inkluzní tělíska rozpouštějí v denaturačních činidlech, např. SDS, močovině nebo guanidium chloridu. Bakteriální expresní systémy zpravidla nedokáží vytvářet disulfidické můstky, opětovné sbalení proteinu (tzv. re-folding) je tedy třeba provádět v oxidativním prostředí. Proces se označuje taky jako renaturace proteinu. Ovšem čím více disulfidických můstků nativní protein obsahuje, tím nižší je výtěžek správně sbalených molekul. Poté, co je protein solubilizován, používá se k další purifikaci konvenčních chromatografických postupů. Ačkoli se agregované struktury jeví na první pohled jako nežádoucí, mohou být výhodné v takových případech, kdy je protein možno rozbalit a zase správně sbalit. Inkluzní tělíska je totiž možné snadno izolovat v čistotě přesahující 50%. Agregované struktury jsou taky odolné k proteázám. 19
20 6.5. Shrnutí kapitoly Pro dosažení optimálních růstových podmínek v bioreaktoru je třeba zabezpečit vhodné složení živného média. Média používaná ke kultivaci buněk jsou komplexní a sestávají ze směsi různých složek, z nichž většina je dostupná jako komerční preparáty, které stačí jen rozpustit ve vodě a sterilizovat. V případě savčích buněk tvoří významnou složku média fetální telecí sérum, jehož složení bývá velmi proměnlivé. Proto byla vyvinuta tzv. sérum-free média, která sérum neobsahují. Obecným trendem je vytvářet média taková, která složité nedefinované složky neobsahují. Kvalita se obvykle vyjadřuje v termínech čistoty a reprodukovatelnosti. Čistota farmaceutických přípravků je většinou vyšší než 99%, pokud jsou podávány parenterálně. Ke kontaminujícím složkám patří viry, bakterie, buněčná DNA nebo proteiny. Procesy purifikace biotechnologických procesů jsou zpravidla finančně náročnější než procesy samotné výroby rekombinantního produkčního organismu. Vývoj procesu purifikace má dvě stádia formulace (design) a zvýšení objemu (scale-up). Vytvoření správného purifikačního postupu je usnadněno, když se podaří definovat hlavní kontaminující složky a popsat fyzikální charakteristiky produktu. Jakákoli substance, která se aplikuje injekčně, musí být sterilní a prostá pyrogenních látek, respektive pyrogenní látky musí být přítomny v podlimitních množstvích, která jsou definována v lékopisu podle typu produktu. K separaci proteinů na základě různých fyzikálně-chemických kritérií (velikost, náboj, hydrofobicita, rozpustnost) existuje celá řada dostupných metod. Většina purifikačních procesů počítá s alespoň jedním krokem, ve kterém jsou odstraněny celé nebo lyzované buňky, nejčastěji se používá centrifugace nebo filtrace. Závislosti rozpustnosti proteinů na fyzikálně-chemických vlastnostech prostředí se využívá při jejich precipitaci. Proteiny lze precipitovat také pomocí organických rozpouštědel mísitelných s vodou. Precipitace je jednoduchá a relativně ekonomická technika, kterou lze snadno převádět z malých do velkých objemů. Používají se často k izolaci proteinů ze supernatantu buněčných kultur. Chromatografické metody (adsorpční, gelová, ionexová, afinitní, hydrofobní) využívají té skutečnosti, že biologicky aktivní látky tvoří rozsáhlou skupinu sloučenin se speciálními funkcemi, které jsou v podmínkách in vivo řízeny malými změnami v jejich okolí. Proto mohou mít změny ph, iontové síly, koncentrace kovových iontů, kofaktorů apod. za následek velké ovlivnění izolovaných molekul. Při chromatografii jsou molekuly separovány na základě rozdílů v distribuci mezi dvěma fázemi, z nichž jedna je stacionární a druhá mobilní. V současnosti jsou téměř všechny stacionární fáze umístěny v koloně a mobilní fáze procházejí skrz pomocí tlaku. Procesy purifikace využívají povětšinou dva až tři chromatografické postupy. Obecně platí, že při volbě purifikačního schématu bychom měli dbát na to, aby se neopakovaly metody založené na stejném dělícím principu. Při purifikaci proteinů se setkává biotechnolog s komplikujícími prvky jako je heterogenita N- a C- konců, změna konformace, proteolýza, deaminace, hydroxylace nebo oxidace sulfhydrylových skupin. Specifickou pozornost je třeba věnovat glykosylovaným proteinům jejichž oligosacharidová složka je u různých expresních systémů různá. V cytoplasmě bakterií vytvářejí proteiny inkluzní tělíska. Ta se často tvoří také v bakteriálních buňkách, které exprimují velká množství rekombinantního proteinu. Ačkoli se inkluzní tělíska jeví jako nežádoucí, mohou být výhodné tehdy, když je protein možno rozbalit a zase správně sbalit. Inkluzní tělíska je možné snadno izolovat v čistotě přesahující 50% a jsou taky odolná k proteázám. 20
21 6.6. Příklady a úlohy k zamyšlení 1) Z uvedeného seznamu dekontaminačních metod vyberte ty, které jsou vhodné k odstranění virů, bakterií, kontaminující DNA nebo proteinů: Filtrace přes 0,2 μm filtr Nanofiltrace Chromatografie 2) Přiřaďte vhodný způsob sterilizace příslušného materiálu Metoda sterilizace horkým vzduchem při 180 C autoklávování filtrace Materiál Živná média Antibiotika Skleněné nástroje 3) Jestliže v jednom mililitru lidské krve je obsaženo přibližně 4 až 10 milionů leukocytů, kolik μg DNA je možno maximálně izolovat z 200 μl plné krve? Přitom jeden leukocyt obsahuje DNA o celkové délce 2,9 miliardy nukleotidů, a že průměrná molekulová hmotnost jednoho nukleotidu je ) Jaké množství vodného roztoku gentamycinu o zásobní koncentraci 50mg/ml použijete k dekontaminaci μl buněčné kultury od mykoplasmat, jestliže pracovní koncentrace antibiotika má být 100 μg/ml? 5) Jaké množství buněčné kultury (v litrech) potřebujete k získání 5g rekombinantního proteinu, jestliže jste dokázali z 500 ml kultury izolovat 100 mg tohoto proteinu? 6) Při jakých otáčkách budete separovat bakteriální buňky od živného média, jestliže máte provádět centrifugaci při 1 000g po dobu 10 minut a máte k dispozici centrifugu s rotorem o poloměru 10cm? 7) Jestliže se kvasinky usazují v centrifuze o poloměru 10 cm při rpm, jaká je hodnota relativního odstředivého zrychlení, která na ně působí? 21
Izolace nukleových kyselin
 Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti CHROMATOGRAFIE
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti CHROMATOGRAFIE Chromatografie co je to? : široká škála fyzikálních metod pro analýzu nebo separaci komplexních směsí proč je to super?
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti CHROMATOGRAFIE Chromatografie co je to? : široká škála fyzikálních metod pro analýzu nebo separaci komplexních směsí proč je to super?
Stručný úvod ke cvičnému programu purifikace proteinů:
 Stručný úvod ke cvičnému programu purifikace proteinů: zopakovaní základních principů a postupů Mirka Šafaříková Tel. 38777 5627 mirkasaf@usbe.cas.cz Na Sádkách 7, 1. patro, č. dveří 140 Acidobazické rovnováhy
Stručný úvod ke cvičnému programu purifikace proteinů: zopakovaní základních principů a postupů Mirka Šafaříková Tel. 38777 5627 mirkasaf@usbe.cas.cz Na Sádkách 7, 1. patro, č. dveří 140 Acidobazické rovnováhy
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti ELEKTROMIGRAČNÍ METODY
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti ELEKTROMIGRAČNÍ METODY ELEKTROFORÉZA K čemu to je? kritérium čistoty preparátu stanovení molekulové hmotnosti makromolekul stanovení izoelektrického
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti ELEKTROMIGRAČNÍ METODY ELEKTROFORÉZA K čemu to je? kritérium čistoty preparátu stanovení molekulové hmotnosti makromolekul stanovení izoelektrického
Metody práce s proteinovými komplexy
 Metody práce s proteinovými komplexy Zora Nováková, Zdeněk Hodný Proteinové komplexy tvořeny dvěma a více proteiny spojenými nekovalentními vazbami Van der Waalsovy síly vodíkové můstky hydrofobní interakce
Metody práce s proteinovými komplexy Zora Nováková, Zdeněk Hodný Proteinové komplexy tvořeny dvěma a více proteiny spojenými nekovalentními vazbami Van der Waalsovy síly vodíkové můstky hydrofobní interakce
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253
 Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 16 Iontová chromatografie Iontová chromatografie je speciální technika vyvinutá pro separaci anorganických iontů a organických
Příprava materiálu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Část 16 Iontová chromatografie Iontová chromatografie je speciální technika vyvinutá pro separaci anorganických iontů a organických
Izolace RNA. doc. RNDr. Jan Vondráček, PhD..
 Izolace RNA doc. RNDr. Jan Vondráček, PhD.. Metodiky izolace RNA celková buněčná RNA ( total RNA) zahrnuje řadu typů RNA, které se mohou lišit svými fyzikálněchemickými vlastnostmi a tedy i nároky na jejich
Izolace RNA doc. RNDr. Jan Vondráček, PhD.. Metodiky izolace RNA celková buněčná RNA ( total RNA) zahrnuje řadu typů RNA, které se mohou lišit svými fyzikálněchemickými vlastnostmi a tedy i nároky na jejich
Typy molekul, látek a jejich vazeb v organismech
 Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Imunochemické metody. na principu vazby antigenu a protilátky
 Imunochemické metody na principu vazby antigenu a protilátky ANTIGEN (Ag) specifická látka (struktura) vyvolávající imunitní reakci a schopná vazby na protilátku PROTILÁTKA (Ab antibody) molekula bílkoviny
Imunochemické metody na principu vazby antigenu a protilátky ANTIGEN (Ag) specifická látka (struktura) vyvolávající imunitní reakci a schopná vazby na protilátku PROTILÁTKA (Ab antibody) molekula bílkoviny
Zkušební okruhy k přijímací zkoušce do magisterského studijního oboru:
 Biotechnologie interakce, polarita molekul. Hydrofilní, hydrofobní a amfifilní molekuly. Stavba a struktura prokaryotní a eukaryotní buňky. Viry a reprodukce virů. Biologické membrány. Mikrobiologie -
Biotechnologie interakce, polarita molekul. Hydrofilní, hydrofobní a amfifilní molekuly. Stavba a struktura prokaryotní a eukaryotní buňky. Viry a reprodukce virů. Biologické membrány. Mikrobiologie -
Molekulární biotechnologie č.9. Cílená mutageneze a proteinové inženýrství
 Molekulární biotechnologie č.9 Cílená mutageneze a proteinové inženýrství Gen kódující jakýkoliv protein lze izolovat z přírody, klonovat, exprimovat v hostitelském organismu. rekombinantní protein purifikovat
Molekulární biotechnologie č.9 Cílená mutageneze a proteinové inženýrství Gen kódující jakýkoliv protein lze izolovat z přírody, klonovat, exprimovat v hostitelském organismu. rekombinantní protein purifikovat
SPE je metoda vhodná pro rychlou přípravu vzorků, která užívá
 Extrakce na pevné fázi (SPE) Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Extrakce na pevné fázi (SPE) (Solid Phase Extraction) SPE je metoda vhodná pro rychlou přípravu vzorků,
Extrakce na pevné fázi (SPE) Příprava předmětu byla podpořena projektem OPPA č. CZ.2.17/3.1.00/33253 Extrakce na pevné fázi (SPE) (Solid Phase Extraction) SPE je metoda vhodná pro rychlou přípravu vzorků,
Gelová permeační chromatografie
 Gelová permeační chromatografie (Gel Permeation Chromatography - GPC) - separační a čisticí metoda - umožňuje separaci skupin sloučenin s podobnou molekulovou hmotností (frakcionace) - analyty jsou po
Gelová permeační chromatografie (Gel Permeation Chromatography - GPC) - separační a čisticí metoda - umožňuje separaci skupin sloučenin s podobnou molekulovou hmotností (frakcionace) - analyty jsou po
Lékařská chemie a biochemie modelový vstupní test ke zkoušce
 Lékařská chemie a biochemie modelový vstupní test ke zkoušce 1. Máte pufr připravený smísením 150 ml CH3COOH o c = 0,2 mol/l a 100 ml CH3COONa o c = 0,25 mol/l. Jaké bude ph pufru, pokud přidáme 10 ml
Lékařská chemie a biochemie modelový vstupní test ke zkoušce 1. Máte pufr připravený smísením 150 ml CH3COOH o c = 0,2 mol/l a 100 ml CH3COONa o c = 0,25 mol/l. Jaké bude ph pufru, pokud přidáme 10 ml
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ TÉMATA PŘEDNÁŠEK
 VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ TÉMATA PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI Transport látek porézními membránami - Plouživý tok nestlačitelných tekutin vrstvou částic - Plouživý tok stlačitelných tekutin
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ TÉMATA PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI Transport látek porézními membránami - Plouživý tok nestlačitelných tekutin vrstvou částic - Plouživý tok stlačitelných tekutin
Chromatofokusace. separace proteinů na základě jejich pi vysoké rozlišení. není potřeba připravovat ph gradient zaostřovací efekt jednoduchost
 Chromatofokusace separace proteinů na základě jejich pi vysoké rozlišení není potřeba připravovat ph gradient zaostřovací efekt jednoduchost Polypufry - amfolyty Stacionární fáze Polybuffer 96 - ph 9-6
Chromatofokusace separace proteinů na základě jejich pi vysoké rozlišení není potřeba připravovat ph gradient zaostřovací efekt jednoduchost Polypufry - amfolyty Stacionární fáze Polybuffer 96 - ph 9-6
ÚPRAVA VODY V ENERGETICE. Ing. Jiří Tomčala
 ÚPRAVA VODY V ENERGETICE Ing. Jiří Tomčala Úvod Voda je v elektrárnách po palivu nejdůležitější surovinou Její množství v provozních systémech elektráren je mnohonásobně větší než množství spotřebovaného
ÚPRAVA VODY V ENERGETICE Ing. Jiří Tomčala Úvod Voda je v elektrárnách po palivu nejdůležitější surovinou Její množství v provozních systémech elektráren je mnohonásobně větší než množství spotřebovaného
Vysokoúčinná kapalinová chromatografie
 Vysokoúčinná kapalinová chromatografie HPLC High Performance Liquid Chromatography Vysokoúčinná...X... Vysoceúčinná kapalinová chromatografie RRLC Rapid Resolution Liquid Chromatography Rychle rozlišovací
Vysokoúčinná kapalinová chromatografie HPLC High Performance Liquid Chromatography Vysokoúčinná...X... Vysoceúčinná kapalinová chromatografie RRLC Rapid Resolution Liquid Chromatography Rychle rozlišovací
Chromatografie. Petr Breinek
 Chromatografie Petr Breinek Chromatografie-I 2012 Společným znakem všech chromatografických metod je kontinuální dělení složek analyzované směsi mezi dvěma fázemi. Pohyblivá fáze (mobilní), eluent Nepohyblivá
Chromatografie Petr Breinek Chromatografie-I 2012 Společným znakem všech chromatografických metod je kontinuální dělení složek analyzované směsi mezi dvěma fázemi. Pohyblivá fáze (mobilní), eluent Nepohyblivá
Seminář izolačních technologií
 Seminář izolačních technologií Zpracoval: Karel Bílek a Kateřina Svobodová Podpořeno FRVŠ 2385/2007 a 1305/2009 Úpravy a aktualizace: Pavla Chalupová ÚMFGZ MZLU v Brně 1 Lokalizace jaderné DNA 2 http://www.paternityexperts.com/basicgenetics.html
Seminář izolačních technologií Zpracoval: Karel Bílek a Kateřina Svobodová Podpořeno FRVŠ 2385/2007 a 1305/2009 Úpravy a aktualizace: Pavla Chalupová ÚMFGZ MZLU v Brně 1 Lokalizace jaderné DNA 2 http://www.paternityexperts.com/basicgenetics.html
1. Metodika. Protokol č. F1-4 Metodika: Srovnávací analýza efektivity přípravy rekombinantního proteinu ve fermentoru
 Protokol č.: F1-4 Datum: 20.12.2010 Metodika: analýza efektivity přípravy výběr z výsledků ze zkušebních provozů výroby antigenů. Vypracoval: Ing. Václav Filištein, Mgr. Tereza Chrudimská, Spolupracující
Protokol č.: F1-4 Datum: 20.12.2010 Metodika: analýza efektivity přípravy výběr z výsledků ze zkušebních provozů výroby antigenů. Vypracoval: Ing. Václav Filištein, Mgr. Tereza Chrudimská, Spolupracující
Analýza kofeinu v kávě pomocí kapalinové chromatografie
 Analýza kofeinu v kávě pomocí kapalinové chromatografie Kofein (obr.1) se jako přírodní alkaloid vyskytuje v mnoha rostlinách (např. fazolích, kakaových bobech, černém čaji apod.) avšak nejvíce je spojován
Analýza kofeinu v kávě pomocí kapalinové chromatografie Kofein (obr.1) se jako přírodní alkaloid vyskytuje v mnoha rostlinách (např. fazolích, kakaových bobech, černém čaji apod.) avšak nejvíce je spojován
METODY ČIŠTĚNÍ ORGANICKÝCH LÁTEK
 METODY ČIŠTĚNÍ ORGANICKÝCH LÁTEK Chemické sloučeniny se připravují z jiných chemických sloučenin. Tento děj se nazývá chemická reakce, kdy z výchozích látek (reaktantů) vznikají nové látky (produkty).
METODY ČIŠTĚNÍ ORGANICKÝCH LÁTEK Chemické sloučeniny se připravují z jiných chemických sloučenin. Tento děj se nazývá chemická reakce, kdy z výchozích látek (reaktantů) vznikají nové látky (produkty).
Název: Vypracovala: Datum: Zuzana Lacková. záleží na tom, co chceme dělat 1) METHALOTIONEIN 2) GFP
 Název: Vypracovala: Zuzana Lacková Datum: 7. 2. 2014 Reg.č.projektu: CZ.1.07/2.4.00/323 Název projektu: Partnerská síť centra excelentního bionanotechnologického výzkumu MĚLI BYCHOM ZNÁT: informace, které
Název: Vypracovala: Zuzana Lacková Datum: 7. 2. 2014 Reg.č.projektu: CZ.1.07/2.4.00/323 Název projektu: Partnerská síť centra excelentního bionanotechnologického výzkumu MĚLI BYCHOM ZNÁT: informace, které
Molekulárně biologické metody v mikrobiologii. Mgr. Martina Sittová Jaro 2014
 Molekulárně biologické metody v mikrobiologii Mgr. Martina Sittová Jaro 2014 Harmonogram 1. den Izolace DNA 2. den Měření koncentrace DNA spektrofotometricky, real-time PCR 3. den Elektroforéza Molekulární
Molekulárně biologické metody v mikrobiologii Mgr. Martina Sittová Jaro 2014 Harmonogram 1. den Izolace DNA 2. den Měření koncentrace DNA spektrofotometricky, real-time PCR 3. den Elektroforéza Molekulární
Struktura proteinů. - testík na procvičení. Vladimíra Kvasnicová
 Struktura proteinů - testík na procvičení Vladimíra Kvasnicová Mezi proteinogenní aminokyseliny patří a) kyselina asparagová b) kyselina glutarová c) kyselina acetoctová d) kyselina glutamová Mezi proteinogenní
Struktura proteinů - testík na procvičení Vladimíra Kvasnicová Mezi proteinogenní aminokyseliny patří a) kyselina asparagová b) kyselina glutarová c) kyselina acetoctová d) kyselina glutamová Mezi proteinogenní
Aminokyseliny, peptidy a bílkoviny
 Aminokyseliny, peptidy a bílkoviny Dělení aminokyselin Z hlediska obsahu v živé hmotě Z hlediska významu ve výživě Z chemického hlediska Z hlediska rozpustnosti Dělení aminokyselin Z hlediska obsahu v
Aminokyseliny, peptidy a bílkoviny Dělení aminokyselin Z hlediska obsahu v živé hmotě Z hlediska významu ve výživě Z chemického hlediska Z hlediska rozpustnosti Dělení aminokyselin Z hlediska obsahu v
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ SYLABY PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI MEMBRÁNOVÉ MATERIÁLY
 VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ SYLABY PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI zodpovědni: P. Mikulášek, H. Jiránková, M. Šípek, K. Friess, K. Bouzek Transport látek porézními membránami (P. Mikulášek)
VÝUKOVÝ MODUL MEMBRÁNOVÝCH PROCESŮ SYLABY PŘEDNÁŠEK TRANSPORT LÁTEK MEMBRÁNAMI zodpovědni: P. Mikulášek, H. Jiránková, M. Šípek, K. Friess, K. Bouzek Transport látek porézními membránami (P. Mikulášek)
Analýza magnetických mikročástic mikroskopií atomárních sil
 Analýza magnetických mikročástic mikroskopií atomárních sil Zapletalová 1 H., Tvrdíková 2 J., Kolářová 1 H. 1 Ústav lékařské biofyziky, LF UP Olomouc 2 Ústav chemie potravin a biotechnologií, CHF VUT Brno
Analýza magnetických mikročástic mikroskopií atomárních sil Zapletalová 1 H., Tvrdíková 2 J., Kolářová 1 H. 1 Ústav lékařské biofyziky, LF UP Olomouc 2 Ústav chemie potravin a biotechnologií, CHF VUT Brno
NAŘÍZENÍ KOMISE (EU) /... ze dne , kterým se mění nařízení (ES) č. 847/2000, pokud jde o definici pojmu podobný léčivý přípravek
 EVROPSKÁ KOMISE V Bruselu dne 29.5.2018 C(2018) 3193 final NAŘÍZENÍ KOMISE (EU) /... ze dne 29.5.2018, kterým se mění nařízení (ES) č. 847/2000, pokud jde o definici pojmu podobný léčivý přípravek (Text
EVROPSKÁ KOMISE V Bruselu dne 29.5.2018 C(2018) 3193 final NAŘÍZENÍ KOMISE (EU) /... ze dne 29.5.2018, kterým se mění nařízení (ES) č. 847/2000, pokud jde o definici pojmu podobný léčivý přípravek (Text
Exprese rekombinantních proteinů
 Exprese rekombinantních proteinů Exprese rekombinantních proteinů je proces, při kterém můžeme pomocí různých expresních systémů vytvořit protein odvozený od konkrétního genu, nebo části genu. Tento protein
Exprese rekombinantních proteinů Exprese rekombinantních proteinů je proces, při kterém můžeme pomocí různých expresních systémů vytvořit protein odvozený od konkrétního genu, nebo části genu. Tento protein
V organismu se bílkoviny nedají nahradit žádnými jinými sloučeninami, jen jako zdroj energie je mohou nahradit sacharidy a lipidy.
 BÍLKOVINY Bílkoviny jsou biomakromolekulární látky, které se skládají z velkého počtu aminokyselinových zbytků. Vytvářejí látkový základ života všech organismů. V tkáních vyšších organismů a člověka je
BÍLKOVINY Bílkoviny jsou biomakromolekulární látky, které se skládají z velkého počtu aminokyselinových zbytků. Vytvářejí látkový základ života všech organismů. V tkáních vyšších organismů a člověka je
Víme, co vám nabízíme
 PDF vygenerováno: 30.12.2016 5:20: Katalog / Laboratorní pomůcky / ace / Nástavce a filtrační špičky na injekční stříkačky Nástavec filtrační na injekční stříkačky MACHEREY-NAGEL Jednoúčelové nástavce
PDF vygenerováno: 30.12.2016 5:20: Katalog / Laboratorní pomůcky / ace / Nástavce a filtrační špičky na injekční stříkačky Nástavec filtrační na injekční stříkačky MACHEREY-NAGEL Jednoúčelové nástavce
RADIOIMUNOANALÝZA (RADIOIMMUNOASSAY) Převzato: sciencephoto.com Test krve hepatitis virus
 RADIOIMUNOANALÝZA (RADIOIMMUNOASSAY) Převzato: sciencephoto.com Test krve hepatitis virus RADIOIMUNOANALÝZA Stanovení látek, proti kterým lze připravit protilátky ng (10-9 g) až pg (10-12 g) ve složitých
RADIOIMUNOANALÝZA (RADIOIMMUNOASSAY) Převzato: sciencephoto.com Test krve hepatitis virus RADIOIMUNOANALÝZA Stanovení látek, proti kterým lze připravit protilátky ng (10-9 g) až pg (10-12 g) ve složitých
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Struktura. Velikost ionexových perliček Katex. Iontová výměna. Ionex (ion exchanger) Iontoměnič Měnič iontů. Katex (cation exchanger) Měnič kationtů
 Ionex (ion exchanger) Iontoměnič Měnič iontů gelová Struktura makroporézní Katex (cation exchanger) Měnič kationtů Anex (anion exchanger) Měnič aniontů Velikost ionexových perliček Katex Silně kyselý katex
Ionex (ion exchanger) Iontoměnič Měnič iontů gelová Struktura makroporézní Katex (cation exchanger) Měnič kationtů Anex (anion exchanger) Měnič aniontů Velikost ionexových perliček Katex Silně kyselý katex
1) Pojem biotechnologický proces a jeho fázování 2) Suroviny pro fermentaci 3) Procesy sterilizace 4) Bioreaktory a fermentory 5) Procesy kultivace,
 1) Pojem biotechnologický proces a jeho fázování 2) Suroviny pro fermentaci 3) Procesy sterilizace 4) Bioreaktory a fermentory 5) Procesy kultivace, růstové parametry buněčných kultur 2 Biomasa Extracelulární
1) Pojem biotechnologický proces a jeho fázování 2) Suroviny pro fermentaci 3) Procesy sterilizace 4) Bioreaktory a fermentory 5) Procesy kultivace, růstové parametry buněčných kultur 2 Biomasa Extracelulární
Ultrastopová laboratoř České geologické služby
 Ultrastopová laboratoř České geologické služby Jitka Míková Česká geologická služba Praha - Barrandov Laboratorní koloběh Zadavatel TIMS Analýza vzorku Vojtěch Erban Jakub Trubač Lukáš Ackerman Jitka Míková
Ultrastopová laboratoř České geologické služby Jitka Míková Česká geologická služba Praha - Barrandov Laboratorní koloběh Zadavatel TIMS Analýza vzorku Vojtěch Erban Jakub Trubač Lukáš Ackerman Jitka Míková
Membránové procesy a jejich využití
 Membránové procesy a jejich využití Vedoucí projektu: Vypracovali: Sponzor: Ing. Petr Dřevikovský Tomáš Fuka, Lukáš Fuka W.P.E. a.s. Prezentace je majetkem firmy W.P.E. Všechny práva vyhrazena Cíle projektu
Membránové procesy a jejich využití Vedoucí projektu: Vypracovali: Sponzor: Ing. Petr Dřevikovský Tomáš Fuka, Lukáš Fuka W.P.E. a.s. Prezentace je majetkem firmy W.P.E. Všechny práva vyhrazena Cíle projektu
IMUNOANALÝZA elektroforetické separační metody. 3. ročník Klinická biologie a chemie
 IMUNOANALÝZA elektroforetické separační metody 3. ročník Klinická biologie a chemie Princip elektroforézy I. Separační metoda využívající různé pohyblivosti různých iontů (složek směsi) ve stejnosměrném
IMUNOANALÝZA elektroforetické separační metody 3. ročník Klinická biologie a chemie Princip elektroforézy I. Separační metoda využívající různé pohyblivosti různých iontů (složek směsi) ve stejnosměrném
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
BIOLOGICKÁ MEMBRÁNA Prokaryontní Eukaryontní KOMPARTMENTŮ
 BIOMEMRÁNA BIOLOGICKÁ MEMBRÁNA - všechny buňky na povrchu plazmatickou membránu - Prokaryontní buňky (viry, bakterie, sinice) - Eukaryontní buňky vnitřní členění do soustavy membrán KOMPARTMENTŮ - za
BIOMEMRÁNA BIOLOGICKÁ MEMBRÁNA - všechny buňky na povrchu plazmatickou membránu - Prokaryontní buňky (viry, bakterie, sinice) - Eukaryontní buňky vnitřní členění do soustavy membrán KOMPARTMENTŮ - za
Inovace studia molekulární a buněčné biologie
 Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. MBIO1/Molekulární biologie 1 Tento projekt je spolufinancován
Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. MBIO1/Molekulární biologie 1 Tento projekt je spolufinancován
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto SUBSTITUČNÍ DERIVÁTY KARBOXYLOVÝCH O KYSELIN R C O X karboxylových kyselin - substituce na vedlejším uhlovodíkovém řetězci aminokyseliny - hydroxykyseliny
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto SUBSTITUČNÍ DERIVÁTY KARBOXYLOVÝCH O KYSELIN R C O X karboxylových kyselin - substituce na vedlejším uhlovodíkovém řetězci aminokyseliny - hydroxykyseliny
PLANÁRNÍ (PLOŠNÁ) CHROMATOGRAFIE
 PLANÁRNÍ (PLOŠNÁ) CHROMATOGRAFIE Tenkovrstvá chromatografie je technika pro identifikaci a separaci směsi organických látek Identifikace složek směsi (nutné použít standard) analysa frakcí sbíraných během
PLANÁRNÍ (PLOŠNÁ) CHROMATOGRAFIE Tenkovrstvá chromatografie je technika pro identifikaci a separaci směsi organických látek Identifikace složek směsi (nutné použít standard) analysa frakcí sbíraných během
Princip ionexové chromatografie a analýza aminokyselin
 Princip ionexové chromatografie a analýza aminokyselin Teoretická část: vysvětlení principu ionexové (iontové) chromatografie, příprava vzorku pro analýzu aminokyselin (kyselá a alkalická hydrolýza), derivatizace
Princip ionexové chromatografie a analýza aminokyselin Teoretická část: vysvětlení principu ionexové (iontové) chromatografie, příprava vzorku pro analýzu aminokyselin (kyselá a alkalická hydrolýza), derivatizace
Hybridizace nukleových kyselin
 Hybridizace nukleových kyselin Tvorba dvouřetězcových hybridů za dvou jednořetězcových a komplementárních molekul Založena na schopnosti denaturace a renaturace DNA. Denaturace DNA oddělení komplementárních
Hybridizace nukleových kyselin Tvorba dvouřetězcových hybridů za dvou jednořetězcových a komplementárních molekul Založena na schopnosti denaturace a renaturace DNA. Denaturace DNA oddělení komplementárních
Separační metody používané v proteomice
 Separační metody používané v proteomice Proteome = komplexní směsi proteinů Lidská buňka 10,000 typů proteinů Rozdíl v koncentraci 10 6,plasma10 9 Nutnost separace, frakcionace Na úrovni Proteinů Obtížně
Separační metody používané v proteomice Proteome = komplexní směsi proteinů Lidská buňka 10,000 typů proteinů Rozdíl v koncentraci 10 6,plasma10 9 Nutnost separace, frakcionace Na úrovni Proteinů Obtížně
Zpráva o postupu projektu TA03010189
 Zpráva o postupu projektu TA03010189 Efektivní separace Laktoferinu z kravského mléka Vypracovalo: Regionální centrum pokročilých technologií a materiálů, 2014 V rámci spolupráce s Regionálním centrem
Zpráva o postupu projektu TA03010189 Efektivní separace Laktoferinu z kravského mléka Vypracovalo: Regionální centrum pokročilých technologií a materiálů, 2014 V rámci spolupráce s Regionálním centrem
Rekombinantní protilátky, bakteriofágy, aptamery a peptidové scaffoldy pro analytické a terapeutické účely Luděk Eyer
 Rekombinantní protilátky, bakteriofágy, aptamery a peptidové scaffoldy pro analytické a terapeutické účely Luděk Eyer Virologie a diagnostika Výzkumný ústav veterinárního lékařství, v.v.i., Brno Alternativní
Rekombinantní protilátky, bakteriofágy, aptamery a peptidové scaffoldy pro analytické a terapeutické účely Luděk Eyer Virologie a diagnostika Výzkumný ústav veterinárního lékařství, v.v.i., Brno Alternativní
Manganový zeolit MZ 10
 Manganový zeolit MZ 10 SPECIFIKACE POPIS PRODUKTU PUROLITE MZ 10 je manganový zeolit, oxidační a filtrační prostředek, který je připraven z glaukonitu, přírodního produktu, lépe známého jako greensand.
Manganový zeolit MZ 10 SPECIFIKACE POPIS PRODUKTU PUROLITE MZ 10 je manganový zeolit, oxidační a filtrační prostředek, který je připraven z glaukonitu, přírodního produktu, lépe známého jako greensand.
Nativní a rekombinantní Ag
 Antigeny z hlediska diagnostiky a pro potřeby imunizace Nativní a rekombinantní Ag Ag schopna vyvolat I odpověď, komplexní, nekomplexní Ag, hapten, determinanty, nosič V laboratořích: Stanovení Ab proti:
Antigeny z hlediska diagnostiky a pro potřeby imunizace Nativní a rekombinantní Ag Ag schopna vyvolat I odpověď, komplexní, nekomplexní Ag, hapten, determinanty, nosič V laboratořích: Stanovení Ab proti:
KATALOG PRODUKTŮ PRO FILTRACI A SEPARACI Mikrofiltrace
 UNIPRO-ALPHA C.S.,spol. s r.o. www.unipro-alpha.com Výstaviště 67 170 00 Praha 7 T +420 283 852 301 F + 420 283 853 177 info@unipro-alpha.com KATALOG PRODUKTŮ PRO FILTRACI A SEPARACI Mikrofiltrace Hahnemühle
UNIPRO-ALPHA C.S.,spol. s r.o. www.unipro-alpha.com Výstaviště 67 170 00 Praha 7 T +420 283 852 301 F + 420 283 853 177 info@unipro-alpha.com KATALOG PRODUKTŮ PRO FILTRACI A SEPARACI Mikrofiltrace Hahnemühle
Využití chromatografických metod při analýze nukleových kyselin
 Využití chromatografických metod při analýze nukleových kyselin doc. RNDr. Milan Bartoš, Ph.D. bartosm@vfu.cz Přírodovědecká fakulta MU, 2013 Obsah přednášky 1) Chromatografie základní informace 2) Druhy
Využití chromatografických metod při analýze nukleových kyselin doc. RNDr. Milan Bartoš, Ph.D. bartosm@vfu.cz Přírodovědecká fakulta MU, 2013 Obsah přednášky 1) Chromatografie základní informace 2) Druhy
Testové úlohy aminokyseliny, proteiny. post test
 Testové úlohy aminokyseliny, proteiny post test 1. Které aminokyseliny byste hledali na povrchu proteinů umístěných uvnitř fosfolipidových membrán a které na povrchu proteinů vyskytujících se ve vodném
Testové úlohy aminokyseliny, proteiny post test 1. Které aminokyseliny byste hledali na povrchu proteinů umístěných uvnitř fosfolipidových membrán a které na povrchu proteinů vyskytujících se ve vodném
Název: Vypracovala: Datum: 7. 2. 2014. Zuzana Lacková
 Název: Vypracovala: Zuzana Lacková Datum: 7. 2. 2014 Reg.č.projektu: CZ.1.07/2.4.00/31.0023 Název projektu: Partnerská síť centra excelentního bionanotechnologického výzkumu MĚLI BYCHOM ZNÁT: informace,
Název: Vypracovala: Zuzana Lacková Datum: 7. 2. 2014 Reg.č.projektu: CZ.1.07/2.4.00/31.0023 Název projektu: Partnerská síť centra excelentního bionanotechnologického výzkumu MĚLI BYCHOM ZNÁT: informace,
Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie
 Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie IZOLACE GENOMOVÉ DNA Deoxyribonukleová kyselina (DNA) představuje základní genetický materiál většiny
Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie IZOLACE GENOMOVÉ DNA Deoxyribonukleová kyselina (DNA) představuje základní genetický materiál většiny
ZÁKLADNÍ MODELY TOKU PORÉZNÍ MEMBRÁNOU
 ZÁKLADNÍ MODELY TOKU PORÉZNÍ MEMBRÁNOU Znázornění odporů způsobujících snižování průtoku permeátu nástřik porézní membrána Druhy odporů R p blokování pórů R p R a R m R a R m R g R cp adsorbce membrána
ZÁKLADNÍ MODELY TOKU PORÉZNÍ MEMBRÁNOU Znázornění odporů způsobujících snižování průtoku permeátu nástřik porézní membrána Druhy odporů R p blokování pórů R p R a R m R a R m R g R cp adsorbce membrána
První testový úkol aminokyseliny a jejich vlastnosti
 První testový úkol aminokyseliny a jejich vlastnosti Vysvětlete co znamená pojem α-aminokyselina Jaký je rozdíl mezi D a L řadou aminokyselin Kolik je základních stavebních aminokyselin a z čeho jsou odvozeny
První testový úkol aminokyseliny a jejich vlastnosti Vysvětlete co znamená pojem α-aminokyselina Jaký je rozdíl mezi D a L řadou aminokyselin Kolik je základních stavebních aminokyselin a z čeho jsou odvozeny
Pevné lékové formy. Vlastnosti pevných látek. Charakterizace pevných látek ke zlepšení vlastností je vhodné využít materiálové inženýrství
 Pevné lékové formy Vlastnosti pevných látek stabilita Vlastnosti léčiva rozpustnost krystalinita ke zlepšení vlastností je vhodné využít materiálové inženýrství Charakterizace pevných látek difraktometrie
Pevné lékové formy Vlastnosti pevných látek stabilita Vlastnosti léčiva rozpustnost krystalinita ke zlepšení vlastností je vhodné využít materiálové inženýrství Charakterizace pevných látek difraktometrie
Stanovení koncentrace (kvantifikace) proteinů
 Stanovení koncentrace (kvantifikace) proteinů Bioanalytické metody Prof. RNDr. Pavel Peč, CSc. Úvod Kritéria výběru metod stanovení koncentrace proteinů jsou založena na možnostech pro vlastní analýzu,
Stanovení koncentrace (kvantifikace) proteinů Bioanalytické metody Prof. RNDr. Pavel Peč, CSc. Úvod Kritéria výběru metod stanovení koncentrace proteinů jsou založena na možnostech pro vlastní analýzu,
EXTRAKČNÍ METODY. Studijní materiál. 1. Obecná charakteristika extrakce. 2. Extrakce kapalina/kapalina LLE. 3. Alkalická hydrolýza
 Studijní materiál EXTRAKČNÍ METODY 1. Obecná charakteristika extrakce 2. Extrakce kapalina/kapalina LLE 3. Alkalická hydrolýza 4. Soxhletova extrakce 5. Extrakce za zvýšené teploty a tlaku PLE, ASE, PSE
Studijní materiál EXTRAKČNÍ METODY 1. Obecná charakteristika extrakce 2. Extrakce kapalina/kapalina LLE 3. Alkalická hydrolýza 4. Soxhletova extrakce 5. Extrakce za zvýšené teploty a tlaku PLE, ASE, PSE
Udržitelný rozvoj v průmyslových prádelnách
 Leonardo da Vinci Project Udržitelný rozvoj v průmyslových prádelnách Modul 1 Voda v prádelnách Kapitola 3b Změkčování vody Modul 1 Voda v prádelnách Kapitola 3 Změkčování vody 1 Obsah Tvrdost vody (opakování)
Leonardo da Vinci Project Udržitelný rozvoj v průmyslových prádelnách Modul 1 Voda v prádelnách Kapitola 3b Změkčování vody Modul 1 Voda v prádelnách Kapitola 3 Změkčování vody 1 Obsah Tvrdost vody (opakování)
VODA FARMACEUTICKOU VÝROBU 6.12.2012 PRO. VODA PRO FARMACEUTICKÉ ÚČELY Český lékopis 2002 uvádí 3 druhy vody pro farmaceutickou výrobu
 6122012 RDrJiří Sajvera VOD PRO FRMCUICOU VÝROBU ÚOR 2002 VOD PRO FRMCUICÉ ÚČLY Český lékopis 2002 uvádí 3 druhy vody pro farmaceutickou výrobu čištěná voda qua purificata voda na injekci qua pro iniectione
6122012 RDrJiří Sajvera VOD PRO FRMCUICOU VÝROBU ÚOR 2002 VOD PRO FRMCUICÉ ÚČLY Český lékopis 2002 uvádí 3 druhy vody pro farmaceutickou výrobu čištěná voda qua purificata voda na injekci qua pro iniectione
MagPurix Blood DNA Extraction Kit 200
 MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
Základy imunologických metod: interakce antigen-protilátka využití v laboratorních metodách
 Základy imunologických metod: interakce antigen-protilátka využití v laboratorních metodách Obecné principy reakce antigenprotilátka 1929 Kendall a Heidelberg Precipitační reakce Oblast nadbytku protilátky
Základy imunologických metod: interakce antigen-protilátka využití v laboratorních metodách Obecné principy reakce antigenprotilátka 1929 Kendall a Heidelberg Precipitační reakce Oblast nadbytku protilátky
Biologie buňky. systém schopný udržovat se a rozmnožovat
 Biologie buňky 1665 - Robert Hook (korek, cellulae = buňka) Cytologie - věda zabývající se studiem buňek Buňka ozákladní funkční a stavební jednotka živých organismů onejmenší známý uspořádaný dynamický
Biologie buňky 1665 - Robert Hook (korek, cellulae = buňka) Cytologie - věda zabývající se studiem buňek Buňka ozákladní funkční a stavební jednotka živých organismů onejmenší známý uspořádaný dynamický
Separační metody v analytické chemii. Plynová chromatografie (GC) - princip
 Plynová chromatografie (GC) - princip Plynová chromatografie (Gas chromatography, zkratka GC) je typ separační metody, kdy se od sebe oddělují složky obsažené ve vzorku a které mohou být převedeny do plynné
Plynová chromatografie (GC) - princip Plynová chromatografie (Gas chromatography, zkratka GC) je typ separační metody, kdy se od sebe oddělují složky obsažené ve vzorku a které mohou být převedeny do plynné
TLAKOVÉ MEMBRÁNOVÉ PROCESY A JEJICH VYUŽITÍ V OBLASTI LIKVIDACE ODPADNÍCH VOD
 TLAKOVÉ MEMBRÁNOVÉ PROCESY A JEJICH VYUŽITÍ V OBLASTI LIKVIDACE ODPADNÍCH VOD Petr Mikulášek Univerzita Pardubice Fakulta chemicko-technologická Ústav environmentálního a chemického inženýrství petr.mikulasek@upce.cz
TLAKOVÉ MEMBRÁNOVÉ PROCESY A JEJICH VYUŽITÍ V OBLASTI LIKVIDACE ODPADNÍCH VOD Petr Mikulášek Univerzita Pardubice Fakulta chemicko-technologická Ústav environmentálního a chemického inženýrství petr.mikulasek@upce.cz
Elektromigrační metody
 Elektromigrační metody Princip: molekuly nesoucí náboj se pohybují ve stejnosměrném elektrickém Arne Tiselius rozdělil proteiny krevního séra na základě jejich rozdílných rychlostí pohybu v elektrickém
Elektromigrační metody Princip: molekuly nesoucí náboj se pohybují ve stejnosměrném elektrickém Arne Tiselius rozdělil proteiny krevního séra na základě jejich rozdílných rychlostí pohybu v elektrickém
5. Bioreaktory. Schematicky jsou jednotlivé typy bioreaktorů znázorněny na obr. 5.1. Nejpoužívanějšími bioreaktory jsou míchací tanky.
 5. Bioreaktory Bioreaktor (fermentor) je nejdůležitější částí výrobní linky biotechnologického procesu. Jde o nádobu různého objemu, ve které probíhá biologický proces. Dochází zde k růstu buněk a tvorbě
5. Bioreaktory Bioreaktor (fermentor) je nejdůležitější částí výrobní linky biotechnologického procesu. Jde o nádobu různého objemu, ve které probíhá biologický proces. Dochází zde k růstu buněk a tvorbě
Bílkoviny - proteiny
 Bílkoviny - proteiny Proteiny jsou složeny z 20 kódovaných aminokyselin L-enantiomery Chemická struktura aminokyselin R představuje jeden z 20 různých typů postranních řetězců R Hlavní řetězec je neměnný
Bílkoviny - proteiny Proteiny jsou složeny z 20 kódovaných aminokyselin L-enantiomery Chemická struktura aminokyselin R představuje jeden z 20 různých typů postranních řetězců R Hlavní řetězec je neměnný
Teorie chromatografie - I
 Teorie chromatografie - I Veronika R. Meyer Practical High-Performance Liquid Chromatography, Wiley, 2010 http://onlinelibrary.wiley.com/book/10.1002/9780470688427 Příprava předmětu byla podpořena projektem
Teorie chromatografie - I Veronika R. Meyer Practical High-Performance Liquid Chromatography, Wiley, 2010 http://onlinelibrary.wiley.com/book/10.1002/9780470688427 Příprava předmětu byla podpořena projektem
Ing. Milan Vodehnal, AITEC s.r.o., Ledeč nad Sázavou
 Technologie zneškodňování odpadních vod z galvanického vylučování povlaků ZnNi Ing. Milan Vodehnal, AITEC s.r.o., Ledeč nad Sázavou Používání galvanických lázní pro vylučování slitinových povlaků vzhledem
Technologie zneškodňování odpadních vod z galvanického vylučování povlaků ZnNi Ing. Milan Vodehnal, AITEC s.r.o., Ledeč nad Sázavou Používání galvanických lázní pro vylučování slitinových povlaků vzhledem
DĚLÍCÍ METODY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 28. 5. 2012. Ročník: osmý. Vzdělávací oblast: Člověk a příroda / Chemie / Směsi
 Autor: Mgr. Stanislava Bubíková DĚLÍCÍ METODY Datum (období) tvorby: 28. 5. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Směsi 1 Anotace: Žáci se seznámí s nejčastěji používanými separačními
Autor: Mgr. Stanislava Bubíková DĚLÍCÍ METODY Datum (období) tvorby: 28. 5. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Směsi 1 Anotace: Žáci se seznámí s nejčastěji používanými separačními
7. Biofyzikální a biochemická analýza rekombinantních proteinů
 7. Biofyzikální a biochemická analýza rekombinantních proteinů Rekombinantní proteiny, které se mají použít jako proteiny terapeutické, je nutné dobře charakterizovat z hlediska jejich biofyzikálních a
7. Biofyzikální a biochemická analýza rekombinantních proteinů Rekombinantní proteiny, které se mají použít jako proteiny terapeutické, je nutné dobře charakterizovat z hlediska jejich biofyzikálních a
BÍLKOVINY. V organismu se nedají nahradit jinými sloučeninami, jen jako zdroj energie je mohou nahradit sacharidy a lipidy.
 BÍLKOVINY o makromolekulární látky, z velkého počtu AMK zbytků o základ všech organismů o rostliny je vytvářejí z anorganických sloučenin (dusičnanů) o živočichové je musejí přijímat v potravě, v trávicím
BÍLKOVINY o makromolekulární látky, z velkého počtu AMK zbytků o základ všech organismů o rostliny je vytvářejí z anorganických sloučenin (dusičnanů) o živočichové je musejí přijímat v potravě, v trávicím
Tabulace učebního plánu. Obecná chemie. Vzdělávací obsah pro vyučovací předmět : Ročník: 1.ročník a kvinta
 Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
VYSOKOÚČINNÁ KAPALINOVÁ CHROMATOGRAFIE (HPLC) HPLC = high performance liquid chromatography high pressure liquid chromatography
 VYSOKOÚČINNÁ KAPALINOVÁ CHROMATOGRAFIE (HPLC) HPLC = high performance liquid chromatography high pressure liquid chromatography Separační principy kapalinové chromatografie adsorpce: anorg. sorbenty Al
VYSOKOÚČINNÁ KAPALINOVÁ CHROMATOGRAFIE (HPLC) HPLC = high performance liquid chromatography high pressure liquid chromatography Separační principy kapalinové chromatografie adsorpce: anorg. sorbenty Al
Specifická imunitní odpověd. Veřejné zdravotnictví
 Specifická imunitní odpověd Veřejné zdravotnictví MHC molekuly glykoproteiny exprimovány na všech jaderných buňkách (MHC I) nebo jenom na antigen prezentujících buňkách (MHC II) u lidí označovány jako
Specifická imunitní odpověd Veřejné zdravotnictví MHC molekuly glykoproteiny exprimovány na všech jaderných buňkách (MHC I) nebo jenom na antigen prezentujících buňkách (MHC II) u lidí označovány jako
Organická chemie 1. ročník studijního oboru - gastronomie.
 Organická chemie 1. ročník studijního oboru - gastronomie. T-4 Metody oddělování složek směsí. Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu: CZ.1.07/1.5.00/34.0639
Organická chemie 1. ročník studijního oboru - gastronomie. T-4 Metody oddělování složek směsí. Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu: CZ.1.07/1.5.00/34.0639
Pražské analytické centrum inovací Projekt CZ / /0002 spolufinancovaný ESF a Státním rozpočtem ČR
 Pražské analytické centrum inovací Projekt CZ.04.3.07/4.2.01.1/0002 spolufinancovaný ESF a Státním rozpočtem ČR SEPARACE PROTEINŮ Preparativní x analytická /měřítko, účel/ Zvláštnosti dané povahou materiálu
Pražské analytické centrum inovací Projekt CZ.04.3.07/4.2.01.1/0002 spolufinancovaný ESF a Státním rozpočtem ČR SEPARACE PROTEINŮ Preparativní x analytická /měřítko, účel/ Zvláštnosti dané povahou materiálu
Zdrojem je mrna. mrna. zpětná transkriptáza. jednořetězcová DNA. DNA polymeráza. cdna
 Obsah přednášky 1) Klonování složených eukaryotických genů 2) Úprava rekombinantních genů 3) Produkce rekombinantních proteinů v expresních systémech 4) Promotory 5) Vektory 6) Reportérové geny Zdrojem
Obsah přednášky 1) Klonování složených eukaryotických genů 2) Úprava rekombinantních genů 3) Produkce rekombinantních proteinů v expresních systémech 4) Promotory 5) Vektory 6) Reportérové geny Zdrojem
Problematika separace uranu z pitné vody
 ÚJV Řež, a. s. Problematika separace uranu z pitné vody (Projekt TA02010044 Zefektivnění systému čištění pitných vod ze zdrojů s nadlimitní koncentrací uranu (regenerační stanice pro radioaktivně kontaminované
ÚJV Řež, a. s. Problematika separace uranu z pitné vody (Projekt TA02010044 Zefektivnění systému čištění pitných vod ze zdrojů s nadlimitní koncentrací uranu (regenerační stanice pro radioaktivně kontaminované
Metody gravimetrické
 Klíčový požadavek - kvantitativní vyloučení stanovované složky z roztoku - málorozpustná sloučenina - SRÁŽECÍ ROVNOVÁHY VYLUČOVACÍ FORMA se převede na (sušení, žíhání) CHEMICKY DEFINOVANÝ PRODUKT - vážitelný
Klíčový požadavek - kvantitativní vyloučení stanovované složky z roztoku - málorozpustná sloučenina - SRÁŽECÍ ROVNOVÁHY VYLUČOVACÍ FORMA se převede na (sušení, žíhání) CHEMICKY DEFINOVANÝ PRODUKT - vážitelný
PŘÍPRAVKY NA BÁZI LIGNOSULFONÁTŮ
 PŘÍPRAVKY NA BÁZI LIGNOSULFONÁTŮ LIGNOSULFONÁTY Lignin představuje heterogenní amorfní polymer potřebný pro pevnost a tuhost dřevnatých buněčných stěn rostlin. Po celulóze je to druhá nejrozšířenější látka
PŘÍPRAVKY NA BÁZI LIGNOSULFONÁTŮ LIGNOSULFONÁTY Lignin představuje heterogenní amorfní polymer potřebný pro pevnost a tuhost dřevnatých buněčných stěn rostlin. Po celulóze je to druhá nejrozšířenější látka
COSY + - podmínky měření a zpracování dat ztráta rozlišení ve spektru. inphase dublet, disperzní. antiphase dublet, absorpční
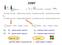 y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
Co je proteomika? Proteom? Protein? Experimentální strategie proteomiky Vlastnosti AMK a proteinů
 2018 Co je proteomika? Proteom? Protein? Experimentální strategie proteomiky Vlastnosti AMK a proteinů METODY PRÁCE S PROTEINY dezintegrace, lyzace, frakcionace detergenty srážení, precipitace, denaturace
2018 Co je proteomika? Proteom? Protein? Experimentální strategie proteomiky Vlastnosti AMK a proteinů METODY PRÁCE S PROTEINY dezintegrace, lyzace, frakcionace detergenty srážení, precipitace, denaturace
Bílkoviny a rostlinná buňka
 Bílkoviny a rostlinná buňka Bílkoviny Rostliny --- kontinuální diferenciace vytváření orgánů: - mitotická dělení -zvětšování buněk a tvorba buněčné stěny syntéza bílkovin --- fotosyntéza syntéza bílkovin
Bílkoviny a rostlinná buňka Bílkoviny Rostliny --- kontinuální diferenciace vytváření orgánů: - mitotická dělení -zvětšování buněk a tvorba buněčné stěny syntéza bílkovin --- fotosyntéza syntéza bílkovin
Trendy v moderní HPLC
 Trendy v moderní HPLC Josef Cvačka, 5.1.2011 CHROMATOGRAFIE NA ČIPECH Miniaturizace separačních systémů Mikrofluidní čipy Mikrofabrikace Chromatografické mikrofluidní čipy s MS detekcí Praktické využití
Trendy v moderní HPLC Josef Cvačka, 5.1.2011 CHROMATOGRAFIE NA ČIPECH Miniaturizace separačních systémů Mikrofluidní čipy Mikrofabrikace Chromatografické mikrofluidní čipy s MS detekcí Praktické využití
MTI Cvičení č. 2 Pasážování buněk / Jana Horáková
 MTI Cvičení č. 2 Pasážování buněk 15.11./16.11.2016 Jana Horáková Doporučená literatura M. Vejražka: Buněčné kultury http://bioprojekty.lf1.cuni.cz/3381/sylabyprednasek/textova-verze-prednasek/bunecnekultury-vejrazka.pdf
MTI Cvičení č. 2 Pasážování buněk 15.11./16.11.2016 Jana Horáková Doporučená literatura M. Vejražka: Buněčné kultury http://bioprojekty.lf1.cuni.cz/3381/sylabyprednasek/textova-verze-prednasek/bunecnekultury-vejrazka.pdf
Prezentace navazuje na základní znalosti z biochemie (lipidy, proteiny, sacharidy) Dynamický fluidní model membrány 2008/11
 RNDr. Ivana Fellnerová, Ph.D. Katedra zoologie PřF UP Olomouc Prezentace navazuje na základní znalosti z biochemie (lipidy, proteiny, sacharidy) Rozšiřuje přednášky: Stavba cytoplazmatické membrány Membránový
RNDr. Ivana Fellnerová, Ph.D. Katedra zoologie PřF UP Olomouc Prezentace navazuje na základní znalosti z biochemie (lipidy, proteiny, sacharidy) Rozšiřuje přednášky: Stavba cytoplazmatické membrány Membránový
Separační metody Historie: Rozvoj separačních metod od minulého století Postavení separačních metod v rámci analytické chemie Význam chromatografie a
 Úvod do separačních metod pro analýzu léčiv Příprava předmětu byla podpořena projektem OPP č. CZ..7/3..00/3353 Separační metody Historie: Rozvoj separačních metod od minulého století Postavení separačních
Úvod do separačních metod pro analýzu léčiv Příprava předmětu byla podpořena projektem OPP č. CZ..7/3..00/3353 Separační metody Historie: Rozvoj separačních metod od minulého století Postavení separačních
Humorální imunita. Nespecifické složky M. Průcha
 Humorální imunita Nespecifické složky M. Průcha Humorální imunita Výkonné složky součásti séra Komplement Proteiny akutní fáze (RAF) Vztah k zánětu rozdílná funkce zánětu Zánět jako fyziologický kompenzační
Humorální imunita Nespecifické složky M. Průcha Humorální imunita Výkonné složky součásti séra Komplement Proteiny akutní fáze (RAF) Vztah k zánětu rozdílná funkce zánětu Zánět jako fyziologický kompenzační
J. Kubíček FSI Brno 2018
 J. Kubíček FSI Brno 2018 Fosfátování je povrchová úprava, kdy se na povrch povlakovaného kovu vylučují nerozpustné fosforečnany. Povlak vzniká reakcí iontů z pracovní lázně s ionty rozpuštěnými z povrchu
J. Kubíček FSI Brno 2018 Fosfátování je povrchová úprava, kdy se na povrch povlakovaného kovu vylučují nerozpustné fosforečnany. Povlak vzniká reakcí iontů z pracovní lázně s ionty rozpuštěnými z povrchu
Tlakové membránové procesy
 Membránová operace Tlakové membránové technologie Retentát (Koncentrát) Vstupní roztok Permeát Tlakové membránové procesy Mikrofiltrace Ultrafiltrace Nanofiltrace Reverzní osmóza -hnací silou rozdíl tlaků
Membránová operace Tlakové membránové technologie Retentát (Koncentrát) Vstupní roztok Permeát Tlakové membránové procesy Mikrofiltrace Ultrafiltrace Nanofiltrace Reverzní osmóza -hnací silou rozdíl tlaků
