I. tøídy { vodivost zpùsobena pohybem elektronù uvnitø møí¾ky (kovy, grat, polovodièe)
|
|
|
- Adam Lubomír Matoušek
- před 6 lety
- Počet zobrazení:
Transkript
1 Elektrochemie 1/26 Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky) Vodièe: I. tøídy { vodivost zpùsobena pohybem elektronù uvnitø møí¾ky (kovy, grat, polovodièe) II. tøídy { vodivost zpùsobena pohybem iontù (iontové roztoky, taveniny solí) III. tøídy { vodivost zpùsobena pohybem iontù a volných elektronù (plazma)
2 Elektrolytický a galvanický èlánek 2/26 Øada napìtí kovù (Beketov, cca 1860): Li, Ca, Al, Mn, Cr Zn, Cd Fe, Pb, [H 2 ], Cu, Ag, Au Èlánek = soustava slo¾ená ze dvou elektrod a elektrolytu, kterou prochází èi mù¾e procházet elektrický proud elektrolytický èlánek { dodávám energii, abych uskuteènil reakci galvanický èlánek { získávám energii galvanický èlánek rovnová¾ný Elektrody anoda = elektroda, na které dochází k oxidaci (odnímání elektronù) Cu Cu e 2 Cl Cl e katoda = elektroda, na které dochází k redukci (pøíjem elektronù) Cu e Cu Cl e 2 Cl Oxidace a redukce jsou v èlánku oddìleny, pøevod náboje se uskuteèòuje uzavøením obvodu.
3 Anoda a katoda 3/26 elektrolytický èlánek galvanický èlánek I I Cl 2 Cl Cu2+ Cu Cu 2+ Cu Pt Cl Cl2 CuCl 2 (aq.) CuCl 2 (aq.) anoda katoda anoda katoda þanionty jdou k anodìÿ
4 Galvanické èlánky: elektrody, konvence 4/26 Elektrody (= poloèlánky) mohou být oddìleny pórovitou pøepá¾kou, solným mùstkem, membránou aj. Katoda je vpravo (redukce) Anoda je vlevo (oxidace) záporná elektroda (anoda) kladná elektroda (katoda) kapalinové rozhraní fázové rozhraní. (pórovitá pøepá¾ka) solný mùstek.. polopropustná membrána Pøíklady: Cu(s) CuCl 2 (c = 0.1 mol dm 3 ) Cl 2 (p = 95 kpa) Pt Ag(s) AgCl(s) NaCl(m = 4 mol kg 1 ) Na(Hg) NaCl(m = 0.1 mol kg 1 ) AgCl(s) Ag(s) Pt Sn 2+ (0.1 mol dm 3 ) + Sn 4+ (0.01 mol dm 3 ) Fe 3+ (0.2 mol dm 3 ) Fe
5 Rovnová¾né napìtí èlánku I 5/26 Star¹í názvy: elektromotorické napìtí, elektromotorická síla (EMS), cell potential (electromotive force, emf) Nutno mìøit v bezproudovém stavu (vyvá¾ený mùstek, citlivý voltmetr) Nelze mìøit napìtí jedné elektrody nula se denuje pomocí standardní vodíkové elektrody, co¾ je elektroda s reakcí 2 H + (aq) + 2 e H 2 (g) kde a H + = 1 (ph=0) a a H2 = 1 (p H2 = p st ). Realizace vodíkové elektrody: platinový plí¹ek pokrytý platinovou èerní, sycený vodíkem credit: wikipedie znaèení: E, E, φ; ve fyzice U
6 Rovnová¾né napìtí èlánku II 6/26 Elektrodový potenciál elektrody X je roven napìtí èlánku Pozn.: je to v¾dy redukèní potenciál H 2 (a = 1) H + (a = 1) X Standardní (redukèní) potenciál elektrody: v¹echny látky úèastnící se reakce mají jednotkové aktivity. Pøíklady: E Cu 2+ Cu = V, E Cl 2 2Cl = V (pøi 25 C) Jestli¾e reakce pí¹eme tak, jak probíhají, kdy¾ èlánek dává proud: reakce = (redukce na katodì) + (oxidace na anodì) Jestli¾e reakce pí¹eme redukènì: E = E red katoda + Eox anoda reakce = (redukce na katodì) (redukce na anodì) E = E red katoda Ered anoda
7 Termodynamika vratného èlánku 7/26 Vratnost = dìje lze obrátit malou zmìnou napìtí od rovnová¾ného (¾ádné parazitní reakce (rozpou¹tìní kovu), difuze èi pøevod pøes kapalinové rozhraní aj.) r G m = W el = qe = zfe [p, T] Nernstova rovnice E = E RT zf ln i a ν i i kde r G m = zfe, K = exp[ r G m/rt] = exp[zfe /RT] E = E,red katoda + E,ox anoda = E,red katoda E,red anoda r G < 0 tj. E > 0 èlánek dává proud E = 0 tj. r G = 0 = vybitý èlánek (rovnováha) { nezamìòujte s rovnová¾ným napìtím (vyvá¾ený èlánek) E Cu 2+ Cu = E Cu Cu 2+ (oxidace) ale E Cl 2 2Cl = E 1 2 Cl 2 Cl vodíková elektroda vpravo pøi 25 C: E = E 0 ph V
8 Termodynamika vratného èlánku II 8/26 koná se elektrická práce W el vratný dìj za [p, T] ( ) r G m r S m = T r H m = T 2 ( ( r G m /T) T ) p p = zf ( ) E T p = zft 2 ( (E/T) T ) p Q m = T r S m (II. vìta pro vratné dìje) Zrada! W obj r U = Q + W = Q p r V + W el r H = r U + r (pv) [p] = r U + p r V = Q + W el Vztah Q = r H platí pouze tehdy, koná-li se jen objemová práce (W jiná = 0). A stejnì pro standardní velièiny (p = p st, jednotkové aktivity), napø.: ( ) ( r S r G ) m E m = = zf T T p p
9 Redukèní potenciály mezi rùznými oxidaèními èísly 9/26 Pøíklad. E (Cr 3+ Cr 2+ ). E (Cr 2+ Cr) = V, E (Cr 3+ Cr) = V. Vypoètìte Nesèítají se volty (E jsou intenzivní velièiny), ale Gibbsovy energie! Cr e Cr r G m = 2F ( V) Cr e Cr r G m = 3F ( V) Cr e Cr 2+ r G m = 1F E (Cr 3+ Cr 2+ ) 1F E (Cr 3+ Cr 2+ ) = 3F ( V) + 2F ( V) E (Cr 3+ Cr 2+ ) = 3 ( V) 2 ( V) = V
10 Pøírodopis elektrod 10/26 prvního druhu (jediná reakce mezi materiálem elektrody a iontem) { kationtové, aniontové { kovové, amalgamové (kov v Hg), nekovové, plynové druhého druhu (nerozp. sùl { dvì reakce) tøetího druhu (dvì soli { tøi reakce) redox (mezi dvìma oxidaèními stupni) iontovì selektivní
11 Elektrody prvního druhu 11/26 kationtová, kovová oxidaènì: Zn Zn 2+, redukènì: Zn 2+ Zn pozn.: nikoliv Fe, Al + ionty { pokryjí se oxidem kationtová, amalgamová oxidaènì: Na(Hg) Na +, redukènì: Na + Na(Hg) E Na + Na = E Na + Na RT F ln a Na(Hg) a Na + Je-li amalgám kovem M nasycen, pak a M(Hg)=1 kationtová plynová: vodíková aniontová plynová: chlorová, kyslíková Cl Cl 2 Pt : Cl e 2 Cl OH O 2 Pt : 1 2 O e + H 2 O 2 OH : 1 2 O e + 2H + H 2 O aniontová nekov/ionty: Br Br 2 Pt
12 Elektrody druhého druhu 12/26 chloridostøíbrná (argentochloridová) Cl AgCl Ag AgCl(s) Ag + + Cl Ag + + e Ag(s) AgCl(s) + e Ag + Cl E AgCl Ag Cl = E AgCl Ag Cl RT F ln a Ag a Cl a AgCl = E AgCl Ag Cl RT F ln a Cl kalomelová Cl Hg 2 Cl 2 Hg Hg 2 Cl 2 (s) + 2 e 2 Hg + 2 Cl Vyu¾ití: referenèní elektrody Pictures by: Analytical chemistry an introduction, 7th edition, Harcourt College, 2000
13 Kuriozita: elektrody tøetího druhu + 13/26 Pozor, názvosloví není jednotné! Tøi reakce: Ca 2+ (aq.) Ca(COO) 2 (s) Zn(COO) 2 (s) Zn(s) Ca 2+ + (COO) 2 2 Ca(COO) 2 Zn(COO) 2 (COO) Zn 2+ Zn e Zn Ca 2+ + Zn(COO) e Ca(COO) 2 + Zn E = E RT 2F ln 1 a Ca 2+ Takto se dá zmìøit c Ca 2+ { elektroda Ca Ca 2+ (aq.) toti¾ neexistuje, proto¾e Ca se ve vodì rozpou¹tí. (Výhodnìj¹í jsou v¹ak iontovì selektivní elektrody.)
14 Redox elektrody 14/26 rùzné oxidaèní stupnì kovu: Sn 4+ Sn 2+ Pt Sn e Sn 2+ chinhydronová (quinhydrone) elektroda (ph 1{8): chinon (p-benzochinon, quinone) + hydrochinon 1:1, nasyc. v pufru O O (s) + 2 H e HO OH (s) chinon (Q) Nernstova rovnice pro poloèlánek: Vyu¾ití: mìøení ph E Q QH = E Q QH RT 2F ln. = ( ph) V hydrochinon (QH) 1 a QH a Q a 2 = E Q QH + RT H + F ln a H +
15 Iontovì selektivní elektrody 15/26 Membrána propustná jen pro nìkteré ionty Sklenìná elektroda Membrána ze speciálního tenkého skla þpropou¹tí H + ÿ (pøesnìji: pøevod pomocí Na + aj.). Rozdíl chem. pot. na obou stranách membrány µ(h +, ) µ(h +, elektroda) = 1 RT ln a(h +, ) a(h +, elektroda) je v rovnováze kompenzován el. prací FE. Platí credit: referenèní argentochloridová tedy opìt Nernstova rovnice sklenìná credit: wikipedie E = konst RT F ln a(h+, ) = konst RT F Vyu¾ití: mìøení ph (2{12) i dal¹ích iontù ln 10 ph
16 Pøírodopis èlánkù 16/26 Podle zdroje G: Chemický èlánek bez pøevodu: chemické èlánky koncentraèní èlánky { elektrolytové { elektrodové Podle pøevodu iontù membránou, solným mùstkem aj.: bez pøevodu s pøevodem credit: payitoweb.blogspot.com anoda: Fe(s) Fe 3+ (aq.) + 3 e ( 0.04 V) Fe(s) Fe 2+ (aq.) + 2 e ( 0.44 V) katoda: 1 2 O e + 2H + H 2 O (1.23 V) pøíp. redukce rùzných organických látek (vitamin C)
17 Chemický èlánek bez pøevodu [xcat ev/clanekagcl.ev] 17/26 Jeden elektrolyt s ponoøenými elektrodami. Pøíklad. Na vrcholu Snì¾ky (1602 m n.m.) jsme do roztoku HCl (c = 0.01 mol dm 3 ) ponoøili platinovou elektrodu sycenou vodíkem a støíbrný drátek pokrytý AgCl. Standardní redukèní napìtí argentochloridové elektrody je V (p st = Pa). Jaké napìtí namìøíme? V TV hlásili tlak 999 mbar (pøepoèteno na hladinu moøe). Teplota vzduchu (M = 29 g mol 1 ) byla 25 C. p = Pa V (γ = 1) V (Debye{Hückel)
18 Chemický èlánek s pøevodem 18/26 Pórovitá pøepá¾ka (kapalinové rozhraní) (.). V principu nevratné dìje (difuze) kapalinový (difuzní) potenciál. Omezí se solným mùstkem ( ). Pøi výpoètu mùstek þignorujemeÿ. Pøíklad: Zn(s) ZnSO 4 CuSO 4 Cu(s) Elektrodový koncentraèní èlánek Pøíklad: Pt H 2 (p 1 ) HCl(aq) H 2 (p 2 ) Pt (Uvedená polarita pro p 1 > p 2 )
19 Baterie 19/26 þbaterieÿ = soustava elektrochemických èlánkù Alkalický èlánek (Zn prá¹ek, burel + uhlík) Zn KOH (gel) MnO 2 Zn + 2 OH ZnO + H 2 O + 2 e 2 MnO 2 + H 2 O + 2e Mn 2 O OH Lithiové èlánky (lithium je lehké a má vysoký potenciál) Elektrolyt = sùl (napø. LiBF 4 ) v organickém polárním rozpou¹tìdle. Rùzné varianty, napø.: Li Li + + e Mn IV O 2 + Li + + e Mn III LiO 2
20 Akumulátory 20/26 Li-ion, Li-polymer: Li je v C (max. 1 Li v 6 C) Li (v C) LiBF 4 nebo polymer LiCoO 2.CoO 2 Kladná elektroda napø. (ve vybité formì) LiCoO 2 = vrstvy CoO 2 interkalované vrstvami Li +. Nabíjení èást: Li + do roztoku, Co III na Co IV Ni-MH: vodík v metal hydridu (M = LaNi 5, CeAl 5, TiNi 2... ) H MH KOH(aq ) Ni(OH) 2 β-niooh Ni olovìný akumulátor (velký proud) Pb PbSO 4 (s) H 2 SO 4 (20{30 hm. %) PbO 2 (s) PbSO 4 (s) Pb Celková reakce pøi vybíjení je Pb + PbO H 2 SO 4 a po rozepsání na anodu a katodu vybíjení nabíjení 2 PbSO H 2 O Pb + SO 4 2 PbSO 4 (s) + 2 e PbO 2 + SO H + + 2e PbSO 4 (s) + 2 H 2 O
21 Palivové èlánky 21/26 napø. kyslík+vodík : H 2 2 H e protony prochází membránou : 1 2 O H e H 2 O drahé katalyzátory po¾adavky na èistotu (CO) èlánek na isopropanol
22 Souèin rozpustnosti 22/26 Pøíklad. Stanovte souèin rozpustnosti AgCl ze standardních redukèních potenciálù pøi 25 C. Data: E (Ag Ag + ) = V, E (Ag AgCl Cl ) = V. Ag AgCl(aq) AgCl(s) Ag, red : Ag + + e Ag r G = FE Ag + Ag ( 1), red : AgCl + e Ag + Cl r G = FE Ag AgCl Cl (+1) AgCl Ag + + Cl r G = F(E Ag AgCl Cl E Ag + Ag ) K s = exp ( ) rg = exp RT [ ] F RT (E Ag AgCl Cl E Ag + Ag ) = Pro èlánek nakrátko (virtuální Ag v AgCl) pøejde Nernstova rovnice E = 0 = (E Ag AgCl Cl E Ag + Ag ) RT F ln(a Cl a Ag +) v podmínku rovnováhy a Cl a Ag + = K s
23 Kinetika elektrodových dìjù 23/26 Elektrodová reakce: 1. difuze výchozích látek k elektrodì, ( 2. reakce ve vrstvì roztoku, která tìsnì pøiléhá k povrchu elektrody), 3. adsorpce výchozích látek na elektrodì, 4. pøenos elektronù mezi adsorbovanými molekulami èi ionty výchozích látek a elektrodou, 5. desorpce produktù z elektrody, ( 6. reakce ve vrstvì roztoku, která tìsnì pøiléhá k povrchu elektrody), 7. difuze produktù smìrem od elektrody. Kdy¾ to nìkde vázne (øídící dìj), nastává polarizace elektrod: koncentraèní polarizace (1., 7.) chemická polarizace (þotravaÿ produkty reakce)
24 Pøepìtí 24/26 Pøepìtí (overpotential) η je napìtí, o které musíme zvý¹it napìtí oproti rovnová¾nému, aby probíhala elektrolýza. (Elektrochemická analogie aktivaèní energie.) závisí na materiálu elektrod (vodík na Pt èerni: 0.07 V, Pt: 0.16 V, Pb: 0.71 V, Hg: 0.85 V) klesá mírnì s teplotou závisí ponìkud na proudové hustotì (η a + b ln J) zvy¹uje spotøebu energie pøi elektrolýze + vysoké pøepìtí vodíku na kovech umo¾òuje vybíjet i ménì u¹lechtilé kovy (elektrolýza, Pb akumulátor); nìkt. látky (i bio) katalyzují vývoj vodíku pøepìtí lze vyu¾ít analyticky Koroze anodická fáze: kov se rozpou¹tí katodická fáze: kov (èi vodík... ) se usazuje Katodická ochrana: chránìný kov nabijeme, rozpou¹tí se anoda
25 Elektroanalytické metody 25/26 coulometrie { mìøí se proud èi náboj pro danou chemickou pøemìnu { stanovení pro¹lého náboje (kalibrace ampérmetrù) { coulometrická titrace (konst. proud, mìøím èas do bodu ekvivalence) potenciometrie { mìøí se napìtí (èlánku), v (témìø) bezproudovém stavu stanoví se aktivita/koncentrace látky a z ní napø.: { ph (sklenìná elektroda, chinhydronová, vodíková) { koncentrace dal¹ích iontù { stanovení konstant kyselosti { stanovení souèinù rozpustnosti { stanovení aktivitních koecientù { potenciometrické titrace (ph aj.) voltametrie { mìøí se závislost proudu na napìtí: { cyklická voltametrie (vpravo) { polarograe credit:
26 Polarograe 26/26 Voltametrická technika se rtu»ovou kapkovou elektrodou Lineární prùbìh E: citlivost do mol dm 3 Problém: kapacitní proud Diferenciální pulsní polarograe (DPP) do mol dm 3 Jaroslav Heyrovský credits: picture of polarograph by Lukáš Mižoch, CC BY-SA 3.0,
Elektrochemie. Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky)
 Elektrochemie 1 Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky) Vodièe: I. tøídy { vodivost zpùsobena pohybem elektronù uvnitø
Elektrochemie 1 Pøedmìt elektrochemie: disociace (roztoky elektrolytù, taveniny solí) vodivost jevy na rozhraní s/l (elektrolýza, èlánky) Vodièe: I. tøídy { vodivost zpùsobena pohybem elektronù uvnitø
Oxidace a redukce. Hoření = slučování s kyslíkem = oxidace. 2 Mg + O 2 2 MgO S + O 2 SO 2. Redukce = odebrání kyslíku
 Oxidace a redukce Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe + 3 CO CuO + H 2 Cu + H 2 O 1 Oxidace a redukce Širší pojem oxidace
Oxidace a redukce Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe + 3 CO CuO + H 2 Cu + H 2 O 1 Oxidace a redukce Širší pojem oxidace
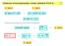
Galvanický článek. Li Rb K Na Be Sr Ca Mg Al Be Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi As CU Hg Ag Pt Au
 Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
Oxidace a redukce. Objev kyslíku nový prvek, vyvrácení flogistonové teorie. Hoření = slučování s kyslíkem = oxidace. 2 Mg + O 2 2 MgO S + O 2 SO 2
 Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Lavoisier Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe
Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Lavoisier Redukce = odebrání kyslíku Fe 2 O 3 + 3 C 2 Fe
Oxidace a redukce. Objev kyslíku nový prvek, vyvrácení flogistonové teorie. Hoření = slučování s kyslíkem = oxidace. 2 Mg + O 2 2 MgO S + O 2 SO 2
 Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Antoine Lavoisier (1743-1794) Redukce = odebrání kyslíku
Oxidace a redukce Objev kyslíku nový prvek, vyvrácení flogistonové teorie Hoření = slučování s kyslíkem = oxidace 2 Mg + O 2 2 MgO S + O 2 SO 2 Antoine Lavoisier (1743-1794) Redukce = odebrání kyslíku
12. Elektrochemie základní pojmy
 Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
Důležité veličiny Elektroda, článek Potenciometrie Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité veličiny proud I (ampér - A) náboj Q (coulomb - C) Q t 0 I dt napětí, potenciál
3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE
 3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE (Elektrochemické články kinetické aspekty) Nerovnovážné elektrodové děje = děje probíhající na elektrodách při průchodu proudu. 3.1. Polarizace Pojem polarizace se používá
3. NEROVNOVÁŽNÉ ELEKTRODOVÉ DĚJE (Elektrochemické články kinetické aspekty) Nerovnovážné elektrodové děje = děje probíhající na elektrodách při průchodu proudu. 3.1. Polarizace Pojem polarizace se používá
Potenciometrie. Obr.1 Schema základního uspořádání elektrochemické cely pro potenciometrická měření
 Potenciometrie 1.Definice Rovnovážná potenciometrie je analytickou metodou, při níž se analyt stanovuje ze změřeného napětí elektrochemického článku, tvořeného indikační elektrodou ponořenou do analyzovaného
Potenciometrie 1.Definice Rovnovážná potenciometrie je analytickou metodou, při níž se analyt stanovuje ze změřeného napětí elektrochemického článku, tvořeného indikační elektrodou ponořenou do analyzovaného
AKUMULÁTORY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 15. 3. 2012. Ročník: devátý
 Autor: Mgr. Stanislava Bubíková AKUMULÁTORY Datum (období) tvorby: 15. 3. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí se zdroji elektrického
Autor: Mgr. Stanislava Bubíková AKUMULÁTORY Datum (období) tvorby: 15. 3. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí se zdroji elektrického
Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály
 Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály Elektrochemie rovnováhy a děje v soustavách nesoucích elektrický náboj Krystal kovu ponořený do destilované vody + +
Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály Elektrochemie rovnováhy a děje v soustavách nesoucích elektrický náboj Krystal kovu ponořený do destilované vody + +
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
ELEKTROCHEMIE A KOROZE Ing. Jiří Vondrák, DrSc. ÚACH AV ČR
 ELEKTROCHEMIE A KOROZE Ing. Jiří Vondrák, DrSc. ÚACH AV ČR Elektrochemie: chemické reakce vyvolané elektrickým proudem a naopak vznik elektrického proudu z chemických reakcí Historie: L. Galvani - žabí
ELEKTROCHEMIE A KOROZE Ing. Jiří Vondrák, DrSc. ÚACH AV ČR Elektrochemie: chemické reakce vyvolané elektrickým proudem a naopak vznik elektrického proudu z chemických reakcí Historie: L. Galvani - žabí
Na www.studijni-svet.cz zaslal(a): Téra2507. Elektrochemické metody
 Na www.studijni-svet.cz zaslal(a): Téra2507 Elektrochemické metody Elektrolýza Do roztoku elektrolytu ponoříme dvě elektrody a vložíme na ně dostatečně velké vnější stejnosměrné napětí. Roztok elektrolytu
Na www.studijni-svet.cz zaslal(a): Téra2507 Elektrochemické metody Elektrolýza Do roztoku elektrolytu ponoříme dvě elektrody a vložíme na ně dostatečně velké vnější stejnosměrné napětí. Roztok elektrolytu
Elektrochemie. 2. Elektrodový potenciál
 Elektrochemie 1. Poločlánky Ponoříme-li kov do roztoku jeho solí mohou nastav dva různé děje: a. Do roztoku se z kovu uvolňují kationty (obr. a), na elektrodě vzniká převaha elektronů. Elektroda se tedy
Elektrochemie 1. Poločlánky Ponoříme-li kov do roztoku jeho solí mohou nastav dva různé děje: a. Do roztoku se z kovu uvolňují kationty (obr. a), na elektrodě vzniká převaha elektronů. Elektroda se tedy
Sekundární elektrochemické články
 Sekundární elektrochemické články méně odborně se jim říká také akumulátory všechny elektrochemické reakce jsou vratné (ideálně na 100%) řeší problém ekonomický (vícenásobné použití snižuje náklady) řeší
Sekundární elektrochemické články méně odborně se jim říká také akumulátory všechny elektrochemické reakce jsou vratné (ideálně na 100%) řeší problém ekonomický (vícenásobné použití snižuje náklady) řeší
Ú L O H Y
 Ú L O H Y 1. Vylučování kovů - Faradayův zákon; Př. 8.1 Stejný náboj, 5789 C, projde při elektrolýze každým z roztoků těchto solí: (a) AgNO 3, (b) CuSO 4, (c) Na 2 SO 4, (d) Al(NO 3 ) 3, (e) Al 2 (SO 4
Ú L O H Y 1. Vylučování kovů - Faradayův zákon; Př. 8.1 Stejný náboj, 5789 C, projde při elektrolýze každým z roztoků těchto solí: (a) AgNO 3, (b) CuSO 4, (c) Na 2 SO 4, (d) Al(NO 3 ) 3, (e) Al 2 (SO 4
GALAVANICKÝ ČLÁNEK. V běžné životě používáme název baterie. Odborné pojmenování pro baterii je galvanický článek.
 GALAVANICKÝ ČLÁNEK V běžné životě používáme název baterie. Odborné pojmenování pro baterii je galvanický článek. Galvanický článek je zařízení, které využívá redoxní reakce jako zdroj energie. Je zdrojem
GALAVANICKÝ ČLÁNEK V běžné životě používáme název baterie. Odborné pojmenování pro baterii je galvanický článek. Galvanický článek je zařízení, které využívá redoxní reakce jako zdroj energie. Je zdrojem
Elektrochemické reakce
 Elektrochemické reakce elektrochemie, základní pojmy mechanismus elektrochem. reakce elektrodový potenciál Faradayův zákon kinetika elektrodové reakce 1 Elektrochemie Elektrochemické reakce - využívají
Elektrochemické reakce elektrochemie, základní pojmy mechanismus elektrochem. reakce elektrodový potenciál Faradayův zákon kinetika elektrodové reakce 1 Elektrochemie Elektrochemické reakce - využívají
= vědní disciplína zabývající se ději a rovnováhami v soustavách, ve kterých se vyskytují elektricky nabité částice
 Otázka: Elektrochemie Předmět: Chemie Přidal(a): j. Elektrochemie = vědní disciplína zabývající se ději a rovnováhami v soustavách, ve kterých se vyskytují elektricky nabité částice Př. soustav s el. nábojem
Otázka: Elektrochemie Předmět: Chemie Přidal(a): j. Elektrochemie = vědní disciplína zabývající se ději a rovnováhami v soustavách, ve kterých se vyskytují elektricky nabité částice Př. soustav s el. nábojem
Elektrochemie Elektrochemie je nauka o vzájemných vztazích energie chemické a elektrické. Nejlépe a nejdéle známe elektrolytický účinek proudu.
 Elektrochemie Elektrochemie je nauka o vzájemných vztazích energie chemické a elektrické. Nejlépe a nejdéle známe elektrolytický účinek proudu. Elektrochemie se zabývá rovnováhami a ději v soustavách,
Elektrochemie Elektrochemie je nauka o vzájemných vztazích energie chemické a elektrické. Nejlépe a nejdéle známe elektrolytický účinek proudu. Elektrochemie se zabývá rovnováhami a ději v soustavách,
Elektrochemické zdroje elektrické energie
 Dělení: 1) Primární články 2) Sekundární 3) Palivové články Elektrochemické zdroje elektrické energie Primární články - Články suché. C Zn článek Anoda: oxidace Zn Zn 2+ + 2 e - (Zn 2+ se rozpouští v elektrolytu;
Dělení: 1) Primární články 2) Sekundární 3) Palivové články Elektrochemické zdroje elektrické energie Primární články - Články suché. C Zn článek Anoda: oxidace Zn Zn 2+ + 2 e - (Zn 2+ se rozpouští v elektrolytu;
Průvodka. CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Pořadí DUMu v sadě 08
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
ELEKTROCHEMIE. - studuje soustavy, které obsahují elektricky nabité částice.
 ELEKTROCHEMIE - studuje soustavy, které obsahují elektricky nabité částice. ZÁKLADNÍ POJMY Vodiče látky, které vedou elektrický proud. Vodiče I. třídy přenos elektrického náboje je zprostředkován volně
ELEKTROCHEMIE - studuje soustavy, které obsahují elektricky nabité částice. ZÁKLADNÍ POJMY Vodiče látky, které vedou elektrický proud. Vodiče I. třídy přenos elektrického náboje je zprostředkován volně
Elektrochemické metody
 Elektrochemické metody Konduktometrie Coulometrie Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie) Biosenzory Petr Breinek Elektrochemie_N2012 Elektrochemie Elektrochemie
Elektrochemické metody Konduktometrie Coulometrie Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie) Biosenzory Petr Breinek Elektrochemie_N2012 Elektrochemie Elektrochemie
Elektrický proud v kapalinách
 Elektrický proud v kapalinách Elektrické vlastnosti kapalin Čisté kapaliny omezíme se na vodu jsou poměrně dobrými izolanty. Když však ve vodě rozpustíme sůl, kyselinu anebo zásadu, získáme tzv. elektrolyt,
Elektrický proud v kapalinách Elektrické vlastnosti kapalin Čisté kapaliny omezíme se na vodu jsou poměrně dobrými izolanty. Když však ve vodě rozpustíme sůl, kyselinu anebo zásadu, získáme tzv. elektrolyt,
ELEKTRICKÝ PROUD V KAPALINÁCH
 ELEKTRICKÝ PROUD V KPLINÁCH 1. Elektrolyt a elektrolýza elektrolyt kapalina, která může vést elektrický proud (musí obsahovat ionty kyselin, zásad nebo solí - rozpuštěné nebo roztavené) elektrolýza proces,
ELEKTRICKÝ PROUD V KPLINÁCH 1. Elektrolyt a elektrolýza elektrolyt kapalina, která může vést elektrický proud (musí obsahovat ionty kyselin, zásad nebo solí - rozpuštěné nebo roztavené) elektrolýza proces,
Elektrolýza. (procesy v elektrolytických článcích) ch) Základní pojmy a představy z elektrolýzy. V rovnováze E = 0 (I = 0)
 Elektrolýza (procesy v elektrolytických článcích) ch) V rovnováze Základní pojmy a představy z elektrolýzy E = (I = ) Ag Ag + ϕ Ag Ag E RT F r = E + + ln aag + Ag / Ag roztok AgNO 3 Po připojení zdroje
Elektrolýza (procesy v elektrolytických článcích) ch) V rovnováze Základní pojmy a představy z elektrolýzy E = (I = ) Ag Ag + ϕ Ag Ag E RT F r = E + + ln aag + Ag / Ag roztok AgNO 3 Po připojení zdroje
Elektrické jevy na membránách
 Elektrické jevy na membránách Polopropustná (semipermeabilní) membrána; frita, diafragma propou¹tí ionty, vzniká el. napìtí rùzné koncentrace iontù na obou stranách rùzná propustnost/difuzivita pro rùzné
Elektrické jevy na membránách Polopropustná (semipermeabilní) membrána; frita, diafragma propou¹tí ionty, vzniká el. napìtí rùzné koncentrace iontù na obou stranách rùzná propustnost/difuzivita pro rùzné
Rovnováha kapalina{pára u binárních systémù
 Rovnováha kapalina{pára u binárních systémù 1 Pøedpoklad: 1 kapalná fáze Oznaèení: molární zlomky v kapalné fázi: x i molární zlomky v plynné fázi: y i Poèet stupòù volnosti: v = k f + 2 = 2 stav smìsi
Rovnováha kapalina{pára u binárních systémù 1 Pøedpoklad: 1 kapalná fáze Oznaèení: molární zlomky v kapalné fázi: x i molární zlomky v plynné fázi: y i Poèet stupòù volnosti: v = k f + 2 = 2 stav smìsi
Elektrolyty. Disociace termická disociace (pomocí zvýšené teploty) elektrolytická disociace (pomocí polárního rozpouštědla)
 Elektrolyty Elektrolyty látky, které při rozpouštění nebo tavení disociují (štěpí se) na elektricky nabité částice (ionty) jejich roztoky a taveniny jsou elektricky vodivé kyseliny, hydroxidy, soli Ionty
Elektrolyty Elektrolyty látky, které při rozpouštění nebo tavení disociují (štěpí se) na elektricky nabité částice (ionty) jejich roztoky a taveniny jsou elektricky vodivé kyseliny, hydroxidy, soli Ionty
E = E red,pravý E red,levý + E D = E red,pravý + E ox,levý + E D
 11. GALVANICKÉ ČLÁNKY 01 Výočet E článku, γ ± 1... 0 Střední aktvtní koefcent z E článku... 03 Výočet E článku, γ ± 1... 04 Tlak lnu na elektrodě z E článku; aktvtní koefcent... 05 E článku a dsocační
11. GALVANICKÉ ČLÁNKY 01 Výočet E článku, γ ± 1... 0 Střední aktvtní koefcent z E článku... 03 Výočet E článku, γ ± 1... 04 Tlak lnu na elektrodě z E článku; aktvtní koefcent... 05 E článku a dsocační
STEJNOSMĚRNÝ PROUD Galvanické články TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY.
 STEJNOSMĚRNÝ PROUD Galvanické články TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Galvanické články Většina kovů ponořených do vody nebo elektrolytu
STEJNOSMĚRNÝ PROUD Galvanické články TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY. Galvanické články Většina kovů ponořených do vody nebo elektrolytu
U = E a - E k + IR Znamená to, že vložené napětí je vyrovnáváno
 Voltametrie a polarografie Princip. Do roztoku vzorku (elektrolytu) jsou ponořeny dvě elektrody (na rozdíl od potenciometrie prochází obvodem el. proud) - je vytvořen elektrochemický článek. Na elektrody
Voltametrie a polarografie Princip. Do roztoku vzorku (elektrolytu) jsou ponořeny dvě elektrody (na rozdíl od potenciometrie prochází obvodem el. proud) - je vytvořen elektrochemický článek. Na elektrody
Výukový materiál zpracován v rámci projektu EU peníze školám
 Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.4.00/21.3665 Šablona: III/2 č. materiálu: VY_32_INOVACE_173 Jméno autora: Ing. Kateřina Lisníková Třída/ročník:
Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.4.00/21.3665 Šablona: III/2 č. materiálu: VY_32_INOVACE_173 Jméno autora: Ing. Kateřina Lisníková Třída/ročník:
9. ročník Galvanický článek
 9. ročník Galvanický článek Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. fotografie v prezentaci
9. ročník Galvanický článek Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. fotografie v prezentaci
Elektrický proud v kapalinách
 Elektrický proud v kapalinách Kovy obsahují volné (valenční) elektrony a ty způsobují el. proud. Látka se chemicky nemění (vodiče 1. třídy). V polovodičích volné náboje připravíme uměle (teplota, příměsi,
Elektrický proud v kapalinách Kovy obsahují volné (valenční) elektrony a ty způsobují el. proud. Látka se chemicky nemění (vodiče 1. třídy). V polovodičích volné náboje připravíme uměle (teplota, příměsi,
Elektrický proud v elektrolytech
 Elektrolytický vodič Elektrický proud v elektrolytech Vezěe nádobu s destilovanou vodou (ta nevede el. proud) a vlože do ní dvě elektrody, které připojíe do zdroje stejnosěrného napětí. Do vody nasypee
Elektrolytický vodič Elektrický proud v elektrolytech Vezěe nádobu s destilovanou vodou (ta nevede el. proud) a vlože do ní dvě elektrody, které připojíe do zdroje stejnosěrného napětí. Do vody nasypee
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto Oxidace a redukce jsou chemické reakce spojené s výměnou elektronů. Při oxidaci látka elektrony uvolňuje a její oxidační číslo se zvyšuje.
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto Oxidace a redukce jsou chemické reakce spojené s výměnou elektronů. Při oxidaci látka elektrony uvolňuje a její oxidační číslo se zvyšuje.
ANODA KATODA elektrolyt:
 Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Ukázky z pracovních listů 1) Naznač pomocí šipek, které částice putují k anodě a které ke katodě. Co je elektrolytem? ANODA KATODA elektrolyt: Zn 2+ Cl - Zn 2+ Zn 2+ Cl - Cl - Cl - Cl - Cl - Zn 2+ Cl -
Složení látek a chemická vazba Číslo variace: 1
 Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Konduktometrie. Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie)
 Elektrochemické metody Konduktometrie Coulometrie Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie) Biosenzory Petr Breinek Elektrochemie-I 2012 Elektrochemie
Elektrochemické metody Konduktometrie Coulometrie Potenciometrie, Iontově selektivní elektrody (ISE) Voltametrie (Ampérometrie, Polarografie) Biosenzory Petr Breinek Elektrochemie-I 2012 Elektrochemie
Elektroanalytické metody
 Elektroanalytické metody Elektroanalytické metody (EAM) zkoumají elektrochemické chování roztoku analytu v závislosti na jeho složení a koncentraci. Analyzovaný roztok je v kontaktu s elektrodami, které
Elektroanalytické metody Elektroanalytické metody (EAM) zkoumají elektrochemické chování roztoku analytu v závislosti na jeho složení a koncentraci. Analyzovaný roztok je v kontaktu s elektrodami, které
Předmět: Ročník: Vytvořil: Datum: CHEMIE PRVNÍ Mgr. Tomáš MAŇÁK 29. květen 2013. Název zpracovaného celku: REDOXNÍ REAKCE REDOXNÍ REAKCE
 Předmět: Ročník: Vytvořil: Datum: CHEMIE PRVNÍ Mgr. Tomáš MAŇÁK 29. květen 2013 Název zpracovaného celku: REDOXNÍ REAKCE REDOXNÍ REAKCE Oxidačně redukční neboli redoxní reakce jsou všechny chemické reakce,
Předmět: Ročník: Vytvořil: Datum: CHEMIE PRVNÍ Mgr. Tomáš MAŇÁK 29. květen 2013 Název zpracovaného celku: REDOXNÍ REAKCE REDOXNÍ REAKCE Oxidačně redukční neboli redoxní reakce jsou všechny chemické reakce,
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 08.04.2013 Číslo DUMu: VY_32_INOVACE_13_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 08.04.2013 Číslo DUMu: VY_32_INOVACE_13_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 08.04.2013 Číslo DUMu: VY_32_INOVACE_13_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
ELEKTROLÝZA. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 13. 3. 2012. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková ELEKTROLÝZA Datum (období) tvorby: 13. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s elektrolýzou. V rámci
Autor: Mgr. Stanislava Bubíková ELEKTROLÝZA Datum (období) tvorby: 13. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s elektrolýzou. V rámci
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Galvanické pokovování a reakce kovů autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Galvanické pokovování a reakce kovů autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Elektrochemie. Zn, + + e. red. 1 Standardní vodíková elektroda je elektroda vytvořená z platiny, pokrytá platinovou černí, sycená plynným
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE 1 LF UK Elektrochemie v biochemii Martin Vejražka Praha, 8 Elektrodové děje Ponoříme-li do roztoku kovového iontu (např Cu ) elektrodu ze stejného kovu (v daném případě mědi),
ÚSTAV LÉKAŘSKÉ BIOCHEMIE 1 LF UK Elektrochemie v biochemii Martin Vejražka Praha, 8 Elektrodové děje Ponoříme-li do roztoku kovového iontu (např Cu ) elektrodu ze stejného kovu (v daném případě mědi),
ELEKTROCHEMIE. Danielův článek e
 ELEKTROCHEMIE Při reakcích v elektrochemických soustavách vzniká nebo se spotřebovává elektrická energie. Praktické aplikace elektrochemie: 1. Využití elektrochemických soustav jako zdroje elektrické energie
ELEKTROCHEMIE Při reakcích v elektrochemických soustavách vzniká nebo se spotřebovává elektrická energie. Praktické aplikace elektrochemie: 1. Využití elektrochemických soustav jako zdroje elektrické energie
Nultá věta termodynamická
 TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
 OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
OBECNÁ CHEMIE František Zachoval CHEMICKÉ ROVNOVÁHY 1. Rovnovážný stav, rovnovážná konstanta a její odvození Dlouhou dobu se chemici domnívali, že jakákoliv chem.
Ústřední komise Chemické olympiády. 53. ročník 2016/2017. KONTROLNÍ TEST ŠKOLNÍHO KOLA kategorie C. ZADÁNÍ: 60 BODŮ časová náročnost: 120 minut
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 KONTROLNÍ TEST ŠKOLNÍHO KOLA kategorie C ZADÁNÍ: 60 BODŮ časová náročnost: 120 minut Zadání kontrolního testu školního kola ChO kat. A a E Úloha
Ústřední komise Chemické olympiády 53. ročník 2016/2017 KONTROLNÍ TEST ŠKOLNÍHO KOLA kategorie C ZADÁNÍ: 60 BODŮ časová náročnost: 120 minut Zadání kontrolního testu školního kola ChO kat. A a E Úloha
 Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie obecná elektrochemie 1. ročník Datum tvorby 3.1.2014 Anotace
Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie obecná elektrochemie 1. ročník Datum tvorby 3.1.2014 Anotace
Masarykova střední škola zemědělská a Vyšší odborná škola, Opava, příspěvková organizace
 Číslo projektu Číslo materiálu Název školy Autor Průřezové téma Tematický celek CZ.1.07/1.5.00/34.0565 VY_32_INOVACE_356_Kovy Masarykova střední škola zemědělská a Vyšší odborná škola, Opava, příspěvková
Číslo projektu Číslo materiálu Název školy Autor Průřezové téma Tematický celek CZ.1.07/1.5.00/34.0565 VY_32_INOVACE_356_Kovy Masarykova střední škola zemědělská a Vyšší odborná škola, Opava, příspěvková
Vyučující po spuštění prezentace může provádět výklad a zároveň vytvářet zápis. Výklad je doprovázen cvičeními k osvojení probírané tématiky.
 Projekt: Příjemce: Tvořivá škola, registrační číslo projektu CZ.1.07/1.4.00/21.3505 Základní škola Ruda nad Moravou, okres Šumperk, Sportovní 300, 789 63 Ruda nad Moravou Zařazení materiálu: Šablona: Sada:
Projekt: Příjemce: Tvořivá škola, registrační číslo projektu CZ.1.07/1.4.00/21.3505 Základní škola Ruda nad Moravou, okres Šumperk, Sportovní 300, 789 63 Ruda nad Moravou Zařazení materiálu: Šablona: Sada:
Soli. ph roztoků solí - hydrolýza
 Soli Soli jsou iontové sloučeniny vzniklé neutralizační reakcí. Např. NaCl je sůl vzniklá reakcí kyseliny HCl a zásady NaOH. Př.: Napište neutralizační reakce jejichž produktem jsou CH 3 COONa, NaCN, NH
Soli Soli jsou iontové sloučeniny vzniklé neutralizační reakcí. Např. NaCl je sůl vzniklá reakcí kyseliny HCl a zásady NaOH. Př.: Napište neutralizační reakce jejichž produktem jsou CH 3 COONa, NaCN, NH
Klasická termodynamika (aneb pøehled FCH I)
 Klasická termodynamika (aneb pøehled FCH I) 1/16 0. zákon 1. zákon id. plyn: pv = nrt pv κ = konst (id., ad.) id. plyn: U = U(T) }{{} Carnotùv cyklus dq T = 0 2. zákon rg, K,... lim S = 0 T 0 S, ds = dq
Klasická termodynamika (aneb pøehled FCH I) 1/16 0. zákon 1. zákon id. plyn: pv = nrt pv κ = konst (id., ad.) id. plyn: U = U(T) }{{} Carnotùv cyklus dq T = 0 2. zákon rg, K,... lim S = 0 T 0 S, ds = dq
Úvod do koroze. (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají)
 Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
RNDr. Daniela Kravecová, PhD. Premonštrátske gymnázium, Kováčska 28, Košice
 Redoxné reakcie RNDr. Daniela Kravecová, PhD. Premonštrátske gymnázium, Kováčska 28, Košice Redoxné reakcie Redoxné reakcie sú chemické reakcie, pri ktorých dochádza k zmene oxidačného čísla atómov alebo
Redoxné reakcie RNDr. Daniela Kravecová, PhD. Premonštrátske gymnázium, Kováčska 28, Košice Redoxné reakcie Redoxné reakcie sú chemické reakcie, pri ktorých dochádza k zmene oxidačného čísla atómov alebo
Průvodka. CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Pořadí DUMu v sadě 07
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově. 07_4_Elektrický proud v kapalinách a plynech
 Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 07_4_Elektrický proud v kapalinách a plynech Ing. Jakub Ulmann 4.1 Elektrický proud v kapalinách Sestavíme
Zavádění inovativních metod a výukových materiálů do přírodovědných předmětů na Gymnáziu v Krnově 07_4_Elektrický proud v kapalinách a plynech Ing. Jakub Ulmann 4.1 Elektrický proud v kapalinách Sestavíme
Koroze kovových materiálů. Kovy, mechanismy koroze, ochrana před korozí
 Koroze kovových materiálů Kovy, mechanismy koroze, ochrana před korozí 1 Kovy Kovy Polokovy Nekovy 2 Kovy Vysoká elektrická a tepelná vodivost Lesklé Kujné a tažné V přírodě se vyskytují převážně ve formě
Koroze kovových materiálů Kovy, mechanismy koroze, ochrana před korozí 1 Kovy Kovy Polokovy Nekovy 2 Kovy Vysoká elektrická a tepelná vodivost Lesklé Kujné a tažné V přírodě se vyskytují převážně ve formě
PRVKY 17. (VII. A) SKUPINY
 PRVKY 17. (VII. A) SKUPINY TEST Úkol č. 1 Doplň následující text správnými informacemi o prvcích 17. skupiny: Prvky 17. skupiny periodické soustavy prvků jsou společným názvem označovány halogeny. Do této
PRVKY 17. (VII. A) SKUPINY TEST Úkol č. 1 Doplň následující text správnými informacemi o prvcích 17. skupiny: Prvky 17. skupiny periodické soustavy prvků jsou společným názvem označovány halogeny. Do této
KOROZE A TECHNOLOGIE POVRCHOVÝCH ÚPRAV
 KOROZE A TECHNOLOGIE POVRCHOVÝCH ÚPRAV Přednáška č. 02: Elektrochemická koroze Autor přednášky: Ing. Vladimír NOSEK Pracoviště: TUL FS, Katedra materiálu Elektrochemická koroze Elektrochemická koroze probíhá
KOROZE A TECHNOLOGIE POVRCHOVÝCH ÚPRAV Přednáška č. 02: Elektrochemická koroze Autor přednášky: Ing. Vladimír NOSEK Pracoviště: TUL FS, Katedra materiálu Elektrochemická koroze Elektrochemická koroze probíhá
Koroze kovů. Koroze lat. corode = rozhlodávat
 Koroze kovů Koroze lat. corode = rozhlodávat Koroze kovů Koroze kovů, plastů, silikátových materiálů Principy korozních procesů = korozní inženýrství Strojírenství Mechanická pevnost Vzhled Elektotechnika
Koroze kovů Koroze lat. corode = rozhlodávat Koroze kovů Koroze kovů, plastů, silikátových materiálů Principy korozních procesů = korozní inženýrství Strojírenství Mechanická pevnost Vzhled Elektotechnika
Název školy: Číslo a název sady: klíčové aktivity: VY_32_INOVACE_131_Elektrochemická řada napětí kovů_pwp
 Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: Předmět, ročník, obor: Číslo a název sady: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ
Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: Předmět, ročník, obor: Číslo a název sady: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ
Stanislav Labík. Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost
 Stanislav Labík Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost 325 labik@vscht.cz 220 444 257 http://www.vscht.cz/fch/ Výuka Letní semestr N403032 Základy fyzikální chemie
Stanislav Labík Ústav fyzikální chemie V CHT Praha budova A, 3. patro u zadního vchodu, místnost 325 labik@vscht.cz 220 444 257 http://www.vscht.cz/fch/ Výuka Letní semestr N403032 Základy fyzikální chemie
Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje.
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Pufry, pufrační kapacita. Oxidoredukce, elektrodové děje. Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka, Tomáš Navrátil
7.3.3.1 ROVNOVÁŽNÉ NAPĚTÍ ČLÁNKU... 14
 7. LKTROCHMI ZÁKLADNÍ POJMY... 1 7.1 ROVNOVÁHY V ROZTOCÍCH LKTROLYTŮ... 7.1.1 SILNÉ LKTROLYTY, AKTIVITA A AKTIVITNÍ KOFICINTY... 7.1. DISOCIAC SLABÝCH LKTROLYTŮ... 7.1.3 VÝPOČT PH... 3 7.1.4 OMZNĚ ROZPUSTNÉ
7. LKTROCHMI ZÁKLADNÍ POJMY... 1 7.1 ROVNOVÁHY V ROZTOCÍCH LKTROLYTŮ... 7.1.1 SILNÉ LKTROLYTY, AKTIVITA A AKTIVITNÍ KOFICINTY... 7.1. DISOCIAC SLABÝCH LKTROLYTŮ... 7.1.3 VÝPOČT PH... 3 7.1.4 OMZNĚ ROZPUSTNÉ
Elektrochemie. Koroze kovových materiálů. Kovy. Kovy. Kovy. Kovy, mechanismy koroze, ochrana před korozí 1. Kovy Polokovy Nekovy
 Koroze kovových materiálů Polokovy Nekovy, mechanismy koroze, ochrana před korozí 1 2 Vysoká elektrická a tepelná vodivost Lesklé Kujné a tažné V přírodě se vyskytují převážně ve formě sloučenin, výjimku
Koroze kovových materiálů Polokovy Nekovy, mechanismy koroze, ochrana před korozí 1 2 Vysoká elektrická a tepelná vodivost Lesklé Kujné a tažné V přírodě se vyskytují převážně ve formě sloučenin, výjimku
Kovové povlaky. Kovové povlaky. Z hlediska funkce. V el. vodivém prostředí. velmi ušlechtilé méně ušlechtile (vzhledem k železu) tloušťka pórovitost
 Kovové povlaky Kovové povlaky Kovové povlaky velmi ušlechtilé méně ušlechtile (vzhledem k železu) Z hlediska funkce tloušťka pórovitost V el. vodivém prostředí katodický anodický charakter 2 Kovové povlaky
Kovové povlaky Kovové povlaky Kovové povlaky velmi ušlechtilé méně ušlechtile (vzhledem k železu) Z hlediska funkce tloušťka pórovitost V el. vodivém prostředí katodický anodický charakter 2 Kovové povlaky
Přeměna chemické energie na elektrickou energii GALVANICKÝ ČLÁNEK
 Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Přeměna chemické energie na elektrickou energii GALVANICKÝ ČLÁNEK Pokus: Ponořte dva různé kovy vzdáleně od
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Přeměna chemické energie na elektrickou energii GALVANICKÝ ČLÁNEK Pokus: Ponořte dva různé kovy vzdáleně od
6. Elektrický proud v elektrolytech
 6. Elektrický proud v elektrolytech 6.1 Elektrolytický vodič Vyjděme z modelu krystalu kuchyňské soli, který se za normálních podmínek chová jako izolant. Při teplotě 810 C krystal taje a mění se na soustavu
6. Elektrický proud v elektrolytech 6.1 Elektrolytický vodič Vyjděme z modelu krystalu kuchyňské soli, který se za normálních podmínek chová jako izolant. Při teplotě 810 C krystal taje a mění se na soustavu
Metody kalibrace. Důležité pojmy. Metoda kalibrační křivky (external standards)
 Důležité pojmy Metody kalibrace Metoda kalibrační křivky (external standards) připravíme sérii kalibračních roztoků stanovovaného analytu, pokrývající zamýšlený koncentrační rozsah snažíme se, aby bylo
Důležité pojmy Metody kalibrace Metoda kalibrační křivky (external standards) připravíme sérii kalibračních roztoků stanovovaného analytu, pokrývající zamýšlený koncentrační rozsah snažíme se, aby bylo
4.4.3 Galvanické články
 ..3 Galvanické články Předpoklady: 01 Zapíchnu do citrónu dva plíšky z různých kovů mezi kovy se objeví napětí (měřitelné voltmetrem) získal jsem baterku, ale žárovku nerozsvítím (citrobaterie dává pouze
..3 Galvanické články Předpoklady: 01 Zapíchnu do citrónu dva plíšky z různých kovů mezi kovy se objeví napětí (měřitelné voltmetrem) získal jsem baterku, ale žárovku nerozsvítím (citrobaterie dává pouze
Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9.
 Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9. Školní rok 0/03, 03/04 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup) Počet hodin pro kapitolu Úvod
Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9. Školní rok 0/03, 03/04 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup) Počet hodin pro kapitolu Úvod
Název materiálu: Vedení elektrického proudu v kapalinách
 Název materiálu: Vedení elektrického proudu v kapalinách Jméno autora: Mgr. Magda Zemánková Materiál byl vytvořen v období: 2. pololetí šk. roku 2010/2011 Materiál je určen pro ročník: 9. Vzdělávací oblast:
Název materiálu: Vedení elektrického proudu v kapalinách Jméno autora: Mgr. Magda Zemánková Materiál byl vytvořen v období: 2. pololetí šk. roku 2010/2011 Materiál je určen pro ročník: 9. Vzdělávací oblast:
Fyzikální chemie. ochrana životního prostředí analytická chemie chemická technologie denní. Platnost: od 1. 9. 2009 do 31. 8. 2013
 Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
Učební osnova předmětu Fyzikální chemie Studijní obor: Aplikovaná chemie Zaměření: Forma vzdělávání: Celkový počet vyučovacích hodin za studium: Analytická chemie Chemická technologie Ochrana životního
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Vzdělávací oblast: Člověk a příroda. Vyučovací předmět: Chemie. Třída: tercie. Očekávané výstupy. Poznámky. Přesahy. Žák: Průřezová témata
 Vzdělávací oblast: Člověk a příroda Vyučovací předmět: Chemie Třída: tercie Očekávané výstupy Uvede příklady chemického děje a čím se zabývá chemie Rozliší tělesa a látky Rozpozná na příkladech fyzikální
Vzdělávací oblast: Člověk a příroda Vyučovací předmět: Chemie Třída: tercie Očekávané výstupy Uvede příklady chemického děje a čím se zabývá chemie Rozliší tělesa a látky Rozpozná na příkladech fyzikální
instrumentální Většina instrumentálních metod vyžaduje kalibraci. Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
 Kvantitativní analýza - instrumentální Většina instrumentálních metod vyžaduje kalibraci. Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité pojmy Metody kalibrace Metoda kalibrační
Kvantitativní analýza - instrumentální Většina instrumentálních metod vyžaduje kalibraci. Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Důležité pojmy Metody kalibrace Metoda kalibrační
H - -I (hydridy kovů) vlastnosti: plyn - nekov 14x lehčí než vzduch bez barvy, chuti, zápachu se vzduchem tvoří výbušnou směs redukční činidlo
 Otázka: Vodík, kyslík Předmět: Chemie Přidal(a): Prang Vodík 1. Charakteristika 1 1 H 1s 1 ; 1 proton, jeden elektron nejlehčí prvek výskyt: volný horní vrstva atmosféry, vesmír - elementární vázaný- anorganické,
Otázka: Vodík, kyslík Předmět: Chemie Přidal(a): Prang Vodík 1. Charakteristika 1 1 H 1s 1 ; 1 proton, jeden elektron nejlehčí prvek výskyt: volný horní vrstva atmosféry, vesmír - elementární vázaný- anorganické,
Přechodné prvky, jejich vlastnosti a sloučeniny
 Přechodné prvky, jejich vlastnosti a sloučeniny - jsou to d-prvky, nazývají se také přechodné prvky - v PSP jsou umístěny mezi s a p prvky - nacházejí se ve 4. 7. periodě - atomy přechodných prvků mají
Přechodné prvky, jejich vlastnosti a sloučeniny - jsou to d-prvky, nazývají se také přechodné prvky - v PSP jsou umístěny mezi s a p prvky - nacházejí se ve 4. 7. periodě - atomy přechodných prvků mají
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939. Název projektu: Investice do vzdělání - příslib do budoucnosti
 Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
Registrační číslo projektu: CZ.1.07/1.4.00/21.2939 Název projektu: Investice do vzdělání - příslib do budoucnosti Číslo přílohy: VY_číslo šablony_inovace_číslo přílohy Autor Datum vytvoření vzdělávacího
