Atomové a molekulové orbitaly Ion molekuly vodíku. Molekula vodíku Heitler-Londonovou metodou. Metoda LCAO. Báze atomových orbitalů.
|
|
|
- Klára Ivana Jandová
- před 5 lety
- Počet zobrazení:
Transkript
1 Atomové a molekulové orbitaly Ion molekuly vodíku. Molekula vodíku Heitler-Londonovou metodou. Metoda LCAO. Báze atomových orbitalů. Ion molekuly vodíku H + 2 První použití metody je demonstrováno při řešení H + 2 se Schrödingerovou rovnicí H ψ = E ψ, které je hledáno ve tvaru lineární kombinace ψ = c a ψ a + c b ψ b, () kde ψ a a ψ b jsou vhodně zvolené atomové orbitaly. V tomto případě jsou voleny jako normalizované vlnové funkce základního stavu atomu H s polohami jader a a b ψ a = e r a a B, analogicky pro ψ πa 3 b, (2) B kde a B je Bohrův poloměr. Rovnice () určuje vlnovou funkci označovanou jako molekulový orbital. Dále s využitím předpokladu pevných jader, tj. Born-Oppenheimerovy aproximace, dosadíme do Schrödingerovy rovnice tvar () a hamiltonián H = 2 2m e2 e2 + e2 r a r b R, (3) kde e je náboj elektronu (v soustavě CGS), poslední člen popisuje elektrostatickou repulzi jader. Navíc si uvědomíme, že použité atomové orbitaly ψ a a ψ b jsou vlnové funkce základního stavu H, takže ) ( 2 2m e2 ψ a = E ψ a, analogicky pro jádro b,. (4) r a kde E = e2 2a B je energie základního stavu H. Integrací pak dostaneme C c a + A c b = (E E ) (c a + S c b ), opět analogicky pro ψ b A c a + C c b = (E E ) (S c a + c b ), (5) kde S = ψaψ b dv se nazývá překryvový integrál. Tento vyjadřuje míru překryvu atomových orbitalů. Integrál C = ( ) ψa e2 r b + e2 ψ R a dv se nazývá Coulombovský a integrál A = ( ψa e2 r a + e2 R řešení, symetrické c a = c b a antisymetrické c a = c b tvaru ) ψ b dv je výměnný integrál. Vyřešením problému (5) dostaneme dvě ψ S = 2( + S) (ψ a + ψ b ) E S = E + C + A, respektive + S ψ A = (ψ a ψ b ) 2( S) E A = E + C A S (6)
2 Integrály A, C a S lze vypočítat analyticky v eliptických souřadnicích. Závisí na R, tudíž i celková energie závisí na vzdálenosti jader. Symetrický stav s energií E S má minimum energie, kdežto excitovaný antisymetrický stav s E A minimum nemá, jak lze vidět v Obrázku. Obrázek : Celková energie H + 2, plnou čarou symetrický stav a čárkovaně antisymetrický. Shoda s experimentem není nijak závratná (asi třikrát vyšší než skutečná). Informaci o charakteru vazby získáme z hustoty pravděpodobnosti ψ S 2 resp. ψ A 2, ve středu spojnice jader pak vyjde hustota pravděpodobnosti antisymetrického stavu nulová a tudíž se pro tento stav nevytváří vazba. Pro symetrický stav vyjde hustota pravděpodobnosti nenulová, dokonce vyšší než pro dva neinteragující atomy vodíku. Podstata vazby v symetrickém, vazebném, stavu tkví v současném přitahování elektronu oběma jádry, přičemž elektron je částečně delokalizován do oblasti vazby. Doplňme tvar celkové vlnové funkce elektronu v základním stavu H + 2, podle Skály je to zřejmé Ψ = ψ S χ, (7) kde χ je spinová vlnová funkce elektronu χ = α nebo β, kde α a β jsou spinory ( ) ( ) 0 α =, β =. (8) 0 je tedy dubletní. Detailnější informace ve Skálově Kvantové teorii mo- Základní stav H + 2 lekul, str Molekula vodíku H 2 Stejným způsobem lze řešit i molekulu vodíku Heitlerovou-Londonovou metodou. Hamiltonián se zesložití na Řešení hledáme ve tvaru H = 2 2m ( + 2 ) e2 r a e2 r a 2 e2 r b e2 r b 2 + e2 r 2 + e2 R. (9) ψ S = c S (ψ ab + ψ ba ), respektive (0) ψ A = c A (ψ ab ψ ba ), () 2
3 kde zvolíme do pozic atomových orbitalů vlnové funkce, které popisují dva vzdálené neinteragující atomy vodíku ψ ab = ψ a ( r )ψ b ( r 2 ) ψ ba = ψ b ( r )ψ a ( r 2 ), (2) kde funkce ψ ab odpovídá prvnímu elektronu v základním stavu atomu H s jádrem a a druhému elektronu v základním stavu H s jádrem b (u ψ ba je to opačně). Pro obě funkce (2) platí analogie rovnice (2) se složitějším hamiltoniánem (9). Z důvodu symetrie jsou koeficienty u ψ ab a ψ ba v rovnici () v absolutní hodnotě stejné, stejně jako u H + 2. Výsledné vzorce pro H 2 dostaneme z výsledků pro H + 2 (viz 6) záměnou ψ a ψ ab, (3) ψ b ψ ba, (4) E 2E. (5) Příslušným způsobem se pozmění i překryvový, coulombovský a výměnný integrál (vzorce ve Skálovi str. 37) a platí: Překryvový integrál pro H 2 je pro stejnou vzdálenost roven kvadrátu překryvovému integrálu pro H + 2. Coulombovský integrál je střední hodnota coulombovské interakce mezi dvěma spojitě rozprostřenými náboji s hustotou náboje e ψ a 2 a e ψ b 2. Výměnný integrál nemá klasickou analogii, je důsledkem konstrukce vlnové funkce. Celkovou energii si můžeme přepsat do tvaru E SA = 2 E + C ± S ± A ± S, (6) kde druhý člen se nazývá coulombovská energie a třetí člen výměnná energie. Pomocí eliptických souřadnic lze vypočítat integrály A, C a S a platí C > 0, A < 0, E S < E A. (7) Analogicky iontu H + 2 je prostorová část vlnové funkce základního stavu symetrická. Existence vazby v molekule H 2 je podmíněna nenulovou velikostí překryvového integrálu. Závislost celkové energie na mezijaderné velikosti je podobná jako u H + 2 (Obrázek ) a shoda s experimentem zase není nejlepší. Nakonec zkonstruujeme celkovou vlnovou funkci, která má být antisymetrická. Proto je třeba symetrickou prostorovou část násobit antisymetrickou spinovou částí a naopak. Základní stav je tudíž singletní a excitovaný stav je tripletní s vlnovými funkcemi Ψ = ψ S 2 (αβ βα) (8) Ψ = ψ A αα Ψ = ψ A 2 (αβ + βα) Ψ = ψ A ββ. (9) 3
4 Výpočet se dá vylepšit. zavedením náboje jádra jako parametru do rovnic definujících atomové orbitaly (2), tj. v čitateli argumentu exponenciály přibyde člen Z a minimum energie se pak hledá v prostoru proměnných R a Z. 2. Dalšího zlepšení výsledků se dosáhne zavedením iontových stavů do vlnové funkce základního stavu. 3. Dosud uvažované atomové orbitaly byly sféricky symetrické vzledem k polohám jader, což však není vždy oprávněný předpoklad (ani u H 2 ). Tudíž se nabízí zavedení vzájemné polarizace atomů vodíku. 4. Hundova-Mullikenova metoda zase nejdřív konstruuje molekulové orbitaly jednotlivých elektronů a z nich potom sestaví dvouelektronovou vlnovou funkci. 5. Konečně je potřeba zahrnout do výpočtů korelaci pohybu elektronů ve dvou stupních: Statická korelace znamená respektování antisymetrie úplné mnohaelektronové vlnové funkce. Dynamická korelace započítává korelaci pohybu elektronů způsobenou vzájemnou coulombovskou interakcí elektronů, tj. vlnová funkce musí obecně záviset na vzdálenosti jader. Korelace pohybu elektronů je i tématem výpočtu Jamese a Coolidge. 3 Metoda LCAO Mnohaelektronovou vlnovou funkci lze sestrojit jako lineární kombinaci Slaterových determinantů sestavených z jednoelektronových vlnových funkcí. Tak vlnová funkce základního singletního stavu H 2 z rovnice (8) by byla Ψ = ψ a(r )α() ψ b (r )β() ψ a (r 2 )α(2) ψ b (r 2 )β(2) ψ a (r )β() ψ b (r )α() ψ a (r 2 )β(2) ψ b (r 2 )α(2) (20) Vlnové funkce tripletního excitovaného stavu si lze prohlédnout ve Skálovi na str. 47 a 48. Lineární kombinace Slaterových determinantů sestrojených z atomových spinorbitalů je základem metody valenčních vazeb (VB, valence bonds). Naproti tomu lineární kombinace Sl. det. konstruovaných z molekulových spinorbitalů je základem metody LCAO (linear combination of atomic orbitals). V této metodě se předpokládá prostorová část molekulových orbitalů ve tvaru ψ i (r) = µ c µi ϕ µ (r), (2) kde ψ i jsou molekulové orbitaly a ϕ µ jsou atomové orbitaly. Počet Slaterových determinantů v rozvoji vlnové funkce Ψ podle metody VB rychle roste s počtem elektronů. Ale přesnější výpočty podle metody LCAO často vyžaduje také velký počet Sl. determinantů. 4
5 4 Báze atomových orbitalů Metoda LCAO využívá lineární kombinaci atomových orbitalů pro sestrojení molekulových orbitalů podle vztahu (2). Obecně bázi by mohl tvořit libovolný úplný systém funkcí lokalizovaných na jednom z jader, to by bylo ale nevýhodné. Praktičtější je neúplný systém atomových orbitalů na jednotlivých jádrech ve smyslu přibližného výpočtu Ritzovou variační metodou. Atomové orbitaly je vhodné vybrat tak, aby dobře vystihovaly skutečné atomární vlnové funkce a bylo možné aspoň část maticových elementů hamiltoniánu spočítat analyticky. Reálné kulové funkce Schrödingerova rovnice má v kvantové teorii molekul obvykle reálný hamiltonián. Tudíž reálná i imaginární část vlnové funkce splňují každá zvlášť Schrödingerovu rovnici a lze se proto omezit na reálné vlnové funkce ψ i. Místo komplexních kulových funkcí se obvykle používají jejich reálné kombinace Y lm (θ, ϕ) = Θ lm (θ)φ m (ϕ). (22) Konkrétní tvar je zběsilý a lze ho nalézt ve Skálovi na str. 62 a 63. Snad jenom dodejme, že v nich vystupují Legendreovy polynomy. Radiální části pro vodíkupodobný atom Dají se volit různě, např. lze použít radiální část vlnových funkcí z řešení vodíkupodobného atomu s nábojem jádra Z e. Jejich tvary jsou opět komplikované a někdy je potřeba provádět výpočty numericky. Slaterovy funkce Slaterovy funkce (STO, Slater type orbitals) jsou podstatně jednodušší než výše zmíněné a jsou také široce používané. Mají tvar R(r) = (2ζ) n+ 2 [(2n)!] 2 r n e ζr, (23) kde ζ je orbitální Slaterův exponent udávající maximum elektronové hustoty směrem od jádra a vyjadřují vliv stínění jádra elektrony. Vypočítá se ζ = Z s n, (24) kde s je stínicí konstanta a n efektivní kvantové číslo. Hodnoty Sl. exponentů jsou tabelovány. Jejich nevýhodou je to, že jejich radiální části nemají nulové body, jako např. vodíkovské funkce, navíc ne všechny maticové elementy lze s nimi spočítat analyticky. Gaussovské funkce Nemají předchozí nevýhodu v nemožnosti spočítat všechny maticové elementy analyticky. Jsou definovány jako R(r) = Nr n e a( r r A) 2, (25) kde N je normalizační faktor, a kladný exponent a r A je poloha jádra, na kterém je funkce lokalizována. Zajímavou vlastností je to, že součin dvou takových funkcí v různých místech lze napsat jako jednu gaussovskou funkci na spojnici těchto míst. Díky tomu lze transformovat vícecentrové integrály na jedno a dvoucentrové. Nevýhodou je nevhodné chování pro r a pro r 0. To ale lze potlačit použitím lineárních kombinací několika gaussovských funkcí namísto jednotlivých. Na použití gaussovských funkcí je založen program GAUSSIAN. Nezbývá než dodat, že bází atomových orbitalů je množství. 5
Od kvantové mechaniky k chemii
 Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
Ab initio výpočty v chemii a biochemii
 Ab initio výpočty v chemii a biochemii Doc. RNDr. Ing. Jaroslav Burda, CSc., jaroslav.burda@mff.cuni.cz Dr. Vladimír Sychrovský vladimir.sychrovsky@uochb.cas.cz Studijní literatura Szabo A., Ostlund N.S.
Ab initio výpočty v chemii a biochemii Doc. RNDr. Ing. Jaroslav Burda, CSc., jaroslav.burda@mff.cuni.cz Dr. Vladimír Sychrovský vladimir.sychrovsky@uochb.cas.cz Studijní literatura Szabo A., Ostlund N.S.
Atom vodíku. Nejjednodušší soustava: p + e Řešitelná exaktně. Kulová symetrie. Potenciální energie mezi p + e. e =
 Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Operátory a maticové elementy
 Operátory a matice Operátory a maticové elementy operátory je výhodné reprezentovat maticemi maticové elementy operátorů jsou dány vztahy mezi Slaterovými determinanty obsahujícími ortonormální orbitaly
Operátory a matice Operátory a maticové elementy operátory je výhodné reprezentovat maticemi maticové elementy operátorů jsou dány vztahy mezi Slaterovými determinanty obsahujícími ortonormální orbitaly
ATOM VODÍKU MODEL : STOJÍCÍ BODOVÉ JÁDRO A ELEKTRON VZÁJEMNĚ ELEKTROSTATICKY INTERAGUJÍCÍ SCHRÖDINGEROVA ROVNICE PRO PŘÍPAD POTENCIÁLNÍ ENERGIE.
 ATOMY + MOLEKULY ATOM VODÍKU MODEL : STOJÍCÍ BODOVÉ JÁDRO A ELEKTRON VZÁJEMNĚ ELEKTROSTATICKY INTERAGUJÍCÍ SCHRÖDINGEROVA ROVNICE H ˆψ = Eψ PRO PŘÍPAD POTENCIÁLNÍ ENERGIE Vˆ = Ze 2 4πε o r ŘEŠENÍ HLEDÁME
ATOMY + MOLEKULY ATOM VODÍKU MODEL : STOJÍCÍ BODOVÉ JÁDRO A ELEKTRON VZÁJEMNĚ ELEKTROSTATICKY INTERAGUJÍCÍ SCHRÖDINGEROVA ROVNICE H ˆψ = Eψ PRO PŘÍPAD POTENCIÁLNÍ ENERGIE Vˆ = Ze 2 4πε o r ŘEŠENÍ HLEDÁME
13 Elektronová struktura molekul
 13 Elektronová struktura molekul Ústředním úkolem kvantové chemie po zavedení Bornovy-Oppenheimerovy aproximace je výpočet elektronové energie molekul Ĥ e ψ e ( r, R) = E e ( R)ψ e ( r, R), (13.1) kde
13 Elektronová struktura molekul Ústředním úkolem kvantové chemie po zavedení Bornovy-Oppenheimerovy aproximace je výpočet elektronové energie molekul Ĥ e ψ e ( r, R) = E e ( R)ψ e ( r, R), (13.1) kde
17 Vlastnosti molekul
 17 Vlastnosti molekul Experimentálně molekuly charakterizujeme pomocí nejrůznějších vlastností: můžeme změřit třeba NMR posuny, elektrické či magnetické parametry či třeba jejich optickou otáčivost. Tyto
17 Vlastnosti molekul Experimentálně molekuly charakterizujeme pomocí nejrůznějších vlastností: můžeme změřit třeba NMR posuny, elektrické či magnetické parametry či třeba jejich optickou otáčivost. Tyto
Modelové výpočty na H 2 a HeH +
 Modelové výpočty na H 2 a HeH + Minimální báze Všechny teoretické poznatky je užitečné ilustrovat modelovým výpočtem. Budeme aplikovat Hartree-Fockovy výpočty na uzavřených slupkách systémů H 2 a HeH +.
Modelové výpočty na H 2 a HeH + Minimální báze Všechny teoretické poznatky je užitečné ilustrovat modelovým výpočtem. Budeme aplikovat Hartree-Fockovy výpočty na uzavřených slupkách systémů H 2 a HeH +.
Přehled Ab Initio a semiempirických metod
 Přehled Ab Initio a semiempirických metod Pokud se vám bude zdát, že je v tom nějaký blud, tak tam asi je. Budu rád, když mě na něj upozorníte. Ab initio metody - od počátku, z prvotních principů, tzn.
Přehled Ab Initio a semiempirických metod Pokud se vám bude zdát, že je v tom nějaký blud, tak tam asi je. Budu rád, když mě na něj upozorníte. Ab initio metody - od počátku, z prvotních principů, tzn.
Hamiltonián popisující atom vodíku ve vnějším magnetickém poli:
 Orbitální a spinový magnetický moment a jejich interakce s vnějším polem Vše na příkladu atomu H: Elektron (e - ) a jádro (u atomu H pouze p + ) mají vlastní magnetický moment (= spin). Tyto dva dipóly
Orbitální a spinový magnetický moment a jejich interakce s vnějším polem Vše na příkladu atomu H: Elektron (e - ) a jádro (u atomu H pouze p + ) mají vlastní magnetický moment (= spin). Tyto dva dipóly
Mul$determinantální metody: CASSCF
 Mul$determinantální metody: CASSCF Mul%konfiguračni (mnohadeterninantálni MC SCF) metody použivají narozdíl od metody Hartreeho- Focka pro popis N- elektronového systému větší počet Slaterových determinantů.
Mul$determinantální metody: CASSCF Mul%konfiguračni (mnohadeterninantálni MC SCF) metody použivají narozdíl od metody Hartreeho- Focka pro popis N- elektronového systému větší počet Slaterových determinantů.
Řešit atom vodíku znamená nalézt řešení Schrödingerovy rovnice s příslušným hamiltoniánem. 1 4πǫ 0. 2m e
 8 Atom vodíku Správné řešení atomu vodíku je jedním z velkých vítězství kvantové mechaniky. Podle klasické fyziky náboj, který se pohybuje se zrychlením (elektron obíhající vodíkové jádro proton), by měl
8 Atom vodíku Správné řešení atomu vodíku je jedním z velkých vítězství kvantové mechaniky. Podle klasické fyziky náboj, který se pohybuje se zrychlením (elektron obíhající vodíkové jádro proton), by měl
Skalární a vektorový popis silového pole
 Skalární a vektorový popis silového pole Elektrické pole Elektrický náboj Q [Q] = C Vlastnost materiálových objektů Interakce (vzájemné silové působení) Interakci (vzájemné silové působení) mezi dvěma
Skalární a vektorový popis silového pole Elektrické pole Elektrický náboj Q [Q] = C Vlastnost materiálových objektů Interakce (vzájemné silové působení) Interakci (vzájemné silové působení) mezi dvěma
Teorie chemické vazby a molekulární geometrie Molekulární geometrie VSEPR
 Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
METODY VÝPOČETNÍ CHEMIE
 METODY VÝPOČETNÍ CHEMIE Metody výpočetní chemie Ab initio metody Semiempirické metody Molekulová mechanika Molekulová simulace Ab initio metody Ab initio - od počátku Metody kvantově-mechanické vycházejí
METODY VÝPOČETNÍ CHEMIE Metody výpočetní chemie Ab initio metody Semiempirické metody Molekulová mechanika Molekulová simulace Ab initio metody Ab initio - od počátku Metody kvantově-mechanické vycházejí
Laserová technika prosince Katedra fyzikální elektroniky.
 Laserová technika 1 Aktivní prostředí Šíření rezonančního záření dvouhladinovým prostředím Jan Šulc Katedra fyzikální elektroniky České vysoké učení technické jan.sulc@fjfi.cvut.cz 22. prosince 2016 Program
Laserová technika 1 Aktivní prostředí Šíření rezonančního záření dvouhladinovým prostředím Jan Šulc Katedra fyzikální elektroniky České vysoké učení technické jan.sulc@fjfi.cvut.cz 22. prosince 2016 Program
Molekuly 1 12/4/2011. Molekula definice IUPAC. Molekuly. Proč existují molekuly? Kosselův model. Představy o molekulách
 1/4/011 Molekuly 1 Molekula definice IUPC elektricky neutrální entita sestávající z více nežli jednoho atomu. Přesně, molekula, v níž je počet atomů větší nežli jedna, musí odpovídat snížení na ploše potenciální
1/4/011 Molekuly 1 Molekula definice IUPC elektricky neutrální entita sestávající z více nežli jednoho atomu. Přesně, molekula, v níž je počet atomů větší nežli jedna, musí odpovídat snížení na ploše potenciální
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
14. přednáška. Přímka
 14 přednáška Přímka Začneme vyjádřením přímky v prostoru Přímku v prostoru můžeme vyjádřit jen parametricky protože obecná rovnice přímky v prostoru neexistuje Přímka v prostoru je určena bodem A= [ a1
14 přednáška Přímka Začneme vyjádřením přímky v prostoru Přímku v prostoru můžeme vyjádřit jen parametricky protože obecná rovnice přímky v prostoru neexistuje Přímka v prostoru je určena bodem A= [ a1
10 Více-elektronové atomy
 1 Více-elektronové atomy Atom vodíku je asi nejsložitější soustava, kterou jsme schopni analyticky přesně vyřešit. Tato situace je pro chemika pochopitelně málo uspokojivá. Pomocí kvantové teorie bychom
1 Více-elektronové atomy Atom vodíku je asi nejsložitější soustava, kterou jsme schopni analyticky přesně vyřešit. Tato situace je pro chemika pochopitelně málo uspokojivá. Pomocí kvantové teorie bychom
John Dalton Amadeo Avogadro
 Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Teoretická chemie 1. cvičení
 Teoretická chemie 1. cvičení Teoretická část Základní úlohou kvantové chemie je nalézt elektronovou vlnovou funkci zkoumané molekuly Ψ a z ní poté odvodit všechny zajímavé vlastnosti této molekuly, např.
Teoretická chemie 1. cvičení Teoretická část Základní úlohou kvantové chemie je nalézt elektronovou vlnovou funkci zkoumané molekuly Ψ a z ní poté odvodit všechny zajímavé vlastnosti této molekuly, např.
1. Náhodný vektor (X, Y ) má diskrétní rozdělení s pravděpodobnostní funkcí p, kde. p(x, y) = a(x + y + 1), x, y {0, 1, 2}.
 VIII. Náhodný vektor. Náhodný vektor (X, Y má diskrétní rozdělení s pravděpodobnostní funkcí p, kde p(x, y a(x + y +, x, y {,, }. a Určete číslo a a napište tabulku pravděpodobnostní funkce p. Řešení:
VIII. Náhodný vektor. Náhodný vektor (X, Y má diskrétní rozdělení s pravděpodobnostní funkcí p, kde p(x, y a(x + y +, x, y {,, }. a Určete číslo a a napište tabulku pravděpodobnostní funkce p. Řešení:
Molekuly. Všeobecně známý fakt: atomy se slučujou do molekul, pokud to zrovna nejsou atomy inertních plynů v posledním sloupci periodické tabulky
 Molekuly Všeobecně známý fakt: atomy se slučujou do molekul, pokud to zrovna nejsou atomy inertních plynů v posledním sloupci periodické tabulky Nejjednodušší případ: molekulární iont H +, tj. dva protony
Molekuly Všeobecně známý fakt: atomy se slučujou do molekul, pokud to zrovna nejsou atomy inertních plynů v posledním sloupci periodické tabulky Nejjednodušší případ: molekulární iont H +, tj. dva protony
Diferenciální rovnice 3
 Diferenciální rovnice 3 Lineární diferenciální rovnice n-tého řádu Lineární diferenciální rovnice (dále jen LDR) n-tého řádu je rovnice tvaru + + + + = kde = je hledaná funkce, pravá strana a koeficienty
Diferenciální rovnice 3 Lineární diferenciální rovnice n-tého řádu Lineární diferenciální rovnice (dále jen LDR) n-tého řádu je rovnice tvaru + + + + = kde = je hledaná funkce, pravá strana a koeficienty
1 Tyto materiály byly vytvořeny za pomoci grantu FRVŠ číslo 1145/2004.
 Prostá regresní a korelační analýza 1 1 Tyto materiály byly vytvořeny za pomoci grantu FRVŠ číslo 1145/2004. Problematika závislosti V podstatě lze rozlišovat mezi závislostí nepodstatnou, čili náhodnou
Prostá regresní a korelační analýza 1 1 Tyto materiály byly vytvořeny za pomoci grantu FRVŠ číslo 1145/2004. Problematika závislosti V podstatě lze rozlišovat mezi závislostí nepodstatnou, čili náhodnou
Úvod do moderní fyziky. lekce 3 stavba a struktura atomu
 Úvod do moderní fyziky lekce 3 stavba a struktura atomu Vývoj představ o stavbě atomu 1904 J. J. Thomson pudinkový model atomu 1909 H. Geiger, E. Marsden experiment s ozařováním zlaté fólie alfa částicemi
Úvod do moderní fyziky lekce 3 stavba a struktura atomu Vývoj představ o stavbě atomu 1904 J. J. Thomson pudinkový model atomu 1909 H. Geiger, E. Marsden experiment s ozařováním zlaté fólie alfa částicemi
Elektronový obal atomu
 Elektronový obal atomu Vlnění o frekvenci v se může chovat jako proud částic (kvant - fotonů) o energii E = h.v Částice pohybující se s hybností p se může chovat jako vlna o vlnové délce λ = h/p Kde h
Elektronový obal atomu Vlnění o frekvenci v se může chovat jako proud částic (kvant - fotonů) o energii E = h.v Částice pohybující se s hybností p se může chovat jako vlna o vlnové délce λ = h/p Kde h
7. Derivace složené funkce. Budeme uvažovat složenou funkci F = f(g), kde některá z jejich součástí
 202-m3b2/cvic/7slf.tex 7. Derivace složené funkce. Budeme uvažovat složenou funkci F = fg, kde některá z jejich součástí může být funkcí více proměnných. Předpokládáme, že uvažujeme funkce, které mají
202-m3b2/cvic/7slf.tex 7. Derivace složené funkce. Budeme uvažovat složenou funkci F = fg, kde některá z jejich součástí může být funkcí více proměnných. Předpokládáme, že uvažujeme funkce, které mají
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/
 Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Předmět: LRR/CHPB1/Chemie pro biology 1 Elektronový obal Mgr. Karel Doležal Dr. Cíl přednášky: seznámit posluchače se stavbou
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Předmět: LRR/CHPB1/Chemie pro biology 1 Elektronový obal Mgr. Karel Doležal Dr. Cíl přednášky: seznámit posluchače se stavbou
Matematika 1 MA1. 1 Analytická geometrie v prostoru - základní pojmy. 4 Vzdálenosti. 12. přednáška ( ) Matematika 1 1 / 32
 Matematika 1 12. přednáška MA1 1 Analytická geometrie v prostoru - základní pojmy 2 Skalární, vektorový a smíšený součin, projekce vektoru 3 Přímky a roviny 4 Vzdálenosti 5 Příčky mimoběžek 6 Zkouška;
Matematika 1 12. přednáška MA1 1 Analytická geometrie v prostoru - základní pojmy 2 Skalární, vektorový a smíšený součin, projekce vektoru 3 Přímky a roviny 4 Vzdálenosti 5 Příčky mimoběžek 6 Zkouška;
Chemická vazba. John Dalton Amadeo Avogadro
 Chemická vazba John Dalton 1766-1844 Amadeo Avogadro 1776-1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904-1981 Fritz W. London 1900-1954 Teorie molekulových orbitalů Friedrich und 1896-1997
Chemická vazba John Dalton 1766-1844 Amadeo Avogadro 1776-1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904-1981 Fritz W. London 1900-1954 Teorie molekulových orbitalů Friedrich und 1896-1997
Inovace studia molekulární a buněčné biologie
 Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
16 Semiempirické přístupy
 16 Semiempirické přístupy V této kapitole se podíváme na skupinu semiempirických metod. Ačkoli semiempirické metody také vycházejí z řešení elektronové Schrödingerovy rovnice, jejich rovnice obsahují dodatečné
16 Semiempirické přístupy V této kapitole se podíváme na skupinu semiempirických metod. Ačkoli semiempirické metody také vycházejí z řešení elektronové Schrödingerovy rovnice, jejich rovnice obsahují dodatečné
1. Kvantové jámy. Tabulka 1: Efektivní hmotnosti nosičů v krystalech GaAs, AlAs, v jednotkách hmotnosti volného elektronu m o.
 . Kvantové jámy Pokročilé metody růstu krystalů po jednotlivých vrstvách (jako MBE) dovolují vytvořit si v krystalu libovolný potenciál. Jeden z hojně používaných materiálů je: GaAs, AlAs a jejich ternární
. Kvantové jámy Pokročilé metody růstu krystalů po jednotlivých vrstvách (jako MBE) dovolují vytvořit si v krystalu libovolný potenciál. Jeden z hojně používaných materiálů je: GaAs, AlAs a jejich ternární
Elektronový obal atomu
 Elektronový obal atomu Ondřej Havlíček.ročník F-Vt/SŠ Jsoucno je vždy něco, co jsme si sami zkonstruovali ve své mysli. Podstata takovýchto konstrukcí nespočívá v tom, že by byly odvozeny ze smyslových
Elektronový obal atomu Ondřej Havlíček.ročník F-Vt/SŠ Jsoucno je vždy něco, co jsme si sami zkonstruovali ve své mysli. Podstata takovýchto konstrukcí nespočívá v tom, že by byly odvozeny ze smyslových
PRIMITIVNÍ FUNKCE. Primitivní funkce primitivní funkce. geometrický popis integrály 1 integrály 2 spojité funkce konstrukce prim.
 PRIMITIVNÍ FUNKCE V předchozích částech byly zkoumány derivace funkcí a hlavním tématem byly funkce, které derivace mají. V této kapitole se budou zkoumat funkce, které naopak jsou derivacemi jiných funkcí
PRIMITIVNÍ FUNKCE V předchozích částech byly zkoumány derivace funkcí a hlavním tématem byly funkce, které derivace mají. V této kapitole se budou zkoumat funkce, které naopak jsou derivacemi jiných funkcí
Úvod do kvantového počítání
 2. přednáška Katedra počítačů, Fakulta elektrotechnická České vysoké učení technické v Praze 17. března 2005 Opakování Část I Přehled z minulé hodiny Opakování Alternativní výpočetní modely Kvantové počítače
2. přednáška Katedra počítačů, Fakulta elektrotechnická České vysoké učení technické v Praze 17. března 2005 Opakování Část I Přehled z minulé hodiny Opakování Alternativní výpočetní modely Kvantové počítače
Elektromagnetické pole je generováno elektrickými náboji a jejich pohybem. Je-li zdroj charakterizován nábojovou hustotou ( r r
 Záření Hertzova dipólu, kulové vlny, Rovnice elektromagnetického pole jsou vektorové diferenciální rovnice a podle symetrie bývá vhodné je řešit v křivočarých souřadnicích. Základní diferenciální operátory
Záření Hertzova dipólu, kulové vlny, Rovnice elektromagnetického pole jsou vektorové diferenciální rovnice a podle symetrie bývá vhodné je řešit v křivočarých souřadnicích. Základní diferenciální operátory
PRIMITIVNÍ FUNKCE DEFINICE A MOTIVACE
 PIMITIVNÍ FUNKCE V předchozích částech byly zkoumány derivace funkcí a hlavním tématem byly funkce, které derivace mají. V této kapitole se budou zkoumat funkce, které naopak jsou derivacemi jiných funkcí
PIMITIVNÍ FUNKCE V předchozích částech byly zkoumány derivace funkcí a hlavním tématem byly funkce, které derivace mají. V této kapitole se budou zkoumat funkce, které naopak jsou derivacemi jiných funkcí
Elektronový obal atomu
 Elektronový obal atomu Chemické vlastnosti atomů (a molekul) jsou určeny vlastnostmi elektronového obalu. Chceme znát energii a prostorové rozložení elektronů Znalosti o elektronovém obalu byly získány
Elektronový obal atomu Chemické vlastnosti atomů (a molekul) jsou určeny vlastnostmi elektronového obalu. Chceme znát energii a prostorové rozložení elektronů Znalosti o elektronovém obalu byly získány
Fyzika atomového jádra
 Fyzika atomového jádra (NJSF064) František Knapp http://www-ucjf.troja.mff.cuni.cz/~knapp/jf/ frantisek.knapp@mff.cuni.cz Slupkový model jádra evidence magických čísel: hmoty, separační energie, vazbové
Fyzika atomového jádra (NJSF064) František Knapp http://www-ucjf.troja.mff.cuni.cz/~knapp/jf/ frantisek.knapp@mff.cuni.cz Slupkový model jádra evidence magických čísel: hmoty, separační energie, vazbové
Elementární částice. 1. Leptony 2. Baryony 3. Bosony. 4. Kvarkový model 5. Slabé interakce 6. Partonový model
 Elementární částice 1. Leptony 2. Baryony 3. Bosony 4. Kvarkový model 5. Slabé interakce 6. Partonový model I.S. Hughes: Elementary Particles M. Leon: Particle Physics W.S.C. Williams Nuclear and Particle
Elementární částice 1. Leptony 2. Baryony 3. Bosony 4. Kvarkový model 5. Slabé interakce 6. Partonový model I.S. Hughes: Elementary Particles M. Leon: Particle Physics W.S.C. Williams Nuclear and Particle
1. 5 I N T E R A K C E A T O MŮ
 1. Atomová fyzika 99 1. 5 I N T E R A K C E A T O MŮ V této kapitole se dozvíte: jakými způsoby mezi sebou atomy interagují; za jakých podmínek vzniká mezi atomy chemická vazba; které základní metody kvantové
1. Atomová fyzika 99 1. 5 I N T E R A K C E A T O MŮ V této kapitole se dozvíte: jakými způsoby mezi sebou atomy interagují; za jakých podmínek vzniká mezi atomy chemická vazba; které základní metody kvantové
37 MOLEKULY. Molekuly s iontovou vazbou Molekuly s kovalentní vazbou Molekulová spektra
 445 37 MOLEKULY Molekuly s iontovou vazbou Molekuly s kovalentní vazbou Molekulová spektra Soustava stabilně vázaných atomů tvoří molekulu. Podle počtu atomů hovoříme o dvoj-, troj- a více atomových molekulách.
445 37 MOLEKULY Molekuly s iontovou vazbou Molekuly s kovalentní vazbou Molekulová spektra Soustava stabilně vázaných atomů tvoří molekulu. Podle počtu atomů hovoříme o dvoj-, troj- a více atomových molekulách.
Orbitaly, VSEPR 1 / 18
 rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment 1 / 18 Formální náboj Rozdíl mezi
rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment 1 / 18 Formální náboj Rozdíl mezi
Odhad parametrů N(µ, σ 2 )
 Odhad parametrů N(µ, σ 2 ) Mějme statistický soubor x 1, x 2,, x n modelovaný jako realizaci náhodného výběru z normálního rozdělení N(µ, σ 2 ) s neznámými parametry µ a σ. Jaký je maximální věrohodný
Odhad parametrů N(µ, σ 2 ) Mějme statistický soubor x 1, x 2,, x n modelovaný jako realizaci náhodného výběru z normálního rozdělení N(µ, σ 2 ) s neznámými parametry µ a σ. Jaký je maximální věrohodný
Korelační energie. Celkovou elektronovou energii molekuly lze experimentálně určit ze vztahu. E vib. = E at. = 39,856, E d
 Korelační energe Referenční stavy Energ molekul a atomů lze vyjádřt vzhledem k různým referenčním stavům. V kvantové mechance za referenční stav s nulovou energí bereme stav odpovídající nenteragujícím
Korelační energe Referenční stavy Energ molekul a atomů lze vyjádřt vzhledem k různým referenčním stavům. V kvantové mechance za referenční stav s nulovou energí bereme stav odpovídající nenteragujícím
2.6. Koncentrace elektronů a děr
 Obr. 2-11 Rozložení nosičů při poloze Fermiho hladiny: a) v horní polovině zakázaného pásu (p. typu N), b) uprostřed zakázaného pásu (vlastní p.), c) v dolní polovině zakázaného pásu (p. typu P) 2.6. Koncentrace
Obr. 2-11 Rozložení nosičů při poloze Fermiho hladiny: a) v horní polovině zakázaného pásu (p. typu N), b) uprostřed zakázaného pásu (vlastní p.), c) v dolní polovině zakázaného pásu (p. typu P) 2.6. Koncentrace
Dnešní látka: Literatura: Kapitoly 3 a 4 ze skript Karel Rektorys: Matematika 43, ČVUT, Praha, Text přednášky na webové stránce přednášejícího.
 Předmět: MA4 Dnešní látka: Od okrajových úloh v 1D k o. ú. ve 2D Laplaceův diferenciální operátor Variačně formulované okrajové úlohy pro parciální diferenciální rovnice a metody jejich přibližného řešení
Předmět: MA4 Dnešní látka: Od okrajových úloh v 1D k o. ú. ve 2D Laplaceův diferenciální operátor Variačně formulované okrajové úlohy pro parciální diferenciální rovnice a metody jejich přibližného řešení
Orbitaly, VSEPR. Zdeněk Moravec, 16. listopadu / 21
 rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment Zdeněk Moravec, http://z-moravec.net
rbitaly, VSEPR Rezonanční struktury, atomové a molekulové orbitaly, hybridizace, určování tvaru molekuly pomocí teorie VSEPR, úvod do symetrie molekul, dipólový moment Zdeněk Moravec, http://z-moravec.net
Interpolace, ortogonální polynomy, Gaussova kvadratura
 Interpolace, ortogonální polynomy, Gaussova kvadratura Petr Tichý 20. listopadu 2013 1 Úloha Lagrangeovy interpolace Dán omezený uzavřený interval [a, b] a v něm n + 1 různých bodů x 0, x 1,..., x n. Nechť
Interpolace, ortogonální polynomy, Gaussova kvadratura Petr Tichý 20. listopadu 2013 1 Úloha Lagrangeovy interpolace Dán omezený uzavřený interval [a, b] a v něm n + 1 různých bodů x 0, x 1,..., x n. Nechť
1 Projekce a projektory
 Cvičení 3 - zadání a řešení úloh Základy numerické matematiky - NMNM20 Verze z 5. října 208 Projekce a projektory Opakování ortogonální projekce Definice (Ortogonální projekce). Uvažujme V vektorový prostor
Cvičení 3 - zadání a řešení úloh Základy numerické matematiky - NMNM20 Verze z 5. října 208 Projekce a projektory Opakování ortogonální projekce Definice (Ortogonální projekce). Uvažujme V vektorový prostor
Vektorový prostor. Př.1. R 2 ; R 3 ; R n Dvě operace v R n : u + v = (u 1 + v 1,...u n + v n ), V (E 3 )...množina vektorů v E 3,
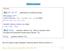 Vektorový prostor Příklady: Př.1. R 2 ; R 3 ; R n...aritmetický n-rozměrný prostor Dvě operace v R n : součet vektorů u = (u 1,...u n ) a v = (v 1,...v n ) je vektor u + v = (u 1 + v 1,...u n + v n ),
Vektorový prostor Příklady: Př.1. R 2 ; R 3 ; R n...aritmetický n-rozměrný prostor Dvě operace v R n : součet vektorů u = (u 1,...u n ) a v = (v 1,...v n ) je vektor u + v = (u 1 + v 1,...u n + v n ),
SPECIÁLNÍCH PRIMITIVNÍCH FUNKCÍ INTEGRACE RACIONÁLNÍCH FUNKCÍ
 VÝPOČET PEIÁLNÍH PRIMITIVNÍH FUNKÍ Obecně nelze zadat algoritmus, který by vždy vedl k výpočtu primitivní funkce. Nicméně eistují jisté třídy funkcí, pro které eistuje algoritmus, který vždy vede k výpočtu
VÝPOČET PEIÁLNÍH PRIMITIVNÍH FUNKÍ Obecně nelze zadat algoritmus, který by vždy vedl k výpočtu primitivní funkce. Nicméně eistují jisté třídy funkcí, pro které eistuje algoritmus, který vždy vede k výpočtu
Polynomy. Mgr. Veronika Švandová a Mgr. Zdeněk Kříž, Ph. D. 1.1 Teorie Zavedení polynomů Operace s polynomy...
 Polynomy Obsah Mgr. Veronika Švandová a Mgr. Zdeněk Kříž, Ph. D. 1 Základní vlastnosti polynomů 2 1.1 Teorie........................................... 2 1.1.1 Zavedení polynomů................................
Polynomy Obsah Mgr. Veronika Švandová a Mgr. Zdeněk Kříž, Ph. D. 1 Základní vlastnosti polynomů 2 1.1 Teorie........................................... 2 1.1.1 Zavedení polynomů................................
2. Schurova věta. Petr Tichý. 3. října 2012
 2. Schurova věta Petr Tichý 3. října 2012 1 Podobnostní transformace a výpočet vlastních čísel Obecný princip: Úloha: Řešíme-li matematickou úlohu, je často velmi vhodné hledat její ekvivalentní formulaci
2. Schurova věta Petr Tichý 3. října 2012 1 Podobnostní transformace a výpočet vlastních čísel Obecný princip: Úloha: Řešíme-li matematickou úlohu, je často velmi vhodné hledat její ekvivalentní formulaci
Nejdřív spočítáme jeden příklad na variaci konstant pro lineární diferenciální rovnici 2. řádu s kostantními koeficienty. y + y = 4 sin t.
 1 Variace konstanty Nejdřív spočítáme jeden příklad na variaci konstant pro lineární diferenciální rovnici 2. řádu s kostantními koeficienty. Příklad 1 Najděte obecné řešení rovnice: y + y = 4 sin t. Co
1 Variace konstanty Nejdřív spočítáme jeden příklad na variaci konstant pro lineární diferenciální rovnici 2. řádu s kostantními koeficienty. Příklad 1 Najděte obecné řešení rovnice: y + y = 4 sin t. Co
Dvojné a trojné integrály příklad 3. x 2 y dx dy,
 Spočtěte = { x, y) ; 4x + y 4 }. Dvojné a trojné integrály příklad 3 x y dx dy, Řešení: Protože obor integrace je symetrický vzhledem k ose x, tj. vzhledem k substituci [x; y] [x; y], a funkce fx, y) je
Spočtěte = { x, y) ; 4x + y 4 }. Dvojné a trojné integrály příklad 3 x y dx dy, Řešení: Protože obor integrace je symetrický vzhledem k ose x, tj. vzhledem k substituci [x; y] [x; y], a funkce fx, y) je
Teorie hybridizace. Vysvětluje vznik energeticky rovnocenných kovalentních vazeb a umožňuje předpovědět prostorový tvar molekul.
 Chemická vazba co je chemická vazba charakteristiky chemické vazby jak vzniká vazba znázornění chemické vazby kovalentní a koordinační vazba vazba σ a π jednoduchá, dvojná a trojná vazba polarita vazby
Chemická vazba co je chemická vazba charakteristiky chemické vazby jak vzniká vazba znázornění chemické vazby kovalentní a koordinační vazba vazba σ a π jednoduchá, dvojná a trojná vazba polarita vazby
ANALYTICKÁ GEOMETRIE V ROVINĚ
 ANALYTICKÁ GEOMETRIE V ROVINĚ Analytická geometrie vyšetřuje geometrické objekty (body, přímky, kuželosečky apod.) analytickými metodami. Podle prostoru, ve kterém pracujeme, můžeme analytickou geometrii
ANALYTICKÁ GEOMETRIE V ROVINĚ Analytická geometrie vyšetřuje geometrické objekty (body, přímky, kuželosečky apod.) analytickými metodami. Podle prostoru, ve kterém pracujeme, můžeme analytickou geometrii
Struktura elektronového obalu
 Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Struktura elektronového obalu Představy o modelu atomu se vyvíjely tak, jak se zdokonalovaly možnosti vědy
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Struktura elektronového obalu Představy o modelu atomu se vyvíjely tak, jak se zdokonalovaly možnosti vědy
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STROJNÍHO INŽENÝRSTVÍ
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STROJNÍHO INŽENÝRSTVÍ ÚSTAV MECHANIKY TĚLES, MECHATRONIKY A BIOMECHANIKY Komentovaný metodický list č. 1/4 Vytvořil: Ing. Oldřich Ševeček & Ing. Tomáš Profant, Ph.D.
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STROJNÍHO INŽENÝRSTVÍ ÚSTAV MECHANIKY TĚLES, MECHATRONIKY A BIOMECHANIKY Komentovaný metodický list č. 1/4 Vytvořil: Ing. Oldřich Ševeček & Ing. Tomáš Profant, Ph.D.
Lineární zobrazení. 1. A(x y) = A(x) A(y) (vlastnost aditivity) 2. A(α x) = α A(x) (vlastnost homogenity)
 4 Lineární zobrazení Definice: Nechť V a W jsou vektorové prostory Zobrazení A : V W (zobrazení z V do W nazýváme lineárním zobrazením, pokud pro všechna x V, y V a α R platí 1 A(x y = A(x A(y (vlastnost
4 Lineární zobrazení Definice: Nechť V a W jsou vektorové prostory Zobrazení A : V W (zobrazení z V do W nazýváme lineárním zobrazením, pokud pro všechna x V, y V a α R platí 1 A(x y = A(x A(y (vlastnost
Vazby v pevných látkách
 Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
Kvantová mechanika - model téměř volných elektronů. model těsné vazby
 Kvantová mechanika - model téměř volných elektronů model těsné vazby Částice (elektron) v periodickém potenciálu- Blochův teorém Dále už nebudeme považovat elektron za zcela volný (Sommerfeld), ale připustíme
Kvantová mechanika - model téměř volných elektronů model těsné vazby Částice (elektron) v periodickém potenciálu- Blochův teorém Dále už nebudeme považovat elektron za zcela volný (Sommerfeld), ale připustíme
Arnoldiho a Lanczosova metoda
 Arnoldiho a Lanczosova metoda 1 Částečný problém vlastních čísel Ne vždy je potřeba (a někdy to není ani technicky možné) nalézt celé spektrum dané matice (velké řídké matice). Úloze, ve které chceme aproximovat
Arnoldiho a Lanczosova metoda 1 Částečný problém vlastních čísel Ne vždy je potřeba (a někdy to není ani technicky možné) nalézt celé spektrum dané matice (velké řídké matice). Úloze, ve které chceme aproximovat
1 Mnohočleny a algebraické rovnice
 1 Mnohočleny a algebraické rovnice 1.1 Pojem mnohočlenu (polynomu) Připomeňme, že výrazům typu a 2 x 2 + a 1 x + a 0 říkáme kvadratický trojčlen, když a 2 0. Číslům a 0, a 1, a 2 říkáme koeficienty a písmenem
1 Mnohočleny a algebraické rovnice 1.1 Pojem mnohočlenu (polynomu) Připomeňme, že výrazům typu a 2 x 2 + a 1 x + a 0 říkáme kvadratický trojčlen, když a 2 0. Číslům a 0, a 1, a 2 říkáme koeficienty a písmenem
ELEKTRONOVÝ OBAL ATOMU. kladně nabitá hmota. elektron
 MODELY ATOMU ELEKTRONOVÝ OBAL ATOMU Na základě experimentálních výsledků byly vytvořeny různé teorie o struktuře atomu, tzv. modely atomu. Thomsonův model: Roku 1897 se jako první pokusil o popis stavby
MODELY ATOMU ELEKTRONOVÝ OBAL ATOMU Na základě experimentálních výsledků byly vytvořeny různé teorie o struktuře atomu, tzv. modely atomu. Thomsonův model: Roku 1897 se jako první pokusil o popis stavby
Otázku, kterými body prochází větev implicitní funkce řeší následující věta.
 1 Implicitní funkce Implicitní funkce nejsou funkce ve smyslu definice, že funkce bodu z definičního oboru D přiřadí právě jednu hodnotu z oboru hodnot H. Přesnější termín je funkce zadaná implicitně.
1 Implicitní funkce Implicitní funkce nejsou funkce ve smyslu definice, že funkce bodu z definičního oboru D přiřadí právě jednu hodnotu z oboru hodnot H. Přesnější termín je funkce zadaná implicitně.
3.2. ANALYTICKÁ GEOMETRIE ROVINY
 3.2. ANALYTICKÁ GEOMETRIE ROVINY V této kapitole se dozvíte: jak popsat rovinu v třídimenzionálním prostoru; jak analyzovat vzájemnou polohu bodu a roviny včetně jejich vzdálenosti; jak analyzovat vzájemnou
3.2. ANALYTICKÁ GEOMETRIE ROVINY V této kapitole se dozvíte: jak popsat rovinu v třídimenzionálním prostoru; jak analyzovat vzájemnou polohu bodu a roviny včetně jejich vzdálenosti; jak analyzovat vzájemnou
Čebyševovy aproximace
 Čebyševovy aproximace Čebyševova aproximace je tzv hledání nejlepší stejnoměrné aproximace funkce v daném intervalu Hledáme funkci h x, která v intervalu a,b minimalizuje maximální absolutní hodnotu rozdílu
Čebyševovy aproximace Čebyševova aproximace je tzv hledání nejlepší stejnoměrné aproximace funkce v daném intervalu Hledáme funkci h x, která v intervalu a,b minimalizuje maximální absolutní hodnotu rozdílu
Příklad 1: Komutační relace [d/dx, x] Příklad 2: Operátor B = i d/dx
![Příklad 1: Komutační relace [d/dx, x] Příklad 2: Operátor B = i d/dx Příklad 1: Komutační relace [d/dx, x] Příklad 2: Operátor B = i d/dx](/thumbs/91/106542832.jpg) 1 Příklad 1: Komutační relace [d/, x] Mějme na dva operátory: ˆ d/ a ˆ 5 D X x, například na prvek x působí takto Určeme jejich komutátor ˆ 5 d 5 4 ˆ 5 5 6 D x x 5 x, X x xx x ˆ ˆ ˆ ˆ ˆ ˆ d d [ DX, ] f
1 Příklad 1: Komutační relace [d/, x] Mějme na dva operátory: ˆ d/ a ˆ 5 D X x, například na prvek x působí takto Určeme jejich komutátor ˆ 5 d 5 4 ˆ 5 5 6 D x x 5 x, X x xx x ˆ ˆ ˆ ˆ ˆ ˆ d d [ DX, ] f
10. cvičení z Matematické analýzy 2
 . cvičení z Matematické analýzy 3. - 7. prosince 8. (dvojný integrál - Fubiniho věta Vhodným způsobem integrace spočítejte daný integrál a načrtněte oblast integrace (a (b (c y ds, kde : y & y 4. e ma{,y
. cvičení z Matematické analýzy 3. - 7. prosince 8. (dvojný integrál - Fubiniho věta Vhodným způsobem integrace spočítejte daný integrál a načrtněte oblast integrace (a (b (c y ds, kde : y & y 4. e ma{,y
přičemž předpokládáme A malé, U zahrnuje coulombické členy. Když roznásobíme závorku, p 2 reprezentuje kinetickou energii nabitých částic, člen
 Výběrová pravidla Absorpce/stim. emise Kde se výběrová pravidla vezmou? Použijeme semiklasické přiblížení, tzn. s nabitými částicemi (s indexy 1...N) zacházíme kvantově, s vnějším elektromagnetickým polem
Výběrová pravidla Absorpce/stim. emise Kde se výběrová pravidla vezmou? Použijeme semiklasické přiblížení, tzn. s nabitými částicemi (s indexy 1...N) zacházíme kvantově, s vnějším elektromagnetickým polem
ANALYTICKÁ GEOMETRIE LINEÁRNÍCH ÚTVARŮ V ROVINĚ
 ANALYTICKÁ GEOMETRIE LINEÁRNÍCH ÚTVARŮ V ROVINĚ Parametrické vyjádření přímky v rovině Máme přímku p v rovině určenou body A, B. Sestrojíme vektor u = B A. Pro bod B tím pádem platí: B = A + u. Je zřejmé,
ANALYTICKÁ GEOMETRIE LINEÁRNÍCH ÚTVARŮ V ROVINĚ Parametrické vyjádření přímky v rovině Máme přímku p v rovině určenou body A, B. Sestrojíme vektor u = B A. Pro bod B tím pádem platí: B = A + u. Je zřejmé,
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/
 Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Předmět: LRR/CHPB1/Chemie pro biology 1 Chemická vazba II Mgr. Karel Doležal Dr. Cíl přednášky: seznámit posluchače s principem
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Předmět: LRR/CHPB1/Chemie pro biology 1 Chemická vazba II Mgr. Karel Doležal Dr. Cíl přednášky: seznámit posluchače s principem
Atom vodíku. Klasicky nestabilní, pak jsme studovali v rámci staré kvantové mechaniky
 ATOMY + MOLEKULY Atom vodíku Klasicky nestabilní, pak jsme studovali v rámci staré kvantové mechaniky Teď úplně kvantově: --Bohrův model Hodnoty a vlastní stavy energie dostaneme z bezčasové Schrodingerovy
ATOMY + MOLEKULY Atom vodíku Klasicky nestabilní, pak jsme studovali v rámci staré kvantové mechaniky Teď úplně kvantově: --Bohrův model Hodnoty a vlastní stavy energie dostaneme z bezčasové Schrodingerovy
Lehký úvod do kvantové teorie II
 1 Lehký úvod do kvantové teorie II 5 Harmonický oscilátor Na příkladu harmonického oscilátoru, jehož klasické řešení známe z Fyziky 1, si ukážeme typické postupy při hledání vlastních hodnot operátoru
1 Lehký úvod do kvantové teorie II 5 Harmonický oscilátor Na příkladu harmonického oscilátoru, jehož klasické řešení známe z Fyziky 1, si ukážeme typické postupy při hledání vlastních hodnot operátoru
Úvod do lineární algebry
 Úvod do lineární algebry 1 Aritmetické vektory Definice 11 Mějme n N a utvořme kartézský součin R n R R R Každou uspořádanou n tici x 1 x 2 x, x n budeme nazývat n rozměrným aritmetickým vektorem Prvky
Úvod do lineární algebry 1 Aritmetické vektory Definice 11 Mějme n N a utvořme kartézský součin R n R R R Každou uspořádanou n tici x 1 x 2 x, x n budeme nazývat n rozměrným aritmetickým vektorem Prvky
VÍTEJTE V MIKROSVĚTĚ
 VÍTEJTE V MIKROSVĚTĚ Klasická vs. Moderní fyzika Klasická fyzika fyzika obyčejných věcí viditelných pouhým okem Moderní fyzika Relativita zabývá se tím co se pohybuje rychle nebo v silovém gravitačním
VÍTEJTE V MIKROSVĚTĚ Klasická vs. Moderní fyzika Klasická fyzika fyzika obyčejných věcí viditelných pouhým okem Moderní fyzika Relativita zabývá se tím co se pohybuje rychle nebo v silovém gravitačním
Požadavky k písemné přijímací zkoušce z matematiky do navazujícího magisterského studia pro neučitelské obory
 Požadavky k písemné přijímací zkoušce z matematiky do navazujícího magisterského studia pro neučitelské obory Zkouška ověřuje znalost základních pojmů, porozumění teorii a schopnost aplikovat teorii při
Požadavky k písemné přijímací zkoušce z matematiky do navazujícího magisterského studia pro neučitelské obory Zkouška ověřuje znalost základních pojmů, porozumění teorii a schopnost aplikovat teorii při
12 DYNAMIKA SOUSTAVY HMOTNÝCH BODŮ
 56 12 DYNAMIKA SOUSTAVY HMOTNÝCH BODŮ Těžiště I. impulsová věta - věta o pohybu těžiště II. impulsová věta Zákony zachování v izolované soustavě hmotných bodů Náhrada pohybu skutečných objektů pohybem
56 12 DYNAMIKA SOUSTAVY HMOTNÝCH BODŮ Těžiště I. impulsová věta - věta o pohybu těžiště II. impulsová věta Zákony zachování v izolované soustavě hmotných bodů Náhrada pohybu skutečných objektů pohybem
Oddělení pohybu elektronů a jader
 Oddělení pohybu elektronů a ader Adiabatická aproximace Born-Oppenheimerova aproximace Důležité vztahy sou 4, 5, 7, 0,,, udělal sem to zbytečně podrobně, e to samostatný okruh Separace translačního pohybu:
Oddělení pohybu elektronů a ader Adiabatická aproximace Born-Oppenheimerova aproximace Důležité vztahy sou 4, 5, 7, 0,,, udělal sem to zbytečně podrobně, e to samostatný okruh Separace translačního pohybu:
1 Analytická geometrie
 1 Analytická geometrie 11 Přímky Necht A E 3 a v R 3 je nenulový Pak p = A + v = {X E 3 X = A + tv, t R}, je přímka procházející bodem A se směrovým vektorem v Rovnici X = A + tv, t R, říkáme bodová rovnice
1 Analytická geometrie 11 Přímky Necht A E 3 a v R 3 je nenulový Pak p = A + v = {X E 3 X = A + tv, t R}, je přímka procházející bodem A se směrovým vektorem v Rovnici X = A + tv, t R, říkáme bodová rovnice
Odhady - Sdružené rozdělení pravděpodobnosti
 Odhady - Sdružené rozdělení pravděpodobnosti 4. listopadu 203 Kdybych chtěl znát maximum informací o náhodné veličině, musel bych znát všechny hodnoty, které mohou padnout, a jejich pravděpodobnosti. Tedy
Odhady - Sdružené rozdělení pravděpodobnosti 4. listopadu 203 Kdybych chtěl znát maximum informací o náhodné veličině, musel bych znát všechny hodnoty, které mohou padnout, a jejich pravděpodobnosti. Tedy
Aproximace posuvů [ N ],[G] Pro každý prvek se musí nalézt vztahy
![Aproximace posuvů [ N ],[G] Pro každý prvek se musí nalézt vztahy Aproximace posuvů [ N ],[G] Pro každý prvek se musí nalézt vztahy](/thumbs/97/130835283.jpg) Aproimace posuvů Pro každý prvek se musí nalézt vztahy kde jsou prozatím neznámé transformační matice. Neznámé funkce posuvů se obvykle aproimují ve formě mnohočlenů kartézských souřadnic. Například 1.
Aproimace posuvů Pro každý prvek se musí nalézt vztahy kde jsou prozatím neznámé transformační matice. Neznámé funkce posuvů se obvykle aproimují ve formě mnohočlenů kartézských souřadnic. Například 1.
Odhad parametrů N(µ, σ 2 )
 Odhad parametrů N(µ, σ 2 ) Mějme statistický soubor x 1, x 2,, x n modelovaný jako realizaci náhodného výběru z normálního rozdělení N(µ, σ 2 ) s neznámými parametry µ a σ. Jaký je maximální věrohodný
Odhad parametrů N(µ, σ 2 ) Mějme statistický soubor x 1, x 2,, x n modelovaný jako realizaci náhodného výběru z normálního rozdělení N(µ, σ 2 ) s neznámými parametry µ a σ. Jaký je maximální věrohodný
Vlastní čísla a vlastní vektory
 5 Vlastní čísla a vlastní vektor Poznámka: Je-li A : V V lineární zobrazení z prostoru V do prostoru V někd se takové zobrazení nazývá lineárním operátorem, pak je přirozeným požadavkem najít takovou bázi
5 Vlastní čísla a vlastní vektor Poznámka: Je-li A : V V lineární zobrazení z prostoru V do prostoru V někd se takové zobrazení nazývá lineárním operátorem, pak je přirozeným požadavkem najít takovou bázi
1 Polynomiální interpolace
 Polynomiální interpolace. Metoda neurčitých koeficientů Příklad.. Nalezněte polynom p co nejmenšího stupně, pro který platí p() = 0, p(2) =, p( ) = 6. Řešení. Polynom hledáme metodou neurčitých koeficientů,
Polynomiální interpolace. Metoda neurčitých koeficientů Příklad.. Nalezněte polynom p co nejmenšího stupně, pro který platí p() = 0, p(2) =, p( ) = 6. Řešení. Polynom hledáme metodou neurčitých koeficientů,
Řešíme tedy soustavu dvou rovnic o dvou neznámých. 2a + b = 3, 6a + b = 27,
 Přijímací řízení 2015/16 Přírodovědecká fakulta Ostravská univerzita v Ostravě Navazující magisterské studium, obor Aplikovaná matematika (1. červen 2016) Příklad 1 Určete taková a, b R, aby funkce f()
Přijímací řízení 2015/16 Přírodovědecká fakulta Ostravská univerzita v Ostravě Navazující magisterské studium, obor Aplikovaná matematika (1. červen 2016) Příklad 1 Určete taková a, b R, aby funkce f()
Teorie náhodných matic aneb tak trochu jiná statistika
 Teorie náhodných matic aneb tak trochu jiná statistika B. Vlková 1, M.Berg 2, B. Martínek 3, O. Švec 4, M. Neumann 5 Gymnázium Uničov 1, Gymnázium Václava Hraběte Hořovice 2, Mendelovo gymnázium Opava
Teorie náhodných matic aneb tak trochu jiná statistika B. Vlková 1, M.Berg 2, B. Martínek 3, O. Švec 4, M. Neumann 5 Gymnázium Uničov 1, Gymnázium Václava Hraběte Hořovice 2, Mendelovo gymnázium Opava
15 Fourierova transformace v hypersférických souřadnicích
 15 HYPERSFÉRICKÉ SOUŘADNICE 1 15 Fourierova transformace v hypersférických souřadnicích 151 Definice hypersférických souřadnic r, ϑ N,, ϑ 1, ϕ v E N Hypersférické souřadnice souvisejí s kartézskými souřadnicemi
15 HYPERSFÉRICKÉ SOUŘADNICE 1 15 Fourierova transformace v hypersférických souřadnicích 151 Definice hypersférických souřadnic r, ϑ N,, ϑ 1, ϕ v E N Hypersférické souřadnice souvisejí s kartézskými souřadnicemi
Dnešní látka Variačně formulované okrajové úlohy zúplnění prostoru funkcí. Lineární zobrazení.
 Předmět: MA4 Dnešní látka Variačně formulované okrajové úlohy zúplnění prostoru funkcí. Lineární zobrazení. Literatura: Kapitola 2 a)-c) a kapitola 4 a)-c) ze skript Karel Rektorys: Matematika 43, ČVUT,
Předmět: MA4 Dnešní látka Variačně formulované okrajové úlohy zúplnění prostoru funkcí. Lineární zobrazení. Literatura: Kapitola 2 a)-c) a kapitola 4 a)-c) ze skript Karel Rektorys: Matematika 43, ČVUT,
Matematika (CŽV Kadaň) aneb Úvod do lineární algebry Matice a soustavy rovnic
 Přednáška třetí (a pravděpodobně i čtvrtá) aneb Úvod do lineární algebry Matice a soustavy rovnic Lineární rovnice o 2 neznámých Lineární rovnice o 2 neznámých Lineární rovnice o dvou neznámých x, y je
Přednáška třetí (a pravděpodobně i čtvrtá) aneb Úvod do lineární algebry Matice a soustavy rovnic Lineární rovnice o 2 neznámých Lineární rovnice o 2 neznámých Lineární rovnice o dvou neznámých x, y je
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno
 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno 1 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno Struktura
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno 1 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno Struktura
Opakování: shrnutí základních poznatků o struktuře atomu
 11. Polovodiče Polovodiče jsou krystalické nebo amorfní látky, jejichž elektrická vodivost leží mezi elektrickou vodivostí kovů a izolantů a závisí na teplotě nebo dopadajícím optickém záření. Elektrické
11. Polovodiče Polovodiče jsou krystalické nebo amorfní látky, jejichž elektrická vodivost leží mezi elektrickou vodivostí kovů a izolantů a závisí na teplotě nebo dopadajícím optickém záření. Elektrické
