c) příjemcem osoba, která obdržela transfuzi krve nebo krevních
|
|
|
- Andrea Tomanová
- před 6 lety
- Počet zobrazení:
Transkript
1 L 256/32 Úřední věstník Evropské unie SMĚRNICE KOMISE 2005/61/ES ze dne 30. září 2005, kterou se provádí směrnice Evropského parlamentu a Rady 2002/98/ES, pokud jde o požadavky na sledovatelnost a oznamování závažných nežádoucích reakcí a událostí (Text s významem pro EHP) KOMISE EVROPSKÝCH SPOLEČENSTVÍ, s ohledem na Smlouvu o založení Evropského společenství, kterou se provádí směrnice Evropského parlamentu a Rady 2002/98/ES, pokud jde o některé technické požadavky na krev a krevní složky ( 4 ), a některá doporučení Rady Evropy. s ohledem na směrnici Evropského parlamentu a Rady 2002/98/ES ze dne 27. ledna 2003, kterou se stanoví standardy jakosti a bezpečnosti pro odběr, vyšetření, zpracování, skladování a distribuci lidské krve a krevních složek a kterou se mění směrnice 2001/83/ES ( 1 ), a zejména na čl. 29 odst. 2 písm. a) a i) uvedené směrnice, vzhledem k těmto důvodům: (5) Krev a krevní složky dovážené ze třetích zemí, a to i krev a krevní složky používané jako výchozí materiál nebo surovina pro výrobu léčivých přípravků z lidské krve a z lidské plazmy určených pro distribuci ve Společenství, by tedy měly splňovat rovnocenné standardy Společenství a specifikace Společenství týkající se sledovatelnosti a požadavků na oznamování závažných nežádoucích reakcí a závažných nežádoucích událostí stanovených v této směrnici. (1) Směrnice 2002/98/ES stanoví standardy jakosti a bezpečnosti pro odběr a vyšetření lidské krve a krevních složek bez ohledu na jejich zamýšlený účel, a pro zpracování, skladování a distribuci, pokud jsou určeny pro transfuzi, aby byla zajištěna vysoká úroveň ochrany lidského zdraví. (2) Aby se předcházelo přenosu onemocnění krví a krevními složkami a aby se zajistila rovnocenná úroveň jakosti a bezpečnosti, vyzývá směrnice 2002/98/ES k vytvoření specifických technických požadavků týkajících se sledovatelnosti, postupu Společenství pro oznamování závažných nežádoucích reakcí a závažných nežádoucích událostí a oznamovacího formuláře. (6) Je nezbytné stanovit společné definice pro odbornou terminologii, aby se zajistilo konsistentní provedení směrnice 2002/98/ES. (7) Opatření této směrnice jsou v souladu se stanoviskem výboru zřízeného směrnicí 2002/98/ES, PŘIJALA TUTO SMĚRNICI: Článek 1 (3) Oznamování podezření na závažné nežádoucí reakce nebo závažné nežádoucí události je třeba podávat příslušnému orgánu ihned po jeho zjištění. Tato směrnice proto stanoví oznamovací formulář s vymezením potřebných minimálních údajů, aniž je dotčena způsobilost členského státu ponechat si nebo zavést na svém území přísnější ochranná opatření, která jsou v souladu s ustanoveními Smlouvy podle čl. 4. odst. 2 směrnice 2002/98/ES. (4) Tato směrnice stanoví uvedené technické požadavky, přičemž se zohledňuje doporučení Rady 98/463/ES ze dne 29. června 1998 o vhodnosti dárců krve a krevní plazmy a vyšetřování darované krve v Evropském společenství ( 2 ), směrnice Evropského parlamentu a Rady 2001/83/ES ze dne 6. listopadu 2001 o kodexu Společenství týkajícím se humánních léčivých přípravků ( 3 ), směrnice Komise 2004/33/ES ze dne 22. března 2004, Definice Pro účely této směrnice se rozumí: a) sledovatelností schopnost vysledovat každou jednotlivou jednotku krve nebo krevní složky z ní získané od dárce po její konečné určení, bez ohledu na to, zda jde o příjemce, výrobce léčivých přípravků nebo o znehodnocení, a naopak; b) oznamujícím zařízením transfuzní zařízení, nemocniční krevní banka nebo zařízení, kde se provádí transfuze, které oznamuje závažné nežádoucí reakce a/nebo závažné nežádoucí události příslušnému orgánu; c) příjemcem osoba, která obdržela transfuzi krve nebo krevních složek; ( 1 )Úř. věst. L 33, , s. 30. ( 2 )Úř. věst. L 203, , s. 14. ( 3 )Úř. věst. L 311, , s. 67. Směrnice naposledy pozměněná směrnicí 2004/27/ES (Úř. věst. L 136, , s. 34). ( 4 )Úř. věst. L 91, , s. 25.
2 Úřední věstník Evropské unie L 256/33 d) vydáním poskytnutí krve nebo krevní složky transfuzním zařízením nebo krevní bankou nemocnice příjemci pro transfuzi; e) přisuzovatelností pravděpodobnost, že závažná nežádoucí reakce u příjemce může být připsána krvi nebo krevní složce z transfuze nebo že závažná nežádoucí reakce u dárce může být připsána procesu darování; f) zařízeními nemocnice, kliniky, výrobci a biologicko-zdravotnické výzkumné ústavy, kterým může být dodávána krev nebo krevní složky. vhodném a čitelném nosiči alespoň po dobu 30 let, aby se zajistila sledovatelnost. Článek 5 Oznamování závažných nežádoucích reakcí 1. Členské státy zajistí, aby zařízení, kde dochází ke transfuzi, měla zavedené postupy pro evidenci transfuzí a pro neprodlené oznamování transfuzním zařízením veškeré závažné nežádoucí reakce pozorované u příjemců během transfuze nebo po transfuzi, které je možno přisoudit jakosti nebo bezpečnosti krve nebo krevních složek. Článek 2 Sledovatelnost 1. Členské státy zajistí sledovatelnost krve a krevních složek prostřednictvím přesných identifikačních postupů, udržování záznamů a vhodného systému označování. 2. Členské státy zajistí, aby oznamující zařízení měla zavedené postupy pro oznamování příslušnému orgánu ihned, jakmile se je dozví, veškerých relevantních informací o podezřeních na závažné nežádoucí reakce. Používají se k tomu oznamovací formuláře stanovené v části A a části C přílohy II. 2. Členské státy zajistí, aby systém sledovatelnosti zavedený v transfuzním zařízení umožňoval vysledování krevních složek k jejich umístění a etapě zpracování. 3. Členské státy zajistí, aby každé transfuzní zařízení mělo zavedený systém pro jednoznačnou identifikaci každého dárce, každé odebrané jednotky krve a každé připravené krevní složky bez ohledu na její zamýšlené určení, jakož i zařízení, kterým byla dotyčná krevní složka dodána. 4. Členské státy zajistí, aby všechna zařízení měla zavedený systém evidence každé přijaté jednotky krve nebo krevní složky, ať byla zpracována na místě či nikoliv, a konečného určení této přijaté jednotky, ať se jedná o transfuzi, odstranění nebo vrácení distribuujícímu transfuznímu zařízení. 5. Členské státy zajistí, aby každé transfuzní zařízení mělo jedinečný identifikační kód, který umožní, aby bylo přesně spojeno s každou jednotkou krve, kterou odebralo, a s každou krevní složkou, kterou připravilo. 3. Členské státy zajistí, aby oznamující zařízení: a) oznamovala příslušnému orgánu veškeré relevantní informace o závažných nežádoucích reakcích stupně přisuzovatelnosti 2 nebo 3 ve smyslu části B přílohy II, jež lze přisoudit jakosti a bezpečnosti krve a krevních složek; b) oznamovala příslušnému orgánu každý případ přenosu infekčního agens krví nebo krevními složkami, jakmile se o něm dozví; c) popisovala opatření učiněná ohledně ostatních dotčených krevních složek, které byly distribuovány pro transfuzi nebo pro použití jako plazma pro frakcionaci; d) hodnotila podezření na závažné nežádoucí reakce podle stupňů přisuzovatelnosti stanovených v části B přílohy II; Článek 3 Postup ověřování při vydávání krve nebo krevních složek Členské státy zajistí, aby transfuzní zařízení nebo nemocniční krevní banky měly při vydávání jednotek krve nebo krevních složek k transfuzi zavedený postup ověřování toho, že každá vydaná jednotka byla použita k transfuzi pro zamýšleného příjemce nebo, pokud nebyla použita k transfuzi, toho, jak s ní bylo následně naloženo. Článek 4 Evidence údajů o sledovatelnosti Členské státy zajistí, aby transfuzní zařízení, nemocniční krevní banky nebo zařízení uchovávaly údaje stanovené v příloze I na e) po uzavření šetření vyplnila oznámení o závažné nežádoucí reakci za použití formuláře v části C přílohy II; f) každoročně předkládala úplnou zprávu o závažných nežádoucích reakcích příslušnému orgánu za použití formuláře v části D přílohy II. Článek 6 Oznamování závažných nežádoucích událostí 1. Členské státy zajistí, aby transfuzní zařízení a nemocniční krevní banky měly zavedeny postupy pro evidenci všech závažných nežádoucích událostí, jimiž může být dotčena jakost nebo bezpečnost krve a krevních složek.
3 L 256/34 Úřední věstník Evropské unie Členské státy zajistí, aby oznamující zařízení měla zavedeny postupy pro oznamování za pomoci oznamovacího formuláře stanoveného v části A přílohy III příslušnému orgánu ihned, jakmile se je dozví, veškerých relevantních informací o závažných nežádoucích událostech, jež mohou ohrozit jiné dárce nebo příjemce kromě osob přímo zúčastněných na dotyčné události. 3. Členské státy zajistí, aby oznamující zařízení: a) hodnotila závažné nežádoucí události tak, aby identifikovala v procesu příčiny, jimž lze předejít; b) po uzavření šetření podala oznámení o závažné nežádoucí události za použití formuláře v části B přílohy III; c) každoročně předkládala úplnou zprávu o závažných nežádoucích událostech příslušnému orgánu za použití formuláře v části C přílohy III. Článek 7 Požadavky na dovezenou krev a dovezené krevní složky 1. Členské státy zajistí, aby při dovozu krve a krevních složek z transfuzních zařízení ze třetích zemí byl zaveden systém sledovatelnosti rovnocenný systému stanovenému v čl. 2 odst. 2 až Členské státy zajistí, aby pro dovoz krve a krevních složek z transfuzních zařízení ze třetích zemí byl zaveden systém oznamování rovnocenný systému stanovenému v článcích 5 a6. Článek 8 Výroční zprávy Členské státy předkládají Komisi do 30. června následujícího roku výroční zprávu o oznámení závažných nežádoucích reakcí a událostí, které obdržel příslušný orgán, za použití formulářů v části D přílohy II a části C přílohy III. Článek 9 Sdělování informací mezi příslušnými orgány Členské státy zajistí, aby si jejich příslušné orgány navzájem sdělovaly veškeré relevantní informace ohledně závažných nežádoucích reakcí a závažných nežádoucích událostí s cílem zaručit, aby krev nebo krevní složky, o nichž je známo, že jsou vadné, nebo u nichž je podezření, že jsou vadné, byly staženy z používání a odstraněny. Článek 10 Provedení 1. Aniž je dotčen článek 7 směrnice 2002/98/ES, uvedou členské státy v účinnost právní a správní předpisy nezbytné pro dosažení souladu s touto směrnicí nejpozději do 31. srpna Neprodleně sdělí Komisi znění těchto předpisů a srovnávací tabulku mezi ustanoveními těchto předpisů a této směrnice. Tyto předpisy přijaté členskými státy musí obsahovat odkaz na tuto směrnici nebo musí být takový odkaz učiněn při jejich úředním vyhlášení. Způsob odkazu si stanoví členské státy. 2. Členské státy sdělí Komisi znění hlavních ustanovení vnitrostátních právních předpisů, které přijmou v oblasti působnosti této směrnice. Článek 11 Vstup v platnost Tato směrnice vstupuje v platnost dvacátým dnem po vyhlášení v Úředním věstníku Evropské unie. Článek 12 Určení Tato směrnice je určena členským státům. V Bruselu dne 30. září Za Komisi Markos KYPRIANOU člen Komise
4 Úřední věstník Evropské unie L 256/35 PŘÍLOHA I Evidence údajů o sledovatelnosti podle článku 4 TRANSFUZNÍ ZAŘÍZENÍ ZAZNAMENÁVAJÍ TYTO ÚDAJE: 1. Identifikace transfuzního zařízení 2. Identifikace dárce krve 3. Identifikace jednotky krve 4. Identifikace jednotlivé krevní složky 5. Datum odběru (rok/měsíc/den) 6. Zařízení, do kterých se distribuují jednotky krve nebo krevní složky, nebo následné nakládání s nimi ZAŘÍZENÍ ZAZNAMENÁVAJÍ TYTO ÚDAJE: 1. Identifikace dodavatele krevní složky 2. Identifikace vydané krevní složky 3. Identifikace příjemce transfuze 4. U jednotek krve, které nebyly použity k transfuzi, potvrzení o následném naložení s nimi 5. Datum transfuze nebo jiného naložení s jednotkami (rok/měsíc/den) 6. Případné číslo šarže složky
5 L 256/36 Úřední věstník Evropské unie PŘÍLOHA II OZNAMOVÁNÍ ZÁVAŽNÝCH NEŽÁDOUCÍCH REAKCÍ ČÁST A Formulář pro rychlé oznámení podezření na závažné nežádoucí reakce Identifikace oznámení Datum oznámení (rok/měsíc/den) Datum transfuze (rok/měsíc/den) Věk a pohlaví příjemce Datum závažné nežádoucí reakce (rok/měsíc/den) Závažná nežádoucí reakce se týká: plné krve erytrocytů trombocytů plazmy ostatních (specifikujte) Druh závažných nežádoucích reakcí: imunitní hemolýza kvůli neslučitelnosti ABO imunitní hemolýza kvůli jiné alloprotilátce hemolýza z jiných než imunitních příčin bakteriální infekce přenesená transfuzí anafylaxe/hypersensitivita akutní poškození plic v souvislosti s transfuzí virová infekce přenesená transfuzí (HBV) virová infekce přenesená transfuzí (HCV) virová infekce přenesená transfuzí (HIV-1/2) virová infekce přenesená transfuzí, ostatní (specifikujte) parazitická infekce přenesená transfuzí (malárie) parazitická infekce přenesená transfuzí, ostatní (specifikujte) potransfuzní purpura nemoc z reakce štěpu proti hostiteli ostatní závažné reakce (specifikujte) Stupeň přisuzovatelnosti (NP, 0-3)
6 Úřední věstník Evropské unie L 256/37 ČÁST B Závažné nežádoucí reakce stupně přisuzovatelnosti Stupně přisuzovatelnosti pro vyhodnocení závažných nežádoucích reakcí Stupeň přisuzovatelnosti Vysvětlení NP Nelze posoudit Pokud nejsou k dispozici dostatečné údaje pro posouzení přisuzovatelnosti. 0 Vyloučena Pokud existují přesvědčivé důkazy mimo rozumnou pochybnost, že nežádoucí reakce vyplývá z jiných příčin. Nepravděpodobná Pokud důkazy jasně nasvědčují tomu, že nežádoucí reakce vyplývá z jiných příčin než z krve nebo z krevních složek. 1 Možná Pokud neexistují jasné důkazy nasvědčující tomu, že nežádoucí reakce vyplývá z krve či z krevních složek, anebo z jiných příčin. 2 Pravděpodobná Pokud důkazy jasně nasvědčují tomu, že nežádoucí reakce vyplývá z krve nebo z krevní složky. 3 Jistá Pokud existují přesvědčivé důkazy mimo rozumnou pochybnost, že nežádoucí reakce vyplývá z krve nebo krevní složky. ČÁST C Formulář pro potvrzení závažných nežádoucích reakcí Identifikace oznámení Datum potvrzení (rok/měsíc/den) Datum závažné nežádoucí reakce (rok/měsíc/den) Potvrzení závažné nežádoucí reakce (ano/ne) Stupeň přisuzovatelnosti (NP, 0-3) Změna druhu závažné nežádoucí reakce (ano/ne) Pokud ano, specifikujte Klinický závěr (pokud je znám): úplné uzdravení lehké následky závažné následky úmrtí
7 L 256/38 Úřední věstník Evropské unie ČÁST D Formulář pro výroční oznamování závažných nežádoucích reakcí Oznamovací období Tato tabulka se týká: [ ] plné krve [ ] erytrocytů [ ] trombocytů [ ] plazmy [ ] ostatních (použijte samostatnou tabulku pro každou složku) Počet vydaných jednotek (celkový počet vydaných jednotek s daným počtem krevních složek) Počet příjemců, kteří obdrželi transfuzi (celkový počet příjemců, kteří obdrželi transfuzi daného počtu krevních složek) (pokud je k dispozici) Počet jednotek podaných transfuzí (celkový počet krevních složek (jednotek) podaných transfuzí v oznamovacím období) (pokud je k dispozici) Celkový oznámený počet Počet úmrtí Počet závažných nežádoucích reakcí se stupněm přisuzovatelnosti 0 až 3 po potvrzení (viz příloha IIA) Nelze posoudit stupeň 0 stupeň 1 stupeň 2 stupeň 3 Imunitní hemolýza kvůli neslučitelnosti ABO kvůli jiné alloprotilátce Hemolýza z jiných než imunitních příčin Bakteriální infekce přenesená transfuzí Anafylaxe/hypersensitivita Akutní poškození plic v souvislosti s transfuzí Virová infekce přenesená transfuzí Parazitická infekce přenesená transfuzí (malárie) HBV HCV HIV-1/2 Ostatní (specifikujte) Malárie Ostatní (specifikujte)
8 Úřední věstník Evropské unie L 256/39 Potransfuzní purpura Nemoc z reakce štěpu proti hostiteli Ostatní závažné reakce (specifikujte)
9 L 256/40 Úřední věstník Evropské unie PŘÍLOHA III OZNAMOVÁNÍ ZÁVAŽNÝCH NEŽÁDOUCÍCH UDÁLOSTÍ ČÁST A Formulář pro rychlé oznámení závažných nežádoucích událostí Identifikace oznámení Datum oznámení (rok/měsíc/den) Datum závažné nežádoucí události (rok/měsíc/den) Závažná nežádoucí událost, kterou může být dotčena jakost a bezpečnost krevní složky kvůli odchylce v souvislosti s: Závada přípravku Selhání zařízení Specifikace Chyba člověka Ostatní (specifikujte) odběrem plné krve aferezou vyšetřením darované krve zpracováním skladováním distribucí materiály ostatní (specifikujte) ČÁST B Formulář pro potvrzení závažných nežádoucích událostí Identifikace oznámení Datum potvrzení (rok/měsíc/den) Datum nežádoucí události (rok/měsíc/den) Analýza základní příčiny (bližší údaje) Učiněná opatření k nápravě (bližší údaje) ČÁST C Formulář pro výroční oznámení závažných nežádoucích událostí Oznamovací období 1. ledna 31. prosince (rok) Celkový počet zpracovaných jednotek krve a zpracovaných krevních složek: Závažná nežádoucí událost, kterou je dotčena jakost a bezpečnost krevní složky kvůli odchylce v souvislosti s: odběrem plné krve aferezou vyšetřením darované krve zpracováním skladováním distribucí materiály ostatní (specifikujte) Celkový počet Závada přípravku Selhání zařízení Specifikace Chyba člověka Ostatní (specifikujte)
Návod k vyplnění výročních zpráv o závažných nežádoucích reakcích a závažných nežádoucích událostech:
 Návod k vyplnění výročních zpráv o závažných nežádoucích reakcích a závažných nežádoucích událostech: Prázdné tabulky (vzory) z vyhlášky 143/2008 Sb. jsou k dispozici na webových stránkách SÚKLu: http://www.sukl.cz/zdravotnicka-zarizeni/formulare
Návod k vyplnění výročních zpráv o závažných nežádoucích reakcích a závažných nežádoucích událostech: Prázdné tabulky (vzory) z vyhlášky 143/2008 Sb. jsou k dispozici na webových stránkách SÚKLu: http://www.sukl.cz/zdravotnicka-zarizeni/formulare
Roční výkaz o činnosti ZZ A (MZ) 1-01
 Ministerstvo zdravotnictví Schváleno ČSÚ pro Ministerstvo zdravotnictví. ČV 177/10 ze dne 20.10.2009 v rámci Programu statistických zjišťování na rok 2010. Vyplněný výkaz laskavě předložte pracovišti státní
Ministerstvo zdravotnictví Schváleno ČSÚ pro Ministerstvo zdravotnictví. ČV 177/10 ze dne 20.10.2009 v rámci Programu statistických zjišťování na rok 2010. Vyplněný výkaz laskavě předložte pracovišti státní
Roční výkaz o činnosti poskytovatele ZS A (MZ) 1-01
 Ministerstvo zdravotnictví Schváleno ČSÚ pro Ministerstvo zdravotnictví. ČV 126/14 ze dne 30.10.2013 v rámci Programu statistických zjišťování na rok 2014. Vyplněný výkaz předložte pracovišti státní statistické
Ministerstvo zdravotnictví Schváleno ČSÚ pro Ministerstvo zdravotnictví. ČV 126/14 ze dne 30.10.2013 v rámci Programu statistických zjišťování na rok 2014. Vyplněný výkaz předložte pracovišti státní statistické
SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2002/98/ES
 SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2002/98/ES ze dne 27. ledna 2003, kterou se stanoví standardy jakosti a bezpečnosti pro odběr, vyšetření, zpracování, skladování a distribuci lidské krve a krevních
SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2002/98/ES ze dne 27. ledna 2003, kterou se stanoví standardy jakosti a bezpečnosti pro odběr, vyšetření, zpracování, skladování a distribuci lidské krve a krevních
SDĚLENÍ KOMISE RADĚ, EVROPSKÉMU PARLAMENTU, EVROPSKÉMU HOSPODÁŘSKÉMU A SOCIÁLNÍMU VÝBORU A VÝBORU REGIONŮ
 EVROPSKÁ KOMISE V Bruselu dne 19.1.2010 KOM(2010)3 v konečném znění SDĚLENÍ KOMISE RADĚ, EVROPSKÉMU PARLAMENTU, EVROPSKÉMU HOSPODÁŘSKÉMU A SOCIÁLNÍMU VÝBORU A VÝBORU REGIONŮ o provádění směrnice 2002/98/ES,
EVROPSKÁ KOMISE V Bruselu dne 19.1.2010 KOM(2010)3 v konečném znění SDĚLENÍ KOMISE RADĚ, EVROPSKÉMU PARLAMENTU, EVROPSKÉMU HOSPODÁŘSKÉMU A SOCIÁLNÍMU VÝBORU A VÝBORU REGIONŮ o provádění směrnice 2002/98/ES,
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU)
 18.12.2015 L 332/19 NAŘÍZENÍ PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2015/2378 ze dne 15. prosince 2015, kterým se stanoví prováděcí pravidla k některým ustanovením směrnice Rady 2011/16/EU o správní spolupráci
18.12.2015 L 332/19 NAŘÍZENÍ PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2015/2378 ze dne 15. prosince 2015, kterým se stanoví prováděcí pravidla k některým ustanovením směrnice Rady 2011/16/EU o správní spolupráci
Směrnice 2000/25/ES se mění takto: 1. V článku 1 se doplňuje nová odrážka, která zní: 2. V článku 3 se doplňuje nový odstavec, který zní:
 1.3.2005 Úřední věstník Evropské unie L 55/35 SMĚRNICE KOMISE 2005/13/ES ze dne 21. února 2005, kterou se mění směrnice Evropského parlamentu a Rady 2000/25/ES týkající se emisí plynných znečišťujících
1.3.2005 Úřední věstník Evropské unie L 55/35 SMĚRNICE KOMISE 2005/13/ES ze dne 21. února 2005, kterou se mění směrnice Evropského parlamentu a Rady 2000/25/ES týkající se emisí plynných znečišťujících
Návrh SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY
 EVROPSKÁ KOMISE V Bruselu dne 5.3.2012 COM(2012) 90 final 2012/0040 (COD) C7-0061/12 Návrh SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY kterou se mění směrnice Rady 92/65/EHS, pokud jde o veterinární předpisy
EVROPSKÁ KOMISE V Bruselu dne 5.3.2012 COM(2012) 90 final 2012/0040 (COD) C7-0061/12 Návrh SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY kterou se mění směrnice Rady 92/65/EHS, pokud jde o veterinární předpisy
SMĚRNICE. (Text s významem pro EHP)
 L 238/44 SMĚRNICE SMĚRNICE KOMISE (EU) 2017/1572 ze dne 15. září 2017, kterou se doplňuje směrnice Evropského parlamentu a Rady 2001/83/ES, pokud jde o zásady a pokyny pro správnou výrobní praxi pro humánní
L 238/44 SMĚRNICE SMĚRNICE KOMISE (EU) 2017/1572 ze dne 15. září 2017, kterou se doplňuje směrnice Evropského parlamentu a Rady 2001/83/ES, pokud jde o zásady a pokyny pro správnou výrobní praxi pro humánní
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne
 EVROPSKÁ KOMISE V Bruselu dne 12.2.2019 C(2019) 873 final PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne 12.2.2019 o vzorech ES prohlášení a certifikátů pro železniční prvky interoperability a subsystémy,
EVROPSKÁ KOMISE V Bruselu dne 12.2.2019 C(2019) 873 final PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne 12.2.2019 o vzorech ES prohlášení a certifikátů pro železniční prvky interoperability a subsystémy,
EVROPSKÁ KOMISE. V Bruselu dne 23.6.2011 KOM(2011) 377 v konečném znění 2011/0164 (NLE) Návrh SMĚRNICE RADY
 EVROPSKÁ KOMISE V Bruselu dne 23.6.2011 KOM(2011) 377 v konečném znění 2011/0164 (NLE) Návrh SMĚRNICE RADY kterou se mění směrnice 76/768/EHS týkající se kosmetických prostředků za účelem přizpůsobení
EVROPSKÁ KOMISE V Bruselu dne 23.6.2011 KOM(2011) 377 v konečném znění 2011/0164 (NLE) Návrh SMĚRNICE RADY kterou se mění směrnice 76/768/EHS týkající se kosmetických prostředků za účelem přizpůsobení
členským státům stanovit zkrácení lhůty pro podání Nařízení Komise (ES) č. 1564/2005 ze dne 7. září 2005, ( 1 ) Úř. věst. L 395, 30.12.1989, s. 33.
 CS 28.11.2009 Úřední věstník Evropské unie L 313/3 NAŘÍZENÍ KOMISE (ES) č. 1150/2009 ze dne 10. listopadu 2009, kterým se mění nařízení (ES) č. 1564/2005, pokud jde o standardní formuláře pro zveřejňování
CS 28.11.2009 Úřední věstník Evropské unie L 313/3 NAŘÍZENÍ KOMISE (ES) č. 1150/2009 ze dne 10. listopadu 2009, kterým se mění nařízení (ES) č. 1564/2005, pokud jde o standardní formuláře pro zveřejňování
RADA EVROPSKÉ UNIE. Brusel 17. ledna 2012 (OR. en) 5403/12 ENV 17 ENT 7
 RADA EVROPSKÉ UNIE Brusel 17. ledna 2012 (OR. en) 5403/12 ENV 17 ENT 7 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 12. ledna 2012 Příjemce: Generální sekretariát Rady Evropské unie Č.
RADA EVROPSKÉ UNIE Brusel 17. ledna 2012 (OR. en) 5403/12 ENV 17 ENT 7 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 12. ledna 2012 Příjemce: Generální sekretariát Rady Evropské unie Č.
Návrh SMĚRNICE RADY,
 EVROPSKÁ KOMISE V Bruselu dne 15.7.2010 KOM(2010)381 v konečném znění 2010/0205 (CNS) Návrh SMĚRNICE RADY, kterou se mění Směrnice 2008/9/ES, kterou se stanoví prováděcí pravidla pro vrácení daně z přidané
EVROPSKÁ KOMISE V Bruselu dne 15.7.2010 KOM(2010)381 v konečném znění 2010/0205 (CNS) Návrh SMĚRNICE RADY, kterou se mění Směrnice 2008/9/ES, kterou se stanoví prováděcí pravidla pro vrácení daně z přidané
2. Evropský parlament a Evropský hospodářský a sociální výbor vydaly svá stanoviska dne 24. dubna 2009 a dne 14. května 2009.
 RADA EVROPSKÉ UNIE Brusel 28. května 2009 (02.06) (OR. en) Interinstitucionální spis: 2008/0228 (CNS) 10430/09 FISC 77 POZNÁMKA K BODU I/A Odesílatel: Generální sekretariát Příjemce: COREPER/Rada Předmět:
RADA EVROPSKÉ UNIE Brusel 28. května 2009 (02.06) (OR. en) Interinstitucionální spis: 2008/0228 (CNS) 10430/09 FISC 77 POZNÁMKA K BODU I/A Odesílatel: Generální sekretariát Příjemce: COREPER/Rada Předmět:
(Text s významem pro EHP) (5) Riziko pro zdraví zvířat, které cirkusy či poutě představují,
 22.10.2005 Úřední věstník Evropské unie L 279/47 NAŘÍZENÍ KOMISE (ES) č. 1739/2005 ze dne 21. října 2005, kterým se stanoví veterinární požadavky na přesun cirkusových zvířat mezi členskými státy (Text
22.10.2005 Úřední věstník Evropské unie L 279/47 NAŘÍZENÍ KOMISE (ES) č. 1739/2005 ze dne 21. října 2005, kterým se stanoví veterinární požadavky na přesun cirkusových zvířat mezi členskými státy (Text
Rada Evropské unie Brusel 17. prosince 2014 (OR. en)
 Rada Evropské unie Brusel 17. prosince 2014 (OR. en) Interinstitucionální spis: 2013/0400 (CNS) 16633/14 FISC 228 ECOFIN 1179 PRÁVNÍ PŘEDPISY A JINÉ AKTY Předmět: SMĚRNICE RADY, kterou se mění směrnice
Rada Evropské unie Brusel 17. prosince 2014 (OR. en) Interinstitucionální spis: 2013/0400 (CNS) 16633/14 FISC 228 ECOFIN 1179 PRÁVNÍ PŘEDPISY A JINÉ AKTY Předmět: SMĚRNICE RADY, kterou se mění směrnice
KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY
 Požadavky na vstupní materiál lidské tkáně a buňky 1 KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY MUDr. Ivana Koblihová Inspektor lidských tkání a buněk Požadavky na vstupní
Požadavky na vstupní materiál lidské tkáně a buňky 1 KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY MUDr. Ivana Koblihová Inspektor lidských tkání a buněk Požadavky na vstupní
Veterinární předpisy pro obchod se psy, kočkami a fretkami ***I
 P7_TA-PROV(2013)0221 Veterinární předpisy pro obchod se psy, kočkami a fretkami ***I Legislativní usnesení Evropského parlamentu ze dne 23. května 2013 o návrhu směrnice Evropského parlamentu a Rady, kterou
P7_TA-PROV(2013)0221 Veterinární předpisy pro obchod se psy, kočkami a fretkami ***I Legislativní usnesení Evropského parlamentu ze dne 23. května 2013 o návrhu směrnice Evropského parlamentu a Rady, kterou
ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne ,
 EVROPSKÁ KOMISE V Bruselu dne 14.3.2019 C(2019) 2029 final ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne 14.3.2019, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 305/2011, pokud
EVROPSKÁ KOMISE V Bruselu dne 14.3.2019 C(2019) 2029 final ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne 14.3.2019, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 305/2011, pokud
1992L0080 CS 27.02.2010 004.001 1
 1992L0080 CS 27.02.2010 004.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B SMĚRNICE RADY 92/80/EHS ze dne 19. října 1992 o sbližování
1992L0080 CS 27.02.2010 004.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B SMĚRNICE RADY 92/80/EHS ze dne 19. října 1992 o sbližování
Úřední věstník Evropské unie. (Nelegislativní akty) NAŘÍZENÍ
 4.1.2017 L 1/1 II (Nelegislativní akty) NAŘÍZENÍ PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2017/1 ze dne 3. ledna 2017 o postupech identifikace plavidel podle směrnice Evropského parlamentu a Rady 2013/53/EU o rekreačních
4.1.2017 L 1/1 II (Nelegislativní akty) NAŘÍZENÍ PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2017/1 ze dne 3. ledna 2017 o postupech identifikace plavidel podle směrnice Evropského parlamentu a Rady 2013/53/EU o rekreačních
2006R2023 CS
 2006R2023 CS 17.04.2008 001.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ KOMISE (ES) č. 2023/2006 ze dne 22. prosince
2006R2023 CS 17.04.2008 001.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ KOMISE (ES) č. 2023/2006 ze dne 22. prosince
SMĚRNICE. (Text s významem pro EHP) PŘIJALA TUTO SMĚRNICI: Příloha III směrnice 2006/22/ES se nahrazuje zněním přílohy této směrnice.
 31.1.2009 Úřední věstník Evropské unie L 29/45 SMĚRNICE SMĚRNICE KOMISE 2009/5/ES ze dne 30. ledna 2009, kterou se mění příloha III směrnice Evropského parlamentu a Rady 2006/22/ES o minimálních podmínkách
31.1.2009 Úřední věstník Evropské unie L 29/45 SMĚRNICE SMĚRNICE KOMISE 2009/5/ES ze dne 30. ledna 2009, kterou se mění příloha III směrnice Evropského parlamentu a Rady 2006/22/ES o minimálních podmínkách
SMĚRNICE RADY. ze dne 25. června 1987,
 SMĚRNICE RADY ze dne 25. června 1987, kterou se mění určité směrnice o sbližování právních předpisů členských států vztahujících se na průmyslové výrobky, pokud se týká rozlišovacích čísel a písmen označujících
SMĚRNICE RADY ze dne 25. června 1987, kterou se mění určité směrnice o sbližování právních předpisů členských států vztahujících se na průmyslové výrobky, pokud se týká rozlišovacích čísel a písmen označujících
NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) /... ze dne ,
 EVROPSKÁ KOMISE V Bruselu dne 4.9.2017 C(2017) 5467 final NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) /... ze dne 4.9.2017, kterým se stanoví vědecká kritéria pro určení vlastností vyvolávajících narušení
EVROPSKÁ KOMISE V Bruselu dne 4.9.2017 C(2017) 5467 final NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) /... ze dne 4.9.2017, kterým se stanoví vědecká kritéria pro určení vlastností vyvolávajících narušení
(Nelegislativní akty) NAŘÍZENÍ
 16.10.2015 L 271/1 II (Nelegislativní akty) NAŘÍZENÍ PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2015/1850 ze dne 13. října 2015, kterým se stanoví prováděcí pravidla k nařízení Evropského parlamentu a Rady (ES) č.
16.10.2015 L 271/1 II (Nelegislativní akty) NAŘÍZENÍ PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2015/1850 ze dne 13. října 2015, kterým se stanoví prováděcí pravidla k nařízení Evropského parlamentu a Rady (ES) č.
SMĚRNICE KOMISE 2003/94/ES. ze dne 8. října 2003,
 SMĚRNICE KOMISE 2003/94/ES ze dne 8. října 2003, kterou se stanoví zásady a pokyny pro správnou výrobní praxi pro humánní léčivé přípravky a hodnocené humánní léčivé přípravky (Text s významem pro EHP)
SMĚRNICE KOMISE 2003/94/ES ze dne 8. října 2003, kterou se stanoví zásady a pokyny pro správnou výrobní praxi pro humánní léčivé přípravky a hodnocené humánní léčivé přípravky (Text s významem pro EHP)
Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah
 2013R1337 CS 17.12.2013 000.002 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 1337/2013 ze dne 13.
2013R1337 CS 17.12.2013 000.002 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 1337/2013 ze dne 13.
SMĚRNICE RADY 1999/22/ES. ze dne 29. března o chovu volně žijících živočichů v zoologických zahradách
 SMĚRNICE RADY 1999/22/ES ze dne 29. března 1999 o chovu volně žijících živočichů v zoologických zahradách RADA EVROPSKÉ UNIE, s ohledem na Smlouvu o založení Evropského společenství, a zejména na čl. 130s
SMĚRNICE RADY 1999/22/ES ze dne 29. března 1999 o chovu volně žijících živočichů v zoologických zahradách RADA EVROPSKÉ UNIE, s ohledem na Smlouvu o založení Evropského společenství, a zejména na čl. 130s
L 320/8 Úřední věstník Evropské unie 17.11.2012
 L 320/8 Úřední věstník Evropské unie 17.11.2012 NAŘÍZENÍ KOMISE (EU) č. 1078/2012 ze dne 16. listopadu 2012 o společné bezpečnostní metodě sledování, kterou mají používat železniční podniky, provozovatelé
L 320/8 Úřední věstník Evropské unie 17.11.2012 NAŘÍZENÍ KOMISE (EU) č. 1078/2012 ze dne 16. listopadu 2012 o společné bezpečnostní metodě sledování, kterou mají používat železniční podniky, provozovatelé
(Legislativní akty) NAŘÍZENÍ
 29.12.2017 L 348/1 I (Legislativní akty) NAŘÍZENÍ NAŘÍZENÍ RADY (EU) 2017/2454 ze dne 5. prosince 2017, kterým se mění nařízení Rady (EU) č. 904/2010 o správní spolupráci a boji proti podvodům v oblasti
29.12.2017 L 348/1 I (Legislativní akty) NAŘÍZENÍ NAŘÍZENÍ RADY (EU) 2017/2454 ze dne 5. prosince 2017, kterým se mění nařízení Rady (EU) č. 904/2010 o správní spolupráci a boji proti podvodům v oblasti
Delegace naleznou v příloze dokument D039870/02.
 Rada Evropské unie Brusel 30. července 2015 (OR. en) 11290/15 MAR 81 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 27. července 2015 Příjemce: Předmět: Generální sekretariát Rady SMĚRNICE
Rada Evropské unie Brusel 30. července 2015 (OR. en) 11290/15 MAR 81 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 27. července 2015 Příjemce: Předmět: Generální sekretariát Rady SMĚRNICE
L 65/22 Úřední věstník Evropské unie
 L 65/22 Úřední věstník Evropské unie 7.3.2006 SMĚRNICE KOMISE 2006/26/ES ze dne 2. března 2006, kterou se mění směrnice Rady 74/151/EHS, 77/311/EHS, 78/933/EHS a 89/173/EHS o kolových zemědělských a lesnických
L 65/22 Úřední věstník Evropské unie 7.3.2006 SMĚRNICE KOMISE 2006/26/ES ze dne 2. března 2006, kterou se mění směrnice Rady 74/151/EHS, 77/311/EHS, 78/933/EHS a 89/173/EHS o kolových zemědělských a lesnických
Prováděcí nařízení Komise (EU) č. 607/2012 ze dne 6. července 2012 o prováděcích pravidlech pro systém náležité péče a pro četnost
 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 607/2012 ze dne 6. července 2012 o prováděcích pravidlech pro systém náležité péče a pro četnost a povahu kontrol kontrolních organizací podle nařízení Evropského parlamentu
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 607/2012 ze dne 6. července 2012 o prováděcích pravidlech pro systém náležité péče a pro četnost a povahu kontrol kontrolních organizací podle nařízení Evropského parlamentu
SMĚRNICE. (Text s významem pro EHP) (kodifikované znění) (4) Spotřebitelé však mají být informováni o používání takových
 L 27/12 Úřední věstník Evropské unie 31.1.2008 SMĚRNICE SMĚRNICE KOMISE 2008/5/ES ze dne 30. ledna 2008 o povinném uvádění jiných údajů, než jsou údaje stanovené ve směrnici Evropského parlamentu a Rady
L 27/12 Úřední věstník Evropské unie 31.1.2008 SMĚRNICE SMĚRNICE KOMISE 2008/5/ES ze dne 30. ledna 2008 o povinném uvádění jiných údajů, než jsou údaje stanovené ve směrnici Evropského parlamentu a Rady
SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 1999/4/ES ze dne 22. února 1999 o kávových a cikorkových extraktech. (Úř. věst. L 66, , s.
 1999L0004 CS 18.11.2013 003.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 1999/4/ES ze dne
1999L0004 CS 18.11.2013 003.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 1999/4/ES ze dne
L 302/28 Úřední věstník Evropské unie
 L 302/28 Úřední věstník Evropské unie 19.11.2005 NAŘÍZENÍ KOMISE (ES) č. 1895/2005 ze dne 18. listopadu 2005 o omezení použití některých epoxyderivátů v materiálech a předmětech určených pro styk s potravinami
L 302/28 Úřední věstník Evropské unie 19.11.2005 NAŘÍZENÍ KOMISE (ES) č. 1895/2005 ze dne 18. listopadu 2005 o omezení použití některých epoxyderivátů v materiálech a předmětech určených pro styk s potravinami
302 Úřední věstník Evropské unie ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ
 302 Úřední věstník Evropské unie 32000D0571 L 240/14 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 23.9.2000 ROZHODNUTÍ KOMISE ze dne 8. září 2000, kterým se stanoví metody veterinárních kontrol produktů ze třetích
302 Úřední věstník Evropské unie 32000D0571 L 240/14 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 23.9.2000 ROZHODNUTÍ KOMISE ze dne 8. září 2000, kterým se stanoví metody veterinárních kontrol produktů ze třetích
Návrh SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY
 EVROPSKÁ KOMISE V Bruselu dne 11.11.2011 KOM(2011) 710 v konečném znění 2011/0327 (COD) C7-0400/11 Návrh SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY kterou se mění směrnice Evropského parlamentu a Rady 2006/126/ES,
EVROPSKÁ KOMISE V Bruselu dne 11.11.2011 KOM(2011) 710 v konečném znění 2011/0327 (COD) C7-0400/11 Návrh SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY kterou se mění směrnice Evropského parlamentu a Rady 2006/126/ES,
Úřední věstník Evropské unie
 Úřední věstník Evropské unie L 1 České vydání Právní předpisy Ročník 60 4. ledna 2017 Obsah II Nelegislativní akty NAŘÍZENÍ Prováděcí nařízení Komise (EU) 2017/1 ze dne 3. ledna 2017 o postupech identifikace
Úřední věstník Evropské unie L 1 České vydání Právní předpisy Ročník 60 4. ledna 2017 Obsah II Nelegislativní akty NAŘÍZENÍ Prováděcí nařízení Komise (EU) 2017/1 ze dne 3. ledna 2017 o postupech identifikace
RADA EVROPSKÉ UNIE. Brusel, 25. února 2005 (OR. en) 6558/05 AGRI 52 PHYTOSAN 8 OC 92
 RADA EVROPSKÉ UNIE Brusel, 25. února 2005 (OR. en) 6558/05 AGRI 52 PHYTOSAN 8 OC 92 PRÁVNÍ PŘEDPISY A JINÉ AKTY Předmět : Směrnice Rady, kterou se mění příloha IV směrnice 2000/29/ES o ochranných opatřeních
RADA EVROPSKÉ UNIE Brusel, 25. února 2005 (OR. en) 6558/05 AGRI 52 PHYTOSAN 8 OC 92 PRÁVNÍ PŘEDPISY A JINÉ AKTY Předmět : Směrnice Rady, kterou se mění příloha IV směrnice 2000/29/ES o ochranných opatřeních
Zákon o lidských tkáních a buňkách
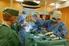 [ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Zákon o lidských tkáních a buňkách 296/2008 Sb. o zajištění jakosti a bezpečnosti lidských tkání a buněk určených k použití u člověka a o změně souvisejících
[ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Zákon o lidských tkáních a buňkách 296/2008 Sb. o zajištění jakosti a bezpečnosti lidských tkání a buněk určených k použití u člověka a o změně souvisejících
ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne
 EVROPSKÁ KOMISE V Bruselu dne 19.2.2018 C(2018) 884 final ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne 19.2.2018 o systémech posuzování a ověřování stálosti vlastností použitelných na sendvičové
EVROPSKÁ KOMISE V Bruselu dne 19.2.2018 C(2018) 884 final ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne 19.2.2018 o systémech posuzování a ověřování stálosti vlastností použitelných na sendvičové
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU)
 24.11.2012 Úřední věstník Evropské unie L 326/3 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 1097/2012 ze dne 23. listopadu 2012, kterým se mění, pokud jde o odesílání vedlejších produktů živočišného původu a získaných
24.11.2012 Úřední věstník Evropské unie L 326/3 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 1097/2012 ze dne 23. listopadu 2012, kterým se mění, pokud jde o odesílání vedlejších produktů živočišného původu a získaných
s ohledem na Smlouvu o fungování Evropské unie, a zejména na čl. 127 odst. 6 a článek 132 této smlouvy,
 L 314/66 1.12.2015 ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2015/2218 ze dne 20. listopadu 2015 o postupu při vyloučení předpokladu, že zaměstnanci mají podstatný vliv na rizikový profil dohlížené úvěrové
L 314/66 1.12.2015 ROZHODNUTÍ EVROPSKÉ CENTRÁLNÍ BANKY (EU) 2015/2218 ze dne 20. listopadu 2015 o postupu při vyloučení předpokladu, že zaměstnanci mají podstatný vliv na rizikový profil dohlížené úvěrové
Rada Evropské unie Brusel 10. června 2016 (OR. en)
 Rada Evropské unie Brusel 10. června 2016 (OR. en) Interinstitucionální spis: 2012/0102 (CNS) 8741/16 FISC 70 ECOFIN 378 PRÁVNÍ PŘEDPISY A JINÉ AKTY Předmět: SMĚRNICE RADY, kterou se mění směrnice 2006/112/ES,
Rada Evropské unie Brusel 10. června 2016 (OR. en) Interinstitucionální spis: 2012/0102 (CNS) 8741/16 FISC 70 ECOFIN 378 PRÁVNÍ PŘEDPISY A JINÉ AKTY Předmět: SMĚRNICE RADY, kterou se mění směrnice 2006/112/ES,
Úřední věstník Evropské unie L 320/13
 6.12.2007 Úřední věstník Evropské unie L 320/13 NAŘÍZENÍ KOMISE (ES) č. 1432/2007 ze dne 5. prosince 2007, kterým se mění přílohy I, II a VI nařízení Evropského parlamentu a Rady (ES) č. 1774/2002, pokud
6.12.2007 Úřední věstník Evropské unie L 320/13 NAŘÍZENÍ KOMISE (ES) č. 1432/2007 ze dne 5. prosince 2007, kterým se mění přílohy I, II a VI nařízení Evropského parlamentu a Rady (ES) č. 1774/2002, pokud
1999L0004 CS SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 1999/4/ES ze dne 22. února 1999 o kávových a cikorkových extraktech
 1999L0004 CS 11.12.2008 002.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 1999/4/ES ze dne
1999L0004 CS 11.12.2008 002.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 1999/4/ES ze dne
KOMISE EVROPSKÝCH SPOLEČENSTVÍ. Návrh SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY
 CS CS CS KOMISE EVROPSKÝCH SPOLEČENSTVÍ V Bruselu dne 22.12.2006 KOM(2006) 916 v konečném znění 2006/0300 (COD) Návrh SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY kterou se mění směrnice 2002/87/ES o doplňkovém
CS CS CS KOMISE EVROPSKÝCH SPOLEČENSTVÍ V Bruselu dne 22.12.2006 KOM(2006) 916 v konečném znění 2006/0300 (COD) Návrh SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY kterou se mění směrnice 2002/87/ES o doplňkovém
Návrh NAŘÍZENÍ RADY,
 Ref. Ares(2018)2964154-06/06/2018 EVROPSKÁ KOMISE V Bruselu dne 31.5.2018 COM(2018) 371 final 2018/0219 (APP) Návrh NAŘÍZENÍ RADY, kterým se rozšiřuje použitelnost nařízení (EU) č..../2018, kterým se zavádí
Ref. Ares(2018)2964154-06/06/2018 EVROPSKÁ KOMISE V Bruselu dne 31.5.2018 COM(2018) 371 final 2018/0219 (APP) Návrh NAŘÍZENÍ RADY, kterým se rozšiřuje použitelnost nařízení (EU) č..../2018, kterým se zavádí
(Text s významem pro EHP)
 13.2.2019 L 42/9 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2019/250 ze dne 12. února 2019 o vzorech ES prohlášení a certifikátů pro železniční prvky interoperability a subsystémy, o vzoru prohlášení o shodě s povoleným
13.2.2019 L 42/9 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2019/250 ze dne 12. února 2019 o vzorech ES prohlášení a certifikátů pro železniční prvky interoperability a subsystémy, o vzoru prohlášení o shodě s povoleným
KOMISE EVROPSKÝCH SPOLEČENSTVÍ. Předloha. NAŘÍZENÍ KOMISE (ES) č. /2005. ze dne [ ],
![KOMISE EVROPSKÝCH SPOLEČENSTVÍ. Předloha. NAŘÍZENÍ KOMISE (ES) č. /2005. ze dne [ ], KOMISE EVROPSKÝCH SPOLEČENSTVÍ. Předloha. NAŘÍZENÍ KOMISE (ES) č. /2005. ze dne [ ],](/thumbs/88/116648783.jpg) KOMISE EVROPSKÝCH SPOLEČENSTVÍ V Bruselu dne 13. července 2005. Předloha NAŘÍZENÍ KOMISE (ES) č. /2005 ze dne [ ], kterým se stanoví prováděcí pravidla k nařízení Rady (ES) č. 2494/95, pokud jde o společné
KOMISE EVROPSKÝCH SPOLEČENSTVÍ V Bruselu dne 13. července 2005. Předloha NAŘÍZENÍ KOMISE (ES) č. /2005 ze dne [ ], kterým se stanoví prováděcí pravidla k nařízení Rady (ES) č. 2494/95, pokud jde o společné
(Text s významem pro EHP)
 L 96/26 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2016/561 ze dne 11. dubna 2016, kterým se mění příloha IV prováděcího nařízení (EU) č. 577/2013, pokud jde o vzorové veterinární osvědčení pro neobchodní přesuny
L 96/26 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2016/561 ze dne 11. dubna 2016, kterým se mění příloha IV prováděcího nařízení (EU) č. 577/2013, pokud jde o vzorové veterinární osvědčení pro neobchodní přesuny
SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2002/74/ES. ze dne 23. září 2002,
 SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2002/74/ES ze dne 23. září 2002, kterou se mění směrnice Rady 80/987/EHS o sbližování právních předpisů členských států týkajících se ochrany zaměstnanců v případě
SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2002/74/ES ze dne 23. září 2002, kterou se mění směrnice Rady 80/987/EHS o sbližování právních předpisů členských států týkajících se ochrany zaměstnanců v případě
SMĚRNICE KOMISE 2006/86/ES
 L 294/32 Úřední věstník Evropské unie 25.10.2006 SMĚRNICE KOMISE 2006/86/ES ze dne 24. října 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o požadavky na sledovatelnost,
L 294/32 Úřední věstník Evropské unie 25.10.2006 SMĚRNICE KOMISE 2006/86/ES ze dne 24. října 2006, kterou se provádí směrnice Evropského parlamentu a Rady 2004/23/ES, pokud jde o požadavky na sledovatelnost,
RADA EVROPSKÉ UNIE. Brusel 9. března 2007 (21.03) (OR. en) 7207/07 Interinstitucionální spis: 2007/0035 (COD) DRS 18 COMPET 70 CODEC 202 NÁVRH
 RADA EVROPSKÉ UNIE Brusel 9. března 2007 (21.03) (OR. en) 7207/07 Interinstitucionální spis: 2007/0035 (COD) DRS 18 COMPET 70 CODEC 202 NÁVRH Odesílatel: Evropská komise Ze dne: 7. března 2007 Předmět:
RADA EVROPSKÉ UNIE Brusel 9. března 2007 (21.03) (OR. en) 7207/07 Interinstitucionální spis: 2007/0035 (COD) DRS 18 COMPET 70 CODEC 202 NÁVRH Odesílatel: Evropská komise Ze dne: 7. března 2007 Předmět:
Revidovaný překlad právního předpisu Evropských společenství. NAŘÍZENÍ RADY (ES) č. 150/2003. ze dne 21. ledna 2003
 NAŘÍZENÍ RADY (ES) č. 150/2003 ze dne 21. ledna 2003 o pozastavení dovozního cla pro některé zbraně a vojenskou výzbroj RADA EVROPSKÉ UNIE, s ohledem na Smlouvu o založení Evropského společenství, a zejména
NAŘÍZENÍ RADY (ES) č. 150/2003 ze dne 21. ledna 2003 o pozastavení dovozního cla pro některé zbraně a vojenskou výzbroj RADA EVROPSKÉ UNIE, s ohledem na Smlouvu o založení Evropského společenství, a zejména
DOPORUČENÍ. DOPORUČENÍ KOMISE ze dne 24. září 2013 o auditech a posouzeních prováděných oznámenými subjekty v oblasti zdravotnických prostředků
 25.9.2013 Úřední věstník Evropské unie L 253/27 DOPORUČENÍ DOPORUČENÍ KOMISE ze dne 24. září 2013 o auditech a posouzeních prováděných oznámenými subjekty v oblasti zdravotnických prostředků (Text s významem
25.9.2013 Úřední věstník Evropské unie L 253/27 DOPORUČENÍ DOPORUČENÍ KOMISE ze dne 24. září 2013 o auditech a posouzeních prováděných oznámenými subjekty v oblasti zdravotnických prostředků (Text s významem
Delegace naleznou v příloze dokument D033542/02.
 Rada Evropské unie Brusel 14. července 2014 (OR. en) 11888/14 ENV 672 ENT 161 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 11. července 2014 Příjemce: Č. dok. Komise: D033542/02 Předmět:
Rada Evropské unie Brusel 14. července 2014 (OR. en) 11888/14 ENV 672 ENT 161 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 11. července 2014 Příjemce: Č. dok. Komise: D033542/02 Předmět:
NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU)
 19.6.2014 L 179/17 NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 664/2014 ze dne 18. prosince 2013, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 1151/2012, pokud jde o stanovení symbolů
19.6.2014 L 179/17 NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 664/2014 ze dne 18. prosince 2013, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 1151/2012, pokud jde o stanovení symbolů
B NAŘÍZENÍ KOMISE (EU) č. 211/2013 ze dne 11. března 2013 o požadavcích na osvědčení pro dovoz klíčků a semen určených k produkci klíčků do Unie
 2013R0211 CS 16.07.2014 001.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ KOMISE (EU) č. 211/2013 ze dne 11. března 2013
2013R0211 CS 16.07.2014 001.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B NAŘÍZENÍ KOMISE (EU) č. 211/2013 ze dne 11. března 2013
SMĚRNICE KOMISE V PŘENESENÉ PRAVOMOCI / /EU. ze dne 30.1.2015,
 EVROPSKÁ KOMISE V Bruselu dne 30.1.2015 C(2015) 328 final SMĚRNICE KOMISE V PŘENESENÉ PRAVOMOCI / /EU ze dne 30.1.2015, kterou se pro účely přizpůsobení technickému pokroku mění příloha IV směrnice Evropského
EVROPSKÁ KOMISE V Bruselu dne 30.1.2015 C(2015) 328 final SMĚRNICE KOMISE V PŘENESENÉ PRAVOMOCI / /EU ze dne 30.1.2015, kterou se pro účely přizpůsobení technickému pokroku mění příloha IV směrnice Evropského
POŽADAVKY PLYNOUCÍ ZE SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2014/30/EU
 POŽADAVKY PLYNOUCÍ ZE SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2014/30/EU (revize textu k 1. 5. 2014) Dodávání na trh a uvádění do provozu (článek 4 směrnice) Členské státy přijmou veškerá vhodná opatření,
POŽADAVKY PLYNOUCÍ ZE SMĚRNICE EVROPSKÉHO PARLAMENTU A RADY 2014/30/EU (revize textu k 1. 5. 2014) Dodávání na trh a uvádění do provozu (článek 4 směrnice) Členské státy přijmou veškerá vhodná opatření,
(1) Je třeba stanovit podrobnosti systému registračních čísel evropských politických stran a evropských politických nadací.
 L 318/28 4.12.2015 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2015/2246 ze dne 3. prosince 2015, kterým se stanoví podrobná pravidla týkající se systému registračních čísel používaného pro rejstřík evropských politických
L 318/28 4.12.2015 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2015/2246 ze dne 3. prosince 2015, kterým se stanoví podrobná pravidla týkající se systému registračních čísel používaného pro rejstřík evropských politických
EVROPSKÁ UNIE EVROPSKÝ PARLAMENT
 EVROPSKÁ UNIE EVROPSKÝ PARLAMENT RADA Brusel 8. srpna 2008 (OR. en) 2006/0146(COD) PE-CONS 3627/08 CODIF 54 TRANS 128 CODEC 521 PRÁVNÍ PŘEDPISY A JINÉ AKTY Předmět: NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY
EVROPSKÁ UNIE EVROPSKÝ PARLAMENT RADA Brusel 8. srpna 2008 (OR. en) 2006/0146(COD) PE-CONS 3627/08 CODIF 54 TRANS 128 CODEC 521 PRÁVNÍ PŘEDPISY A JINÉ AKTY Předmět: NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY
(Akty, jejichž zveřejnění není povinné) KOMISE
 L 86/6 Úřední věstník Evropské unie 5.4.2005 II (Akty, jejichž zveřejnění není povinné) KOMISE ROZHODNUTÍ KOMISE ze dne 22. března 2005, kterým se stanoví formáty vztahující se k databázovému systému podle
L 86/6 Úřední věstník Evropské unie 5.4.2005 II (Akty, jejichž zveřejnění není povinné) KOMISE ROZHODNUTÍ KOMISE ze dne 22. března 2005, kterým se stanoví formáty vztahující se k databázovému systému podle
Systém řízení kvality, SVP a výroba TP
 Systém řízení kvality, SVP a výroba TP Pacasová R. Transfuzní a tkáňové oddělení FN Brno LF MU bakalářské studium Zdravotní laborant, 2015 Legislativa ZTS - EU Výrobu transfuzních přípravků v Evropě (EU)
Systém řízení kvality, SVP a výroba TP Pacasová R. Transfuzní a tkáňové oddělení FN Brno LF MU bakalářské studium Zdravotní laborant, 2015 Legislativa ZTS - EU Výrobu transfuzních přípravků v Evropě (EU)
RADA EVROPSKÉ UNIE. Brusel 27. července 2011 (OR. en) 13263/11 CONSOM 133
 RADA EVROPSKÉ UNIE Brusel 27. července 2011 (OR. en) 13263/11 CONSOM 133 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 25. července 2011 Příjemce: Generální sekretariát Rady Č. dok. Komise:
RADA EVROPSKÉ UNIE Brusel 27. července 2011 (OR. en) 13263/11 CONSOM 133 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 25. července 2011 Příjemce: Generální sekretariát Rady Č. dok. Komise:
Žádosti členských států o aktualizaci seznamu Společenství
 L 84/8 Úřední věstník Evropské unie 23.3.2006 NAŘÍZENÍ KOMISE (ES) č. 473/2006 ze dne 22. března 2006, kterým se stanoví prováděcí pravidla pro seznam Společenství uvádějící letecké dopravce, kteří podléhají
L 84/8 Úřední věstník Evropské unie 23.3.2006 NAŘÍZENÍ KOMISE (ES) č. 473/2006 ze dne 22. března 2006, kterým se stanoví prováděcí pravidla pro seznam Společenství uvádějící letecké dopravce, kteří podléhají
2006L0008 CS 13.02.2006 000.001 1
 2006L0008 CS 13.02.2006 000.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B SMĚRNICE KOMISE 2006/8/ES ze dne 23. ledna 2006, kterou
2006L0008 CS 13.02.2006 000.001 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B SMĚRNICE KOMISE 2006/8/ES ze dne 23. ledna 2006, kterou
B PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU)
 02013R1352 CS 15.05.2018 001.001 1 Tento dokument slouží výhradně k informačním účelům a nemá žádný právní účinek. Orgány a instituce Evropské unie nenesou za jeho obsah žádnou odpovědnost. Závazná znění
02013R1352 CS 15.05.2018 001.001 1 Tento dokument slouží výhradně k informačním účelům a nemá žádný právní účinek. Orgány a instituce Evropské unie nenesou za jeho obsah žádnou odpovědnost. Závazná znění
Návrh. NAŘÍZENÍ KOMISE (ES) č. /.. ze dne [ ]
![Návrh. NAŘÍZENÍ KOMISE (ES) č. /.. ze dne [ ] Návrh. NAŘÍZENÍ KOMISE (ES) č. /.. ze dne [ ]](/thumbs/93/111678229.jpg) Návrh NAŘÍZENÍ KOMISE (ES) č. /.. ze dne [ ] kterým se mění nařízení Komise (ES) č. 1702/2003, kterým se stanoví prováděcí pravidla pro certifikaci letové způsobilosti letadel a souvisejících výrobků,
Návrh NAŘÍZENÍ KOMISE (ES) č. /.. ze dne [ ] kterým se mění nařízení Komise (ES) č. 1702/2003, kterým se stanoví prováděcí pravidla pro certifikaci letové způsobilosti letadel a souvisejících výrobků,
***I POSTOJ EVROPSKÉHO PARLAMENTU
 Evropský parlament 2014-2019 Konsolidovaný legislativní dokument 14.3.2018 EP-PE_TC1-COD(2017)0329 ***I POSTOJ EVROPSKÉHO PARLAMENTU přijatý v prvním čtení dne 14. března 2018 k přijetí směrnice Evropského
Evropský parlament 2014-2019 Konsolidovaný legislativní dokument 14.3.2018 EP-PE_TC1-COD(2017)0329 ***I POSTOJ EVROPSKÉHO PARLAMENTU přijatý v prvním čtení dne 14. března 2018 k přijetí směrnice Evropského
[ 1 ] RNDr. Olga Hanzlíčková 2012 Státní ústav pro kontrolu léčiv
![[ 1 ] RNDr. Olga Hanzlíčková 2012 Státní ústav pro kontrolu léčiv [ 1 ] RNDr. Olga Hanzlíčková 2012 Státní ústav pro kontrolu léčiv](/thumbs/93/112264798.jpg) [ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Návrh novely zákona č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů vedoucí sekce DOZ [ 3 ] Směrnice Evropského parlamentu a Rady 2010/84/EU
[ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Návrh novely zákona č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů vedoucí sekce DOZ [ 3 ] Směrnice Evropského parlamentu a Rady 2010/84/EU
(Nelegislativní akty) NAŘÍZENÍ
 25.11.2014 L 337/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 1252/2014 ze dne 28. května 2014 doplňující směrnici Evropského parlamentu a Rady 2001/83/ES, pokud jde
25.11.2014 L 337/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 1252/2014 ze dne 28. května 2014 doplňující směrnici Evropského parlamentu a Rady 2001/83/ES, pokud jde
L 92/12 Úřední věstník Evropské unie
 L 92/12 Úřední věstník Evropské unie 3.4.2008 NAŘÍZENÍ KOMISE (ES) č. 304/2008 ze dne 2. dubna 2008, kterým se podle nařízení Evropského parlamentu a Rady (ES) č. 842/2006 stanoví minimální požadavky na
L 92/12 Úřední věstník Evropské unie 3.4.2008 NAŘÍZENÍ KOMISE (ES) č. 304/2008 ze dne 2. dubna 2008, kterým se podle nařízení Evropského parlamentu a Rady (ES) č. 842/2006 stanoví minimální požadavky na
(Text s významem pro EHP)
 26.4.2017 Úřední věstník Evropské unie L 109/9 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2017/717 ze dne 10. dubna 2017, kterým se stanoví prováděcí pravidla k nařízení Evropského parlamentu a Rady (EU) 2016/1012,
26.4.2017 Úřední věstník Evropské unie L 109/9 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2017/717 ze dne 10. dubna 2017, kterým se stanoví prováděcí pravidla k nařízení Evropského parlamentu a Rady (EU) 2016/1012,
ROZHODNUTÍ KOMISE. ze dne 11. března 2004,
 ROZHODNUTÍ KOMISE ze dne 11. března 2004, týkající se dotazníku pro zprávy členských států o provádění směrnice 2002/96/ES Evropského parlamentu a Rady o odpadních elektrických a elektronických zařízeních
ROZHODNUTÍ KOMISE ze dne 11. března 2004, týkající se dotazníku pro zprávy členských států o provádění směrnice 2002/96/ES Evropského parlamentu a Rady o odpadních elektrických a elektronických zařízeních
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne ,
 EVROPSKÁ KOMISE V Bruselu dne 10.4.2017 C(2017) 2234 final PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne 10.4.2017, kterým se stanoví prováděcí pravidla k nařízení Evropského parlamentu a Rady (EU) 2016/1012,
EVROPSKÁ KOMISE V Bruselu dne 10.4.2017 C(2017) 2234 final PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne 10.4.2017, kterým se stanoví prováděcí pravidla k nařízení Evropského parlamentu a Rady (EU) 2016/1012,
(Akty, jejichž zveřejnění je povinné) NAŘÍZENÍ RADY (ES) č. 2182/2004 ze dne 6. prosince 2004 o medailích a žetonech podobných euromincím
 21.12.2004 Úřední věstník Evropské unie L 373/1 I (Akty, jejichž zveřejnění je povinné) NAŘÍZENÍ RADY (ES) č. 2182/2004 ze dne 6. prosince 2004 o medailích a žetonech podobných euromincím RADA EVROPSKÉ
21.12.2004 Úřední věstník Evropské unie L 373/1 I (Akty, jejichž zveřejnění je povinné) NAŘÍZENÍ RADY (ES) č. 2182/2004 ze dne 6. prosince 2004 o medailích a žetonech podobných euromincím RADA EVROPSKÉ
Návrh. NAŘÍZENÍ KOMISE (EU) č. / ze dne [ ],
![Návrh. NAŘÍZENÍ KOMISE (EU) č. / ze dne [ ], Návrh. NAŘÍZENÍ KOMISE (EU) č. / ze dne [ ],](/thumbs/92/109304866.jpg) CS CS CS EVROPSKÁ KOMISE V Bruselu dne C Návrh NAŘÍZENÍ KOMISE (EU) č. / ze dne [ ], kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 216/2008 o společných pravidlech v oblasti civilního letectví
CS CS CS EVROPSKÁ KOMISE V Bruselu dne C Návrh NAŘÍZENÍ KOMISE (EU) č. / ze dne [ ], kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 216/2008 o společných pravidlech v oblasti civilního letectví
PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne ,
 EVROPSKÁ KOMISE V Bruselu dne 28.5.2018 C(2018) 3120 final PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne 28.5.2018, kterým se stanoví pravidla pro použití čl. 26 odst. 3 nařízení Evropského parlamentu a Rady
EVROPSKÁ KOMISE V Bruselu dne 28.5.2018 C(2018) 3120 final PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) /... ze dne 28.5.2018, kterým se stanoví pravidla pro použití čl. 26 odst. 3 nařízení Evropského parlamentu a Rady
Návrh SMĚRNICE RADY,
 EVROPSKÁ KOMISE V Bruselu dne 8.5.2018 COM(2018) 261 final 2018/0124 (CNS) Návrh SMĚRNICE RADY, kterou se mění směrnice 2006/112/ES a 2008/118/ES, pokud jde o zahrnutí italské obce Campione d Italia a
EVROPSKÁ KOMISE V Bruselu dne 8.5.2018 COM(2018) 261 final 2018/0124 (CNS) Návrh SMĚRNICE RADY, kterou se mění směrnice 2006/112/ES a 2008/118/ES, pokud jde o zahrnutí italské obce Campione d Italia a
FARMACEUTICKÁ DOKUMENTACE VÝROBA A DOVOZ LÉČIVÝCH PŘÍPRAVKŮ ZNAČENÍ OBALŮ
 1 FARMACEUTICKÁ DOKUMENTACE VÝROBA A DOVOZ LÉČIVÝCH PŘÍPRAVKŮ ZNAČENÍ OBALŮ Ing. Lucie Zmatlíková Ing. Dagmar Pospíšilová FARMACEUTICKÁ DOKUMENTACE 2 Kapitola IV Dokumentace k žádosti Dokumentace k žádosti
1 FARMACEUTICKÁ DOKUMENTACE VÝROBA A DOVOZ LÉČIVÝCH PŘÍPRAVKŮ ZNAČENÍ OBALŮ Ing. Lucie Zmatlíková Ing. Dagmar Pospíšilová FARMACEUTICKÁ DOKUMENTACE 2 Kapitola IV Dokumentace k žádosti Dokumentace k žádosti
ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne 1.7.2015
 EVROPSKÁ KOMISE V Bruselu dne 1.7.2015 C(2015) 4359 final ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne 1.7.2015 o systémech použitelných pro posuzování a ověřování stálosti vlastností výrobků
EVROPSKÁ KOMISE V Bruselu dne 1.7.2015 C(2015) 4359 final ROZHODNUTÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) / ze dne 1.7.2015 o systémech použitelných pro posuzování a ověřování stálosti vlastností výrobků
(Nelegislativní akty) NAŘÍZENÍ
 11.5.2016 L 121/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) 2016/698 ze dne 8. dubna 2016, kterým se opravuje nařízení v přenesené pravomoci (EU) 2016/341, kterým se
11.5.2016 L 121/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) 2016/698 ze dne 8. dubna 2016, kterým se opravuje nařízení v přenesené pravomoci (EU) 2016/341, kterým se
Úřední věstník Evropské unie L 201/21
 26.7.2013 Úřední věstník Evropské unie L 201/21 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 716/2013 ze dne 25. července 2013, kterým se stanoví prováděcí pravidla k nařízení Evropského parlamentu a Rady (ES) č.
26.7.2013 Úřední věstník Evropské unie L 201/21 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 716/2013 ze dne 25. července 2013, kterým se stanoví prováděcí pravidla k nařízení Evropského parlamentu a Rady (ES) č.
SMĚRNICE. s ohledem na Smlouvu o fungování Evropské unie, a zejména na článek 113 této smlouvy, s ohledem na návrh Evropské komise,
 7.12.2018 L 311/3 SMĚRNICE SMĚRNICE RADY (EU) 2018/1910 ze dne 4. prosince 2018, kterou se mění směrnice 2006/112/ES, pokud jde o harmonizaci a zjednodušení určitých pravidel v systému daně z přidané hodnoty
7.12.2018 L 311/3 SMĚRNICE SMĚRNICE RADY (EU) 2018/1910 ze dne 4. prosince 2018, kterou se mění směrnice 2006/112/ES, pokud jde o harmonizaci a zjednodušení určitých pravidel v systému daně z přidané hodnoty
SMĚRNICE KOMISE 2010/62/EU
 9.9.2010 Úřední věstník Evropské unie L 238/7 SMĚRNICE SMĚRNICE KOMISE 2010/62/EU ze dne 8. září 2010, kterou se za účelem přizpůsobení jejich technických ustanovení mění směrnice Rady 80/720/EHS a 86/297/EHS
9.9.2010 Úřední věstník Evropské unie L 238/7 SMĚRNICE SMĚRNICE KOMISE 2010/62/EU ze dne 8. září 2010, kterou se za účelem přizpůsobení jejich technických ustanovení mění směrnice Rady 80/720/EHS a 86/297/EHS
Úř. věst. č. L 267, , s. 23 SMĚRNICE KOMISE 2002/78/ES. ze dne 1. října 2002,
 SMĚRNICE KOMISE ze dne 1. října 2002, kterou se přizpůsobuje technickému pokroku směrnice Rady 71/320/EHS o sbližování právních předpisů členských států týkajících se brzdových zařízení určitých kategorií
SMĚRNICE KOMISE ze dne 1. října 2002, kterou se přizpůsobuje technickému pokroku směrnice Rady 71/320/EHS o sbližování právních předpisů členských států týkajících se brzdových zařízení určitých kategorií
(Nelegislativní akty) NAŘÍZENÍ
 22.5.2010 Úřední věstník Evropské unie L 126/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE (EU) č. 440/2010 ze dne 21. května 2010 o poplatcích placených Evropské agentuře pro chemické látky podle
22.5.2010 Úřední věstník Evropské unie L 126/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE (EU) č. 440/2010 ze dne 21. května 2010 o poplatcích placených Evropské agentuře pro chemické látky podle
11.11.2010 Úřední věstník Evropské unie L 293/15
 11.11.2010 Úřední věstník Evropské unie L 293/15 NAŘÍZENÍ KOMISE (EU) č. 1014/2010 ze dne 10. listopadu 2010 o sledování a hlášení údajů o registraci nových osobních automobilů podle nařízení Evropského
11.11.2010 Úřední věstník Evropské unie L 293/15 NAŘÍZENÍ KOMISE (EU) č. 1014/2010 ze dne 10. listopadu 2010 o sledování a hlášení údajů o registraci nových osobních automobilů podle nařízení Evropského
Úřední věstník Evropské unie L 153/23
 12.6.2008 Úřední věstník Evropské unie L 153/23 NAŘÍZENÍ KOMISE (ES) č. 523/2008 ze dne 11. června 2008, kterým se mění přílohy VIII, X a XI nařízení Evropského parlamentu a Rady (ES) č. 1774/2002, pokud
12.6.2008 Úřední věstník Evropské unie L 153/23 NAŘÍZENÍ KOMISE (ES) č. 523/2008 ze dne 11. června 2008, kterým se mění přílohy VIII, X a XI nařízení Evropského parlamentu a Rady (ES) č. 1774/2002, pokud
NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY (ES) č. 1830/2003. ze dne 22. září 2003
 NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY (ES) č. 1830/2003 ze dne 22. září 2003 o sledovatelnosti a označování geneticky modifikovaných organismů a sledovatelnosti potravin a krmiv vyrobených z geneticky
NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY (ES) č. 1830/2003 ze dne 22. září 2003 o sledovatelnosti a označování geneticky modifikovaných organismů a sledovatelnosti potravin a krmiv vyrobených z geneticky
PROVÁDĚCÍ ROZHODNUTÍ KOMISE (EU) / ze dne ,
 EVROPSKÁ KOMISE V Bruselu dne 25.10.2018 C(2018) 6929 final PROVÁDĚCÍ ROZHODNUTÍ KOMISE (EU) / ze dne 25.10.2018, kterým se stanoví specifikace registrů vozidel uvedených v článku 47 směrnice Evropského
EVROPSKÁ KOMISE V Bruselu dne 25.10.2018 C(2018) 6929 final PROVÁDĚCÍ ROZHODNUTÍ KOMISE (EU) / ze dne 25.10.2018, kterým se stanoví specifikace registrů vozidel uvedených v článku 47 směrnice Evropského
Delegace naleznou v příloze dokument D045810/01.
 Rada Evropské unie Brusel 22. července 2016 (OR. en) 11453/16 STATIS 52 COMPET 430 UD 169 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 22. července 2016 Příjemce: Č. dok. Komise: D045810/01
Rada Evropské unie Brusel 22. července 2016 (OR. en) 11453/16 STATIS 52 COMPET 430 UD 169 PRŮVODNÍ POZNÁMKA Odesílatel: Evropská komise Datum přijetí: 22. července 2016 Příjemce: Č. dok. Komise: D045810/01
(Text s významem pro EHP)
 12.11.2015 L 295/11 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2015/2014 ze dne 11. listopadu 2015, kterým se stanoví prováděcí technické normy, pokud jde o postupy a šablony pro předkládání informací orgánu dohledu
12.11.2015 L 295/11 PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) 2015/2014 ze dne 11. listopadu 2015, kterým se stanoví prováděcí technické normy, pokud jde o postupy a šablony pro předkládání informací orgánu dohledu
SMĚRNICE RADY. ze dne 16. prosince 1991. o vzájemném uznávání licencí pro výkon funkcí v civilním letectví (91/670/EHS)
 SMĚRNICE RADY ze dne 16. prosince 1991 o vzájemném uznávání licencí pro výkon funkcí v civilním letectví (91/670/EHS) RADA EVROPSKÝCH SPOLEČENSTVÍ, s ohledem na Smlouvu o založení Evropského společenství,
SMĚRNICE RADY ze dne 16. prosince 1991 o vzájemném uznávání licencí pro výkon funkcí v civilním letectví (91/670/EHS) RADA EVROPSKÝCH SPOLEČENSTVÍ, s ohledem na Smlouvu o založení Evropského společenství,
NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU)
 28.5.2014 L 159/41 NAŘÍZENÍ NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 574/2014 ze dne 21. února 2014, kterým se mění příloha III nařízení Evropského parlamentu a Rady (EU) č. 305/2011 o vzoru, který
28.5.2014 L 159/41 NAŘÍZENÍ NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 574/2014 ze dne 21. února 2014, kterým se mění příloha III nařízení Evropského parlamentu a Rady (EU) č. 305/2011 o vzoru, který
