Příbalová informace: informace pro uživatele. Pegvisomantum
|
|
|
- Monika Horáková
- před 9 lety
- Počet zobrazení:
Transkript
1 Příbalová informace: informace pro uživatele SOMAVERT 10 mg prášek a rozpouštědlo pro injekční roztok SOMAVERT 15 mg prášek a rozpouštědlo pro injekční roztok SOMAVERT 20 mg prášek a rozpouštědlo pro injekční roztok SOMAVERT 25 mg prášek a rozpouštědlo pro injekční roztok SOMAVERT 30 mg prášek a rozpouštědlo pro injekční roztok Pegvisomantum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje. - Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. - Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry. - Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy. - Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4. Co naleznete v této příbalové informaci 1. Co je přípravek SOMAVERT a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete přípravek SOMAVERT používat 3. Jak se přípravek SOMAVERT používá 4. Možné nežádoucí účinky 5. Jak přípravek SOMAVERT uchovávat 6. Obsah balení a další informace 1. Co je přípravek SOMAVERT a k čemu se používá Přípravek SOMAVERT se používá k léčbě akromegalie, což je hormonální porucha, která je důsledkem zvýšené sekrece růstového hormonu (GH) a IGF-I (inzulínu podobný růstový faktor I) a je charakterizována nadměrným růstem kostí, měkkých tkání, otoky, onemocněním srdce a příbuznými chorobami. Přípravek SOMAVERT je biotechnologickým produktem. Léčivou látkou přípravku SOMAVERT je pegvisomant, což je antagonista receptoru růstového hormonu. Tyto látky snižují účinek GH a hladinu inzulínu podobných růstových faktorů I v krvi. 2. Čemu musíte věnovat pozornost, než začnete přípravek SOMAVERT používat Nepoužívejte přípravek SOMAVERT: jestliže jste alergický(á) na pegvisomant nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6). Upozornění a opatření Před použitím přípravku SOMAVERT se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou. pokud budete při užívání přípravku SOMAVERT pozorovat poruchy zraku nebo bolesti hlavy, obraťte se ihned na svého lékaře Váš lékař nebo sestra budou monitorovat hladiny IGF-I (inzulínu podobný růstový faktor I) obíhajících v krvi a podle potřeby přizpůsobovat dávku přípravku SOMAVERT 1
2 Váš lékař bude sledovat Váš adenom (nezhoubný nádor) Váš lékař nebo sestra budou monitorovat hladiny jaterních enzymů v krvi každých 4 6 týdnů během prvních 6 měsíců léčby přípravkem SOMAVERT. Podání přípravku SOMAVERT musí být při prvních známkách onemocnění jater ukončeno pokud máte cukrovku, Váš lékař Vám může upravit dávku inzulínu nebo jiných léků, které užíváte pacientky musí užívat vhodnou kontracepci, protože se může zvýšit plodnost. Viz též níže bod Těhotenství. Další léčivé přípravky a přípravek SOMAVERT Oznamte svému lékaři, pokud jste v minulosti užíval(a) nějaké jiné léky k léčbě akromegalie nebo cukrovky. Informujte svého lékaře, lékárníka nebo zdravotní sestru o všech lécích, které používáte, nebo které jste v nedávné době používal(a), a to i o lécích, které jsou dostupné bez lékařského předpisu. Součástí Vaší léčby může být i užívání dalších léků. Je důležité, abyste užíval/a všechny léky, včetně přípravku SOMAVERT, pokud Vám neurčí Váš lékař, lékárník nebo zdravotní sestra jinak. Těhotenství a kojení Účinky přípravku SOMAVERT u těhotných žen nejsou známy, proto se užívání tohoto přípravku u těhotných žen nedoporučuje. Doporučujeme Vám, abyste v průběhu léčby pegvisomantem neotěhotněla. V případě, že otěhotníte, musíte se obrátit na svého lékaře. Poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než začnete užívat jakýkoliv lék. Není známo, zda se pegvisomant vylučuje do lidského mateřského mléka. Během léčby přípravkem SOMAVERT nesmíte kojit, pokud s Vámi Váš lékař tuto otázku neprojedná. Řízení dopravních prostředků a obsluha strojů Nebyly provedeny žádné studie týkající se účinků na schopnost řídit motorová vozidla nebo obsluhovat stroje. Přípravek SOMAVERT obsahuje sodík Tento léčivý přípravek obsahuje méně než 1 mg sodíku v jedné dávce, tj. v podstatě bez sodíku. 3. Jak se přípravek SOMAVERT používá Vždy aplikujte injekci tohoto přípravku přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem. Zahajovací dávku 80 mg pegvisomantu Vám podá podkožně Váš lékař. Poté je obvyklá denní dávka pegvisomantu 10 mg, která se podává podkožní injekcí. Každých 4 až 6 týdnů provede Váš lékař příslušnou úpravu dávky, která se provádí postupným zvyšováním dávky pegvisomantu o 5 mg denně na základě koncentrací tzv. IGF-I tak, aby se udržela optimální léčebná odpověď. Způsob a cesta podání léku: Přípravek SOMAVERT se podává podkožně. Injekci si můžete aplikovat sám/sama, případně Vám ji může aplikovat jiná osoba, např. Váš lékař nebo zdravotní sestra. Je zapotřebí, abyste dodržoval(a) podrobné pokyny ohledně postupu při podávání injekce, které jsou uvedeny na konci tohoto letáku. V podávání injekcí tohoto přípravku pokračujte po celou dobu, kterou Vám určil Váš lékař. 2
3 Před použitím musí být tento přípravek rozpuštěn. Injekce se nesmí míchat ve stejné stříkačce nebo lahvičce jako jiné léky. V místě vpichu injekce může dojít ke zmnožení podkožní tukové tkáně (nahromadění podkožního tuku). Abyste tomu zabránil/a, použijte při každém podání odlišné místo vpichu, jak je uvedeno v Kroku 2 Návod na přípravu a podání injekce přípravku SOMAVERT na konci této příbalové informace. Tím umožníte kůži a podkoží, aby se po podání injekce regenerovaly dříve, než bude do stejného místa podána další injekce. Pokud máte dojem, že účinek tohoto přípravku je příliš silný nebo slabý, oznamte to svému lékaři, lékárníkovi nebo zdravotní sestře. Jestliže jste použila(a) více přípravku SOMAVERT, než jste měl(a) Pokud jste si náhodně aplikoval(a) větší množství přípravku SOMAVERT než Vám naordinoval Váš lékař, není pravděpodobné, že by se jednalo o závažnou příhodu, měl(a) byste však ihned kontaktovat svého lékaře, lékárníka nebo zdravotní sestru. Jestliže jste zapomněl(a) použít přípravek SOMAVERT Pokud jste si zapomněl(a) aplikovat injekci přípravku SOMAVERT, měl(a) byste si aplikovat další dávku co nejdříve, jakmile si vzpomenete a dále pokračovat v injekcích přípravku SOMAVERT podle ordinace Vašeho lékaře. Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku. Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry. 4. Možné nežádoucí účinky Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. U některých pacientů léčených přípravkem SOMAVERT byly hlášeny mírné až vážné alergické (anafylaktické) reakce. Příznaky závažné alergické reakce mohou zahrnovat 1 nebo více z následujících: otok obličeje, jazyka, rtů nebo hrdla; sípot nebo obtížné dýchání (stažení hrtanu); celková kožní vyrážka, kopřivka nebo svědění; závrať. Při výskytu některého z těchto příznaků kontaktujte ihned svého lékaře. Časté nežádoucí účinky (mohou postihnout až 1 osobu z 10) zahrnují: Zvýšení hladin látek, podle kterých se měří funkce jater. Lze je nalézt ve výsledcích krevních testů. Zvýšení krevního tlaku. Průjem, zácpa, pocit na zvracení nebo zvracení, pocit nadmutí, špatné trávení, plynatost. Bolesti hlavy, závratě, ospalost, nekontrolovaný třes. Tvorba modřin nebo krvácení v místě vpichu injekce, bolestivost nebo otok v místě vpichu injekce, nahromadění tuku v podkoží v místě vpichu injekce, otok končetin, slabost. Pocení, svědění, vyrážka. Bolest kloubů, bolest svalů. Zvýšení krevního cholesterolu, přírůstek tělesné hmotnosti, zvýšení hladiny krevní glukózy, zvýšená chuť k jídlu. Příznaky podobné chřipce, únava. Nepřirozené sny či potíže se spánkem. Méně časté nežádoucí účinky (mohou postihnout až 1 osobu ze 100) zahrnují: 3
4 Pocit krátkého dechu. Krev v moči, bílkovina v moči, zvýšené množství moči, onemocnění ledvin. Zlost, nedostatek zájmu, pocit zmatenosti, zvýšení sexuální touhy, panika, ztráta paměti. Snížený počet krevních destiček, zvýšený nebo snížený počet bílých krvinek v krvi, sklon ke krvácení. Horečka, abnormální pocity, špatné hojení. Únava očí, bolest očí, potíže vnitřního ucha. Otok obličeje, suchá kůže, sklon k tvorbě modřin, noční pocení. Zvýšená hladina tuků krvi, snížení krevní glukózy. Sucho v ústech, zvýšené slinění, problémy se zuby, hemoroidy. Snížená citlivost, abnormální vnímání chutí, migréna. Zánět kloubu. U přibližně 17% pacientů se během léčby vytvořily protilátky na růstový hormon. Tyto protilátky zřejmě nebrání působení tohoto přípravku. Hlášení nežádoucích účinků Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova Praha 10 Webové stránky: Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku. 5. Jak přípravek SOMAVERT uchovávat Uchovávejte tento přípravek mimo dohled a dosah dětí. Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na injekční lahvičce a krabičce za Použitelné do:. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Uchovávejte v chladničce (2 C 8 C). Chraňte před mrazem. Uchovávejte injekční lahvičky v krabičce, aby byl přípravek chráněn před světlem. Po naředění musí být přípravek SOMAVERT použit okamžitě. Nepoužívejte tento přípravek, pokud si všimnete, že je roztok zakalený nebo obsahuje částice. Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí. 6. Obsah balení a další informace Co přípravek SOMAVERT obsahuje - Léčivou látkou je pegvisomantum. 4
5 - SOMAVERT 10 mg: Jedna injekční lahvička s práškem obsahuje pegvisomantum 10 mg. Po rozpuštění v 1 ml rozpouštědla 1 ml roztoku obsahuje pegvisomantum 10 mg. - SOMAVERT 15 mg: Jedna injekční lahvička s práškem obsahuje pegvisomantum 15 mg. Po rozpuštění v 1 ml rozpouštědla 1 ml roztoku obsahuje pegvisomantum 15 mg. - SOMAVERT 20 mg: Jedna injekční lahvička s práškem obsahuje pegvisomantum 20 mg. Po rozpuštění v 1 ml rozpouštědla 1 ml roztoku obsahuje pegvisomantum 20 mg. - SOMAVERT 25 mg: Jedna injekční lahvička s práškem obsahuje pegvisomantum 25 mg. Po rozpuštění v 1 ml rozpouštědla 1 ml roztoku obsahuje pegvisomantum 25 mg. - SOMAVERT 30 mg: Jedna injekční lahvička s práškem obsahuje pegvisomantum 30 mg. Po rozpuštění v 1 ml rozpouštědla 1 ml roztoku obsahuje pegvisomantum 30 mg. - Dalšími složkami jsou glycin, mannitol (E421), hydrogenfosforečnan sodný bezvodý a monohydrát dihydrogenfosforečnanu sodného. - Rozpouštědlem je voda na injekci. Jedna lahvička rozpouštědla obsahuje 8 ml vody na injekci. Jak přípravek SOMAVERT vypadá a co obsahuje toto balení Přípravek SOMAVERT je ve formě prášku a rozpouštědla, v injekčních lahvičkách. Prášek je bílý a rozpouštědlo je čiré a bezbarvé. Prášek je v injekční lahvičce (buď 10 mg, 15 mg, 20 mg, 25 mg nebo 30 mg pegvisomantu) a rozpouštědlo je v injekční lahvičce (8 ml). Velikost balení je 1 a 30. Na trhu nemusí být všechny velikosti balení. Držitel rozhodnutí o registraci Pfizer Limited Ramsgate Road Sandwich Kent CT13 9NJ Velká Británie Výrobce Pfizer Manufacturing Belgium NV Rijksweg Puurs Belgie Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci: België/Belgique/Belgien Lietuva Pfizer S.A./N.V. Pfizer Luxembourg SARL filialas Lietuvoje Tél/Tel: +32 (0) Tel България Luxembourg/Luxemburg Пфайзер Люксембург САРЛ, Клон България Pfizer S.A. Тел.: Tél/Tel: +32 (0) Česká republika Magyarország Pfizer spol. s r.o. Pfizer Kft. Tel: Tel.: Danmark Malta Pfizer ApS V.J. Salomone Pharma Ltd. Tlf: Tel:
6 Deutschland Nederland Pfizer Pharma GmbH Pfizer bv Tel: +49 (0) Tel: +31 (0) Eesti Norge Pfizer Luxembourg SARL Eesti filiaal Pfizer AS Tel: Tlf: Ελλάδα Österreich PFIZER ΕΛΛΑΣ Α.Ε. Pfizer Corporation Austria Ges.m.b.H. Τηλ: Tel: +43 (0) España Polska Pfizer S.L. Pfizer Polska Sp. z o.o. Tel: Tel.: France Portugal Pfizer Laboratórios Pfizer, Lda. Tél: +33 (0) Tel: Hrvatska Pfizer Croatia d.o.o. Tel: Ireland Pfizer Healthcare Ireland Tel: (toll free) +44 (0) România Pfizer România S.R.L. Tel: +40 (0) Slovenija Pfizer Luxembourg SARL, Pfizer, podružnica za svetovanje s področja farmacevtske dejavnosti, Ljubljana Tel: (0) Ísland Slovenská republika Icepharma hf. Pfizer Luxembourg SARL, organizačná zložka Sími: Tel: Italia Suomi/Finland Pfizer Italia S.r.l. Pfizer Oy Tel: Puh/Tel: +358 (0) Κύπρος Sverige PFIZER ΕΛΛΑΣ Α.Ε. (Cyprus Branch) Pfizer AB Τηλ: Τηλ: Tel: +46 (0) Latvija United Kingdom Pfizer Luxembourg SARL filiāle Latvijā Pfizer Limited Tel: Tel: +44 (0) Tato příbalová informace byla naposledy revidována 07/2015 Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky Na těchto stránkách naleznete též odkazy na další webové stránky týkající se vzácných onemocnění a jejich léčby. 6
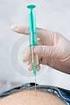
7 NÁVOD NA PŘÍPRAVU A PODÁNÍ INJEKCE PŘÍPRAVKU SOMAVERT Úvod V následujícím návodu je vysvětleno, jak připravovat a podávat přípravek SOMAVERT. Přečtěte si pečlivě tento návod a postupujte přesně podle něj. Váš lékař nebo zdravotní sestra Vás poučí, jak si sami injekci aplikovat. Nepokoušejte si sami píchat injekce, dokud si nebudete jist/a, že jste porozuměl/a tomu, jak připravovat a podávat injekce. Před použitím musí být prášek rozpuštěn pomocí rozpouštědla. Tato injekce se nesmí míchat s jinými léčivými přípravky. KROK 1. VÝBĚR ZPŮSOBU PŘÍPRAVY ROZTOKU PŘÍPRAVKU SOMAVERT Roztok přípravku SOMAVERT je možno připravit 2 způsoby. Zkonzultujte se svým lékařem nebo zdravotní sestrou, která z metod bude pro Vás vhodnější: a) Za použití nástavce na injekční lahvičku (MIXJECT) nemusí být na trhu ve všech zemích b) Bez použití nástavce. a) PŘÍPRAVA ROZTOKU S PŘÍPRAVKEM SOMAVERT ZA POUŽITÍ NÁSTAVCE NA INJEKČNÍ LAHVIČKU (MIXJECT) ZAČÍNÁME Pečlivě si umyjte ruce. Přichystejte si: 1 lahvičku s práškem (SOMAVERT), 1 lahvičku s rozpouštědlem (voda na injekci), 1 injekční stříkačku Luer-lock o objemu 1 ml (pro rozpuštění roztoku přípravku SOMAVERT a podání injekce) toto je doporučeno, mohou být ale použity injekční stříkačky i jiného druhu a jiných velikostí. Pro další informace se, prosím, obraťte na lékaře nebo zdravotní sestru. 2 nástavce na injekční lahvičku MIXJECT, 1 snímatelnou jehlu (25-30 gauge). Tampony s alkoholem nebo dezinfekční látkou a vhodnou nádobku na zneškodnění použitých jehel. Zkontrolujte datum použitelnosti na štítcích lahvičky i injekční stříkačky. Nelze je použít po uplynutí vyznačeného měsíce a roku. Po smísení s 1 ml rozpouštědla obsahuje 1 ml čirého roztoku buď 10 mg, 15 mg, 20 mg, 25 mg nebo 30 mg pegvisomantu. PŘÍPRAVA DÁVKY PŘÍPRAVKU SOMAVERT K INJEKCI Obrázek 1 7
8 1. Odstraňte ochranné umělohmotné víčko z lahvičky s rozpouštědlem a z lahvičky s práškem přípravku SOMAVERT (Obr. 1). Dávejte pozor, abyste se nedotkl/a gumových zátek. Zátky lahviček musí zůstat čisté. Pokud se jich dotknete nebo jsou-li jinak kontaminovány, musíte je před nasazením nástavce na injekční lahvičku očistit pomocí tamponu s alkoholem nebo dezinfekční látkou. 2. Otevřete pouze jeden nástavec na injekční lahvičku stržením ochranného papírového obalu. Ponechejte nástavec v plastovém obalu a nedotýkejte se jeho hrotu. Obrázek 2 3. Přidržujte stále nástavec v plastovém obalu a připojte nástavec k lahvičce s rozpouštědlem zatlačením svisle dolů proti rovné ploše, dokud nezapadne na místo a hrot nepronikne skrz gumovou zátku lahvičky s rozpouštědlem (Obr. 2). Z nástavce odstraňte plastový obal a zahoďte ho. Obrázek 3 4. Vyjměte injekční stříkačku z ochranného obalu. Píst injekční stříkačky povytáhněte ke značce 1 ml. V jedné ruce přidržujte lahvičku s rozpouštědlem položenou na rovnou plochu a šroubovitým pohybem ve směru hodinových ručiček spojte hrot injekční stříkačky s nástavcem (Obr. 3). Lehce zatlačte na píst, ať se do lahvičky s rozpouštědlem vtlačí vzduch. PŘIDÁNÍ ROZPOUŠTĚDLA Obrázek 4 5. Pevně uchopte sestavu lahvičky s rozpouštědlem, nástavcem a injekční stříkačkou. Opatrně ji převraťte dnem vzhůru. Zvedněte ji do výše očí (Obr. 4). 8
9 6. Ruku opatrně posuňte po lahvičce s rozpouštědlem tak, abyste ji pevně držel/a palcem a ukazovákem za hrdlo a zbylými prsty svíral/a horní část injekční stříkačky. Druhou rukou pomalu natáhněte píst injekční stříkačky lehce za značku 1 ml. Zkontrolujte, zda v roztoku rozpouštědla v injekční stříkačce nejsou vzduchové bublinky. Pokud ano, poklepávejte na injekční stříkačku, dokud bublinky nevystoupají k hladině. Opatrně zatlačte na píst, abyste bublinky vrátil/a zpět do lahvičky. Ověřte si, že v injekční stříkačce zůstává 1 ml rozpouštědla. Opatrně sestavu lahvičky s rozpouštědlem, nástavcem a injekční stříkačkou obraťte a postavte ji na čistý povrch. V tomto okamžiku ještě injekční stříkačku neoddělujte od nástavce. Obrázek 5 7. Stejně jako u prvního nástavce na injekční lahvičku, i druhý otevřete stržením ochranného papírového obalu. Nedotýkejte se ho. Přidržujte stále nástavec v plastovém obalu a připojte nástavec k lahvičce s přípravkem SOMAVERT zatlačením svisle dolů proti rovné ploše, dokud nezapadne na místo a hrot nepronikne skrz gumovou zátku přípravku SOMAVERT (Obr. 5). Sejměte plastový obal z nástavce a zahoďte ho. Obrázek 6 8. Odpojte injekční stříkačku od nástavce nasazeného na lahvičku s rozpouštědlem (otáčením proti směru hodinových ručiček) a připojte ji k nástavci na lahvičce s přípravkem SOMAVERT (otáčením proti směru hodinových ručiček). Sestavu lahvičky s přípravkem SOMAVERT, nástavcem a injekční lahvičkou nakloňte a opatrně rozpouštědlo vstříkněte dovnitř, po stěně lahvičky s přípravkem SOMAVERT (Obr. 6). Lahvičku od rozpouštědla zlikvidujte podle instrukcí lékaře nebo zdravotní sestry. 9
10 Obrázek 7 9. Držte lahvičku s přípravkem SOMAVERT a rozpouštědlem, přes nástavec stále spojenou s injekční stříkačkou, mezi oběma rukama a zlehka jí otáčejte, aby se prášek rozpustil (Obr. 7). LAHVIČKOU NETŘEPEJTE. Roztok by měl být po rozpuštění prášku čirý. Je-li zkalený nebo zamlžený, nepodávejte ho. Upozorněte na to lékárnu a požádejte o náhradní lahvičku. Lahvičku se zakaleným roztokem nevyhazujte, protože by ji lékárna mohla chtít vrátit. PŘÍPRAVA INJEKCE 10. Pevně uchopte sestavu lahvičky obsahující rozpuštěný roztok přípravku SOMAVERT, nástavec a injekční stříkačku. Opatrně ji převraťte dnem vzhůru. Zvedněte ji do výše očí. 10
11 Obrázek Stejně jako předtím, jednu ruku opatrně posuňte po lahvičce tak, abyste ji pevně držel/a palcem a ukazovákem za hrdlo a zbylými prsty svíral/a horní část injekční stříkačky. Druhou rukou pomalu natáhněte píst injekční stříkačky, abyste odsál/a celý obsah lahvičky (1 ml). (Obr.8). Zkontrolujte, zda v roztoku injekční stříkačky nejsou vzduchové bublinky. Pokud ano, poklepávejte na injekční stříkačku, dokud bublinky nevystoupají k hladině. Opatrně zatlačte na píst, abyste vtlačil/a bublinky zpět do lahvičky. Ověřte si, že v injekční stříkačce zůstává 1 ml roztoku. Opatrně sestavu lahvičky obsahující roztok rozpuštěného přípravku SOMAVERT, nástavec a injekční stříkačku obraťte a postavte ji na čistý povrch. V tomto okamžiku ještě injekční stříkačku neoddělujte od nástavce. Obrázek Otevřete obal jehly tak, aby vyčníval pouze její konus (plastová koncovka). Jehla zčásti zůstane v obalu. Položte jehlu i s obalem na stůl. Injekční stříkačku odpojte od nástavce/ spojky otáčením proti směru hodinových ručiček. Odstraňte ochranný obal a jehlu napojte na injekční stříkačku. Zatímco budete připravovat místo pro aplikaci injekce, ponechejte na jehle plastovou krytku. (Obr. 9). Ihned po rozpuštění přípravek SOMAVERT aplikujte. Postupujte podle odstavce Krok 2 Podání injekce. b) PŘÍPRAVA ROZTOKU S PŘÍPRAVKEM SOMAVERT BEZ POUŽITÍ NÁSTAVCE NA INJEKČNÍ LAHVIČKU Začínáme Pečlivě si umyjte ruce. Vezměte jednu lahvičku s práškem (SOMAVERT) a jednu lahvičku s rozpouštědlem (voda na injekci), jednu 3 ml injekční stříkačku s oddělitelnou jehlou tloušťky 21 gaugue a délky 2,54 centimetru (1 palec), jednu standardní 1ml inzulínovou stříkačku, tampony s alkoholem nebo dezinfekční látkou a vhodnou nádobku na zneškodnění použitých jehel. Zkontrolujte datum použitelnosti na štítku na lahvičce a na stříkačce. Nelze je použít po uplynutí vyznačeného měsíce a roku. 11
12 Po smísení s 1 ml rozpouštědla obsahuje 1 ml čirého roztoku 10 mg, 15 mg, 20 mg, 25 mg nebo 30 mg pegvisomantu. Příprava injekční dávky přípravku SOMAVERT Odstraňte z obou lahviček ochrannou plastovou čepičku. Dávejte pozor, abyste se nedotkl/a gumových zátek na lahvičkách. V tomto okamžiku jsou zátky čisté. Pokud se zátek dotknete nebo dojde jakýmkoliv způsobem k jejich znečištění, musíte je ještě před proniknutím jehly zátkou očistit tamponem s dezinfekční látkou nebo alkoholem. Opatrně odstraňte kryt z jehly větší stříkačky (3 ml). To je stříkačka pro rozpouštědlo. Obrázek 1 1. Vytáhněte píst až na značku pro 1 ml. Jednou rukou držte bezpečně lahvičku s rozpouštědlem a druhou rukou vpíchněte jehlu stříkačky s rozpouštědlem přímo středem gumové zátky hluboko do lahvičky. Jemným tlakem tlačte píst, až je vzduch vstříknut do lahvičky (obr. 1). PŘIDÁNÍ ROZPOUŠTĚDLA Obrázek 2 2. Uchopte bezpečně lahvičku s rozpouštědlem a stříkačku s jehlou stále ještě hluboko vpíchnutou do lahvičky. Opatrně otočte lahvičku se stříkačkou dnem vzhůru. Umístěte ji do výše očí (obr. 2). 12
13 Obrázek 3 3. Posuňte opatrně jednu ruku dolů po lahvičce s rozpouštědlem, takže palcem a ukazovákem můžete pevně uchopit hrdlo lahvičky a dalšími prsty horní část stříkačky. Druhou rukou pomalu táhněte píst stříkačky směrem dolů a lehce jím posunujte až na značku označující 1 ml. Zkontrolujte, zda roztok ve stříkačce neobsahuje vzduchové bubliny. Pokud jsou bubliny přítomny, poklepávejte na tělo stříkačky do té doby, než se bubliny dostanou na horní konec stříkačky. Opatrně tlačte pístem, abyste vystříkl/a zpět do lahvičky pouze vzduchové bubliny. Zkontrolujte, zda ve stříkačce zůstává 1 ml rozpouštědla a potom odstraňte jehlu z lahvičky (obr. 3). Obrázek 4 4. Vpíchněte jehlu stříkačky s rozpouštědlem přímo zátkou lahvičky s práškem (SOMAVERT). Nakloňte stříkačku na stranu a lehce vystřikujte roztok po vnitřní stěně lahvičky s přípravkem SOMAVERT. Když je stříkačka s rozpouštědlem prázdná, vytáhněte ji z lahvičky. Zlikvidujte lahvičku s rozpouštědlem, stříkačku a jehlu podle pokynů Vašeho lékaře nebo zdravotní sestry (obr. 4). 13
14 Obrázek 5 5. Držte lahvičku svisle ve dlaních a lehce mezi dlaněmi válejte, aby se rozpustil prášek. LAHVIČKOU NETŘEPEJTE. Po rozpuštění prášku by měl být roztok čirý. Nepíchejte si injekci, pokud je roztok zkalený nebo zamlžený. Oznamte to ve své lékárně a požádejte o výměnu lahvičky. Lahvičku nevyhazujte, protože lékárna může požadovat, abyste ji vrátil/a. SOMAVERT si píchněte ihned (obr. 5). PŘÍPRAVA INJEKCE Obrázek 6 6. Očistěte gumovou zátku lahvičky s přípravkem SOMAVERT tamponem s dezinfekční látkou nebo alkoholem. Odstraňte kryt z jehly na stříkačce (1 ml). Vytáhněte píst stříkačky na značku označující 1 ml. Jednou rukou držte bezpečně lahvičku s rozpouštědlem a druhou rukou vpíchněte jehlu stříkačky s rozpouštědlem přímo středem gumové zátky hluboko do lahvičky. Jemným tlakem tlačte píst, až je vzduch vstříknut do lahvičky. Uchopte bezpečně lahvičku s rozpouštědlem a stříkačku s jehlou stále ještě hluboko vpíchnutou do lahvičky. Opatrně otočte lahvičku se stříkačkou dnem vzhůru. Umístěte ji do výše očí (obr. 6). Obrázek 7 14
15 7. Tak jako předtím, posuňte opatrně jednu ruku dolů po lahvičce s rozpouštědlem, takže palcem a ukazovákem můžete pevně uchopit hrdlo lahvičky a dalšími prsty horní část stříkačky. Druhou rukou pomalu táhněte píst stříkačky směrem dolů a odeberte celý obsah lahvičky (1 ml). Abyste ponechal/a po celou dobu jehlu v tekutině, budete ji muset spolu s nasáváním tekutiny pomalu vytahovat přes gumovou zátku. Zkontrolujte, zda roztok ve stříkačce neobsahuje vzduchové bubliny. Pokud jsou bubliny přítomny, poklepávejte na tělo stříkačky do té doby, než se bubliny dostanou na horní konec stříkačky. Opatrně tlačte pístem, abyste vystříkl/a zpět do lahvičky pouze vzduchové bubliny. Zkontrolujte, zda ve stříkačce zůstává 1 ml roztoku a potom odstraňte jehlu z lahvičky (obr. 7). KROK 2. PODÁNÍ INJEKCE Zvolte si místo vpichu injekce na paži, horní části stehna, na břiše či na hýždích. Místa vpichu střídejte vždy po každé injekci. Může Vám pomoci, pokud si budete zaznamenávat místa vpichů při každodenním podávání přípravku SOMAVERT. Nepoužívejte k vpichu oblast, kde je vyrážka nebo poškozená kůže, případně pokud je přítomna krevní podlitina nebo boule. Místo vpichu očistěte tamponem s dezinfekční látkou nebo alkoholem a před podáním injekce nechejte kůži oschnout. Obrázek A a. Jednou rukou jemně vytvořte kožní řasu v místě, kam budete píchat injekci. Druhou rukou držte stříkačku a jedním plynulým pohybem vtlačte celou jehlu přímo do kůže (pod úhlem 90 stupňů) (obr. A). Obrázek B b. Pomalu tlačte píst stříkačky, až je stříkačka prázdná, přitom musí být jehla po celou dobu pod kůží. Uvolněte kožní řasu a vytáhněte jehlu (obr. B). 15
16 Obrázek C c. Oblast, kde byla injekce píchnuta, netřete. Může dojít k malému krvácení. Pokud je to potřebné, přiložte na plochu čistý a suchý bavlněný tampon a jemně ho tiskněte po dobu 1 nebo 2 minut nebo dokud se nezastaví krvácení (obr. C). Likvidace použitého materiálu NIKDY nepoužívejte opakovaně stříkačku ani jehlu. Jehlu a stříkačku zlikvidujte podle pokynů Vašeho lékaře, zdravotní sestry nebo lékárníka a v souladu s místními zdravotními a bezpečnostními předpisy. Na všechny otázky by měl odpovědět lékař, zdravotní sestra nebo lékárník, který(á) je seznámen(a) s přípravkem SOMAVERT. 16
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: Informace pro pacienta
 Příbalová informace: Informace pro pacienta CONBRIZA 20 mg potahované tablety Bazedoxifenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: Informace pro pacienta CONBRIZA 20 mg potahované tablety Bazedoxifenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje důležité
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje důležité
Příbalová informace: informace pro pacienta. Azomyr 0,5 mg/ml perorální roztok desloratadinum
 Příbalová informace: informace pro pacienta Azomyr 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta Azomyr 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CAMILIA perorální roztok v jednodávkovém obalu
 sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
Příbalová informace: informace pro uživatele. Vyndaqel 20 mg měkké tobolky tafamidisum
 Příbalová informace: informace pro uživatele Vyndaqel 20 mg měkké tobolky tafamidisum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro uživatele Vyndaqel 20 mg měkké tobolky tafamidisum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90
 Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro pacienta. Zurampic 200 mg potahované tablety lesinuradum
 Příbalová informace: informace pro pacienta Zurampic 200 mg potahované tablety lesinuradum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro pacienta Zurampic 200 mg potahované tablety lesinuradum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Nepoužívejte přípravek SOMAVERT: jestliže jste alergický(á) na pegvisomant nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
 Příbalová informace: informace pro uživatele SOMAVERT 10 mg prášek a rozpouštědlo pro injekční roztok SOMAVERT 15 mg prášek a rozpouštědlo pro injekční roztok SOMAVERT 20 mg prášek a rozpouštědlo pro injekční
Příbalová informace: informace pro uživatele SOMAVERT 10 mg prášek a rozpouštědlo pro injekční roztok SOMAVERT 15 mg prášek a rozpouštědlo pro injekční roztok SOMAVERT 20 mg prášek a rozpouštědlo pro injekční
Příbalová informace: informace pro pacienta. Zinforo 600 mg prášek pro koncentrát pro infuzní roztok ceftarolinum fosamilum
 Příbalová informace: informace pro pacienta Zinforo 600 mg prášek pro koncentrát pro infuzní roztok ceftarolinum fosamilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro pacienta Zinforo 600 mg prášek pro koncentrát pro infuzní roztok ceftarolinum fosamilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příbalová informace: informace pro pacienta. Fasturtec 1,5 mg/ml, prášek a rozpouštědlo pro koncentrát pro infuzní roztok rasburicasum
 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Fasturtec 1,5 mg/ml, prášek a rozpouštědlo pro koncentrát pro infuzní roztok rasburicasum Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Fasturtec 1,5 mg/ml, prášek a rozpouštědlo pro koncentrát pro infuzní roztok rasburicasum Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro pacienta. Integrilin 0,75 mg/ml infuzní roztok eptifibatidum
 Příbalová informace: informace pro pacienta Integrilin 0,75 mg/ml infuzní roztok eptifibatidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro pacienta Integrilin 0,75 mg/ml infuzní roztok eptifibatidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Používání Apidry v 10 ml injekčních lahvičkách
 NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
Návod k použití EDUKAČNÍ MATERIÁLY. mecasermin. Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex
 EDUKAČNÍ MATERIÁLY mecasermin Návod k použití Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
EDUKAČNÍ MATERIÁLY mecasermin Návod k použití Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro pacienta
 Příbalová informace: informace pro pacienta Trumenba injekční suspenze v předplněné injekční stříkačce Vakcína proti meningokokům skupiny B (rekombinantní, adsorbovaná) Tento přípravek podléhá dalšímu
Příbalová informace: informace pro pacienta Trumenba injekční suspenze v předplněné injekční stříkačce Vakcína proti meningokokům skupiny B (rekombinantní, adsorbovaná) Tento přípravek podléhá dalšímu
Příbalová informace: informace pro uživatele. Spinraza 12 mg injekční roztok. nusinersenum
 Příbalová informace: informace pro uživatele Spinraza 12 mg injekční roztok nusinersenum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro uživatele Spinraza 12 mg injekční roztok nusinersenum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bonviva 3 mg injekční roztok Acidum ibandronicum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bonviva 3 mg injekční roztok Acidum ibandronicum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bonviva 3 mg injekční roztok Acidum ibandronicum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE LYRICA 25 tvrdé tobolky LYRICA 50 tvrdé tobolky LYRICA 75 tvrdé tobolky LYRICA 100 tvrdé tobolky LYRICA 150 tvrdé tobolky LYRICA 200 tvrdé tobolky LYRICA 225
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE LYRICA 25 tvrdé tobolky LYRICA 50 tvrdé tobolky LYRICA 75 tvrdé tobolky LYRICA 100 tvrdé tobolky LYRICA 150 tvrdé tobolky LYRICA 200 tvrdé tobolky LYRICA 225
Příprava a podání injekce
 Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Příbalová informace: informace pro pacienta. Maltofer, 10 mg/ml sirup. polymaltosum ferricum
 sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: Informace pro uživatele. NovoThirteen 2 500 IU prášek pro přípravu injekčního roztoku s rozpouštědlem
 Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek pro přípravu injekčního roztoku s rozpouštědlem catridecacogum (rekombinantní koagulační faktor XIII) Tento přípravek podléhá dalšímu
Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek pro přípravu injekčního roztoku s rozpouštědlem catridecacogum (rekombinantní koagulační faktor XIII) Tento přípravek podléhá dalšímu
sp.zn. sukls107935/2012
 sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
Příbalová informace: informace pro pacienta. Lyrica 20 mg/ml perorální roztok pregabalinum
 Příbalová informace: informace pro pacienta Lyrica 20 mg/ml perorální roztok pregabalinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta Lyrica 20 mg/ml perorální roztok pregabalinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn. sukls110147/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA SOMATULINE AUTOGEL 60 mg, injekční roztok v předplněné stříkačce SOMATULINE AUTOGEL 90 mg, injekční roztok v předplněné stříkačce SOMATULINE
sp.zn. sukls110147/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA SOMATULINE AUTOGEL 60 mg, injekční roztok v předplněné stříkačce SOMATULINE AUTOGEL 90 mg, injekční roztok v předplněné stříkačce SOMATULINE
Příbalová informace: Informace pro uživatele. NovoThirteen IU prášek a rozpouštědlo pro injekční roztok
 Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek a rozpouštědlo pro injekční roztok catridecacogum (rekombinantní koagulační faktor XIII) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek a rozpouštědlo pro injekční roztok catridecacogum (rekombinantní koagulační faktor XIII) Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE. TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum
 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Nimenrix prášek pro injekční roztok a rozpouštědlo v předplněné injekční stříkačce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y Tento léčivý
Příbalová informace: informace pro uživatele Nimenrix prášek pro injekční roztok a rozpouštědlo v předplněné injekční stříkačce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y Tento léčivý
Příbalová informace: informace pro uživatele. Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum
 sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE. Galvus 50 mg tablety Vildagliptinum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE Galvus 50 mg tablety Vildagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, neţ začnete tento přípravek uţívat. - Ponechte si příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE Galvus 50 mg tablety Vildagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, neţ začnete tento přípravek uţívat. - Ponechte si příbalovou informaci
PŘÍLOHA III OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
 PŘÍLOHA III OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE 1 B. PŘÍBALOVÁ INFORMACE 2 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dasselta 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou
PŘÍLOHA III OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE 1 B. PŘÍBALOVÁ INFORMACE 2 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dasselta 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: Informace pro pacienta. Aerius 0,5 mg/ml perorální roztok desloratadinum
 Příbalová informace: Informace pro pacienta Aerius 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: Informace pro pacienta Aerius 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bronchostop sirup. Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt
 Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro pacienta. TAGRISSO 40 mg potahované tablety TAGRISSO 80 mg potahované tablety osimertinibum
 Příbalová informace: informace pro pacienta TAGRISSO 40 mg potahované tablety TAGRISSO 80 mg potahované tablety osimertinibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro pacienta TAGRISSO 40 mg potahované tablety TAGRISSO 80 mg potahované tablety osimertinibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Nimenrix prášek pro přípravu injekčního roztoku s rozpouštědlem v ampulce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y Tento léčivý přípravek
Příbalová informace: informace pro uživatele Nimenrix prášek pro přípravu injekčního roztoku s rozpouštědlem v ampulce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y Tento léčivý přípravek
Příbalová informace: Informace pro uživatele. Ebixa 5 mg/dávka, perorální roztok Memantini hydrochloridum
 Příbalová informace: Informace pro uživatele Ebixa 5 mg/dávka, perorální roztok Memantini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: Informace pro uživatele Ebixa 5 mg/dávka, perorální roztok Memantini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
prášek pro infuzní roztok
 sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Vyndaqel 20 mg měkké tobolky tafamidisi megluminum
 Příbalová informace: informace pro uživatele Vyndaqel 20 mg měkké tobolky tafamidisi megluminum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete
Příbalová informace: informace pro uživatele Vyndaqel 20 mg měkké tobolky tafamidisi megluminum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
Příbalová informace: Informace pro uživatele
 Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze v jednodávkové injekční lahvičce Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně
Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze v jednodávkové injekční lahvičce Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele CELVAPAN injekční suspenze Vakcína proti chřipce (H1N1)v (celý virion, namnožená na buňkách Vero, inaktivovaná) Přečtěte si pozorně
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele CELVAPAN injekční suspenze Vakcína proti chřipce (H1N1)v (celý virion, namnožená na buňkách Vero, inaktivovaná) Přečtěte si pozorně
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Gardasil 9 injekční suspenze v předplněné injekční stříkačce 9valentní očkovací látka proti lidskému papilomaviru (rekombinantní, adsorbovaná) Tento přípravek
Příbalová informace: informace pro uživatele Gardasil 9 injekční suspenze v předplněné injekční stříkačce 9valentní očkovací látka proti lidskému papilomaviru (rekombinantní, adsorbovaná) Tento přípravek
Příbalová informace: Informace pro uživatele. Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná)
 Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
sp. zn. sukls180859/2015
 sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
Příbalová informace: informace pro uživatele. Ferriprox 500 mg potahované tablety Deferipronum
 Příbalová informace: informace pro uživatele Ferriprox 500 mg potahované tablety Deferipronum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatele Ferriprox 500 mg potahované tablety Deferipronum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro pacienta. Fasenra 30 mg injekční roztok v předplněné injekční stříkačce benralizumabum
 Příbalová informace: informace pro pacienta Fasenra 30 mg injekční roztok v předplněné injekční stříkačce benralizumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: informace pro pacienta Fasenra 30 mg injekční roztok v předplněné injekční stříkačce benralizumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: Informace pro pacienta. Aerius 5 mg potahované tablety desloratadinum
 Příbalová informace: Informace pro pacienta Aerius 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: Informace pro pacienta Aerius 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE. OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas
 PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA)
 Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Příbalová informace: informace pro uživatele. Baraclude 0,05 mg/ml perorální roztok entecavirum
 Příbalová informace: informace pro uživatele Baraclude 0,05 mg/ml perorální roztok entecavirum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatele Baraclude 0,05 mg/ml perorální roztok entecavirum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro pacienta
 Příbalová informace: informace pro pacienta Briviact 10 mg potahované tablety Briviact 25 mg potahované tablety Briviact 50 mg potahované tablety Briviact 75 mg potahované tablety Briviact 100 mg potahované
Příbalová informace: informace pro pacienta Briviact 10 mg potahované tablety Briviact 25 mg potahované tablety Briviact 50 mg potahované tablety Briviact 75 mg potahované tablety Briviact 100 mg potahované
Dacogen 50 mg prášek pro koncentrát pro infuzní roztok Decitabinum
 Příbalová informace: informace pro uživatele Dacogen 50 mg prášek pro koncentrát pro infuzní roztok Decitabinum Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: informace pro uživatele Dacogen 50 mg prášek pro koncentrát pro infuzní roztok Decitabinum Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
1. Co je přípravek Maltofer Fol žvýkací tablety a k čemu se používá. Maltofer Fol se používá k léčbě a prevenci nedostatku železa v organismu.
 sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
Příbalová informace: Informace pro pacienta. Aerius 5 mg tablety dispergovatelné v ústech desloratadinum
 Příbalová informace: Informace pro pacienta Aerius 5 mg tablety dispergovatelné v ústech desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: Informace pro pacienta Aerius 5 mg tablety dispergovatelné v ústech desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro pacienta. Forxiga 5 mg potahované tablety Forxiga 10 mg potahované tablety dapagliflozinum
 Příbalová informace: informace pro pacienta Forxiga 5 mg potahované tablety Forxiga 10 mg potahované tablety dapagliflozinum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: informace pro pacienta Forxiga 5 mg potahované tablety Forxiga 10 mg potahované tablety dapagliflozinum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
Příbalová informace: informace pro uživatele. Spinraza 12 mg injekční roztok. nusinersenum
 Příbalová informace: informace pro uživatele Spinraza 12 mg injekční roztok nusinersenum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro uživatele Spinraza 12 mg injekční roztok nusinersenum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro pacienta. ANACID 258 mg/388 mg perorální suspenze. Magnesii hydroxidum, Algeldrati suspensio
 sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 35 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Menveo prášek a roztok pro přípravu injekčního roztoku Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si
B. PŘÍBALOVÁ INFORMACE 35 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Menveo prášek a roztok pro přípravu injekčního roztoku Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si
Příbalová informace: informace pro pacienta. Ristaben 50 mg potahované tablety Sitagliptinum
 Příbalová informace: informace pro pacienta Ristaben 50 mg potahované tablety Sitagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta Ristaben 50 mg potahované tablety Sitagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: Informace pro uživatele. Bridion 100 mg/ml injekční roztok sugammadexum
 Příbalová informace: Informace pro uživatele Bridion 100 mg/ml injekční roztok sugammadexum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám bude přípravek podán, protože obsahuje pro Vás
Příbalová informace: Informace pro uživatele Bridion 100 mg/ml injekční roztok sugammadexum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám bude přípravek podán, protože obsahuje pro Vás
Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná), které nejsou uvedeny v
 INFORMACE PRO UŽIVATELE Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) vakcínou. Máte-l, které nejsou uvedeny v V : 1. Co je vakcína Synflorix a k 2. nflorix. 3. Jak se vakcína Synflorix
INFORMACE PRO UŽIVATELE Pneumokoková polysacharidová konjugovaná vakcína (adsorbovaná) vakcínou. Máte-l, které nejsou uvedeny v V : 1. Co je vakcína Synflorix a k 2. nflorix. 3. Jak se vakcína Synflorix
Příbalová informace: Informace pro uživatele Maltofer 50 mg/ml, perorální kapky, roztok. železo ve formě polymaltosum ferricum
 sp.zn. sukls238918/2016 Příbalová informace: Informace pro uživatele Maltofer 50 mg/ml, perorální kapky, roztok železo ve formě polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls238918/2016 Příbalová informace: Informace pro uživatele Maltofer 50 mg/ml, perorální kapky, roztok železo ve formě polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Relistor 12 mg/0,6 ml injekční roztok Methylnaltrexonii bromidum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Relistor 12 mg/0,6 ml injekční roztok Methylnaltrexonii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Relistor 12 mg/0,6 ml injekční roztok Methylnaltrexonii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
Příbalová informace: informace pro pacienta. Zerbaxa 1 g/0,5 g prášek pro koncentrát pro infuzní roztok ceftolozanum/tazobactamum
 Příbalová informace: informace pro pacienta Zerbaxa 1 g/0,5 g prášek pro koncentrát pro infuzní roztok ceftolozanum/tazobactamum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro pacienta Zerbaxa 1 g/0,5 g prášek pro koncentrát pro infuzní roztok ceftolozanum/tazobactamum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro pacienta. Maltofer 50 mg/ml perorální kapky, roztok
 sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE. Příbalová informace: Informace pro uživatele
 PŘÍBALOVÁ INFORMACE Příbalová informace: Informace pro uživatele ReFacto AF 250 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 500 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 1000
PŘÍBALOVÁ INFORMACE Příbalová informace: Informace pro uživatele ReFacto AF 250 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 500 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 1000
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
Příbalová informace: informace pro uživatele AESCIN-TEVA. 20 mg, enterosolventní tablety. escinum alfa
 sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE. Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13 valentní, adsorbovaná)
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13 valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13 valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele ZOSTAVAX Prášek a rozpouštědlo pro injekční suspenzi očkovací látka proti pásovému oparu (herpes zoster) (živá) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele ZOSTAVAX Prášek a rozpouštědlo pro injekční suspenzi očkovací látka proti pásovému oparu (herpes zoster) (živá) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace informace pro uživatele. RILUTEK 50 mg potahované tablety Riluzolum
 PŘÍBALOVÁ INFORMACE Příbalová informace informace pro uživatele RILUTEK 50 mg potahované tablety Riluzolum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat, protože
PŘÍBALOVÁ INFORMACE Příbalová informace informace pro uživatele RILUTEK 50 mg potahované tablety Riluzolum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat, protože
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum)
 sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
Příbalová informace: informace pro pacienta. Zinforo 600 mg prášek pro koncentrát pro infuzní roztok ceftarolinum fosamilum
 Příbalová informace: informace pro pacienta Zinforo 600 mg prášek pro koncentrát pro infuzní roztok ceftarolinum fosamilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro pacienta Zinforo 600 mg prášek pro koncentrát pro infuzní roztok ceftarolinum fosamilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Nimenrix prášek pro injekční roztok a rozpouštědlo v ampulce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele Nimenrix prášek pro injekční roztok a rozpouštědlo v ampulce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele ZOSTAVAX Prášek a rozpouštědlo pro injekční suspenzi očkovací látka proti pásovému oparu (herpes zoster) (živá) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele ZOSTAVAX Prášek a rozpouštědlo pro injekční suspenzi očkovací látka proti pásovému oparu (herpes zoster) (živá) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: Informace pro pacienta
 sp.zn.sukls98480/2015 Příbalová informace: Informace pro pacienta Mucoplant břečťanový sirup proti kašli sirup Léčivá látka: Hederae helicis folii extractum siccum (suchý extrakt z břečťanového listu)
sp.zn.sukls98480/2015 Příbalová informace: Informace pro pacienta Mucoplant břečťanový sirup proti kašli sirup Léčivá látka: Hederae helicis folii extractum siccum (suchý extrakt z břečťanového listu)
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace Informace pro uživatele
 Příbalová informace Informace pro uživatele Trobalt 50 mg potahované tablety Trobalt 100 mg potahované tablety Trobalt 200 mg potahované tablety Trobalt 300 mg potahované tablety Trobalt 400 mg potahované
Příbalová informace Informace pro uživatele Trobalt 50 mg potahované tablety Trobalt 100 mg potahované tablety Trobalt 200 mg potahované tablety Trobalt 300 mg potahované tablety Trobalt 400 mg potahované
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret
 sp.zn.sukls240326/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn.sukls240326/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
PANTOLOC Control 20 mg enterosolventní tablety Pantoprazolum
 PANTOLOC Control 20 mg enterosolventní tablety Pantoprazolum - - - Musíte se poradit s po 2 týdnech. - Bez porady s - V 1. Co je PANTOLOC Control a k 2. 3. Jak se PANTOLOC Control používá 4. Možné nežádoucí
PANTOLOC Control 20 mg enterosolventní tablety Pantoprazolum - - - Musíte se poradit s po 2 týdnech. - Bez porady s - V 1. Co je PANTOLOC Control a k 2. 3. Jak se PANTOLOC Control používá 4. Možné nežádoucí
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SUSTANON 250 250 mg/ml, injekční roztok Testosteroni
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SUSTANON 250 250 mg/ml, injekční roztok Testosteroni
Příbalová informace: Informace pro uživatele. Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná)
 Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: Informace pro uživatele. Prevenar 13 injekční suspenze
 Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. Maltofer 10 mg/ml sirup
 sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Sp.zn.sukls133559/2018
 Sp.zn.sukls133559/2018 Příbalová informace: informace pro uživatele Betahistin Actavis 24 mg tablety betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls133559/2018 Příbalová informace: informace pro uživatele Betahistin Actavis 24 mg tablety betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa
 Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Zvláštní opatrnosti při použití KOGENATE Bayer 250 IU je zapotřebí
 Příbalová informace: informace pro uživatele KOGENATE Bayer 250 IU Prášek a rozpouštědlo pro injekční roztok Rekombinantní koagulační faktor VIII (octocogum alfa) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele KOGENATE Bayer 250 IU Prášek a rozpouštědlo pro injekční roztok Rekombinantní koagulační faktor VIII (octocogum alfa) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele. Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum
 sp.zn. sukls154670/2013 Příbalová informace: informace pro uživatele Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls154670/2013 Příbalová informace: informace pro uživatele Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: Informace pro uživatele
 Příbalová informace: Informace pro uživatele Adempas 0,5 mg potahované tablety Adempas 1 mg potahované tablety Adempas 1,5 mg potahované tablety Adempas 2 mg potahované tablety Adempas 2,5 mg potahované
Příbalová informace: Informace pro uživatele Adempas 0,5 mg potahované tablety Adempas 1 mg potahované tablety Adempas 1,5 mg potahované tablety Adempas 2 mg potahované tablety Adempas 2,5 mg potahované
