B. PŘÍBALOVÁ INFORMACE
|
|
|
- Eduard Kopecký
- před 6 lety
- Počet zobrazení:
Transkript
1 B. PŘÍBALOVÁ INFORMACE 1
2 Příbalová informace: informace pro uživatele TAKHZYRO 300 mg injekční roztok lanadelumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Jak hlásit nežádoucí účinky je popsáno v závěru bodu 4. Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje. Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry. Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy. Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4. Co naleznete v této příbalové informaci 1. Co je přípravek TAKHZYRO a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete přípravek TAKHZYRO používat 3. Jak se přípravek TAKHZYRO používá 4. Možné nežádoucí účinky 5. Jak přípravek TAKHZYRO uchovávat 6. Obsah balení a další informace 7. Návod k použití 1. Co je přípravek TAKHZYRO a k čemu se používá Přípravek TAKHZYRO obsahuje léčivou látku lanadelumab. K čemu se přípravek TAKHZYRO používá TAKHZYRO je léčivý přípravek používaný u dospělých a dospívajících ve věku 12 let a starších k prevenci atak angioedému, u pacientů s hereditárním angioedémem (HAE). Co je hereditární angioedém (HAE) HAE je onemocnění, které se dědí v rodině. Při tomto onemocnění ve Vaší krvi není dostatek bílkoviny zvané inhibitor C 1 nebo inhibitor C1 nefunguje správně. To vede k příliš velkému množství plazmatického kalikreinu, který zase produkuje vyšší úrovně bradykininu v krevním oběhu. Příliš mnoho bradykininu způsobuje příznaky HAE jako otok a bolest rukou a nohou, obličeje, očních víček, rtů nebo jazyka, hrtanu (laryngu), což může ztěžovat dýchání, pohlavních orgánů. Jak přípravek TAKHZYRO funguje Přípravek TAKHZYRO je typ bílkoviny, který blokuje aktivitu plazmatického kalikreinu. To pomáhá snížit množství bradykininu ve Vašem cévním oběhu a předchází příznakům HAE. 2
3 2. Čemu musíte věnovat pozornost, než začnete přípravek TAKHZYRO používat Nepoužívejte přípravek TAKHZYRO: jestliže jste alergický(á) na lanadelumab nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6). Upozornění a opatření Před použitím přípravku TAKHZYRO se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou. Pokud se u Vás vyskytne závažná alergická reakci na přípravek TAKHZYRO s příznaky, jako je vyrážka, tlak na hrudi, sípání nebo rychlý srdeční tep, ihned informujte svého lékaře, lékárníka nebo zdravotní sestru. Vedení záznamů Důrazně se doporučuje, abyste si při každém podání dávky přípravku TAKHZYRO zapsali název a číslo šarže léku. Je to proto, abyste měli záznam o použitých šaržích. Laboratorní testy Před absolvováním laboratorních testů ke změření srážlivosti Vaší krve svému lékaři sdělte, že užíváte přípravek TAKHZYRO. Je to proto, že přípravek Takzhyro v krvi může narušovat některé laboratorní testy, což vede k nepřesným výsledkům. Děti a dospívající Přípravek TAKHZYRO se nedoporučuje používat u dětí mladších 12 let. Je to proto, že v této věkové skupině nebyl zkoumán. Další léčivé přípravky a přípravek TAKHZYRO Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Není známo, že by přípravek TAKHZYRO ovlivňoval jiné léky nebo byl ovlivňován jinými léky. Těhotenství a kojení Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete používat přípravek TAKHZYRO. Existují pouze omezené informace o bezpečnosti použití přípravku TAKHZYRO během těhotenství a kojení. Z preventivních důvodů je vhodné se podávání lanadelumabu v těhotenství a během kojení vyhnout. Váš lékař s Vámi prodiskutuje rizika a přínosy užívání tohoto léku. Řízení dopravních prostředků a obsluha strojů Tento lék má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje. Přípravek TAKHZYRO obsahuje sodík Přípravek obsahuje méně než 1 mmol sodíku (23 mg) na jeden ml roztoku, to znamená, že je v podstatě bez sodíku. 3
4 3. Jak se přípravek TAKHZYRO používá Přípravek TAKHZYRO se dodává v jednorázových injekčních lahvičkách jako roztok připravený k použití. Vaše léčba bude zahájena a řízena pod dohledem lékaře, který má zkušenosti s péčí o pacienty s HAE. Vždy používejte tento přípravek přesně v souladu s příbalovou informací, nebo podle pokynů svého lékaře, lékárníka nebo zdravotní sestry. Pokud si nejste jistý(á) nebo máte nějaké další otázky ohledně používání tohoto přípravku, poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou. Kolik přípravku TAKHZYRO používat Doporučená počáteční dávka je 300 mg každé 2 týdny. Pokud jste dlouhou dobu neprodělal(a) žádnou ataku, Váš lékař může dávku změnit na 300 mg každé 4 týdny, zejména pokud máte nízkou tělesnou hmotnost. Jak přípravek TAKHZYRO aplikovat Pokud si přípravek TAKHZYRO aplikujete sami nebo pokud ho aplikuje Váš pečovatel, musíte si Vy nebo Váš pečovatel pečlivě přečíst pokyny uvedené v části 7 Návod k použití a dodržovat je. Přípravek TAKHZYRO je určen k injekci pod kůži ( subkutánní injekce ). Injekci můžete aplikovat buď Vy, nebo pečovatel. Lékař, lékárník nebo zdravotní sestra by Vám před jeho prvním použitím měli ukázat, jak správně přípravek TAKHZYRO připravit a aplikovat. Dokud nebudete proškoleni v injekční aplikaci přípravku, neaplikujte injekci sobě ani nikomu jinému. Vpíchněte jehlu do tukové tkáně na břiše, stehně nebo horní části paže. Při každé injekci přípravku použijte jiné místo. Každou injekční lahvičku přípravku TAKHZYRO použijte pouze jednou. Jestliže jste použil(a) více přípravku TAKHZYRO, než jste měl(a) Pokud užijete příliš mnoho přípravku TAKHZYRO, informujte svého lékaře, lékárníka nebo zdravotní sestru. Jestliže jste zapomněl(a) použít přípravek TAKHZYRO Pokud vynecháte dávku přípravku TAKHZYRO, aplikujte svou dávku co nejdříve, ale mezi každou dávkou musí být nejméně 10 dnů. Pokud si nejste jistý(jistá), kdy přípravek TAKHZYRO po vynechání dávky aplikovat, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry. Jestliže jste přestal(a) používat přípravek TAKHZYRO Je důležité, abyste stále aplikoval(a) přípravek TAKHZYRO podle pokynů svého lékaře, i když se budete cítit lépe. Máte-li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry. 4. Možné nežádoucí účinky Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. 4
5 Pokud se u Vás vyskytne závažná alergická reakci na přípravek TAKHZYRO s příznaky, jako je vyrážka, tlak na hrudi, sípání nebo rychlý srdeční tep, ihned informujte svého lékaře, lékárníka nebo zdravotní sestru. Pokud si všimnete kterýchkoli z následujících vedlejších účinků, informujte svého lékaře, lékárníka nebo zdravotní sestru. Velmi časté (mohou postihnout více než 1 z 10 osob): Reakce na místě, kam byla aplikována injekce k příznakům patří bolest, zarudnutí kůže, podlitina, nepohodlí, otok, krvácení, svědění, ztvrdnutí kůže, brnění, teplo a vyrážka. Časté (mohou postihnout až 1 z 10 osob): Alergické reakce včetně svědění, nepohodlí a brnění jazyka Závratě, pocit na omdlení Vystouplá kožní vyrážka Bolest svalů Krevní testy ukazující změny na játrech Hlášení nežádoucích účinků Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku. 5. Jak přípravek TAKHZYRO uchovávat Uchovávejte tento přípravek mimo dohled a dosah dětí. Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na štítku za EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Uchovávejte v chladničce (2 C 8 C). Chraňte před mrazem. Injekční lahvičku uchovávejte v krabičce, aby byl přípravek chráněn před světlem. Injekční lahvičky lze uchovávat při teplotách nižších než 25 C po jednorázovou dobu 14 dnů, ale nikoli po datu použitelnosti. Po uchovávání při pokojové teplotě nevracejte přípravek TAKHZYRO do chladničky. Nepoužívejte tento přípravek, pokud si všimnete známek snížené jakosti, jako jsou částice v injekční lahvičce nebo změněná barva injekčního roztoku. Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí. 5
6 6. Obsah balení a další informace Co přípravek TAKHZYRO obsahuje Léčivou látkou je lanadelumab. Každá injekční lahvička obsahuje lanadelumabum 300 mg ve 2 ml. Dalšími složkami jsou dihydrát hydrogenfosforečnanu sodného, monohydrát kyseliny citrónové, histidin, chlorid sodný, polysorbát 80 a voda pro injekci viz část 2 Přípravek TAKHZYRO obsahuje sodík Jak přípravek TAKHZYRO vypadá a co obsahuje toto balení Přípravek TAKHZYRO se dodává jako čirý, bezbarvý až světle žlutý injekční roztok ve skleněné injekční lahvičce. Přípravek TAKHZYRO je k dispozici jako jednotlivé balení obsahující injekční lahvičku o objemu 2 ml a vícenásobné balení obsahující 2 nebo 6 krabiček, přičemž každá obsahuje 1 injekční lahvičku. Na trhu nemusí být všechny velikosti balení. Každé balení obsahuje také následující položky: Prázdná stříkačka o objemu 3 ml Jehla o velikosti 18 G s tupou špičkou pro přístup do injekční lahvičky Jehla o velikosti 27 G ½ palce (0,4 13 mm) s ostrou špičkou pro aplikaci (injekci). Držitel rozhodnutí o registraci a výrobce Shire Pharmaceuticals Ireland Limited Blocks 2 & 3 Miesian Plaza Baggot Street Lower Dublin 2 IRSKO Tel: +44(0) medinfoemea@shire.com Tato příbalová informace byla naposledy revidována 03/2019. Další zdroje informací Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky Na těchto stránkách naleznete též odkazy na další webové stránky týkající se vzácných onemocnění a jejich léčby. Na webových stránkách Evropské agentury pro léčivé přípravky je tato příbalová informace k dispozici ve všech úředních jazycích EU/EHP. 6
7 7. Návod k použití Je nutno přečíst si podrobné pokyny pro aplikaci injekcí přípravku TAKHZYRO, porozumět jim a dodržovat je krok po kroku. Pokud máte jakékoli otázky, kontaktujte svého lékaře, lékárníka nebo zdravotní sestru. Kromě injekční lahvičky každé balení přípravku TAKHZYRO také obsahuje: Jednu prázdnou stříkačku o objemu 3 ml. Jednu jehlu o velikosti 18 G s tupou špičkou pro přístup do injekční lahvičky. Používá se k natažení roztoku přípravku z injekční lahvičky do stříkačky. Jednu jehlu o velikosti 27 G ½ palce (0,4 13 mm) s ostrou špičkou pro injekci. Používá se k injekci pod kůži (subkutánní). Používejte pouze stříkačky, jehly s tupou špičkou pro přístup do injekční lahvičky a jehly s ostrou špičkou pro injekci v tomto balení nebo takové, které Vám předepsal lékař. Stříkačky, jehly s tupou špičkou pro přístup do injekční lahvičky a jehly s ostrou špičkou pro injekci používejte pouze jednou. Veškeré použité stříkačky a jehly vložte do nádoby na ostré předměty. Nepoužívejte stříkačky, jehly s tupou špičkou pro přístup do injekční lahvičky a jehly s ostrou špičkou pro injekci, které se zdají být poškozené. Také budete potřebovat: ubrousky s alkoholem, nádobu na ostré předměty na použité injekční lahvičky, jehly a stříkačky. Materiály můžete získat od svého lékaře, lékárníka nebo zdravotní sestry. Injekci přípravku TAKHZYRO lze shrnout do 5 kroků: 1. Připravte si injekční lahvičku s přípravkem TAKHZYRO 2. Připojte ke stříkačce jehlu s tupou špičkou pro přístup do injekční lahvičky 3. Natáhněte přípravek TAKHZYRO do stříkačky a vyměňte jehlu za jehlu s ostrou špičkou pro injekci 4. Vyberte a připravte místo injekce 5. Aplikujte přípravek TAKHZYRO 7
8 Krok 1: Připravte si injekční lahvičku s přípravkem TAKHZYRO a) Vyjměte injekční lahvičku z chladničky 15 minut před použitím, aby před přípravou injekce dosáhla pokojové teploty (15 C až 25 C). b) Před přípravou dávky očistěte pracovní plochu a umyjte si ruce. Po umytí rukou se před aplikací injekce nedotýkejte žádného povrchu nebo svého těla, zejména obličeje. c) Vezměte přípravek TAKHZYRO a potřebný materiál a položte je na dobře osvětlenou pracovní plochu. d) Vyjměte injekční lahvičku z obalu. Pokud na injekční lahvičce není kryt překrývající zátku, injekční lahvičku nepoužívejte. e) Lahvičku 3krát až 5krát opatrně obraťte, aby se roztok promíchal. Injekční lahvičkou netřepejte, protože to může způsobit vznik pěny. f) Zkontrolujte roztok v injekční lahvičce, zda neobsahuje částice nebo zda není neobvykle zbarvený (běžně je bezbarvý nebo světle žlutý). Pokud roztok obsahuje částice nebo má změněnou barvu, nepoužívejte ho. Důležité: Netřepejte. g) Sundejte z injekční lahvičky plastový kryt. Nevyndávejte z injekční lahvičky pryžovou zátku. h) Položte injekční lahvičku na rovný povrch. Očistěte pryžovou zátku injekční lahvičky alkoholovým ubrouskem a nechte ji uschnout. 8
9 Krok 2: Připojte ke stříkačce jehlu s tupou špičkou pro přístup do injekční lahvičky a) Na stříkačku o objemu 3 ml našroubujte jehlu o velikosti 18 G s tupou špičkou pro přístup do injekční lahvičky. Důležité: Při připojování jehly ke stříkačce nesundávejte krytku jehly. b) Zatáhněte za píst a naplňte stříkačku stejným množstvím vzduchu, jako je množství roztoku v injekční lahvičce. c) Stáhněte krytku jehly přímo ze stříkačky, aniž byste se dotkli jehly. Netahejte za píst. 9
10 Krok 3: Natáhněte přípravek TAKHZYRO do stříkačky a vyměňte jehlu za jehlu s ostrou špičkou pro injekci a) Vložte jehlu do středu pryžové zátky. b) Stlačením pístu vstříkněte vzduch do injekční lahvičky a držte píst stlačený. c) Pomalu otočte injekční lahvičku s připojenou jehlou a stříkačkou vzhůru nohama. Zatáhněte za píst a natáhněte celou dávku z injekční lahvičky. Důležité: Dbejte na to, aby špička jehly byla ponořena do kapaliny, aby při vytažení pístu nedošlo k nasátí vzduchu. d) Odstraňte velké vzduchové bubliny tak, že prsty opatrně poklepete na stříkačku, aby bubliny vystoupaly do horní části stříkačky. Pomalu stlačte píst a vytlačujte vzduch zpět do lahvičky, dokud roztok nedosáhne horní strany stříkačky. Opakujte tyto kroky, dokud nebudou velké vzduchové bubliny odstraněny. 10
11 e) Aniž byste vytáhli jehlu z injekční lahvičky, odšroubujte stříkačku tak, že uchopíte horní část jehly a otočíte stříkačkou proti směru hodinových ručiček. Vraťte stříkačku do vzpřímené polohy. f) Vložte jehlu o velikosti 18 G s tupou špičkou pro přístup do injekční lahvičky a injekční lahvičku do nádoby na ostré předměty. g) Našroubujte na stříkačku jehlu o velikosti 27 G ½ palce (0,4 13 mm) s ostrou špičkou pro injekci. Důležité: Při připojování jehly ke stříkačce nesundávejte krytku jehly. Nepoužívejte jehlu s tupou špičkou pro přístup do injekční lahvičky k aplikaci přípravku TAKHZYRO, protože by to mohlo způsobit bolest a krvácení. 11
12 Krok 4: Vyberte a připravte místo injekce a) Vyberte místo injekce na břiše, stehnu nebo horní části paže. Injekci je nutno aplikovat podkožně. b) Očistěte místo injekce alkoholovým ubrouskem a nechte pokožku zcela uschnout. Důležité: Je důležité používat různá místa injekce, aby pokožka zůstala zdravá. Místo, které vyberete pro injekci, by mělo být nejméně 5 cm od jakýchkoli jizev nebo pupku. Nevybírejte místo, které je zhmožděné, oteklé nebo bolestivé. Horní zevní část paže se nedoporučuje, pokud si injekci aplikujete sám/sama. 12
13 Krok 5: Aplikujte přípravek TAKHZYRO c) Stáhněte krytku jehly přímo ze stříkačky, aniž byste se dotkli jehly. Netahejte za píst. Nedotýkejte se špičky jehly a zabraňte jejímu kontaktu s jakýmkoli jiným povrchem. Důležité: Aplikujte přípravek TAKHZYRO do 2 hodin od přípravy stříkačky s dávkou při pokojové teplotě. Případně můžete stříkačku s dávkou vložit do chladničky o teplotě 2 C až 8 C a musíte ji použít do 8 hodin. d) Jemně stiskněte přibližně 3 cm pokožky na vyčištěném místě pro injekci a vpíchněte do ní jehlu. Důležité: Je nutno aplikovat injekci do podkožního prostoru, který není příliš mělký (vrstva kůže) nebo příliš hluboký (sval). e) Pomalu stlačujte píst, dokud nebude vstříknut veškerý přípravek. Uvolněte kožní záhyb a opatrně vyjměte jehlu. Na jehlu už nenasazujte krytku. f) Vložte jehlu o velikosti 27 G ½ palce (0,4 13 mm) s ostrou špičkou pro injekci a stříkačku do nádoby na ostré předměty. * 13
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CAMILIA perorální roztok v jednodávkovém obalu
 sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele AESCIN-TEVA. 20 mg, enterosolventní tablety. escinum alfa
 sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls107935/2012
 sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
prášek pro infuzní roztok
 sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: Informace pro uživatele. NovoThirteen IU prášek a rozpouštědlo pro injekční roztok
 Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek a rozpouštědlo pro injekční roztok catridecacogum (rekombinantní koagulační faktor XIII) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek a rozpouštědlo pro injekční roztok catridecacogum (rekombinantní koagulační faktor XIII) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: Informace pro uživatele. NovoThirteen 2 500 IU prášek pro přípravu injekčního roztoku s rozpouštědlem
 Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek pro přípravu injekčního roztoku s rozpouštědlem catridecacogum (rekombinantní koagulační faktor XIII) Tento přípravek podléhá dalšímu
Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek pro přípravu injekčního roztoku s rozpouštědlem catridecacogum (rekombinantní koagulační faktor XIII) Tento přípravek podléhá dalšímu
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bronchostop sirup. Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt
 Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro pacienta. Maltofer, 10 mg/ml sirup. polymaltosum ferricum
 sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: informace pro uživatele. VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa
 Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro pacienta. ANACID 258 mg/388 mg perorální suspenze. Magnesii hydroxidum, Algeldrati suspensio
 sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele. Firazyr 30 mg injekční roztok v předplněné injekční stříkačce Icatibantum
 Příbalová informace: informace pro uživatele Firazyr 30 mg injekční roztok v předplněné injekční stříkačce Icatibantum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele Firazyr 30 mg injekční roztok v předplněné injekční stříkačce Icatibantum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum
 sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
Příbalová informace: informace pro uživatele
 sp.zn. sukls136451/2013 a sp.zn. sukls36933/2014 Příbalová informace: informace pro uživatele Aprokam50 mg prášek pro injekční roztok cefuroximum Přečtěte si pozorně celou příbalovou informaci dříve, než
sp.zn. sukls136451/2013 a sp.zn. sukls36933/2014 Příbalová informace: informace pro uživatele Aprokam50 mg prášek pro injekční roztok cefuroximum Přečtěte si pozorně celou příbalovou informaci dříve, než
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90
 Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: Informace pro uživatele Maltofer 50 mg/ml, perorální kapky, roztok. železo ve formě polymaltosum ferricum
 sp.zn. sukls238918/2016 Příbalová informace: Informace pro uživatele Maltofer 50 mg/ml, perorální kapky, roztok železo ve formě polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls238918/2016 Příbalová informace: Informace pro uživatele Maltofer 50 mg/ml, perorální kapky, roztok železo ve formě polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
1. Co je přípravek Maltofer Fol žvýkací tablety a k čemu se používá. Maltofer Fol se používá k léčbě a prevenci nedostatku železa v organismu.
 sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Venoruton gel 20 mg/g, gel oxerutina
 sp.zn. sukls196201/2016 a sp.zn. sukls192934/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Venoruton gel 20 mg/g, gel oxerutina Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn. sukls196201/2016 a sp.zn. sukls192934/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Venoruton gel 20 mg/g, gel oxerutina Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum)
 sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp. zn. sukls180859/2015
 sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
Sp.zn.sukls265114/2016 a sp.zn.sukls274542/2016
 Sp.zn.sukls265114/2016 a sp.zn.sukls274542/2016 Příbalová informace: informace pro pacienta Ajax pomeranč a med 3 mg pastilky benzydamini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls265114/2016 a sp.zn.sukls274542/2016 Příbalová informace: informace pro pacienta Ajax pomeranč a med 3 mg pastilky benzydamini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. Maltofer 10 mg/ml sirup
 sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Používání Apidry v 10 ml injekčních lahvičkách
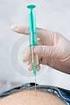 NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. Soolantra 10 mg/g krém ivermectinum
 Sp.zn. sukls63811/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Soolantra 10 mg/g krém ivermectinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Sp.zn. sukls63811/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Soolantra 10 mg/g krém ivermectinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Návod k použití EDUKAČNÍ MATERIÁLY. mecasermin. Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex
 EDUKAČNÍ MATERIÁLY mecasermin Návod k použití Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
EDUKAČNÍ MATERIÁLY mecasermin Návod k použití Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro pacienta. Maltofer 50 mg/ml perorální kapky, roztok
 sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příprava a podání injekce
 Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Příbalová informace: informace pro uživatele. Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum
 sp.zn. sukls154670/2013 Příbalová informace: informace pro uživatele Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls154670/2013 Příbalová informace: informace pro uživatele Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Alpicort 2 mg/ml + 4 mg/ml kožní roztok prednisolonum, acidum salicylicum
 sp.zn. sukls176806/2014 Příbalová informace: informace pro uživatele Alpicort 2 mg/ml + 4 mg/ml kožní roztok prednisolonum, acidum salicylicum Přečtěte si pozorně celou příbalovou informaci dříve, než
sp.zn. sukls176806/2014 Příbalová informace: informace pro uživatele Alpicort 2 mg/ml + 4 mg/ml kožní roztok prednisolonum, acidum salicylicum Přečtěte si pozorně celou příbalovou informaci dříve, než
Příbalová informace: informace pro uživatele. Strensiq 40 mg/ml injekční roztok (12 mg/0,3 ml 18 mg/0,45 ml 28 mg/0,7 ml 40 mg/1,0 ml) Asfotasum alfa
 B. PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro uživatele Strensiq 40 mg/ml injekční roztok (12 mg/0,3 ml 18 mg/0,45 ml 28 mg/0,7 ml 40 mg/1,0 ml) Asfotasum alfa Tento léčivý přípravek podléhá
B. PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro uživatele Strensiq 40 mg/ml injekční roztok (12 mg/0,3 ml 18 mg/0,45 ml 28 mg/0,7 ml 40 mg/1,0 ml) Asfotasum alfa Tento léčivý přípravek podléhá
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí trachey (průdušnice)
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
Příbalová informace: informace pro pacienta. Betahistin Actavis 8 mg Betahistin Actavis 16 mg tablety. betahistini dihydrochloridum
 sp.zn. sukls175357/2017 a sukls175360/2017 Příbalová informace: informace pro pacienta Betahistin Actavis 8 mg Betahistin Actavis 16 mg tablety betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou
sp.zn. sukls175357/2017 a sukls175360/2017 Příbalová informace: informace pro pacienta Betahistin Actavis 8 mg Betahistin Actavis 16 mg tablety betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls229950/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls229950/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Mycosten 10 mg/g Shampoo Ciclopiroxum šampon Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls229950/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Mycosten 10 mg/g Shampoo Ciclopiroxum šampon Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. fentikonazoli nitras
 sp.zn.sukls33807/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Lomexin 20 mg/g vaginální krém fentikonazoli nitras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls33807/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Lomexin 20 mg/g vaginální krém fentikonazoli nitras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace : Informace pro uživatele. Aknemycin 2000 Mast Erythromycinum
 sp.zn. sukls182807/2012 Příbalová informace : Informace pro uživatele Aknemycin 2000 Mast Erythromycinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls182807/2012 Příbalová informace : Informace pro uživatele Aknemycin 2000 Mast Erythromycinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pacienta. LIVOSTIN nosní sprej, suspenze. levocabastini hydrochloridum
 sp.zn.sukls94010/2015 Příbalová informace: informace pacienta LIVOSTIN nosní sprej, suspenze levocabastini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls94010/2015 Příbalová informace: informace pacienta LIVOSTIN nosní sprej, suspenze levocabastini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret
 sp.zn.sukls240326/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn.sukls240326/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele
 sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
Sp.zn.sukls133559/2018
 Sp.zn.sukls133559/2018 Příbalová informace: informace pro uživatele Betahistin Actavis 24 mg tablety betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls133559/2018 Příbalová informace: informace pro uživatele Betahistin Actavis 24 mg tablety betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok
 sp.zn. sukls301709/2016 Příbalová informace: informace pro uživatele Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok Natrii chromas ( 51 Cr) Přečtěte si pozorně celou příbalovou
sp.zn. sukls301709/2016 Příbalová informace: informace pro uživatele Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok Natrii chromas ( 51 Cr) Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro pacienta. Septabene 1,5 mg/ml + 5,0 mg/ml orální sprej, roztok benzydamini hydrochloridum/cetylpyridinii chloridum
 Sp. zn. sukls56216/2014 Příbalová informace: informace pro pacienta Septabene 1,5 mg/ml + 5,0 mg/ml orální sprej, roztok benzydamini hydrochloridum/cetylpyridinii chloridum Přečtěte si pozorně tuto příbalovou
Sp. zn. sukls56216/2014 Příbalová informace: informace pro pacienta Septabene 1,5 mg/ml + 5,0 mg/ml orální sprej, roztok benzydamini hydrochloridum/cetylpyridinii chloridum Přečtěte si pozorně tuto příbalovou
Příbalová informace: informace pro uživatele. Strensiq 40 mg/ml injekční roztok (12 mg/0,3 ml 18 mg/0,45 ml 28 mg/0,7 ml 40 mg/1 ml) Asfotasum alfa
 Příbalová informace: informace pro uživatele Strensiq 40 mg/ml injekční roztok (12 mg/0,3 ml 18 mg/0,45 ml 28 mg/0,7 ml 40 mg/1 ml) Asfotasum alfa Tento léčivý přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Strensiq 40 mg/ml injekční roztok (12 mg/0,3 ml 18 mg/0,45 ml 28 mg/0,7 ml 40 mg/1 ml) Asfotasum alfa Tento léčivý přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele AESCIN-TEVA. 20 mg, enterosolventní tablety. escinum alfa
 sp.zn. sukls193227/2011 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls193227/2011 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE:INFORMACE PRO PACIENTA. EFFLUMIDEX Liquifilm oční kapky, suspenze fluorometholonum
 PŘÍBALOVÁ INFORMACE:INFORMACE PRO PACIENTA EFFLUMIDEX Liquifilm oční kapky, suspenze fluorometholonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte
PŘÍBALOVÁ INFORMACE:INFORMACE PRO PACIENTA EFFLUMIDEX Liquifilm oční kapky, suspenze fluorometholonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte
Příbalová informace: informace pro pacienta. Loceryl 50 mg/ml léčivý lak na nehty amorolfini hydrochloridum
 Sp.zn. sukls73205/2017 Příbalová informace: informace pro pacienta Loceryl 50 mg/ml léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn. sukls73205/2017 Příbalová informace: informace pro pacienta Loceryl 50 mg/ml léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. Bronchipret tymián a břečťan sirup Thymi extractum fluidum, Hederae helicis folii extractum fluidum
 sp.zn.sukls205603/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Bronchipret tymián a břečťan sirup Thymi extractum fluidum, Hederae helicis folii extractum fluidum Přečtěte si pozorně tuto příbalovou
sp.zn.sukls205603/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Bronchipret tymián a břečťan sirup Thymi extractum fluidum, Hederae helicis folii extractum fluidum Přečtěte si pozorně tuto příbalovou
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
Příbalová informace: informace pro uživatele. SMECTA 3 g prášek pro perorální suspenzi. diosmectitum
 sp. zn. sukls76878/2017 Příbalová informace: informace pro uživatele SMECTA 3 g prášek pro perorální suspenzi diosmectitum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp. zn. sukls76878/2017 Příbalová informace: informace pro uživatele SMECTA 3 g prášek pro perorální suspenzi diosmectitum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
Inflamalgin 10 mg/1 g gel diclofenacum natricum
 sp.zn. sukls241489/2011 a sp.zn. sukls53598/2015 Příbalová informace: informace pro uživatele Inflamalgin 10 mg/1 g gel diclofenacum natricum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
sp.zn. sukls241489/2011 a sp.zn. sukls53598/2015 Příbalová informace: informace pro uživatele Inflamalgin 10 mg/1 g gel diclofenacum natricum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
sp.zn.sukls195792/2018 a sp.zn.sukls195821/2018 Příbalová informace: informace pro pacienta
 sp.zn.sukls195792/2018 a sp.zn.sukls195821/2018 Příbalová informace: informace pro pacienta NEUROMULTIVIT injekční roztok Léčivé látky: Thiamini hydrochloridum (vitamín B1), pyridoxini hydrochloridum (vitamín
sp.zn.sukls195792/2018 a sp.zn.sukls195821/2018 Příbalová informace: informace pro pacienta NEUROMULTIVIT injekční roztok Léčivé látky: Thiamini hydrochloridum (vitamín B1), pyridoxini hydrochloridum (vitamín
Příbalová informace: informace pro uživatele. IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara)
 Příbalová informace: informace pro uživatele IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara) Tento přípravek podléhá dalšímu sledování. To umožní rychlé
Příbalová informace: informace pro uživatele IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara) Tento přípravek podléhá dalšímu sledování. To umožní rychlé
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. HYPNOMIDATE, 2 mg/ml, injekční roztok Etomidatum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HYPNOMIDATE, 2 mg/ml, injekční roztok Etomidatum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HYPNOMIDATE, 2 mg/ml, injekční roztok Etomidatum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Silkis 3 mikorgramy/g mast (calcitriolum)
 Sp.zn. sukls210281/2016 a k sp.zn. sukls63246/2017 Příbalová informace: informace pro uživatele Silkis 3 mikorgramy/g mast (calcitriolum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Sp.zn. sukls210281/2016 a k sp.zn. sukls63246/2017 Příbalová informace: informace pro uživatele Silkis 3 mikorgramy/g mast (calcitriolum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SUSTANON 250 250 mg/ml, injekční roztok Testosteroni
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SUSTANON 250 250 mg/ml, injekční roztok Testosteroni
Příbalová informace: informace pro uživatele Bromhexin Berlin-Chemie 12 mg/ml perorální kapky, roztok bromhexini hydrochloridum
 sp. zn. sukls212749/2018 Příbalová informace: informace pro uživatele Bromhexin Berlin-Chemie 12 mg/ml perorální kapky, roztok bromhexini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve,
sp. zn. sukls212749/2018 Příbalová informace: informace pro uživatele Bromhexin Berlin-Chemie 12 mg/ml perorální kapky, roztok bromhexini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls257864/2016
 Sp.zn.sukls257864/2016 Příbalová informace: informace pro uživatele Garganta 1,5 mg/ml orální sprej, roztok benzydamini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
Sp.zn.sukls257864/2016 Příbalová informace: informace pro uživatele Garganta 1,5 mg/ml orální sprej, roztok benzydamini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F)
 sp.zn. sukls298615/2018 Příbalová informace: informace pro uživatele Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F) Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls298615/2018 Příbalová informace: informace pro uživatele Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F) Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls101534/2012 Příbalová informace: informace pro pacienta GLABRILUX 0,3 mg/ml oční kapky, roztok bimatoprostum
 sp.zn. sukls101534/2012 Příbalová informace: informace pro pacienta GLABRILUX 0,3 mg/ml oční kapky, roztok bimatoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls101534/2012 Příbalová informace: informace pro pacienta GLABRILUX 0,3 mg/ml oční kapky, roztok bimatoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Canespor 1x denně roztok kožní roztok bifonazolum
 sukls46174/2014 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE Canespor 1x denně roztok kožní roztok bifonazolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
sukls46174/2014 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE Canespor 1x denně roztok kožní roztok bifonazolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Flonidan 10 mg tablety Flonidan 5 mg/5 ml suspenze loratadinum
 sp.zn.sukls60188/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE loratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité
sp.zn.sukls60188/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE loratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele Replagal 1 mg/ml koncentrát pro infúzní roztok Agalsidasum alfa Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele Replagal 1 mg/ml koncentrát pro infúzní roztok Agalsidasum alfa Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: Informace pro uživatele. Strepsils Plus Spray orální sprej dichlorbenzenmethanolum, amylmetacresolum, lidocainum
 sp.zn.sukls188553/2013 Příbalová informace: Informace pro uživatele Strepsils Plus Spray orální sprej dichlorbenzenmethanolum, amylmetacresolum, lidocainum Přečtěte si pozorně tuto příbalovou informaci
sp.zn.sukls188553/2013 Příbalová informace: Informace pro uživatele Strepsils Plus Spray orální sprej dichlorbenzenmethanolum, amylmetacresolum, lidocainum Přečtěte si pozorně tuto příbalovou informaci
Příbalová informace: informace pro uživatele. Zinkorot 25 mg tablety zincum
 1 sp.zn. sukls264417/2017 Příbalová informace: informace pro uživatele Zinkorot 25 mg tablety zincum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
1 sp.zn. sukls264417/2017 Příbalová informace: informace pro uživatele Zinkorot 25 mg tablety zincum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA)
 Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Příbalová informace: informace pro uživatele. Betahistin Actavis 24 mg Tablety. Betahistini dihydrochloridum
 sp.zn.sukls161321/2015 Příbalová informace: informace pro uživatele Tablety Betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
sp.zn.sukls161321/2015 Příbalová informace: informace pro uživatele Tablety Betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro uživatele. FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele. Metastron 37 MBq/ml, injekční roztok
 sp.zn. sukls72263/2019 Příbalová informace: informace pro uživatele Metastron 37 MBq/ml, injekční roztok Strontii chloridum 89 Sr Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls72263/2019 Příbalová informace: informace pro uživatele Metastron 37 MBq/ml, injekční roztok Strontii chloridum 89 Sr Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. Fosfomycin LadeePharma 3 g granule pro perorální roztok fosfomycinum trometamoli
 Sp.zn.sukls207380/2013 Příbalová informace: informace pro uživatele Fosfomycin LadeePharma 3 g granule pro perorální roztok fosfomycinum trometamoli Přečtěte si pozorně celou příbalovou informaci dříve,
Sp.zn.sukls207380/2013 Příbalová informace: informace pro uživatele Fosfomycin LadeePharma 3 g granule pro perorální roztok fosfomycinum trometamoli Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele. Ofloxacin-POS 3 mg/ml oční kapky, roztok. Ofloxacinum
 Sp. zn. sukls201848/2013 Příbalová informace: informace pro uživatele Ofloxacin-POS 3 mg/ml oční kapky, roztok Ofloxacinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp. zn. sukls201848/2013 Příbalová informace: informace pro uživatele Ofloxacin-POS 3 mg/ml oční kapky, roztok Ofloxacinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls13612/2011
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls13612/2011 Příbalová informace: Informace pro uživatele Alvotadin 0,5 mg/ml perorální roztok Desloratadinum Přečtěte si pozorně tuto příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls13612/2011 Příbalová informace: Informace pro uživatele Alvotadin 0,5 mg/ml perorální roztok Desloratadinum Přečtěte si pozorně tuto příbalovou informaci
Příbalová informace: informace pro uživatele DUKORAL, suspenze a šumivé granule pro perorální suspenzi Vakcína proti choleře (inaktivovaná, perorální)
 Příbalová informace: informace pro uživatele DUKORAL, suspenze a šumivé granule pro perorální suspenzi Vakcína proti choleře (inaktivovaná, perorální) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele DUKORAL, suspenze a šumivé granule pro perorální suspenzi Vakcína proti choleře (inaktivovaná, perorální) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele
 sp.zn. sukls55434/2017 Příbalová informace: informace pro uživatele Kybernin P 500 IU prášek a rozpouštědlo pro injekční/infuzní roztok Kybernin P 1000 IU prášek a rozpouštědlo pro injekční/infuzní roztok
sp.zn. sukls55434/2017 Příbalová informace: informace pro uživatele Kybernin P 500 IU prášek a rozpouštědlo pro injekční/infuzní roztok Kybernin P 1000 IU prášek a rozpouštědlo pro injekční/infuzní roztok
Příbalová informace: Informace pro pacienta
 sp.zn.sukls98480/2015 Příbalová informace: Informace pro pacienta Mucoplant břečťanový sirup proti kašli sirup Léčivá látka: Hederae helicis folii extractum siccum (suchý extrakt z břečťanového listu)
sp.zn.sukls98480/2015 Příbalová informace: Informace pro pacienta Mucoplant břečťanový sirup proti kašli sirup Léčivá látka: Hederae helicis folii extractum siccum (suchý extrakt z břečťanového listu)
Příbalová informace: informace pro uživatele. Jox 85 mg/1 ml+1 mg/1 ml orální sprej, roztok povidonum iodinatum, allantoinum
 sp.zn.sukls19836/2015 Příbalová informace: informace pro uživatele Jox 85 mg/1 ml+1 mg/1 ml orální sprej, roztok povidonum iodinatum, allantoinum Přečtěte si pozorně tuto příbalovou informaci dříve, než
sp.zn.sukls19836/2015 Příbalová informace: informace pro uživatele Jox 85 mg/1 ml+1 mg/1 ml orální sprej, roztok povidonum iodinatum, allantoinum Přečtěte si pozorně tuto příbalovou informaci dříve, než
Sp.zn.sukls88811/2015
 Sp.zn.sukls88811/2015 Příbalová informace: informace pro uživatele Garganta 1,5 mg/ml orální sprej, roztok benzydamini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
Sp.zn.sukls88811/2015 Příbalová informace: informace pro uživatele Garganta 1,5 mg/ml orální sprej, roztok benzydamini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. AZELASTIN-POS 1 mg/ml nosní sprej, roztok. Léčivá látka: azelastini hydrochloridum
 Sp.zn.sukls198230/2016 Příbalová informace: informace pro uživatele AZELASTIN-POS 1 mg/ml nosní sprej, roztok Léčivá látka: azelastini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls198230/2016 Příbalová informace: informace pro uživatele AZELASTIN-POS 1 mg/ml nosní sprej, roztok Léčivá látka: azelastini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve,
Clotrimazol AL spray 1% kožní sprej, roztok clotrimazolum
 sp.zn.sukls107226/2015 Příbalová informace: informace pro pacienta Clotrimazol AL spray 1% kožní sprej, roztok clotrimazolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls107226/2015 Příbalová informace: informace pro pacienta Clotrimazol AL spray 1% kožní sprej, roztok clotrimazolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. URIFOS 3 g granule pro perorální roztok fosfomycinum trometamoli
 Příbalová informace: informace pro uživatele URIFOS 3 g granule pro perorální roztok fosfomycinum trometamoli Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro uživatele URIFOS 3 g granule pro perorální roztok fosfomycinum trometamoli Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE NovoSeven 1 mg (50 KIU) prášek a rozpouštědlo pro injekční roztok NovoSeven 2 mg (100 KIU) prášek a rozpouštědlo pro injekční roztok NovoSeven 5 mg (250 KIU)
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE NovoSeven 1 mg (50 KIU) prášek a rozpouštědlo pro injekční roztok NovoSeven 2 mg (100 KIU) prášek a rozpouštědlo pro injekční roztok NovoSeven 5 mg (250 KIU)
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Jovesto 0,5 mg/ml perorální roztok desloratadinum
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls12104/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Jovesto 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls12104/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Jovesto 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro pacienta. Stabilised Ceretec 500 mikrogramů kit pro radiofarmakum
 sp.zn. sukls442884/2018 Příbalová informace: informace pro pacienta Stabilised Ceretec 500 mikrogramů kit pro radiofarmakum Exametazimum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám bude
sp.zn. sukls442884/2018 Příbalová informace: informace pro pacienta Stabilised Ceretec 500 mikrogramů kit pro radiofarmakum Exametazimum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám bude
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
Příbalová informace: informace pro pacienta. Ichtoxyl 90 mg/g mast ichthammolum
 sp.zn.sukls229456/2018 Příbalová informace: informace pro pacienta Ichtoxyl 90 mg/g mast ichthammolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn.sukls229456/2018 Příbalová informace: informace pro pacienta Ichtoxyl 90 mg/g mast ichthammolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Azelastin COMOD 0,5 mg/ml oční kapky, roztok. Azelastini hydrochloridum
 Sp. zn. sukls230046/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Azelastin COMOD 0,5 mg/ml oční kapky, roztok Azelastini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
Sp. zn. sukls230046/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Azelastin COMOD 0,5 mg/ml oční kapky, roztok Azelastini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
Příbalová informace: informace pro uživatele. Dorzoptic 20 mg/ml oční kapky, roztok Dorzolamidum
 Sp. zn. sukls203996/2015 Příbalová informace: informace pro uživatele Dorzoptic 20 mg/ml oční kapky, roztok Dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp. zn. sukls203996/2015 Příbalová informace: informace pro uživatele Dorzoptic 20 mg/ml oční kapky, roztok Dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Neiraxin 100 mg/100 mg/1 mg/20 mg/2 ml injekční roztok
 Sp.zn.sukls177390/2017 Příbalová informace: informace pro uživatele Neiraxin 100 mg/100 mg/1 mg/20 mg/2 ml injekční roztok pyridoxini hydrochoridum, thiamini hydrochloridum, cyanocobalaminum, lidocaini
Sp.zn.sukls177390/2017 Příbalová informace: informace pro uživatele Neiraxin 100 mg/100 mg/1 mg/20 mg/2 ml injekční roztok pyridoxini hydrochoridum, thiamini hydrochloridum, cyanocobalaminum, lidocaini
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn. sukls110147/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA SOMATULINE AUTOGEL 60 mg, injekční roztok v předplněné stříkačce SOMATULINE AUTOGEL 90 mg, injekční roztok v předplněné stříkačce SOMATULINE
sp.zn. sukls110147/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA SOMATULINE AUTOGEL 60 mg, injekční roztok v předplněné stříkačce SOMATULINE AUTOGEL 90 mg, injekční roztok v předplněné stříkačce SOMATULINE
