Edukační materiály PRŮVODCE PŘEDEPISOVÁNÍM PRO LÉKAŘE. sublingvální tableta. 67, 133, 267, 400, 533, 800 mikrogramů.
|
|
|
- Marta Musilová
- před 5 lety
- Počet zobrazení:
Transkript
1 Edukační materiály sublingvální tableta 67, 133, 267, 400, 533, 800 mikrogramů fentanyli citras PRŮVODCE PŘEDEPISOVÁNÍM PRO LÉKAŘE
2 Informace pro zdravotnické pracovníky s kvalifikací pro vystavování předpisů. Před předepsáním nebo výdejem přípravku Vellofent si, prosím, přečtěte souhrn údajů o přípravku. Tento průvodce pouze shrnuje základní informace týkající se diagnostiky průlomové bolesti a bezpečného, vhodného užívání přípravku Vellofent.
3 OBSAH 4 Chronická bolest u onkologických pacientů 5 Farmakologická léčba chronické onkologické bolesti 6 Průlomová bolest (BTP) u onkologických onemocnění 8 Hodnocení BTP 9 Algoritmus diagnostiky pro hodnocení BTP 11 Léčba BTP 13 Představení přípravku Vellofent 14 Způsob podání 15 Titrace dávky přípravku Vellofent 16 Schéma titrace dávky přípravku Vellofent 17 Udržovací léčba a úprava dávky 18 Nežádoucí účinky 18 Zvláštní kategorie pacientů 19 Předávkování 20 Další zjištěná rizika 3
4 CHRONICKÁ BOLEST U ONKOLOGICKÝCH PACIENTŮ Bolest je častým symptomem, který působí na onkologické pacienty a který má někdy ničivější účinky než vlastní nádor. Dopad neléčené nebo nedostatečně léčené bolesti na fyzické fungování, duševní pohodu a osobní vztahy pacienta může být velice zhoubný. 1 Bolestí související s onkologickým onemocněním může trpět až % pacientů v pokročilých fázích onemocnění, 2 a až 53 % všech pacientů s karcinomem bez ohledu na druh nebo stádium nádoru % 53% POKROČILÉ ONEMOCNĚNÍ VŠECHNA STÁDIA NÁDORU Onkologičtí pacienti mívají dva klinické projevy bolesti: 4 > akutní bolest (u obou klinických projevů: akutní bolest v nejpřísnějším smyslu a akutní exacerbace léčených symptomů chronické bolesti), > chronickou bolest, která je projevem neoplastického onemocnění nebo výsledkem léčby. Chronická bolest je definována jako konstantní nebo neustálá, dlouhotrvající bolest obvykle trvající více než 12 hodin denně. 4 4
5 FARMAKOLOGICKÁ LÉČBA CHRONICKÉ ONKOLOGICKÉ BOLESTI Existují různé farmakologické možnosti léčby chronické onkologické bolesti. 5 Neopioidní analgetika se běžně používají ke snížení mírné až středně silné onkologické bolesti. 5 Podle směrnic WHO jsou opioidy primárním způsobem léčby středně silné až silné onkologické bolesti. 6,7 ZÁKLADNÍ BODY LÉČBY BOLESTI U ONKOLOGICKÝCH PACIENTŮ 7,8 Brzký nástup První volba perorální podání Předem stanovená dávka léku Podávání v pravidelných intervalech Možnost podání záchranné dávky Rychlá úprava, pokud se snižuje účinek tlumení bolesti Přizpůsobení dávkování, způsobů a cest podání Aby bylo užívání opioidů při léčbě onkologické bolesti účinné, je třeba vzít v úvahu různé faktory: 8 > předchozí užívání jiných opioidů, > síla a charakter bolesti, > věk pacienta, > rozsah nádoru, > souběžná onemocnění. Vzhledem k různorodosti odpovědí pacientů je pro každý individuální případ nutné vybrat nejvhodnější lék a správné dávkování (směrnice WHO). 7 5
6 PRŮLOMOVÁ BOLEST (BTP) U ONKOLOGICKÝCH ONEMOCNĚNÍ U pacientů s onkologickou bolestí se často vyskytují velké výkyvy intenzity bolesti, která se může skutečně prudce zvýšit nad běžnou úroveň bolesti pociťovanou po většinu dne. 9 Tyto ataky se označují termínem průlomová bolest (breakthrough pain BTP) u onkologických onemocnění. 9 Tento jev je zvláště častý u onkologických pacientů, u nichž se vyskytuje ve 40-80% případů 10, a nejčastěji je spojován s nedostatečným tlumením základní bolesti, zvýšenou psychickou nepohodou, sníženou tělesnou aktivitou a špatnou kvalitou života. 9 Klinické projevy BTP se mohou u každého lišit v závislosti na epizodě a průběhu léčby. BTP se často nachází ve stejném místě jako základní bolest. 11 DEFINICE BTP 9 BTP je přechodná exacerbace bolesti středně vysoké až vysoké intenzity, která vzniká buďto spontánně nebo v důsledku spouštěcího faktoru u pacientů, u nichž je základní bolest zmírněna nebo má po většinu dne menší intenzitu. 6
7 Dalším rysem BTP je různorodost kauzálního i klinického obrazu: 9 Spontánní/idiopatická bolest (40 60 %) Spouštěná bolest (40 60 %) > vědomě (vyvolaná pohybem nebo otřením o kůži), > nevědomě (vyvolaná neočekávanou příčinou), > v souvislosti s úkonem (předvídatelná, ale ne spontánní, například při léčení rány). U většiny těchto obrazů je společný časový prvek rychlý nástup (do několika minut) a obecně krátké trvání (průměrně minut) a intenzita bolesti (středně vysoká až vysoká). 9 RŮZNORODOST EPIZOD BTP PODLE DÉLKY TRVÁNÍ A INTENZITY BOLESTI 12 KRÁTKÁ PRUDKÁ BOLEST POMALÝ NÁSTUP / DLOUHÉ TRVÁNÍ Intenzita bolesti OPIOIDY CELODENNĚ Intenzita bolesti OPIOIDY CELODENNĚ CHRONICKÁ ONKOLOGICKÁ BOLEST CHRONICKÁ ONKOLOGICKÁ BOLEST Čas Čas RYCHLÝ NÁSTUP / DLOUHÉ TRVÁNÍ RYCHLÝ NÁSTUP / KRÁTKÉ TRVÁNÍ Intenzita bolesti OPIOIDY CELODENNĚ Intenzita bolesti OPIOIDY CELODENNĚ CHRONICKÁ ONKOLOGICKÁ BOLEST CHRONICKÁ ONKOLOGICKÁ BOLEST Čas Čas 7
8 HODNOCENÍ BTP U všech pacientů s BTP musí být na začátku provedeno specifické vyhodnocení (etiologie, délky trvání, intenzity a fyziopatologických mechanismů), což je nutné opakovat po zahájení léčby, po její modifikaci nebo v případě změny klinického obrazu. 9 Protože jsou příčiny a klinické projevy nanejvýš rozmanité, hodnocení BTP zahrnuje řadu prvků nezbytných k získání všech informací o tomto jevu, aby bylo možné léčbu přizpůsobit danému jedinci. Po počátečním posouzení musí následovat opětovné hodnocení ke stanovení účinnosti, a to v závislosti na volbě léčby. 9 Byly vypracovány systémy, které v zásadě představují sérii otázek kladených pacientovi: 9 > Jaká je u vás intenzita základní bolesti v posledních několika dnech? > Jaké léky užíváte v pravidelných intervalech ke zmírnění základní bolesti? > Jaké dávky a na jak dlouho? > Zmírňuje tato léčba dostatečně Vaši základní bolest po většinu dne? > Máte epizody náhlé intenzivní bolesti? > Jak intenzivní je epizoda v průměru? > Kolik epizod míváte za jeden týden/ den? > Jak rychlý je jejich nástup? > Jak dlouho trvají? > Jaká je jejich intenzita? > Je bolest stejná jako základní bolest nebo je jiná? > Vznikají tyto epizody spontánně nebo je vyvolává nějaká činnost? > Objevují se pravidelně, před podáním plánované dávky léků proti bolesti? > Jak ovlivňují Váš každodenní život? > Je v takových případech nějaká činnost, které se vyhýbáte? > Co bolest dokáže zmírnit? > Jakou konkrétní léčbu máte a na jak dlouho? > Jaké se používají léky a v jakých dávkách? > Byly účinné? Pokud pacient není v dané chvíli schopen nebo ochoten odpovídat, při shromažďování údajů může pomoci, když si vede deník. 9 8
9 ALGORITMUS DIAGNOSTIKY PRO HODNOCENÍ BTP 12 Trpí pacient základní bolestí? Základní bolest = bolest pociťovaná v předchozím týdnu 12 hodin denně (nebo která by byla pociťována, kdyby pacient neužíval analgetika) ANO NE Je základní bolest adekvátně tlumena? Adekvátně tlumena: bolest označovaná za žádnou nebo slabou, ale ne středně silnou nebo silnou po 12 hodin denně v předchozím týdnu ANO NE Pacient nemá BTP, ale má netlumenou základní bolest Má pacient přechodnou exacerbaci bolesti? ANO NE Pacient má BTP Pacient nemá BTP 9
10 ZÁZNAM EPIZOD PRŮLOMOVÉ BOLESTI (BTP) Jak často pociťujete bolest? Je bolest něčím spouštěna? Kde se bolest nachází? (místo na obrázku označte křížkem) Brání Vám bolesti v provádění nějakých činností? Jaké léky proti bolesti užíváte k léčbě BTP? Jak jsou tyto léky proti bolesti účinné? Neulevují Malá úleva Dostatečná úleva Úplná úleva Jak dlouho trvá, než tyto léky proti bolesti začnou účinkovat? Jak byste bolest popsal(a)? Jak byste označil(a) intenzitu bolesti? Mírná Středně silná Silná Velmi silná Jak dlouho bolest trvá? Zhoršuje bolest něco? Jaké nežádoucí účinky tyto léky proti bolesti vyvolávají? Jaké jiné způsoby léčby používáte ke zmírnění BTP? (uveďte všechny) Zmírňuje bolest něco? 10
11 LÉČBA BTP Pro lepší zvládání BTP a zlepšení kvality života pacienta je třeba tlumit základní bolest léky nebo jinými dostupnými způsoby léčby. Podávání medikace podle potřeby je klíčem k léčbě BTP. 9 V případě spontánní nebo nevědomky vyvolané bolesti se medikace předepisuje při nástupu epizody, kdežto u předvídatelné bolesti nebo bolesti související s určitým úkonem by se měla podávat i předtím, než k této události dojde. 9 Po předepsání léčby BTP ve většině případů nenásleduje skutečné podání léku. Některé hlavní důvody jsou tyto: epizoda není přespříliš bolestivá, různé epizody se během dne značně liší a symptomy se spontánně zlepšují. Tento postoj je posilován faktem, že farmakologický profil perorálních opioidů neodpovídá krátkodobé povaze BTP. 9 Vzhledem k farmakokinetickým vlastnostem podávání perorálního morfinu neodpovídá krátkodobé povaze BTP. 9 11
12 Ideální medikace pro léčbu BTP musí mít tyto vlastnosti: 9 > rychlá úleva od krátkodobé bolesti, > nástup účinku odpovídá krátkodobé povaze BTP, > praktický způsob podání. Je jasné, že terapie BTP musí být vždy zvolena podle potřeby a specifického klinického stavu daného pacienta. V rámci rozhodování je nalezena specifická indikace pro opioidy s rychlým nástupem účinku (ROO rapid onset opioids) nejnovější generace. 9 Nové přípravky na bázi fentanyl citrátu, například přípravky rozpustné v ústech, sublingvální a intranazální přípravky, nabízejí při léčbě BTP výrazné výhody jak co se týče farmakokinetiky (rychlá absorpce, větší biologická dostupnost a účinnost), tak compliance (snazší cesta podání). 9 V dalších odstavcích jsou uvedeny podrobné informace o vlastnostech a způsobech použití léčivého přípravku Vellofent indikovaného pro léčbu BTP. 12
13 PŘEDSTAVENÍ PŘÍPRAVKU VELLOFENT Informace o přípravku Vellofent je indikován pro léčbu průlomové bolesti (BTP) u dospělých s onkologickým onemocněním, kteří již dostávají udržovací léčbu chronické onkologické bolesti pomocí opioidů. 14 Definice pacienta s udržovací léčbou opioidy Pacient, který užívá: > alespoň 60 mg perorálně podávaného morfinu denně, > alespoň 25 mikrogramů transdermálně podávaného fentanylu za hodinu, > alespoň 30 mg oxykodonu denně, > alespoň 8 mg perorálně podávaného hydromorfonu denně nebo > ekvianalgetickou dávku jiného opioidu po dobu jednoho týdne nebo déle Vellofent se musí užívat přesně podle indikací, pro které byl schválen. Vellofent využívá technologii, která umožňuje rychlé uvolňování fentanylu a zvyšuje procento a stupeň jeho absorpce sliznicí v ústech; absolutní biologická dostupnost přípravku Vellofent nebyla stanovena, ale odhaduje se na cca 70 %. 14 Vellofent se dodává ve formě sublingválních tablet v těchto silách: > 67 µg > 133 µg > 267 µg > 400 µg > 533 µg > 800 µg Velmi rychlý účinek Vellofent je ROO (opioid s rychlým nástupem účinku) s nejrychlejším analgetickým účinkem: 6 minut po podání, přičemž účinek trvá více než 60 minut
14 ZPŮSOB PODÁNÍ Léčbu musí zahájit a sledovat lékař se zkušenostmi s léčbou opioidy u onkologických pacientů. Lékaři musí mít u fentanylu na paměti potenciál jeho abusu. 14 PŘECHOD NA VELLOFENT: UPOZORNĚNÍ A DOPORUČENÍ, KTERÁ JE TŘEBA SDĚLIT PACIENTOVI 14 Pro léčbu BTP nepoužívejte dvě různé formy fentanylu zároveň. Vypusťte případný jiný přípravek na bázi fentanylu, který máte předepsaný pro tento stav. Počet dostupných dávek je vždy třeba snížit na nejnutnější minimum, aby se zabránilo záměně a možnosti předávkování. 1. Vellofent si položte přímo pod jazyk, na nejnižší místo. 2. Nepolykejte jej: přípravek nechejte zcela rozpustit pod jazykem, nežvýkejte jej ani nesajte. 3. Dokud se sublingvální tableta zcela nerozpustí, nejezte ani nepijte. Pacientovi připomeňte, že: 14 Pokud po 30 minutách v ústech zůstanou kousky tablety, může je spolknout. Pokud má pacient sucho v ústech, před užitím přípravku Vellofent je možné se napít vody ke zvlhčení ústní sliznice. Tableta se po vyjmutí z blistru nesmí skladovat, protože nelze zaručit její neporušenost a může dojít k náhodnému kontaktu s tabletou. Vellofent skladujte vždy uzamčený. 14
15 TITRACE DÁVKY PŘÍPRAVKU VELLOFENT Po stanovení vhodné dávky která může být více než jedna tableta musí pacient tuto dávku dodržovat a spotřebu omezit na maximálně 4 dávky přípravku Vellofent denně. 14 POZNÁMKY K TITRACI 14 A. Určete ideální udržovací léčbu aktuálních epizod BTP. B. Ideální dávka musí bolest dostatečně tlumit a nežádoucí reakce musí pacient považovat za přijatelné. C. Ideální dávku je třeba stanovit postupným zvyšováním dávky pro každého pacienta individuálně. D. Počáteční dávka přípravku Vellofent je 133 mikrogramů, přičemž dávkování se zvyšuje podle potřeby v rozsahu dostupného dávkování. E. Až do dosažení ideální dávky pacienta pečlivě sledujte. F. Přechod z jiných přípravků obsahujících fentanyl na Vellofent nesmí být v poměru 1:1. G. Jestliže léčba epizody BTP vyžaduje více než jednu dávkovací jednotku, zvažte zvýšení dávky použitím nejbližší vyšší koncentrace léčivého přípravku. 15
16 SCHÉMA TITRACE DÁVKY PŘÍPRAVKU VELLOFENT 14 Počáteční dávka: 133 μg Adekvátní úleva od bolesti je dosažena (během minut) Ano NE Použijte tuto dávku k léčbě dalších epizod průlomové bolesti Užijte další tabletu (viz tabulka pro určení síly druhé tablety) Pro další epizodu průlomové bolesti užijte jako první tabletu následující vyšší sílu přípravku. Pokud vyšší dávka zajistí adekvátní úlevu od bolesti, ale nežádoucí účinky bude pacient považovat za nepřijatelné, je možné použít střední dávku (pomocí tablet o síle 67 μg nebo 133 μg). SÍLA (μg) PRVNÍ TABLETY PROTI PRŮLOMOVÉ BOLESTI SÍLA (μg) DODATEČNÉ (DRUHÉ) TABLETY, KTERÁ SE UŽIJE MINUT PO PODÁNÍ PRVNÍ TABLETY, JE-LI TŘEBA
17 UDRŽOVACÍ LÉČBA A ÚPRAVA DÁVKY 14 Začátek léčby přípravkem Vellofent Před začátkem podávání přípravku Vellofent je důležité, aby léčba opioidy s dlouhodobým účinkem, používaná k tlumení trvalých bolestí pacienta, byla stabilizovaná; pacient musí navíc při užívání přípravku Vellofent pokračovat v dlouhodobé léčbě opioidy. 14 Po stanovení vhodné dávky která může být více než jedna tableta musí pacient tuto dávku dodržovat a spotřebu omezit na maximálně 4 dávky přípravku Vellofent denně. 14 Počáteční dávka přípravku Vellofent BTP je dostatečně kontrolovaná 4 epizody BTP denně Neměňte dávkování udržovací léčba * opioid s dlouhodobým účinkem Znovu zhodnoťte dávkování LAO* a proveďte nové hodnocení/titraci následné dávky přípravku Vellofent Aby byla rizika nežádoucích účinků v souvislosti s opioidy minimální a abychom určili účinnou dávku, je naprosto nezbytné, aby pacienty během titrace dávky pečlivě sledovali zdravotníci. 14 Vysazení léčby Podávání přípravku Vellofent je nutné ihned vysadit, pokud se u pacienta epizody průlomové bolesti již neobjevují. Je-li nutné vysazení celé léčby opioidy, lékař musí pacienta pečlivě sledovat, neboť hrozí riziko náhlých abstinenčních příznaků
18 NEŽÁDOUCÍ ÚČINKY Je velmi důležité informovat pacienta o možných nežádoucích účincích, které se mohou během podávání přípravku Vellofent objevit, a sdělit mu, že lze očekávat nástup nežádoucích účinků typických pro opioidy a ujistit ho, že po určení správného dávkování tyto účinky často zmizí nebo se jejich intenzita po čase užívání sníží. 14 K nejčastěji udávaným nežádoucím reakcím patří: nevolnost, zvracení, zácpa, bolesti hlavy, ospalost/únava a závratě. 14 ZVLÁŠTNÍ KATEGORIE PACIENTŮ 14 Starší pacienti Titrace dávky musí být velmi pečlivá a pacienta je nutné pečlivě sledovat z hlediska případných známek toxicity fentanylu. Pacienti s poruchou funkce jater a ledvin Děti Těhotenství Kojení Během titrace dávky přípravku Vellofent je nutné pacienty s poruchou funkce jater nebo ledvin pečlivě sledovat z hlediska známek nástupu toxicity fentanylu. Vellofent se nedoporučuje u dětí a dospívajících mladších 18 let z důvodu nedostatečných údajů o bezpečnosti a účinnosti. Potenciální riziko u člověka není známo. Pokud to není naprosto nezbytné, Vellofent se nesmí v těhotenství používat. Doporučuje se fentanyl nepoužívat na začátku porodu a během něj (včetně císařského řezu). Kojící ženy nesmí fentanyl užívat a s kojením je možné znovu začít nejméně za 5 dnů po posledním podání fentanylu. 18
19 Předávkování 14 Symptomy předávkování fentanylem se nejpravděpodobněji dosti podobají symptomům pozorovaným u nitrožilně podávaného fentanylu a jiných opioidů a představují prodloužení jejich farmakologického účinku. Nejzávažnější symptomy předávkování jsou: > změny duševního stavu, > ztráta vědomí, > kóma, > kardiorespirační zástava, > respirační deprese, respirační tíseň a respirační selhání. Okamžitá léčba předávkování opioidem zahrnuje vyjmutí zbytků přípravku Vellofent z úst; ověření průchodnosti dýchacích cest; fyzická a verbální stimulace pacienta; určení, nakolik je pacient při vědomí, stavu dýchání a krevního oběhu; a podle potřeby použití asistované ventilace (podpory ventilace). 19
20 DALŠÍ ZJIŠTĚNÁ RIZIKA Nesprávné užití, abusus a závislost Fentanyl je velmi silný opioidní agonista, u něhož existuje riziko nesprávného užití podobně jako u ostatních opioidních agonistů. 16 Po opakovaném podávání opioidů, např. fentanylu, může vzniknout tolerance a fyzická a psychická závislost. Iatrogenní závislost po léčebném použití opioidů je vzácná. 14 Pacienti, kteří v minulosti prodělali závislost na lécích nebo alkoholu jsou v průběhu léčby opioidy více ohroženi vznikem závislostí a abusu. 16 Použití mimo rozsah indikací (Off-label use) Použití fentanylu je indikováno jen pro léčbu BTP u onkologických pacientů, kteří již podstupují léčbu opioidy a u nichž byla prokázána snášenlivost léčby chronické onkologické bolesti pomocí opioidů. Fentanyl není dovoleno předepisovat pacientům, kteří opioidy nesnášejí (např. pacientům, kteří opioidy neužívají pravidelně), ani pacientům s akutní bolestí, pooperační bolestí, bolestmi hlavy/migrénami nebo sportovními úrazy, ačkoliv jiné opioidy mohou být podle potřeby podávány. 16 Farmakovigilance a hlášení podezření na nežádoucí účinky Po registraci léčivého přípravku je důležité hlásit podezření na nežádoucí účinky. Umožňuje další sledování poměru přínosu a rizik léčivého přípravku. Jakékoliv podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí být hlášeno Státnímu ústavu pro kontrolu léčiv. Podrobnosti o hlášení najdete na: Adresa pro zasílání je Státní ústav pro kontrolu léčiv, oddělení farmakovigilance, Šrobárova 48, Praha 10, , farmakovigilance@sukl.cz. Tato informace může být také hlášena společnosti: Angelini Pharma Česká republika s.r.o. Páteřní 7, Brno mobil (+420) farmakovig@angelini.cz 20
21 Literatura 1. Breivik H et al. Annals of Oncology 2009; 20: Haugen DF et al. PAIN 2010; 149: Davies A et al. J Pain Symptom Manage 2013; 46(5): Associazione Italiana di Oncologia Medica (AIOM) [Italská společnost pro onkologii] Linee Guida Terapia del dolore in Oncologia [Směrnice pro léčbu bolesti v onkologii] vydání z r Lee SK et al. International Journal of General Medicine 2014;7: Wang Y et al. Experimental and Therapeutic Medicine 2012; 4: Světová zdravotnická organizace (WHO). Cancer pain relief. With a guide to opioid availability. (Úleva od bolesti při onkologických onemocněních. S průvodcem pro dostupnost opioidů.) Druhé vydání. 8. Regione Autonoma della Sardegna [Autonomní oblast Sardinie]. Linee Guida per il Trattamento del Dolore Oncologico [Směrnice pro léčbu onkologické bolesti]. Říjen Mercadante S. Amadori D et al. La Rivista Italiana di Cure Palliative [Italský odborný časopis zaměřený na paliativní péči] 2010; 1: Mercadante S. et al. Support Care Cancer 2011; 19(7): Wengström Y et al. European Oncology Nursing Society breakthrough cancer pain guidelines. Eur J Oncol Nurs 2014; 18(2): Rhiner MI et al. J SupportOncol 2010;8(6): Davies A et al. Eur J Pain 2009; 13(4): Vellofent. Souhrn údajů o přípravku. 15. Novotna S et al. Clinical Therapeutics 2014; 36(3): Transmucosal Immediate Release Fentanyl (TIRF). Risk Evaluation and Mitigation Strategy (REMS). (Fentanyl s okamžitým transmukózním uvolňováním (TIRF). Hodnocení rizik a strategie zmírňování (REMS).) 21
22 ZÁZNAM EPIZOD PRŮLOMOVÉ BOLESTI (BTP) Jak často pociťujete bolest? Je bolest něčím spouštěna? Kde se bolest nachází? (místo na obrázku označte křížkem) Brání Vám bolesti v provádění nějakých činností? Jaké léky proti bolesti užíváte k léčbě BTP? Jak jsou tyto léky proti bolesti účinné? Neulevují Malá úleva Dostatečná úleva Úplná úleva Jak dlouho trvá, než tyto léky proti bolesti začnou účinkovat? Jak byste bolest popsal(a)? Jak byste označil(a) intenzitu bolesti? Mírná Středně silná Silná Velmi silná Jak dlouho bolest trvá? Zhoršuje bolest něco? Jaké nežádoucí účinky tyto léky proti bolesti vyvolávají? Jaké jiné způsoby léčby používáte ke zmírnění BTP? (uveďte všechny) Zmírňuje bolest něco? 23
23 ZÁZNAM EPIZOD PRŮLOMOVÉ BOLESTI (BTP) Jak často pociťujete bolest? Je bolest něčím spouštěna? Kde se bolest nachází? (místo na obrázku označte křížkem) Brání Vám bolesti v provádění nějakých činností? Jaké léky proti bolesti užíváte k léčbě BTP? Jak jsou tyto léky proti bolesti účinné? Neulevují Malá úleva Dostatečná úleva Úplná úleva Jak dlouho trvá, než tyto léky proti bolesti začnou účinkovat? Jak byste bolest popsal(a)? Jak byste označil(a) intenzitu bolesti? Mírná Středně silná Silná Velmi silná Jak dlouho bolest trvá? Zhoršuje bolest něco? Jaké nežádoucí účinky tyto léky proti bolesti vyvolávají? Jaké jiné způsoby léčby používáte ke zmírnění BTP? (uveďte všechny) Zmírňuje bolest něco? 25
24 ZÁZNAM EPIZOD PRŮLOMOVÉ BOLESTI (BTP) Jak často pociťujete bolest? Je bolest něčím spouštěna? Kde se bolest nachází? (místo na obrázku označte křížkem) Brání Vám bolesti v provádění nějakých činností? Jaké léky proti bolesti užíváte k léčbě BTP? Jak jsou tyto léky proti bolesti účinné? Neulevují Malá úleva Dostatečná úleva Úplná úleva Jak dlouho trvá, než tyto léky proti bolesti začnou účinkovat? Jak byste bolest popsal(a)? Jak byste označil(a) intenzitu bolesti? Mírná Středně silná Silná Velmi silná Jak dlouho bolest trvá? Zhoršuje bolest něco? Jaké nežádoucí účinky tyto léky proti bolesti vyvolávají? Jaké jiné způsoby léčby používáte ke zmírnění BTP? (uveďte všechny) Zmírňuje bolest něco? 27
25 ZÁZNAM EPIZOD PRŮLOMOVÉ BOLESTI (BTP) Jak často pociťujete bolest? Je bolest něčím spouštěna? Kde se bolest nachází? (místo na obrázku označte křížkem) Brání Vám bolesti v provádění nějakých činností? Jaké léky proti bolesti užíváte k léčbě BTP? Jak jsou tyto léky proti bolesti účinné? Neulevují Malá úleva Dostatečná úleva Úplná úleva Jak dlouho trvá, než tyto léky proti bolesti začnou účinkovat? Jak byste bolest popsal(a)? Jak byste označil(a) intenzitu bolesti? Mírná Středně silná Silná Velmi silná Jak dlouho bolest trvá? Zhoršuje bolest něco? Jaké nežádoucí účinky tyto léky proti bolesti vyvolávají? Jaké jiné způsoby léčby používáte ke zmírnění BTP? (uveďte všechny) Zmírňuje bolest něco? 29
26 ZÁZNAM EPIZOD PRŮLOMOVÉ BOLESTI (BTP) Jak často pociťujete bolest? Je bolest něčím spouštěna? Kde se bolest nachází? (místo na obrázku označte křížkem) Brání Vám bolesti v provádění nějakých činností? Jaké léky proti bolesti užíváte k léčbě BTP? Jak jsou tyto léky proti bolesti účinné? Neulevují Malá úleva Dostatečná úleva Úplná úleva Jak dlouho trvá, než tyto léky proti bolesti začnou účinkovat? Jak byste bolest popsal(a)? Jak byste označil(a) intenzitu bolesti? Mírná Středně silná Silná Velmi silná Jak dlouho bolest trvá? Zhoršuje bolest něco? Jaké nežádoucí účinky tyto léky proti bolesti vyvolávají? Jaké jiné způsoby léčby používáte ke zmírnění BTP? (uveďte všechny) Zmírňuje bolest něco? 31
Edukační materiály PRŮVODCE VYDÁVÁNÍM PRO LÉKÁRNÍKA. sublingvální tableta. 67, 133, 267, 400, 533, 800 mikrogramů.
 Edukační materiály sublingvální tableta 67, 133, 267, 400, 533, 800 mikrogramů fentanyli citras PRŮVODCE VYDÁVÁNÍM PRO LÉKÁRNÍKA Informace pro lékárníka. Před výdejem přípravku Vellofent si, prosím, přečtěte
Edukační materiály sublingvální tableta 67, 133, 267, 400, 533, 800 mikrogramů fentanyli citras PRŮVODCE VYDÁVÁNÍM PRO LÉKÁRNÍKA Informace pro lékárníka. Před výdejem přípravku Vellofent si, prosím, přečtěte
sublingvální tableta 67, 133, 267, 400, 533, 800 mikrogramů PRŮVODCE UŽÍVÁNÍM PŘÍPRAVKU VELLOFENT PRO PACIENTA A PEČOVATELE
 sublingvální tableta 67,, 67, 00,, 800 mikrogramů PRŮVODCE UŽÍVÁNÍM PŘÍPRAVKU VELLOFENT PRO PACIENTA A PEČOVATELE Tento průvodce obsahuje důležité informace pro pacienty a pečující osoby ohledně průlomové
sublingvální tableta 67,, 67, 00,, 800 mikrogramů PRŮVODCE UŽÍVÁNÍM PŘÍPRAVKU VELLOFENT PRO PACIENTA A PEČOVATELE Tento průvodce obsahuje důležité informace pro pacienty a pečující osoby ohledně průlomové
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL - Pioglitazone Accord
 Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Verze 6, JAK POUŽÍVAT VÁŠ INSTANYL NOSNÍ SPREJ S JEDNOU DÁVKOU Fentanyl v intranazálním spreji
 JAK POUŽÍVAT VÁŠ INSTANYL NOSNÍ SPREJ S JEDNOU DÁVKOU Fentanyl v intranazálním spreji DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE O PŘÍPRAVKU INSTANYL Seznamte se prosím s následujícími důležitými informacemi a určitě
JAK POUŽÍVAT VÁŠ INSTANYL NOSNÍ SPREJ S JEDNOU DÁVKOU Fentanyl v intranazálním spreji DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE O PŘÍPRAVKU INSTANYL Seznamte se prosím s následujícími důležitými informacemi a určitě
Příloha C. (změna v národně registrovaných léčivých přípravcích)
 Příloha C (změna v národně registrovaných léčivých přípravcích) PŘÍLOHA I VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ DOPORUČUJÍCÍ ZMĚNU PODMÍNEK ROZHODNUTÍ O REGISTRACI(ÍCH) Vědecké závěry S ohledem na hodnotící zprávu
Příloha C (změna v národně registrovaných léčivých přípravcích) PŘÍLOHA I VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ DOPORUČUJÍCÍ ZMĚNU PODMÍNEK ROZHODNUTÍ O REGISTRACI(ÍCH) Vědecké závěry S ohledem na hodnotící zprávu
Definice průlomové bolesti (Breakthrough pain)
 Definice průlomové bolesti (Breakthrough pain) Za průlomovou bolest považujeme náhlé, přechodné a krátkodobé vzplanutí bolesti, které se nejčastěji objevuje u pacientů s trvalou léčbou opioidy Průlomová
Definice průlomové bolesti (Breakthrough pain) Za průlomovou bolest považujeme náhlé, přechodné a krátkodobé vzplanutí bolesti, které se nejčastěji objevuje u pacientů s trvalou léčbou opioidy Průlomová
KONTROLNÍ SEZNAM ČINNOSTÍ PRO PŘEDEPISUJÍCÍ LÉKÁRNÍKY
 KONTROLNÍ SEZNAM ČINNOSTÍ PRO PŘEDEPISUJÍCÍ LÉKÁRNÍKY Seznam činností pro lékárníka vydávajícího přípravek Instanyl nosní sprej s jednou dávkou Následující činnosti musejí být provedeny před tím, než je
KONTROLNÍ SEZNAM ČINNOSTÍ PRO PŘEDEPISUJÍCÍ LÉKÁRNÍKY Seznam činností pro lékárníka vydávajícího přípravek Instanyl nosní sprej s jednou dávkou Následující činnosti musejí být provedeny před tím, než je
Příloha II. Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci
 Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 21 Vědecké závěry Celkové závěry vědeckého hodnocení přípravků Oxynal a Targin a souvisejících názvů (viz příloha I) Podkladové
Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 21 Vědecké závěry Celkové závěry vědeckého hodnocení přípravků Oxynal a Targin a souvisejících názvů (viz příloha I) Podkladové
Příloha II. Vědecké závěry a zdůvodnění zrušení či změny podmínek rozhodnutí o registraci a podrobné vysvětlení rozdílů oproti doporučení výboru PRAC
 Příloha II Vědecké závěry a zdůvodnění zrušení či změny podmínek rozhodnutí o registraci a podrobné vysvětlení rozdílů oproti doporučení výboru PRAC 68 Vědecké závěry Koordinační skupina pro vzájemné uznávání
Příloha II Vědecké závěry a zdůvodnění zrušení či změny podmínek rozhodnutí o registraci a podrobné vysvětlení rozdílů oproti doporučení výboru PRAC 68 Vědecké závěry Koordinační skupina pro vzájemné uznávání
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
KONTROLNÍ SEZNAM ČINNOSTÍ PRO PŘEDEPISUJÍCÍ LÉKAŘE
 KONTROLNÍ SEZNAM ČINNOSTÍ PRO PŘEDEPISUJÍCÍ LÉKAŘE Seznam činností pro lékaře předepisující přípravek Instanyl nosní sprej s jednou dávkou Následující činnosti musejí být provedeny před tím, než je přípravek
KONTROLNÍ SEZNAM ČINNOSTÍ PRO PŘEDEPISUJÍCÍ LÉKAŘE Seznam činností pro lékaře předepisující přípravek Instanyl nosní sprej s jednou dávkou Následující činnosti musejí být provedeny před tím, než je přípravek
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
Edukační materiál. Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera
 Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Příloha III. Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Léčba bolesti u mnohočetného myelomu. O. Sláma, MOU Brno
 Léčba bolesti u mnohočetného myelomu O. Sláma, MOU Brno Proč je důležité, aby si lékař s pacientem dobře rozuměli, když je řeč o bolesti Několik poznámek k léčbě bolesti morfinem a silnými opioidy Sedmero
Léčba bolesti u mnohočetného myelomu O. Sláma, MOU Brno Proč je důležité, aby si lékař s pacientem dobře rozuměli, když je řeč o bolesti Několik poznámek k léčbě bolesti morfinem a silnými opioidy Sedmero
Dostávali v roce 2006 čeští pacienti se silnou bolestí méně léků?
 Omezení spotřeb léků v ČR v roce 2006 Dostávali v roce 2006 čeští pacienti se silnou bolestí méně léků? MUDr. Michal Prokeš INFOPHARM a.s. Zpracováno na základě údajů SÚKL získaných z programu AISLP verze
Omezení spotřeb léků v ČR v roce 2006 Dostávali v roce 2006 čeští pacienti se silnou bolestí méně léků? MUDr. Michal Prokeš INFOPHARM a.s. Zpracováno na základě údajů SÚKL získaných z programu AISLP verze
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE
 EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
LÉČBA BOLESTI - POHLED SÚKL NA KLINICKÁ HODNOCENÍ
 Léčba bolesti pohled SÚKL na klinická hodnocení 1 LÉČBA BOLESTI - POHLED SÚKL NA KLINICKÁ HODNOCENÍ MUDr. Alice Němcová MUDr. Alena Trunečková Léčba bolesti pohled SÚKL na klinická hodnocení 2 Klinická
Léčba bolesti pohled SÚKL na klinická hodnocení 1 LÉČBA BOLESTI - POHLED SÚKL NA KLINICKÁ HODNOCENÍ MUDr. Alice Němcová MUDr. Alena Trunečková Léčba bolesti pohled SÚKL na klinická hodnocení 2 Klinická
EDUKAČNÍ MATERIÁLY. KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
Zvažte oddálení podání regadenosonu u pacientů s nekontrolovanou hypertenzí.
 CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
Edukační materiály. KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře
 Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Důležité informace o užívání přípravku TASIGNA
 Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Léčba bolesti u mnohočetného myelomu
 Léčba bolesti u mnohočetného myelomu O. Sláma, IHOK FN Brno Bolest u MM Při postižení kostí je bolest častá Intenzita bolesti v průběhu léčby výrazně kolísá V pokročilých stádiích onemocnění je bolest
Léčba bolesti u mnohočetného myelomu O. Sláma, IHOK FN Brno Bolest u MM Při postižení kostí je bolest častá Intenzita bolesti v průběhu léčby výrazně kolísá V pokročilých stádiích onemocnění je bolest
O co jde? Uveden na trh 1991 na Novém Zélandu. Subutex = buprenorfin v tabletě. Subuxon = buprenorfin + naloxon v tabletě v poměru 4 x 1
 Suboxone je tu!!! O co jde? Uveden na trh 1991 na Novém Zélandu Subutex = buprenorfin v tabletě Subuxon = buprenorfin + naloxon v tabletě v poměru 4 x 1 Složení Sublingvální tableta (k rozpuštění pod jazyk)
Suboxone je tu!!! O co jde? Uveden na trh 1991 na Novém Zélandu Subutex = buprenorfin v tabletě Subuxon = buprenorfin + naloxon v tabletě v poměru 4 x 1 Složení Sublingvální tableta (k rozpuštění pod jazyk)
Indikace přípravku Zetamac v ordinaci praktického lékaře
 Indikace přípravku Zetamac v ordinaci praktického lékaře MUDr. Igor Karen 13.10. 2009 Zetamac léková forma azithromycinum 2g granule s prodlouženým uvolňováním pro přípravu perorální suspenze s příchutí
Indikace přípravku Zetamac v ordinaci praktického lékaře MUDr. Igor Karen 13.10. 2009 Zetamac léková forma azithromycinum 2g granule s prodlouženým uvolňováním pro přípravu perorální suspenze s příchutí
Rozměr zavřeného průkazu mm
 Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
PRŮKAZ PACIENTA. užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1
 PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA. užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019
 PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
Doplněk MM guidelines: Doplněk č. 1 k doporučení z 9/2012 diagnostika a léčba mnohočetného myelomu
 Doplněk MM guidelines: Doplněk č. 1 k doporučení z 9/2012 diagnostika a léčba mnohočetného myelomu Marta Krejčí XIII. MM workshop a setkání CMG, Mikulov 11.4.2015 Doplněk č. 1 k doporučení z 9/2012: Diagnostika
Doplněk MM guidelines: Doplněk č. 1 k doporučení z 9/2012 diagnostika a léčba mnohočetného myelomu Marta Krejčí XIII. MM workshop a setkání CMG, Mikulov 11.4.2015 Doplněk č. 1 k doporučení z 9/2012: Diagnostika
KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin. Informace pro lékaře EU
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
Od opia k melatoninu aneb Práce s nespavým pacientem
 Soubor pøednášek ze semináøe Od opia k melatoninu aneb Práce s nespavým pacientem Semináøe se konají na 14 místech ÈR v období únor duben 2009 1. Péèe o pacienta s nespavostí Diagnostika a nefarmakologická
Soubor pøednášek ze semináøe Od opia k melatoninu aneb Práce s nespavým pacientem Semináøe se konají na 14 místech ÈR v období únor duben 2009 1. Péèe o pacienta s nespavostí Diagnostika a nefarmakologická
Vývoj nových léčiv. Preklinický výzkum Klinický výzkum
 Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍLOHA II VĚDECKÉ ZÁVĚRY
 PŘÍLOHA II VĚDECKÉ ZÁVĚRY 22 Vědecké závěry Podkladové informace Přípravek Durogesic je transdermální náplast obsahující fentanyl, což je silné syntetické opioidní analgetikum, které patří do skupiny piperidinových
PŘÍLOHA II VĚDECKÉ ZÁVĚRY 22 Vědecké závěry Podkladové informace Přípravek Durogesic je transdermální náplast obsahující fentanyl, což je silné syntetické opioidní analgetikum, které patří do skupiny piperidinových
ACTYNOX 50 % / 50 % V/V Oxid dusný (dinitrogenii oxidum) / kyslík (oxygenum) Medicinální plyn, stlačený PRŮVODCE PRO ZDRAVOTNICKÉ PRACOVNÍKY
 Edukační materiály Orgány veřejného zdraví stanovily určité podmínky pro tržní rozvoj přípravku ACTYNOX. Jednou z nich je předávat tyto informace zdravotnickým pracovníkům jako součást povinného plánu
Edukační materiály Orgány veřejného zdraví stanovily určité podmínky pro tržní rozvoj přípravku ACTYNOX. Jednou z nich je předávat tyto informace zdravotnickým pracovníkům jako součást povinného plánu
PŘÍLOHA III ZMĚNY PŘÍSLUŠNÝCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Poznámka:
 PŘÍLOHA III ZMĚNY PŘÍSLUŠNÝCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Změny v souhrnu údajů o přípravku a příbalové informaci možná bude následně třeba nechat (v případě potřeby
PŘÍLOHA III ZMĚNY PŘÍSLUŠNÝCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Změny v souhrnu údajů o přípravku a příbalové informaci možná bude následně třeba nechat (v případě potřeby
Vše co potřebujete vědět o hemoroidech. Rady pro pacienty
 Vše co potřebujete vědět o hemoroidech Rady pro pacienty CO? CO? JAK? JAK? KDY? KDY? PROČ? PROČ? CO CO jsou hemoroidy? je hemoroidální onemocnění? Anatomie řitního kanálu a konečníku Hemoroidy jsou přirozenou
Vše co potřebujete vědět o hemoroidech Rady pro pacienty CO? CO? JAK? JAK? KDY? KDY? PROČ? PROČ? CO CO jsou hemoroidy? je hemoroidální onemocnění? Anatomie řitního kanálu a konečníku Hemoroidy jsou přirozenou
Důležité informace k užívání přípravku Tasigna
 Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
Familiární středomořská (Mediterranean) horečka (Fever)
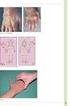 www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Flexove 625 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje glukosaminum 625 mg (ve formě glukosamini hydrochloridum). Úplný seznam
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Flexove 625 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje glukosaminum 625 mg (ve formě glukosamini hydrochloridum). Úplný seznam
Nebido EDUKAČNÍ MATERIÁL. Jak úspěšně aplikovat přípravek. (testosterone undecanoate)
 EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH)
 Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Bolest. v paliativní medicíně. prim.mudr.dagmar Palasová
 Bolest. v paliativní medicíně Beskydy 20.4.2013 prim.mudr.dagmar Palasová Bílovecká nemocnice, a.s. Paliativní péče je aktivní péče poskytovaná pacientovi, který trpí nevyléčitelnou chorobou v pokročilém
Bolest. v paliativní medicíně Beskydy 20.4.2013 prim.mudr.dagmar Palasová Bílovecká nemocnice, a.s. Paliativní péče je aktivní péče poskytovaná pacientovi, který trpí nevyléčitelnou chorobou v pokročilém
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls11810/2008
 Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls11810/2008 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Buprenorphine SMB 0,4 mg sublingvální tableta Buprenorphini hydrochloridum Přečtěte si pozorně
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls11810/2008 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Buprenorphine SMB 0,4 mg sublingvální tableta Buprenorphini hydrochloridum Přečtěte si pozorně
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jedna tableta obsahuje glukosaminum 625 mg (ve formě glukosamini hydrochloridum).
 Sp.zn.sukls137614/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Flexove 625 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje glukosaminum 625 mg (ve formě glukosamini hydrochloridum).
Sp.zn.sukls137614/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Flexove 625 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje glukosaminum 625 mg (ve formě glukosamini hydrochloridum).
32. FARMAKOTERAPIE NÁDOROVÉ BOLESTI
 32. FARMAKOTERAPIE NÁDOROVÉ BOLESTI Úvod Bolest představuje jeden z nejzávažnějších projevů nádorového onemocnění. Léčba bolesti je nedílnou součástí onkologické péče. Úleva od bolesti obvykle neznamená
32. FARMAKOTERAPIE NÁDOROVÉ BOLESTI Úvod Bolest představuje jeden z nejzávažnějších projevů nádorového onemocnění. Léčba bolesti je nedílnou součástí onkologické péče. Úleva od bolesti obvykle neznamená
ANO. MUDr. Roman Škulec, Ph.D.
 OPIOIDY JSOU INDIKOVÁNY V ANALGETICKÉ PŘEDNEMOCNIČNÍ LÉČBĚ PACIENTŮ S NPB ANO MUDr. Roman Škulec, Ph.D. Klinika anesteziologie, perioperační a intenzivní medicíny, Masarykova nemocnice v Ústí nad Labem,
OPIOIDY JSOU INDIKOVÁNY V ANALGETICKÉ PŘEDNEMOCNIČNÍ LÉČBĚ PACIENTŮ S NPB ANO MUDr. Roman Škulec, Ph.D. Klinika anesteziologie, perioperační a intenzivní medicíny, Masarykova nemocnice v Ústí nad Labem,
CZ PAR. QUETIAPINI FUMARAS Seroquel. NL/W/0004/pdWS/002
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Verze 9, JAK POUŽÍVAT VÁŠ INSTANYL Fentanyl v intranazálním spreji
 JAK POUŽÍVAT VÁŠ INSTANYL Fentanyl v intranazálním spreji DŮLEŽITÉ INFORMACE O PŘÍPRAVKU INSTANYL Seznamte se prosím s následujícími důležitými informacemi a určitě si přečtěte Příbalovou informaci před
JAK POUŽÍVAT VÁŠ INSTANYL Fentanyl v intranazálním spreji DŮLEŽITÉ INFORMACE O PŘÍPRAVKU INSTANYL Seznamte se prosím s následujícími důležitými informacemi a určitě si přečtěte Příbalovou informaci před
JAK POUŽÍVAT VÁŠ INSTANYL
 KONTAKTNÍ INFORMACE Uveďte prosím níže, koho je možné kontaktovat v případě, že budete mít jakékoli dotazy týkající se Vaší léčby přípravkem Instanyl ZÁZNAMOVÉ KARTY DÁVKOVÁNÍ 50 mikrogramů v dávce 00
KONTAKTNÍ INFORMACE Uveďte prosím níže, koho je možné kontaktovat v případě, že budete mít jakékoli dotazy týkající se Vaší léčby přípravkem Instanyl ZÁZNAMOVÉ KARTY DÁVKOVÁNÍ 50 mikrogramů v dávce 00
SPECIALIZOVANÁ DOMÁCÍ
 SPECIALIZOVANÁ DOMÁCÍ PALIATIVNÍ PÉČE ANEB CO JE A JAK NÁM MŮŽE POMOCI DOMÁCÍ HOSPIC MUDr. Hana Miličková Spolek Konipaska Domácí hospicová péče na znojemsku Paliativní medicína Jak funguje domácí hospic
SPECIALIZOVANÁ DOMÁCÍ PALIATIVNÍ PÉČE ANEB CO JE A JAK NÁM MŮŽE POMOCI DOMÁCÍ HOSPIC MUDr. Hana Miličková Spolek Konipaska Domácí hospicová péče na znojemsku Paliativní medicína Jak funguje domácí hospic
Atestační otázky z nástavbového oboru Paliativní medicína Verze 1-2012
 Atestační otázky z nástavbového oboru Paliativní medicína Verze 1-2012 Obecná část 1. Základní koncepty paliativní medicíny (nevyléčitelné onemocnění, terminální onemocnění, pacient v terminálním stavu,
Atestační otázky z nástavbového oboru Paliativní medicína Verze 1-2012 Obecná část 1. Základní koncepty paliativní medicíny (nevyléčitelné onemocnění, terminální onemocnění, pacient v terminálním stavu,
JAK POUŽÍVAT VÁŠ INSTANYL
 KONTAKTNÍ INFORMACE Uveďte prosím níže, koho je možné kontaktovat v případě, že budete mít jakékoli dotazy týkající se Vaší léčby přípravkem Instanyl, například telefonní číslo na Vašeho lékaře: Pro více
KONTAKTNÍ INFORMACE Uveďte prosím níže, koho je možné kontaktovat v případě, že budete mít jakékoli dotazy týkající se Vaší léčby přípravkem Instanyl, například telefonní číslo na Vašeho lékaře: Pro více
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím
 Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Důležité informace pro pacienty
 MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
Kelapril 5mg 7x14tbl.
 Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
NeuroBloc. botulinový toxin typu B injekční roztok, U/ml
 NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
Světle modré, kulaté, bikonvexní obalené tablety, průměr přibližně 12,4 mm, výška přibližně 7,5 mm.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Baldriparan obalené tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje Valerianae extractum siccum 6,0 7,4 : 1, extrahováno ethanolem
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Baldriparan obalené tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje Valerianae extractum siccum 6,0 7,4 : 1, extrahováno ethanolem
2012 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 2 Jak sledovat bezpečnost léčivých přípravků v ČR problémy a výzvy MUDr. Jana Mladá Státní ústav pro kontrolu léčiv 3 O čem dnes? Monitorování bezpečnosti léčivých přípravků Farmakovigilanční systém Chyby
2 Jak sledovat bezpečnost léčivých přípravků v ČR problémy a výzvy MUDr. Jana Mladá Státní ústav pro kontrolu léčiv 3 O čem dnes? Monitorování bezpečnosti léčivých přípravků Farmakovigilanční systém Chyby
Simdax Příbalová informace
 Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
Jedna obalená tableta obsahuje Valerianae extractum siccum (3-6:1), extrahováno ethanolem 70% (V/V) 445 mg.
 Sp.zn.sukls16435/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU PERSEN mono obalená tableta 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje Valerianae extractum siccum (3-6:1),
Sp.zn.sukls16435/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU PERSEN mono obalená tableta 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna obalená tableta obsahuje Valerianae extractum siccum (3-6:1),
Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Příbalová informace: informace pro uživatele. DULCOLAX 10 mg čípky bisacodylum
 sp. zn. sukls69505/2016 Příbalová informace: informace pro uživatele DULCOLAX 10 mg čípky bisacodylum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp. zn. sukls69505/2016 Příbalová informace: informace pro uživatele DULCOLAX 10 mg čípky bisacodylum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
Farmakoterapie nádorové bolesti
 Farmakoterapie nádorové bolesti Úvod Bolest představuje jeden z nejzávažnějších projevů nádorového onemocnění. Léčba bolesti je nedílnou součástí onkologické péče. Úleva od bolesti obvykle neznamená úplnou
Farmakoterapie nádorové bolesti Úvod Bolest představuje jeden z nejzávažnějších projevů nádorového onemocnění. Léčba bolesti je nedílnou součástí onkologické péče. Úleva od bolesti obvykle neznamená úplnou
Přecitlivělost na léčivé látky nebo na kteroukoliv z pomocných látek uvedených v bodě 6.1.
 sp.zn.: sukls50035/2010, sukls106419/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H rektální mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 g Selachiorum
sp.zn.: sukls50035/2010, sukls106419/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H rektální mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 g Selachiorum
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
Souhrn údajů o přípravku
 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU. Metacam 5 mg/ml injekční roztok pro skot a prasata
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Metacam 5 mg/ml injekční roztok pro skot a prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje: Léčivá látka: Meloxicamum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Metacam 5 mg/ml injekční roztok pro skot a prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje: Léčivá látka: Meloxicamum
POKYNY PRO PRESKRIPCI OPIOIDŮ U PACIENTŮ S PRŮLOMOVOU BOLESTÍ PR I ONKOLOGICKÝCH ONEMOCNE NÍCH TITRAČNÍ SCHÉMA A INFORMACE PRO LÉKAŘE
 POKYNY PRO PRESKRIPCI OPIOIDŮ U PACIENTŮ S PRŮLOMOVOU BOLESTÍ PR I ONKOLOGICKÝCH ONEMOCNE NÍCH TITRAČNÍ SCHÉMA A INFORMACE PRO LÉKAŘE fentanyl bukální tablety 2 fentanyl bukální tablety POKYNY PRO PRESKRIPCI
POKYNY PRO PRESKRIPCI OPIOIDŮ U PACIENTŮ S PRŮLOMOVOU BOLESTÍ PR I ONKOLOGICKÝCH ONEMOCNE NÍCH TITRAČNÍ SCHÉMA A INFORMACE PRO LÉKAŘE fentanyl bukální tablety 2 fentanyl bukální tablety POKYNY PRO PRESKRIPCI
Transdermální buprenorfin. Pavel Ševčík KARIM LF MU a FN Brno
 Transdermální buprenorfin Pavel Ševčík KARIM LF MU a FN Brno Náplasťové systémy Spolu s p.o. aplikací nejúspěšnější způsob řízeného podávání léčiv Přes 35 náplastí v EU a USA Přibližně 70 přípravků v registraci
Transdermální buprenorfin Pavel Ševčík KARIM LF MU a FN Brno Náplasťové systémy Spolu s p.o. aplikací nejúspěšnější způsob řízeného podávání léčiv Přes 35 náplastí v EU a USA Přibližně 70 přípravků v registraci
PŘÍLOHA I NÁZEV, LÉKOVÁ FORMA, OBSAH LÉČIVÝCH LÁTEK, ŽIVOČIŠNÉ DRUHY, ZPŮSOB PODÁNÍ A DRŽITEL ROZHODNUTÍ O REGISTRACI 1/7
 PŘÍLOHA I NÁZEV, LÉKOVÁ FORMA, OBSAH LÉČIVÝCH LÁTEK, ŽIVOČIŠNÉ DRUHY, ZPŮSOB PODÁNÍ A DRŽITEL ROZHODNUTÍ O REGISTRACI 1/7 Členský stát Žadatel nebo držitel rozhodnutí o registraci Vymyšlený název přípravku
PŘÍLOHA I NÁZEV, LÉKOVÁ FORMA, OBSAH LÉČIVÝCH LÁTEK, ŽIVOČIŠNÉ DRUHY, ZPŮSOB PODÁNÍ A DRŽITEL ROZHODNUTÍ O REGISTRACI 1/7 Členský stát Žadatel nebo držitel rozhodnutí o registraci Vymyšlený název přípravku
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. DOXIUM 500 mg tvrdé tobolky. Calcii dobesilas monohydricus
 sp.zn. sukls178298/2011 a sp.zn. sukls285789/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DOXIUM 500 mg tvrdé tobolky Calcii dobesilas monohydricus Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls178298/2011 a sp.zn. sukls285789/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DOXIUM 500 mg tvrdé tobolky Calcii dobesilas monohydricus Přečtěte si pozorně celou příbalovou informaci dříve,
Návod pro pacienta / pečovatele
 Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Léčebné konopí v managementu symptomů onkologického onemocnění
 Léčebné konopí v managementu symptomů onkologického onemocnění MUDr. Ondřej Sláma, Ph.D. Masarykův onkologický ústav Brno Česká společnost paliativní medicíny ČLS JEP Klinický kontext Publikovaná data
Léčebné konopí v managementu symptomů onkologického onemocnění MUDr. Ondřej Sláma, Ph.D. Masarykův onkologický ústav Brno Česká společnost paliativní medicíny ČLS JEP Klinický kontext Publikovaná data
Celkové shrnutí vědeckého hodnocení přípravku Kytril a souvisejících názvů (viz příloha I)
 PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÉ INFORMACE PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 11 Vědecké závěry Celkové
PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÉ INFORMACE PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 11 Vědecké závěry Celkové
Celkové shrnutí vědeckého hodnocení přípravku Atacand Plus a související názvy (viz Příloha I)
 PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÝCH INFORMACÍ PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 14 Vědecké závěry Celkové
PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÝCH INFORMACÍ PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 14 Vědecké závěry Celkové
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
CZ PAR. QUETIAPINI FUMARAS Seroquel. UK/W/0004/pdWS/001 NL/W/0004/pdWS/001
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
PŘÍBALOVÁ INFORMACE PRO: Carporal 160 mg tablety pro psy
 PŘÍBALOVÁ INFORMACE PRO: Carporal 160 mg tablety pro psy 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ ŠARŽE, POKUD SE NESHODUJE Držitel rozhodnutí
PŘÍBALOVÁ INFORMACE PRO: Carporal 160 mg tablety pro psy 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ ŠARŽE, POKUD SE NESHODUJE Držitel rozhodnutí
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
po 5 letech ... s excelentním kosmetickým výsledkem 2
 ... s excelentním kosmetickým výsledkem 2 pred lécbou 6. týden 12. týden po 1 roku po 3 letech po 5 letech Správný výber pro Vaše pacienty se superficiálními BCC - krátkodobá lécba s velice dobrým kosmetickým
... s excelentním kosmetickým výsledkem 2 pred lécbou 6. týden 12. týden po 1 roku po 3 letech po 5 letech Správný výber pro Vaše pacienty se superficiálními BCC - krátkodobá lécba s velice dobrým kosmetickým
MINISTERSTVO ZDRAVOTNICTVÍ ČESKÉ REPUBLIKY P Ř E D B Ě Ž N É O P A T Ř E N Í O B E C N É P O V A HY
 MINISTERSTVO ZDRAVOTNICTVÍ ČESKÉ REPUBLIKY V Praze 26. dubna 2018 Č.j.: MZDR 16343/2018-4/FAR *MZDRX0128PEI* MZDRX0128PEI P Ř E D B Ě Ž N É O P A T Ř E N Í O B E C N É P O V A HY České republiky (dále
MINISTERSTVO ZDRAVOTNICTVÍ ČESKÉ REPUBLIKY V Praze 26. dubna 2018 Č.j.: MZDR 16343/2018-4/FAR *MZDRX0128PEI* MZDRX0128PEI P Ř E D B Ě Ž N É O P A T Ř E N Í O B E C N É P O V A HY České republiky (dále
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obal na tablety se 400 mg potahovanými tabletami 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibuprofen Dr.Max 400 mg potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obal na tablety se 400 mg potahovanými tabletami 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibuprofen Dr.Max 400 mg potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Úzkost u seniorů. Stres, úzkost a nespavost ve stáří. Úzkost a poruchy chování ve stáří. Sborník přednášek z Jarního sympozia 2011
 Úzkost u seniorů Stres, úzkost a nespavost ve stáří MUDr. Petr Hrubeš Hradec Králové Úzkost a poruchy chování ve stáří MUDr. Vanda Franková Dobřany Sborník přednášek z Jarního sympozia 2011 Moderní trendy
Úzkost u seniorů Stres, úzkost a nespavost ve stáří MUDr. Petr Hrubeš Hradec Králové Úzkost a poruchy chování ve stáří MUDr. Vanda Franková Dobřany Sborník přednášek z Jarního sympozia 2011 Moderní trendy
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum)
 sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90
 Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
EXELON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY
 XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
