příloha č.1 ke sdělení sp.zn.sukls116313/2012
|
|
|
- Iveta Horáková
- před 10 lety
- Počet zobrazení:
Transkript
1 příloha č.1 ke sdělení sp.zn.sukls116313/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cordarone injekční roztok Amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. - Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka. - Tento přípravek byl předepsán Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné příznaky jako Vy. - Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi. V příbalové informaci naleznete: 1. Co je Cordarone a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete Cordarone užívat 3. Jak se Cordarone užívá 4. Možné nežádoucí účinky 5 Jak Cordarone uchovávat 6. Další informace 1. CO JE CORDARONE A K ČEMU SE POUŽÍVÁ Indikační skupina Antiarytmikum. Charakteristika Antiarytmické vlastnosti: Prodloužení 3. fáze stažení vláken srdečního svalu, které vede k poklesu proudu draslíku (III. třída podle Vaughan Williamsovy klasifikace), toto prodloužení není ovlivněno srdeční frekvencí. Snížení sinusové automaticity vedoucí k bradykardii neodpovídající na podání atropinu. Nekompetitivní alfa- a beta-adrenergní inhibice. Zpomalení sinoatriálního, atriálního a nodálního vedení, které je výraznější, pokud je rytmus rychlý. Intraventrikulární vedení není ovlivněno. Prodloužení refrakterní periody a snížení excitability myokardu na atriální, nodální i ventrikulární úrovni. Zpomalení vedení a prodloužení refrakterní periody v přídatných atrioventrikulárních spojích. Antianginózní vlastnosti: Střední pokles periferního odporu a snížení srdeční frekvence vedoucí k poklesu spotřeby kyslíku. Nekompetitivní alfa- a beta- adrenergní inhibice. Zvýšení koronárního průtoku díky přímému účinku na hladké svaly artérií myokardu. Udržování srdečního výdeje díky poklesu aortálního tlaku a periferního odporu. Jiné vlastnosti: Amiodaron má jen mírný negativně inotropní účinek. Farmakokinetické údaje 1/7
2 Koncentrace amiodaronu v krvi dosažená po intravenózním podání rychle klesá, protože látka proniká do tkání. Amiodaron má maximální účinek 15 minut po i.v. podání, do 4 hodin účinek vymizí. Pokud se injekce nezopakuje, látka se postupně vyloučí. Zásoby ve tkáních se tvoří až po opakovaných injekcích nebo při pokračování léčby perorálním podáváním. Indikace Amiodaron je indikován pouze v léčbě těžkých poruch rytmu, zvláště u: těžkých supraventrikulárních poruch rytmu s rychlou frekvencí komor, tachykardie spojené s Wolff-Parkinson-Whiteovým syndromem. doložených symptomatických a hemodynamicky závažných poruch rytmu (komorové tachykardie, závažné formy komorových extrasystol). Intravenózní podání amiodaronu je vhodné zejména tam, kde je nutno dosáhnout rychlé odpovědi nebo kde perorální podání není možné. Přípravek je určen k léčbě dospělých pacientů. 2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE CORDARONE UŽÍVAT Neužívejte Cordarone v těchto případech: Sinusová bradykardie, sinoatriální blok a sick sinus syndrom (riziko sinusové zástavy), těžké poruchy atrioventrikulárního vedení, pokud pacient nemá zaveden kardiostimulátor Bi- nebo tri-fascikulární poruchy vedení, pokud pacient nemá kardiostimulátor, nebo je umístěn na jednotce intenzívní péče a je zajištěn elektrosystolický pacing. Oběhové selhávání, těžká arteriální hypotenze. Kombinovaná léčba s léky, které mohou způsobit Torsades de Pointes. Thyreoidální dysfunkce. Známá přecitlivělost na jód, amiodaron nebo pomocné látky obsažené v přípravku. Intravenózní injekce amiodaronu je kontraindikována v případě hypotenze, těžké respirační nedostatečnosti, kardiomyopatie a srdečního selhávání (možné zhoršení). Těhotenství, vyjma výjimečných okolností. Kojení. Přípravek Cordarone nesmí užívat předčasně narozené děti ani novorozenci a děti do 3 let vzhledem k obsahu benzylalkoholu. Žádná z výše uvedených kontraindikací neplatí při použití amiodaronu při kardiopulmonální resuscitaci pro komorovou fibrilaci rezistentní na elektrickou kardioverzi. Kombinace amiodaronu s léky, které mohou vyvolat Torsade de Pointes, jsou kontraindikovány. Jde o: - antiarytmika třídy Ia, bepridil, sotalol, - další látky bez antiarytmického účinku: např. vinkamin, sultoprid, některá neuroleptika, cisaprid, erythromycin intravenózně, pentamidin parenterálně, kvůli zvýšenému riziku potenciálně letální komorové tachykardie typu torsades de pointes. Zvláštní opatrnosti při použití Cordarone je zapotřebí Nelze doporučit kombinace s těmito látkami: - beta-blokátory a některé blokátory kalciového kanálu (verapamil, diltiazem) - může dojít k poruchám automaticity (vážná bradykardie) nebo vedení. - stimulující laxativa, která mohou způsobit hypokalémii a tedy riziko Torsade de Pointes. Ostatní laxativa používat lze. - Pacienti léčení amiodaronem by neměli užívat fluorochinolony. Jen s velkou opatrností lze amiodaron kombinovat s následujícími léky: Látky, které mohou způsobit hypokalémii: - Diuretika způsobující hypokalémii, samotná i v kombinaci. 2/7
3 - Systémové kortikoidy, tetracosactid. - Amfotericin B podávaný intravenózně. Je nezbytné zabránit vzniku hypokalémie a event. vzniklou hypokalémii korigovat; QT interval by měl být monitorován; v případě vzniku komorové tachykardie typu torsades de pointes nesmějí být podána antiarytmika (měl by být zahájen komorový pacing, může být použito i.v. magnézium). Zvláštní upozornění a opatření pro použití Zvláštní upozornění Podávání amiodaronu intravenózní injekcí se obecně nedoporučuje vzhledem k riziku poruch hemodynamiky (těžká hypotenze, oběhový kolaps; pokud je to možné, je třeba vždy dát přednost infúzi. Intravenózní injekci lze podávat jen v krajním případě, kdy ostatní možnosti léčby selhaly, a vždy jen na kardiologické jednotce intenzivní péče za neustálého monitorování EKG a TK. Dávka je 5 mg/kg tělesné hmotnosti. S výjimkou kardiopulmonální resuscitace pro komorovou fibrilaci rezistentní na elektrickou kardioverzi by měl být amiodaron podán během minimálně 3 minut. Intravenózní injekci nelze opakovat dříve než za 15 minut po první injekci, a to i kdyby druhá dávka činila pouze množství odpovídající 1 ampuli (hrozí nezvládnutelný kolaps). Přípravek nelze mísit s jinými léky ve stejné stříkačce. Nepodávejte ostatní přípravky stejným katetrem. Pokud je nutno v terapii pokračovat, je třeba přejít na intravenózní infúzi. Srdeční poruchy Byl hlášen vznik nových arytmií nebo zhoršení léčených arytmií, někdy s fatálním zakončením. Je důležité, ale obtížné, rozlišit nedostatečnou účinnost léčiva od proarytmického působení, ať už je spojeno se zhoršením srdečního stavu či nikoli. Proarytmické působení je hlášeno u amiodaronu řidčeji než u ostatních antiarytmik, a obecně se vyskytuje v souvislosti s lékovými interakcemi a/nebo poruchami elektrolytů. Plicní onemocnění Výskyt dyspnoe nebo neproduktivního kašle může souviset s plicní toxicitou jako je intersticiální pneumonitida. Velmi vzácně byly po podání intravenózního amiodaronu hlášeny případy intersticiální pneumonitidy. Při podezření na tuto diagnózu by měl být proveden RTG hrudníku. Terapie amiodaronem by měla být přehodnocena, protože intersticiální pneumonitida je obecně reverzibilní, pokud je amiodaron vysazen včas, a měla by být zvážena terapie kortikosteroidy. Dále bylo zaznamenáno několik případů vážných respiračních komplikací, někdy i s fatálním koncem, nejčastěji krátce po chirurgickém výkonu (syndrom akutní respirační tísně dospělých), které lze dát do souvislosti s podáním vyšších koncentrací kyslíku. Jaterní onemocnění Důkladné sledování jaterních testů (transamináz) je doporučeno, jakmile je zahájena léčba amiodaronem, a dále pravidelně během léčby. U perorální a intravenózní formy a během prvních 24 hodin po IV podání se může vyskytnout akutní postižení jater (včetně závažné hepatocelulární nedostatečnosti nebo jaterního selhání, někdy smrtelného) a chronické jaterní onemocnění. Dávka amiodaronu by proto měla být snížena nebo by měla být léčba přerušena, jestliže dojde k vzestupu převyšujícímu 3x normální hodnoty transamináz. Klinické a biologické příznaky chronické jaterní poruchy mohou být minimální (hepatomegalie, zvýšení transamináz až 5násobně nad normální rozsah hodnot) a reverzibilní po ukončení léčby, nicméně byly hlášeny i fatální případy. Zvláštní opatření Intravenózní injekci amiodaronu lze podávat jen na kardiologické jednotce intenzívní péče za neustálého monitorování EKG a TK. Pokud je to možné, měl by být amiodaron podáván centrálním žilním katetrem, kvůli zabránění reakce v místě vpichu 3/7
4 Je třeba být zvlášť opatrný v případech hypotenze, těžkého respiračního selhání a dekompenzovaného nebo těžkého srdečního selhání. Děti Bezpečnost a účinnost amiodaronu u dětí nebyla hodnocena, proto jeho užití není doporučeno. Ampule s roztokem amiodaronu pro intravenózní podání obsahují benzylalkohol. Byly hlášeny případy gasping syndromu s fatálním zakončením u novorozenců (dětí mladších než 1 měsíc) po podání IV roztoku obsahujícího toto konzervační činidlo. Symptomy zahrnují náhlý začátek výše uvedeného syndromu, hypotenzi, bradykardii a oběhový kolaps. Anestézie Před chirurgickým zákrokem by měl být anesteziolog upozorněn, že pacient užívá amiodaron. Vzájemné působení s dalšími léčivými přípravky Perorální antikoagulancia: Amiodaron zvyšuje plazmatickou koncentraci warfarinu přes inhibicí cytochromu P450 2C9. Kombinace warfarinu s amiodaronem může proto vést k předávkování warfarinem což zvyšuje riziko krvácení. Je nezbytné sledovat protrombinový čas častěji a podle aktuálních hodnot upravit dávku warfarinu jak během léčby amiodaronem, tak po jeho vysazení. Digoxin: Mohou se objevit poruchy automaticity (vážná bradykardie) nebo atrioventrikulárního vedení (synergické působení). Kromě toho nelze vyloučit vzestup plazmatické hladiny digoxinu (vzhledem k poklesu jeho clearance). Je třeba monitorovat EKG a plazmatickou hladinu digoxinu a pacienti by měli být sledováni pro vznik klinických příznaků toxicity digoxinu. Je nutné přizpůsobit léčebnou dávku digitalisu. Fenytoin: Amiodaron zvyšuje plazmatickou koncentraci fenytoinu inhibicí cytochromu P450 2C9. Kombinace fenytoinu s amiodaronem může proto vést k předávkování fenytoinem, vyvolávající neurologické příznaky. Musí se provádět klinické sledování a dávka fenytoinu musí být snížena, jakmile se objeví příznaky předávkování; hladina plazmatického fenytoinu má být rozhodující. Flekainid: Amiodaron zvyšuje plazmatickou koncentraci flekainidu inhibicí cytochromu CYP 2D6, dávka amiodaronu by proto měla být upravena. Léčiva metabolizovaná cytochromem P450 3A4: Společné podávání takových léčiv s amiodaronem, inhibitorem CYP 3A4, může vést ke zvýšení jejich plazmatické koncentrace a tím k možnému zvýšení jejich toxicity: Cyklosporin: jeho kombinace s amiodaronem může zvýšit plazmatickou hladinu cyklosporinu. Dávky mají být upraveny. Fentanyl: jeho kombinace s amiodaronem může zvýšit farmakologický účinek fentanylu a zvyšuje riziko jeho toxicity. Statiny: kombinací amiodaronu se statiny metabolizovanými CYP 3A4 jako jsou simvastatin, atorvastatin a lovastatin se zvyšuje riziko svalové toxicity. Pokud je podáván amiodaron, doporučuje se používat statiny nemetabolizované CYP 3A4. Jiné léky metabolizované CYP 3A4: lidokain, takrolimus, silfdenafil, midazolam, triazolam, dihydroergotamin, ergotamin. Anestézie Byly zaznamenány potenciálně vážné komplikace u pacientů s celkovou anestézií: bradykardie (neodpovídající na atropin), hypotenze, poruchy vedení, snížený srdeční výdej. Ve velmi vzácných případech byly hlášeny závažné respirační komplikace (akutní syndrom respirační nedostatečnosti dospělých), někdy smrtící, bývají obvykle pozorovány v období bezprostředně 4/7
5 následujícím po chirurgickém výkonu. Mohou vyplývat z možné interakce s vysoko koncentrovaným kyslíkem. Těhotenství a kojení Poraďte se se svým lékařem nebo lékárníkem dříve, než začnete užívat jakýkoliv lék. Těhotenství: Vzhledem ke svým účinkům na štítnou žlázu plodu je amiodaron v těhotenství až na výjimky kontraindikován. V těchto zvláštních případech je třeba velmi pečlivě zvážit potenciální přínos terapie. Kojení: Amiodaron je vylučován ve významném množství do mateřského mléka, je tedy kontraindikován v období kojení. Řízení dopravních prostředků a obsluha strojů Amiodaron nemá žádný vliv na schopnost řídit nebo obsluhovat stroje. Důležité informace o některých složkách přípravku Cordarone Tento léčivý přípravek obsahuje benzylalkohol (20 mg/ml) jako konzervační látku. Benzlyalkohol může zapříčinit toxické a alergické reakce u kojenců a dětí do 3 let. 3. JAK SE CORDARONE UŽÍVÁ Vždy užívejte Cordarone přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem. Intravenózní infúze: Počáteční dávka: obvykle 5 mg/kg tělesné hmotnosti podáno v 250 ml 5% dextrózy v rozmezí 20 minut až 2 hodin. Tuto infuzi lze opakovat 2x až 3x během 24 hodin. Rychlost podávání je třeba stanovit na základě výsledků vyšetření. Terapeutické účinky se objeví během prvních minut podávání a pak se postupně snižují. Infuzi je tedy třeba podle toho regulovat. Udržovací dávka: 10 až 20 mg/kg tělesné hmotnosti za 24 hodin (obvykle mg/24 hodin, nevíce než 1200 mg/24 hodin) s 250 ml 5% dextrózy po dobu několika dnů. Od prvního dne podávání infuze lze nahradit perorálním podáváním. Intravenózní injekce: Intravenózní injekce se podává jen ve zcela výjimečných případech. Obvykle se podává 5 mg/kg tělesné hmotnosti, pomalu, během alespoň 3 minut. Opakované podání injekce je možné nejdříve za 15 minut. V další terapii je třeba pokračovat i.v. infúzí. Nelze mísit s jinými přípravky. Kardiopulmonální resuscitace komorové fibrilace resistentní na elektrickou kardioverzi: počáteční dávka je 300 mg amiodaronu (nebo 5 mg/kg tělesné hmotnosti) zředěného ve 20 ml 5% dextrózy podané jako IV bolus. Při přetrvávající komorové fibrilaci je možno zvážit podání dalších 150 mg IV (nebo 2,5 mg/kg tělesné hmotnosti). Přípravek nelze používat v koncentracích nižších než 600 mg/l. Podávat pouze s 5% dextrózou. Předávkování : O předávkování intravenózním amiodaronem nejsou k dispozici žádné informace. Existují omezené údaje o akutním předávkování amiodaronem podaným perorálně. Bylo zaznamenáno několik málo případů sinusové bradykardie, srdeční zástavy, záchvatů komorové tachykardie, torsades de pointes, oběhového selhání a poškození jater. Léčba by měla být symptomatická. Ani amiodaron, ani jeho metabolity nejsou dialyzovatelné. 5/7
6 Jsou k dispozici pouze omezené údaje týkající se bezpečnosti a účinnosti přípravku CORDARONE u dětí. O vhodné dávce rozhodne lékař. Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka. 4. MOŽNÉ NEŽÁDOUCÍ ÚČINKY Podobně jako všechny léky, může mít i Cordarone nežádoucí účinky, které se ale nemusí vyskytnout u každého. Následující nežádoucí účinky jsou setříděny podle orgánových systémů a zařazeny do seznamu dle frekvence výskytu následovně: velmi časté ( 1/10); časté ( 1/100 až <1/10); méně časté ( 1/1000 až <1/100); vzácné ( 1/10000 až <1/1000); velmi vzácné <1/10000); není známo (z dostupných údajů nelze určit). Srdeční poruchy: - Časté: bradykardie, převážně středně závažná. - Velmi vzácné: významná bradykardie, sinusová zástava, vyžadující přerušení podávání amiodaronu, zvláště u pacientů s dysfunkcí sinusového uzlu a/nebo u starších pacientů; začátek nebo zhoršení arytmie, někdy následované srdeční zástavou. Endokrinní poruchy: - Není známo: hypertyreóza. Gastrointestinální poruchy: - Velmi vzácné: nausea. Celkové poruchy a reakce v místě aplikace: -Časté: reakce v místě vpichu injekce, jako např. bolest, zarudnutí kůže, otok, nekróza, extravazát, infiltrace, zánět, zatvrdnutí, tromboflebitida, flebitida, celulitida, infekce, změna pigmentace. Poruchy jater a žlučových cest: - Velmi vzácné: - izolovaný vzestup sérových transamináz, který je obvykle středně závažný (1,5x až 3x nad normu) objevující se v začátku léčby. Toto se může vrátit k normě po snížení dávky nebo dokonce spontánně. - akutní onemocnění jater s vysokými transaminázami a/nebo žloutenkou, včetně jaterního selhání, které někdy bývá smrtelné. Poruchy imunitního systému: - Velmi vzácné: anafylaktický šok. - Není známo: angioneurotický edém (Quinckeho edém). Poruchy svalové a kosterní soustavy a pojivové tkáně: - Není známo: bolest zad. Poruchy nervového systému: - Velmi vzácné: benigní intrakraniální hypertenze (pseudotumor cerebri), bolest hlavy. Respirační, hrudní a mediastinální poruchy: - Velmi vzácné: intersticiální pneumonitida, vážné respirační komplikace (akutní syndrom respirační nedostatečnosti dospělých) někdy s fatálním koncem, bronchospasmus a/nebo apnoe u pacientů s vážnou respirační nedostatečností, zvláště u astmatických pacientů. Poruchy kůže a podkožní tkáně: 6/7
7 - Velmi vzácné: svědění - Není známo (z dostupných údajů nelze určit): kopřivka Cévní poruchy: - Časté: pokles krevního tlaku, obvykle mírný a přechodný. Případy závažné hypotenze nebo kolapsu se vyskytly po předávkování nebo po příliš rychlé aplikaci injekce. - Velmi vzácné: zčervenání. Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi. 5. JAK CORDARONE UCHOVÁVAT Varování Uchovávejte mimo dosah a dohled dětí. Nepoužívejte po uplynutí doby použitelnosti vyznačené na obalu. Doba použitelnosti 2 roky. Uchovávání Uchovávejte při teplotě do 25 C. 6. DALŠÍ INFORMACE Co Cordarone obsahuje Léčivou látkou je amiodaroni hydrochloridum 150 mg ve 3 ml injekčního roztoku. Pomocné látky jsou benzylalkohol (50 mg/ml), polysorbát 80, voda na injekci. Jak Cordarone vypadá a co obsahuje toto balení Cordarone je čirý, slabě žlutý injekční roztok Velikost balení: 6 ampulí po 3 ml 10 ampulí po 3 ml Držitel rozhodnutí o registraci sanofi-aventis, s.r.o., Praha, Česká republika Výrobce Sanofi Winthrop Industrie, Ambares, Francie Sanofi Winthrop Industrie, Quetigny, Francie Datum poslední revize /7
příloha č.2 ke sdělení sp.zn.sukls116313/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 příloha č.2 ke sdělení sp.zn.sukls116313/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORDARONE injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amiodaroni hydrochloridum 150 mg ve 3 ml injekčního
příloha č.2 ke sdělení sp.zn.sukls116313/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORDARONE injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amiodaroni hydrochloridum 150 mg ve 3 ml injekčního
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls58194/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORDARONE injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amiodaroni hydrochloridum 150 mg ve 3 ml injekčního roztoku. Pomocné
sp.zn. sukls58194/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORDARONE injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amiodaroni hydrochloridum 150 mg ve 3 ml injekčního roztoku. Pomocné
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls31037/2008 a příloha k sp.zn.: sukls84062/2011
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls31037/2008 a příloha k sp.zn.: sukls84062/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Sedacoron Injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls31037/2008 a příloha k sp.zn.: sukls84062/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Sedacoron Injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls187398/2013 1. NÁZEV PŘÍPRAVKU Sedacoron Injekční roztok SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amiodaroni hydrochloridum 150 mg ve 3 ml (1 ampule) Pomocné látky:
sp.zn. sukls187398/2013 1. NÁZEV PŘÍPRAVKU Sedacoron Injekční roztok SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amiodaroni hydrochloridum 150 mg ve 3 ml (1 ampule) Pomocné látky:
Příbalová informace: informace pro uživatele. CORDARONE 150 mg/3 ml injekční roztok. amiodaroni hydrochloridum
 sp.zn.sukls33439/2016 Příbalová informace: informace pro uživatele CORDARONE 150 mg/3 ml injekční roztok amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.sukls33439/2016 Příbalová informace: informace pro uživatele CORDARONE 150 mg/3 ml injekční roztok amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Intravenózní podání amiodaronu je vhodné zejména tam, kde je nutno dosáhnout rychlé odpovědi nebo kde perorální podání není možné.
 sp.zn.sukls33439/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORDARONE 150 mg/3 ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního roztoku obsahuje amiodaroni hydrochloridum
sp.zn.sukls33439/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORDARONE 150 mg/3 ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml injekčního roztoku obsahuje amiodaroni hydrochloridum
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Fluorochinolony a riziko prodloužení QT intervalu Finální text SPC a PIL odsouhlasený PhVWP v prosinci 2010
 Fluorochinolony a riziko prodloužení QT intervalu Finální text SPC a PIL odsouhlasený PhVWP v prosinci 2010 Gemifloxacin 1 and moxifloxacin SPC 4.3 Kontraindikace V preklinickém i klinickém hodnocení byly
Fluorochinolony a riziko prodloužení QT intervalu Finální text SPC a PIL odsouhlasený PhVWP v prosinci 2010 Gemifloxacin 1 and moxifloxacin SPC 4.3 Kontraindikace V preklinickém i klinickém hodnocení byly
Simdax Příbalová informace
 Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Chirocaine 5 mg/ml Chirocaine 7,5 mg/ml injekční roztok (Levobupivacaini hydrochloridum)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Chirocaine 5 mg/ml Chirocaine 7,5 mg/ml injekční roztok (Levobupivacaini hydrochloridum) V příbalové informaci naleznete: 1. Co je přípravek Chirocaine a k
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Chirocaine 5 mg/ml Chirocaine 7,5 mg/ml injekční roztok (Levobupivacaini hydrochloridum) V příbalové informaci naleznete: 1. Co je přípravek Chirocaine a k
Příloha č.2 k rozhodnutí o změně registrace sp.zn.sukls2721/2013 a příloha k sp.zn.sukls115428/2012 a71477/2011
 Příloha č.2 k rozhodnutí o změně registrace sp.zn.sukls2721/2013 a příloha k sp.zn.sukls115428/2012 a71477/2011 1. NÁZEV PŘÍPRAVKU CORDARONE tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č.2 k rozhodnutí o změně registrace sp.zn.sukls2721/2013 a příloha k sp.zn.sukls115428/2012 a71477/2011 1. NÁZEV PŘÍPRAVKU CORDARONE tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn. sukls131383/2009 a příloha ke sp.zn. sukls85044/2008, sukls33584/2011
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn. sukls131383/2009 a příloha ke sp.zn. sukls85044/2008, sukls33584/2011 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE XATRAL 5-SR tablety s prodlouženým
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn. sukls131383/2009 a příloha ke sp.zn. sukls85044/2008, sukls33584/2011 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE XATRAL 5-SR tablety s prodlouženým
Chirocaine Příbalová informace
 Chirocaine Příbalová informace Informace pro použití, čtěte pozorně Chirocaine 2,5 mg/ml Chirocaine 5 mg/ml Chirocaine 7,5 mg/ml (Levobupivacaini hydrochloridum) Injekční roztok Držitel rozhodnutí o registraci
Chirocaine Příbalová informace Informace pro použití, čtěte pozorně Chirocaine 2,5 mg/ml Chirocaine 5 mg/ml Chirocaine 7,5 mg/ml (Levobupivacaini hydrochloridum) Injekční roztok Držitel rozhodnutí o registraci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Pavulon 4mg = 2ml injekční roztok. Pancuronii bromidum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pavulon 4mg = 2ml injekční roztok Pancuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pavulon 4mg = 2ml injekční roztok Pancuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. AMIOKORDIN 200mg, tablety amiodaroni hydrochloridum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AMIOKORDIN 200mg, tablety amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AMIOKORDIN 200mg, tablety amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si
Příbalová informace: informace pro uživatele. CORDARONE 200 mg tablety. amiodaroni hydrochloridum
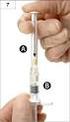 sp.zn. sukls180041/2015 Příbalová informace: informace pro uživatele CORDARONE 200 mg tablety amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls180041/2015 Příbalová informace: informace pro uživatele CORDARONE 200 mg tablety amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. MUCOSOLVAN junior Sirup Ambroxoli hydrochloridum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE MUCOSOLVAN junior Sirup Ambroxoli hydrochloridum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek je
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE MUCOSOLVAN junior Sirup Ambroxoli hydrochloridum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek je
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls19362/2007
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls19362/2007 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Rivodaron 200 Tablety 2. SLOŽENÍ KVALITATIVNÍ I KVANTITATIVNÍ Amiodaroni hydrochloridum
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls19362/2007 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Rivodaron 200 Tablety 2. SLOŽENÍ KVALITATIVNÍ I KVANTITATIVNÍ Amiodaroni hydrochloridum
prášek pro infuzní roztok
 sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Co je Voltaren Ophtha CD Léčivou látkou přípravku Voltaren Ophtha CD je diklofenak sodný (diclofenacum natricum).
 Příloha č.1 ke sdělení sp.zn.sukls23896/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VOLTAREN OPHTHA CD oční kapky, roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha č.1 ke sdělení sp.zn.sukls23896/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VOLTAREN OPHTHA CD oční kapky, roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SUSTANON 250 250 mg/ml, injekční roztok Testosteroni
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SUSTANON 250 250 mg/ml, injekční roztok Testosteroni
Příbalová informace: informace pro pacienta MOLSIHEXAL RETARD. tablety s prodlouženým uvolňováním (molsidominum)
 sp.zn. sukls30749/2015 Příbalová informace: informace pro pacienta MOLSIHEXAL RETARD tablety s prodlouženým uvolňováním (molsidominum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls30749/2015 Příbalová informace: informace pro pacienta MOLSIHEXAL RETARD tablety s prodlouženým uvolňováním (molsidominum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90
 Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. HYPNOMIDATE, 2 mg/ml, injekční roztok Etomidatum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HYPNOMIDATE, 2 mg/ml, injekční roztok Etomidatum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HYPNOMIDATE, 2 mg/ml, injekční roztok Etomidatum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: Informace pro uživatele. Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum)
 sp.zn. sukls273948/2016 Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls273948/2016 Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls197811/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RIVODARON 200 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amiodaroni hydrochloridum 200 mg. Pomocná látka
sp.zn. sukls197811/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RIVODARON 200 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amiodaroni hydrochloridum 200 mg. Pomocná látka
PŘÍLOHA III DODATKY K SOUHRN ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACI
 PŘÍLOHA III DODATKY K SOUHRN ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACI 1 DODATKY MAJÍ BÝT ZAŘAZENY DO ODPOVÍDAJÍCÍCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH MOXIFLOXACIN Následující
PŘÍLOHA III DODATKY K SOUHRN ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACI 1 DODATKY MAJÍ BÝT ZAŘAZENY DO ODPOVÍDAJÍCÍCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH MOXIFLOXACIN Následující
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Kytril inj/inf koncentrát pro přípravu injekčního nebo infuzního roztoku Granisetroni hydrochloridum
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls211402/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kytril inj/inf koncentrát pro přípravu injekčního nebo infuzního roztoku Granisetroni hydrochloridum
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls211402/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kytril inj/inf koncentrát pro přípravu injekčního nebo infuzního roztoku Granisetroni hydrochloridum
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. APAURIN 10 mg/2 ml injekční roztok (diazepamum)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APAURIN 10 mg/2 ml injekční roztok (diazepamum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APAURIN 10 mg/2 ml injekční roztok (diazepamum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 1 ke sdělení sp. zn. sukls230808/2010 1. NÁZEV PŘÍPRAVKU AMIOKORDIN 2. SLOŽENÍ Amiodaroni hydrochloridum 200 mg v 1 tabletě SOUHRN ÚDAJŮ O PŘÍPRAVKU 3. LÉKOVÁ FORMA Tablety. Popis přípravku:
Příloha č. 1 ke sdělení sp. zn. sukls230808/2010 1. NÁZEV PŘÍPRAVKU AMIOKORDIN 2. SLOŽENÍ Amiodaroni hydrochloridum 200 mg v 1 tabletě SOUHRN ÚDAJŮ O PŘÍPRAVKU 3. LÉKOVÁ FORMA Tablety. Popis přípravku:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls200606/2015 1. NÁZEV PŘÍPRAVKU Sedacoron 200 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amiodaroni hydrochloridum 200 mg. Pomocná látka
sp.zn. sukls200606/2015 1. NÁZEV PŘÍPRAVKU Sedacoron 200 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amiodaroni hydrochloridum 200 mg. Pomocná látka
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. PROPAFENON AL 150 PROPAFENON AL 300 potahované tablety propafenoni hydrochloridum
 Příloha č.1 ke sdělení sp.zn.sukls8522/2012 a sukls8523/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PROPAFENON AL 150 PROPAFENON AL 300 potahované tablety propafenoni hydrochloridum Přečtěte si pozorně
Příloha č.1 ke sdělení sp.zn.sukls8522/2012 a sukls8523/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PROPAFENON AL 150 PROPAFENON AL 300 potahované tablety propafenoni hydrochloridum Přečtěte si pozorně
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. FENTANYL-JANSSEN, 0,5 mg/10 ml, injekční roztok Fentanylum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE FENTANYL-JANSSEN, 0,5 mg/10 ml, injekční roztok Fentanylum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE FENTANYL-JANSSEN, 0,5 mg/10 ml, injekční roztok Fentanylum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte
Příbalová informace: informace pro pacienta. RIVODARON 200 mg tablety amiodaroni hydrochloridum
 sp.zn. sukls257312/2018 a sukls249485/2018 Příbalová informace: informace pro pacienta RIVODARON 200 mg tablety amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls257312/2018 a sukls249485/2018 Příbalová informace: informace pro pacienta RIVODARON 200 mg tablety amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příbalová informace: informace pro uživatele. AMIOKORDIN 200mg, tablety amiodaroni hydrochloridum
 sp.zn. sukls 69030/2014 Příbalová informace: informace pro uživatele AMIOKORDIN 200mg, tablety amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls 69030/2014 Příbalová informace: informace pro uživatele AMIOKORDIN 200mg, tablety amiodaroni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls115710/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLYPRESSIN 1 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna ampule s 8,5 ml
Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls115710/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLYPRESSIN 1 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna ampule s 8,5 ml
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Příbalová informace: informace pro uživatele. PROPANORM 35 mg/10 ml injekční/infuzní roztok Injekční/infuzní roztok propafenoni hydrochloridum
 sp.zn. sukls330174/2017 Příbalová informace: informace pro uživatele PROPANORM 35 mg/10 ml injekční/infuzní roztok Injekční/infuzní roztok propafenoni hydrochloridum Přečtěte si pozorně celou příbalovou
sp.zn. sukls330174/2017 Příbalová informace: informace pro uživatele PROPANORM 35 mg/10 ml injekční/infuzní roztok Injekční/infuzní roztok propafenoni hydrochloridum Přečtěte si pozorně celou příbalovou
2. Čemu musíte věnovat pozornost, než začnete přípravek Duphalac užívat
 sp.zn.sukls247606/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Duphalac 667 g/l, perorální roztok lactulosum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje.
sp.zn.sukls247606/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Duphalac 667 g/l, perorální roztok lactulosum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. MedDex Vicks pastilky na suchý kašel s medem 7, 33 mg pastilky dextromethorphanum
 Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls125353/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE MedDex Vicks pastilky na suchý kašel s medem 7, 33 mg pastilky dextromethorphanum Přečtěte si
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls125353/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE MedDex Vicks pastilky na suchý kašel s medem 7, 33 mg pastilky dextromethorphanum Přečtěte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CAMILIA perorální roztok v jednodávkovém obalu
 sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls20181/2014
 sp.zn. sukls20181/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ADENOCOR injekční roztok Adenosinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
sp.zn. sukls20181/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ADENOCOR injekční roztok Adenosinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte
Ebrantil 25 mg injekční roztok Ebrantil 50 mg injekční roztok urapidilum
 sp. zn. sukls441128/2018 Příbalová informace: informace pro pacienta Ebrantil 25 mg injekční roztok Ebrantil 50 mg injekční roztok urapidilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp. zn. sukls441128/2018 Příbalová informace: informace pro pacienta Ebrantil 25 mg injekční roztok Ebrantil 50 mg injekční roztok urapidilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls180041/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORDARONE 200 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amiodaroni hydrochloridum 200 mg. Pomocná látka
sp.zn. sukls180041/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORDARONE 200 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amiodaroni hydrochloridum 200 mg. Pomocná látka
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
sp.zn. sukls145178/2014
 sp.zn. sukls145178/2014 Příbalová informace: informace pro uživatele COROTROP injekční roztok milrinonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
sp.zn. sukls145178/2014 Příbalová informace: informace pro uživatele COROTROP injekční roztok milrinonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro uživatele AESCIN-TEVA. 20 mg, enterosolventní tablety. escinum alfa
 sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Ardeaosmosol Ma 10 Ardeaosmosol Ma 15 Ardeaosmosol Ma 20 Infúzní roztok (Mannitolum)
 sp.zn. sukls166874/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Ardeaosmosol Ma 10 Ardeaosmosol Ma 15 Ardeaosmosol Ma 20 Infúzní roztok (Mannitolum) Přečtěte si pozorně celou příbalovou informaci
sp.zn. sukls166874/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Ardeaosmosol Ma 10 Ardeaosmosol Ma 15 Ardeaosmosol Ma 20 Infúzní roztok (Mannitolum) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele. FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
Příloha č.1 k rozhodnutí o změně registrace sp.zn.sukls233573/2012. Příbalová informace: Informace pro uživatele
 Příloha č.1 k rozhodnutí o změně registrace sp.zn.sukls233573/2012 Příbalová informace: Informace pro uživatele Mesocain 1 % injekční roztok Trimecaini hydrochloridum Přečtěte si pozorně celou příbalovou
Příloha č.1 k rozhodnutí o změně registrace sp.zn.sukls233573/2012 Příbalová informace: Informace pro uživatele Mesocain 1 % injekční roztok Trimecaini hydrochloridum Přečtěte si pozorně celou příbalovou
sp. zn. sukls180859/2015
 sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Pomocná látka se známým účinkem: jedna tableta obsahuje monohydrát laktosy 50 mg. Úplný seznam pomocných látek viz bod 6.1.
 sp.zn. sukls257312/2018 a sukls249485/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RIVODARON 200 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amiodaroni hydrochloridum
sp.zn. sukls257312/2018 a sukls249485/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RIVODARON 200 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amiodaroni hydrochloridum
Příbalová informace: informace pro uživatele. Esmeron 10 mg/ml injekční/infuzní roztok rocuronii bromidum
 Příbalová informace: informace pro uživatele Esmeron 10 mg/ml injekční/infuzní roztok rocuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pro uživatele Esmeron 10 mg/ml injekční/infuzní roztok rocuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls90890/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls90890/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE DICLOREUM, injekční roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls90890/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE DICLOREUM, injekční roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Dorsiflex 200 mg tablety (Mephenoxalonum)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dorsiflex 200 mg tablety (Mephenoxalonum) Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dorsiflex 200 mg tablety (Mephenoxalonum) Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn. sukls4312/2006 a příloha ke sp. zn sukls22191/2008
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn. sukls4312/2006 a příloha ke sp. zn sukls22191/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SPIROPENT Tablety Clenbuteroli hydrochloridum Přečtěte
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn. sukls4312/2006 a příloha ke sp. zn sukls22191/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SPIROPENT Tablety Clenbuteroli hydrochloridum Přečtěte
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Poznámka: Tyto úpravy souhrnu údajů o přípravku a
 PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. DULCOLAX čípky (Bisacodylum)
 Příloha č. 2 ke sdělení sp.zn. sukls26205/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DULCOLAX čípky (Bisacodylum) Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité
Příloha č. 2 ke sdělení sp.zn. sukls26205/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DULCOLAX čípky (Bisacodylum) Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité
SOUHRN ÚDAJŮ O PŘÍPRAVKU. PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová
 sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bronchostop sirup. Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt
 Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn.sukls195792/2018 a sp.zn.sukls195821/2018 Příbalová informace: informace pro pacienta
 sp.zn.sukls195792/2018 a sp.zn.sukls195821/2018 Příbalová informace: informace pro pacienta NEUROMULTIVIT injekční roztok Léčivé látky: Thiamini hydrochloridum (vitamín B1), pyridoxini hydrochloridum (vitamín
sp.zn.sukls195792/2018 a sp.zn.sukls195821/2018 Příbalová informace: informace pro pacienta NEUROMULTIVIT injekční roztok Léčivé látky: Thiamini hydrochloridum (vitamín B1), pyridoxini hydrochloridum (vitamín
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. SPIROPENT Sirup Clenbuteroli hydrochloridum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SPIROPENT Sirup Clenbuteroli hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SPIROPENT Sirup Clenbuteroli hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
CONOXIA, stlačený medicinální plyn PŘÍBALOVÁ INFORMACE
 PŘÍBALOVÁ INFORMACE CONOXIA, stlačený medicinální plyn Oxygenium Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou informaci pro případ,
PŘÍBALOVÁ INFORMACE CONOXIA, stlačený medicinální plyn Oxygenium Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou informaci pro případ,
Kelapril 5mg 7x14tbl.
 Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
2. Čemu musíte věnovat pozornost, než začnete APO-DONEPEZIL užívat
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls122778/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-DONEPEZIL 5 mg potahované tablety APO-DONEPEZIL 10 mg potahované tablety Přečtěte si
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls122778/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-DONEPEZIL 5 mg potahované tablety APO-DONEPEZIL 10 mg potahované tablety Přečtěte si
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn. sukls222512/2009 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn. sukls222512/2009 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Dilceren pro infusione infuzní roztok (nimodipinum) Přečtěte si pozorně celou příbalovou
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn. sukls222512/2009 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Dilceren pro infusione infuzní roztok (nimodipinum) Přečtěte si pozorně celou příbalovou
sp.zn.: sukls70708/2013, sukls70714/2013
 sp.zn.: sukls70708/2013, sukls70714/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Roxithromycin-ratiopharm 150 mg Roxithromycin-ratiopharm 300 mg potahované tablety (roxithromycinum) Přečtěte si pozorně
sp.zn.: sukls70708/2013, sukls70714/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Roxithromycin-ratiopharm 150 mg Roxithromycin-ratiopharm 300 mg potahované tablety (roxithromycinum) Přečtěte si pozorně
Rytmonorm injekční roztok (Propafenoni hydrochloridum)
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Rytmonorm injekční roztok (Propafenoni hydrochloridum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Rytmonorm injekční roztok (Propafenoni hydrochloridum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
Příloha III. Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. PERFALGAN 10 mg/ml, infuzní roztok paracetamolum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PERFALGAN 10 mg/ml, infuzní roztok paracetamolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PERFALGAN 10 mg/ml, infuzní roztok paracetamolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CARVESAN 6,25 CARVESAN 25 tablety carvedilolum
 Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn. sukls249285/2011, sukls249280/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CARVESAN 6,25 CARVESAN 25 tablety carvedilolum Přečtěte si pozorně
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn. sukls249285/2011, sukls249280/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CARVESAN 6,25 CARVESAN 25 tablety carvedilolum Přečtěte si pozorně
IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná)
 Příloha č. 1 ke sdělení sp. zn. sukls205477/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná)
Příloha č. 1 ke sdělení sp. zn. sukls205477/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná)
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls173913/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls173913/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Transmetil 500 mg tablety Ademetioninum enterosolventní tablety Přečtěte si pozorně celou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls173913/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Transmetil 500 mg tablety Ademetioninum enterosolventní tablety Přečtěte si pozorně celou
Příbalová informace: informace pro uživatele. Neiraxin 100 mg/100 mg/1 mg/20 mg/2 ml injekční roztok
 Sp.zn.sukls177390/2017 Příbalová informace: informace pro uživatele Neiraxin 100 mg/100 mg/1 mg/20 mg/2 ml injekční roztok pyridoxini hydrochoridum, thiamini hydrochloridum, cyanocobalaminum, lidocaini
Sp.zn.sukls177390/2017 Příbalová informace: informace pro uživatele Neiraxin 100 mg/100 mg/1 mg/20 mg/2 ml injekční roztok pyridoxini hydrochoridum, thiamini hydrochloridum, cyanocobalaminum, lidocaini
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. TIAPRIDAL injekční roztok (tiapridi hydrochloridum)
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls88973/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE TIAPRIDAL injekční roztok (tiapridi hydrochloridum) Přečtěte si pozorně celou příbalovou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls88973/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE TIAPRIDAL injekční roztok (tiapridi hydrochloridum) Přečtěte si pozorně celou příbalovou
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
Torella 5 mg, tablety Torella 10 mg, tablety
 Příloha č. 2 ke sdělení sp.zn. sukls161411, sukls161423 PŘÍBALOVÁ INFORMACE Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci pro
Příloha č. 2 ke sdělení sp.zn. sukls161411, sukls161423 PŘÍBALOVÁ INFORMACE Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci pro
Srdeční zástava: Dospělí: 1 mg intravenózně nebo intraoseálně, event. 2-3 mg kanylou endotracheálně v 10 ml aq. pro inj každých 3 5 minut.
 sp.zn. sukls60536/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Adrenalin Léčiva injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Epinephrini hydrochloridum 1,2 mg (= Epinephrinum 1 mg) v 1 ml
sp.zn. sukls60536/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Adrenalin Léčiva injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Epinephrini hydrochloridum 1,2 mg (= Epinephrinum 1 mg) v 1 ml
Příbalová informace: informace pro uživatele Flexbumin 200 g/l infuzní roztok Albuminum humanum
 Příbalová informace: informace pro uživatele Flexbumin 200 g/l infuzní roztok Albuminum humanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Flexbumin 200 g/l infuzní roztok Albuminum humanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro pacienta. Maltofer 50 mg/ml perorální kapky, roztok
 sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Ataralgin tablety PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Paracetamolum, Guaifenesinum, Coffeinum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Ataralgin tablety Paracetamolum, Guaifenesinum, Coffeinum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Ataralgin tablety Paracetamolum, Guaifenesinum, Coffeinum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Cefotaxime Lek 1 g prášek pro injekční roztok cefotaximum
 sp.zn.sukls149832/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cefotaxime Lek 1 g prášek pro injekční roztok cefotaximum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek
sp.zn.sukls149832/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cefotaxime Lek 1 g prášek pro injekční roztok cefotaximum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek
Léčba arytmií v anestezii a intenzivní péči
 Léčba arytmií v anestezii a intenzivní péči Miroslav Solař I. interní kardioangiologická klinika Fakultní nemocnice Hradec Králové Lékařská fakulta UK v Hradci Králové Arytmie v anestezii Poruchy srdečního
Léčba arytmií v anestezii a intenzivní péči Miroslav Solař I. interní kardioangiologická klinika Fakultní nemocnice Hradec Králové Lékařská fakulta UK v Hradci Králové Arytmie v anestezii Poruchy srdečního
Příbalová informace: informace pro pacienta
 sp. zn. sukls56073/2015 Příbalová informace: informace pro pacienta LACTULOSA BIOMEDICA (lactulosi solutio) sirup Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat,
sp. zn. sukls56073/2015 Příbalová informace: informace pro pacienta LACTULOSA BIOMEDICA (lactulosi solutio) sirup Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat,
