LEMTRADA. Pokyny pro pacienty. Důležité informace pro pacienty začínající léčbu přípravkem LEMTRADA. alemtuzumab 12mg i.v.
|
|
|
- Alžběta Konečná
- před 10 lety
- Počet zobrazení:
Transkript
1 Pokyny pro pacienty Důležité informace pro pacienty začínající léčbu přípravkem Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí být hlášeny Státnímu ústavu pro kontrolu léčiv. Podrobnosti o hlášení najdete na: Adresa pro zasílání je Státní ústav pro kontrolu léčiv, oddělení farmakovigilance, Šrobárova 48, Praha 10, , farmakovigilance@sukl.cz. Je třeba doplnit i přesný obchodní název a číslo šarže. Tato informace může být také hlášena společnosti sanofi-aventis, s.r.o..
2 Obsah 1. Co je a jaký má mechanismus účinku? 3 2. Přehled informací o léčbě přípravkem 4 3. Nežádoucí účinky 6 4. Další užitečné informace Plánování časového harmonogramu pro monitorování Vašeho stavu Užitečné pojmy Jak kontaktovat lékaře 15 Vítáme Vás Váš lékař Vám předepsal lék na roztroušenou sklerózu (RS), který se nazývá (alemtuzumab). Tyto pokyny jsou určeny speciálně pro Vás a obsahují důležité informace o přípravku. V jedné z částí následujícího textu jsou objasněny lékařské pojmy uvedené v této brožuře. Další část obsahuje seznam všech lékařů, které můžete v případě potřeby navštívit. Včetně ošetřujícího lékaře, který vede vaši léčbu RS, a všech ostatních lékařů, které pravidelně navštěvujete. Pečlivým pročtením tohoto dokumentu získáte nové informace o přípravku a o jeho možných nežádoucích účincích. Tyto pokyny neslouží jako náhrada za diskusi s lékařem nebo s jinými zdravotnickými pracovníky, kteří léčí vaši roztroušenou sklerózu. Kromě tohoto textu si rovněž přečtěte příbalovou informaci k přípravku. Informujte svého lékaře nebo zdravotnického pracovníka, pokud se u Vás vyskytnou příznaky nebo projevy popsané v těchto pokynech. Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Kromě těchto pokynů pro pacienta naleznete další informace po přihlášení na: 1. Co je a jaký má mechanismus účinku? je lék na předpis, který se používá k léčbě relaps-remitentní roztroušené sklerózy (RS) u dospělých. Přípravek nedokáže roztroušenou sklerózu vyléčit, ale může snížit počet relapsů RS. Dále může zpomalit nebo zvrátit některé příznaky a projevy RS. Roztroušená skleróza (RS) je autoimunitní onemocnění, které postihuje centrální nervový systém (mozek a míchu). Látka označovaná jako myelin chrání nervová vlákna v centrálním nervovém systému a pomáhá tak rychlejšímu a hladšímu přenosu signálů mezi mozkem a ostatními částmi těla. Váš imunitní systém za normálních okolností chrání Vaše tělo před organismy, které způsobují různá onemocnění. U roztroušené sklerózy mohou buňky zodpovědné za boj s cizími organismy (tzv. lymfocyty, které jsou jedním z několika typů bílých krvinek) omylem napadat myelin, který tvoří ochrannou vrstvu kolem nervových vláken. Pokud lymfocyty napadnou nervový systém, vznikne zánět, který je často spojen s relapsem. Výskyt projevů nemoci je určován tím, která část centrálního nervového systému je postižena. Poškození vzniklé během zánětu může být vratné (reverzibilní), ale s progresí (vývojem) Vašeho onemocnění se mohou poškození hromadit a stávají se trvalými. Přípravek mění imunitní systém takovým způsobem, aby omezil jeho útoky na nervový systém. Po absolvování léčebného cyklu přípravkem se u Vás může zvýšit riziko vzniku jiných autoimunitních stavů nebo se u Vás mohou vyskytnout závažné infekce. Proto je důležité, abyste byl/a informován/a o těchto rizicích a o možnostech a způsobech jejich sledování. 2 Pokyny pro pacienty Pokyny pro pacienty 3
3 2. Přehled informací o léčbě přípravkem Jak se podává? se podává do žíly pomocí jehly (infuze). se podává ve dvou léčebných cyklech. První cyklus trvá 5 po sobě jdoucích dnů. O jeden rok později proběhne druhý cyklus léčby, který trvá 3 po sobě jdoucí dny. Přípravek se liší od ostatních léků, které účinkují pouze tehdy, pokud jsou užívány pravidelně (například 1x denně). V klinických hodnoceních bylo prokázáno, že uvedené 2 léčebné cykly u většiny pacientů účinkují po dobu 2 let, někdy i déle. Proto bude zapotřebí, abychom Vás monitorovali na výskyt nežádoucích účinků po dobu 4 let od poslední podané infuze přípravku. Další informace jsou uvedeny níže. Musím podstoupit nějaká vyšetření dříve, než u mě bude zahájena léčba přípravkem? Před zahájením léčby přípravkem Vám lékař provede krevní testy. Účelem těchto testů je stanovit, zda můžete užívat přípravek. Před zahájením léčby přípravkem lékař rovněž ověří, zda se u Vás nevyskytují určité zdravotní stavy nebo poruchy. Podrobnější informace o těchto stavech a poruchách naleznete v těchto pokynech. V případě jakýchkoli dotazů ohledně přípravku se zeptejte svého lékaře nebo příslušného zdravotnického pracovníka. Musím podstoupit nějaká vyšetření po léčbě přípravkem? V rámci kontroly a monitorování na případný vývoj autoimunitních stavů (které jsou popsány v části 4 těchto pokynů) Vás budeme sledovat 1x měsíčně prostřednictvím krevních testů a vyšetření moči. Váš lékař zkontroluje výsledky těchto testů a vyšetření a ověří, zda jsou u Vás přítomny nežádoucí účinky. Je velmi důležité, abyste docházel/a na tyto kontroly po dobu 4 let od ukončení posledního léčebného cyklu přípravkem, a to i tehdy, pokud se budete cítit dobře (tj. nebudete mít žádné příznaky nemoci nebo vedlejší účinky) a projevy vaší RS budou pod kontrolou. Vedlejší účinky se mohou objevit i mnoho let po posledním léčebném cyklu přípravkem, a (ve vzácných případech) mohou být život ohrožující, proto je velmi důležité, abyste pokračoval/a v kontrolách a sledoval/a případný výskyt symptomů. Tento postup umožní včasné odhalení a zahájení léčby případných problémů. To znamená, že budete jednou měsíčně docházet na laboratorní testy, a to po dobu 4 let od posledního léčebného cyklu přípravkem. Termíny jednotlivých testů si sjednáte a naplánujete ve spolupráci s lékařem s přihlédnutím k vašim normálním aktivitám. Pokud jste žena, nemělo by se vyšetření moči provádět během menstruace, protože by mohlo dojít ke zkreslení výsledků. Prohlédněte si níže uvedené schéma, ve kterém je pro lepší orientaci znázorněna doba trvání účinků léčby a potřebná délka následného sledování. Začátek monitorování vyšetření vzorků krve a moči před léčbou 1. cyklus léčby 5 dnů léčby Pokračujte v monitorování po dobu 4 let od poslední infuze 2. cyklus léčby 3 dny léčby Rok 1 Rok 2 Rok 3 Rok 4 Rok 5 Poznámka: 2 cykly léčby účinkují u většiny pacientů po dobu 2 let nebo i déle MONITOROVÁNÍ LÉČBY V následující tabulce je uvedeno, jaké testy, kdy a jak dlouho se budou provádět. Shrnutí doporučených postupů monitorování Test Kdy Jak dlouho? Krevní test Vyšetření moči U pacientek Lidský papilomavir (HPV) screeningové vyšetření HPV Před zahájením léčby a jednou měsíčně po léčbě Před zahájením léčby a jednou měsíčně po léčbě Před zahájením léčby 1x ročně Pro plánování vašich vyšetření jsou k dispozici různé nástroje, které Vás upozorní na blížící se termín. Další informace jsou uvedeny v části 5 této brožury. Jak se podává infuze? se podává do žíly pomocí jehly (infuze). Infuze se provádí v nemocnici a trvá přibližně 4 hodiny nebo i déle, pokud se u Vás vyskytnou nežádoucí účinky, vyžadující případně přerušení nebo zpomalení infuze. V průběhu infuze a po dobu 2 hodin po jejím dokončení budete pozorován/a lékařem nebo jeho personálem. V případě závažných reakcí může být infuze ukončena. Jak je popsáno výše, nejprve podstoupíte první cyklus léčby a poté si naplánujete s lékařem druhý cyklus, který proběhne o jeden rok později. Kromě těchto dvou léčebných cyklů s roční četností podání nesmíte zapomenout na každoměsíční laboratorní testy, které budou probíhat po dobu 4 let od vaší poslední léčby. Stejně jako u všech ostatních léků se mohou vyskytnout 4 Pokyny pro pacienty Pokyny pro pacienty 5
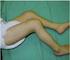
4 nežádoucí účinky. V těchto pokynech nejsou uvedeny všechny nežádoucí účinky, které se mohou u přípravku vyskytnout. Jejich úplný výčet je uveden v příbalové informaci. V následující části textu jsou uvedeny nežádoucí účinky, které se mohu vyskytnout po infuzi, včetně autoimunitních stavů a závažných infekcí (Část 3). 3. Nežádoucí účinky Pozdní nežádoucí účinky Jak je uvedeno výše, u pacientů užívajících přípravek je rovněž přítomno riziko určitých autoimunitních stavů. Mezi autoimunitní stavy patří: > stav označovaný jako Imunitní trombocytopenická purpura (ITP) popis je uveden v následující části, > určité typy onemocněn ledvin, > poruchy štítné žlázy. Příčina těchto vedlejších účinků není plně objasněna. Je však známo, že u pacientů užívajících přípravek je přítomno zvýšené riziko jejich vzniku. Všechny tyto stavy lze léčit, pokud jsou zjištěny včas, oddalování léčby však zvyšuje riziko komplikací. Proto je velmi důležité rozpoznat veškeré příznaky a projevy autoimunitních stavů a neprodleně o nich informovat lékaře. V následujících částech získáte podrobnější informace o jednotlivých nežádoucích účincích, včetně příznaků a projevů, které se u Vás mohou vyskytnout, a popisu jak postupovat v případě jejich výskytu. > Krvácení z řezných ran je obtížně zastavitelné > Silnější, delší nebo častější menstruační krvácení než obvykle. Krvácení mezi menstruací může být rovněž příznakem ITP > Krvácení z dásní nebo z nosu u osob, které na toto krvácení běžně netrpí, nebo delší než obvyklá doba k jeho zastavení > Vykašlávání krve Pokud se u Vás vyskytne některý z uvedených příznaků nebo projevů, ihned volejte svému lékaři. Pokud se svému lékaři nedovoláte, vyhledejte neprodleně lékařskou pomoc. Co mám dělat, pokud se u mě vyskytne ITP? Optimální je identifikovat a léčit ITP co nejdříve. Proto je důležité, abyste docházel/a na každoměsíční krevní testy (které mohou odhalit problém dříve, než se vyskytnout jeho projevy). Dále je důležité, abyste vy sám/a, členové vaší rodiny a/nebo pečovatelé pečlivě sledovali každý z projevů a příznaků popsaných v tomto textu. Oddalování léčby ITP zvyšuje pravděpodobnost vzniku závažných problémů. Na následujících obrázcích jsou uvedeny příklady krevních výronů (modřin) a kožních projevů způsobených ITP Poznámka: Následující snímky mají pouze informační charakter a slouží jako příklad krevních výronů a kožních projevů při ITP. Imunitní trombocytopenická purpura (ITP) (krvácivá porucha) ITP je stav, který vede ke snížení počtu krevních destiček v krvi. Krevní destičky jsou nezbytné pro normální srážení krve. ITP může vyvolat závažné krvácení. Je-li ITP včas detekována, je léčitelná. Pokud však není léčena, může vést k závažným zdravotním problémům až případně k úmrtí pacienta. Váš lékař Vám bude provádět krevní testy, které odhalí případné změny v počtu krevních destiček a umožní včasné rozpoznání tohoto vedlejšího účinku. Vyšetření vzorku vaší krve bude provedeno před zahájením léčby přípravkem, a dále po úvodním léčebném cyklu v pravidelných měsíčních intervalech. Každoměsíční testy musí pokračovat po dobu 4 let od Vašeho posledního léčebného cyklu. ITP lze rovněž zjistit podle určitých příznaků a projevů, s nimiž se musíte důkladně obeznámit. Jaké jsou příznaky a projevy ITP? > Drobné roztroušené skvrnky na kůži, červené, růžové nebo purpurové barvy > Snadná tvorba modřin Na tomto příkladu jsou patrné tzv. petechie drobné, roztroušené skvrnky pod kůží, které nabývají červené, fialové nebo purpurové barvy. Svým vzhledem připomínají ranku vzniklou po píchnutí špendlíkem. Zde je důležité poznamenat, že petechie se mohou vyskytnout kdekoli na těle, nikoli jen na nohou. Na tomto příkladu jsou patrné rozsáhlé modřiny na rukou. Zde je důležité poznamenat, že modřiny se mohou vyskytnout kdekoli na těle, nikoli jen na rukou. Na tomto příkladu jsou patrné skvrnky v důsledku krvácení pod jazykem. Tyto skvrnky se mohou objevit na kterémkoli místě v ústech: pod jazykem, na patře, na vnitřní části tváří, na jazyku nebo dásních. 6 Pokyny pro pacienty Pokyny pro pacienty 7
5 Pokud je ITP zjištěna včas, je zpravidla léčitelná. Pokud se u Vás vyvine ITP, Váš lékař s vaší pomocí stanoví, jaká léčba je pro Vás nejlepší. Pokud si všimnete, že se u Vás vyvinul jakýkoli z výše uvedených příznaků nebo projevů, zavolejte neprodleně svému lékaři a informujte ho o svých problémech. Pokud se svému lékaři nedovoláte, vyhledejte neprodleně lékařskou pomoc. Postižení ledvin (např. onemocnění s tvorbou protilátek proti glomerulární bazální membráně neboli anti-gbm) může způsobit stav označovaný jako onemocnění s tvorbou protilátek proti glomerulární bazální membráně neboli onemocnění anti-gbm. Anti-GBM onemocnění je autoimunitní stav, který může vést k závažnému poškození ledvin. Anti-GBM onemocnění může dále poškodit plíce, ačkoli toto postižení nebylo zaznamenáno v klinických hodnoceních přípravku. Není-li onemocnění anti-gbm léčeno, může způsobit selhání ledvin vyžadující chronickou dialýzu nebo transplantaci nebo může vést k úmrtí pacienta. Lékař bude sledovat příznaky onemocnění ledvin pomocí krevních testů a vyšetření moči, aby mohl včas odhalit případný výskyt tohoto vedlejšího účinku. Pro tento účel bude lékař provádět vyšetření krve a moči před zahájením léčby přípravkem a dále v pravidelných měsíčních intervalech po úvodním léčebném cyklu. Vyšetření moči bude rovněž prováděno jednou měsíčně. Pokud jste žena, nemělo by se vyšetření moči provádět během menstruace, protože by mohlo dojít ke zkreslení výsledků. Tato vyšetření budou pokračovat po dobu 4 let od podání poslední infuze. Onemocnění anti-gbm lze rovněž zjistit podle určitých příznaků a projevů, s nimiž se musíte důkladně obeznámit. Jaké jsou příznaky a projevy ledvinových problémů nebo onemocnění anti-gbm? > Krev v moči: Moč může mít červenou barvu nebo barvu černého čaje. > Otoky: Otoky nohou nebo chodidel. > Vykašlávání krve: Můžete odkašlávat krev. Co mám dělat, pokud se u mě objeví ledvinové problémy? Lékaři většinou dokáží onemocnění ledvin vyléčit. Léčbu je třeba zahájit co nejdříve. V tomto ohledu je důležité, abyste byl/a dobře obeznámen/a s příznaky a projevy ledvinového postižení a onemocnění anti-gbm a abyste docházel/a na pravidelné laboratorní testy (krevní testy a vyšetření moči). Ledvinové problémy vyžadují téměř vždy lékařskou péči. V případě potřeby je nezbytné zahájit léčbu neodkladně. Pokud si všimnete, že se u Vás vyvinul jakýkoli z výše uvedených příznaků nebo projevů, zavolejte neprodleně svému lékaři a informujte ho o svých problémech. Pokud se svému lékaři nedovoláte, vyhledejte neprodleně lékařskou pomoc. Poruchy štítné žlázy Štítná žláza je žláza, která se nachází ve spodní polovině krku. Štítná žláza produkuje hormony, které jsou důležité pro celý organismus. U některých jedinců může imunitní systém omylem napadat vlastní buňky štítné žlázy (autoimunitní postižení štítné žlázy), což má dopad na schopnost tvořit hormony a kontrolovat jejich hladinu v těle. Přípravek může vyvolat poruchy štítné žlázy, jakou jsou například: > Nadměrně aktivní štítná žláza neboli hypertyreóza: Tento stav vzniká, pokud štítná žláza vytváří příliš mnoho hormonu. > Nedostatečně aktivní štítná žláza neboli hypotyreóza: Tento stav vzniká, pokud štítná žláza nevytváří dostatečné množství hormonu. Vyšetření krve podstoupíte před zahájením léčby přípravkem, a dále po úvodním léčebném cyklu v intervalu jednou za 3 měsíce, celkem po dobu 4 let od podání poslední infuze. Tyto krevní testy umožní lékaři včas odhalit případné poruchy štítné žlázy. Jaké jsou příznaky a projevy nadměrně aktivní štítné žlázy? Mezi hlavní projevy patří: > nadměrné pocení, > nevysvětlitelný úbytek tělesné hmotnosti, > otoky očí, > nervozita, > zrychlený srdeční tep. Jaké jsou příznaky a projevy nedostatečné aktivity štítné žlázy? Mezi hlavní projevy patří: > nevysvětlitelný přírůstek tělesné hmotnosti, > zimomřivost, > zhoršení únavy, > nově vzniklá zácpa. Co mám dělat, pokud se u mě vyvine porucha štítné žlázy? Informujte lékaře, pokud se u Vás vyskytnou uvedené projevy. Váš lékař rozhodne, jaká léčba je pro Vás nejlepší, v závislosti na typu poruchy štítné žlázy. Je důležité, abyste dodržoval/a doporučení svého lékaře a mohl/a tak získat z léčby maximální užitek. V některých případech je nezbytné užívat léky na poruchy štítné žlázy po celý život. Za určitých okolností je nezbytné štítnou žlázu odstranit. 8 Pokyny pro pacienty Pokyny pro pacienty 9
6 Dojde-li u Vás ke vzniku onemocnění štítné žlázy, je velmi důležité, aby Vám byla tato porucha náležitě léčena. To platí zejména u pacientek, které otěhotnění po předchozím užívání přípravku. Neléčená porucha štítné žlázy může vést k poškození nenarozeného plodu nebo dítěte po jeho narození. DŮLEŽITÉ upozornění Vzhledem k tomu, že se všechny autoimunitní stavy mohou objevit až dlouhou dobu po léčbě přípravkem, je velmi důležité, abyste pokračoval/a v každoměsíčních testech (a to i tehdy, pokud se cítíte dobře). Musíte i nadále pečlivě sledovat příznaky a projevy, které se u Vás případně vyskytnou. V tomto sledování pokračujte po dobu 4 let od vaší poslední léčby přípravkem. Časná detekce a diagnóza Vám může poskytnout nejlepší příležitost ke zlepšení stavu. Noste u sebe neustále Kartu pacienta a ukažte ji každému zdravotnickému pracovníkovi, který Vám bude poskytovat léčbu nebo péči (včetně jiných stavů než RS) nebo v případě léčby na pohotovostním oddělení. Závažné infekce U pacientů léčených přípravkem existuje zvýšené riziko vzniku závažných infekcí. Dojde-li u Vás ke vzniku závažné infekce, je možné, že budete potřebovat léčbu v nemocnici. V takovém případě je důležité, abyste lékaře v nemocnici informoval/a, že užíváte přípravek. Pokud se u Vás vyskytne infekce před zahájením léčby přípravkem, Váš lékař zváží odložení léčby na dobu, až infekce odezní nebo se dostane pod kontrolu. 4. Další užitečné informace Co potřebuji vědět o vakcinaci? Před podáním každého cyklu léčby přípravkem Váš lékař zkontroluje, zda jste řádně očkován/a. Pokud potřebujete vakcínu, musíte po vakcinaci vyčkat 6 týdnů, než Vám bude přípravek podán. Informujte lékaře, pokud Vám byla během posledních 6 týdnů podána jakákoli vakcína. Plodnost/Těhotenství/Antikoncepce Není známo, zda přípravek bude mít vliv na plodnost během doby, kdy bude ve Vašem organismu. Informujte lékaře, pokud zvažujete otěhotnění. Není známo, zda může přípravek poškodit nenarozený plod. V průběhu léčebného cyklu přípravkem a po dobu minimálně 4 měsíců po každém cyklu léčby přípravkem proto musíte používat účinnou antikoncepci (pokud Vám lékař neoznámí, že antikoncepci nepotřebujete, protože nemůžete mít děti z důvodu, že jste podstoupila hysterektomii). Tímto opatřením se zajistí, že před početím dítěte nebudete mít v těle přípravek. Pokud plánujete otěhotnění, nezapomeňte vše prodiskutovat se svým lékařem. Jste-li již těhotná, musíte se společně s lékařem rozhodnout, zda přínos z léčby převýší potenciální riziko pro Vaše nenarozené dítě. Není známo, zda se vylučuje u lidí do mateřského mléka, existuje však možnost, že ano. Proto se doporučuje, abyste nekojila v průběhu každého léčebného cyklu přípravkem a po dobu 4 měsíců po každém léčebném cyklu. Kojení je však spojeno s mnoha přínosy (např. může chránit dítě před infekcí), a pokud tedy plánujete kojení, poraďte se s lékařem. Lékař Vám vysvětlí, co je vhodné pro Vás a pro Vaše dítě. Jaké další informace bych měl/a sdělit svému lékaři? Nezapomeňte informovat lékaře a členy kolektivu zdravotnických pracovníků o všech nových zdravotních problémech, které se u Vás případně vyvinou, a o všech nových lécích, které jste případně užíval/a od vaší poslední návštěvy. To platí pro všechny léky na předpis i volně prodejné léky, včetně vitaminů a rostlinných doplňků. Pro lékaře je důležité, aby byl o lécích informován a mohl tak lépe vést vaší léčbu. 10 Pokyny pro pacienty Pokyny pro pacienty 11
7 5. Plánování časového harmonogramu pro monitorování Vašeho stavu Autoimunitní stavy popsané v těchto pokynech se mohou objevit i dlouhou dobu po léčbě přípravkem. Je velmi důležité, abyste pokračoval/a v každoměsíčních testech (a to i tehdy, pokud se cítíte dobře) po dobu 4 let od Vašeho posledního léčebného cyklu. Protože je Vám přípravek podáván pouze ve dvou ročních cyklech, je třeba Vaše testování plánovat samostatně. Přihlaste se na a pomocí přístupového hesla, které je uvedeno ve vaší příručce k přípravku Lemtrada, získejte elektronický přístup ke vzdělávacím materiálům (včetně těchto pokynů). Webové stránky obsahují užitečné informace týkající se Vašeho užívání přípravku a nástroje, které Vás upozorní na blížící se termín vyšetření nebo testů. Následující nástroj Vám může být užitečný, protože Vám připomene termíny testů a vyšetření v rámci monitorování. > Výzva přes internet: Z adresy se můžete registrovat k elektronickému zasílání měsíčních výzev a pozvánek na sjednané vyšetření. Vyplňte svou ovou adresu a prostřednictvím u budete dostávat automatické měsíční výzvy a pozvánky na každoměsíční laboratorní testy. Uvedená služba je nabízena prostřednictvím třetí strany, která bude shromažďovat a zpracovávat Vaše osobní údaje v souladu s platnými předpisy pro ochranu údajů. Vaše osobní údaje budou uchovávány na zabezpečeném místě a nebudou předány jiným osobám, včetně výrobce přípravku. Zde je vhodné připomenout, že tato služba je volitelná a můžete se k ní kdykoli přihlásit a odhlásit se. Nezapomeňte, pokud se u Vás vyskytnou jakékoli příznaky a projevy popsané v těchto pokynech, pak je vždy nejlepším předpokladem pro jejich případné zmírnění časné odhalení a diagnóza. Docházejte pečlivě na vyšetření a testy a pokračujte ve sledování příznaků a projevů, které jsou popsány v těchto pokynech, po dobu 4 let od poslední infuze. Shrnutí doporučených postupů monitorování Test Kdy Jak dlouho? Krevní test Vyšetření moči U pacientek Lidský papilomavir (HPV) screeningové vyšetření HPV Před zahájením léčby a jednou měsíčně po léčbě Před zahájením léčby a jednou měsíčně po léčbě Před zahájením léčby 1 x ročně 12 Pokyny pro pacienty Pokyny pro pacienty 13
8 6. Užitečné pojmy Onemocnění s tvorbou protilátek proti glomerulární bazální membráně (anti-gbm): onemocnění způsobené imunitním systémem, který napadá vlastní ledviny (nebo někdy plíce). Dochází k poškození ledvin, ledviny nepracují správně nebo dochází k jejich úplnému selhání. V důsledku postižení mohu být pacienti odkázáni na dialýzu a/nebo potřebují transplantací ledviny. Při včasné detekci je onemocnění léčitelné. Není-li však léčeno, může vést k úmrtí pacienta. Autoimunitní nemoci/poruchy: Imunitní systém zpravidla chrání organismus před bakteriemi, viry a dalšími škodlivými organismy. Pokud se imunitní systém obrátí proto vlastním buňkám a orgánům, hovoříme o autoimunitní poruše nebo autoimunitním stavu. U RS imunitní systém napadá mylně mozek nebo míchu jako cizí struktury a způsobuje jejich poškození. Jiná autoimunitní onemocnění mohou vést k poškození jiných orgánů nebo krevních buněk. Autoimunitní onemocnění štítné žlázy: Imunitní systém mylně napadá buňky štítné žlázy. Autoimunitní onemocnění štítné žlázy je léčitelné. Níže jsou uvedeny dva příklady: > Hypertyreóza: Štítná žláza produkuje příliš mnoho hormonů. > Hypotyreóza: Štítná žláza produkuje nedostatečné množství hormonů. Dialýza: Proces k odstranění odpadních látek a nadbytečné vody z krve u pacientů, kteří mají funkční postižení ledvin. Imunitní systém: Obranný systém organismu proti původcům infekcí, cizím tělesům a abnormálním buňkám. Infuze: Pomalé podání roztoku (tekutiny obsahující lék) do žíly prostřednictvím infuzní jehly. ITP (Imunitní trombocytopenická purpura): ITP je stav, který vede ke snížení počtu krevních destiček v krvi. Krevní destičky jsou nezbytné pro normální srážení krve. ITP může vyvolat závažné krvácení. Je-li ITP včas detekována, je léčitelná. Pokud však není léčena, může vést k závažným zdravotním problémům až případně k úmrtí pacienta. Lymfocyty (typ bílých krvinek): buňky v krvi (krvinky), které pomáhají v boji proti infekcím. Lymfocyty tvoří součást imunitního systému. Krevní destičky: Krevní destičky jsou nezbytné pro normální srážení krve. Krevní destičky cestují krevním řečištěm. Pomáhají při zástavě krvácení tak, že se shlukují a tvoří sraženinu. Sraženina pomáhá uzavřít drobné ranky nebo poruchy kůže. Štítná žláza: Žláza nacházející se v dolní polovině krku. Produkuje hormony, které jsou důležité pro regulaci metabolismu. 7. Jak kontaktovat lékaře Pro snazší kontaktování lékařů nebo zdravotnických pracovníků prosím vyplňte do následující tabulky příslušná telefonní čísla a adresy. Lékař (zdravotní tým) Telefon Adresa 14 Pokyny pro pacienty Pokyny pro pacienty 15
9 Určeno výhradně jako edukační materiál pro pacienty, kterým byl předepsán přípravek Lemtrada. Tento edukační materiál obsahuje pouze vybrané informace a není náhradou příbalové informace. Než začnete užívat přípravek Lemtrada, přečtěte si pozorně příbalovou informaci. Není určeno pro distribuci v čekárnách. sanofi-aventis, s.r.o. Evropská 846/ Praha 6 Tel.: Fax: officecz@genzyme.com
Informovaný souhlas pacienta(tky) s výkonem. Nitrožilní aplikace monoklonální protilátky alemtuzumab (LEMTRADA)
 Informovaný souhlas pacienta(tky) s výkonem Nitrožilní aplikace monoklonální protilátky alemtuzumab (LEMTRADA) Vážená paní, Vážený pane, vzhledem k tomu, že jako svéprávný jedinec se podílíte významným
Informovaný souhlas pacienta(tky) s výkonem Nitrožilní aplikace monoklonální protilátky alemtuzumab (LEMTRADA) Vážená paní, Vážený pane, vzhledem k tomu, že jako svéprávný jedinec se podílíte významným
LEMTRADA alemtuzumab 12 mg i.v.
 POKYNY PRO PACIENTY Důležité informace pro pacienty začínající léčbu přípravkem LEMTRADA Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte
POKYNY PRO PACIENTY Důležité informace pro pacienty začínající léčbu přípravkem LEMTRADA Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte
PRŮKAZ PACIENTA. užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1
 PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
BAVENCIO (avelumab) Váš průvodce informacemi pro pacienta
 Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
PRŮKAZ PACIENTA. užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019
 PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
Rozměr zavřeného průkazu mm
 Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Co byste měl(a) vědět o léčivém přípravku
 Co byste měl(a) vědět o léčivém přípravku Důležité bezpečnostní informace pro pacienty léčené přípravkem MabThera 1 Co byste měl(a) vědět o přípravku MabThera Pokud máte revmatoidní artritidu (RA), granulomatózu
Co byste měl(a) vědět o léčivém přípravku Důležité bezpečnostní informace pro pacienty léčené přípravkem MabThera 1 Co byste měl(a) vědět o přípravku MabThera Pokud máte revmatoidní artritidu (RA), granulomatózu
Pokyny pro zdravotnické pracovníky
 Edukační materiál Pokyny pro zdravotnické pracovníky Použití přípravku (alemtuzumab) u pacientů s relabující-remitující roztroušenou sklerózou (RRRS) Tento léčivý přípravek podléhá dalšímu sledování. To
Edukační materiál Pokyny pro zdravotnické pracovníky Použití přípravku (alemtuzumab) u pacientů s relabující-remitující roztroušenou sklerózou (RRRS) Tento léčivý přípravek podléhá dalšímu sledování. To
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
Důležité informace pro pacienty
 MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Návod pro pacienta / pečovatele
 Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge
 Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge Erivedge může způsobit závažné vrozené vady Může vést
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge Erivedge může způsobit závažné vrozené vady Může vést
Příručka k přípravku KEYTRUDA. (pembrolizumab) Informace pro pacienty. Informace pro pacienty
 Příručka k přípravku KEYTRUDA (pembrolizumab) Informace pro pacienty Informace pro pacienty Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příručka k přípravku KEYTRUDA (pembrolizumab) Informace pro pacienty Informace pro pacienty Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Klinické hodnocení ARAMIS pro muže s rakovinou prostaty
 Klinické hodnocení ARAMIS pro muže s rakovinou prostaty Brožura pro účastníky DĚKUJEME VÁM, že jste se rozhodl zúčastnit klinického hodnocení ARAMIS pro muže s rakovinou prostaty. V této brožuře najdete
Klinické hodnocení ARAMIS pro muže s rakovinou prostaty Brožura pro účastníky DĚKUJEME VÁM, že jste se rozhodl zúčastnit klinického hodnocení ARAMIS pro muže s rakovinou prostaty. V této brožuře najdete
PNEUMOKOKOVÉ INFEKCE A MOŽNOSTI PREVENCE aneb CO MŮŽE ZPŮSOBIT PNEUMOKOK
 PNEUMOKOKOVÉ INFEKCE A MOŽNOSTI PREVENCE aneb CO MŮŽE ZPŮSOBIT PNEUMOKOK Očkování! Nejvýznamnější možnost prevence infekčních chorob! Lepší infekční chorobě předcházet než ji léčit! Významný objev v medicíně,
PNEUMOKOKOVÉ INFEKCE A MOŽNOSTI PREVENCE aneb CO MŮŽE ZPŮSOBIT PNEUMOKOK Očkování! Nejvýznamnější možnost prevence infekčních chorob! Lepší infekční chorobě předcházet než ji léčit! Významný objev v medicíně,
EDUKAČNÍ MATERIÁL - Pioglitazone Accord
 Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití)
 CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Průvodce použitím přípravku YERVOY (ipilimumab)
 Průvodce použitím přípravku YERVOY (ipilimumab) Informační brožura pro pacienty Yervoy podléhá dalšímu sledování, které umožní rychlé získávání nových informací o bezpečnosti. Pokud se u Vás vyskytne jakýkoli
Průvodce použitím přípravku YERVOY (ipilimumab) Informační brožura pro pacienty Yervoy podléhá dalšímu sledování, které umožní rychlé získávání nových informací o bezpečnosti. Pokud se u Vás vyskytne jakýkoli
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
POKYNY PRO ZDRAVOTNICKÉ PRACOVNÍKY, JAK OMEZIT ZÁVAŽNÁ RIZIKA PŘÍPRAVKU LEMTRADA
 EDUKAČNÍ MATERIÁL LEMTRADA POKYNY PRO ZDRAVOTNICKÉ PRACOVNÍKY, JAK OMEZIT ZÁVAŽNÁ RIZIKA PŘÍPRAVKU LEMTRADA Použití přípravku LEMTRADA (alemtuzumab) u pacientů s relabující-remitující roztroušenou sklerózou
EDUKAČNÍ MATERIÁL LEMTRADA POKYNY PRO ZDRAVOTNICKÉ PRACOVNÍKY, JAK OMEZIT ZÁVAŽNÁ RIZIKA PŘÍPRAVKU LEMTRADA Použití přípravku LEMTRADA (alemtuzumab) u pacientů s relabující-remitující roztroušenou sklerózou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Brožura s informacemi pro pacienta a rodiče pacienta s ahus
 Brožura s informacemi pro pacienta a rodiče pacienta s ahus Schválena SÚKL dne 18. března 2019 SLOVNÍK POJMŮ Atypický hemolytickouremický syndrom (ahus) Vzácná porucha způsobená chronickou a nadměrnou
Brožura s informacemi pro pacienta a rodiče pacienta s ahus Schválena SÚKL dne 18. března 2019 SLOVNÍK POJMŮ Atypický hemolytickouremický syndrom (ahus) Vzácná porucha způsobená chronickou a nadměrnou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE
 EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
Důležité informace k užívání přípravku Tasigna
 Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
Příbalová informace: informace pro uživatele. Adriblastina CS injekční roztok 2 mg/ml doxorubicini hydrochloridum
 Příbalová informace: informace pro uživatele Adriblastina CS injekční roztok 2 mg/ml doxorubicini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro uživatele Adriblastina CS injekční roztok 2 mg/ml doxorubicini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Důležité informace o užívání přípravku TASIGNA
 Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Klinické hodnocení u bolestí spojených s endometriózou. Bolest, kterou cítíte, je skutečná... i když to ostatní nevidí. A822523
 Klinické hodnocení u bolestí spojených s endometriózou Bolest, kterou cítíte, je skutečná... i když to ostatní nevidí. A822523 Studie SOLSTICE se provádí v přibližně 200 výzkumných centrech na celém světě.
Klinické hodnocení u bolestí spojených s endometriózou Bolest, kterou cítíte, je skutečná... i když to ostatní nevidí. A822523 Studie SOLSTICE se provádí v přibližně 200 výzkumných centrech na celém světě.
OCHRÁNIT. VAKCÍNU, VAŠE BUDOUCNOST JE JEN JEDNA. ZEPTEJTE SE NA KTERÁ VÁS MÙ E POMOCI
 VAŠE BUDOUCNOST JE JEN JEDNA. ZEPTEJTE SE NA VAKCÍNU, KTERÁ VÁS MÙ E POMOCI OCHRÁNIT. Registrovaná ochranná známka MERCK & CO., INC., Whitehouse Station, N.J., U.S.A. Copyright MERCK & CO., INC., Whitehouse
VAŠE BUDOUCNOST JE JEN JEDNA. ZEPTEJTE SE NA VAKCÍNU, KTERÁ VÁS MÙ E POMOCI OCHRÁNIT. Registrovaná ochranná známka MERCK & CO., INC., Whitehouse Station, N.J., U.S.A. Copyright MERCK & CO., INC., Whitehouse
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Fludeoxyglucose (18F) Biont 200 1300 MBq/ml injekční roztok FLUDEOXYGLUCOSUM ( 18 F)
 Sp.zn. sukls117503/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Fludeoxyglucose (18F) Biont 200 1300 MBq/ml injekční roztok FLUDEOXYGLUCOSUM ( 18 F) Přečtěte si pozorně celou příbalovou informaci
Sp.zn. sukls117503/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Fludeoxyglucose (18F) Biont 200 1300 MBq/ml injekční roztok FLUDEOXYGLUCOSUM ( 18 F) Přečtěte si pozorně celou příbalovou informaci
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Léky užívané při dialýze. Vítejte na našem dialyzačním středisku
 Léky užívané při dialýze Vítejte na našem dialyzačním středisku Budu při dialýze užívat nějaké léky? Dialýza sice nahradí některé funkce, které vykonávaly Vaše ledviny, zároveň je ale nutné užívat jako
Léky užívané při dialýze Vítejte na našem dialyzačním středisku Budu při dialýze užívat nějaké léky? Dialýza sice nahradí některé funkce, které vykonávaly Vaše ledviny, zároveň je ale nutné užívat jako
Edukační materiál. Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera
 Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Příbalová informace: informace pro pacienta. Maltofer, 10 mg/ml sirup. polymaltosum ferricum
 sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Léčba přípravkem. co byste měli vědět
 Informace pro pacienty, kterým byl předepsán přípravek Volibris. Léčba přípravkem co byste měli vědět Tato brožurka přináší informace a doporučení týkající se léčby přípravkem Volibris. Pečlivě si ji pročtěte
Informace pro pacienty, kterým byl předepsán přípravek Volibris. Léčba přípravkem co byste měli vědět Tato brožurka přináší informace a doporučení týkající se léčby přípravkem Volibris. Pečlivě si ji pročtěte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90
 Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Simdax Příbalová informace
 Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
EXELON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY
 XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
ANAMNÉZA DÁRKYNĚ PUPEČNÍKOVÉ KRVE
 ANAMNÉZA DÁRKYNĚ PUPEČNÍKOVÉ KRVE JMÉNO A PŘÍJMENÍ DÁRKYNÉ DATUM NAROZENÍ RODNÉ ČÍSLO ZAMĚSTNÁNÍ TELEFON ULICE A ČÍSLO POPISNÉ MĚSTO PSČ PORODNÍK MINULÉ TĚHOTENSTVÍ počet předchozích porodů počet spontánních
ANAMNÉZA DÁRKYNĚ PUPEČNÍKOVÉ KRVE JMÉNO A PŘÍJMENÍ DÁRKYNÉ DATUM NAROZENÍ RODNÉ ČÍSLO ZAMĚSTNÁNÍ TELEFON ULICE A ČÍSLO POPISNÉ MĚSTO PSČ PORODNÍK MINULÉ TĚHOTENSTVÍ počet předchozích porodů počet spontánních
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
ZÁZNAM POHOVORU S LÉKAŘEM
 Strana 1 / 5 Vážená pacientko, vážený paciente, vážení rodiče, vzhledem k Vašemu zdravotnímu stavu (zdravotnímu stavu Vašeho dítěte) je Vám doporučeno provedení výše uvedeného zákroku (výkonu). Před vlastním
Strana 1 / 5 Vážená pacientko, vážený paciente, vážení rodiče, vzhledem k Vašemu zdravotnímu stavu (zdravotnímu stavu Vašeho dítěte) je Vám doporučeno provedení výše uvedeného zákroku (výkonu). Před vlastním
léky užívané při dialýze Vítejte na našem dialyzačním středisku
 léky užívané při dialýze Vítejte na našem dialyzačním středisku Budu při dialýze užívat nějaké léky? Dialýza sice nahradí některé funkce, které vykonávaly Vaše ledviny, zároveň je ale nutné užívat jako
léky užívané při dialýze Vítejte na našem dialyzačním středisku Budu při dialýze užívat nějaké léky? Dialýza sice nahradí některé funkce, které vykonávaly Vaše ledviny, zároveň je ale nutné užívat jako
Příbalová informace: informace pro uživatele AESCIN-TEVA. 20 mg, enterosolventní tablety. escinum alfa
 sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH)
 Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Příbalová informace: informace pro uživatele. Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F)
 sp.zn. sukls298615/2018 Příbalová informace: informace pro uživatele Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F) Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls298615/2018 Příbalová informace: informace pro uživatele Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F) Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Volibris co byste měli vědět
 EDUKAČNÍ MATERIÁL Informace pro pacienty, kterým byl předepsán přípravek Volibris. Léčba přípravkem Volibris co byste měli vědět Tato brožurka přináší informace a doporučení týkající se léčby přípravkem
EDUKAČNÍ MATERIÁL Informace pro pacienty, kterým byl předepsán přípravek Volibris. Léčba přípravkem Volibris co byste měli vědět Tato brožurka přináší informace a doporučení týkající se léčby přípravkem
Příbalová informace: informace pro uživatele. IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara)
 Příbalová informace: informace pro uživatele IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara) Tento přípravek podléhá dalšímu sledování. To umožní rychlé
Příbalová informace: informace pro uživatele IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara) Tento přípravek podléhá dalšímu sledování. To umožní rychlé
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SUSTANON 250 250 mg/ml, injekční roztok Testosteroni
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls79892/2011 a příloha ke sp. zn. sukls136154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SUSTANON 250 250 mg/ml, injekční roztok Testosteroni
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bronchostop sirup. Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt
 Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
INFLECTRA SCREENINGOVÝ LIST. a výběru pacientů pro všechny schválené indikace. Obsahuje pokyny ke správnému screeningu
 Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Vše co potřebujete vědět o hemoroidech. Rady pro pacienty
 Vše co potřebujete vědět o hemoroidech Rady pro pacienty CO? CO? JAK? JAK? KDY? KDY? PROČ? PROČ? CO CO jsou hemoroidy? je hemoroidální onemocnění? Anatomie řitního kanálu a konečníku Hemoroidy jsou přirozenou
Vše co potřebujete vědět o hemoroidech Rady pro pacienty CO? CO? JAK? JAK? KDY? KDY? PROČ? PROČ? CO CO jsou hemoroidy? je hemoroidální onemocnění? Anatomie řitního kanálu a konečníku Hemoroidy jsou přirozenou
Příbalová informace: informace pro uživatele. Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok
 sp.zn. sukls301709/2016 Příbalová informace: informace pro uživatele Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok Natrii chromas ( 51 Cr) Přečtěte si pozorně celou příbalovou
sp.zn. sukls301709/2016 Příbalová informace: informace pro uživatele Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok Natrii chromas ( 51 Cr) Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
Příloha IV. Vědecké závěry
 Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
1. CO JE PŘÍPRAVEK VIDAZA A K ČEMU SE POUŽÍVÁ
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Vidaza 25 mg/ml prášek pro přípravu injekční suspenze Azacitidinum Přečtěte si pozorně celou příbalovou informaci dříve, než vám začne být tento přípravek podáván.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Vidaza 25 mg/ml prášek pro přípravu injekční suspenze Azacitidinum Přečtěte si pozorně celou příbalovou informaci dříve, než vám začne být tento přípravek podáván.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum)
 sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
ZOVIRAX DUO KRÉM 1X2GM Krém
 ZOVIRAX DUO KRÉM 1X2GM Krém Výrobce: GLAXOSMITHKLINE BIOLOGICALS S.A., RIXENSART Značka: ZOVIRAX Charakteristika: Léčivý přípravek Kód výrobku: 229859 Kód EAN:8590335009103 Kód SUKL:0180938 Farmakoterapeutická
ZOVIRAX DUO KRÉM 1X2GM Krém Výrobce: GLAXOSMITHKLINE BIOLOGICALS S.A., RIXENSART Značka: ZOVIRAX Charakteristika: Léčivý přípravek Kód výrobku: 229859 Kód EAN:8590335009103 Kód SUKL:0180938 Farmakoterapeutická
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
Vysoký krevní tlak High Blood Pressure. Chronic kidney disease chapter 2. Chronické onemocnění ledvin
 High Blood Pressure Chronic kidney disease chapter 2 Chronické onemocnění ledvin je jednou z hlavních příčin chronického onemocnění ledvin. Kromě toho může nedostatečně léčený vysoký krevní tlak vést k
High Blood Pressure Chronic kidney disease chapter 2 Chronické onemocnění ledvin je jednou z hlavních příčin chronického onemocnění ledvin. Kromě toho může nedostatečně léčený vysoký krevní tlak vést k
Možná Vás bude zajímat klinické hodnocení (studie) AZURE.
 Příručka pacienta Bylo Vám diagnostikováno onemocnění se syndromem chronické pánevní bolesti? Zažili jste pánevní bolest nebo nepříjemné pocity po dobu nejméně 3 z posledních 6 měsíců? Jste starší 18 let?
Příručka pacienta Bylo Vám diagnostikováno onemocnění se syndromem chronické pánevní bolesti? Zažili jste pánevní bolest nebo nepříjemné pocity po dobu nejméně 3 z posledních 6 měsíců? Jste starší 18 let?
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí trachey (průdušnice)
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
Edukační materiály. KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře
 Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
sp.zn. sukls107935/2012
 sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
Důležité informace o přípravcích. předepsaných lékařem ke snížení rizika nákazy virem lidské imunodeficience (HIV)
 Důležité informace o přípravcích s obsahem emtricitabin/tenofovirdisoproxilu předepsaných lékařem ke snížení rizika nákazy virem lidské imunodeficience (HIV) Informace pro osoby, kterým byl předepsán přípravek
Důležité informace o přípravcích s obsahem emtricitabin/tenofovirdisoproxilu předepsaných lékařem ke snížení rizika nákazy virem lidské imunodeficience (HIV) Informace pro osoby, kterým byl předepsán přípravek
Příbalová informace: informace pro pacienta. Maltofer 50 mg/ml perorální kapky, roztok
 sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
1. Co je přípravek Maltofer Fol žvýkací tablety a k čemu se používá. Maltofer Fol se používá k léčbě a prevenci nedostatku železa v organismu.
 sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
Příbalová informace: informace pro uživatele. Metastron 37 MBq/ml, injekční roztok
 sp.zn. sukls72263/2019 Příbalová informace: informace pro uživatele Metastron 37 MBq/ml, injekční roztok Strontii chloridum 89 Sr Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls72263/2019 Příbalová informace: informace pro uživatele Metastron 37 MBq/ml, injekční roztok Strontii chloridum 89 Sr Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Život s karcinomem ledviny
 Život s karcinomem ledviny Život s karcinomem ledviny není lehký. Ale nikdo na to nemusí být sám. Rodina, přátelé i poskytovatelé zdravotní péče, všichni mohou pomoci. Péče o pacienta s karcinomem buněk
Život s karcinomem ledviny Život s karcinomem ledviny není lehký. Ale nikdo na to nemusí být sám. Rodina, přátelé i poskytovatelé zdravotní péče, všichni mohou pomoci. Péče o pacienta s karcinomem buněk
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE. MYGREF 250 MG tvrdá tobolka. mofetilis mycophenolas
 Sp.zn. sukls82417/2013 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE MYGREF 250 MG tvrdá tobolka mofetilis mycophenolas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
Sp.zn. sukls82417/2013 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE MYGREF 250 MG tvrdá tobolka mofetilis mycophenolas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn. sukls33384/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn. sukls33384/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sodium Iodide (I131) injection Injekční / perorální roztok 131 I jako jodid sodný
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn. sukls33384/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sodium Iodide (I131) injection Injekční / perorální roztok 131 I jako jodid sodný
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. ALBUNORM 5% 50g/l, infuzní roztok Lidský albumin
 Sp.zn.sukls151598/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ALBUNORM 5% 50g/l, infuzní roztok Lidský albumin Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Sp.zn.sukls151598/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ALBUNORM 5% 50g/l, infuzní roztok Lidský albumin Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro pacienta. ANACID 258 mg/388 mg perorální suspenze. Magnesii hydroxidum, Algeldrati suspensio
 sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: Informace pro uživatele. Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum)
 sp.zn. sukls273948/2016 Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls273948/2016 Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CAMILIA perorální roztok v jednodávkovém obalu
 sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
Příloha III. Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příbalová informace: informace pro uživatele. Aminoplasmal Hepa - 10% infuzní roztok
 sp.zn. sukls143336/2012 Příbalová informace: informace pro uživatele Aminoplasmal Hepa - 10% infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls143336/2012 Příbalová informace: informace pro uživatele Aminoplasmal Hepa - 10% infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
RÁDCE PACIENTA. Pro aplikaci přípravku Metoject 50 mg/ml injekční roztok, předplněné injekční stříkačky s obsahem metotrexátu
 RÁDCE PACIENTA Pro aplikaci přípravku Metoject 50 mg/ml injekční roztok, předplněné injekční stříkačky s obsahem metotrexátu RYCHLÝ PŘEHLED Tento materiál je určen výhradně pacientům užívajícím přípravek
RÁDCE PACIENTA Pro aplikaci přípravku Metoject 50 mg/ml injekční roztok, předplněné injekční stříkačky s obsahem metotrexátu RYCHLÝ PŘEHLED Tento materiál je určen výhradně pacientům užívajícím přípravek
Příbalová informace: informace pro uživatele. Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum
 sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
Účinný boj s LDL-cholesterolem? STATINY?!
 Účinný boj s LDL-cholesterolem? STATINY?! BRÁT! SAMOZŘEJMĚ! Pověry o statinech aneb Nevěřte všemu, co se povídá a píše O statinech, tedy lécích na snížení množství cholesterolu v krvi, koluje mezi laiky,
Účinný boj s LDL-cholesterolem? STATINY?! BRÁT! SAMOZŘEJMĚ! Pověry o statinech aneb Nevěřte všemu, co se povídá a píše O statinech, tedy lécích na snížení množství cholesterolu v krvi, koluje mezi laiky,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. ATG-Fresenius S (Immunoglobulinum antithymocytarum cuniculum) Koncentrát pro přípravu infuzního roztoku
 Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls242661/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ATG-Fresenius S (Immunoglobulinum antithymocytarum cuniculum) Koncentrát pro přípravu
Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls242661/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ATG-Fresenius S (Immunoglobulinum antithymocytarum cuniculum) Koncentrát pro přípravu
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Dorsiflex 200 mg tablety (Mephenoxalonum)
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dorsiflex 200 mg tablety (Mephenoxalonum) Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dorsiflex 200 mg tablety (Mephenoxalonum) Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
Deficit antagonisty IL-1 receptoru (DIRA)
 www.printo.it/pediatric-rheumatology/cz/intro Deficit antagonisty IL-1 receptoru (DIRA) Verze č 2016 1. CO JE DIRA? 1.1 O co se jedná? Deficit antagonisty IL-1Receptoru (DIRA) je vzácné vrozené onemocnění.
www.printo.it/pediatric-rheumatology/cz/intro Deficit antagonisty IL-1 receptoru (DIRA) Verze č 2016 1. CO JE DIRA? 1.1 O co se jedná? Deficit antagonisty IL-1Receptoru (DIRA) je vzácné vrozené onemocnění.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU {Krabička na blistry a lahvičky z HDPE } 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Sandoz 60mg Orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tvrdá tobolka obsahuje orlistatum
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU {Krabička na blistry a lahvičky z HDPE } 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Sandoz 60mg Orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tvrdá tobolka obsahuje orlistatum
