dnavou artritidou (GA)
|
|
|
- Václav Pavlík
- před 5 lety
- Počet zobrazení:
Transkript
1 EDUKAČNÍ MATERIÁLY ILARIS (kanakinumab) Průvodce pro lékaře k používání přípravku Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí být hlášeno Státnímu ústavu pro kontrolu léčiv. Podrobnosti o hlášení najdete na: Adresa pro zasílání je Státní ústav pro kontrolu léčiv, oddělení farmakovigilance, Šrobárova 48, Praha 10, , farmakovigilance@sukl.cz. Ilaris je biologický léčivý přípravek. V hlášení je proto nutné uvést jeho přesný obchodní název (Ilaris) a číslo šarže. Tato informace může být také hlášena společnosti Novartis na adresu: Novartis s.r.o., Gemini, budova B, Na Pankráci 1724/129, Praha 4, tel: , fax: , farmakovigilance.cz@novartis.com Na této adrese a telefonním čísle můžete rovněž požádat o další zásilku edukačních materiálů. Dříve než přípravek Ilaris předepíšete, přečtěte si pečlivě souhrn údajů o přípravku (SmPC). Průvodce pro lékaře k používání přípravku ILARIS (kanakinumab) pro léčbu pacientů se: syndromy periodických horeček: CAPS TRAPS HIDS/MKD FMF Stillovou chorobou (včetně AOSD a SJIA) nebo dnavou artritidou (GA)
2 Indikace Syndromy periodických horeček: Přípravek Ilaris je indikován k léčbě následujících autoinflamatorních syndromů periodických horeček u dospělých, dospívajících a dětí starších 2 let: CAPS Přípravek ILARIS je indikován k léčbě kryopyrinasociovaných periodických syndromů (CAPS), včetně: Muckle-Wellsova syndromu (MWS) Multisystémového zánětlivého onemocnění se začátkem v novorozeneckém věku (NOMID) / chronického infantilního neurologického, kožního a kloubního syndromu (CINCA) Těžkých forem familiárního chladového autozánětlivého syndromu (FCAS) / familiární chladové kopřivky (FCU), projevující se známkami a příznaky mimo chladem indukovanou kopřivku TRAPS Přípravek ILARIS je indikován k léčbě periodického syndromu asociovaného s receptorem pro tumornekrotizující faktor (TNF) (TRAPS). HIDS/MKD Přípravek ILARIS je indikován k léčbě syndromu hyperimunoglobulinemie D (HIDS) / deficitu mevalonátkinázy (MKD). FMF Přípravek ILARIS je indikován k léčbě familiární středomořské horečky (FMF). Je-li to vhodné, může se podávat v kombinaci s kolchicinem. Stillova choroba (včetně AOSD a SJIA) Přípravek ILARIS je indikován k léčbě aktivní Stillovy choroby včetně Stillovy choroby se začátkem v dospělém věku (AOSD) a systémové juvenilní idiopatické artritidy (SJIA) u pacientů starších 2 let, kteří adekvátně neodpověděli na předchozí léčbu nesteroidními antirevmatiky (NSAID) a systémovými kortikosteroidy. Přípravek Ilaris lze podávat ve formě monoterapie nebo v kombinaci s metotrexátem. Dnavá artritida Přípravek ILARIS je indikován k symptomatické léčbě dospělých pacientů s častými záchvaty dnavé artritidy (nejméně 3 záchvaty během posledních 12 měsíců), u nichž jsou kontraindikovány nesteroidní protizánětlivé léky (NSAID) a kolchicin, nejsou tolerovány nebo neposkytují odpovídající léčebnou odpověď a u nichž není vhodné opakované podávání kortikosteroidů. Důležité bezpečnostní informace Co je potřeba vědět před zahájením léčby kanakinumabem. S léčbou jsou spojena následující rizika: Infekce včetně infekcí závažných a oportunních U pacientů léčených kanakinumabem existuje zvýšené riziko infekcí včetně infekcí závažných. U pacientů je nutno během léčby kanakinumabem a po ní pozorně sledovat případné známky a příznaky infekcí. Při podávání kanakinumabu pacientům s infekcemi, s rekurentními infekcemi v anamnéze nebo se základními onemocnění, které je mohou činit náchylnými k infekcím, je nutno postupovat opatrně. V případě syndromů periodických horeček a Stillovy choroby (včetně AOSD a SJIA): Léčba kanakinumabem se nemá zahajovat nebo by se nemělo v léčbě pokračovat u pacientů s probíhající aktivní infekcí vyžadující lékařský zásah. Při dnavé artritidě: Léčba se nesmí podávat pacientům s aktivní infekcí. Při podávání kanakinumabu byly hlášeny izolované případy neobvyklých nebo oportunních infekcí. Není známo, zda podávání inhibitorů IL-1, jako je kanakinumab, nezvyšuje riziko reaktivace tuberkulózy nebo oportunních infekcí. Před zahájením léčby je nutno u všech pacientů vyhodnotit aktivní i latentní infekci tuberkulózou. Syndrom aktivace makrofágů Pouze při Stillově chorobě (včetně AOSD a SJIA): Syndrom aktivace makrofágů (MAS) je známá, život ohrožující porucha, která se může rozvinout při revmatických postiženích, zejména u pacientů se Stillovou chorobou (včetně AOSD a SJIA). Dojde-li k MAS nebo vznikne-li podezření na MAS, je nutné diagnostikovat a zahájit léčbu co možná nejdříve. Je třeba, aby lékaři věnovali pozornost příznakům infekce nebo zhoršení Stillovy choroby (včetně AOSD a SJIA), jelikož se jedná o známé spouštěče MAS. Podle aktuálně dostupných zkušeností z klinických hodnocení se nezdá, že by kanakinumab u pacientů se SJIA zvyšoval četnost výskytu MAS, nelze nicméně učinit definitivní závěry.
3 Důležité bezpečnostní informace (pokračování) Co je potřeba vědět před zahájením léčby kanakinumabem. S léčbou jsou spojena následující rizika: Neutropenie U léčivých přípravků inhibujících IL-1, včetně kanakinumabu, byla pozorována neutropenie (absolutní počet neutrofilů <1,5x 109/l). Léčba kanakinumabem se u pacientů s neutropenií nemá zahajovat. Doporučuje se vyhodnotit hladinu neutrofilů ještě před zahájením léčby, dále po 1 až 2 měsících a vyšetřovat ji pravidelně během léčby kanakinumabem. Pokud se u pacienta rozvine neutropenie, je nutno sledovat absolutní počet neutrofilů a zvážit přerušení léčby. Očkování Ohledně rizika sekundárního přenosu infekce živými (oslabenými) vakcínami nejsou pro pacienty léčené kanakinumabem k dispozici žádné údaje. Pacientům léčeným kanakinumabem by se tudíž živé vakcíny neměly podávat současně s léčbou, pokud přínosy jednoznačně nepřevažují nad riziky. Před zahájením léčby kanakinumabem se doporučuje dospělým i pediatrickým pacientům, aby absolvovali veškerá doporučená očkování včetně očkování proti pneumokokovým nákazám a inaktivovaných vakcín proti chřipce. Pokud je pacientům léčených kanakinumabem nutno podat živou vakcínu, je třeba vyčkat nejméně 3 měsíce po poslední injekci i před následující injekcí. Potenciální riziko imunogenicity a reakcí z přecitlivělosti U malé části pacientů léčených kanakinumabem byly pozorovány protilátky proti kanakinumabu. Jejich výskyt by mohl způsobovat imunitně mediované příznaky včetně reakcí z přecitlivělosti. Během klinického výzkumu nebyly pozorovány žádné anafylaktické ani anafylaktoidní reakce. Nebyly zjištěny žádné neutralizující protilátky. Nebyla pozorována žádná zjevná korelace mezi vývojem protilátek a klinickou odpovědí či nežádoucími příhodami. Při dnavé artritidě: Intermitentní léčba nebo opětovná expozice po dlouhém období bez léčby, což bývá případ léčby dnavé artritidy, mohou být spojeny se zesílenou imunitní odpovědí (nebo ztrátou imunitní tolerance) na kanakinumab. Opakovaně léčené pacienty je tudíž nutno považovat za rizikové z hlediska reakcí z přecitlivělosti. U pacientů s dnavou artritidou léčených po vzplanutí onemocnění nebyly pozorovány žádné anafylaktické reakce ani nežádoucí příhody související s imunogenicitou/alergenicitou. Malignity U pacientů léčených kanakinumabem v průběhu klinického vývoje byly hlášeny malignity. Výše rizika rozvoje maligního onemocnění při anti-interleukin (IL)-1 terapii není známa. U pacientů léčených kanakinumabem nelze vyloučit potenciální riziko. V případě syndromů periodických horeček a Stillovy choroby (včetně AOSD a SJIA): U pacientů léčených kanakinumabem je nutné vyšetření jednou ročně na přítomnost malignit. Neznámá bezpečnost u těhotných a kojících žen Není známo, zda se kanakinumab vylučuje do mateřského mléka. Nebyly provedeny žádné formální studie potenciálního vlivu kanakinumabu na plodnost u člověka. Ženy, které jsou těhotné nebo hodlají otěhotnět, by měly být léčeny pouze na základě důkladného vyhodnocení přínosů a rizik. Pokud pacientka otěhotní nebo plánuje-li otěhotnět, je třeba, aby s ní lékař prodiskutoval rizika ohledně neznámé bezpečnosti kanakinumabu u těhotných a kojících žen. Poruchy metabolismu lipoproteinů Během léčby je nutno u pacientů pravidelně sledovat případné změny v lipidovém profilu. V klinických hodnoceních dnavé artritidy s aktivním komparátorem vykazovali pacienti léčení kanakinumabem změny metabolismu lipoproteinů (zvýšená hladina triglyceridů a frakcí cholesterolu). Klinický význam tohoto zjištění není znám. V klinických hodnoceních dnavé artritidy s aktivním komparátorem byl zjištěn průměrný nárůst hladiny triglyceridů o 33,5 mg/dl u pacientů léčených kanakinumabem v porovnání s mírným poklesem o 3,1 mg/dl u pacientů léčených triamcinolon acetonidem. Incidence pacientů se zvýšením hladiny triglyceridů o více než pětinásobek horní meze normálních hodnot (ULN) byla 2,4% v případě kanakinumabu a 0,7% v případě triamcinolon acetonidu.
4 Doporučené dávkování u CAPS dospělí a starší děti Doporučená úvodní dávka kanakinumabu u pacientů s CAPS závisí na jejich věku a tělesné hmotnosti. Ověřte si, že čtete oddíl věnovaný správné diagnóze a věkové skupině. Poté vyberte příslušný řádek v tabulce podle tělesné hmotnosti pacienta. Dospělí a děti ve věku 4 let s tělesnou hmotností 15 kg: 150 mg v případě tělesné hmotnosti >40 kg 2 mg/kg v případě tělesné hmotnosti 15 kg a 40 kg V případě tělesné hmotnosti <15 kg viz další tabulka Podává se jednou za 8 týdnů jako jednorázová dávka ve formě subkutánní injekce. Jak je popsáno níže, lze zvážit vyšší dávky, pokud se nedosáhne uspokojivé klinické odpovědi (upravení vyrážky a jiných generalizovaných zánětlivých příznaků). Tělesná hmotnost (kg) Úvodní dávka (2 mg/kg nebo 150 mg) První zvýšená dávka1 (4 mg/kg nebo 300 mg) Druhá zvýšená dávka2 (8 mg/kg nebo 600 mg) 15 <17 0,2 30 0,4 60 0, <21 0,25 37,5 0, ,3 45 0,6 90 1,2 180 > ,35 52,5 0, ,4 210 >28 <32 0,4 60 0, , <36 0,45 67,5 0, , ,5 75 1, ,0 300 >40 1, , ,0 600 Pro dávky >150 mg (1 ml) je nutno použít více než 1 ampulku přípravku ILARIS. 1 Pokud se po 7 dnech od zahájení léčby nedosáhne uspokojivé klinické odpovědi, lze zvážit podání druhé dávky (shodné s úvodní dávkou) kanakinumabu. Pokud se následně dosáhne terapeutické odpovědi na léčbu, je vhodné zachovat intenzivnější režim dávkování 300 mg nebo 4 mg/kg (u dětí 15 kg a 40 kg) jednou za 8 týdnů. 2 Pokud se po 7 dnech od podání druhé dávky nedosáhne uspokojivé klinické odpovědi, lze zvážit podání třetí dávky kanakinumabu (dalších 300 mg nebo 4 mg/kg [u dětí 15 kg a 40 kg]). Pokud se následně dosáhne úplné odpovědi na léčbu, je vhodné dle individuálního klinického posouzení zvážit zachování tohoto intenzivnějšího režimu dávkování 600 mg nebo 8 mg/kg jednou za 8 týdnů.
5 Doporučené dávkování u CAPS malé děti Doporučená úvodní dávka kanakinumabu u pacientů s CAPS závisí na jejich věku a tělesné hmotnosti. Ověřte si, že čtete oddíl věnovaný správné diagnóze a věkové skupině. Poté vyberte příslušný řádek v tabulce podle tělesné hmotnosti. Děti ve věku 2 až <4 roky s tělesnou hmotností 7,5 kg a Děti ve věku 4 roky s tělesnou hmotností 7,5 až <15 kg: 4 mg/kg V případě tělesné hmotnosti 15 kg viz předchozí tabulka Podává se jednou za 8 týdnů jako jednorázová dávka ve formě subkutánní injekce. Jak je popsáno níže, lze zvážit vyšší dávku, pokud se nedosáhne uspokojivé klinické odpovědi (upravení vyrážky a jiných generalizovaných zánětlivých příznaků). Tělesná hmotnost (kg) Úvodní dávka (4 mg/kg) První zvýšená dávka 1 (8 mg/kg) 7,5 8,5 0,2 30 0,4 60 >8,5 10 0,25 37,5 0,5 75 > ,3 45 0,6 90 > ,35 52,5 0,7 105 >14 <16 0,4 60 0, <18 0,45 67,5 0, <20 0, <22 0,55 82,5 1, ,6 90 1,2 180 > ,65 97,5 1,3 195 > , ,4 210 > ,75 112,5 1, <31 0, , <33 0,85 127,5 1, <35 0, , <37 0,95 142,5 1, , Pro dávky >150 mg (1 ml) je nutno použít 2 ampulky přípravku ILARIS. 1 Pokud se po 7 dnech od zahájení léčby nedosáhne uspokojivé klinické odpovědi, lze zvážit podání druhé dávky (shodné s úvodní dávkou, 4 mg/kg) kanakinumabu. Pokud se následně dosáhne úplné odpovědi na léčbu, je vhodné dle individuálního klinického posouzení zvážit zachování intenzivnějšího režimu dávkování 8 mg/kg jednou za 8 týdnů.
6 Doporučené dávkování u TRAPS, HIDS/MKD a FMF Ověřte si, že čtete oddíl věnovaný správné diagnóze. Doporučená úvodní dávka kanakinumabu při TRAPS, HIDS/MKD a FMF je: Dospělí, dospívající a děti ve věku 2 roky: 150 mg v případě tělesné hmotnosti >40 kg 2 mg/kg v případě tělesné hmotnosti 7,5 kg a 40 kg Podává se jednou za 4 týdny jako jednorázová dávka ve formě subkutánní injekce. Jak je popsáno níže, lze zvážit vyšší dávku, pokud se nedosáhne uspokojivé klinické odpovědi. Tělesná hmotnost (kg) Úvodní dávka (2 mg/kg nebo 150 mg) Zvýšená dávka1 (4 mg/kg nebo 300 mg) 7,5 0,1 15 0,2 30 >7,5 11,2 0,15 22,5 0,3 45 >11,2 15,0 0,2 30 0,4 60 >15,0 18,7 0,25 37,5 0,5 75 >18,7 22,5 0,3 45 0,6 90 >22,5 26,2 0,35 52,5 0,7 105 >26,2 30,0 0,4 60 0,8 120 >30,0 33,7 0,45 67,5 0,9 135 >33,7 37,5 0,5 75 1,0 150 >37,5 40,0 0,55 82,5 1,1 165 >40,0 1, ,0 300 Pro dávky >150 mg (1 ml) je nutno použít 2 ampulky přípravku ILARIS. 1 Pokud se po 7 dnech od zahájení léčby nedosáhne uspokojivé klinické odpovědi, lze zvážit podání druhé dávky kanakinumabu, 150 mg nebo 2 mg/kg. Pokud se následně dosáhne úplné odpovědi na léčbu, je vhodné zachovat intenzivnější režim dávkování 300 mg (nebo 4 mg/kg u pacientů s tělesnou hmotností 40 kg) jednou za 4 týdny.
7 Doporučené dávkování u Stillovy choroby (včetně AOSD a SJIA) Doporučená dávka kanakinumabu u pacientů se Stillovou chorobou (včetně AOSD a SJIA) a s tělesnou hmotností 7,5 kg je 4 mg/kg (až do maximální dávky 300 mg) a podává se jednou za 4 týdny ve formě subkutánní injekce. Tělesná hmotnost (kg) Úvodní dávka (2 mg/kg nebo 150 mg) 7,5 8,5 0,2 30 >8,5 10 0,25 37,5 > ,3 45 > ,35 52,5 >14 <16 0, <18 0,45 67,5 18 <20 0, <22 0,55 82, ,6 90 > ,65 97,5 > ,7 105 > ,75 112,5 >29 <31 0, <33 0,85 127,5 33 <35 0, <37 0,95 142,5 37 <39 1, <41 1,05 157, ,1 165 > ,15 172,5 > ,2 180 > ,25 187,5 > ,3 195 > ,35 202,5 >52 <54 1, ,45 217,5 > ,5 225 > ,55 232,5 > ,6 240 > ,65 247,5 > ,7 255 > ,75 262,5 >67 <68 1, <71 1,85 277,5 71 <73 1, ,95 292,5 >74 2,0 300 Pro dávky >150 mg (1 ml) je nutno použít 2 ampulky přípravku ILARIS.
8 Doporučené dávkování u dnavé artritidy Doporučená dávka kanakinumabu u dospělých pacientů s dnavou artritidou je 150 mg a podává se jednorázově při záchvatu ve formě subkutánní injekce. Pro dosažení maximálního účinku se má kanakinumab podat co nejdříve po nástupu záchvatu dnavé artritidy. U pacientů, kteří na počáteční léčbu nereagují, se léčba kanakinumabem nemá opakovat. U pacientů, kteří na léčbu reagují a potřebují její opakované podání, má před opětovným podáním nové dávky kanakinumabu uběhnout interval nejméně 12 týdnů. Při léčbě záchvatů dnavé artritidy se má kanakinumab používat jako léčba dle potřeby. Současně je třeba nasadit nebo optimalizovat léčbu hyperurikemie pomocí přípravků snižující hladinu urátů (angl. ULT). Co najdete v těchto edukačních materiálech Pro vás a vaše pacienty Tyto edukační materiály dostáváte jako doplněk k oficiálnímu souhrnu údajů o přípravku (SmPC) s cílem zvýšit porozumění o bezpečném a efektivním používání kanakinumabu. V těchto edukačních materiálech jsou zdůrazněny následující aspekty: Průvodce pro lékaře: Indikace Důležité bezpečnostní informace Doporučené dávkování Kartička pro pacienty Než dáte kartičku pacientovi, vyplňte všechna prázdná pole na kartičce (jméno pacienta, datum podání první dávky a skutečně podanou dávku, jméno a telefonní číslo lékaře). Kartička pacientovi slouží jako připomínka použité dávky a obsahuje důležité informace, které by pacient měl o léčbě kanakinumabem vědět. Samostatné podávání Je-li plánováno samostatné podávání, je nutné, aby lékař pacienta nebo pečovatele poučil o řádném postupu podávání léčby. Schémata a pokyny jsou uvedeny v příbalové informaci. Než kanakinumab předepíšete, pozorně si všechny informace pročtěte. CZ /06/17
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ilaris 150 mg, prášek pro injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna lahvička obsahuje canakinumabum* 150 mg. Po rekonstituci
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ilaris 150 mg, prášek pro injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna lahvička obsahuje canakinumabum* 150 mg. Po rekonstituci
INFLECTRA SCREENINGOVÝ LIST. a výběru pacientů pro všechny schválené indikace. Obsahuje pokyny ke správnému screeningu
 Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Edukační materiál. Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera
 Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
PRŮKAZ PACIENTA. užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019
 PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
U pacientů, jejichž tělesná hmotnost je vyšší než 100 kg, se dávky přesahující 800 mg/infuzi nedoporučují.
 EDUKAČNÍ MATERIÁLY RoActemra (tocilizumab) Kapesní dávkovací karta pro revmatoidní artritidu Přípravek RoActemra v kombinaci s metotrexátem (MTX) je indikován k léčbě středně těžké až těžké aktivní revmatoidní
EDUKAČNÍ MATERIÁLY RoActemra (tocilizumab) Kapesní dávkovací karta pro revmatoidní artritidu Přípravek RoActemra v kombinaci s metotrexátem (MTX) je indikován k léčbě středně těžké až těžké aktivní revmatoidní
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
 www.printo.it/pediatric-rheumatology/cz/intro Terapie Verze č 2016 13. Biologická léčba Nové perspektivy v léčbě se rozvinuly v posledních letech s nástupem tzv. biologických léků. Tento název je používán
www.printo.it/pediatric-rheumatology/cz/intro Terapie Verze č 2016 13. Biologická léčba Nové perspektivy v léčbě se rozvinuly v posledních letech s nástupem tzv. biologických léků. Tento název je používán
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
EDUKAČNÍ MATERIÁL - Pioglitazone Accord
 Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
PRŮKAZ PACIENTA. užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1
 PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
Rozměr zavřeného průkazu mm
 Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Zvažte oddálení podání regadenosonu u pacientů s nekontrolovanou hypertenzí.
 CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
EDUKAČNÍ MATERIÁLY. TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM)
 EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA)
 Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
Důležité informace pro pacienty
 MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE
 EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
CZ PAR. QUETIAPINI FUMARAS Seroquel. UK/W/0004/pdWS/001 NL/W/0004/pdWS/001
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
Návod pro pacienta / pečovatele
 Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
EXELON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY
 XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
Příloha II. Vědecké závěry a zdůvodnění změny v registraci
 Příloha II Vědecké závěry a zdůvodnění změny v registraci 6 Vědecké závěry Celkové shrnutí vědeckého hodnocení přípravku Cymevene i.v. a souvisejících názvů (viz příloha I) Evropská komise jménem všech
Příloha II Vědecké závěry a zdůvodnění změny v registraci 6 Vědecké závěry Celkové shrnutí vědeckého hodnocení přípravku Cymevene i.v. a souvisejících názvů (viz příloha I) Evropská komise jménem všech
RoACTEMRA pro systémovou juvenilní idiopatickou artritidu (sjia) CO BYSTE MĚLI VĚDĚT
 RoACTEMRA pro systémovou juvenilní idiopatickou artritidu (sjia) CO BYSTE MĚLI VĚDĚT Tato brožura poskytuje klíčové informace pomáhající pacientům se sjia a jejich rodičům/zákonným zástupcům porozumět
RoACTEMRA pro systémovou juvenilní idiopatickou artritidu (sjia) CO BYSTE MĚLI VĚDĚT Tato brožura poskytuje klíčové informace pomáhající pacientům se sjia a jejich rodičům/zákonným zástupcům porozumět
Příprava a podání injekce
 Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Rekurentní horečka spojená s NRLP21
 www.printo.it/pediatric-rheumatology/cz/intro Rekurentní horečka spojená s NRLP21 Verze č 2016 1. CO JE TO REKURENTNÍ HOREČKA SPOJENÁ S NRLP12 1.1 Co je to? Rekurentní horečka spojená s NRLP12 patří mezi
www.printo.it/pediatric-rheumatology/cz/intro Rekurentní horečka spojená s NRLP21 Verze č 2016 1. CO JE TO REKURENTNÍ HOREČKA SPOJENÁ S NRLP12 1.1 Co je to? Rekurentní horečka spojená s NRLP12 patří mezi
CZ PAR QUETIAPINUM. Seroquel. UK/W/0004/pdWS/001. NL/W/0004/pdWS/001
 CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
Edukační materiály. Imnovid (pomalidomid) Informace pro zdravotnické pracovníky. Brožura pokyny pro bezpečné použití přípravku
 Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pokyny pro bezpečné použití přípravku Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Brožura pokyny
Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pokyny pro bezpečné použití přípravku Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Brožura pokyny
CAVE! Informační dopis pro zdravotnické pracovníky
 CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ přijetí hlášení společností Roche (den-měsíc-rok): Lokální číslo: AER: OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení:
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ přijetí hlášení společností Roche (den-měsíc-rok): Lokální číslo: AER: OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení:
EDUKAČNÍ MATERIÁLY. Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce
 EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
EDUKAČNÍ MATERIÁLY. GILENYA (fingolimod)
 EDUKAČNÍ MATERIÁLY GILENYA (fingolimod) Souhrn doporučení pro předepisující lékaře Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
EDUKAČNÍ MATERIÁLY GILENYA (fingolimod) Souhrn doporučení pro předepisující lékaře Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
EDUKAČNÍ MATERIÁLY. KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
EDUKAČNÍ MATERIÁL. Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid)
 EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
DODATKY, KTERÉ MAJÍ BÝT DOPLNĚNY DO PŘÍSLUŠNÝCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH NIMESULID (SYSTÉMOVÉ FORMULACE)
 PŘÍLOHA III 1 DODATKY, KTERÉ MAJÍ BÝT DOPLNĚNY DO PŘÍSLUŠNÝCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH NIMESULID (SYSTÉMOVÉ FORMULACE) Dodatky jsou psány kurzívou a podtrženě, vymazané
PŘÍLOHA III 1 DODATKY, KTERÉ MAJÍ BÝT DOPLNĚNY DO PŘÍSLUŠNÝCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH NIMESULID (SYSTÉMOVÉ FORMULACE) Dodatky jsou psány kurzívou a podtrženě, vymazané
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
Edukační materiály. KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře
 Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Hemlibra (emicizumab) Subkutánní injekce. Návod pro zdravotnické pracovníky
 EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Poznámka: Tyto úpravy souhrnu údajů o přípravku a
 PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH)
 Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Doplněk MM guidelines: Doplněk č. 1 k doporučení z 9/2012 diagnostika a léčba mnohočetného myelomu
 Doplněk MM guidelines: Doplněk č. 1 k doporučení z 9/2012 diagnostika a léčba mnohočetného myelomu Marta Krejčí XIII. MM workshop a setkání CMG, Mikulov 11.4.2015 Doplněk č. 1 k doporučení z 9/2012: Diagnostika
Doplněk MM guidelines: Doplněk č. 1 k doporučení z 9/2012 diagnostika a léčba mnohočetného myelomu Marta Krejčí XIII. MM workshop a setkání CMG, Mikulov 11.4.2015 Doplněk č. 1 k doporučení z 9/2012: Diagnostika
Nebido EDUKAČNÍ MATERIÁL. Jak úspěšně aplikovat přípravek. (testosterone undecanoate)
 EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
Složení vakcíny odpovídá doporučení SZO (pro severní polokouli) a EU rozhodnutí pro sezónu2007/2008
 Příbalová informace - RP Informace pro použití, čtěte pozorně! Begrivac (vakcína proti chřipce) Injekční suspenze Sezóna 2007/2008 Držitel rozhodnutí o registraci a výrobce Novartis Vaccines and Diagnostics
Příbalová informace - RP Informace pro použití, čtěte pozorně! Begrivac (vakcína proti chřipce) Injekční suspenze Sezóna 2007/2008 Držitel rozhodnutí o registraci a výrobce Novartis Vaccines and Diagnostics
SOUHRN ÚDAJŮ O PŘÍPRAVKU. PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová
 sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha III. Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Kelapril 5mg 7x14tbl.
 Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
Příloha II. Vědecké závěry a zdůvodnění zrušení či změny podmínek rozhodnutí o registraci a podrobné vysvětlení rozdílů oproti doporučení výboru PRAC
 Příloha II Vědecké závěry a zdůvodnění zrušení či změny podmínek rozhodnutí o registraci a podrobné vysvětlení rozdílů oproti doporučení výboru PRAC 68 Vědecké závěry Koordinační skupina pro vzájemné uznávání
Příloha II Vědecké závěry a zdůvodnění zrušení či změny podmínek rozhodnutí o registraci a podrobné vysvětlení rozdílů oproti doporučení výboru PRAC 68 Vědecké závěry Koordinační skupina pro vzájemné uznávání
Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti.
 Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti. I V A N A K O V Á Ř O V Á C E N T R U M P R O D E M Y E L I N I Z A Č N Í O N E M O C N Ě N Í N E U R O L O G I C
Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti. I V A N A K O V Á Ř O V Á C E N T R U M P R O D E M Y E L I N I Z A Č N Í O N E M O C N Ě N Í N E U R O L O G I C
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE
 LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE Léčba by měla být zahájena a sledována specialistou se zkušenostmi v léčbě revmatoidní artritidy a psoriatické artritidy. Lékař by měl poučit pacienty
LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE Léčba by měla být zahájena a sledována specialistou se zkušenostmi v léčbě revmatoidní artritidy a psoriatické artritidy. Lékař by měl poučit pacienty
Příloha IV. Vědecké závěry
 Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
BAVENCIO (avelumab) Váš průvodce informacemi pro pacienta
 Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel)
 EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití)
 CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
RÁDCE PACIENTA. Pro aplikaci přípravku Metoject 50 mg/ml injekční roztok, předplněné injekční stříkačky s obsahem metotrexátu
 RÁDCE PACIENTA Pro aplikaci přípravku Metoject 50 mg/ml injekční roztok, předplněné injekční stříkačky s obsahem metotrexátu RYCHLÝ PŘEHLED Tento materiál je určen výhradně pacientům užívajícím přípravek
RÁDCE PACIENTA Pro aplikaci přípravku Metoject 50 mg/ml injekční roztok, předplněné injekční stříkačky s obsahem metotrexátu RYCHLÝ PŘEHLED Tento materiál je určen výhradně pacientům užívajícím přípravek
PÁSOVÝ OPAR A JEHO NÁSLEDKY. Prof. MUDr. Petr Arenberger, DrSc., MBA
 PÁSOVÝ OPAR A JEHO NÁSLEDKY Prof. MUDr. Petr Arenberger, DrSc., MBA Obtíže Už se vám někdy zakousl pes do obličeje? Karel Černý, pacient se zosterem Jeden virus (VZV) dvě nemoci Pásový opar (PO) Bolestivý
PÁSOVÝ OPAR A JEHO NÁSLEDKY Prof. MUDr. Petr Arenberger, DrSc., MBA Obtíže Už se vám někdy zakousl pes do obličeje? Karel Černý, pacient se zosterem Jeden virus (VZV) dvě nemoci Pásový opar (PO) Bolestivý
KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin. Informace pro lékaře EU
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
Edukační materiály. Anakinrum, Kineret 100 mg, injekční roztok v předplněné injekční stříkačce Návod pro zdravotnické pracovníky (ZP)
 Edukační materiály Anakinrum, Kineret 100 mg, injekční roztok v předplněné injekční stříkačce Návod pro zdravotnické pracovníky (ZP) Při předepisování přípravku Kineret u kryopyrin-asociovaných periodických
Edukační materiály Anakinrum, Kineret 100 mg, injekční roztok v předplněné injekční stříkačce Návod pro zdravotnické pracovníky (ZP) Při předepisování přípravku Kineret u kryopyrin-asociovaných periodických
ACTYNOX 50 % / 50 % V/V Oxid dusný (dinitrogenii oxidum) / kyslík (oxygenum) Medicinální plyn, stlačený PRŮVODCE PRO ZDRAVOTNICKÉ PRACOVNÍKY
 Edukační materiály Orgány veřejného zdraví stanovily určité podmínky pro tržní rozvoj přípravku ACTYNOX. Jednou z nich je předávat tyto informace zdravotnickým pracovníkům jako součást povinného plánu
Edukační materiály Orgány veřejného zdraví stanovily určité podmínky pro tržní rozvoj přípravku ACTYNOX. Jednou z nich je předávat tyto informace zdravotnickým pracovníkům jako součást povinného plánu
Familiární středomořská (Mediterranean) horečka (Fever)
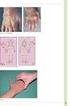 www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
CZ PAR. QUETIAPINI FUMARAS Seroquel. NL/W/0004/pdWS/002
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příbalová informace: informace pro uživatele
 sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy (PSUR) pro bendamustin-hydrochlorid byly
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy (PSUR) pro bendamustin-hydrochlorid byly
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Kineret 100 mg/0,67 ml injekční roztok v předplněné injekční stříkačce. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Kineret 100 mg/0,67 ml injekční roztok v předplněné injekční stříkačce. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
Deficit antagonisty IL-1 receptoru (DIRA)
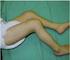 www.printo.it/pediatric-rheumatology/cz/intro Deficit antagonisty IL-1 receptoru (DIRA) Verze č 2016 1. CO JE DIRA? 1.1 O co se jedná? Deficit antagonisty IL-1Receptoru (DIRA) je vzácné vrozené onemocnění.
www.printo.it/pediatric-rheumatology/cz/intro Deficit antagonisty IL-1 receptoru (DIRA) Verze č 2016 1. CO JE DIRA? 1.1 O co se jedná? Deficit antagonisty IL-1Receptoru (DIRA) je vzácné vrozené onemocnění.
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
HEMOFILIE - DIAGNOSTIKA A LÉČBA V SOUČASNOSTI
 HEMOFILIE - DIAGNOSTIKA A LÉČBA V SOUČASNOSTI Patofyziologie hemofilie Deficit koagulačního faktoru VIII (hemofilie A) nebo IX (hemofilie B), jeho dysfunkce nebo přítomnost jeho inhibitorů vede k poruše
HEMOFILIE - DIAGNOSTIKA A LÉČBA V SOUČASNOSTI Patofyziologie hemofilie Deficit koagulačního faktoru VIII (hemofilie A) nebo IX (hemofilie B), jeho dysfunkce nebo přítomnost jeho inhibitorů vede k poruše
Souhrn doporučení pro předepisujícího lékaře
 G Souhrn doporučení pro předepisujícího lékaře Kritéria výběru pacientů pro léčbu přípravkem GILENYA (fingolimod) Přípravek GILENYA je vhodný pro dospělé pacienty k léčbě vysoce aktivní relabující-remitentní
G Souhrn doporučení pro předepisujícího lékaře Kritéria výběru pacientů pro léčbu přípravkem GILENYA (fingolimod) Přípravek GILENYA je vhodný pro dospělé pacienty k léčbě vysoce aktivní relabující-remitentní
Příloha II. Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci
 Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 21 Vědecké závěry Celkové závěry vědeckého hodnocení přípravků Oxynal a Targin a souvisejících názvů (viz příloha I) Podkladové
Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 21 Vědecké závěry Celkové závěry vědeckého hodnocení přípravků Oxynal a Targin a souvisejících názvů (viz příloha I) Podkladové
Váš průvodce léčbou poškození zraku v důsledku diabetického makulárního edému (DME) přípravkem Lucentis (ranibizumab)
 Váš průvodce léčbou poškození zraku v důsledku diabetického makulárního edému (DME) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu poškození
Váš průvodce léčbou poškození zraku v důsledku diabetického makulárního edému (DME) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu poškození
Příbalová informace: Informace pro pacienta. Yttrium ( 90 Y) colloid suspension for local injection YTTRII-( 90 Y) CITRAS injekční suspenze
 sp.zn. sukls174761/2012 Příbalová informace: Informace pro pacienta Yttrium ( 90 Y) colloid suspension for local injection YTTRII-( 90 Y) CITRAS injekční suspenze (V této příbalové informaci dále nazývaný
sp.zn. sukls174761/2012 Příbalová informace: Informace pro pacienta Yttrium ( 90 Y) colloid suspension for local injection YTTRII-( 90 Y) CITRAS injekční suspenze (V této příbalové informaci dále nazývaný
Příloha II. Vědecké závěry
 Příloha II Vědecké závěry 74 Vědecké závěry Dne 7. července 2016 zahájila Velká Británie na základě farmakovigilančních údajů postup podle článku 31 směrnice 2001/83/ES a požádalo výbor PRAC, aby přezkoumal
Příloha II Vědecké závěry 74 Vědecké závěry Dne 7. července 2016 zahájila Velká Británie na základě farmakovigilančních údajů postup podle článku 31 směrnice 2001/83/ES a požádalo výbor PRAC, aby přezkoumal
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU. Přípavek již není registrován
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rilonacept Regeneron 80 mg/ml prášek pro přípravu injekčního roztoku s rozpouštědlem. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Rilonacept Regeneron 80 mg/ml prášek pro přípravu injekčního roztoku s rozpouštědlem. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička
BIOVISC ORTHO M. Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci.
 Česky BIOVISC ORTHO M Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová Mannitol 20 mg 5 mg Fosfátem pufrovaný
Česky BIOVISC ORTHO M Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová Mannitol 20 mg 5 mg Fosfátem pufrovaný
Celkové shrnutí vědeckého hodnocení přípravku Atacand Plus a související názvy (viz Příloha I)
 PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÝCH INFORMACÍ PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 14 Vědecké závěry Celkové
PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÝCH INFORMACÍ PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 14 Vědecké závěry Celkové
NeuroBloc. botulinový toxin typu B injekční roztok, U/ml
 NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls221497/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucicort Krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Acidum fusidicum 20,0 mg (jako acidum fusidicum hemihydricum) Betamethasonum
sp.zn. sukls221497/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucicort Krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Acidum fusidicum 20,0 mg (jako acidum fusidicum hemihydricum) Betamethasonum
Souhrn údajů o přípravku
 sp. zn. sukls208148/2014 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Povrchové
sp. zn. sukls208148/2014 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Povrchové
Důležité informace o užívání přípravku TASIGNA
 Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Brožura s informacemi pro pacienta a rodiče pacienta s ahus
 Brožura s informacemi pro pacienta a rodiče pacienta s ahus Schválena SÚKL dne 18. března 2019 SLOVNÍK POJMŮ Atypický hemolytickouremický syndrom (ahus) Vzácná porucha způsobená chronickou a nadměrnou
Brožura s informacemi pro pacienta a rodiče pacienta s ahus Schválena SÚKL dne 18. března 2019 SLOVNÍK POJMŮ Atypický hemolytickouremický syndrom (ahus) Vzácná porucha způsobená chronickou a nadměrnou
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
 www.printo.it/pediatric-rheumatology/cz/intro Blauův syndrom Verze č 2016 1. CO JE BLAUŮV SYNDROM/ JUVENILNÍ SARKOIDÓZA? 1.1 Co je to? Blauův syndrom je dědičné onemocnění. Pacienti trpí kombinací projevů:
www.printo.it/pediatric-rheumatology/cz/intro Blauův syndrom Verze č 2016 1. CO JE BLAUŮV SYNDROM/ JUVENILNÍ SARKOIDÓZA? 1.1 Co je to? Blauův syndrom je dědičné onemocnění. Pacienti trpí kombinací projevů:
Pioneer in Rare Diseases. Pozvánka na satelitní sympozium společnosti SOBI. Co přináší Fc technologie do léčby dětských pacientů s hemofilií A i B?
 Pioneer in Rare Diseases Pozvánka na satelitní sympozium společnosti SOBI Co přináší Fc technologie do léčby dětských pacientů s hemofilií A i B? Vážená paní doktorko, vážený pane doktore, dovolte, abychom
Pioneer in Rare Diseases Pozvánka na satelitní sympozium společnosti SOBI Co přináší Fc technologie do léčby dětských pacientů s hemofilií A i B? Vážená paní doktorko, vážený pane doktore, dovolte, abychom
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Struktura parametrické dokumentace registru ATTRA Diagnóza: Juvenilní idiopatická artritida
 Struktura parametrické dokumentace registru ATTRA Diagnóza: Juvenilní idiopatická artritida Vstupní údaje... 1 Identifikační údaje pacienta... 1 Identifikační údaje centra... 1 Vstupní vyšetření... 2 Vstupní
Struktura parametrické dokumentace registru ATTRA Diagnóza: Juvenilní idiopatická artritida Vstupní údaje... 1 Identifikační údaje pacienta... 1 Identifikační údaje centra... 1 Vstupní vyšetření... 2 Vstupní
Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1
![Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1 Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1](/thumbs/102/154291766.jpg) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím
 Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
PŘÍLOHA I. Page 1 of 5
 PŘÍLOHA I SEZNAM NÁZVŮ, LÉKOVÁ FORMA, KONCENTRACE VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU, ŽIVOČIŠNÉ DRUHY, ZPŮSOB(Y) PODÁNÍ, DRŽITEL ROZHODNUTÍ O REGISTRACI V ČLENSKÝCH STÁTECH Page 1 of 5 Členský stát Žadatel
PŘÍLOHA I SEZNAM NÁZVŮ, LÉKOVÁ FORMA, KONCENTRACE VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU, ŽIVOČIŠNÉ DRUHY, ZPŮSOB(Y) PODÁNÍ, DRŽITEL ROZHODNUTÍ O REGISTRACI V ČLENSKÝCH STÁTECH Page 1 of 5 Členský stát Žadatel
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 sp.zn. sukls33645/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls33645/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Souhrn údajů o přípravku. Typhoidi capsulae Vi polysaccharidum purificatum (stirpe Ty 2)
 sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
