Příbalová informace: Informace pro uživatele
|
|
|
- Alžběta Lišková
- před 7 lety
- Počet zobrazení:
Transkript
1 Příbalová informace: Informace pro uživatele ReFacto AF 250 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 500 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 1000 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 2000 IU prášek a rozpouštědlo pro injekční roztok Moroctocogum alfa (rekombinantní lidský koagulační faktor VIII) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje. - Ponechte si příbalovou informaci. Možná, že si ji budete potřebovat přečíst znovu. - Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy. - Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4. Co naleznete v této příbalové informaci 1. Co je přípravek ReFacto AF a k čemu se používá. 2. Čemu musíte věnovat pozornost, než začnete přípravek ReFacto AF používat. 3. Jak se přípravek ReFacto AF používá. 4. Možné nežádoucí účinky. 5. Jak přípravek ReFacto AF uchovávat. 6. Obsah balení a další informace 1. Co je přípravek ReFacto AF a k čemu se používá Přípravek ReFacto AF obsahuje léčivou látku moroktokog alfa, lidský koagulační faktor VIII. Faktor VIII je nezbytný k tvorbě krevních sraženin a k zastavení krvácení. U pacientů s hemofilií A (vrozený nedostatek faktoru VIII) chybí nebo správně nefunguje. Přípravek ReFacto AF se používá k léčbě nebo prevenci krvácení (profylaxe) u dospělých a dětí všech věkových skupin (včetně novorozenců) s hemofilií A. 2. Čemu musíte věnovat pozornost, než začnete přípravek ReFacto AF používat Nepoužívejte ReFacto AF - jestliže jste alergický(á) na moroctocog alfa nebo na kteroukoliv další složku tohoto přípravku (uvedenou v bodě 6). - jestliže jste alergický(á) na křeččí proteiny. Pokud si nejste jistý(a), zeptejte se svého lékaře. Upozornění a opatření Před použitím přípravku ReFacto AF se poraďte se svým lékařem nebo lékárníkem 1
2 - pokud dostanete alergickou reakci. Takovými příznaky alergické reakce jsou dechové potíže, dušnost, otok, kopřivka, svědění, tísnivý pocit na prsou, sípání a nízký krevní tlak. Anafylaxe je závažná alergická reakce, která může způsobit obtíže při polykání a/nebo dýchání, zrudnutí či otok tváře a/nebo rukou. Pokud se vyskytnou některé z těchto známek, zastavte ihned infuzi a spojte se s lékařem či vyhledejte pohotovostní lékařskou pomoc. V případě závažných alergických reakcí je třeba zvážit alternativní léčbu. - nedojde-li k zastavení krvácení podle očekávání, spojte se s lékařem či vyhledejte lékařskou pohotovostní službu. - jestliže se nepodaří zastavit krvácení obvyklou dávkou. U pacientů, kteří dostávají přípravky obsahující faktor VIII, se mohou někdy vyvinout protilátky proti faktoru VIII (též známé jako inhibitory faktoru VIII), které mohou zabránit správnému účinku přípravků obsahujících faktor VIII. Pokud jste léčen(a) faktorem VIII, měl(a) byste být sledován(a) na rozvoj inhibitorů faktoru VIII. Další léčivé přípravky a přípravek ReFacto AF Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte nebo jste užíval(a) v nedávné době nebo které možná budete užívat. Těhotenství, kojení a plodnost Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek používat. Řízení dopravních prostředků a obsluha strojů: Přípravek ReFacto AF nemá žádný vliv na schopnost řídit nebo obsluhovat stroje. Přípravek ReFacto AF obsahuje sodík. Přípravek ReFacto AF obsahuje 1,23 mmol (nebo 29 mg) sodíku v jedné injekční lahvičce rozpuštěného prášku. Informujte svého lékaře, pokud jste na řízené sodíkové dietě. 3. Jak se přípravek ReFacto AF používá Vždy používejte tento přípravek přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem. Léčbu přípravkem ReFacto AF má zahajovat lékař se zkušeností s léčbou pacientů s hemofilií A. Váš lékař Vám stanoví dávku přípravku ReFacto AF, kterou dostanete. Tato dávka a trvání léčby bude záviset na Vaší individuální potřebě náhrady faktoru VIII. Přípravek ReFacto AF se podává injekcí do žíly po dobu několika minut. Pacienti nebo jejich pečovatelé mohou podávat injekce přípravku ReFacto AF, pokud byli řádně proškoleni. V průběhu léčby může lékař rozhodnout o změně dávky přípravku ReFacto AF, kterou dostáváte. Před cestováním se, prosím, poraďte se svým poskytovatelem zdravotní péče. Na cestu byste si měl(a) opatřit dostatečnou zásobu přípravku obsahující faktor VIII ke své předpokládané léčbě. Doporučuje se, kdykoli použijete přípravek ReFacto AF, zaznamenat si z obalu název přípravku a číslo šarže. Pro účely hlášení nežádoucích účinků můžete dokumentovat číslo šarže odlepením štítku z jedné injekční lahvičky a jeho nalepením do svého diáře. 2
3 Rekonstituce (rozpuštění) a podání Níže popsaný postup slouží jako obecný návod pro rekonstituci a podávání přípravku ReFacto AF. Pacienti by měli sledovat specifický postup rekonstituce a podávání přípravku lékařem. K rekonstituci použijte pouze předplněnou injekční stříkačku dodávanou v krabičce. K podání přípravku může být použita jiná sterilní injekční stříkačka pro jednorázové použití. Přípravek ReFacto AF se podává intravenózní (i.v.) infuzí po rekonstituci lyofilizovaného prášku na injekci přiloženým rozpouštědlem [roztok chloridu sodného 9 mg/ml (0,9%)] v injekční stříkačce. Přípravek ReFacto AF nemá být mísen s jinými infuzními roztoky. Před rekonstitucí a podáním léku si vždy umyjte ruce. Během rekonstituce musí být dodrženy zásady aseptické přípravy (tj. čisté a bezmikrobiální). Rekonstituce: 1. Nechejte injekční lahvičku s lyofilizovaným přípravkem ReFacto AF a rozpouštědlo v předplněné injekční stříkačce zahřát na pokojovou teplotu. 2. Odstraňte plastové víčko z injekční lahvičky ReFacto AF, aby se odkryla střední část gumového uzávěru. 3. Otřete vršek lahvičky přiloženým tampónem s alkoholem nebo použijte jiný antiseptický roztok a nechejte oschnout. Po očištění se už nedotýkejte rukama gumové zátky a nedovolte, aby se zátka něčeho dotkla. 4. Odloupněte víčko z čirého plastového obalu adaptéru injekční lahvičky. Nevyjímejte adaptér z obalu. 5. Položte injekční lahvičku na plochý povrch. Vezměte obal s adaptérem, položte adaptér na injekční lahvičku a přitlačte obal silně dolů, až adaptér pronikne shora na vrchol injekční lahvičky a jehla adaptéru pronikne gumovou zátkou. 6. Sejměte obal z adaptéru a vyhoďte jej. 3
4 7. Připevněte táhlo s pístem k injekční stříkačce s rozpouštědlem vložením táhla do otvoru v zátce injekční stříkačky za stálého tlaku a otáčení, až bezpečně sedí v zátce. 8. Odlomte bezpečnostní kryt hrotu injekční stříkačky rozpouštědla ulomením perforace krytky. To se provede střídavým ohýbáním krytu nahoru a dolů dokud se perforace neulomí. Nedotýkejte se vnitřní části krytu ani hrotu stříkačky. Možná že kryt bude muset být znovu nasazen (jestliže se rekonstituovaný přípravek ReFacto AF nepodává bezprostředně), proto jej umístěte stranou a postavte na jeho vrchol. 9. Postavte injekční lahvičku na rovnou plochu. Vložením hrotu do otvoru adaptéru spojte injekční stříkačku rozpouštědla s adaptérem injekční lahvičky za stálého tlaku a otáčení stříkačky ve směru hodinových ručiček až do zajištění spojení. 10. Pomalým tlakem na táhlo pístu vstříkněte veškeré rozpouštědlo do injekční lahvičky ReFacto AF. 11. Zatímco injekční stříkačka je stále spojena s adaptérem, jemně otáčejte injekční lahvičkou až do rozpuštění prášku. 12. Připravený roztok musí být před podáním vizuálně zkontrolován, aby neobsahoval mechanické částice. Roztok musí být čirý až mírně opalescentní a bezbarvý. 4
5 Poznámka: Jestliže použijete na infuzi více než jednu injekční lahvičku přípravku ReFacto AF, obsah každé injekční lahvičky má být rozpuštěn podle předchozího návodu. Injekční stříkačka rozpouštědla se má odstranit, přičemž adaptér injekční lahvičky se ponechá na místě a ke stažení rozpuštěného obsahu jednotlivých injekčních lahviček může být použita samostatná velká injekční stříkačka s otvorem luer. 13. Přesvědčte se, že táhlo pístu je stále úplně stlačené a převraťte injekční lahvičku dnem vzhůru. Pomalu stáhněte všechen roztok přes adaptér lahvičky zpět do injekční stříkačky. 14. Odpojte injekční stříkačku od adaptéru injekční lahvičky jemným tahem a otáčením injekční stříkačky proti směru hodinových ručiček. Zlikvidujte injekční lahvičku s připojeným adaptérem. Poznámka: Jestliže roztok nemá být podán bezprostředně, na stříkačku se musí opatrně nasadit kryt. Nedotýkejte se hrotu stříkačky ani vnitřní strany krytu. Přípravek ReFacto AF musí být použit nejpozději do 3 hodin po rekonstituci. Připravený roztok může být před podáním uchováván při pokojové teplotě. Podání (intravenózní infuze): Přípravek ReFacto AF má být podán přiloženou infuzní soupravou a předplněnou injekční stříkačkou s rozpouštědlem nebo samostatnou sterilní injekční stříkačkou z plastické hmoty k jednorázovému použití s otvorem luer. 1. Nasaďte injekční stříkačku na konec luer hadičky infuzního setu. 2. Přiložte škrtidlo a připravte si injekční místo otřením kůže alkoholovým tampónem, dodaným v soupravě. 5
6 3. Napíchněte žílu jehlou s infuzní soupravou podle pokynů lékaře a sejměte škrtidlo. Odstraňte veškerý vzduch z infuzní soupravy tak, že natáhnete roztok zpět do injekční stříkačky. Rozpuštěný přípravek musí být podán intravenózně během několika minut. Lékař může změnit rychlost infuze tak, aby to bylo pro Vás pohodlnější. Veškerý nespotřebovaný roztok, prázdné injekční lahvičky a použité jehly a stříkačky vyhoďte do vhodného kontejneru mimo zdravotnický odpad, protože tyto materiály by mohly při neopatrné likvidaci někoho poranit. Jestliže jste užil(a) více přípravku ReFacto AF než jste měl(a) Poraďte se s lékařem nebo lékárníkem. Jestliže jste přestal(a) užívat ReFacto AF Nepřerušujte podávání přípravku ReFacto AF, aniž byste se předem poradil(a) se svým lékařem. Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka. 4. Možné nežádoucí účinky Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Alergické reakce Pokud se náhle vyskytnou závažné alergické (anafylaktické) reakce, musí se infuze ihned přerušit. Pokud máte některý z následujících časných příznaků alergických reakcí, musíte ihned informovat svého lékaře: vyrážka, kopřivka, místní otok kůže, celkové svědění otok rtů a jazyka problémy s dýcháním, sípot, tíha na hrudi celkový pocit nemoci závratě a ztráta vědomí Závažné příznaky zahrnující problémy s dýcháním a (téměř) mdloby vyžadují neodkladnou léčbu. Závažné náhlé alergické (anafylaktické) reakce jsou méně časté (postihují až 1 ze 100 pacientů). Vytvoření inhibitorů U pacientů s hemofilií A se mohou vyvinout neutralizační protilátky (inhibitory) proti faktoru VIII. Pokud se takové inhibitory vyskytnou, mohou se projevit zvýšeným množstvím přípravku ReFacto AF typicky potřebným k léčbě krvácení a/nebo pokračujícím krvácením po léčbě. V takových případech se doporučuje kontaktovat specializované centrum pro hemofiliky. Lékař může požadovat sledování 6
7 možného vyvinutí inhibitoru. V klinických studiích došlo k vyvinutí inhibitorů přibližně u 2% pacientů léčených přípravkem ReFacto AF. Velmi časté nežádoucí účinky (postihují více než 1 z 10 pacientů) zvracení vývoj inhibitorů u pacientů, kteří nikdy předtím nebyli léčeni přípravky obsahujícími faktor VIII Některé krevní testy mohou ukázat zvýšení hladiny bílkovin (protilátek) produkovaných proti ovariálním buňkám čínského křečka (buňky používané k produkci rekombinantního faktoru VIII v přípravku ReFacto AF) a faktoru VIII. Avšak u těchto proteinů není známo, zda působí na klinickou účinnost nebo zda vyvolávají nějaké účinky. Časté nežádoucí účinky (postihují až 1 z 10 pacientů) krvácení vývoj inhibitorů u pacientů, kteří již byli léčeni přípravky obsahujícími faktor VIII bolest hlavy, pocit na zvracení bolest kloubů, bolest svalů únava, horečka komplikace cévního přístupu u katetrizovaných cév včetně komplikace trvalého cévního přístupu u katetrizovaných cév Méně časté nežádoucí účinky (postihují až 1 ze 100 pacientů) závažné alergické reakce, závratě, pocit na omdlení, kopřivka, svědění, vyrážka, zrudnutí bolest na hrudi, dušnost, zrychlený srdeční rytmus průjem, ztráta chuti k jídlu, bolest břicha změny chuti zimnice, pocení, svalová slabost spavost kašel reakce v místě injekce (jako pálení a bodavý pocit v místě injekce), nepříjemné pocity a otok v místě vpichu do žíly mírné zvýšení hladin srdečních enzymů zvýšení hladin jaterních enzymů, zvýšení hladiny bilirubinu Hlášení nežádoucích účinků Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova Praha 10 Webové stránky: Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku. 5. Jak přípravek ReFacto AF uchovávat Uchovávejte tento přípravek mimo dohled a dosah dětí. 7
8 Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a štítku lahvičky za EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Uchovávejte a přepravujte chlazené (2 C 8 C). Chraňte před mrazem, aby se předešlo poškození předplněné injekční stříkačky s rozpouštědlem. Pro Vaše pohodlí je možno léčivý přípravek vyjmout z chladničky na jediné období trvající maximálně 3 měsíce a uchovávat při pokojové teplotě (do 25 C). Po uplynutí tohoto období uchovávání při pokojové teplotě se přípravek nesmí vrátit do chladničky, ale musí se spotřebovat, či zlikvidovat. Na krabičce si zaznamenejte datum, kdy byl přípravek ReFacto AF vyjmut z chladničky a uchováván při pokojové teplotě (do 25 C). Uchovávejte lahvičku ve vnější krabičce, aby byl přípravek chráněn před světlem. Rozpuštěný přípravek použijte nejpozději do 3 hodin od rozpuštění. Přípravek je bezbarvý a čirý až mírně opalescentní. Nepoužívejte tento přípravek, pokud zjistíte, že je roztok zakalený nebo obsahuje viditelné částice. Nevyhazujte žádné léčivé přípravky do odpadních vod nebo do domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí. 6. Obsah balení a další informace Co přípravek ReFacto AF obsahuje - Léčivou látkou je moroctocogum alfa (rekombinantní koagulační faktor VIII). Jedna injekční lahvička ReFacto AF obsahuje moroctocogum alfa 250, 500, 1000, nebo 2000 IU. - Pomocnými látkami jsou sacharosa, dihydrát chloridu vápenatého, histidin, polysorbát 80 a chlorid sodný. Přiloženo je také rozpouštědlo k rozpuštění [roztok chloridu sodného 9mg/ml (0,9%) na injekci]. - Po rozpuštění dodaným rozpouštědlem [roztok chloridu sodného 9mg/ml (0,9%)] jedna injekční lahvička připraveného injekčního roztoku obsahuje 62,5; 125; 250 nebo 500 IU moroctocogum alfa (podle síly moroctocogum alfa, tj. 250, 500, 1000, nebo 2000 IU). Jak přípravek ReFacto AF vypadá a co obsahuje toto balení Přípravek ReFacto AF se dodává jako prášek na injekci ve skleněné injekční lahvičce a s rozpouštědlem v předplněné injekční stříkačce. Obsahem balení je: - jedna injekční lahvička s práškem moroctocogum alfa 250, 500, 1000, nebo 2000 IU - jedna předplněná injekční stříkačka s rozpouštědlem, 4 ml sterilního roztoku chloridu sodného 9 mg/ml (0,9%) k rozpuštění, s táhlem a pístem - jeden sterilní adaptér lahvičky - jedna sterilní infuzní souprava - dva alkoholové tampony - jedna náplast - jeden gázový polštářek 8
9 Držitel rozhodnutí o registraci Pfizer Limited Ramsgate Road Sandwich Kent CT13 9NJ Velká Británie Výrobce Wyeth Farma S.A Autovia del Norte A-1 Km 23 Desvio Algete Km San Sebastian de los Reyes Madrid Španělsko Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci. 9
10 België /Belgique / Belgien Pfizer S.A./N.V. Tél/Tel: +32 (0) България Пфайзер Люксембург САРЛ, Клон България Тел.: Česká republika Pfizer s.r.o. Tel: Danmark Pfizer ApS Tlf: Deutschland Pfizer Pharma GmbH Tel: +49 (0) Eesti Pfizer Luxembourg SARL Eesti filiaal Tel: Ελλάδα PFIZER ΕΛΛΑΣ Α.Ε Τηλ: España Pfizer S.L. Tel: France Pfizer Tél: +33 (0) Hrvatska Pfizer Croatia d.o.o. Tel: Ireland Pfizer Healthcare Ireland Tel: (toll free) +44 (0) Ísland Icepharma hf. Sími: Lietuva Pfizer Luxembourg SARL filialas Lietuvoje Tel Luxembourg/Luxemburg Pfizer S.A. Tél/Tel: +32 (0) Magyarország Pfizer Kft. Tel.: Malta Vivian Corporation Ltd. Tel: Nederland Pfizer bv Tel: +31 (0) Norge Pfizer AS Tlf: Österreich Pfizer Corporation Austria Ges.m.b.H. Tel: +43 (0) Polska Pfizer Polska Sp. z o.o., Tel.: Portugal Pfizer Biofarmacêutica, Sociedade Unipessoal Lda Tel: România Pfizer România S.R.L. Tel: Slovenija Pfizer Luxembourg SARL Pfizer, podružnica za svetovanje s področja farmacevtske dejavnosti, Ljubljana Tel: (0) Slovenská republika Pfizer Luxembourg SARL, organizačná zložka Tel:
11 Italia Pfizer S.r.l. Tel: Κύπρος PFIZER ΕΛΛΑΣ A.E. (CYPRUS BRANCH) Τηλ: Latvija Pfizer Luxembourg SARL filiāle Latvijā Tel: Suomi/Finland Pfizer Oy Puh/Tel: +358 (0) Sverige Pfizer AB Tel: + 46 (0) United Kingdom Pfizer Limited Tel: +44 (0) Tato příbalová informace byla naposledy revidována 06/2015 Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky 11
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: Informace pro pacienta
 Příbalová informace: Informace pro pacienta CONBRIZA 20 mg potahované tablety Bazedoxifenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: Informace pro pacienta CONBRIZA 20 mg potahované tablety Bazedoxifenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta. Azomyr 0,5 mg/ml perorální roztok desloratadinum
 Příbalová informace: informace pro pacienta Azomyr 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta Azomyr 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta. Zurampic 200 mg potahované tablety lesinuradum
 Příbalová informace: informace pro pacienta Zurampic 200 mg potahované tablety lesinuradum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro pacienta Zurampic 200 mg potahované tablety lesinuradum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro pacienta. Integrilin 0,75 mg/ml infuzní roztok eptifibatidum
 Příbalová informace: informace pro pacienta Integrilin 0,75 mg/ml infuzní roztok eptifibatidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro pacienta Integrilin 0,75 mg/ml infuzní roztok eptifibatidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje důležité
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje důležité
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bonviva 3 mg injekční roztok Acidum ibandronicum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bonviva 3 mg injekční roztok Acidum ibandronicum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bonviva 3 mg injekční roztok Acidum ibandronicum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE. Příbalová informace: Informace pro uživatele
 PŘÍBALOVÁ INFORMACE Příbalová informace: Informace pro uživatele ReFacto AF 250 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 500 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 1000
PŘÍBALOVÁ INFORMACE Příbalová informace: Informace pro uživatele ReFacto AF 250 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 500 IU prášek a rozpouštědlo pro injekční roztok ReFacto AF 1000
Zvláštní opatrnosti při použití KOGENATE Bayer 250 IU je zapotřebí
 Příbalová informace: informace pro uživatele KOGENATE Bayer 250 IU Prášek a rozpouštědlo pro injekční roztok Rekombinantní koagulační faktor VIII (octocogum alfa) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele KOGENATE Bayer 250 IU Prášek a rozpouštědlo pro injekční roztok Rekombinantní koagulační faktor VIII (octocogum alfa) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Gardasil 9 injekční suspenze v předplněné injekční stříkačce 9valentní očkovací látka proti lidskému papilomaviru (rekombinantní, adsorbovaná) Tento přípravek
Příbalová informace: informace pro uživatele Gardasil 9 injekční suspenze v předplněné injekční stříkačce 9valentní očkovací látka proti lidskému papilomaviru (rekombinantní, adsorbovaná) Tento přípravek
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele CELVAPAN injekční suspenze Vakcína proti chřipce (H1N1)v (celý virion, namnožená na buňkách Vero, inaktivovaná) Přečtěte si pozorně
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele CELVAPAN injekční suspenze Vakcína proti chřipce (H1N1)v (celý virion, namnožená na buňkách Vero, inaktivovaná) Přečtěte si pozorně
Příbalová informace: informace pro pacienta. TAGRISSO 40 mg potahované tablety TAGRISSO 80 mg potahované tablety osimertinibum
 Příbalová informace: informace pro pacienta TAGRISSO 40 mg potahované tablety TAGRISSO 80 mg potahované tablety osimertinibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro pacienta TAGRISSO 40 mg potahované tablety TAGRISSO 80 mg potahované tablety osimertinibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Betaserc 24 tablety Betahistini dihydrochloridum
 sp.zn. sukls142274/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Betaserc 24 tablety Betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls142274/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Betaserc 24 tablety Betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: informace pro pacienta. Lyrica 20 mg/ml perorální roztok pregabalinum
 Příbalová informace: informace pro pacienta Lyrica 20 mg/ml perorální roztok pregabalinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta Lyrica 20 mg/ml perorální roztok pregabalinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Kovaltry 250 IU prášek a rozpouštědlo pro injekční roztok Kovaltry 500 IU prášek a rozpouštědlo pro injekční roztok Kovaltry 1000 IU prášek a rozpouštědlo pro
Příbalová informace: informace pro uživatele Kovaltry 250 IU prášek a rozpouštědlo pro injekční roztok Kovaltry 500 IU prášek a rozpouštědlo pro injekční roztok Kovaltry 1000 IU prášek a rozpouštědlo pro
Příbalová informace: informace pro pacienta. Ristaben 50 mg potahované tablety Sitagliptinum
 Příbalová informace: informace pro pacienta Ristaben 50 mg potahované tablety Sitagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta Ristaben 50 mg potahované tablety Sitagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 35 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Menveo prášek a roztok pro přípravu injekčního roztoku Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si
B. PŘÍBALOVÁ INFORMACE 35 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Menveo prášek a roztok pro přípravu injekčního roztoku Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si
Příbalová informace: Informace pro uživatele. Sclefic 50 mg potahované tablety riluzolum
 sp.zn. sukls94414/2013 Příbalová informace: Informace pro uživatele Sclefic 50 mg potahované tablety riluzolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls94414/2013 Příbalová informace: Informace pro uživatele Sclefic 50 mg potahované tablety riluzolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: Informace pro uživatele
 Příbalová informace: Informace pro uživatele Adempas 0,5 mg potahované tablety Adempas 1 mg potahované tablety Adempas 1,5 mg potahované tablety Adempas 2 mg potahované tablety Adempas 2,5 mg potahované
Příbalová informace: Informace pro uživatele Adempas 0,5 mg potahované tablety Adempas 1 mg potahované tablety Adempas 1,5 mg potahované tablety Adempas 2 mg potahované tablety Adempas 2,5 mg potahované
- jestliže jste alergický/á na sildenafil nebo na kteroukoliv další složku tohoto přípravku (uvedenou v bodě 6).
 Příbalová informace: informace pro pacienta Revatio 10 mg/ml prášek pro přípravu perorální suspenze sildenafilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: informace pro pacienta Revatio 10 mg/ml prášek pro přípravu perorální suspenze sildenafilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE. OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas
 PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Baraclude 0,05 mg/ml perorální roztok entecavirum
 Příbalová informace: informace pro uživatele Baraclude 0,05 mg/ml perorální roztok entecavirum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatele Baraclude 0,05 mg/ml perorální roztok entecavirum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro pacienta
 Příbalová informace: informace pro pacienta Briviact 10 mg potahované tablety Briviact 25 mg potahované tablety Briviact 50 mg potahované tablety Briviact 75 mg potahované tablety Briviact 100 mg potahované
Příbalová informace: informace pro pacienta Briviact 10 mg potahované tablety Briviact 25 mg potahované tablety Briviact 50 mg potahované tablety Briviact 75 mg potahované tablety Briviact 100 mg potahované
Příbalová informace: informace pro pacienta. Altargo 10 mg/g mast. Retapamulinum
 Příbalová informace: informace pro pacienta Altargo 10 mg/g mast Retapamulinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité
Příbalová informace: informace pro pacienta Altargo 10 mg/g mast Retapamulinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité
Příbalová informace: informace pro uživatele. Ferriprox 500 mg potahované tablety Deferipronum
 Příbalová informace: informace pro uživatele Ferriprox 500 mg potahované tablety Deferipronum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatele Ferriprox 500 mg potahované tablety Deferipronum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek užívat, protože obsahuje
PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Mimpara 30 mg potahované tablety Mimpara 60 mg potahované tablety Mimpara 90 mg potahované tablety Cinacalceti hydrochloridum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gardasil, injekční suspenze Vakcína proti lidskému papilomaviru [typy 6, 11, 16, 18] (rekombinantní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gardasil, injekční suspenze Vakcína proti lidskému papilomaviru [typy 6, 11, 16, 18] (rekombinantní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE LYRICA 25 tvrdé tobolky LYRICA 50 tvrdé tobolky LYRICA 75 tvrdé tobolky LYRICA 100 tvrdé tobolky LYRICA 150 tvrdé tobolky LYRICA 200 tvrdé tobolky LYRICA 225
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE LYRICA 25 tvrdé tobolky LYRICA 50 tvrdé tobolky LYRICA 75 tvrdé tobolky LYRICA 100 tvrdé tobolky LYRICA 150 tvrdé tobolky LYRICA 200 tvrdé tobolky LYRICA 225
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Relistor 12 mg/0,6 ml injekční roztok Methylnaltrexonii bromidum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Relistor 12 mg/0,6 ml injekční roztok Methylnaltrexonii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Relistor 12 mg/0,6 ml injekční roztok Methylnaltrexonii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
Pomocné látky: natrium-kalcium-edetát trometamol-hydrochlorid trometamol roztok hydroxidu sodného 1mol/l kyselina chlorovodíková 25% voda na injekci
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Vnější obal 20ml/ 50ml/ 60ml/ 100ml/ 150ml/ 200ml/ 500ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU XENETIX 300 300 mgi/ml Iobitridolum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Iobitridolum
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Vnější obal 20ml/ 50ml/ 60ml/ 100ml/ 150ml/ 200ml/ 500ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU XENETIX 300 300 mgi/ml Iobitridolum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Iobitridolum
Příbalová informace: informace pro pacienta. KEYTRUDA 50 mg prášek pro koncentrát pro infuzní roztok pembrolizumabum
 Příbalová informace: informace pro pacienta KEYTRUDA 50 mg prášek pro koncentrát pro infuzní roztok pembrolizumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: informace pro pacienta KEYTRUDA 50 mg prášek pro koncentrát pro infuzní roztok pembrolizumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Sp.zn.sukls74932/2014 Příbalová informace: informace pro uživatele. Desloratadin STADA 5 mg potahované tablety desloratadinum
 Sp.zn.sukls74932/2014 Příbalová informace: informace pro uživatele Desloratadin STADA 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp.zn.sukls74932/2014 Příbalová informace: informace pro uživatele Desloratadin STADA 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace Informace pro uživatele
 Příbalová informace Informace pro uživatele Trobalt 50 mg potahované tablety Trobalt 100 mg potahované tablety Trobalt 200 mg potahované tablety Trobalt 300 mg potahované tablety Trobalt 400 mg potahované
Příbalová informace Informace pro uživatele Trobalt 50 mg potahované tablety Trobalt 100 mg potahované tablety Trobalt 200 mg potahované tablety Trobalt 300 mg potahované tablety Trobalt 400 mg potahované
Příbalová informace: Informace pro uživatele. Ebixa 5 mg/dávka, perorální roztok Memantini hydrochloridum
 Příbalová informace: Informace pro uživatele Ebixa 5 mg/dávka, perorální roztok Memantini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: Informace pro uživatele Ebixa 5 mg/dávka, perorální roztok Memantini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Eliquis 2,5 mg potahované tablety Apixabanum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Eliquis 2,5 mg potahované tablety Apixabanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Eliquis 2,5 mg potahované tablety Apixabanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE. Galvus 50 mg tablety Vildagliptinum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE Galvus 50 mg tablety Vildagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, neţ začnete tento přípravek uţívat. - Ponechte si příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE Galvus 50 mg tablety Vildagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, neţ začnete tento přípravek uţívat. - Ponechte si příbalovou informaci
Příbalová informace: informace pro pacienta. Forxiga 5 mg potahované tablety Forxiga 10 mg potahované tablety dapagliflozinum
 Příbalová informace: informace pro pacienta Forxiga 5 mg potahované tablety Forxiga 10 mg potahované tablety dapagliflozinum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: informace pro pacienta Forxiga 5 mg potahované tablety Forxiga 10 mg potahované tablety dapagliflozinum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: Informace pro uživatele
 Příbalová informace: Informace pro uživatele ReFacto AF 250 IU prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce ReFacto AF 500 IU prášek a rozpouštědlo pro injekční roztok v předplněné
Příbalová informace: Informace pro uživatele ReFacto AF 250 IU prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce ReFacto AF 500 IU prášek a rozpouštědlo pro injekční roztok v předplněné
Příbalová informace: Informace pro uživatele
 Příbalová informace: Informace pro uživatele ReFacto AF 250 IU prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce ReFacto AF 500 IU prášek a rozpouštědlo pro injekční roztok v předplněné
Příbalová informace: Informace pro uživatele ReFacto AF 250 IU prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce ReFacto AF 500 IU prášek a rozpouštědlo pro injekční roztok v předplněné
Příbalová informace: informace pro pacienta. Panadol Baby čípky paracetamolum čípky
 sp. zn. sukls29099/2016 Příbalová informace: informace pro pacienta Panadol Baby čípky paracetamolum čípky Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp. zn. sukls29099/2016 Příbalová informace: informace pro pacienta Panadol Baby čípky paracetamolum čípky Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Menveo prášek a roztok pro injekční roztok Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele Menveo prášek a roztok pro injekční roztok Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele. Vizarsin 25 mg tablety dispergovatelné v ústech Sildenafilum
 Příbalová informace: informace pro uživatele Vizarsin 25 mg tablety dispergovatelné v ústech Sildenafilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro uživatele Vizarsin 25 mg tablety dispergovatelné v ústech Sildenafilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Anbinex 50 IU/ml, prášek a rozpouštědlo pro injekční roztok Antithrombinum III
 sp.zn. sukls43174/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Anbinex 50 IU/ml, prášek a rozpouštědlo pro injekční roztok Antithrombinum III Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls43174/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Anbinex 50 IU/ml, prášek a rozpouštědlo pro injekční roztok Antithrombinum III Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha č. 2 k rozhodnutí o nové registraci sp.zn.sukls219594/2010, sukls219596/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 2 k rozhodnutí o nové registraci sp.zn.sukls219594/2010, sukls219596/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Wilate 500, 500 IU FVIII/500 IU VWF, prášek pro přípravu injekčního roztoku
Příloha č. 2 k rozhodnutí o nové registraci sp.zn.sukls219594/2010, sukls219596/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Wilate 500, 500 IU FVIII/500 IU VWF, prášek pro přípravu injekčního roztoku
Příbalová informace: informace pro pacienta. Levoftamid 5 mg/ml, oční kapky, roztok Levofloxacinum hemihydricum
 Sp. zn. sukls178097/2014 Příbalová informace: informace pro pacienta Levoftamid 5 mg/ml, oční kapky, roztok Levofloxacinum hemihydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Sp. zn. sukls178097/2014 Příbalová informace: informace pro pacienta Levoftamid 5 mg/ml, oční kapky, roztok Levofloxacinum hemihydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro pacienta
 Příbalová informace: informace pro pacienta Trumenba injekční suspenze v předplněné injekční stříkačce Vakcína proti meningokokům skupiny B (rekombinantní, adsorbovaná) Tento přípravek podléhá dalšímu
Příbalová informace: informace pro pacienta Trumenba injekční suspenze v předplněné injekční stříkačce Vakcína proti meningokokům skupiny B (rekombinantní, adsorbovaná) Tento přípravek podléhá dalšímu
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE. Raloxifen Teva 60 mg potahované tablety Raloxifeni hydrochloridum
 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Raloxifen Teva 60 mg potahované tablety Raloxifeni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Raloxifen Teva 60 mg potahované tablety Raloxifeni hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat.
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE. TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum
 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. JEVTANA 60 mg koncentrát pro přípravu infuzního roztoku s rozpouštědlem kabazitaxelum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE JEVTANA 60 mg koncentrát pro přípravu infuzního roztoku s rozpouštědlem kabazitaxelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE JEVTANA 60 mg koncentrát pro přípravu infuzního roztoku s rozpouštědlem kabazitaxelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 55 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cervarix injekční suspenze Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná) Přečtěte si
B. PŘÍBALOVÁ INFORMACE 55 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cervarix injekční suspenze Vakcína proti lidskému papilomaviru [typy 16, 18] (rekombinantní, adjuvovaná, adsorbovaná) Přečtěte si
Příbalová informace: informace pro uživatele. Febichol 100 mg měkké tobolky (fenipentolum)
 sp.zn.: sukls41365/2009 Příbalová informace: informace pro uživatele Febichol 100 mg měkké tobolky (fenipentolum) Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn.: sukls41365/2009 Příbalová informace: informace pro uživatele Febichol 100 mg měkké tobolky (fenipentolum) Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat,
Voda na injekci, hydrogenuhličitan sodný, hydroxid sodný, kyselina chlorovodíková
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU (KARTONOVÁ KRABICE) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU balance 2,3% glucose, 1,75 mmol/l calcium 2. OBSAH LÉČIVÝCH LÁTEK 1 litr roztoku připraveného k použití obsahuje: Natrii chloridum
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU (KARTONOVÁ KRABICE) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU balance 2,3% glucose, 1,75 mmol/l calcium 2. OBSAH LÉČIVÝCH LÁTEK 1 litr roztoku připraveného k použití obsahuje: Natrii chloridum
PŘÍBALOVÁ INFORMACE. EMADINE 0,5 mg/ml, Oční Kapky, roztok. Emedastinum
 PŘÍBALOVÁ INFORMACE EMADINE 0,5 mg/ml, Oční Kapky, roztok. Emedastinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou informaci.pro případ,
PŘÍBALOVÁ INFORMACE EMADINE 0,5 mg/ml, Oční Kapky, roztok. Emedastinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou informaci.pro případ,
Příbalová informace: informace pro pacienta. Brintellix 10 mg potahované tablety Vortioxetinum
 Příbalová informace: informace pro pacienta Brintellix 10 mg potahované tablety Vortioxetinum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete
Příbalová informace: informace pro pacienta Brintellix 10 mg potahované tablety Vortioxetinum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Protopic 0,03% mast Tacrolimusum monohydricum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Protopic 0,03% mast Tacrolimusum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Protopic 0,03% mast Tacrolimusum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
Příbalová informace: Informace pro pacienta
 Sp.zn.sukls112683/2014 Příbalová informace: Informace pro pacienta Betahistin-ratiopharm 16 mg tablety (betahistini dihydrochloridum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls112683/2014 Příbalová informace: Informace pro pacienta Betahistin-ratiopharm 16 mg tablety (betahistini dihydrochloridum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. Cezera 5 mg potahované tablety levocetirizini dihydrochloridum
 Sp.zn.sukls125653/2015 Příbalová informace: informace pro uživatele Cezera 5 mg potahované tablety levocetirizini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls125653/2015 Příbalová informace: informace pro uživatele Cezera 5 mg potahované tablety levocetirizini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: Informace pro pacienta
 Sp.zn.sukls55678/2015 Příbalová informace: Informace pro pacienta Flonidan 10 mg DISTAB Tableta dispergovatelná v ústech loratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls55678/2015 Příbalová informace: Informace pro pacienta Flonidan 10 mg DISTAB Tableta dispergovatelná v ústech loratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. Adriblastina CS injekční roztok 2 mg/ml doxorubicini hydrochloridum
 Příbalová informace: informace pro uživatele Adriblastina CS injekční roztok 2 mg/ml doxorubicini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro uživatele Adriblastina CS injekční roztok 2 mg/ml doxorubicini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: Informace pro uživatele
 Příbalová informace: Informace pro uživatele Immunate Stim Plus 1000 IU FVIII/750 IU VWF Prášek a rozpouštědlo pro injekční roztok Léčivé látky: Factor VIII coagulationis humanus/ Factor von Willebrand
Příbalová informace: Informace pro uživatele Immunate Stim Plus 1000 IU FVIII/750 IU VWF Prášek a rozpouštědlo pro injekční roztok Léčivé látky: Factor VIII coagulationis humanus/ Factor von Willebrand
Příbalová informace: informace pro uživatele. Temodal 2,5 mg/ml prášek pro infuzní roztok temozolomidum
 Příbalová informace: informace pro uživatele Temodal 2,5 mg/ml prášek pro infuzní roztok temozolomidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pro uživatele Temodal 2,5 mg/ml prášek pro infuzní roztok temozolomidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele INVANZ 1 g prášek pro přípravu koncentrátu pro přípravu infuzního roztoku ertapenemum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek
Příbalová informace: informace pro uživatele INVANZ 1 g prášek pro přípravu koncentrátu pro přípravu infuzního roztoku ertapenemum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele Prolia 60 mg injekční roztok v předplněné injekční stříkačce denosumabum Přečtěte si pozorně celou příbalovou informaci dříve, než
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele Prolia 60 mg injekční roztok v předplněné injekční stříkačce denosumabum Přečtěte si pozorně celou příbalovou informaci dříve, než
Příbalová informace: informace pro uživatele. Bretaris Genuair 322 mikrogramů, prášek k inhalaci Aclidinium (aclidinii bromidum)
 Příbalová informace: informace pro uživatele Bretaris Genuair 322 mikrogramů, prášek k inhalaci Aclidinium (aclidinii bromidum) Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro uživatele Bretaris Genuair 322 mikrogramů, prášek k inhalaci Aclidinium (aclidinii bromidum) Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro uživatele. Ovitrelle 250 mikrogramů, injekční roztok v předplněném peru Choriogonadotropin alfa
 Příbalová informace: informace pro uživatele Ovitrelle 250 mikrogramů, injekční roztok v předplněném peru Choriogonadotropin alfa Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele Ovitrelle 250 mikrogramů, injekční roztok v předplněném peru Choriogonadotropin alfa Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Canifug-Lösung 1%
 sp.zn. :sukls129584/2012 a sp.zn.:sukls 130459/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Canifug-Lösung 1% Kožní sprej, roztok (Clotrimazolum) Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. :sukls129584/2012 a sp.zn.:sukls 130459/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Canifug-Lösung 1% Kožní sprej, roztok (Clotrimazolum) Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro pacienta. Zinforo 600 mg prášek pro koncentrát pro infuzní roztok ceftarolinum fosamilum
 Příbalová informace: informace pro pacienta Zinforo 600 mg prášek pro koncentrát pro infuzní roztok ceftarolinum fosamilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro pacienta Zinforo 600 mg prášek pro koncentrát pro infuzní roztok ceftarolinum fosamilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Zyllt 75 mg potahované tablety Clopidogrelum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Zyllt 75 mg potahované tablety Clopidogrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Zyllt 75 mg potahované tablety Clopidogrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechte si příbalovou
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA na HDPE lahvičky 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna potahovaná tableta obsahuje 10 mg (jako calcicum trihydricum). Jedna potahovaná tableta obsahuje 20 mg
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA na HDPE lahvičky 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna potahovaná tableta obsahuje 10 mg (jako calcicum trihydricum). Jedna potahovaná tableta obsahuje 20 mg
Příbalová informace: Informace pro uživatele
 Příbalová informace: Informace pro uživatele Flolan 0,5 mg, prášek a rozpouštědlo pro infuzní roztok Flolan 1,5 mg, prášek a rozpouštědlo pro infuzní roztok Epoprostenolum Přečtěte si pozorně celou příbalovou
Příbalová informace: Informace pro uživatele Flolan 0,5 mg, prášek a rozpouštědlo pro infuzní roztok Flolan 1,5 mg, prášek a rozpouštědlo pro infuzní roztok Epoprostenolum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele. Benepali 50 mg, injekční roztok v předplněném peru etanerceptum
 Příbalová informace: informace pro uživatele Benepali 50 mg, injekční roztok v předplněném peru etanerceptum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro uživatele Benepali 50 mg, injekční roztok v předplněném peru etanerceptum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Dracenax 2,5 mg Letrozolum potahované tablety
 Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls172883/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dracenax 2,5 mg Letrozolum potahované tablety Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls172883/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dracenax 2,5 mg Letrozolum potahované tablety Přečtěte si pozorně celou příbalovou informaci
Vlastnosti přípravku, příprava a podání Návod k přípravku NovoThirteen
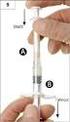 Vlastnosti přípravku, příprava a podání Návod k přípravku NovoThirteen NovoThirteen : rekombinantní léčba vrozeného nedostatku podjednotky A faktoru XIII Před použitím přípravku NovoThirteen je důležité
Vlastnosti přípravku, příprava a podání Návod k přípravku NovoThirteen NovoThirteen : rekombinantní léčba vrozeného nedostatku podjednotky A faktoru XIII Před použitím přípravku NovoThirteen je důležité
Příbalová informace: informace pro pacienta. Acetylcystein Saneca 600 mg šumivé tablety acetylcysteinum
 Sp.zn.sukls32697/2015 Příbalová informace: informace pro pacienta Acetylcystein Saneca 600 mg šumivé tablety acetylcysteinum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
Sp.zn.sukls32697/2015 Příbalová informace: informace pro pacienta Acetylcystein Saneca 600 mg šumivé tablety acetylcysteinum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
BIOVISC ORTHO SINGLE
 Česky BIOVISC ORTHO SINGLE Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová 30 mg Fosfátem pufrovaný fyziologický
Česky BIOVISC ORTHO SINGLE Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová 30 mg Fosfátem pufrovaný fyziologický
Příbalová informace: informace pro uživatele. Vyndaqel 20 mg měkké tobolky tafamidisum
 Příbalová informace: informace pro uživatele Vyndaqel 20 mg měkké tobolky tafamidisum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro uživatele Vyndaqel 20 mg měkké tobolky tafamidisum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příloha č. 1 k opravě sdělení sp.zn. sukls226519/2009. PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE PARALEN 500 tablety Paracetamolum
 Příloha č. 1 k opravě sdělení sp.zn. sukls226519/2009 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE PARALEN 500 tablety Paracetamolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příloha č. 1 k opravě sdělení sp.zn. sukls226519/2009 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE PARALEN 500 tablety Paracetamolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Kyprolis 60 mg prášek pro infuzní roztok carfilzomibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Kyprolis 60 mg prášek pro infuzní roztok carfilzomibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Příbalová informace: informace pro uživatele Engerix-B 20 µg. antigenum tegiminis hepatitidis B injekční suspenze
 sp.zn. sukls204563/2014 Příbalová informace: informace pro uživatele Engerix-B 10 µg Engerix-B 20 µg antigenum tegiminis hepatitidis B injekční suspenze Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls204563/2014 Příbalová informace: informace pro uživatele Engerix-B 10 µg Engerix-B 20 µg antigenum tegiminis hepatitidis B injekční suspenze Přečtěte si pozorně celou příbalovou informaci dříve,
1. CO JE PŘÍPRAVEK OFTAQUIX OČNÍ KAPKY A K ČEMU SE POUŽÍVÁ
 Příloha č. 2 k rozhodnutí o prodloužení registrace č.j. sukls1207/2006 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Oftaquix 5 mg/ml oční kapky Levofloxacinum Přečtěte si, prosím, pozorně celou příbalovou
Příloha č. 2 k rozhodnutí o prodloužení registrace č.j. sukls1207/2006 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Oftaquix 5 mg/ml oční kapky Levofloxacinum Přečtěte si, prosím, pozorně celou příbalovou
Příbalová informace: informace pro uživatele
 sp.zn.: sukls236606/2012 Příbalová informace: informace pro uživatele MENJUGATE, prášek a rozpouštědlo pro injekční suspenzi Konjugovaná oligosacharidová vakcína proti meningitidě C Přečtěte si pozorně
sp.zn.: sukls236606/2012 Příbalová informace: informace pro uživatele MENJUGATE, prášek a rozpouštědlo pro injekční suspenzi Konjugovaná oligosacharidová vakcína proti meningitidě C Přečtěte si pozorně
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 2 k rozhodnutí o registraci sp. zn. sukls153370-72/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gemtex 200 mg, prášek pro přípravu infuzního roztoku Gemtex 1 000 mg, prášek pro přípravu
Příloha č. 2 k rozhodnutí o registraci sp. zn. sukls153370-72/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gemtex 200 mg, prášek pro přípravu infuzního roztoku Gemtex 1 000 mg, prášek pro přípravu
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU. Krabička pro PVC-Al blistry a HDPE lahvičky 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU. Pregabalin Archie Samuel 150 mg tvrdé tobolky
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička pro PVC-Al blistry a 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Pregabalin Archie Samuel 25 mg tvrdé tobolky Pregabalin Archie Samuel 50 mg tvrdé tobolky Pregabalin Archie Samuel
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička pro PVC-Al blistry a 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Pregabalin Archie Samuel 25 mg tvrdé tobolky Pregabalin Archie Samuel 50 mg tvrdé tobolky Pregabalin Archie Samuel
Příbalová informace: informace pro uživatele. Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum
 Příbalová informace: informace pro uživatele Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: Informace pro uživatele. Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná)
 Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: Informace pro uživatele Prevenar 13 injekční suspenze Pneumokoková polysacharidová konjugovaná vakcína (13valentní, adsorbovaná) Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE 22
 PŘÍBALOVÁ INFORMACE 22 Příbalová informace: Informace pro uživatele VELETRI 0,5 mg prášek pro infuzní roztok VELETRI 1,5 mg prášek pro infuzní roztok Epoprostenolum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE 22 Příbalová informace: Informace pro uživatele VELETRI 0,5 mg prášek pro infuzní roztok VELETRI 1,5 mg prášek pro infuzní roztok Epoprostenolum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele. GUTTALAX 7,5 mg, perorální kapky, roztok natrii picosulfas
 sp.zn. sukls115768/2009 a sp.zn. sukls226721/2015 Příbalová informace: informace pro uživatele GUTTALAX 7,5 mg, perorální kapky, roztok natrii picosulfas Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls115768/2009 a sp.zn. sukls226721/2015 Příbalová informace: informace pro uživatele GUTTALAX 7,5 mg, perorální kapky, roztok natrii picosulfas Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele. Nimbex Injekční roztok Cisatracurii besilas
 Příbalová informace: informace pro uživatele Nimbex Injekční roztok Cisatracurii besilas Přečtěte si pozorně celou příbalovou informaci dříve, než vám bude tento přípravek podán, protože obsahuje pro Vás
Příbalová informace: informace pro uživatele Nimbex Injekční roztok Cisatracurii besilas Přečtěte si pozorně celou příbalovou informaci dříve, než vám bude tento přípravek podán, protože obsahuje pro Vás
Příloha č. 2 k rozhodnutí o převodu registrace sp.zn.sukls156759/2010
 Příloha č. 2 k rozhodnutí o převodu registrace sp.zn.sukls156759/2010 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Pantoprazol Pliva 40 mg I.V. prášek pro přípravu injekčního roztoku Pantoprazolum Přečtete
Příloha č. 2 k rozhodnutí o převodu registrace sp.zn.sukls156759/2010 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE Pantoprazol Pliva 40 mg I.V. prášek pro přípravu injekčního roztoku Pantoprazolum Přečtete
Příbalová informace: informace pro pacienta. Fredomat 40 mikrogramů/ml oční kapky, roztok. travoprostum
 sp.zn.sukls190238/2015 Příbalová informace: informace pro pacienta Fredomat 40 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls190238/2015 Příbalová informace: informace pro pacienta Fredomat 40 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Elmetacin 1% kožní sprej, roztok Indometacinum
 sp.zn. sukls148976/2012 Příbalová informace: informace pro uživatele Elmetacin 1% kožní sprej, roztok Indometacinum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn. sukls148976/2012 Příbalová informace: informace pro uživatele Elmetacin 1% kožní sprej, roztok Indometacinum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn. sukls110147/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA SOMATULINE AUTOGEL 60 mg, injekční roztok v předplněné stříkačce SOMATULINE AUTOGEL 90 mg, injekční roztok v předplněné stříkačce SOMATULINE
sp.zn. sukls110147/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA SOMATULINE AUTOGEL 60 mg, injekční roztok v předplněné stříkačce SOMATULINE AUTOGEL 90 mg, injekční roztok v předplněné stříkačce SOMATULINE
Příbalová informace: informace pro uživatele STOPTUSSIN. Perorální kapky, roztok. (Butamirati citras, guaifenesinum )
 sp.zn. sukls233319/2009 Příbalová informace: informace pro uživatele STOPTUSSIN Perorální kapky, roztok. (Butamirati citras, guaifenesinum ) Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
sp.zn. sukls233319/2009 Příbalová informace: informace pro uživatele STOPTUSSIN Perorální kapky, roztok. (Butamirati citras, guaifenesinum ) Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
Příbalová informace: Informace pro uživatele. Dynastat 40 mg prášek pro injekční roztok parecoxibum
 Příbalová informace: Informace pro uživatele Dynastat 40 mg prášek pro injekční roztok parecoxibum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: Informace pro uživatele Dynastat 40 mg prášek pro injekční roztok parecoxibum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele. Brilique 60 mg potahované tablety ticagrelorum
 Příbalová informace: informace pro uživatele Brilique 60 mg potahované tablety ticagrelorum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro uživatele Brilique 60 mg potahované tablety ticagrelorum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Nimenrix prášek pro přípravu injekčního roztoku s rozpouštědlem v ampulce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y Tento léčivý přípravek
Příbalová informace: informace pro uživatele Nimenrix prášek pro přípravu injekčního roztoku s rozpouštědlem v ampulce Konjugovaná vakcína proti meningokokům skupin A, C, W-135 a Y Tento léčivý přípravek
Příloha č. 2 k rozhodnutí o registraci sp.zn.sukls68299/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Gelaspan 4 %, infuzní roztok
 Příloha č. 2 k rozhodnutí o registraci sp.zn.sukls68299/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE 4 %, infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příloha č. 2 k rozhodnutí o registraci sp.zn.sukls68299/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE 4 %, infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
