Základní principy rozlišování humánních léčivých přípravků od jiných výrobků
|
|
|
- Oldřich Kubíček
- před 8 lety
- Počet zobrazení:
Transkript
1 UST-30 verze 1 Základní principy rozlišování humánních léčivých přípravků od jiných výrobků Tento pokyn, s platností od , nahrazuje pokyn SÚKL UST-30 Vzhledem k účinnosti nového zákona č. 378/2007 Sb. o léčivech a o změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů (dále jen zákon o léčivech ), se vydává verze 1 tohoto pokynu, ve které jsou aktualizovány texty a odkazy v souladu s novou legislativou. Rozlišování mezi hromadně vyráběnými léčivými přípravky podléhajícími registraci, včetně rozlišování homeopatických přípravků, přípravky individuálně připravovanými v lékárně, na pracovišti nukleární medicíny, na pracovišti imunologickém či mikrobiologickém či vyráběnými v zařízení transfuzní služby, léčivými látkami a jinými typy výrobků (např. doplňky stravy, kosmetika či zdravotnické prostředky) má význam nejen pro určení regulačního režimu výrobku ve vztahu k bezpečnosti výrobku a jeho deklarovaným vlastnostem, ale má i značný praktický dopad pro výrobce či dovozce a distribuční řetězec. Jednoznačné stanovení povahy výrobku je rovněž podstatné pro součinnost orgánů státního dozoru, neboť dozor nad výrobky, které mohou být zaměněny s humánními léčivými přípravky, vykonávají četné instituce, zejména Česká obchodní inspekce (ČOI), Státní zemědělská a potravinářská inspekce (SZPI), orgány ochrany veřejného zdraví (krajské hygienické stanice), Ministerstvo zdravotnictví (MZ ČR), Ministerstvo životního prostředí (MŽP) a celní a finanční úřady. Analogicky situaci v EU neexistuje v České republice žádná speciální právně vymezená skupina hraničních přípravků, parafarmaceutik ani podpůrných přípravků. V souladu s existující legislativou se jednotlivé výrobky, u kterých může vznikat pochybnost o jejich zařazení, považují buď za léčivé látky či léčivé přípravky (včetně homeopatik), nebo za jiné výrobky, které nejsou regulovány v režimu léčivých přípravků (např. doplňky stravy, kosmetika, zdravotnické prostředky či další kategorie výrobků se zvláštním regulačním režimem). Samostatnou kapitolu tvoří přípravky pro veterinární použití, jejichž posuzování spadá do kompetence Ústavu pro státní kontrolu veterinárních biopreparátů a léčiv (ÚSKVBL). Jeden výrobek by neměl podléhat současně několika regulačním režimům. Zařazení výrobku do příslušné kategorie určuje regulační režim, kterému výrobek podléhá, včetně instituce, která je podle příslušné legislativy za regulaci výrobku odpovědná. U léčivých přípravků je s ohledem na rizika, která přinášejí, rozsah státního dozoru největší. SÚKL rozhoduje v případech pochybností o tom, zda jde o léčivý přípravek, léčivou látku, léčivý přípravek podléhající registraci, homeopatický přípravek nebo o jiný výrobek, a to na žádost, nebo z vlastního podnětu [ 13 odst. 2 písm. h) zákona o léčivech]. Pokud nejde o léčivý přípravek, další zařazení výrobku SÚKL neposuzuje a je třeba se obrátit na příslušné odpovědné instituce. Základem rozhodování o zařazení výrobku mezi léčivé přípravky jsou definice uvedené v předpisech Evropských společenství, které jsou povinně implementovány do legislativy všech členských států EU. Rozlišování léčivých přípravků od jiných výrobků však v rámci EU není harmonizováno a probíhá na národní úrovni. Výsledkem může být rozdílný přístup jednotlivých členských zemí k zařazení některých výrobků. Jeden výrobek tak může spadat do různých regulačních kategorií, což může vést k omezení jeho volného pohybu na trhu EU. V případě sporů o zařazení výrobku je poslední instancí Evropský soudní dvůr, který řeší výklad evropské legislativy, a jeho rozhodnutí jsou vzhledem k členství ČR v EU pro ČR závazná. Nicméně i Evropský soudní dvůr ve svých rozhodnutích potvrdil právo národního orgánu na takové rozhodování. Základní definice uplatnitelné při rozlišování léčivých přípravků od jiných výrobků Pro upřesnění uvádíme základní definice ze zákona o léčivech, které se vztahují k problematice vymezení hraničních přípravků, včetně případného vysvětlujícího komentáře. ( 2 odst. 1) Léčivým přípravkem se rozumí a) látka nebo kombinace látek prezentovaná s tím, že má léčebné nebo preventivní vlastnosti v případě onemocnění lidí nebo zvířat, nebo b) látka nebo kombinace látek, kterou lze použít u lidí nebo podat lidem, nebo použít u zvířat či podat zvířatům, a to buď za účelem obnovy, úpravy či ovlivnění fyziologických funkcí prostřednictvím farmakologického, imunologického nebo metabolického účinku, nebo za účelem stanovení lékařské diagnózy. 1
2 ( 2 odst. 3) Látkou se rozumí jakákoli látka, bez ohledu na její původ, který může být a) lidský, například lidská krev, její složky a přípravky z lidské krve, b) živočišný, například mikroorganismy, toxiny, celí živočichové, části orgánů, živočišné sekrety, extrakty nebo přípravky z krve, c) rostlinný, nebo d) chemický. Obě tyto definice jsou převzaty z předpisů Evropských společenství. Definice jsou konstruovány velmi široce látka, kterou může obsahovat léčivý přípravek, může být jakéhokoliv původu, nejen tedy chemicky definovaná entita, ale i např. krev a její složky, mikroorganismy, toxiny, celí živočichové, části orgánů, živočišné a rostlinné sekrety, extrakty, rostliny a části rostlin či látka získaná biotechnologicky. Vymezení látky tedy není v definici léčivého přípravku žádným omezením, protože v praxi může být látkou prakticky cokoli. Definice léčivého přípravku obsahuje dvě podmínky, z nichž alespoň jedna musí být splněna, aby se jednalo o léčivý přípravek. První podmínkou je vymezení účelu použití k léčení nebo prevenci onemocnění, resp. prezentace, že přípravek má v případě onemocnění léčebné nebo preventivní vlastnosti (tzv. definice podle prezentace), a druhou podmínkou je skutečnost, že přípravek lze podat za účelem obnovy, úpravy či ovlivnění fyziologických funkcí, nebo za účelem stanovení lékařské diagnózy (tzv. definice podle funkce). Vzhledem k šíři definic již existuje v EU řada soudních případů poskytujících doplňující výklad k těmto definicím a ze závěrů těchto soudních případů vychází i tento pokyn. ( 2 odst. 4, písm. a) Léčivé látky jsou určené k tomu, aby byly součástí léčivého přípravku. Jsou to látky, které způsobují jeho účinek; tento účinek je zpravidla farmakologický, imunologický nebo spočívá v ovlivnění metabolismu. Definice léčivé látky není obsažena v předpisech Evropských společenství, ale byla zařazena do zákona o léčivech zejména pro účely ustanovení upravujících dozor nad výrobou a distribucí léčivých látek a jejich použití v lékárnách. Při posuzování, zda jde o léčivou látku, se v rámci odhadu rizik zohledňuje i nutnost podřízení výroby či distribuce léčivé látky ( suroviny pro další výrobu nebo přípravu) definovanému režimu správné výrobní či distribuční praxe a kontrolám. Vymezení mechanismu účinku léčivé látky napomáhá odlišení od zdravotnických prostředků, které svých hlavních zamýšlených funkcí v lidském organismu nebo na jeho povrchu nedosahují farmakologickým nebo imunologickým účinkem nebo ovlivněním metabolismu (viz níže uvedená definice zdravotnického prostředku). Jiné základní definice významné pro rozlišování léčivých přípravků od jiných výrobků Zákon č. 110/1997 Sb., o potravinách a tabákových výrobcích, ve znění pozdějších předpisů ( 2 písm. i) Doplňkem stravy je potravina, jejímž účelem je doplňovat běžnou stravu a která je koncentrovaným zdrojem vitaminů a minerálních látek nebo dalších látek s nutričním nebo fyziologickým účinkem, obsažených v potravině samostatně nebo v kombinaci, určená k přímé spotřebě v malých odměřených množstvích. Vyhláška Ministerstva zdravotnictví č. 225/2008 Sb., kterou se stanoví požadavky na doplňky stravy a na obohacování potravin ( 3 odst. 5) Označování doplňků stravy nesmí doplňkům stravy přisuzovat vlastnosti týkající se prevence, léčby nebo vyléčení lidských onemocnění nebo na tyto vlastnosti odkazovat. Vyhláška Ministerstva zdravotnictví č. 54/2004 Sb., o potravinách určených pro zvláštní výživu a o způsobu jejich použití, ve znění pozdějších předpisů ( 1 odst. 2) Potravinami určenými pro zvláštní výživu se rozumějí potraviny, které jsou určeny pro výživové účely stanovené v této vyhlášce a uvádějí se do oběhu s označením účelu použití. ( 3 odst. 3) Potraviny určené pro zvláštní výživu nelze na obalu označit informací připisující výrobkům vlastnosti vztahující se k předcházení, ošetřování nebo léčení lidských chorob nebo takové vlastnosti naznačovat (to však nesmí u potravin pro zvláštní lékařské účely bránit uvádění informací nebo doporučení určených výhradně osobám kvalifikovaným v oboru lékařství, výživy nebo farmacie). Kategorie potravin pro zvláštní výživu jsou vymezeny v 2 této vyhlášky. Nespadají sem doplňky stravy, které jsou samostatnou kategorií potravin a jsou regulovány vyhláškou č. 225/2008 Sb. (viz výše). 2
3 Zákon č. 258/2000 Sb. o ochraně veřejného zdraví a o změně některých souvisejících zákonů, ve znění pozdějších předpisů ( 25 odst. 2) Kosmetickým prostředkem je látka nebo prostředek určený pro styk se zevními částmi lidského těla (pokožka, vlasový systém, nehty, rty a zevní pohlavní orgány), zuby a sliznicí dutiny ústní s cílem výlučně nebo převážně je čistit, parfémovat, měnit jejich vzhled, chránit je, udržovat je v dobrém stavu nebo korigovat lidské pachy, nejde- li o léčivo. Zákon č. 123/2000 Sb., o zdravotnických prostředcích a o změně některých souvisejících zákonů, ve znění pozdějších předpisů ( 2 odst. 1) Zdravotnickým prostředkem se rozumí nástroj, přístroj, pomůcka, zařízení, materiál nebo jiný předmět anebo výrobek používaný samostatně nebo v kombinaci, včetně potřebného programového vybavení, který je výrobcem nebo dovozcem určen pro použití u člověka pro účely: a) diagnózy, prevence, monitorování, léčby nebo mírnění nemoci, b) diagnózy, monitorování, léčby, mírnění nebo kompenzace poranění nebo zdravotního postižení, c) vyšetřování, náhrady anebo modifikace anatomické struktury či fyziologického procesu, d) kontroly početí, a který nedosahuje své hlavní zamýšlené funkce v lidském organismu nebo na jeho povrchu farmakologickým nebo imunologickým účinkem nebo ovlivněním metabolismu, jehož funkce však může být takovými účinky podpořena. Zákon č. 120/2002 Sb. o podmínkách uvádění biocidních přípravků a účinných látek na trh a o změně některých souvisejících zákonů ( 2 odst. 2) Biocidním přípravkem je přípravek obsahující jednu nebo více účinných látek určený k ničení, odpuzování, zneškodňování, zabránění účinku nebo dosažení jiného regulačního účinku na jakýkoliv škodlivý organismus chemickým nebo biologickým způsobem. ( 2 odst. 3) Škodlivým organismem je každý organismus, který má nepříznivý účinek na člověka nebo jehož přítomnost je nežádoucí, nepříznivě ovlivňuje činnost lidí nebo předměty, které užívají nebo vyrábějí, nebo působí nepříznivě na ostatní živé organismy. Při používání biocidních přípravků je škodlivý organismus cílovým organismem. Pro úplnost uvádíme typy biocidních přípravků uvedené v příloze k citovanému zákonu, které souvisí s hraniční problematikou. Jedná se o: Typ 1: Biocidní přípravky osobní hygieny - přípravky používané pro účely všeobecné dezinfekce s výjimkou přípravků s léčivým účinkem a přípravků, jejichž primární účinek a účel použití je kosmetický a účinek biocidní je doplňkový, jako např. antimikrobiální mýdla, šampony proti lupům a ústní vody. Typ 19: Repelenty - přípravky používané k odpuzování škodlivých organismů (např. komárů), aniž by přípravek na ně měl smrtící účinek. Insekticidy, akaricidy a přípravky, které jsou používány pro regulaci stavu hmyzu, roztočů a klíšťat, spadají do kategorie biocidních přípravků (typ 18), ovšem pouze v případě, že nejsou určené k přímému styku s organismem člověka. Posouzení hraničních případů Rozlišení léčivého přípravku od jiného výrobku je v praxi nejčastější. Výrobek se vždy hodnotí jako celek. Při hodnocení se posuzuje: kvalitativní a kvantitativní složení vztažené na jednotku dávky či lékové formy, navržený účel použití výrobku, mechanismus účinku, navržený způsob použití výrobku, včetně cesty podání, doporučené dávkování (zejména nejvyšší jednotlivá a denní dávka, délka užívání/používání) a případná omezení použití (kontraindikace), interakce, nežádoucí účinky, upozornění atd., vymezení skupiny uživatelů, návrh textu na obalu a informací určených pro spotřebitele, informace o skutečnostech podstatných pro posouzení zdravotního rizika předkládaného výrobku, informace o klasifikaci výrobku při uvedení na trh v jiných zemích (přednostně v zemích EU). Informace provázející výrobek a prezentace výrobku jsou z pohledu rozlišení mezi léčivým přípravkem a jiným výrobkem velmi podstatné, protože jde o prvky určující účel použití. V závislosti na navrženém 3
4 způsobu užití může být stejný výrobek v případě, že nejsou uvedeny indikace, považován za neléčivo nebo v případě, že jsou uvedeny indikace, může být považován za léčivý přípravek. Např. i výrobky z látek běžně využívaných v jiných průmyslových odvětvích (např. v potravinářství, kosmetickém průmyslu, při výrobě biocidů) se stávají léčivými přípravky, pokud je za účel jejich použití označena léčba či předcházení onemocnění (viz definice léčivého přípravku), a podléhají pak příslušným ustanovením zákona o léčivech. Složení výrobku je důležitým kritériem pro rozlišení léčivého přípravku od jiného typu výrobku. Tam, kde je ve výrobku obsaženo farmakologicky významné množství léčivé látky, může jít o léčivý přípravek nebo o zdravotnický prostředek s obsahem léčivé látky. Naopak i výrobek bez obsahu farmakologicky významného množství léčivé látky je považován za léčivý přípravek podléhající registraci v případě, že může představovat nebezpečí pro veřejné zdraví, pokud by byl uváděn na trh jako neléčivo. Mechanismus účinku je dalším důležitým rozlišovacím kritériem, neboť u některých výrobků je zakotven přímo v jejich definici. Např. léčivý přípravek dosahuje své funkce prostřednictvím farmakologického, imunologického nebo metabolického účinku, u zdravotnického prostředku není jeho hlavního účinku dosaženo farmakologickým nebo imunologickým účinkem nebo ovlivněním metabolismu. Klasifikace v zahraničí, především v ostatních státech Evropské unie, je dalším pomocným kritériem pro rozlišení, zda výrobek má být v ČR registrován jako léčivý přípravek. Přestože rozhodování je národní záležitostí, snahou SÚKL je harmonizované posuzování regulační kategorizace v případech, kdy to je možné. Postup pro žadatele o posouzení hraničních přípravků A) Vydání Rozhodnutí SÚKL, zda výrobek je či není léčivým přípravkem Posuzování hraničních přípravků je v tomto případě správním řízením. Vztahuje se na něj jednak zákon o léčivech, jednak obecné předpisy o správním řízení (zákon č. 500/2004 Sb., správní řád, ve znění pozdějších předpisů). V souladu s 112 zákona o léčivech podléhají odborné úkony spojené s posuzováním hraničních přípravků, které provádí SÚKL na žádost, náhradě výdajů. Náležitosti náhrady výdajů jsou dány prováděcím předpisem k zákonu o léčivech a pokynem SÚKL UST-29 (příloha 2 Sazebník úhrad nákladů za odborné úkony vykonávané v působnosti ústavu, kód K-006) zveřejněném na webových stránkách SÚKL ( Sazebník a poplatky). Na tomto místě pouze uvádíme, že náhradu výdajů je nutno provést před podáním žádosti. Posouzení hraničního přípravku se provádí na základě žádosti předložené na formuláři UST-19 (Žádost o vydání rozhodnutí, zda výrobek je léčivým přípravkem) a dokladu o náhradě výdajů. Pro každý jednotlivý přípravek se předkládá žádost na samostatném formuláři. Žádost lze podat buď v listinné podobě, nebo elektronicky prostřednictvím interaktivního formuláře zveřejněného na webové stránce SÚKL. Doručením písemné žádosti nebo elektronické žádosti podepsané zaručeným elektronickým podpisem je zahájeno správní řízení a nadále se postupuje v souladu s výše uvedenými právními předpisy. S ohledem na specifickou povahu jednotlivých případů si SÚKL v případě potřeby vyžádá doplňující informace. V tomto případě se správní řízení přeruší (viz správní řád) a vlastní řízení pokračuje dnem následujícím po dni předložení úplného doplnění. Po posouzení žádosti žadatel obdrží nejpozději do 60 dnů ode dne doručení žádosti rozhodnutí SÚKL, zda výrobek je či není léčivým přípravkem. Do této lhůty se nezapočítává doba přerušení správního řízení. Rozhodnutí je vydáváno v listinné podobě, a to na každý jednotlivý výrobek samostatně. B) Odborné stanovisko k zařazení výrobku Kromě žádosti o vydání rozhodnutí (viz bod A) může žadatel požádat SÚKL též o vydání odborného stanoviska k zařazení určitého výrobku. V tomto případě musí žadatel předložit údaje o výrobku nutné k posouzení (viz níže) a doklad o náhradě výdajů (viz pokyn UST-29, příloha 2 Sazebník úhrad nákladů za odborné úkony vykonávané v působnosti ústavu, kód O-002). Podáním žádosti o stanovisko není zahájeno správní řízení. Stanovisko Ústav vydá v souladu s částí IV. zákona č. 500/2004 Sb., správní řád, ve znění pozdějších předpisů. Odborné stanovisko vyjadřuje názor SÚKL k otázce možného zařazení výrobku. SÚKL v tomto případě nevydává rozhodnutí. Odborné stanovisko nemá právní platnost, a tudíž se proti němu nelze odvolat. 4
5 C) Konzultace K předběžnému projednání sporných případů rozlišení hraničních přípravků může žadatel využít konzultace s posuzovateli-koordinátory oddělení registrační agendy (referát hraničních přípravků a klasifikace pro výdej). Postup, jakým se žádá o konzultaci a informace o náležitostech platby za poskytnutou konzultaci jsou uvedeny v pokynu UST-29. Pro všechny zúčastněné strany žadatel z konzultace vypracuje zápis s krátkým písemným shrnutím závěrů. Zápis nenahrazuje rozhodnutí SÚKL. Požadavky SÚKL na předkládanou dokumentaci A) Žádost o vydání rozhodnutí: 1. Žadatel (název a sídlo právnické osoby nebo jméno a bydliště fyzické osoby, kontakty). Je-li kontaktní osoba odlišná od žadatele, je nutno předložit zmocnění k jednání od žadatele. 2. Výrobce (název a sídlo). 3. Název výrobku, forma výrobku (např. tablety, čaj, mast apod.) a velikost balení. 4. Kvalitativní a kvantitativní složení stanovené na jednotku dávky či lékové formy. V případě rostlin žádáme o uvádění názvů přednostně latinsky s uvedením rodového i druhového názvu a použité části, v případě chemických látek uveďte nechráněné názvy WHO (INN) nebo mezinárodní označení organických sloučenin (IUPAC). 5. Navržený účel použití výrobku, mechanismus účinku. 6. Vymezení skupiny uživatelů. 7. Navržený způsob použití, včetně cesty podání, doporučené dávkování (zejména nejvyšší jednotlivá a denní dávka, délka užívání/používání) a případně způsob přípravy (např. u čajů), případná omezení použití (kontraindikace), interakce, nežádoucí účinky, upozornění atd. 8. Návrh textu na obalu a informací určených pro spotřebitele. 9. Informace o skutečnostech podstatných pro posouzení zdravotního rizika předkládaného výrobku (je vhodné doložit i dostupnou tuzemskou i zahraniční literaturu v jazyce českém, slovenském nebo anglickém, případně odkazy na dostupné literární zdroje). 10. Údaje o klasifikaci výrobku v jiných zemích, certifikáty, či jiná rozhodnutí považovaná žadatelem za přínosná pro posouzení výrobku. Požadované údaje se uvádí přímo do formuláře žádosti UST-19. Rozsáhlejší informace (např. návrh textu na obalu) a případná další dokumentace související s žádostí se předloží ve formě příloh k žádosti. B), C) Žádost o vydání odborného stanoviska, žádost o konzultaci: Pro tyto případy postačí předložení údajů o složení, dávkování, způsobu použití, mechanismu účinku a návrhu textu na obalu. Požadované údaje se uvedou přímo do dokumentu, kterým žadatel žádá o vydání stanoviska či konzultaci (pro tyto žádosti neexistuje formulář). 5
AKTUÁLNÍ ZMĚNY SPRÁVNÍ PRAXE DOZOROVÝCH ORGÁNŮ A PRAKTICKÉ DOPADY. Efektivní právní služby
 AKTUÁLNÍ ZMĚNY SPRÁVNÍ PRAXE DOZOROVÝCH ORGÁNŮ A PRAKTICKÉ DOPADY Efektivní právní služby 1 Definice produktů základní vymezení produktů v oblasti farmacie. Hraniční výrobky rozlišování podle prezentace
AKTUÁLNÍ ZMĚNY SPRÁVNÍ PRAXE DOZOROVÝCH ORGÁNŮ A PRAKTICKÉ DOPADY Efektivní právní služby 1 Definice produktů základní vymezení produktů v oblasti farmacie. Hraniční výrobky rozlišování podle prezentace
Efektivní právní služby
 PROBLEMATIKA HRANIČIČNÍCH PŘÍPRAVKŮ - VÝCHODISKA, PRŮBĚH ŘÍZENÍ A CELKOVÉ SHRNUTÍ Efektivní právní služby 1 Definice produktů shrnutí/připomenutí základního vymezení produktů v oblasti farmacie hraničních
PROBLEMATIKA HRANIČIČNÍCH PŘÍPRAVKŮ - VÝCHODISKA, PRŮBĚH ŘÍZENÍ A CELKOVÉ SHRNUTÍ Efektivní právní služby 1 Definice produktů shrnutí/připomenutí základního vymezení produktů v oblasti farmacie hraničních
Efektivní právní služby
 HRANIČNÍ PŘÍPRAVKY - PRAXE, PRÁVNÍ OMEZENÍ A ODPOVĚDNOST Efektivní právní služby 1 HRANIČNÍ PŘÍPRAVKY 2 HRANIČNÍ VÝROBKY NEJČASTĚJI MEZI: LÉČIVÝMI PŘÍPRAVKY DOPLŇKY STRAVY ZDRAVOTNICKÝMI PROSTŘEDKY KOSMETICKÝMI
HRANIČNÍ PŘÍPRAVKY - PRAXE, PRÁVNÍ OMEZENÍ A ODPOVĚDNOST Efektivní právní služby 1 HRANIČNÍ PŘÍPRAVKY 2 HRANIČNÍ VÝROBKY NEJČASTĚJI MEZI: LÉČIVÝMI PŘÍPRAVKY DOPLŇKY STRAVY ZDRAVOTNICKÝMI PROSTŘEDKY KOSMETICKÝMI
Hraniční výrobky v oblasti zdravotnických prostředků. Mgr. Karolína Peštová odbor farmacie oddělení zdravotnických prostředků 23.
 Hraniční výrobky v oblasti zdravotnických prostředků Mgr. Karolína Peštová odbor farmacie oddělení zdravotnických prostředků 23. dubna 2014 Osnova prezentace co je hraniční výrobek kdo je oprávněný ke
Hraniční výrobky v oblasti zdravotnických prostředků Mgr. Karolína Peštová odbor farmacie oddělení zdravotnických prostředků 23. dubna 2014 Osnova prezentace co je hraniční výrobek kdo je oprávněný ke
OTC cesta k profitabilitě české lékárny a vazba na pacienta. Ing. Robert Sýkora, MHA Cluster Market Access Director, IPSEN Pharma
 OTC cesta k profitabilitě české lékárny a vazba na pacienta Ing. Robert Sýkora, MHA Cluster Market Access Director, IPSEN Pharma Obsah vystoupení Evropská srovnání v oblasti OTC Legislativa e-shop a OTC
OTC cesta k profitabilitě české lékárny a vazba na pacienta Ing. Robert Sýkora, MHA Cluster Market Access Director, IPSEN Pharma Obsah vystoupení Evropská srovnání v oblasti OTC Legislativa e-shop a OTC
DOPLŇKY STRAVY. Ing. Sylvie kršková, Státní zemědělská a potravinářská inspekce
 Ing. Sylvie kršková, Státní zemědělská a potravinářská inspekce = potravina! jejímž účelem je doplňovat běžnou stravu a která je koncentrovaným zdrojem vitaminů a minerálních látek nebo dalších látek s
Ing. Sylvie kršková, Státní zemědělská a potravinářská inspekce = potravina! jejímž účelem je doplňovat běžnou stravu a která je koncentrovaným zdrojem vitaminů a minerálních látek nebo dalších látek s
20.B. Podpora na zlepšení životních podmínek v Přípravky chovu drůbeže na bázi oxidu křemičitého a fylosilikátů
 Uvádíme seznamy přípravků, které spadají mezi ty, které jsou regulovány ÚSKVBL (veterinární přípravky, veterinární technické prostředky), a ty, které jako biocidy reguluje Ministerstvo zdravotnictví ČR.
Uvádíme seznamy přípravků, které spadají mezi ty, které jsou regulovány ÚSKVBL (veterinární přípravky, veterinární technické prostředky), a ty, které jako biocidy reguluje Ministerstvo zdravotnictví ČR.
3/5.3 DOPLŇKY STRAVY PODLE PLATNÉ LEGISLATIVY
 VÝROBA POTRAVIN A JEJICH UVÁDĚNÍ DO OBĚHU V souladu s ustanovením 3d (Informační povinnost provozovatele potravinářského podniku) zákona č. 110/1997 Sb., o potravinách a tabákových výrobcích a o změně
VÝROBA POTRAVIN A JEJICH UVÁDĚNÍ DO OBĚHU V souladu s ustanovením 3d (Informační povinnost provozovatele potravinářského podniku) zákona č. 110/1997 Sb., o potravinách a tabákových výrobcích a o změně
Medical devices specificities: opportunities for a dedicated product development methodology
 Medical devices specificities: opportunities for a dedicated product development methodology Isa C.T. Santos G. Scott Gazelle Luis A. Rocha Joao Manuel R.S. Tavares Jakub Vacek Shrnutí Existuje mnoho definic
Medical devices specificities: opportunities for a dedicated product development methodology Isa C.T. Santos G. Scott Gazelle Luis A. Rocha Joao Manuel R.S. Tavares Jakub Vacek Shrnutí Existuje mnoho definic
446/2004 Sb. VYHLÁŠKA ze dne 16. července 2004, kterou se stanoví požadavky na doplňky stravy a na obohacování potravin potravními doplňky
 446/2004 Sb. VYHLÁŠKA ze dne 16. července 2004, kterou se stanoví požadavky na doplňky stravy a na obohacování potravin potravními doplňky Ministerstvo zdravotnictví stanoví podle 19 odst. 1 písm. a) a
446/2004 Sb. VYHLÁŠKA ze dne 16. července 2004, kterou se stanoví požadavky na doplňky stravy a na obohacování potravin potravními doplňky Ministerstvo zdravotnictví stanoví podle 19 odst. 1 písm. a) a
HLAVA VIII VETERINÁRNÍ PŘÍPRAVKY A VETERINÁRNÍ TECHNICKÉ PROSTŘEDKY
 Působnost Ústavu pro státní kontrolu veterinárních biopreparátů a léčiv 65 HLAVA VIII VETERINÁRNÍ PŘÍPRAVKY A VETERINÁRNÍ TECHNICKÉ PROSTŘEDKY 65 [Působnost Ústavu pro státní kontrolu veterinárních biopreparátů
Působnost Ústavu pro státní kontrolu veterinárních biopreparátů a léčiv 65 HLAVA VIII VETERINÁRNÍ PŘÍPRAVKY A VETERINÁRNÍ TECHNICKÉ PROSTŘEDKY 65 [Působnost Ústavu pro státní kontrolu veterinárních biopreparátů
SBÍRKA ZÁKONŮ. Profil aktualizovaného znění: VYHLÁŠKA. kterou se stanoví požadavky na doplňky stravy a na obohacování potravin
 Page 1 of 5 SBÍRKA ZÁKONŮ ČESKÉ REPUBLIKY Profil aktualizovaného znění: Titul původního předpisu: Vyhláška kterou se stanoví požadavky na doplňky stravy a na obohacování potravin Citace pův. předpisu:
Page 1 of 5 SBÍRKA ZÁKONŮ ČESKÉ REPUBLIKY Profil aktualizovaného znění: Titul původního předpisu: Vyhláška kterou se stanoví požadavky na doplňky stravy a na obohacování potravin Citace pův. předpisu:
Systém úřední kontroly v ČR
 Systém úřední kontroly v ČR Úřední kontrola v ČR Úřední kontroly v celém potravinovém řetězci od prvovýroby až po prodej spotřebiteli provádějí příslušné orgány státního dozoru (dozorové orgány ) v působnosti
Systém úřední kontroly v ČR Úřední kontrola v ČR Úřední kontroly v celém potravinovém řetězci od prvovýroby až po prodej spotřebiteli provádějí příslušné orgány státního dozoru (dozorové orgány ) v působnosti
Používání zdravotnických prostředků v ambulantní praxi
 Používání zdravotnických prostředků v ambulantní praxi Dnem 1. dubna 2015 vstoupil v účinnost nový zákon o zdravotnických prostředcích (zákon č. 268/2014 Sb.), který přináší komplexní zákonnou úpravu regulace
Používání zdravotnických prostředků v ambulantní praxi Dnem 1. dubna 2015 vstoupil v účinnost nový zákon o zdravotnických prostředcích (zákon č. 268/2014 Sb.), který přináší komplexní zákonnou úpravu regulace
VOLNĚ PRODEJNÝ FARMA SORTIMENT A PRAVIDLA KOMUNIKACE SOUČASNÁ I BUDOUCÍ. Efektivní právní služby
 VOLNĚ PRODEJNÝ FARMA SORTIMENT A PRAVIDLA KOMUNIKACE SOUČASNÁ I BUDOUCÍ Efektivní právní služby 24.10.2013 1 OTC přípravky pravidla propagace OTC; co je a už není reklama. doplňky stravy regulace reklamy
VOLNĚ PRODEJNÝ FARMA SORTIMENT A PRAVIDLA KOMUNIKACE SOUČASNÁ I BUDOUCÍ Efektivní právní služby 24.10.2013 1 OTC přípravky pravidla propagace OTC; co je a už není reklama. doplňky stravy regulace reklamy
Školící materiály pro cyklus vzdělávacích seminářů Tradiční využívání planých rostlin Legislativa v kosmetice.
 Školící materiály pro cyklus vzdělávacích seminářů Tradiční využívání planých rostlin Legislativa v kosmetice. 9. 3. 2012 Autor školícího materiálu: Mgr.Miriam Popelková PP8: Mendelova univerzita v Brně
Školící materiály pro cyklus vzdělávacích seminářů Tradiční využívání planých rostlin Legislativa v kosmetice. 9. 3. 2012 Autor školícího materiálu: Mgr.Miriam Popelková PP8: Mendelova univerzita v Brně
Zákon č. 268/2014 o zdravotnických prostředcích. přehled některých jeho ustanovení
 Zákon č. 268/2014 o zdravotnických prostředcích přehled některých jeho ustanovení Definice ZP nástroj, přístroj, zařízení, programové vybavení včetně programového vybavení určeného jeho výrobcem ke specifickému
Zákon č. 268/2014 o zdravotnických prostředcích přehled některých jeho ustanovení Definice ZP nástroj, přístroj, zařízení, programové vybavení včetně programového vybavení určeného jeho výrobcem ke specifickému
CS Jednotná v rozmanitosti CS A8-0046/291. Pozměňovací návrh. Mireille D'Ornano za skupinu ENF
 7.3.2016 A8-0046/291 Pozměňovací návrh 291 Mireille D'Ornano za skupinu ENF Zpráva Françoise Grossetête Veterinární léčivé přípravky COM(2014)0558 C8-0164/2014 2014/0257(COD) A8-0046/2016 Návrh nařízení
7.3.2016 A8-0046/291 Pozměňovací návrh 291 Mireille D'Ornano za skupinu ENF Zpráva Françoise Grossetête Veterinární léčivé přípravky COM(2014)0558 C8-0164/2014 2014/0257(COD) A8-0046/2016 Návrh nařízení
ZP-22 Metodika kontrol distributorů a dovozců zdravotnických prostředků
 ZP-22 Metodika kontrol distributorů a dovozců zdravotnických prostředků Tento pokyn je platný od 11. 03. 2019. ÚVOD Tato metodika obsahuje informace určené zejména pro dovozce a distributory zdravotnických
ZP-22 Metodika kontrol distributorů a dovozců zdravotnických prostředků Tento pokyn je platný od 11. 03. 2019. ÚVOD Tato metodika obsahuje informace určené zejména pro dovozce a distributory zdravotnických
Dozor nad potravinami
 Hejmalová Michaela Dozor nad potravinami Úřední kontroly v celém potravinovém řetězci od prvovýroby až po prodej spotřebiteli provádějí příslušné orgány státního dozoru (dozorové orgány) v působnosti:
Hejmalová Michaela Dozor nad potravinami Úřední kontroly v celém potravinovém řetězci od prvovýroby až po prodej spotřebiteli provádějí příslušné orgány státního dozoru (dozorové orgány) v působnosti:
Pokyn DIS-13 verze 6 Hlášení dodávek distribuovaných humánních léčivých přípravků
 Pokyn DIS-13 verze 6 Hlášení dodávek distribuovaných humánních léčivých přípravků Tento pokyn nahrazuje DIS-13 verze 5 s účinností od 1.1.2019. Pokyn je vydáván na základě 77 odst. 1 písm. f) zákona č.
Pokyn DIS-13 verze 6 Hlášení dodávek distribuovaných humánních léčivých přípravků Tento pokyn nahrazuje DIS-13 verze 5 s účinností od 1.1.2019. Pokyn je vydáván na základě 77 odst. 1 písm. f) zákona č.
ZBIERKA ZÁKONOV SLOVENSKEJ REPUBLIKY. Ročník Vyhlásená verzia v Zbierke zákonov Slovenskej republiky
 ZBIERKA ZÁKONOV SLOVENSKEJ REPUBLIKY Ročník 1987 Vyhlásené: 25.05.1987 Vyhlásená verzia v Zbierke zákonov Slovenskej republiky Obsah tohto dokumentu má informatívny charakter. 43 V Y H L Á Š K A ministerstva
ZBIERKA ZÁKONOV SLOVENSKEJ REPUBLIKY Ročník 1987 Vyhlásené: 25.05.1987 Vyhlásená verzia v Zbierke zákonov Slovenskej republiky Obsah tohto dokumentu má informatívny charakter. 43 V Y H L Á Š K A ministerstva
Zajímavé dotazy, důležitá upozornění a dobré rady na konec
 [ 1 ] Zajímavé dotazy, důležitá upozornění a dobré rady na konec MUDr. Alice Němcová Změny v dokumentaci schválené posouzení CTA a vydání povolení/schválení ohlášeného KH Text vložený do rozhodnutí: Klinické
[ 1 ] Zajímavé dotazy, důležitá upozornění a dobré rady na konec MUDr. Alice Němcová Změny v dokumentaci schválené posouzení CTA a vydání povolení/schválení ohlášeného KH Text vložený do rozhodnutí: Klinické
Problematika oznamování a povolování biocidních přípravků uváděných na trh v ČR
 Problematika oznamování a povolování biocidních přípravků uváděných na trh v ČR Mgr. Jan Mikoláš Ministerstvo zdravotnictví Odbor strategie a řízení ochrany a podpory veřejného zdraví Oddělení Registru
Problematika oznamování a povolování biocidních přípravků uváděných na trh v ČR Mgr. Jan Mikoláš Ministerstvo zdravotnictví Odbor strategie a řízení ochrany a podpory veřejného zdraví Oddělení Registru
SBÍRKA ZÁKONŮ. Ročník 2018 ČESKÁ REPUBLIKA. Částka 29 Rozeslána dne 12. dubna 2018 Cena Kč 106, O B S A H :
 Ročník 2018 SBÍRKA ZÁKONŮ ČESKÁ REPUBLIKA Částka 29 Rozeslána dne 12. dubna 2018 Cena Kč 106, 58. Vyhláška o doplňcích stravy a složení potravin O B S A H : 59. Sdělení Ministerstva školství, mládeže a
Ročník 2018 SBÍRKA ZÁKONŮ ČESKÁ REPUBLIKA Částka 29 Rozeslána dne 12. dubna 2018 Cena Kč 106, 58. Vyhláška o doplňcích stravy a složení potravin O B S A H : 59. Sdělení Ministerstva školství, mládeže a
Uvádění dezinfekčních přípravků na trh v ČR jako zdravotnické prostředky
 Uvádění dezinfekčních přípravků na trh v ČR jako zdravotnické prostředky Věra Melicherčíková SZÚ, NRL/DS, Praha XXIV. mezinárodní konference: Nemocniční epidemiologie a hygiena Surveillance infekcí spojených
Uvádění dezinfekčních přípravků na trh v ČR jako zdravotnické prostředky Věra Melicherčíková SZÚ, NRL/DS, Praha XXIV. mezinárodní konference: Nemocniční epidemiologie a hygiena Surveillance infekcí spojených
2015 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 2 ZMĚNY V OBLASTI VIGILANCE ZP od 1. 4. 2015 Ing. Mgr. Jakub Machálek ZMĚNY V OBLASTI VIGILANCE ZDRAVOTNICKÝCH PROSTŘEDKŮ OD 1.DUBNA 2015 3 Právní rámec zákon č. 268/2014 Sb., o zdravotnických prostředcích
2 ZMĚNY V OBLASTI VIGILANCE ZP od 1. 4. 2015 Ing. Mgr. Jakub Machálek ZMĚNY V OBLASTI VIGILANCE ZDRAVOTNICKÝCH PROSTŘEDKŮ OD 1.DUBNA 2015 3 Právní rámec zákon č. 268/2014 Sb., o zdravotnických prostředcích
PŘÍLOHA PŘÍLOHA I VZOR PRŮVODNÍHO DOPISU K ŽÁDOSTI O KONZULTACI PRO URČENÍ STATUSU NOVÉ POTRAVINY
 CS PŘÍLOHA PŘÍLOHA I VZOR PRŮVODNÍHO DOPISU K ŽÁDOSTI O KONZULTACI PRO URČENÍ STATUSU NOVÉ POTRAVINY Příslušný orgán členského státu Datum: Předmět: Žádost o konzultaci pro určení statusu nové potraviny
CS PŘÍLOHA PŘÍLOHA I VZOR PRŮVODNÍHO DOPISU K ŽÁDOSTI O KONZULTACI PRO URČENÍ STATUSU NOVÉ POTRAVINY Příslušný orgán členského státu Datum: Předmět: Žádost o konzultaci pro určení statusu nové potraviny
2012 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 2 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV, KOMPETENCE, ORGANIZACE, POLITIKA Mgr. Irena Storová Zástupkyně ředitele Státního ústavu pro kontrolu léčiv STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV 3 Státní ústav pro kontrolu
2 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV, KOMPETENCE, ORGANIZACE, POLITIKA Mgr. Irena Storová Zástupkyně ředitele Státního ústavu pro kontrolu léčiv STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV 3 Státní ústav pro kontrolu
Aktuální změny v legislativě zdravotnických prostředků. Odbor farmacie Mgr. Kateřina Pavlíková
 Aktuální změny v legislativě zdravotnických prostředků Odbor farmacie Mgr. Kateřina Pavlíková Základní ustanovení Nový zákon o zdravotnických prostředcích účinnost: 1.4 2015 sjednocuje význam pojmů tak,
Aktuální změny v legislativě zdravotnických prostředků Odbor farmacie Mgr. Kateřina Pavlíková Základní ustanovení Nový zákon o zdravotnických prostředcích účinnost: 1.4 2015 sjednocuje význam pojmů tak,
2012 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 2012 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV 9.6.2016 KONZULTACE POSKYTOVANÉ SEKCÍ REGISTRACÍ MUDr. Radka Montoniová Sekce registrací 3 Obsah: Odborné konzultace vs. Clarification meeting Odborné konzultace Jak
2012 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV 9.6.2016 KONZULTACE POSKYTOVANÉ SEKCÍ REGISTRACÍ MUDr. Radka Montoniová Sekce registrací 3 Obsah: Odborné konzultace vs. Clarification meeting Odborné konzultace Jak
Klasifikace analytických účtů vypořádání zaslaných připomínek. Ing. Markéta Bartůňková 21.10.2015
 Klasifikace analytických účtů vypořádání zaslaných připomínek Ing. Markéta Bartůňková 21.10.2015 ÚČETNICTVÍ REFERENČNÍCH NEMOCNIC REFERENČNÍ NEMOCNICE PRÁVNÍ FORMA: PŘÍSPĚVKOVÁ ORGANIZACE PRÁVNÍ FORMA:
Klasifikace analytických účtů vypořádání zaslaných připomínek Ing. Markéta Bartůňková 21.10.2015 ÚČETNICTVÍ REFERENČNÍCH NEMOCNIC REFERENČNÍ NEMOCNICE PRÁVNÍ FORMA: PŘÍSPĚVKOVÁ ORGANIZACE PRÁVNÍ FORMA:
Pokyn DIS-13 verze 5 Hlášení dodávek distribuovaných humánních léčivých přípravků
 Pokyn DIS-13 verze 5 Hlášení dodávek distribuovaných humánních léčivých přípravků Platnost od 1. 5. 2017, účinnost od 1. 9. 2017 Pokyn je vydáván na základě a v souladu s ustanovením 77 odst. 1 písm. f)
Pokyn DIS-13 verze 5 Hlášení dodávek distribuovaných humánních léčivých přípravků Platnost od 1. 5. 2017, účinnost od 1. 9. 2017 Pokyn je vydáván na základě a v souladu s ustanovením 77 odst. 1 písm. f)
Čl. I. Změna zákona o léčivech
 ZÁKON ze dne... 2012, kterým se mění zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Parlament se usnesl na tomto zákoně České
ZÁKON ze dne... 2012, kterým se mění zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Parlament se usnesl na tomto zákoně České
Registrace biocidů. MUDr. Daniela Bittnerová, CSc. Ministerstvo zdravotnictví Odbor strategie a řízení ochrany a podpory veřejného zdraví
 Registrace biocidů MUDr. Daniela Bittnerová, CSc. Ministerstvo zdravotnictví Odbor strategie a řízení ochrany a podpory veřejného zdraví Oddělení Registru chemických látek MZ ČR bittnerova@szu.cz tel.:
Registrace biocidů MUDr. Daniela Bittnerová, CSc. Ministerstvo zdravotnictví Odbor strategie a řízení ochrany a podpory veřejného zdraví Oddělení Registru chemických látek MZ ČR bittnerova@szu.cz tel.:
Rozdílová tabulka návrhu předpisu ČR s legislativou EU
 Rozdílová tabulka návrhu předpisu ČR s legislativou EU Návrh zákona, kterým se mění zákon č. 156/1998 Sb., o hnojivech, pomocných půdních látkách, pomocných rostlinných přípravcích a substrátech a o agrochemickém
Rozdílová tabulka návrhu předpisu ČR s legislativou EU Návrh zákona, kterým se mění zákon č. 156/1998 Sb., o hnojivech, pomocných půdních látkách, pomocných rostlinných přípravcích a substrátech a o agrochemickém
Žádost o dovoz veterinárního léčivého přípravku registrovaného v jiném členském státě
 Pokyn Ústavu pro státní kontrolu veterinárních biopreparátů a léčiv ÚSKVBL / REG 1/2008 Žádost o dovoz veterinárního léčivého přípravku registrovaného v jiném členském státě Platnost od: 17.3. 2008 Platnost
Pokyn Ústavu pro státní kontrolu veterinárních biopreparátů a léčiv ÚSKVBL / REG 1/2008 Žádost o dovoz veterinárního léčivého přípravku registrovaného v jiném členském státě Platnost od: 17.3. 2008 Platnost
DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ
 1 DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ MUDr. Alice Němcová Oddělení klinického hodnocení, Sekce registrací DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ 2 Obsah prezentace: Pravidla distribuce
1 DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ MUDr. Alice Němcová Oddělení klinického hodnocení, Sekce registrací DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ 2 Obsah prezentace: Pravidla distribuce
11. funkční období. (Navazuje na sněmovní tisk č. 669 ze 7. volebního období PS PČR) Lhůta pro projednání Senátem uplyne 19.
 36 11. funkční období 36 Návrh zákona, kterým se mění zákon č. 156/1998 Sb., o hnojivech, pomocných půdních látkách, pomocných rostlinných přípravcích a substrátech a o agrochemickém zkoušení zemědělských
36 11. funkční období 36 Návrh zákona, kterým se mění zákon č. 156/1998 Sb., o hnojivech, pomocných půdních látkách, pomocných rostlinných přípravcích a substrátech a o agrochemickém zkoušení zemědělských
Parlament se usnesl na tomto zákoně České republiky:
 Strana 624 Sbírka zákonů č. 61 / 2017 61 ZÁKON ze dne 19. ledna 2017, kterým se mění zákon č. 156/1998 Sb., o hnojivech, pomocných půdních látkách, pomocných rostlinných přípravcích a substrátech a o agrochemickém
Strana 624 Sbírka zákonů č. 61 / 2017 61 ZÁKON ze dne 19. ledna 2017, kterým se mění zákon č. 156/1998 Sb., o hnojivech, pomocných půdních látkách, pomocných rostlinných přípravcích a substrátech a o agrochemickém
Novelizace zákona o biocidech Zákon č. 86/2009 Sb. ZÁKON o podmínkách uvádění biocidních přípravků a účinných látek na trh
 Legislativa (Závazná pro dovozce, výrobce nebo distributory dezinfekčních prostředků pro oblast komunální hygieny, zdravotnictví a veterinárního lékařství) HLAVA I Novelizace zákona o biocidech Zákon č.
Legislativa (Závazná pro dovozce, výrobce nebo distributory dezinfekčních prostředků pro oblast komunální hygieny, zdravotnictví a veterinárního lékařství) HLAVA I Novelizace zákona o biocidech Zákon č.
Efektivní právní služby
 NOVINKY V OBLASTI PROPAGACE A PRODEJE VOLNĚ PRODEJNÝCH LÉČIV A DOPLŇKŮ STRAVY Efektivní právní služby 1 NOVINKY V OBLASTI PROPAGACE A PRODEJE LÉČIVÝCH PŘÍPRAVKŮ 2 NÁVRH NOVELY ZÁKONA O LÉČIVECH 3 novela
NOVINKY V OBLASTI PROPAGACE A PRODEJE VOLNĚ PRODEJNÝCH LÉČIV A DOPLŇKŮ STRAVY Efektivní právní služby 1 NOVINKY V OBLASTI PROPAGACE A PRODEJE LÉČIVÝCH PŘÍPRAVKŮ 2 NÁVRH NOVELY ZÁKONA O LÉČIVECH 3 novela
[ 1 ] RNDr. Olga Hanzlíčková 2012 Státní ústav pro kontrolu léčiv
![[ 1 ] RNDr. Olga Hanzlíčková 2012 Státní ústav pro kontrolu léčiv [ 1 ] RNDr. Olga Hanzlíčková 2012 Státní ústav pro kontrolu léčiv](/thumbs/93/112264798.jpg) [ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Návrh novely zákona č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů vedoucí sekce DOZ [ 3 ] Směrnice Evropského parlamentu a Rady 2010/84/EU
[ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Návrh novely zákona č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů vedoucí sekce DOZ [ 3 ] Směrnice Evropského parlamentu a Rady 2010/84/EU
Politika kvality Ústavu pro kontrolu veterinárních biopreparátů a léčiv
 Politika kvality Ústavu pro kontrolu veterinárních biopreparátů a léčiv Ústav pro státní kontrolu veterinárních biopreparátů a léčiv uplatňuje na všechny důležité procesy systém jištění kvality. Nedílnou
Politika kvality Ústavu pro kontrolu veterinárních biopreparátů a léčiv Ústav pro státní kontrolu veterinárních biopreparátů a léčiv uplatňuje na všechny důležité procesy systém jištění kvality. Nedílnou
Aktuální legislativní rámec doplňků stravy v ČR a EU
 Aktuální legislativní rámec doplňků stravy v ČR a EU Ministerstvo zemědělství České republiky Sekce potravinářských výrob - Úřad pro potraviny Mgr. Ing. Kateřina Melenovská Praha 24. 10. 2018 Přehled aktuální
Aktuální legislativní rámec doplňků stravy v ČR a EU Ministerstvo zemědělství České republiky Sekce potravinářských výrob - Úřad pro potraviny Mgr. Ing. Kateřina Melenovská Praha 24. 10. 2018 Přehled aktuální
CS Jednotná v rozmanitosti CS A8-0046/92. Pozměňovací návrh. Sylvie Goddyn za skupinu ENF
 21.10.2015 A8-0046/92 92 Bod odůvodnění 8 (8) Na vitaminy, minerální látky a jiné látky, které jsou určené k použití v doplňcích stravy nebo které mají být přidávány do potravin, včetně počáteční a pokračovací
21.10.2015 A8-0046/92 92 Bod odůvodnění 8 (8) Na vitaminy, minerální látky a jiné látky, které jsou určené k použití v doplňcích stravy nebo které mají být přidávány do potravin, včetně počáteční a pokračovací
SRS - správní úřad rostlinolékařské péče s působností na území ČR
 ČESKÁ REPUBLIKA STÁTNÍ ROSTLINOLÉKAŘSKÁ SPRÁVA STATE PHYTOSANITARY ADMINISTRATION SRS - správní úřad rostlinolékařské péče s působností na území ČR 1. workshop projektu OP VK 2.2: Inovace a rozšíření výuky
ČESKÁ REPUBLIKA STÁTNÍ ROSTLINOLÉKAŘSKÁ SPRÁVA STATE PHYTOSANITARY ADMINISTRATION SRS - správní úřad rostlinolékařské péče s působností na území ČR 1. workshop projektu OP VK 2.2: Inovace a rozšíření výuky
13/sv. 15 CS. Úřední věstník Evropské unie ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ L 35/1
 3 31995R0297 15.2.1995 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ L 35/1 NAŘÍZENÍ RADY (ES) č. 297/95 ze dne 10. února 1995 o poplatcích, které se platí Evropské agentuře pro hodnocení léčivých přípravků RADA
3 31995R0297 15.2.1995 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ L 35/1 NAŘÍZENÍ RADY (ES) č. 297/95 ze dne 10. února 1995 o poplatcích, které se platí Evropské agentuře pro hodnocení léčivých přípravků RADA
FV systémy a jejich QM Základní dokument FV systému
 Státní ústav pro kontrolu léčiv [ 1 ] FV systémy a jejich QM Základní dokument FV systému Oddělení farmakovigilance Státní ústav pro kontrolu léčiv [ 2 ] Co v dnešní prezentaci? Stručné představení modulů
Státní ústav pro kontrolu léčiv [ 1 ] FV systémy a jejich QM Základní dokument FV systému Oddělení farmakovigilance Státní ústav pro kontrolu léčiv [ 2 ] Co v dnešní prezentaci? Stručné představení modulů
A. Klasifikace analytických účtů
 A. Klasifikace analytických účtů Autor / Autoři: Hlavní autor: Ing. Markéta Bartůňková Spoluautoři: Ing. Petr Mašek Verze: 0.0 Datum: 17. 06. 2015 Ústav zdravotnických informací a statistiky ČR Palackého
A. Klasifikace analytických účtů Autor / Autoři: Hlavní autor: Ing. Markéta Bartůňková Spoluautoři: Ing. Petr Mašek Verze: 0.0 Datum: 17. 06. 2015 Ústav zdravotnických informací a statistiky ČR Palackého
Vybrané předpisy EU vztahující se k chemické bezpečnosti. Mirka Hornychová Státní zdravotní ústav
 Vybrané předpisy EU vztahující se k chemické bezpečnosti Mirka Hornychová Státní zdravotní ústav CHEMICKÉ LÁTKY TRH nařízen zení 1907/2006 REACH nařízen zení 1272/2008 CLP nařízen zení 689/2008 dovoz a
Vybrané předpisy EU vztahující se k chemické bezpečnosti Mirka Hornychová Státní zdravotní ústav CHEMICKÉ LÁTKY TRH nařízen zení 1907/2006 REACH nařízen zení 1272/2008 CLP nařízen zení 689/2008 dovoz a
2016 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 1 2 NEINTERVENČNÍ POREGISTRAČNÍ STUDIE MONITOROVÁNÍ, POSUZOVACÍ PRAXE Mgr. Natália Svršková Velký sál SÚKL 3 Obsah Neintervenční poregistrační studie definice, monitorování Neintervenční poregistrační
1 2 NEINTERVENČNÍ POREGISTRAČNÍ STUDIE MONITOROVÁNÍ, POSUZOVACÍ PRAXE Mgr. Natália Svršková Velký sál SÚKL 3 Obsah Neintervenční poregistrační studie definice, monitorování Neintervenční poregistrační
Doporučení Ústavu pro státní kontrolu veterinárních biopreparátů a léčiv
 Strana 1 (celkem 6) Ústav pro státní kontrolu veterinárních biopreparátů a léčiv Institute for State Control of Veterinary Biologicals and Medicines Hudcova 56a, Brno-Medlánky Postal Code: 621 00, Czech
Strana 1 (celkem 6) Ústav pro státní kontrolu veterinárních biopreparátů a léčiv Institute for State Control of Veterinary Biologicals and Medicines Hudcova 56a, Brno-Medlánky Postal Code: 621 00, Czech
POZMĚŇOVACÍ NÁVRHY 4-9
 EVROPSKÝ PARLAMENT 2009-2014 Výbor pro průmysl, výzkum a energetiku 3. 2. 2010 2008/0255(COD) POZMĚŇOVACÍ NÁVRHY 4-9 Návrh stanoviska Jorgo Chatzimarkakis (PE430.863v01-00) k návrhu nařízení Evropského
EVROPSKÝ PARLAMENT 2009-2014 Výbor pro průmysl, výzkum a energetiku 3. 2. 2010 2008/0255(COD) POZMĚŇOVACÍ NÁVRHY 4-9 Návrh stanoviska Jorgo Chatzimarkakis (PE430.863v01-00) k návrhu nařízení Evropského
VYHLÁŠKA č. 450/2004 Sb. ze dne 21. července 2004, o označování výživové hodnoty potravin, ve znění vyhlášky č. 330/2009 Sb.
 VYHLÁŠKA č. 450/2004 Sb. ze dne 21. července 2004, o označování výživové hodnoty potravin, ve znění vyhlášky č. 330/2009 Sb. Změna: 330/2009 Sb. Ministerstvo zdravotnictví stanoví podle 19 odst. 1 písm.
VYHLÁŠKA č. 450/2004 Sb. ze dne 21. července 2004, o označování výživové hodnoty potravin, ve znění vyhlášky č. 330/2009 Sb. Změna: 330/2009 Sb. Ministerstvo zdravotnictví stanoví podle 19 odst. 1 písm.
ROZDÍLOVÁ TABULKA NÁVRHU PŘEDPISU ČR S LEGISLATIVOU EU
 ROZDÍLOVÁ TABULKA NÁVRHU PŘEDPISU ČR S LEGISLATIVOU EU Návrh zákona ze dne.., kterým se mění zákon č. 235/2004 Sb., ve znění Čl. I Zákon č. 235/2004 Sb., o dani z přidané hodnoty, ve znění zákona č. 635/2004
ROZDÍLOVÁ TABULKA NÁVRHU PŘEDPISU ČR S LEGISLATIVOU EU Návrh zákona ze dne.., kterým se mění zákon č. 235/2004 Sb., ve znění Čl. I Zákon č. 235/2004 Sb., o dani z přidané hodnoty, ve znění zákona č. 635/2004
 EVROPSKÁ KOMISE GENERÁLNÍ ŘEDITELSTVÍ PRO VNITŘNÍ TRH, PRŮMYSL, PODNIKÁNÍ A MALÉ A STŘEDNÍ PODNIKY Brusel 1. února 2019 OTÁZKY A ODPOVĚDI TÝKAJÍCÍ SE VYSTOUPENÍ SPOJENÉHO KRÁLOVSTVÍ Z EVROPSKÉ UNIE S OHLEDEM
EVROPSKÁ KOMISE GENERÁLNÍ ŘEDITELSTVÍ PRO VNITŘNÍ TRH, PRŮMYSL, PODNIKÁNÍ A MALÉ A STŘEDNÍ PODNIKY Brusel 1. února 2019 OTÁZKY A ODPOVĚDI TÝKAJÍCÍ SE VYSTOUPENÍ SPOJENÉHO KRÁLOVSTVÍ Z EVROPSKÉ UNIE S OHLEDEM
NÁVRH. VYHLÁŠKA ze dne 2017,
 NÁVRH II. VYHLÁŠKA ze dne 2017, kterou se mění vyhláška č. 54/2004 Sb., o potravinách určených pro zvláštní výživu a o způsobu jejich použití, ve znění pozdějších předpisů Ministerstvo zdravotnictví stanoví
NÁVRH II. VYHLÁŠKA ze dne 2017, kterou se mění vyhláška č. 54/2004 Sb., o potravinách určených pro zvláštní výživu a o způsobu jejich použití, ve znění pozdějších předpisů Ministerstvo zdravotnictví stanoví
JAK ZAJISTIT BEZPEČNĚJŠÍ, ÚČINNĚJŠÍ A INOVATIVNĚJŠÍ ZDRAVOTNICKÉ PROSTŘEDKY?
 HTA saminář, ČVUT FBMI, 16.5.2013 JAK ZAJISTIT BEZPEČNĚJŠÍ, ÚČINNĚJŠÍ A INOVATIVNĚJŠÍ ZDRAVOTNICKÉ PROSTŘEDKY? Návrh zákona o zdravotnických prostředcích a nová role SÚKL Ing. Aleš Martinovský sekce zdravotnických
HTA saminář, ČVUT FBMI, 16.5.2013 JAK ZAJISTIT BEZPEČNĚJŠÍ, ÚČINNĚJŠÍ A INOVATIVNĚJŠÍ ZDRAVOTNICKÉ PROSTŘEDKY? Návrh zákona o zdravotnických prostředcích a nová role SÚKL Ing. Aleš Martinovský sekce zdravotnických
[ 1 ] MUDr. Ivana Koblihová 2009 Státní ústav pro kontrolu léčiv
![[ 1 ] MUDr. Ivana Koblihová 2009 Státní ústav pro kontrolu léčiv [ 1 ] MUDr. Ivana Koblihová 2009 Státní ústav pro kontrolu léčiv](/thumbs/92/109768502.jpg) [ 1 ] [ 2 ] OTC s omezením nová kategorie léčivých přípravků Ivana Koblihová, MUDr. Náměstek ředitele pro odborné činnosti Obsah prezentace [ 3 ] Co znamená OTC s omezením? Obecné možnosti omezení a z
[ 1 ] [ 2 ] OTC s omezením nová kategorie léčivých přípravků Ivana Koblihová, MUDr. Náměstek ředitele pro odborné činnosti Obsah prezentace [ 3 ] Co znamená OTC s omezením? Obecné možnosti omezení a z
Povinnosti odpovědných osob ( výrobců / dovozců ) a distributorů dle Nařízení pro kosmetiku
 Povinnosti odpovědných osob ( výrobců / dovozců ) a distributorů dle Nařízení pro kosmetiku MUDr.Dagmar Jírová,CSc. Národní referenční centrum pro kosmetiku Státní zdravotní ústav Praha 1 Platná legislativa
Povinnosti odpovědných osob ( výrobců / dovozců ) a distributorů dle Nařízení pro kosmetiku MUDr.Dagmar Jírová,CSc. Národní referenční centrum pro kosmetiku Státní zdravotní ústav Praha 1 Platná legislativa
Zákon o lidských tkáních a buňkách
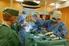 [ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Zákon o lidských tkáních a buňkách 296/2008 Sb. o zajištění jakosti a bezpečnosti lidských tkání a buněk určených k použití u člověka a o změně souvisejících
[ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Zákon o lidských tkáních a buňkách 296/2008 Sb. o zajištění jakosti a bezpečnosti lidských tkání a buněk určených k použití u člověka a o změně souvisejících
Podrobná pravidla postupů při špatném hodnocení. dovážených potravin. Vyhláška AQSIQ č. 43 (2014)
 Podrobná pravidla postupů při špatném hodnocení dovážených potravin Vyhláška AQSIQ č. 43 (2014) I. Všeobecná ustanovení 1. Tato pravidla byla stanovena v souladu se Zákonem Čínské lidové republiky o zdravotní
Podrobná pravidla postupů při špatném hodnocení dovážených potravin Vyhláška AQSIQ č. 43 (2014) I. Všeobecná ustanovení 1. Tato pravidla byla stanovena v souladu se Zákonem Čínské lidové republiky o zdravotní
OPATŘENI OBECNÉ POVAHY
 MINISTERSTVO ZDRAVOTNICTVÍ ČESKÉ REPUBLIKY V Praze dne 7. ledna 2019 Č. j.: MZDR 32517/2017-9/FAR Sp. zn. OLZP: S22/2018 llllllllllllllllllllllllllllllulllllllulllllll MZDRX014T6DT OPATŘENI OBECNÉ POVAHY
MINISTERSTVO ZDRAVOTNICTVÍ ČESKÉ REPUBLIKY V Praze dne 7. ledna 2019 Č. j.: MZDR 32517/2017-9/FAR Sp. zn. OLZP: S22/2018 llllllllllllllllllllllllllllllulllllllulllllll MZDRX014T6DT OPATŘENI OBECNÉ POVAHY
Rozdílová tabulka návrhu předpisu ČR s legislativou EU. Obsah Celex č. Ustanovení (čl., odst., písm., bod., apod.)
 Ustanovení (část,, odst., písm., apod.) Navrhovaný právní předpis (resp. jiný právní předpis) Rozdílová tabulka návrhu předpisu ČR s legislativou EU Obsah Celex č. Ustanovení (čl., odst., písm., bod.,
Ustanovení (část,, odst., písm., apod.) Navrhovaný právní předpis (resp. jiný právní předpis) Rozdílová tabulka návrhu předpisu ČR s legislativou EU Obsah Celex č. Ustanovení (čl., odst., písm., bod.,
Holičství, kadeřnictví, pedikúry a manikúry
 5.6.17.6. Holičství, kadeřnictví, pedikúry a manikúry http://www.guard7.cz/lexikon/lexikon-bozp/sektory-bozp/holicstvikadernictvi-pedikury-a-manikury Pracovní činnosti při provozování kadeřnictví, pedikúry,
5.6.17.6. Holičství, kadeřnictví, pedikúry a manikúry http://www.guard7.cz/lexikon/lexikon-bozp/sektory-bozp/holicstvikadernictvi-pedikury-a-manikury Pracovní činnosti při provozování kadeřnictví, pedikúry,
DOSTUPNOST LÉČIVÝCH PŘÍPRAVKŮ PRO PACIENTY. Ing. Karolína Górecká
 1 DOSTUPNOST LÉČIVÝCH PŘÍPRAVKŮ PRO PACIENTY 2016 Ing. Karolína Górecká 2 TATO PREZENTACE JE URČENA POUZE PRO INTRANET VŠCHT. JE CHRÁNĚNA AUTORSKÝMI PRÁVY A JAKÉKOLIV ZVEŘEJNĚNÍ ČI ZNEUŽITÍ BUDE POSUZOVÁNO
1 DOSTUPNOST LÉČIVÝCH PŘÍPRAVKŮ PRO PACIENTY 2016 Ing. Karolína Górecká 2 TATO PREZENTACE JE URČENA POUZE PRO INTRANET VŠCHT. JE CHRÁNĚNA AUTORSKÝMI PRÁVY A JAKÉKOLIV ZVEŘEJNĚNÍ ČI ZNEUŽITÍ BUDE POSUZOVÁNO
Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah
 2013R1337 CS 17.12.2013 000.002 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 1337/2013 ze dne 13.
2013R1337 CS 17.12.2013 000.002 1 Tento dokument je třeba brát jako dokumentační nástroj a instituce nenesou jakoukoli odpovědnost za jeho obsah B PROVÁDĚCÍ NAŘÍZENÍ KOMISE (EU) č. 1337/2013 ze dne 13.
Nemocniční výjimka pokyn UST-37
 1 Nemocniční výjimka pokyn UST-37 2 Právní rámec Zákon č. 378/2007 Sb., o léčivech a změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Vyhláška č. 228/2008 Sb., o
1 Nemocniční výjimka pokyn UST-37 2 Právní rámec Zákon č. 378/2007 Sb., o léčivech a změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Vyhláška č. 228/2008 Sb., o
Zdravotnické prostředky v klinických hodnoceních. FoEK MUDr. Alice Němcová STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 1 Zdravotnické prostředky v klinických hodnoceních FoEK 27.4.2017 MUDr. Alice Němcová 2 Zdravotnické prostředky v KH 55 odst.(9) zákona o léčivech 378/2007 Sb. platné do nabytí účinnosti nařízení KH (9)
1 Zdravotnické prostředky v klinických hodnoceních FoEK 27.4.2017 MUDr. Alice Němcová 2 Zdravotnické prostředky v KH 55 odst.(9) zákona o léčivech 378/2007 Sb. platné do nabytí účinnosti nařízení KH (9)
KLH-EK-01 ŽÁDOST O STANOVISKO ETICKÉ KOMISE K PROVEDENÍ KLINICKÉHO HODNOCENÍ V ČESKÉ REPUBLICE - požadavky na předkládanou dokumentaci
 KLH-EK-01 ŽÁDOST O STANOVISKO ETICKÉ KOMISE K PROVEDENÍ KLINICKÉHO HODNOCENÍ V ČESKÉ REPUBLICE - požadavky na předkládanou dokumentaci Tento pokyn se vydává za účelem harmonizace činnosti etických komisí
KLH-EK-01 ŽÁDOST O STANOVISKO ETICKÉ KOMISE K PROVEDENÍ KLINICKÉHO HODNOCENÍ V ČESKÉ REPUBLICE - požadavky na předkládanou dokumentaci Tento pokyn se vydává za účelem harmonizace činnosti etických komisí
Parlament se usnesl na tomto zákoně České republiky:
 Strana 2386 Sbírka zákonů č. 202 / 2015 Částka 83 202 ZÁKON ze dne 23. července 2015, kterým se mění zákon č. 40/1995 Sb., o regulaci reklamy a o změně a doplnění zákona č. 468/1991 Sb., o provozování
Strana 2386 Sbírka zákonů č. 202 / 2015 Částka 83 202 ZÁKON ze dne 23. července 2015, kterým se mění zákon č. 40/1995 Sb., o regulaci reklamy a o změně a doplnění zákona č. 468/1991 Sb., o provozování
Nový zákon o zdravotnických prostředcích a zdravotní pojišťovny. Jan Beneš předseda Komise pro ZP SZP ČR Praha, 19. 11. 2014
 Novýzákonozdravotnických prostředcíchazdravotnípojišťovny JanBeneš předsedakomiseprozpszpčr Praha,19.11.2014 1 2 (1) Zdravotnickým prostředkem se rozumí... (2) Při splnění obecného vymezení podle odstavce
Novýzákonozdravotnických prostředcíchazdravotnípojišťovny JanBeneš předsedakomiseprozpszpčr Praha,19.11.2014 1 2 (1) Zdravotnickým prostředkem se rozumí... (2) Při splnění obecného vymezení podle odstavce
Opravdu chceme snížit úroveň ochrany veřejného zdraví?
 Opravdu chceme snížit úroveň ochrany veřejného zdraví? Pavel Dlouhý 3. lékařská fakulta Univerzity Karlovy v Praze Společnost hygieny a komunitní medicíny ČLS JP 1 Kompetence a úkoly kontrolních orgánů
Opravdu chceme snížit úroveň ochrany veřejného zdraví? Pavel Dlouhý 3. lékařská fakulta Univerzity Karlovy v Praze Společnost hygieny a komunitní medicíny ČLS JP 1 Kompetence a úkoly kontrolních orgánů
Úloha SUKL v uplatňování farmakoekonomiky a HTA
 Úloha SUKL v uplatňování farmakoekonomiky a HTA [ 1 ] Činnost SUKL jako organizační slo ky státu Je dána zákonem 378/2007 Sb. ZABEZPEČOVÁNÍ LÉČIV Díl 1 Úkoly orgánů vykonávajících státní správu v oblasti
Úloha SUKL v uplatňování farmakoekonomiky a HTA [ 1 ] Činnost SUKL jako organizační slo ky státu Je dána zákonem 378/2007 Sb. ZABEZPEČOVÁNÍ LÉČIV Díl 1 Úkoly orgánů vykonávajících státní správu v oblasti
SBÍRKA ZÁKONŮ ČESKÉ REPUBLIKY. Profil aktualizovaného znění: Titul původního předpisu: Vyhláška o označování výživové hodnoty potravin
 Stránka č. 1 z 6 SBÍRKA ZÁKONŮ ČESKÉ REPUBLIKY Profil aktualizovaného znění: Titul původního předpisu: Vyhláška o označování výživové hodnoty potravin Citace pův. předpisu: 450/2004 Sb. Částka: 150/2004
Stránka č. 1 z 6 SBÍRKA ZÁKONŮ ČESKÉ REPUBLIKY Profil aktualizovaného znění: Titul původního předpisu: Vyhláška o označování výživové hodnoty potravin Citace pův. předpisu: 450/2004 Sb. Částka: 150/2004
SP-CAU W. Postup při soutěži o nejnižší cenu
 str. 1 z 5 1. CÍL Stanovit postup při soutěži o nejnižší cenu za účelem zajištění plně hrazených léčivých přípravků a potravin pro zvláštní lékařské účely a k zajištění účelného vynakládání prostředků
str. 1 z 5 1. CÍL Stanovit postup při soutěži o nejnižší cenu za účelem zajištění plně hrazených léčivých přípravků a potravin pro zvláštní lékařské účely a k zajištění účelného vynakládání prostředků
ZÁKON ze dne 19. března 1997 o léčivech a o změnách a doplnění některých souvisejících zákonů. Parlament se usnesl na tomto zákoně České republiky:
 79 ZÁKON ze dne 19. března 1997 o léčivech a o změnách a doplnění některých souvisejících zákonů Parlament se usnesl na tomto zákoně České republiky: ČÁST PRVNÍ ZÁKON O LÉČIVECH HLAVA PRVNÍ ÚVODNÍ USTANOVENÍ
79 ZÁKON ze dne 19. března 1997 o léčivech a o změnách a doplnění některých souvisejících zákonů Parlament se usnesl na tomto zákoně České republiky: ČÁST PRVNÍ ZÁKON O LÉČIVECH HLAVA PRVNÍ ÚVODNÍ USTANOVENÍ
VEDENÍ PROVOZNÍ DOKUMENTACE U ZDRAVOTNICKÝCH PROSTŘEDKŮ SE ZVÝŠENÝM RIZIKEM NA OPERAČNÍM SÁLE
 VEDENÍ PROVOZNÍ DOKUMENTACE U ZDRAVOTNICKÝCH PROSTŘEDKŮ SE ZVÝŠENÝM RIZIKEM NA OPERAČNÍM SÁLE Vohrnová Ivana Operační sály Lochotín FN Plzeň OPERAČNÍ SÁLY LOCHOTÍN FN PLZEŇ OS Lochotín: 12 - operačních
VEDENÍ PROVOZNÍ DOKUMENTACE U ZDRAVOTNICKÝCH PROSTŘEDKŮ SE ZVÝŠENÝM RIZIKEM NA OPERAČNÍM SÁLE Vohrnová Ivana Operační sály Lochotín FN Plzeň OPERAČNÍ SÁLY LOCHOTÍN FN PLZEŇ OS Lochotín: 12 - operačních
ZBIERKA ZÁKONOV SLOVENSKEJ REPUBLIKY. Ročník Vyhlásená verzia v Zbierke zákonov Slovenskej republiky
 ZBIERKA ZÁKONOV SLOVENSKEJ REPUBLIKY Ročník 1991 Vyhlásené: 01.11.1991 Vyhlásená verzia v Zbierke zákonov Slovenskej republiky Obsah tohto dokumentu má informatívny charakter. 437 Z Á K O N České národní
ZBIERKA ZÁKONOV SLOVENSKEJ REPUBLIKY Ročník 1991 Vyhlásené: 01.11.1991 Vyhlásená verzia v Zbierke zákonov Slovenskej republiky Obsah tohto dokumentu má informatívny charakter. 437 Z Á K O N České národní
Žádost o zápis do evidence zemědělského podnikatele
 Žádost o zápis do evidence zemědělského podnikatele 1 Identifikační číslo 196 2 Kód 3 Pojmenování (název) životní situace Žádost o zápis do evidence zemědělského podnikatele 4 Základní informace k životní
Žádost o zápis do evidence zemědělského podnikatele 1 Identifikační číslo 196 2 Kód 3 Pojmenování (název) životní situace Žádost o zápis do evidence zemědělského podnikatele 4 Základní informace k životní
Legislativa upravující distribuci léčiv Alena Tomášková MZ ČR, ODBOR FARMACIE
 Legislativa upravující distribuci léčiv Alena Tomášková MZ ČR, ODBOR FARMACIE 5. 12. 2017 Zákon o léčivech - Práva a povinnosti držitele rozhodnutí o registraci - 33 (3) Držitel rozhodnutí o registraci
Legislativa upravující distribuci léčiv Alena Tomášková MZ ČR, ODBOR FARMACIE 5. 12. 2017 Zákon o léčivech - Práva a povinnosti držitele rozhodnutí o registraci - 33 (3) Držitel rozhodnutí o registraci
Aktuální legislativa v oblasti integrované prevence 2014 Základní zpráva
 Aktuální legislativa v oblasti integrované prevence 2014 Základní zpráva Ondřej Skoba Odbor životního prostředí a zemědělství Oddělení hodnocení ekologických rizik Praha, 11.09.2014 Struktura prezentace
Aktuální legislativa v oblasti integrované prevence 2014 Základní zpráva Ondřej Skoba Odbor životního prostředí a zemědělství Oddělení hodnocení ekologických rizik Praha, 11.09.2014 Struktura prezentace
P A R L A M E N T Č E S K É R E P U B L I K Y
 P A R L A M E N T Č E S K É R E P U B L I K Y P o s l a n e c k á s n ě m o v n a 2000 3. volební období 407/3 Pozměňovací návrhy k vládnímu návrhu zákona, kterým se mění zákon č. 79/1997 Sb., o léčivech
P A R L A M E N T Č E S K É R E P U B L I K Y P o s l a n e c k á s n ě m o v n a 2000 3. volební období 407/3 Pozměňovací návrhy k vládnímu návrhu zákona, kterým se mění zákon č. 79/1997 Sb., o léčivech
Požadavky na farmaceutickou dokumentaci
 1 Požadavky na farmaceutickou dokumentaci Druhá část Ing. Lucie Zmatlíková Oddělení posuzování farmaceutické dokumentace 2 Obsah prezentace Žádost o klinické hodnocení (Clinical Trial Application Form)
1 Požadavky na farmaceutickou dokumentaci Druhá část Ing. Lucie Zmatlíková Oddělení posuzování farmaceutické dokumentace 2 Obsah prezentace Žádost o klinické hodnocení (Clinical Trial Application Form)
Státní ústav pro kontrolu léčiv
 [ 1 ] [ 2 ] Změna zákona o léčivech Eva Niklíčková Odd. SVP [ 3 ] Směrnice 2011/62/EU ze dne 8. června 2011, kterou se mění směrnice 2001/83/ES o kodexu Společenství týkajícím se humánních léčivých přípravků,
[ 1 ] [ 2 ] Změna zákona o léčivech Eva Niklíčková Odd. SVP [ 3 ] Směrnice 2011/62/EU ze dne 8. června 2011, kterou se mění směrnice 2001/83/ES o kodexu Společenství týkajícím se humánních léčivých přípravků,
Jak vyhledávat v databázi léků.
 Jak vyhledávat v databázi léků www.sukl.cz Kde najít databázi léků? Databázi léků naleznete na webové stránce Státního ústavu pro kontrolu léčiv www.sukl.cz na titulní straně v levém sloupci (viz obr.
Jak vyhledávat v databázi léků www.sukl.cz Kde najít databázi léků? Databázi léků naleznete na webové stránce Státního ústavu pro kontrolu léčiv www.sukl.cz na titulní straně v levém sloupci (viz obr.
NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU)
 19.6.2014 L 179/17 NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 664/2014 ze dne 18. prosince 2013, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 1151/2012, pokud jde o stanovení symbolů
19.6.2014 L 179/17 NAŘÍZENÍ KOMISE V PŘENESENÉ PRAVOMOCI (EU) č. 664/2014 ze dne 18. prosince 2013, kterým se doplňuje nařízení Evropského parlamentu a Rady (EU) č. 1151/2012, pokud jde o stanovení symbolů
Dopady BPR legislativy na výrobce a spotřebitele dezinfekčních přípravků
 Dopady BPR legislativy na výrobce a spotřebitele dezinfekčních přípravků 11. Mezinárodní kongres 23.- 24.05.2019 Brno Ing. Jarmila Fafílková Obsah 1. Legislativní rámec 2. Terminologie 3. Produktové typy
Dopady BPR legislativy na výrobce a spotřebitele dezinfekčních přípravků 11. Mezinárodní kongres 23.- 24.05.2019 Brno Ing. Jarmila Fafílková Obsah 1. Legislativní rámec 2. Terminologie 3. Produktové typy
2012 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 2 SÚKL A LÉKÁRNY - NEPŘÁTELÉ NEBO SPOLUPRACOVNÍCI? Zdeněk Blahuta, ředitel SÚKL XV. Beskydský slet lékárníků, Malenovice 3 Počet lékáren v čase 3000 2500 235 240 247 244 243 253 250 243 241 248 2000 1500
2 SÚKL A LÉKÁRNY - NEPŘÁTELÉ NEBO SPOLUPRACOVNÍCI? Zdeněk Blahuta, ředitel SÚKL XV. Beskydský slet lékárníků, Malenovice 3 Počet lékáren v čase 3000 2500 235 240 247 244 243 253 250 243 241 248 2000 1500
Vědecký výbor pro potraviny
 Vědecký výbor pro potraviny Klasifikace: Draft Pro vnitřní potřebu VVP Oponovaný draft Pro vnitřní potřebu VVP Finální dokument Pro oficiální použití Deklasifikovaný dokument X Pro veřejné použití Název
Vědecký výbor pro potraviny Klasifikace: Draft Pro vnitřní potřebu VVP Oponovaný draft Pro vnitřní potřebu VVP Finální dokument Pro oficiální použití Deklasifikovaný dokument X Pro veřejné použití Název
K VYDÁNÍ STANOVISKA EK
 Jednání Lokální etické komise (LEK) Nemocnice Mělník (jednací řád) o nové žádosti o udělení souhlasu s provedením klinického hodnocení léčivého přípravku nebo s klinickou zkouškou zdravotnického prostředku
Jednání Lokální etické komise (LEK) Nemocnice Mělník (jednací řád) o nové žádosti o udělení souhlasu s provedením klinického hodnocení léčivého přípravku nebo s klinickou zkouškou zdravotnického prostředku
MZ A POHLED NA LÉKOVÉ INTERAKCE. PharmDr. Alena Tomášková 24. únor 2015
 MZ A POHLED NA LÉKOVÉ INTERAKCE PharmDr. Alena Tomášková 24. únor 2015 Lékové interakce O lékové interakci mluvíme tehdy, když při současném podávání dvou nebo více léčivých přípravků dojde ke změně účinku
MZ A POHLED NA LÉKOVÉ INTERAKCE PharmDr. Alena Tomášková 24. únor 2015 Lékové interakce O lékové interakci mluvíme tehdy, když při současném podávání dvou nebo více léčivých přípravků dojde ke změně účinku
STRUKTURA NÁZVŮ LP DLE REG-29 VERZE 4 A JEJÍ PRAKTICKÉ DOPADY
 1 STRUKTURA NÁZVŮ LP DLE REG-29 VERZE 4 A JEJÍ PRAKTICKÉ DOPADY Ing. Anna Ondruchová Sekce registrací Struktura názvů LP dle REG-29 verze 4 a její praktické dopady 2 Obsah: REG-29 verze 4 Nové registrace
1 STRUKTURA NÁZVŮ LP DLE REG-29 VERZE 4 A JEJÍ PRAKTICKÉ DOPADY Ing. Anna Ondruchová Sekce registrací Struktura názvů LP dle REG-29 verze 4 a její praktické dopady 2 Obsah: REG-29 verze 4 Nové registrace
STAHOVÁNÍ LÉČIVÉHO PŘÍPRAVKU CALCIUM PANTOTHENICUM ZENITVA METODICKÝ POSTUP PRO LÉKÁRNY, LÉKAŘE A DISTRIBUTORY
 STAHOVÁNÍ LÉČIVÉHO PŘÍPRAVKU CALCIUM PANTOTHENICUM ZENITVA METODICKÝ POSTUP PRO LÉKÁRNY, LÉKAŘE A DISTRIBUTORY 1. Kterých léčivých přípravků se stahování týká? Stahování se týká všech šarží s platnou dobou
STAHOVÁNÍ LÉČIVÉHO PŘÍPRAVKU CALCIUM PANTOTHENICUM ZENITVA METODICKÝ POSTUP PRO LÉKÁRNY, LÉKAŘE A DISTRIBUTORY 1. Kterých léčivých přípravků se stahování týká? Stahování se týká všech šarží s platnou dobou
SP-CAU W. Metodika stanovení úhrady individuálně připravovaných parenterálních výživ pro domácí použití
 str. 1 z 4 1. CÍL Stanovit metodiku pro postup stanovení úhrady individuálně připravovaných léčivých přípravků skupiny (dále DPV). 2. UŽIVATELÉ Postup je závazný pro pracovníky sekce cenové a úhradové
str. 1 z 4 1. CÍL Stanovit metodiku pro postup stanovení úhrady individuálně připravovaných léčivých přípravků skupiny (dále DPV). 2. UŽIVATELÉ Postup je závazný pro pracovníky sekce cenové a úhradové
Parlament se usnesl na tomto zákoně České republiky: ČÁST PRVNÍ ZÁKON O LÉČIVECH HLAVA PRVNÍ ÚVODNÍ USTANOVENÍ. Účel zákona
 PLATNÉ ZNĚNÍ ZÁKONA Č. 79/1997 SB., O LÉČIVECH A O ZMĚNÁCH A DOPLNĚNÍ NĚKTERÝCH SOUVISEJÍCÍCH ZÁKONŮ, VE ZNĚNÍ POZDĚJŠÍCH PŘEDPISŮ, A ZÁKON Č. 368/1992 SB., O SPRÁVNÍCH POPLATCÍCH, VE ZNĚNÍ POZDĚJŠÍCH
PLATNÉ ZNĚNÍ ZÁKONA Č. 79/1997 SB., O LÉČIVECH A O ZMĚNÁCH A DOPLNĚNÍ NĚKTERÝCH SOUVISEJÍCÍCH ZÁKONŮ, VE ZNĚNÍ POZDĚJŠÍCH PŘEDPISŮ, A ZÁKON Č. 368/1992 SB., O SPRÁVNÍCH POPLATCÍCH, VE ZNĚNÍ POZDĚJŠÍCH
Návod k aplikaci nařízení vlády č. 317/2012 Sb., kterým se stanoví formulář dokladu o původu některých druhů lihu, destilátu a některých druhů lihovin
 Návod k aplikaci nařízení vlády č. 317/2012 Sb., kterým se stanoví formulář dokladu o původu některých druhů lihu, destilátu a některých druhů lihovin revize ke dni 2.10.12 Prokázání původu každá šarže
Návod k aplikaci nařízení vlády č. 317/2012 Sb., kterým se stanoví formulář dokladu o původu některých druhů lihu, destilátu a některých druhů lihovin revize ke dni 2.10.12 Prokázání původu každá šarže
Co přináší novela zákona o léčivech? PharmDr. Alena Tomášková odbor farmacie
 Co přináší novela zákona o léčivech? PharmDr. Alena Tomášková odbor farmacie Zákon o léčivech Návrh zákona, kterým se mění zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů (zákon
Co přináší novela zákona o léčivech? PharmDr. Alena Tomášková odbor farmacie Zákon o léčivech Návrh zákona, kterým se mění zákon č. 378/2007 Sb., o léčivech a o změnách některých souvisejících zákonů (zákon
