Průvodce aplikací a monitoringem pro zdravotnické pracovníky
|
|
|
- Martin Vaněk
- před 9 lety
- Počet zobrazení:
Transkript
1 Průvodce aplikací a monitoringem pro zdravotnické pracovníky Rychlá odpověď. Rychlá volba.
2
3 Průvodce aplikací a monitoringem pro zdravotnické pracovníky Cimzia je, v kombinaci s methotrexatem, indikována pro léčbu středně závažné až závažné aktivní formy revmatoidní artritidy (RA) u dospělých pacientů, u kterých je odpověď na léčbu antirevmatiky (DMARD), včetně methotrexatu, nedostatečná. Cimzii lze podávat v monoterapii v případě nesnášenlivosti methotrexatu nebo je-li pokračování léčby methotrexatem nevhodné. Cimzia, v kombinaci s methotrexatem, snižuje rychlost progrese poškození kloubu hodnocené rentgenem a zlepšuje fyzickou funkci. Cimzia Cimzia k léčbě revmatoidní artritidy (RA) je podávána jako subkutánní injekce. Tento průvodce poskytuje informace o správné aplikaci Cimzie a potřebě monitoringu po aplikaci Cimzie. Tato příručka je součástí sady obsahující informačněvzdělávací materiály, jejímž obsahem jsou také: Kartička pro upozornění pacienta určeno pro všechny pacienty léčené Cimzií; Informace pro pacienta určeno pro všechny pacienty léčené Cimzií; Informace pro lékaře určeno pro všechny lékaře předepisující Cimzii. Pokud potřebujete další informace o bezpečném podání Cimzie, kontaktujte, prosím, předepisujícího lékaře. Po vhodném zaškolení v technice aplikace injekcí si mohou pacienti Cimzii aplikovat sami, pokud lékař usoudí, že je to vhodné, a zabezpečí následný lékařský dohled dle potřeby. Pacientům, kteří chtějí být zaškoleni v technice aplikace injekce sami sobě, je určena zvláštní příručka. Tato příručka je též určena k podpoře při samostatné aplikaci injekcí pacientem a pro školení techniky pacientů, radí pacientům ohledně sledování nežádoucích účinků a obsahuje vhodná opatření pro případ výskytu nežádoucích účinků. Revmatoidní artritida Revmatoidní artritida (RA) je chronické systémové zánětlivé onemocnění s významnou morbiditou a mortalitou. Toto onemocnění je charakterizováno zánětem synoviálních kloubů, což vede k bolesti, otokům a kloubnímu poškození se sekundárními deformitami a progredující invaliditou, chronické únavě a také zhoršení fyzických funkcí pacienta a se zdravím spojené kvality života. Cimzia - přehled Cimzia je rekombinantní humanizovaný Fab fragment protilátky proti tumor nekrotizujícímu faktoru alfa (TNFα) konjugovaný s polyethylenglykolem (PEG). Cimzia je inhibitor TNFα s vysokou afinitou k humánnímu TNFα (klíčový prozánětlivý cytokin s ústřední rolí v zánětlivých procesech). Cimzia neobsahuje oblast krystalizovatelného fragmentu (Fc), která je normálně součástí kompletní protilátky, a proto nevede k fixaci komplementu a projevům na protilátkách závislé buňkami zprostředkované cytotoxicity in vitro. Nenavozuje apoptózu in vitro u humánních monocytů nebo lymfocytů z periferní krve, nebo degranulaci neutrofilů. Indikace přípravku Cimzia Cimzia je, v kombinaci s methotrexatem (MTX), indikována pro léčbu středně závažné až závažné aktivní formy revmatoidní artritidy (RA) u dospělých pacientů, u kterých je odpověď na léčbu antirevmatiky (DMARD), včetně methotrexatu, nedostatečná. Cimzii lze podávat v monoterapii v případě nesnášenlivosti methotrexatu nebo je-li pokračování léčby methotrexatem nevhodné. Cimzia, v kombinaci s methotrexatem, snižuje rychlost progrese poškození kloubu hodnocené rentgenem a zlepšuje fyzickou funkci. Cimzia musí být podávána jako subkutánní injekce Cimzia musí být podávána subkutánně. Léčba Cimzií musí být zahájena a sledována lékařem se zkušenostmi v diagnostice a léčbě RA. Pacienti musí obdržet Kartičku pro upozornění pacienta, která obsahuje důležité bezpečnostní informace. Tuto kartičku by měli pacienti nosit neustále při sobě a ukázat ji každému lékaři, který je bude v průběhu léčby Cimzií a ještě 5 měsíců po ukončení léčby ošetřovat. Kontraindikace Cimzia je kontraindikována v případech: hypersenzitivity na léčivou látku nebo na kteroukoli
4 pomocnou látku tohoto přípravku; aktivní tuberkulózy nebo jiné závažné infekce jako sepse nebo oportunní infekce; středně závažného až závažného srdečního selhání (NYHA třída III/IV). Dávkování Cimzie Doporučená počáteční dávka Cimzie je pro dospělého pacienta s RA 400 mg (jako 2 injekce po 200 mg/den) v týdnech 0, 2 a 4. Pak následují udržovací dávky 200 mg každé 2 týdny, počínaje týdnem 6. Pokud je třeba, podávání MTX by se nemělo přerušovat. Dostupné údaje naznačují, že klinické odpovědi je obvykle dosaženo během 12 týdnů léčby. Pokračování v léčbě je třeba znovu pečlivě zvážit u pacientů, kteří nevykazují žádné známky terapeutického přínosu během prvních 12 týdnů léčby. Balení Cimzie Cimzia je podávána subkutánně. Cimzia je dodávána v předplněné injekční stříkačce. Každé balení obsahuje: 2 jednorázové skleněné předplněné 1 ml injekční stříkačky s pevnou jehlou 25G, z nichž každá obsahuje 200 mg (1 ml) Cimzie; 2 alkoholové tampony. Jedna předplněná injekční stříkačka obsahuje 200 mg Cimzie. Jedna dávka 200 mg vyžaduje subkutánní podání 1 ml injekce. Jedna dávka 400 mg vyžaduje podání dvou subkutánních 1 ml injekcí. Jsou k dispozici balení se 2 stříkačkami a vícečetné balení obsahující 6 injekčních stříkaček (3 balení po 2). Na trhu nemusí být všechny velikosti balení. Uchovávání Cimzie Cimzia se uchovává v chladničce při teplotě 2 až 8 C. Chraňte Cimzii před mrazem. Nepoužívejte po datu použitelnosti uvedeném na obalu. Doba použitelnosti je 18 měsíců. Uchovávejte předplněnou injekční stříkačku v krabičce, aby byl přípravek chráněn před světlem. Uchovávejte mimo dosah a dohled dětí. Interakce s jinými léčivými přípravky Současná léčba MTX, kortikosteroidy, nesteroidními protizánětlivými léky (NSA) a analgetiky neměla podle souboru farmakokinetických analýz žádný vliv na farmakokinetiku Cimzie. Kombinace Cimzie a léčivých látek anakinra nebo abatacept se nedoporučuje. Než je Cimzie podána Kontaktujte předepisujícího lékaře před podáním Cimzie, pokud: se pacient domnívá, že má infekci. Cimzia by neměla být podána pacientům, pokud mají jakoukoli infekci; je pacient léčen na infekci; má pacient příznaky infekce jako horečku, kašel nebo projevy podobné chřipce; pacient má nebo měl hepatitidu B; pacient má na těle otevřené rány nebo odřeniny; pacient trpí mnoha infekcemi nebo má infekci, která se neustále vrací; je pacient HIV pozitivní; pacient má TBC nebo byl v blízkém kontaktu s osobou trpící TBC; se pacient narodil, žil nebo v minulosti cestoval do zemí, kde je vyšší riziko nákazy TBC; se pacient narodil nebo žil v zemích se zvýšeným rizikem nákazy určitými plísňovými infekcemi (histo plazmóza, kokcidiomykóza nebo blastomykóza); pacient má jakýkoli typ rakoviny; pacient trpí srdečním selháním - Cimzia nemá být užívána pacienty se středně těžkým až těžkým srdečním selháním; má pacient záchvaty, trpí necitlivostí či brněním nebo onemocněním napadajícím nervový systém, jako je např. roztroušená skleróza; má pacient být očkován - Pacienti by během léčby Cimzií neměli být očkováni živou či atenuovanou vakcínou; jde o pacientku těhotnou, těhotenství plánující či kojící - Cimzia nebyla zkoumána u těhotných a kojících žen; má pacient plánovaný chirurgický či stomatologický zákrok - Pacienti vyžadující chirurgický či stomatologický zákrok a zároveň léčení Cimzií vyžadují pečlivé sledování kvůli infekcím; jsou u pacienta plánována koagulační vyšetření - Cimzia může způsobit, že tato vyšetření nesprávně indikují prodlouženou dobu srážlivosti, i když tomu tak není;
5 pacient je alergický na jakoukoli ze složek Cimzie; pacient užívá Kineret (anakinra) nebo Orencii (abatacept) - současné podávání těchto přípravků a Cimzie zvyšuje pravděpodobnost vzniku závažných infekcí. Nepoužívejte předplněnou stříkačku Cimzia, pokud je na obalu či označení stříkačky napsán jiný název než Cimzia ; uplynula doba použitelnosti uvedená na obalu (doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce); je poškozen obal nebo je bezpečnostní přelepka na horní i spodní části obalu porušena nebo zcela chybí; byla předplněná stříkačka vystavena mrazu nebo přímému slunci; přípravek ve stříkačce není čirý až světle žlutý nebo obsahuje velké zabarvené částice. V závislosti na předepsané dávce vyjměte jednu, nebo dvě předplněné injekční stříkačky Cimzia a alkoholové tampony z chladničky. Pokud je v balení ještě další stříkačka, vraťte ji neprodleně do krabičky a krabičku zpět do chladničky. Před podáním injekce nechte přípravek ve stříkačce vytemperovat při pokojové teplotě. To trvá asi 30 minut. Nepokoušejte se stříkačku zahřívat. Předplněnou injekční stříkačku před použitím neprotřepávejte. Výběr a příprava místa pro aplikaci Příprava na podání injekce Na jednu 200 mg injekci použijete: 1 předplněnou injekční stříkačku s jehlou, 1 alkoholový tampón. Cimzia může být aplikována pacientovi do oblasti břicha či stehen. Pokud podáváte více než jednu injekci, každá z nich by měla být podána do jiného místa na břiše či stehnech. Před podáním injekce si pečlivě umyjte ruce. Pokaždé zvolte jiné místo na břiše a/nebo stehnech. Nikdy injekci nepodávejte do míst, kde je kůže křehká, zhmožděná, začervenalá, tvrdá nebo do míst, kde má pacient jizvy nebo strie. Dbejte na střídání míst aplikace mezi břichem a stehny, aby bylo zabráněno vzniku infekce. Může Vám pomoci vedení poznámek o předchozích pacientových místech aplikace injekcí. Po vybrání místa aplikace otřete toto místo a jeho okolí alkoholový tampónem. Dbejte na to, abyste se místa znovu nedotkli až do doby, kdy budete připraveni na aplikaci injekce.
6 Aplikace injekce Sejměte krytku jehly zatažením za plastové očko. Dbejte na to, abyste se jehly nedotkli a také aby se jehla ničeho nedotkla. Odložte krytku jehly. Jednou rukou držte stříkačku jehlou dolů; dbejte na to, abyste se nedotkli jehly nebo se jehla čehokoli nedotkla. Druhou rukou stiskněte záhyb pacientovy očištěné kůže a subkutánně zaveďte jedním rychlým krátkým pohybem jehlu ve zhruba 45 úhlu. Stiskněte píst a aplikujte roztok. Vyprázdnění stříkačky může trvat až 10 vteřin. Když je stříkačka prázdná, opatrně vyjměte jehlu z kůže v tom samém úhlu, ve kterém byla zavedena. Uvolněte stisknutí kůže. Přitiskněte čistý vatový tampón nebo gázový čtvereček na několik vteřin přes místo vpichu. Poučte pacienta, aby si místo vpichu netřel. Pokud je třeba, můžete místo vpichu přelepit náplastí. Stříkačku znovu NEPOUŽÍVEJTE, krytku jehly NEVRACEJTE zpátky na jehlu. Vyhoďte použitou předplněnou stříkačku a jehlu do zvláštní nádoby odolné proti propíchnutí. Likvidace jehel a stříkaček Podržte stříkačku jehlou nahoru a jemně na ni poklepejte, aby se všechny bublinky dostaly nahoru. Pomalu stlačte píst, dokud není vytlačen všechen vzduch. Přestaňte v okamžiku, kdy se na hrotu jehly objeví malá kapka. Jehly a stříkačky musí být odhazovány do nádob odolných vůči propíchnutí (nádoba na ostré předměty). Když je nádoba zhruba ze dvou třetin plná, uzavřete víčko. Nádoba s použitými jehlami a stříkačkami se vrací do zdravotnického zařízení. Nevyhazujte nádobu do směsného odpadu či recyklace.
7 Opomenutá dávka Jestliže pacient zapomene si podat dávku Cimzie, je nutné, aby si dávku podal ihned, jak si na to vzpomene. Následující dávky si pak aplikuje každé 2 týdny, jak bylo původně určeno. Aplikace injekce pacientem Po vhodném zaškolení injekční techniky si pacienti mohou přípravek aplikovat sami v případě, že lékař usoudí, že je to vhodné, a jsou zajištěny lékařské kontroly dle potřeby. Byla vytvořena samostatná příručka pro pacienty, kteří mají zájem o trénink injekční techniky. Reakce v místě podání Nakládání s nepoužitým přípravkem a odpadním materiálem Všechen nepoužitý přípravek a odpadní materiál musí být zlikvidován v souladu s místními požadavky. Selhání injekční stříkačky Pokud dojde k selhání mechanismu stříkačky, kontaktujte medicínské oddělení společnosti UCB v ČR. Chyby při podávání Všechny chyby v podávání Cimzie musí být hlášeny ošetřujícímu lékaři a místnímu zástupci držitele rozhodnutí o registraci UCB s.r.o., Palác Karlín, Thámova 11-13, Praha 8, info.prague@ucb.com, telefon , fax nebo oddělení farmakovigilance Státního ústavu pro kontrolu léčiv ( Rozlití přípravku Pokud během podávání injekce dojde k rozlití jakéhokoli množství přípravku, kontaktujte, prosím, ošetřujícího lékaře a medicínské oddělení společnosti UCB v ČR. V placebem kontrolovaných studiích s RA se u 6,4% pacientů léčených Cimzií objevily reakce v místě vpichu (erytém, svědění, hematom, bolest, otok, podlitiny), ve skupině s placebem to bylo 6,5%. Bolest v místě vpichu byla pozorována u 1,5% pacientů léčených Cimzií, přičemž žádný z těchto případů nebyl důvodem k ukončení účasti ve studii. Nežádoucí účinky během a krátce po podání Cimzie Závažné hypersenzitivní reakce (včetně akutní reakce na injekci a opožděné systémové reakce) po podání Cimzie byly ve studiích hlášeny vzácně. Jestliže dojde k závažné reakci, je nutno podávání Cimzie ihned přerušit a zahájit vhodnou léčbu. Informace o podání Cimzie pacientům se závažnou hypersenzitivní reakcí na antagonisty TNF v anamnéze jsou omezené; u těchto pacientů je třeba zvláštní pozornosti. Monitoring pacientů a důležité bezpečnostní informace o Cimzii Jako všichni antagonisté TNF má Cimzia možné nežádoucí účinky. Proto je důležité, aby byli pacienti po podání přípravku monitorováni za účelem optimalizace užívání Cimzie. Úplný seznam nežádoucích účinků si, prosím, vyhledejte v Souhrnu údajů o přípravku.
8 Pacienti, kteří si injekce aplikují sami, musí být poučeni za pomoci této příručky o potřebě sledování nežádoucích účinků. Další informace pacient nalezne v pacientské příručce Informace pro pacienta. Riziko závažných infekcí U pacientů léčených antagonisty TNF, včetně Cimzie, byly hlášeny závažné infekce (bakteriální, virové i plísňové), včetně sepse, TBC (včetně miliární, diseminované a extrapulmonální) a oportunních infekcí (např. histoplazmóza, nokardióza, kandidiáza). V placebem kontrolovaných klinických studiích se objevilo více nových případů závažných infekcí ve skupině s Cimzií (0,06 na pacient-rok, všechny dávky) než ve skupině s placebem (0,02 na pacient-rok). Některé z těchto případů byly smrtelné. U pacientů by měly být pozorně sledovány případné projevy a příznaky nových infekcí, včetně TBC, během léčby a 5 měsíců po léčbě Cimzií při uvážení dlouhého poločasu přípravku. Před zahájením léčby by měl být zvážen možný vznik TBC u pacientů, kteří měli před zahájením léčby Cimzií negativní test na latentní TBC. Pokud byla před zahájením nebo během léčby Cimzií diagnostikována aktivní TBC, léčba Cimzií nesmí být zahájena, resp. musí být ukončena. Pacienty je třeba poučit, aby vyhledali lékařskou pomoc, pokud se u nich během léčby Cimzií nebo po jejím ukončení projeví příznaky/projevy naznačující možnou infekci TBC. Ty zahrnují: nedávné a probíhající infekce, předchozí a stávající problémy dýchacího ústrojí, noční pocení či jiné systémové projevy TBC, neprospívání/úbytek tělesné hmotnosti. Pacienty je třeba poučit, aby vyhledali lékařskou pomoc v případě: rodinného či jiného kontaktu s osobou trpící TBC, očkování proti TBC v anamnéze (v nedávné minulosti), pozitivního PPD testu, nedávných cest do zemí se zýšeným rizikem nákazy TBC nebo vysokým výskytem infekcí oportunními patogeny. V případě závažné infekce či sepse musí být kontaktován ošetřující lékař, který zváží přerušení léčby Cimzií. Reaktivace hepatitidy B Antagonisté TNF, včetně Cimzie, jsou spojováni s reaktivací viru hepatitidy B (HBV) u pacientů, kteří jsou jeho chronickými přenašeči. Je třeba, aby pacient vyhledal okamžitě lékařskou pomoc, pokud se u něj projeví kterýkoli z následujících příznaků: pacient se celkově necítí dobře, ztráta chuti k jídlu, únava, horečka, kožní vyrážka, bolest kloubů. Malignity (včetně lymfomu a leukemie) Potenciální role léčby antagonisty TNF ve vývoji malignit není známa. V klinických studiích bylo hlášeno více případů lymfomů a jiných malignit u pacientů s antagonisty TNF než u pacientů s placebem. RA pacienti s dlouhodobým, vysoce aktivním zánětlivým onemocněním podléhají zvýšenému riziku vzniku lymfomu, což komplikuje zhodnocení rizika. Dle současných zkušeností není možné riziko vzniku lymfomu či jiných malignit u pacientů léčených antagonisty TNF vyloučit. U pacientů je třeba sledovat projevy lymfomu, včetně: zduření lymfatických uzlin na krku, v podpaží, tříslech a jiných místech, nadměrného pocení, zvláště během nočního spánku, horečky, intenzivního svědění, nechtěného úbytku na váze. Ve výzkumné klinické studii hodnotící využití dalšího antagonisty TNF, infliximabu, u pacientů se středně závažnou až závažnou formou chronické obstrukční plicní nemoci (CHOPN) byl hlášen větší výskyt malignit, zejména plic, hlavy a krku, u pacientů s infliximabem než u pacientů z kontrolní skupiny. Všichni pacienti byli těžcí kuřáci. Proto je třeba dbát zvláštní opatrnosti u pacientů s CHOPN, stejně jako u pacientů se zvýšeným rizikem vzniku malignit v důsledku těžkého kouření. Je třeba, aby pacienti okamžitě vyhledali lékařskou pomoc, pokud se u nich projeví příznaky naznačující vznik malignit. Městnavé srdeční selhání Bylo pozorováno zhoršení městnavého srdečního selhání (CHF Congestive Heart Failure) při léčbě antagonisty TNF, včetně Cimzie. Při léčbě antagonisty TNF byl též pozorován vznik nových případů CHF. U pacientů je třeba sledovat projevy CHF, včetně: kašle, dušnosti, otoků nohou a kotníků,
9 nárůstu tělesné hmotnosti. Je třeba, aby pacienti okamžitě vyhledali lékařskou pomoc, pokud se u nich projeví příznaky naznačující CHF. Neurologické příhody Použití antagonistů TNF, včetně Cimzie, bylo spojeno se vzácnými případy nového vypuknutí nebo exacerbace demyelinizačního onemocnění. U pacientů je třeba sledovat projevy demyelinizačního onemocnění, zejména roztroušené sklerózy, včetně: závratí, necitlivosti nebo brnění, poruchy vidění, slabosti rukou a nohou. Je třeba, aby pacienti okamžitě vyhledali lékařskou pomoc, pokud se u nich projeví některý z těchto příznaků. Hematologické reakce Při léčbě Cimzií byly hlášeny případy zhoršení cytopenie. Pacienty je třeba monitorovat kvůli projevům cytopenie. Je třeba, aby pacienti okamžitě vyhledali lékařskou pomoc, jestliže se u nich objeví projevy spojované s krevními problémy, včetně: přetrvávající horečky, snadno se tvořících podlitin, snadného vzniku krvácení, obzvláštní bledosti. Autoimunita, lupus a lupusu podobná onemocnění Léčba Cimzií může vést ke vzniku autoprotilátek, méně často k vývoji autoimunitního onemocnění syndromu napodobujícího systémový lupus (lupus-like syndrom). Je třeba, aby pacienti okamžitě vyhledali lékařskou pomoc, jestliže se u nich objeví projevy připomínající systémový lupus, včetně: dušnosti, bolesti kloubů, vyrážky na tvářích a pažích, která se zhoršuje po vystavení slunci. Hypersenzitivita Závažné hypersenzitivní reakce po podání Cimzie byly ve studiích hlášeny vzácně. Jestliže dojde k závažné reakci, je nutno podávání Cimzie ihned přerušit a zahájit vhodnou léčbu. U pacientů, kteří prodělali závažnou hypersenzitivní reakci po podání jiného antagonisty TNF, je nutná opatrnost. Úplný seznam nežádoucích účinků a další informace týkající se Cimzie najdete v Souhrnu údajů o přípravku. Klinická účinnost Cimzie Cimzia byla zkoumána u 2367 pacientů s RA v kontrolovaných a otevřených studiích po dobu až 57 měsíců. Účinnost a bezpečnost Cimzie byly hodnoceny ve dvou randomizovaných, placebem kontrolovaných, dvojitě zaslepených studiích u pacientů ve věku od 18 let, s aktivní RA diagnostikovanou podle kritérií Americké revmatologické společnosti (ACR = American College of Rheumatology): RAPID 1 (52týdenní studie) 1 a RAPID 2 (24týdenní studie) 2. Cimzia byla podávána subkutánně v kombinaci s perorálním methotrexatem (MTX). Bylo požadováno, aby pacienti užívali MTX po dobu nejméně 6 měsíců a stálou dávku alespoň 10 mg týdně po dobu 2 měsíců před zahrnutím do obou studií. ACR odpověď V porovnání s placebem bylo v obou klinických studiích dosaženo statisticky významně vyšší odpovědi ACR 20 od 1.týdne. Statisticky významně vyšší odpovědi ACR 50 bylo dosahováno od 2.týdne. Odpovědi se udržely až do 52.týdne (RAPID 1) a 24.týdne (RAPID 2). Z 783 pacientů, na počátku randomizovaných k aktivní léčbě ve studii Rapid 1, 508 pacientů dokončilo 52 týdnů placebem kontrolovanou léčbu a započalo otevřenou prodlouženou studii. Z těchto pacientů 427 ukončilo 2letou otevřenou studii, což znamená celkovou léčbu Cimzií po dobu 148 týdnů. Pozorované ACR skóre v tomto časovém bodě bylo 91%. Únava a fyzické funkce RAPID 1 a RAPID 2: Pacienti léčení Cimzií uváděli v porovnání s placebem významné zlepšení ve fyzickém fungování při hodnocení dotazníkem Health Assessment Questionnaire Disability Index (HAQ-DI), už v 1.týdnu a pak v průběhu celé studie až do jejího konce (52.týden u RAPID 1 a 24.týden u RAPID 2). Zlepšení fyzického fungování bylo udrženo po dobu alespoň 2 let v otevřené prodloužené studii k RAPID 1. Pacienti léčení Cimzií uváděli v porovnání s placebem
10 výrazné zlepšení v únavě, která byla hodnocena dle FAS (Fatigue Assmessment Scale), už v 1.týdnu a pak v průběhu celé studie až do jejího konce (52.týden u RAPID 1 a 24.týden u RAPID 2). SF-36 V obou klinických studiích uváděli pacienti významně vyšší zlepšení v SF-36 PCS a MCS (= Physical and Mental Component Summaries = Souhrn fyzických a mentálních komponent), a ve všech skóre doménách indikujících zlepšení kvality života související se zdravím. Zlepšení kvality života se udržovalo po celé 2 roky v otevřené prodloužené studii k RAPID 1. Reference: 1. Keystone E, van der Neujde D, Mason D J ret al. Certolizumab pegol plus methotrexate is significantly more effective than placebo in active rheumatoid arthritis: findings of a fifty- two week, phase III, multicenter, randomized, double- blind, placebo controlled study. Arthritis Rheum 2008;58: Smolen J, Landewé RB, Mease P, et al. Efficacy and safety of certolizumab pegol plus methotrexate in active rheumatoid arthritis: the RAPID 2 study. A randomised controlled trial. Ann Rheum Dis. 2009;68: RTG odpověď V RAPID 1 byl rentgenologicky hodnocen stupeň strukturálního kloubního poškození v 52.týdnu oproti výchozímu stavu a byl vyjádřen jako změna mtss (Total Sharp Score) a jeho komponent, erozního skóre a skóre zúžení kloubní štěrbiny (skóre JSN = joint space narrowing score). Ve 24.týdnu a 52.týdnu prokázali pacienti užívající Cimzii významně menší radiografickou progresi než pacienti užívající placebo. V 52.týdnu nevykazovalo ve skupině placeba 52% pacientů žádnou rentgenologickou progresi (mtss 0,0 = modifikovaný Total Sharp Score) ve srovnání s 69% pacientů ve skupině léčených Cimzií 200 mg. Z 783 pacientů na počátku randomizovaných k aktivní léčbě ve studii RAPID 1, 508 dokončilo 52 týdnů placebem kontrolovanou léčbu a započalo otevřenou prodlouženou klinickou studii. Setrvalá inhibice progrese strukturálního poškození byla pozorována ve skupině 449 pacientů, kteří dokončili 2letou léčbu Cimzií (RAPID 1 a otevřená prodloužená studie) a pro které byla po 2 letech k dispozici hodnotící data. Produktivita v práci a doma Pacienti léčení Cimzií uváděli v porovnání s pacienty s placebem statisticky významná zlepšení v oblasti sledování produktivity práce. Cimzia je, v kombinaci s methotrexatem, indikována pro léčbu středně závažné až závažné aktivní formy revmatoidní artritidy (RA) u dospělých pacientů, u kterých je odpověď na léčbu antirevmatiky (DMARD), včetně methotrexatu, nedostatečná. Cimzii lze podávat v monoterapii v případě nesnášenlivosti methotrexatu nebo je-li pokračování léčby methotrexatem nevhodné. Cimzia, v kombinaci s methotrexatem, snižuje rychlost progrese poškození kloubu hodnocené rentgenem a zlepšuje fyzickou funkci.
11
12 rychlá odpověď. rychlá volba. týden 1 týden 6 týden 12 CIMZIA umožňuje rozhodnutí o léčbě v týdnu 12 1,2 Reference: 1. CIMZIA, Souhrn údajů o přípravku, 02/ Keystone E, van der Heijde D, Mason D Jr, et al. Certolizumab pegol plus methotrexate is significantly more effective than placebo plus methotrexate in active rheumatoid arthritis. Arthritis Rheum. 2008;58: Zkrácená informace o přípravku: CIMZIA 200 mg injekční roztok. Složení: Jedna předplněná injekční stříkačka obsahuje certolizumabum pegolum 200 mg/ml. Indikace: Cimzia je indikována v kombinaci s methotrexatem (MTX) pro léčbu středně závažné až závažné formy aktivní revmatoidní artritidy (RA) u dospělých pacientů, u kterých je odpověď na léčbu antirevmatiky (DMARD), včetně methotrexatu, nedostatečná. Cimzia se může podávat v monoterapii v případě nesnášenlivosti methotrexatu nebo je-li pokračování léčby methotrexatem nevhodné. Dávkování: Doporučená úvodní dávka přípravku Cimzia u dospělých pacientů s revmatoidní artritidou je 400 mg (jako 2 injekce, každá po 200 mg denně) v týdnu 0, 2 a 4, následovaná udržovací dávkou 200 mg každé 2 týdny. Pokud je třeba, podávání MTX by se nemělo přerušovat. Kontraindikace: Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku tohoto přípravku; aktivní tuberkulóza nebo jiné závažné infekce jako sepse nebo oportunní infekce; středně závažné až závažné srdeční selhání (NYHA třída III/IV). Zvláštní upozornění a opatření při používání: Pacienti musí být pečlivě monitorováni na známky a příznaky infekcí včetně tuberkulózy před, během a po léčbě. Před zahájením léčby přípravkem Cimzia musí být všichni pacienti vyšetřeni na přítomnost aktivní i neaktivní (latentní) tuberkulózní infekce. Pokud je diagnostikována aktivní tuberkulóza před zahájením léčby nebo během ní, terapie Cimzií nesmí být zahájena, respektive je nutno ji přerušit. Živé nebo oslabené vakcíny by neměly být souběžně s přípravkem Cimzia podávány. Interakce: Cimzia by se neměla podávat v kombinaci s anakinrou nebo abataceptem. Nežádoucí účinky: Časté: bakteriální infekce, virové infekce, eozinofilní poruchy, leukopenie, bolesti hlavy, senzorické abnormality, hypertenze, hepatitida, vyrážka, pyrexie, bolest (v kterémkoli místě), astenie, pruritus, reakce v místě aplikace. Uchovávání: Uchovávejte v chladničce (2 8 C) v krabičce, aby byl přípravek chráněn před světlem. Chraňte před mrazem. Dostupné lékové formy/velikosti balení: 2 injekční stříkačky. Držitel rozhodnutí o registraci: UCB Pharma SA, Brusel, Belgie. Reg. číslo: EU/1/09/544/001. Datum revize textu: 02/2011. Výdej léčivého přípravku je vázán na lékařský předpis. Přípravek je hrazen z prostředků veřejného zdravotního pojištění. Podrobné údaje najdete v Souhrnu údajů o přípravku. UCB s.r.o. Palác Karlín, Thámova Praha 8, Karlín tel.: , fax: info.prague@ucb.com CI_CR_PM_08_11
Informace pro lékaře.
 Informace pro lékaře. Rychlá odpověď. Rychlá volba. Informace pro lékaře Cimzia je, v kombinaci s methotrexatem, indikována pro léčbu středně závažné až závažné aktivní formy revmatoidní artritidy (RA)
Informace pro lékaře. Rychlá odpověď. Rychlá volba. Informace pro lékaře Cimzia je, v kombinaci s methotrexatem, indikována pro léčbu středně závažné až závažné aktivní formy revmatoidní artritidy (RA)
Informace pro lékaře
 Informace pro lékaře Cimzia je, v kombinaci s methotrexátem, indikována pro léčbu středně závažné až závažné aktivní formy revmatoidní artritidy (RA) u dospělých pacientů, u kterých je odpověď na léčbu
Informace pro lékaře Cimzia je, v kombinaci s methotrexátem, indikována pro léčbu středně závažné až závažné aktivní formy revmatoidní artritidy (RA) u dospělých pacientů, u kterých je odpověď na léčbu
Informace pro pacienty léčené přípravkem CIMZIA
 Informace pro pacienty léčené přípravkem CIMZIA Informace pro pacienta Cimzia se používá k léčbě středně závažné až závažné revmatoidní artritidy u dospělých pacientů, když jiné další léky nestačí ke
Informace pro pacienty léčené přípravkem CIMZIA Informace pro pacienta Cimzia se používá k léčbě středně závažné až závažné revmatoidní artritidy u dospělých pacientů, když jiné další léky nestačí ke
INFLECTRA SCREENINGOVÝ LIST. a výběru pacientů pro všechny schválené indikace. Obsahuje pokyny ke správnému screeningu
 Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
PRŮKAZ PACIENTA. užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019
 PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
Rozměr zavřeného průkazu mm
 Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
PRŮKAZ PACIENTA. užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1
 PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
SOUHRN ÚDAJŮ O PŘÍPRAVKU. PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová
 sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příprava a podání injekce
 Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
RÁDCE PACIENTA. Pro aplikaci přípravku Metoject 50 mg/ml injekční roztok, předplněné injekční stříkačky s obsahem metotrexátu
 RÁDCE PACIENTA Pro aplikaci přípravku Metoject 50 mg/ml injekční roztok, předplněné injekční stříkačky s obsahem metotrexátu RYCHLÝ PŘEHLED Tento materiál je určen výhradně pacientům užívajícím přípravek
RÁDCE PACIENTA Pro aplikaci přípravku Metoject 50 mg/ml injekční roztok, předplněné injekční stříkačky s obsahem metotrexátu RYCHLÝ PŘEHLED Tento materiál je určen výhradně pacientům užívajícím přípravek
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA)
 Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Souhrn údajů o přípravku. Typhoidi capsulae Vi polysaccharidum purificatum (stirpe Ty 2)
 sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Kelapril 5mg 7x14tbl.
 Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
*Lidská IgG1κ monoklonální protilátka produkovaná linií hybridomových buněk myší technologií rekombinance DNA.
 1. NÁZEV PŘÍPRAVKU Simponi 50 mg injekční roztok v předplněné injekční stříkačce. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka 0,5 ml obsahuje golimumabum* 50 mg. *Lidská
1. NÁZEV PŘÍPRAVKU Simponi 50 mg injekční roztok v předplněné injekční stříkačce. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka 0,5 ml obsahuje golimumabum* 50 mg. *Lidská
NeuroBloc. botulinový toxin typu B injekční roztok, U/ml
 NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
EDUKAČNÍ MATERIÁL - Pioglitazone Accord
 Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Návod k použití EDUKAČNÍ MATERIÁLY. mecasermin. Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex
 EDUKAČNÍ MATERIÁLY mecasermin Návod k použití Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
EDUKAČNÍ MATERIÁLY mecasermin Návod k použití Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Cimzia 200 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje certolizumabum pegolum 200 mg
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Cimzia 200 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje certolizumabum pegolum 200 mg
POKYNY PRO POUŽITÍ. Budete potřebovat následující položky, které jsou obsaženy v balení:
 POKYNY PRO POUŽITÍ Jak používat předplněné pero PegIntron Následující pokyny vysvětlují, jak si můžete aplikovat injekci sám/sama pomocí předplněného pera. Prosím, přečtěte si pečlivě pokyny a krok za
POKYNY PRO POUŽITÍ Jak používat předplněné pero PegIntron Následující pokyny vysvětlují, jak si můžete aplikovat injekci sám/sama pomocí předplněného pera. Prosím, přečtěte si pečlivě pokyny a krok za
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (0,5
1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná) 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 dávka (0,5
Praxbind doporučení pro podávání (SPC)
 Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
Popis přípravku : Prášek: bílý lyofilizát. Rozpouštědlo: čirá bezbarvá tekutina
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (0,5 ml) rozpuštěné
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (0,5 ml) rozpuštěné
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Cimzia 200 mg injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Cimzia 200 mg injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje
Příloha IV. Vědecké závěry
 Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
INSTRUKCE PRO INTRAVENÓZNÍ A SUBKUTÁNNÍ PODÁNÍ KROK ZA KROKEM
 EDUKAČNÍ MATERIÁLY RoActemra (tocilizumab) pro revmatoidní artritidu INSTRUKCE PRO INTRAVENÓZNÍ A SUBKUTÁNNÍ PODÁNÍ KROK ZA KROKEM Návod určený zdravotnickým odborníkům jako pomoc s přípravou a podáním
EDUKAČNÍ MATERIÁLY RoActemra (tocilizumab) pro revmatoidní artritidu INSTRUKCE PRO INTRAVENÓZNÍ A SUBKUTÁNNÍ PODÁNÍ KROK ZA KROKEM Návod určený zdravotnickým odborníkům jako pomoc s přípravou a podáním
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011. Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
* Přípravek MabThera s.c. je indikován pouze k léčbě dospělých pacientů s non-hodgkinským lymfomem (NHL):
 Tyto edukační materiály týkající se bezpečného a účinného používání přípravku MabThera 1 400 mg roztoku pro subkutánní injekci (dále jen MabThera s.c.) je příručkou pro lékaře, zdravotní sestry a lékárníky.
Tyto edukační materiály týkající se bezpečného a účinného používání přípravku MabThera 1 400 mg roztoku pro subkutánní injekci (dále jen MabThera s.c.) je příručkou pro lékaře, zdravotní sestry a lékárníky.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
Příbalová informace: Informace pro pacienta
 sp.zn.sukls17470/2014 Příbalová informace: Informace pro pacienta ERMM-1 111 MBq/ml, injekční suspenze Erbii-( 169 Er) citras (Citronan erbný-( 169 Er) v koloidní suspenzi) (V této příbalové informaci
sp.zn.sukls17470/2014 Příbalová informace: Informace pro pacienta ERMM-1 111 MBq/ml, injekční suspenze Erbii-( 169 Er) citras (Citronan erbný-( 169 Er) v koloidní suspenzi) (V této příbalové informaci
Příbalová informace: informace pro uživatele
 sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
BIOVISC ORTHO M. Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci.
 Česky BIOVISC ORTHO M Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová Mannitol 20 mg 5 mg Fosfátem pufrovaný
Česky BIOVISC ORTHO M Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová Mannitol 20 mg 5 mg Fosfátem pufrovaný
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CAMILIA perorální roztok v jednodávkovém obalu
 sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
Nebido EDUKAČNÍ MATERIÁL. Jak úspěšně aplikovat přípravek. (testosterone undecanoate)
 EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Používání Apidry v 10 ml injekčních lahvičkách
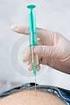 NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
Příbalová informace: informace pro uživatele Engerix-B 20 µg. antigenum tegiminis hepatitidis B injekční suspenze
 sp.zn. sukls204563/2014 Příbalová informace: informace pro uživatele Engerix-B 10 µg Engerix-B 20 µg antigenum tegiminis hepatitidis B injekční suspenze Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls204563/2014 Příbalová informace: informace pro uživatele Engerix-B 10 µg Engerix-B 20 µg antigenum tegiminis hepatitidis B injekční suspenze Přečtěte si pozorně celou příbalovou informaci dříve,
Složení vakcíny odpovídá doporučení SZO (pro severní polokouli) a EU rozhodnutí pro sezónu2007/2008
 Příbalová informace - RP Informace pro použití, čtěte pozorně! Begrivac (vakcína proti chřipce) Injekční suspenze Sezóna 2007/2008 Držitel rozhodnutí o registraci a výrobce Novartis Vaccines and Diagnostics
Příbalová informace - RP Informace pro použití, čtěte pozorně! Begrivac (vakcína proti chřipce) Injekční suspenze Sezóna 2007/2008 Držitel rozhodnutí o registraci a výrobce Novartis Vaccines and Diagnostics
Přípravek BI ve srovnání s přípravkem Humira u pacientů se středně těžkou až těžkou ložiskovou lupénkou
 Přípravek ve srovnání s přípravkem u pacientů se středně těžkou až těžkou ložiskovou lupénkou Toto je shrnutí klinické studie, které se účastnili pacienti s ložiskovou lupénkou. Je vypracováno pro širokou
Přípravek ve srovnání s přípravkem u pacientů se středně těžkou až těžkou ložiskovou lupénkou Toto je shrnutí klinické studie, které se účastnili pacienti s ložiskovou lupénkou. Je vypracováno pro širokou
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.:sukls59594/25009, a příloha k sp.zn.: sukls230271/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.:sukls59594/25009, a příloha k sp.zn.: sukls230271/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.sukls158765/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.sukls158765/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Důležité informace pro pacienty
 MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Vanguard R injekční suspenze pro psy, kočky, skot, prasata, ovce, kozy, koně a fretky
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Vanguard R injekční suspenze pro psy, kočky, skot, prasata, ovce, kozy, koně a fretky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Vanguard R injekční suspenze pro psy, kočky, skot, prasata, ovce, kozy, koně a fretky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka
IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná)
 Příloha č. 1 ke sdělení sp. zn. sukls205477/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná)
Příloha č. 1 ke sdělení sp. zn. sukls205477/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE IMOVAX POLIO, injekční suspenze v předplněné injekční stříkačce Vakcína proti poliomyelitidě (inaktivovaná)
Tento návod Vás provede procesem infuze léku RoActemra v
 Tento návod Vás provede procesem infuze léku RoActemra v Před zahájením terapie 6 krocích. Před zahájením terapie přípravkem RoActemra je důležité, abyste si s každým pacientem prošli brožuru Co byste
Tento návod Vás provede procesem infuze léku RoActemra v Před zahájením terapie 6 krocích. Před zahájením terapie přípravkem RoActemra je důležité, abyste si s každým pacientem prošli brožuru Co byste
Příbalová informace: informace pro uživatele. VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa
 Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Cimzia 200 mg injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Cimzia 200 mg injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka obsahuje
U pacientů, jejichž tělesná hmotnost je vyšší než 100 kg, se dávky přesahující 800 mg/infuzi nedoporučují.
 EDUKAČNÍ MATERIÁLY RoActemra (tocilizumab) Kapesní dávkovací karta pro revmatoidní artritidu Přípravek RoActemra v kombinaci s metotrexátem (MTX) je indikován k léčbě středně těžké až těžké aktivní revmatoidní
EDUKAČNÍ MATERIÁLY RoActemra (tocilizumab) Kapesní dávkovací karta pro revmatoidní artritidu Přípravek RoActemra v kombinaci s metotrexátem (MTX) je indikován k léčbě středně těžké až těžké aktivní revmatoidní
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele. IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara)
 Příbalová informace: informace pro uživatele IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara) Tento přípravek podléhá dalšímu sledování. To umožní rychlé
Příbalová informace: informace pro uživatele IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara) Tento přípravek podléhá dalšímu sledování. To umožní rychlé
Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti.
 Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti. I V A N A K O V Á Ř O V Á C E N T R U M P R O D E M Y E L I N I Z A Č N Í O N E M O C N Ě N Í N E U R O L O G I C
Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti. I V A N A K O V Á Ř O V Á C E N T R U M P R O D E M Y E L I N I Z A Č N Í O N E M O C N Ě N Í N E U R O L O G I C
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU Lahev s obsahem 300 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Levetiracetam UCB 100 mg/ml, perorální roztok levetiracetamum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU Lahev s obsahem 300 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Levetiracetam UCB 100 mg/ml, perorální roztok levetiracetamum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls59573/2009
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls59573/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TETAVAX, injekční suspenze v předplněné injekční stříkačce Vakcína proti tetanu (adsorbovaná)
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls59573/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TETAVAX, injekční suspenze v předplněné injekční stříkačce Vakcína proti tetanu (adsorbovaná)
CO BYSTE MĚLI VĚDĚT O PŘÍPRAVKU RoACTEMRA
 RoActemra IV a SC pro revmatoidní artritidu CO BYSTE MĚLI VĚDĚT O PŘÍPRAVKU RoACTEMRA Určeno pouze pro pacienty Tato brožura poskytuje klíčové informace pomáhající pacientům porozumět přínosům i rizikům
RoActemra IV a SC pro revmatoidní artritidu CO BYSTE MĚLI VĚDĚT O PŘÍPRAVKU RoACTEMRA Určeno pouze pro pacienty Tato brožura poskytuje klíčové informace pomáhající pacientům porozumět přínosům i rizikům
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro uživatele. Cimzia 200 mg, injekční roztok v předplněné injekční stříkačce certolizumabum pegolum
 Příbalová informace: informace pro uživatele Cimzia 200 mg, injekční roztok v předplněné injekční stříkačce certolizumabum pegolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele Cimzia 200 mg, injekční roztok v předplněné injekční stříkačce certolizumabum pegolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
CO BYSTE MĚLI VĚDĚT. RoActemra pro revmatoidní artritidu
 RoActemra pro revmatoidní artritidu CO BYSTE MĚLI VĚDĚT Tato brožura poskytuje klíčové informace pomáhající pacientům porozumět přínosům i rizikům souvisejícím s léčbou přípravkem RoActemra. Tento edukační
RoActemra pro revmatoidní artritidu CO BYSTE MĚLI VĚDĚT Tato brožura poskytuje klíčové informace pomáhající pacientům porozumět přínosům i rizikům souvisejícím s léčbou přípravkem RoActemra. Tento edukační
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ
 OZNAČENÍ NA OBALU ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Text na krabičku 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU suspenze Paracetamolum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Paracetamolum 120 mg v 5 ml suspenze 3. SEZNAM
OZNAČENÍ NA OBALU ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Text na krabičku 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU suspenze Paracetamolum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Paracetamolum 120 mg v 5 ml suspenze 3. SEZNAM
Příbalová informace: informace pro uživatele
 sp. zn. sukls167840/2014 Příbalová informace: informace pro uživatele Priorix inj.stříkačka, prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce Živá atenuovaná vakcína proti spalničkám,
sp. zn. sukls167840/2014 Příbalová informace: informace pro uživatele Priorix inj.stříkačka, prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce Živá atenuovaná vakcína proti spalničkám,
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Feligen CRP Lyofilizát pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizovaná složka Léčivé
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Feligen CRP Lyofilizát pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizovaná složka Léčivé
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Poznámka: Tyto úpravy souhrnu údajů o přípravku a
 PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
Ferrum. Opakovaná léčba Diafer 50 mg/ml injekčním roztokem je používána k doplnění a udržení zásob železa v těle.
 sp.zn. sukls57833/2014 Příbalová informace: informace pro pacienta 50 mg/ml injekční roztok Ferrum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete
sp.zn. sukls57833/2014 Příbalová informace: informace pro pacienta 50 mg/ml injekční roztok Ferrum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete
Příbalová informace: informace pro pacienta. Panadol Baby 125 mg čípky paracetamolum čípky
 sp. zn. sukls62708/2018 Příbalová informace: informace pro pacienta Panadol Baby 125 mg čípky paracetamolum čípky Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
sp. zn. sukls62708/2018 Příbalová informace: informace pro pacienta Panadol Baby 125 mg čípky paracetamolum čípky Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele VAQTA Adult 50 U/ml injekční suspenze v předplněné injekční stříkačce Očkovací látka proti hepatitidě typu A, inaktivovaná, adsorbovaná Pro dospělé Přečtěte
Příbalová informace: informace pro uživatele VAQTA Adult 50 U/ml injekční suspenze v předplněné injekční stříkačce Očkovací látka proti hepatitidě typu A, inaktivovaná, adsorbovaná Pro dospělé Přečtěte
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU {Krabička na blistry a lahvičky z HDPE } 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Sandoz 60mg Orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tvrdá tobolka obsahuje orlistatum
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU {Krabička na blistry a lahvičky z HDPE } 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Sandoz 60mg Orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tvrdá tobolka obsahuje orlistatum
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn.: sukls59573/2009
 Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn.: sukls59573/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE TETAVAX Injekční suspenze v předplněné injekční stříkačce Vakcína proti tetanu (adsorbovaná)
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn.: sukls59573/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE TETAVAX Injekční suspenze v předplněné injekční stříkačce Vakcína proti tetanu (adsorbovaná)
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Co je Voltaren Ophtha CD Léčivou látkou přípravku Voltaren Ophtha CD je diklofenak sodný (diclofenacum natricum).
 Příloha č.1 ke sdělení sp.zn.sukls23896/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VOLTAREN OPHTHA CD oční kapky, roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha č.1 ke sdělení sp.zn.sukls23896/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VOLTAREN OPHTHA CD oční kapky, roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou informaci dříve,
po 5 letech ... s excelentním kosmetickým výsledkem 2
 ... s excelentním kosmetickým výsledkem 2 pred lécbou 6. týden 12. týden po 1 roku po 3 letech po 5 letech Správný výber pro Vaše pacienty se superficiálními BCC - krátkodobá lécba s velice dobrým kosmetickým
... s excelentním kosmetickým výsledkem 2 pred lécbou 6. týden 12. týden po 1 roku po 3 letech po 5 letech Správný výber pro Vaše pacienty se superficiálními BCC - krátkodobá lécba s velice dobrým kosmetickým
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
sp.zn. sukls107935/2012
 sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Pavulon 4mg = 2ml injekční roztok. Pancuronii bromidum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pavulon 4mg = 2ml injekční roztok Pancuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pavulon 4mg = 2ml injekční roztok Pancuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Immunoglobulinum humanum normale Jeden ml injekčního roztoku obsahuje Immunoglobulinum humanum normale 160 mg.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IGAMPLIA 160 mg/ml, injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale Jeden ml injekčního roztoku obsahuje Immunoglobulinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IGAMPLIA 160 mg/ml, injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale Jeden ml injekčního roztoku obsahuje Immunoglobulinum
BAVENCIO (avelumab) Váš průvodce informacemi pro pacienta
 Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
dnavou artritidou (GA)
 EDUKAČNÍ MATERIÁLY ILARIS (kanakinumab) Průvodce pro lékaře k používání přípravku Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
EDUKAČNÍ MATERIÁLY ILARIS (kanakinumab) Průvodce pro lékaře k používání přípravku Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
Propofol MCT Fresenius 10 mg/ml: Jeden ml obsahuje propofolum 10 mg. Propofol MCT Fresenius 20 mg/ml: Jeden ml obsahuje propofolum 20 mg.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU 1x 50 ml předplněná injekční stříkačka 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Propofol MCT Fresenius 10 mg/ml injekční/infuzní emulze v předplněné injekční stříkačce Propofol MCT Fresenius
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU 1x 50 ml předplněná injekční stříkačka 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Propofol MCT Fresenius 10 mg/ml injekční/infuzní emulze v předplněné injekční stříkačce Propofol MCT Fresenius
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obal na tablety se 400 mg potahovanými tabletami 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibuprofen Dr.Max 400 mg potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obal na tablety se 400 mg potahovanými tabletami 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibuprofen Dr.Max 400 mg potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
3. LÉKOVÁ FORMA Injekční suspenze vpředplněné injekční stříkačce; bezbarvá průhledná tekutina, v jednodávkových inj. stříkačkách (sklo, typu I).
 Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls97832/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna
Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls97832/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Influvac Injekční suspenze (vakcína proti chřipce, povrchový antigen, inaktivovaná) Sezóna
Důležité informace o užívání přípravku TASIGNA
 Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Od opia k melatoninu aneb Práce s nespavým pacientem
 Soubor pøednášek ze semináøe Od opia k melatoninu aneb Práce s nespavým pacientem Semináøe se konají na 14 místech ÈR v období únor duben 2009 1. Péèe o pacienta s nespavostí Diagnostika a nefarmakologická
Soubor pøednášek ze semináøe Od opia k melatoninu aneb Práce s nespavým pacientem Semináøe se konají na 14 místech ÈR v období únor duben 2009 1. Péèe o pacienta s nespavostí Diagnostika a nefarmakologická
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn. sukls110147/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA SOMATULINE AUTOGEL 60 mg, injekční roztok v předplněné stříkačce SOMATULINE AUTOGEL 90 mg, injekční roztok v předplněné stříkačce SOMATULINE
sp.zn. sukls110147/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA SOMATULINE AUTOGEL 60 mg, injekční roztok v předplněné stříkačce SOMATULINE AUTOGEL 90 mg, injekční roztok v předplněné stříkačce SOMATULINE
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
Struktura parametrické dokumentace registru ATTRA Diagnóza: Juvenilní idiopatická artritida
 Struktura parametrické dokumentace registru ATTRA Diagnóza: Juvenilní idiopatická artritida Vstupní údaje... 1 Identifikační údaje pacienta... 1 Identifikační údaje centra... 1 Vstupní vyšetření... 2 Vstupní
Struktura parametrické dokumentace registru ATTRA Diagnóza: Juvenilní idiopatická artritida Vstupní údaje... 1 Identifikační údaje pacienta... 1 Identifikační údaje centra... 1 Vstupní vyšetření... 2 Vstupní
CZ PAR. QUETIAPINI FUMARAS Seroquel. NL/W/0004/pdWS/002
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Jedna předplněná injekční stříkačka na jedno použití o objemu 0,8 ml obsahuje adalimumabum 40 mg.
 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Podrobnosti
Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Podrobnosti
Humira 40 mg injekční roztok v předplněné injekční stříkačce s ochranným krytem jehly
 1. NÁZEV PŘÍPRAVKU Humira 40 mg injekční roztok v předplněné injekční stříkačce s ochranným krytem jehly 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka na jedno použití o objemu
1. NÁZEV PŘÍPRAVKU Humira 40 mg injekční roztok v předplněné injekční stříkačce s ochranným krytem jehly 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka na jedno použití o objemu
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
