VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY
|
|
|
- Tomáš Bureš
- před 4 lety
- Počet zobrazení:
Transkript
1 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF POWER ELECTRICAL AND ELECTRONIC ENGINEERING MODIFIKACE KATODOVÉHO MATERIÁLU NA BÁZI NIKLU A MANGANU PRO LI-ION ČLÁNKY BAKALÁŘSKÁ PRÁCE BACHELOR THESIS AUTOR PRÁCE AUTHOR IVANA BUKÁČKOVÁ BRNO 2014
2 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF ELECTRICAL AND ELECTRONIC TECHNOLOGY MODIFIKACE KATODOVÉHO MATERIÁLU NA BÁZI NIKLU A MANGANU PRO LI-ION ČLÁNKY MODIFICATION OF CATHODE MATERIAL BASED ON NICKEL AND MANGANESE FOR LI-ION CELL BAKALÁŘSKÁ PRÁCE BACHELOR THESIS AUTOR PRÁCE AUTHOR VEDOUCÍ PRÁCE SUPERVISOR IVANA BUKÁČKOVÁ Ing. TOMÁŠ KAZDA BRNO 2014
3 Abstrakt Tato bakalářská práce se zabývá katodovými materiály pro lithiové články s napětím okolo 5V. První část práce je věnovaná charakteristice Li-ion baterií, elektrochemickým reakcím a vlastnostem elektrodových materiálů. Dále je věnována pozornost přípravě a měření materiálů LiNi 0,5 Mn 1,5 O 4, LiNi 0,45 Mn 1,55 O 4 a LiNi 0,55 Mn 1,45 O 4. Vybraný materiál byl zkoumán pomocí metody elektronové mikroskopie, prvkovou analýzou a galvanostatického měření. Abstract This bachelor s thesis deals with cathode materials for lithium batteries with cell voltage approaching 5V. The first part of the thesis is devoted to the characteristics of Li-ion batteries, electrochemical reactions and properties of electrode materials. She also pays attention to the preparation and measurement of materials LiNi 0,5 Mn 1,5 O 4, LiNi 0,45 Mn 1,55 O 4 and LiNi 0,55 Mn 1,45 O 4. Observed material was measured by electron microscopy, elemental analysis and galvanostatic method,
4 Klíčová slova Lithno-iontové akumulátory, lithium, elektroda, katoda, LiNi 0,5 Mn 1,5 O 4. Keywords Lithium-ions accumulators, lithium, electrode, cathode, LiNi 0,5 Mn 1,5 O 4.
5 Bibliografická citace BUKÁČKOVÁ, I. Modifikace katodového materiálu na bázi niklu a manganu pro Li-ion články. Brno: Vysoké učení technické v Brně, Fakulta elektrotechniky a komunikačních technologií, s. Vedoucí bakalářské práce Ing. Tomáš Kazda.
6 Prohlášení Prohlašuji, že svou bakalářskou práci na téma Modifikace katodového materiálu na bázi niklu a manganu pro Li-ion články jsem vypracovala samostatně pod vedením vedoucího bakalářské práce a s použitím odborné literatury a dalších informačních zdrojů, které jsou všechny citovány v práci a uvedeny v seznamu literatury na konci práce. Jako autor uvedené bakalářské práce dále prohlašuji, že v souvislosti s vytvořením této bakalářské práce jsem neporušila autorská práva třetích osob, zejména jsem nezasáhla nedovoleným způsobem do cizích autorských práv osobnostních a jsem si plně vědoma následků porušení ustanovení 11 a následujících autorského zákona č. 121/2000 Sb., včetně možných trestněprávních důsledků vyplývajících z ustanovení 152 trestního zákona č. 140/1961 Sb. V Brně dne Podpis autora.. Poděkování Děkuji vedoucímu bakalářské práce Ing. Tomáši Kazdovi za účinnou metodickou, pedagogickou a odbornou pomoc a další cenné rady při zpracování mé bakalářské práce. V Brně dne Podpis autora..
7 OBSAH ÚVOD HISTORIE VÝHODY A NEVÝHODY LI-ION AKUMULÁTORŮ KONSTRUKCE LI-ION AKUMULÁTORŮ Interkalační proces a princip funkce Li-ion akumulátoru MATERIÁLY PRO ZÁPORNOU ELEKTRODU MATERIÁLY PRO KLADNOU ELEKTRODU LiCoO LiNiO LiNiCoO 2 modifikace z LiNiO LiFePO LiMn 2 O LiMnO LiNi 0,5 Mn 1,5 O POUŽITÉ ZAŘÍZENÍ A ELEKTROCHEMICKÉ MĚŘÍCÍ METODY GALVANOSTATICKÉ NABÍJENÍ/VYBÍJENÍ RASTROVACÍ ELEKTRONOVÁ MIKROSKOPIE (SEM) PRVKOVÁ ANALÝZA (EDS) PRAKTICKÁ ČÁST VÝROBA ELEKTRODOVÝCH MATERIÁLŮ Metodou třístupňového žíhání LiNi 0,5 Mn 1,5 O Příprava metodou prudkého ohřevu: LiNi 0,5 Mn 1,5 O 4, LiNi 0,45 Mn 1,55 O 4 a LiNi 0,55 Mn 1,45 O MĚŘENÍ A DOSAŽENÉ VÝSLEDKY Metoda prudkého ohřevu LiNi 0,5 Mn 1,5 O Metoda třístupňového žíhání LiNi 0,5 Mn 1,5 O Metoda prudkého ohřevu LiNi 0,45 Mn 1,55 O Metoda prudkého ohřevu LiNi 0,55 Mn 1,45 O ZÁVĚR SEZNAM LITERATURY
8 Seznam obrázků Obrázek 1:Řez prizmatickým Li-ion akumulátorem [19] Obrázek 2:Model interkalační reakce [3] Obrázek 3:Princip přenosu volných iontů při vybíjení a nabíjení [20] Obrázek 4: Struktura a uspořádání prvků [4] Obrázek 5:Nabíjecí a vybíjecí charakteristika LiNiO 2 [13] Obrázek 6:Vybíjecí a nabíjecí charakteristika LiNiCoO 2 [17] Obrázek 7:Materiály pro kladnou elektrodu LiCoO 2, LiMn 2 O 4, LiFePO 4 [6] Obrázek 8: A:Vybíjecí křivka materiálu LiMnO 2, B: Nabíjecí křivka LiMnO 2 [11] Obrázek 9: Nabíjecí a vybíjecí charakteristiky některých materiálů [9] Obrázek 10:Vlevo rozložení prvků v plošně centrované struktuře, Vpravo rozložení v kubické struktuře [10] Obrázek 11:Rukavicový box Jacomex Obrázek 12: Měřící cela El-Cell ECC-STD Obrázek 13: Průběh prvních dvou nabíjecích a vybíjecích cyklů materiálu LiNi 0,5 Mn 1,5 O Obrázek 14: Deset vybíjecích cyklů LiNi 0,5 Mn 1,5 O Obrázek 15: Čtyři vybíjecí cykly LiNi 0,5 Mn 1,5 O Obrázek 16: Znovu deset vybíjecích cyklů LiNi 0,5 Mn 1,5 O Obrázek 17:Porovnání kapacity v závislosti na zatížení materiálu LiNi 0,5 Mn 1,5 O Obrázek 18:SEM analýza LiNi 0,5 Mn 1,5 O Obrázek 19: Průběh prvních dvou nabíjecích a vybíjecích cyklů LiNi 0,5 Mn 1,5 O 4 [22] Obrázek 20: Průběh kapacity v prvních dvou vybíjecích cyklech materiálu LiNi 0,5 Mn 1,5 O 4 [22] Obrázek 21: Deset vybíjecích cyklů materiálu LiNi 0,5 Mn 1,5 O 4 proudem 0,5C [22] Obrázek 22: Čtyři vybíjecí cykly materiálu LiNi 0,5 Mn 1,5 O 4 proudem 1C [22] Obrázek 23: Posledních 10 vybíjecích cyklů materiálu LiNi 0,5 Mn 1,5 O 4 proudem 0,5C [22].. 34 Obrázek 24:Porovnání kapacity v závislosti na zatížení materiálu LiNi 0,5 Mn 1,5 O 4 [22] Obrázek 25:SEM analýza materiálu LiNi 0,5 Mn 1,5 O 4 : A - zvětšeno 1kx a B - zvětšeno 5kx [22] Obrázek 26: Mapování vzorku LiNi 0,5 Mn 1,5 O 4 A) SEM částice materiálu LiNi 0,5 Mn 1,5 O 4 B) rozložení niklu C) rozložení kyslíku D) rozložení manganu [22] Obrázek 27: Průběh prvních dvou nabíjecích a vybíjecích cyklů materiálu LiNi 0,45 Mn 1,55 O 4 37 Obrázek 28: Deset vybíjecích cyklů LiNi 0,45 Mn 1,55 O Obrázek 29: Čtyři vybíjecí cykly LiNi 0,45 Mn 1,55 O Obrázek 30: Znovu deset vybíjecích cyklů LiNi 0,45 Mn 1,55 O Obrázek 31:Porovnání kapacity v závislosti na zatížení materiálu LiNi 0,45 Mn 1,55 O Obrázek 32: Průběh prvních dvou nabíjecích a vybíjecích cyklů materiálu LiNi 0,55 Mn 1,45 O 4 40 Obrázek 33: Deset vybíjecích cyklů LiNi 0,55 Mn 1,45 O Obrázek 34: Čtyři vybíjecí cykly LiNi 0,55 Mn 1,45 O Obrázek 35: Znovu deset vybíjecích cyklů LiNi 0,55 Mn 1,45 O Obrázek 36:Porovnání kapacity v závislosti na zatížení materiálu LiNi 0,55 Mn 1,45 O
9 Seznam tabulek Tabulka 1:Prekurzory Tabulka 2:Prekurzory jednotlivých materiálů Tabulka 3:Procentuální pokles kapacity během cyklování LiNi 0,5 Mn 1,5 O 4 metodou prudkého ohřevu Tabulka 4:Procentuální pokles kapacity během cyklování LiNi 0,5 Mn 1,5 O 4 [22] Tabulka 5:Procentuální pokles kapacity během cyklování LiNi 0,45 Mn 1,55 O Tabulka 6:Procentuální pokles kapacity během cyklování LiNi 0,55 Mn 1,45 O
10 Úvod Problematika lithno-iontových akumulátorů se neustále vyvíjí. Nacházejí uplatnění v mnoha aplikacích. Patří mezi zdroje elektrické energie zvlášť vhodné pro mobilní účely a pro vyrovnávání rozdílu mezi kolísavou výrobou a spotřebou energie například získávané z alternativních zdrojů. Na tyto zdroje jsou kladeny čím dál vyšší nároky, proto je nutné se jimi zabývat. Díky své vysoké energetické hustotě vytlačují NiCd a NiMH článků z mobilních přístrojů a dalších přenosných zařízení. Trh je těmito zdroji plný a liší se pouze ve velikosti, hmotnosti, tvaru a především svojí výdrží a výkonností. Výrobci se snaží tyto vlastnosti minimalizovat až na výdrž dodávané energie, kterou se naopak snaží maximalizovat. Tato bakalářská práce se zaměřuje na problematiku Li-ion akumulátorů specificky na katodové materiály s napětím okolo 5V. Jedná se o materiály odvozené od základního materiálu LiMn 2 O 4. V teoretické části práce je popsaná historie a vývoj, dále vysvětlen princip funkčnosti těchto akumulátorů a popis jejich vlastností. Součástí jsou i výhody a nevýhody. [22] Teoretická část práce je zaměřena na přípravu a proměření následujících materiálů: LiNi 0,5 Mn 1,5 O 4, LiNi 0,45 Mn 1,55 O 4 a LiNi 0,55 Mn 1,45 O 4, na jejich fyzikální a elektrochemickou analýzu a porovnání metod výroby těchto materiálů. 10
11 1 Historie Primární lithiové články byly vynalezeny v polovině šedesátých let dvacátého století. Již od začátku se vyznačovaly vysokou měrnou energií a kapacitou, nízkým samovybíjením a dalšími kladnými vlastnostmi. Následný výzkum ukázal, že se tyto články dají vyrobit nejen jako primární články, ale také jako články sekundární. V polovině sedmdesátých let byly provedeny pokusy, kde kladnou elektrodu tvořily sulfidy kovu a zápornou kovové lithium. Výsledky nebyly uspokojivé, neboť na elektrodách docházelo ke korozi. Dalším problémem těchto článků bylo, že při nabíjení nízkými proudy lithium mělo snahu tvořit tzv. dendrity, které pak perforovaly separátor, a následkem toho docházelo k vnitřním zkratům v akumulátoru. Zároveň vznikaly nepředvídatelné teplotní pochody. Začátkem osmdesátých let začaly pokusy s články, kde zápornou katodu tvořily sloučeniny typu LiWO 2, LiFe 2 O 3 nebo Li 9 MoSe 6 a kladnou katodou elektrodu sloučeniny titanu, wolframu, niobu, vanadia nebo molybdenu. Tyto články měly velmi nízké napětí (1,8 V 2,7 V), nízkou kapacitu a energeticky náročnou, komplikovanou a drahou výrobu. Velký pokrok nastal v roce 1990, kdy firma Sony představily novou technologii, která využívala jako aktivní materiál pro zápornou elektrodu směs grafitu (uhlíku) obohaceného lithiem a polyolefinu. Název Li-ion akumulátory pro zdroj spojený s vysokým napětím, možností nabíjení a vybíjení, s dlouhou životností, vysokou kapacitou a dobrou bezpečností, zavedl výkonný ředitel firmy Sony Energytek pan K. Tozawa. Název,,Ion je použit díky iontům Li+, které přecházejí při nabíjení z kladné elektrody na zápornou a při vybíjení je tomu naopak. Většinou se setkáváme s označením lithiový akumulátor, lithno-iontový akumulátor, akumulátor Li nebo Li-Ion akumulátor. Do této kategorie ale patří i akumulátor Lithiumpolymer, většinou označovaný jako Li-Pol. První komerční aplikace s Li-Ion technologií se na trhu objevila v lednu Jednalo se o mobilní telefon Sony,,Handyphone HP-211, který přinesl okamžitý úspěch. O rok později, v září 1992, se objevuje první videokamera od firmy Sony s Li-Ionovým akumulátorem. Japonští výrobci akumulátoru využily zkušeností firmy Sony a získávají tím velký náskok ve výrobě Li-Ionových akumulátorů a přichází s vlastními verzemi válcových a prizmatických akumulátorů. Ve skutečnosti dominují světové produkci. [1] Koncem roku 1996, Padhi a Goodenough objevili jako vhodný materiál pro kladnou elektrodu Li-Ion baterií kombinaci železa, fosforu (LiFePO 4 ) a dalších prvků. Vzhledem k obrovské převaze nad ostatními materiály vhodnými pro kladnou elektrodu, které se týkaly 11
12 nákladů, bezpečnosti, stability a výkonu, LiFePO 4 je používané především jako napájení přenosných zařízení, např. přenosné počítače a elektrické nářadí. LiFePO 4 je nejvhodnější pro velké baterie do automobilů. V roce 1997 bylo vyrobeno 193 milionů Li-iontových článků. Z toho bylo 98% vyrobeno na území Japonska v osmi továrnách. Produkce Li-iontových akumulátorů v této zemi je větší než produkce NiCd a NiMH akumulátorů. [1] Rok 2002, Ming Chiang s jeho skupinou publikovali inovaci, která vedla k dramatickému zlepšení výkonnosti Li-ion baterií posílením materiálu tzv. dopingem hliníku, niobu a zirkonu. Tyto prvky tvoří nepatrnou část celkového materiálu použitého pro kladnou elektrodu. V únoru 2005 malý podnik Altair nanotechnologie se sídlem v Renu vynalezl nanoelektrodové materiály pro lithium-ion baterie. Tento prototyp baterie má třikrát vyšší výkon než stávající baterie a může být plně nabita za šest minut. V tomto roce také Toshiba vyrobila další rychlonabíjecí Li-ion baterie také založeny na nové nanotechnologii, která umožňuje ještě rychlejší nabíjení, větší kapacitu a delší životnost. Tyto baterie byly použity především v průmyslových odvětvích v roce Další výzkumy se zabývají převážně těmito nanomateriály a jejich postupným inovováním. 12
13 2 Výhody a nevýhody Li-ion akumulátorů Výhody: Vysoké napětí typické jmenovité napětí 3,6 V Vysoká energie Nízká hmotnost Dlouhá životnost lze dosáhnout 500 až 1500 cyklů a vývoj neustále pokračuje Nízké samovybíjení okolo 8% za měsíc při +20 C Nemají tzv. paměťový efekt Dobrá bezpečnost a možnost dopravy bez jakéhokoliv omezení oproti primárním lithiovým článkům neobsahují lithium v čistě kovovém stavu Nezávadné pro životní prostředí neobsahují olovo, rtuť nebo kadmium Nevýhody: Nabíjecí proud je ve většině případů omezen nabíjí se konstantním napětím, plně je akumulátor nabit za 2 až 3 hodiny Nízký maximální vybíjecí proud V průběhu vybíjení dochází k poklesu napětí Velký vnitřní odpor Pracovní teplota je do -20 C Velká náchylnost na přebíjení a podvybíjení, proto většina baterií musí obsahovat řídicí elektronické obvody. Při poklesu napětí při vybíjení pod povolenou mez dochází k trvalému zničení akumulátorové baterie Nabíječe lithiových akumulátorů nejsou zaměnitelné s nabíječi pro NiCd a NiMH akumulátory. Li-ion baterie opatřené elektronickým obvodem je však možné nabíjet nabíječem pro NiCd nebo NiMH akumulátory. Tím je umožněna vzájemná zaměnitelnost těchto zdrojů např. v mobilních telefonech 13
14 2.1 Konstrukce Li-ion akumulátorů Každý Li-ion článek se skládá: Záporná elektroda je tvořena uhlíkovými materiály do jejichž struktury se interkaluje lithium Kladná elektroda je tvořena interkalačními látkami. Jedná se o různé druhy krystalických materiálů, které slouží jako zdroj lithia při nabíjení lithno iontového akumulátoru Interkalační látky při elektrochemické reakci způsobují přesun iontů lithia buď z kladné elektrody na zápornou anebo naopak. Separátor jedná se o nevodič, odděluje kladnou elektrodu od záporné. Bývá vyroben z plstěného nebo tkaného nylonu. Musí být dost porézní, aby zajistil co největší iontovou propustnost elektrolytu. Obrázek 1:Řez prizmatickým Li-ion akumulátorem [19] Elektrolyt úkolem elektrolytu je zajistit přenos náboje v článku mezi katodou a anodou. Obvykle je složen z lithných solí nebo z organických agresivních rozpouštědel, kde jsou obsaženy rozpuštěné chemické látky zajišťující iontovou vodivost. Jako vodivostní sůl je v největší míře používán LiClO 4 (chloristan lithný) nebo LiPF 6 (lithium hexafluorofosfát lithný). 14
15 2.1.1 Interkalační proces a princip funkce Li-ion akumulátoru Pojem interkalace nám vyznačuje proces, při kterém se molekula nebo iont jedné látky začleňuje do hostitelské mřížky druhé látky. I když se v mřížce hostitele nyní vyskytuje jiná částice, zůstává tato nově vzniklá mřížka téměř stejná jako mřížka původní. Mnohdy jsou pro termín interkalace používané i jiné formulace jako například: inzerce, inkluze nebo topotaktická reakce, ovšem veškeré tyto termíny spadají do uvedené definice. Probíhající interkalační reakce jsou chemicky nebo termálně reverzibilní a funkčností nám umožňují cestu k syntéze nových pevných látek, které nám umožňují systematické fyzikální změny jejich vlastností. Tento druh materiálu se především hodí jako senzory, elektrochemické displeje a hlavně v našem případě pro sekundární lithno-iontové články. [3] Obrázek 2:Model interkalační reakce [3] Základní princip funkce lithno-iontových akumulátorů je naznačen na Obr.3. Z tohoto obrázku je patrné, že v okamžiku, kdy je akumulátor nabíjen, dochází k deinterkalaci iontu lithia a elektrony prochází vnějším obvodem do anody do níž se interkalují ionty lithia po průchodu elektrolytem. V případě vybíjení akumulátoru dochází k přesně opačnému procesu. 15
16 Obrázek 3:Princip přenosu volných iontů při vybíjení a nabíjení [20] Elektrochemické procesy probíhající při nabíjení a vybíjení lze zjednodušeně vyjádřit následujícími rovnicemi: Děje na kladné elektrodě: 2 2, kde M představuje některý z kovů tvořících aktivní sloučeninu kladné elektrody. Děje na záporné elektrodě: 16
17 3 Materiály pro zápornou elektrodu Jako první se používal pro zápornou elektrodu materiál z kovového lithia pro jeho vysokou kapacitu. Ovšem díky bezpečnostním problémům s kovovým lithiem se začal průmysl soustředit na využití interkalace lithných iontů do uhlíku, protože tyto elektrody jsou stabilnější. První Li-ion baterie, které byly uvedeny na trh, využívaly jako záporný elektrodový materiál koks. Materiály z koksu nabízejí kapacitu 180 mah/g a jsou stabilnější v přítomnosti propylenu karbonátu (PC základ elektrolytů) oproti grafitových materiálům. Poruchy, které mohou nastat v koksových materiálech, jsou přichycení vrstev potlačující reakce nebo jejich odlupování v přítomnosti propylen karbonátu. V polovině devadesátých let většina Li-ion článků využívala elektrody z grafitu, zejména Mesocarbon Microbead (MCMB) carbon. MCMB uhlík nabízí kapacitu 300 mah/g a malou povrchovou plochu. Tím jsou zajištěny menší ztráty kapacity a dobré bezpečnostní vlastnosti. V současné době je u Li-ion baterií anoda založena na bázi uhlíku. Uhlík utváří grafitové vrstvy hexagonálně uspořádaných atomů, kdy atomy jsou od sebe vzdáleny 0,142 nm a tvoří tak obrovskou rovinnou molekulu. V této molekule jsou k sobě vázány silnými kovalentními vazbami. Vrstvy atomů jsou složeny ze dvou fází: 2H fáze a 3R fáze. Fáze 2H je tvořena dvěma vrstvami, které jsou oproti sobě posunuty. V případě 3R fáze jsou oproti sobě posunuty tři vrstvy. Vzdálenost mezi uhlíkovými atomy i mezi jednotlivými vrstvami je stejná pro obě fáze. V grafitových materiálech majoritní část představuje fáze 2H, fáze 3R zabírá cca 5-20% podíl. Vyšší stabilitu vykazuje 2H fáze, 3R při teplotách nad 2000 C přechází do uspořádání 2H. [8] 17
18 4 Materiály pro kladnou elektrodu LiCoO 2 LiCoO2 je dosud nejvíce používaný katodový materiál v Li-ion bateriích díky vysokému pracovnímu napětí a dlouhou životností. Byl jako první využit v sériově vyráběné baterii firmy Sony s anodou z ropného koksu. Tento katodový materiál se vyznačuje vrstvenou strukturou. Plný napěťový potenciál kobaltitou litného se pohybuje na hodnotě 4,7 V, což by bylo pro aplikace velice dobré, ale při takto vysoké hodnotě napětí dochází k nevratným strukturálním změnám, které jsou převážně způsobeny exotermními reakcemi e elektrolytem. Z tohoto důvodu se v komerčních bateriích dovoluje extrahovat pouze jedna polovina lithia. Proto hodnota napětí nikdy nepřekročí 4,2 V s teoretickou kapacitou 130 mahg-1. Nicméně od tohoto materiálu se postupně upouští a to hned ze dvou důvodů. Kobalt jako samostatný prvek periodické soustavy je příliš drahý a druhý problém vyvstává z environmentálního hlediska, protože kobalt je dosti toxický. Z těchto důvodů se hledají jiné přijatelnější materiály, které budou mít lepší dopad na ekologii a také se budou vyznačovat lepšími elektrochemickými vlastnostmi. Strukturu a uspořádání prvků ve sloučenině LiCoO 2 ukazuje obr.5. [5] Obrázek 4: Struktura a uspořádání prvků [4] LiNiO 2 Byl vytvořen jako náhrada k LiCoO 2. Stejně jako LiCoO 2 má vrstvenou strukturu, ale má mnohem vyšší specifickou kapacitu 200 mah/g. Články na bázi niklu poskytují až o 30% více energie než je tomu například u kobaltu. Nicméně jejich napěťová hodnota je nižší a pohybuje se okolo 3,6 V. Protože materiály LiNiO 2 a LiCoO 2 jsou tvořené pevným roztokem, byly důkladně zkoumány jejich kombinace. Vykazují mnohem vyšší teplotní nestabilitu Vyznačují se také tím, že mají vyšší exotermické reakce při nižších teplotách. Zvláště pokud by se použili u aplikací s vyšším výkonem. Kvůli tomuto se tyto články mnoho nevyužívají. [5] 18
19 Obrázek 5:Nabíjecí a vybíjecí charakteristika LiNiO 2 [13] LiNiCoO 2 modifikace z LiNiO 2 Vznikl jako další náhrada LiCoO 2. Kombinuje vlastnosti LiNiO 2 a LiCoO 2. Velikost kapacity a napětí proti lithiu závisí na zastoupení Co. Nabízí kapacitu větší než LiCoO 2 a pohybuje se v rozmezí 190 mah/g až 220 mah/g. Napětí se pohybuje kolem 3,75 V opět v závislosti zastoupení Co. Nicméně jejich provozní napětí, které je nižší než u LiCoO 2, po přepočítání na energetickou hustotu, znehodnotí jejich vyšší kapacitu. Obrázek 6:Vybíjecí a nabíjecí charakteristika LiNiCoO 2 [17] 19
20 4.1.4 LiFePO 4 Železo lithium fosfát byl objeven roku Vyznačuje se olivínovou strukturou. Má vynikající tepelnou i chemickou stabilitu než LiCoO 2 a nedochází v něm k degradaci struktury během interkalace a deinterkalace Li iontů. Je nehořlavý a teplotně odolný, proto není náchylný na nesprávné zacházení při nabíjení či vybíjení. Je šetrnější k životnímu prostředí a jeho náklady na výrobu jsou nízké. Teoretická kapacita je 170 mah/g. Napětí vůči lithiu je nižší než u ostatních typů katodových materiálů, pohybuje se okolo 3,3 V. Nevýhoda je nízká vodivost a to má za následek sníženou schopnost nabíjení a vybíjení vysokými proudy. Tento materiál nahrazuje starší LiCoO 2. [6] LiMn 2 O 4 Byl vyvinut jako alternativa k materiálu LiCoO 2, je také izostrukturální s LiCoO 2 nicméně dosahuje nižší kapacity. Nabízí větší teplotní stabilitu při cyklování než LiCoO 2. Je to vrstevnatý materiál, dosahuje napětí 3,95-4,1 V a teoretickou kapacitu 148 mah/g. Díky využití Mn je tento materiál málo toxický a málo exotermicky rozkladatelný. Obrázek 7:Materiály pro kladnou elektrodu LiCoO 2, LiMn 2 O 4, LiFePO 4 [6] LiMnO 2 Je také izostrukturální s LiCoO 2. Bohužel je strukturálně nestabilní v důsledku přesunu iontů manganu, při němž dochází k vytváření neuspořádané spinelové struktury. Bylo provedeno několik studií s cílem stabilizovat tento materiál. Zjistilo se, že pokud je více než 50% iontů lithia odstraněno během nabíjení, má tendenci se přeměňovat na spinelovou strukturu. Této přeměně lze zabránit výměnou poloviny iontů Mn za chrom. Potom je kapacita (190 mah/g) větší než kapacita, které se může dosáhnout nezávislou redukční reakci. Používání chromu je nežádoucí, neboť je toxický. [6] 20
21 A B Obrázek 8: A:Vybíjecí křivka materiálu LiMnO 2, B: Nabíjecí křivka LiMnO 2 [11] LiNi 0,5 Mn 1,5 O 4 Tento materiál lze nabíjet do 5 V a jeho napětí proti lithiu se pohybuje okolo 4,7 V tj. o 1V více než u ostatních materiálů. Teoretická kapacita je cca 147 mah/g, díky své kapacitě a vysokému napětí je jeho energetická hustota blížící se 700Wh/kg přibližněě o 20% vyšší než u LiCoO 2 a o 30% vyšší než u LiFePO 4. Díky spinelové struktuře je tento materiál dlouhodobě stabilní při cyklování a dobře zvládá zatížení vyššími proudy. Tato vlastnost se dá využít například pro automobily. Obrázek 9: Nabíjecí a vybíjecí charakteristiky některých materiálů [9] K poklesu kapacity tohoto materiálu při cyklování za pokojové teploty proudem 0,2 C dojde po 400 nabíjecích/vybíjecích cyklech okolo 6%, obdobný pokles nastane i při cyklování proudem 1C. 21
22 Existují dva druhy krystalové struktury materiálu LiNi 0,5 Mn 1,5 O 4. Plošně centrovaná a kubická struktura. Pro plošně centrovanou strukturu jsou ionty umístěny ve struktuře v místech 8a, manganové a niklové ionty jsou náhodně v místech 16d. Kyslíkové ionty zabírají pozice v mřížce 32e. V případě kubické struktury jsou ionty manganu na pozicích 12d a ionty niklu v 4a. Kyslíkové ionty zabírají 24e a 8c pozice, zatímco ionty lithia se nachází na pozici 8c. Jestli LiNi 0,5 Mn 1,5 O 4 má strukturu plošně centrovanou nebo kubickou je závislé na syntetických cestách. Proces žíhání na 700 C po kalcinaci vede k uspořádání a přemístění Ni a Mn iontů z plošně centrované do kubické mřížky. Schematický nákres obou struktur LiNi 0,5 Mn 1,5 O 4 je znázorněn na obr.10. Pro rozlišení struktury je vhodná infračervená spektroskopie. [10] Obrázek 10:Vlevo rozložení prvků v plošně centrované struktuře, Vpravo rozložení v kubické struktuře [10] 22
23 5 Použité zařízení a elektrochemické měřící metody Jeden z důležitých prvků při konstrukci lithium-iontových článků je dodržení prostředí bez vlhkosti při manipulaci s elektrodovými materiály před a v průběhu měření. K tomu slouží rukavicový box Jacomex, který je naplněn inertní argonovou atmosférou s trvale udržovaným množstvím vody a kyslíku. Obrázek 11:Rukavicový box Jacomex Na elektrochemická měření byly využity měřící cely El-Cell ECC-STD. Tyto cely jsou určeny k měření lithno-iontových článků a aprotických chemikálií. Cely se sestavovaly v již zmíněném rukavicovém boxu. Pro samotné měření se používal potenciostat-galvanostat firmy BioLogic s 16ti kanály a PC programem EC-Lab V10. [22] Obrázek 12: Měřící cela El-Cell ECC-STD 23
24 5.1 Galvanostatické nabíjení/vybíjení Tuto metodu používáme pro analýzu a předpověď výkonu aktivních materiálů v reálných provozních podmínkách. Pracovní elektrodou prochází konstantní proud (nabíjecí nebo vybíjecí) a zaznamenáváme napětí jako funkci času mezi minimálními a maximálními hodnotami. Proud je nastavován jako podíl nebo jako násobek stanovené vybíjecí kapacity elektrody (C), kde C je náboj dodaný za jednu hodinu. Primární poznatky získané z těchto měření jsou kapacita elektrody, změna potenciálu jako funkce stavu nabití, cyklovatelnost a odhad ohmického poklesu. Testování materiálů citlivých na vlhkost je nejvhodnější provádět v boxu s argonovou atmosférou nebo ve speciálních uzavřených celách. Cyklování může být také prováděno v termostatickém boxu pro zjišťování vlivu teploty. [22] 5.2 Rastrovací elektronová mikroskopie (SEM) Činnost rastrovacího elektronového mikroskopu je založena na použití úzkého svazku elektronů emitovaných ze žhavené katody a urychlovaných v elektronové trysce, která je tvořena systémem katoda - Wehneltův válec - anoda. Paprsek je poté dále zpracován elektromagnetickými čočkami a je rozmítán po povrchu pozorovaného objektu. Synchronně s tímto svazkem elektronů je rozmítán elektronový svazek paprsku v pozorovací obrazovce. [] Interakcí elektronového svazku s povrchem objektu, který pozorujeme, vznikají sekundární elektrony (zároveň s fotony, odraženými elektrony aj.). Ty po detekci a zesílení modulují jas elektronového paprsku v pozorovací obrazovce, tudíž na obrazovce vznikne obraz odpovídající povrchu pozorovaného vzorku. [22] 5.3 Prvková analýza (EDS) EDS je analýza, která se zabývá strukturou materiálu a analyzuje zastoupení prvku v proměřovaném materiálu. Při této metodě se využívá EDS detektoru RTG záření v rastrovacím elektronovém mikroskopu. Při dopadu elektronu na zkoumaný vzorek dochází ke generaci charakteristického RTG záření. Toto záření je zachyceno detektorem a následně vyhodnoceno. Po vyhodnocení je možné určit jednotlivé prvky, které zkoumaný vzorek obsahuje. [22] 24
25 6 Praktická část 6.1 Výroba elektrodových materiálů Na výrobu materiálů byly použity dvě metody výroby elektrod. Známá metoda třístupňového žíhání, kterou se vyrobil materiál v rámci semestrálního projektu LiNi 0,5 Mn 1,5 O 4 a metoda prudkého ohřevu pro otestování vlastností materiálů LiNi 0,5 Mm 1,5 O 4, LiNi 0,45 Mn 1,55 O 4 a LiNi 0,55 Mn 1,45 O Metodou třístupňového žíhání LiNi 0,5 Mn 1,5 O 4 Při přípravě materiálu LiNi 0,5 Mn 1,5 O 4 byly použity základní materiály na bázi uhličitanů. Níže je uvedena tabulka s prekurzory a příklad výpočtu. Tabulka 1:Prekurzory Chemikálie Vzorec M r [g/mol] m [g] Uhličitan lithný Li 2 CO 3 73,8909 1,6256 Uhličitan manganatý MnCO 3 114,9469 6,8968 Oxid nikelnatý NiO 74,6928 1,4939 Množství jednotlivých prvků bylo stanoveno na 0,04M. Příklad výpočtu hmotnosti pro Li 2 CO 2 : =, kde m hmotnost [g] M r molární hmotnost [g/mol] n koncentrace [mol/l] a zastoupení prvku ve sloučenině x procentuální zastoupení materiálu v aktivní hmotě Pro Li 2 CO 3 výpočet: = =73,8909 0,04 0,5 1,1=1,6256% Pozn. Uvedený výpočet je shodný pro zbylé prekurzory a pro ostatní materiály. 25
26 Postup přípravy: 1) Dle vypočtených hmotností byly jednotlivé materiály naváženy váhou KERN ALS ) Materiál po 40ti minutovém chodu byl rozmíchán v planetovém mlýnu za pomoci železných kuliček průměr 10mm při 500 ot/min. 3) Po rozmíchání materiál opět zvážíme a vložíme do žíhací misky. 4) Výsledná směs byla třikrát žíhaná v peci za přístupu vzduchu Po dobu 10h při 600 C Po dobu 15h při 900 C při teplotě ohřevu 3 C/min a rychlosti chlazení 1 C/min Po dobu 15h při 700 C při rychlosti ohřevu 3 C/min a rychlosti chlazení 0,2 C/min 5) Postup výroby elektrodové hmoty na nanesení na hliníkovou folii: Na celkové množství pasty 0,4 g použijeme: 80% aktivní hmoty = 0,32 g, pojiva PVDF (polyvinylfluorid) 10% = 0,04g a 10% super P (uhlík) = 0,04 g Celé zakápneme rozpouštědlem NMP (N-methyl 2-pyrrolidone) množstvím 18 ul a necháme směs míchat 10 h 6) Tuto elektrodovou pastu naneseme na folii a necháme vysušit v sušičce. 7) Výsečníkem vysekneme elektrodu z folie a slisujeme v lisu silou 800 kg/cm 2 [22] Příprava metodou prudkého ohřevu: LiNi 0,5 Mn 1,5 O 4, LiNi 0,45 Mn 1,55 O 4 a LiNi 0,55 Mn 1,45 O 4 Touto metodou byly vytvořeny materiály s různým poměrem zastoupení niklu a manganu. Množství jednotlivých prekurzorů je vypočítáno stejně jako u metody třístupňového žíhání. Tabulka 2:Prekurzory jednotlivých materiálů 26
27 Postup přípravy: 1) Dle vypočtených hmotností byly jednotlivé materiály naváženy váhou KERN ALS ) Materiály byly po dobu 1 min při 100 rpm rozemílány na planetovém mlýně s kuličkami 10 mm. Následně byly znovu rozemílány po dobu 10 min při 300 rpm 3) Následně byly peletovány po dobu 15 min tlakem 2T. 4) Vzorky byly po mletí zváženy a vloženy do pece na žíhání: rychlý ohřev na 900 C vzduchem a čekání na teplotě po dobu 5 min, následně prudké zchlazení na 600 C za přístupu kyslíku. Na 600 C setrvá po dobu 24 h, poté následuje prudký pokles na pokojovou teplotu. 5) Po žíhání byly vzorky chlazeny přibližnou rychlostí 8 C/min. 6) Vzorky byly z pece vytaženy a rozemílány 10 min při 300 rpm. 7) Před mletím a po mletí byly materiály zváženy. 8) Postup výroby elektrodové hmoty na nanesení na hliníkovou folii: Na celkové množství pasty 0,4 g použijeme: 80% aktivní hmoty = 0,32 g, pojiva PVDF (polyvinylfluorid) 10% = 0,04g a 10% super P (uhlík) = 0,04 g Celé zakápneme rozpouštědlem NMP (N-methyl 2-pyrrolidone) množstvím 18 ul a necháme směs míchat 10 h 9) Tuto elektrodovou pastu naneseme na folii a necháme vysušit v sušičce. 10) Výsečníkem vysekneme elektrodu z folie a slisujeme v lisu silou 800 kg/cm Měření a dosažené výsledky U všech vyrobených materiálů bylo nejprve provedeno měření dvou nabíjecích a vybíjecích cyklů při 0,5C za předpokladu kapacity 120mAh/g. Potenciálové okno bylo nastaveno v rozmezí 5,1 3 V. Následovalo proměření 10 cyklů při 0,5C, poté je ověřovala schopnost vyššího zatížení proudem 1C po čtyři cykly. Nakonec jsme znovu snížili proud na 0,5 C a proměřili pokles kapacity u každého materiálu po dalších 10 cyklů. Z takto získaných dat jsem spočítala procentuelní pokles kapacity u všech materiálů. 27
28 6.2.1 Metoda prudkého ohřevu LiNi 0,5 Mn 1,5 O 4 5,0 4,5 U [V] 4,0 3,5 3, t [h] Obrázek 13: Průběh prvních dvou nabíjecích a vybíjecích cyklů materiálu LiNi 0,5 Mn 1,5 O 4 Po změření prvních dvou nabíjecích a vybíjecích cyklů bylo provedeno měření 10 cyklů proudem 0,5C. Z grafu je patrné, že kapacita klesala velmi pomalu. První cyklus dosáhla kapacita 70,9 mah/g, desátý cyklus poklesla na 68,8 mah/g. Tento materiál vykazoval nepatrné plato při 4V. U [V] 5,0 4,8 4,6 4,4 4,2 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 14: Deset vybíjecích cyklů LiNi 0,5 Mn 1,5 O 4 28
29 Druhým krokem v proměřování vyrobeného materiálu spočíval v měření odezvy materiálu na rostoucí zatížení proudem 1C po 4 cykly viz.obr.15. Zde došlo ke změně kapacity z 54,2 mah/g na hodnotu 51,1 mah/g. Materiál tak prokázal dobrou zatížitelnost. U [V] 4,8 4,6 4,4 4,2 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 15: Čtyři vybíjecí cykly LiNi 0,5 Mn 1,5 O 4 Následovalo snížení proudu znovu na 0,5C a proměřit dalších 10 cyklů. V prvním cyklu materiál dosáhl kapacity 66,2 mah/h, v posledním cyklu poklesla kapacita na 62,2 mah/g. 4,8 4,6 4,4 4,2 U [V] 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 16: Znovu deset vybíjecích cyklů LiNi 0,5 Mn 1,5 O 4 29
30 Pro přehlednost jsem vypočítala procentuální pokles kapacity během cyklování materiálu viz. Tab.3. Vidíme, že největší pokles kapacity materiál vykazoval při dalších 10 cyklech proudem 0,5C. Pod Tab.3 vidíme graf poklesu materiálu LiNi 0,5 Mn 1,5 O 4 v průběhu celého cyklování. Tabulka 3:Procentuální pokles kapacity během cyklování LiNi 0,5 Mn 1,5 O 4 metodou prudkého ohřevu Kapacita [mah/g] ,5C 1C 0,5C Počet cyklů Obrázek 17:Porovnání kapacity v závislosti na zatížení materiálu LiNi 0,5 Mn 1,5 O 4 Byl pořízen snímek materiálu LiNi 0,5 Mn 1,5 O 4 viz. Obr.18. Na snímku vidíme krystalovou strukturu a uspořádání krystalů. Velikost jednotlivých krystalů je přibližně 3um. 30
31 Obrázek 18:SEM analýza LiNi 0,5 Mn 1,5 O Metoda třístupňového žíhání LiNi 0,5 Mn 1,5 O 4 Na proměření byla použita metoda výroby elektrody třístupňovým žíháním. Měření tohoto materiálu proběhlo pomocí již v textu teoreticky rozebíraných elektrochemických metod a to galvanostatického cyklování, rastrovací elektronovou mikroskopií a prvkovou analýzou. U tohoto materiálu bylo provedeno určení kapacity pomocí dvou cyklů při 0,5C za předpokladu kapacity 120 mah/g viz. Obr.19. Potenciálové okno bylo nastaveno v rozmezí 5,1 3 V. Z grafů je patrné, že tento materiál má stabilní plato při 4,6 V a poté napětí klesá, žádné nižší plato již nevykazuje. V prvních dvou cyklech byla dosažena kapacita 109 a 105 mah/g. [22] 31
32 5,0 4,5 U [V] 4,0 3,5 3, t [h] Obrázek 19: Průběh prvních dvou nabíjecích a vybíjecích cyklů LiNi 0,5 Mn 1,5 O 4 [22] 4,8 4,6 4,4 4,2 U [V] 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 20: Průběh kapacity v prvních dvou vybíjecích cyklech materiálu LiNi 0,5 Mn 1,5 O 4 [22] Po těchto dvou cyklech bylo provedeno měření 10 nabíjecích i vybíjecích cyklů korigovaným proudem 0,5C dle výsledků předchozích dvou cyklů viz. Obr.21. Z těchto deseti cyklů je patrné, že dochází k mírnému poklesu kapacity ze 101 mah/g na 92 mah/g. [22] 32
33 4,8 4,6 4,4 4,2 U [V] 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 21: Deset vybíjecích cyklů materiálu LiNi 0,5 Mn 1,5 O 4 proudem 0,5C [22] Další krok spočíval v měření odezvy materiálu na rostoucí zatížení proudem 1C po 4 cykly viz. Obr.22. Při změně zatížení došlo pouze k malému poklesu kapacity z 92,9 mah/g na 84,6 mah/g. Tento mírný pokles kapacity svědčí o dobré zatížitelnosti tohoto materiálu. [22] 4,8 4,6 4,4 4,2 U [V] 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 22: Čtyři vybíjecí cykly materiálu LiNi 0,5 Mn 1,5 O 4 proudem 1C [22] 33
34 U [V] 4,8 4,6 4,4 4,2 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 23: Posledních 10 vybíjecích cyklů materiálu LiNi 0,5 Mn 1,5 O 4 proudem 0,5C [22] V poslední řadě bylo provedeno opět 10 cyklů proudem 0,5C viz. Obr.23. Po předchozích 4 cyklech při 1C došlo opět při snížení proudu na 0,5C k nárůstu kapacity takřka na hodnotu před změnou proudu. Obecně kapacita klesá výrazně pomaleji oproti jiným druhům materiálů. Po 24 cyklech kapacita poklesla o 16%. Pokles kapacity je zobrazen na Obr.24. [22] Tabulka 4:Procentuální pokles kapacity během cyklování LiNi 0,5 Mn 1,5 O 4 [22] Označení vybíjecího cyklu LiNi 0,5 Mn 1,5 O 4 Pokles [%] 0,5C - cyklus č.1 101,3 0,5C - cyklus č.10 92,9 1C - cyklus č.1 84,6 1C - cyklus č.4 81,7 0,5C - cyklus č.1 89,1 0,5C - cyklus č.10 84,2 8,3 3,4 5,5 34
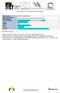
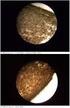
35 100 0,5C 1C 0,5C Kapacita [mah/g] Počet cyklů 25 Obrázek 24:Porovnání kapacity v závislosti na zatížení materiálu LiNi 0,5 Mn 1,5 5O 4 [22] SEM a EDS analýza vzorku LiNi 0,5 Mn 1,5 O 4 Kromě elektrochemických měření byl vytvořený materiál LiNi 0,5 Mn 1,5 O 4 také podroben fyzikálním analýzám pomocí rastrovacího elektronového mikroskopu. Bylo pořízeno několik obrázků částice materiálu LiNi 0,5 Mn 1,5 O 4. Na Obr.25 A vidíme několik částic, z nichž největší je přibližně 75µm. Na Obr. 25 B je tato částice LiNi 0,5 Mn 1,5 O 4 přiblížena při využitém zvětšení 5000krát a jeho krystalová struktura, kde jednotlivé krystaly jsou asi 3µm velké. Na tomto obrázku jsou patrné krystaly, které bylyy vytvořeny během procesu přípravy, velikost jednotlivých krystalů je menší než 5µm. [22] A B Obrázek 25:SEM analýza materiálu LiNi 0,5 Mn 1,5 O 4 : A - zvětšeno 1kx a B - zvětšeno 5kx [22] Poslední provedené měření tohoto materiálu bylo pomocí prvkové analýzy. Zde vidíme jednotlivé rozložení prvků v materiálu LiNi 0,5 Mn 1,5 O 4. Na Obr.26 A jsou zobrazeny částice 35
36 materiálu LiNi 0,5 Mn 1,5 O 4. Obr.26 B ukazuje rozložení niklu v materiálu, Popis rozložení kyslíku je na Obr.26 C a Obr.26 D reprezentuje rozložení manganu. Všechny snímky byly 6665krát zvětšeny a vidíme, že prvky jsou v materiálu rovnoměrně rozloženy a převážná část částic je menších než 5µm. [22] A B C D Obrázek 26: Mapování vzorku LiNi 0,5 Mn 1,5 O 4 A) SEM částice materiálu LiNi 0,5 Mn 1,5 O 4 B) rozložení niklu C) rozložení kyslíku D) rozložení manganu [22] 36
37 6.2.3 Metoda prudkého ohřevu LiNi 0,45 Mn 1,55 O 4 5,0 4,5 U [V] 4,0 3,5 3, t [h] Obrázek 27: Průběh prvních dvou nabíjecích a vybíjecích cyklů materiálu LiNi 0,45 Mn 1,55 O 4 Tento materiál po výrobě má dlouhé vybíjecí plato při 4,7V. Nejvyšší dosažená kapacita je 68,7 mah/g, kterou LiNi 0,45 Mn 1,55 O 4 dosáhl v prvním z 10 cyklů proudem 0,5C. Desátý cyklus téhož proudu kapacita poklesla na 59,9 mah/g. U [V] 4,8 4,6 4,4 4,2 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 28: Deset vybíjecích cyklů LiNi 0,45 Mn 1,55 O 4 37
38 Při zatěžování proudem 1C během 4 cyklů, kapacita LiNi 0,45 Mn 1,55 O 4 se snižovala pomalu. Nejvyšší kapacita dosažená tímto proudem byla 44,8 mah/g v prvním cyklu a nejnižší hodnota 43,1 mah/g v posledním tj. čtvrtém cyklu. 4,8 4,6 4,4 4,2 U [V] 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 29: Čtyři vybíjecí cykly LiNi 0,45 Mn 1,55 O 4 Po snížení proudu z 1C na 0,5C jsme změřili dalších 10 cyklů. Zde nastal větší pokles kapacit. Nejvyšší hodnotu kapacity materiál dosáhl v prvním cyklu hodnotou 52,9 mah/g a postupně se snižovala až na hodnotu desátého cyklu 44 mah/g viz.obr.30. Za 24 změřených cyklů poklesla kapacita o 37%. Procentuální pokles kapacity LiNI 0,45 Mn 1,55 O 4 během cyklování popisuje Tab.4. Na Obr. 31 je pokles kapacity v závislosti na zatížení materiálu. 38
39 U [V] 4,8 4,6 4,4 4,2 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 30: Znovu deset vybíjecích cyklů LiNi 0,45 Mn 1,55 O 4 Tabulka 5:Procentuální pokles kapacity během cyklování LiNi 0,45 Mn 1,55 O ,5C 1C 0,5C 60 Kapacita [mah/g] Počet cyklů Obrázek 31:Porovnání kapacity v závislosti na zatížení materiálu LiNi 0,45 Mn 1,55 O 4 39
40 6.2.4 Metoda prudkého ohřevu LiNi 0,55 Mn 1,45 O 4 5,0 4,5 U [V] 4,0 3,5 3, t [h] Obrázek 32: Průběh prvních dvou nabíjecích a vybíjecích cyklů materiálu LiNi 0,55 Mn 1,45 O 4 Poslední vyrobený materiál byl LiNi 0,55 Mn 1,45 O 4. Má vybíjecí plato při 4,6V a tendenci k vytvoření nižšího vybíjecího plata kolem 4V. V průběhu cyklování proudem 0,5C dosáhla kapacita na 75,7 mah/g v prvním cyklu, v posledním cyklu došlo ke snížení kapacity na hodnotu 59,6 mah/g. U [V] 5,0 4,8 4,6 4,4 4,2 4,0 3,8 3,6 3,4 3,2 3, Cvvyb [mah/g] Obrázek 33: Deset vybíjecích cyklů LiNi 0,55 Mn 1,45 O 4 40
41 Zatížitelnosti tohoto materiálu se neprokázala dobrá, neboť při proudu 1C dosáhl v prvním cyklu 31,0 mah/g a v posledním čtvrtém cyklu kapacita se snížila na 23,2 mah/g viz Obr.34. 4,6 4,4 4,2 4,0 U [V] 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 34: Čtyři vybíjecí cykly LiNi 0,55 Mn 1,45 O 4 Poslední zatěžování LiNi 0,55 Mn 1,45 O 4 bylo proudem 0,5C po 10 cyklů. Z Obr. 35 je patrné, že první cyklus má nejdelší vybíjecí plato a s počtem cyklů se plato neustále zkracuje a materiál rychle ztrácí svou kapacitu. V prvním cyklu dosáhl kapacity 52,5 mah/g a v posledním cyklu pouze 19,5 mah/g.v Tab.5 poukazuji na procentuální pokles kapacity v různých fázích cyklování. Celkově po 24 nabíjecích a vybíjecích cyklech kapacita poklesla o 74%. Na Obr.36 je porovnaná kapacita v závislosti na zatížení, kde dochází k rychlému klesání kapacity v závislosti na počtu cyklů. 41
42 4,8 4,6 4,4 4,2 U [V] 4,0 3,8 3,6 3,4 3,2 3, Cvyb [mah/g] Obrázek 35: Znovu deset vybíjecích cyklů LiNi 0,55 Mn 1,45 O 4 Tabulka 6:Procentuální pokles kapacity během cyklování LiNi 0,55 Mn 1,45 O O 4 Kapacita [mah/g] Počet cyklů Obrázek 36:Porovnání kapacity v závislosti na zatížení materiálu LiNi 0,55 Mn 1,45 O 4 42
43 7 Závěr Tato práce se zabývala studiem katodových materiálů pro lithiové články s napětím okolo 5V. V teoretické části byly popsány materiály pro kladné a záporné elektrody, konstrukce a princip funkce Li-ion akumulátorů, použité zařízení a elektrochemické měřící metody. Úkolem praktické části práce bylo seznámení se s principem elektrochemických reakcí v lithiových akumulátorech a připravit vzorky materiálů odvozených od oxidu manganičitolithného a popsat elektrochemické vlastnosti z hlediska stability a zatížitelnosti. V této bakalářské práci byly vyrobeny tři materiály novou metodou prudkého ohřevu: LiNi 0,5 Mn 1,5 O 4, LiNi 0,45 Mn 1,55 O 4 a LiNi 0,55 Mn 1,45 O 4. Každá elektroda byla proměřena pro zjištění elektrochemických vlastností metodou galvanostatického cyklování. Materiál LiNi 0,5 Mn 1,5 O 4 vytvořený jak metodou prudkého ohřevu tak třístupňovým žíháním byl navíc pozorován pomocí rastrovací elektronové mikroskopie a podroben prvkové analýze. LiNi 0,5 Mn 1,5 O 4 má delší vybíjecí plato při 4,6V a nepatrné plato při 4V. Nejvyšší dosažená kapacita je 70,9 mah/g. Zatěžování proudem 1C po 4 cykly klesla kapacita o 5,7%. V posledních 10 cyklech docházelo k rychlejšímu poklesu kapacity. Celkový pokles kapacity za 24 změřených cyklů byl 23%. LiNi 0,45 Mn 1,55 O 4 vykazoval pouze dlouhé vybíjecí plato 4,6V při 0,5C a při 1C dojde k poklesu na 4,5V. Při zatěžování proudem 1C došlo při 4 cyklech k poklesu kapacity o 3,7%. Nejvyšší změřená kapacita byla 68,7 mah/g. U tohoto materiálu dochází ke strmějšímu poklesu kapacity a celkově kapacita za 24 cyklů poklesla o 37%. LiNi 0,55 Mn 1,45 O 4 má největší pokles kapacity při zatěžování proudem 1C. Po 4 cyklech došlo k úbytku kapacity o 25,1%. Vybíjecí plato je na 4,6V. Cyklování probíhalo bez kapacitních výkyvů. Vykazoval nejvyšší změřenou kapacitu 75,7 mah/g. Během posledních 10 cyklů došlo ke snížení kapacity o 62,8% a celkový pokles po 24 cyklech je 74%. Tento materiál se prokázal být ze všech nejhorší, ať už se jedná o velkou ztrátu kapacity při cyklování proudem 0,5C, tak při zatížení proudem 1C. Pro porovnání vlastností v závislosti na použité metodě byl vyroben materiál LiNi 0,5 Mn 1,5 O 4 také pomocí metody třístupňového žíhání. Materiál vyrobený třístupňovým žíháním vykazoval delší a stabilnější vybíjecí plato kolem 4,7V bez tendence k vytvoření nižších plat. V průběhu celého cyklování docházelo ke slabému poklesu kapacity. Po proměřených 24 cyklech kapacita poklesla o 16%. Materiál zvládal i vyšší zatížení proudem 1C, po 4 změřených cyklech došlo k poklesu o 3,4%. Porovnáním krystalů materiálů LiNi 0,5 Mn 1,5 O 4 vidíme menší krystaly utvořené ve shlucích metodou prudkého ohřevu, kdežto u metody třístupňového žíhání došlo k vytvoření krystalové struktury rovnoměrně v celém materiálu. Vzhledem k naměřeným 43
44 elektrochemickým výsledkům materiál vyrobený třístupňovým žíháním s rovnoměrně vytvořenou krystalovou strukturou dosahoval lepších vlastností. Přestože je metoda prudkého ohřevu rychlejší a jednodušší, tak vyrobený materiál vykazoval horší vlastnosti než u materiálu vyrobeného třístupňovým žíháním. Materiál má delší vybíjecí plato při 4,6V a nepatrné plato při 4V. V posledních 10 cyklech materiál rychleji snižoval svou kapacitu. Po 24 cyklech celkově kapacita poklesla o 23%, což je o 7% vyšší pokles než u prvního materiálu. Při zvýšení zatížení proudem 1C se po 4 cyklech snížila o 5,7%. Po proměření vyrobených materiálů má nejlepší vlastnosti LiNi 0,5 Mn 1,5 O 4 s poměrem Ni a Mn 0,5 a 1,5, neboť kapacita po delším cyklování i po zatěžování vyšším proudem klesala mírně. Toto zjištění odpovídá poznatkům uváděným ve studovaných článcích. 44
45 8 Seznam literatury [1] MAREK, J.; STEHLÍK, L. Hermetické akumulátory v praxi. Brno, s. [cit ] [2] ČENĚK, M. Akumulátory od teorie k praxi s. ISBN: [3] Univerzita Pardubice Fakulta chemicko-technologická: Interkalační sloučeniny [online],[cit ]. Dostupné z: [4] KISHIDA, K., WADA, N., ADACHI, H., TANAKA, K., INUI, H., YADA, C., IRIYAMA, Y. A OGUMI, Z., Microstructure of the LiCoO 2 (cathode ) /La 2/3- xli 3x TiO 3 (electrolyte) interface and its influences on the electrochemical properties. Acta Materialia. Roč. 55, č.14, s ISSN [5] Electropaedia: Rechargeable Lithium Batterie [online]. [cit ]. Dostupné z: [6] OHZUKU, Tsutomu a Ralph J. BRODD. An overview of positive-electrode materials for advanced lithium-ion batteries. Journal of Power Sources. Roč. 174, č.2, s ISSN [7] HUANG, Yanghui, Haibo REN, Zhenghe PENG a Yunhong ZHOU. Synthesi sof LIFePO4/carbon composite from nano-fepo4 by a novel stearin acid assisted rheological phase method. Electrochimica Acta. Roč. 55, č.1, s ISSN [8] LINDEN, David a Thomas B Reddy. Handbook of bateries. 3rd ed. New York: MCGraw-Hill, 2002, ISBN [9] PATOUX, Sebastien, Lucas SANNIER, Héléne LIGNIER, Yvan REYNIER, Carol BOURBON, Séverine JOUANNEAU, Frédéric LE CRAS, Sébastien MARTINET, Ji-Guang ZHANG, Héléne LIGNIER, High voltage nickel manganem spinel oxides for Li-ion batteries. Electrochimica Acta. Roč. 53, č. 12, s ISSN [10] GUOQUANG, Liu, LiNi 0,5 Mn 1,5 O 4 spinel and its derivatives as cathodes for Li-Ion batteries. Lithium Ion batteries-new developments. ISBN: [11] WANG, G.X., YAO, P., ZHONG, S., BRADHURST, D. H., DOU, S. X., LIU, H.K. Electrochemical study on orthorhombic LiMnO 2 as cathode in rechargeable lithium batteries. Institute for Superconducting & Electronic materials
46 [12] WU SHE-HUANG, YU MING-TLAU. Preparation and characterization of o- LiMnO 2 cathode materials. Journal of Power Sources. Roč. 165, s [13] ZHANG, Y., WANG, CH. Cycle-life characterization of automotive lithium- Ion batteries with LiNiO 2 cathode. Journal of The Electrochemical Society. Roč. 156, s [14] WHITTINGHAM, M. S., Lithium Batteries and Cathode Materials.Department of Chemistry and Materials Science, State University of New York [15] LIU, C., NAN, J., ZUO, X., XIAO, X., SHU, D. Synthesis and Electrochemical Characteristics of an Orthorhombic LiMnO 2 Cathode Material Modified With Poly (Vinyl-Pyrrolidone) for Lithium Ion Batteries. School of Chemistry and Environment [16] MOLENDA, J., ZIEMNICKI, M., MOLENDA, M., BUČKO, M., MARZEC, J. Transport and electrochemical properties of orthorhombic LiMnO 2 cathode material for Li-ion batteries. University of Science and Technology. Roč. 24. Cracow [17] ITOU, Y., UKYO, Y. Performance of LiNiCoO 2 Based Materials for Advanced Lithium-Ion Batteries. The Electrochemical Society. Japan [18] ARAI, H., OKADA, S., SAKURAI, Y., YAMAKI, J. Reversibility of LiNiO 2 cathode. NTT Interdisciplinary Research Laboratories Tokai, s Japan [19] Li-ion baterie: Li-ion baterie:principy, provoz, rady (1.část) [online] Dostupné z: 1cast/strana/0/2 [20] FEDORKOVÁ, A.: Analytical characterization of polypyrrole-lipepo4 powder as positive electrode material for lithium-ion batteries. Bratislava, Disertační práce. Univerzita Komenského v Bratislavě. [21] FANG, H., WANG, Z., LI, X., GUO, H., PENG, W.: Exploration of high capacity LiNi0,5Mn1,5O4 synthesized by solid-state reaction. China, School of Metallurgical Science and Engineering. [22] BUKÁČKOVÁ, I. Katodové materiály pro lithiové články s napětím okolo 5V. [cit ]. Brno: Vysoké učení technické v Brně, Fakulta elektrotechniky a komunikačních technologií,
Úprava struktury materiálu LiCoO 2 pomocí sodíku
 Rok / Year: Svazek / Volume: Číslo / Number: 2013 15 6 Úprava struktury materiálu LiCoO 2 pomocí sodíku Modifying of the structure of the material LiCoO 2 with sodium Tomáš Kazda, Jiří Vondrák, Marie Sedlaříková,
Rok / Year: Svazek / Volume: Číslo / Number: 2013 15 6 Úprava struktury materiálu LiCoO 2 pomocí sodíku Modifying of the structure of the material LiCoO 2 with sodium Tomáš Kazda, Jiří Vondrák, Marie Sedlaříková,
Sekundární elektrochemické články
 Sekundární elektrochemické články méně odborně se jim říká také akumulátory všechny elektrochemické reakce jsou vratné (ideálně na 100%) řeší problém ekonomický (vícenásobné použití snižuje náklady) řeší
Sekundární elektrochemické články méně odborně se jim říká také akumulátory všechny elektrochemické reakce jsou vratné (ideálně na 100%) řeší problém ekonomický (vícenásobné použití snižuje náklady) řeší
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
ELEKTRODY PRO LITHNO-IONTOVÉ BATERIE NA BÁZI KOBALTITANU LITHNÉHO ELECTRODES FOR LITHIUM-IONS BATTERIES BASED ON LICoO 2
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNILOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNILOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
Akumulátory Li-S. Připravil: Ing. Tomáš Kazda, Ph.D.
 Připravil: Ing. Tomáš Kazda, Ph.D. Využití a růst produkce Li-Ion akumulátorů Obr.1: Příklady použit Li-ion akumulátorů [1] Využití a růst produkce Li-Ion akumulátorů Obr.2: Zastoupení jednotlivých typů
Připravil: Ing. Tomáš Kazda, Ph.D. Využití a růst produkce Li-Ion akumulátorů Obr.1: Příklady použit Li-ion akumulátorů [1] Využití a růst produkce Li-Ion akumulátorů Obr.2: Zastoupení jednotlivých typů
Li S akumulátory pro dopravu. Autor: Ing. Tomáš Kazda, Ph.D
 Li S akumulátory pro dopravu Autor: Ing. Tomáš Kazda, Ph.D. 6.6.2017 Výhody Li-Ion akumulátorů Vysoký potenciál Vysoká gravimetrická hustota energie Vysoká volumetrická hustota energie Dlouhá životnost
Li S akumulátory pro dopravu Autor: Ing. Tomáš Kazda, Ph.D. 6.6.2017 Výhody Li-Ion akumulátorů Vysoký potenciál Vysoká gravimetrická hustota energie Vysoká volumetrická hustota energie Dlouhá životnost
Baterie minulost, současnost a perspektivy
 Baterie minulost, současnost a perspektivy Prof. Ing. Jiří Vondrák, DrSc. Doc. Ing. Marie Sedlaříková, CSc. Ústav elektrotechnologie, Fakulta elektrotechniky a komunikačních technologií, Vysoké učení technické
Baterie minulost, současnost a perspektivy Prof. Ing. Jiří Vondrák, DrSc. Doc. Ing. Marie Sedlaříková, CSc. Ústav elektrotechnologie, Fakulta elektrotechniky a komunikačních technologií, Vysoké učení technické
AKUMULÁTORY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 15. 3. 2012. Ročník: devátý
 Autor: Mgr. Stanislava Bubíková AKUMULÁTORY Datum (období) tvorby: 15. 3. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí se zdroji elektrického
Autor: Mgr. Stanislava Bubíková AKUMULÁTORY Datum (období) tvorby: 15. 3. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí se zdroji elektrického
Základy elektrotechniky
 A) Elektrický obvod je vodivé spojení elektrických prvků (součástek) plnící zadanou funkci např. generování elektrického signálu o určitých vlastnostech, zesílení el. signálu, přeměna el. energie na jiný
A) Elektrický obvod je vodivé spojení elektrických prvků (součástek) plnící zadanou funkci např. generování elektrického signálu o určitých vlastnostech, zesílení el. signálu, přeměna el. energie na jiný
Elektrochemické akumulátory. přehled
 Elektrochemické akumulátory přehled Porovnání měrných parametrů akumulátorů SEKUNDÁRNÍ ČLÁNKY - AKUMULÁTORY Vsoučasnosti jsou nejrozšířenější akumulátory na bázi olova, niklu a lithia Podle acidity elektrolytu
Elektrochemické akumulátory přehled Porovnání měrných parametrů akumulátorů SEKUNDÁRNÍ ČLÁNKY - AKUMULÁTORY Vsoučasnosti jsou nejrozšířenější akumulátory na bázi olova, niklu a lithia Podle acidity elektrolytu
Kobaltem dopované LiFePO4 pro katody li-ion akumulátorů připravené metodou GAC
 Rok / Year: Svazek / Volume: Číslo / Issue: 2012 14 1 Kobaltem dopované LiFePO4 pro katody li-ion akumulátorů připravené metodou GAC Cobalt-doped LiFePO4 cathode for lithium-ion batteries prepared by GAC
Rok / Year: Svazek / Volume: Číslo / Issue: 2012 14 1 Kobaltem dopované LiFePO4 pro katody li-ion akumulátorů připravené metodou GAC Cobalt-doped LiFePO4 cathode for lithium-ion batteries prepared by GAC
Technické sekundární články - AKUMULÁTOR
 Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Technické sekundární články - AKUMULÁTOR Galvanické články, které je možno opakovaně nabíjet a vybíjet se nazývají
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Technické sekundární články - AKUMULÁTOR Galvanické články, které je možno opakovaně nabíjet a vybíjet se nazývají
Jak funguje baterie?
 Jak funguje baterie? S bateriemi se setkáváme na každém kroku, v nejrůznějších velikostech a s nejrůznějším účelem použití od pohonu náramkových hodinek po pohon elektromobilu nebo lodě. Základem baterie
Jak funguje baterie? S bateriemi se setkáváme na každém kroku, v nejrůznějších velikostech a s nejrůznějším účelem použití od pohonu náramkových hodinek po pohon elektromobilu nebo lodě. Základem baterie
VYSOKÉ U ENÍ TECHNICKÉ V BRN. Fakulta elektrotechniky a komunika ních technologií
 VYSOKÉ U ENÍ TECHNICKÉ V BRN Fakulta elektrotechniky a komunika ních technologií DIPLOMOVÁ PRÁCE Brno, 2016 Bc. Miloslav Kulhavý VYSOKÉ U ENÍ TECHNICKÉ V BRN BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY
VYSOKÉ U ENÍ TECHNICKÉ V BRN Fakulta elektrotechniky a komunika ních technologií DIPLOMOVÁ PRÁCE Brno, 2016 Bc. Miloslav Kulhavý VYSOKÉ U ENÍ TECHNICKÉ V BRN BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY
Technický pokrok v oblasti akumulátorových baterií
 Technický pokrok v oblasti akumulátorových baterií Ing. Libor Kozubík Vedoucí sektoru energetiky IBM Global Business Services Laboratoře IBM, Almaden, San Jose, CA 2 PROJEKT BATTERY 500 Cíl: Výzkum a vývoj
Technický pokrok v oblasti akumulátorových baterií Ing. Libor Kozubík Vedoucí sektoru energetiky IBM Global Business Services Laboratoře IBM, Almaden, San Jose, CA 2 PROJEKT BATTERY 500 Cíl: Výzkum a vývoj
Úvod do koroze. (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají)
 Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Úvod do koroze (kapitola, která bude společná všem korozním laboratorním pracím a kterou studenti musí znát bez ohledu na to, jakou práci dělají) Koroze je proces degradace kovu nebo slitiny kovů působením
Elektrochemie. 2. Elektrodový potenciál
 Elektrochemie 1. Poločlánky Ponoříme-li kov do roztoku jeho solí mohou nastav dva různé děje: a. Do roztoku se z kovu uvolňují kationty (obr. a), na elektrodě vzniká převaha elektronů. Elektroda se tedy
Elektrochemie 1. Poločlánky Ponoříme-li kov do roztoku jeho solí mohou nastav dva různé děje: a. Do roztoku se z kovu uvolňují kationty (obr. a), na elektrodě vzniká převaha elektronů. Elektroda se tedy
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
ELEKTRICKÝ PROUD V KAPALINÁCH
 ELEKTRICKÝ PROUD V KPLINÁCH 1. Elektrolyt a elektrolýza elektrolyt kapalina, která může vést elektrický proud (musí obsahovat ionty kyselin, zásad nebo solí - rozpuštěné nebo roztavené) elektrolýza proces,
ELEKTRICKÝ PROUD V KPLINÁCH 1. Elektrolyt a elektrolýza elektrolyt kapalina, která může vést elektrický proud (musí obsahovat ionty kyselin, zásad nebo solí - rozpuštěné nebo roztavené) elektrolýza proces,
15. Elektrický proud v kovech, obvody stejnosměrného elektrického proudu
 15. Elektrický proud v kovech, obvody stejnosměrného elektrického proudu 1. Definice elektrického proudu 2. Jednoduchý elektrický obvod a) Ohmův zákon pro část elektrického obvodu b) Elektrický spotřebič
15. Elektrický proud v kovech, obvody stejnosměrného elektrického proudu 1. Definice elektrického proudu 2. Jednoduchý elektrický obvod a) Ohmův zákon pro část elektrického obvodu b) Elektrický spotřebič
Akumulátory. Ing. Dušan Pauček
 Akumulátory Ing. Dušan Pauček Při výrobě elektrické energie pomocí netradičních zdrojů výroby, jako je třeba vítr nebo slunce, je nutno řešit problém co s vyrobenou energií. Kde ji uchovat než dojde k
Akumulátory Ing. Dušan Pauček Při výrobě elektrické energie pomocí netradičních zdrojů výroby, jako je třeba vítr nebo slunce, je nutno řešit problém co s vyrobenou energií. Kde ji uchovat než dojde k
DOUTNAVÝ VÝBOJ. Další technologie využívající doutnavý výboj
 DOUTNAVÝ VÝBOJ Další technologie využívající doutnavý výboj Plazma doutnavého výboje je využíváno v technologiích depozice povlaků nebo modifikace povrchů. Jedná se zejména o : - depozici povlaků magnetronovým
DOUTNAVÝ VÝBOJ Další technologie využívající doutnavý výboj Plazma doutnavého výboje je využíváno v technologiích depozice povlaků nebo modifikace povrchů. Jedná se zejména o : - depozici povlaků magnetronovým
Návrh akumulačního systému
 Návrh akumulačního systému Charakter výroby hybridního zdroje elektrické energie s využitím větrné a fotovoltaické elektrárny vyžaduje pro zajištění ostrovního provozu doplnění celého napájecího systému
Návrh akumulačního systému Charakter výroby hybridního zdroje elektrické energie s využitím větrné a fotovoltaické elektrárny vyžaduje pro zajištění ostrovního provozu doplnění celého napájecího systému
Elektrický proud. Elektrický proud : Usměrněný pohyb částic s elektrickým nábojem. Kovy: Usměrněný pohyb volných elektronů
 Elektrický proud Elektrický proud : Usměrněný pohyb částic s elektrickým nábojem. Kovy: Usměrněný pohyb volných elektronů Vodivé kapaliny : Usměrněný pohyb iontů Ionizované plyny: Usměrněný pohyb iontů
Elektrický proud Elektrický proud : Usměrněný pohyb částic s elektrickým nábojem. Kovy: Usměrněný pohyb volných elektronů Vodivé kapaliny : Usměrněný pohyb iontů Ionizované plyny: Usměrněný pohyb iontů
VEDENÍ ELEKTRICKÉHO PROUDU V LÁTKÁCH
 VEDENÍ ELEKTRICKÉHO PROUDU V LÁTKÁCH Jan Hruška TV-FYZ Ahoj, tak jsme tady znovu a pokusíme se Vám vysvětlit problematiku vedení elektrického proudu v látkách. Co je to vlastně elektrický proud? Na to
VEDENÍ ELEKTRICKÉHO PROUDU V LÁTKÁCH Jan Hruška TV-FYZ Ahoj, tak jsme tady znovu a pokusíme se Vám vysvětlit problematiku vedení elektrického proudu v látkách. Co je to vlastně elektrický proud? Na to
5.0 ZJIŠŤOVÁNÍ FÁZOVÝCH PŘEMĚN
 5.0 ZJIŠŤOVÁNÍ FÁZOVÝCH PŘEMĚN Metody zkoumání fázových přeměn v kovech a slitinách jsou založeny na využití změn převážně fyzikálních vlastností, které fázovou přeměnu a s ní spojenou změnu struktury
5.0 ZJIŠŤOVÁNÍ FÁZOVÝCH PŘEMĚN Metody zkoumání fázových přeměn v kovech a slitinách jsou založeny na využití změn převážně fyzikálních vlastností, které fázovou přeměnu a s ní spojenou změnu struktury
Testování akumulátorových baterií na bázi Lithia v aplikaci pro PZS
 Testování akumulátorových baterií na bázi Lithia v aplikaci pro PZS Ivan Konečný, ZČU Plzeň 1. Úvod Pro zabezpečení nepřetržitého napájení zabezpečovacích zařízení se na železnici používaly do počátku
Testování akumulátorových baterií na bázi Lithia v aplikaci pro PZS Ivan Konečný, ZČU Plzeň 1. Úvod Pro zabezpečení nepřetržitého napájení zabezpečovacích zařízení se na železnici používaly do počátku
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION ÚSTAV ELEKTROTECHNOLOGIE DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION ÚSTAV ELEKTROTECHNOLOGIE DEPARTMENT OF
Proč elektronový mikroskop?
 Elektronová mikroskopie Historie 1931 E. Ruska a M. Knoll sestrojili první elektronový prozařovací mikroskop,, 1 1939 první vyrobený elektronový mikroskop firma Siemens rozlišení 10 nm 1965 první komerční
Elektronová mikroskopie Historie 1931 E. Ruska a M. Knoll sestrojili první elektronový prozařovací mikroskop,, 1 1939 první vyrobený elektronový mikroskop firma Siemens rozlišení 10 nm 1965 první komerční
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF ELECTRICAL
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF ELECTRICAL
Fyzikální vzdělávání. 1. ročník. Učební obor: Kuchař číšník Kadeřník. Implementace ICT do výuky č. CZ.1.07/1.1.02/02.0012 GG OP VK
 Fyzikální vzdělávání 1. ročník Učební obor: Kuchař číšník Kadeřník 1 Elektřina a magnetismus - elektrický náboj tělesa, elektrická síla, elektrické pole, kapacita vodiče - elektrický proud v látkách, zákony
Fyzikální vzdělávání 1. ročník Učební obor: Kuchař číšník Kadeřník 1 Elektřina a magnetismus - elektrický náboj tělesa, elektrická síla, elektrické pole, kapacita vodiče - elektrický proud v látkách, zákony
Elektronová mikroskopie SEM, TEM, AFM
 Elektronová mikroskopie SEM, TEM, AFM Historie 1931 E. Ruska a M. Knoll sestrojili první elektronový prozařovací mikroskop 1939 první vyrobený elektronový mikroskop firma Siemens rozlišení 10 nm 1965 první
Elektronová mikroskopie SEM, TEM, AFM Historie 1931 E. Ruska a M. Knoll sestrojili první elektronový prozařovací mikroskop 1939 první vyrobený elektronový mikroskop firma Siemens rozlišení 10 nm 1965 první
Na Zemi tvoří vodík asi 15 % atomů všech prvků. Chemické slučování je děj, při kterém z látek jednodušších vznikají látky složitější.
 Nejjednodušší prvek. Na Zemi tvoří vodík asi 15 % atomů všech prvků. Chemické slučování je děj, při kterém z látek jednodušších vznikají látky složitější. Vodík tvoří dvouatomové molekuly, je lehčí než
Nejjednodušší prvek. Na Zemi tvoří vodík asi 15 % atomů všech prvků. Chemické slučování je děj, při kterém z látek jednodušších vznikají látky složitější. Vodík tvoří dvouatomové molekuly, je lehčí než
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY STUDIE TURBÍNY S VÍŘIVÝM OBĚŽNÝM KOLEM STUDY OF TURBINE WITH SIDE CHANNEL RUNNER
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA STROJNÍHO INŽENÝRSTVÍ ENERGETICKÝ ÚSTAV FACULTY OF MECHANICAL ENGINEERING ENERGY INSTITUTE STUDIE TURBÍNY S VÍŘIVÝM OBĚŽNÝM KOLEM STUDY
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA STROJNÍHO INŽENÝRSTVÍ ENERGETICKÝ ÚSTAV FACULTY OF MECHANICAL ENGINEERING ENERGY INSTITUTE STUDIE TURBÍNY S VÍŘIVÝM OBĚŽNÝM KOLEM STUDY
Uhlík a jeho alotropy
 Uhlík Uhlík a jeho alotropy V přírodě se uhlík nachází zejména v karbonátových usazeninách, naftě, uhlí, a to jako směs grafitu a amorfní formy C. Rozeznáváme dvě základní krystalické formy uhlíku: a)
Uhlík Uhlík a jeho alotropy V přírodě se uhlík nachází zejména v karbonátových usazeninách, naftě, uhlí, a to jako směs grafitu a amorfní formy C. Rozeznáváme dvě základní krystalické formy uhlíku: a)
ELEKTROLÝZA. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 13. 3. 2012. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková ELEKTROLÝZA Datum (období) tvorby: 13. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s elektrolýzou. V rámci
Autor: Mgr. Stanislava Bubíková ELEKTROLÝZA Datum (období) tvorby: 13. 3. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s elektrolýzou. V rámci
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE. Úloha 11: Termická emise elektronů
 FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 15.4.2011 Jméno: Jakub Kákona Pracovní skupina: 4 Ročník a kroužek: Pa 9:30 Spolupracovníci: Jana Navrátilová Hodnocení: Úloha 11: Termická emise elektronů
FYZIKÁLNÍ PRAKTIKUM FJFI ČVUT V PRAZE Datum měření: 15.4.2011 Jméno: Jakub Kákona Pracovní skupina: 4 Ročník a kroužek: Pa 9:30 Spolupracovníci: Jana Navrátilová Hodnocení: Úloha 11: Termická emise elektronů
Zdroje elektrického napětí
 Anotace Učební materiál EU V2 1/F15 je určen k výkladu učiva zdroje elektrického napětí fyzika 8. ročník. UM se váže k výstupu: žák uvede hlavní jednotku elektrického napětí, její násobky a díly Zdroje
Anotace Učební materiál EU V2 1/F15 je určen k výkladu učiva zdroje elektrického napětí fyzika 8. ročník. UM se váže k výstupu: žák uvede hlavní jednotku elektrického napětí, její násobky a díly Zdroje
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
Baterie OPzS. Řešení pro nejvyšší nároky
 Baterie OPzS Řešení pro nejvyšší nároky Baterie OPzS T I radice a novace Tato bateriová řada s pancéřovými kladnými deskami (podle DIN: OPzS) je vyráběna podle unikátního know-how výrobce. Sofistikovaná
Baterie OPzS Řešení pro nejvyšší nároky Baterie OPzS T I radice a novace Tato bateriová řada s pancéřovými kladnými deskami (podle DIN: OPzS) je vyráběna podle unikátního know-how výrobce. Sofistikovaná
9. ročník Galvanický článek
 9. ročník Galvanický článek Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. fotografie v prezentaci
9. ročník Galvanický článek Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. fotografie v prezentaci
VÝZKUM MOŽNOSTÍ ZVÝŠENÍ ŽIVOTNOSTI LOŽISEK CESTOU POVRCHOVÝCH ÚPRAV
 VÝZKUM MOŽNOSTÍ ZVÝŠENÍ ŽIVOTNOSTI LOŽISEK CESTOU POVRCHOVÝCH ÚPRAV RESEARCH INTO POSSIBILITY OF INCREASING SERVICE LIFE OF BEARINGS VIA SURFACE TREATMENT Zdeněk Spotz a Jiří Švejcar a Vratislav Hlaváček
VÝZKUM MOŽNOSTÍ ZVÝŠENÍ ŽIVOTNOSTI LOŽISEK CESTOU POVRCHOVÝCH ÚPRAV RESEARCH INTO POSSIBILITY OF INCREASING SERVICE LIFE OF BEARINGS VIA SURFACE TREATMENT Zdeněk Spotz a Jiří Švejcar a Vratislav Hlaváček
Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály
 Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály Elektrochemie rovnováhy a děje v soustavách nesoucích elektrický náboj Krystal kovu ponořený do destilované vody + +
Elektrochemický potenciál Standardní vodíková elektroda Oxidačně-redukční potenciály Elektrochemie rovnováhy a děje v soustavách nesoucích elektrický náboj Krystal kovu ponořený do destilované vody + +
III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Pracovní list č.3 k prezentaci Křivky chladnutí a ohřevu kovů
 Číslo projektu CZ.1.07/1.5.00/34.0514 Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast Strojírenská technologie, vy_32_inovace_ma_22_06 Autor
Číslo projektu CZ.1.07/1.5.00/34.0514 Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast Strojírenská technologie, vy_32_inovace_ma_22_06 Autor
- zabývá se pozorováním a zkoumáním vnitřní stavby neboli struktury (slohu) kovů a slitin
 2. Metalografie - zabývá se pozorováním a zkoumáním vnitřní stavby neboli struktury (slohu) kovů a slitin Vnitřní stavba kovů a slitin ATOM protony, neutrony v jádře elektrony v obalu atomu ve vrstvách
2. Metalografie - zabývá se pozorováním a zkoumáním vnitřní stavby neboli struktury (slohu) kovů a slitin Vnitřní stavba kovů a slitin ATOM protony, neutrony v jádře elektrony v obalu atomu ve vrstvách
CHARAKTERIZACE MATERIÁLU POMOCÍ DIFRAKČNÍ METODY DEBYEOVA-SCHERREROVA NA ZPĚTNÝ ODRAZ
 CHARAKTERIZACE MATERIÁLU POMOCÍ DIFRAKČNÍ METODY DEBYEOVA-SCHERREROVA NA ZPĚTNÝ ODRAZ Lukáš ZUZÁNEK Katedra strojírenské technologie, Fakulta strojní, TU v Liberci, Studentská 2, 461 17 Liberec 1, CZ,
CHARAKTERIZACE MATERIÁLU POMOCÍ DIFRAKČNÍ METODY DEBYEOVA-SCHERREROVA NA ZPĚTNÝ ODRAZ Lukáš ZUZÁNEK Katedra strojírenské technologie, Fakulta strojní, TU v Liberci, Studentská 2, 461 17 Liberec 1, CZ,
Hodnocení opotřebení a změn tribologických vlastností brzdových kotoučů
 Hodnocení opotřebení a změn tribologických vlastností brzdových kotoučů Vedoucí práce: Doc. Ing. Milan Honner, Ph.D. Konzultant: Doc. Dr. Ing. Antonín Kříž Bc. Roman Voch Obsah 1) Cíle diplomové práce
Hodnocení opotřebení a změn tribologických vlastností brzdových kotoučů Vedoucí práce: Doc. Ing. Milan Honner, Ph.D. Konzultant: Doc. Dr. Ing. Antonín Kříž Bc. Roman Voch Obsah 1) Cíle diplomové práce
ČESKÉ VYSOKÉ UČENÍ TECHNICKÉ FAKULTA ELEKTROTECHNICKÁ. Katedra Elektrotechnologie BAKALÁŘSKÁ PRÁCE
 ČESKÉ VYSOKÉ UČENÍ TECHNICKÉ FAKULTA ELEKTROTECHNICKÁ Katedra Elektrotechnologie BAKALÁŘSKÁ PRÁCE Samovybíjení elektrochemických zdrojů pro teplotní charakteristiky Autor - Radek Strnad Vedoucí práce -
ČESKÉ VYSOKÉ UČENÍ TECHNICKÉ FAKULTA ELEKTROTECHNICKÁ Katedra Elektrotechnologie BAKALÁŘSKÁ PRÁCE Samovybíjení elektrochemických zdrojů pro teplotní charakteristiky Autor - Radek Strnad Vedoucí práce -
ZŠ ÚnO, Bratří Čapků 1332
 Úvodní obrazovka Menu (vlevo nahoře) Návrat na hlavní stránku Obsah Výsledky Poznámky Záložky edunet Konec Chemie 1 (pro 12-16 let) LangMaster Obsah (střední část) výběr tématu - dvojklikem v seznamu témat
Úvodní obrazovka Menu (vlevo nahoře) Návrat na hlavní stránku Obsah Výsledky Poznámky Záložky edunet Konec Chemie 1 (pro 12-16 let) LangMaster Obsah (střední část) výběr tématu - dvojklikem v seznamu témat
Úvod. Povrchové vlastnosti jako jsou koroze, oxidace, tření, únava, abraze jsou často vylepšovány různými technologiemi povrchového inženýrství.
 Laserové kalení Úvod Povrchové vlastnosti jako jsou koroze, oxidace, tření, únava, abraze jsou často vylepšovány různými technologiemi povrchového inženýrství. poslední době se začínají komerčně prosazovat
Laserové kalení Úvod Povrchové vlastnosti jako jsou koroze, oxidace, tření, únava, abraze jsou často vylepšovány různými technologiemi povrchového inženýrství. poslední době se začínají komerčně prosazovat
Základní experiment fyziky plazmatu
 Základní experiment fyziky plazmatu D. Vašíček 1, R. Skoupý 2, J. Šupík 3, M. Kubič 4 1 Gymnázium Velké Meziříčí, david.vasicek@centrum.cz 2 Gymnázium Ostrava-Hrabůvka příspěvková organizace, jansupik@gmail.com
Základní experiment fyziky plazmatu D. Vašíček 1, R. Skoupý 2, J. Šupík 3, M. Kubič 4 1 Gymnázium Velké Meziříčí, david.vasicek@centrum.cz 2 Gymnázium Ostrava-Hrabůvka příspěvková organizace, jansupik@gmail.com
Principy chemických snímačů
 Principy chemických snímačů Název školy: SPŠ Ústí nad Labem, středisko Resslova Autor: Ing. Pavel Votrubec Název: VY_32_INOVACE_05_AUT_99_principy_chemickych_snimacu.pptx Téma: Principy chemických snímačů
Principy chemických snímačů Název školy: SPŠ Ústí nad Labem, středisko Resslova Autor: Ing. Pavel Votrubec Název: VY_32_INOVACE_05_AUT_99_principy_chemickych_snimacu.pptx Téma: Principy chemických snímačů
Osnova: 1. Zdroje stejnosměrného napětí 2. Zatěžovací charakteristika
 K620ZENT Základy elektroniky Přednáška č. 4 Osnova: 1. Zdroje stejnosměrného napětí 2. Zatěžovací charakteristika Výroba elektrická energie z energie mechanické - prostřednictvím točivých elektrických
K620ZENT Základy elektroniky Přednáška č. 4 Osnova: 1. Zdroje stejnosměrného napětí 2. Zatěžovací charakteristika Výroba elektrická energie z energie mechanické - prostřednictvím točivých elektrických
VY_32_INOVACE_6/15_ČLOVĚK A PŘÍRODA. Předmět: Fyzika Ročník: 6. Poznámka: Vodiče a izolanty Vypracoval: Pták
 VY_32_INOVACE_6/15_ČLOVĚK A PŘÍRODA Předmět: Fyzika Ročník: 6. Poznámka: Vodiče a izolanty Vypracoval: Pták Izolant je látka, která nevede elektrický proud izolant neobsahuje volné částice s elektrický
VY_32_INOVACE_6/15_ČLOVĚK A PŘÍRODA Předmět: Fyzika Ročník: 6. Poznámka: Vodiče a izolanty Vypracoval: Pták Izolant je látka, která nevede elektrický proud izolant neobsahuje volné částice s elektrický
1 Výkonová akumulace. Průběhy elektrických veličin pro denní diagram jsou na následujícím obrázku.
 1 Výkonová Cílem této varianty je eliminovat náhlé změny dodávaného výkonu např. při přechodu oblačnosti přes FVE. Poměr výkonu a kapacity baterie je větší nebo roven 1, jedná se tedy o výkonový typ. Průběhy
1 Výkonová Cílem této varianty je eliminovat náhlé změny dodávaného výkonu např. při přechodu oblačnosti přes FVE. Poměr výkonu a kapacity baterie je větší nebo roven 1, jedná se tedy o výkonový typ. Průběhy
Elektronová Mikroskopie SEM
 Elektronová Mikroskopie SEM 26. listopadu 2012 Historie elektronové mikroskopie První TEM Ernst Ruska (1931) Nobelova cena za fyziku 1986 Historie elektronové mikroskopie První SEM Manfred von Ardenne
Elektronová Mikroskopie SEM 26. listopadu 2012 Historie elektronové mikroskopie První TEM Ernst Ruska (1931) Nobelova cena za fyziku 1986 Historie elektronové mikroskopie První SEM Manfred von Ardenne
Metody využívající rentgenové záření. Rentgenovo záření. Vznik rentgenova záření. Metody využívající RTG záření
 Metody využívající rentgenové záření Rentgenovo záření Rentgenografie, RTG prášková difrakce 1 2 Rentgenovo záření Vznik rentgenova záření X-Ray Elektromagnetické záření Ionizující záření 10 nm 1 pm Využívá
Metody využívající rentgenové záření Rentgenovo záření Rentgenografie, RTG prášková difrakce 1 2 Rentgenovo záření Vznik rentgenova záření X-Ray Elektromagnetické záření Ionizující záření 10 nm 1 pm Využívá
ZDROJE ELEKTRICKÉ ENERGIE MOTOROVÝCH VOZIDEL
 ZDROJE ELEKTRICKÉ ENERGIE MOTOROVÝCH VOZIDEL Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je Ing. Zdeněk Vala. Dostupné z Metodického portálu www.rvp.cz; ISSN 1802-4785, financovaného z
ZDROJE ELEKTRICKÉ ENERGIE MOTOROVÝCH VOZIDEL Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je Ing. Zdeněk Vala. Dostupné z Metodického portálu www.rvp.cz; ISSN 1802-4785, financovaného z
A:Měření odporových teploměrů v ultratermostatu B:Měření teploty totálním pyrometrem KET/MNV (8. cvičení)
 A:Měření odporových teploměrů v ultratermostatu B:Měření teploty totálním pyrometrem KET/MNV (8. cvičení) Vypracoval : Martin Dlouhý Osobní číslo : A8B268P A:Měření odporových teploměrů v ultratermostatu
A:Měření odporových teploměrů v ultratermostatu B:Měření teploty totálním pyrometrem KET/MNV (8. cvičení) Vypracoval : Martin Dlouhý Osobní číslo : A8B268P A:Měření odporových teploměrů v ultratermostatu
Opakování: shrnutí základních poznatků o struktuře atomu
 11. Polovodiče Polovodiče jsou krystalické nebo amorfní látky, jejichž elektrická vodivost leží mezi elektrickou vodivostí kovů a izolantů a závisí na teplotě nebo dopadajícím optickém záření. Elektrické
11. Polovodiče Polovodiče jsou krystalické nebo amorfní látky, jejichž elektrická vodivost leží mezi elektrickou vodivostí kovů a izolantů a závisí na teplotě nebo dopadajícím optickém záření. Elektrické
Datum: 21. 8. 2013 Projekt: Využití ICT techniky především v uměleckém vzdělávání Registrační číslo: CZ.1.07./1.5.00/34.
 Datum: 21. 8. 2013 Projekt: Využití ICT techniky především v uměleckém vzdělávání Registrační číslo: CZ.1.07./1.5.00/34.1013 Číslo DUM: VY_32_INOVACE_93 Škola: Akademie VOŠ, Gymn. a SOŠUP Světlá nad Sázavou
Datum: 21. 8. 2013 Projekt: Využití ICT techniky především v uměleckém vzdělávání Registrační číslo: CZ.1.07./1.5.00/34.1013 Číslo DUM: VY_32_INOVACE_93 Škola: Akademie VOŠ, Gymn. a SOŠUP Světlá nad Sázavou
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION ÚSTAV ELEKTROTECHNOLOGIE DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION ÚSTAV ELEKTROTECHNOLOGIE DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ BRNO UNIVERSITY OF TECHNOLOGY FAKULTA ELEKTROTECHNIKY A KOMUNIKAČNÍCH TECHNOLOGIÍ ÚSTAV ELEKTROTECHNOLOGIE FACULTY OF ELECTRICAL ENGINEERING AND COMMUNICATION DEPARTMENT OF
Nauka o materiálu. Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny
 Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie 2. ročník a sexta 2 hodiny týdně Školní tabule, interaktivní tabule, tyčinkové a kalotové modely molekul, zpětný
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie 2. ročník a sexta 2 hodiny týdně Školní tabule, interaktivní tabule, tyčinkové a kalotové modely molekul, zpětný
Metody využívající rentgenové záření. Rentgenografie, RTG prášková difrakce
 Metody využívající rentgenové záření Rentgenografie, RTG prášková difrakce 1 Rentgenovo záření 2 Rentgenovo záření X-Ray Elektromagnetické záření Ionizující záření 10 nm 1 pm Využívá se v lékařství a krystalografii.
Metody využívající rentgenové záření Rentgenografie, RTG prášková difrakce 1 Rentgenovo záření 2 Rentgenovo záření X-Ray Elektromagnetické záření Ionizující záření 10 nm 1 pm Využívá se v lékařství a krystalografii.
STEJNOSMĚRNÝ PROUD Elektrický odpor TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY.
 STEJNOSMĚNÝ POUD Elektrický odpor TENTO POJEKT JE SPOLUFINANCOVÁN EVOPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM OZPOČTEM ČESKÉ EPUBLIKY. Elektrický odpor Mějme uzavřený proudový obvod skládající se ze zdroje a delšího
STEJNOSMĚNÝ POUD Elektrický odpor TENTO POJEKT JE SPOLUFINANCOVÁN EVOPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM OZPOČTEM ČESKÉ EPUBLIKY. Elektrický odpor Mějme uzavřený proudový obvod skládající se ze zdroje a delšího
Nové pohledy na aprotické polymerní elektrolyty. J. Vondrák, Ústav anorganické chemie AV ČR, Řež
 Nové pohledy na aprotické polymerní elektrolyty J. Vondrák, Ústav anorganické chemie AV ČR, Řež M. Sedlaříková, O. Krejza, P. Barath Ústav elektrotechnologie FEKT VUT Brno J.Kliment, Solartec, Rožnov p.
Nové pohledy na aprotické polymerní elektrolyty J. Vondrák, Ústav anorganické chemie AV ČR, Řež M. Sedlaříková, O. Krejza, P. Barath Ústav elektrotechnologie FEKT VUT Brno J.Kliment, Solartec, Rožnov p.
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
4. Stanovení teplotního součinitele odporu kovů
 4. Stanovení teplotního součinitele odporu kovů 4.. Zadání úlohy. Změřte teplotní součinitel odporu mědi v rozmezí 20 80 C. 2. Změřte teplotní součinitel odporu platiny v rozmezí 20 80 C. 3. Vyneste graf
4. Stanovení teplotního součinitele odporu kovů 4.. Zadání úlohy. Změřte teplotní součinitel odporu mědi v rozmezí 20 80 C. 2. Změřte teplotní součinitel odporu platiny v rozmezí 20 80 C. 3. Vyneste graf
4.4.3 Galvanické články
 ..3 Galvanické články Předpoklady: 01 Zapíchnu do citrónu dva plíšky z různých kovů mezi kovy se objeví napětí (měřitelné voltmetrem) získal jsem baterku, ale žárovku nerozsvítím (citrobaterie dává pouze
..3 Galvanické články Předpoklady: 01 Zapíchnu do citrónu dva plíšky z různých kovů mezi kovy se objeví napětí (měřitelné voltmetrem) získal jsem baterku, ale žárovku nerozsvítím (citrobaterie dává pouze
TEPELNÉ ÚČINKY EL. PROUDU
 Univerzita Pardubice Fakulta elektrotechniky a informatiky Materiály pro elektrotechniku Laboratorní cvičení č. 1 TEPELNÉ ÚČINKY EL. POUDU Jméno(a): Mikulka oman, Havlíček Jiří Stanoviště: 6 Datum: 19.
Univerzita Pardubice Fakulta elektrotechniky a informatiky Materiály pro elektrotechniku Laboratorní cvičení č. 1 TEPELNÉ ÚČINKY EL. POUDU Jméno(a): Mikulka oman, Havlíček Jiří Stanoviště: 6 Datum: 19.
Lukáš Feřt SPŠ dopravní, Plzeň, Karlovarská 99, 326 00
 Lukáš Feřt SPŠ dopravní, Plzeň, Karlovarská 99, 326 00 V rámci projektu: Inovace odborného vzdělávání na středních školách zaměřené na využívání energetických zdrojů pro 21. století El. proud I je určen
Lukáš Feřt SPŠ dopravní, Plzeň, Karlovarská 99, 326 00 V rámci projektu: Inovace odborného vzdělávání na středních školách zaměřené na využívání energetických zdrojů pro 21. století El. proud I je určen
25 A Vypracoval : Zdeněk Žák Pyrometrie υ = -40 C.. +10000 C. Výhody termovize Senzory infračerveného záření Rozdělení tepelné senzory
 25 A Vypracoval : Zdeněk Žák Pyrometrie Bezdotykové měření Pyrometrie (obrázky viz. sešit) Bezdotykové měření teplot je měření povrchové teploty těles na základě elektromagnetického záření mezi tělesem
25 A Vypracoval : Zdeněk Žák Pyrometrie Bezdotykové měření Pyrometrie (obrázky viz. sešit) Bezdotykové měření teplot je měření povrchové teploty těles na základě elektromagnetického záření mezi tělesem
Metodika hodnocení strukturních změn v ocelích při tepelném zpracování
 Metodika hodnocení strukturních změn v ocelích při tepelném zpracování Bc. Pavel Bílek Ing. Jana Sobotová, Ph.D Abstrakt Předložená práce se zabývá volbou metodiky hodnocení strukturních změn ve vysokolegovaných
Metodika hodnocení strukturních změn v ocelích při tepelném zpracování Bc. Pavel Bílek Ing. Jana Sobotová, Ph.D Abstrakt Předložená práce se zabývá volbou metodiky hodnocení strukturních změn ve vysokolegovaných
Některé poznatky z charakterizace nano železa. Marek Šváb Tereza Nováková Martina Müllerová Jan Šubrt Karel Závěta Eva Gregorová
 Některé poznatky z charakterizace nano železa Marek Šváb Tereza Nováková Martina Müllerová Jan Šubrt Karel Závěta Eva Gregorová Nanotechnologie 60. a 70. léta 20. st.: období miniaturizace 90. léta 20.
Některé poznatky z charakterizace nano železa Marek Šváb Tereza Nováková Martina Müllerová Jan Šubrt Karel Závěta Eva Gregorová Nanotechnologie 60. a 70. léta 20. st.: období miniaturizace 90. léta 20.
Fakulta elektrotechniky a komunikačních technologíı Ústav automatizace a měřicí techniky v Brně
 Vysoké učení technické v Brně Fakulta elektrotechniky a komunikačních technologíı Ústav automatizace a měřicí techniky Algoritmy řízení topného článku tepelného hmotnostního průtokoměru Autor práce: Vedoucí
Vysoké učení technické v Brně Fakulta elektrotechniky a komunikačních technologíı Ústav automatizace a měřicí techniky Algoritmy řízení topného článku tepelného hmotnostního průtokoměru Autor práce: Vedoucí
ELECTROCHEMICAL HYDRIDING OF MAGNESIUM-BASED ALLOYS
 ELEKTROCHEMICKÉ SYCENÍ HOŘČÍKOVÝCH SLITIN VODÍKEM ELECTROCHEMICAL HYDRIDING OF MAGNESIUM-BASED ALLOYS Dalibor Vojtěch a, Alena Michalcová a, Magda Morťaniková a, Borivoj Šustaršič b a Ústav kovových materiálů
ELEKTROCHEMICKÉ SYCENÍ HOŘČÍKOVÝCH SLITIN VODÍKEM ELECTROCHEMICAL HYDRIDING OF MAGNESIUM-BASED ALLOYS Dalibor Vojtěch a, Alena Michalcová a, Magda Morťaniková a, Borivoj Šustaršič b a Ústav kovových materiálů
Struktura elektronového obalu
 Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Struktura elektronového obalu Představy o modelu atomu se vyvíjely tak, jak se zdokonalovaly možnosti vědy
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Struktura elektronového obalu Představy o modelu atomu se vyvíjely tak, jak se zdokonalovaly možnosti vědy
High Energy 3D Accumulator Vysokokapacitní 3D Akumulátor
 High Energy 3D Accumulator Vysokokapacitní 3D Akumulátor OBSAH PREZENTACE PŘEDSTAVENÍ SPOLEČNOSTI KONSTRUKCE 3D LITHIOVÉHO AKUMULÁTORU KONKUREČNÍ VÝHODY 3D ELEKTROD PROTI STÁVAJÍCÍ TECHNOLOGII VLASTNOSTI
High Energy 3D Accumulator Vysokokapacitní 3D Akumulátor OBSAH PREZENTACE PŘEDSTAVENÍ SPOLEČNOSTI KONSTRUKCE 3D LITHIOVÉHO AKUMULÁTORU KONKUREČNÍ VÝHODY 3D ELEKTROD PROTI STÁVAJÍCÍ TECHNOLOGII VLASTNOSTI
DIFRAKCE ELEKTRONŮ V KRYSTALECH, ZOBRAZENÍ ATOMŮ
 DIFRAKCE ELEKTRONŮ V KRYSTALECH, ZOBRAZENÍ ATOMŮ T. Jeřábková Gymnázium, Brno, Vídeňská 47 ter.jer@seznam.cz V. Košař Gymnázium, Brno, Vídeňská 47 vlastik9a@atlas.cz G. Malenová Gymnázium Třebíč malena.vy@quick.cz
DIFRAKCE ELEKTRONŮ V KRYSTALECH, ZOBRAZENÍ ATOMŮ T. Jeřábková Gymnázium, Brno, Vídeňská 47 ter.jer@seznam.cz V. Košař Gymnázium, Brno, Vídeňská 47 vlastik9a@atlas.cz G. Malenová Gymnázium Třebíč malena.vy@quick.cz
1 Teoretický úvod. 1.2 Braggova rovnice. 1.3 Laueho experiment
 RTG fázová analýza Michael Pokorný, pok@rny.cz, Střední škola aplikované kybernetiky s.r.o. Tomáš Jirman, jirman.tomas@seznam.cz, Gymnázium, Nad Alejí 1952, Praha 6 Abstrakt Rengenová fázová analýza se
RTG fázová analýza Michael Pokorný, pok@rny.cz, Střední škola aplikované kybernetiky s.r.o. Tomáš Jirman, jirman.tomas@seznam.cz, Gymnázium, Nad Alejí 1952, Praha 6 Abstrakt Rengenová fázová analýza se
U = E a - E k + IR Znamená to, že vložené napětí je vyrovnáváno
 Voltametrie a polarografie Princip. Do roztoku vzorku (elektrolytu) jsou ponořeny dvě elektrody (na rozdíl od potenciometrie prochází obvodem el. proud) - je vytvořen elektrochemický článek. Na elektrody
Voltametrie a polarografie Princip. Do roztoku vzorku (elektrolytu) jsou ponořeny dvě elektrody (na rozdíl od potenciometrie prochází obvodem el. proud) - je vytvořen elektrochemický článek. Na elektrody
ELEKTROCHEMIE A KOROZE Ing. Jiří Vondrák, DrSc. ÚACH AV ČR
 ELEKTROCHEMIE A KOROZE Ing. Jiří Vondrák, DrSc. ÚACH AV ČR Elektrochemie: chemické reakce vyvolané elektrickým proudem a naopak vznik elektrického proudu z chemických reakcí Historie: L. Galvani - žabí
ELEKTROCHEMIE A KOROZE Ing. Jiří Vondrák, DrSc. ÚACH AV ČR Elektrochemie: chemické reakce vyvolané elektrickým proudem a naopak vznik elektrického proudu z chemických reakcí Historie: L. Galvani - žabí
Uhlíkové struktury vázající ionty těžkých kovů
 Uhlíkové struktury vázající ionty těžkých kovů 7. června/june 2013 9:30 h 17:30 h Laboratoř metalomiky a nanotechnologií, Mendelova univerzita v Brně a Středoevropský technologický institut Budova D, Zemědělská
Uhlíkové struktury vázající ionty těžkých kovů 7. června/june 2013 9:30 h 17:30 h Laboratoř metalomiky a nanotechnologií, Mendelova univerzita v Brně a Středoevropský technologický institut Budova D, Zemědělská
J. Kubíček FSI Brno 2018
 J. Kubíček FSI Brno 2018 Fosfátování je povrchová úprava, kdy se na povrch povlakovaného kovu vylučují nerozpustné fosforečnany. Povlak vzniká reakcí iontů z pracovní lázně s ionty rozpuštěnými z povrchu
J. Kubíček FSI Brno 2018 Fosfátování je povrchová úprava, kdy se na povrch povlakovaného kovu vylučují nerozpustné fosforečnany. Povlak vzniká reakcí iontů z pracovní lázně s ionty rozpuštěnými z povrchu
Gel. AGM baterie. baterie % baterie %
 ové a AGM www.victronenergy.com 1. VRLA technologie VRLA je zkratkou pro Valve Regulated Lead Acid, což znamená, že jsou uzavřené. Plyn uniká přes bezpečnostní ventily pouze v případě selhání článku nebo
ové a AGM www.victronenergy.com 1. VRLA technologie VRLA je zkratkou pro Valve Regulated Lead Acid, což znamená, že jsou uzavřené. Plyn uniká přes bezpečnostní ventily pouze v případě selhání článku nebo
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Inovace profesní přípravy budoucích učitelů chemie
 Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Inovace profesní přípravy budoucích učitelů chemie I n v e s t i c e d o r o z v o j e v z d ě l á v á n í CZ.1.07/2.2.00/15.0324 Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem
Carbovet - mechanismus vyvazování mykotoxinů neschopných adsorpce
 Dos 1654 July 25 nd, 2011 Carbovet - mechanismus vyvazování mykotoxinů neschopných adsorpce Catherine Ionescu Pancosma R&D, Carbovet expert 1 Představení Většina zákazníků požaduje vysvětlení jaký je mechanismus
Dos 1654 July 25 nd, 2011 Carbovet - mechanismus vyvazování mykotoxinů neschopných adsorpce Catherine Ionescu Pancosma R&D, Carbovet expert 1 Představení Většina zákazníků požaduje vysvětlení jaký je mechanismus
