B. PŘÍBALOVÁ INFORMACE
|
|
|
- Květa Marešová
- před 8 lety
- Počet zobrazení:
Transkript
1 B. PŘÍBALOVÁ INFORMACE 1
2 Příbalová informace: informace pro uživatele Repatha 140 mg injekční roztok v předplněné injekční stříkačce evolocumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Jak hlásit nežádoucí účinky je popsáno v závěru bodu 4. Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje. Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry. Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy. Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4. Co naleznete v této příbalové informaci 1. Co je přípravek Repatha a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete přípravek Repatha používat 3. Jak se přípravek Repatha používá 4. Možné nežádoucí účinky 5. Jak přípravek Repatha uchovávat 6. Obsah balení a další informace 1. Co je přípravek Repatha a k čemu se používá Co je přípravek Repatha a jak účinkuje Přípravek Repatha je lék, který snižuje hladinu "špatného" cholesterolu, druhu tuku, v krvi. Přípravek Repatha obsahuje léčivou látku evolokumab, lidskou monoklonální protilátku (typ speciálního proteinu vyvinutého tak, aby se navázal na cílové látky v těle). Evolokumab je navržen tak, aby se navázal na látku nazývanou PCSK9, která ovlivňuje schopnost jater přijmout cholesterol. Navázáním se a vyčištěním PCSK9 zvyšuje lék množství cholesterolu vstupujícího do jater, a tak snižuje hladinu cholesterolu v krvi. Přípravek Repatha se používá u pacientů, u kterých nemůže být kontrolováno snížení hladin cholesterolu pouze dietou. Po dobu užívání léku byste měli nadále dodržovat dietu na snížení cholesterolu. K čemu se přípravek Repatha používá Přípravek Repatha se používá spolu s dietou na snížení cholesterolu, pokud jste: dospělá osoba s vysokou hladinou cholesterolu v krvi (primární hypercholesterolemie [heterozygotní familiární a nefamiliární] nebo smíšená dyslipidemie). Podává se: spolu se statinem nebo jiným lékem na snížení cholesterolu v případě, že maximální dávka statinu nesnižuje dostatečně hladiny cholesterolu. samostatně nebo spolu s jinými léky na snížení cholesterolu v případech, kdy statiny neúčinkují dostatečně nebo je nelze používat. 2
3 ve věku 12 let a starší s vysokou hladinou cholesterolu v krvi z důvodu onemocnění ve Vaší rodině (homozygotní familiární hypercholesterolemie, neboli HoFH). Podává se: spolu s další léčbou na snížení cholesterolu. 2. Čemu musíte věnovat pozornost, než začnete přípravek Repatha používat Nepoužívejte přípravek Repatha, jestliže jste alergický(á) na evolokumab nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6). Upozornění a opatření Před použitím přípravku Repatha informujte svého lékaře, lékárníka nebo zdravotní sestru, pokud máte: onemocnění jater závažné potíže s ledvinami. Kryt jehly skleněné předplněné injekční stříkačky je vyroben ze suchého přírodního kaučuku (derivát latexu), který může způsobovat alergické reakce. Děti a dospívající Používání přípravku Repatha nebylo studováno u dětí mladších 18 let léčených pro primární hypercholesterolemii a smíšenou dyslipidemii. Používání přípravku Repatha nebylo studováno u dětí mladších 12 let léčených pro homozygotní familiární hypercholesterolemii. Další léčivé přípravky a Repatha Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Těhotenství, kojení a plodnost Přípravek Repatha nebyl zkoušen u těhotných žen. Není známo, zda přípravek Repatha poškodí Vaše dosud nenarozené dítě. Informujte svého lékaře, pokud se pokoušíte během užívání přípravku Repatha otěhotnět, domníváte se, že můžete být těhotná nebo otěhotníte. Není známo, zda se přípravek Repatha vylučuje do mateřského mléka. Je důležité, abyste svého lékaře informovala, pokud kojíte nebo se chystáte kojit. Váš lékař Vám pomůže se rozhodnout, zda přestat kojit nebo zda ukončit léčbu přípravkem Repatha. Je třeba zvážit prospěšnost kojení pro dítě a prospěšnost léčby přípravkem Repatha pro matku. Řízení dopravních prostředků a obsluha strojů Repatha nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje. Repatha obsahuje sodík Tento léčivý přípravek obsahuje méně než 1 mmol (23 mg) sodíku v jedné dávce, tj. je v podstatě bez sodíku a neměl by tedy mít vliv na dietu s kontrolovaným obsahem sodíku. 3
4 3. Jak se přípravek Repatha používá Vždy používejte tento přípravek přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem. Přípravek Repatha se podává jako injekce pod kůži (subkutánně). Doporučená dávka závisí na typu onemocnění: u primární hypercholesterolemie a smíšené dyslipidemie je dávka buď 140 mg každé dva týdny nebo 420 mg 1x měsíčně. u homozygotní familiární hypercholesterolemie je doporučená úvodní dávka 420 mg 1x měsíčně. Po 12 týdnech se Váš lékař může rozhodnout zvýšit tuto dávku na 420 mg každé dva týdny. Jestliže jste léčen(a) rovněž aferézou, procedurou podobnou dialýze, při které jsou cholesterol a další tuky odstraňovány z krve, může se Váš lékař rozhodnout zahájit léčbu dávkou 420 mg každé dva týdny, aby byla ve shodě s léčbou aferézou. Pokud lékař předepíše dávku 420 mg, musíte použít tři předplněné injekční stříkačky, protože každá předplněná injekční stříkačka obsahuje pouze 140 mg léku. Po dosažení pokojové teploty mají být všechny injekce podány do 30 minut. Jestliže Váš lékař rozhodne, že si injekce přípravku Repatha můžete aplikovat sami nebo je může aplikovat osoba, která o Vás pečuje, budete Vy nebo Váš pečovatel proškoleni jak správně připravit a podat injekce přípravku Repatha. Nezkoušejte podávat injekce přípravku Repatha, dokud Vám lékař nebo zdravotní sestra neukáží, jak ho podávat. Přečtěte si, prosím, podrobné pokyny na konci této příbalové informace, abyste věděli, jak doma uchovávat, připravovat a podávat přípravek Repatha. Před zahájením léčby přípravkem Repatha byste měli být na dietě snižující cholesterol. Po dobu používání přípravku Repatha byste měli dodržovat dietu snižující cholesterol. Pokud Vám lékař předepsal přípravek Repatha spolu s jiným lékem na snížení cholesterolu, dodržujte pokyny lékaře, jak užívat tyto léky dohromady. V takovém případě si, prosím, rovněž přečtěte pokyny o dávkování uvedené v příbalové informaci příslušného léku. Jestliže jste použil(a) více přípravku Repatha než jste měl(a) Obraťte se ihned na svého lékaře nebo lékárníka. Jestliže jste zapomněl(a) použít přípravek Repatha Vezměte si přípravek Repatha co nejdříve po vynechané dávce. Poté se obraťte na svého lékaře, který Vám řekne, na kdy si máte naplánovat příští dávku a dodržujte tento nový harmonogram přesně podle lékaře. 4. Možné nežádoucí účinky Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Časté nežádoucí účinky: mohou se vyskytnout u 1 z 10 léčených osob chřipka (vysoká teplota, bolesti v krku, rýma, kašel a zimnice) nachlazení projevující se jako rýma, bolesti v krku nebo infekce vedlejších dutin (zánět nosohltanu nebo infekce horních cest dýchacích) nevolnost (pocit na zvracení) bolesti zad 4
5 bolesti kloubů (artralgie) reakce v místě injekčního vpichu, zarudnutí, modřina nebo bolest vyrážka Méně časté nežádoucí účinky: mohou se vyskytnout u 1 ze 100 léčených osob kopřivka, zarudlé svědivé bouličky na pokožce (urtikárie) Hlášení nežádoucích účinků Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo (viz pokyny níže). Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku. Státní ústav pro kontrolu léčiv Šrobárova Praha 10 Webové stránky: 5. Jak přípravek Repatha uchovávat Uchovávejte tento přípravek mimo dohled a dosah dětí. Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na štítku a krabičce za EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Uchovávejte v chladničce (2 C 8 C). Chraňte před mrazem. Uchovávejte v původním vnějším obalu, aby byl přípravek chráněn před světlem. Předplněnou injekční stříkačku můžete po vyjmutí z chladničky nechat před podáním ohřát na pokojovou teplotu (do 25 C). Tímto opatřením bude injekce příjemnější. Po vyjmutí z chladničky může být přípravek Repatha uchováván při pokojové teplotě (do 25 C) v původním obalu a musí se použít do 1 týdne. Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí. 6. Obsah balení a další informace Co přípravek Repatha obsahuje Léčivou látkou je evolocumabum. Jedna předplněná injekční stříkačka obsahuje evolocumabum 140 mg v 1 ml roztoku. Pomocnými látkami jsou prolin, kyselina octová 98%, polysorbát 80, hydroxid sodný a voda na injekci. Jak přípravek Repatha vypadá a co obsahuje toto balení Repatha je čirý až opalescentní, bezbarvý až nažloutlý roztok, který neobsahuje prakticky žádné částice. Nepoužívejte tento lék, pokud zpozorujete změnu barvy nebo pokud lék obsahuje velké kousky, šupinky nebo barevné částice. Balení obsahuje jednu jednorázovou předplněnou injekční stříkačku. 5
6 Držitel rozhodnutí o registraci a výrobce: Amgen Europe B.V. Minervum ZK Breda Nizozemsko Držitel rozhodnutí o registraci: Amgen Europe B.V. Minervum ZK Breda Nizozemsko Výrobce: Amgen Technology Ireland Pottery Road Dun Laoghaire Co Dublin Irsko Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci. Amgen s.r.o. Tel: Tato příbalová informace byla naposledy revidována: červenec Další zdroje informací Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky 6
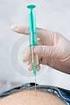
7 Návod k použití: Repatha předplněná injekční stříkačka na jedno použití Popis jednotlivých částí Táhlo pístu Před použitím Použitý píst Po použití Použité tělo stříkačky Lék Tělo stříkačky Použitá jehla Nasazený šedý kryt jehly Sejmutý šedý kryt jehly Jehla je uvnitř 7
8 Důležité Před použitím Repatha předplněné injekční stříkačky na jedno použití si přečtěte tyto důležité informace: Zdravotnický pracovník Vám řekne, kolik Repatha předplněných stříkaček potřebujete na Vaši dávku. Pokud použijete více než jednu Repatha předplněnou injekční stříkačku, mají být po dosažení pokojové teploty všechny injekce podány do 30 minut. Uchovávejte Repatha předplněnou injekční stříkačku v původním obalu, aby byla chráněna před světlem. Uchovávejte Repatha předplněnou injekční stříkačku v chladničce (2 C až 8 C). Je důležité, abyste se nepokoušel(a) podat si sám(sama) injekci, dokud Vás neproškolí váš lékař nebo zdravotnický pracovník. Šedý kryt jehly na Repatha předplněné injekční stříkačce se skládá ze suchého přírodního kaučuku, který je vyroben z latexu. Pokud jste na latex alergický(á), řekněte to svému zdravotnickému pracovníkovi. Uchovávejte Repatha předplněnou injekční stříkačku mimo dohled a dosah dětí. POZOR: Nepoužívejte Repatha předplněnou injekční stříkačku, pokud je balení otevřené nebo poškozené. Nezmrazujte Repatha předplněnou injekční stříkačku nebo nepoužívejte stříkačku, která byla zmrazena. Nepoužívejte Repatha předplněnou injekční stříkačku, pokud Vám spadla na tvrdý povrch. Část stříkačky může být poškozena, i když to není vidět. Použijte novou Repatha předplněnou injekční stříkačku. Nesnímejte z Repatha předplněné injekční stříkačky šedý kryt jehly, dokud nejste připraveni si injekci podat. A Krok 1: Příprava Vyndejte krabičku s Repatha předplněnou injekční stříkačkou z chladničky a počkejte 30 minut. Počkejte alespoň 30 minut, aby se předplněná injekční stříkačka přirozeně ohřála před injekcí na pokojovou teplotu. Zkontrolujte, že krabička je označena názvem Repatha. POZOR: Nepokoušejte se ohřívat Repatha předplněnou injekční stříkačku pomocí zdrojů tepla jako je horká voda nebo mikrovlná trouba. Nevystavujte Repatha předplněnou injekční stříkačku přímému slunečnímu světlu. Netřepejte Repatha předplněnou injekční stříkačkou. 8
9 B Připravte si vše, co potřebujete pro injekci. Důkladně si umyjte ruce vodou a mýdlem. Na čisté, dobře osvětlené a rovné místo si dejte: Jednu Repatha předplněnou injekční stříkačku ve vaničce. Tampóny navlhčené alkoholem. Smotek vaty nebo gázové polštářky. Náplast. Nádobu na ostrý odpad. NEPOUŽÍVEJTE Repatha předplněnou injekční stříkačku, pokud uplynula doba použitelnosti uvedená na krabičce. C Vyberte si místo pro injekci. Horní část paže Břicho Stehno Můžete použít: Stehno. Břicho kromě oblasti 5 cm (2 palce) okolo pupku. Vnější stranu horní části paže (pouze pokud Vám injekci podává někdo jiný). NEVYBÍREJTE si oblast, kde je kůže citlivá, pohmožděná, červená nebo tvrdá. Nepodávejte injekci do oblastí s jizvami nebo strijemi. Pokaždé si k aplikaci injekce, kterou si podáváte, vyberte jiné místo. Pokud potřebujete použít stejné místo, ujistěte se, že to není stejný bod v místě, které jste použili minule. D Očistěte místo pro injekci. Místo pro injekci očistěte tampónem navlhčeným alkoholem. Před injekcí nechte kůži uschnout. Před aplikací se místa injekce znovu NEDOTÝKEJTE. 9
10 E Předplněnou injekční stříkačku vyjměte z vaničky. Vaničku obraťte Lehce zatlačte Pro vyjmutí: Odtrhněte papír z vaničky. Vaničku si položte na dlaň. Vaničku obraťte a jemně zatlačte zezadu na střed vaničky, abyste stříkačku vyndali na dlaň. Pokud se předplněná injekční stříkačka z vaničky neuvolní, jemně zatlačte zezadu na vaničku. POZOR: Neberte nebo nevytahujte předplněnou injekční stříkačku za táhlo pístu nebo šedý kryt jehly. To by ji mohlo poškodit. Nesnímejte z předplněné injekční stříkačky šedý kryt jehly, dokud nejste připraveni si injekci podat. Vždy držte předplněnou injekční stříkačku za tělo stříkačky. F Zkontrolujte lék a stříkačku. Táhlo pístu Tělo stříkačky Štítek stříkačky s dobou použitelnosti Nasazený šedý kryt jehly Lék Vždy držte předplněnou injekční stříkačku za tělo stříkačky. Zkontrolujte že: Na štítku předplněné injekční stříkačky je název Repatha. Lék v předplněné injekční stříkačce je čirý a bezbarvý až lehce nažloutlý. Předplněnou injekční stříkačku NEPOUŽÍVEJTE, pokud: se některá její část zdá být prasklá nebo rozbitá. chybí šedý kryt jehly nebo není bezpečně nasazen. je lék zbarvený nebo obsahuje velké shluky, vločky nebo barevné částice. uplynula doba použitelnosti na předplněné injekční stříkačce. 10
11 Krok 2: Připravte se A Stáhněte opatrně šedý kryt jehly rovně směrem od těla Je běžné, když se na konci jehly objeví kapka léku. POZOR: Kryt ihned dejte do nádoby na ostrý odpad Šedým krytem jehly nekruťte ani ho neohýbejte. Mohla by se tím poškodit jehla. Šedý kryt jehly nenasazujte zpět na předplněnou injekční stříkačku. B Odstraňte vzduchové bubliny / mezery. V Repatha předplněné injekční stříkačce si můžete všimnout vzduchových bublin/mezer. Pokud vzduchové bubliny/mezery zaznamenáte: Držte předplněnou injekční stříkačku jehlou nahoru. Jemně poklepávejte prsty na tělo stříkačky, dokud se vzduchové bubliny/mezery nedostanou ve stříkačce nahoru. Pomalu a jemně vytlačte pístem vzduch z předplněné injekční stříkačky. Buďte velmi opatrní, abyste nevytlačili ven žádný lék. NEKLEPEJTE na jehlu stříkačky. C STISKNĚTE místo injekce a vytvořte pevný povrch. Stiskněte pokožku pevně mezi palec a ostatní prsty, abyste vytvořili oblast širokou asi 5 cm (2 palce). Při aplikaci injekce je důležité držet kůži stisknutou. 11
12 A Krok 3: Podání injekce Udržujte STISK. Vpíchněte jehlu do kůže pod úhlem 45 až 90 stupňů. Při zavádění jehly NEDÁVEJTE prsty na píst. B STLAČUJTE píst pomalu a rovnoměrně až dolů, dokud není stříkačka prázdná. C Po dokončení UVOLNĚTE palec a lehce vytáhněte stříkačku z pokožky. Šedý kryt jehly NENASAZUJTE zpět na použitou stříkačku. 12
13 A Krok 4: Dokončení Použitou stříkačku ihned dejte do nádoby na ostrý odpad. Zeptejte se svého zdravotnického pracovníka na správný způsob likvidace. Pro likvidaci mohou platit místní předpisy. NEPOUŽÍVEJTE znovu použitou stříkačku. NEPOUŽÍVEJTE lék, který zbyl v použité stříkačce. NERECYKLUJTE stříkačku nebo nádobu na ostrý odpad, ani je NEVYHAZUJTE do domácího odpadu. Použitou stříkačku a nádobu na ostrý odpad uchovávejte mimo dohled a dosah dětí. B Prohlédněte místo injekce. Pokud se objeví krev, přiložte na místo injekce smotek vaty nebo gázový polštářek. Pokud je třeba, použijte náplast. Místo vpichu NETŘETE. 13
14 Příbalová informace: informace pro uživatele Repatha 140 mg injekční roztok v předplněném peru evolocumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Jak hlásit nežádoucí účinky je popsáno v závěru bodu 4. Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje. Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry. Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy. Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4. Co naleznete v této příbalové informaci 1. Co je přípravek Repatha a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete přípravek Repatha používat 3. Jak se přípravek Repatha používá 4. Možné nežádoucí účinky 5. Jak přípravek Repatha uchovávat 6. Obsah balení a další informace 1. Co je přípravek Repatha a k čemu se používá Co je přípravek Repatha a jak účinkuje Přípravek Repatha je lék, který snižuje hladinu "špatného" cholesterolu, druhu tuku, v krvi. Přípravek Repatha obsahuje léčivou látku evolokumab, lidskou monoklonální protilátku (typ speciálního proteinu vyvinutého tak, aby se navázal na cílové látky v těle). Evolokumab je navržen tak, aby se navázal na látku nazývanou PCSK9, která ovlivňuje schopnost jater přijmout cholesterol. Navázáním se a vyčištěním PCSK9 zvyšuje lék množství cholesterolu vstupujícího do jater, a tak snižuje hladinu cholesterolu v krvi. Přípravek Repatha se používá u pacientů, u kterých nemůže být kontrolováno snížení hladin cholesterolu pouze dietou. Po dobu užívání léku byste měli nadále dodržovat dietu na snížení cholesterolu. K čemu se přípravek Repatha používá Přípravek Repatha se používá spolu s dietou na snížení cholesterolu, pokud jste: dospělá osoba s vysokou hladinou cholesterolu v krvi (primární hypercholesterolemie [heterozygotní familiární a nefamiliární] nebo smíšená dyslipidemie). Podává se: spolu se statinem nebo jiným lékem na snížení cholesterolu v případě, že maximální dávka statinu nesnižuje dostatečně hladiny cholesterolu. samostatně nebo spolu s jinými léky na snížení cholesterolu v případech, kdy statiny neúčinkují dostatečně nebo je nelze používat. 14
15 ve věku 12 let a starší s vysokou hladinou cholesterolu v krvi z důvodu onemocnění ve Vaší rodině (homozygotní familiární hypercholesterolemie, neboli HoFH). Podává se: spolu s další léčbou na snížení cholesterolu. 2. Čemu musíte věnovat pozornost, než začnete přípravek Repatha používat Nepoužívejte přípravek Repatha, jestliže jste alergický(á) na evolokumab nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6). Upozornění a opatření Před užíváním přípravku Repatha informujte svého lékaře, lékárníka nebo zdravotní sestru, pokud máte: onemocnění jater závažné potíže s ledvinami. Kryt jehly skleněného předplněného pera je vyroben ze suchého přírodního kaučuku (derivát latexu), který může způsobovat alergické reakce. Děti a dospívající Používání přípravku Repatha nebylo studováno u dětí mladších 18 let léčených pro primární hypercholesterolemii a smíšenou dyslipidemii. Používání přípravku Repatha nebylo studováno u dětí mladších 12 let léčených pro homozygotní familiární hypercholesterolemii. Další léčivé přípravky a Repatha Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Těhotenství, kojení a plodnost Přípravek Repatha nebyl zkoušen u těhotných žen. Není známo, zda přípravek Repatha poškodí Vaše dosud nenarozené dítě. Informujte svého lékaře, pokud se pokoušíte během užívání přípravku Repatha otěhotnět, domníváte se, že můžete být těhotná nebo otěhotníte. Není známo, zda se přípravek Repatha vylučuje do mateřského mléka. Je důležité, abyste svého lékaře informovala, pokud kojíte nebo se chystáte kojit. Váš lékař Vám pomůže se rozhodnout, zda přestat kojit nebo zda ukončit léčbu přípravkem Repatha. Je třeba zvážit prospěšnost kojení pro dítě a prospěšnost léčby přípravkem Repatha pro matku. Řízení dopravních prostředků a obsluha strojů Repatha nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje. Repatha obsahuje sodík Tento léčivý přípravek obsahuje méně než 1 mmol (23 mg) sodíku v jedné dávce, tj. je v podstatě bez sodíku a neměl by tedy mít vliv na dietu s kontrolovaným obsahem sodíku. 15
16 3. Jak se přípravek Repatha používá Vždy používejte tento přípravek přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem. Přípravek Repatha se podává jako injekce pod kůži (subkutánně). Doporučená dávka závisí na typu onemocnění: u primární hypercholesterolemie a smíšené dyslipidemie je dávka buď 140 mg každé dva týdny nebo 420 mg 1x měsíčně. u homozygotní familiární hypercholesterolemie je doporučená úvodní dávka 420 mg 1x měsíčně. Po 12 týdnech se Váš lékař může rozhodnout zvýšit tuto dávku na 420 mg každé dva týdny. Jestliže jste léčen(a) rovněž aferézou, procedurou podobnou dialýze, při které jsou cholesterol a další tuky odstraňovány z krve, může se Váš lékař rozhodnout zahájit léčbu dávkou 420 mg každé dva týdny, aby byla ve shodě s léčbou aferézou. Pokud lékař předepíše dávku 420 mg, musíte použít tři předplněná pera, protože jedno předplněné pero obsahuje pouze 140 mg léku. Po dosažení pokojové teploty mají být všechny injekce podány do 30 minut. Jestliže Váš lékař rozhodne, že si injekce přípravku Repatha můžete aplikovat sami nebo je může aplikovat osoba, která o Vás pečuje, budete Vy nebo Váš pečovatel proškoleni jak správně připravit a podat injekce přípravku Repatha. Nezkoušejte podávat injekce přípravku Repatha, dokud Vám lékař nebo zdravotní sestra neukáží, jak ho podávat. Přečtěte si, prosím, podrobné pokyny na konci této příbalové informace, abyste věděli, jak doma uchovávat, připravovat a podávat přípravek Repatha. Před zahájením léčby přípravkem Repatha byste měli být na dietě snižující cholesterol. Po dobu používání přípravku Repatha byste měli dodržovat dietu snižující cholesterol. Pokud Vám lékař předepsal přípravek Repatha spolu s jiným lékem na snížení cholesterolu, dodržujte pokyny lékaře, jak užívat tyto léky dohromady. V takovém případě si, prosím, rovněž přečtěte pokyny o dávkování uvedené v příbalové informaci příslušného léku. Jestliže jste použil(a) více přípravku Repatha než jste měl(a) Obraťte se ihned na svého lékaře nebo lékárníka. Jestliže jste zapomněl(a) použít přípravek Repatha Vezměte si přípravek Repatha co nejdříve po vynechané dávce. Poté se obraťte na svého lékaře, který Vám řekne, na kdy si máte naplánovat příští dávku a dodržujte tento nový harmonogram přesně podle lékaře. 4. Možné nežádoucí účinky Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Časté nežádoucí účinky: mohou se vyskytnout u 1 z 10 léčených osob chřipka (vysoká teplota, bolesti v krku, rýma, kašel a zimnice) nachlazení projevující se jako rýma, bolesti v krku nebo infekce vedlejších dutin (zánět nosohltanu nebo infekce horních cest dýchacích) nevolnost (pocit na zvracení) bolesti zad 16
17 bolesti kloubů (artralgie) reakce v místě injekčního vpichu, zarudnutí, modřina nebo bolest vyrážka Méně časté nežádoucí účinky: mohou se vyskytnout u 1 ze 100 léčených osob kopřivka, zarudlé svědivé bouličky na pokožce (urtikárie) Hlášení nežádoucích účinků Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo (viz pokyny níže). Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku. Státní ústav pro kontrolu léčiv Šrobárova Praha 10 Webové stránky: 5. Jak přípravek Repatha uchovávat Uchovávejte tento přípravek mimo dohled a dosah dětí. Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na štítku a krabičce za EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Uchovávejte v chladničce (2 C 8 C). Chraňte před mrazem. Uchovávejte v původním obalu, aby byl přípravek chráněn před světlem. Předplněné pero můžete po vyjmutí z chladničky nechat před podáním ohřát na pokojovou teplotu (do 25 C). Tímto opatřením bude injekce příjemnější. Po vyjmutí z chladničky může být přípravek Repatha uchováván při pokojové teplotě (do 25 C) v původním obalu a musí se použít do 1 týdne. Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí. 6. Obsah balení a další informace Co přípravek Repatha obsahuje Léčivou látkou je evolocumabum. Jedno předplněné pero obsahuje evolocumabum 140 mg v 1 ml roztoku. Pomocnými látkami jsou prolin, kyselina octová 98%, polysorbát 80, hydroxid sodný a voda na injekci. Jak přípravek Repatha vypadá a co obsahuje toto balení Repatha je čirý až opalescentní, bezbarvý až nažloutlý roztok, který neobsahuje prakticky žádné částice. Nepoužívejte tento lék, pokud zpozorujete změnu barvy nebo pokud lék obsahuje velké kousky, šupinky nebo barevné částice. Balení obsahuje jedno, dvě, tři nebo šest jednorázových předplněných per SureClick. 17
18 Držitel rozhodnutí o registraci a výrobce: Amgen Europe B.V. Minervum ZK Breda Nizozemsko Držitel rozhodnutí o registraci: Amgen Europe B.V. Minervum ZK Breda Nizozemsko Výrobce: Amgen Technology Ireland Pottery Road Dun Laoghaire Co Dublin Irsko Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci. Amgen s.r.o. Tel: Tato příbalová informace byla naposledy revidována: červenec Další zdroje informací Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky 18
19 Návod k použití: Repatha SureClick předplněné pero na jedno použití Popis jednotlivých částí Před použitím Po použití Šedé dávkovací tlačítko Okénko Žluté okénko (injekce dokončena) je Lék Nasazený oranžový kryt Žlutý bezpečnostní chránič Sejmutý kryt oranžový Jehla je uvnitř 19
20 Důležité Před použitím Repatha předplněného pera si přečtěte tyto důležité informace: Zdravotnický pracovník Vám řekne, kolik Repatha předplněných per potřebujete na Vaši dávku. Pokud použijete více než jedno Repatha předplněné pero, mají být po dosažení pokojové teploty všechny injekce podány do 30 minut. Uchovávejte Repatha předplněné pero v původním obalu, aby bylo chráněno před světlem. Uchovávejte Repatha předplněné pero v chladničce (2 C až 8 C). Je důležité, abyste se nepokoušel(a) podat si sám/sama injekci, dokud Vás neproškolí váš lékař nebo zdravotnický pracovník. Oranžový kryt na Repatha předplněném peru obsahuje chránič jehly (umístěný uvnitř krytu), který se skládá ze suchého přírodního kaučuku, který je vyroben z latexu. Pokud jste na latex alergický(á), řekněte to svému zdravotnickému pracovníkovi. Uchovávejte Repatha předplněné pero mimo dohled a dosah dětí. POZOR: nezmrazujte Repatha předplněné pero nebo nepoužívejte pero, které bylo zmrazeno. netřepejte Repatha předplněným perem. nesnímejte z Repatha předplněného pera oranžový kryt, dokud nejste připraveni si injekci podat. nepoužívejte Repatha předplněné pero, pokud Vám spadlo na tvrdý povrch. Část pera může být poškozena, i když to není vidět. nepoužívejte Repatha předplněné pero, pokud uplynula doba použitelnosti. A Krok 1: Příprava Vyndejte Repatha předplněné pero z balení. 1. Předplněné pero opatrně vytáhněte rovně z krabičky. 2. Původní balení s nepoužitými předplněnými pery vraťte do chladničky. 3. Počkejte alespoň 30 minut, aby se předplněné pero přirozeně ohřálo před injekcí na pokojovou teplotu. POZOR: Nepokoušejte se ohřívat předplněné pero pomocí zdrojů tepla jako je horká voda nebo mikrovlná trouba. Nevystavujte předplněné pero přímému slunečnímu světlu. Netřepejte předplněným perem. Neodstraňujte zatím z předplněného pera oranžový kryt. 20
21 B Zkontrolujte Repatha předplněné pero. Ujistěte se, že lék v okénku je čirý a bezbarvý až lehce nažloutlý. Zkontrolujte dobu použitelnosti. Předplněné pero NEPOUŽÍVEJTE, pokud: je lék zakalený nebo zabarvený nebo obsahuje velké shluky, vločky nebo částice. se některá část zdá být prasklá nebo rozbitá. Vám předplněné pero upadlo. chybí oranžový kryt nebo není bezpečně nasazen. uplynula doba použitelnosti. Ve všech těchto případech použijte nové předplněné pero. C Připravte si vše, co potřebujete pro injekci. Důkladně si umyjte ruce vodou a mýdlem. Na čisté, dobře osvětlené místo si dejte: Nové předplněné pero. Tampóny navlhčené alkoholem. Smotek vaty nebo gázové polštářky. Náplast. Nádobu na ostrý odpad. D Připravte si a očistěte místo pro injekci. Horní část paže Břicho Stehno Můžete použít: Stehno. Břicho kromě oblasti 5 cm (2 palce) okolo pupku. Vnější stranu horní části paže (pouze pokud Vám injekci podává někdo jiný). Místo pro injekci očistěte tampónem navlhčeným alkoholem. Před injekcí nechte kůži uschnout. Před aplikací se místa injekce znovu NEDOTÝKEJTE. Pokaždé si k aplikaci injekce, kterou si podáváte, vyberte jiné místo. Pokud potřebujete použít stejné místo, ujistěte se, že to není stejný bod v místě, které jste použili minule. Injekci si NEPODÁVEJTE do oblastí, kde je kůže citlivá, pohmožděná, červená nebo tvrdá. Nepodávejte injekci do oblastí s jizvami nebo strijemi. 21
Příbalová informace: informace pro uživatele. Repatha 140 mg injekční roztok v předplněném peru evolocumabum
 Příbalová informace: informace pro uživatele Repatha 140 mg injekční roztok v předplněném peru evolocumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro uživatele Repatha 140 mg injekční roztok v předplněném peru evolocumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro uživatele. Repatha 140 mg injekční roztok v předplněném peru evolocumabum
 Příbalová informace: informace pro uživatele Repatha 140 mg injekční roztok v předplněném peru evolocumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro uživatele Repatha 140 mg injekční roztok v předplněném peru evolocumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro uživatele. Repatha 140 mg injekční roztok v předplněném peru evolocumabum
 Příbalová informace: informace pro uživatele Repatha 140 mg injekční roztok v předplněném peru evolocumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro uživatele Repatha 140 mg injekční roztok v předplněném peru evolocumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CAMILIA perorální roztok v jednodávkovém obalu
 sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90
 Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls107935/2012
 sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
Příbalová informace: informace pro pacienta. ANACID 258 mg/388 mg perorální suspenze. Magnesii hydroxidum, Algeldrati suspensio
 sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
Příbalová informace: informace pro pacienta. Maltofer, 10 mg/ml sirup. polymaltosum ferricum
 sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bronchostop sirup. Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt
 Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Návod k použití EDUKAČNÍ MATERIÁLY. mecasermin. Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex
 EDUKAČNÍ MATERIÁLY mecasermin Návod k použití Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
EDUKAČNÍ MATERIÁLY mecasermin Návod k použití Tento leták je rychlým návodem k přípravě a podání injekce přípravku Increlex Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových
Příbalová informace: informace pro uživatele. Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum
 sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
Příbalová informace: informace pro uživatele. Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum
 Příbalová informace: informace pro uživatele Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro pacienta. Maltofer 50 mg/ml perorální kapky, roztok
 sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
POKYNY PRO POUŽITÍ. Budete potřebovat následující položky, které jsou obsaženy v balení:
 POKYNY PRO POUŽITÍ Jak používat předplněné pero PegIntron Následující pokyny vysvětlují, jak si můžete aplikovat injekci sám/sama pomocí předplněného pera. Prosím, přečtěte si pečlivě pokyny a krok za
POKYNY PRO POUŽITÍ Jak používat předplněné pero PegIntron Následující pokyny vysvětlují, jak si můžete aplikovat injekci sám/sama pomocí předplněného pera. Prosím, přečtěte si pečlivě pokyny a krok za
1. Co je přípravek Maltofer Fol žvýkací tablety a k čemu se používá. Maltofer Fol se používá k léčbě a prevenci nedostatku železa v organismu.
 sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
Příbalová informace: informace pro uživatele. VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa
 Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro uživatele. Firazyr 30 mg injekční roztok v předplněné injekční stříkačce Icatibantum
 Příbalová informace: informace pro uživatele Firazyr 30 mg injekční roztok v předplněné injekční stříkačce Icatibantum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele Firazyr 30 mg injekční roztok v předplněné injekční stříkačce Icatibantum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
prášek pro infuzní roztok
 sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pro uživatele. Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum
 sp.zn. sukls154670/2013 Příbalová informace: informace pro uživatele Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls154670/2013 Příbalová informace: informace pro uživatele Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Kyprolis 60 mg prášek pro infuzní roztok carfilzomibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Kyprolis 60 mg prášek pro infuzní roztok carfilzomibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
sp. zn. sukls180859/2015
 sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum)
 sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Používání Apidry v 10 ml injekčních lahvičkách
 NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
Příbalová informace: informace pro uživatele
 sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
Příbalová informace: informace pro uživatele AESCIN-TEVA. 20 mg, enterosolventní tablety. escinum alfa
 sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls113741/2015 Příbalová informace: informace pro uživatele AESCIN-TEVA 20 mg, enterosolventní tablety escinum alfa Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Prolia 60 mg injekční roztok v předplněné injekční stříkačce denosumabum
 Příbalová informace: informace pro uživatele Prolia 60 mg injekční roztok v předplněné injekční stříkačce denosumabum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro uživatele Prolia 60 mg injekční roztok v předplněné injekční stříkačce denosumabum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: Informace pro uživatele Maltofer 50 mg/ml, perorální kapky, roztok. železo ve formě polymaltosum ferricum
 sp.zn. sukls238918/2016 Příbalová informace: Informace pro uživatele Maltofer 50 mg/ml, perorální kapky, roztok železo ve formě polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls238918/2016 Příbalová informace: Informace pro uživatele Maltofer 50 mg/ml, perorální kapky, roztok železo ve formě polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: Informace pro uživatele. NovoThirteen 2 500 IU prášek pro přípravu injekčního roztoku s rozpouštědlem
 Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek pro přípravu injekčního roztoku s rozpouštědlem catridecacogum (rekombinantní koagulační faktor XIII) Tento přípravek podléhá dalšímu
Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek pro přípravu injekčního roztoku s rozpouštědlem catridecacogum (rekombinantní koagulační faktor XIII) Tento přípravek podléhá dalšímu
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
Příbalová informace: informace pro uživatele
 sp.zn. sukls136451/2013 a sp.zn. sukls36933/2014 Příbalová informace: informace pro uživatele Aprokam50 mg prášek pro injekční roztok cefuroximum Přečtěte si pozorně celou příbalovou informaci dříve, než
sp.zn. sukls136451/2013 a sp.zn. sukls36933/2014 Příbalová informace: informace pro uživatele Aprokam50 mg prášek pro injekční roztok cefuroximum Přečtěte si pozorně celou příbalovou informaci dříve, než
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret
 sp.zn.sukls240326/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn.sukls240326/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. Maltofer 10 mg/ml sirup
 sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: Informace pro pacienta
 sp.zn.sukls98480/2015 Příbalová informace: Informace pro pacienta Mucoplant břečťanový sirup proti kašli sirup Léčivá látka: Hederae helicis folii extractum siccum (suchý extrakt z břečťanového listu)
sp.zn.sukls98480/2015 Příbalová informace: Informace pro pacienta Mucoplant břečťanový sirup proti kašli sirup Léčivá látka: Hederae helicis folii extractum siccum (suchý extrakt z břečťanového listu)
Příbalová informace: Informace pro uživatele. NovoThirteen IU prášek a rozpouštědlo pro injekční roztok
 Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek a rozpouštědlo pro injekční roztok catridecacogum (rekombinantní koagulační faktor XIII) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek a rozpouštědlo pro injekční roztok catridecacogum (rekombinantní koagulační faktor XIII) Přečtěte si pozorně celou příbalovou informaci
Příprava a podání injekce
 Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. HYPNOMIDATE, 2 mg/ml, injekční roztok Etomidatum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HYPNOMIDATE, 2 mg/ml, injekční roztok Etomidatum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HYPNOMIDATE, 2 mg/ml, injekční roztok Etomidatum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele. Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok
 sp.zn. sukls301709/2016 Příbalová informace: informace pro uživatele Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok Natrii chromas ( 51 Cr) Přečtěte si pozorně celou příbalovou
sp.zn. sukls301709/2016 Příbalová informace: informace pro uživatele Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok Natrii chromas ( 51 Cr) Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. Bronchipret tymián a břečťan sirup Thymi extractum fluidum, Hederae helicis folii extractum fluidum
 sp.zn.sukls205603/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Bronchipret tymián a břečťan sirup Thymi extractum fluidum, Hederae helicis folii extractum fluidum Přečtěte si pozorně tuto příbalovou
sp.zn.sukls205603/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Bronchipret tymián a břečťan sirup Thymi extractum fluidum, Hederae helicis folii extractum fluidum Přečtěte si pozorně tuto příbalovou
Příbalová informace: Informace pro uživatele. NEO-BRONCHOL 15 mg pastilky ambroxoli hydrochloridum
 sp.zn. sukls221673/2011 Příbalová informace: Informace pro uživatele NEO-BRONCHOL 15 mg pastilky ambroxoli hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls221673/2011 Příbalová informace: Informace pro uživatele NEO-BRONCHOL 15 mg pastilky ambroxoli hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Venoruton gel 20 mg/g, gel oxerutina
 sp.zn. sukls196201/2016 a sp.zn. sukls192934/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Venoruton gel 20 mg/g, gel oxerutina Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn. sukls196201/2016 a sp.zn. sukls192934/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Venoruton gel 20 mg/g, gel oxerutina Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn.sukls195792/2018 a sp.zn.sukls195821/2018 Příbalová informace: informace pro pacienta
 sp.zn.sukls195792/2018 a sp.zn.sukls195821/2018 Příbalová informace: informace pro pacienta NEUROMULTIVIT injekční roztok Léčivé látky: Thiamini hydrochloridum (vitamín B1), pyridoxini hydrochloridum (vitamín
sp.zn.sukls195792/2018 a sp.zn.sukls195821/2018 Příbalová informace: informace pro pacienta NEUROMULTIVIT injekční roztok Léčivé látky: Thiamini hydrochloridum (vitamín B1), pyridoxini hydrochloridum (vitamín
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele TAKHZYRO 300 mg injekční roztok lanadelumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele TAKHZYRO 300 mg injekční roztok lanadelumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. fentikonazoli nitras
 sp.zn.sukls33807/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Lomexin 20 mg/g vaginální krém fentikonazoli nitras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls33807/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Lomexin 20 mg/g vaginální krém fentikonazoli nitras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele SOLMUCOL 100
 sp.zn. sukls170392/2012 Příbalová informace: informace pro uživatele SOLMUCOL 100 Granule pro perorální roztok Acetylcysteinum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls170392/2012 Příbalová informace: informace pro uživatele SOLMUCOL 100 Granule pro perorální roztok Acetylcysteinum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: Informace pro uživatele. Strepsils Plus Spray orální sprej dichlorbenzenmethanolum, amylmetacresolum, lidocainum
 sp.zn.sukls188553/2013 Příbalová informace: Informace pro uživatele Strepsils Plus Spray orální sprej dichlorbenzenmethanolum, amylmetacresolum, lidocainum Přečtěte si pozorně tuto příbalovou informaci
sp.zn.sukls188553/2013 Příbalová informace: Informace pro uživatele Strepsils Plus Spray orální sprej dichlorbenzenmethanolum, amylmetacresolum, lidocainum Přečtěte si pozorně tuto příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
NÁVOD K SAMOSTATNÉ APLIKACI PŘÍPRAVKU ENBREL 50 MG V PŘEDPLNĚNÉM AUTOINJEKČNÍM PERU MYCLIC
 NÁVOD K SAMOSTATNÉ APLIKACI PŘÍPRAVKU ENBREL 50 MG V PŘEDPLNĚNÉM AUTOINJEKČNÍM PERU MYCLIC Tento tištěný materiál může lékař poskytnout pouze pacientùm, kterým předepsal přípravek ENBREL 50 mg injekční
NÁVOD K SAMOSTATNÉ APLIKACI PŘÍPRAVKU ENBREL 50 MG V PŘEDPLNĚNÉM AUTOINJEKČNÍM PERU MYCLIC Tento tištěný materiál může lékař poskytnout pouze pacientùm, kterým předepsal přípravek ENBREL 50 mg injekční
Příbalová informace : Informace pro uživatele. Aknemycin 2000 Mast Erythromycinum
 sp.zn. sukls182807/2012 Příbalová informace : Informace pro uživatele Aknemycin 2000 Mast Erythromycinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls182807/2012 Příbalová informace : Informace pro uživatele Aknemycin 2000 Mast Erythromycinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pro uživatele. Zinkorot 25 mg tablety zincum
 1 sp.zn. sukls264417/2017 Příbalová informace: informace pro uživatele Zinkorot 25 mg tablety zincum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
1 sp.zn. sukls264417/2017 Příbalová informace: informace pro uživatele Zinkorot 25 mg tablety zincum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
sp.zn.sukls170650/2014
 sp.zn.sukls170650/2014 Příbalová informace: informace pro uživatele AMBROXOL AL KAPKY 7,5 mg / ml ambroxoli hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls170650/2014 Příbalová informace: informace pro uživatele AMBROXOL AL KAPKY 7,5 mg / ml ambroxoli hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele Prolia 60 mg injekční roztok v předplněné injekční stříkačce denosumabum Přečtěte si pozorně celou příbalovou informaci dříve, než
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele Prolia 60 mg injekční roztok v předplněné injekční stříkačce denosumabum Přečtěte si pozorně celou příbalovou informaci dříve, než
Příbalová informace: informace pro uživatele. Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F)
 sp.zn. sukls298615/2018 Příbalová informace: informace pro uživatele Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F) Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls298615/2018 Příbalová informace: informace pro uživatele Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F) Přečtěte si pozorně celou příbalovou informaci dříve,
Alpicort 2 mg/ml + 4 mg/ml kožní roztok prednisolonum, acidum salicylicum
 sp.zn. sukls176806/2014 Příbalová informace: informace pro uživatele Alpicort 2 mg/ml + 4 mg/ml kožní roztok prednisolonum, acidum salicylicum Přečtěte si pozorně celou příbalovou informaci dříve, než
sp.zn. sukls176806/2014 Příbalová informace: informace pro uživatele Alpicort 2 mg/ml + 4 mg/ml kožní roztok prednisolonum, acidum salicylicum Přečtěte si pozorně celou příbalovou informaci dříve, než
Příbalová informace: informace pro pacienta
 Příbalová informace: informace pro pacienta Trulicity 0,75 mg injekční roztok v předplněném peru Trulicity 1,5 mg injekční roztok v předplněném peru dulaglutidum Přečtěte si pozorně tuto příbalovou informaci
Příbalová informace: informace pro pacienta Trulicity 0,75 mg injekční roztok v předplněném peru Trulicity 1,5 mg injekční roztok v předplněném peru dulaglutidum Přečtěte si pozorně tuto příbalovou informaci
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Imlygic 10 6 jednotek tvořících plaky (PFU)/ml injekční roztok Imlygic 10 8 jednotek tvořících plaky (PFU)/ml injekční roztok talimogenum
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Imlygic 10 6 jednotek tvořících plaky (PFU)/ml injekční roztok Imlygic 10 8 jednotek tvořících plaky (PFU)/ml injekční roztok talimogenum
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí trachey (průdušnice)
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
NÁVOD K SAMOSTATNÉ APLIKACI PŘÍPRAVKU. ENBREL 25 mg a 50 mg v PŘEDPLNĚNÝCH PERECH MYCLIC
 NÁVOD K SAMOSTATNÉ APLIKACI PŘÍPRAVKU ENBREL 25 mg a 50 mg v PŘEDPLNĚNÝCH PERECH MYCLIC Tento tištěný materiál může lékař poskytnout pouze pacientům, kterým předepsal přípravek ENBREL 25 mg nebo 50 mg
NÁVOD K SAMOSTATNÉ APLIKACI PŘÍPRAVKU ENBREL 25 mg a 50 mg v PŘEDPLNĚNÝCH PERECH MYCLIC Tento tištěný materiál může lékař poskytnout pouze pacientům, kterým předepsal přípravek ENBREL 25 mg nebo 50 mg
Příbalová informace: informace pro uživatele. FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
Sp.zn.sukls133559/2018
 Sp.zn.sukls133559/2018 Příbalová informace: informace pro uživatele Betahistin Actavis 24 mg tablety betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls133559/2018 Příbalová informace: informace pro uživatele Betahistin Actavis 24 mg tablety betahistini dihydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls36849/2016 Příbalová informace: informace pro uživatele Technescan DMSA 1,2 mg, kit pro radiofarmakum succimerum
 sp.zn. sukls36849/2016 Příbalová informace: informace pro uživatele Technescan DMSA 1,2 mg, kit pro radiofarmakum succimerum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls36849/2016 Příbalová informace: informace pro uživatele Technescan DMSA 1,2 mg, kit pro radiofarmakum succimerum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pacienta. LIVOSTIN nosní sprej, suspenze. levocabastini hydrochloridum
 sp.zn.sukls94010/2015 Příbalová informace: informace pacienta LIVOSTIN nosní sprej, suspenze levocabastini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls94010/2015 Příbalová informace: informace pacienta LIVOSTIN nosní sprej, suspenze levocabastini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ADDITIVA VITAMIN C ZITRONE 1 000 mg Šumivé tablety acidum ascorbicum
 sp.zn.: sukls212899/2012 a sp.zn.: sukls9339/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ADDITIVA VITAMIN C ZITRONE 1 000 mg Šumivé tablety acidum ascorbicum Přečtěte si pozorně tuto příbalovou informaci
sp.zn.: sukls212899/2012 a sp.zn.: sukls9339/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ADDITIVA VITAMIN C ZITRONE 1 000 mg Šumivé tablety acidum ascorbicum Přečtěte si pozorně tuto příbalovou informaci
Příbalová informace: informace pro uživatele. Trusopt free bez konzervačních přísad 20 mg/ml, oční kapky, roztok, v jednodávkovém obalu Dorzolamidum
 Příbalová informace: informace pro uživatele Trusopt free bez konzervačních přísad 20 mg/ml, oční kapky, roztok, v jednodávkovém obalu Dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele Trusopt free bez konzervačních přísad 20 mg/ml, oční kapky, roztok, v jednodávkovém obalu Dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele Silkis 3 mikorgramy/g mast (calcitriolum)
 Sp.zn. sukls210281/2016 a k sp.zn. sukls63246/2017 Příbalová informace: informace pro uživatele Silkis 3 mikorgramy/g mast (calcitriolum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Sp.zn. sukls210281/2016 a k sp.zn. sukls63246/2017 Příbalová informace: informace pro uživatele Silkis 3 mikorgramy/g mast (calcitriolum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příbalová informace: informace pro pacienta
 sp. zn. sukls56073/2015 Příbalová informace: informace pro pacienta LACTULOSA BIOMEDICA (lactulosi solutio) sirup Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat,
sp. zn. sukls56073/2015 Příbalová informace: informace pro pacienta LACTULOSA BIOMEDICA (lactulosi solutio) sirup Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: informace pro pacienta. Septabene 1,5 mg/ml + 5,0 mg/ml orální sprej, roztok benzydamini hydrochloridum/cetylpyridinii chloridum
 Sp. zn. sukls56216/2014 Příbalová informace: informace pro pacienta Septabene 1,5 mg/ml + 5,0 mg/ml orální sprej, roztok benzydamini hydrochloridum/cetylpyridinii chloridum Přečtěte si pozorně tuto příbalovou
Sp. zn. sukls56216/2014 Příbalová informace: informace pro pacienta Septabene 1,5 mg/ml + 5,0 mg/ml orální sprej, roztok benzydamini hydrochloridum/cetylpyridinii chloridum Přečtěte si pozorně tuto příbalovou
Příbalová informace: informace pro pacienta
 Příbalová informace: informace pro pacienta Otezla 10 mg potahované tablety Otezla 20 mg potahované tablety Otezla 30 mg potahované tablety Apremilastum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro pacienta Otezla 10 mg potahované tablety Otezla 20 mg potahované tablety Otezla 30 mg potahované tablety Apremilastum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele. Jox 85 mg/1 ml+1 mg/1 ml orální sprej, roztok povidonum iodinatum, allantoinum
 sp.zn.sukls19836/2015 Příbalová informace: informace pro uživatele Jox 85 mg/1 ml+1 mg/1 ml orální sprej, roztok povidonum iodinatum, allantoinum Přečtěte si pozorně tuto příbalovou informaci dříve, než
sp.zn.sukls19836/2015 Příbalová informace: informace pro uživatele Jox 85 mg/1 ml+1 mg/1 ml orální sprej, roztok povidonum iodinatum, allantoinum Přečtěte si pozorně tuto příbalovou informaci dříve, než
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 sp.zn. sukls33645/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls33645/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: Informace pro uživatele. Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum)
 sp.zn. sukls273948/2016 Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls273948/2016 Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
Desloratadin Apotex 5 mg potahované tablety desloratadinum
 PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Desloratadin Apotex 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Desloratadin Apotex 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro pacienta. Loceryl 50 mg/ml léčivý lak na nehty amorolfini hydrochloridum
 Sp.zn. sukls73205/2017 Příbalová informace: informace pro pacienta Loceryl 50 mg/ml léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn. sukls73205/2017 Příbalová informace: informace pro pacienta Loceryl 50 mg/ml léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Canespor 1x denně roztok kožní roztok bifonazolum
 sukls46174/2014 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE Canespor 1x denně roztok kožní roztok bifonazolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
sukls46174/2014 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE Canespor 1x denně roztok kožní roztok bifonazolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls32991/2012 a sp.zn.: sukls148548/2014
 sp.zn.: sukls32991/2012 a sp.zn.: sukls148548/2014 Příbalová informace: Informace pro uživatele TRUSOPT 20 mg/ml, oční kapky, roztok dorzolamidi hydrochloridum Přečtěte si pozorně celou příbalovou informaci
sp.zn.: sukls32991/2012 a sp.zn.: sukls148548/2014 Příbalová informace: Informace pro uživatele TRUSOPT 20 mg/ml, oční kapky, roztok dorzolamidi hydrochloridum Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro pacienta. Desloratadin Actavis 0,5 mg/ml Perorální roztok desloratadinum
 Sp.zn.sukls20953/2015 Příbalová informace: informace pro pacienta Desloratadin Actavis 0,5 mg/ml Perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls20953/2015 Příbalová informace: informace pro pacienta Desloratadin Actavis 0,5 mg/ml Perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA)
 Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Příbalová informace: informace pro uživatele. TEARS NATURALE II oční kapky, roztok dextranum 70, hypromelosum
 sp.zn.sukls29736/2015 Příbalová informace: informace pro uživatele TEARS NATURALE II oční kapky, roztok dextranum 70, hypromelosum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.sukls29736/2015 Příbalová informace: informace pro uživatele TEARS NATURALE II oční kapky, roztok dextranum 70, hypromelosum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE PREPARATION H. 23 mg / 69 mg. čípky. (Faecis extractum fluidum, Squali oleum)
 sp.zn. sukls186765/2014 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE PREPARATION H 23 mg / 69 mg čípky (Faecis extractum fluidum, Squali oleum) Přečtěte si pozorně tuto příbalovou informaci dříve, než
sp.zn. sukls186765/2014 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE PREPARATION H 23 mg / 69 mg čípky (Faecis extractum fluidum, Squali oleum) Přečtěte si pozorně tuto příbalovou informaci dříve, než
Příbalová informace: informace pro uživatele. SMECTA 3 g prášek pro perorální suspenzi. diosmectitum
 sp. zn. sukls76878/2017 Příbalová informace: informace pro uživatele SMECTA 3 g prášek pro perorální suspenzi diosmectitum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp. zn. sukls76878/2017 Příbalová informace: informace pro uživatele SMECTA 3 g prášek pro perorální suspenzi diosmectitum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. DOXIUM 500 mg tvrdé tobolky. Calcii dobesilas monohydricus
 sp.zn. sukls178298/2011 a sp.zn. sukls285789/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DOXIUM 500 mg tvrdé tobolky Calcii dobesilas monohydricus Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls178298/2011 a sp.zn. sukls285789/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DOXIUM 500 mg tvrdé tobolky Calcii dobesilas monohydricus Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Neulasta 6 mg, injekční roztok v předplněné injekční stříkačce pegfilgrastimum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro pacienta. Ichtoxyl 90 mg/g mast ichthammolum
 sp.zn.sukls229456/2018 Příbalová informace: informace pro pacienta Ichtoxyl 90 mg/g mast ichthammolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn.sukls229456/2018 Příbalová informace: informace pro pacienta Ichtoxyl 90 mg/g mast ichthammolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls229950/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls229950/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Mycosten 10 mg/g Shampoo Ciclopiroxum šampon Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls229950/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Mycosten 10 mg/g Shampoo Ciclopiroxum šampon Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret
 sp.zn. sukls224154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn. sukls224154/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. Strensiq 40 mg/ml injekční roztok (12 mg/0,3 ml 18 mg/0,45 ml 28 mg/0,7 ml 40 mg/1,0 ml) Asfotasum alfa
 B. PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro uživatele Strensiq 40 mg/ml injekční roztok (12 mg/0,3 ml 18 mg/0,45 ml 28 mg/0,7 ml 40 mg/1,0 ml) Asfotasum alfa Tento léčivý přípravek podléhá
B. PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro uživatele Strensiq 40 mg/ml injekční roztok (12 mg/0,3 ml 18 mg/0,45 ml 28 mg/0,7 ml 40 mg/1,0 ml) Asfotasum alfa Tento léčivý přípravek podléhá
Příbalová informace: informace pro uživatele. Metastron 37 MBq/ml, injekční roztok
 sp.zn. sukls72263/2019 Příbalová informace: informace pro uživatele Metastron 37 MBq/ml, injekční roztok Strontii chloridum 89 Sr Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls72263/2019 Příbalová informace: informace pro uživatele Metastron 37 MBq/ml, injekční roztok Strontii chloridum 89 Sr Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
