PŘÍLOHA III SOUHRN ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
|
|
|
- Jindřich Esterka
- před 8 lety
- Počet zobrazení:
Transkript
1 PŘÍLOHA III SOUHRN ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE Poznámka: Tato verze SPC, označení na obalu a příbalové informace je verze platná v době vydání Rozhodnutí Komise. Po vydání Rozhodnutí Komise oprávněné orgány členského státu ve spolupráci s referenčním členským státem provedou požadovanou aktualizaci informací o přípravku. Z tohoto důvodu toto SPC, označení na obalu a příbalová informace nemusejí nutně souhlasit s aktuálními texty. 7
2 SOUHRN ÚDAJŮ O PŘÍPRAVKU 8
3 Platný souhrn údajů o přípravku je konečnou verzí, které bylo dosaženo v průběhu procedury Koordinační skupiny s následujícími změnami: 9
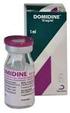
4 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Prevora 100mg/ml zubní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml přípravku Prevora zubní roztok (chlordexidinový nátěr 1.stupeň) obsahuje 100 mg chlorhexidini diacetas Úplný seznam pomocných látek viz bod FARMACEUTICKÁ ÚPRAVA Zubní roztok Chlorhexidinový nátěr 1.stupeň Průzračný, lehce nahnědlý roztok s charakteristickou vůní, bez viditelných částic. Tmelicí nátěr- 2. stupeň Mléčně bílá tekutina o nízké vizkozitě se slabou charakteristickou vůní, bez viditelných částic. 4. KLINICKÉ ÚDAJE 4.1 Terapeutické indikace Prevora 100/ml zubní roztok je antiseptický roztok, který je aplikován místně na chrup pacientů k prevenci korunkových a kořenových kazů u dospělých pacientů, u kterých je vysoké riziko zubních kazů (např. u pacientů trpících xerostomií, nebo u těch, kteří mají 3, nebo více kazů na počátku léčebného plánu). K použití v zubních ordinacích pouze zubními specialisty. Pacienti mají být informováni o důležitosti ústní hygieny a o požívání cukru: Pacienty se špatnou ústní hygienou, nebo častým požíváním cukru je třeba upozornit, že pravidelné a časté čištění zubů fluoridovanou zubní pastou, spojené s kontrolovaným požíváním cukru, jsou důležitými podmínkami celkového úspěchu léčby. 4.2 Dávkování a způsob podání Dávkování Přípravek se dávkuje individuálně a dávka pro dopělé se pohybuje mezi 300 µl a 600 µl přípravku Prevora 100 mg/ml zubní roztok. Pacient je podroben 5 léčebným procedurám během prvního roku léčby, z nichž 4 jsou provedeny během prvního měsíce v týdenních intervalech a poslední dávka je podána v 6. měsíci. Následující léčba pacienta se řídí podle odborného klinického posouzení rizika zubního kazu. Prevora 100 mg/ml zubní roztok se nanáší topicky na celý chrup pacienta vatovým tampónem nebo jemným štětečkem. Vatový tampón nebo štěteček se namočí do přípravku Prevora 100 mg/ml zubní roztok a nanese se na povrch zubu (Obrázek 1). 10
5 Obrázek 1 Nanášení přípravku Prevora 100 mg/ml zubní roztok Namočte vatový tampón, nebo štěteček do injekční lahvičky (ampulky) a naneste roztok na povrch zubů. Pacienty je třeba upozornit, že: Zaschlý nátěr přípravku Prevora začne se ze zubů začne stírat během prvního jídla. Pacienti by neměli jíst tvrdé pokrmy (např. maso, jablka) nejméně po dobu 4 hodin po léčbě. Pacienti by neměli po dobu alespoň 24 hodin žvýkat žvýkačku. Pacienti by si neměli po dobu alespoň 24 hodin po léčbě čistit zuby. Poté si mají začít čistit zuby novým kartáčkem a fluoridovanou zubní pastou 2 až 3 krát denně. Pacienti by si neměli čistit zuby dentální nití po dobu 3 dnů po léčbě. Poté mají používat dentální nit denně.. Pokud má pacient zubní protézu, je třeba, aby ji pravidelně před použitím čistil a dezinfikoval. K dezinfikování se má používat mýdlo a teplá voda. Způsob podávání Vnější (orální) topické podání v zubní ordinaci zubním specialistou. Tento přípravek nemá být polykán. 4.3 Kontraindikace Hypersenzitivita na chlorhexidin, sumaterskou benzoovou pryskyřici nebo ethanol. 4.4 Zvláštní upozornění a opatření pro použití Pouze k vnějšímu (orálnímu) topickému podání - chraňte oči a uši před kontaktem. Při kontaktu s očima proveďte okamžitě důkladné opláchnutí vodou. Prevora 100 mg/ml zubní roztok musí být u pacientů s astmatem nebo ekzémy v anamnéze s opatrností.. Přípravek Prevora 100 mg/ml zubní roztok nemá být nanášen na měkké tkáně. Při kontaktu s měkkými tkáněmi může roztok způsobit dočasný pocit pálení nebo mírný zánět měkkých tkání. 4.5 Interakce s jinými léčivými přípravky a jiné formy interakce Prevora 100 mg/ml zubní roztok se nemá nanášet okamžitě po použití profylaktické pasty s olejovým základem a až po dobu 3 dnů po aplikaci fluoridového dentálního laku. Chlorhexidin není kompatibilní s anionogenními činidly. 4.6 Fertilita, těhotenství a kojení Nebyly provedeny žádné kontrolované studie s cílem zjistit, zda aplikace přípravku Prevora 100 mg/ml zubní roztok na chrup fertilních, těhotných a kojících žen způsobuje nějaké nežádoucí účinky. 11
6 Proto se podávání přípravku Prevora 100 mg/ml zubní roztok během těhotenství nedoporučuje. Protože se mnoho léčiv vylučuje mateřským mlékem a protože nebyly provedeny žádné studie hodnotící podávání přípravku Prevora 100 mg/ml zubní roztok kojícím matkám, podávání tohoto přípravku kojícím matkám se nedoporučuje. 4.7 Účinky na schopnost řídit a obsluhovat stroje Žádné studie hodnotící účinky na schopnost řídit a obsluhovat stroje nebyly provedeny. 4.8 Nežádoucí účinky V každé skupině četností jsou nežádoucí účinky uvedeny podle klesající závažnosti. Poruchy kůže a podkožní tkáně Celkové poruchy a reakce v místě aplikace 4.9 Předávkování Méně časté ( 1/1000 až <1/100) Zrudnutí a/nebo přechodné pálení sliznice ústní dutiny Nepříjemná hořká chuť při kontaktu přípravku Prevora 100 mg/ml zubní rozotok se slinami nebo se sliznicí ústní dutiny Nejsou známy (z dostupných údajů nelze určit) Okamžité hypersenzitivní reakce na chlorhexidin (kopřivka nebo anafylaxe) Přechodná citlivost zubů a ztráta vnímání chuti Zabarvení zubů a silikátových, nebo kompozitových výplní Nebylo zaznamenáno předávkování přípravkem Prevora 100 mg/ml zubní roztok. Známky a symptomy předávkování nebyly tudíž identifikovány. Pokud dojde k předávkování, je třeba jej léčit symptomaticky. 5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti Farmakoterapeutická skupina: A01AB antiinfektiva a antiseptika k lokální orální léčbě. Kód ATC: A01AB03 chlorhexidin. Chlorhexidin je účinný proti široké škále důležitých orálních mikroorganismů, které mají souvislost se vznikem zubních kazů. Měřením kapalinovou chromatografií (HPLC) bylo zjištěno, že chlorhexidin obsažený v tomto léčivém přípravku si na povrchu chrupu dospělých pacientů zachovává baktericidní hladiny vůči Streptococcus mutans po dobu 24 až 48 hodin po aplikaci. Nebyly publikovány zprávy o vzniku trvalé rezistence Streptococcus mutans při opakovaném používání chlorhexidinu až po dobu 2 let. Po více než roční léčbě dospělých pacientů přípravkem Prevora nebyl pozorován vznik signifikantní rezistence Streptococcus mutans na tento přípravek, ani výskyt oportunních infekcí Candida albicans. Střední hodnota kumulativní měsíční dávky chlorhexidinu dodaná v přípravku Prevora 100 mg/ml zubní roztok je přibližně rovna 1,0% (v hmotnostních procentech- w/w) chlorhexidinového dentálního gelu a přibližně polovině dávky dodané při podávání 0,2% (v objemových procentech -w/v) chlorhexidinové ústní vody. 12
7 5.2 Farmakokinetické vlastnosti Chlorhexidin se silně váže k orální sliznici a k chrupu, a proto má velmi nízkou systémovou absorpci. Po orálním použití nebyly v krvi zjištěny žádné detekovatelné hladiny chlorhexidinu. 5.3 Předklinické údaje vztahující se k bezpečnosti Předklinické údaje neodhalily žádné zvláštní riziko pro člověka. 6. FARMACEUTICKÉ ÚDAJE 6.1 Seznam pomocných látek Chlorhexidinový nátěr -1. stupeň: sumaterská benzoová pryskyřice Ethanol Tmelicí nátěr- 2. stupeň: Methakrylátový kopolymer typ RS PM Triethyl-citrát 6.2 Incompatibility Studie kompatibility nejsou k dispozici, a proto tento topický léčivý přípravek nesmí být mísen s žádnými dalšími topickými léčivými přípravky. 6.3 Doba použitelnosti 18 měsíců. Po použití zbylý roztok okamžitě znehodnoťte. 6.4 Zvláštní opatření pro uchovávání Uchovávejte v chladničce ( 2º až 8ºC) 6.5 Druh obalu a obsah balení Prevora 100 mg/ml zubní roztok obsahuje: Chlorhexidinový nátěr 1. stupeň: Chlorhexidin-diacetát Benzoin Sumatra Ethanol Tmelicí nátěr stupeň 2: Disperze amonio-methakrylátového kopolymeru, typ B Triethyl-citrát Jedna krabička přípravku Prevora zubní roztok obsahuje 6 injekčních lahviček ze skla typu 1, obsahujících chlorhexidinový natěr 1. stupeň a 6 injekčních lahviček ze skla typu 1, obsahujících tmelicí nátěr- 2. stupeň. 6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním 13
8 Krok č. 1. Příprava: Přesvědčte se, že na chrupu nejsou otevřené léze zubního kazu, nebo výplně s neúplnými okraji. K aplikaci si připravte podnos (Obrázek 2) s vatovými tampóny, nebo jemnými štětečky, peán/pinzetu, vzduchovou stříkačku a ampulku (injekční lahvičku) s chlorhexidinem 1. stupeň a ampulku (injekční lahvičku) s tmelicím nátěrem- 2. stupeň. Obrázek 2: Podnos připravený pro jednotlivé stupně Léčba Chlorhexidinovmý nátěrem- 1. stupeň a tmelicím nátěrem 2. stupeň. Krok č. 2. Profylaxe: Proveďte profylaxi gumovým profylaktickým lešticím kalíškem a abrazivním pudrem s vodou. Nepoužívejte profylaktickou pastu bez olejového základu. Krok č. 3. Vyčistěte chrup dentální nití: Důkladně propláchněte a vyčistěte pacientův chrup nevoskovanou dentální nití, abyste odstranili zbytky brusného pudru a zubního plaku.. Důkladně očistěte distální plochu posledního zubu každého patrového oblouku otřením vatovým tampónem upevněným v pinzetě/peánu. Krok č. 4. Izolujte jeden kvadrant: Izolujte jeden kvadrant chrupu vatovými tampóny a ejektorem slin. Krok č. 5. Zuby osušte: Vzduchovou stříkačkou osušte všechny zuby v tomto kvadrantu. Krok č. 6. Naneste chlorhexidinový nátěr- 1. stupeň do na interproximální plochy: Vatovým tampónem v pinzetě/peánu, nebo jemným štětečkem vhodným k dosažení interproximálních prostor, naneste vrstvu chlorhexidinu- 1. stupeň- na interproximální plochy všech zadních zubů v kvadrantu a dávejte pozor, abyste nenatřeli měkké tkáně. Poté vysušte povrchy zubů vzduchovou stříkačkou. Obrázek 3: Jemným štětečkem naneste chlorhexidinový nátěr Prevora- 1. stupeň k okraji dásní a stejným způsobem pokračujte s tmelicím nátěrem Prevora- 2. stupeň. Krok č. 7. Naneste chlorhexidinový nátěr-1. stupeň na ostaní plochy zubů: Aplikujte tento nátěr na všechny ostatní plochy zubů (Obrázek 3) ve stejném kvadrantu a poté je vysušte vzduchem. Buďte opatrní, abyste chlorhexidinový nátěr -1. stupeň- nenanesli na měkké tkáně, neboť by to mohlo pacientovi způsobit pálení dásní a jazyka. Krok č. 8. Naneste tmelicí nátěr- 2. stupeň: Aplikujte tento druhý nátěr (s bílým uzávěrem) na stejný kvadrant, přičemž použijte nový vatový tampón, nebo nový jemný štěteček. Poté tento druhý nátěr vysušte vzduchovou stříkačkou. Krok č. 9. Opakujte natírání na ostatních kvadrantech: Opakujte krok 4 až 8 na zbylých kvadrantech chrupu. 14
9 Krok č. 10. Upozorněte pacienta: Poskytněte pacientovi tyto instrukce: Zaschlý nátěr Prevora se začne ze zubů stírat během prvního jídla. Pacient nemá po dobu alespoň 4 hodin po léčbě jíst trvdé pokrmy (např. maso, jablka). Pacient nemá po dobu nejméně 24 hodin žvýkat žvýkačku. Pacient by si neměl po dobu alespoň 24 hodin po léčbě čistit zuby. Poté si má začít čistit zuby novým kartáčkem a fluoridovanou zubní pastou 2 až 3 krát denně. Pacient by si neměl čistit zuby dentální nití po dobu 3 dnů po léčbě. Poté má používat dentální nit denně. Pokud má pacient zubní protézu, je třeba, aby ji pravidelně před použitím čistil a dezinfikoval. K dezinfekci se má používat mýdlo a teplá voda. Krok č. 11. Naplánujte opakování léčby: Opakujte výše uvedenou aplikaci přípravku Prevora každý týden ještě další 3 týdny po této první léčbě. Poté se má přípravek ještě jednou aplikovat za 6 měsíců po první léčbě přípravkem a poté dále dle klinického zvážení. Nástroje a oděvy, které přišly do kontaktu s nátěrem chlorhexidinu- 1. stupeň, lze vyčistit alkoholem. Nástroje a oděvy, které přišly do kontaktu s tmelicím nátěrem-2. stupeň, lze vyčistit vodou. Nepoužitý výrobek a odpad musí být odstraněn v souladu s místními požadavky. 7. DRŽITEL ROZHODNUTÍ O REGISTRACI CHX Technologies Europe Limited Guinness Enterprise Centre Taylor s Lane Dublin 8, Ireland Irsko 8. REGISTRAČNÍ ČÍSLO (A) PA 1205/1/1 9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE Datum první registrace: 5. května, DATUM REVIZE TEXTU Září 2010 Podrobné informace o tomto léčivém přípravku jsou dostupné na webových stránkách 15
10 OZNAČENÍ NA OBALU 16
11 Platné označení na obalu je konečnou verzí, které bylo dosaženo v průběhu procedury Koordinační skupiny: 17
12 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU VNĚJŠÍ OBAL- PAPÍROVÁ SKLÁDAČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Prevora 100 mg/ml zubní roztok Chlorhexidin-diacetát 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml Dentálního Roztoku Prevora (chlorhexidinový nátěr stupeň 1) obsahuje 100 mg chlorhexidini diacetas 3. SEZNAM POMOCNÝCH LÁTEK 1. stupeň : sumaterská benzoová pryskyřice Ethanol 2.stupeň : Methakrylátový kopolymer typ RS PM Triethyl-citrát 4. LÉKOVÁ FORMA A VELIKOST BALENÍ Zubní roztok Léčebné sady sestávají ze: 6 injekčních lahviček obsahujících chlorhexidinový nátěr( 1.stupeň). Injekční lahvičky mají objem 2 ml a jsou ze skla typu 1 6 injekčních lahviček obsahujících tmelicí nátěr (2. stupeň). Injekční lahvičky mají objem 2 ml a jsou ze skla typu 1 5. ZPŮSOB A CESTA/CESTY PODÁNÍ Před použitím si přečtěte příbalovou informaci. Pouze pro vnější (orální) topické podání. 6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ Uchovávejte mimo dosah a dohled dětí. 7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ Neuplatňuje se 8. POUŽITELNOST EXP. 9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ Uchovávejte ve svislé poloze v chladničce při teplotě 2-8 C. 10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ 18
13 11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI CHX Technologies Europe Limited Guinness Enterprise Centre Taylor s Lane Dublin 8, Irsko 12. REGISTRAČNÍ ČÍSLO/ČÍSLA <[Bude doplněno na národní úrovni]> 13. ČÍSLO ŠARŽE Lot 14. KLASIFIKACE PRO VÝDEJ <Výdej léčivého přípravku vázán na lékařský předpis.> <Výdej léčivého přípravku možný bez lékařského předpisu.> 15. NÁVOD K POUŽITÍ Před použitím si přečtěte příbalovou informaci. 16. INFORMACE V BRAILLOVU PÍSMU < Nevyžaduje se - odůvodnění přijato > 19
14 MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU injekční lahvička - 2ML 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Chlorhexidinový nátěr (1. stupeň) Zubní roztok 100 mg/ml, chlorhexidiini diacetas Tmelicí nátěr (2. stupeň) 2. ZPŮSOB PODÁNÍ Dentální podání 3. SEZNAM POMOCNÝCH LÁTEK MM/RRRR 4. LÉKOVÁ FORMA A VELIKOST BALENÍ Lot 5. ZPŮSOB A CESTA/CESTY PODÁNÍ Jedna injekční lahvička obsahuje 1 ml chlorhexidinového nátěru stupeň 1 6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ číslo rozhodnutí oregistraci Před použitím si přečtěte příbalovou informaci. 20
15 PŘÍBALOVÁ INFORMACE 21
16 Platná příbalová informace je konečnou verzí, které bylo dosaženo v průběhu procedury Koordinační skupiny s následujícími změnami: 22
17 PŘÍBALOVÉ INFORMACE: INFORMACE PRO UŽIVATELE Prevora 100 mg/ml zubní roztok Chlorhexidini diacetas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. Máte-li jakékoli další otázky, zeptejte se svého zubního lékaře. Tento nátěr byl doporučen na Váš chrup Vaším zubním lékařem a bude na Vaše zuby nanesen při několika návštěvách. Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému zubnímu lékaři. V příbalové informaci naleznete: 1. Co je <přípravek>x a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete<přípravek> X <užívat> <používat> 3. Jak léčení roztokem Prevora probíhá. 4. Možné nežádoucí účinky. 5. Jak roztok Prevora uchovávat. 6. Další informace. 1. CO JE PREVORA A K ČEMU SE POUŽÍVÁ. Tento dentální nátěr je místní léčba k prevenci zubních kazů zubní korunky a kořenů zubů u dospělých pacientů, u kterých je vysoké riziko vzniku zubního kazu (např. u osob trpících suchostí v ústech, nebo u osob s velkým počtem kazů při návštěvě zubního lékaře). Tento nátěr dočasně pokryje Váš chrup a sníží množství baktérií na Vašich zubech, které způsobují zubní kaz. Ústní hygiena a požívání cukru: Pokud máte špatnou ústní hygienu a/nebo často požíváte cukry, musíte si čistit zuby fluoridovanou zubní pastou a snížit konzumaci cukru. Obojí je důležité k celkovému úspěchu léčby přípravkem Prevora. 2. ČEMU MUSÍTE VĚNOVAT POZORNOST PŘED ZAHÁJENÍM LÉČBY PŘÍPRAVKEM PREVORA. Nezahajujte léčbu roztokem Prevora Jestliže jste alergický/á (přecitlivělý/á) na chlorhexidin, sumaterskou benzoovou pryskyřici nebo ethanol. Jestliže jste alergický/á (přecitlivělý/á) na pomocné látky obsažené ve tmelicím nátěru (2. stupeň), který je druhým nátěrem aplikovaným bezprostředně po prvním nátěru (1. stupeň). Pomocnými látkami obsženými v tomto druhém nátěru jsou: Methakrylátový kopolymer typ RS PM, triethyl-citrát a čištěná voda Jestliže byl v posledních 3 dnech na Vaše zuby aplikován fluoridový lak. Zvláštní opatrnosti při použití přípravku Prevora je zapotřebí Před zahájením léčby roztokem Prevora informujte svého zubního lékaře, pokud trpíte astmatem, ekzémy nebo jinými druhy alergických onemocnění.. Vzájemné působení s dalšími léčivými přípravky Prosím, informujte svého zubního lékaře o všech lécích, které užíváte nebo jste užíval(a) v nedávné době, a to i o lécích, které jsou dostupné bez lékařského předpisu. Těhotenství a kojení Poraďte se se svým lékařem dříve, než začnete užívat nebo než Vám má být podán jakýkoliv lék. 23
18 Řízení dopravních prostředků a obsluha strojů U roztoku Prevora nebyl zjištěn vliv na schopnost řídit motorová vozidla. U roztoku Prevora nebyl zjištěn vliv na schopnost obsluhovat stroje. Důležité informace o některých složkách přípravku Prevora Tento zubní nátěr může způsobit dočasné podráždění, nebo pálení dásní, rtů nebo jazyka a může také mít hořkou chuť. Chlorhexidin, léčivá látka přípravku Prevora, může také způsobit zbarvení zubů. Pokud je ale chlorhexidin používán místně, jako dočasný nátěr zubů, dochází k zabarvení zubu jen vzácně. 3. JAK LÉČBA PŘÍPRAVKEM PREVORA PROBÍHÁ Místní dočasný nátěr na Vašem chrupu je aplikován Vaším zubním specialistou během krátké návštěvy v zubní ordinaci. Zubní specialista nejdříve očistí Vaše zuby a nanese první vrstvu (1. stupeň) na všechny plochy zubů (Obrázek 1) a okamžitě poté nanese druhý nátěr (2. stupeň). Druhý nátěr dočasně chrání první nátěr před slinami a před obrušováním potravou. Obrázek 1 první vrstva (1. stupeň) s následným druhým nátěrem bude aplikována na Vaše zuby k zamezení rizika zubního kazu. Na počátku léčby přípravkem Prevora bude nutné, aby Vám byl přípravek aplikován 4x, v týdenních intervalech, po kterých bude následovat jedna léčba za 6 měsíců po první aplikaci přípravku. Poté Váš zubní specialista uváží, zda je další podávání přípravku Prevora nutné. Váš zubní lékař Vám řekne že: Zaschlý nátěr Prevora se začne ze zubů stírat během prvního jídla. Po dobu alespoň 4 hodin po ošapliketření zubů se máte vyhýbat tvrdým pokrmům (např. maso, jablka). Po dobu nejméně 24 hodin nemáte žvýkat žvýkačku. Po dobu nejméně 24 hodin si nemáte čistit zuby. Poté si máte začít čistit zuby novým kartáčkem a fluoridovanou zubní pastou 2 až 3 krát denně. Po dobu 3 dnů po ošetření si nemáte si čistit zuby zubní nití Poté máte začít používat zubní nit denně.. Pokud máte zubní protézu, je třeba, abyste pravidelně před použitím čistil(a) a dezinfikoval(a). K dezinfekci se má používat mýdlo a teplá voda. Účinky po ukončení léčby přípravkem Prevora Dočasně můžete pociťovat hořkou chuť, vnímat nátěr na zubech a/nebo pálení podél linie dásní nebo na jazyku. Pálivý pocit může trvat několik minut, nátěr můžete vnímat několik hodin. Nátěr na Vašich 24
19 zubech nebude vidět. Chlorhexidin, léčivá látka přípravku Prevora, může zbarvit zuby, pokud je používán v ústní vodě nebo v gelu. Avšak při používání v kontrolovaných klinických studiích a při používání v zubních ordinacích byly případy, kdy došlo ke zbarvení zubů zubním nátěrem Prevora, vzácné. Pokud zbarvení nastane, není trvalé a lze jej většinou odstranit čištěním zubů běžnou fluoridovanou zubní pastou poté, co si 24 hodin po aplikaci přípravku Prevora znovu začnete čistit zuby. Odborné čištění také odstraní zbarvení, ale pokud je provedeno méně než 7 dnů po zákroku, účinek přípravku Prevora se sníží. Odborné čištění by mělo být provedeno nejméně 7 dnů po aplikaci přípravku Prevora. Co dělat po aplikaci přípravku Prevora Aby nátěr na zubech zůstal co nejdéle, jezte po aplikaci přípravku pouze měkká jídla (např. polévku). Vyhýbejte se tvrdým pokrmům (např. maso, jablka) nejméně po dobu 4 hodin po ošetření zubů.. Nejméně po dobu 24 hodin nežvýkejte žvýkačku. Nejméně po dobu 24 hodin po ošetření zubů si nečistěte zuby. Poté si znovu začněte čistit zuby novým kartáčkem a fluoridovanou zubní pastou 2 až 3 krát denně Nejméně po dobu 3 hodin po ošetření zubů si nečistěte zuby zubní nití.. Poté si čistěte zuby zubní nití každý den. Pokud máte zubní protézu, musíte ji doma pravidelně čistit a dezinfikovat před každým použitím. K dezinfekci používejte mýdlo a teplou vodu. Podrobte se všem ošetřením přípravkem Prevora podle doporučení Vašeho zubaře. Důležitým přínosem k celkovému úspěchu léčby je pravidelné čištění zubů fluoridovanou zubní pastou a omezení příjmu jídla a pití s vysokým obsah cukru a kyselin. Máte-li jakékoli další otázky, týkající se používání tohoto přípravku, zeptejte se svého zubního lékaře. 4. MOŽNÉ NEŽÁDOUCÍ ÚČINKY Podobně jako všechny léky, může mít i přípravek Prevora nežádoucí účinky, které se ale nemusí vyskytnout u každého. Pokud pociťujete přetrvávajíci pálivý pocit na dásních, na rtech, nebo na jazyku, neprodleně navštivte svého zubního lékaře. Pokud jsou Vaše zuby po ošetření roztokem Prevora zbarvené, informujte, prosím, svého zubního lékaře. Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému zubnímu lékaři. 5. JAK PŘÍPRAVEK PREVORA UCHOVÁVAT Uchovávejte mimo dosah a dohled dětí. Přípravek Prevora nepoužívejte po uplynutí doby použitelnosti, uvedené na papírovém vnějším obalu a jednotlivých injekčních lahvičkách (ampulkách) za výrazem EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Po použití zbylý roztok okamžitě zlikvidujte. 25
20 Prevora musí být uchovávaná v chladničce (2ºC - 8ºC) v zubní ordinaci. Léčivé přípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak máte likvidovat přípravky, které již nepotřebujete. Tato opatření pomáhají chránit životní prostředí.. 6. DALŠÍ INFORMACE Co Prevora obsahuje: Chlorhexidinový nátěr -1. vrstva (1.stupeň): 100 mg/ml zubní roztok Léčivou látkou je chlorhexidin-diacetát. Pomocnými látkami jsou: sumaterská benzoová pryskyřice a ethanol Tmelicí nátěr -2. vrstav (2.stupeň): Pomocnými látkami jsou : Methakrylátový kopolymer typ RS PM Triethyl-citrát Jak Prevora vypadá a co obsahuje toto balení: Zubní roztok Chlorhexidinový nátěr je čirý, lehce nahnědlý roztok s patrnou vůní a bez plovoucích částeček. Tmelicí nátěr je mléčně bílá tekutina se slabou vůní. jedna léčebná sada přípravku Prevora 100 mg/ml zubní roztok obsahuje: 6 injekčních lahbiček (ampulek) obsahujících chlorhexidinový nátěr- 1. vrstva (1.stupeň ). Injekční lahvičky mají objem 2ml a jsou ze skla typu 1. 6 injekčních lahbiček (ampulek) obsahujících tmelicí nátěr -2. vrstva (2.stupeň ). Injekční lahvičky mají objem 2ml a jsou ze skla typu 1. Držitel rozhodnutí o registraci a výrobce Držitel rozhodnutí o registraci: CHX Technologies Europe Limited Guinness Enterprise Centre Taylor s Lane Dublin 8, Irsko Tel: (01) Výrobce: United Drug Plc United Drug House Magna Drive, Magna Business Park Citywest Road Dublin 24, Irsko Tel (353) Tato příbalová informace byla schválena v 26
21 Podrobné informace o tomto léčivém přípravku jsou dostupné na webových stránkách 27
PŘÍLOHA I SEZNAM NÁZVŮ, LÉKOVÁ FORMA, SÍLA LÉČIVÉHO PŘÍPRAVKU, CESTA PODÁNÍ, ŽADATEL, DRŽITEL ROZHODNUTÍ O REGISTRACI V ČLENSKÝCH STÁTECH
 PŘÍLOHA I SEZNAM NÁZVŮ, LÉKOVÁ FORMA, SÍLA LÉČIVÉHO PŘÍPRAVKU, CESTA PODÁNÍ, ŽADATEL, DRŽITEL ROZHODNUTÍ O REGISTRACI V ČLENSKÝCH STÁTECH 1 Členský stát EU/EEA Irsko Velká Británie Držitel rozhodnutí o
PŘÍLOHA I SEZNAM NÁZVŮ, LÉKOVÁ FORMA, SÍLA LÉČIVÉHO PŘÍPRAVKU, CESTA PODÁNÍ, ŽADATEL, DRŽITEL ROZHODNUTÍ O REGISTRACI V ČLENSKÝCH STÁTECH 1 Členský stát EU/EEA Irsko Velká Británie Držitel rozhodnutí o
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CAMILIA perorální roztok v jednodávkovém obalu
 sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU Lahev s obsahem 300 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Levetiracetam UCB 100 mg/ml, perorální roztok levetiracetamum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU Lahev s obsahem 300 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Levetiracetam UCB 100 mg/ml, perorální roztok levetiracetamum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
OZNAČENÍ NA OBALU: Fraxiparine Forte 2x0,6 ml
 OZNAČENÍ NA OBALU: Fraxiparine Forte 2x0,6 ml ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fraxiparine forte 0,6 ml Nadroparinum calcicum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Léčivá
OZNAČENÍ NA OBALU: Fraxiparine Forte 2x0,6 ml ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fraxiparine forte 0,6 ml Nadroparinum calcicum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Léčivá
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bronchostop sirup. Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt
 Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls107935/2012
 sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls229950/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls229950/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Mycosten 10 mg/g Shampoo Ciclopiroxum šampon Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls229950/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Mycosten 10 mg/g Shampoo Ciclopiroxum šampon Přečtěte si pozorně celou příbalovou informaci
ZOVIRAX DUO KRÉM 1X2GM Krém
 ZOVIRAX DUO KRÉM 1X2GM Krém Výrobce: GLAXOSMITHKLINE BIOLOGICALS S.A., RIXENSART Značka: ZOVIRAX Charakteristika: Léčivý přípravek Kód výrobku: 229859 Kód EAN:8590335009103 Kód SUKL:0180938 Farmakoterapeutická
ZOVIRAX DUO KRÉM 1X2GM Krém Výrobce: GLAXOSMITHKLINE BIOLOGICALS S.A., RIXENSART Značka: ZOVIRAX Charakteristika: Léčivý přípravek Kód výrobku: 229859 Kód EAN:8590335009103 Kód SUKL:0180938 Farmakoterapeutická
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí trachey (průdušnice)
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
Paracetamol Actavis 250 mg Paracetamol Actavis 500 mg Paracetamol Actavis 1000 mg potahované tablety paracetamolum
 ÚDAJE ÚVÁDĚNÉ NA VNĚJŠÍM A VNITŘNÍM OBALU Krabička na blistry 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Paracetamol Actavis 250 mg Paracetamol Actavis 500 mg Paracetamol Actavis 1000 mg potahované tablety paracetamolum
ÚDAJE ÚVÁDĚNÉ NA VNĚJŠÍM A VNITŘNÍM OBALU Krabička na blistry 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Paracetamol Actavis 250 mg Paracetamol Actavis 500 mg Paracetamol Actavis 1000 mg potahované tablety paracetamolum
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90
 Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro pacienta. ANACID 258 mg/388 mg perorální suspenze. Magnesii hydroxidum, Algeldrati suspensio
 sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
Vnější krabice (obsahující 5 nebo 40 krabiček s lahvičkami se 100 ml infuzního roztoku)
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Vnější krabice (obsahující 5 nebo 40 krabiček s lahvičkami se 100 ml infuzního roztoku) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ciprobay 200 Infuzní roztok ciprofloxacinum 2. OBSAH LÉČIVÉ
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Vnější krabice (obsahující 5 nebo 40 krabiček s lahvičkami se 100 ml infuzního roztoku) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ciprobay 200 Infuzní roztok ciprofloxacinum 2. OBSAH LÉČIVÉ
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU SKLÁDAČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Butamirati citras, guaifenesinum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Butamirati citras 4 mg, guaifenesinum 100 mg
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU SKLÁDAČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Butamirati citras, guaifenesinum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Butamirati citras 4 mg, guaifenesinum 100 mg
Pomocné látky se známým účinkem: prostý sirup 67%, usušená tekutá glukosa.
 sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ
 OZNAČENÍ NA OBALU ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Text na krabičku 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU suspenze Paracetamolum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Paracetamolum 120 mg v 5 ml suspenze 3. SEZNAM
OZNAČENÍ NA OBALU ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Text na krabičku 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU suspenze Paracetamolum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Paracetamolum 120 mg v 5 ml suspenze 3. SEZNAM
Příbalová informace: informace pro pacienta. Corsodyl 1 % gel zubní gel chlorhexidini digluconas
 sp.zn.sukls64237/2015 Příbalová informace: informace pro pacienta Corsodyl 1 % gel zubní gel chlorhexidini digluconas Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.sukls64237/2015 Příbalová informace: informace pro pacienta Corsodyl 1 % gel zubní gel chlorhexidini digluconas Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat,
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU. Kartonová krabice (skleněné/polyethylenové lahve) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabice (skleněné/polyethylenové lahve) 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 1000 ml infuzního roztoku obsahuje: 55,0 g (odpovídá Glucosum 50,0 g) Energetická hodnota
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabice (skleněné/polyethylenové lahve) 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 1000 ml infuzního roztoku obsahuje: 55,0 g (odpovídá Glucosum 50,0 g) Energetická hodnota
Isopropylalkohol, hyprolosa, glyceromakrogol-hydroxystearát, trihydrát octanu sodného, silice máty peprné, levomenthol a čištěná voda.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU CORSODYL 1% GEL Zubní gel Chlorhexidini digluconas 1% 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Chlorhexidini digluconas 1,0 g, odpovídá Chlorhexidini
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU CORSODYL 1% GEL Zubní gel Chlorhexidini digluconas 1% 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Chlorhexidini digluconas 1,0 g, odpovídá Chlorhexidini
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ 7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KARTON 50 x 50 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Voda na injekci Viaflo 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Aqua pro injectione 100% w/v 3. SEZNAM POMOCNÝCH LÁTEK 4. LÉKOVÁ
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KARTON 50 x 50 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Voda na injekci Viaflo 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Aqua pro injectione 100% w/v 3. SEZNAM POMOCNÝCH LÁTEK 4. LÉKOVÁ
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
Příbalová informace: informace pro uživatele. FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
Trihydrát octanu sodného Kyselina octová Chlorid sodný Hydroxid sodný a/nebo kyselina chlorovodíková pro úpravu ph Voda na injekci
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU VAK 250 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Brevibloc 10 mg/ml infuzní roztok Esmololi hydrochloridum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml obsahuje 10 mg esmololi hydrochloridum
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU VAK 250 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Brevibloc 10 mg/ml infuzní roztok Esmololi hydrochloridum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml obsahuje 10 mg esmololi hydrochloridum
Kartonová krabička obsahující injekční lahvičku s práškem, předplněná injekční stříkačka s rozpouštědlem a příslušenství.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabička obsahující injekční lahvičku s práškem, předplněná injekční stříkačka s rozpouštědlem a příslušenství. 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fanhdi 50 IU/ml Fanhdi
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabička obsahující injekční lahvičku s práškem, předplněná injekční stříkačka s rozpouštědlem a příslušenství. 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fanhdi 50 IU/ml Fanhdi
Příbalová informace: informace pro pacienta. Maltofer 50 mg/ml perorální kapky, roztok
 sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Léčivá látka: 100 ml roztoku obsahuje chlorhexidini digluconas 0,2 g, jako chlorhexidini digluconatis solutio 1 ml ve 100 ml roztoku.
 sp.zn. sukls108682/2012 a sp.zn. sukls64237/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Corsodyl 2 mg/ml Roztok pro ústní výplach 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 100 ml roztoku
sp.zn. sukls108682/2012 a sp.zn. sukls64237/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Corsodyl 2 mg/ml Roztok pro ústní výplach 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 100 ml roztoku
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (předplněná injekční stříkačka se zasazenou jehlou) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Metoject 50 mg/ml injekční roztok Methotrexatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (předplněná injekční stříkačka se zasazenou jehlou) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Metoject 50 mg/ml injekční roztok Methotrexatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele. Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum
 sp.zn. sukls154670/2013 Příbalová informace: informace pro uživatele Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls154670/2013 Příbalová informace: informace pro uživatele Loceryl 5% léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU {Krabička na blistry a lahvičky z HDPE } 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Sandoz 60mg Orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tvrdá tobolka obsahuje orlistatum
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU {Krabička na blistry a lahvičky z HDPE } 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Sandoz 60mg Orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tvrdá tobolka obsahuje orlistatum
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum)
 sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls8590/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE BENZOCAIN LIFE PHARMA 8 MG Pastilky (benzocainum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
prášek pro infuzní roztok
 sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
5 ml připravené suspenze obsahuje azithromycinum 200 mg ve formě azithromycinum dihydricum
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 5 ml připravené suspenze obsahuje azithromycinum 200 mg ve formě azithromycinum dihydricum 3. SEZNAM
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 5 ml připravené suspenze obsahuje azithromycinum 200 mg ve formě azithromycinum dihydricum 3. SEZNAM
Příbalová informace: informace pro uživatele. Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum
 sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
Obsahuje monohydrát laktózy. Pro více informací čtěte příbalovou informaci.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička GLYMEXAN 1 mg 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tableta obsahuje glimepiridum1 mg. 3. SEZNAM POMOCNÝCH LÁTEK Obsahuje monohydrát laktózy. Pro více informací
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička GLYMEXAN 1 mg 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tableta obsahuje glimepiridum1 mg. 3. SEZNAM POMOCNÝCH LÁTEK Obsahuje monohydrát laktózy. Pro více informací
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. Maltofer 10 mg/ml sirup
 sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace : Informace pro uživatele. Aknemycin 2000 Mast Erythromycinum
 sp.zn. sukls182807/2012 Příbalová informace : Informace pro uživatele Aknemycin 2000 Mast Erythromycinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls182807/2012 Příbalová informace : Informace pro uživatele Aknemycin 2000 Mast Erythromycinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls71941/2012 a sukls103573/2013, sukls103568/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucidin Mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Natrii fusidas 20,0 mg v 1 g masti.
sp.zn. sukls71941/2012 a sukls103573/2013, sukls103568/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucidin Mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Natrii fusidas 20,0 mg v 1 g masti.
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU, NEBO POKUD NENÍ VNĚJŠÍ OBAL NA VNITŘNÍM OBALU
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU, NEBO POKUD NENÍ VNĚJŠÍ OBAL NA VNITŘNÍM OBALU Papírová krabička; 1 injekční lahvička (2 ml) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml roztoku
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU, NEBO POKUD NENÍ VNĚJŠÍ OBAL NA VNITŘNÍM OBALU Papírová krabička; 1 injekční lahvička (2 ml) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml roztoku
Příbalová informace: informace pro pacienta. Maltofer, 10 mg/ml sirup. polymaltosum ferricum
 sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AMOL. Perorální kapky, roztok (
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AMOL Perorální kapky, roztok ( Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek je dostupný bez lékařského
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AMOL Perorální kapky, roztok ( Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek je dostupný bez lékařského
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU {Krabička pro blistry a HDPE lahvičky} 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Teva 60 mg, tvrdé tobolky Orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tobolka obsahuje
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU {Krabička pro blistry a HDPE lahvičky} 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Teva 60 mg, tvrdé tobolky Orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tobolka obsahuje
Příbalová informace: informace pro pacienta. Corsodyl 2 mg/ml roztok pro ústní výplach chlorhexidini digluconas
 sp.zn. sukls108682/2012 a sp.zn. sukls64237/2015 Příbalová informace: informace pro pacienta Corsodyl 2 mg/ml roztok pro ústní výplach chlorhexidini digluconas Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls108682/2012 a sp.zn. sukls64237/2015 Příbalová informace: informace pro pacienta Corsodyl 2 mg/ml roztok pro ústní výplach chlorhexidini digluconas Přečtěte si pozorně tuto příbalovou informaci
Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Hydroxid sodný, hyetelóza, karbomer, propylenglykol, střední nasycené triacylglyceroly, propylenparaben, methylparaben, čištěná voda.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Diclofenacum natricum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden gram u obsahuje diclofenacum natricum 10 mg (1%). 3. SEZNAM POMOCNÝCH
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Diclofenacum natricum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden gram u obsahuje diclofenacum natricum 10 mg (1%). 3. SEZNAM POMOCNÝCH
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
Jeden ml injekčního roztoku obsahuje granisetronum 1 mg (ve formě hydrochloridu)
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 3 mg/3 ml 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml injekčního roztoku obsahuje granisetronum 1 mg (ve formě hydrochloridu) 3. SEZNAM
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 3 mg/3 ml 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml injekčního roztoku obsahuje granisetronum 1 mg (ve formě hydrochloridu) 3. SEZNAM
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Paracetamol/Guaifenesin/Phenylephrine Hydrochloride Perrigo 500mg/200mg/10mg, prášek pro perorální roztok
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Paracetamol/Guaifenesin/Phenylephrine Hydrochloride Perrigo 500mg/200mg/10mg, prášek pro perorální roztok paracetamolum, guaifenesinum,
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Paracetamol/Guaifenesin/Phenylephrine Hydrochloride Perrigo 500mg/200mg/10mg, prášek pro perorální roztok paracetamolum, guaifenesinum,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls93493/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA BRONCHIPRET TYMIÁN A PRVOSENKA, POTAHOVANÉ TABLETY 160 mg/60 mg Thymi extractum siccum, Primulae extractum siccum Přečtěte si pozorně tuto
Jedna lahvička s práškem také obsahuje arginin, kyselinu fosforečnou 85% a polysorbát 80. Rozpouštědlo: voda na injekci.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (VELIKOST BALENÍ 10 MG) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Actilyse 10 mg Alteplasum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna lahvička obsahuje 10 mg alteplasy (což odpovídá
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (VELIKOST BALENÍ 10 MG) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Actilyse 10 mg Alteplasum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna lahvička obsahuje 10 mg alteplasy (což odpovídá
Příbalová informace: informace pro pacienta. Loceryl 50 mg/ml léčivý lak na nehty amorolfini hydrochloridum
 Sp.zn. sukls73205/2017 Příbalová informace: informace pro pacienta Loceryl 50 mg/ml léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn. sukls73205/2017 Příbalová informace: informace pro pacienta Loceryl 50 mg/ml léčivý lak na nehty amorolfini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
Perorální podání. Před použitím čtěte příbalovou informaci. TEXT NA VNĚJŠÍ OBAL. Krabička pro blistry a lahvičky HDPE 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
 TEXT NA VNĚJŠÍ OBAL Krabička pro blistry a lahvičky HDPE 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Polpharma 60 mg, tvrdé tobolky orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tvrdá tobolka obsahuje
TEXT NA VNĚJŠÍ OBAL Krabička pro blistry a lahvičky HDPE 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Orlistat Polpharma 60 mg, tvrdé tobolky orlistatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna tvrdá tobolka obsahuje
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU. Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Omeprazol Dr.Max 10 mg enterosolventní tvrdé tobolky Omeprazol Dr.Max 20 mg enterosolventní tvrdé tobolky Omeprazol Dr.Max 40 mg enterosolventní
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Omeprazol Dr.Max 10 mg enterosolventní tvrdé tobolky Omeprazol Dr.Max 20 mg enterosolventní tvrdé tobolky Omeprazol Dr.Max 40 mg enterosolventní
Uchovávejte při teplotě do 25 C v dobře uzavřené lahvičce, lahvičku uchovávejte v krabičce, aby byl přípravek chráněn před světlem a vlhkostí.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička (lahvička) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibalgin 400 potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Ibuprofenum 400 mg v 1 potahované tabletě.
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička (lahvička) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibalgin 400 potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Ibuprofenum 400 mg v 1 potahované tabletě.
Softa-Man Kožní roztok
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM A VNITŘNÍM OBALU Karton/ Polyethylenové lahve / kanystr 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Softa-Man Kožní roztok 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Složení: 100 ml roztoku obsahuje:
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM A VNITŘNÍM OBALU Karton/ Polyethylenové lahve / kanystr 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Softa-Man Kožní roztok 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Složení: 100 ml roztoku obsahuje:
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obaly na tablety se 400 mg potahovanými tabletami 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna potahovaná tableta obsahuje 400 mg. 3. SEZNAM POMOCNÝCH LÁTEK 4. LÉKOVÁ FORMA
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obaly na tablety se 400 mg potahovanými tabletami 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna potahovaná tableta obsahuje 400 mg. 3. SEZNAM POMOCNÝCH LÁTEK 4. LÉKOVÁ FORMA
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obal na tablety se 400 mg potahovanými tabletami 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibuprofen Dr.Max 400 mg potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obal na tablety se 400 mg potahovanými tabletami 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibuprofen Dr.Max 400 mg potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. Perioxept 1,2 mg/ml roztok pro ústní výplach Léčivá látka: chlorhexidini digluconas
 Sp. zn. sukls9983/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Perioxept 1,2 mg/ml roztok pro ústní výplach Léčivá látka: chlorhexidini digluconas Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp. zn. sukls9983/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Perioxept 1,2 mg/ml roztok pro ústní výplach Léčivá látka: chlorhexidini digluconas Přečtěte si pozorně tuto příbalovou informaci dříve,
Propofol MCT Fresenius 10 mg/ml: Jeden ml obsahuje propofolum 10 mg. Propofol MCT Fresenius 20 mg/ml: Jeden ml obsahuje propofolum 20 mg.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU 1x 50 ml předplněná injekční stříkačka 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Propofol MCT Fresenius 10 mg/ml injekční/infuzní emulze v předplněné injekční stříkačce Propofol MCT Fresenius
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU 1x 50 ml předplněná injekční stříkačka 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Propofol MCT Fresenius 10 mg/ml injekční/infuzní emulze v předplněné injekční stříkačce Propofol MCT Fresenius
Příbalová informace: informace pro pacienta. Septabene 1,5 mg/ml + 5,0 mg/ml orální sprej, roztok benzydamini hydrochloridum/cetylpyridinii chloridum
 Sp. zn. sukls56216/2014 Příbalová informace: informace pro pacienta Septabene 1,5 mg/ml + 5,0 mg/ml orální sprej, roztok benzydamini hydrochloridum/cetylpyridinii chloridum Přečtěte si pozorně tuto příbalovou
Sp. zn. sukls56216/2014 Příbalová informace: informace pro pacienta Septabene 1,5 mg/ml + 5,0 mg/ml orální sprej, roztok benzydamini hydrochloridum/cetylpyridinii chloridum Přečtěte si pozorně tuto příbalovou
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU APIGUARD gel (25% Thymolum) pro podání ve včelím úlu Vyhrazený veterinární léčivý přípravek 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU APIGUARD gel (25% Thymolum) pro podání ve včelím úlu Vyhrazený veterinární léčivý přípravek 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příbalová informace: informace pro uživatele. VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa
 Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Příbalová informace: Informace pro uživatele. Strepsils Plus Spray orální sprej dichlorbenzenmethanolum, amylmetacresolum, lidocainum
 sp.zn.sukls188553/2013 Příbalová informace: Informace pro uživatele Strepsils Plus Spray orální sprej dichlorbenzenmethanolum, amylmetacresolum, lidocainum Přečtěte si pozorně tuto příbalovou informaci
sp.zn.sukls188553/2013 Příbalová informace: Informace pro uživatele Strepsils Plus Spray orální sprej dichlorbenzenmethanolum, amylmetacresolum, lidocainum Přečtěte si pozorně tuto příbalovou informaci
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
Příbalová informace: informace pro uživatele. Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F)
 sp.zn. sukls298615/2018 Příbalová informace: informace pro uživatele Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F) Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls298615/2018 Příbalová informace: informace pro uživatele Fluorid (18F) sodný RadioMedic 1 10 GBq injekční roztok Natrii fluoridum ( 18 F) Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU. APIGUARD gel (25% Thymolum) pro podání ve včelím úlu
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU APIGUARD gel (25% Thymolum) pro podání ve včelím úlu Vyhrazený veterinární léčivý přípravek 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Thymolum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU APIGUARD gel (25% Thymolum) pro podání ve včelím úlu Vyhrazený veterinární léčivý přípravek 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Thymolum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KARTONOVÁ KRABICE 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna transdermální náplast 5 cm 2 o obsahu rivastigminum 9 mg, ze které se uvolní 4,6
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KARTONOVÁ KRABICE 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna transdermální náplast 5 cm 2 o obsahu rivastigminum 9 mg, ze které se uvolní 4,6
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Skleněná lahvička vnitřní obal 20 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Iodixanolum 2. OBSAH LÉČIVÉ LÁTKY 20 ml = 6,4 g I 1 ml injekčního roztoku obsahuje: Iodixanolum 652 mg (odp.
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Skleněná lahvička vnitřní obal 20 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Iodixanolum 2. OBSAH LÉČIVÉ LÁTKY 20 ml = 6,4 g I 1 ml injekčního roztoku obsahuje: Iodixanolum 652 mg (odp.
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU. BALENÍ 30 mg/ 5 ml
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU BALENÍ 30 mg/ 5 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÁTEK Jedna 5 ml lahvička obsahuje 30 mg 3. SEZNAM POMOCNÝCH LÁTEK Také obsahuje: Glyceromakrogol-ricinoleát
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU BALENÍ 30 mg/ 5 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÁTEK Jedna 5 ml lahvička obsahuje 30 mg 3. SEZNAM POMOCNÝCH LÁTEK Také obsahuje: Glyceromakrogol-ricinoleát
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Locatim perorální roztok pro novorozená telata mladší než 12 hodin 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Bovinní
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Locatim perorální roztok pro novorozená telata mladší než 12 hodin 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Bovinní
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. fentikonazoli nitras
 sp.zn.sukls33807/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Lomexin 20 mg/g vaginální krém fentikonazoli nitras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls33807/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Lomexin 20 mg/g vaginální krém fentikonazoli nitras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 1 potahovaná tableta obsahuje: bromelaina 90 mg (odp.: 450 F.I.P.-j.) trypsinum 48 mg (odp.: 24 µkat) rutosidum trihydricum
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 1 potahovaná tableta obsahuje: bromelaina 90 mg (odp.: 450 F.I.P.-j.) trypsinum 48 mg (odp.: 24 µkat) rutosidum trihydricum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Sp.zn.sukls265114/2016 a sp.zn.sukls274542/2016
 Sp.zn.sukls265114/2016 a sp.zn.sukls274542/2016 Příbalová informace: informace pro pacienta Ajax pomeranč a med 3 mg pastilky benzydamini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls265114/2016 a sp.zn.sukls274542/2016 Příbalová informace: informace pro pacienta Ajax pomeranč a med 3 mg pastilky benzydamini hydrochloridum Přečtěte si pozorně tuto příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Fludeoxyglucose (18F) Biont 200 1300 MBq/ml injekční roztok FLUDEOXYGLUCOSUM ( 18 F)
 Sp.zn. sukls117503/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Fludeoxyglucose (18F) Biont 200 1300 MBq/ml injekční roztok FLUDEOXYGLUCOSUM ( 18 F) Přečtěte si pozorně celou příbalovou informaci
Sp.zn. sukls117503/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Fludeoxyglucose (18F) Biont 200 1300 MBq/ml injekční roztok FLUDEOXYGLUCOSUM ( 18 F) Přečtěte si pozorně celou příbalovou informaci
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
1. Co je přípravek Maltofer Fol žvýkací tablety a k čemu se používá. Maltofer Fol se používá k léčbě a prevenci nedostatku železa v organismu.
 sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
sp.zn. sukls238178/2016 Příbalová informace: Informace pro uživatele Maltofer Fol tablety 100 mg / 0,35 mg, žvýkací tablety železo ve formě polymaltosum ferricum / kyselina listová Přečtěte si pozorně
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA Pro dospělé a dospívající od 14 let 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna šumivá tableta obsahuje acetylcysteinum 600 mg. 3. SEZNAM POMOCNÝCH LÁTEK Obsahuje
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA Pro dospělé a dospívající od 14 let 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna šumivá tableta obsahuje acetylcysteinum 600 mg. 3. SEZNAM POMOCNÝCH LÁTEK Obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
Příbalová informace: informace pro pacienta. Septabene 3 mg/1 mg pastilky benzydamini hydrochloridum/cetylpyridinii chloridum
 Sp.zn.sukls62712/2018 Příbalová informace: informace pro pacienta Septabene 3 mg/1 mg pastilky benzydamini hydrochloridum/cetylpyridinii chloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než
Sp.zn.sukls62712/2018 Příbalová informace: informace pro pacienta Septabene 3 mg/1 mg pastilky benzydamini hydrochloridum/cetylpyridinii chloridum Přečtěte si pozorně tuto příbalovou informaci dříve, než
Příloha č.1 k rozhodnutí o změně registrace sp.zn.sukls28549/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č.1 k rozhodnutí o změně registrace sp.zn.sukls28549/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DICLOFENAC GALMED EMULGEL Diclofenacum natricum Přečtěte si pozorně tuto příbalovou informaci,
Příloha č.1 k rozhodnutí o změně registrace sp.zn.sukls28549/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DICLOFENAC GALMED EMULGEL Diclofenacum natricum Přečtěte si pozorně tuto příbalovou informaci,
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Algogesic 12,5 mikrogramů/h Algogesic 25 mikrogramů/h Algogesic 50 mikrogramů/h Algogesic 75 mikrogramů/h Algogesic 100 mikrogramů/h
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Algogesic 12,5 mikrogramů/h Algogesic 25 mikrogramů/h Algogesic 50 mikrogramů/h Algogesic 75 mikrogramů/h Algogesic 100 mikrogramů/h
Léčivá látka: 1 g masti obsahuje collagenasum 0,48-3,00 mg (to odp.. collagenasum 1,2 I.U a. proteasum 0,24 I.U)
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU IRUXOL Mono mast Collagenasum 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: 1 g masti obsahuje collagenasum 0,48-3,00 mg (to odp.. collagenasum
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU IRUXOL Mono mast Collagenasum 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: 1 g masti obsahuje collagenasum 0,48-3,00 mg (to odp.. collagenasum
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Kytril inj/inf koncentrát pro přípravu injekčního nebo infuzního roztoku Granisetroni hydrochloridum
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls211402/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kytril inj/inf koncentrát pro přípravu injekčního nebo infuzního roztoku Granisetroni hydrochloridum
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls211402/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kytril inj/inf koncentrát pro přípravu injekčního nebo infuzního roztoku Granisetroni hydrochloridum
Fluimucil 100 Fluimucil 200 Granule pro přípravu perorálního roztoku Fluimucil 600 Šumivé tablety. (Acetylcysteinum)
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Fluimucil 100 Fluimucil 200 Granule pro přípravu perorálního roztoku Fluimucil 600 Šumivé tablety (Acetylcysteinum) Přečtěte si pozorně tuto příbalovou informaci,
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Fluimucil 100 Fluimucil 200 Granule pro přípravu perorálního roztoku Fluimucil 600 Šumivé tablety (Acetylcysteinum) Přečtěte si pozorně tuto příbalovou informaci,
