Rozhodnutí nabylo právní moci dne 20. února ODESÍLATEL: ADRESÁT:
|
|
|
- Drahomíra Musilová
- před 6 lety
- Počet zobrazení:
Transkript
1 Rozhodnutí nabylo právní moci dne 20. února ODESÍLATEL: Ing. Karel Bláha, CSc. ředitel odboru environmentálních rizik a ekologických škod Ministerstvo životního prostředí Vršovická Praha 10 ADRESÁT: Vážený pan prof. MUDr. Petr Cetkovský, Ph.D., MBA ředitel ÚHKT Ústav hematologie a krevní transfuze U Nemocnice Praha 2 V Praze dne Č.j.: Vyřizuje: Tel.: 29. ledna 2018 MZP/2017/750/1213 Ing. Routa R o z h o d n u t í Ministerstvo životního prostředí jako správní úřad příslušný podle 5 zákona č. 78/2004 Sb., o nakládání s geneticky modifikovanými organismy a genetickými produkty, ve znění pozdějších předpisů, (dále jen zákon ) a 10 zákona č. 500/2004 Sb., správní řád, ve znění pozdějších předpisů, r o z h o d l o podle 5 odst. 8 zákona ve věci žádosti Ústavu hematologie a krevní transfuze, se sídlem U Nemocnice 1, Praha 2, IČ: , o udělení povolení k uvádění geneticky modifikovaného organismu (dále jen GMO ) do životního prostředí pro účely klinického hodnocení léčivého přípravku CART19 (projekt Ověření bezpečnosti CART19 buněk vyrobených pomocí transpozonu piggybac pro terapii lymfoidních malignit) takto: Ústavu hematologie a krevní transfuze U Nemocnice 1, Praha 2 s e u děluje povolení k uvádění GMO do životního prostředí pro účely klinického hodnocení léčivého přípravku CART19.
2 Náležitosti povolení podle 18 odst. 6 zákona: Oprávněná osoba Název: Ústav hematologie a krevní transfuze, U Nemocnice 1, Praha 2 IČ: Specifikace geneticky modifikovaného organismu Léčivý přípravek obsahuje geneticky modifikované T lymfocyty - CART19 (linie primárních lidských lymfocytů T), které produkují chimerický antigení receptor specifický pro antigen CD19. CART19 se připraví ex vivo z lymfocytů izolovaných z periferní krve vnesením genu CAR19 prostřednictvím transposonového vektoru piggybac. Lymfocyty CART19 budou před aplikací pacientům připravovány v laboratoři ÚHKT v rámci uzavřeného nakládání. Specifikace genetické modifikace Typ genetické modifikace je vnesení cizorodého dědičného materiálu. Stabilita vloženého dědičného materiálu a stabilita jeho umístění - insert se integruje trvale do genomu buňky, neodchází k jeho uvolňování do prostředí. Dárcovský organismus je: člověk (Homo sapiens), myš domácí (Mus musculus), tur domácí (Bos taurus), kovolesklec cizokrajný (Trichoplusia ni). Výsledky hodnocení rizika Údaje o vektoru Terapeutický vektor je transposon piggybac, který exprimuje transgen CAR19. Do organismu příjemce se vnáší ex vivo do lymfocytů ve formě holé plasmidové DNA prostřednictvím fyzikálního postupu elektroporace. Tento transgen se integruje do hostitelské DNA prostřednictvím aktivity genu pbase, který exprimuje hyperaktivní transponasu piggybac. Gen CAR19 je obsažen v plasmidu PB19 a gen HyPBase v plasmidu PBASE. Tyto plasmidy se vnášejí současně pomocí elektroporace do lymfocytů. Transponasa HyPBase integruje do genomu hostitelské buňky náhodným způsobem sekvence z plasmidu PB19 ohraničenou raménky 3 arm a 5 arm, která obsahuje DNA sekvence kódující ubiquitinový promotor (UbC), CAR19 a bgh poly A (bovine growth hormone polyadenylation signal). Plasmid PBASE se neintegruje do genomu a HyPBase je exprimována pouze přechodně. Vektory PB19 a PBASE jsou specifické přítomností genu aph(3')-ia (aminoglycoside phosphotransferase) odpovědného za rezistenci na kanamycin. 2/12
3 Vektor obsahuje jenom známé sekvence, exprese z genů je limitovaná pouze na produkty genů CAR19 a HyPbase. Metody a kritéria použitá pro selekci - produkt genu CAR19 vede k expresi chimerického receptoru CAR19 na povrchu T lymfocytu, což způsobí selektivní expanzi modifikovaných T lymfocytů během in vitro kultivace v důsledku stimulace T lymfocytů prostřednictvím CAR19. Údaje o insertu 1/ 5' arm 339 bp - 5' arm nekódující sekvence je specificky rozpoznána HyPbase během integrace do DNA. Pochází z organismu Trichoplusia ni. 2/ UbC promotor 1231 bp - UbC promotor- nekódující sekvence, jež umožňuje expresi genu CAR19 po integraci do genomu, jedná se o lidskou DNA sekvenci. 3/ CAR bp - CAR19 sekvence kóduje chimerický antigenní receptor, což je povrchový receptor rozpoznávající antigen CD19 na povrchu B-lymfocytů. Část (771 bp) je odvozena z myší protilátky (Mus musculus) specifické na antigen CD19. Zbylé sekvence jsou lidské. 4/ bgh poly(a) signal 237 bp - bgh nekódující poly(a) signalizační sekvence umožňující tvorbu funkční mrna kódující CAR19. Sekvence pochází z Bos taurus. 5/ 3' arm 261 bp - 3' arm nekódující sekvence je specificky rozpoznána HyPbase během integrace do DNA. Pochází z organismu Trichoplusia ni. Inzert je náhodně integrován do genomu buňky, preferenčně se integruje do tzv. otevřeného chromatinu, který obsahuje transkripčně aktivní sekvence. Insert neobsahuje části, jejichž produkty nebo funkce nejsou známé. Počet kopií insertu je v rozmezí 1-10/kopií na buňku, počet kopií nemá vliv na funkčnost CART19 lymfocytů pokud vede k účinné expresi detekovatelné na proteinové úrovni. Léčebným postupem je ex vivo genová terapie. Pacienti s CD19-pozitivní akutní lymfoblastovou leukemií nebo non-hodgkinským lymfomem podstoupí infúzi autologních CART19 lymfocytů připravených ex vivo. Infuzí podané CART19 rozpoznají prostřednictvím produktu transgenu CAR19 nádorové buňky, což povede k eliminaci nebo významné redukci nádorového postižení. Stejný GMO nebyl dosud použit v klinickém hodnocení, protože se jedná o zcela nový a originální léčivý přípravek vyvinutý v ÚHKT. Existují však podobné GMO, které byly aplikovány pacientům v mnoha klinických studiích. CART19 připravené pomocí genové manipulace lentiviry byly v roce 2017 schváleny v USA pro terapii B- ALL a do současnosti byly aplikovány řádově stovkám pacientů. V současnosti probíhá několik klinických studií s CAR19 T lymfocty připravenými pomocí 3/12
4 transposonu SleepingBeauty, jehož charakteristiky a mechanismus účinku jsou velmi podobné transposonu piggybac. Transposon piggybac je v současnosti testován v klinickém hodnocení, v kterém se ověřuje účinnost CAR T lymfocytů specifických na antigen BCMA u pacientů s mnohočetným myelomem. Dostupná preklinická data ukazují, že transposon piggybac má analogická rizika jako transposon Sleeping Beauty, obecně se genová modifikace pomocí transposonů považuje za bezpečnější než modifikace pomocí lentivirů nebo retrovirů a transposony tak jsou považovány za nejbezpečnější vektory pro genovou terapii. Výsledný GMO CART19: podstatou rizika je 1/ patogenní efekt na B lymfocyty, potenciálním škodlivým účinkem může být deplece B lymfocytů a 2/ přenos maligních buněk do lidského organizmu, potenciálním škodlivým účinkem může být vznik nádoru z přenesených buněk. Při transferu genů do buněk, ale i v důsledku expanze CART19 buněk in vitro může v důsledku narušení stability genomu dojít k jejich maligní transformaci. Přesný mechanizmus a příčinu lze těžko zjistit, avšak pokud by takovéto buňky vznikly a byly neúmyslně přeneseny jinému příjemci (člověk nebo zvíře), tak by byly beze zbytku eliminovány jeho imunitním systémem. Pravděpodobnost vzniku nádorů z přenesených buněk je u cizorodého organizmu velmi nízká, riziko škodlivého účinku je velmi nízké, pravděpodobnost maligní transformace diferencovaných CART19 buněk je nízká a riziko vzniku nádorů u pacientů je nízké. Vektor: podstatou rizika je u plasmidů ppb19 (eukaryotický expresní vektor) a ppbase (eukaryotický expresní vektor) možný přenos genu pro (aph(3')-ia) do bakterií, potenciálním škodlivým účinkem může být ztráta citlivosti bakterií k antibiotiku. Plazmidy nesou gen (aph(3')-ia) pro rezistenci na kanamycin. Gen (aph(3')-ia) je v plasmidu regulován pouze bakteriálním promotorem, při genové modifikaci CART19 buněk není selekčním markerem, díky čemuž je jeho integrace do genomu T buněk velmi málo pravděpodobná. Kanamycin se pro svou toxicitu nepoužívá pro léčbu systémových infekcí u lidí, a proto je to vhodný selekční marker pro přípravu vektorů pro genovou terapii. Pravděpodobnost vzniku bakterií rezistentních na kanamycin přenesením genu (aph(3')-ia) z použitých plasmidů je velmi nízká. Riziko škodlivého účinku není žádné. Vkládaný gen: podstatou rizika u genu HyPBase (gen pro hyperaktivní transponasu) může být potenciální škodlivý účinek, který se projeví jako mutagenní efekt a u genu CAR19 může nastat horizontální přenos genů do jiných organizmů, jehož potenciálním škodlivým účinkem může být deplece B lymfocytů. Gen CAR19 bude ve výsledném GMO stabilně integrován do genomu. Pokud by v buňkách byl přítomen protein s PB transponázovou aktivitou, mohlo by dojít k vyštěpení vloženého genu CAR19. Transposonový systém PB je unikátní v tom, že provádí přesnou excisi inzertu, po kterém nezůstávají v genomové sekvenci žádné stopy, což je výhodné z hlediska bezpečnosti. Vyštěpená rekombinantní sekvence CAR19 sama o sobě 4/12
5 nemá integrační potenciál. Pravděpodobnost přenosu CAR19 do jiných organizmů je proto velmi nízká. Riziko ovlivnění diverzity je velmi nízké. Pravděpodobnost přenosu genu HyPBase do jiných organizmů velmi nízká. Riziko ovlivnění diverzity je velmi nízké. CART19 se nešíří do životního prostředí, nepřežívají vně organismus pacienta, neinteragují s organismy v životním prostředí, možnost prudkého nárůstu populace GMO v životním prostředí je velmi nízká, pravděpodobnost přenosu CART19 po vertikální linii (in vivo) je velmi nízká. Pravděpodobnost imunosuprese v důsledku neúmyslného přenosu CART19 buněk je u cizorodého organizmu velmi nízká. Riziko škodlivého účinku je velmi nízké. Pravděpodobnost, že dojde k selekci po uvedení do životního prostředí, je velmi nízká, možnost přenosu dědičného materiálu z GMO do jiného organismu po uvedení do životního prostředí je velmi nízká Možnost přenosu dědičného materiálu z přirozeně se vyskytujícího organismu do GMO po uvedení do životního prostředí a důsledky takového přenosu - tato pravděpodobnost je velmi nízká Další možné účinky na životní prostředí a biologickou rozmanitost nejsou známy. Shrnutí hodnocení rizika - riziko spojené s nakládáním s CART19 buňkami v rámci klinické studie je nízké. Podmínky nakládání Nakládat s výše uvedeným GMO lze jen způsobem popsaným v žádosti č.j. MZP/2017/750/1213 doručené na MŽP dne 14. listopadu 2017, při dodržování všech uvedených podmínek, zejména: - veškerá manipulace s geneticky modifikovaným materiálem bude probíhat za kontrolovaných podmínek minimalizujících nebo vylučujících únik transgenů do okolního prostředí, - experimentální práce jsou navrženy a prováděny tak, aby riziko šíření GMO bylo minimalizováno, - před uváděním do životního prostředí bude uvedený GMO CART19 připraven v laboratoři ÚHKT, v izolátoru v místnosti B376. Oznámení o uzavřeném nákládání s CART19 jako s GMO 1. kategorie je registrováno na MŽP pod č.j /ENV/15 (GMO nebude dovážen ani vyvážen). Připravené CART19 budou uskladněny v kryoskladu v místnosti B326 v uzavřených obalech a řádně označeny, - uzavřené nakládání v prvé fázi klinické studie bude probíhat v uzavřené místnosti J05, budova B 2.NP. Místnost je uzavřená s oddělenou vzduchotechnikou. Při 5/12
6 transportu GMO uvnitř ÚHKT musí být materiál neustále pod dozorem odpovědného pracovníka. Musí být neprodyšně uzavřen v plastových nebo plechových obalech s víkem se značkou Biohazard, - prostory Jednotky intenzivní péče a místnosti J05 jsou uzavřené, oddělené od okolního prostředí vzduchovými filtry. Dveře místnosti J05, kde se nakládá s GMO, jsou uzamčeny a označeny značkou "BIOHAZARD" s uvedením kategorie rizika, - přeprava léčivého přípravku CART19 z výrobních prostor do skladovacích prostor a ze skladovacích prostor do aplikačních prostor se provádí v uzavřeném kontejneru označeném GMO. Všechny prostory, kde se nachází GMO, jsou v ÚHKT v budově B. CART19 se nebudou přepravovat mimo budovu B, ÚHKT, - první vyhodnocení klinické studie bude za 1 rok po jejím zahájení, dále každý rok po dobu života pacientů léčených CART19, - všichni zúčastnění zaměstnanci a pracovníci jednotky intenzivní péče budou proškoleni bezprostředně před zahájením klinické studie. Školení probíhá jednou ročně. Stávající pracovníci byli pro práci s GMO 1. kategorie proškoleni. Záznam o tomto proškolení je zakládán, - na pracoviště je zakázán vstup osobám mladším 18 let, - CART19 se aplikují pacientům s CD19-pozitivní akutní lymfoblastovou leukemií nebo Non-Hodgkinským lymfomem, kteří budou splňovat vstupní kritéria pro klinické hodnocení, během léčby nedochází k uvolňování CART19 do okolního prostředí, což je kontrolováno prostřednictvím PCR detekce specifických sekvencí, - pacienti budou trvale sledováni v ÚHKT. Pacienti nebudou vyřazeni z klinického hodnocení, budou sledováni po celou dobu jejich života a bude se opakovaně provádět stanovení přítomnosti CART19 v jejich organismu, - po aplikaci CART19 budou pacienti sledováni na jednotce intenzívní péče (JIP) a bude monitorováno uvolňování GMO do okolního prostředí z biologických sekretů (moč, stolice, sliny) a bude sledována přítomnosti CART19 v periferní krvi, - metody detekce a identifikace jsou založené na průkazu specifických DNA sekvencí pro CART19 pomocí kvantitativní PCR (qpcr) v kombinaci s detekcí produktu pomocí hydrolyzační próby (systém TaqMan), - základní metoda detekce přítomnosti lidských CART19 buněk spočívá v izolaci jejich DNA. Následuje PCR amplifikace transgenu pomocí specifických oligonukleotidů. Získaný DNA fragment se ztotožní s transgenem podle velikosti, 6/12
7 zjištěné na gelu po elektroforéze. Metoda detekce pro testování přítomnosti DNA sekvencí specifických pro CART19 bude qpcr. Z krve pacientů se bude provádět testování na přítomnosti CART19 buněk pomocí průtokové cytometrie. Tyto testy se budou provádět každý den po dobu 7 dnů po aplikaci, následně budou pacienti propuštěni do domácí péče a sledováni ambulantně cca 1x týdně po dobu 1 měsíce a následně 1x každý měsíc trvale. O každé kontrole bude prováděn zápis, - vzorky pro identifikaci DNA budou odebírány do odběrových zkumavek s fixačním médiem RNAlater pro stanovení DNA a do zkumavky s fixačním médiem TransFix. Po fixaci vzorků, kdy dojde k usmrcení GMO, bude s materiálem zacházeno jako s non-gmo, - citlivost detekce je na úrovni 100 kopií/ml vzorku se spolehlivostí 90%, při >1000 kopií/ml je spolehlivost detekce 100%, specifita detekce je 100%, - techniky (metody) detekce přenosu vloženého dědičného materiálu na další organismy není nutné provádět, - metody zjišťování účinků GMO na necílové organismy není nutné provádět, - kdyby došlo k uvolnění CART19 z organismu pacientů po aplikaci, tak bariérová opatření zabrání rozšíření mimo určené prostory. CART19 nemohou přežívat mimo organismus pacienta a nemohou se tedy rozšířit do životního prostředí. Při úniku GMO bude prováděna dekontaminace desinfekčními prostředky dle havarijního plánu, - v klinickém hodnocení se od roku 2018 plánuje léčba 12 pacientů. Dávka bude podána v eskalačním režimu, nejprve se podá 1x10e6 CART19 buněk, při nepřítomnosti nežádoucích účinkú se za 1 měsíc podá 1x10e7 a opět při nepřítomnosti nežádoucích účinků se za 1 měsíc podá 1x10e7 CART19 buněk. Cekem tedy každý pacient dostane maximálně 3 dávky v celkovém množství cca 1x10e7 CART19 buněk, - vstup do pacientského pokoje bude umožněn pouze určeným osobám (zdravotnický personál, rodinní příslušníci), - osoby, která budou v bezprostředním kontaktu s pacientem během hospitalizace v ÚHKT, budou používat jednorázové ochranné prostředky (plášť, ústenka, rukavice). Pacient bude trvale vyloučen z dárcovství krve a tkání, - pracovníci mají povinnost používat v prostorách pro práci s GMO jednorázové ochranné prostředky, které nepoužívají mimo úsek GMO. Oděvy a prádlo pacientů se musí po použití autoklávovat, 7/12
8 - při práci s GMO jsou pracovníci povinni dodržovat postupy uvedené v provozním řádu, pracovníci musí být také poučeni, kde se nachází hlavní uzávěr vody, plynů a hlavní elektrický jistič, - pracovníci údržby jsou povinni při údržbářských pracích v prostorách pro práci s GMO používat pláště pro práci s rekombinovanou DNA, které není možno používat mimo pracoviště pro GMO. Jsou povinni dbát pokynů vedoucího pracoviště, v jehož prostorách údržbu provádějí, - veškerý odpad (CART19 atd.) a použité lékařské prostředky budou umístěny do kontejnerů pro infekční odpad označených BIOHAZARD a autoklávovány (121 o C/20 min.) v prostorách budovy B v ÚHKT, následně budou zlikvidovány jako nebezpečný odpad kat. č (Odpady, na jejichž sběr a odstraňování jsou kladeny zvláštní požadavky s ohledem na prevenci infekce) dle vyhlášky č. 381/2001 Sb. zákona 185/2001 Sb. o odpadech, likvidovány specializovanou firmou EKOM CZ a.s., Průmyslová 1472/11, Praha 10, IČO Inaktivované odpady jsou netoxické. Použité diagnostické přístroje, zařízení a nástroje budou po použití dekontaminovány dle platného SOP, budou desinfikovány 2% roztokem Sekusept po dobu 30 min, - během výroby CART19 pro jednoho pacienta vznikne cca 1l tekutých i tuhých odpadů, které se zlikvidují autoklávováním 121 o C/20min, - po každém skončení práce s GMO se provede sanitace prostoru. Kontrolu prostoru provádí pravidelně pracovník zodpovědný za nakládání s GMO. Do zvláštního sešitu se zapisují záznamy o prováděné sanitaci. Zodpovědní pracovníci vedou protokoly o skladování a manipulaci s preparáty obsahujícími GMO a též o haváriích a jejich likvidaci, - asanační prostředky použitelné k likvidaci GMO a dekontaminaci zasaženého prostoru jsou roztok chlornanu sodného (2-10% Savo), 2% roztok Sekusept, 1% Incidur nebo 2% chloramin B. Jsou místěny v označených skříních umístěných v prostorách pro práci s GMO - místnost J05, budova B, - zařízení a nástroje budou desinfikovány 2% roztokem Sekusept, 1% Incidur, 2-10% Savo nebo 2% chloramin T, - o všech manipulacích s GMO se provádí záznam do pracovního protokolu. Podrobné protokoly o práci s GMO povedou jednotliví proškolení pracovníci na oddělení imunoterapie, budova B, ÚHKT, - v prostorech určených pro práci s GMO a vybavených okny je zakázáno větrat (aby došlo k vyloučení přenašečů GMO, např. hmyzu a hlodavců) a cirkulace vzduchu je zajišťována výhradně pomocí vzduchotechniky. 8/12
9 Veškerý kontaminovaný materiál je desinfikován a likvidován jako infekční materiál (chemická desinfekce, autokláv). Další podmínky nakládání stanovené podle 5 odst. 10 zákona - Ústav hematologie a krevní transfuze, se sídlem U Nemocnice 1, Praha 2, musí v souladu s 19 písm. c) zákona každoročně předat ministerstvu v listinné a elektronické podobě vždy k 15. únoru kalendářního roku přehled GMO, údaje o jejich množství, o způsobu nakládání s nimi a vyjádření k přezkoumání hodnocení rizika za uplynulý kalendářní rok a v souladu s 19 písm. d) zákona zaslat do 60 dnů od ukončení nakládání s GMO závěrečnou zprávu o průběhu, důsledcích této činnosti, zejména s ohledem na rizika ohrožení zdraví a životního prostředí. - Ústav hematologie a krevní transfuze, se sídlem U Nemocnice 1, Praha 2, musí v souladu s 19 písm. h) zákona poskytnout správním orgánům (Ministerstvo životního prostředí, ČIŽP) podle 28 a 31 až 33 součinnost při kontrole prostorů a zařízení určených k nakládání s GMO nebo prostorů a zařízení, v nichž k tomuto nakládání dochází nebo může docházet, včetně poskytnutí písemností a kdykoliv v průběhu nakládání strpění bezúplatného odebírání vzorků pro kontrolní účely. Účel nakládání CART19 se aplikují pacientům s CD19-pozitivní akutní lymfoblastovou leukemií nebo non-hodgkinským lymfomem v uzavřených prostorách Jednotky intenzívní péče (JIP) Ústavu Hematologie a Krevní Transfúze. Zamýšleným výsledkem genetické modifikace je integrace genu CAR19 do genomu buňky. Cílem studie je ex vivo genová terapie. Pacienti s CD19-pozitivní akutní lymfoblastovou leukemií nebo non-hodgkinským lymfomem podstoupí infúzi autologních CART19 lymfocytů připravených ex vivo. Infuzí podané CART19 rozpoznají prostřednictvím produktu transgenu CAR19 nádorové buňky, což povede k eliminaci nebo významné redukci nádorového postižení. Další požadavky na označení Pro nakládání s GMO platí obecné podmínky označování, které jsou dány zákonem. Místo uzavřeného nakládání Ústav hematologie a krevní transfuze, U nemocnice 1, Praha 2 plánuje uvádění GMO do životního prostředí (infúze CART19) v budově B, ve 2. NP, v místnosti J05 na Jednotce intenzívní péče. Příprava CART19 bude v rámci 9/12
10 uzavřeného nakládání realizována na stejném pracovišti v laboratoři ÚHKT, v izolátoru v místnosti B376. Požadavky na monitoring a podávání zpráv o jeho výsledcích Během klinického hodnocení se bude pravidelně monitorovat přítomnost DNA sekvencí specifických pro CAR19 z biologických vzorků (moč, krev, stolice, sliny) získaných od pacientů. Získaná data budou zaznamenávána. Řádné plánované kontroly jsou prováděny odpovědnou osobou (či osobou jí pověřenou) a zahrnují celkovou kontrolu prostoru (výrobní prostory a transplantační oddělení ÚHKT) a kontrolu dodržování provozního řádu a havarijního plánu. Monitoring bude prováděn 1x měsíčně po celou dobu výroby CART19 a během hospitalizace pacientů léčených CART19. Všechny projevy jakýchkoliv nežádoucích účinků a nestandardních situací vyplývajících z uvádění GMO do životního prostředí budou okamžitě nahlášeny ministerstvu a příslušným úřadům. Doba platnosti povolení Doba platnosti povolení k uvádění do životního prostředí je do konce prosince roku O d ů v o d n ě n í Dne 14. listopadu 2017 byla doručena na MŽP žádost Ústavu hematologie a krevní transfuze, se sídlem U Nemocnice 1, Praha 2, IČ , o udělení povolení pro uvádění GMO do životního prostředí, a to pro klinické hodnocení léčivého přípravku CART19 buněk. Tato žádost je vedená pod čj. MZP/2017/750/1213. Ministerstvo životního prostředí posoudilo výše uvedenou žádost a dne 27. listopadu 2017 ji podle 5 odst. 4 zákona zaslalo k vyjádření Ministerstvu zdravotnictví, Ministerstvu zemědělství a Magistrátu hlavního města Prahy. MŽP neobdrželo žádné vyjádření veřejnosti ve smyslu 5 odst. 6 zákona. Žádost v elektronické podobě byla též zaslána k posouzení České komisi pro nakládání s geneticky modifikovanými organismy a genetickými produkty (ČK GMO) a určeným odborným posuzovatelům. Shrnutí obsahu žádosti bylo podle 18 odst. 4 zákona poskytnuto Evropské komisi a bylo zveřejněno v příslušné databázi pod označením B/CZ/17/02. Ostatní členské státy nevznesly k žádosti žádné připomínky. Ústavu hematologie a krevní transfuze bylo zasláno potvrzení o přijetí žádosti dne 16. listopadu /12
11 Dne 18. prosince 2017 vydala své stanovisko k žádosti ČK GMO. Ve svém stanovisku uvedla, že na základě posouzení potenciálního rizika pro zdraví člověka, zvířat, životní prostředí a biodiverzitu, souhlasí s nakládáním s CART19 buňkami v rámci klinické studie bez připomínek. Dne 13. prosince 2017 vydalo své stanovisko k žádosti Ministerstvo zemědělství. Ve svém stanovisku MZe uvedlo, že k žádosti Ústavu hematologie a krevní transfuze nevznáší žádné požadavky na doplnění údajů. Ministerstvo zdravotnictví podáním doručeným MŽP dne 15. prosince 2017 uvedlo, že z formálního hlediska chybí v závěru žádosti o udělení povolení chybí jméno a podpis odborného poradce, který souhlasí s výše uvedenými skutečnostmi. MŽP dne 12. prosince 2017 obdrželo informaci zaslanou Státním ústavem pro kontrolu léčiv, že subjekt prozatím nemá platné povolení k výrobě hodnoceného léčivého přípravku genové terapie, nicméně toto není překážkou pro řízení o uvádění GMO doživotního prostředí podle zákona. MŽP dne 15. ledna 2018 zaslalo v souladu se zákonem č. 634/2004 Sb., o správních poplatcích, žadateli výzvu k zaplacení správního poplatku za vydání povolení pro uvádění GMO do životního prostředí, a to pro klinické hodnocení léčivého přípravku CART19 buněk. Dne 17. ledna 2018 žadatel požadovanou částku zaplatil a zaslal MŽP informaci a potvrzení o zaplacení správního poplatku. Vzhledem k tomu, že výše uvedená žádost vyhovuje ustanovením zákona a jeho prováděcích předpisů a nakládání v režimu uvádění GMO do životního prostředí za daných podmínek nepředstavuje zvýšené riziko pro zdraví člověka a zvířat ani pro životní prostředí, a dále s přihlédnutím ke kladným stanoviskům MZe, MZ a ČK GMO, a dalším výše uvedeným skutečnostem, vydává MŽP žadateli povolení pro uvádění GMO do životního prostředí, a to pro klinické hodnocení léčivého přípravku CART19 buněk. 11/12
12 P o u č e n í Proti tomuto rozhodnutí je možno podle 152 odst. 1 zákona č. 500/2004 Sb., správní řád, podat do 15 dní od jeho oznámení rozklad, o němž rozhodne ministr životního prostředí, a to podáním adresovaným Ministerstvu životního prostředí, Vršovická 65, Praha 10. Ing. Karel Bláha, CSc. ředitel odboru Toto rozhodnutí obdrží: A. Účastník řízení do vlastních rukou: Ústav hematologie a krevní transfuze, se sídlem U Nemocnice 1, Praha 2 B. Na vědomí: 1. Ministerstvo zdravotnictví 2. Ministerstvo zemědělství 3. Magistrát hl. města Prahy 12/12
[K 17 odst. 3 písm. c) zákona]
![[K 17 odst. 3 písm. c) zákona] [K 17 odst. 3 písm. c) zákona]](/thumbs/79/79631257.jpg) ČÁST B ŽÁDOST O UDĚLENÍ POVOLENÍ K UVÁDĚNÍ DO ŽIVOTNÍHO PROSTŘEDÍ PRO ÚČELY KLINICKÉHO HODNOCENÍ LÉČIVÉHO PŘÍPRAVKU CART19 Datum podání 2.11.2017 1. Název projektu [K 17 odst. 3 písm. c) zákona] Ověření
ČÁST B ŽÁDOST O UDĚLENÍ POVOLENÍ K UVÁDĚNÍ DO ŽIVOTNÍHO PROSTŘEDÍ PRO ÚČELY KLINICKÉHO HODNOCENÍ LÉČIVÉHO PŘÍPRAVKU CART19 Datum podání 2.11.2017 1. Název projektu [K 17 odst. 3 písm. c) zákona] Ověření
Školení GMO Ústav biochemie a mikrobiologie
 Školení GMO Ústav biochemie a mikrobiologie 2.2.2018 Agrobacterium tumefaciens OZNÁMENÍ o uzavřeném nakládání první a druhé kategorie rizika na Ústavu biochemie a mikrobiologie VŠCHT a Ústavu biotechnologie
Školení GMO Ústav biochemie a mikrobiologie 2.2.2018 Agrobacterium tumefaciens OZNÁMENÍ o uzavřeném nakládání první a druhé kategorie rizika na Ústavu biochemie a mikrobiologie VŠCHT a Ústavu biotechnologie
Školení GMO Ústav biochemie a mikrobiologie
 Školení GMO Ústav biochemie a mikrobiologie 8.2.2019 Agrobacterium tumefaciens OZNÁMENÍ o uzavřeném nakládání první a druhé kategorie rizika na Ústavu biochemie a mikrobiologie VŠCHT a Ústavu biotechnologie
Školení GMO Ústav biochemie a mikrobiologie 8.2.2019 Agrobacterium tumefaciens OZNÁMENÍ o uzavřeném nakládání první a druhé kategorie rizika na Ústavu biochemie a mikrobiologie VŠCHT a Ústavu biotechnologie
Terapeutické klonování, náhrada tkání a orgánů
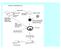 Transfekce, elektroporace, retrovirová infekce Vnesení genů Vrstva fibroblastů, LIF Terapeutické klonování, náhrada tkání a orgánů Selekce ES buněk, v nichž došlo k začlenění vneseného genu homologní rekombinací
Transfekce, elektroporace, retrovirová infekce Vnesení genů Vrstva fibroblastů, LIF Terapeutické klonování, náhrada tkání a orgánů Selekce ES buněk, v nichž došlo k začlenění vneseného genu homologní rekombinací
Informace o havarijním plánu
 Informace o havarijním plánu a) Laboratoř salmonelových infekcí a experimentální stáje jsou součástí Výzkumného ústavu veterinárního lékařství (VÚVeL), Hudcova 70, 621 32 Brno. b) K možným haváriím může
Informace o havarijním plánu a) Laboratoř salmonelových infekcí a experimentální stáje jsou součástí Výzkumného ústavu veterinárního lékařství (VÚVeL), Hudcova 70, 621 32 Brno. b) K možným haváriím může
s geneticky modifikovanými organismy a genetickými
 Strana 5811 372 VYHLÁŠKA ze dne 25. října 2016, kterou se mění vyhláška č. 209/2004 Sb., o bližších podmínkách nakládání s geneticky modifikovanými organismy a genetickými produkty, ve znění pozdějších
Strana 5811 372 VYHLÁŠKA ze dne 25. října 2016, kterou se mění vyhláška č. 209/2004 Sb., o bližších podmínkách nakládání s geneticky modifikovanými organismy a genetickými produkty, ve znění pozdějších
Metodika kontrol uzavřeného prostoru při nakládání s geneticky modifikovanými mikroorganismy. Školení pracovníků
 Metodika kontrol uzavřeného prostoru při nakládání s geneticky modifikovanými mikroorganismy Školení pracovníků Miroslav Pátek Mikrobiologický ústav AV ČR, v.v.i. Laboratoř molekulární genetiky bakterií
Metodika kontrol uzavřeného prostoru při nakládání s geneticky modifikovanými mikroorganismy Školení pracovníků Miroslav Pátek Mikrobiologický ústav AV ČR, v.v.i. Laboratoř molekulární genetiky bakterií
Školení GMO Ústav biochemie a mikrobiologie
 Školení GMO Ústav biochemie a mikrobiologie 2.2.2016 Agrobacterium tumefaciens OZNÁMENÍ o uzavřeném nakládání první a druhé kategorie rizika na Ústavu biochemie a mikrobiologie VŠCHT Praha Ministerstvo
Školení GMO Ústav biochemie a mikrobiologie 2.2.2016 Agrobacterium tumefaciens OZNÁMENÍ o uzavřeném nakládání první a druhé kategorie rizika na Ústavu biochemie a mikrobiologie VŠCHT Praha Ministerstvo
Klonování DNA a fyzikální mapování genomu
 Klonování DNA a fyzikální mapování genomu. Terminologie Klonování je proces tvorby klonů Klon je soubor identických buněk (příp. organismů) odvozených ze společného předka dělením (např. jedna bakteriální
Klonování DNA a fyzikální mapování genomu. Terminologie Klonování je proces tvorby klonů Klon je soubor identických buněk (příp. organismů) odvozených ze společného předka dělením (např. jedna bakteriální
[K 17 odst. 3 písm. c) zákona]
![[K 17 odst. 3 písm. c) zákona] [K 17 odst. 3 písm. c) zákona]](/thumbs/100/145136181.jpg) ČÁST B ŽÁDOST O UDĚLENÍ POVOLENÍ K UVÁDĚNÍ DO ŽIVOTNÍHO PROSTŘEDÍ PRO ÚČELY KLINICKÉHO HODNOCENÍ LÉČIVÝCH PŘÍPRAVKŮ [K 17 odst. 3 písm. c) zákona] 1. Název projektu: Klinické hodnocení fáze I-IIa k posouzení
ČÁST B ŽÁDOST O UDĚLENÍ POVOLENÍ K UVÁDĚNÍ DO ŽIVOTNÍHO PROSTŘEDÍ PRO ÚČELY KLINICKÉHO HODNOCENÍ LÉČIVÝCH PŘÍPRAVKŮ [K 17 odst. 3 písm. c) zákona] 1. Název projektu: Klinické hodnocení fáze I-IIa k posouzení
Vakcíny z nádorových buněk
 Protinádorové terapeutické vakcíny Vakcíny z nádorových buněk V. Vonka, ÚHKT, Praha Výhody vakcín z nádorových buněk 1.Nabízejí imunitnímu systému pacienta celé spektrum nádorových antigenů. 2. Jejich
Protinádorové terapeutické vakcíny Vakcíny z nádorových buněk V. Vonka, ÚHKT, Praha Výhody vakcín z nádorových buněk 1.Nabízejí imunitnímu systému pacienta celé spektrum nádorových antigenů. 2. Jejich
R o z h o d n u t í. rozhodlo
 Ministerstvo životního prostředí odbor environmentálních rizik Praze dne 30. dubna 2007 Čj.: 4675/ENV/07 R o z h o d n u t í Ministerstvo životního prostředí jako správní úřad příslušný podle 5 zákona
Ministerstvo životního prostředí odbor environmentálních rizik Praze dne 30. dubna 2007 Čj.: 4675/ENV/07 R o z h o d n u t í Ministerstvo životního prostředí jako správní úřad příslušný podle 5 zákona
Rekombinantní protilátky, bakteriofágy, aptamery a peptidové scaffoldy pro analytické a terapeutické účely Luděk Eyer
 Rekombinantní protilátky, bakteriofágy, aptamery a peptidové scaffoldy pro analytické a terapeutické účely Luděk Eyer Virologie a diagnostika Výzkumný ústav veterinárního lékařství, v.v.i., Brno Alternativní
Rekombinantní protilátky, bakteriofágy, aptamery a peptidové scaffoldy pro analytické a terapeutické účely Luděk Eyer Virologie a diagnostika Výzkumný ústav veterinárního lékařství, v.v.i., Brno Alternativní
Molekulární biotechnologie č.12. Využití poznatků molekulární biotechnologie. Transgenní rostliny.
 Molekulární biotechnologie č.12 Využití poznatků molekulární biotechnologie. Transgenní rostliny. Transgenní organismy Transgenní organismus: Organismus, jehož genom byl geneticky modifikován cizorodou
Molekulární biotechnologie č.12 Využití poznatků molekulární biotechnologie. Transgenní rostliny. Transgenní organismy Transgenní organismus: Organismus, jehož genom byl geneticky modifikován cizorodou
Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/
 I n v e s t i c e d o r o z v o j e v z d ě l á v á n í Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Tento projekt je spolufinancován Evropským sociálním fondem a státním
I n v e s t i c e d o r o z v o j e v z d ě l á v á n í Inovace studia molekulární a buněčné biologie reg. č. CZ.1.07/2.2.00/07.0354 Tento projekt je spolufinancován Evropským sociálním fondem a státním
Co nás učí nádory? Prof. RNDr. Jana Šmardová, CSc. Ústav patologie FN Brno Přírodovědecká a Lékařská fakulta MU Brno
 Co nás učí nádory? Prof. RNDr. Jana Šmardová, CSc. Ústav patologie FN Brno Přírodovědecká a Lékařská fakulta MU Brno Brno, 17.5.2011 Izidor (Easy Door) Osnova přednášky 1. Proč nás rakovina tolik zajímá?
Co nás učí nádory? Prof. RNDr. Jana Šmardová, CSc. Ústav patologie FN Brno Přírodovědecká a Lékařská fakulta MU Brno Brno, 17.5.2011 Izidor (Easy Door) Osnova přednášky 1. Proč nás rakovina tolik zajímá?
KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY
 Požadavky na vstupní materiál lidské tkáně a buňky 1 KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY MUDr. Ivana Koblihová Inspektor lidských tkání a buněk Požadavky na vstupní
Požadavky na vstupní materiál lidské tkáně a buňky 1 KLINICKÁ HODNOCENÍ S LPMT POŽADAVKY NA VSTUPNÍ MATERIÁL LIDSKÉ TKÁNĚ A BUŇKY MUDr. Ivana Koblihová Inspektor lidských tkání a buněk Požadavky na vstupní
Tematické okruhy k SZZ v bakalářském studijním oboru Zdravotní laborant bakalářského studijního programu B5345 Specializace ve zdravotnictví
 Tematické okruhy k SZZ v bakalářském studijním oboru Zdravotní laborant bakalářského studijního programu B5345 Specializace ve zdravotnictví Dle čl. 7 odst. 2 Směrnice děkana pro realizaci bakalářských
Tematické okruhy k SZZ v bakalářském studijním oboru Zdravotní laborant bakalářského studijního programu B5345 Specializace ve zdravotnictví Dle čl. 7 odst. 2 Směrnice děkana pro realizaci bakalářských
1. Obecné informace Evropské číslo oznámení (viz databáze SNIF na B/CZ/09/ Oprávněná osoba: Ing.
 FORMULÁŘ PRO PŘEDKLÁDÁNÍ VÝSLEDKŮ UVÁDĚNÍ GETICKY MODIFIKOVANÝCH VYŠŠÍCH ROSTLIN DO ŽIVOTNÍHO PROSTŘEDÍ podle 19 písm. d) zákona č. 78/2004 Sb., popřípadě zpráv o monitoringu Oprávněná osoba vyplní formulář
FORMULÁŘ PRO PŘEDKLÁDÁNÍ VÝSLEDKŮ UVÁDĚNÍ GETICKY MODIFIKOVANÝCH VYŠŠÍCH ROSTLIN DO ŽIVOTNÍHO PROSTŘEDÍ podle 19 písm. d) zákona č. 78/2004 Sb., popřípadě zpráv o monitoringu Oprávněná osoba vyplní formulář
DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ
 1 DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ MUDr. Alice Němcová Oddělení klinického hodnocení, Sekce registrací DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ 2 Obsah prezentace: Pravidla distribuce
1 DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ MUDr. Alice Němcová Oddělení klinického hodnocení, Sekce registrací DISTRIBUCE NEREGISTROVANÝCH LÉČIVÝCH PŘÍPRAVKŮ 2 Obsah prezentace: Pravidla distribuce
ZP-22 Metodika kontrol distributorů a dovozců zdravotnických prostředků
 ZP-22 Metodika kontrol distributorů a dovozců zdravotnických prostředků Tento pokyn je platný od 11. 03. 2019. ÚVOD Tato metodika obsahuje informace určené zejména pro dovozce a distributory zdravotnických
ZP-22 Metodika kontrol distributorů a dovozců zdravotnických prostředků Tento pokyn je platný od 11. 03. 2019. ÚVOD Tato metodika obsahuje informace určené zejména pro dovozce a distributory zdravotnických
Molekulární biotechnologie č.8. Produkce heterologního proteinu v eukaryontních buňkách
 Molekulární biotechnologie č.8 Produkce heterologního proteinu v eukaryontních buňkách Eukaryontní buňky se využívají v případě, když Eukaryontní proteiny syntetizované v baktériích postrádají biologickou
Molekulární biotechnologie č.8 Produkce heterologního proteinu v eukaryontních buňkách Eukaryontní buňky se využívají v případě, když Eukaryontní proteiny syntetizované v baktériích postrádají biologickou
Školení o práci s GMO
 Školení o práci s GMO Pracoviště MU v Brně, na nichž se nakládá s GMO Přírodovědecká fakulta: Oddělení genetiky a molekulární biologie ÚEB Oddělení mikrobiologie ÚEB Ústav biochemie Laboratoř funkční genomiky
Školení o práci s GMO Pracoviště MU v Brně, na nichž se nakládá s GMO Přírodovědecká fakulta: Oddělení genetiky a molekulární biologie ÚEB Oddělení mikrobiologie ÚEB Ústav biochemie Laboratoř funkční genomiky
Školení o práci s GMO
 Školení o práci s GMO Pracoviště MU v Brně, na nichž se nakládá s GMO PřF: -Oddělení genetiky a molekulární biologie ÚEB -Oddělení mikrobiologie ÚEB - Ústav biochemie - Laboratoř funkční genomiky a proteomiky
Školení o práci s GMO Pracoviště MU v Brně, na nichž se nakládá s GMO PřF: -Oddělení genetiky a molekulární biologie ÚEB -Oddělení mikrobiologie ÚEB - Ústav biochemie - Laboratoř funkční genomiky a proteomiky
1. Definice a historie oboru molekulární medicína. 3. Základní laboratorní techniky v molekulární medicíně
 Obsah Předmluvy 1. Definice a historie oboru molekulární medicína 1.1. Historie molekulární medicíny 2. Základní principy molekulární biologie 2.1. Historie molekulární biologie 2.2. DNA a chromozomy 2.3.
Obsah Předmluvy 1. Definice a historie oboru molekulární medicína 1.1. Historie molekulární medicíny 2. Základní principy molekulární biologie 2.1. Historie molekulární biologie 2.2. DNA a chromozomy 2.3.
Protinádorová imunita. Jiří Jelínek
 Protinádorová imunita Jiří Jelínek Imunitní systém vs. nádor l imunitní systém je poslední přirozený nástroj organismu jak eliminovat vlastní buňky které se vymkly kontrole l do boje proti nádorovým buňkám
Protinádorová imunita Jiří Jelínek Imunitní systém vs. nádor l imunitní systém je poslední přirozený nástroj organismu jak eliminovat vlastní buňky které se vymkly kontrole l do boje proti nádorovým buňkám
STANDARDY SPECIFICKÁ ČÁST
 STANDARDY SPECIFICKÁ ČÁST K. Nábor dárců a výběr dárce pro nemocného K.1. Obecné podmínky vstupu do registru K.2. Organizace náboru K.3. Specifické skupiny dárců K.4. Charakteristika dárce v době náboru
STANDARDY SPECIFICKÁ ČÁST K. Nábor dárců a výběr dárce pro nemocného K.1. Obecné podmínky vstupu do registru K.2. Organizace náboru K.3. Specifické skupiny dárců K.4. Charakteristika dárce v době náboru
FN Hradec Králové JIP GMK. Vypracovala: Monika Uhlířová Dis.
 Nozokomiální nákazy FN Hradec Králové JIP GMK Vypracovala: Monika Uhlířová Dis. Definice: Vznikají v souvislosti s hospitalizací. Máme-li infekci označit za nozokomiální, musí být zřejmé, že nebyla přítomna
Nozokomiální nákazy FN Hradec Králové JIP GMK Vypracovala: Monika Uhlířová Dis. Definice: Vznikají v souvislosti s hospitalizací. Máme-li infekci označit za nozokomiální, musí být zřejmé, že nebyla přítomna
Havarijní plán pro uzavřené nakládání s GMO
 Havarijní plán pro uzavřené nakládání s GMO Název, právní forma sídlo a identifikační číslo uživatele: Mendelova univerzita v Brně Sídlo: Zemědělská 1, 613 00 Brno Právní forma: Veřejná vysoká škola IČO:
Havarijní plán pro uzavřené nakládání s GMO Název, právní forma sídlo a identifikační číslo uživatele: Mendelova univerzita v Brně Sídlo: Zemědělská 1, 613 00 Brno Právní forma: Veřejná vysoká škola IČO:
Vývoj nových léčiv. Preklinický výzkum Klinický výzkum
 Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
Co je to transplantace krvetvorných buněk?
 Co je to transplantace krvetvorných buněk? Transplantace krvetvorných buněk je přenos vlastní (autologní) nebo dárcovské (alogenní) krvetvorné tkáně. Účelem je obnova kostní dřeně po vysoce dávkové chemoterapii
Co je to transplantace krvetvorných buněk? Transplantace krvetvorných buněk je přenos vlastní (autologní) nebo dárcovské (alogenní) krvetvorné tkáně. Účelem je obnova kostní dřeně po vysoce dávkové chemoterapii
Citlivost a rezistence mikroorganismů na antimikrobiální léčiva
 Citlivost a rezistence mikroorganismů na antimikrobiální léčiva Sylva Janovská Univerzita Pardubice Fakulta chemicko-technologická Katedra biologických a biochemických věd Centralizovaný rozvojový projekt
Citlivost a rezistence mikroorganismů na antimikrobiální léčiva Sylva Janovská Univerzita Pardubice Fakulta chemicko-technologická Katedra biologických a biochemických věd Centralizovaný rozvojový projekt
Havarijní plán pro práci s geneticky modifikovanými mikroorganismy Mikrobiologický ústav AV ČR
 Mikrobiologický ústav AV ČR Příloha 6 Havarijní plán 1/5 Havarijní plán pro práci s geneticky modifikovanými mikroorganismy Mikrobiologický ústav AV ČR a) Adresa pracoviště Mikrobiologický ústav AV ČR
Mikrobiologický ústav AV ČR Příloha 6 Havarijní plán 1/5 Havarijní plán pro práci s geneticky modifikovanými mikroorganismy Mikrobiologický ústav AV ČR a) Adresa pracoviště Mikrobiologický ústav AV ČR
Výroční zpráva tkáňového zařízení za rok 2015
 Ústav hematologie a krevní transfuze, p. o. IČO 23736 128 20 Praha 2, U Nemocnice 1 telefon: 224 436 018, E-mail: cryo@uhkt.cz Pracoviště FN Motol, Nová budova kliniky dětské onkologie číslo 23, ulice
Ústav hematologie a krevní transfuze, p. o. IČO 23736 128 20 Praha 2, U Nemocnice 1 telefon: 224 436 018, E-mail: cryo@uhkt.cz Pracoviště FN Motol, Nová budova kliniky dětské onkologie číslo 23, ulice
Organizace transfuzní služby. I.Sulovská
 Organizace transfuzní služby I.Sulovská Transfuzní oddělení Výroba transfuzních přípravků (TP) řízena zákony, vyhláškami a metodickými pokyny 2 druhy TO: výrobci TP odběrová střediska Výrobci TP mají uděleno
Organizace transfuzní služby I.Sulovská Transfuzní oddělení Výroba transfuzních přípravků (TP) řízena zákony, vyhláškami a metodickými pokyny 2 druhy TO: výrobci TP odběrová střediska Výrobci TP mají uděleno
Tekuté biopsie u mnohočetného myelomu
 Tekuté biopsie u mnohočetného myelomu Mgr. Veronika Kubaczková Babákova myelomová skupina ÚPF LF MU Pacientský seminář 11. května 2016, Brno Co jsou tekuté biopsie? Představují méně zatěžující vyšetření
Tekuté biopsie u mnohočetného myelomu Mgr. Veronika Kubaczková Babákova myelomová skupina ÚPF LF MU Pacientský seminář 11. května 2016, Brno Co jsou tekuté biopsie? Představují méně zatěžující vyšetření
pro vybrané pracovníky radioterapeutických pracovišť č. dokumentu: VF A-9132-M0801T3 Jméno Funkce Podpis Datum
 Výukový program č. dokumentu: Jméno Funkce Podpis Datum Zpracoval Ing. Jiří Filip srpen 2008 Kontroloval Ing. Jan Binka SPDRO 13.2.2009 Schválil strana 1/7 Program je určen pro vybrané pracovníky připravované
Výukový program č. dokumentu: Jméno Funkce Podpis Datum Zpracoval Ing. Jiří Filip srpen 2008 Kontroloval Ing. Jan Binka SPDRO 13.2.2009 Schválil strana 1/7 Program je určen pro vybrané pracovníky připravované
Úplný přehled zkušebních okruhů
 Úplný přehled zkušebních okruhů Zkušební okruhy teoretických znalostí pro zkoušku z odborné způsobilosti k zajišťování úkolů v prevenci rizik dle přílohy č. 1 k nařízení vlády č. 592/2006 Sb.: a) znalost
Úplný přehled zkušebních okruhů Zkušební okruhy teoretických znalostí pro zkoušku z odborné způsobilosti k zajišťování úkolů v prevenci rizik dle přílohy č. 1 k nařízení vlády č. 592/2006 Sb.: a) znalost
RNDr K.Roubalová CSc.
 Cytomegalovirus RNDr K.Roubalová CSc. www.vidia.cz kroubalova@vidia.cz Lidský cytomegalovirus Β-herpesviridae, p největší HV (240 nm), cca 160 genů Příbuzné viry: myší, krysí, opičí, morčecí Kosmopolitní
Cytomegalovirus RNDr K.Roubalová CSc. www.vidia.cz kroubalova@vidia.cz Lidský cytomegalovirus Β-herpesviridae, p největší HV (240 nm), cca 160 genů Příbuzné viry: myší, krysí, opičí, morčecí Kosmopolitní
PRŮZKUM V OBLASTI PŘÍPRAVY CYTOSTATIK
 Země: ČESKÁ REPUBLIKA PRŮZKUM V OBLASTI PŘÍPRAVY CYTOSTATIK Datum: 1. Identifikace vašeho zařízení Instituce: Počet oddělení: Počet onkologických oddělení: Počet onkologických ambulancí v nemocnici: Počet
Země: ČESKÁ REPUBLIKA PRŮZKUM V OBLASTI PŘÍPRAVY CYTOSTATIK Datum: 1. Identifikace vašeho zařízení Instituce: Počet oddělení: Počet onkologických oddělení: Počet onkologických ambulancí v nemocnici: Počet
Rizika přípravy GMO. B. Šíření GMO mimo vyhrazený prostor (laboratoř, životní prostředí pole, vodní plochy ) vliv na ekosystém, ovlivnění biodiverzity
 Rizika přípravy GMO A. Klonování nebezpečných genů zdravotní riziko nových transgenních organismů a jejich produktů - geny pro toxiny (zvýšení virulence patogenních kmenů) - rezistence k antibiotikům (komplikace
Rizika přípravy GMO A. Klonování nebezpečných genů zdravotní riziko nových transgenních organismů a jejich produktů - geny pro toxiny (zvýšení virulence patogenních kmenů) - rezistence k antibiotikům (komplikace
Zjišťování toxicity látek
 Zjišťování toxicity látek 1. Úvod 2. Literární údaje 3. Testy in vitro 4. Testy na zvířatech in vivo 5. Epidemiologické studie 6. Zjišťování úrovně expozice Úvod Je známo 2 10 7 chemických látek. Prostudování
Zjišťování toxicity látek 1. Úvod 2. Literární údaje 3. Testy in vitro 4. Testy na zvířatech in vivo 5. Epidemiologické studie 6. Zjišťování úrovně expozice Úvod Je známo 2 10 7 chemických látek. Prostudování
Bezpečnostní list pro Bionorm U C00.001
 1 IDENTIFIKACE PRODUKTU OBCHODNÍ NÁZEV : Bionorm U KATALOGOVÉ ČÍSLO : VÝROBCE: POUŽITÍ: BioVendor - Laboratorní medicína a.s.; sídlo: Tůmova 2265/60, 616 00 Brno Provozovna: Karásek 1767/1, 621 00 Brno
1 IDENTIFIKACE PRODUKTU OBCHODNÍ NÁZEV : Bionorm U KATALOGOVÉ ČÍSLO : VÝROBCE: POUŽITÍ: BioVendor - Laboratorní medicína a.s.; sídlo: Tůmova 2265/60, 616 00 Brno Provozovna: Karásek 1767/1, 621 00 Brno
Bezpečnostní list. Styrodur* 3035 CS 1265x615x40mm 1. IDENTIFIKACE LÁTKY NEBO PŘÍPRAVKU A VÝROBCE NEBO DOVOZCE
 Bezpečnostní list Strana: 1/5 1. IDENTIFIKACE LÁTKY NEBO PŘÍPRAVKU A VÝROBCE NEBO DOVOZCE Styrodur* 3035 CS 1265x615x40mm Použití: extrudované pěnové desky pro tepelnou izolaci ve stavebnictví Výrobce:
Bezpečnostní list Strana: 1/5 1. IDENTIFIKACE LÁTKY NEBO PŘÍPRAVKU A VÝROBCE NEBO DOVOZCE Styrodur* 3035 CS 1265x615x40mm Použití: extrudované pěnové desky pro tepelnou izolaci ve stavebnictví Výrobce:
Havarijní plán. (podle 2, vyhlášky č.399/2005 Z.z.)
 Havarijní plán (podle 2, vyhlášky č.399/2005 Z.z.) Tento havarijní plán slouží pro zajištění přepravy geneticky modifikovaného materiálu kukuřice MON 88017, MON 89034 a MON 89034 MON 88017 1. Obchodní
Havarijní plán (podle 2, vyhlášky č.399/2005 Z.z.) Tento havarijní plán slouží pro zajištění přepravy geneticky modifikovaného materiálu kukuřice MON 88017, MON 89034 a MON 89034 MON 88017 1. Obchodní
Nemocniční výjimka pokyn UST-37
 1 Nemocniční výjimka pokyn UST-37 2 Právní rámec Zákon č. 378/2007 Sb., o léčivech a změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Vyhláška č. 228/2008 Sb., o
1 Nemocniční výjimka pokyn UST-37 2 Právní rámec Zákon č. 378/2007 Sb., o léčivech a změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Vyhláška č. 228/2008 Sb., o
ZPRÁVA O VÝSLEDCÍCH UVÁDĚNÍ GENETICKY MODIFIKOVANÝCH VYŠŠÍCH ROSTLIN DO ŽIVOTNÍHO PROSTŘEDÍ podle 18 odst. 9 zákona č. 78/2004 Sb.
 ZPRÁVA O VÝSLEDCÍCH UVÁDĚNÍ GENETICKY MODIFIKOVANÝCH VYŠŠÍCH ROSTLIN DO ŽIVOTNÍHO PROSTŘEDÍ podle 18 odst. 9 zákona č. 78/2004 Sb., v platném znění 1. Obecné informace 1.1. Evropské číslo oznámení B/CZ/11/3
ZPRÁVA O VÝSLEDCÍCH UVÁDĚNÍ GENETICKY MODIFIKOVANÝCH VYŠŠÍCH ROSTLIN DO ŽIVOTNÍHO PROSTŘEDÍ podle 18 odst. 9 zákona č. 78/2004 Sb., v platném znění 1. Obecné informace 1.1. Evropské číslo oznámení B/CZ/11/3
Příprava vektoru IZOLACE PLASMIDU ALKALICKÁ LYZE, KOLONKOVÁ IZOLACE DNA GELOVÁ ELEKTROFORÉZA RESTRIKČNÍ ŠTĚPENÍ. E. coli. lyze buňky.
 Příprava vektoru IZOLCE PLSMIDU LKLICKÁ LYZE, KOLONKOVÁ IZOLCE DN E. coli plasmidová DN proteiny proteiny + + vysrážená plasmidová lyze buňky + snížení ph chromosomální DN centrifugace DN chromosomální
Příprava vektoru IZOLCE PLSMIDU LKLICKÁ LYZE, KOLONKOVÁ IZOLCE DN E. coli plasmidová DN proteiny proteiny + + vysrážená plasmidová lyze buňky + snížení ph chromosomální DN centrifugace DN chromosomální
VÝZVA K PODÁNÍ NABÍDEK DO VÝBĚROVÉHO ŘÍZENÍ NA VEŘEJNOU ZAKÁZKU MALÉHO ROZSAHU
 VÝZVA K PODÁNÍ NABÍDEK DO VÝBĚROVÉHO ŘÍZENÍ NA VEŘEJNOU ZAKÁZKU MALÉHO ROZSAHU ZADÁVACÍ PODMÍNKY Název zakázky: Dodávka laboratorních lednic II 1. Identifikační údaje zadavatele Název zadavatele: ÚSTAV
VÝZVA K PODÁNÍ NABÍDEK DO VÝBĚROVÉHO ŘÍZENÍ NA VEŘEJNOU ZAKÁZKU MALÉHO ROZSAHU ZADÁVACÍ PODMÍNKY Název zakázky: Dodávka laboratorních lednic II 1. Identifikační údaje zadavatele Název zadavatele: ÚSTAV
2017 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 2 NOVELA ZÁKONA A VYHLÁŠKY DOVOZ TKÁNÍ A BUNĚK ZE TŘETÍCH ZEMÍ Mgr. Eva Tomková, Ph.D. 3 Obsah Písemná smlouva mezi dovážejícím tkáňovým zařízením a dodavatelem ze třetí země Žádost o povolení dovážejícího
2 NOVELA ZÁKONA A VYHLÁŠKY DOVOZ TKÁNÍ A BUNĚK ZE TŘETÍCH ZEMÍ Mgr. Eva Tomková, Ph.D. 3 Obsah Písemná smlouva mezi dovážejícím tkáňovým zařízením a dodavatelem ze třetí země Žádost o povolení dovážejícího
Molekulární biotechnologie. Nový obor, který vznikl koncem 70. let 20. století (č.1)
 Molekulární biotechnologie Nový obor, který vznikl koncem 70. let 20. století (č.1) Molekulární biotechnologie je založena Na přenosu genů z jednoho organismu do druhého Jeden organismus má gen, který
Molekulární biotechnologie Nový obor, který vznikl koncem 70. let 20. století (č.1) Molekulární biotechnologie je založena Na přenosu genů z jednoho organismu do druhého Jeden organismus má gen, který
VYHLÁŠKA ze dne 15. března 2012 o požadavcích na minimální technické a věcné vybavení zdravotnických zařízení a kontaktních pracovišť domácí péče
 Strana 1522 Sbírka zákonů č. 92 / 2012 Částka 36 92 VYHLÁŠKA ze dne 15. března 2012 o požadavcích na minimální technické a věcné vybavení zdravotnických zařízení a kontaktních pracovišť domácí péče Ministerstvo
Strana 1522 Sbírka zákonů č. 92 / 2012 Částka 36 92 VYHLÁŠKA ze dne 15. března 2012 o požadavcích na minimální technické a věcné vybavení zdravotnických zařízení a kontaktních pracovišť domácí péče Ministerstvo
1 ZDRAVOTNICKE PROSTREDKY.EU v. 1 LEGISLATIVNÍ POŽADAVKY VYPLÝVAJÍCÍ ZE ZÁKONA O ZDRAVOTNICKÝCH PROSTŘEDCÍCH * PŘI POSKYTOVÁNÍ ZDRAVOTNÍCH SLUŽEB
 1 LEGISLATIVNÍ POŽADAVKY VYPLÝVAJÍCÍ ZE ZÁKONA O ZDRAVOTNICKÝCH PROSTŘEDCÍCH * PŘI POSKYTOVÁNÍ ZDRAVOTNÍCH SLUŽEB Obsah Zákon 268/2014 Sb. (ZoZP)... 2 Hlava VIII používání... 2 58 Obecné ustanovení...
1 LEGISLATIVNÍ POŽADAVKY VYPLÝVAJÍCÍ ZE ZÁKONA O ZDRAVOTNICKÝCH PROSTŘEDCÍCH * PŘI POSKYTOVÁNÍ ZDRAVOTNÍCH SLUŽEB Obsah Zákon 268/2014 Sb. (ZoZP)... 2 Hlava VIII používání... 2 58 Obecné ustanovení...
IMUNOGENETIKA I. Imunologie. nauka o obraných schopnostech organismu. imunitní systém heterogenní populace buněk lymfatické tkáně lymfatické orgány
 IMUNOGENETIKA I Imunologie nauka o obraných schopnostech organismu imunitní systém heterogenní populace buněk lymfatické tkáně lymfatické orgány lymfatická tkáň thymus Imunita reakce organismu proti cizorodým
IMUNOGENETIKA I Imunologie nauka o obraných schopnostech organismu imunitní systém heterogenní populace buněk lymfatické tkáně lymfatické orgány lymfatická tkáň thymus Imunita reakce organismu proti cizorodým
Výkon agendy podle ustanovení 47 odst. 2 zákona č. 372/2011 Sb., o zdravotních službách a podmínkách jejich poskytování.
 Příloha č. 1 zveřejnění informací o kontrolách Odbor správních činností ve zdravotnictví a sociální péči, oddělení zdravotnictví, Magistrátu hlavního města Prahy, zveřejňuje ve smyslu ustanovení 26 zákona
Příloha č. 1 zveřejnění informací o kontrolách Odbor správních činností ve zdravotnictví a sociální péči, oddělení zdravotnictví, Magistrátu hlavního města Prahy, zveřejňuje ve smyslu ustanovení 26 zákona
Šrobárova Praha 10. Vyřizuje/linka Koblihová/949 ROZHODNUTÍ
 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Šrobárova 48 100 41 Praha 10 Telefon: +420 272 185 111 Fax: +420 271 732 377 E-mail: posta@sukl.cz Web: www.sukl.cz ADRESÁT Fakultní nemocnice Hradec Králové Sokolská 581
STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Šrobárova 48 100 41 Praha 10 Telefon: +420 272 185 111 Fax: +420 271 732 377 E-mail: posta@sukl.cz Web: www.sukl.cz ADRESÁT Fakultní nemocnice Hradec Králové Sokolská 581
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ
 HOO/O13 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 6 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 6 číslo tkáňové banky: odpovědná osoba:
HOO/O13 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 6 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 6 číslo tkáňové banky: odpovědná osoba:
KLH-EK-01 ŽÁDOST O STANOVISKO ETICKÉ KOMISE K PROVEDENÍ KLINICKÉHO HODNOCENÍ V ČESKÉ REPUBLICE - požadavky na předkládanou dokumentaci
 KLH-EK-01 ŽÁDOST O STANOVISKO ETICKÉ KOMISE K PROVEDENÍ KLINICKÉHO HODNOCENÍ V ČESKÉ REPUBLICE - požadavky na předkládanou dokumentaci Tento pokyn se vydává za účelem harmonizace činnosti etických komisí
KLH-EK-01 ŽÁDOST O STANOVISKO ETICKÉ KOMISE K PROVEDENÍ KLINICKÉHO HODNOCENÍ V ČESKÉ REPUBLICE - požadavky na předkládanou dokumentaci Tento pokyn se vydává za účelem harmonizace činnosti etických komisí
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ
 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 4 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 6 číslo tkáňové banky: odpovědná osoba: ICCBBA
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 4 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 34 6 číslo tkáňové banky: odpovědná osoba: ICCBBA
Rozhodnutí nabylo právní moci dne 9. srpna 2019.
 Praha dne 24. července 2019 Č. j.: MZP/2019/750/2158 Sp. zn.: ZN/MZP/2019/750/182 Vyřizuje: Ing. Václav Routa Tel.: 267 122 554 E-mail: václav routa@mzp.cz Vážený pan MUDr. Jiří Havrlant, MHA ředitel FN
Praha dne 24. července 2019 Č. j.: MZP/2019/750/2158 Sp. zn.: ZN/MZP/2019/750/182 Vyřizuje: Ing. Václav Routa Tel.: 267 122 554 E-mail: václav routa@mzp.cz Vážený pan MUDr. Jiří Havrlant, MHA ředitel FN
Bezpečnostní list pro CAST 2000 ELISA BH-EK-CAST, BH-EK-CAST5
 Bezpečnostní list pro CAST 2000 ELISA BH-EK-CAST, BH-EK-CAST5 1 IDENTIFIKACE PRODUKTU OBCHODNÍ NÁZEV : KATALOGOVÉ ČÍSLO : VÝROBCE : DOVOZCE: POUŽITÍ: Cellular Antigen Stimulation Test BH-EK-CAST / CAST5
Bezpečnostní list pro CAST 2000 ELISA BH-EK-CAST, BH-EK-CAST5 1 IDENTIFIKACE PRODUKTU OBCHODNÍ NÁZEV : KATALOGOVÉ ČÍSLO : VÝROBCE : DOVOZCE: POUŽITÍ: Cellular Antigen Stimulation Test BH-EK-CAST / CAST5
ADRESÁT: R o z h o d n u t í. r o z h o d l o. Ústavu organické chemie a biochemie AV ČR v.v.i. Flemingovo nám Praha 6
 Rozhodnutí nabylo právní moci dne 22. listopadu 2012. ODESÍLATEL: Ing. Karel Bláha, CSc. ředitel odboru environmentálních rizik a ekologických škod Ministerstvo životního prostředí Vršovická 65 100 10
Rozhodnutí nabylo právní moci dne 22. listopadu 2012. ODESÍLATEL: Ing. Karel Bláha, CSc. ředitel odboru environmentálních rizik a ekologických škod Ministerstvo životního prostředí Vršovická 65 100 10
Biologická léčiva. Co jsou to biosimilars a jak se vyrábějí. Michal Hojný
 Biologická léčiva Co jsou to biosimilars a jak se vyrábějí Michal Hojný Zadání Jsou to opravdu generické kopie originálů? Jsou tam nějaká nebezpečí při výrobě? Jsou ty léky úplně stejné? Jak těžké je vyrobit
Biologická léčiva Co jsou to biosimilars a jak se vyrábějí Michal Hojný Zadání Jsou to opravdu generické kopie originálů? Jsou tam nějaká nebezpečí při výrobě? Jsou ty léky úplně stejné? Jak těžké je vyrobit
Úplný přehled zkušebních okruhů
 Úplný přehled zkušebních okruhů Zkušební okruhy teoretických znalostí pro zkoušku z odborné způsobilosti k zajišťování úkolů v prevenci rizik dle přílohy č. 1 k nařízení vlády č. 592/2006 Sb.: a) znalost
Úplný přehled zkušebních okruhů Zkušební okruhy teoretických znalostí pro zkoušku z odborné způsobilosti k zajišťování úkolů v prevenci rizik dle přílohy č. 1 k nařízení vlády č. 592/2006 Sb.: a) znalost
Bezpečnostní list. podle nařízení (ES) č. 1907/2006. Electrolyte PAA_1024558
 Strana 1 z 5 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1 Identifikátor výrobku Zkratka: Materialnr. 1024558 1.2 Příslušná určená použití látky nebo směsi a nedoporučená použití Použití
Strana 1 z 5 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1 Identifikátor výrobku Zkratka: Materialnr. 1024558 1.2 Příslušná určená použití látky nebo směsi a nedoporučená použití Použití
Bezpečnost a ochrana zdraví; Zdravotní pojištění, zdravotní péče Normy:
 Název předpisu: Vyhláška, kterou se stanoví podmínky pro zařazování prací do kategorií, limitní hodnoty ukazatelů biologických expozičních testů, podmínky odběru biologického materiálu pro provádění biologických
Název předpisu: Vyhláška, kterou se stanoví podmínky pro zařazování prací do kategorií, limitní hodnoty ukazatelů biologických expozičních testů, podmínky odběru biologického materiálu pro provádění biologických
Zákon o zdravotních službách Zákon o specifických zdravotních službách
 Zákon o zdravotních službách Zákon o specifických zdravotních službách 4.jarní konference prezidia ČAS Současná legislativa v českém zdravotnictví JUDr. Milada Džupinková, MBA Právní předpisy upravující
Zákon o zdravotních službách Zákon o specifických zdravotních službách 4.jarní konference prezidia ČAS Současná legislativa v českém zdravotnictví JUDr. Milada Džupinková, MBA Právní předpisy upravující
v1. RS - BEZPEČNOSTNÍ LIST S606 SILICONE THERMAL GREASE Tento výrobek nemá žádné popisné prvky. Tato látka není identifikována jako látka PBT/vPvB.
 RS review date: 01/ /1 Strana: 1 Datum kompilace: 08/10/2015 Revize: 01/12/2016 Číslo revize: 2 Oddíl 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Název produktu: Kód produktu:
RS review date: 01/ /1 Strana: 1 Datum kompilace: 08/10/2015 Revize: 01/12/2016 Číslo revize: 2 Oddíl 1: Identifikace látky/směsi a společnosti/podniku 1.1. Identifikátor výrobku Název produktu: Kód produktu:
Bezpečnostní list. podle nařízení (ES) č. 1907/2006. L2301 Silica 3 Reagent. emea.productstewardship@ge.com
 Strana 1 z 5 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1 Identifikátor výrobku Číslo CAS: Číslo ES: 7757-83-7 231-821-4 1.2 Příslušná určená použití látky nebo směsi a nedoporučená použití
Strana 1 z 5 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1 Identifikátor výrobku Číslo CAS: Číslo ES: 7757-83-7 231-821-4 1.2 Příslušná určená použití látky nebo směsi a nedoporučená použití
V Praze dne 11. července 2008 K čj.: 24722/ENV/08 Čj.: 51699/ENV/08. R o z h o d n u t í
 Ministerstvo životního prostředí odbor environmentálních rizik Rozhodnutí nabylo právní moci 15. červenec 2008. V Praze dne 11. července 2008 K čj.: 24722/ENV/08 Čj.: 51699/ENV/08 R o z h o d n u t í Ministerstvo
Ministerstvo životního prostředí odbor environmentálních rizik Rozhodnutí nabylo právní moci 15. červenec 2008. V Praze dne 11. července 2008 K čj.: 24722/ENV/08 Čj.: 51699/ENV/08 R o z h o d n u t í Ministerstvo
BEZPEČNOSTNÍ LIST (podle Nařízení vlády k (ES) 1907/2006 (REACH) ) Datum vydání: Strana: 1 ze 5 Datum revize: Název výrobku:
 Datum vydání:7.6.2011 Strana: 1 ze 5 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A VÝROBCE A DOVOZCE 1.1 Chemický název látky / obchodní název přípravku Název: Další názvy látky: Číslo výrobku: 1.2 Použití látky
Datum vydání:7.6.2011 Strana: 1 ze 5 1. IDENTIFIKACE LÁTKY / PŘÍPRAVKU A VÝROBCE A DOVOZCE 1.1 Chemický název látky / obchodní název přípravku Název: Další názvy látky: Číslo výrobku: 1.2 Použití látky
Mgr. et Mgr. Lenka Falková. Laboratoř agrogenomiky. Ústav morfologie, fyziologie a genetiky zvířat Mendelova univerzita
 Mgr. et Mgr. Lenka Falková Laboratoř agrogenomiky Ústav morfologie, fyziologie a genetiky zvířat Mendelova univerzita 9. 9. 2015 Šlechtění Užitek hospodářská zvířata X zájmová zvířata Zemědělství X chovatelství
Mgr. et Mgr. Lenka Falková Laboratoř agrogenomiky Ústav morfologie, fyziologie a genetiky zvířat Mendelova univerzita 9. 9. 2015 Šlechtění Užitek hospodářská zvířata X zájmová zvířata Zemědělství X chovatelství
1. Indráková Vanda Změna č.1 na listech č. 1, 3, 4,
 Standardizovaný operační postup (SOP) Číslo dokumentu: SOP-522 Vydání: 2. Výtisk: 1. Zpracoval: MUDr. Koudová Monika Název: Ověřil: ODBĚR BIOLOGICKÉHO MATERIÁLU PRO MOLEKULÁRNĚ GENETICKÉ VYŠETŘENÍ: Mgr.
Standardizovaný operační postup (SOP) Číslo dokumentu: SOP-522 Vydání: 2. Výtisk: 1. Zpracoval: MUDr. Koudová Monika Název: Ověřil: ODBĚR BIOLOGICKÉHO MATERIÁLU PRO MOLEKULÁRNĚ GENETICKÉ VYŠETŘENÍ: Mgr.
Parlament se usnesl na tomto zákoně České republiky:
 Strana 624 Sbírka zákonů č. 61 / 2017 61 ZÁKON ze dne 19. ledna 2017, kterým se mění zákon č. 156/1998 Sb., o hnojivech, pomocných půdních látkách, pomocných rostlinných přípravcích a substrátech a o agrochemickém
Strana 624 Sbírka zákonů č. 61 / 2017 61 ZÁKON ze dne 19. ledna 2017, kterým se mění zákon č. 156/1998 Sb., o hnojivech, pomocných půdních látkách, pomocných rostlinných přípravcích a substrátech a o agrochemickém
Tématické okruhy pro státní závěrečné zkoušky
 Tématické okruhy pro státní závěrečné zkoušky Obor Povinný okruh Volitelný okruh (jeden ze dvou) Forenzní biologická Biochemie, pathobiochemie a Toxikologie a bioterorismus analýza genové inženýrství Kriminalistické
Tématické okruhy pro státní závěrečné zkoušky Obor Povinný okruh Volitelný okruh (jeden ze dvou) Forenzní biologická Biochemie, pathobiochemie a Toxikologie a bioterorismus analýza genové inženýrství Kriminalistické
Návrh VYHLÁŠKA. ze dne. o minimálních požadavcích na některé postupy vymezené vnitřními předpisy
 Návrh VYHLÁŠKA ze dne. o minimálních požadavcích na některé postupy vymezené vnitřními předpisy Ministerstvo zdravotnictví stanoví podle. zákona č. /2009 Sb., o zdravotních službách a podmínkách jejich
Návrh VYHLÁŠKA ze dne. o minimálních požadavcích na některé postupy vymezené vnitřními předpisy Ministerstvo zdravotnictví stanoví podle. zákona č. /2009 Sb., o zdravotních službách a podmínkách jejich
Závěrečná zpráva. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality) PT#M/32/2010 (č. 677) Identifikace herpetických virů
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Organizátor programů zkoušení způsobilosti akreditovaný ČIA, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady Závěrečná zpráva Zkoušení
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Organizátor programů zkoušení způsobilosti akreditovaný ČIA, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady Závěrečná zpráva Zkoušení
IZS a chemický terorismus
 IZS a chemický terorismus Jiří Kassa Katedra toxikologie Fakulta vojenského zdravotnictví UO Hradec Králové TERORISTICKÝ ÚTOK NA WTC New York 11.září 2001 1 TERORISTICKÝ ÚTOK V TOKIJSKÉM METRU 1994 - Matsumoto
IZS a chemický terorismus Jiří Kassa Katedra toxikologie Fakulta vojenského zdravotnictví UO Hradec Králové TERORISTICKÝ ÚTOK NA WTC New York 11.září 2001 1 TERORISTICKÝ ÚTOK V TOKIJSKÉM METRU 1994 - Matsumoto
Závěrečná zpráva. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Téměř polovina Evropanů se mylně domnívá, že antibiotika působí proti nachlazení a chřipce
 TISKOVÁ ZPRÁVA 18. 11. 2014 Téměř polovina Evropanů se mylně domnívá, že antibiotika působí proti nachlazení a chřipce U příležitosti již sedmého Evropského antibiotického dne, který se koná každoročně
TISKOVÁ ZPRÁVA 18. 11. 2014 Téměř polovina Evropanů se mylně domnívá, že antibiotika působí proti nachlazení a chřipce U příležitosti již sedmého Evropského antibiotického dne, který se koná každoročně
Desinfekce a sterilizace. MUDr. Lenka Černohorská, Ph.D.
 Desinfekce a sterilizace MUDr. Lenka Černohorská, Ph.D. Přehled dekontaminačních metod Sterilizace Vyšší stupeň desinfekce Desinfekce Desinsekce Deratizace Zničení všech mikrobů v daném prostředí Zničení
Desinfekce a sterilizace MUDr. Lenka Černohorská, Ph.D. Přehled dekontaminačních metod Sterilizace Vyšší stupeň desinfekce Desinfekce Desinsekce Deratizace Zničení všech mikrobů v daném prostředí Zničení
Havarijní plán PřF UP
 Havarijní plán PřF UP v němž se nakládá s geneticky modifikovanými organismy (GMO), zpracovaný podle 20, odst. 4 zákona č. 78/2004 Sb. pro pracoviště kateder Buněčné biologie a genetiky a Oddělení molekulární
Havarijní plán PřF UP v němž se nakládá s geneticky modifikovanými organismy (GMO), zpracovaný podle 20, odst. 4 zákona č. 78/2004 Sb. pro pracoviště kateder Buněčné biologie a genetiky a Oddělení molekulární
VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ
 HOO/O1 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 15 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 4 6 číslo tkáňové banky: odpovědná osoba:
HOO/O1 VÝROČNÍ ZPRÁVA O ČINNOSTI TKÁŇOVÉHO ZAŘÍZENÍ ROK: 15 tkáňové zařízení: Hematologicko - onkologické oddělení Fakultní nemocnice Plzeň alej Svobody 8, Plzeň 4 6 číslo tkáňové banky: odpovědná osoba:
Používání zdravotnických prostředků v ambulantní praxi
 Používání zdravotnických prostředků v ambulantní praxi Dnem 1. dubna 2015 vstoupil v účinnost nový zákon o zdravotnických prostředcích (zákon č. 268/2014 Sb.), který přináší komplexní zákonnou úpravu regulace
Používání zdravotnických prostředků v ambulantní praxi Dnem 1. dubna 2015 vstoupil v účinnost nový zákon o zdravotnických prostředcích (zákon č. 268/2014 Sb.), který přináší komplexní zákonnou úpravu regulace
BEZPEČNOSTNÍ LIST. podle Nařízení (ES) č. 1907/2006/EC (REACH), ve znění nařízení č. 453/2010/EC Datum vydání: Datum revize: 1.5.
 ODDÍL 1. IDENTIFIKACE LÁTKY / SMĚSI A SPOLEČNOSTI / PODNIKU 1.1 Identifikátor výrobku Název: Registrační číslo: Indexové číslo: Číslo CAS: Číslo ES (EINECS): Další názvy látky: Molární hmotnost: Molekulový
ODDÍL 1. IDENTIFIKACE LÁTKY / SMĚSI A SPOLEČNOSTI / PODNIKU 1.1 Identifikátor výrobku Název: Registrační číslo: Indexové číslo: Číslo CAS: Číslo ES (EINECS): Další názvy látky: Molární hmotnost: Molekulový
Dle EC Direktivy 91/155/EEC Strana 1 z 5
 Dle EC Direktivy 91/155/EEC Strana 1 z 5 1. Identifikace látky nebo přípravku / výrobce nebo dovozce Identifikace produktu Jméno produktu: ClinCal Plasma Calibrator for Catecholamines, lyophilised Objednací
Dle EC Direktivy 91/155/EEC Strana 1 z 5 1. Identifikace látky nebo přípravku / výrobce nebo dovozce Identifikace produktu Jméno produktu: ClinCal Plasma Calibrator for Catecholamines, lyophilised Objednací
Specifická imunitní odpověd. Veřejné zdravotnictví
 Specifická imunitní odpověd Veřejné zdravotnictví MHC molekuly glykoproteiny exprimovány na všech jaderných buňkách (MHC I) nebo jenom na antigen prezentujících buňkách (MHC II) u lidí označovány jako
Specifická imunitní odpověd Veřejné zdravotnictví MHC molekuly glykoproteiny exprimovány na všech jaderných buňkách (MHC I) nebo jenom na antigen prezentujících buňkách (MHC II) u lidí označovány jako
BEZPEČNOSTNÍ LIST NYCOCARD D-DIMER WASHING SOLUTION. 1. POPIS PRODUKTU A VÝROBCE Název produktu: NycoCard D-Dimer Washing Solution Aplikace:
 BEZPEČNOSTNÍ LIST NYCOCARD D-DIMER WASHING SOLUTION 1. POPIS PRODUKTU A VÝROBCE Název produktu: NycoCard D-Dimer Washing Solution Aplikace: Určeno k užití s sety NycoCard D-Dimer. NycoCard D-Dimer Single
BEZPEČNOSTNÍ LIST NYCOCARD D-DIMER WASHING SOLUTION 1. POPIS PRODUKTU A VÝROBCE Název produktu: NycoCard D-Dimer Washing Solution Aplikace: Určeno k užití s sety NycoCard D-Dimer. NycoCard D-Dimer Single
Bezpečnostní list. podle nařízení (ES) č. 1907/2006. Buffer ph 7_1001389-791437-506253-506258-150536. Product Safety/Produktsicherheit
 Strana 1 z 5 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1 Identifikátor výrobku Jiné obchodní název výrobku 1001389; 791437; 506253; 150536 1.2 Příslušná určená použití látky nebo směsi
Strana 1 z 5 ODDÍL 1: Identifikace látky/směsi a společnosti/podniku 1.1 Identifikátor výrobku Jiné obchodní název výrobku 1001389; 791437; 506253; 150536 1.2 Příslušná určená použití látky nebo směsi
Nemocniční hygiena a kvalita. RNDr. Renata Podstatová Úsek hygieny FN Ostrava
 Nemocniční hygiena a kvalita RNDr. Renata Podstatová Úsek hygieny FN Ostrava Hygiena, epidemiologie a protiepidemická opatření Prevence a snižování rizik, redukce a monitorování rizik NN a PI personálu
Nemocniční hygiena a kvalita RNDr. Renata Podstatová Úsek hygieny FN Ostrava Hygiena, epidemiologie a protiepidemická opatření Prevence a snižování rizik, redukce a monitorování rizik NN a PI personálu
BEZPEČNOSTNÍ LIST (podle Nařízení ES č. 1907/2006) CALCIDENT. Datum vydání: 18.7.2013 Strana 1 z 5
 Datum vydání: 18.7.2013 Strana 1 z 5 1. Identifikace látky/směsi a společnosti/podniku 1.1 Identifikace výrobku: Název výrobku: Calcident 1.2 Příslušná určená použití látky nebo směsi a nedoporučená použití:
Datum vydání: 18.7.2013 Strana 1 z 5 1. Identifikace látky/směsi a společnosti/podniku 1.1 Identifikace výrobku: Název výrobku: Calcident 1.2 Příslušná určená použití látky nebo směsi a nedoporučená použití:
b) obsah návrhu na prodloužení platnosti pověření
 Strana 1832 Sbírka zákonů č. 94 / 2016 Částka 38 94 VYHLÁŠKA ze dne 23. března 2016 o hodnocení nebezpečných vlastností odpadů Ministerstvo životního prostředí a Ministerstvo zdravotnictví stanoví podle
Strana 1832 Sbírka zákonů č. 94 / 2016 Částka 38 94 VYHLÁŠKA ze dne 23. března 2016 o hodnocení nebezpečných vlastností odpadů Ministerstvo životního prostředí a Ministerstvo zdravotnictví stanoví podle
102/2012 Sb. VYHLÁŠKA
 102/2012 Sb. VYHLÁŠKA ze dne 22. března 2012 o hodnocení kvality a bezpečí lůžkové zdravotní péče Ministerstvo zdravotnictví stanoví podle 120 zákona č. 372/2011 Sb., o zdravotních službách a podmínkách
102/2012 Sb. VYHLÁŠKA ze dne 22. března 2012 o hodnocení kvality a bezpečí lůžkové zdravotní péče Ministerstvo zdravotnictví stanoví podle 120 zákona č. 372/2011 Sb., o zdravotních službách a podmínkách
SRS - správní úřad rostlinolékařské péče s působností na území ČR
 ČESKÁ REPUBLIKA STÁTNÍ ROSTLINOLÉKAŘSKÁ SPRÁVA STATE PHYTOSANITARY ADMINISTRATION SRS - správní úřad rostlinolékařské péče s působností na území ČR 1. workshop projektu OP VK 2.2: Inovace a rozšíření výuky
ČESKÁ REPUBLIKA STÁTNÍ ROSTLINOLÉKAŘSKÁ SPRÁVA STATE PHYTOSANITARY ADMINISTRATION SRS - správní úřad rostlinolékařské péče s působností na území ČR 1. workshop projektu OP VK 2.2: Inovace a rozšíření výuky
Organizace a kontrola pěstování GM plodin v ČR. Ing. Jana Trnková MZe, odbor rostlinných komodit
 Organizace a kontrola pěstování GM plodin v ČR Ing. Jana Trnková MZe, odbor rostlinných komodit Geneticky modifikované plodiny GM plodiny, transgenní rostliny změněn dědičný materiál (DNA) pomocí genových
Organizace a kontrola pěstování GM plodin v ČR Ing. Jana Trnková MZe, odbor rostlinných komodit Geneticky modifikované plodiny GM plodiny, transgenní rostliny změněn dědičný materiál (DNA) pomocí genových
Imunologie krevní skupiny 109.3059
 Imunologie krevní skupiny 109.3059 Strana 1 z 22 SIMULAČNÍ SOUPRAVA PRO AB0 & Rh TYPIZACI KRVE Strana 2 z 22 SOMERSET educational (Pty) LTD SIMULOVANÉ SOUPRAVY PRO STANOVENÍ KREVNÍ SKUPINY AB0 a Rh FAKTORU
Imunologie krevní skupiny 109.3059 Strana 1 z 22 SIMULAČNÍ SOUPRAVA PRO AB0 & Rh TYPIZACI KRVE Strana 2 z 22 SOMERSET educational (Pty) LTD SIMULOVANÉ SOUPRAVY PRO STANOVENÍ KREVNÍ SKUPINY AB0 a Rh FAKTORU
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace
 Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
Bariérová ošetřovatelská péče.
 Bariérová ošetřovatelská péče https://www.youtube.com/watch?v=yw9gnbgqa1e Bariérová ošetřovatelská péče systém pracovních a organizačních opatření, které mají zabránit vzniku a šíření nozokomiálních nákaz.
Bariérová ošetřovatelská péče https://www.youtube.com/watch?v=yw9gnbgqa1e Bariérová ošetřovatelská péče systém pracovních a organizačních opatření, které mají zabránit vzniku a šíření nozokomiálních nákaz.
VYHLÁŠKA. č. 209/2004 Sb., o bližších podmínkách nakládání s geneticky modifikovanými organismy a genetickými produkty
 VYHLÁŠKA č. 209/2004 Sb., o bližších podmínkách nakládání s geneticky modifikovanými organismy a genetickými produkty Změna: 86/2006 Sb. Změna: 29/2010 Sb. Ministerstvo životního prostředí v dohodě s Ministerstvem
VYHLÁŠKA č. 209/2004 Sb., o bližších podmínkách nakládání s geneticky modifikovanými organismy a genetickými produkty Změna: 86/2006 Sb. Změna: 29/2010 Sb. Ministerstvo životního prostředí v dohodě s Ministerstvem
Závěrečná zpráva. Zkoušení způsobilosti v lékařské mikrobiologii (Externí hodnocení kvality)
 Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
Státní zdravotní ústav Expertní skupina pro zkoušení způsobilosti Poskytovatel programů zkoušení způsobilosti akreditovaný ČIA podle ČSN EN ISO/IEC 17043, reg. č. 7001 Šrobárova 48, 100 42 Praha 10 Vinohrady
