Volibris 5mg Volibris 10mg. Informace pro zdravotníky
|
|
|
- Jakub Šmíd
- před 8 lety
- Počet zobrazení:
Transkript
1 Volibris 5mg Volibris 10mg Informace pro zdravotníky
2 Obsah Úvod 1 Edukační materiály pro pacienty 1 Důležité informace o rizikových faktorech 2 Teratogenita 2 Ženy, které mohou otěhotnět 2 Pokud žena otěhotní při léčbě přípravkem Volibris 4 Mužská plodnost 4 Jaterní funkce 5 Pacienti se zvýšenými jaterními enzymy 5 Edukace pacientů 5 Koncentrace hemoglobinu 6 Dodatečné informace o bezpečnosti 7 Postmarketingový observační program VOLT 8
3 Úvod! Seznamte se, prosím, s úplným zněním Souhrnu údajů o přípravku Volibris ještě předtím, než přípravek předepíšete nebo vydáte. Tato příručka pouze shrnuje některé z nejdůležitějších informací o přípravku Volibris. Volibris je perorálně podávaný ETA-selektivní antagonista endotelinových receptorů (ERA). Volibris je indikován k léčbě pacientů s plicní arteriální hypertenzí (PAH) II. a III. funkční třídy podle klasifikace WHO ke zlepšení zátěžové kapacity. Účinnost byla prokázána u idiopatické PAH a u PAH spojené s onemocněním pojivové tkáně. Léčbu by měl zahajovat pouze lékař, který má zkušenosti s léčbou PAH. Při předepsání přípravku Volibris je třeba: l zajistit, že pacient je schopen dodržovat požadavky na bezpečné užívání přípravku Volibris l poskytnout pacientovi srozumitelným způsobem potřebné rady a informace l předat pacientovi příslušné informační brožurky a připomínkové karty l zvážit předepisování přípravku vždy pouze na 1 měsíc, aby bylo zajištěno vyšetření pacienta v měsíčních intervalech a zhodnocení výsledků důležitých testů před další preskripcí léčiva l vzhledem k tomu, že je databáze údajů o bezpečnosti přípravku Volibris omezená, je doporučeno zařadit pacienty do Postmarketingového observačního programu VOLT l hlásit suspektní nežádoucí účinky a těhotenství. Edukační materiály pro pacienty Při první preskripci přípravku Volibris vydejte pacientům: l brožurku Léčba přípravkem Volibris 5mg (Volibris 10mg) co byste měli vědět, která obsahuje informace a doporučení ohledně léčby přípravkem Volibris. l Kontrolní kartu pacienta, která obsahuje prostor pro záznam kontrolních vyšetření, včetně vyšetření krve, což zajistí, že se pacienti dostaví na kontrolu podle doporučených směrnic. Informace pro zdravotníky 1
4 Brožurka i Informační karta pacienta obsahují místo pro zapsání kontaktních údajů na lékaře a dalších důležitých informací. Informační karta také obsahuje prostor pro záznam vstupních výsledků vyšetření daného pacienta. Pro partnery pacientek, které by mohly otěhotnět a které užívají přípravek Volibris, je určena příručka: l Informace pro partnery pacientek v reprodukčním věku užívajících přípravek Volibris 5mg (Volibris 10mg), která vysvětluje důležitost používání spolehlivé antikoncepce. Důležité informace o rizikových faktorech Teratogenita Studie na zvířatech prokázaly teratogenitu ambrisentanu. Nejsou žádné důkazy o tom, zda je přípravek Volibris teratogenní také u lidí. Volibris je kontraindikován u těhotných a kojících žen. Ženy, které mohou otěhotnět Volibris je kontraindikován u žen, které mohou otěhotnět a které neužívají spolehlivou antikoncepci. Žena která může otěhotnět je žena, která nesplňuje nejméně jedno z následujících kriterií: l věk nejméně 50 let a přirozená zástava menstruace po dobu nejméně 1 roku (amenorea při protinádorové léčbě nevylučuje možnost otěhotnění) l předčasné selhání funkce vaječníků, potvrzené specializovaným gynekologem l další doložená porucha funkce vejcovodů nebo dělohy, která by způsobila sterilitu l anamnéza oboustranné ovariektomie nebo hysterektomie l genotyp XY, Turnerův syndrom nebo ageneze dělohy. Do této skupiny tedy patří i ženy s oligomenoreou, ženy které jsou v perimenopause a mladé ženy, kterým začíná menstruace (ačkoliv Volibris není indikován pro použití u pacientů ve věku do 18 let). 2 Informace pro zdravotníky
5 Pokud máte jakékoliv pochybnosti o možnosti otěhotnění u dané pacientky, nebo o vhodné antikoncepci pro danou pacientku, vyžádejte si odbornou radu gynekologa. Ženy, které by mohly otěhotnět, nesmí začít užívat přípravek Volibris pokud: l neužívají spolehlivou antikoncepci a l nemají negativní těhotenský test. U těchto žen se doporučuje provádět těhotenský test každý měsíc po celou dobu léčby přípravkem Volibris. U žen, které by mohly otěhotnět, je důležité specificky probrat důležitost spolehlivé antikoncepce a zabránění těhotenství. Mezi obecně uznávané účinné metody antikoncepce (to znamená pravděpodobnost selhání méně než 1 % ročně při setrvalém a správném použití a v souladu s příbalovými informacemi) se považují: l perorální antikoncepce, buď kombinovaná nebo samotný gestagen l injekční gestagen l implantáty levonorgestrelu l estrogenní vaginální kroužek l perkutánní antikoncepční náplast l nitroděložní tělísko (IUD) nebo nitroděložní systém (IUS) l sterilizace mužského partnera (vasektomie s doloženou azoospermií) l dvoubarierová metoda: kondom nebo okluzivní klobouček (pesar nebo cervikální klobouček) plus spermicidní látka (pěna/gel/film/ krém/čípek) l pohlavní abstinence. V průběhu léčby pravidelně zdůrazňujte důležitost spolehlivé antikoncepce a zjišťujte, zda-li pacientka dodržuje antikoncepční doporučení. Účinnou antikoncepci je potřeba používat po celou dobu léčby a dále ještě jeden měsíc po ukončení podávání přípravku Volibris. Pokud žena, léčená přípravkem Volibris, musí změnit antikoncepci nebo ukončit její užívání, musí učinit následující kroky: l oznámit lékaři, který předepisuje antikoncepci, že užívá přípravek Volibris l oznámit lékaři, který předepisuje přípravek Volibris, změnu/ukončení užívání antikoncepce. Informace pro zdravotníky 3
6 Zajistěte, že partneři těchto žen také dostanou výtisk Informace pro partnery pacientek v reprodukčním věku užívajících přípravek Volibris 5mg (Volibris 10mg). Ženy, které užívají přípravek Volibris, by měly vědět o riziku poškození plodu. Pokud žena otěhotní při léčbě přípravkem Volibris! l měla by dostat alternativní léčbu PAH l pokud v těhotenství pokračuje, měla by být odeslána na speciální prenatální pracoviště k teratologickému vyšetření a doporučení dalšího postupu. Pacientky, které se domnívají, že mohou být těhotné, by se měly dostavit ke svému lékaři co nejdříve. V takovém případě je nutné co nejdříve provést těhotenský test. Prosíme, hlaste veškerá těhotenství a výsledek těchto těhotenství společnosti GSK. Sem patří i případy zjištěné do 1 měsíce po ukončení léčby (viz kontakt na straně 8). Mužská plodnost Ve studiích na zvířatech bylo dlouhodobé podávání přípravku Volibris spojeno s tubulární atrofií varlat a poruchou fertility. Pacienti by měli být o této skutečnosti informováni. Účinek přípravku Volibris na testikulární funkci u lidí a mužskou plodnost není znám. V klinických studiích nebylo chronické podání ambrisentanu spojeno se změnou v plazmatické koncentraci testosteronu. Pacienti, kteří mají zvláštní obavy z možného účinku ambrisentanu na budoucí plodnost, mohou zvážit uložení vzorku spermatu. 4 Informace pro zdravotníky
7 Jaterní funkce Volibris je kontraindikován u pacientů s těžkým poškozením jater (s cirhózou nebo bez ní) a u pacientů s výchozími hodnotami jaterních aminotransferáz (ALT a/nebo AST) nad trojnásobek horní hranice normy. Při léčbě ERA bylo pozorováno zvýšení jaterních enzymů potenciálně vztažené k léčbě. Proto je nutné před zahájením léčby přípravkem Volibris vyšetřit hodnoty jaterních aminotransferáz (alanin aminotransferáza -[ALT] a aspartát aminotransferáza [AST]). Hodnoty jaterních aminotransferáz (ALT a AST) musí být posouzeny před zahájením léčby a dále pak monitorovány 1x měsíčně. Pacient by měl být také klinicky sledován, zda se u něj nevyskytnou známky či příznaky poškození jater. Pacienti se zvýšenými jaterními enzymy Pokud u pacientů dojde k přetrvávajícímu, nejasnému, klinicky významnému zvýšení hodnot ALT a/nebo AST, nebo pokud je zvýšení ALT a/nebo AST provázeno známkami či příznaky poškození jater (např. žloutenka), přerušte léčbu přípravkem Volibris. Tyto pacienty pečlivě monitorujte. Pokud tito pacienti nemají klinické příznaky poškození jater nebo žloutenku, může být po úpravě hodnot jaterních enzymů zváženo opětovné podávání přípravku Volibris. Zvažte vyžádání odborné konzultace hepatologa. Edukace pacientů Edukujte pacienty o důležitosti pravidelné měsíční kontroly a sledování možných známek a příznaků poškození jater.! Prosíme hlaste společnosti GSK klinicky významné elevace ALT a/ nebo AST nebo jakékoli další nežádoucí účinky vztažené k játrům (viz kontakt na straně 8). Informace pro zdravotníky 5
8 Koncentrace hemoglobinu! Při léčbě ERA, včetně Volibrisu, byl zaznamenán pokles koncentrace hemoglobinu a hladiny hematokritu, a to většinou během prvních 4 týdnů léčby. Později se koncentrace hemoglobinu obvykle stabilizuje. Zahájení léčby přípravkem Volibris se nedoporučuje u pacientů s klinicky významnou anémií. Pacienti léčení přípravkem Volibris by měli mít pravidelně kontrolovánu koncentraci hemoglobinu a/nebo hodnotu hematokritu například po 1 měsíci, po 3 měsících léčby a dále pravidelně v souladu s klinickou praxí. Pokud výsledky vyšetření ukazují klinicky významný pokles hemoglobinu nebo hematokritu a další příčiny jsou vyloučeny, zvažte snížení dávky přípravku Volibris nebo zastavení léčby. Prosíme hlaste klinicky významné poklesy hemoglobinu nebo hematokritu a nežádoucí příhody společnosti GSK (viz kontakt na straně 8). 6 Informace pro zdravotníky
9 Dodatečné informace o bezpečnosti U pacientů s těžkým poškozením funkce ledvin postupujte při zahajování léčby přípravkem Volibris s opatrností. Při léčbě ERA, včetně Volibrisu, jsou popisovány periferní edémy. Mohou být také klinickým důsledkem PAH. V klinických studiích Volibrisu byla většina případů periferních edémů mírného až středně těžkého stupně, zdá se však, že se vyskytoval častěji a že byl závažnější u pacientů nad 65 let. Z post-marketingového sledování je hlášena retence tekutin, ke které došlo během několika týdnů po zahájení léčby přípravkem Volibris. V některých případech bylo nutné k obnovení rovnováhy tekutin podat diuretikum, nebo pacienta hospitalizovat. Dojde-li k rozvoji klinicky významné retence tekutin (s nárůstem tělesné hmotnosti nebo bez něj), proveďte další vyšetření ke stanovení příčiny (např. odlišení vlivu Volibrisu od srdečního selhání) a v případě nutnosti zvažte přerušení léčby Volibrisem. Nežádoucí účinky spojené s přípravkem Volibris jsou shodné s nežádoucími účinky typickými pro ERA: l bolesti hlavy, návaly horka, palpitace, kongesce horních dýchacích cest včetně nosu a vedlejších nosních dutin, sinusitida, nasofaryngitida l gastrointestinální potíže, např. zácpa a bolesti břicha. Případy hypersenzitivity (např. angioedém a vyrážka) byly hlášeny méně často. Informace pro zdravotníky 7
10 Postmarketingový observační program VOLT Domníváme se, že hlavní rizika a možná rizika spojená s přípravkem Volibris již byla identifikována v programu klinického vývoje. Jako u každého nového léku však dosud nebyl zcela objasněn bezpečnostní profil přípravku Volibris v klinické praxi. Proto byl zahájen Postmarketingový observační program VOLT (pro více informací kontaktujte společnost GSK). Proto je důležité, abyste neprodleně hlásili všechna podezření na nežádoucí účinky přípravku Volibris, a tím napomohli k lepšímu objasnění bezpečnostního profilu tohoto přípravku. Navíc je nutné společnosti GSK hlásit veškeré případy těhotenství. Kontaktujte společnost GSK Podezření na nežádoucí účinky a veškerá těhotenství je nutné ohlásit společnosti GSK: GlaxoSmithKline s.r.o. MUDr. Vlasta Trojanová odd. farmakovigilance Na Pankráci 17/ Praha 4 tel.: , fax: cz.safety@gsk.com Reference: SPC Volibris Tento materiál byl připraven na základě požadavku SUKLu a European Medicines Agency. EMA [online] EMA [cit ]. Volibris - Podmínky nebo omezení s ohledem na bezpečné a účinné používání. Dostupné z WWW: < safe_and_effective_use_-_annex_iv/human/000839/wc pdf> 8 Informace pro zdravotníky
11
12 Datum přípravy: 09/2010 CZ/ABT/0003/10
Volibris 5 mg. Volibris 10 mg. ambrisentan. Edukační materiál. potahované tablety. potahované tablety
 Edukační materiál Volibris 5 mg potahované tablety Volibris 10 mg potahované tablety ambrisentan Informace o přípravku VOLIBRIS určená pro zdravotnické pracovníky Obsah Úvod 3 Edukační materiály pro pacienty
Edukační materiál Volibris 5 mg potahované tablety Volibris 10 mg potahované tablety ambrisentan Informace o přípravku VOLIBRIS určená pro zdravotnické pracovníky Obsah Úvod 3 Edukační materiály pro pacienty
Opsumit macitentan 10 mg
 EDUKAČNÍ MATERIÁLY informace pro zdravotnické pracovníky Opsumit macitentan 10 mg Příručka často kladených otázek pro zdravotnické pracovníky q Tento léčivý přípravek podléhá dalšímu sledování. To umožní
EDUKAČNÍ MATERIÁLY informace pro zdravotnické pracovníky Opsumit macitentan 10 mg Příručka často kladených otázek pro zdravotnické pracovníky q Tento léčivý přípravek podléhá dalšímu sledování. To umožní
INFORMACE PRO ZDRAVOTNÍKY O PŘÍPRAVKU BOSENTAN ACCORD
 EDUKAČNÍ MATERIÁLY INFORMACE PRO ZDRAVOTNÍKY O PŘÍPRAVKU BOSENTAN ACCORD Předtím, než předepíšete přípravek Bosentan Accord jakémukoli pacientovi, přečtěte si prosím pečlivě příslušný Souhrn údajů o přípravku.
EDUKAČNÍ MATERIÁLY INFORMACE PRO ZDRAVOTNÍKY O PŘÍPRAVKU BOSENTAN ACCORD Předtím, než předepíšete přípravek Bosentan Accord jakémukoli pacientovi, přečtěte si prosím pečlivě příslušný Souhrn údajů o přípravku.
Volibris co byste měli vědět
 EDUKAČNÍ MATERIÁL Informace pro pacienty, kterým byl předepsán přípravek Volibris. Léčba přípravkem Volibris co byste měli vědět Tato brožurka přináší informace a doporučení týkající se léčby přípravkem
EDUKAČNÍ MATERIÁL Informace pro pacienty, kterým byl předepsán přípravek Volibris. Léčba přípravkem Volibris co byste měli vědět Tato brožurka přináší informace a doporučení týkající se léčby přípravkem
Léčba přípravkem. co byste měli vědět
 Informace pro pacienty, kterým byl předepsán přípravek Volibris. Léčba přípravkem co byste měli vědět Tato brožurka přináší informace a doporučení týkající se léčby přípravkem Volibris. Pečlivě si ji pročtěte
Informace pro pacienty, kterým byl předepsán přípravek Volibris. Léčba přípravkem co byste měli vědět Tato brožurka přináší informace a doporučení týkající se léčby přípravkem Volibris. Pečlivě si ji pročtěte
Edukační materiály. Imnovid (pomalidomid) Informace pro zdravotnické pracovníky
 Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické
Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
PŘÍLOHA I VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ ZMĚNY V REGISTRACI
 PŘÍLOHA I VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ ZMĚNY V REGISTRACI 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) mofetil-mykofenolátu,
PŘÍLOHA I VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ ZMĚNY V REGISTRACI 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) mofetil-mykofenolátu,
EDUKAČNÍ MATERIÁL - Pioglitazone Accord
 Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
TOCTINO (ALITRETINOIN)
 EDUKAČNÍ MATERIÁLY TOCTINO (ALITRETINOIN) PROGRAM PREVENCE TĚHOTENSTVÍ POKYNY PRO LÉKAŘE A LÉKÁRNÍKY Pokyny pro lékaře předepisující TOCTINO Prosíme, abyste si tyto pokyny pečlivě přečetli před tím, než
EDUKAČNÍ MATERIÁLY TOCTINO (ALITRETINOIN) PROGRAM PREVENCE TĚHOTENSTVÍ POKYNY PRO LÉKAŘE A LÉKÁRNÍKY Pokyny pro lékaře předepisující TOCTINO Prosíme, abyste si tyto pokyny pečlivě přečetli před tím, než
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE
 EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH)
 Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE
 LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE Léčba by měla být zahájena a sledována specialistou se zkušenostmi v léčbě revmatoidní artritidy a psoriatické artritidy. Lékař by měl poučit pacienty
LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE Léčba by měla být zahájena a sledována specialistou se zkušenostmi v léčbě revmatoidní artritidy a psoriatické artritidy. Lékař by měl poučit pacienty
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge
 Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge Erivedge může způsobit závažné vrozené vady Může vést
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge Erivedge může způsobit závažné vrozené vady Může vést
EDUKAČNÍ MATERIÁLY. Erivedge (vismodegib) Program prevence početí při léčbě přípravkem Erivedge:
 EDUKAČNÍ MATERIÁLY Erivedge (vismodegib) Program prevence početí při léčbě přípravkem Erivedge: Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Erivedge (vismodegib) Program prevence početí při léčbě přípravkem Erivedge: Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁL. Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid)
 EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
RADA A POUČENÍ LÉKAŘE
 RADA A POUČENÍ LÉKAŘE Obsah: Uživatelky kombinované hormonální antikoncepce Léčebné účinky kombinované hormonální antikoncepce Kontraindikace kombinované hormonální antikoncepce Vysvětlivky: COC = z anglického
RADA A POUČENÍ LÉKAŘE Obsah: Uživatelky kombinované hormonální antikoncepce Léčebné účinky kombinované hormonální antikoncepce Kontraindikace kombinované hormonální antikoncepce Vysvětlivky: COC = z anglického
Důležité informace pro pacienty
 MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Edukační materiál. Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera
 Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Zvažte oddálení podání regadenosonu u pacientů s nekontrolovanou hypertenzí.
 CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Edukační materiály. Imnovid (pomalidomid) Informace pro zdravotnické pracovníky. Brožura pokyny pro bezpečné použití přípravku
 Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pokyny pro bezpečné použití přípravku Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Brožura pokyny
Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pokyny pro bezpečné použití přípravku Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Brožura pokyny
Program prevence těhotenství a expozice plodu Neotigason 10 mg, Neotigason 25 mg tvrdé tobolky acitretinum
 EDUKAČNÍ MATERIÁL Program prevence těhotenství a expozice plodu Neotigason 10 mg, Neotigason 25 mg tvrdé tobolky acitretinum Obsah 1. Úvod k edukačním materiálům 2. Příručka pro lékaře předepisujícího
EDUKAČNÍ MATERIÁL Program prevence těhotenství a expozice plodu Neotigason 10 mg, Neotigason 25 mg tvrdé tobolky acitretinum Obsah 1. Úvod k edukačním materiálům 2. Příručka pro lékaře předepisujícího
Příloha II. Vědecké závěry
 Příloha II Vědecké závěry 74 Vědecké závěry Dne 7. července 2016 zahájila Velká Británie na základě farmakovigilančních údajů postup podle článku 31 směrnice 2001/83/ES a požádalo výbor PRAC, aby přezkoumal
Příloha II Vědecké závěry 74 Vědecké závěry Dne 7. července 2016 zahájila Velká Británie na základě farmakovigilančních údajů postup podle článku 31 směrnice 2001/83/ES a požádalo výbor PRAC, aby přezkoumal
Příloha IV. Vědecké závěry
 Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
PREKLINIKA V KH. MUDr. Lucie Kraváčková Oddělení klinického hodnocení STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 1 PREKLINIKA V KH MUDr. Lucie Kraváčková Oddělení klinického hodnocení 2 Požadavky na prekliniku dle Guideline ICH Topic M3 (R2) (June 2009) 3 R proti předchozí - reduce, refine, replace Studie farmakologie
1 PREKLINIKA V KH MUDr. Lucie Kraváčková Oddělení klinického hodnocení 2 Požadavky na prekliniku dle Guideline ICH Topic M3 (R2) (June 2009) 3 R proti předchozí - reduce, refine, replace Studie farmakologie
RADA A POUČENÍ LÉKAŘE
 RADA A POUČENÍ LÉKAŘE KOMBINOVANÁ HORMONÁLNÍ ANTIKONCEPCE (MOŽNÉ UŽITÍ K YUZPEHO METODĚ) Obsah: a. Uživatelky kombinované hormonální antikoncepce b. Léčebné účinky kombinované hormonální antikoncepce c.
RADA A POUČENÍ LÉKAŘE KOMBINOVANÁ HORMONÁLNÍ ANTIKONCEPCE (MOŽNÉ UŽITÍ K YUZPEHO METODĚ) Obsah: a. Uživatelky kombinované hormonální antikoncepce b. Léčebné účinky kombinované hormonální antikoncepce c.
NeuroBloc. botulinový toxin typu B injekční roztok, U/ml
 NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Zvláštní bezpečnostní informace
 Zvláštní bezpečnostní informace Edukační materiál pro lékaře Součást Plánu řízení rizik léčivého přípravku Arava Schváleno Státním ústavem pro kontrolu léčiv Zvláštní bezpečnostní informace Arava (leflunomid),
Zvláštní bezpečnostní informace Edukační materiál pro lékaře Součást Plánu řízení rizik léčivého přípravku Arava Schváleno Státním ústavem pro kontrolu léčiv Zvláštní bezpečnostní informace Arava (leflunomid),
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Klinické hodnocení u bolestí spojených s endometriózou. Bolest, kterou cítíte, je skutečná... i když to ostatní nevidí. A822523
 Klinické hodnocení u bolestí spojených s endometriózou Bolest, kterou cítíte, je skutečná... i když to ostatní nevidí. A822523 Studie SOLSTICE se provádí v přibližně 200 výzkumných centrech na celém světě.
Klinické hodnocení u bolestí spojených s endometriózou Bolest, kterou cítíte, je skutečná... i když to ostatní nevidí. A822523 Studie SOLSTICE se provádí v přibližně 200 výzkumných centrech na celém světě.
Příloha III. Změny příslušných bodů informace o přípravku
 Příloha III Změny příslušných bodů informace o přípravku Poznámka: Tyto změny v příslušných bodech souhrnu údajů a přípravku a příbalové informace jsou výsledkem postupu přezkoumání. Informace o přípravku
Příloha III Změny příslušných bodů informace o přípravku Poznámka: Tyto změny v příslušných bodech souhrnu údajů a přípravku a příbalové informace jsou výsledkem postupu přezkoumání. Informace o přípravku
Příloha III. Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Klinické hodnocení ARAMIS pro muže s rakovinou prostaty
 Klinické hodnocení ARAMIS pro muže s rakovinou prostaty Brožura pro účastníky DĚKUJEME VÁM, že jste se rozhodl zúčastnit klinického hodnocení ARAMIS pro muže s rakovinou prostaty. V této brožuře najdete
Klinické hodnocení ARAMIS pro muže s rakovinou prostaty Brožura pro účastníky DĚKUJEME VÁM, že jste se rozhodl zúčastnit klinického hodnocení ARAMIS pro muže s rakovinou prostaty. V této brožuře najdete
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy o bezpečnosti (PSUR) pro ibuprofen, ibuprofen-lysin
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy o bezpečnosti (PSUR) pro ibuprofen, ibuprofen-lysin
Příloha I Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
satelitní sympozium společnosti Amgen Když ODPOVĚĎ je výjimečná
 satelitní sympozium společnosti Amgen Když ODPOVĚĎ je výjimečná Vážená paní doktorko, vážený pane doktore, rádi bychom Vás pozvali na satelitní sympozium společnosti Amgen, které proběhne u příležitosti
satelitní sympozium společnosti Amgen Když ODPOVĚĎ je výjimečná Vážená paní doktorko, vážený pane doktore, rádi bychom Vás pozvali na satelitní sympozium společnosti Amgen, které proběhne u příležitosti
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím
 Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ přijetí hlášení společností Roche (den-měsíc-rok): Lokální číslo: AER: OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení:
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ přijetí hlášení společností Roche (den-měsíc-rok): Lokální číslo: AER: OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení:
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
EDUKAČNÍ MATERIÁLY. TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM)
 EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Důležité informace o užívání přípravku TASIGNA
 Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Brožura o antikoncepci - informace pro pacientky užívající perorální izotretinoin
 Brožura o antikoncepci - informace pro pacientky užívající perorální izotretinoin Obsah: A) MÝTY A FALEŠNÁ TVRZENÍ O TĚHOTENSTVÍ...3 B) JAK DOJDE K OTĚHOTNĚNÍ?...3 C) ANTIKONCEPCE: JAK FUNGUJE?...5 I.
Brožura o antikoncepci - informace pro pacientky užívající perorální izotretinoin Obsah: A) MÝTY A FALEŠNÁ TVRZENÍ O TĚHOTENSTVÍ...3 B) JAK DOJDE K OTĚHOTNĚNÍ?...3 C) ANTIKONCEPCE: JAK FUNGUJE?...5 I.
Důležité informace k užívání přípravku Tasigna
 Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
Souhrn doporučení pro předepisujícího lékaře
 G Souhrn doporučení pro předepisujícího lékaře Kritéria výběru pacientů pro léčbu přípravkem GILENYA (fingolimod) Přípravek GILENYA je vhodný pro dospělé pacienty k léčbě vysoce aktivní relabující-remitentní
G Souhrn doporučení pro předepisujícího lékaře Kritéria výběru pacientů pro léčbu přípravkem GILENYA (fingolimod) Přípravek GILENYA je vhodný pro dospělé pacienty k léčbě vysoce aktivní relabující-remitentní
Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pro pacienty. Imnovid (pomalidomid) Brožura pro pacienty.
 Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pro pacienty Imnovid (pomalidomid) Brožura pro pacienty Celgene Strana 1 z 24 Tento přípravek podléhá dalšímu sledování. To umožní
Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pro pacienty Imnovid (pomalidomid) Brožura pro pacienty Celgene Strana 1 z 24 Tento přípravek podléhá dalšímu sledování. To umožní
INFLECTRA SCREENINGOVÝ LIST. a výběru pacientů pro všechny schválené indikace. Obsahuje pokyny ke správnému screeningu
 Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Tablety Bosentan Apotex obsahují bosentan a patří ke skupině léků zvaných antagonisté endothelinových receptorů.
 sp.zn. sukls159189/2012 a sukls 159190/2012 Příbalová informace: informace pro uživatele Bosentan Apotex 62,5 mg potahované tablety Bosentan Apotex 125 mg potahované tablety Bosentanum monohydricum Přečtěte
sp.zn. sukls159189/2012 a sukls 159190/2012 Příbalová informace: informace pro uživatele Bosentan Apotex 62,5 mg potahované tablety Bosentan Apotex 125 mg potahované tablety Bosentanum monohydricum Přečtěte
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
Návod pro pacienta / pečovatele
 Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
PRŮKAZ PACIENTA. užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1
 PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
Příbalová informace: informace pro uživatele. Bosentan Sandoz 62,5 mg Bosentan Sandoz 125 mg potahované tablety. Bosentanum
 Sp.zn. sukls165516/2015 Příbalová informace: informace pro uživatele Bosentan Sandoz 62,5 mg Bosentan Sandoz 125 mg potahované tablety Bosentanum Přečtěte si pozorně celou příbalovou informaci dříve, než
Sp.zn. sukls165516/2015 Příbalová informace: informace pro uživatele Bosentan Sandoz 62,5 mg Bosentan Sandoz 125 mg potahované tablety Bosentanum Přečtěte si pozorně celou příbalovou informaci dříve, než
Biologie člověka Uspořádání pohlavních orgánů Vnitřní pohlavní orgány ženy Ve vaječnících dozrávají vajíčka (největší buňka lidského těla, obsahuje 23
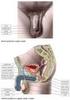 Výchova ke zdraví, sexuální výchova Lekce 3 Obsah: 1) krátké zopakování minulé lekce (anatomické uspořádání pohlavních orgánů a jejich funkce, menstruační cyklus, početí a vývoj plodu, těhotenství ) 2)
Výchova ke zdraví, sexuální výchova Lekce 3 Obsah: 1) krátké zopakování minulé lekce (anatomické uspořádání pohlavních orgánů a jejich funkce, menstruační cyklus, početí a vývoj plodu, těhotenství ) 2)
TOCTINO (ALITRETINOIN) INFORMACE O ANTIKONCEPCI. Obsah 1. FAKTA A MÝTY... 2 2. PREVENCE TĚHOTENSTVÍ A TOCTINO... 2 3. TĚHOTENSKÉ TESTY...
 EDUKAČNÍ MATERIÁLY Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky
EDUKAČNÍ MATERIÁLY Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky
PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta. UTROGESTAN 100 mg, měkké tobolky progesteronum
 sp.zn. sukls125023/2011 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta UTROGESTAN 100 mg, měkké tobolky progesteronum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls125023/2011 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta UTROGESTAN 100 mg, měkké tobolky progesteronum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Your journey inspires ours.
 Lilly Diabetes Your journey inspires ours. V Praze dne 20. ledna 2012 Vážená paní doktorko, vážený pane doktore, v zastoupení společnosti Takeda Pharmaceuticals Europe Ltd. Vám v příloze zasíláme edukační
Lilly Diabetes Your journey inspires ours. V Praze dne 20. ledna 2012 Vážená paní doktorko, vážený pane doktore, v zastoupení společnosti Takeda Pharmaceuticals Europe Ltd. Vám v příloze zasíláme edukační
DODATKY, KTERÉ MAJÍ BÝT DOPLNĚNY DO PŘÍSLUŠNÝCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH NIMESULID (SYSTÉMOVÉ FORMULACE)
 PŘÍLOHA III 1 DODATKY, KTERÉ MAJÍ BÝT DOPLNĚNY DO PŘÍSLUŠNÝCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH NIMESULID (SYSTÉMOVÉ FORMULACE) Dodatky jsou psány kurzívou a podtrženě, vymazané
PŘÍLOHA III 1 DODATKY, KTERÉ MAJÍ BÝT DOPLNĚNY DO PŘÍSLUŠNÝCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH NIMESULID (SYSTÉMOVÉ FORMULACE) Dodatky jsou psány kurzívou a podtrženě, vymazané
EDUKAČNÍ MATERIÁLY. KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
EDUKAČNÍ MATERIÁLY. GILENYA (fingolimod)
 EDUKAČNÍ MATERIÁLY GILENYA (fingolimod) Souhrn doporučení pro předepisující lékaře Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
EDUKAČNÍ MATERIÁLY GILENYA (fingolimod) Souhrn doporučení pro předepisující lékaře Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti.
 Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti. I V A N A K O V Á Ř O V Á C E N T R U M P R O D E M Y E L I N I Z A Č N Í O N E M O C N Ě N Í N E U R O L O G I C
Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti. I V A N A K O V Á Ř O V Á C E N T R U M P R O D E M Y E L I N I Z A Č N Í O N E M O C N Ě N Í N E U R O L O G I C
PRŮKAZ PACIENTA. užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019
 PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Fluorochinolony a riziko prodloužení QT intervalu Finální text SPC a PIL odsouhlasený PhVWP v prosinci 2010
 Fluorochinolony a riziko prodloužení QT intervalu Finální text SPC a PIL odsouhlasený PhVWP v prosinci 2010 Gemifloxacin 1 and moxifloxacin SPC 4.3 Kontraindikace V preklinickém i klinickém hodnocení byly
Fluorochinolony a riziko prodloužení QT intervalu Finální text SPC a PIL odsouhlasený PhVWP v prosinci 2010 Gemifloxacin 1 and moxifloxacin SPC 4.3 Kontraindikace V preklinickém i klinickém hodnocení byly
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy o bezpečnosti (PSUR) letrozolu byly přijaty
Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy o bezpečnosti (PSUR) letrozolu byly přijaty
Příloha IV. Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci
 Příloha IV Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 27 Vědecké závěry Celkové shrnutí vědeckého hodnocení postkoitálních antikoncepčních léčivých přípravků obsahujících levonorgestrel
Příloha IV Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 27 Vědecké závěry Celkové shrnutí vědeckého hodnocení postkoitálních antikoncepčních léčivých přípravků obsahujících levonorgestrel
BAVENCIO (avelumab) Váš průvodce informacemi pro pacienta
 Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Rozměr zavřeného průkazu mm
 Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Doporučený postup Diagnostika a léčba děložních myomů v ambulantní gynekologické péči" Definice
 Doporučený postup Diagnostika a léčba děložních ů v ambulantní gynekologické péči" Definice Myom (leio) monoklonální nádor z hladkých svalových buněk etria. Jedná se o nejčastěji se vyskytující nezhoubný
Doporučený postup Diagnostika a léčba děložních ů v ambulantní gynekologické péči" Definice Myom (leio) monoklonální nádor z hladkých svalových buněk etria. Jedná se o nejčastěji se vyskytující nezhoubný
CZ PAR QUETIAPINUM. Seroquel. UK/W/0004/pdWS/001. NL/W/0004/pdWS/001
 CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Příbalová informace: Informace pro pacienta
 sp.zn.sukls17470/2014 Příbalová informace: Informace pro pacienta ERMM-1 111 MBq/ml, injekční suspenze Erbii-( 169 Er) citras (Citronan erbný-( 169 Er) v koloidní suspenzi) (V této příbalové informaci
sp.zn.sukls17470/2014 Příbalová informace: Informace pro pacienta ERMM-1 111 MBq/ml, injekční suspenze Erbii-( 169 Er) citras (Citronan erbný-( 169 Er) v koloidní suspenzi) (V této příbalové informaci
Příbalová informace: informace pro uživatele. Bosentan Actavis 62,5 mg Bosentan Actavis 125 mg. potahované tablety bosentanum
 sp. zn. sukls93322/2014 a sukls93324/2014 Příbalová informace: informace pro uživatele 62,5 mg 125 mg potahované tablety bosentanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp. zn. sukls93322/2014 a sukls93324/2014 Příbalová informace: informace pro uživatele 62,5 mg 125 mg potahované tablety bosentanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Sp. zn. sukls132399/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pioglitazon Apotex 15 mg tablety Pioglitazon Apotex 30 mg tablety Pioglitazon Apotex 45 mg tablety Pioglitazonum Přečtěte si pozorně
Sp. zn. sukls132399/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pioglitazon Apotex 15 mg tablety Pioglitazon Apotex 30 mg tablety Pioglitazon Apotex 45 mg tablety Pioglitazonum Přečtěte si pozorně
Příloha II. Vědecké závěry a zdůvodnění zrušení či změny podmínek rozhodnutí o registraci a podrobné vysvětlení rozdílů oproti doporučení výboru PRAC
 Příloha II Vědecké závěry a zdůvodnění zrušení či změny podmínek rozhodnutí o registraci a podrobné vysvětlení rozdílů oproti doporučení výboru PRAC 68 Vědecké závěry Koordinační skupina pro vzájemné uznávání
Příloha II Vědecké závěry a zdůvodnění zrušení či změny podmínek rozhodnutí o registraci a podrobné vysvětlení rozdílů oproti doporučení výboru PRAC 68 Vědecké závěry Koordinační skupina pro vzájemné uznávání
Příloha III. Úpravy příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy příslušných bodů souhrnu údajů o přípravku a příbalové informace 26 Stávající informace o přípravcích se mění (vložení, náhrada nebo zrušení textu podle potřeby) tak, aby odpovídaly
Příloha III Úpravy příslušných bodů souhrnu údajů o přípravku a příbalové informace 26 Stávající informace o přípravcích se mění (vložení, náhrada nebo zrušení textu podle potřeby) tak, aby odpovídaly
Příbalová informace: informace pro pacienta. Maltofer, 10 mg/ml sirup. polymaltosum ferricum
 sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům
 25 January 2018 EMA/PRAC/35612/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům Přijato na zasedání výboru PRAC konaném
25 January 2018 EMA/PRAC/35612/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům Přijato na zasedání výboru PRAC konaném
EXELON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY
 XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
PROVERA 5 mg tablety (medroxyprogesteroni acetas)
 Příbalová informace: Informace pro uživatele PROVERA 5 mg tablety (medroxyprogesteroni acetas) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: Informace pro uživatele PROVERA 5 mg tablety (medroxyprogesteroni acetas) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Co byste měl(a) vědět o léčivém přípravku
 Co byste měl(a) vědět o léčivém přípravku Důležité bezpečnostní informace pro pacienty léčené přípravkem MabThera 1 Co byste měl(a) vědět o přípravku MabThera Pokud máte revmatoidní artritidu (RA), granulomatózu
Co byste měl(a) vědět o léčivém přípravku Důležité bezpečnostní informace pro pacienty léčené přípravkem MabThera 1 Co byste měl(a) vědět o přípravku MabThera Pokud máte revmatoidní artritidu (RA), granulomatózu
Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel)
 EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
Edukační materiál. Yervoy (ipilimumab) Časté otázky Brožura pro. zdravotníky
 Edukační materiál Yervoy (ipilimumab) Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Tento léčivý
Edukační materiál Yervoy (ipilimumab) Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Tento léčivý
Příbalová informace: informace pro uživatelku. POSTINOR mikrogramů tablety levonorgestrelum
 Příbalová informace: informace pro uživatelku POSTINOR-2 750 mikrogramů tablety levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Příbalová informace: informace pro uživatelku POSTINOR-2 750 mikrogramů tablety levonorgestrelum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje
Možná Vás bude zajímat klinické hodnocení (studie) AZURE.
 Příručka pacienta Bylo Vám diagnostikováno onemocnění se syndromem chronické pánevní bolesti? Zažili jste pánevní bolest nebo nepříjemné pocity po dobu nejméně 3 z posledních 6 měsíců? Jste starší 18 let?
Příručka pacienta Bylo Vám diagnostikováno onemocnění se syndromem chronické pánevní bolesti? Zažili jste pánevní bolest nebo nepříjemné pocity po dobu nejméně 3 z posledních 6 měsíců? Jste starší 18 let?
Informační brožura. pro pacientky a pacienty užívající perorální izotretinoin
 Informační brožura pro pacientky a pacienty užívající perorální izotretinoin Informace pro ženy a muže užívající perorální izotretinoin Dokument slouží k minimalizaci rizika při užívání perorálního izotretinoinu.
Informační brožura pro pacientky a pacienty užívající perorální izotretinoin Informace pro ženy a muže užívající perorální izotretinoin Dokument slouží k minimalizaci rizika při užívání perorálního izotretinoinu.
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g masti obsahuje calcitriolum 0,003 mg (3 mikrogramy). Úplný seznam pomocných látek viz bod 6.1.
 Sp. zn. sukls155368/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Silkis mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g masti obsahuje calcitriolum 0,003 mg (3 mikrogramy). Úplný seznam pomocných
Sp. zn. sukls155368/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Silkis mast 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 g masti obsahuje calcitriolum 0,003 mg (3 mikrogramy). Úplný seznam pomocných
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Flexove 625 mg tablety. Glukosaminum
 sp.zn.sukls163996/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Flexove 625 mg tablety Glukosaminum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechejte
sp.zn.sukls163996/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Flexove 625 mg tablety Glukosaminum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechejte
PŘÍLOHA III DODATKY K SOUHRN ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACI
 PŘÍLOHA III DODATKY K SOUHRN ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACI 1 DODATKY MAJÍ BÝT ZAŘAZENY DO ODPOVÍDAJÍCÍCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH MOXIFLOXACIN Následující
PŘÍLOHA III DODATKY K SOUHRN ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACI 1 DODATKY MAJÍ BÝT ZAŘAZENY DO ODPOVÍDAJÍCÍCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH MOXIFLOXACIN Následující
KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin. Informace pro lékaře EU
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
Psychofarmaka a gravidita. MUDr. Zdeňka Vyhnánková
 Psychofarmaka a gravidita MUDr. Zdeňka Vyhnánková ZÁKLADNÍ PRAVIDLA PRO FARMAKOTERAPII V TĚHOTENSTVÍ nemoc většinou znamená větší riziko než léčba indikace by měla být podložená a ne alibistická většina
Psychofarmaka a gravidita MUDr. Zdeňka Vyhnánková ZÁKLADNÍ PRAVIDLA PRO FARMAKOTERAPII V TĚHOTENSTVÍ nemoc většinou znamená větší riziko než léčba indikace by měla být podložená a ne alibistická většina
