Důležité informace pro lékaře o závažných rizicích spojených s přípravkem CAPRELSA (vandetanibum)
|
|
|
- Pavlína Doležalová
- před 6 lety
- Počet zobrazení:
Transkript
1 EDUKAČNÍ MATERIÁL Důležité informace pro lékaře o závažných rizicích spojených s přípravkem CAPRELSA (vandetanibum) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Vážná rizika pro pediatrickou a dospělou populaci. U pacientů, u nichž mutace Rearranged during Transfection (RET) není známa nebo je negativní, je třeba před provedením individuálního rozhodnutí o léčbě zohlednit možnost nízkého přínosu. VAROVÁNÍ: PRODLOUŽENÍ INTERVALU QTc, TORSADES DE POINTES, NÁHLÉ ÚMRTÍ A SYNDROM REVERZIBILNÍ ZADNÍ ENCEFALOPATIE (PRES) OZNAČOVANÝ TÉŽ JAKO SYNDROM REVERZIBILNÍ ZADNÍ LEUKOENCEFALOPATIE (RPLS) Přípravek CAPRELSA může prodloužit interval QTc. U pacientů užívajících přípravek CAPRELSA byly hlášeny případy torsades de pointes, náhlého úmrtí a syndromu PRES (označovaného též jako RPLS). Přípravek CAPRELSA by se neměl používat u pacientů s hypokalcémii, hypokalémií nebo hypomagnesemií. Léčba přípravkem CAPRELSA nesmí být zahájena u pacientů o s intervalem QTc > 480 ms, o kteří mají vrozený syndrom dlouhého intervalu QTc o kteří mají v anamnéze torsades de pointes, pokud u nich nebyly korigovány všechny rizikové faktory přispívající k torsades de pointes. o Hypokalcémie, hypokalémie a/nebo hypomagnesemie musí být upraveny před podáním přípravku CAPRELSA a měly by být pravidelně sledovány. Souběžné podávání přípravku CAPRELSA s léky, které prodlužují interval QTc, je kontraindikováno nebo se nedoporučuje. Kombinace kontraindikované: cisaprid, intravenózní erythromycin (i.v.), toremifen, mizolastin, moxifloxacin, arsen, antiarytmika třídy IA a III. Kombinace, které se nedoporučují: methadon, haloperidol, amisulprid, chlorpromazin, sulpirid, zuklopenthixol, halofantrin, pentamidin a lumefantrin. GZCS.CAPR
2 Pokud je přesto nezbytné podávat lék, o němž je známo, že prodlužuje interval QTc, doporučuje se častější monitorování EKG. Vzhledem k poločasu 19 dnů je třeba provést EKG vyšetření z důvodu sledování intervalu QTc před zahájením léčby a dále 1, 3, 6 a 12 týdnů po zahájení léčby přípravkem CAPRELSA, a následně každé 3 měsíce po dobu nejméně jednoho roku. Po případném snížení dávky z důvodu prodloužení intervalu QTc nebo při jakémkoliv přerušení léčby na dobu delší než 2 týdny je třeba provést vyhodnocení intervalu QTc, jak je popsáno výše. Vzhledem k poločasu 19 dnů nemusí nežádoucí účinky, včetně prodloužení intervalu QTc, rychle odeznít. Zajistěte náležité sledování. Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí být hlášeny Státnímu ústavu pro kontrolu léčiv. Podrobnosti o hlášení najdete na: Adresa pro zasílání je Státní ústav pro kontrolu léčiv, oddělení farmakovigilance, Šrobárova 48, Praha 10, 41, farmakovigilance@sukl.cz Tato informace může být také hlášena společnosti sanofi-aventis, s.r.o., Evropská 846/176, Praha, PRG.CZ_PHV@sanofi.com
3 Lékaři předepisující přípravek CAPRELSA (vandetanibum) by měli: Prostudovat edukační materiály pro zdravotnické pracovníky a úplnou informaci o přípravu CAPRELSA, včetně: informace o rizicích, včetně prodloužení intervalu QTc, torsades de pointes, náhlého úmrtí a syndromu PRES (označovaného také jako RPLS) důležitých informací pro výběr pacientů, požadavků na EKG vyšetření a sledování elektrolytů, informací o lékových interakcích. Zkontrolovat kartu pacienta a vysvětlit její význam a použití pacientům, kteří budou užívat přípravek CAPRELSA. Pacient by měl obdržet kartu pro pacienta při každém předepsání léku. Je důležité poučit pacienty o riziku prodloužení intervalu QTc a syndromu PRES a informovat pacienty o tom, s jakými příznaky a projevy musí být obeznámeni a jaká opatření mají uplatňovat.
4 Prodloužení QT intervalu, torsades de pointes a náhlé úmrtí U pacientů užívajících přípravek CAPRELSA byly hlášeny případy torsades de pointes, komorové tachykardie a náhlého úmrtí. Vandetanib v dávce je spojen s podstatným a na koncentraci závislým prodloužením intervalu QTc (v průměru 28 ms, medián 35 ms). K prvnímu prodloužení intervalu QTc dochází nejčastěji v průběhu prvních 3 měsíců léčby, ale může se objevit i později. Prodloužení intervalu QTc je zvláště problematické s ohledem na poločas vandetanibu (19 dnů). Průjem může způsobit nerovnováhu elektrolytů, která může zvýšit riziko prodloužení intervalu QTc na elektrokardiogramu (EKG). Lékové interakce Kontraindikované kombinace: cisaprid, nitrožilní (i.v.) erythromycin, toremifen, mizolastin, moxifoxacin, arsen a antiarytmika třídy IA a III, Nedoporučené kombinace: ondansetron, amisulprid, chlorpromazin, haloperidol, sulpirid, zuclopenthixol, halofantrin, pentamidin, lumefantrin a methadon. Pokud není k dispozici žádná vhodná alternativní léčba, mohou se použít nedoporučené kombinace s přípravkem CAPRELSA za podmínky, že bude zajištěno další monitorování intervalu QTc pomocí EKG, vyhodnocení elektrolytů a budou provedeny další kontroly při nástupu nebo zhoršení průjmu. Důležité informace pro výběr pacientů Nepoužívejte přípravek CAPRELSA u pacientů s vrozeným syndromem dlouhého intervalu QTc. Léčba přípravkem CAPRELSA nesmí být zahájena u pacientů s intervalem QTc > 480 ms. Přípravek CAPRELSA by se neměl podávat pacientům, kteří mají v anamnéze: torsades de pointes, bradyarytmie, nekompenzované srdeční selhání. Přípravek CAPRELSA nebyl studován u pacientů s komorovými arytmiemi nebo nedávným infarktem myokardu. Další informace U pacientů s preexistující hypertenzí je třeba před zahájením léčby zajistit kompenzaci krevního tlaku. Mezi nežádoucí účinky přípravku patří únava, slabost a úbytek hmotnosti; výskyt některého z těchto stavů, zejména u starších pacientů, může zvýšit riziko vzniku pneumonie.
5 Monitorování EKG Doporučení pro monitorování EKG a hladiny elektrolytů ( K+, Mg+, Ca+, TSH) EKG i stanovení sérové hladiny draslíku, vápníku, hořčíku a hormonu stimulujícího štítnou žlázu (TSH) je třeba provést: na počátku léčby, 1, 3, 6 a 12 týdnů po zahájení léčby a poté každé 3 měsíce po dobu alespoň jednoho roku další EKG vyšetření a krevní testy během této periody a po jejím ukončení je třeba provést v klinicky indikovaných případech, po jakékoli redukci dávky z důvodu prodloužení intervalu QTc nebo po každém přerušení dávky na dobu > 2 týdny (provádějte sledování, jak je popsáno výše). Pacienti, u nichž se jednorázově vyskytne hodnota intervalu QTc 500 ms, musí o přerušit užívání přípravku CAPRELSA. o Dávkování může být obnoveno při snížené dávce po potvrzeném návratu intervalu QTc do stavu před léčbou a korekci případné nerovnováhy elektrolytů. Pokud dojde k výraznému zvýšení intervalu QTc, který však zůstane pod hodnotou 500 ms, je třeba požádat o konzultaci kardiologa. Ke snížení rizika prodloužení intervalu QTc: o je třeba udržovat sérové hladiny draslíku, hořčíku a vápníku v normálním rozmezí. Syndrom reverzibilní zadní encefalopatie (syndrom reverzibilní zadní leukoencefalopatie) Syndrom reverzibilní zadní encefalopatie (PRES) označovaný též jako syndrom reverzibilní zadní leukoencefalopatie (PRLS) je syndrom subkortikálního vazogenního edému diagnostikovaný při MRI mozku. Syndrom PRES byl u pacientů léčených přípravkem CAPRELSA pozorován s frekvencí méně často ( 1/0 až < 1/). Tento syndrom je třeba zvážit u každého pacienta, u kterého se vyskytnou záchvaty, bolesti hlavy, poruchy zraku, zmatenost nebo změny mentálních funkcí. Pacienti by měli být informováni o příznacích syndromu PRES a měli by být vyzváni, aby neprodleně kontaktovali lékaře, pokud se u nich objeví některý z uvedených příznaků. Pokud se u pacienta vyskytne jakýkoli příznak naznačující syndrom PRES, doporučuje se, aby lékaři u daného pacienta neprodleně provedli MRI vyšetření mozku.
6 Rizika platná pouze pro pediatrickou populaci: Potenciální riziko abnormalit zubů a kostí V preklinických studiích prováděných u mladých psů a potkanů, kterým byl podáván vandetanib, byly pozorovány případy fyzární dysplázie s otevřenými růstovými ploténkami a vliv na zuby. Tyto účinky byly důsledkem inhibice receptoru pro vaskulární endoteliální růstový faktor (VEGFR) nebo receptoru pro epidermální růstový faktor (EGFR) vandetanibem. V předklinických studiích zaměřených na jiné antiangiogenní látky zacílené na VEGF byla navíc zjištěna suprese růstu trabekulární kosti v oblasti epifyzární růstové ploténky. Ve studii fáze I/II hodnotící vandetanib v National Institute of Health (NIH), realizované u dětí a dospívajících (věk 5-17 let) s medulárním karcinomem štítné žlázy, bylo provedeno sériové MRI vyšetření kolene (13 pacientů) ke kvantifikaci objemu růstové ploténky za účelem monitorování potenciální kostní toxicity a při každé návštěvě pacienta byl monitorován lineární růst. Bylo zjištěno, že vandetanib nenarušuje lineární růst. Vzhledem k výsledkům z neklinických studií jsou však abnormality zubů a kostí v pediatrické populaci považovány za důležité potenciální riziko, a jako takové by měly být pečlivě sledovány. Potenciální riziko chyb při medikaci Pro zamezení možnému riziku chyb při medikaci v důsledku různých dávkovacích režimů musíte postupovat následujícím způsobem: přečtěte si pokyny pro předepisování u pediatrických pacientů, vyplňte přehled dávkování a monitorování pacienta (denní kontrolní tabulku) při prvním předepsání léku a při každé další úpravě dávky.
7 Část 2: Pokyny pro lékaře ohledně předepisování a monitorování léčby přípravkem Caprelsa u pediatrických pacientů Pro zamezení možnému riziku omylů a chyb při medikaci v důsledku různých dávkovacích režimů musíte zároveň vyplnit přehled dávkování a monitorování pacienta (denní kontrolní tabulku) při prvním předepsání léku a pak při každé další úpravě dávky. Přípravek Caprelsa je indikován u dětí nad 5 let a dospívajících s tělesným povrchem (BSA) 0,7 m 2. U pacientů, u nichž mutace Rearranged during Transfection (RET) není známa nebo je negativní, je třeba před provedením individuálního rozhodnutí o léčbě zohlednit možnost nízkého přínosu. Přípravek se dodává ve formě tablet s okamžitým uvolňováním léčivé látky ve dvou různých silách. Tablety - - vyražený symbol Z na jedné straně. Tablety - - vyražený symbol Z na jedné straně.
8 Výpočet dávky Stanovení dávky u pediatrických pacientů se má provádět na základě hodnoty BSA v /m 2 vypočtené podle následujícího vzorce (nebo podle jiného vzorce přizpůsobeného pro dětské pacienty): Příklad výpočtu dávky Pokud má pacient výšku = 125 cm a hmotnost = 35 kg Hodnotu BSA je třeba zaokrouhlit na 2 desetinná místa. Dávkovací režimy přípravku Caprelsa podle hodnoty BSA pacienta K dispozici jsou 4 hlavní dávkovací režimy, Každý režim zahrnuje zahajovací dávku, kterou lze následně změnit na: zvýšenou dávku, pokud je vandetanib dobře tolerován po 8 týdnech léčby zahajovací dávkou, sníženou dávku, v případě nežádoucích vedlejších účinků. V závislosti na jednotlivých případech odpovídá režim dávkování jednomu ze 3 následujících režimů: * režim jednou denně (stejná dávka každý den: D1 = D2 = D3, atd.) * režim obden (stejná dávka každý druhý den D1 = D3 = D5, atd.) * 7-denní režim (dvě dávky střídavě; mějte na paměti, že D1 = D8, což zahrnuje 2 po sobě jdoucí dny se stejnou dávkou)
9 Tabulka 1: Dávkovací nomogram pro pediatrické pacienty s MTC BSA (m 2 ) Zahajovací dávka* () Zvýšení dávky () pokud je dobře tolerováno po 8 týdnech léčby zahajovací dávkou Snížení dávky () 0,7 - <0,9 obden jednou denně - 0,9 - <1,2 jednou denně 1,2 - <1,6 7denní schéma: denní schéma: ,6 jednou denně jednou denně obden jednou denně jednou denně 7denní schéma: Dávky vandetanibu vyšší než 150 /m 2 nebyly u pediatrických pacientů v klinických studiích použity. Celková denní dávka u dětí nesmí být vyšší než. Poškození ledvin Nejsou žádné zkušenosti s užíváním vandetanibu u pediatrických pacientů s poruchou funkce ledvin. U dětí se středně těžkou poruchou funkce ledvin, lze použít sníženou dávku, jak je uvedeno v tabulce 1. Ze strany lékaře je vyžadován Individuální přístup k léčbě pacientů, a to zejména u dětských pacientů s malým BSA. U dětských pacientů s těžkou poruchou funkce ledvin se vandetanib nedoporučuje. U dětí s poruchou funkce jater se vandetanib nedoporučuje. Pacienti, u nichž se vyskytnou nežádoucí účinky vyžadující snížení dávky, by měli přerušit užívání vandetanibu minimálně na dobu jednoho týdne. Léčba může být obnovena ve snížené dávce, jakmile dojde k plnému zotavení z nežádoucích účinků. V případě toxicity stupně 3 nebo vyšší nebo prodloužení intervalu QTc na EKG je třeba dávkování vandetanibu alespoň dočasně přerušit a znovu zahájit sníženou dávkou po odeznění toxických projevů nebo zlepšení toxicity na stupeň 1 podle CTCAE: u pacientů, kteří jsou na zahajovací dávce, je třeba obnovit léčbu pomocí snížené dávky, u pacientů, kteří jsou na zvýšené dávce, je třeba obnovit léčbu pomocí zahajovací dávky. V případě dalšího výskytu toxicity stupně 3 nebo vyšší nebo prodloužení intervalu QTc na EKG je třeba dávkování vandetanibu alespoň dočasně přerušit a znovu zahájit sníženou dávkou až po odeznění toxických projevů nebo zlepšení toxicity na stupeň 1 podle CTCAE. V případě dalšího výskytu toxicity stupně 3 nebo vyšší podle CTCAE nebo při dalším prodloužení intervalu QTc na EKG je třeba léčbu vandetanibem trvale ukončit.
10 Zvýšená dávka b Zahajovací dávka a Dávka Pacient musí být vhodným způsobem monitorován (viz poslední část pokynů a oddíl 4.4 souhrnu údajů o přípravku). Nežádoucí účinky včetně prodloužení intervalu QTc nemusí vzhledem k 19-dennímu poločasu odeznít rychle. Podrobná doporučení podle hodnot BSA pro 14denní schéma léčby (tabulky 2 až 5) Mějte na paměti, že 7-denní schéma zahrnuje 2 po sobě jdoucí dny se stejnou dávkou. Tabulka 2: Režim pro dávkování přípravku Caprelsa u dětí s BSA 0,7 m 2 až <0,9 m 2 * Po 8 týdnech * Snížená dávka není použitelná: v případě výskytu nežádoucích účinků musí být léčba přerušena, jak je popsáno výše.
11 Snížená dávka c Zvýšená dávka b Zahajovací dávka a Dávka Tabulka 3: Režim pro dávkování přípravku Caprelsa u dětí s BSA 0,9 m 2 až <1,2 m 2 Po 8 týdnech Při výskytu nežádoucích účinků vyžadujících snížení dávky následně po týdenní přerušení léčby Vyšší dávky než 150 /m2 vandetanibu nebyly u pediatrických pacientů v klinických studiích použity. c Pacienti, u nichž se vyskytnou nežádoucí účinky vyžadující snížení dávky, by měli přerušit užívání vandetanibu minimálně na dobu jednoho týdne. Léčba může být obnovena ve snížené dávce, jakmile nežádoucí účinky plně odezní.
12 Snížená dávka c Zvýšená dávka b Zahajovací dávka a Dávka Tabulka 4: Režim pro dávkování přípravku Caprelsa u dětí s BSA 1,2m 2 až <1,6 m 2 Po 8 týdnech Při výskytu nežádoucích účinků vyžadujících snížení dávky následně po týdenní přerušení léčby Vyšší dávky než 150 /m2 vandetanibu nebyly u pediatrických pacientů v klinických studiích použity. c Pacienti, u nichž se vyskytnou nežádoucí účinky vyžadující snížení dávky, by měli přerušit užívání vandetanibu minimálně na dobu jednoho týdne. Léčba může být obnovena ve snížené dávce, jakmile nežádoucí účinky plně odezní.
13 Snížená dávka c Zvýšená dávka b Zahajovací dávka a Dávka Tabulka 5: Režim pro dávkování přípravku Caprelsa u dětí s BSA 1,6 m 2 Po 8 týdnech Při výskytu nežádoucích účinků vyžadujících snížení dávky následně po týdenní přerušení léčby Vyšší dávky než 150 /m2 vandetanibu nebyly u pediatrických pacientů v klinických studiích použity. c Pacienti, u nichž se vyskytnou nežádoucí účinky vyžadující snížení dávky, by měli přerušit užívání vandetanibu minimálně na dobu jednoho týdne. Léčba může být obnovena ve snížené dávce, jakmile nežádoucí účinky plně odezní.
14 Způsob podávání Vypočtená dávka by se měla užívat s jídlem nebo bez jídla zhruba ve stejnou denní dobu. U pacientů, kteří mají potíže s polykáním, lze tablety s vandetanibem dispergovat v polovině sklenky nesycené pitné vody. Neměla by se používat jiná tekutina. Tableta se vhodí do vody a bez drcení se míchá, až se rozpadne (asi 10 minut) a vzniklá disperze se ihned vypije. Ulpělé částice se znovu dispergují v polovině sklenky vody a vypijí. Tuto disperzi je možné podat též nasogastrickou sondou nebo přes gastrostomickou trubici. Pokud dojde k vynechání dávky u dětských pacientů dodržujících léčebný režim jednou denně, je třeba užít dávku vandetanibu co nejdříve, jakmile si pacient nebo jeho pečovatel vzpomene. Pokud do další dávky zbývá méně než 12 hodin, pacient si vynechanou dávku nevezme. Pacient by neměl užívat dvojnásobnou dávku (dvě dávky ve stejnou dobu), aby nahradil zapomenutou dávku. Průvodce dávkováním a monitorováním pro dětské pacienty a ošetřovatele pacientů léčených vandetanibem. Pacienti léčení vandetanibem a/nebo jejich ošetřovatelé musí obdržet pokyny ohledně dávkování a pohotovostní kartu pro pacienta, jejichž účelem je: informovat pacienta nebo jeho pečovatele a případně zdravotnické pracovníky o rizicích spojených s léčbou vandetanibem a s dávkovacími režimy, podpořit dodržování a monitorování léčby s cílem snížit riziko vedlejších účinků a omylů a chyb při medikaci. Lékař musí vyplnit do části pro předepisujícího lékaře" hodnotu BSA pacienta a doporučený dávkovací režim. Pacient musí denně vyplňovat kontrolní přehled, včetně možnosti přidávat komentáře. Na počátku léčby a při každé následné úpravě dávky (zvýšení, snížení, nebo změna rozmezí BSA) je zapotřebí použít nový list denního kontrolního přehledu, která se předá pacientovi nebo jeho pečovateli. Společně s pokyny pro lékaře je třeba předat také souhrn údajů o přípravku
CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití)
 CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Fluorochinolony a riziko prodloužení QT intervalu Finální text SPC a PIL odsouhlasený PhVWP v prosinci 2010
 Fluorochinolony a riziko prodloužení QT intervalu Finální text SPC a PIL odsouhlasený PhVWP v prosinci 2010 Gemifloxacin 1 and moxifloxacin SPC 4.3 Kontraindikace V preklinickém i klinickém hodnocení byly
Fluorochinolony a riziko prodloužení QT intervalu Finální text SPC a PIL odsouhlasený PhVWP v prosinci 2010 Gemifloxacin 1 and moxifloxacin SPC 4.3 Kontraindikace V preklinickém i klinickém hodnocení byly
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE
 EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL - Pioglitazone Accord
 Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Caprelsa 100 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje vandetanibum 100 mg. Úplný seznam pomocných
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Caprelsa 100 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje vandetanibum 100 mg. Úplný seznam pomocných
Edukační materiál. Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera
 Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III. Úpravy příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace jsou výsledkem referral procedury. Informace o přípravku
Příloha III Úpravy příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace jsou výsledkem referral procedury. Informace o přípravku
CZ PAR. QUETIAPINI FUMARAS Seroquel. UK/W/0004/pdWS/001 NL/W/0004/pdWS/001
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
PRŮKAZ PACIENTA. užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1
 PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
CZ PAR QUETIAPINUM. Seroquel. UK/W/0004/pdWS/001. NL/W/0004/pdWS/001
 CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
PŘÍLOHA III DODATKY K SOUHRN ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACI
 PŘÍLOHA III DODATKY K SOUHRN ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACI 1 DODATKY MAJÍ BÝT ZAŘAZENY DO ODPOVÍDAJÍCÍCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH MOXIFLOXACIN Následující
PŘÍLOHA III DODATKY K SOUHRN ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACI 1 DODATKY MAJÍ BÝT ZAŘAZENY DO ODPOVÍDAJÍCÍCH BODŮ SOUHRNU ÚDAJŮ O PŘÍPRAVKU LÉČIVÝCH PŘÍPRAVKŮ OBSAHUJÍCÍCH MOXIFLOXACIN Následující
CZ PAR. QUETIAPINI FUMARAS Seroquel. NL/W/0004/pdWS/002
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Zvažte oddálení podání regadenosonu u pacientů s nekontrolovanou hypertenzí.
 CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
EDUKAČNÍ MATERIÁLY. TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM)
 EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH)
 Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Doporučení pro dávkování a způsob podávání přípravku Tasigna
 Klinické studie a přípravek Tasigna Ukázalo se, že přípravek Tasigna u některých pacientů prodlužuje QT interval. V klinické studii fáze II u pacientů s CML s přítomností Ph chromozomu v chronické či akcelerované
Klinické studie a přípravek Tasigna Ukázalo se, že přípravek Tasigna u některých pacientů prodlužuje QT interval. V klinické studii fáze II u pacientů s CML s přítomností Ph chromozomu v chronické či akcelerované
Kulaté bikonvexní bílé potahované tablety s vyraženým Z100 na jedné straně.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí
SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí
Oválné bikonvexní bílé potahované tablety s vyraženým Z300 na jedné straně.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí
SOUHRN ÚDAJŮ O PŘÍPRAVKU Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí
Rozměr zavřeného průkazu mm
 Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
PRŮKAZ PACIENTA. užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019
 PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
EDUKAČNÍ MATERIÁL. Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid)
 EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
INFLECTRA SCREENINGOVÝ LIST. a výběru pacientů pro všechny schválené indikace. Obsahuje pokyny ke správnému screeningu
 Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Edukační materiály. KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře
 Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Souhrn doporučení pro předepisujícího lékaře
 G Souhrn doporučení pro předepisujícího lékaře Kritéria výběru pacientů pro léčbu přípravkem GILENYA (fingolimod) Přípravek GILENYA je vhodný pro dospělé pacienty k léčbě vysoce aktivní relabující-remitentní
G Souhrn doporučení pro předepisujícího lékaře Kritéria výběru pacientů pro léčbu přípravkem GILENYA (fingolimod) Přípravek GILENYA je vhodný pro dospělé pacienty k léčbě vysoce aktivní relabující-remitentní
Co byste měl(a) vědět o léčivém přípravku
 Co byste měl(a) vědět o léčivém přípravku Důležité bezpečnostní informace pro pacienty léčené přípravkem MabThera 1 Co byste měl(a) vědět o přípravku MabThera Pokud máte revmatoidní artritidu (RA), granulomatózu
Co byste měl(a) vědět o léčivém přípravku Důležité bezpečnostní informace pro pacienty léčené přípravkem MabThera 1 Co byste měl(a) vědět o přípravku MabThera Pokud máte revmatoidní artritidu (RA), granulomatózu
BAVENCIO (avelumab) Váš průvodce informacemi pro pacienta
 Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Celkové shrnutí vědeckého hodnocení přípravku Atacand Plus a související názvy (viz Příloha I)
 PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÝCH INFORMACÍ PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 14 Vědecké závěry Celkové
PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÝCH INFORMACÍ PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 14 Vědecké závěry Celkové
Edukační materiály. Imnovid (pomalidomid) Informace pro zdravotnické pracovníky. Brožura pokyny pro bezpečné použití přípravku
 Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pokyny pro bezpečné použití přípravku Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Brožura pokyny
Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pokyny pro bezpečné použití přípravku Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Brožura pokyny
Důležité informace k užívání přípravku Tasigna
 Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
CAVE! Informační dopis pro zdravotnické pracovníky
 CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin. Informace pro lékaře EU
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
NeuroBloc. botulinový toxin typu B injekční roztok, U/ml
 NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím
 Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Důležité informace o užívání přípravku TASIGNA
 Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
EDUKAČNÍ MATERIÁLY. GILENYA (fingolimod)
 EDUKAČNÍ MATERIÁLY GILENYA (fingolimod) Souhrn doporučení pro předepisující lékaře Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
EDUKAČNÍ MATERIÁLY GILENYA (fingolimod) Souhrn doporučení pro předepisující lékaře Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
Příbalová informace: informace pro uživatele. DULCOLAX 10 mg čípky bisacodylum
 sp. zn. sukls69505/2016 Příbalová informace: informace pro uživatele DULCOLAX 10 mg čípky bisacodylum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp. zn. sukls69505/2016 Příbalová informace: informace pro uživatele DULCOLAX 10 mg čípky bisacodylum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příloha I. Vědecké závěry a důvody pro změnu v podmínkách rozhodnutí o registraci
 Příloha I Vědecké závěry a důvody pro změnu v podmínkách rozhodnutí o registraci Vědecké závěry S přihlédnutím k hodnotící zprávě PRAC k PSUR pro anagrelid, vědecké závěry výboru CHMP jsou následující:
Příloha I Vědecké závěry a důvody pro změnu v podmínkách rozhodnutí o registraci Vědecké závěry S přihlédnutím k hodnotící zprávě PRAC k PSUR pro anagrelid, vědecké závěry výboru CHMP jsou následující:
Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel)
 EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Poznámka: Tyto úpravy souhrnu údajů o přípravku a
 PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha III. Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Návod pro pacienta / pečovatele
 Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Příbalová informace: informace pro pacienta Caprelsa 300 mg potahované tablety vandetanibum
 Příbalová informace: informace pro pacienta Caprelsa 300 mg potahované tablety vandetanibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro pacienta Caprelsa 300 mg potahované tablety vandetanibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jedna tvrdá tobolka s prodlouženým uvolňováním obsahuje tolterodini hydrogenotartras 4 mg (odpovídá tolterodinum 2,74 mg).
 1. NÁZEV PŘÍPRAVKU DETRUSITOL SR 4 mg tvrdé tobolky s prodlouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka s prodlouženým uvolňováním obsahuje tolterodini
1. NÁZEV PŘÍPRAVKU DETRUSITOL SR 4 mg tvrdé tobolky s prodlouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tvrdá tobolka s prodlouženým uvolňováním obsahuje tolterodini
Familiární středomořská (Mediterranean) horečka (Fever)
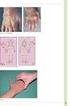 www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
satelitní sympozium společnosti Amgen Když ODPOVĚĎ je výjimečná
 satelitní sympozium společnosti Amgen Když ODPOVĚĎ je výjimečná Vážená paní doktorko, vážený pane doktore, rádi bychom Vás pozvali na satelitní sympozium společnosti Amgen, které proběhne u příležitosti
satelitní sympozium společnosti Amgen Když ODPOVĚĎ je výjimečná Vážená paní doktorko, vážený pane doktore, rádi bychom Vás pozvali na satelitní sympozium společnosti Amgen, které proběhne u příležitosti
Kelapril 5mg 7x14tbl.
 Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Apo-Amisulprid 200 mg Tablety. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amisulpridum 200 mg Pomocné látky: Monohydrát laktosy. Jedna tableta
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Apo-Amisulprid 200 mg Tablety. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amisulpridum 200 mg Pomocné látky: Monohydrát laktosy. Jedna tableta
EDUKAČNÍ MATERIÁLY. KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
Your journey inspires ours.
 Lilly Diabetes Your journey inspires ours. V Praze dne 20. ledna 2012 Vážená paní doktorko, vážený pane doktore, v zastoupení společnosti Takeda Pharmaceuticals Europe Ltd. Vám v příloze zasíláme edukační
Lilly Diabetes Your journey inspires ours. V Praze dne 20. ledna 2012 Vážená paní doktorko, vážený pane doktore, v zastoupení společnosti Takeda Pharmaceuticals Europe Ltd. Vám v příloze zasíláme edukační
Příloha IV. Vědecké závěry
 Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
PŘÍLOHA I NÁZEV, LÉKOVÁ FORMA, OBSAH LÉČIVÝCH LÁTEK, ŽIVOČIŠNÉ DRUHY, ZPŮSOB PODÁNÍ A DRŽITEL ROZHODNUTÍ O REGISTRACI 1/7
 PŘÍLOHA I NÁZEV, LÉKOVÁ FORMA, OBSAH LÉČIVÝCH LÁTEK, ŽIVOČIŠNÉ DRUHY, ZPŮSOB PODÁNÍ A DRŽITEL ROZHODNUTÍ O REGISTRACI 1/7 Členský stát Žadatel nebo držitel rozhodnutí o registraci Vymyšlený název přípravku
PŘÍLOHA I NÁZEV, LÉKOVÁ FORMA, OBSAH LÉČIVÝCH LÁTEK, ŽIVOČIŠNÉ DRUHY, ZPŮSOB PODÁNÍ A DRŽITEL ROZHODNUTÍ O REGISTRACI 1/7 Členský stát Žadatel nebo držitel rozhodnutí o registraci Vymyšlený název přípravku
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
Trendy rizik lékových interakcí u klientů Zdravotní pojišťovny Škoda v letech 2001-2005
 Trendy rizik lékových interakcí u klientů Zdravotní pojišťovny Škoda v letech 21-25 Prokeš M, Vitásek Z, Kolář J WWW.INFOPHARM.CZ Zdravotní pojišťovna Škoda ZPŠ a její klienti PRAHA Počet klientů ZPŠ:
Trendy rizik lékových interakcí u klientů Zdravotní pojišťovny Škoda v letech 21-25 Prokeš M, Vitásek Z, Kolář J WWW.INFOPHARM.CZ Zdravotní pojišťovna Škoda ZPŠ a její klienti PRAHA Počet klientů ZPŠ:
Pimobendan Randomized Occult DCM Trial to Evaluate
 Randomizovaná studie léčby okultní DCM pimobendanem s cílem vyhodnotit klinické příznaky a dobu do nástupu srdečního selhání Pimobendan Randomized Occult DCM Trial to Evaluate Clinical symptoms and Time
Randomizovaná studie léčby okultní DCM pimobendanem s cílem vyhodnotit klinické příznaky a dobu do nástupu srdečního selhání Pimobendan Randomized Occult DCM Trial to Evaluate Clinical symptoms and Time
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Zvláštní bezpečnostní informace
 Zvláštní bezpečnostní informace Edukační materiál pro lékaře Součást Plánu řízení rizik léčivého přípravku Arava Schváleno Státním ústavem pro kontrolu léčiv Zvláštní bezpečnostní informace Arava (leflunomid),
Zvláštní bezpečnostní informace Edukační materiál pro lékaře Součást Plánu řízení rizik léčivého přípravku Arava Schváleno Státním ústavem pro kontrolu léčiv Zvláštní bezpečnostní informace Arava (leflunomid),
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Iclusig (ponatinib) potahované tablety 15 mg, 30 mg a 45 mg* Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály Iclusig (ponatinib) potahované tablety 15 mg, 30 mg a 45 mg* Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály Iclusig (ponatinib) potahované tablety 15 mg, 30 mg a 45 mg* Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Celkové shrnutí vědeckého hodnocení přípravku Kytril a souvisejících názvů (viz příloha I)
 PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÉ INFORMACE PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 11 Vědecké závěry Celkové
PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÉ INFORMACE PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 11 Vědecké závěry Celkové
Klinické hodnocení ARAMIS pro muže s rakovinou prostaty
 Klinické hodnocení ARAMIS pro muže s rakovinou prostaty Brožura pro účastníky DĚKUJEME VÁM, že jste se rozhodl zúčastnit klinického hodnocení ARAMIS pro muže s rakovinou prostaty. V této brožuře najdete
Klinické hodnocení ARAMIS pro muže s rakovinou prostaty Brožura pro účastníky DĚKUJEME VÁM, že jste se rozhodl zúčastnit klinického hodnocení ARAMIS pro muže s rakovinou prostaty. V této brožuře najdete
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1
![Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1 Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1](/thumbs/102/154291766.jpg) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
EDUKAČNÍ MATERIÁLY. Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce
 EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příloha C. (změna v národně registrovaných léčivých přípravcích)
 Příloha C (změna v národně registrovaných léčivých přípravcích) PŘÍLOHA I VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ DOPORUČUJÍCÍ ZMĚNU PODMÍNEK ROZHODNUTÍ O REGISTRACI(ÍCH) Vědecké závěry S ohledem na hodnotící zprávu
Příloha C (změna v národně registrovaných léčivých přípravcích) PŘÍLOHA I VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ DOPORUČUJÍCÍ ZMĚNU PODMÍNEK ROZHODNUTÍ O REGISTRACI(ÍCH) Vědecké závěry S ohledem na hodnotící zprávu
Hemlibra (emicizumab) Subkutánní injekce. Návod pro zdravotnické pracovníky
 EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
ACTYNOX 50 % / 50 % V/V Oxid dusný (dinitrogenii oxidum) / kyslík (oxygenum) Medicinální plyn, stlačený PRŮVODCE PRO ZDRAVOTNICKÉ PRACOVNÍKY
 Edukační materiály Orgány veřejného zdraví stanovily určité podmínky pro tržní rozvoj přípravku ACTYNOX. Jednou z nich je předávat tyto informace zdravotnickým pracovníkům jako součást povinného plánu
Edukační materiály Orgány veřejného zdraví stanovily určité podmínky pro tržní rozvoj přípravku ACTYNOX. Jednou z nich je předávat tyto informace zdravotnickým pracovníkům jako součást povinného plánu
Váš průvodce léčbou poškození zraku v důsledku diabetického makulárního edému (DME) přípravkem Lucentis (ranibizumab)
 Váš průvodce léčbou poškození zraku v důsledku diabetického makulárního edému (DME) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu poškození
Váš průvodce léčbou poškození zraku v důsledku diabetického makulárního edému (DME) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu poškození
Simdax Příbalová informace
 Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls78539/2011 a sp.zn. sukls208461/2014
 sp.zn. sukls78539/2011 a sp.zn. sukls208461/2014 Příbalová informace: informace pro uživatele Aminoven 5%, infuzní roztok Aminoven 10%, infuzní roztok Aminoven 15%, infuzní roztok Přečtěte si pozorně celou
sp.zn. sukls78539/2011 a sp.zn. sukls208461/2014 Příbalová informace: informace pro uživatele Aminoven 5%, infuzní roztok Aminoven 10%, infuzní roztok Aminoven 15%, infuzní roztok Přečtěte si pozorně celou
Pomocná látka se známým účinkem: Jedna tableta obsahuje 75 mg monohydrátu laktosy. Úplný seznam pomocných látek viz bod 6.1.
 sp.zn.: sukls81995/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Loratadin-ratiopharm 10 mg Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se
sp.zn.: sukls81995/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Loratadin-ratiopharm 10 mg Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se
Psychofarmaka a gravidita. MUDr. Zdeňka Vyhnánková
 Psychofarmaka a gravidita MUDr. Zdeňka Vyhnánková ZÁKLADNÍ PRAVIDLA PRO FARMAKOTERAPII V TĚHOTENSTVÍ nemoc většinou znamená větší riziko než léčba indikace by měla být podložená a ne alibistická většina
Psychofarmaka a gravidita MUDr. Zdeňka Vyhnánková ZÁKLADNÍ PRAVIDLA PRO FARMAKOTERAPII V TĚHOTENSTVÍ nemoc většinou znamená větší riziko než léčba indikace by měla být podložená a ne alibistická většina
PŘÍLOHA I. SEZNAM NÁZVŮ LÉČIVých PŘÍPRAVKŮ, LÉKOVÉ FORMY, KONCENTRACE, ZPŮSOBY PODÁNÍ, žadatelé, DRŽITELÉ ROZHODNUTÍ O REGISTRACI V ČLENSKÝCH STÁTECH
 PŘÍLOHA I SEZNAM NÁZVŮ LÉČIVých PŘÍPRAVKŮ, LÉKOVÉ FORMY, KONCENTRACE, ZPŮSOBY PODÁNÍ, žadatelé, DRŽITELÉ ROZHODNUTÍ O REGISTRACI V ČLENSKÝCH STÁTECH 1 Členský stát EU/EEA Bulharsko Francie Německo Irsko
PŘÍLOHA I SEZNAM NÁZVŮ LÉČIVých PŘÍPRAVKŮ, LÉKOVÉ FORMY, KONCENTRACE, ZPŮSOBY PODÁNÍ, žadatelé, DRŽITELÉ ROZHODNUTÍ O REGISTRACI V ČLENSKÝCH STÁTECH 1 Členský stát EU/EEA Bulharsko Francie Německo Irsko
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) pro ibuprofen / pseudoefedrin
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) pro ibuprofen / pseudoefedrin
sp.zn. sukls219558/2011
 sp.zn. sukls219558/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Talcid žvýkací tablety hydrotalcitum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože
sp.zn. sukls219558/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Talcid žvýkací tablety hydrotalcitum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro pacienta. ANACID 258 mg/388 mg perorální suspenze. Magnesii hydroxidum, Algeldrati suspensio
 sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn. sukls277451/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Azelastin COMOD 0,5 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azelastini hydrochloridum 0,05 % (0,50 mg/ml) Jedna
Sp.zn. sukls277451/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Azelastin COMOD 0,5 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Azelastini hydrochloridum 0,05 % (0,50 mg/ml) Jedna
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls212686/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Chlorid sodný 0,9% Braun Infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 000 ml roztoku obsahuje: natrii chloridum Koncentrace
sp.zn. sukls212686/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Chlorid sodný 0,9% Braun Infuzní roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 000 ml roztoku obsahuje: natrii chloridum Koncentrace
Nebido EDUKAČNÍ MATERIÁL. Jak úspěšně aplikovat přípravek. (testosterone undecanoate)
 EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
Příbalová informace: informace pro uživatele. Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum
 sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Flexove 625 mg tablety. Glukosaminum
 sp.zn.sukls163996/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Flexove 625 mg tablety Glukosaminum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechejte
sp.zn.sukls163996/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Flexove 625 mg tablety Glukosaminum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. - Ponechejte
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
