PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
|
|
|
- Josef Havlíček
- před 8 lety
- Počet zobrazení:
Transkript
1 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1
2 1. NÁZEV PŘÍPRAVKU AZARGA 10 mg/ml + 5 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Jeden ml suspenze obsahuje 10 mg brinzolamidum a 5 mg timololum (jako timolol-maleinátu). Pomocné látky: Jeden ml suspenze obsahuje 0,10 mg benzalkonium-chloridu. Úplný seznam pomocných látek viz bod LÉKOVÁ FORMA Oční kapky, suspenze (oční kapky) Bílá až našedlá stejnoměrná suspenze, ph 7,2 (přibližně). 4. KLINICKÉ ÚDAJE 4.1 Terapeutické indikace Snížení nitroočního tlaku (IOP) u dospělých pacientů s glaukomem s otevřeným úhlem nebo oční hypertenzí, u kterých monoterapie neposkytuje dostatečné snížení IOP (viz bod 5.1). 4.2 Dávkování a způsob podání Použití u dospělých včetně starších pacientů Dávka je jedna kapka přípravku AZARGA do spojivkového vaku postiženého oka (postižených očí) dvakrát denně. Doporučuje se nasolakrimální okluze nebo lehké zavření víčka po vkápnutí přípravku. Tím se může snížit systémová absorpce léčivých přípravků, podávaných oční cestou, čímž se také sníží systémové nežádoucí účinky. Používá-li se více než jeden topický oční léčivý přípravek, je třeba přípravky podávat s odstupem minimálně 5 minut. Při vynechání jedné dávky by měla léčba pokračovat další plánovanou dávkou. Dávka by neměla překročit jednu kapku do postiženého oka (postižených očí) dvakrát denně. Nahrazuje-li se přípravkem AZARGA jiné oční antiglaukomatikum, mělo by se podávání jiného přípravku ukončit a AZARGA by se měla začít podávat další den. Podávání dětem AZARGA se nedoporučuje pro použití u dětí mladších 18 let vzhledem k nedostatku údajů o bezpečnosti a účinnosti. 2
3 Užívání při zhoršené funkci jater a ledvin S přípravkem AZARGA nebo s timololem 5 mg/ml oční kapky nebyly provedeny žádné studie na pacientech se zhoršenou funkcí jater nebo ledvin. U pacientů se sníženou funkcí jater nebo mírnou nebo středně těžkou poruchou funkce ledvin není potřeba dávkování upravovat. Přípravek AZARGA nebyl studován na pacientech s těžkou poruchou funkce ledvin (s clearancí kreatininu <30 ml/min.) nebo na pacientech s hyperchloremickou acidózou. Protože brinzolamid a jeho hlavní metabolit se vylučují převážně ledvinami, je přípravek AZARGA kontraindikován u pacientů s těžkou poruchou funkce ledvin (viz bod 4.3). Způsob podání Oční podání. Upozorněte pacienty, aby lahvičku před použitím dobře protřepali. Aby se zabránilo kontaminaci hrotu kapátka a roztoku, je třeba dbát na to, aby se hrot kapátka lahvičky nedotkl víčka, okolních tkání nebo jiných povrchů. Upozorněte pacienty, aby uchovávali lahvičku pevně uzavřenou, pokud ji právě nepoužívají. 4.3 Kontraindikace Hypersensitivita na léčivé látky nebo na kteroukoli pomocnou látku tohoto přípravku. Průduškové astma, průduškové astma v anamnéze nebo závažná chronická obstrukční plicní nemoc. Sinusová bradykardie, druhý nebo třetí stupeň atrioventrikulární blokády, zjevné srdeční selhání nebo kardiogenní šok. Těžká alergická rýma a hyperreaktivita průdušek; hypersensitivita na jiné betablokátory. Hyperchloremická acidóza (viz bod 4.2). Těžká porucha funkce ledvin. Hypersensitivita na sulfonamidy (viz bod 4.4). 4.4 Zvláštní upozornění a opatření pro použití Systémové účinky Podobně jako u jiných topicky podávaných očních přípravků, jsou brinzolamid a timolol absorbovány systémově. Vzhledem ke složce- timololu s betoblokátorovým účinkem, se mohou objevit stejné typy kardiovaskulárních a plicních nežádoucích účinků jako při podávání systémových betablokátorů. Srdeční selhání by mělo být před počátkem léčby timololem odpovídajícím způsobem léčeno. Pacienti s těžkým srdečním onemocněním v anamnéze by měli být sledování, jestli se u nich neobjeví známky srdečního selhání a měl by se kontrolovat jejich puls. Po podání timolol-maleinátu byly hlášeny respirační a srdeční nežádoucí účinky, včetně úmrtí v důsledku bronchospasmu u pacientů s astmatem a vzácně i úmrtí v souvislosti se selháním srdce. Betablokátory by se měly podávat s opatrností u pacientů, u nichž dochází ke spontánní hypoglykémii nebo u pacientů s labilní cukrovkou, závislou na inzulinu, protože betablokátory mohou známky a symptomy akutní hypoglykémie maskovat. Mohou také zamaskovat známky hypertyreózy a způsobit zhoršení Prinzmetalovy anginy, těžkých periferních a centrálních poruch oběhu a hypotenze. AZARGA obsahuje brinzolamid, který patří mezi sulfonamidy. Po topickém podání se mohou objevit stejné typy nežádoucích účinků, jako při podávání sulfonamidů. U perorálně podávaných inhibitorů karboanhydrázy byly hlášeny poruchy acidobazické rovnováhy. Objeví-li se známky závažných účinků nebo přecitlivělosti, používání tohoto léčivého přípravku přerušte. Existuje možnost aditivního účinku ke známým systémovým účinkům inhibice karboanhydrázy u pacientů, jimž je perorálně podáván inhibitor karboanhydrázy a AZARGA. Souběžné podávání přípravku AZARGA a perorálně podávaných inhibitorů karboanhydrázy nebylo studováno a nedoporučuje se (viz bod 4.5). 3
4 Anafylaktické reakce Při léčbě betablokátory nemusí pacienti s atopií nebo těžkou anafylaktickou reakcí na řadu alergenů reagovat na obvyklé dávky adrenalinu, používané pro léčbu anafylaktických reakcí. Souběžná léčba Timolol může interagovat s jiným léčivými přípravky (viz bod 4.5). Účinek na nitrooční tlak nebo dobře známé účinky v důsledku podání systémových betablokátorů mohou být zesíleny, když je přípravek AZARGA podán pacientům, kteří již dostávají perorální betablokátor. Užívání dvou lokálně působících betablokátorů nebo dvou lokálních inhibitorů karboanhydrázy se nedoporučuje. Účinky na oči S léčbou pacientů s pseudoexfoliativním glaukomem nebo pigmentovým glaukomem přípravkem AZARGA jsou jen omezené zkušenosti. Těmto pacientům by měla být věnována zvýšená opatrnost a je doporučováno časté monitorování jejich IOP. Přípravek AZARGA nebyl studován u pacientů s glaukomem s úzkým úhlem a není u těchto pacientů doporučován. Perorálně podávané inhibitory karboanhydrázy mohou u starších pacientů zhoršovat schopnost provádět činnosti vyžadující duševní bdělost a/nebo fyzickou koordinaci. AZARGA se absorbuje systémově a proto může po topickém podání k podobným účinkům dojít. Možný účinek brinzolamidu na endoteliální funkci rohovky nebyl zkoumán u pacientů s poškozenou rohovkou (především u pacientů s nízkým počtem buněk endotelu). Konkrétně nebyli studováni pacienti nosící kontaktní čočky a doporučuje se pečlivé monitorování těchto pacientů, když užívají brinzolamid, protože inhibitory karboanhydrázy mohou ovlivnit hydrataci rohovky a nošení kontaktních čoček může zvýšit riziko pro rohovku. Doporučuje se pečlivé monitorování pacientů s poškozenou rohovkou, jako jsou pacienti s cukrovkou nebo dystrofií rohovky. Benzalkonium-chlorid, který je běžně používán v očních přípravcích jako konzervační činidlo, je uváděn jako látka, vyvolávající tečkovitou keratopatii a/nebo toxickou ulcerativní keratopatii. Protože přípravek AZARGA obsahuje benzalkonium-chlorid, je při častém nebo dlouhodobém užívání nezbytné pacienta pečlivě sledovat. AZARGA obsahuje benzalkonium-chlorid, který může vyvolávat podráždění oka, a o němž je známo, že zbarvuje měkké kontaktní čočky. Kontaktu s měkkými kontaktními čočkami je třeba zamezit. Pacienti musí být poučeni, že si mají před aplikací přípravku AZARGA čočky vyjmout, vyčkat po nakapání dávky přípravku 15 minut a teprve potom si čočky opět nasadit. 4.5 Interakce s jinými léčivými přípravky a jiné formy interakce S přípravkem AZARGA nebyly provedeny žádné studie interakcí. AZARGA obsahuje brinzolamid, což je inhibitor karboanhydrázy, a i když je podáván topicky, absorbuje se systémově. U perorálních inhibitorů karboanhydrázy byly hlášeny poruchy acidobazické rovnováhy. U pacientů léčených přípravkem AZARGA je třeba vzít v úvahu možnost interakcí. Mezi izoenzymy cytochromu P-450, odpovědné za metabolismus brinzolamidu, patří CYP3A4 (hlavní), CYP2A6, CYP2B6, CYP2C8 a CYP2C9. Předpokládá se, že inhibitory CYP3A4 jako ketokonazol, itrakonazol, klotrimazol, ritonavir a troleandomycin budou inhibovat metabolismus brinzolamidu izoenzymem CYP3A4. Když se souběžně podávají inhibitory CYP3A4, doporučuje se opatrnost. Akumulace brinzolamidu je však nepravděpodobná, protože hlavní cestu představuje vylučování ledvinami. Brinzolamid není inhibitorem izoenzymů cytochromu P
5 Existuje potenciál pro aditivní účinky, jež vedou k hypotenzi a/nebo výrazné bradykardii, když se podávají oční kapky s timololem souběžně s perorálními blokátory kalciových kanálů, guanetidinem nebo betablokátory, antiarytmiky, digitalisovými glykosidy nebo parasympatomimetiky. Při užívání betablokátorů se může zesílit hypertenzní reakce na náhlé vysazení klonidinu. Při kombinované léčbě inhibitory CYP2D6 (např. chinidinem, cimetidinem) a timololem byla hlášena zvýšená systémová beta-blokáda (např. snížení srdeční frekvence). Betablokátory mohou zvyšovat hypoglykemický účinek antidiabetik. Betablokátory mohou maskovat známky a symptomy hypoglykémie (viz bod 4.4). 4.6 Těhotenství a kojení Těhotenství Adekvátní údaje o podávání brinzolamidu těhotným ženám nejsou k dispozici.. Studie na zvířatech prokázaly reprodukční toxicitu (viz bod 5.3). Potenciální riziko pro člověka není známé. Kontrolované epidemiologické studie systémového užívání betablokátorů nenaznačují malformační účinky, u plodů nebo novorozenců však byly pozorovány některé farmakologické účinky jako bradykardie. Data z omezeného počtu exponovaných těhotenství neuvádějí žádné nežádoucí účinky timololu v očních kapkách na těhotenství nebo na zdraví plodu či novorozence, u jednoho případu plodu ženy, léčené očními kapkami s timololem, však byla hlášena bradykardie a arytmie. nejsou k Žádné další relevantní epidemiologické údaje nejsou v současné době k dispozici. AZARGA by se neměla v těhotenství používat, není-li to jednoznačně nutné. Kojení Není známo, zda se brinzolamid vylučuje do mateřského mléka. Studie na zvířatech ukázaly, že u zvířat se brinzolamid do mléka vylučuje. V mateřském mléku u člověka se objevuje timolol. Při terapeutických dávkách přípravku AZARGA se však žádné účinky na novorozence nebo batolata neočekávají. V období kojení se může přípravek AZARGA používat. 4.7 Účinky na schopnost řídit a obsluhovat stroje Podobně jako u všech očních kapek může být schopnost řídit nebo obsluhovat stroje ovlivněna dočasně rozmazaným viděním nebo jinými vizuálními poruchami. Dojde-li při nakapání k zastřenému vidění, musí pacient vyčkat, dokud se vidění opět neprojasní, a teprve potom může řídit nebo obsluhovat stroje. Perorálně podávané inhibitory karboanhydrázy mohou zhoršit schopnost starších pacientů provádět činnosti vyžadující duševní bdělost a/nebo fyzickou koordinaci (viz bod 4.4). 4.8 Nežádoucí účinky Souhrn bezpečnostního profilu Ve dvou klinických hodnoceních v délce 6 a 12 měsíců, zahrnujících 394 pacientů léčených přípravkem AZARGA, bylo nejčastěji hlášeným nežádoucím účinkem přechodně rozmazané vidění po nakapání (3,6%), trvající od několika sekund do několika minut. Shrnutí nežádoucích účinků do tabulek Níže uvedené nežádoucí účinky byly roztříděny podle následující klasifikace: velmi časté ( 1/10), časté ( 1/100 až <1/10), méně časté ( 1/1000 až <1/100), vzácné ( 1/ až <1/1000) nebo velmi vzácné (<1/10 000). V každé skupině četnosti jsou nežádoucí účinky uvedeny v pořadí klesající závažnosti. 5
6 Třídy orgánových systémů Psychiatrické poruchy Poruchy nervového systému Poruchy oka Cévní poruchy Respirační, hrudní a mediastinální poruchy Poruchy kůže a podkožní tkáně Používaný výraz MedDRA Méně časté: nespavost Časté: dysgeusie Časté: rozmazané vidění, bolest oka, podráždění oka, pocit cizího tělíska v očích Méně časté: eroze rohovky, tečkovaná keratitida, suché oko, výtok z oka, svědění oka, hyperémie oka, blefaritida, alergická konjunktivitida, porucha rohovky, zarudnutí přední komory, hyperémie spojivek, tvorba krust na okraji očního víčka, astenopie, nenormální pocit v oku, svědění očního víčka, alergická blefaritida, erytém očního víčka Méně časté: pokles krevního tlaku Méně časté: chronické obstrukční plicní onemocnění, faryngolaryngeální bolest, výtok z nosu, kašel Méně časté: vlasové problémy, lichen planus Popis vybraných nežádoucích účinků Dysgeusie (hořkost nebo neobvyklá chuť v ústech po nakapání) byla často hlášeným systémovým nežádoucím účinkem, spojeným s použitím přípravku AZARGA během klinických hodnocení. Je pravděpodobné, že je vyvolána průchodem očních kapek nasolakrimálním kanálem do nosohltanu, přičítá se brinzolamidu. Nasolakrimální okluze nebo lehké zavření očního víčka po nakapání může pomoci tento účinek snížit (viz bod 4.2). AZARGA obsahuje brinzolamid, který je sulfonamidovým inhibitorem karboanhydrázy se systémovou absorpcí. Účinky na zažívací systém, nervový systém, účinky hematologické, na ledviny a metabolismus jsou obvykle spojeny se systémovými inhibitory karboanhydrázy. Stejný typ nežádoucích účinků, jenž se připisuje perorálně podávaným inhibitorům karboanhydrázy, se může objevit i při topickém podání. AZARGA obsahuje brinzolamid a timolol (jako timolol-maleinát). Další nežádoucí účinky, spojené s používáním jednotlivých složek a pozorované v klinickém hodnocení a na základě zkušeností po uvedení na trh, jež se mohou potenciálně objevit u přípravku AZARGA, zahrnují: 6
7 Třídy orgánových systémů Infekce a infestace Poruchy krve a lymfatického systému Poruchy imunitního systému: Poruchy metabolismu a výživy Psychiatrické poruchy Poruchy nervového systému Poruchy oka Poruchy ucha a labyrintu Srdeční poruchy Cévní poruchy Respirační, hrudní a mediastinální poruchy Brinzolamid 10 mg/ml Timolol 5 mg/ml Používaný výraz MedDRA nasofaryngitida, faryngitida, sinusitida, rinitida pokles počtu červených krvinek, zvýšení chloridových iontů v krvi hypersensitivita hypoglykémie apatie, deprese, zhoršená nálada, deprese snížení libida, zlé sny, nervozita somnolence, motorická mozková ischémie, dysfunkce, amnézie, zhoršení cerebrovaskulární příhoda, paměti, závratě, parestézie, synkopa, myasthenia gravis, tremor, bolest hlavy, hypestézie, parestézie, bolest hlavy, ageusie závrať keratitida, keratopatie, zvětšení poměru průměru exkavace k průměru terče zrakového nervu, defekt epitelu rohovky, porucha epitelu rohovky, zvýšení nitroočního tlaku, deposita v oku, zbarvení rohovky, edém rohovky, konjunktivitida, meibomanitida, diplopie, oslnění, fotofobie, fotopsie, snížení vizuální ostrosti, pterygium,, nepříjemný pocit v oku, keratoconjunctivitis sicca, hypestézie, pigmentace skléry, subkonjunktivální cysta, zvýšené slzení, poruchy vidění, otok oka, oční alergie, madaróza, poruchy očních víček, otok očních víček tinnitus, vertigo kardiorespirační potíže, angina pectoris, bradykardie, nepravidelná srdeční frekvence, arytmie, palpitace, tachykardie, zvýšená srdeční frekvence zvýšení krevního tlaku, hypertenze dyspnoe, astma, bronchiální hyperaktivita, epistaxe, dráždění v hrdle, ucpání nosu, kongesce horních cest dýchacích, zatékání hlenu z nosní dutiny do hrtanu, kýchání, sucho v nose konjunktivitida, diplopie, ptóza očního víčka, keratitida, vizuální poruchy srdeční zástava, srdeční selhání, arytmie, atrioventrikulární blok, bradykardie, palpitace hypotenze respirační selhání, bronchospasmus, dyspnoe, nazální kongesce 7
8 Gastrointestinální poruchy Poruchy jater a žlučových cest Poruchy kůže a podkožní tkáně Poruchy svalové a kosterní soustavy a pojivové tkáně Poruchy ledvin a močových cest Poruchy reprodukčního systému a prsu Celkové poruchy a reakce v místě aplikace Poranění, otravy a procedurální komplikace sucho v ústech, esofagitida, zvracení, průjem, nausea, dyspepsie, bolest v nadbřišku, abdominální diskomfort, žaludeční diskomfort, časté střevní pohyby, gastrointestinální poruchy, orální hypestezie, orální parestezie, flatulence abnormální testy jaterních funkcí kopřivka, makulopapulózní vyrážka, vyrážka, generalizovaný pruritus, alopecie, napětí v kůži, dermatitida, erytém bolest v zádech, svalové spasmy, myalgie, artralgie, bolest končetin bolest ledvin, polakisurie erektilní dysfunkce bolest, astenie, hrudní diskomfort, únava, abnormální pocity, pocity nervozity, podrážděnost, bolest na hrudi, periferní edém, malátnost, rezidua léku cizí tělísko v oku průjem, nausea alopecie, vyrážka astenie, bolest na hrudi Dětská populace AZARGA se nedoporučuje u dětí mladších 18 let vzhledem k nedostatečným údajům o bezpečnosti a účinnosti. 4.9 Předávkování Nebyl hlášen žádný případ předávkování. Dojde-li k předávkování očními kapkami AZARGA, měla by být léčba symptomatická a podpůrná. Může dojít k nerovnováze elektrolytů, rozvoji acidózy a možná i účinkům na centrální nervový systém. Měly by se monitorovat hladiny elektrolytů v séru (především draslíku) a hladiny ph krve. Studie prokázaly, že timolol není snadné odstranit dialýzou. 5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti Farmakoterapeutická skupina: Antiglaukomatika a miotika ATC kód: S01ED51 Mechanismus účinku AZARGA obsahuje dvě léčivé látky: brinzolamid a timolol-maleinát. Tyto dvě složky snižují zvýšený nitrooční tlak především snížením sekrece komorové vody, jejich mechanismy účinku jsou ale odlišné. Kombinovaný účinek těchto dvou léčivých látek má za následek další snížení nitroočního tlaku ve srovnání s každou jednotlivou složkou. 8
9 Brinzolamid je silný inhibitor lidské karboanhydrázy II (CA-II), což je převládající izoenzym v oku. Inhibice karboanhydrázy v ciliárních procesech oka snižuje sekreci komorové vody, pravděpodobně zpomalením tvorby bikarbonátových iontů s následným snížením transportu sodíku a tekutin. Timolol je neselektivní adrenergní blokátor, jenž nemá žádný vnitřní sympatomimetický účinek, přímý depresivní účinek na myokard ani účinek na stabilizaci membrány. Tonografické a fluorofotometrické studie u člověka naznačují, že jeho převládající účinek je spojen se sníženou tvorbou komorové vody a mírným zvýšením jejího odtoku. Farmakodynamické účinky Klinické účinky: Ve dvanáctiměsíčním kontrolovaném klinickém hodnocení na pacientech s glaukomem s otevřeným úhlem nebo oční hypertenzí, kteří dle mínění zkoušejícího mohli mít prospěch z kombinované léčby a kteří měli při zahájení studie průměrný nitrooční tlak 25 až 27 mm Hg, činilo střední snížení nitroočního tlaku přípravkem AZARGA, podávaným dvakrát denně, 7 až 9 mm Hg. Bylo prokázáno, že při podávání přípravku AZARGA není snížení středních hodnot nitroočního tlaku ve všech časových bodech při všech návštěvách horší než při podávání dorzolamidu 20 mg/ml + timolol 5 mg/ml. V šestiměsíční kontrolované klinické studii na pacientech s glaukomem s otevřeným úhlem nebo oční hypertenzí a průměrným nitroočním tlakem na počátku hodnocení 25 až 27 mm Hg vedlo podávání přípravku AZARGA, dávkovaného dvakrát denně, ke střednímu snížení nitroočního tlaku o 7 až 9 mm Hg, což bylo až od 3 mm Hg více než při podávání brinzolamidu 10 mg/ml, dávkovaného dvakrát denně, a až o 2 mm Hg více než při podávání samotného timololu 5 mg/ml, dávkovaného dvakrát denně. Statisticky lepší snížení středních hodnot nitroočního tlaku bylo pozorováno jak vzhledem k brinzolamidu tak timololu ve všech časových bodech a návštěvách během celé studie. Ve třech kontrolovaných klinických hodnoceních byl oční diskomfort po nakapání přípravku AZARGA výrazně nižší, než tomu bylo u dorzolamidu 20 mg/ml + timololu 5 mg/ml. 5.2 Farmakokinetické vlastnosti Absorpce Po topickém podání do oka se brinzolamid a timolol absorbují přes rohovku a do systémového oběhu. Ve farmakokinetické studii dostávaly zdravé subjekty perorálně dvakrát denně brinzolamid (1 mg) po dobu 2 týdnů, aby se zkrátila doba do dosažení ustáleného stavu před zahájením podávání přípravku AZARGA. Po podávání přípravku AZARGA dvakrát denně po dobu 13 týdnů dosáhly průměrné koncentrace brinzolamidu v červených krvinkách (RBC) v týdnu 4, 10 resp. 15 následujích hodnot: 18,8 ± 3,29 µm, 18,1 ± 2,68 µm a 18,4 ± 3,01 µm. To naznačuje, že se v červených krvinkách udržovaly ustálené hodnoty koncentrace brinzolamidu. V ustáleném stavu byly po podání přípravku AZARGA střední hodnoty C max a AUC 0-12h timololu v plazmě o 27% a 28% nižší (C max : 0,824 ±,.453 ng/ml; AUC 0-12h : 4,71 ± 4,29 ng h/ml) oproti podání timololu 5 mg/ml (C max : 1,13 ± 0,494 ng/ml; AUC 0-12h : 6,58 ± 3,18 ng h/ml). Nižší systémová expozice timololem po podání přípravku AZARGA není klinicky relevantní. Po podání přípravku AZARGA bylo střední hodnoty C max timololu dosaženo za 0,79 ± 0,45 hodiny. Distribuce Vazba brinzolamidu na bílkoviny plazmy je středně silná (kolem 60%). Brinzolamid je sekvestrován v erytrocytech díky své vysoké afinitě k vazbě na CA-II a v menším rozsahu na CA-I. Jeho aktivní N-desetyl metabolit se také akumuluje v červených krvinkách, kde se váže především na CA-I. Afinita brinzolamidu a metabolitu na červené krvinky a tkáňové CA má za následek nízké koncentrace v plazmě. 9
10 Data o distribuci v oční tkáni králíků ukázala, že timolol lze v komorové vodě naměřit ještě až 48 hodin po podání přípravku AZARGA. V ustáleném stavu je timolol detekován v lidské plazmě po dobu až 12 hodin po podání přípravku AZARGA. Metabolismus Metabolické dráhy pro metabolismus brinzolamidu zahrnují N-dealkylaci, O-dealkylaci a oxidaci jeho N-propylového bočního řetězce. N-desetyl-brinzolamid je hlavním metabolitem brinzolamidu, který se vytváří u člověka, který se také váže na CA-I v přítomnosti brinzolamidu a akumuluje se v červených krvinkách. Studie in vitro ukazují, že metabolismus brinzolamidu zahrnuje především CYP3A4 a také minimálně čtyři další izoenzymy (CYP2A6, CYP2B6, CYP2C8 a CYP2C9). Timolol je metabolizován dvěma cestami. Jedna vede k etanolaminovému bočnímu řetězci na thiadiazolovém kruhu a druhá vytváří etanolový boční řetězec na morfolinovém dusíku a druhý podobný postranní řetězec s karbonylovou skupinou, přiléhající k dusíku. Metabolismus timololu je zprostředkován především CYP2D6. Exkrece Brinzolamid se vylučuje především renální exkrecí (přibližně 60%). Zhruba 20% dávky bylo prokázáno v moči jako metabolit. Brinzolamid a N-desetyl-brinzolamid jsou hlavní složky, nalezené v moči spolu se stopovými hladinami (<1%) N-desmetoxypropyl- a O-desmetylmetabolitů. Timolol a jeho metabolity se především vylučují ledvinami. Přibližně 20% dávky timololu se vylučuje močí v nezměněné formě a zbytek močí jako metabolity. Plazmatický poločas timololu t 1/2 je 4,8 hodiny po podání přípravku AZARGA. 5.3 Předklinické údaje vztahující se k bezpečnosti Brinzolamid Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a hodnocení kancerogenního potenciálu neodhalily žádné zvláštní riziko pro člověka. Studie vývojové toxicity u králíků s perorálními dávkami brinzolamidu do 6 mg/kg/den (214-násobek doporučené denní klinické dávky 28 µg/kg/den)) neodhalily žádné účinky na vývoj plodu i přes významnou toxicitu pro matku. Podobné studie s potkany vedly k mírně snížené osifikaci lebky a segmentů sterna plodů matek, které dostávaly brinzolamid v dávkách 18 mg/kg/den (642-násobek doporučené denní klinické dávky), ne však 6 mg/kg/den. K těmto nálezům docházelo při dávkách, které vyvolávaly metabolickou acidózu se sníženým přírůstkem hmotnosti u matek a sníženými hmotnostmi plodu. U mláďat samic, jež dostávaly brinzolamid perorálně, byly pozorovány na dávce závislé poklesy hmotnosti plodu od mírného poklesu (zhruba 5-6%) při 2 mg/kg/den až po téměř 14% při dávce 18 mg/kg/den.v době kojení byla dávka, která nepůsobila žádné nežádoucí účinky na potomky, 5 mg/kg/den. Timolol Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a kancerogenního potenciálu neodhalily žádné zvláštní riziko pro člověka. Studie reprodukční toxicity s timololem prokázaly opožděnou osifikaci plodů potkanů bez jakýchkoliv nežádoucích účinků na postnatální vývoj ( při dávce 50 mg/kg/den neboli 3500-násobku denní klinické dávky 14 µg/kg/den) a zvýšenou resorpci plodů u králíků ( při dávce 90 mg/kg/den neboli 6400-násobku denní klinické dávky). 10
11 6. FARMACEUTICKÉ ÚDAJE 6.1 Seznam pomocných látek Benzalkonium-chlorid Mannitol (E421) Karbomer 974 P Tyloxapol Dinatrium-edetát Chlorid sodný Kyselina chlorovodíková a/nebo hydroxid sodný (pro úpravu ph) Čištěná voda 6.2 Inkompatibility Neuplatňuje se. 6.3 Doba použitelnosti 2 roky. 4 týdny po prvním otevření. 6.4 Zvláštní upozornění pro uchovávání Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání. 6.5 Druh obalu a velikost balení 5 ml kulaté lahve z polyetylénu o nízké hustotě s dávkovací zátkou a bílým polypropylénovým šroubovacím uzávěrem (DROP-TAINER), obsahující 5 ml suspenze. Papírové skládačky obsahující 1 nebo 3 lahve. Na trhu nemusí být všechny velikosti balení. 6.6 Zvláštní opatření pro likvidaci přípravku Žádné zvláštní požadavky. 7. DRŽITEL ROZHODNUTÍ O REGISTRACI Alcon Laboratories (UK) Ltd. Pentagon Park Boundary Way Hemel Hempstead Herts HP2 7UD Velká Británie 8. REGISTRAČNÍ ČÍSLO (A) 9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE 11
12 10. DATUM REVIZE TEXTU Podrobná informace o tomto léku je dostupná na webové stránce European Medicines Agency (EMEA): 12
13 PŘÍLOHA II A. VÝROBCE ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ B. PODMÍNKY REGISTRACE 13
14 A. VÝROBCE ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ Název a adresa výrobce odpovědného za propouštění šarží S.A. Alcon-Couvreur N.V. Rijksweg 14 B-2870 Puurs Belgie B. PODMÍNKY REGISTRACE PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ, KLADENÉ NA DRŽITELE ROZHODNUTÍ O REGISTRACI Výdej léčivého přípravku je vázán na lékařský předpis. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU Neuplatňuje se. DALŠÍ PODMÍNKY Systém farmakovigilance Držitel rozhodnutí o registraci musí zajistit, aby byl zaveden funkční systém farmakovigilance, tak jak je popsán ve verzi 4.0, uvedené v Modulu k datu 21. června 2007 Žádosti o registraci, předtím, než bude přípravek uveden na trh, a dále po celou dobu, kdy bude přípravek na trhu. Plán řízení rizik Držitel rozhodnutí o registraci se zavazuje, že uskuteční studie a další činnosti v oblasti farmakovigilance podrobně uvedené v plánu farmakovigilance, tak jak bylo schváleno ve verzi 01 z 30. září 2007 (platné od 16. května 2008) Plánu řízení rizik (RMP) uvedeném v Modulu Žádosti o registraci a v příštích aktualizacích RMP schválených CHMP. V souladu s pokynem Výboru pro humánní léčivé přípravky (CHMP) k systémům řízení rizik pro humánní léčivé přípravky má být aktualizovaný plán řízení rizik předložen současně s příští Periodicky aktualizovanou zprávou o bezpečnosti (PSUR). Dále má být aktualizovaný Plán řízení rizik (RMP) předložen: Jestliže byly obdrženy nové informace, které mohou mít dopad na současné specifikace bezpečnosti, farmakovigilanční plán nebo na činnosti k minimalizaci rizik Do 60 dní po dosažení důležitého milníku (farmakovigilance nebo minimalizace rizik) Na žádost EMEA 14
15 PŘÍLOHA III OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE 15
16 A. OZNAČENÍ NA OBALU 16
17 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU PAPÍROVÁ SKLÁDAČKA PRO JEDNU LAHEV 5 ml + PAPÍROVÁ SKLÁDAČKA PRO 3 x 5 ml LAHVE 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU AZARGA 10 mg/ml + 5 mg/ml oční kapky suspenze Brinzolamidum/Timololum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 1 ml suspenze obsahuje 10 mg brinzolamidu a 5 mg timololu (jako timolol-maleinát) 3. SEZNAM POMOCNÝCH LÁTEK Obsahuje: Chlorid benzalkonia, manitol (E421), carbopol 974P, tyloxapol, edetan disodný, chlorid sodný, kyselina chlorovodíková a/nebo hydroxid sodný (pro úpravu ph), čištěná voda. Další informace jsou uvedeny v příbalové informaci. 4. LÉKOVÁ FORMA A VELIKOST BALENÍ Oční kapky, suspenze 1 x 5 ml 3 x 5 ml 5. ZPŮSOB A CESTA/CESTY PODÁNÍ Oční podání. Před použitím dobře protřepejte. Před použitím si přečtěte příbalovou informaci. 6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ Uchovávejte mimo dosah a dohled dětí. 7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ 8. POUŽITELNOST EXP: Zlikvidujte 4 týdny po prvním otevření. Otevřeno: 17
18 9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ 10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ 11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI Alcon Laboratories (UK) Ltd. Pentagon Park Boundary Way Hemel Hempstead Herts HP2 7UD Velká Británie 12. REGISTRAČNÍ ČÍSLO/ČÍSLA EU/0/00/000/001 1 x 5 ml EU/0/00/000/002 3 x 5 ml 13. ČÍSLO ŠARŽE Č.š.: 14. KLASIFIKACE PRO VÝDEJ Výdej léčivého přípravku vázán na lékařský předpis. 15. NÁVOD K POUŽITÍ 16 INFORMACE V BRAILLOVĚ PÍSMU azarga 18
19 MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU ŠTÍTEK LAHVIČKY 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ AZARGA 10 mg/ml + 5 mg/ml oční kapky Brinzolamidum/Timololum Oční podání 2. ZPŮSOB PODÁNÍ Před použitím si přečtěte příbalovou informaci. 3. POUŽITELNOST EXP: Zlikvidujte 4 týdny po prvním otevření. Otevřeno: 4. ČÍSLO ŠARŽE Č.š.: 5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET 5 ml 6. JINÉ 19
20 PŘÍBALOVÁ INFORMACE 20
21 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE AZARGA 10 mg/ml + 5 mg/ml oční kapky, suspenze Brinzolamidum/Timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. - Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka. - Tento přípravek byl předepsán Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné příznaky jako Vy. - Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi V příbalové informaci naleznete: 1. Co je přípravek AZARGA a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete přípravek AZARGA používat 3. Jak se přípravek AZARGA používá 4. Možné nežádoucí účinky 5. Jak přípravek AZARGA uchovávat 6. Další informace 1. CO JE PŘÍPRAVEK AZARGA A K ČEMU SE POUŽÍVÁ AZARGA se používá k léčbě vysokého tlaku v oku. Tento tlak může vést k onemocnění zvanému glaukom. AZARGA je kombinace léků na glaukom. Obsahuje dvě léčivé látky, jež spolu účinkují, aby snížily tlak v oku. 2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE PŘÍPRAVEK AZARGA POUŽÍVAT Nepoužívejte přípravek AZARGA jestliže jste alergický/á na kteroukoli složku přípravku AZARGA. Úplný seznam složek tohoto přípravku je uveden v bodu 6. jestliže máte problémy s dýcháním jako je astma, bronchitida (zánět průdušek) nebo jiný typ dýchacích problémů. jestliže Vám srdce pomalu bije, máte srdeční selhání nebo poruchu srdečního rytmu. jestliže máte překyselenou krev (onemocnění zvané hyperchloremická acidóza). jestliže máte závážné problémy s ledvinami. Zvláštní opatrnosti při použití přípravku AZARGA je zapotřebí jestliže trpíte anginou (bolestmi na hrudi), problémy krevního oběhu nebo nízkým krevním tlakem. AZARGA může tato onemocnění zhoršit. Jestliže máte obavy ze změn těchto příznaků, řekněte to co nejdříve svému lékaři. jestliže se u Vás vyskytne jakákoliv těžká alergická reakce v době, kdy užíváte přípravek AZARGA, ať je již její příčina jakákoliv, léčba adrenalinem nemusí být tak účinná. Dostanete-li tedy jakýkoliv jiný lék, řekněte prosím zdravotnickému odborníkovi, že používáte přípravek AZARGA. 21
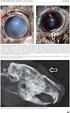
22 jestliže máte cukrovku; přípravek AZARGA může zamaskovat příznaky nízké hladiny cukru v krvi (hypoglykémie), jako je třes a závratě, je proto třeba, abyste jej používali s opatrností. jestliže máte problémy s játry. Informujte svého lékaře. jestliže máte suché oči nebo problémy s rohovkou. Informujte svého lékaře. Použití přípravku AZARGA se nedoporučuje u dětí mladších 18 let. Vzájemné působení s dalšími léčivými přípravky Přípravek AZARGA může ovlivňovat nebo být ovlivněn jinými léky, které užíváte, včetně jiných očních kapek pro léčbu glaukomu. Informujte svého lékaře o všech lécích, které užíváte nebo se chystáte užívat pro snížení krevního tlaku, lécích na srdce, lécích pro léčbu cukrovky, pro léčbu žaludečních vředů, dále léků fungicidních (protiplísňových), protivirových nebo antibiotik. Prosím informujte svého lékaře nebo lékárníka o všech lécích, které užíváte nebo jste užíval(a) v nedávné době, a to i o lécích, které jsou dostupné bez lékařského předpisu. Těhotenství a kojení Jste-li těhotná nebo pokud můžete otěhotnět, neměla byste přípravek AZARGA používat. Před použitím přípravku AZARGA se poraďte se svým lékařem. Jestliže kojíte, můžete přípravek AZARGA používat. Poraďte se se svým lékařem dříve, než začnete užívat jakýkoli lék. Řízení dopravních prostředků a obsluha strojů Neřiďte dopravní prostředek ani neobsluhujte žádné stroje, dokud se Vaše vidění neprojasní. Vaše vidění může být po určitou dobu po použití přípravku AZARGA rozmazané. Jedna z léčivých látek tohoto přípravku může zhoršit schopnost starších pacientů provádět činnosti, vyžadující mentální bdělost a/nebo fyzickou koordinaci. Jste-li tím postiženi, buďte při řízení nebo používání strojů opatrní. Důležité informace o některých složkách přípravku AZARGA V přípravku AZARGA je konzervační látka (benzalkonium-chlorid), jež může zbarvovat měkké kontaktní oční čočky a může způsobovat podráždění oka. Proto nenoste při používání přípravku AZARGA oční čočky. Po použití přípravku AZARGA počkejte 15 minut a teprve pak si čočky opět nasaďte. 3. JAK SE PŘÍPRAVEK AZARGA POUŽÍVÁ Vždy používejte přípravek AZARGA přesně podle pokynů svého lékaře. Pokud si nejste jistý/á, poraďte se se svým lékařem nebo lékárníkem. Obvyklá dávka je Dospělí: jedna kapka do postiženého oka (postižených očí) dvakrát denně-ráno a večer. Přípravek AZARGA používejte do obou očích pouze tehdy, když Vám to řekl Váš lékař. Užívejte jej tak dlouho, jak Vám řekl Váš lékař. 22
23 1 2 3 Připravte si lahvičku s přípravkem AZARGA a zrcadlo. Umyjte si ruce. Před použitím lahvičku dobře protřepejte. Odšroubujte víčko lahvičky. Držte lahvičku dnem vzhůru mezi palcem a prsty. Zakloňte hlavu. Stáhněte víčko čistým prstem dolů tak, aby mezi víčkem a okem vznikla jakási kapsa. Kapka se vkápne do tohoto místa (obrázek 1). Přibližte hrot lahvičky k oku. Jestli Vám to pomůže, použijte zrcadlo. Nedotýkejte se kapátkem oka nebo očního víčka, okolních tkání nebo jiných povrchů. Mohlo by tak dojít ke znečištění kapek. Lehce zatlačte na dno lahvičky, aby se uvolnila vždy jenom jedna kapka přípravku AZARGA. Lahvičku nestlačujte: je navržena tak, aby stačilo lehké zatlačení na dno (obrázek 2). Po použití přípravku AZARGA stiskněte prstem koutek oka u nosu (obrázek 3). Tím se napomůže tomu, aby se přípravek AZARGA nedostal do celého těla. Když používáte kapky do obou očí, opakujte výše uvedené kroky pro druhé oko. Ihned po použití pevně uzavřete uzávěr lahvičky. Před otevřením další lahvičky spotřebujte nejprve celý obsah první lahvičky. Netrefíte-li se kapkou do oka, zkuste to znovu. Jestliže jste použil(a) více přípravku AZARGA než jste měl(a), vypláchněte oko teplou vodou. Nevkapávejte žádné další kapky, dokud není čas Vaší další pravidelné dávky. Jestliže jste zapomněl(a) použít přípravek AZARGA, pokračujte až další plánovanou dávkou. Nezdvojujte následující dávku, abyste vynechanou dávku nahradil(a). Nepoužívejte více než jednu kapku do postiženého oka (očí) dvakrát denně. Jestliže jste přestal(a) používat přípravek AZARGA, aniž byste se poradil(a) se svým lékařem, oční tlak ve Vašem oku nebude kontrolován, což by mohlo vést i ke ztrátě Vašeho zraku. Jestliže používáte jiné oční kapky, vyčkejte mezi použitím přípravku AZARGA a dalšího přípravku minimálně 5 minut. Máte-li jakékoli další otázky, týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka. 4. MOŽNÉ NEŽÁDOUCÍ ÚČINKY Podobně jako všechny léky může mít i přípravek AZARGA nežádoucí účinky, které se ale nemusí vyskytnout u každého. Obvykle můžete v používání kapek pokračovat, pokud nejsou účinky závažné. Máte-li obavy, sdělte to svému lékaři nebo lékárníkovi. Při používání přípravku AZARGA byly pozorovány následující nežádoucí účinky : 23
24 Časté nežádoucí účinky (objevují se u 1 až 10 uživatelů ze 100) Účinky na oko: rozmazané vidění, podráždění oka, bolest oka, abnormální pocit v očích Celkové nežádoucí účinky: špatná chuť Méně časté nežádoucí účinky (objevují se u 1 až 10 uživatelů z 1000) Účinky na oko: zánět povrchu oka s poškozením povrchu, zánět uvnitř oka, červené oko, svědění oka; svědění víčka, zčervenání, otok nebo tvorba krusty očního víčka; výtok z oka, oční alergie, suché oko, unavené oči Celkové nežádoucí účinky: chronické plicní onemocnění, snížení krevního tlaku, dráždění v hrdle, kašel, potíže se spánkem, kožní zánět, zčervenání nebo svědění, výtok z nosu, potíže s vlasy Dále: Přípravek AZARGA je kombinací 2 v současné době prodávaných léčivých přípravků. Další nežádoucí účinky, jež byly pozorovány u jednotlivých léků, které se mohou vyskytnout i u přípravku AZARGA, jsou následující: Účinky na oko: poškození optického nervu, zvýšený tlak v oku, usazeniny na povrchu oka, poruchy rohovky, snížené vnímání v oku, zánět nebo infekce spojivky, abnormální, dvojité nebo snížené vidění, zvýšená pigmentace oka, růst na povrchu oka, zvýšená produkce slz, otok oka, citlivost na světlo, zpomalený růst nebo snížení počtu očních řas, pokles očních víček, zánět žláz v očním víčku. Celkové nežádoucí účinky: Srdce a oběh: změny srdeční frekvence nebo rytmu, bolest na hrudi, snížená funkce srdce, srdeční zástava, zvýšený krevní tlak, snížení krevního toku do mozku, mozková příhoda, otoky končetin Dýchání: dušnost nebo obtíže s dýcháním, známky nachlazení, otok dýchacích cest, infekce dutin, kýchání, ucpaný nos, sucho v nose, krvácení z nosu, astma Nervový systém a celkové poruchy: deprese, potíže s pamětí, bolest hlavy, nervozita, podrážděnost, únava, třes, abnormální pocity, mdloby, závrať, ospalost, celková nebo velká slabost Zažívání: nucení k zvracení, zvracení, průjem, střevní plyny nebo bolest břicha, zánět hrdla, sucho nebo abnormální pocity v ústech, snížení vnímání chuti, porucha trávení, bolest břicha Krev: abnormální nálezy při vyšetření funkce jater, zvýšené hladiny chloridových iontů, nebo snížený počet červených krvinek při vyšetření krve Alergie: zhoršené příznaky alergie Uši: zvonění v uších, pocit motání nebo závratě Kůže: svědění, vyrážka, abnormální nebo snížený cit kůže, ztráta vlasů Svaly: všeobecná bolest zad, kloubů nebo svalů, stahy (křeče) svalstva, bolest končetin, svalová slabost 24
25 Ledviny: bolest ledvin jako bolest v dolní části zad, časté močení Reprodukce: snížení pohlavního pudu, sexuální obtíže u mužů Metabolismus: nízká hladina cukru v krvi Pokud se některý z nežádoucích účinků vyskytne v závažné míře nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi. 5. JAK PŘÍPRAVEK AZARGA UCHOVÁVAT Uchovávejte mimo dosah a dohled dětí. Přípravek AZARGA nepoužívejte po uplynutí doby použitelnosti, uvedené na lahvičce a papírové skládačce (krabičce) za EXP (zkratka používaná pro dobu použitelnosti). Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Tento přípravek nevyžaduje žádné zvláštní podmínky uchovávání. Lahvičku zlikvidujte za 4 týdny po prvním otevření, aby se zabránilo infekcím, a použijte novou lahvičku. Zapište si datum jejího otevření na štítek lahvičky a na štítek papírové krabičky, na příslušné vyznačené místo. Léčivé přípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak máte likvidovat přípravky, které již nepotřebujete. Tato opatření pomáhají chránit životní prostředí. 6. DALŠÍ INFORMACE Co přípravek AZARGA obsahuje Léčivými látkami jsou brinzolamid a timolol. Jeden ml suspenze obsahuje 10 mg brinzolamidu a 5 mg timololu. Dalšími složkami jsou chlorid benzalkonia, carbopol 974P, edetan disodný, manitol (E421), čištěná voda, chlorid sodný, tyloxapol, kyselina chlorovodíková a/nebo hydroxid sodný. Malé množství kyseliny chlorovodíkové/hydroxidu sodného se přidává proto, aby se udržely normální hodnoty kyselosti (úrovně ph). Jak přípravek AZARGA vypadá a co obsahuje toto balení AZARGA je tekutina (bílá až našedlá stejnoměrná suspenze), dodávaná v balení obsahujícím 5 ml plastovou lahvičku se šroubovacím uzávěrem, nebo v balení obsahujícím tři 5 ml lahvičky. Všechny velikosti balení nemusí být na trhu. 25
26 Držitel rozhodnutí o registraci Alcon Laboratories (UK) Ltd. Boundary Way Hemel Hempstead Herts HP2 7UD Velká Británie Výrobce S.A. Alcon-Couvreur N.V Rijksweg 14 B-2870 Puurs Belgie 26
27 Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci: België/Belgique/Belgien Luxembourg/Luxemburg SA Alcon-Couvreur NV + 32 (0) (België/Belgique/Belgien) България Алкон България ЕООД Česká republika Alcon Pharmaceuticals (Czech Republic) s.r.o Danmark Alcon Danmark A/S Deutschland Alcon Pharma GmbH + 49 (0) Ελλάδα Κύπρος Άλκον Λαμποράτορις Ελλάς ΑΕΒΕ (Ελλάδα) Eesti Alcon Eesti España Alcon Cusí, S.A France Laboratoires Alcon + 33 (0) Ireland Malta United Kingdom Alcon Laboratories (UK) Ltd (0) (United Kingdom) Ísland K. Pétursson ehf Lietuva Alcon Pharmaceuticals Ltd. atstovybė Magyarország Alcon Hungária Gyógyszerkereskedelmi Kft Nederland Alcon Nederland BV + 31 (0) Norge Alcon Norge AS Österreich Alcon Ophthalmika GmbH + 43 (0) Polska Alcon Polska Sp. z o.o Portugal Alcon Portugal Produtos e Equipamentos Oftalmológicos, Lda România S.C. Alcon Romania S.R.L. : Slovenija Alcon d.o.o Slovenská Republika Alcon Pharmaceuticals Ltd oz Suomi/Finland Alcon Finland Oy (0)
28 Italia Alcon Italia S.p.A Sverige Alcon Sverige AB + 46 (0) E-post: receptionen@alconlabs.com Latvija Alcon Pharmaceuticals Ltd Tato příbalová informace byla naposledy schválena dne Podrobné informace o tomto přípravku jsou uveřejněny na webových stránkách Evropské lékové agentury (EMEA): 28
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE. AZOPT 10 mg/ml oční kapky, suspenze Brinzolamid
 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE AZOPT 10 mg/ml oční kapky, suspenze Brinzolamid Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE AZOPT 10 mg/ml oční kapky, suspenze Brinzolamid Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE. TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum
 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
1. NÁZEV PŘÍPRAVKU. AZOPT 10 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ. Brinzolamidum 10 mg/ml. Pomocné látky viz bod 6.1.
 1. NÁZEV PŘÍPRAVKU AZOPT 10 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Brinzolamidum 10 mg/ml. Pomocné látky viz bod 6.1. 3. LÉKOVÁ FORMA Oční kapky, suspenze. Azopt je bílá až
1. NÁZEV PŘÍPRAVKU AZOPT 10 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Brinzolamidum 10 mg/ml. Pomocné látky viz bod 6.1. 3. LÉKOVÁ FORMA Oční kapky, suspenze. Azopt je bílá až
PŘÍBALOVÁ INFORMACE. EMADINE 0,5 mg/ml, Oční Kapky, roztok. Emedastinum
 PŘÍBALOVÁ INFORMACE EMADINE 0,5 mg/ml, Oční Kapky, roztok. Emedastinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou informaci.pro případ,
PŘÍBALOVÁ INFORMACE EMADINE 0,5 mg/ml, Oční Kapky, roztok. Emedastinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou informaci.pro případ,
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE. OPATANOL 1 mg/ml oční kapky, roztok. Olopatadinum.
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE OPATANOL 1 mg/ml oční kapky, roztok. Olopatadinum. Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE OPATANOL 1 mg/ml oční kapky, roztok. Olopatadinum. Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn.: sukls152570/2010 a příloha k sp.zn.: sukls /2011
 Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn.: sukls152570/2010 a příloha k sp.zn.: sukls1519211/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Flarex 1 mg/ml oční kapky, suspenze fluorometholoni
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn.: sukls152570/2010 a příloha k sp.zn.: sukls1519211/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Flarex 1 mg/ml oční kapky, suspenze fluorometholoni
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls208364/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls208364/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VISTAGAN Liquifilm 0,5 % Oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Levobunololi
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls208364/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU VISTAGAN Liquifilm 0,5 % Oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Levobunololi
sp.zn. sukls127336/2013 sukls53259/2014
 sp.zn. sukls127336/2013 sukls53259/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU BETOPTIC S oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml suspenze obsahuje betaxololum 2,5 mg
sp.zn. sukls127336/2013 sukls53259/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU BETOPTIC S oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml suspenze obsahuje betaxololum 2,5 mg
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. FOTIL FOTIL FORTE oční kapky, roztok pilocarpinum hydrochloridum, timololi maleas
 sp.zn. sukls154707/2012 sukls154712/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA FOTIL FOTIL FORTE oční kapky, roztok pilocarpinum hydrochloridum, timololi maleas Přečtěte si pozorně celou příbalovou
sp.zn. sukls154707/2012 sukls154712/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA FOTIL FOTIL FORTE oční kapky, roztok pilocarpinum hydrochloridum, timololi maleas Přečtěte si pozorně celou příbalovou
sp.zn.: sukls59875/2012 a k sp.zn.: sukls58444/2012
 sp.zn.: sukls59875/2012 a k sp.zn.: sukls58444/2012 Příbalová informace: informace pro pacienta BETALMIC 0,5% Oční kapky, roztok Betaxololi hydrochloridum Přečtěte si pozorně celou příbalovou informaci
sp.zn.: sukls59875/2012 a k sp.zn.: sukls58444/2012 Příbalová informace: informace pro pacienta BETALMIC 0,5% Oční kapky, roztok Betaxololi hydrochloridum Přečtěte si pozorně celou příbalovou informaci
BETOPTIC oční kapky, roztok betaxololum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE BETOPTIC oční kapky, roztok betaxololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou informaci
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE BETOPTIC oční kapky, roztok betaxololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si příbalovou informaci
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE VIGAMOX 5 mg/ml OČNÍ KAPKY oční kapky, roztok Moxifloxacinum HYDROCHLORIDUM
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE VIGAMOX 5 mg/ml OČNÍ KAPKY oční kapky, roztok Moxifloxacinum HYDROCHLORIDUM Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE VIGAMOX 5 mg/ml OČNÍ KAPKY oční kapky, roztok Moxifloxacinum HYDROCHLORIDUM Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE:INFORMACE PRO PACIENTA. EFFLUMIDEX Liquifilm oční kapky, suspenze fluorometholonum
 PŘÍBALOVÁ INFORMACE:INFORMACE PRO PACIENTA EFFLUMIDEX Liquifilm oční kapky, suspenze fluorometholonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte
PŘÍBALOVÁ INFORMACE:INFORMACE PRO PACIENTA EFFLUMIDEX Liquifilm oční kapky, suspenze fluorometholonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte
Příbalová informace: informace pro pacienta. Fredomat 40 mikrogramů/ml oční kapky, roztok. travoprostum
 sp.zn.sukls190238/2015 Příbalová informace: informace pro pacienta Fredomat 40 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls190238/2015 Příbalová informace: informace pro pacienta Fredomat 40 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE. OPATANOL 1 mg/ml oční kapky, roztok Olopatadinum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE OPATANOL 1 mg/ml oční kapky, roztok Olopatadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE OPATANOL 1 mg/ml oční kapky, roztok Olopatadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AZOPT 10 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Každý ml suspense obsahuje 10 mg brinzolamidum. Pomocné látky : Každý ml suspenze
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AZOPT 10 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Každý ml suspense obsahuje 10 mg brinzolamidum. Pomocné látky : Každý ml suspenze
BETOPTIC S oční kapky, suspenze betaxololum
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.:98089/2009 a příloha k sp.zn.: sukls98117/2010 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE BETOPTIC S oční kapky, suspenze betaxololum Přečtěte
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.:98089/2009 a příloha k sp.zn.: sukls98117/2010 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE BETOPTIC S oční kapky, suspenze betaxololum Přečtěte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Akistan 50 mikrogramů/ml oční kapky, roztok (latanoprostum)
 Sp. zn. sukls79185/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Akistan 50 mikrogramů/ml oční kapky, roztok (latanoprostum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete používat
Sp. zn. sukls79185/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Akistan 50 mikrogramů/ml oční kapky, roztok (latanoprostum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete používat
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Latanoprost Apotex 0,005% oční kapky, roztok latanoprostum
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls10153/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Latanoprost Apotex 0,005% oční kapky, roztok latanoprostum Přečtěte si pozorně celou příbalovou
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls10153/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Latanoprost Apotex 0,005% oční kapky, roztok latanoprostum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele. FLAREX 1 mg/ml oční kapky, suspenze. fluorometholoni acetas
 sp.zn.sukls53205/2014 Příbalová informace: informace pro uživatele FLAREX 1 mg/ml oční kapky, suspenze fluorometholoni acetas Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek
sp.zn.sukls53205/2014 Příbalová informace: informace pro uživatele FLAREX 1 mg/ml oční kapky, suspenze fluorometholoni acetas Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek
Použití a dětí a dospívajících OPATANOL lze použít u dětských pacientů (ve věku tří let a starších) se stejným dávkováním jako u dospělých.
 1. NÁZEV PŘÍPRAVKU OPATANOL 1 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje 1 mg olopatadinum (jako hydrochlorid). Pomocné látky viz. 6.1. 3. LÉKOVÁ FORMA Oční kapky, roztok.
1. NÁZEV PŘÍPRAVKU OPATANOL 1 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje 1 mg olopatadinum (jako hydrochlorid). Pomocné látky viz. 6.1. 3. LÉKOVÁ FORMA Oční kapky, roztok.
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls154079/2012
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls154079/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OPTODROP COMBI 2% + 0,5% oční kapky, roztok (dorzolamidi hydrochloridum, timololi maleas)
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls154079/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OPTODROP COMBI 2% + 0,5% oční kapky, roztok (dorzolamidi hydrochloridum, timololi maleas)
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls29736/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TEARS NATURALE II oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml roztoku obsahuje dextranum 70 1,0 mg a hypromelosum 3,0
sp.zn.sukls29736/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TEARS NATURALE II oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml roztoku obsahuje dextranum 70 1,0 mg a hypromelosum 3,0
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU EMADINE 0,5 mg/ml, Oční Kapky, roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml roztoku obsahuje emedastinum 0,5 mg (jako difumarát) Pomocné látky: Benzalkonium-chloride
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU EMADINE 0,5 mg/ml, Oční Kapky, roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml roztoku obsahuje emedastinum 0,5 mg (jako difumarát) Pomocné látky: Benzalkonium-chloride
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU. NEVANAC 1 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ. 1 ml suspenze obsahuje nepafenacum 1 mg.
 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU NEVANAC 1 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml suspenze obsahuje nepafenacum 1 mg. Pomocné látky: benzalkonium-chlorid 0,05 mg Úplný seznam
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU NEVANAC 1 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml suspenze obsahuje nepafenacum 1 mg. Pomocné látky: benzalkonium-chlorid 0,05 mg Úplný seznam
sp.zn.sukls57081/2014
 sp.zn.sukls57081/2014 Příbalová informace: informace pro uživatele tobramycinum 0,3% Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás
sp.zn.sukls57081/2014 Příbalová informace: informace pro uživatele tobramycinum 0,3% Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás
Příbalová informace: Informace pro uživatele. Nolodon 1 mg/ml oční kapky, roztok. Olopatadini hydrochloridum
 Sp.zn. sukls17707/2015 Příbalová informace: Informace pro uživatele Nolodon 1 mg/ml oční kapky, roztok Olopatadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn. sukls17707/2015 Příbalová informace: Informace pro uživatele Nolodon 1 mg/ml oční kapky, roztok Olopatadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro pacienty. EMADINE 0,5 mg/ml, oční kapky, roztok Emedastinum
 Příbalová informace: informace pro pacienty EMADINE 0,5 mg/ml, oční kapky, roztok Emedastinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro pacienty EMADINE 0,5 mg/ml, oční kapky, roztok Emedastinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele. IZBA 30 mikrogramů/ml oční kapky, roztok travoprostum
 Příbalová informace: informace pro uživatele IZBA 30 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele IZBA 30 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
Příbalová informace: informace pro uživatele. AZOPT 10 mg/ml oční kapky, suspenze Brinzolamidum
 Příbalová informace: informace pro uživatele AZOPT 10 mg/ml oční kapky, suspenze Brinzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele AZOPT 10 mg/ml oční kapky, suspenze Brinzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU OPATANOL 1 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml roztoku obsahuje 1 mg olopatadinum (jako hydrochlorid). Pomocné
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU OPATANOL 1 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml roztoku obsahuje 1 mg olopatadinum (jako hydrochlorid). Pomocné
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90
 Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Cynt 0,2 Cynt 0,3 Cynt 0,4 potahované tablety moxonidinum
 Příloha č. 1 k rozhodnutí o převodu registrace sp.zn. sukls212727/2012, sukls212733/2012 a sukls212739/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cynt 0,2 Cynt 0,3 Cynt 0,4 potahované tablety moxonidinum
Příloha č. 1 k rozhodnutí o převodu registrace sp.zn. sukls212727/2012, sukls212733/2012 a sukls212739/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cynt 0,2 Cynt 0,3 Cynt 0,4 potahované tablety moxonidinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
Příbalová informace: informace pro uživatele. AZARGA 10 mg/ml + 5 mg/ml oční kapky, suspenze Brinzolamidum/Timololum
 Příbalová informace: informace pro uživatele AZARGA 10 mg/ml + 5 mg/ml oční kapky, suspenze Brinzolamidum/Timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro uživatele AZARGA 10 mg/ml + 5 mg/ml oční kapky, suspenze Brinzolamidum/Timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Brizadopt 10 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml suspenze obsahuje brinzolamidum10 mg. Jedna kapka obsahuje brinzolamidum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Brizadopt 10 mg/ml oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml suspenze obsahuje brinzolamidum10 mg. Jedna kapka obsahuje brinzolamidum
2. Čemu musíte věnovat pozornost, než začnete APO-DONEPEZIL užívat
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls122778/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-DONEPEZIL 5 mg potahované tablety APO-DONEPEZIL 10 mg potahované tablety Přečtěte si
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls122778/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-DONEPEZIL 5 mg potahované tablety APO-DONEPEZIL 10 mg potahované tablety Přečtěte si
sp.zn.: sukls165485/2011
 sp.zn.: sukls165485/2011 Příbalová informace: informace pro uživatele SPERSALLERG antazolini hydrochloridum, tetryzolini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn.: sukls165485/2011 Příbalová informace: informace pro uživatele SPERSALLERG antazolini hydrochloridum, tetryzolini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příbalová informace: informace pro uživatele. Dorzoptic 20 mg/ml oční kapky, roztok Dorzolamidum
 Sp. zn. sukls203996/2015 Příbalová informace: informace pro uživatele Dorzoptic 20 mg/ml oční kapky, roztok Dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp. zn. sukls203996/2015 Příbalová informace: informace pro uživatele Dorzoptic 20 mg/ml oční kapky, roztok Dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jeden ml roztoku obsahuje brimonidini tartas 2 mg, což odpovídá brimonidinum 1,3 mg.
 sp.zn.sukls41147/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LUXFEN, 2mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje brimonidini tartas 2 mg, což odpovídá
sp.zn.sukls41147/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LUXFEN, 2mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje brimonidini tartas 2 mg, což odpovídá
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn. sukls73712/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Bimican 0,3 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje bimatoprostum 0,3 mg. Jedna kapka
Sp.zn. sukls73712/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Bimican 0,3 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje bimatoprostum 0,3 mg. Jedna kapka
Příbalová informace: informace pro pacienta. Zurampic 200 mg potahované tablety lesinuradum
 Příbalová informace: informace pro pacienta Zurampic 200 mg potahované tablety lesinuradum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro pacienta Zurampic 200 mg potahované tablety lesinuradum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příbalová informace: informace pro pacienta. brinzolamidum
 Příbalová informace: informace pro pacienta Brizadopt 10 mg/ml oční kapky, suspenze brinzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro pacienta Brizadopt 10 mg/ml oční kapky, suspenze brinzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
PŘÍBALOVÁ INFORMACE 2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE TOBRADEX POUŽÍVAT
 PŘÍBALOVÁ INFORMACE TOBRADEX, 3mg/ml + 1mg/ml, oční kapky, suspenze (tobramycinum/dexamethasonum ) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte
PŘÍBALOVÁ INFORMACE TOBRADEX, 3mg/ml + 1mg/ml, oční kapky, suspenze (tobramycinum/dexamethasonum ) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte
Příbalová informace: informace pro pacienta. NEVANAC 1 mg/ml oční kapky, suspenze Nepafenacum
 Příbalová informace: informace pro pacienta NEVANAC 1 mg/ml oční kapky, suspenze Nepafenacum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro pacienta NEVANAC 1 mg/ml oční kapky, suspenze Nepafenacum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro pacienta. Tears Naturale II oční kapky, roztok dextranum 70, hypromelosum
 sp.zn.sukls103625/2017 Příbalová informace: informace pro pacienta Tears Naturale II oční kapky, roztok dextranum 70, hypromelosum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.sukls103625/2017 Příbalová informace: informace pro pacienta Tears Naturale II oční kapky, roztok dextranum 70, hypromelosum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Co je Voltaren Ophtha CD Léčivou látkou přípravku Voltaren Ophtha CD je diklofenak sodný (diclofenacum natricum).
 Příloha č.1 ke sdělení sp.zn.sukls23896/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VOLTAREN OPHTHA CD oční kapky, roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha č.1 ke sdělení sp.zn.sukls23896/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VOLTAREN OPHTHA CD oční kapky, roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Timlatan 50 mikrogramů/ml + 5 mg/ml oční kapky, roztok Latanoprostum /timololum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Timlatan 50 mikrogramů/ml + 5 mg/ml oční kapky, roztok Latanoprostum /timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Timlatan 50 mikrogramů/ml + 5 mg/ml oční kapky, roztok Latanoprostum /timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU LUMIGAN 0,1 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje bimatoprostum 0,1 mg. Pomocné látky se známým
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU LUMIGAN 0,1 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje bimatoprostum 0,1 mg. Pomocné látky se známým
PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE. OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas
 PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE : INFORMACE PRO UŽIVATELE OSSEOR 2 g - zrněný prášek pro přípravu perorální suspenze Strontii ranelas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro pacienta. Azomyr 0,5 mg/ml perorální roztok desloratadinum
 Příbalová informace: informace pro pacienta Azomyr 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: informace pro pacienta Azomyr 0,5 mg/ml perorální roztok desloratadinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Jeden ml obsahuje dorzolamidi hydrochloridum 22,26 mg odpovídající dorzolamidum 20 mg.
 1. NÁZEV PŘÍPRAVKU Trusopt free bez konzervačních přísad 20 mg/ml oční kapky, roztok v jednodávkovém obalu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje dorzolamidi hydrochloridum 22,26 mg
1. NÁZEV PŘÍPRAVKU Trusopt free bez konzervačních přísad 20 mg/ml oční kapky, roztok v jednodávkovém obalu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje dorzolamidi hydrochloridum 22,26 mg
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. JODID DRASELNÝ 2% UNIMED PHARMA oční kapky, roztok
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE JODID DRASELNÝ 2% UNIMED PHARMA oční kapky, roztok Kalii iodidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete používat tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE JODID DRASELNÝ 2% UNIMED PHARMA oční kapky, roztok Kalii iodidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete používat tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE. Galvus 50 mg tablety Vildagliptinum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE Galvus 50 mg tablety Vildagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, neţ začnete tento přípravek uţívat. - Ponechte si příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŢIVATELE Galvus 50 mg tablety Vildagliptinum Přečtěte si pozorně celou příbalovou informaci dříve, neţ začnete tento přípravek uţívat. - Ponechte si příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PURIVIST 0,5 mg/ml oční kapky, roztok Epinastini hydrochloridum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PURIVIST 0,5 mg/ml oční kapky, roztok Epinastini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE PURIVIST 0,5 mg/ml oční kapky, roztok Epinastini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
sp. zn. sukls180859/2015
 sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
sp. zn. sukls180859/2015 Příbalová informace: informace pro pacienta DONA 1500 mg, prášek pro perorální roztok glucosamini sulfas cristallicus Přečtěte si pozorně celou příbalovou informaci dříve, než
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Arulatan 50 mikrogramů/ml, oční kapky, roztok Latanoprostum
 Příloha č. 2 k rozhodnutí o registraci sp.zn.sukls99149/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Arulatan 50 mikrogramů/ml, oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou
Příloha č. 2 k rozhodnutí o registraci sp.zn.sukls99149/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Arulatan 50 mikrogramů/ml, oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
sp.zn.: sukls17654/2011 a sp.zn.: sukls92536/2011
 sp.zn.: sukls17654/2011 a sp.zn.: sukls92536/2011 Příbalová informace: informace pro uživatele MAXITROL, oční kapky, suspenze Neomycini sulfas, polymyxini B sulfas, dexamethasonum Přečtěte si pozorně celou
sp.zn.: sukls17654/2011 a sp.zn.: sukls92536/2011 Příbalová informace: informace pro uživatele MAXITROL, oční kapky, suspenze Neomycini sulfas, polymyxini B sulfas, dexamethasonum Přečtěte si pozorně celou
PŘÍLOHA III OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
 PŘÍLOHA III OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE 1 B. PŘÍBALOVÁ INFORMACE 2 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dasselta 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou
PŘÍLOHA III OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE 1 B. PŘÍBALOVÁ INFORMACE 2 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dasselta 5 mg potahované tablety desloratadinum Přečtěte si pozorně celou příbalovou
Příbalová informace: informace pro uživatele. Xaloptic 0,005% (0,05 mg/ml), oční kapky, roztok. Latanoprostum
 Sp.zn. sukls116684/2014 Příbalová informace: informace pro uživatele Xaloptic 0,005% (0,05 mg/ml), oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete užívat
Sp.zn. sukls116684/2014 Příbalová informace: informace pro uživatele Xaloptic 0,005% (0,05 mg/ml), oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete užívat
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bronchostop sirup. Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt
 Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele. ARTEOPTIC 2% (carteololi hydrochloridum) oční kapky, roztok
 sp.zn.sukls88189/2014 Příbalová informace: informace pro uživatele ARTEOPTIC 2% (carteololi hydrochloridum) oční kapky, roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls88189/2014 Příbalová informace: informace pro uživatele ARTEOPTIC 2% (carteololi hydrochloridum) oční kapky, roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Azelastin-POS 0,5 mg/ml oční kapky, roztok. Azelastini hydrochloridum
 Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls195317/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Azelastin-POS 0,5 mg/ml oční kapky, roztok Azelastini hydrochloridum Přečtěte si pozorně tuto
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls195317/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Azelastin-POS 0,5 mg/ml oční kapky, roztok Azelastini hydrochloridum Přečtěte si pozorně tuto
Příbalová informace: informace pro pacienta. ANACID 258 mg/388 mg perorální suspenze. Magnesii hydroxidum, Algeldrati suspensio
 sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele. TEARS NATURALE II oční kapky, roztok dextranum 70, hypromelosum
 sp.zn.sukls29736/2015 Příbalová informace: informace pro uživatele TEARS NATURALE II oční kapky, roztok dextranum 70, hypromelosum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.sukls29736/2015 Příbalová informace: informace pro uživatele TEARS NATURALE II oční kapky, roztok dextranum 70, hypromelosum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. Latanoprost Apotex 0,005% oční kapky, roztok latanoprostum
 Příbalová informace: informace pro uživatele Latanoprost Apotex 0,005% oční kapky, roztok latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pro uživatele Latanoprost Apotex 0,005% oční kapky, roztok latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA ALPHAGAN brimonidini tartras oční kapky, roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA ALPHAGAN brimonidini tartras oční kapky, roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AMOL. Perorální kapky, roztok (
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AMOL Perorální kapky, roztok ( Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek je dostupný bez lékařského
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AMOL Perorální kapky, roztok ( Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek je dostupný bez lékařského
Příbalová informace: informace pro pacienta. Maltofer, 10 mg/ml sirup. polymaltosum ferricum
 sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. MUCOSOLVAN junior Sirup Ambroxoli hydrochloridum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE MUCOSOLVAN junior Sirup Ambroxoli hydrochloridum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek je
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE MUCOSOLVAN junior Sirup Ambroxoli hydrochloridum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje pro vás důležité údaje. Tento přípravek je
Příbalová informace: informace pro pacienta. XALATAN oční kapky, roztok (latanoprostum)
 Příbalová informace: informace pro pacienta XALATAN oční kapky, roztok (latanoprostum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete používat tento přípravek, protože obsahuje pro Vás
Příbalová informace: informace pro pacienta XALATAN oční kapky, roztok (latanoprostum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete používat tento přípravek, protože obsahuje pro Vás
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ECALTA 100 mg, prášek pro koncentrát pro infuzní roztok Anidulafunginum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE- VP
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn.: sukls237631/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE- VP ZODAC potahované tablety (cetirizini dihydrochloridum) Přečtěte si pozorně tuto příbalovou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.: sukls237631/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE- VP ZODAC potahované tablety (cetirizini dihydrochloridum) Přečtěte si pozorně tuto příbalovou
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn.: sukls16509/2009 a příloha k sp.zn.: sukls37990/2012
 Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn.: sukls16509/2009 a příloha k sp.zn.: sukls37990/2012 Příbalová informace: informace pro pacienta UNI TIMOLOL 0,5% UNIMED PHARMA Oční kapky, roztok
Příloha č. 1 k rozhodnutí o prodloužení registrace sp.zn.: sukls16509/2009 a příloha k sp.zn.: sukls37990/2012 Příbalová informace: informace pro pacienta UNI TIMOLOL 0,5% UNIMED PHARMA Oční kapky, roztok
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls100905/2011 a příloha ke sp.zn.sukls258988/2011
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls100905/2011 a příloha ke sp.zn.sukls258988/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DICLOABAK 1 mg/ml, oční kapky, roztok Diclofenacum
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls100905/2011 a příloha ke sp.zn.sukls258988/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DICLOABAK 1 mg/ml, oční kapky, roztok Diclofenacum
Příbalová informace: informace pro uživatele. VIGAMOX 5 mg/ml OČNÍ KAPKY oční kapky, roztok moxifloxacinum hydrochloridum
 Příbalová informace: informace pro uživatele VIGAMOX 5 mg/ml OČNÍ KAPKY oční kapky, roztok moxifloxacinum hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele VIGAMOX 5 mg/ml OČNÍ KAPKY oční kapky, roztok moxifloxacinum hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. FLUCON 1 mg/ml, oční kapky, suspenze. fluorometholonum
 Příbalová informace: informace pro uživatele FLUCON 1 mg/ml, oční kapky, suspenze fluorometholonum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele FLUCON 1 mg/ml, oční kapky, suspenze fluorometholonum Přečtěte si pozorně celou příbalovou informace dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro pacienta. EFFLUMIDEX Liquifilm 1 mg/ml oční kapky, suspenze fluorometholonum
 sp.zn. sukls256067/2017 Příbalová informace: informace pro pacienta EFFLUMIDEX Liquifilm 1 mg/ml oční kapky, suspenze fluorometholonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls256067/2017 Příbalová informace: informace pro pacienta EFFLUMIDEX Liquifilm 1 mg/ml oční kapky, suspenze fluorometholonum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
BETOPTIC S oční kapky, suspenze betaxololum
 Příbalová informace: informace pro uživatele BETOPTIC S oční kapky, suspenze betaxololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro
Příbalová informace: informace pro uživatele BETOPTIC S oční kapky, suspenze betaxololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje důležité
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE SYNAGIS 100 mg prášek pro přípravu injekčního roztoku s rozpouštědlem Palivizumabum Přečtěte si pozorně tuto příbalovou informaci, protože obsahuje důležité
sp.zn.sukls192314/2011
 sp.zn.sukls192314/2011 Příbalová informace: Informace pro uživatele Optipres 20 mg/ml oční kapky, roztok dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
sp.zn.sukls192314/2011 Příbalová informace: Informace pro uživatele Optipres 20 mg/ml oční kapky, roztok dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Allergocrom Kombi Allergocrom oční kapky Oční kapky, roztok
 sp.zn.: sukls133828/2008 Příbalová informace: informace pro pacienta Allergocrom Kombi Allergocrom oční kapky Oční kapky, roztok Allergocrom nosní sprej Nosní sprej, roztok Dinatrii cromoglicas Přečtěte
sp.zn.: sukls133828/2008 Příbalová informace: informace pro pacienta Allergocrom Kombi Allergocrom oční kapky Oční kapky, roztok Allergocrom nosní sprej Nosní sprej, roztok Dinatrii cromoglicas Přečtěte
sp.zn. sukls101534/2012 Příbalová informace: informace pro pacienta GLABRILUX 0,3 mg/ml oční kapky, roztok bimatoprostum
 sp.zn. sukls101534/2012 Příbalová informace: informace pro pacienta GLABRILUX 0,3 mg/ml oční kapky, roztok bimatoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls101534/2012 Příbalová informace: informace pro pacienta GLABRILUX 0,3 mg/ml oční kapky, roztok bimatoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Enap i.v. 1,25 mg/1 ml injekční roztok enalaprilatum dihydricum
 sp.zn. sukls184192/2014 Příbalová informace: informace pro uživatele Enap i.v. 1,25 mg/1 ml injekční roztok enalaprilatum dihydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls184192/2014 Příbalová informace: informace pro uživatele Enap i.v. 1,25 mg/1 ml injekční roztok enalaprilatum dihydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele. Bondulc 40 mikrogramů/ml oční kapky, roztok. travoprostum
 Sp.zn.sukls262569/2012 Příbalová informace: informace pro uživatele Bondulc 40 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp.zn.sukls262569/2012 Příbalová informace: informace pro uživatele Bondulc 40 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Ofloxacin-POS 3 mg/ml oční kapky, roztok. Ofloxacinum
 Příloha č. 1 k rozhodnutí o registraci sp. zn. sukls222894/2011 Příbalová informace: informace pro uživatele Ofloxacin-POS 3 mg/ml oční kapky, roztok Ofloxacinum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp. zn. sukls222894/2011 Příbalová informace: informace pro uživatele Ofloxacin-POS 3 mg/ml oční kapky, roztok Ofloxacinum Přečtěte si pozorně celou příbalovou informaci
SOUHRN ÚDAJU O PŘÍPRAVKU. 1 ml očních kapek obsahuje epinastini hydrochloridum 0,5 mg (odpovídá 0,436 mg epinastinum)
 Příloha č. 1. NÁZEV PŘÍPRAVKU PURIVIST 0,5 mg/ml oční kapky, roztok SOUHRN ÚDAJU O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŹENÍ 1 ml očních kapek obsahuje epinastini hydrochloridum 0,5 mg (odpovídá
Příloha č. 1. NÁZEV PŘÍPRAVKU PURIVIST 0,5 mg/ml oční kapky, roztok SOUHRN ÚDAJU O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŹENÍ 1 ml očních kapek obsahuje epinastini hydrochloridum 0,5 mg (odpovídá
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Telmisartan Apotex 40 mg Telmisartan Apotex 80 mg tablety Telmisartanum
 Příloha č. 1 k rozhodnutí o registraci sp. zn. sukls247726-27/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Telmisartan Apotex 40 mg Telmisartan Apotex 80 mg tablety Telmisartanum Přečtěte si pozorně
Příloha č. 1 k rozhodnutí o registraci sp. zn. sukls247726-27/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Telmisartan Apotex 40 mg Telmisartan Apotex 80 mg tablety Telmisartanum Přečtěte si pozorně
Příbalová informace: informace pro pacienta. Latalux 50 mikrogramů/ml oční kapky, roztok Latanoprostum
 Sp. zn. sukls136408/2014 Příbalová informace: informace pro pacienta Latalux 50 mikrogramů/ml oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp. zn. sukls136408/2014 Příbalová informace: informace pro pacienta Latalux 50 mikrogramů/ml oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
