Příloha III Dodatky, které je třeba přidat do příslušných bodů souhrnu údajů o přípravku a příbalové informace
|
|
|
- Richard Rohla
- před 8 lety
- Počet zobrazení:
Transkript
1 Příloha III Dodatky, které je třeba přidat do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté, co Komise přijme rozhodnutí, provedou příslušné vnitrostátní orgány požadované úpravy údajů o přípravku. 8
2 SOUHRN ÚDAJŮ O PŘÍPRAVKU V souhrnu údajů o přípravku Quixil je třeba provést tyto změny: 4.2 Dávkování a způsob podání Text tohoto bodu bude znít takto: Quixil smí používat pouze zkušení chirurgové, kteří absolvovali školení pro použití přípravku QUIXIL Způsob a cesta podání Text tohoto bodu bude znít takto: Epilezionální podání. Aby se předešlo riziku potenciálně život ohrožující vzduchové embolie, smí se Quixil aplikovat pouze pomocí stlačeného CO 2. Při otevřených chirurgických zákrocích pro nástřik přípravku Quixil se smí používat pouze tlakový dodávající maximální tlak ne vyšší než 2,5 barů a používající pouze plynný oxid uhličitý. Před aplikací přípravku Quixil je třeba povrch rány usušit standardní technikou (např. přerušovanou aplikací kompresních obvazů, pomocí tamponů nebo odsávacích zařízení). Přípravek je nutné rekonstituovat a aplikovat podle pokynů a s pomocí prostředků doporučených pro tento výrobek (viz bod 6.6). Konkrétní doporučení ohledně požadovaného tlaku a vzdálenosti od tkáně při nástřiku naleznete v bodech 4.4 a Kontraindikace Na konci bodu se uvede tato kontraindikace: Přípravek Quixil se nesmí aplikovat nástřikem při endoskopických zákrocích. 4.4 Zvláštní upozornění a opatření pro použití Při použití nástřikových zařízení s tlakovým em při aplikaci přípravku Quixil došlo ke vzduchové nebo plynové embolii. Zdá se, že tato příhoda souvisí s použitím nástřikových zařízení při vyšším než doporučeném tlaku nebo v těsné blízkosti povrchu tkáně. Při aplikaci přípravku Quixil pomocí nástřikového zařízení musí být tlak v rozsahu doporučeném výrobcem nástřikového zařízení. Pokud nejsou k dispozici konkrétní doporučení, tlak nesmí překročit 2,0 barů 2,5 barů. Quixil se nesmí nastřikovat z menší vzdálenosti, než jakou doporučuje výrobce nástřikového zařízení. Pokud nejsou k dispozici konkrétní doporučení, Quixil se nesmí nastřikovat ze vzdálenosti menší než 10 cm 15 cm od povrchu tkáně. Při nástřiku přípravku Quixil je třeba monitorovat změny v krevním tlaku, pulzu, nasycení kyslíkem a koncentraci CO 2 na konci výdechu, protože je zde možnost výskytu vzduchové nebo plynové embolie. Při používání přídavných hrotů s tímto výrobkem je třeba se řídit návodem k použití hrotů. se nahradí níže uvedeným textem psaným tučným písmem a podtrženě: 9
3 Při použití nástřikových zařízení s tlakovým em při aplikaci přípravku Quixil došlo k životu ohrožující vzduchové nebo plynové embolii. Zdá se, že tato příhoda souvisí s použitím nástřikových zařízení při vyšším než doporučeném tlaku nebo v těsné blízkosti povrchu tkáně. Quixil se smí aplikovat nástřikem pouze v případech, kdy je možné přesně odhadnout vzdálenost nástřikového zařízení od tkáně podle doporučení výrobce neaplikujte z menší než doporučené vzdálenosti. Při nástřiku přípravku Quixil pomocí nástřikového zařízení udržujte tlak v rozmezí doporučeném výrobcem nástřikového zařízení (tlak a vzdálenost viz tabulka v bodě 6.6). Při nástřiku přípravku Quixil je třeba monitorovat změny krevního tlaku, pulzu, saturace kyslíkem a koncentrace CO 2 na konci výdechu, protože je zde možnost výskytu vzduchové nebo plynové embolie (viz také bod 4.2). 4.8 Nežádoucí účinky Níže uvedený text se přidá na konec tohoto bodu před poslední větu, jak je uvedeno níže: Při použití nástřikových zařízení s tlakovým em při aplikaci přípravku Quixil došlo k životu ohrožující vzduchové nebo plynové embolii. Zdá se, že tato příhoda souvisí s použitím nástřikových zařízení při vyšším než doporučeném tlaku nebo v těsné blízkosti povrchu tkáně. Bezpečnostní opatření ohledně přenosu infekce viz bod Zvláštní opatření pro uchovávání Text bude znít takto: Uchovávejte při teplotě 18C. Uchovávejte injekční lahvičky ve vnějším kartónovém obalu, aby byl přípravek ochráněn před světlem. Znovu nezmrazujte. Po rozmrazení mohou být neotevřené injekční lahvičky chráněné před světlem uchovávány při teplotě 2 C 8 C po dobu až 30 dnů. Jakmile jsou BAC a trombin nataženy do aplikačního zařízení, musí být použity okamžitě. 6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním Manipulace Aplikace nástřikem Celý bod bude znít takto, psaný tučným písmem a podtrženě, kde je uvedeno: Aby se předešlo riziku život ohrožující vzduchové embolie, smí se Quixil aplikovat pouze pomocí stlačeného CO 2. Při aplikaci přípravku Quixil pomocí nástřikového zařízení musí být tlak a vzdálenost od tkáně v rozmezích doporučených výrobcem (viz bod 4.4) Spojte krátkou trubici na aplikačním zařízení s luerovou koncovkou na dlouhé trubici, která přivádí plyn. Připojte luerovou koncovku trubice s plynem (s bakteriostatickým filtrem) k u tlaku. Tlakový je nutné používat v souladu s pokyny výrobce. Při aplikaci přípravku Quixil pomocí nástřikového zařízení dodržujte výrobcem doporučený y tlak a vzdálenost od tkáně, jak jsou uvedeny níže: Operace Použitá nástřiková souprava Použité hroty aplikátoru Použitý tlakový Doporučená vzdálenost od cílové tkáně Doporučený tlak nástřiku 10
4 Otevřená operace Aplikační zařízení Quixil Žlutý ohebný hrot 6 cm Tlakový Omrix 10 cm 15 cm 2,0 2,5 barů Přípravek se poté nastříká na povrch tkáně v krátkých dávkách (0,1 ml 0,2 ml) tak, aby se vytvořila tenká rovnoměrná vrstva. Quixil vytvoří průhledný film přes celou ošetřovanou oblast. Při nástřiku přípravku Quixil je třeba monitorovat změny krevního tlaku, pulzu, saturace kyslíkem a koncentrace CO 2 na konci výdechu, protože je zde možnost výskytu vzduchové nebo plynové embolie (viz body 4.2 a 4.4). Roztok musí být čirý či lehce opalescentní. Nepoužívejte roztoky, které jsou zakalené nebo obsahují usazeniny. PŘÍBALOVÁ INFORMACE V příbalové informaci k přípravku Quixil je třeba provést tyto změny: 2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE QUIXIL POUŽÍVAT Nepoužívejte Quixil: Na konci bodu se uvede tento text: Quixil se nesmí používat při endoskopických a laparoskopických operacích. Zvláštní opatrnosti při použití přípravku Quixil je zapotřebí: Při použití nástřikových zařízení s tlakovým em při aplikaci přípravku Quixil došlo ke vzduchové nebo plynové embolii. Zdá se, že tato příhoda souvisí s použitím nástřikových zařízení při vyšším než doporučeném tlaku nebo v těsné blízkosti povrchu tkáně. Při aplikaci přípravku Quixil pomocí nástřikového zařízení musí být tlak v rozsahu doporučeném výrobcem nástřikového zařízení. Pokud nejsou k dispozici konkrétní doporučení, tlak nesmí překročit 2,0 barů 2,5 barů. Nenastřikujte z menší vzdálenosti, než jakou doporučuje výrobce nástřikového zařízení. Pokud nejsou k dispozici konkrétní doporučení, nenastřikujte ze vzdálenosti menší než 10 cm 15 cm od povrchu tkáně. Při nástřiku přípravku Quixil je třeba monitorovat změny v krevním tlaku, pulzu, nasycení kyslíkem a koncentraci CO 2 na konci výdechu, protože je zde možnost výskytu vzduchové nebo plynové embolie. Při používání přídavných hrotů s tímto výrobkem je třeba se řídit návodem k použití. se nahradí níže uvedeným textem psaným tučným písmem a podtrženě, kde je uvedeno: Při použití nástřikových zařízení s tlakovým em při aplikaci přípravku Quixil došlo k životu ohrožující vzduchové nebo plynové embolii (do krevního oběhu se dostane vzduch, což může být vážné nebo život ohrožující). Zdá se, že tato příhoda souvisí s použitím nástřikových zařízení při vyšším než doporučeném tlaku nebo v těsné blízkosti povrchu tkáně. K nástřikovým zařízením a doplňkovým hrotům jsou k dispozici návody k použití s doporučenými rozmezími tlaku a vzdálenosti nástřiku od povrchu tkáně. Aby se předešlo riziku potenciálně život ohrožující vzduchové embolie, vašemu chirurgovi bylo doporučeno aplikovat Quixil nástřikem pouze pomocí stlačeného CO 2. Při nástřiku přípravku Quixil je třeba monitorovat změny krevního tlaku, pulzu, saturace kyslíkem a koncentrace CO 2 na konci výdechu, protože je zde možnost výskytu vzduchové nebo plynové embolie. 11
5 Při používání přídavného hrotu s tímto výrobkem se pečlivě řiďte návodem k použití. 3. JAK SE QUIXIL POUŽÍVÁ Quixil smějí používat pouze zkušení chirurgové. Při aplikaci přípravku Quixil pomocí nástřikového zařízení musí být tlak v rozsahu doporučeném výrobcem nástřikového zařízení. Pokud nejsou k dispozici konkrétní doporučení, tlak nesmí překročit 2,0 barů 2,5 barů. Nenastřikujte z menší vzdálenosti, než jakou doporučuje výrobce nástřikového zařízení. Pokud nejsou k dispozici konkrétní doporučení, nenastřikujte ze vzdálenosti menší než 10 cm 15 cm od povrchu tkáně. Při nástřiku přípravku Quixil je třeba monitorovat změny v krevním tlaku, pulzu, nasycení kyslíkem a koncentraci CO 2 na konci výdechu, protože je zde možnost výskytu vzduchové nebo plynové embolie. se nahradí níže uvedeným textem psaným tučným písmem a podtrženě, kde je uvedeno: Quixil smějí používat pouze zkušení chirurgové, kteří absolvovali školení pro použití přípravku QUIXIL. Před aplikací přípravku Quixil je třeba povrch rány usušit standardní technikou (např. přerušovanou aplikací kompresních obvazů, pomocí tamponů nebo odsávacích zařízení). Při aplikaci přípravku Quixil pomocí nástřikového zařízení dodržujte výrobcem doporučené rozsahy tlaku a vzdálenosti od tkáně, jak jsou uvedeny níže: Operace Použitá nástřiková souprava Použité hroty aplikátoru Použitý tlakový Doporučená vzdálenost od cílové tkáně Doporučený tlak nástřiku Otevřená operace Aplikační zařízení Quixil Žlutý ohebný hrot 6 cm Tlakový Omrix 10 cm 15 cm 2,0 barů 2,5 barů Při nástřiku přípravku Quixil je třeba monitorovat změny krevního tlaku, pulzu, saturace kyslíkem a koncentrace CO 2 na konci výdechu, protože je zde možnost výskytu vzduchové nebo plynové embolie. 12
Příloha II. Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci
 Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 3 Vědecké závěry Celkové shrnutí vědeckého hodnocení přípravku Quixil Podkladové informace Quixil je fibrinové tkáňové lepidlo
Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 3 Vědecké závěry Celkové shrnutí vědeckého hodnocení přípravku Quixil Podkladové informace Quixil je fibrinové tkáňové lepidlo
PŘÍLOHA III ÚPRAVY RELEVANTNÍCH ČÁSTÍ SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE
 PŘÍLOHA III ÚPRAVY RELEVANTNÍCH ČÁSTÍ SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí.
PŘÍLOHA III ÚPRAVY RELEVANTNÍCH ČÁSTÍ SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí.
Příloha I. Seznam názvů, lékových forem, síly léčivých přípravků, cest podání, držitelů rozhodnutí o registraci v členských státech
 Příloha I Seznam názvů, lékových forem, síly léčivých přípravků, cest podání, držitelů rozhodnutí o registraci v členských státech 1 Členský stát Držitel rozhodnutí o registraci (v EHP) Smyšlený název
Příloha I Seznam názvů, lékových forem, síly léčivých přípravků, cest podání, držitelů rozhodnutí o registraci v členských státech 1 Členský stát Držitel rozhodnutí o registraci (v EHP) Smyšlený název
Příloha II. Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci
 Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 16 Vědecké závěry Celkové shrnutí vědeckého hodnocení Podkladové informace Od roku 2008 do května 2012 souviselo s použitím
Příloha II Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 16 Vědecké závěry Celkové shrnutí vědeckého hodnocení Podkladové informace Od roku 2008 do května 2012 souviselo s použitím
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU EVICEL roztoky pro tkáňové lepidlo. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivými látkami jsou: Složka 1 Proteinum humanum praeparatum obsahující
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU EVICEL roztoky pro tkáňové lepidlo. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivými látkami jsou: Složka 1 Proteinum humanum praeparatum obsahující
Praxbind doporučení pro podávání (SPC)
 Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
Léčivé látky: fibrinogenum humanum, thrombinum humanum, aprotininum (syntetické), calcii chloridum
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU VNĚJŠÍ KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Prášky a rozpouštědla pro tkáňové lepidlo Léčivé látky: fibrinogenum humanum, thrombinum humanum, aprotininum (syntetické), calcii
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU VNĚJŠÍ KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Prášky a rozpouštědla pro tkáňové lepidlo Léčivé látky: fibrinogenum humanum, thrombinum humanum, aprotininum (syntetické), calcii
Kartonová krabička obsahující injekční lahvičku s práškem, předplněná injekční stříkačka s rozpouštědlem a příslušenství.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabička obsahující injekční lahvičku s práškem, předplněná injekční stříkačka s rozpouštědlem a příslušenství. 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fanhdi 50 IU/ml Fanhdi
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabička obsahující injekční lahvičku s práškem, předplněná injekční stříkačka s rozpouštědlem a příslušenství. 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fanhdi 50 IU/ml Fanhdi
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU EVICEL roztoky pro přípravu tkáňového lepidla 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivými látkami jsou: Složka 1 Lidský srážlivý protein obsahující
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU EVICEL roztoky pro přípravu tkáňového lepidla 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivými látkami jsou: Složka 1 Lidský srážlivý protein obsahující
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CAMILIA perorální roztok v jednodávkovém obalu
 sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Přečtěte si pozorně celou příbalovou informaci, než začnete tento přípravek používat, protože obsahuje pro Vás důležité informace.
 Sp.zn. sukls42539/2013 a k sukls204682/2013 Příbalová informace: informace pro uživatele ARTISS Roztoky pro tkáňové lepidlo, zmrazené Léčivé látky: Fibrinogenum humanum, thrombinum humanum, aprotininum,
Sp.zn. sukls42539/2013 a k sukls204682/2013 Příbalová informace: informace pro uživatele ARTISS Roztoky pro tkáňové lepidlo, zmrazené Léčivé látky: Fibrinogenum humanum, thrombinum humanum, aprotininum,
CONOXIA, stlačený medicinální plyn PŘÍBALOVÁ INFORMACE
 PŘÍBALOVÁ INFORMACE CONOXIA, stlačený medicinální plyn Oxygenium Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou informaci pro případ,
PŘÍBALOVÁ INFORMACE CONOXIA, stlačený medicinální plyn Oxygenium Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou informaci pro případ,
Softa-Man Kožní roztok
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM A VNITŘNÍM OBALU Karton/ Polyethylenové lahve / kanystr 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Softa-Man Kožní roztok 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Složení: 100 ml roztoku obsahuje:
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM A VNITŘNÍM OBALU Karton/ Polyethylenové lahve / kanystr 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Softa-Man Kožní roztok 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Složení: 100 ml roztoku obsahuje:
OZNAČENÍ NA OBALU: Fraxiparine Forte 2x0,6 ml
 OZNAČENÍ NA OBALU: Fraxiparine Forte 2x0,6 ml ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fraxiparine forte 0,6 ml Nadroparinum calcicum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Léčivá
OZNAČENÍ NA OBALU: Fraxiparine Forte 2x0,6 ml ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fraxiparine forte 0,6 ml Nadroparinum calcicum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Léčivá
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU Lahev s obsahem 300 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Levetiracetam UCB 100 mg/ml, perorální roztok levetiracetamum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU Lahev s obsahem 300 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Levetiracetam UCB 100 mg/ml, perorální roztok levetiracetamum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU. Léčivý přípravek již není registrován
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
Příprava a podání injekce
 Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
Doporučené dávkování je uvedeno na stranách 2 a 10 Příprava a podání injekce ILARIS 150 mg, prášek pro injekční roztok Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní
BIOVISC ORTHO M. Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci.
 Česky BIOVISC ORTHO M Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová Mannitol 20 mg 5 mg Fosfátem pufrovaný
Česky BIOVISC ORTHO M Sterilní viskoelastický roztok kyseliny hyaluronové k intraartikulární injekci. NÁVOD K POUŽITÍ SLOŽENÍ Jeden ml obsahuje: Kyselina hyaluronová Mannitol 20 mg 5 mg Fosfátem pufrovaný
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ 7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KARTON 50 x 50 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Voda na injekci Viaflo 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Aqua pro injectione 100% w/v 3. SEZNAM POMOCNÝCH LÁTEK 4. LÉKOVÁ
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KARTON 50 x 50 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Voda na injekci Viaflo 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Aqua pro injectione 100% w/v 3. SEZNAM POMOCNÝCH LÁTEK 4. LÉKOVÁ
AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU SKLÁDAČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Butamirati citras, guaifenesinum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Butamirati citras 4 mg, guaifenesinum 100 mg
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU SKLÁDAČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Butamirati citras, guaifenesinum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Butamirati citras 4 mg, guaifenesinum 100 mg
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím
 Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
MEDICINÁLNÍ KYSLÍK KAPALNÝ MESSER
 sp.zn. sukls44436/2013 PŘÍBALOVÁ INFORMACE MEDICINÁLNÍ KYSLÍK KAPALNÝ MESSER Medicinální plyn, kryogenní Oxygenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn. sukls44436/2013 PŘÍBALOVÁ INFORMACE MEDICINÁLNÍ KYSLÍK KAPALNÝ MESSER Medicinální plyn, kryogenní Oxygenum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro uživatele
 sp.zn. sukls136451/2013 a sp.zn. sukls36933/2014 Příbalová informace: informace pro uživatele Aprokam50 mg prášek pro injekční roztok cefuroximum Přečtěte si pozorně celou příbalovou informaci dříve, než
sp.zn. sukls136451/2013 a sp.zn. sukls36933/2014 Příbalová informace: informace pro uživatele Aprokam50 mg prášek pro injekční roztok cefuroximum Přečtěte si pozorně celou příbalovou informaci dříve, než
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU, NEBO POKUD NENÍ VNĚJŠÍ OBAL NA VNITŘNÍM OBALU
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU, NEBO POKUD NENÍ VNĚJŠÍ OBAL NA VNITŘNÍM OBALU Papírová krabička; 1 injekční lahvička (2 ml) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml roztoku
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU, NEBO POKUD NENÍ VNĚJŠÍ OBAL NA VNITŘNÍM OBALU Papírová krabička; 1 injekční lahvička (2 ml) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml roztoku
Používání Apidry v 10 ml injekčních lahvičkách
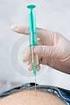 NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
NÁVOD, JAK POUŽÍVAT INJEKČNÍ LAHVIČKY APIDRA 10 ml Apidra 100 jednotek/ml injekční roztok v lahvičce je čirý, bezbarvý vodný roztok, bez jakýchkoli viditelných částic. Každá injekční lahvička obsahuje
Kapesní průvodce. Léčba přípravkem INOmax. Linde: Living healthcare
 Kapesní průvodce. Léčba přípravkem INOmax. Rizika spojená s užíváním přípravku INOmax : Obsah příručky. Tato příručka obsahuje informace o nejdůležitějších rizicích spojených s používáním přípravku INOmax.
Kapesní průvodce. Léčba přípravkem INOmax. Rizika spojená s užíváním přípravku INOmax : Obsah příručky. Tato příručka obsahuje informace o nejdůležitějších rizicích spojených s používáním přípravku INOmax.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabičce 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cupri tetramibi tetrafluoroboras 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: Cupri tetramibi tetrafluoroboras 0,5 mg v jedné injekční lahvičce
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabičce 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cupri tetramibi tetrafluoroboras 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: Cupri tetramibi tetrafluoroboras 0,5 mg v jedné injekční lahvičce
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Pavulon 4mg = 2ml injekční roztok. Pancuronii bromidum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pavulon 4mg = 2ml injekční roztok Pancuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pavulon 4mg = 2ml injekční roztok Pancuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU. Metacam 5 mg/ml injekční roztok pro skot a prasata
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Metacam 5 mg/ml injekční roztok pro skot a prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje: Léčivá látka: Meloxicamum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Metacam 5 mg/ml injekční roztok pro skot a prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje: Léčivá látka: Meloxicamum
Příloha III. Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příbalová informace: informace pro uživatele. Chlorid sodný 0,9% Braun infuzní roztok Natrii chloridum
 sp.zn. sukls212686/2012 Příbalová informace: informace pro uživatele Chlorid sodný 0,9% Braun infuzní roztok Natrii chloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls212686/2012 Příbalová informace: informace pro uživatele Chlorid sodný 0,9% Braun infuzní roztok Natrii chloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Skleněná lahvička vnitřní obal 20 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Iodixanolum 2. OBSAH LÉČIVÉ LÁTKY 20 ml = 6,4 g I 1 ml injekčního roztoku obsahuje: Iodixanolum 652 mg (odp.
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Skleněná lahvička vnitřní obal 20 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Iodixanolum 2. OBSAH LÉČIVÉ LÁTKY 20 ml = 6,4 g I 1 ml injekčního roztoku obsahuje: Iodixanolum 652 mg (odp.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (předplněná injekční stříkačka se zasazenou jehlou) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Metoject 50 mg/ml injekční roztok Methotrexatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (předplněná injekční stříkačka se zasazenou jehlou) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Metoject 50 mg/ml injekční roztok Methotrexatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Příbalová informace: Informace pro uživatele. NovoThirteen IU prášek a rozpouštědlo pro injekční roztok
 Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek a rozpouštědlo pro injekční roztok catridecacogum (rekombinantní koagulační faktor XIII) Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: Informace pro uživatele NovoThirteen 2 500 IU prášek a rozpouštědlo pro injekční roztok catridecacogum (rekombinantní koagulační faktor XIII) Přečtěte si pozorně celou příbalovou informaci
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
Simdax Příbalová informace
 Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
Jedna lahvička s práškem také obsahuje arginin, kyselinu fosforečnou 85% a polysorbát 80. Rozpouštědlo: voda na injekci.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (VELIKOST BALENÍ 10 MG) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Actilyse 10 mg Alteplasum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna lahvička obsahuje 10 mg alteplasy (což odpovídá
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (VELIKOST BALENÍ 10 MG) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Actilyse 10 mg Alteplasum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna lahvička obsahuje 10 mg alteplasy (což odpovídá
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU. Kartonová krabice (skleněné/polyethylenové lahve) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabice (skleněné/polyethylenové lahve) 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 1000 ml infuzního roztoku obsahuje: 55,0 g (odpovídá Glucosum 50,0 g) Energetická hodnota
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabice (skleněné/polyethylenové lahve) 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 1000 ml infuzního roztoku obsahuje: 55,0 g (odpovídá Glucosum 50,0 g) Energetická hodnota
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. ALBUNORM 5% 50g/l, infuzní roztok Lidský albumin
 Sp.zn.sukls151598/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ALBUNORM 5% 50g/l, infuzní roztok Lidský albumin Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Sp.zn.sukls151598/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ALBUNORM 5% 50g/l, infuzní roztok Lidský albumin Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Fludeoxythymidine ( 18 F) 1 8 GBq k datu a hodině kalibrace voda na injekci, chlorid sodný 9 mg/ml
 Příbalová informace Informace pro použití, čtěte pozorně! Název přípravku 3 -[ 18 F]FLT, INJ Kvalitativní i kvantitativní složení 1 lahvička obsahuje: Léčivá látka: Pomocné látky: Léková forma Injekční
Příbalová informace Informace pro použití, čtěte pozorně! Název přípravku 3 -[ 18 F]FLT, INJ Kvalitativní i kvantitativní složení 1 lahvička obsahuje: Léčivá látka: Pomocné látky: Léková forma Injekční
Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1
![Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1 Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1](/thumbs/102/154291766.jpg) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA)
 Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Příprava a podání injekce Návod pro pacienty a lékaře pro přípravu a podání ILARIS pro léčbu systémové juvenilní idiopatické artritidy (SJIA) ILARIS 150 mg, prášek pro injekční roztok Doporučené dávkování
Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům
 17 December 2015 EMA/PRAC/835770/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům Přijato na zasedání výboru PRAC konaném
17 December 2015 EMA/PRAC/835770/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům Přijato na zasedání výboru PRAC konaném
For Internal Use Only
 Souhrnná informace o přípravku NovoSeven stabilního při pokojové teplotě a návod na připravení roztoku Předmět: Poskytuje souhrnné informace, ke kterým došlo u přípravku NovoSeven stabilního
Souhrnná informace o přípravku NovoSeven stabilního při pokojové teplotě a návod na připravení roztoku Předmět: Poskytuje souhrnné informace, ke kterým došlo u přípravku NovoSeven stabilního
Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 1 ke sdělení sp.zn. sukls15871/2012, sukls15908/2012, sukls15852/2012 a sukls15817/2012
 Příloha č. 1 ke sdělení sp.zn. sukls15871/2012, sukls15908/2012, sukls15852/2012 a sukls15817/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Ardeanutrisol G 5 Ardeanutrisol G 10 Ardeanutrisol G 20 Ardeanutrisol
Příloha č. 1 ke sdělení sp.zn. sukls15871/2012, sukls15908/2012, sukls15852/2012 a sukls15817/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Ardeanutrisol G 5 Ardeanutrisol G 10 Ardeanutrisol G 20 Ardeanutrisol
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls102912/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pasteurised Human Antitetanus Immunoglobulin Grifols 250 IU/1 ml a 500 IU/2 ml injekční roztok v předplněné injekční stříkačce Immunoglobulinum
sp.zn. sukls102912/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pasteurised Human Antitetanus Immunoglobulin Grifols 250 IU/1 ml a 500 IU/2 ml injekční roztok v předplněné injekční stříkačce Immunoglobulinum
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
JAK POUŽÍVAT CRINONE 8% (80 mg/g) vaginální gel
 JAK POUŽÍVAT CRINONE 8% (80 mg/g) vaginální gel ZAČÍNÁME S CRINONE V této brožuře naleznete podrobný návod, jak používat přípravek Crinone 8% vaginální gel. Tento návod je určen pouze pro pacientky, kterým
JAK POUŽÍVAT CRINONE 8% (80 mg/g) vaginální gel ZAČÍNÁME S CRINONE V této brožuře naleznete podrobný návod, jak používat přípravek Crinone 8% vaginální gel. Tento návod je určen pouze pro pacientky, kterým
Vnější krabice (obsahující 5 nebo 40 krabiček s lahvičkami se 100 ml infuzního roztoku)
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Vnější krabice (obsahující 5 nebo 40 krabiček s lahvičkami se 100 ml infuzního roztoku) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ciprobay 200 Infuzní roztok ciprofloxacinum 2. OBSAH LÉČIVÉ
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Vnější krabice (obsahující 5 nebo 40 krabiček s lahvičkami se 100 ml infuzního roztoku) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ciprobay 200 Infuzní roztok ciprofloxacinum 2. OBSAH LÉČIVÉ
Příbalová informace: informace pro uživatele TISSEEL Roztoky pro tkáňové lepidlo
 Příbalová informace: informace pro uživatele TISSEEL Roztoky pro tkáňové lepidlo Fibrinogenum humanum, thrombinum humanum, aprotininum (syntetické), calcii chloridum dihydricum Přečtěte si pozorně celou
Příbalová informace: informace pro uživatele TISSEEL Roztoky pro tkáňové lepidlo Fibrinogenum humanum, thrombinum humanum, aprotininum (syntetické), calcii chloridum dihydricum Přečtěte si pozorně celou
Příloha III. Úpravy příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy příslušných bodů souhrnu údajů o přípravku a příbalové informace 26 Stávající informace o přípravcích se mění (vložení, náhrada nebo zrušení textu podle potřeby) tak, aby odpovídaly
Příloha III Úpravy příslušných bodů souhrnu údajů o přípravku a příbalové informace 26 Stávající informace o přípravcích se mění (vložení, náhrada nebo zrušení textu podle potřeby) tak, aby odpovídaly
Isopropylalkohol, hyprolosa, glyceromakrogol-hydroxystearát, trihydrát octanu sodného, silice máty peprné, levomenthol a čištěná voda.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU CORSODYL 1% GEL Zubní gel Chlorhexidini digluconas 1% 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Chlorhexidini digluconas 1,0 g, odpovídá Chlorhexidini
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU CORSODYL 1% GEL Zubní gel Chlorhexidini digluconas 1% 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Chlorhexidini digluconas 1,0 g, odpovídá Chlorhexidini
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Medicinální kyslík plynný SIAD plyn k inhalaci (oxygenum)
 Příloha č. 1 k rozhodnutí sp. zn. sukls46275/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Medicinální kyslík plynný SIAD plyn k inhalaci (oxygenum) Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha č. 1 k rozhodnutí sp. zn. sukls46275/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Medicinální kyslík plynný SIAD plyn k inhalaci (oxygenum) Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabičce 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cuprotetramibi tetrafluoroboras 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: Cuprotetramibi tetrafluoroboras 0,5 mg v jedné injekční lahvičce
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabičce 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cuprotetramibi tetrafluoroboras 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: Cuprotetramibi tetrafluoroboras 0,5 mg v jedné injekční lahvičce
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE MAXIPIME 1 g MAXIPIME 2 g prášek pro injekční roztok cefepimi hydrochloridum monohydricum
 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE MAXIPIME 1 g MAXIPIME 2 g prášek pro injekční roztok cefepimi hydrochloridum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE MAXIPIME 1 g MAXIPIME 2 g prášek pro injekční roztok cefepimi hydrochloridum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Clotrimazol AL 100 (clotrimazolum) Vaginální tablety
 Příloha č. 1 ke sdělení sp. zn. sukls188915/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Clotrimazol AL 100 (clotrimazolum) Vaginální tablety Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha č. 1 ke sdělení sp. zn. sukls188915/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Clotrimazol AL 100 (clotrimazolum) Vaginální tablety Přečtěte si pozorně celou příbalovou informaci dříve,
Doplňky operačních sálů
 Doplňky operačních sálů Kožní popisovač PS 3150 standardní špička + pravítko 30,- Kč PS 31551 jemná špička + pravítko 32,- Kč PS 3158 zdvojená špička + pravítko 37,- Kč - náplň genciánová violeť - jednoduché
Doplňky operačních sálů Kožní popisovač PS 3150 standardní špička + pravítko 30,- Kč PS 31551 jemná špička + pravítko 32,- Kč PS 3158 zdvojená špička + pravítko 37,- Kč - náplň genciánová violeť - jednoduché
Příbalová informace: informace pro uživatele. Haemate P 250 IU/500 IU/1000 IU Prášek a rozpouštědlo pro injekční/infuzní roztok
 sp.zn. sukls355448/2017 Příbalová informace: informace pro uživatele Haemate P 250 IU/500 IU/1000 IU Prášek a rozpouštědlo pro injekční/infuzní roztok Factor VIII coagulationis humanus (lidský koagulační
sp.zn. sukls355448/2017 Příbalová informace: informace pro uživatele Haemate P 250 IU/500 IU/1000 IU Prášek a rozpouštědlo pro injekční/infuzní roztok Factor VIII coagulationis humanus (lidský koagulační
Trihydrát octanu sodného Kyselina octová Chlorid sodný Hydroxid sodný a/nebo kyselina chlorovodíková pro úpravu ph Voda na injekci
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU VAK 250 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Brevibloc 10 mg/ml infuzní roztok Esmololi hydrochloridum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml obsahuje 10 mg esmololi hydrochloridum
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU VAK 250 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Brevibloc 10 mg/ml infuzní roztok Esmololi hydrochloridum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml obsahuje 10 mg esmololi hydrochloridum
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEXVIX PRÁŠEK A ROZPOUŠTĚDLO PRO PŘÍPRAVU ROZTOKU DO MOČOVÉHO MĚCHÝŘE hexylis aminolevulinatis Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEXVIX PRÁŠEK A ROZPOUŠTĚDLO PRO PŘÍPRAVU ROZTOKU DO MOČOVÉHO MĚCHÝŘE hexylis aminolevulinatis Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) pro ibuprofen / pseudoefedrin
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) pro ibuprofen / pseudoefedrin
SCHVÁLENQj
 - Ponechte - Pokud Příloha Č. 2 k rozhodnutí o prodloužení registrace č. j.: sukls93 18/2002 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV I SCHVÁLENQj 21 -- 2009 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽÍVATELE Aminoplasmal
- Ponechte - Pokud Příloha Č. 2 k rozhodnutí o prodloužení registrace č. j.: sukls93 18/2002 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV I SCHVÁLENQj 21 -- 2009 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽÍVATELE Aminoplasmal
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Voda na injekci Viaflo 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Každé balení obsahuje 100% w/v aqua pro iniectione. 3. LÉKOVÁ FORMA Rozpouštědlo pro parenterální
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Voda na injekci Viaflo 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Každé balení obsahuje 100% w/v aqua pro iniectione. 3. LÉKOVÁ FORMA Rozpouštědlo pro parenterální
Kontrolní činnost KHS k povoleným biocidům. Jan Mikoláš Státní zdravotní ústav
 Kontrolní činnost KHS k povoleným biocidům Jan Mikoláš Státní zdravotní ústav 18. 11. 2010 2 18. 11. 2010 3 Zákon č. 120/2002 Sb. 31a Výkon státní kontroly, 32 Správní delikty, 32a Přestupky Povinnosti
Kontrolní činnost KHS k povoleným biocidům Jan Mikoláš Státní zdravotní ústav 18. 11. 2010 2 18. 11. 2010 3 Zákon č. 120/2002 Sb. 31a Výkon státní kontroly, 32 Správní delikty, 32a Přestupky Povinnosti
Jeden ml injekčního roztoku obsahuje granisetronum 1 mg (ve formě hydrochloridu)
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 3 mg/3 ml 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml injekčního roztoku obsahuje granisetronum 1 mg (ve formě hydrochloridu) 3. SEZNAM
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 3 mg/3 ml 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml injekčního roztoku obsahuje granisetronum 1 mg (ve formě hydrochloridu) 3. SEZNAM
Příbalová informace: Informace pro uživatele. Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum)
 sp.zn. sukls273948/2016 Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls273948/2016 Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro infuzní roztok (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU APIGUARD gel (25% Thymolum) pro podání ve včelím úlu Vyhrazený veterinární léčivý přípravek 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU APIGUARD gel (25% Thymolum) pro podání ve včelím úlu Vyhrazený veterinární léčivý přípravek 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
přípravku PROTEUS 110 OD evid. č
 ÚSTŘEDNÍ KONTROLNÍ A ZKUŠEBNÍ ÚSTAV ZEMĚDĚLSKÝ Útvar: ODBOR PŘÍPRAVKŮ NA OCHRANU ROSTLIN Adresa: Zemědělská 1a, 613 00 Brno Sp.zn: SZ UKZUZ 019619/2017/02947 Č.j.: UKZUZ 095639/2017 Datum: 4.10.2017 Vyřizuje:
ÚSTŘEDNÍ KONTROLNÍ A ZKUŠEBNÍ ÚSTAV ZEMĚDĚLSKÝ Útvar: ODBOR PŘÍPRAVKŮ NA OCHRANU ROSTLIN Adresa: Zemědělská 1a, 613 00 Brno Sp.zn: SZ UKZUZ 019619/2017/02947 Č.j.: UKZUZ 095639/2017 Datum: 4.10.2017 Vyřizuje:
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Klosterfrau MELISANA koncentrát Perorální a kožní roztok 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Složení: 100 ml roztoku obsahuje až 65
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Klosterfrau MELISANA koncentrát Perorální a kožní roztok 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Složení: 100 ml roztoku obsahuje až 65
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se aktualizovaných zpráv o bezpečnosti (PSUR) testosteron-undekanoátu (inekce)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se aktualizovaných zpráv o bezpečnosti (PSUR) testosteron-undekanoátu (inekce)
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU. BALENÍ 30 mg/ 5 ml
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU BALENÍ 30 mg/ 5 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÁTEK Jedna 5 ml lahvička obsahuje 30 mg 3. SEZNAM POMOCNÝCH LÁTEK Také obsahuje: Glyceromakrogol-ricinoleát
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU BALENÍ 30 mg/ 5 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÁTEK Jedna 5 ml lahvička obsahuje 30 mg 3. SEZNAM POMOCNÝCH LÁTEK Také obsahuje: Glyceromakrogol-ricinoleát
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příbalová informace: Informace pro pacienta. Octenisept. kožní roztok. octenidini dihydrochloridum, phenoxyethanolum
 sp.zn.sukls232740/2015 Příbalová informace: Informace pro pacienta Octenisept kožní roztok octenidini dihydrochloridum, phenoxyethanolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
sp.zn.sukls232740/2015 Příbalová informace: Informace pro pacienta Octenisept kožní roztok octenidini dihydrochloridum, phenoxyethanolum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE OBAL = PŘÍBALOVÁ INFORMACE PRO: 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ ŠARŽE, POKUD SE NESHODUJE Držitel rozhodnutí
B. PŘÍBALOVÁ INFORMACE OBAL = PŘÍBALOVÁ INFORMACE PRO: 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ ŠARŽE, POKUD SE NESHODUJE Držitel rozhodnutí
Návod k obsluze. Aplikačního zařízení FERMENT EASY - BIO
 Návod k obsluze Aplikačního zařízení FERMENT EASY - BIO 1 OBSAH 1.Účel aplikátoru 2 2.Popis aplikátoru..3 2.1.Základní vybavení...3 2.2.Další vybavení.3 3.Instalace 3 3.1.Umístění na sklízecí řezačce 3
Návod k obsluze Aplikačního zařízení FERMENT EASY - BIO 1 OBSAH 1.Účel aplikátoru 2 2.Popis aplikátoru..3 2.1.Základní vybavení...3 2.2.Další vybavení.3 3.Instalace 3 3.1.Umístění na sklízecí řezačce 3
2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE PŘÍPRAVEK MEDICINÁLNÍ OXID DUSNÝ MESSER POUŽÍVAT
 sp.zn. sukls44162/2013 PŘÍBALOVÁ INFORMACE: : informace pro uživatele MEDICINÁLNÍ OXID DUSNÝ MESSER Medicinální plyn, zkapalněný Dinitrogenii oxidum Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls44162/2013 PŘÍBALOVÁ INFORMACE: : informace pro uživatele MEDICINÁLNÍ OXID DUSNÝ MESSER Medicinální plyn, zkapalněný Dinitrogenii oxidum Přečtěte si pozorně celou příbalovou informaci dříve,
5 ml připravené suspenze obsahuje azithromycinum 200 mg ve formě azithromycinum dihydricum
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 5 ml připravené suspenze obsahuje azithromycinum 200 mg ve formě azithromycinum dihydricum 3. SEZNAM
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 5 ml připravené suspenze obsahuje azithromycinum 200 mg ve formě azithromycinum dihydricum 3. SEZNAM
Návod k použití. Chirurgické kleště dle Netuky Nástavec Kleště. Omnimedics s.r.o. Bělohorská 2328/277a Praha Česká republika
 Chirurgické kleště dle Netuky Nástavec Kleště Návod k použití Výrobce Omnimedics s.r.o. Šafránkova 1243/3 Praha 5 15500 Česká republika Kontaktní adresa: Omnimedics s.r.o. Bělohorská 2328/277a Praha 6
Chirurgické kleště dle Netuky Nástavec Kleště Návod k použití Výrobce Omnimedics s.r.o. Šafránkova 1243/3 Praha 5 15500 Česká republika Kontaktní adresa: Omnimedics s.r.o. Bělohorská 2328/277a Praha 6
Stabilita při pokojové teplotě činí léčbu pohodlnou a okamžitě dostupnou - doma stejně jako mimo domov.
 NovoSeven stabilní při pokojové teplotě: Léčba vždy při ruce Edukační brožura pro lékaře Cíle: Poskytnout informace, které budou shrnuty v edukační brožuře
NovoSeven stabilní při pokojové teplotě: Léčba vždy při ruce Edukační brožura pro lékaře Cíle: Poskytnout informace, které budou shrnuty v edukační brožuře
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Locatim perorální roztok pro novorozená telata mladší než 12 hodin 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Bovinní
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Locatim perorální roztok pro novorozená telata mladší než 12 hodin 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Bovinní
ÚDAJE UVÁDÉNÉ NA VNÉJŠÍM OBALU NEBO NA VNITŘNÍM OBALU, POKUD VNĚJŠÍ OBAL NEEXISTUJE
 Sp.zn.sukls49437/2013 ÚDAJE UVÁDÉNÉ NA VNÉJŠÍM OBALU NEBO NA VNITŘNÍM OBALU, POKUD VNĚJŠÍ OBAL NEEXISTUJE KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU NUROFEN PRO DĚTI (ibuprofenum) 2. OBSAH LÉČIVÉ LÁTKY/LÁTEK
Sp.zn.sukls49437/2013 ÚDAJE UVÁDÉNÉ NA VNÉJŠÍM OBALU NEBO NA VNITŘNÍM OBALU, POKUD VNĚJŠÍ OBAL NEEXISTUJE KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU NUROFEN PRO DĚTI (ibuprofenum) 2. OBSAH LÉČIVÉ LÁTKY/LÁTEK
Příbalová informace: informace pro uživatele. Esmeron 10 mg/ml injekční/infuzní roztok rocuronii bromidum
 Příbalová informace: informace pro uživatele Esmeron 10 mg/ml injekční/infuzní roztok rocuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pro uživatele Esmeron 10 mg/ml injekční/infuzní roztok rocuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Souhrn vlastností biocidního přípravku
 Souhrn vlastností biocidního přípravku Název přípravku: MECDEET Solution Typ přípravku (typy přípravků): Typ přípravku 9 - Repelenty a atraktanty (Regulace živočišných škůdců) Číslo povolení: Referenční
Souhrn vlastností biocidního přípravku Název přípravku: MECDEET Solution Typ přípravku (typy přípravků): Typ přípravku 9 - Repelenty a atraktanty (Regulace živočišných škůdců) Číslo povolení: Referenční
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 VNĚJŠÍ OBAL 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Pět ml suspenze obsahuje amoxicillinum trihydricum 459,1 mg (což odpovídá amoxicilinum 400 mg) a kalii clavulanas 67,9 mg (což odpovídá acidum clavulanicum
VNĚJŠÍ OBAL 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Pět ml suspenze obsahuje amoxicillinum trihydricum 459,1 mg (což odpovídá amoxicilinum 400 mg) a kalii clavulanas 67,9 mg (což odpovídá acidum clavulanicum
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU ECOPORC SHIGA injekční suspenze pro prasata 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka 1 ml obsahuje: Léčivá látka:
