PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
|
|
|
- Monika Kovářová
- před 9 lety
- Počet zobrazení:
Transkript
1 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1
2 1. NÁZEV PŘÍPRAVKU EVICEL roztoky pro přípravu tkáňového lepidla 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivými látkami jsou: Složka 1 Lidský srážlivý protein obsahující hlavně fibrinogen a fibronektin * 1ml injekční lahvička 2ml injekční lahvička 5ml injekční lahvička mg mg mg Složka 2 Lidský trombin IU IU IU * Celkové množství proteinu je mg/ml Úplný seznam pomocných látek viz bod LÉKOVÁ FORMA Roztoky pro přípravu tkáňového lepidla. Čiré nebo lehce opalescentní roztoky. 4. KLINICKÉ ÚDAJE 4.1 Terapeutické indikace EVICEL je používán k podpůrné léčbě v chirurgii ke zlepšení hemostázy, kdy běžné chirurgické techniky nejsou dostačující (viz bod 5.1). EVICEL je určen rovněž na podporu hemostázy při srůstání švů v cévní chirurgii. 4.2 Dávkování a způsob podání EVICEL smí používat pouze zkušení chirurgové. Dávkování Množství přípravku EVICEL a četnost aplikace by měla vždy vycházet z klinických potřeb pacienta. Podávaná dávka závisí na proměnných, mezi něž patří kromě jiného druh chirurgického zákroku, velikost plochy, způsob plánované aplikace a počet aplikací. Aplikace přípravku musí být individuálně upravena ošetřujícím lékařem. V klinických studiích v cévní chirurgii se individuální dávka pohybovala do 4 ml, zatímco při retroperitoneálním nebo intraabdominálním chirurgickém výkonu byla individuální dávka do 10 ml. Při některých postupech (např. traumata jater) je nicméně potřeba většího množství přípravku. Výchozí množství přípravku aplikovaného na danou anatomickou oblast nebo povrch by mělo být natolik velké, aby jím byla zcela pokryta určená plocha. V případě potřeby lze aplikaci opakovat. 2
3 Způsob a cesta podání K použití na lézi. Příprava roztoku je popsána v bodu 6.6. Povrch rány by měl být před aplikací co nejsušší. Podrobné pokyny viz bod Kontraindikace Přípravek EVICEL se nesmí používat intravaskulárně. Přecitlivělost na léčivou látku nebo na některou pomocnou látku. 4.4 Zvláštní upozornění a opatření pro použití Pouze k použití na lézi. Nepoužívejte intravaskulárně. V případě neúmyslné intravaskulární aplikace může dojít k tromboembolickým komplikacím s ohrožením života. Nejsou k dispozici náležité údaje k použití tohoto přípravku k lepení tkání, v neurochirurgii, při podávání pomocí flexibilního endoskopu k léčbě krvácení nebo k použití při gastrointestinálních anastomózách. Před podáním přípravku EVICEL je potřeba zajistit dostatečnou ochranu (zakrytí) všech částí přiléhajících k místu, které má být ošetřeno, aby se zabránilo nechtěné adhezi ostatních tkání. Podobně jako u jiných přípravků obsahujících proteiny může dojít ke vzniku hypersenzitivních reakcí alergického typu. Příznaky hypersenzitivních reakcí zahrnují vyrážku, generalizovanou kopřivku, pocit tíže na hrudi, dušnost, hypotenzi a anafylaxi. Pokud se tyto příznaky vyskytnou, aplikace musí být okamžitě přerušena. V případě šoku je nutno dodržovat standardní lékařské postupy pro léčbu šoku. Standardní opatření zabraňující přenosu infekce v souvislosti s používáním léčivých přípravků vyrobených z lidské krve nebo plazmy zahrnují pečlivý výběr dárců, testování jednotlivých odebraných dávek krve a plazmy na specifické ukazatele infekce a zařazení účinných výrobních postupů k inaktivaci/odstranění virů. Přes všechna tato opatření nemůže být možnost přenosu infekce při podávání léků vyráběných z lidské krve nebo plazmy zcela vyloučena, což platí i v případě dosud neznámých nebo nových virů a jiných patogenů. Prováděná opatření jsou považována za účinná v případě obalených virů, jako je HIV, virus hepatitidy C a virus hepatitidy B, a v případě neobaleného viru hepatitidy A. Omezenou účinnost mohou mít tato opatření u neobalených virů, jako je parvovirus B19. Infekce parvovirem B19 může mít vážné následky u těhotných žen (fetální infekce) a u jedinců se sníženou funkcí imunitního systému nebo se zvýšenou erytropoézou (například hemolytická anémie). Je důrazně doporučováno při každé aplikaci přípravku EVICEL zaznamenat jméno pacienta a číslo šarže přípravku tak, aby bylo možné zpětně přiřadit k pacientovi číslo použité šarže. 4.5 Interakce s jinými léčivými přípravky a jiné formy interakce Žádné formální studie interakcí nebyly provedeny. Stejně jako podobné přípravky nebo roztoky obsahující trombin může být EVICEL denaturován kontaktem s roztoky obsahujícími alkohol, jód nebo těžké kovy (např. antiseptické roztoky). Před aplikací je třeba tyto látky odstranit v maximálně možné míře. 4.6 Těhotenství a kojení Bezpečnost fibrinových tkáňových lepidel/hemostatik u těhotných nebo kojících žen nebyla v kontrolovaných klinických studiích ověřována. Experimentální studie na zvířatech nejsou dostatečné pro posouzení bezpečnosti tohoto přípravku v souvislosti s reprodukcí, vývojem embrya či plodu, průběhem těhotenství a perinatálním a postnatálním vývojem. 3
4 Proto by měl být přípravek podáván těhotným nebo kojícím ženám jen tehdy, je-li to nezbytně nutné. 4.7 Účinky na schopnost řídit a obsluhovat stroje Není relevantní. 4.8 Nežádoucí účinky Nežádoucí účinky, které mohou být hlášeny v souvislosti s fibrinovými tkáňovými lepidly, jsou popsány níže. Vzhledem k tomu, že žádné takové účinky nebyly v průběhu klinických studií u přípravku EVICEL zaznamenány, není jejich četnost v souvislosti s přípravkem EVICEL známa. Přecitlivělost či alergické reakce (které se mohou projevit jako angioedém, pálení a bodání v místě aplikace, bronchospasmus, třesavka, zrudnutí, generalizovaná kopřivka, bolesti hlavy, vyrážka, hypotenze, letargie, nauzea, neklid, tachykardie, pocit tíže na hrudi, mravenčení, zvracení, dušnost) se mohou vyskytnout ve vzácných případech u pacientů, kterým byla podána fibrinová tkáňová lepidla/hemostatika. Tyto nežádoucí účinky se v ojedinělých případech rozvinuly v závažnou anafylaxi. Mohou být zaznamenány zejména tehdy, pokud je přípravek aplikován opakovaně či pokud je podáván pacientům, o nichž je známo, že jsou přecitlivělí na určité složky přípravku. Mírné reakce mohou být zvládnuty pomocí antihistaminik. Závažné reakce s hypotenzí vyžadují okamžitý zásah s použitím běžných zásad léčby šoku. Ve vzácných případech může dojít k vytvoření protilátek proti složkám fibrinového tkáňového lepidla/hemostatik. Neúmyslná intravaskulární aplikace přípravku může vést k tromboembolické příhodě a k diseminované intravaskulární koagulaci, přičemž existuje rovněž riziko anafylaktické reakce (viz 4.4). Informace o bezpečnostních hlediscích v souvislosti s přenosnými agens viz bod 4.4. Následující nežádoucí účinky, které se vyskytly v průběhu klinických studií, byly vyhodnoceny jako účinky, které mohou mít příčinnou souvislost s léčbou přípravkem EVICEL. Veškeré níže uvedené nežádoucí účinky se vyskytly s četností časté (definováno jako > 1/100, < 1/10). Třídy orgánových systémů podle databáze MedDRA Preferovaný termín Nežádoucí účinky ve studii z oblasti retroperitoneální a intraabdominální chirurgie Infekční a parazitární onemocnění Břišní absces Nežádoucí účinky ve studii z oblasti cévní chirurgie Infekční a parazitární onemocnění Infekce štěpu, stafylokoková infekce Cévní poruchy Celkové a jinde nezařazené poruchy a lokální reakce po podání Abnormální klinické a laboratorní nálezy nezařazené jinde Zranění, otravy a komplikace léčebného postupu Hematom Periferní edém Snížená hladina hemoglobinu Krvácení v místě řezu Okluze cévního štěpu Rána Postprocedurální hematom Pooperační komplikace v ráně Výskyt nežádoucích účinků ve studii z oblasti retroperitoneální a intraabdominální chirurgie 4
5 Mezi 135 pacienty podstupujícími retroperitoneální a intraabdominální chirurgický výkon (67 pacientů bylo léčeno přípravkem EVICEL a 68 pacientů bylo zařazeno v kontrolní skupině) nebyly podle posouzení zkoušejících zaznamenány žádné nežádoucí příhody v příčinné souvislosti se sledovanou léčbou. Nicméně 3 závažné nežádoucí příhody (jeden břišní absces ve skupině léčené přípravkem EVICEL a jeden břišní a jeden pánevní absces v kontrolní skupině) byly podle zadavatele studie posouzeny jako příhody s možným vztahem ke sledované léčbě. Nežádoucí účinky cévní chirurgie V kontrolované studii, do které bylo zařazeno 147 pacientů podstupujících zavedení cévního štěpu (75 z nich léčených přípravkem EVICEL a 72 v kontrolní skupině), byla u celkem 16 pacientů v průběhu studie zaznamenána nežádoucí příhoda, při které došlo k trombóze/okluzi štěpu. Tyto příhody byly rovnoměrně rozloženy napříč léčebnými větvemi 8 výskytů jak ve skupině ošetřené přípravek EVICEL, tak v kontrolní skupině. 4.9 Předávkování Nebyl hlášen žádný případ předávkování. 5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti Farmakoterapeutická skupina: lokální hemostatika, ATC kód: B02BC Fibrinadhezní systém spouští poslední fázi fyziologického srážení krve. Přeměna fibrinogenu na fibrin nastává štěpením fibrinogenu na fibrin-monomery a fibrinopeptidy. Fibrin-monomery agregují a vytvářejí fibrinovou sraženinu. Faktor XIIIa, což je trombinem aktivovaný faktor XIII, vytváří fibrinovou síť. Ionty vápníku jsou potřebné jak pro přeměnu fibrinogenu, tak k tvorbě fibrinové sítě. S postupujícím hojením rány se vlivem plazminu zvyšuje fibrinolytická aktivita a začne docházet k degradaci fibrinu na fibrin-degradační produkty. Klinické studie prokazující hemostázu a lepší srůstání švu byly provedeny na celkovém počtu 147 pacientů (75 ošetřených přípravkem EVICEL, 72 v kontrolní skupině), kteří podstoupili cévní operaci s polytetrafluoretylenovými štěpy, a na celkovém počtu 135 pacientů (66 ošetřených přípravkem EVICEL, 69 v kontrolní skupině), kteří podstoupili retroperitoneální nebo intraabdominální chirurgický výkon. K prokázání bezpečnosti a účinnosti přípravku EVICEL u dětí není k dispozici dostatek údajů. Ze 135 pacientů, kteří byli zařazeni do kontrolované studie testující účinky přípravku EVICEL a podstoupili retroperitoneální nebo intraabdominální operaci, byli 4 pacienti ošetření tímto přípravkem ve věku 16 let nebo mladší. Z nich byly 2 děti ve věku 2 a 5 let a 2 byli mladiství ve věku 16 let. V současné době nejsou k dispozici žádné údaje týkající se dětí mladších 2 let. 5.2 Farmakokinetické vlastnosti EVICEL je určen pouze k použití na léze. Intravaskulární podání je kontraindikováno. Intravaskulární farmakokinetické studie nebyly tudíž u lidí prováděny. Studie byly prováděny na králících k vyhodnocení absorpce a eliminace trombinu, je-li aplikován na povrch rány v játrech po parciální hepatektomii. Použitím 125 I-trombinu byla prokázána pomalá absorpce biologicky neaktivních peptidů vzniklých rozkladem trombinu, jejich C max v plazmě bylo dosaženo po 6 8 hodinách. Ve svém maximu (C max ) představovala plasmatická koncentrace pouze 1 2 % z aplikované dávky. Fibrinová tkáňová lepidla/hemostatika jsou metabolizována stejným způsobem jako endogenní fibrin, tedy fibrinolýzou a fagocytózou. 5
6 5.3 Předklinické údaje vztahující se k bezpečnosti Studie prováděné na bakteriích ke stanovení mutagenity byly negativní pro samotný trombin, biologické léčivé složky (obsahující fibrinogen, citrát, glycin, kyselinu tranexamovou a arginin-hydrochlorid), samotný TnBP a samotný Triton X-100 ve všech zkoumaných koncentracích. Ve zkouškách prováděných k posouzení mutagenity u savčích buněk, v testech chromozomových aberací a indukce tvorby mikrojader, byly výsledky pro všechny koncentrace kombinace TnBP a Tritonu X-100 rovněž negativní. Po lokální aplikaci je absorpce trombinu do plasmy pomalá a jde hlavně o degradační produkty trombinu, které jsou eliminovány. Žádné toxikologické účinky v důsledku použití čisticích a rozpouštěcích činidel (TnBP a Triton X-100) k inaktivaci virů nejsou očekávány vzhledem k tomu, že zbytkové hodnoty jsou menší než 5 µg/ml. Studie neurotoxicity prováděné s přípravkem EVICEL potvrdily, že subdurální podání u králíků není spojeno s žádným výskytem neurotoxicity. Neurobehaviorální pozorování po dobu 14±1 dní nezaznamenala žádné abnormální nálezy. Žádné závažné makroskopické známky lokální intolerance a žádné makroskopické nálezy související s léčbou nebyly pozorovány. Analýza mozkomíšního moku neukázala významnější příznaky zánětu. 6. FARMACEUTICKÉ ÚDAJE 6.1 Seznam pomocných látek Injekční lahvička s lidským fibrinogenem: Arginin-hydrochlorid Glycin Chlorid sodný Citrát sodný Chlorid vápenatý Voda na injekce Injekční lahvička s lidským trombinem: Chlorid vápenatý Lidský albumin Manitol Octan sodný Voda na injekce Každý ml obsahuje 11,6 12,9 mg sodíku. 6.2 Inkompatibility Tento přípravek nesmí být mísen s jinými léčivými přípravky. 6.3 Doba použitelnosti 2 roky. 6.4 Zvláštní opatření pro uchovávání Uchovávejte v mrazničce při teplotě -18 C a nižší. Injekční lahvičky uchovávejte ve vnějším kartónovém obalu, aby byly chráněny před světlem. Opakovaně nezmrazujte. Po rozmrazení mohou být neotevřené injekční lahvičky chráněné před světlem uchovávány při teplotě 2 8 C po dobu až 30 dnů. Přípravek během této doby již nelze znovu zmrazit. Nová doba použitelnosti při skladovací teplotě 2 8 C by měla být označena na kartónovém obalu. Na konci této doby musí být přípravek použit nebo zlikvidován. 6
7 Fibrinogenové a trombinové složky jsou stabilní při pokojové teplotě až po dobu 24 hodin, jakmile jsou však nataženy do aplikačního zařízení, musí být okamžitě použity. 6.5 Druh obalu a velikost balení EVICEL je dodáván v balení obsahujícím dvě samostatné injekční lahvičky (sklo typu I) s gumovou zátkou (typ I), z nichž každá obsahuje 1 ml, 2 ml nebo 5 ml roztoku lidského fibrinogenu a lidského trombinu. Aplikační zařízení a příslušné přídatné špičky jsou dodávány zvlášť. Na trhu nemusí být všechny velikosti balení. 6.6 Návod k použití přípravku, zacházení s ním a jeho likvidaci Návod k použití je uveden rovněž v příbalové informaci, resp. v její části určené pro zdravotnické pracovníky. Rozmrazení: Injekční lahvičky je třeba rozmrazit jedním z následujících způsobů: 2 8 C (chladnička): injekční lahvičky se rozmrazují 1 den, nebo C (pokojová teplota): injekční lahvičky se rozmrazují 1 hodinu, nebo 37ºC (např. vodní lázeň za použití aseptických technik nebo ohřívání injekčních lahviček v dlaních): injekční lahvičky by se měly rozmrazit do 10 minut a nesmí být vystaveny této teplotě déle než 10 minut nebo dokud nejsou dostatečně rozmražené. Teplota nesmí přesáhnout 37ºC. Před použitím musí přípravek dosáhnout teploty C. Příprava Roztoky jsou čiré nebo lehce opalescentní. Nepoužívejte roztok, který je zakalený nebo obsahuje usazeniny. EVICEL by měl být aplikován za použití aplikačního zařízení EVICEL označeného známkou CE a podle potřeby též za použití přídatné špičky k této aplikační pomůcce. Příbalové informace s podrobným návodem k použití přípravku EVICEL s pomocí aplikačního zařízení a případně i příslušenství jsou dodávány v balení aplikačního zařízení a jeho příslušenství. Natáhněte obsah obou injekčních lahviček do aplikačního zařízení a postupujte při tom podle návodu k použití aplikačního zařízení. Obě stříkačky by měly být naplněny stejným množstvím tekutiny a neměly by obsahovat žádné vzduchové bubliny. K přípravě podání přípravku EVICEL se nepoužívají jehly. Aplikace kapáním Držte špičku aplikátoru co nejblíže povrchu tkáně, avšak bez toho, aby se jí špička aplikátoru během aplikace dotkla, a pokapejte jednotlivými kapkami ošetřovanou oblast. Jestliže se špička aplikátoru ucpe, špička katétru může být zkracována o 0,5 cm. Aplikace nástřikem EVICEL může být aplikován nástřikem za použití stlačeného CO 2 nebo stlačeného vzduchu. Spojte krátkou trubici na aplikačním zařízení se zasunovací luerovou koncovkou na dlouhé trubici, která přivádí plyn. Zásuvkovou luerovou koncovku přívodové trubice s plynem (vybavené 0,2 μm bakteriostatickým filtrem) zapojte do tlakového regulátoru, který je schopen vyvinout tlak 1,0 až 2,0 barů. Tlakový regulátor by měl být použit v souladu s pokyny výrobce. Při aplikaci přípravku nástřikem by měl být použit tlak 1,4 až 1,7 barů (měřeno tokem plynu). 7
8 Vzdálenost mezi tryskou a povrchem tkáně by v ideálním případě měla být 10 až 15 cm. Přípravek by měl být nastříkán na povrch tkáně v krátkých dávkách (0,1 0,2 ml) tak, aby se vytvořila tenká rovnoměrná vrstva. EVICEL vytvoří průhledný film přes celou ošetřovanou oblast. Likvidace Všechen nepoužitý přípravek nebo odpad musí být zlikvidovány v souladu s místními požadavky. 7. DRŽITEL ROZHODNUTÍ O REGISTRACI OMRIX biopharmaceuticals S.A. 200 Chaussée de Waterloo B-1640 Rhode-St-Genèse Belgie Tel.: Fax: REGISTRAČNÍ ČÍSLO(A) 9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE 10. DATUM REVIZE TEXTU Podrobné informace o tomto přípravku jsou uveřejněny na webových stránkách Evropské agentury pro léčivé přípravky (EMEA) 8
9 PŘÍLOHA II A. VÝROBCE BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCE ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ B. PODMÍNKY REGISTRACE 9
10 A. VÝROBCE BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCE ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ Název a adresa výrobce biologické léčivé látky OMRIX biopharmaceuticals Ltd. MDA Blood Bank Sheba Hospital Ramat Gan POB 888 Kiryat Ono Izrael Název a adresa výrobce odpovědného za propouštění šarží OMRIX biopharmaceuticals S.A. 200 Chaussée de Waterloo 1640 Rhode-St-Genèse Belgie B. PODMÍNKY REGISTRACE PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ, KLADENÉ NA DRŽITELE ROZHODNUTÍ O REGISTRACI Výdej léčivého přípravku je vázán na lékařský předpis s omezením (viz Příloha I: Souhrn údajů o přípravku, bod 4.2). PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU Neuplatňuje se. DALŠÍ PODMÍNKY Systém farmakovigilance Držitel rozhodnutí o registraci musí zajistit, aby byl zaveden funkční systém farmakovigilance tak, jak je popsán ve verzi J/ , uvedené v modulu žádosti o registraci, předtím, než bude přípravek uveden na trh, a dále po celou dobu, kdy bude přípravek na trhu. Plán řízení rizik Držitel rozhodnutí o registraci se zavazuje, že uskuteční studie a další činnosti v oblasti farmakovigilance uvedené podrobně v plánu farmakovigilance tak, jak byly schváleny ve verzi J/ plánu řízení rizik (RMP) uvedeném v modulu žádosti o registraci a v příštích aktualizacích plánu řízení rizik schválených Výborem pro humánní léčivé přípravky (CHMP). V souladu s pokynem Výboru pro humánní léčivé přípravky k systémům řízení rizik pro humánní léčivé přípravky má být aktualizovaný plán řízení rizik předložen současně s příští periodicky aktualizovanou zprávou o bezpečnosti (PSUR). Dále má být aktualizovaný plán řízení rizik předložen: jestliže byly obdrženy nové informace, které mohou mít dopad na současné specifikace bezpečnosti, plán farmakovigilance nebo na činnosti k minimalizaci rizik; do 60 dní po dosažení důležitého milníku (týkajícího se farmakovigilance nebo minimalizace rizik); na žádost EMEA. 10
11 Úřední propouštění šarží: v souladu s článkem 114 směrnice 2001/83/ES, v platném znění, bude úřední propouštění šarží provedeno státní laboratoří nebo laboratoří určenou k takovému účelu. 11
12 PŘÍLOHA III OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE 12
13 A. OZNAČENÍ NA OBALU 13
14 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartónová krabička obsahující 2 injekční lahvičky 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU EVICEL roztoky pro přípravu tkáňového lepidla 2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK Roztoky pro přípravu tkáňového lepidla Léčivé látky v přípravku jsou následující: Složka 1: 1 injekční lahvička obsahuje 1 ml lidského srážlivého proteinu (50 90 mg/ml) Složka 2: 1 injekční lahvička obsahuje 1 ml lidského trombinu ( IU/ml). Léčivé látky v přípravku jsou následující: Složka 1: 1 injekční lahvička obsahuje 2 ml lidského srážlivého proteinu (50 90 mg/ml) Složka 2: 1 injekční lahvička obsahuje 2 ml lidského trombinu ( IU/ml). Léčivé látky v přípravku jsou následující: Složka 1: 1 injekční lahvička obsahuje 5 ml lidského srážlivého proteinu (50 90 mg/ml) Složka 2: 1 injekční lahvička obsahuje 5 ml lidského trombinu ( IU/ml). 3. SEZNAM POMOCNÝCH LÁTEK Lidský fibrinogen: arginin-hydrochlorid, glycin, chlorid sodný, citrát sodný, chlorid vápenatý, voda na injekce. Lidský trombin: chlorid vápenatý, lidský albumin, manitol, octan sodný, voda na injekce. 4. LÉKOVÁ FORMA A VELIKOST BALENÍ Roztoky pro přípravu tkáňového lepidla Léčivé látky v přípravku jsou následující: Složka 1: 1 injekční lahvička obsahuje 1 ml lidského srážlivého proteinu (50 90 mg/ml) Složka 2: 1 injekční lahvička obsahuje 1 ml lidského trombinu ( IU/ml). Léčivé látky v přípravku jsou následující: Složka 1: 1 injekční lahvička obsahuje 2 ml lidského srážlivého proteinu (50 90 mg/ml) Složka 2: 1 injekční lahvička obsahuje 2 ml lidského trombinu ( IU/ml). Léčivé látky v přípravku jsou následující: Složka 1: 1 injekční lahvička obsahuje 5 ml lidského srážlivého proteinu (50 90 mg/ml) Složka 2: 1 injekční lahvička obsahuje 5 ml lidského trombinu ( IU/ml). 14
15 5. ZPŮSOB A CESTA/CESTY PODÁNÍ K použití na lézi. Před použitím si přečtěte příbalovou informaci. 6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ Uchovávejte mimo dosah a dohled dětí. 7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ Nepoužívejte intravaskulárně 8. POUŽITELNOST Použitelné do: 9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ Rozmrazený přípravek znovu nezmrazujte. Uchovávejte ve vnějším kartónovém obalu při teplotě -18 C nebo nižší, aby byl přípravek chráněn před světlem. Po rozmrazení uchovávejte neotevřené injekční lahvičky ve vnějším kartónovém obalu při teplotě 2 8 C po dobu až 30 dnů od: 10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ Všechen nepoužitý přípravek musí být zlikvidován v souladu s místními požadavky. 11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI OMRIX biopharmaceuticals S.A. 200 Chaussée de Waterloo B-1640 Rhode-St-Genèse 12. REGISTRAČNÍ ČÍSLO/ČÍSLA 13. ČÍSLO ŠARŽE Č.š.: 14. KLASIFIKACE PRO VÝDEJ 15
16 Výdej léčivého přípravku vázán na lékařský předpis. 15. NÁVOD K POUŽITÍ 16. INFORMACE V BRAILLOVĚ PÍSMU Nevyžaduje se odůvodnění přijato. 16
17 MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU Štítek injekční lahvičky 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ Lidský fibrinogen: EVICEL roztoky pro přípravu tkáňového lepidla Složka 1: lidský srážlivý protein mg/ml 2. ZPŮSOB PODÁNÍ K použití na lézi. 3. POUŽITELNOST Použitelné do: 4. ČÍSLO ŠARŽE Č.š.: 5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET 1 ml 2 ml 5 ml 6. JINÉ Užívá se jako léčivý přípravek o dvou složkách s dodaným zařízením k aplikaci. 17
18 MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU Štítek injekční lahvičky 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ Lidský trombin: EVICEL roztoky pro přípravu tkáňového lepidla Složka 2: lidský trombin IU/ml 2. ZPŮSOB PODÁNÍ K použití na lézi. 3. POUŽITELNOST Použitelné do: 4. ČÍSLO ŠARŽE Č.š.: 5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET 1 ml 2 ml 5 ml 6. JINÉ Užívá se jako léčivý přípravek o dvou složkách s dodaným zařízením k aplikaci. 18
19 B. PŘÍBALOVÁ INFORMACE 19
20 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE EVICEL roztoky pro přípravu tkáňového lepidla Lidský fibrinogen, lidský trombin Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. - Máte-li jakékoli další otázky, zeptejte se svého lékaře. - Pokud se kterýkoli z vedlejších účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli vedlejších účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi. V příbalové informaci naleznete: 1. Co je EVICEL a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete EVICEL používat 3. Jak se EVICEL používá 4. Možné nežádoucí účinky 5 Jak EVICEL uchovávat 6. Další informace 1. CO JE EVICEL A K ČEMU SE POUŽIVÁ EVICEL je tkáňové lepidlo na bázi lidského fibrinu, které je dodáváno v balení obsahujícím dvě samostatné injekční lahvičky, každá s obsahem 1 ml, 2 ml nebo 5 ml roztoku (buď fibrinogen, nebo trombin) lidského fibrinogenu a lidského trombinu. Aplikační zařízení a příslušné přídatné špičky jsou dodávány zvlášť. Fibrinogen je koncentrát srážlivého proteinu a trombin je enzym, který způsobuje, že se srážlivý protein spojuje. Při smíchání obou složek dochází tudíž k okamžitému srážení. EVICEL se používá při chirurgických operacích ke zmírnění krvácení a mokvání během operace a po operaci. Přípravek je nakapán nebo nastříkán na řezanou tkáň, kde vytvoří tenkou vrstvu, která tkáň zalepí a zastaví krvácení. EVICEL lze použít rovněž při chirurgických operacích cévního řečiště a při operacích v prostoru mezi střevy a zadní stěnou dutiny břišní. 2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE EVICEL POUŽÍVAT Nepoužívejte EVICEL Jestliže jste přecitlivělý/á (alergický/á) na přípravky vyrobené z lidské krve nebo na některou složku přípravku EVICEL. Příznaky přecitlivělosti zahrnují kopřivku, vyrážku, pocit tísně na hrudi, dušnost, pokles krevního tlaku a dýchací obtíže. Pakliže se tyto příznaky objeví, podávání musí být okamžitě přerušeno. Zvláštní opatrnosti při použití přípravku EVICEL je zapotřebí Když je EVICEL během operace podáván, chirurg musí dbát na to, aby přípravek aplikoval pouze na povrch dané tkáně. EVICEL nesmí být vstřikován do tkáně nebo do krevních cév, protože by došlo ke vzniku sraženin a k ohrožení života. Použití přípravku EVICEL v rámci následujících postupů nebylo zkoumáno, a proto nejsou k dispozici 20
21 žádné informace prokazující účinnost přípravku v těchto případech: slepování tkání; chirurgický zákrok na mozku či míše; kontrola krvácení v žaludku či ve střevech prostřednictvím aplikace přípravku endoskopem (trubicí); lepení tkání při chirurgických zákrocích na střevech. Okolí místa aplikace je třeba ochránit, aby se zajistilo, že přípravek EVICEL bude aplikován pouze na povrch určených oblastí. Mohou se vyskytnout hypersenzitivní reakce stejně jako v případě jiných přípravků s obsahem bílkovin. Mezi příznaky těchto reakcí patří kopřivka, vyrážka, pocit tíže na hrudi, dušnost, pokles krevního tlaku a anafylaxe. Při výskytu těchto příznaků je třeba okamžitě přerušit podávání přípravku. Jsou-li léčivé přípravky vyráběné z lidské krve nebo plazmy, musí být učiněna určitá opatření, aby se zabránilo přenosu infekcí. Tato opatření zahrnují pečlivý výběr dárců krve a plazmy, aby bylo zajištěno vyloučení těch, u nichž je riziko infekcí, a rovněž testování jednotlivých odebraných dávek plazmy na příznaky virů/infekcí. Výrobci těchto přípravků používají při zpracování krve a plazmy také postupy, které mohou viry inaktivovat nebo odstranit. Přes všechna tato opatření nemůže být možnost přenosu infekce při podávání léků vyráběných z lidské krve nebo plazmy zcela vyloučena, což platí i v případě dosud neznámých nebo nových virů či jiných druhů infekcí. Opatření uplatňovaná při výrobě fibrinogenu a trombinu jsou považována za účinná v případě lipidem obalených virů, jako je virus lidské imunodeficience (HIV), virus hepatitidy B a virus hepatitidy C, a v případě neobaleného viru hepatitidy A. Omezenou účinnost mohou mít tato opatření u parvoviru B19. Infekce parvovirem B19 může mít vážné následky u těhotných ženy (infekce plodu) a u jedinců se sníženou funkcí imunitního systému nebo s nějakým z typů chudokrevnosti (např. srpkovitá anémie nebo hemolytická anémie). Zdravotničtí pracovníci zaznamenají jméno pacienta a číslo šarže přípravku tak, aby bylo možné dohledat zdroj případné infekce. Vzájemné působení s dalšími léčivými přípravky: Informujte, prosím, svého lékaře či lékárníka o všech lécích, které užíváte nebo jste užíval(a) v nedávné době, a to i o lécích, které jsou dostupné bez lékařského předpisu. Těhotenství a kojení: K posouzení toho, zda existují zvláštní rizika spojená s používáním přípravku EVICEL během těhotenství a kojení, není k dispozici dostatek údajů. Vzhledem k tomu, že EVICEL se používá při operačních zákrocích, měla byste se v případě, že jste těhotná nebo kojíte, poradit se svým lékařem o celkové riskantnosti tohoto zákroku. Použití u dětí K prokázání bezpečnosti a účinnosti přípravku EVICEL u dětí není dostatek údajů. 3. JAK SE EVICEL POUŽÍVÁ Váš ošetřující lékař vám přípravek EVICEL podá během operace. Během operace lékař nakape nebo nastříká EVICEL na tkáň pomocí aplikačního zařízení. Toto zařízení umožňuje nanést ve stejném okamžiku stejné množství obou složek přípravku EVICEL a zajistit jejich rovnoměrné smísení, což je důležité pro optimální účinek tkáňového lepidla. Použité množství přípravku EVICEL závisí na ploše tkáně, která má být v průběhu operace ošetřena. Přípravek se nakape na tkáň v krátkých dávkách nebo se nastříká ve velmi malém množství (0,1 0,2 ml) tak, aby se vytvořila tenká rovnoměrná vrstva. Pokud aplikace jediné vrstvy přípravku EVICEL k zastavení krvácení nepostačuje, je možné nanést druhou vrstvu. 21
22 4. MOŽNÉ NEŽÁDOUCÍ ÚČINKY Podobně jako všechny léky může mít i EVICEL nežádoucí účinky, které se ale nemusí vyskytnout u každého. EVICEL je fibrinové tkáňové lepidlo. Fibrinová tkáňová lepidla mohou obecně, i když pouze ve vzácných případech (1 až 10 pacientů z ), vyvolat alergickou reakci. V případě, že by se u vás alergická reakce vyskytla, mohl(a) byste mít některý z následujících příznaků: kožní vyrážku, kopřivku, pocit tísně na hrudi, třesavku, zrudnutí, bolest hlavy, nízký krevní tlak, otupělost, nevolnost, neklid, zrychlenou srdeční frekvenci, mravenčení, zvracení nebo dušnost. U pacientů ošetřených přípravkem EVICEL nebyla dosud žádná alergická reakce zaznamenána. Je rovněž teoreticky možné, že by se u vás vytvořily protilátky proti proteinům obsaženým v přípravku EVICEL a tyto protilátky by pak mohly mít nepříznivý vliv na srážení krve. Pokud se necítíte dobře, okamžitě to sdělte svému lékaři, a to i v případě, že vaše příznaky se od těch výše popsaných budou lišit. Jestliže zaznamenáte jakýkoliv nežádoucí účinek, který není uveden v této příbalové informaci, oznamte to, prosím, svému lékaři nebo lékárníkovi. V průběhu klinických studií přípravku EVICEL byly zaznamenány určité nežádoucí příhody, u nichž nebylo možné vyloučit příčinnou souvislost s podáváním přípravku EVICEL. Po chirurgických zákrocích v oblasti břicha byl u několika pacientů zaznamenán absces a v případě cévních chirurgických zákroků se objevila uzavření štěpu, která bylo nutné znovu operovat. 5. JAK EVICEL UCHOVÁVAT Uchovávejte mimo dosah a dohled dětí. Uchovávejte v mrazničce při teplotě -18 C nebo nižší. EVICEL nepoužívejte po uplynutí doby použitelnosti, uvedené na štítku a krabičce za nápisem Použitelné do. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Uchovávejte injekční lahvičky v krabičce, aby byl přípravek chráněn před světlem. Znovu nezmrazujte. Po rozmrazení mohou být neotevřené injekční lahvičky chráněné před světlem uchovávány při teplotě 2 8 C po dobu až 30 dní. Fibrinogenové a trombinové složky jsou stabilní při pokojové teplotě až po dobu 24 hodin, jakmile jsou však nataženy do aplikačního zařízení, musí být okamžitě použity. 6. DALŠÍ INFORMACE Co EVICEL obsahuje Léčivými látkami jsou: Složka 1: Lidský srážlivý protein (50 90 mg/ml) Složka 2: Lidský trombin ( IU/ml) Ostatní složky jsou: Složka 1: arginin-hydrochlorid, glycin, chlorid sodný, citrát sodný, chlorid vápenatý a voda na injekce. Složka 2: chlorid vápenatý, lidský albumin, manitol, octan sodný a voda na injekce. 22
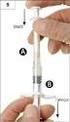
23 Velikost balení: EVICEL je dostupný v následujících baleních: 2 x 1 ml, 2 x 2 ml a 2 x 5 ml. Všechny velikosti balení nemusí být na trhu ve všech zemích. Jak EVICEL vypadá a co obsahuje toto balení EVICEL je tkáňové lepidlo na bázi lidského fibrinu, které je dodáváno v balení obsahujícím dvě samostatné injekční lahvičky, každá s obsahem 1 ml, 2 ml nebo 5 ml roztoku lidského fibrinogenu a lidského trombinu. Aplikační zařízení a příslušné přídatné špičky jsou dodávány zvlášť. Fibrinogen a trombin jsou společně v jednom balení ve dvou injekčních lahvičkách, z nichž každá obsahuje týž objem (1 ml, 2 ml nebo 5 ml) zmrazeného sterilního roztoku, který je po rozmrazení bezbarvý nebo žlutavé barvy. Fibrinogen je koncentrát srážlivého proteinu a trombin je enzym, který způsobuje, že se srážlivý protein spojuje. Při smíchání obou složek dochází tudíž k okamžitému srážení. Držitel rozhodnutí o registraci: OMRIX biopharmaceuticals S.A. 200 Chaussée de Waterloo B-1640 Rhode-St-Genèse Belgie Tel.: Fax: Další informace o tomto přípravku získáte u výrobce: OMRIX Biopharmaceuticals Ltd Plasma Fractionation Institute Sheba Hospital, Tel Hashomer Ramat Gan 52621, Israel Att: Moshe Kamar, MD Head of PV and Medical Director Tel.: Fax: Tato příbalová informace byla naposledy schválena {MM/RRR} Následující informace je určena pouze pro zdravotnické pracovníky. NÁVOD K POUŽITÍ Přečtěte si tuto informaci dříve, než otevřete balení: EVICEL je dodáván ve sterilním balení, a je tudíž důležité používat pouze nepoškozená balení, která nebyla otevřena (přípravek není možné znovu sterilizovat). Příprava: K přípravě podání přípravku EVICEL se nepoužívají jehly. Natáhněte obsah obou injekčních lahviček do aplikačního zařízení podle návodu na obrázku 1. Obě stříkačky by měly být naplněny stejným množstvím tekutiny a neměly by obsahovat žádné vzduchové bubliny. Všechen nepoužitý přípravek nebo odpad musí být zlikvidovány v souladu s místními požadavky. Roztoky by měly být čiré nebo lehce opalescentní. Nepoužívejte roztoky, které jsou zakalené nebo obsahují usazeniny. 23
24 UCHOVÁVÁNÍ PŘÍPRAVKU EVICEL Nepoužívejte po uplynutí doby použitelnosti vyznačené na krabičce a štítku. Uchovávejte mimo dosah a dohled dětí. Fibrinogen a Trombin: Dlouhodobé uchovávání Uchovávejte v mrazničce při teplotě -18 C nebo nižší. Přípravek nepoužívejte po uplynutí doby použitelnosti, uvedené na krabičce. Krátkodobé uchovávání Uchovávejte při teplotě 2 8 C (v chladničce) nejdéle 30 dní. Na krabičce, kde je pro to určené místo, zaznamenejte datum, kdy byl přípravek uložen do chladničky. Znovu nezmrazujte. Fibrinogen a trombin jsou stabilní při pokojové teplotě až po dobu 24 hodin, jakmile jsou však nataženy do aplikačního zařízení, musí být okamžitě použity. Aplikační zařízení: Uchovávejte při pokojové teplotě odděleně od fibrinogenu a trombinu. Rozmrazení: Injekční lahvičky je třeba rozmrazit jedním z následujících způsobů: 2 8 C (chladnička): injekční lahvičky se rozmrazují 1 den, nebo C (pokojová teplota): injekční lahvičky se rozmrazují 1 hodinu, nebo 37ºC (např. vodní lázeň za použití aseptických technik nebo ohřívání injekčních lahviček v dlaních): injekční lahvičky by se měly rozmrazit do 10 minut a nesmí být vystaveny této teplotě déle než 10 minut nebo dokud nejsou dostatečně rozmražené. Teplota nesmí přesáhnout 37ºC. Před použitím musí přípravek dosáhnout teploty C. Příprava Roztoky jsou čiré nebo lehce opalescentní. Nepoužívejte roztoky, které jsou zakalené nebo obsahují usazeniny. EVICEL by měl být aplikován za použití aplikačního zařízení EVICEL označeného známkou CE a podle potřeby též za použití přídatné špičky k této aplikační pomůcce. Příbalové informace s podrobným návodem k použití přípravku EVICEL s pomocí aplikačního zařízení a případně i příslušenství jsou dodávány v balení aplikačního zařízení a jeho příslušenství. Natáhněte obsah obou injekčních lahviček do aplikačního zařízení a postupujte při tom podle návodu k použití aplikačního žařízení. Obě stříkačky by měly být naplněny stejným množstvím tekutiny a neměly by obsahovat žádné vzduchové bubliny. K přípravě podání přípravku EVICEL se nepoužívají jehly. Aplikace kapáním Držte špičku aplikátoru co nejblíže povrchu tkáně, avšak bez toho, aby se jí špička aplikátoru během aplikace dotkla, a pokapejte jednotlivými kapkami ošetřovanou oblast. Jestliže se špička aplikátoru ucpe, špička katétru může být zkracována o 0,5 cm. Aplikace nástřikem EVICEL může být aplikován nástřikem za použití stlačeného CO 2 nebo stlačeného vzduchu. 24
25 Spojte krátkou trubici na aplikačním zařízení se zasunovací luerovou koncovkou na dlouhé trubici, která přivádí plyn. Zásuvkovou luerovou koncovku přívodové trubice s plynem (vybavené 0,2 μm bakteriostatickým filtrem) zapojte do tlakového regulátoru, který je schopen vyvinout tlak 1,0 až 2,0 barů. Tlakový regulátor by měl být použit v souladu s pokyny výrobce. Při aplikaci přípravku nástřikem by měl být použit tlak 1,4 až 1,7 barů (měřeno tokem plynu). Vzdálenost mezi tryskou a povrchem tkáně by v ideálním případě měla být 10 až 15 cm. Přípravek by měl být nastříkán na povrch tkáně v krátkých dávkách (0,1 0,2 ml) tak, aby se vytvořila tenká rovnoměrná vrstva. EVICEL vytvoří průhledný film přes celou ošetřovanou oblast. Likvidace Všechen nepoužitý přípravek nebo odpad musí být zlikvidovány v souladu s místními požadavky. Vyobrazení 1. Návod k použití aplikačního zařízení. Ujistěte se, že všechna spojení těsně přiléhají. Válce stříkaček držte v jedné ruce, posouváním vzad a vpřed uvolněte jejich písty. 1. Vložte dvě injekční lahvičky (fibrinogen a trombin) do dvou sterilních držáků injekčních lahviček. Při manipulaci musí být zachován sterilní postup. 2. Držák injekční lahvičky přidržte a zamáčkněte vrchní část injekční lahvičky do konektoru, který je připevněn k aplikátoru (viz obrázek). Totéž opakujte i s druhou injekční lahvičkou. 3. Jednou rukou držte válce stříkaček a do obou pomalu aspirujte (injekční lahvičky čelní stranou vzhůru). Pokud je potřeba vytlačit vzduch, vstříkněte zpět do injekční lahvičky a aspirujte znovu. 4. Jednou rukou přidržujte válce stříkaček a druhou rukou na injekčních lahvičkách jemně pootočte konektorem proti směru hodinových ručiček. Konektor na injekční lahvičce/injekční lahvička/držák se automaticky rozpojí. 25
26 5. Při použití nástřiku, připojte trubici k tlakovému regulátoru. Aplikátor je tímto připraven k použití. 26
Příloha III Dodatky, které je třeba přidat do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Dodatky, které je třeba přidat do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku
Příloha III Dodatky, které je třeba přidat do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro uživatele
 sp.zn. sukls55434/2017 Příbalová informace: informace pro uživatele Kybernin P 500 IU prášek a rozpouštědlo pro injekční/infuzní roztok Kybernin P 1000 IU prášek a rozpouštědlo pro injekční/infuzní roztok
sp.zn. sukls55434/2017 Příbalová informace: informace pro uživatele Kybernin P 500 IU prášek a rozpouštědlo pro injekční/infuzní roztok Kybernin P 1000 IU prášek a rozpouštědlo pro injekční/infuzní roztok
Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU EVICEL roztoky pro tkáňové lepidlo. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivými látkami jsou: Složka 1 Proteinum humanum praeparatum obsahující
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU EVICEL roztoky pro tkáňové lepidlo. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivými látkami jsou: Složka 1 Proteinum humanum praeparatum obsahující
Kartonová krabička obsahující injekční lahvičku s práškem, předplněná injekční stříkačka s rozpouštědlem a příslušenství.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabička obsahující injekční lahvičku s práškem, předplněná injekční stříkačka s rozpouštědlem a příslušenství. 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fanhdi 50 IU/ml Fanhdi
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabička obsahující injekční lahvičku s práškem, předplněná injekční stříkačka s rozpouštědlem a příslušenství. 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fanhdi 50 IU/ml Fanhdi
Příbalová informace: informace pro uživatele Flexbumin 200 g/l infuzní roztok Albuminum humanum
 Příbalová informace: informace pro uživatele Flexbumin 200 g/l infuzní roztok Albuminum humanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Flexbumin 200 g/l infuzní roztok Albuminum humanum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Léčivé látky: fibrinogenum humanum, thrombinum humanum, aprotininum (syntetické), calcii chloridum
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU VNĚJŠÍ KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Prášky a rozpouštědla pro tkáňové lepidlo Léčivé látky: fibrinogenum humanum, thrombinum humanum, aprotininum (syntetické), calcii
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU VNĚJŠÍ KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Prášky a rozpouštědla pro tkáňové lepidlo Léčivé látky: fibrinogenum humanum, thrombinum humanum, aprotininum (syntetické), calcii
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum
 Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
Příloha č.2 k rozhodnutí o prodloužení registrace sp.zn.sukls83901/2008 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE L- Carnitin,,Fresenius 1 g injekční roztok levocarnitinum Přečtěte si pozorně celou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls102912/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pasteurised Human Antitetanus Immunoglobulin Grifols 250 IU/1 ml a 500 IU/2 ml injekční roztok v předplněné injekční stříkačce Immunoglobulinum
sp.zn. sukls102912/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pasteurised Human Antitetanus Immunoglobulin Grifols 250 IU/1 ml a 500 IU/2 ml injekční roztok v předplněné injekční stříkačce Immunoglobulinum
Příloha 1: Příslušné části "Souhrnu údajů o přípravku", které byly revidované (pozměňovací návrhy k textu jsou zvýrazněny tučně)
 Příloha 1: Příslušné části "Souhrnu údajů o přípravku", které byly revidované (pozměňovací návrhy k textu jsou zvýrazněny tučně) Souhrn údajů o přípravku 4.4 Zvláštní upozornění a opatření pro použití
Příloha 1: Příslušné části "Souhrnu údajů o přípravku", které byly revidované (pozměňovací návrhy k textu jsou zvýrazněny tučně) Souhrn údajů o přípravku 4.4 Zvláštní upozornění a opatření pro použití
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Procto-Glyvenol 400 mg + 40 mg čípky
 sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
sp.zn. sukls74884/2015 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Procto-Glyvenol 400 mg + 40 mg čípky (tribenosidum, lidocaini hydrochloridum monohydricum) Přečtěte si pozorně tuto příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. ALBUNORM 5% 50g/l, infuzní roztok Lidský albumin
 Sp.zn.sukls151598/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ALBUNORM 5% 50g/l, infuzní roztok Lidský albumin Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Sp.zn.sukls151598/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ALBUNORM 5% 50g/l, infuzní roztok Lidský albumin Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
ANTITHROMBIN III NF BAXTER Prášek pro přípravu infuzního roztoku s rozpouštědlem Antithrombinum humanum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE ANTITHROMBIN III NF BAXTER Prášek pro přípravu infuzního roztoku s rozpouštědlem Antithrombinum humanum Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE ANTITHROMBIN III NF BAXTER Prášek pro přípravu infuzního roztoku s rozpouštědlem Antithrombinum humanum Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. CAMILIA perorální roztok v jednodávkovém obalu
 sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
sp.zn. sukls179376/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE CAMILIA perorální roztok v jednodávkovém obalu Chamomilla vulgaris 9 CH, Phytolacca decandra 5 CH, Rheum 5 CH Přečtěte si pozorně tuto
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Immunoglobulinum humanum normale Jeden ml injekčního roztoku obsahuje Immunoglobulinum humanum normale 160 mg.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IGAMPLIA 160 mg/ml, injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale Jeden ml injekčního roztoku obsahuje Immunoglobulinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU IGAMPLIA 160 mg/ml, injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale Jeden ml injekčního roztoku obsahuje Immunoglobulinum
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90
 Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Sp.zn.sukls118606/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OMACOR 1000 mg měkké tobolky Omega-3 acidorum esteri ethylici 90 Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU Vnitřní obal (štítek): Rozpouštědlo ve skleněné lahvičce, typ I, obsah 10 ml
 MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU Vnitřní obal (štítek): Rozpouštědlo ve skleněné lahvičce, typ I, obsah 10 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ Voda na injekci 10 ml 2. ZPŮSOB
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU Vnitřní obal (štítek): Rozpouštědlo ve skleněné lahvičce, typ I, obsah 10 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ Voda na injekci 10 ml 2. ZPŮSOB
INFORMACE: INFORMACE PRO UŽIVATELE. DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum
 INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
INFORMACE: INFORMACE PRO UŽIVATELE DIPIDOLOR, 7,5 mg/ml, injekční roztok Piritramidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. - Ponechte si příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. ATG-Fresenius S (Immunoglobulinum antithymocytarum cuniculum) Koncentrát pro přípravu infuzního roztoku
 Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls242661/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ATG-Fresenius S (Immunoglobulinum antithymocytarum cuniculum) Koncentrát pro přípravu
Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls242661/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE ATG-Fresenius S (Immunoglobulinum antithymocytarum cuniculum) Koncentrát pro přípravu
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
Příbalová informace: informace pro uživatele Parsabiv 2,5 mg injekční roztok Parsabiv 5 mg injekční roztok Parsabiv 10 mg injekční roztok Etelcalcetidum Tento přípravek podléhá dalšímu sledování. To umožní
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU Lahev s obsahem 300 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Levetiracetam UCB 100 mg/ml, perorální roztok levetiracetamum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU A VNITŘNÍM OBALU Lahev s obsahem 300 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Levetiracetam UCB 100 mg/ml, perorální roztok levetiracetamum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden
Příbalová informace: informace pro uživatele. VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa
 Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Příbalová informace: informace pro pacienta. Maltofer 50 mg/ml perorální kapky, roztok
 sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.: sukls229282/2011 Příbalová informace: informace pro pacienta Maltofer 50 mg/ml perorální kapky, roztok polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU, NEBO POKUD NENÍ VNĚJŠÍ OBAL NA VNITŘNÍM OBALU
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU, NEBO POKUD NENÍ VNĚJŠÍ OBAL NA VNITŘNÍM OBALU Papírová krabička; 1 injekční lahvička (2 ml) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml roztoku
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU, NEBO POKUD NENÍ VNĚJŠÍ OBAL NA VNITŘNÍM OBALU Papírová krabička; 1 injekční lahvička (2 ml) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml roztoku
Příbalová informace: informace pro uživatele Rhesonativ 625 IU/ml, injekční roztok Lidský imunoglobulin anti-d
 sp.zn. sukls117295/2013 Příbalová informace: informace pro uživatele Rhesonativ 625 IU/ml, injekční roztok Lidský imunoglobulin anti-d Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls117295/2013 Příbalová informace: informace pro uživatele Rhesonativ 625 IU/ml, injekční roztok Lidský imunoglobulin anti-d Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
prášek pro infuzní roztok
 sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
sp.zn. sukls52667/2015 Příbalová informace: informace pro uživatele Soluvit N prášek pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
Příbalová informace: informace pro uživatele. ANTITHROMBIN III BAXALTA Prášek a rozpouštědlo pro infuzní roztok Antithrombinum III
 Příbalová informace: informace pro uživatele ANTITHROMBIN III BAXALTA Prášek a rozpouštědlo pro infuzní roztok Antithrombinum III Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele ANTITHROMBIN III BAXALTA Prášek a rozpouštědlo pro infuzní roztok Antithrombinum III Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls107935/2012
 sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
sp.zn. sukls107935/2012 PŘÍBALOVÁ INFORMACE Příbalová informace: informace pro pacienta Mucoplant proti kašli s jitrocelem a medem sirup Plantaginis extractum fluidum Přečtěte si pozorně tuto příbalovou
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabičce 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cupri tetramibi tetrafluoroboras 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: Cupri tetramibi tetrafluoroboras 0,5 mg v jedné injekční lahvičce
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabičce 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cupri tetramibi tetrafluoroboras 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: Cupri tetramibi tetrafluoroboras 0,5 mg v jedné injekční lahvičce
Jeden ml injekčního roztoku obsahuje granisetronum 1 mg (ve formě hydrochloridu)
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 3 mg/3 ml 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml injekčního roztoku obsahuje granisetronum 1 mg (ve formě hydrochloridu) 3. SEZNAM
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 3 mg/3 ml 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml injekčního roztoku obsahuje granisetronum 1 mg (ve formě hydrochloridu) 3. SEZNAM
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
Příbalová informace: informace pro pacienta. ATG-Fresenius S (Immunoglobulinum antithymocytarum cuniculum) Koncentrát pro infuzní roztok
 sp.zn. sukls36126/2014 Příbalová informace: informace pro pacienta ATG-Fresenius S (Immunoglobulinum antithymocytarum cuniculum) Koncentrát pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci
sp.zn. sukls36126/2014 Příbalová informace: informace pro pacienta ATG-Fresenius S (Immunoglobulinum antithymocytarum cuniculum) Koncentrát pro infuzní roztok Přečtěte si pozorně celou příbalovou informaci
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
Jedna lahvička s práškem také obsahuje arginin, kyselinu fosforečnou 85% a polysorbát 80. Rozpouštědlo: voda na injekci.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (VELIKOST BALENÍ 10 MG) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Actilyse 10 mg Alteplasum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna lahvička obsahuje 10 mg alteplasy (což odpovídá
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (VELIKOST BALENÍ 10 MG) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Actilyse 10 mg Alteplasum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna lahvička obsahuje 10 mg alteplasy (což odpovídá
Příbalová informace: informace pro uživatele. Haemocomplettan P 2 g Prášek pro injekční/infuzní roztok. (fibrinogenum humanum)
 sp.zn. sukls169431/2015 Příbalová informace: informace pro uživatele Haemocomplettan P 2 g Prášek pro injekční/infuzní roztok (fibrinogenum humanum) Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls169431/2015 Příbalová informace: informace pro uživatele Haemocomplettan P 2 g Prášek pro injekční/infuzní roztok (fibrinogenum humanum) Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Pavulon 4mg = 2ml injekční roztok. Pancuronii bromidum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pavulon 4mg = 2ml injekční roztok Pancuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Pavulon 4mg = 2ml injekční roztok Pancuronii bromidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte si
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
Příbalová informace: informace pro uživatele. Haemocomplettan P 2 g Prášek pro injekční/infuzní roztok. (fibrinogenum humanum)
 sp.zn. sukls223368/2013 Příbalová informace: informace pro uživatele Haemocomplettan P 2 g Prášek pro injekční/infuzní roztok (fibrinogenum humanum) Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls223368/2013 Příbalová informace: informace pro uživatele Haemocomplettan P 2 g Prášek pro injekční/infuzní roztok (fibrinogenum humanum) Přečtěte si pozorně celou příbalovou informaci dříve,
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ANTITHROMBIN III NF BAXTER, prášek pro přípravu infuzního roztoku s rozpouštědlem 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ 1 ml rozpuštěného přípravku obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ANTITHROMBIN III NF BAXTER, prášek pro přípravu infuzního roztoku s rozpouštědlem 2. SLOŽENÍ KVALITATIVNÍ A KVANTITATIVNÍ 1 ml rozpuštěného přípravku obsahuje
TachoSil je téměř bílá matrice pro tkáňové lepidlo. Léčivá strana matrice, která je pokryta fibrinogenem a trombinem, je označena žlutě.
 1. NÁZEV PŘÍPRAVKU TachoSil matrice pro tkáňové lepidlo 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden cm 2 TachoSilu obsahuje: Fibrinogenum humanum Thrombinum humanum 2,0 IU 5,5 mg Úplný seznam pomocných
1. NÁZEV PŘÍPRAVKU TachoSil matrice pro tkáňové lepidlo 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden cm 2 TachoSilu obsahuje: Fibrinogenum humanum Thrombinum humanum 2,0 IU 5,5 mg Úplný seznam pomocných
Pomocné látky se známým účinkem: prostý sirup 67%, usušená tekutá glukosa.
 sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
sp.zn. sukls24303/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Strepsils Pomeranč s vitaminem C pastilky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna pastilka obsahuje amylmetacresolum 0,6 mg, alcohol
Simdax Příbalová informace
 Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
Simdax Příbalová informace Příbalová informace: Informace pro uživatele Simdax 2,5 mg/ml koncentrát pro přípravu infuzního roztoku (Levosimendanum) Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. Maltofer 10 mg/ml sirup
 sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn.: sukls229281/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Maltofer 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: informace pro pacienta. Maltofer, 10 mg/ml sirup. polymaltosum ferricum
 sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
sp.zn. sukls65847/2017 Příbalová informace: informace pro pacienta Maltofer, 10 mg/ml sirup polymaltosum ferricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Vnější krabice (obsahující 5 nebo 40 krabiček s lahvičkami se 100 ml infuzního roztoku)
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Vnější krabice (obsahující 5 nebo 40 krabiček s lahvičkami se 100 ml infuzního roztoku) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ciprobay 200 Infuzní roztok ciprofloxacinum 2. OBSAH LÉČIVÉ
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Vnější krabice (obsahující 5 nebo 40 krabiček s lahvičkami se 100 ml infuzního roztoku) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ciprobay 200 Infuzní roztok ciprofloxacinum 2. OBSAH LÉČIVÉ
Paracetamol Actavis 250 mg Paracetamol Actavis 500 mg Paracetamol Actavis 1000 mg potahované tablety paracetamolum
 ÚDAJE ÚVÁDĚNÉ NA VNĚJŠÍM A VNITŘNÍM OBALU Krabička na blistry 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Paracetamol Actavis 250 mg Paracetamol Actavis 500 mg Paracetamol Actavis 1000 mg potahované tablety paracetamolum
ÚDAJE ÚVÁDĚNÉ NA VNĚJŠÍM A VNITŘNÍM OBALU Krabička na blistry 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Paracetamol Actavis 250 mg Paracetamol Actavis 500 mg Paracetamol Actavis 1000 mg potahované tablety paracetamolum
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Bronchostop sirup. Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt
 Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Sp.zn.sukls391511/2017 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Bronchostop sirup Léčivé látky: suchý tymiánový extrakt, tekutý proskurníkový extrakt Přečtěte si pozorně tuto příbalovou informaci dříve,
Souhrn údajů o přípravku
 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Luivac 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 tableta obsahuje 3 mg Lysatum bacteriale mixtum ex min. 1x10 9 bakterií z každého následujícího
AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva SOUHRN ÚDAJŮ O PŘÍPRAVKU 1.NÁZEV PŘÍPRAVKU: AJATIN PROFARMA tinktura s mechanickým rozprašovačem kožní roztok 2.KVALITATIVNÍ A KVANTITATIVNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabičce 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cuprotetramibi tetrafluoroboras 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: Cuprotetramibi tetrafluoroboras 0,5 mg v jedné injekční lahvičce
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabičce 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Cuprotetramibi tetrafluoroboras 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: Cuprotetramibi tetrafluoroboras 0,5 mg v jedné injekční lahvičce
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. Název přípravku E-Z-HD 2. Kvalitativní a kvantitativní složení Léčivá látka: Barii sulfas (síran barnatý)
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls8465/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. Název přípravku E-Z-HD 2. Kvalitativní a kvantitativní složení Léčivá látka: Barii sulfas (síran barnatý)
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011. Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls124916/2011 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obal na tablety se 400 mg potahovanými tabletami 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibuprofen Dr.Max 400 mg potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obal na tablety se 400 mg potahovanými tabletami 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Ibuprofen Dr.Max 400 mg potahované tablety ibuprofenum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
PŘÍBALOVÁ INFORMACE 2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE STOPTUSSIN SIRUP UŽÍVAT
 PŘÍBALOVÁ INFORMACE Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Tento přípravek je dostupný bez lékařského předpisu. Přesto však Stoptussin sirup musíte užívat
PŘÍBALOVÁ INFORMACE Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Tento přípravek je dostupný bez lékařského předpisu. Přesto však Stoptussin sirup musíte užívat
OZNAČENÍ NA OBALU: Fraxiparine Forte 2x0,6 ml
 OZNAČENÍ NA OBALU: Fraxiparine Forte 2x0,6 ml ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fraxiparine forte 0,6 ml Nadroparinum calcicum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Léčivá
OZNAČENÍ NA OBALU: Fraxiparine Forte 2x0,6 ml ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Fraxiparine forte 0,6 ml Nadroparinum calcicum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Léčivá
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (předplněná injekční stříkačka se zasazenou jehlou) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Metoject 50 mg/ml injekční roztok Methotrexatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA (předplněná injekční stříkačka se zasazenou jehlou) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Metoject 50 mg/ml injekční roztok Methotrexatum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEXVIX PRÁŠEK A ROZPOUŠTĚDLO PRO PŘÍPRAVU ROZTOKU DO MOČOVÉHO MĚCHÝŘE hexylis aminolevulinatis Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEXVIX PRÁŠEK A ROZPOUŠTĚDLO PRO PŘÍPRAVU ROZTOKU DO MOČOVÉHO MĚCHÝŘE hexylis aminolevulinatis Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
Příloha č. 1 k rozhodnutí o změně registrace č. j. MZDR 61316/2014 (sp. zn. sukls204443/2010) PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE HEDELIX SIRUP Hederae helicis folii extractum spissum (hustý extrakt
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
Příloha č. 1 ke sdělení sp.zn. sukls15871/2012, sukls15908/2012, sukls15852/2012 a sukls15817/2012
 Příloha č. 1 ke sdělení sp.zn. sukls15871/2012, sukls15908/2012, sukls15852/2012 a sukls15817/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Ardeanutrisol G 5 Ardeanutrisol G 10 Ardeanutrisol G 20 Ardeanutrisol
Příloha č. 1 ke sdělení sp.zn. sukls15871/2012, sukls15908/2012, sukls15852/2012 a sukls15817/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Ardeanutrisol G 5 Ardeanutrisol G 10 Ardeanutrisol G 20 Ardeanutrisol
Příbalová informace: informace pro uživatele. Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum
 sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
sp.zn.sukls103902/2015, sukls103869/2015 Příbalová informace: informace pro uživatele Harpagofyt ležatý Apomedica 600 mg potahované tablety Harpagophyti radicis extractum siccum Přečtěte si pozorně tuto
Léčivá látka: 1 g masti obsahuje collagenasum 0,48-3,00 mg (to odp.. collagenasum 1,2 I.U a. proteasum 0,24 I.U)
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU IRUXOL Mono mast Collagenasum 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: 1 g masti obsahuje collagenasum 0,48-3,00 mg (to odp.. collagenasum
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU IRUXOL Mono mast Collagenasum 2. OBSAH LÉČIVÉ LÁTKY Léčivá látka: 1 g masti obsahuje collagenasum 0,48-3,00 mg (to odp.. collagenasum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.: sukls102912/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pasteurised Human Antitetanus Immunoglobulin Grifols 250 IU/1 ml a 500 IU/2 ml, injekční roztok v předplněné injekční stříkačce 2. SLOŽENÍ
Sp.zn.: sukls102912/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Pasteurised Human Antitetanus Immunoglobulin Grifols 250 IU/1 ml a 500 IU/2 ml, injekční roztok v předplněné injekční stříkačce 2. SLOŽENÍ
Příbalová informace: informace pro uživatele. Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok
 sp.zn. sukls301709/2016 Příbalová informace: informace pro uživatele Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok Natrii chromas ( 51 Cr) Přečtěte si pozorně celou příbalovou
sp.zn. sukls301709/2016 Příbalová informace: informace pro uživatele Sodium Chromate ( 51 Cr) Solution 37 MBq/ml, radionuklidový prekurzor, roztok Natrii chromas ( 51 Cr) Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Anbinex 50 IU/ml, prášek a rozpouštědlo pro injekční roztok Antithrombinum III
 sp.zn. sukls43174/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Anbinex 50 IU/ml, prášek a rozpouštědlo pro injekční roztok Antithrombinum III Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls43174/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Anbinex 50 IU/ml, prášek a rozpouštědlo pro injekční roztok Antithrombinum III Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele
 sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOSAH A DOHLED DĚTÍ
 OZNAČENÍ NA OBALU ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Text na krabičku 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU suspenze Paracetamolum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Paracetamolum 120 mg v 5 ml suspenze 3. SEZNAM
OZNAČENÍ NA OBALU ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Text na krabičku 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU suspenze Paracetamolum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Paracetamolum 120 mg v 5 ml suspenze 3. SEZNAM
A. OZNAČENÍ NA OBALU
 A. OZNAČENÍ NA OBALU 1 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU BALENÍ OBSAHUJÍCÍ 1 BALENÍ S 50 LAHVIČKAMI SUSPENZE A 2 BALENÍ PO 25 LAHVIČKÁCH S EMULZÍ 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Pandemrix, suspenze a emulze pro
A. OZNAČENÍ NA OBALU 1 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU BALENÍ OBSAHUJÍCÍ 1 BALENÍ S 50 LAHVIČKAMI SUSPENZE A 2 BALENÍ PO 25 LAHVIČKÁCH S EMULZÍ 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Pandemrix, suspenze a emulze pro
Popis přípravku : Prášek: bílý lyofilizát. Rozpouštědlo: čirá bezbarvá tekutina
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (0,5 ml) rozpuštěné
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MENINGOCOCCAL POLYSACCHARIDE A+C VACCINE Prášek pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka (0,5 ml) rozpuštěné
Propofol MCT Fresenius 10 mg/ml: Jeden ml obsahuje propofolum 10 mg. Propofol MCT Fresenius 20 mg/ml: Jeden ml obsahuje propofolum 20 mg.
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU 1x 50 ml předplněná injekční stříkačka 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Propofol MCT Fresenius 10 mg/ml injekční/infuzní emulze v předplněné injekční stříkačce Propofol MCT Fresenius
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU 1x 50 ml předplněná injekční stříkačka 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Propofol MCT Fresenius 10 mg/ml injekční/infuzní emulze v předplněné injekční stříkačce Propofol MCT Fresenius
Souhrn údajů o přípravku. Typhoidi capsulae Vi polysaccharidum purificatum (stirpe Ty 2)
 sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp. zn. sukls133524/2015 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU Typherix, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína proti tyfu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
5 ml připravené suspenze obsahuje azithromycinum 200 mg ve formě azithromycinum dihydricum
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 5 ml připravené suspenze obsahuje azithromycinum 200 mg ve formě azithromycinum dihydricum 3. SEZNAM
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Krabička 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 5 ml připravené suspenze obsahuje azithromycinum 200 mg ve formě azithromycinum dihydricum 3. SEZNAM
Příbalová informace: informace pro uživatele
 sp.zn. sukls136451/2013 a sp.zn. sukls36933/2014 Příbalová informace: informace pro uživatele Aprokam50 mg prášek pro injekční roztok cefuroximum Přečtěte si pozorně celou příbalovou informaci dříve, než
sp.zn. sukls136451/2013 a sp.zn. sukls36933/2014 Příbalová informace: informace pro uživatele Aprokam50 mg prášek pro injekční roztok cefuroximum Přečtěte si pozorně celou příbalovou informaci dříve, než
SOUHRN ÚDAJŮ O PŘÍPRAVKU. PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová
 sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn.: sukls20204/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TYPHIM Vi, injekční roztok v předplněné injekční stříkačce Polysacharidová vakcína
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Immunoglobulinum humanum normale 165 mg/ml* * odpovídá proteinum humanum jehož obsahem je nejméně z 95 % IgG.
 sp.zn. sukls119969/2013 1. NÁZEV PŘÍPRAVKU GAMMANORM 165 mg/ml, injekční roztok SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale (SC/IMIg) Immunoglobulinum
sp.zn. sukls119969/2013 1. NÁZEV PŘÍPRAVKU GAMMANORM 165 mg/ml, injekční roztok SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale (SC/IMIg) Immunoglobulinum
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příbalová informace: informace pro uživatele. IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara)
 Příbalová informace: informace pro uživatele IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara) Tento přípravek podléhá dalšímu sledování. To umožní rychlé
Příbalová informace: informace pro uživatele IMVANEX injekční suspenze Vakcína proti pravým neštovicím (živý modifikovaný virus vakcínie Ankara) Tento přípravek podléhá dalšímu sledování. To umožní rychlé
Příbalová informace: informace pro pacienta. ANACID 258 mg/388 mg perorální suspenze. Magnesii hydroxidum, Algeldrati suspensio
 sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls264215/2017 Příbalová informace: informace pro pacienta ANACID 258 mg/388 mg perorální suspenze Magnesii hydroxidum, Algeldrati suspensio Přečtěte si pozorně tuto příbalovou informaci dříve,
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
Příbalová informace: informace pro uživatele. FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls51148/2011 Příbalová informace: informace pro uživatele FINALGON 4 mg/g + 25 mg/g, mast nonivamidum/nicoboxilum Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Igamad 1500 IU, injekční roztok v předplněné injekční stříkačce Immunoglobulinum humanum anti-d
 sp.zn. sukls79303/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Igamad 1500 IU, injekční roztok v předplněné injekční stříkačce Immunoglobulinum humanum anti-d Přečtěte si pozorně celou příbalovou
sp.zn. sukls79303/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Igamad 1500 IU, injekční roztok v předplněné injekční stříkačce Immunoglobulinum humanum anti-d Přečtěte si pozorně celou příbalovou
Trihydrát octanu sodného Kyselina octová Chlorid sodný Hydroxid sodný a/nebo kyselina chlorovodíková pro úpravu ph Voda na injekci
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU VAK 250 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Brevibloc 10 mg/ml infuzní roztok Esmololi hydrochloridum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml obsahuje 10 mg esmololi hydrochloridum
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU VAK 250 ml 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Brevibloc 10 mg/ml infuzní roztok Esmololi hydrochloridum 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jeden ml obsahuje 10 mg esmololi hydrochloridum
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret
 sp.zn.sukls240326/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn.sukls240326/2018 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Sinupret perorální kapky, roztok Herbarum extractum pro Sinupret Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí trachey (průdušnice)
 www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
www.lekarna-madona.cz zpět na stránku produktu zpět na obdobná léčiva sp.zn. sukls9243/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Hirudoid forte gel 445mg/100g glycosaminoglycani polysulfas z hovězí
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls119969/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gammanorm 165 mg/ml, injekční roztok Immunoglobulinum humanum normale Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls119969/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gammanorm 165 mg/ml, injekční roztok Immunoglobulinum humanum normale Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU. Kartonová krabice (skleněné/polyethylenové lahve) 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
 ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabice (skleněné/polyethylenové lahve) 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 1000 ml infuzního roztoku obsahuje: 55,0 g (odpovídá Glucosum 50,0 g) Energetická hodnota
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU Kartonová krabice (skleněné/polyethylenové lahve) 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK 1000 ml infuzního roztoku obsahuje: 55,0 g (odpovídá Glucosum 50,0 g) Energetická hodnota
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Willfact 1000 IU Prášek pro přípravu injekčního roztoku s rozpouštědlem Factor von Willebrand humanus
 Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls56292/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE 1000 IU Prášek pro přípravu injekčního roztoku s rozpouštědlem Factor von Willebrand humanus Přečtěte
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls56292/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE 1000 IU Prášek pro přípravu injekčního roztoku s rozpouštědlem Factor von Willebrand humanus Přečtěte
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
 ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obaly na tablety se 400 mg potahovanými tabletami 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna potahovaná tableta obsahuje 400 mg. 3. SEZNAM POMOCNÝCH LÁTEK 4. LÉKOVÁ FORMA
ÚDAJE UVÁDĚNÉ NA VNITŘNÍM OBALU Obaly na tablety se 400 mg potahovanými tabletami 2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK Jedna potahovaná tableta obsahuje 400 mg. 3. SEZNAM POMOCNÝCH LÁTEK 4. LÉKOVÁ FORMA
