Metodika časné detekce obnovitelů fertility pro CMS Ogu-INRA v mikrosporových embryích řepky olejky
|
|
|
- David Vopička
- před 6 lety
- Počet zobrazení:
Transkript
1 Metodika časné detekce obnovitelů fertility pro CMS Ogu-INRA v mikrosporových embryích řepky olejky Metodika byla vypracována jako výstup výzkumného projektu NAZV QJ Využití nekonvenčních výchozích materiálů, biotechnologických metod a efektivních postupů v liniovém a hybridním šlechtění ozimé řepky Ing. Miroslav Klíma, Ph.D., Ing. Lenka Havlíčková, Ph.D. Ing. Marie Přibylová, Mgr. Alois Hilgert-Delgado, Ph.D. Ing. Vratislav Kučera, CSc., prof. Ing. Vladislav Čurn, Ph.D. Výzkumný ústav rostlinné výroby, v.v.i. Jihočeská univerzita v Českých Budějovicích Praha, září 2016
2
3 Metodika časné detekce obnovitelů fertility pro CMS Ogu-INRA v mikrosporových embryích řepky olejky Metodika byla vypracována jako výstup výzkumného projektu NAZV QJ Využití nekonvenčních výchozích materiálů, biotechnologických metod a efektivních postupů v liniovém a hybridním šlechtění ozimé řepky Ing. Miroslav Klíma, Ph.D., Ing. Lenka Havlíčková, Ph.D. Ing. Marie Přibylová, Mgr. Alois Hilgert-Delgado, Ph.D. Ing. Vratislav Kučera, CSc., prof. Ing. Vladislav Čurn, Ph.D. Výzkumný ústav rostlinné výroby, v.v.i. Jihočeská univerzita v Českých Budějovicích Praha, září 2016 iii
4 Metodika časné detekce obnovitelů fertility pro CMS Ogu-INRA v mikrosporových embryích řepky olejky Miroslav Klíma a kol. klima@vurv.cz Výzkumný ústav rostlinné výroby, v.v.i., Praha-Ruzyně Jihočeská univerzita v Českých Budějovicích, České Budějovice Metodika byla vypracována jako výstup výzkumného projektu NAZV QJ Využití nekonvenčních výchozích materiálů, biotechnologických metod a efektivních postupů v liniovém a hybridním šlechtění ozimé řepky Oponenty metodiky byli: Ing. Iva Viehmannová, Ph.D., Česká zemědělská univerzita v Praze Ing. Petr Zehnálek, ÚKZÚZ ZS Hradec nad Svitavou Podíl autorů na vypracování metodiky: Ing. Miroslav Klíma, Ph.D. (40 %), Ing. Lenka Havlíčková, Ph.D. (30 %), Ing. Marie Přibylová (10 %), prof. Ing. Vladislav Čurn, Ph.D. (10 %), Mgr. Alois Hilgert-Delgado, Ph.D. (5 %), Ing. Vratislav Kučera, CSc. (5 %) Výzkumný ústav rostlinné výroby, v.v.i., 2016 Jihočeská univerzita v Českých Budějovicích, 2016 Foto: Klíma M. Vydáno bez jazykové úpravy ISBN iv
5 Obsah I. Cíl metodiky... 7 II. Vlastní popis metodiky... 7 III. Srovnání novosti postupů IV. Popis uplatnění metodiky V. Ekonomické aspekty VI. Seznam použité související literatury VII. Seznam publikací, které předcházely metodice VIII. Přílohy Tabulka 1. Médium NLN 13 (Lichter 1985) Tabulka 2. Médium MS (Murashige a Skoog 1962) Tabulka 3. Diferenciační médium DM (Klíma et al. 2004) Tabulka 4. Regenerační médium RM (Klíma et al. 2004) Příprava roztoku trifluralinu Obr. 1. Mikrospory převažující zastoupení středně jednojaderného stádia Obr. 2. Mikrospory převažující zastoupení pozdně jednojaderného až dvoujaderného stádia Obr. 3. Vývojová stádia mikrosporových embryí Obr. 4. Populace mikrosporových embryí na tekutém médiu NLN v různých vývojových stádiích Obr. 5. Dobře vyvinutá kotyledonární embrya k pasážování na tuhé médium Obr. 6. Embrya na diferenciačním médiu před ořezáváním děložních lístků Obr. 7. Embryo před- a po oříznutí děloh na diferenciačním, resp. regeneračním médiu Obr. 8. PCR detekce se specifickými primery pro úsek genu PPR-B
6 6
7 I. Cíl metodiky Cílem předkládané metodiky je etablovat komplexní, rychlejší a spolehlivější postup, umožňující přípravu výchozícho rostlinného materiálu, nedestruktivní identifikaci a následné dopěstování genotypů nesoucích gen obnovy pro CMS Ogu-INRA s využitím metod molekulárního markerování v časných fázích produkce dihaploidů, tj. již ve stádiu mikrosporových embryí. II. Vlastní popis metodiky II.1. Úvod Řepka olejka se řadí mezi nejvýznamnější olejniny, odhad světové produkce pro rok 2016 je 67 mil. tun semene (Anonym 2016). Česká republika patří díky vysoké intenzitě pěstování a propracované agrotechnice stabilně mezi pět největších producentů řepkového semene v EU. Ozimá řepka je tak v ČR po ozimé pšenici a jarním ječmeni třetí nejvýznamnější tržní plodinou na orné půdě, s každoroční plochou pěstování v rozsahu tis. ha. Celosvětovým trendem ve šlechtění řepky olejky je setrvalý růst zastoupení hybridních odrůd; v ČR dnes činí podíl těchto typů odrůd na pěstitelských plochách přes 80 % (Baranyk et al. 2015) a předpokládá se další nárůst. V hybridním šlechtění je v EU nejrozšířenější francouzský systém cytoplazmatické pylové sterility (CMS) Ogu-INRA (Renard et al. 1998), kde 2-liniový, fertilní F 1 hybrid vzniká křížením sterilní mateřské s fertilní otcovskou komponentou obnovitelem fertility (Rf). Tradičním postupem zlepšování Rf linií je jejich křížení s donorem kvality výkonnou liniovou odrůdou či šlechtitelským materiálem, samosprášení F 1 kříženců, dopěstování všech F 2 rostlin do generativní fáze, křížení jednotlivých fertilních rostlin na sterilní mateřské komponenty a stanovení poměru sterilního / fertilního potomstva z každého křížení (Koprna et al. 2009). Tento zdlouhavý proces je u ozimé řepky dále prodlužován nutností jarovizační periody. Výsledkem je vysoká prostorová, časová a tím i finanční náročnost celého postupu. V současnosti se do procesu zlepšování Rf linií pro CMS Ogu-INRA zavádí technologie dihaploidů (DH), kdy lze vytvořit zlepšené, uniformní obnovitele během jedné generace (Klíma et al. 2008). Jelikož je obnova fertility založena jedním dominantním genem, výsledná populace DH linií štěpí v poměru 1 : 1 (tj. jen cca 50 % DH regenerantů nese Rfo gen). Požadované DH linie se pak selektují na základě fenotypového projevu (fertilita a schopnost obnovy fertility po křížení na sterilní mateřskou komponentu, viz výše) nebo pomocí molekulárních markerů (Kučera et al. 2013). Jejich využití v produkci Rf DH linií vyžaduje kultivaci DH regenerantů do stádia, ve kterém je dostatečně velká listová plocha pro izolaci DNA a následné analýzy. Zde popisovaný postup umožňuje odběry rostlinného pletiva v časnějších fázích in vitro kultivace. 7
8 II.2. Příprava a udržování donorových rostlin Technické vybavení a materiál - Výsevní substrát - Květináče o průměru 8 cm a kontejnery cm - Vícesložkové tekuté hnojivo - Klimatizovaná růstová komora fotoperioda 16 / 8 h, teplota 18 / 14 C (den / / noc), intenzita osvětlení 84 µmol / m 2 / s - Skleník fotoperioda 16 / 8 h, teplota / C (den / noc), s přisvětlováním (sodíkové výbojky 210 W) - Jarovizační komora fotoperioda 8 / 16 h, teplota 2 5 C, přisvětlování zářivkami - Lednice teplota 4 5 C Pracovní postup - Výsev semen F 1 kříženců obnovitele fertility a donora kvality ve dvou obdobích, dle etapy odběru poupat: a) Odběr poupat září leden výsev v průběhu června (rostliny ve fázi nástupu kvetení umístit do klimatizované kultivační komory) b) Odběr poupat únor květen výsev září říjen (odběry poupat lze provádět též ve skleníkových podmínkách, pokud teploty nepřesáhnou 25 C) - Přepichování klíčenců do květináčků o průměru 8 cm s výsevním substrátem (10 rostlin od genotypu) - Jarovizace rostlin ve fázi 6 10 pravých listů po dobu 7 8 týdnů - Přesazení jarovizovaných rostlin do kontejnerů cm se zahradnickým substrátem a pěstování ve skleníkových podmínkách (kontrola zdravotního stavu, případné ošetření pesticidy) - Přemístění rostlin ve fázi prodlužování před tvorbou květenství do klimatizované komory nebo do skleníku, pokud není k dispozici klimatizovaná komora - Přihnojování v průběhu kvetení roztokem tekutého vícesložkového hnojiva 1 2 týdně - Pravidelné odstraňování odkvetlých květenství, aby se podpořila tvorba nových poupat II.3. Odběr poupat Technické vybavení a materiál - Nůžky - Kádinky ( ml) s vychlazenou destilovanou vodou - Lihový fix na popis kádinek - Cestovní chladnička (termotaška) 8
9 Pracovní postup - Odstřižení částí terminálních a axilárních květenství s neotevřenými poupaty - Umístění květenství jednotlivých genotypů v kádinkách do termotašky - Uložení květenství v lednici při 4 5 C až do vlastního odběru jednotlivých poupat (po dobu maximálně pěti dnů) II.4. Stanovení vývojové fáze mikrospor Nezralá pylová zrna jsou schopna procházet embryogenezí pouze v určité fázi svého vývoje ve středně až pozdně jednojaderném stádiu. Proto se před založením mikrosporové kultury stanovuje délka poupat, která je v korelaci s vývojovým stadiem mikrospor. Technické vybavení a materiál - Milimetrový papír - Pinzeta - Podložní a krycí sklíčka - Optický mikroskop Pracovní postup - Příprava roztlakových preparátů z prašníků vyjmutých z poupat tří až čtyř velikostí, obvykle v rozsahu 3 4 mm - Hodnocení vývojového stádia mikrospor pod mikroskopem při zvětšení 400 až Stanovení optimální velikosti poupat pro mikrosporové kultury jednotlivých genotypů (převažující zastoupení středně jednojaderných mikrospor, které se vyznačují částečně trojbokým až kulovitým tvarem, čirou cytoplazmou a vakuolou, vyplňující přes 50 % objemu buňky (obr. 1); zřetelné generativní jádro v blízkosti exiny v kombinaci se zrnitou cytoplazmou představuje pozdní jednojaderné nebo dvoujaderné stádium (obr. 2) II.5. Mikrosporové kultury Technické vybavení a materiál - Flowbox pro práci ve sterilním prostředí - Stolní centrifuga - Laboratorní horizontální třepačka - Binokulární lupa - Inverzní mikroskop - Biologický termostat - Lednice - Stolní autokláv - Kultivační místnost fotoperioda 16 / 8 h (den / noc), trubicové zářivky, světelná intenzita 250 µmol / m 2 / s, 25 C - Kultivační místnost fotoperioda 16 / 8 h (den / noc), trubicové zářivky, 9
10 světelná intenzita 250 µmol / m 2 / s; 19 C - Laboratorní sklo a pomůcky plynový nebo lihový kahan, pipety, ky vety (10 20 ml), sterilní plastové (PS) Petriho misky o průměru 90 mm, parafilm, silné skleněné tyčinky, nylonové filtry (40 a 70 μm) - Etanol (čistý a denaturovaný) - SAVO - Tekuté kultivační médium NLN (složení viz příloha) - Roztok diploidizační látky trifluralinu (příprava viz příloha) - Redestilovaná voda Pracovní postup - Odběr poupat odpovídající velikosti do ledem chlazené kádinky v co nejkratším možném čase, aby se předešlo dehydrataci - Sterilizace poupat 70 % etanolem 2 min. nebo 10 % SAVO 10 min. při větším riziku kontaminace - Opláchnutí chlazenou sterilní destilovanou vodou 3 po 5 minutách - Macerace poupat ve 20 ml kádince v chlazeném NLN médiu pomocí skleněné tyčinky - Filtrace přes dvojitý nylonový filtr do 20 ml kádinky a doplnění na celkový objem suspenze mikrospor 9 10 ml - Purifikace mikrospor centrifugací v 10 ml kyvetách při 100 g (1000 RPM) po dobu 10 minut - Odpipetování supernatantu a resuspendování sedimentu v čerstvém chlazeném médiu NLN - Dvě další centrifugace po 5 minutách se stejným postupem - Příprava zásobního a pracovního roztoku diploidizační látky trifluralinu (viz příloha) - Resuspendování pročištěných mikrospor v 10 ml roztoku trifluralinu (5 µmol / l) a v 90 mm sterilní Petriho misce uložení na hodin v termostatu bez osvětlení při 30 C - Přepipetování suspenze do 10 ml centrifugační kyvety a odstředění při 1000 RPM po dobu 10 minut - Resuspendování sedimentovaných mikrospor v temperovaném kultivačním NLN médiu v 50 ml Erlenmeyerově baňce a upravení hustoty na 10 4 mikrospor na 1 ml média - Kultivace mikrospor v 90 mm Petriho misce uzavřené parafilmem v termostatu při 30 C až do objevení globulárních embryí (10 14 dní) - Přemístění kultur na třepačku (70 RPM) do kultivační místnosti s teplotou 25 C, kde dochází k vývoji kotyledonárních embryí (obr. 3, 4) II.6. Odběr materiálu na extrakci DNA a regenerace celistvých rostlin Technické vybavení a materiál - Flowbox - Kultivační místnost pro explantátové kultury - Lednice 10
11 - Mrazicí box ( 20 až 80 C) - Autokláv - Mikrocentrifugační zkumavky s víčkem (tj. eppendorfky o objemu 1,5 ml s kónickým dnem) - Kultivační média (viz příloha) - Etanol čistý Pracovní postup - Subkultivace kotyledonárních embryí o délce 4 7 mm (obr. 5) na agarové diferenciační (DM) médium v 90 mm plastových Petriho miskách po 20 ks - Umístění kultur v kultivační místnosti s teplotou 19 C po dobu 8 14 dnů (obr. 6) - Odříznutí částí obou děložních lístků (2/3 až 3/4) (obr. 7) - přemístění odříznutých děložních lístků do mikrocentrifugačních zkumavek - Očíslování zkumavky a přemístění do mrazicího boxu pro extrakci DNA - Shodné označení embryí a odebraného materiálu pro DNA analýzu, subkultivace na regeneračním médiu (RM) v 90 mm plastových Petriho miskách po 20 ks pro podpoření vývoje vrcholového meristému - Extrakce DNA a markerování genu obnovy (viz kapitola II.8) - Subkultivace vybraných regenerantů s 1 2 pravými lístky (dle výsledků molekulárních analýz) na RM médium v 90 mm plastových Petriho miskách - Subkultivace regenerantů ve fázi 3 4 pravých lístků na MS médium v plastových kultivačních nádobách - Subkultivace regenerantů ve fázi 4 5 pravých lístků na MS médium ve 100 ml Erlenmayerových baňkách - Vysazení regenerantů s dobře vyvinutým kořenovým systémem do nesterilních podmínek II.7. Dopěstování regenerantů do generativní fáze a přemnožení Technické vybavení a materiál - Skleník - Jarovizační komora - Výsevní a zahradnický substrát - Previcur - Vícesložkové tekuté hnojivo - Perforovaná fólie - Izolátory na jednotlivé rostliny z netkané textilie - Květináče o průměru 8 cm - Kontejnery cm Pracovní postup - Vyjmutí regenerantů z kultivačních nádob a opláchnutí pod tekoucí vodou a odstranění zbytků agarového média 11
12 - Ponoření celých rostlinek do 0,15 % roztoku Previcuru na 20 minut - Vysazení rostlin do květináčů o průměru 8 cm s výsevním substrátem a zalití roztokem Previcuru - Zakrytí květináčů perforovanou fólií na 7 10 dní pro vytvoření vlhkého mikroklima a pěstování ve skleníku až do doby aktivního růstu rostlin (14 18 dní) - Jarovizace rostlin v klimatizované komoře po dobu 6 až 8 týdnů - Vysázení jarovizovaných regenerantů do kontejnerů o velikosti cm, naplněných zahradnickým substrátem - Umístění vysázených rostlin do vytápěného skleníku s přisvětlováním (v zimních měsících) nebo do venkovních izolátorů - Provádění pravidelné kontroly zdravotního stavu a preventivní ošetření rostlin proti chorobám a škůdcům - Průběžná izolace celých rostlin před počátkem kvetení sáčky z netkané textilie Poznámka: Přesné rozlišení haploidních a dihaploidních regenerantů se provádí karyologickou analýzou nebo průtokovou cytometrií. V praxi se využívá především hodnocení rostlin podle morfologie květenství a fertility / sterility květů. II.8. Extrakce DNA a markerování genu obnovy pro CMS Ogu-INRA Technické vybavení a materiál - Centrifuga - Mikrohomogenizátor - Sada automatických pipet - Vortex - Třepací vodní lázeň nebo třepací dry-blok - Termostat - Analytické váhy - ph metr - Lednice - Mrazicí box ( 20 C) - Autokláv - PCR thermocykler - Horizontální elektroforéza se zdrojem - Gel-dokumentační systém - Mikrocentrifugační zkumavky s víčkem (eppendorfky o objemu 1,5 ml s kónickým dnem) - SDS extrakční pufr (200 mm Tris-HCl (ph = 7,5), 250 mm NaCl, 25 mm EDTA, 0,5 % SDS) - Isopropylalkohol (2-propanol, isopropanol) - TE pufr (10 mm Tris-HCl, ph = 7,5; 0,1 mm EDTA) - PPP Master Mix (TopBio) 12
13 - Primery (IDT) - BSA (Sigma) - PCR ladder velikostní marker 100 bp DNA ladder (NEB) - TBE pufr pro elektroforézu - Agaróza - Ethidium bromid (Sigma) - dh 2 O (PCR dh 2 O, nebo Millipore dh 2 O) - Rostlinný materiál používaný pro izolaci DNA: somatická embrya, kotyledonární pletiva Pracovní postup - DNA je izolována z čerstvého materiálu (odebraného v in vitro kultuře a ihned zpracovávaného), nebo z materiálu zamraženého (po odebrání je materiál hluboce zmražen a uchováván při teplotě 80 C, krátkodobě je možné uchování i při teplotě 20 C) - Izolace DNA pomocí SDS: tento postup izolace se využívá jako rychlá a jednoduchá metoda izolace DNA při skríningu velkého množství vzorků a vychází z postupu publikovaného v práci Edwards et al. (1991): - Rostlinné pletivo (1 200 mg) rozdrtíme homogenizátorkem přímo v 1,5 ml mikrocentrifugační zkumavce ve 100 µl SDS extrakčního pufru - K homogenátu přidáme 300 µl extrakčního pufru a 5 s vortexujeme (tato extrakční směs může být ponechána při laboratorní teplotě i déle než 1 hodinu, dokud nejsou všechny vzorky homogenizovány) - Extrakt centrifugujeme 1 min při rpm a 300 µl supernatantu přeneseme do čisté mikrocentrifugační zkumavky - K supernatantu přidáme 300 µl isopropylalkoholu vychlazeného na 20 C, jemně promícháme (3 4 převrátit zkumavku) a směs necháme 2 min srážet. Centrifugujeme 5 min při rpm - Osušený pelet rozpustíme v 50 µl TE pufru; DNA je stabilní ve 4 C déle než 1 rok - Postup markerování genu obnovy pro CMS Ogu-INRA je založen na PCR detekci rostlin nesoucích gen pro obnovu fertility (Rfo) pomocí specifických primerů pro úsek genu PPR-B pocházejícího z ředkve (Raphanus sativus). Pro detekci genu Rfo jsou použity primery RsPPRB-F/RsPPRB-R, doplněné o druhý primerový pár 208F/208R, který slouží jako pozitivní kontrola (amplifikace fragmentu vždy přítomného u B. napus) 13
14 - Sekvence primerů používaných pro PCR analýzu (Havlíčková et al. 2015): Primer Sekvence 5 3 Annealing RsPPRB-F GAAGCTCTTGCTACCCATCG 59 C RsPPRB-R TGACATGCTTCGATCTCGTC 59 C 208F TCGGGATGGAAACCATACTC 59 C 208R GGTCCCAGATAAGGGGAAAA 59 C - Duplex PCR byla provedena v objemu 20 μl, tvořeného 1 reakčním pufrem PPP (Top Bio), 1 BSA, 0,25 µm každého primeru (IDT) a 5 10 ng templátové DNA - Schéma pipetování: 10 µl PPP master mixu, 1 µl DNA, 0,5 µl každého primeru (10 µm), 2 µl 10 BSA, 5 µl dh 2 O (voda do objemu 20 µl) - Amplifikace probíhá na Bioer XP Cycler při následujícím teplotním profilu: počáteční denaturace: 5 min, 95 C; 35 cyklů: konečná elongace: stop: 30 s, 95 C, 45 s, 59 C, 2 min, 72 C; 10 min, 72 C; 4 C - PCR produkty se rozdělují na 1,5% agarózovém gelu v 1 TBE pufru Podmínky separace: 30 V 30 min, 90 V 1 hod a 30 min. Jako marker se používá 100 bp DNA ladder (NEB) a DNA fragmenty se barvením pomocí ethidium bromidu na UV transiluminátoru (obr. 8) 14
15 III. Srovnání novosti postupů Předkládaná metodika je svého druhu první česky vydanou komplexní prací, pojednávající o přípravě mikrosporových embryí řepky olejky s následným nedestruktivním markerováním genu obnovy pro CMS Ogu-INRA v dělohách těchto embryí. Metoda extrakce DNA, optimalizovaná na nízké navážky zelené hmoty umožňuje spolehlivou izolaci DNA s následnou PCR reakcí a detekcí příslušného genu. IV. Popis uplatnění metodiky Metodika je určena především pro pracovníky výzkumných a šlechtitelských pracovišť, kteří budou její výsledky využívat ve výzkumu a v zemědělské praxi. Metodika bude uplatněna ve šlechtitelských a výzkumných programech, zaměřených na efektivní produkci dihaploidních linií obnovitelů fertility pro cytoplazmatickou pylovou sterilitu, založenou na systému Ogu-INRA V. Ekonomické aspekty V případě typického průběhu in vitro regenerace je k dispozici pro detekci genu obnovy dostatek rostlinného pletiva ve formě odřezaných děložních lístků již za cca 4 týdny od založení mikrosporové kultury. Je tedy možné provést operativní selekci regenerantů ještě před pasážováním na regenerační médium, čímž se ušetří náklady na udržování, manipulaci a dopěstování regenerantů bez požadovaného genu. V praxi to znamená úsporu minimálně 50 % nákladů na výše uvedenou činnost. Další významná úspora je dána aplikací metody dihaploidů v procesu zlepšování obnovitelů fertility. Klasickým postupem je jejich křížení s donorem kvality, samosprášení F 1 kříženců, dopěstování všech F 2 rostlin do generativní fáze a křížení jednotlivých fertilních rostlin na sterilní mateřské komponenty a stanovení poměru sterilního / fertilního potomstva z každého křížení. Pokud je podíl fertilního potomstva ~100 %, u dané výchozí fertilní rostliny se předpokládá homozygotní stav genu obnovy. Aby bylo možné podíl fertilního / sterilního potomstva objektivně stanovit, je třeba během testů udržovat jednotlivé ověřované rostliny i sterilní mateřské komponenty v technické izolaci. Stanovení obnovy může být dále ovlivněno i extrémními klimatickými podmínkami. Výsledkem je jak vysoká prostorová, časová a tím i finanční náročnost celého postupu, tak i nižší objektivita hodnocení. Dihaploidní systém v kombinaci s časnou selekcí požadovaných genotypů v in vitro výše uvedené nedostatky eliminuje. Aplikace DH systému vede k 100 % homozygotizaci během krátkého časového úseku (na rozdíl od běžných postupů inbreedingu). Takto vysoké hodnoty se prakticky nedá žádnou jinou metodou dosáhnout. Je tak zajištěna genetická čistota obnovitele a jeho naprostá stálost v čase, čímž je dán předpoklad k tvorbě uniformních F 1 hybridů. 15
16 Náklady spojené s aplikací metodiky lze rozdělit do dvou skupin; na fixní náklady, související s pořízením a odpisy kultivačních komor a přístrojového vybavení, koupí nebo pronájmem pozemků, mzdami kmenových pracovníků apod., a na náklady variabilní, jako je např. spotřeba energií, materiálu a úkolových mezd personálu. Nezbytným vybavením je specializovaná kultivační komora(-y) s řízeným světelným a teplotním režimem (250 tis. 1 mil. Kč), laminární box pro práci v aseptickém prostředí ( tis. Kč), autokláv pro přípravu kultivačních médií a sterilizaci nástrojů ( tis. Kč), biologický termostat ( tis. Kč), analytické váhy ( tis. Kč), přístroj pro přípravu deionizované vody (20 60 tis. Kč), laboratorní vařič (10 30 tis. Kč), magnetická míchačka (10 20 tis. Kč), předvážky (5 10 tis. Kč), nástroje pro dávkování kapalin (3 5 tis. Kč) a ph metr (2 10 tis. Kč). V případě udržování donorových rostlin v řízených podmínkách, resp. dopěstování a přemnožení rostlin ve skleníku je třeba kalkulovat i pořízení další kultivační komory (300 tis. 1 mil. Kč), resp. skleníku. Předpokládá se, že uživatelé metodiky již mají částečně nebo kompletně vybavenou laboratoř explantátových kultur, potřebné kultivační komory a zaškolený personál. Významnou položkou nákladů variabilních je spotřeba elektrické energie na provoz osvětlovacích těles kultivačních boxů a chlazení na požadovanou teplotu. Na jednu donorovu rostlinu řepky je třeba počítat s příkonem W (sodíková výbojka), na rostlinu v in vitro podmínkách 1,5 2,0 W (lineární zářivka). Náklady na chlazení se odvíjejí od způsobu odvodu přebytečného tepla (odsávání, izolace osvětlovacích těles od prostoru s rostlinami apod.). Náklady na přípravu kultivačních médií ( Kč / l média) souvisí s kvalitou (čistotou) výchozích chemikálií a složením jednotlivých typů médií. Výsledné jednotkové náklady na produkci požadovaných rostlinných materiálů výrazně ovlivňují i další faktory, jako je fyziologický stav donorových rostlin v průběhu odběrů, regenerační schopnost použitých genotypů, výskyt kontaminací aj. K dalším významným nákladovým položkám patří i např. výdaje spojené s periodickou údržbou a revizí přístrojového vybavení apod. 16
17 VI. Seznam použité související literatury Anonym. Rapeseed Global Rapeseed Production 2016/2017. Global Rapeseed Production. [online] [cit ]. Dostupné z: Baranyk a kol. (2015). Stanovisko k odrůdové skladbě řepky pro rok 2015/16. Praha: Typus Pro Praha s.r.o. ISBN Edwards K., Jihnstone C., Thompson C. (1991). A simple and rapid method for the preparation of plant genomic DNA for PCR analysis. Nucleic Acids Res., 19: Klíma M., Vyvadilová M., Kučera V. (2004): Production and utilization of doubled haploids in Brassica oleracea vegetables. Horticultural Science (Prague), 31: Klíma M., Vyvadilová M., Kučera V. (2008). Chromosome doubling effects of selected antimitotic agents in Brassica napus microspore culture. Czech Journal of Genetics and Plant Breeding, 44: Koprna R., Kučera V., Macháčková I., Horáček J., Ehrenbergerová J. (2009). Development of fertility restorers of winter oilseed rape with low glucosinolate content for the CMS Ogu-INRA system. Czech Journal of Genetics and Plant Breeding, 45(3): Kučera V., Vyvadilová M., Klíma M., Čurn V., Havlíčková L., Jozová E., Macháčková I. (2013). Metodika tvorby rodičovských komponent a hybridů ozimé řepky (Brassica napus L.) na bázi CMS. VÚRV, v.v.i. Praha, Lichter R. (1985). From microspores to rape plants. A tentative way to low glucosinolate strains. In: Sorensen H. (ed.): Advance in the Production and Utilisation of Cruciferous Crops. Martinus Dordecht, Boston, Lancaster, Nijhoff M., Junk W. Publishers, Murashige T., Skoog F. (1962). A revised medium for rapid growth and bioassays with tobacco tissue cultures. Physiol. Plant. 15: Renard M., Delourme R., Vallee P., Pierre J. (1998). Hybrid rapeseed breeding and production. In: Thomas, G. and Monteiro, A. (eds.) Brassica 97, International symposium on Brassicas, Rennes, Acta Hort. 459,
18 18
19 VII. Seznam publikací, které předcházely metodice Havlíčková L., Čurn V., Jozová E., Kučera V., Vyvadilová M., Klíma M. (2012): Sequence analysis of the mtdna region correlated with Shaan 2A cytoplasmic male sterility in rapeseed (Brassica napus L.). Czech J. Genet. Plant Breed. 48: Havlíčková L., Jozová E., Klíma M. Kučera V., Čurn V. (2014): Detection of self-incompatible oilseed rape plants (Brassica napus L.) based on molecular markers for identification of the class I S haplotype. Genetics and molecular biology, 37: Havlíčková L., Jozová E., Rychlá A., Klíma M., Kučera V., Čurn V. (2014): Genetic diversity assessment in winter oilseed rape (Brassica napus L.) collection using AFLP, ISSR and SSR markers. Czech J. Genet. Plant Breed. 50: Havlíčková L., Klíma M., Přibylová M., Hilgert-Delgado A.A., Kučera V., Čurn V. (2015): Non-destructive in vitro selection of microspore-derived embryos with the fertility restorer gene for CMS Ogu-INRA in winter oilseed rape (Brassica napus L.). Electronic Journal of Biotechnology 18: Havlíčková L., Přibylová M., Klíma M., Čurn V. (2014): Molekulární detekce genů obnovy fertility pro CMS Ogu-INRA v mikrosporových embryích řepky. Úroda 12, vědecká příloha časopisu, Klíma M., Vyvadilová M., Kučera V. (2004): Production and utilization of doubled haploids in Brassica oleracea vegetables. Horticultural Science (Prague), 31: Klíma M., Vyvadilová M., Kučera V. (2008): Chromosome doubling effects of selected antimitotic agents in Brassica napus microspore culture. Czech J. Genet. Plant Breed., 42: Kučera V., Schwarzbach E., Klíma M., Vyvadilová M. (2004): Agronomic performance of doubled haploid lines and pedigree derived lines of winter oilseed rape. Czech J. Genet. Plant Breed., 40: Kučera V., Vyvadilová M., Klíma M. (2002): Utilisation of doubled haploids in winter oilseed rape (Brassica napus L.) breeding. Czech J. Genet. Plant Breed. 38: Smýkalová I., Větrovcová M., Klíma M., Macháčková I., Griga M. (2006): Efficiency of Microspore Culture for Doubled Haploid Production in the Breeding Project Czech Winter Rape. Czech J. Genet. Plant Breed., 42: Žaludová J., Havlíčková L., Jozová E., Kučera V., Vyvadilová M., Klíma M., Čurn V. (2013): Marker assisted selection as a tool for detection of Brassica napus plants carrying selfincompatibility alleles, in hybrid breeding programs. Romanian Agricultural Research, 30:
20 20
21 VIII. Přílohy Tabulka 1. Médium NLN 13 (Lichter 1985) Složka Složka A) navážky [mg/l média] ph 5,8 6,0 MgSO 4 7 H 2 O 125,0 navážky B) a C) (v mg na 100 ml zás. roztoku) KNO 3 125,0 navážky mikroprvků KH 2 PO 4 125,0 H 3 BO ,0 Ca(NO 3 ) 2 4 H 2 O 500,0 MnSO 4 H 2 O 1 894,0 L serin 100,0 ZnSO 4 7 H 2 O 1 280,0 L glutamin 800,0 Na 2 MoO 4 H 2 O 25,0 L glutathion 30,0 CuSO 4 5 H 2 O 2,5 myo inositol 100,0 CoCl 2 6 H 2 O 2,5 sacharóza ,0 navážky vitaminů zásobní roztoky (po 1 ml na l média) kys. nikotinová 500,0 B) zásobní roztok mikroprvků thiamin ( I.) 50,0 C) zásobní roztoky vitaminů I. IV. pyridoxin 50,0 D) ostatní složky kys. listová * ( II.) 50,0 Ferrous sulfate/chelate solution 10 ml (na l média) biotin * ( III.) 5,0 1) glycin ( IV.) 200,0 složky I. IV. rozpustit samostatně * rozpustit v 1N KOH 1) firma SIGMA sterilizace filtrací Tabulka 2. Médium MS (Murashige a Skoog 1962) Složka Navážka (mg/l) Složka Navážka (mg/l) NH 4 NO ,000 FeSO 4 7 H 2 O 27,800 KNO ,000 Na 2 EDTA 2 H 2 O 37,300 CaCl 2 2 H 2 O 440,000 kys. nikotinová 0,500 MgSO 4 7 H 2 O 370,000 pyridoxin HCl 0,500 KH 2 PO 4 170,000 thiamin 0,100 KI 0,830 glycin 2,000 H 3 BO 3 6,200 inositol 100,000 MnSO 4 4 H 2 O 22,300 agar 8 000,000 ZnSO 4 7 H 2 O 8,600 sacharóza ,000 Na 2 MoO 4 2 H 2 O 0,250 kasein 1 000,000 CuSO 4 5 H 2 O 0,025 ph 5,8 CoCl 2 6 H 2 O 0,025 21
22 Tabulka 3. Diferenciační médium DM (Klíma et al. 2004) Složka Navážka (mg/l) Makroelementy (NH 4 ) SO KNO NaH 2 PO 4 2 H 2 O 150 MgSO 4 7 H 2 O 500 CaCl 2 2 H 2 O 750 FeNa EDTA 40 Mikroelementy H 3 BO 3 3 MnSO 4 4 H 2 O 10 ZnSO 4 7 H 2 O 2 Na 2 MoO 4 2 H 2 O 0,25 CuSO 4 5 H 2 O 0,025 CoCl 2 6 H 2 O 0,025 Vitamíny Thiamin HCl 10 Pyridoxin HCl 1 Kys. nikotinová 1 Myo inositol 100 Aminokyseliny Glutamin 800 Serin 100 Fytohormony 6 BAP 0,2 IAA 0,2 Sacharóza 20 g Agar 8 g ph 5,8 6,0 22
23 Tabulka 4. Regenerační médium RM (Klíma et al. 2004) Složka Navážka (mg/l) Makroelementy (NH 4 ) NO KNO KH 2 PO MgSO 4 7 H 2 O 370 CaCl 2 2 H 2 O 440 FeNa EDTA 36,7 Mikroelementy H 3 BO 3 6,2 MnSO 4 4 H 2 O 22,3 ZnSO 4 7 H 2 O 8,6 Na 2 MoO 4 2 H 2 O 0,25 CuSO 4 5 H 2 O 0,025 CoCl 2 6 H 2 O 0,025 KI 0,83 Vitamíny Thiamin 0,1 Pyridoxin 0,5 Kys. nikotinová 0,5 Myo inositol 100 Glycin 2 Sacharóza Agar 10 g 10 g ph 5,9 Příprava roztoku trifluralinu - Rozpuštění 16,76 mg trifluralinu v malém množství acetonu ve sterilních podmínkách ve flowboxu, odpaření acetonu - Konečné rozpuštění v dimetylsulfoxidu (DMSO) a upravení koncentrace roztoku na 5 mmol / l - Uložení zásobního roztoku ve sterilních baňkách se šroubovacím víčkem při teplotě 22 C a ve tmě - Příprava pracovního roztoku o koncentraci 5 µmol / l přidáním NLN média o teplotě vyšší než 20 C těsně před použitím pro mikrosporové kultury 23
24 24
25 Obr. 1. Mikrospory převažující zastoupení středně jednojaderného stádia Šipky označují vakuolu (zvětšení 400 ) Obr. 2. Mikrospory převažující zastoupení pozdně jednojaderného až dvoujaderného stádia Šipky označují vegetativní jádro (zvětšení 400 ) 25
26 Obr. 3. Vývojová stádia mikrosporových embryí A globulární, B srdčité, C torpédovité, D kotyledonární, E dobře vyvinuté kotyledonární stádium pro pasážování na diferenciační médium Obr. 4. Populace mikrosporových embryí na tekutém médiu NLN v různých vývojových stádiích Délka největších embryí 5 mm 26
27 Obr. 5. Dobře vyvinutá kotyledonární embrya k pasážování na tuhé médium Délka největších embryí 8 mm Obr. 6. Embrya na diferenciačním médiu před ořezáváním děložních lístků Průměr kultivační misky 90 mm 27
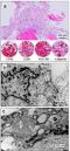
28 Obr. 7. Embryo před- a po oříznutí děloh na diferenciačním, resp. regeneračním médiu Obr. 8. PCR detekce se specifickými primery pro úsek genu PPR-B Pro detekci genu Rfo použity primery RsPPRB-F/RsPPRB-R (1528pb). Druhý primerový pár (208bp) slouží jako pozitivní kontrola. 28
29 Název: Autorský kolektiv: Klíma M. a kol. (2016): Metodika časné detekce obnovitelů fertility pro CMS Ogu-INRA v mikrosporových embryích řepky olejky Ing. Miroslav Klíma, Ph.D. Ing. Lenka Havlíčková, Ph.D. Ing. Marie Přibylová prof. Ing. Vladislav Čurn, Ph.D. Mgr. Alois Hilgert-Delgado, Ph.D. Ing. Vratislav Kučera, CSc. Vydal: Výzkumný ústav rostlinné výroby, v.v.i. Drnovská 507 Praha 6 Ruzyně Vydáno bez jazykové úpravy Metodika byla schválena MZe ČR, osvědčením o certifikaci č /2016-MZE Kontakt na autory: klima@vurv.cz ISBN
30 Poznámky 30
31
32
Metodika produkce dihaploidních linií pro šlechtění řepky ozimé
 Miroslava Vyvadilová a kol. Metodika produkce dihaploidních linií pro šlechtění řepky ozimé METODIKA PRO PRAXI VÝZKUMNÝ ÚSTAV ROSTLINNÉ VÝROBY, V.V.I. PRAHA RUZYNĚ 2008 Miroslava Vyvadilová, Miroslav Klíma,
Miroslava Vyvadilová a kol. Metodika produkce dihaploidních linií pro šlechtění řepky ozimé METODIKA PRO PRAXI VÝZKUMNÝ ÚSTAV ROSTLINNÉ VÝROBY, V.V.I. PRAHA RUZYNĚ 2008 Miroslava Vyvadilová, Miroslav Klíma,
Tkáňové kultury rostlin. Mikropropagace
 Tkáňové kultury rostlin Mikropropagace IN VITRO KULTURY (EXPLANTÁTOVÉ KUTLURY, ROSTLINNÉ EXPLANTÁTY) Izolované rostliny, jejich orgány, pletiva či buňky pěstované in vitro ve sterilních podmínkách Na kultivačních
Tkáňové kultury rostlin Mikropropagace IN VITRO KULTURY (EXPLANTÁTOVÉ KUTLURY, ROSTLINNÉ EXPLANTÁTY) Izolované rostliny, jejich orgány, pletiva či buňky pěstované in vitro ve sterilních podmínkách Na kultivačních
Resyntéza řepky olejky z brukve řepáku a brukve zelné
 Miroslav Klíma a kolektiv Resyntéza řepky olejky z brukve řepáku a brukve zelné Certifikovaná metodika Výzkumný ústav rostlinné výroby, v.v.i. 2018 UPOZORNĚNÍ! Uvedená metodika neprošla dosud oponentním
Miroslav Klíma a kolektiv Resyntéza řepky olejky z brukve řepáku a brukve zelné Certifikovaná metodika Výzkumný ústav rostlinné výroby, v.v.i. 2018 UPOZORNĚNÍ! Uvedená metodika neprošla dosud oponentním
Metodika in vitro kultivace máku setého a produkce homozygotních materiálů pro šlechtitelské využití
 Metodika in vitro kultivace máku setého a produkce homozygotních materiálů pro šlechtitelské využití Metodika byla vypracována jako výstup výzkumného projektu TAČR TA01010375 Využití progresivních biotechnologických
Metodika in vitro kultivace máku setého a produkce homozygotních materiálů pro šlechtitelské využití Metodika byla vypracována jako výstup výzkumného projektu TAČR TA01010375 Využití progresivních biotechnologických
Využití molekulárních technik při selekci rodičovských komponent v programech hybridního šlechtění řepky (Brassica napus L.)
 Využití molekulárních technik při selekci rodičovských komponent v programech hybridního šlechtění řepky (Brassica napus L.) Metodika byla vypracovaná jako výstup výzkumného projektu MZe NAZV QI 111A075
Využití molekulárních technik při selekci rodičovských komponent v programech hybridního šlechtění řepky (Brassica napus L.) Metodika byla vypracovaná jako výstup výzkumného projektu MZe NAZV QI 111A075
Metodika tvorby rodičovských komponent a hybridů ozimé řepky (Brassica napus L.) na bázi CMS
 Metodika tvorby rodičovských komponent a hybridů ozimé řepky (Brassica napus L.) na bázi CMS Metodika byla vypracována jako výstup výzkumného projektu MZe QI 111A075 Využití biotechnologických metod, nových
Metodika tvorby rodičovských komponent a hybridů ozimé řepky (Brassica napus L.) na bázi CMS Metodika byla vypracována jako výstup výzkumného projektu MZe QI 111A075 Využití biotechnologických metod, nových
Metodika fotoautotrofní kultivace rostlin za podmínek in vitro. Dostupný z
 Ševčíková, Hana Dostupný z http://www.nusl.cz/ntk/nusl-263431 Dílo je chráněno podle autorského zákona č. 121/2000 Sb. Tento dokument byl stažen z Národního úložiště šedé literatury (NUŠL). Datum stažení:
Ševčíková, Hana Dostupný z http://www.nusl.cz/ntk/nusl-263431 Dílo je chráněno podle autorského zákona č. 121/2000 Sb. Tento dokument byl stažen z Národního úložiště šedé literatury (NUŠL). Datum stažení:
AKTUÁLNÍ POZNATKY V PĚSTOVÁNÍ, ŠLECHTĚNÍ, OCHRANĚ ROSTLIN A ZPRACOVÁNÍ PRODUKTŮ
 Výzkumný ústav pícninářský, spol. s r.o. Troubsko Zemědělský výzkum, spol. s r.o. Troubsko pod záštitou MZe ČR AKTUÁLNÍ POZNATKY V PĚSTOVÁNÍ, ŠLECHTĚNÍ, OCHRANĚ ROSTLIN A ZPRACOVÁNÍ PRODUKTŮ mediální partner
Výzkumný ústav pícninářský, spol. s r.o. Troubsko Zemědělský výzkum, spol. s r.o. Troubsko pod záštitou MZe ČR AKTUÁLNÍ POZNATKY V PĚSTOVÁNÍ, ŠLECHTĚNÍ, OCHRANĚ ROSTLIN A ZPRACOVÁNÍ PRODUKTŮ mediální partner
1. Metodika. Protokol č. F1-4 Metodika: Srovnávací analýza efektivity přípravy rekombinantního proteinu ve fermentoru
 Protokol č.: F1-4 Datum: 20.12.2010 Metodika: analýza efektivity přípravy výběr z výsledků ze zkušebních provozů výroby antigenů. Vypracoval: Ing. Václav Filištein, Mgr. Tereza Chrudimská, Spolupracující
Protokol č.: F1-4 Datum: 20.12.2010 Metodika: analýza efektivity přípravy výběr z výsledků ze zkušebních provozů výroby antigenů. Vypracoval: Ing. Václav Filištein, Mgr. Tereza Chrudimská, Spolupracující
Článek 1 Předmět smlouvy
 Smluvní strany: Smlouva o uplatnění ověřené technologie VÚRV-OT-02/2018 zpracované v rámci řešení projektu MZe QJ1510172 uzavřená podle ustanovení 11 zákona č. 130/2002 Sb., o podpoře výzkumu, experimentálního
Smluvní strany: Smlouva o uplatnění ověřené technologie VÚRV-OT-02/2018 zpracované v rámci řešení projektu MZe QJ1510172 uzavřená podle ustanovení 11 zákona č. 130/2002 Sb., o podpoře výzkumu, experimentálního
Sure-MeDIP I. with magnetic beads and MNase. www.krd.cz
 Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
Sure-MeDIP I with magnetic beads and MNase www.krd.cz 1 Obsah soupravy a skladování MeDIP souprava obsahuje reagencie na provedení 25 reakcí. Souprava je rozdělen do dvou částí, jedna je distribuována
ZPRÁVA ZA DÍLČÍ VÝSLEDKY ŘEŠENÍ VÝZKUMNÉHO PROGRAMU 3.d ZA ROK 2014
 ZPRÁVA ZA DÍLČÍ VÝSLEDKY ŘEŠENÍ VÝZKUMNÉHO PROGRAMU 3.d ZA ROK 2014 1. TITULNÍ LIST Podpora tvorby rostlinných genotypů s vysokou rezistencí k biotickým i abiotickým faktorům a diferencovanou kvalitou
ZPRÁVA ZA DÍLČÍ VÝSLEDKY ŘEŠENÍ VÝZKUMNÉHO PROGRAMU 3.d ZA ROK 2014 1. TITULNÍ LIST Podpora tvorby rostlinných genotypů s vysokou rezistencí k biotickým i abiotickým faktorům a diferencovanou kvalitou
Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie
 Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie IZOLACE GENOMOVÉ DNA Deoxyribonukleová kyselina (DNA) představuje základní genetický materiál většiny
Izolace genomové DNA ze savčích buněk, stanovení koncentrace DNA pomocí absorpční spektrofotometrie IZOLACE GENOMOVÉ DNA Deoxyribonukleová kyselina (DNA) představuje základní genetický materiál většiny
Jednotné pracovní postupy zkoušení krmiv
 Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
Národní referenční laboratoř Strana KVANTITATIVNÍ STANOVENÍ GENETICKÝCH MODIFIKACÍ METODOU qpcr POMOCÍ ROTOR-GENE PROBE PCR KITU Účel a rozsah Postup slouží ke kvantitativnímu stanovení genetických modifikací
AKTUÁLNÍ POZNATKY V PĚSTOVÁNÍ, ŠLECHTĚNÍ, OCHRANĚ ROSTLIN A ZPRACOVÁNÍ PRODUKTŮ
 Výzkumný ústav pícninářský, spol. s r.o. Troubsko Zemědělský výzkum, spol. s r.o. Troubsko Odbor rostlinolékařství ČAZV Pícninářská komise ORV ČAZV Agrární komora ČR AKTUÁLNÍ POZNATKY V PĚSTOVÁNÍ, ŠLECHTĚNÍ,
Výzkumný ústav pícninářský, spol. s r.o. Troubsko Zemědělský výzkum, spol. s r.o. Troubsko Odbor rostlinolékařství ČAZV Pícninářská komise ORV ČAZV Agrární komora ČR AKTUÁLNÍ POZNATKY V PĚSTOVÁNÍ, ŠLECHTĚNÍ,
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2
 cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
cdna synthesis kit First-Strand cdna Synthesis System Verze 1.2 Obsah soupravy a její skladování Tato souprava pro reverzní transkripci obsahuje reagencie potřebné k provedení reverzní transkripce (RT)
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU KVASINEK RODU SACCHAROMYCES
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KVASINEK RODU SACCHAROMYCES 1 Rozsah a účel Metodika slouží ke stanovení počtu probiotických kvasinek v doplňkových látkách, premixech a krmivech.
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU KVASINEK RODU SACCHAROMYCES 1 Rozsah a účel Metodika slouží ke stanovení počtu probiotických kvasinek v doplňkových látkách, premixech a krmivech.
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU PROBIOTICKÝCH BAKTERIÍ RODU ENTEROCOCCUS
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU PROBIOTICKÝCH BAKTERIÍ RODU ENTEROCOCCUS 1 Rozsah a účel Postup slouží ke stanovení počtu probiotických bakterií v doplňkových látkách, premixech
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU PROBIOTICKÝCH BAKTERIÍ RODU ENTEROCOCCUS 1 Rozsah a účel Postup slouží ke stanovení počtu probiotických bakterií v doplňkových látkách, premixech
Ing. Prokop Šmirous, Ph.D. ŠLECHTĚNÍ KMÍNU V AGRITECU
 Ing. Prokop Šmirous, Ph.D. ŠLECHTĚNÍ KMÍNU V AGRITECU KRÁTCE Z HISTORIE Pesticidní pokusy od 70-80. let minulého stolení (herbicid Afalon, odrůda Rekord (1978)) Začátek šlechtitelské práce na kmínu v roce
Ing. Prokop Šmirous, Ph.D. ŠLECHTĚNÍ KMÍNU V AGRITECU KRÁTCE Z HISTORIE Pesticidní pokusy od 70-80. let minulého stolení (herbicid Afalon, odrůda Rekord (1978)) Začátek šlechtitelské práce na kmínu v roce
Protokoly Transformace plasmidu do elektrokompetentních buněk BL21 Pracovní postup:
 Protokoly Pracovní potřeby, pufry a chemikálie jsou uvedeny na konci protokolu. Pracovní postupy jsou odvozeny od těchto kitů: Champion pet160 Directional TOPO Expression Kit with Lumio Technology (Invitrogen)
Protokoly Pracovní potřeby, pufry a chemikálie jsou uvedeny na konci protokolu. Pracovní postupy jsou odvozeny od těchto kitů: Champion pet160 Directional TOPO Expression Kit with Lumio Technology (Invitrogen)
Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202)
 Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202) Popis Column DNA Lego Kit je základ moderní stavebnicové (Lego) soupravy pro izolaci čisté DNA různého
Column DNA Lego Kit UNIVERZÁLNÍ SOUPRAVY PRO RYCHLOU IZOLACI ČISTÉ DNA (Katalogové číslo D201 + D202) Popis Column DNA Lego Kit je základ moderní stavebnicové (Lego) soupravy pro izolaci čisté DNA různého
Braf V600E StripAssay
 Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
Braf V600E StripAssay Kat. číslo 5-570 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci čerstvých nebo mražených biopsií použijte soupravy Qiagen QIAmp DNA Mini nebo Micro. Pro izolaci
INDUKCE TVORBY MIKROHLÍZEK BRAMBORU IN VITRO
 Úloha č. 14 Indukce tvorby hlíz in vitro na jednonodálních segmentech rostlin bramboru -1 - INDUKCE TVORBY MIKROHLÍZEK BRAMBORU IN VITRO TUBERIZACE BRAMBOR (Solanum tuberosum) Tuberizace je morfogenetický
Úloha č. 14 Indukce tvorby hlíz in vitro na jednonodálních segmentech rostlin bramboru -1 - INDUKCE TVORBY MIKROHLÍZEK BRAMBORU IN VITRO TUBERIZACE BRAMBOR (Solanum tuberosum) Tuberizace je morfogenetický
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU DEKOCHINÁTU METODOU HPLC 1 Rozsah a účel Tato metoda specifikuje podmínky pro stanovení dekochinátu metodou vysokoúčinné kapalinové chromatografie
Metodika izolace DNA a analýzy molekulárních markerů pro účely popisu genetických zdrojů řepky (Brassica napus L.) a hodnocení jejich diverzity
 Metodika izolace DNA a analýzy molekulárních markerů pro účely popisu genetických zdrojů řepky (Brassica napus L.) a hodnocení jejich diverzity Metodika byla vypracovaná jako výstup výzkumného projektu
Metodika izolace DNA a analýzy molekulárních markerů pro účely popisu genetických zdrojů řepky (Brassica napus L.) a hodnocení jejich diverzity Metodika byla vypracovaná jako výstup výzkumného projektu
N217019 - Laboratoř hydrobiologie a mikrobiologie
 ÚSTAV TECHNOLOGIE VODY A PROSTŘEDÍ N217019 - Laboratoř hydrobiologie a mikrobiologie Název úlohy: Hydrobiologie: Stanovení koncentrace chlorofylu-a Vypracováno v rámci projektu: Inovace a restrukturalizace
ÚSTAV TECHNOLOGIE VODY A PROSTŘEDÍ N217019 - Laboratoř hydrobiologie a mikrobiologie Název úlohy: Hydrobiologie: Stanovení koncentrace chlorofylu-a Vypracováno v rámci projektu: Inovace a restrukturalizace
EGFR XL StripAssay. Kat. číslo 5-630. 20 testů 2-8 C
 EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
EGFR XL StripAssay Kat. číslo 5-630 20 testů 2-8 C Popis stripu Pracovní postup 1. Izolace DNA Pro izolaci DNA použijte vhodný izolační kit. Doporučené kity jsou následující: Pro izolaci čerstvých nebo
Metodika analýzy molekulárních markerů u jilmu, Ulmus L.
 Metodika analýzy molekulárních markerů u jilmu, Ulmus L. Metodika byla vypracovaná jako výstup projektu NAZV QI92A247 Charakterizace genetické struktury autochtonních populací jilmů pomocí DNA analýz,
Metodika analýzy molekulárních markerů u jilmu, Ulmus L. Metodika byla vypracovaná jako výstup projektu NAZV QI92A247 Charakterizace genetické struktury autochtonních populací jilmů pomocí DNA analýz,
Biotechnologické metody ve šlechtění rostlin
 KATEDRA SPECIÁLNÍ PRODUKCE ROSTLINNÉ září 2014 prof. Ing. Vladislav Čurn, Ph.D. Jihočeská univerzita v Českých Budějovicích Zemědělská fakulta, Katedra speciální produkce rostlinné Na Sádkách 1780, 370
KATEDRA SPECIÁLNÍ PRODUKCE ROSTLINNÉ září 2014 prof. Ing. Vladislav Čurn, Ph.D. Jihočeská univerzita v Českých Budějovicích Zemědělská fakulta, Katedra speciální produkce rostlinné Na Sádkách 1780, 370
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche
 Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
Konečná zpráva hodnocení různých způsobů přípravy vzorků pro AMPLICOR HPV test firmy Roche Charakteristika testu: Set AMPLICOR HPV vyráběný firmou Roche je určený pro detekci vysoko-rizikových typů lidských
Řasový test ekotoxicity na mikrotitračních destičkách
 Řasový test ekotoxicity na mikrotitračních destičkách 1 Účel Řasové testy toxicity slouží k testování možných toxických účinků látek a vzorků na vodní producenty. Zelené řasy patří do skupiny necévnatých
Řasový test ekotoxicity na mikrotitračních destičkách 1 Účel Řasové testy toxicity slouží k testování možných toxických účinků látek a vzorků na vodní producenty. Zelené řasy patří do skupiny necévnatých
Metodické postupy mikropropagace a rhizogeneze zvonovce liliolistého
 MGSII-17 Záchranný program pro zvonovec liliolistý (Adenophora liliifolia) Metodické postupy mikropropagace a rhizogeneze zvonovce liliolistého Závěrečná zpráva Zpracoval Výzkumný ústav lesního hospodářství
MGSII-17 Záchranný program pro zvonovec liliolistý (Adenophora liliifolia) Metodické postupy mikropropagace a rhizogeneze zvonovce liliolistého Závěrečná zpráva Zpracoval Výzkumný ústav lesního hospodářství
Kdo jsme. Centrum strukturní a funkční genomiky rostlin Ústavu experimentální botaniky AV ČR, v.v.i.
 Kdo jsme Centrum strukturní a funkční genomiky rostlin Ústavu experimentální botaniky AV ČR, v.v.i. Partner Centra regionu Haná pro biotechnologický a zemědělský výzkum v Olomouci (projekt OP VaVpI) Centrum
Kdo jsme Centrum strukturní a funkční genomiky rostlin Ústavu experimentální botaniky AV ČR, v.v.i. Partner Centra regionu Haná pro biotechnologický a zemědělský výzkum v Olomouci (projekt OP VaVpI) Centrum
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B
 MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
MagPurix Viral/Pathogen Nucleic Acids Extraction Kit B Kat. č. ZP02012 Doba zpracování: 45-60 minut pro MagPurix 12S 45-65 minut pro MagPurix 24 Použití Souprava MagPurix Viral/Pathogen Nucleic Acids Extraction
OBECNÁ MIKROBIOLOGIE MIKROBIOLOGICKÁ LABORATOŘ. Petra Lysková [1]
![OBECNÁ MIKROBIOLOGIE MIKROBIOLOGICKÁ LABORATOŘ. Petra Lysková [1] OBECNÁ MIKROBIOLOGIE MIKROBIOLOGICKÁ LABORATOŘ. Petra Lysková [1]](/thumbs/91/107535297.jpg) OBECNÁ MIKROBIOLOGIE MIKROBIOLOGICKÁ LABORATOŘ Petra Lysková [1] BEZPEČNOST PRÁCE tašky zamknout ve skříňce vstup do laboratoře pouze v plášti a přezůvkách bez prstýnků a sepnuté vlasy dochvilnost! vstup
OBECNÁ MIKROBIOLOGIE MIKROBIOLOGICKÁ LABORATOŘ Petra Lysková [1] BEZPEČNOST PRÁCE tašky zamknout ve skříňce vstup do laboratoře pouze v plášti a přezůvkách bez prstýnků a sepnuté vlasy dochvilnost! vstup
IZOLACE DNA (KIT DNeasy Plant Mini)
 17.1 Izolace DNA (kit DNeasy Plant Mini) Strana 1 IZOLACE DNA (KIT DNeasy Plant Mini) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu DNeasy Plant
17.1 Izolace DNA (kit DNeasy Plant Mini) Strana 1 IZOLACE DNA (KIT DNeasy Plant Mini) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu DNeasy Plant
RNA Blue REAGENS PRO RYCHLOU PŘÍPRAVU ČISTÉ A NEDEGRADOVANÉ RNA (katalogové číslo R011, R012, R013)
 RNA Blue REAGENS PRO RYCHLOU PŘÍPRAVU ČISTÉ A NEDEGRADOVANÉ RNA (katalogové číslo R011, R012, R013) Upozornění: RNA Blue obsahuje fenol a další toxické komponenty. Při kontaktu s kůží je nutné omytí velkým
RNA Blue REAGENS PRO RYCHLOU PŘÍPRAVU ČISTÉ A NEDEGRADOVANÉ RNA (katalogové číslo R011, R012, R013) Upozornění: RNA Blue obsahuje fenol a další toxické komponenty. Při kontaktu s kůží je nutné omytí velkým
CVD-T StripAssay. Kat. číslo 4-360. 20 testů 2-8 C
 CVD-T StripAssay Kat. číslo 4-360 20 testů 2-8 C Popis stripu Pracovní postup Izolace DNA Použijte čerstvou nebo zmraženou krev s EDTA nebo citrátem, jako antikoagulans, vyhněte se krvi s obsahem heparinu.
CVD-T StripAssay Kat. číslo 4-360 20 testů 2-8 C Popis stripu Pracovní postup Izolace DNA Použijte čerstvou nebo zmraženou krev s EDTA nebo citrátem, jako antikoagulans, vyhněte se krvi s obsahem heparinu.
Semenné sady systém reprodukce a efektivita
 Genetika a šlechtění lesních dřevin Semenné sady systém reprodukce a efektivita Doc. Ing. RNDr. Eva Palátová, PhD. Ústav zakládání a pěstění lesů LDF MENDELU Brno Tento projekt je spolufinancován Evropským
Genetika a šlechtění lesních dřevin Semenné sady systém reprodukce a efektivita Doc. Ing. RNDr. Eva Palátová, PhD. Ústav zakládání a pěstění lesů LDF MENDELU Brno Tento projekt je spolufinancován Evropským
Metodika detekce a molekulární selekce autoinkompatibilních linií řepky (Brassica napus L.)
 Metodika detekce a molekulární selekce autoinkompatibilních linií řepky (Brassica napus L.) Metodika byla vypracovaná jako výstup výzkumného záměru MSM 6007665806 Trvale udržitelné způsoby zemědělského
Metodika detekce a molekulární selekce autoinkompatibilních linií řepky (Brassica napus L.) Metodika byla vypracovaná jako výstup výzkumného záměru MSM 6007665806 Trvale udržitelné způsoby zemědělského
COMET ASSAY (SINGLE CELL GEL ELECTROPHORESIS)
 COMET ASSAY (SINGLE CELL GEL ELECTROPHORESIS) OBSAH 1. Princip metody 2. Přístroje a zařízení 3. Příprava vzorků 3.1 Kultivace a sklízení buněk A549 3.2 Výpočet koncentrace buněk 3.3 Hodnocení viability
COMET ASSAY (SINGLE CELL GEL ELECTROPHORESIS) OBSAH 1. Princip metody 2. Přístroje a zařízení 3. Příprava vzorků 3.1 Kultivace a sklízení buněk A549 3.2 Výpočet koncentrace buněk 3.3 Hodnocení viability
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC
 Strana 1 STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Postup specifikuje podmínky pro stanovení obsahu semduramicinu v krmivech metodou vysokoúčinné kapalinové chromatografie (HPLC) v koncentračním
Strana 1 STANOVENÍ OBSAHU SEMDURAMICINU METODOU HPLC 1 Rozsah a účel Postup specifikuje podmínky pro stanovení obsahu semduramicinu v krmivech metodou vysokoúčinné kapalinové chromatografie (HPLC) v koncentračním
Kultivační metody stanovení mikroorganismů
 Kultivační metody stanovení mikroorganismů Základní rozdělení půd Syntetická, definovaná media, jednoduché sloučeniny, známé sloţení Komplexní media, vycházejí z ţivočišných nebo rostlinných tkání a pletiv,
Kultivační metody stanovení mikroorganismů Základní rozdělení půd Syntetická, definovaná media, jednoduché sloučeniny, známé sloţení Komplexní media, vycházejí z ţivočišných nebo rostlinných tkání a pletiv,
TECHNIKY EXPLANTÁTOVÝCH KULTUR
 UNIVERZITA PALACKÉHO V OLOMOUCI PŘÍRODOVĚDECKÁ FAKULTA KATEDRA BOTANIKY NÁVODY KE CVIČENÍM TECHNIKY EXPLANTÁTOVÝCH KULTUR BOT/TEKSB Studijní předmět: volitelný LS Garant RNDr. Božena Navrátilová, PhD.
UNIVERZITA PALACKÉHO V OLOMOUCI PŘÍRODOVĚDECKÁ FAKULTA KATEDRA BOTANIKY NÁVODY KE CVIČENÍM TECHNIKY EXPLANTÁTOVÝCH KULTUR BOT/TEKSB Studijní předmět: volitelný LS Garant RNDr. Božena Navrátilová, PhD.
NRAS StripAssay. Kat. číslo 5-610. 20 testů 2-8 C
 NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
NRAS StripAssay Kat. číslo 5-610 20 testů 2-8 C Popis stripu: Pracovní postup 1. Izolace DNA Pro izolaci DNA musí být použita vhodná metoda vzhledem k typu tkáně vzorku. Pro doporučení vhodné metody kontaktujte
Laboratorní pomůcky, chemické nádobí
 Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
Laboratorní pomůcky, chemické nádobí Laboratorní sklo: měkké (tyčinky, spojovací trubice, kapiláry) tvrdé označení SIMAX (většina varného a odměrného skla) Zahřívání skla: Tenkostěnné nádoby (kádinky,
Praktické cvičení: Izolace a purifikace rekombinantního proteinu
 Praktické cvičení: Izolace a purifikace rekombinantního proteinu Toto blokové praktické cvičení spočívá v teoretickém i praktickém seznámení s rekombinantními proteiny, jejich izolací, purifikací a využitím.
Praktické cvičení: Izolace a purifikace rekombinantního proteinu Toto blokové praktické cvičení spočívá v teoretickém i praktickém seznámení s rekombinantními proteiny, jejich izolací, purifikací a využitím.
Inovace studia molekulární a buněčné biologie
 Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
Investice do rozvoje vzdělávání Inovace studia molekulární a buněčné biologie Tento projekt je spolufinancován Evropským sociálním fondem a státním rozpočtem České republiky. Investice do rozvoje vzdělávání
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C
 α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
α-globin StripAssay Kat. číslo 4-160 10 testů 2-8 C Popis stripů: Pracovní postup Izolace DNA Doporučujeme použít následující kit pro izolaci DNA z plné krve nebo jiných typů vzorků: Spin Micro DNA Extraction
Jednotné pracovní postupy analýza půd III TEST VLIVU CHEMIKÁLIÍ NA DÉLKU KOŘENE SALÁTU (LACTUCA SATIVA)
 Národní referenční laboratoř Strana 1 TEST VLIVU CHEMIKÁLIÍ NA DÉLKU KOŘENE SALÁTU (LACTUCA SATIVA) 1 Rozsah a účel Postup je určen pro testování toxicity látek, které nemají silně těkavou povahu. Test
Národní referenční laboratoř Strana 1 TEST VLIVU CHEMIKÁLIÍ NA DÉLKU KOŘENE SALÁTU (LACTUCA SATIVA) 1 Rozsah a účel Postup je určen pro testování toxicity látek, které nemají silně těkavou povahu. Test
TESTOVÁNÍ GMO Praktikum fyziologie rostlin
 Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
Teoretický úvod: TESTOVÁNÍ GMO Praktikum fyziologie rostlin 1 Teoretický úvod: TESTOVÁNÍ GMO Obecně na úvod Určitě jste už slyšeli pojem geneticky modifikovaný organismus (GMO). Úprava vlastností přirozeně
Ústřední komise Chemické olympiády. 53. ročník 2016/2017. KRAJSKÉ KOLO kategorie C. ŘEŠENÍ PRAKTICKÉ ČÁSTI (40 bodů) časová náročnost: 120 minut
 Ústřední komise Chemické olympiády 53. ročník 2016/2017 KRAJSKÉ KOLO kategorie C ŘEŠENÍ PRAKTICKÉ ČÁSTI (40 bodů) časová náročnost: 120 minut Úloha 1 Rychlá příprava mědi 20 bodů 1. Fe + CuSO 4 Cu + FeSO
Ústřední komise Chemické olympiády 53. ročník 2016/2017 KRAJSKÉ KOLO kategorie C ŘEŠENÍ PRAKTICKÉ ČÁSTI (40 bodů) časová náročnost: 120 minut Úloha 1 Rychlá příprava mědi 20 bodů 1. Fe + CuSO 4 Cu + FeSO
ZPRÁVA ZA DÍLČÍ VÝSLEDKY ŘEŠENÍ VÝZKUMNÉHO PROGRAMU 3.d ZA ROK 2014
 ZPRÁVA ZA DÍLČÍ VÝSLEDKY ŘEŠENÍ VÝZKUMNÉHO PROGRAMU 3.d ZA ROK 2014 1. TITULNÍ LIST Podpora tvorby rostlinných genotypů s vysokou rezistencí k biotickým i abiotickým faktorům a diferencovanou kvalitou
ZPRÁVA ZA DÍLČÍ VÝSLEDKY ŘEŠENÍ VÝZKUMNÉHO PROGRAMU 3.d ZA ROK 2014 1. TITULNÍ LIST Podpora tvorby rostlinných genotypů s vysokou rezistencí k biotickým i abiotickým faktorům a diferencovanou kvalitou
DODATEČNÉ INFORMACE K ZADÁVACÍM PODMÍNKÁM
 DODATEČNÉ INFORMACE K ZADÁVACÍM PODMÍNKÁM Zadavatel: Česká zemědělská univerzita v Praze Sídlo: Praha Suchdol, Kamýcká 129, PSČ 165 21 IČ: 604 60 709 Zastoupený: Ing. Janou Vohralíkovou, kvestorkou Profil
DODATEČNÉ INFORMACE K ZADÁVACÍM PODMÍNKÁM Zadavatel: Česká zemědělská univerzita v Praze Sídlo: Praha Suchdol, Kamýcká 129, PSČ 165 21 IČ: 604 60 709 Zastoupený: Ing. Janou Vohralíkovou, kvestorkou Profil
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - FUMONISIN B 1 A B 2 1 Rozsah a účel Metoda je vhodná pro stanovení fumonisinů B 1 a B 2 v krmivech. 2 Princip Fumonisiny
OPTIMALIZACE PROCESU KULTIVACE ZELENÝCH ŘAS S VYUŽITÍM DIGESČNÍCH ZBYTKŮ ZE ZEMĚDĚLSKÝCH BIOPLYNOVÝCH STANIC. Ing. Pavla Hrychová
 OPTIMALIZACE PROCESU KULTIVACE ZELENÝCH ŘAS S VYUŽITÍM DIGESČNÍCH ZBYTKŮ ZE ZEMĚDĚLSKÝCH BIOPLYNOVÝCH STANIC Ing. Pavla Hrychová Cíl Optimalizace růstu zelené řasy Scenedesmus cf. acutus v připravených
OPTIMALIZACE PROCESU KULTIVACE ZELENÝCH ŘAS S VYUŽITÍM DIGESČNÍCH ZBYTKŮ ZE ZEMĚDĚLSKÝCH BIOPLYNOVÝCH STANIC Ing. Pavla Hrychová Cíl Optimalizace růstu zelené řasy Scenedesmus cf. acutus v připravených
Seminář izolačních technologií
 Seminář izolačních technologií Zpracoval: Karel Bílek a Kateřina Svobodová Podpořeno FRVŠ 2385/2007 a 1305/2009 Úpravy a aktualizace: Pavla Chalupová ÚMFGZ MZLU v Brně 1 Lokalizace jaderné DNA 2 http://www.paternityexperts.com/basicgenetics.html
Seminář izolačních technologií Zpracoval: Karel Bílek a Kateřina Svobodová Podpořeno FRVŠ 2385/2007 a 1305/2009 Úpravy a aktualizace: Pavla Chalupová ÚMFGZ MZLU v Brně 1 Lokalizace jaderné DNA 2 http://www.paternityexperts.com/basicgenetics.html
Braf 600/601 StripAssay
 Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Braf 600/601 StripAssay Kat. číslo 5-560 20 testů 2-8 C Popis stripu: Pracovní postup Kit umožňuje detekci 9 mutací v genu BRAF (kodón 600 a 601) Další informace najdete v OMIM Online Mendelian Inheritance
Laboratoř růstových regulátorů Miroslav Strnad. ové kultury. Olomouc. Univerzita Palackého & Ústav experimentální botaniky AV CR
 Laboratoř růstových regulátorů Miroslav Strnad Tkáňov ové kultury Olomouc Univerzita Palackého & Ústav experimentální botaniky AV CR DEFINICE - růst a vývoj rostlinných buněk, pletiv a orgánů lze účinně
Laboratoř růstových regulátorů Miroslav Strnad Tkáňov ové kultury Olomouc Univerzita Palackého & Ústav experimentální botaniky AV CR DEFINICE - růst a vývoj rostlinných buněk, pletiv a orgánů lze účinně
CR Haná LABORATORNÍ MYCÍ AUTOMAT S PŘÍSLUŠENSTVÍM 2
 ODŮVODNĚNÍ VEŘEJNÉ ZAKÁZKY v souladu s 156 zákona č. 137/2006, Sb., o veřejných zakázkách, ve znění pozdějších předpisů Nadlimitní veřejná zakázka na dodávky zadávaná v otevřeném řízení v souladu s ust.
ODŮVODNĚNÍ VEŘEJNÉ ZAKÁZKY v souladu s 156 zákona č. 137/2006, Sb., o veřejných zakázkách, ve znění pozdějších předpisů Nadlimitní veřejná zakázka na dodávky zadávaná v otevřeném řízení v souladu s ust.
Polymorfismus délky restrikčních fragmentů (RFLP)
 ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Polymorfismus délky restrikčních fragmentů (RFLP) Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2017/18 Obsah POLYMORFISMUS
ÚSTAV LÉKAŘSKÉ BIOCHEMIE A LABORATORNÍ DIAGNOSTIKY 1. LF UK Polymorfismus délky restrikčních fragmentů (RFLP) Praktické cvičení z lékařské biochemie Všeobecné lékařství Martin Vejražka 2017/18 Obsah POLYMORFISMUS
Transgenní řepka olejka (Brassica napus L.) její monitoring, molekulární detekce a vliv agrotechniky na eliminaci výdrolu
 Transgenní řepka olejka (Brassica napus L.) její monitoring, molekulární detekce a vliv agrotechniky na eliminaci výdrolu Genové inženýrství umožňuje vnesení hospodářsky významných znaků do zájmových plodin
Transgenní řepka olejka (Brassica napus L.) její monitoring, molekulární detekce a vliv agrotechniky na eliminaci výdrolu Genové inženýrství umožňuje vnesení hospodářsky významných znaků do zájmových plodin
Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/
 Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018 Složky šlechtění lesních dřevin šlechtění testování rozmnožování Ověřování vyšlechtěného
Tento projekt je spolufinancován Evropským sociálním fondem a Státním rozpočtem ČR InoBio CZ.1.07/2.2.00/28.0018 Složky šlechtění lesních dřevin šlechtění testování rozmnožování Ověřování vyšlechtěného
MagPurix Blood DNA Extraction Kit 200
 MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
MagPurix Blood DNA Extraction Kit 200 Kat. č. ZP02001-48 Doba zpracování: 50-60 minut pro MagPurix 12S 50-70 minut pro MagPurix 24 Použití Souprava MagPurix Blood DNA Extraction Kit 200 je určena pro izolátor
Metodika prašníkové kultury lnu setého s aplikací nových syntetických derivátů cytokininů
 Metodika prašníkové kultury lnu setého s aplikací nových syntetických derivátů cytokininů Autorský kolektiv: Ing. Miroslava Vrbová, Ph.D. Ing. Iva Smýkalová, Ph.D. Metodika prašníkové kultury lnu setého
Metodika prašníkové kultury lnu setého s aplikací nových syntetických derivátů cytokininů Autorský kolektiv: Ing. Miroslava Vrbová, Ph.D. Ing. Iva Smýkalová, Ph.D. Metodika prašníkové kultury lnu setého
Mendelova univerzita v Brně Agronomická fakulta Ústav biologie rostlin
 Mendelova univerzita v Brně Agronomická fakulta Ústav biologie rostlin Inovace laboratorních úloh genetických předmětů metodikami pracujícími s ribonukleovými kyselinami pšenice Metodické návody pro laboratorní
Mendelova univerzita v Brně Agronomická fakulta Ústav biologie rostlin Inovace laboratorních úloh genetických předmětů metodikami pracujícími s ribonukleovými kyselinami pšenice Metodické návody pro laboratorní
IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT GENELUTE)
 Strana 1 IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT GENELUTE) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu GenElute. 2 Princip Proces izolace
Strana 1 IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT GENELUTE) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku pomocí komerčního kitu GenElute. 2 Princip Proces izolace
TECHNICKÁ SPECIFIKACE Vybavení genetické laboratoře pro projekt EXTEMIT-K část B
 TECHNICKÁ SPECIFIKACE Vybavení genetické laboratoře pro projekt EXTEMIT-K část B OBSAH Sestava pro vertikální elektroforézu... 2 Jednotka pro elektroforézu... 3 Termocykler... 4 Elektrický zdroj pro elektroforézu...
TECHNICKÁ SPECIFIKACE Vybavení genetické laboratoře pro projekt EXTEMIT-K část B OBSAH Sestava pro vertikální elektroforézu... 2 Jednotka pro elektroforézu... 3 Termocykler... 4 Elektrický zdroj pro elektroforézu...
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - aflatoxin B1, B2, G1 a G2
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - aflatoxin B1, B2, G1 a G2 1 Rozsah a účel Metoda je vhodná pro stanovení aflatoxinů B1, B2, G1 a G2 v krmivech. 2 Princip
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU LC-MS - aflatoxin B1, B2, G1 a G2 1 Rozsah a účel Metoda je vhodná pro stanovení aflatoxinů B1, B2, G1 a G2 v krmivech. 2 Princip
Inovace bakalářského studijního oboru Aplikovaná chemie CZ.1.07/2.2.00/15.0247
 Papírová a tenkovrstvá chromatografie Jednou z nejrozšířenějších analytických metod je bezesporu chromatografie, umožňující účinnou separaci látek nutnou pro spolehlivou identifikaci a kvantifikaci složek
Papírová a tenkovrstvá chromatografie Jednou z nejrozšířenějších analytických metod je bezesporu chromatografie, umožňující účinnou separaci látek nutnou pro spolehlivou identifikaci a kvantifikaci složek
MagPurix Viral Nucleic Acid Extraction Kit
 MagPurix Viral Nucleic Acid Extraction Kit Kat. č. ZP02003 Doba zpracování: 40-55 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Viral Nucleic Acid Extraction Kit je určena
MagPurix Viral Nucleic Acid Extraction Kit Kat. č. ZP02003 Doba zpracování: 40-55 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Viral Nucleic Acid Extraction Kit je určena
ÚLOHA 1: Stanovení koncentrace kyseliny ve vzorku potenciometrickou titrací
 UPOZORNĚNÍ V tabulkách pro jednotlivé úlohy jsou uvedeny předpokládané pomůcky, potřebné pro vypracování experimentální části úlohy. Některé pomůcky (lžička, váženka, stopky, elmag. míchadélko, tyčinka
UPOZORNĚNÍ V tabulkách pro jednotlivé úlohy jsou uvedeny předpokládané pomůcky, potřebné pro vypracování experimentální části úlohy. Některé pomůcky (lžička, váženka, stopky, elmag. míchadélko, tyčinka
ZÁVĚREČNÁ ZPRÁVA PROJEKTU DOTAČNÍHO TITULU 3.d. za dobu řešení TITULNÍ LIST
 ZÁVĚREČNÁ ZPRÁVA PROJEKTU DOTAČNÍHO TITULU 3.d. za dobu řešení 2008-2013 1. TITULNÍ LIST Podpora tvorby rostlinných genotypů s vysokou rezistencí k biotickým i abiotickým faktorům a diferencovanou kvalitou
ZÁVĚREČNÁ ZPRÁVA PROJEKTU DOTAČNÍHO TITULU 3.d. za dobu řešení 2008-2013 1. TITULNÍ LIST Podpora tvorby rostlinných genotypů s vysokou rezistencí k biotickým i abiotickým faktorům a diferencovanou kvalitou
Kultivace révy vinné v in vitro podmínkách
 Ing. Miloš Faltus, Ph.D. RNDr. Ondřej Skala RNDr. Alois Bilavčík, Ph.D. Ing. Jiří Zámečník, CSc. Kultivace révy vinné v in vitro podmínkách CERTIFIKOVANÁ METODIKA Výzkumný ústav rostlinné výroby, v.v.i.
Ing. Miloš Faltus, Ph.D. RNDr. Ondřej Skala RNDr. Alois Bilavčík, Ph.D. Ing. Jiří Zámečník, CSc. Kultivace révy vinné v in vitro podmínkách CERTIFIKOVANÁ METODIKA Výzkumný ústav rostlinné výroby, v.v.i.
Izolace nukleových kyselin
 Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
Izolace nukleových kyselin Požadavky na izolaci nukleových kyselin V nativním stavu z přirozeného materiálu v dostatečném množství požadované čistotě. Nukleové kyseliny je třeba zbavit všech látek, které
Komplement fixační antigen Influenza A (KF Ag Influenza A)
 Komplement fixační antigen Influenza A (KF Ag Influenza A) OD - 109 Návod k použití soupravy VÝROBCE : VIDIA spol. s r.o., Nad Safinou II/365, Vestec, 252 42 Jesenice u Prahy, tel.: 261090565 www.vidia.cz
Komplement fixační antigen Influenza A (KF Ag Influenza A) OD - 109 Návod k použití soupravy VÝROBCE : VIDIA spol. s r.o., Nad Safinou II/365, Vestec, 252 42 Jesenice u Prahy, tel.: 261090565 www.vidia.cz
Jednotné pracovní postupy zkoušení krmiv Stanovení obsahu celkového a volného tryptofanu metodou HPLC
 Strana 1 STANOVENÍ OBSAHU CELKOVÉHO A VOLNÉHO TRYPTOFANU METODOU HPLC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení obsahu celkového a volného tryptofanu v krmivech metodou vysokoúčinné kapalinové
Strana 1 STANOVENÍ OBSAHU CELKOVÉHO A VOLNÉHO TRYPTOFANU METODOU HPLC 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení obsahu celkového a volného tryptofanu v krmivech metodou vysokoúčinné kapalinové
Spektrofotometrické stanovení fosforečnanů ve vodách
 Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
Spektrofotometrické stanovení fosforečnanů ve vodách Úkol: Spektrofotometricky stanovte obsah fosforečnanů ve vodě Chemikálie: 0,07165 g dihydrogenfosforečnan draselný KH 2 PO 4 75 ml kyselina sírová H
HYCOL. Lis tová hno jiva. HYCOL-Zn kulturní rostliny. HYCOL-Cu kulturní rostliny. HYCOL-E OLEJNINA řepka, slunečnice, mák
 Lis tová hno jiva n e j ž e n e... víc HYCOL do e kol o g ic ké p ro d u kce BIHOP-K+ HYCOL-BMgS HYCOL-NPK chmel, kukuřice, mák HYCOL-E OBILNINA řepka, slunečnice, mák zelenina, slunečnice pšenice, ječmen,
Lis tová hno jiva n e j ž e n e... víc HYCOL do e kol o g ic ké p ro d u kce BIHOP-K+ HYCOL-BMgS HYCOL-NPK chmel, kukuřice, mák HYCOL-E OBILNINA řepka, slunečnice, mák zelenina, slunečnice pšenice, ječmen,
Konzervace genetických zdrojů chmele (Humulus lupulus, L.) pomocí metody kryoprezervace
 Ing. Miloš Faltus, Ph.D. Ing. Jiří Zámečník, CSc. Konzervace genetických zdrojů chmele (Humulus lupulus, L.) pomocí metody kryoprezervace METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2008
Ing. Miloš Faltus, Ph.D. Ing. Jiří Zámečník, CSc. Konzervace genetických zdrojů chmele (Humulus lupulus, L.) pomocí metody kryoprezervace METODIKA PRO PRAXI Výzkumný ústav rostlinné výroby, v.v.i. 2008
Metodika řízkování podnoží vybraných ovocných druhů
 Výzkumný a šlechtitelský ústav ovocnářský Holovousy s.r.o. Mendelova univerzita v Brně, Zahradnická fakulta v Lednici Metodika řízkování podnoží vybraných ovocných druhů Tomáš Nečas, Jan Náměstek, Luděk
Výzkumný a šlechtitelský ústav ovocnářský Holovousy s.r.o. Mendelova univerzita v Brně, Zahradnická fakulta v Lednici Metodika řízkování podnoží vybraných ovocných druhů Tomáš Nečas, Jan Náměstek, Luděk
Rostlinné explantáty (kultury in vitro)
 Rostlinné explantáty (kultury in vitro) Jaroslava Dubová Ústav experimentální biologie Oddělení fyziologie a anatomie rostlin a Laboratoř molekulární fyziologie rostlin Přírodovědecká fakulta Masarykova
Rostlinné explantáty (kultury in vitro) Jaroslava Dubová Ústav experimentální biologie Oddělení fyziologie a anatomie rostlin a Laboratoř molekulární fyziologie rostlin Přírodovědecká fakulta Masarykova
1) Pojem biotechnologický proces a jeho fázování 2) Suroviny pro fermentaci 3) Procesy sterilizace 4) Bioreaktory a fermentory 5) Procesy kultivace,
 1) Pojem biotechnologický proces a jeho fázování 2) Suroviny pro fermentaci 3) Procesy sterilizace 4) Bioreaktory a fermentory 5) Procesy kultivace, růstové parametry buněčných kultur 2 Biomasa Extracelulární
1) Pojem biotechnologický proces a jeho fázování 2) Suroviny pro fermentaci 3) Procesy sterilizace 4) Bioreaktory a fermentory 5) Procesy kultivace, růstové parametry buněčných kultur 2 Biomasa Extracelulární
METODIKA TESTOVÁNÍ TOXICITY TĚŽKÝCH KOVŮ POMOCÍ SUSPENZNÍCH KULTUR KONOPÍ SETÉHO (CANNABIS SATIVA ssp. SATIVA L.)
 Agritec Plant Research s.r.o. Zemědělská 2520/16, 787 01 Šumperk METODIKA TESTOVÁNÍ TOXICITY TĚŽKÝCH KOVŮ POMOCÍ SUSPENZNÍCH KULTUR KONOPÍ SETÉHO (CANNABIS SATIVA ssp. SATIVA L.) Autorky: Magdalena Cvečková,
Agritec Plant Research s.r.o. Zemědělská 2520/16, 787 01 Šumperk METODIKA TESTOVÁNÍ TOXICITY TĚŽKÝCH KOVŮ POMOCÍ SUSPENZNÍCH KULTUR KONOPÍ SETÉHO (CANNABIS SATIVA ssp. SATIVA L.) Autorky: Magdalena Cvečková,
13/sv. 8 (85/503/EHS) Tato směrnice je určena členským státům.
 62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
62 31985L0503 L 308/12 ÚŘEDNÍ VĚSTNÍK EVROPSKÝCH SPOLEČENSTVÍ 20.11.1985 PRVNÍ SMĚRNICE KOMISE ze dne 25. října 1985 o metodách pro analýzu potravinářských kaseinů a kaseinátů (85/503/EHS) KOMISE EVROPSKÝCH
UTILIZATION OF OGU-INRA HYBRID SYSTEM IN WINTER RAPESEED BREEDING VYUŽITÍ HYBRIDNÍHO SYSTÉMU OGU-INRA PŘI ŠLECHTĚNÍ ŘEPKY OZIMÉ
 UTILIZATION OF OGU-INRA HYBRID SYSTEM IN WINTER RAPESEED BREEDING VYUŽITÍ HYBRIDNÍHO SYSTÉMU OGU-INRA PŘI ŠLECHTĚNÍ ŘEPKY OZIMÉ Koprna R. 1, Macháčková I. 2, Horáček J. 3, Ehrenbergerová J. 4 1 OSEVA PRO
UTILIZATION OF OGU-INRA HYBRID SYSTEM IN WINTER RAPESEED BREEDING VYUŽITÍ HYBRIDNÍHO SYSTÉMU OGU-INRA PŘI ŠLECHTĚNÍ ŘEPKY OZIMÉ Koprna R. 1, Macháčková I. 2, Horáček J. 3, Ehrenbergerová J. 4 1 OSEVA PRO
Kryokonzervace révy vinné
 Ing. Miloš Faltus, Ph.D. Ing. Renata Kotková RNDr. Alois Bilavčík, Ph.D. Ing. Jiří Zámečník, CSc. Kryokonzervace révy vinné CERTIFIKOVANÁ METODIKA Výzkumný ústav rostlinné výroby, v.v.i. 2012 Metodika
Ing. Miloš Faltus, Ph.D. Ing. Renata Kotková RNDr. Alois Bilavčík, Ph.D. Ing. Jiří Zámečník, CSc. Kryokonzervace révy vinné CERTIFIKOVANÁ METODIKA Výzkumný ústav rostlinné výroby, v.v.i. 2012 Metodika
ÚLOHA C Klonování PCR produktu do plasmidu
 Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
Jméno a učo: Datum: ÚLOHA C Klonování PCR produktu do plasmidu TEORETICKÝ ÚVOD Při klonování PCR produktů do plasmidů se využívá vlastnosti Taq polymerasy, a jiných non-proofreading polymeras, přidávat
5. Bioreaktory. Schematicky jsou jednotlivé typy bioreaktorů znázorněny na obr. 5.1. Nejpoužívanějšími bioreaktory jsou míchací tanky.
 5. Bioreaktory Bioreaktor (fermentor) je nejdůležitější částí výrobní linky biotechnologického procesu. Jde o nádobu různého objemu, ve které probíhá biologický proces. Dochází zde k růstu buněk a tvorbě
5. Bioreaktory Bioreaktor (fermentor) je nejdůležitější částí výrobní linky biotechnologického procesu. Jde o nádobu různého objemu, ve které probíhá biologický proces. Dochází zde k růstu buněk a tvorbě
S filtračními papíry a membránou je nutno manipulovat pinzetou s tupým koncem.
 Western Blotting Příprava blotovacího sendviče... 1 Blotování... 2 Kontrola přenesení proteinů na membránu... 2 Blokování membrány... 2 Aplikace protilátek... 2 Vizualizace... 3 Vyvolání filmu... 4 Chemikálie
Western Blotting Příprava blotovacího sendviče... 1 Blotování... 2 Kontrola přenesení proteinů na membránu... 2 Blokování membrány... 2 Aplikace protilátek... 2 Vizualizace... 3 Vyvolání filmu... 4 Chemikálie
IZOLACE DNA POMOCÍ CTAB PRO STANOVENÍ GMO METODOU PCR
 1253.1 Izolace DNA pomocí CTAB pro stanovení GMO Strana 1 IZOLACE DNA POMOCÍ CTAB PRO STANOVENÍ GMO METODOU PCR 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorků krmiv
1253.1 Izolace DNA pomocí CTAB pro stanovení GMO Strana 1 IZOLACE DNA POMOCÍ CTAB PRO STANOVENÍ GMO METODOU PCR 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorků krmiv
Jednotné pracovní postupy zkoušení krmiv STANOVENÍ OBSAHU MYKOTOXINŮ METODOU HPLC - OCHRATOXIN A
 Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU HPLC - OCHRATOXIN A 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení ochratoxinu A v krmivech. 1 Ochratoxin A patří mezi
Národní referenční laboratoř Strana 1 STANOVENÍ OBSAHU MYKOTOXINŮ METODOU HPLC - OCHRATOXIN A 1 Rozsah a účel Metoda specifikuje podmínky pro stanovení ochratoxinu A v krmivech. 1 Ochratoxin A patří mezi
Cvičení ke kurzu Obecná ekotoxikologie. Úloha A - Stanovení ekotoxicity v testu klíčení rostlin
 Cvičení ke kurzu Obecná ekotoxikologie Nutné potřeby, které studenti přinesou s sebou do cvičení: - Tento návod - Poznámkový sešit, psací potřeby - Nůžky - Pravítko (s milimetrovým rozlišením) - Přezůvky
Cvičení ke kurzu Obecná ekotoxikologie Nutné potřeby, které studenti přinesou s sebou do cvičení: - Tento návod - Poznámkový sešit, psací potřeby - Nůžky - Pravítko (s milimetrovým rozlišením) - Přezůvky
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 10 Bílkoviny Pro potřeby projektu
IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT NUCLEOSPIN FOOD)
 1252.1 Izolace DNA pro stanovení GMO metodou Strana 1 IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT NUCLEOSPIN FOOD) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku
1252.1 Izolace DNA pro stanovení GMO metodou Strana 1 IZOLACE DNA PRO STANOVENÍ GMO METODOU PCR (KIT NUCLEOSPIN FOOD) 1 Účel a rozsah Postup slouží k získání deoxyribonukleové kyseliny (DNA) ze vzorku
Aktuální situace v oblasti ekologických osiv v ČR. Ing. Petr KONVALINA, Ph.D. Jihočeská univerzita v Českých Budějovicích
 Aktuální situace v oblasti Ing. Petr KONVALINA, Ph.D. Jihočeská univerzita v Českých Budějovicích Úvod: Ekologické zemědělství v ČR (31.12.2010) 3 517 registrovaných podniků 448 202 ha zemědělské půdy
Aktuální situace v oblasti Ing. Petr KONVALINA, Ph.D. Jihočeská univerzita v Českých Budějovicích Úvod: Ekologické zemědělství v ČR (31.12.2010) 3 517 registrovaných podniků 448 202 ha zemědělské půdy
ANALÝZA EXTRAKTU PODLE MEHLICHA 3 METODOU ICP-OES
 30074. Analýza extraktu podle Mehlicha 3 Strana ANALÝZA EXTRAKTU PODLE MEHLICHA 3 METODOU ICP-OES Účel a rozsah Postup je určen především pro stanovení obsahu základních živin vápníku, hořčíku, draslíku,
30074. Analýza extraktu podle Mehlicha 3 Strana ANALÝZA EXTRAKTU PODLE MEHLICHA 3 METODOU ICP-OES Účel a rozsah Postup je určen především pro stanovení obsahu základních živin vápníku, hořčíku, draslíku,
VETERINÁRNÍ A FARMACEUTICKÁ UNIVERZITA BRNO FAKULTA VETERINÁRNÍ HYGIENY A EKOLOGIE ÚSTAV EKOLOGIE A CHOROB ZVĚŘE, RYB A VČEL
 VETERINÁRNÍ A FARMACEUTICKÁ UNIVERZITA BRNO FAKULTA VETERINÁRNÍ HYGIENY A EKOLOGIE ÚSTAV EKOLOGIE A CHOROB ZVĚŘE, RYB A VČEL Standardní operační postup - SOP 02 Terestrické testy ekotoxicity Stanovení
VETERINÁRNÍ A FARMACEUTICKÁ UNIVERZITA BRNO FAKULTA VETERINÁRNÍ HYGIENY A EKOLOGIE ÚSTAV EKOLOGIE A CHOROB ZVĚŘE, RYB A VČEL Standardní operační postup - SOP 02 Terestrické testy ekotoxicity Stanovení
MagPurix Forensic DNA Extraction Kit
 MagPurix Forensic DNA Extraction Kit Kat. č. ZP02010 Doba zpracování: 40-50 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Forensic DNA Extraction Kit je určena pro izolátor
MagPurix Forensic DNA Extraction Kit Kat. č. ZP02010 Doba zpracování: 40-50 minut pro MagPurix 12S 40-60 minut pro MagPurix 24 Použití Souprava MagPurix Forensic DNA Extraction Kit je určena pro izolátor
N217019 - Laboratoř hydrobiologie a mikrobiologie
 ÚSTAV TECHNOLOGIE VODY A PROSTŘEDÍ N217019 - Laboratoř hydrobiologie a mikrobiologie Název úlohy: Kultivační stanovení: Stanovení kultivovatelných mikroorganismů při 22 C a 36 C Vypracováno v rámci projektu:
ÚSTAV TECHNOLOGIE VODY A PROSTŘEDÍ N217019 - Laboratoř hydrobiologie a mikrobiologie Název úlohy: Kultivační stanovení: Stanovení kultivovatelných mikroorganismů při 22 C a 36 C Vypracováno v rámci projektu:
