pre 7. roèník základných škôl a 2. roèník gymnázií s osemroèným štúdiom
|
|
|
- Hana Křížová
- před 8 lety
- Počet zobrazení:
Transkript
1 pre 7. roèník základných škôl a 2. roèník gymnázií s osemroèným štúdiom
2 26 1 Spoznávame chemické reakcie v našom okolí 1.3 Chemické zlučovanie a chemický rozklad Chemické zlučovanie Čo budeme skúmať? Vlastnosti síry a železa a ich vzájomnú reakciu. Pomôcky a chemikálie: 1. roztieračka s roztieradlom 2. skúmavka 3. držiak na skúmavku 4. laboratórna lyžička 5. kahan 6. magnet 7. Petriho miska 8. prášková síra 9. práškové železo (ďalšie pomôcky: laboratórne váhy, navažovačka, zápalky, kladivo, papier) Čo budeme potrebovať? Poznámka: Pokus robí učiteľ v digestore. Ako budeme postupovať? 1. Do tabuľky na s. 27 doplníme údaje z pozorovania vlastností síry a železa. 2. 3,2 g síry a 5,6 g železa premiešame a rozotrieme v roztieračke. Získanú zmes rozdelíme na dve časti. 3. Jednu časť zmesi vysypeme do skúmavky a zahrievame. Keď sa zmes na jednom mieste rozžeraví, kahan odložíme a pozorujeme priebeh reakcie. 4. Látku v skúmavke necháme po skončení reakcie vychladnúť. Skúmavku obalíme papierom a produkt z nej získame rozbitím skúmavky kladivom. 5. Druhú časť zmesi vysypeme na Petriho misku a odložíme na porovnanie. 6. Porovnáme vlastnosti zmesi, ktorá vznikla premiešaním síry a železa, a vlastnosti látky, ktorá vznikla po zahriatí. 7. Do tabuľky na s. 27 doplníme ďalšie zistené údaje. Látku vzniknutú zahrievaním síry a železa magnet nepriťahuje. zahrievanie síry a železa prebiehajúca reakcia (bez zahrievania)
3 1 Spoznávame chemické reakcie v našom okolí 27 Z druhej časti zmesi (bod 5) magnet priťahuje práškové železo. Síra je žltá tuhá látka. Podľa gréckeho básnika Homéra ju kňazi spaľovali pri náboženských obradoch. Bola aj súčasťou gréckeho ohňa, ktorý vrhali Turci na ruských vojakov pri obliehaní Carihradu. druhá časť zmesi Čo sme pozorovali? Síra a železo spolu reagovali po zahriatí. Keď sa zmes rozžeravila, reakcia prebiehala ďalej aj bez zahrievania. Vzniknutú látku sme získali rozbitím skúmavky. Tabuľka: síra železo zmes po premiešaní zmes po zahriatí sfarbenie vzhľad magnetické vlastnosti (áno/nie) Vysvetlenie: Zahriatím síry a železa vznikla chemická látka, ktorá má iné vlastnosti, ako mali pôvodné chemické látky. Prebehol teda chemický dej vznikla nová chemická látka. Pri uvedenej chemickej reakcii vznikol z dvoch reaktantov jeden produkt. Takúto chemickú reakciu nazývame chemické zlučovanie. Zlučovaním dvoch odlišných chemických látok vznikla nová chemická látka chemická zlúčenina. Prášková síra Síra je základnou surovinou napr. pri výrobe kyseliny sírovej. Používa sa aj pri výrobe gumy, je súčasťou liekov proti kožným ochoreniam a pod. Horením síry vzniká jedovatá zlúčenina oxid siričitý, ktorý má dezinfekčné účinky. Túto vlastnosť využívajú vinári na sírenie sudov a pivníc proti plesniam. Síru obsahujú aj prípravky na ničenie rastlinných škodcov. Železo je lesklý kov, ktorý má magnetické vlastnosti. Jeho lesk sa však na vzduchu postupne stráca (hrdzavenie). Ľudia ho poznali už v praveku. Je najpoužívanejším kovom v súčasnosti. O chemické zlučovanie ide aj v prípade reakcie železa s kyslíkom zo vzduchu a s vodou, ktorú nazývame hrdzavenie. Táto reakcia spôsobuje veľké škody na železných predmetoch. Chemické zlučovanie je chemická reakcia, pri ktorej z dvoch alebo viacerých jednoduchších reaktantov vzniká jeden zložitejší produkt. R1 + R P reaktanty produkt reaktant reaktant produkt Práškové železo Chemické zlučovanie železa so sírou zapíšeme chemickou rovnicou: Fe + S FeS železo+síra sulfid železnatý reaktanty produkt
4 28 1 Spoznávame chemické reakcie v našom okolí Chemický rozklad Čo budeme skúmať? Vlastnosti hypermangánu a jeho správanie pri zahrievaní. Pomôcky a chemikálie: Čo budeme potrebovať? 1. laboratórna lyžička 2. kahan 3. skúmavka 4. držiak na skúmavku 5. drevená špajdľa 6. hypermangán (ďalšie pomôcky: Petriho miska, zápalky) Ako budeme postupovať? 1. Do skúmavky nasypeme polovicu lyžičky hypermangánu a skúmavku zahrievame. 2. Súčasne zapálime špajdľu, necháme ju rozžeraviť a sfúkneme plameň. Tlejúcu špajdľu vložíme do skúmavky. 3. Skúmavku zahrievame a opakujeme vkladanie špajdle, až kým sa hypermangán úplne nerozloží. Zistíme to tak, že špajdľa sa už nerozhorí. Skúmavku ešte zahrievame asi 1 minútu a pozorujeme. 4. Po ochladnutí skúmavky vysypeme vzniknutú látku na Petriho misku a porovnáme jej sfarbenie a vzhľad so sfarbením a vzhľadom hypermangánu. 5. Doplníme tabuľku na s. 29. zahrievanie hypermangánu tlejúca špajdľa rozhorenie tlejúcej špajdle
5 1 Spoznávame chemické reakcie v našom okolí 29 Čo sme pozorovali? Počas zahrievania kryštáliky hypermangánu praskali a v skúmavke vznikala biela hmla. Tlejúca špajdľa sa po vložení do skúmavky rozhorela. Špajdľu sme sfúkli, opakovane sme ju vkladali do skúmavky a pozorovali jej rozhorenie. Keď sa už nerozhorela, zahrievali sme skúmavku ešte asi 1 minútu. Potom sme pokus skončili. Hypermangán je tuhá látka, ktorá tvorí tmavofialové kryštály. Jej chemický názov je manganistan draselný. Používa sa v lekárstve na dezinfekciu pri ochoreniach kože. Tabuľka: hypermangán tuhá látka vzniknutá zahrievaním sfarbenie vzhľad správanie pri zahrievaní Vysvetlenie: V skúmavke prebiehala chemická reakcia rozklad hypermangánu. Kyslík, ktorý vznikol rozkladom hypermangánu, spôsobil rozhorenie tlejúcej špajdle. Špajdľa sa opakovane rozhorela dovtedy, kým sa uvoľňoval kyslík. Keď rozklad hypermangánu skončil, nevznikal kyslík a špajdľa sa už nerozhorela. Kyslík bol jedným z produktov rozkladu hypermangánu. Tuhá látka v skúmavke sa ďalším zahrievaním už nemenila. Tuhá látka, ktorú sme získali v skúmavke ako ďalší produkt, sa sfarbením aj vzhľadom odlišuje od reaktantu hypermangánu. Je to teda iná chemická látka. Chemickou reakciou vzniklo z jedného reaktantu viac produktov. Takúto chemickú reakciu nazývame chemický rozklad. V laboratóriu sa kyslík často pripravuje rozkladom peroxidu vodíka. Jeho rozkladom vzniká kyslík a voda. Významnou reakciou je chemický rozklad vápenca. Vápenec sa zahrievaním rozkladá na pálené vápno a oxid uhličitý. Pálené vápno sa používa napr. v stavebníctve. Kryštály hypermangánu Produkt získaný zahrievaním hypermangánu Kyslík možno v laboratóriu pripraviť nielen rozkladom hypermangánu, ale aj rozkladom iných zlúčenín. Prípravu kyslíka rozkladom peroxidu vodíka si prakticky vyskúšate na laboratórnej práci. Chemický rozklad je chemická reakcia, pri ktorej z jedného zložitejšieho reaktantu vznikajú dva alebo viac jednoduchších produktov. R P1 + P reaktant produkty reaktant produkt produkt Chemický rozklad peroxidu vodíka zapíšeme chemickou rovnicou: 2H 2 O 2 2H 2 O + O 2 peroxid vodíka voda+kyslík reaktant produkty
6 30 1 Spoznávame chemické reakcie v našom okolí Premýšľame a objavujeme Po skončení pokusu s rozkladom hypermangánu (s. 28) urobte ešte tento jednoduchý, no zaujímavý pokus: Do vysokého odmerného valca s vodou pomaly nasypte tuhý zvyšok (produkt), ktorý vznikol v skúmavke rozkladom hypermangánu. Pozorujte oproti dennému svetlu. Opíšte farebné zmeny v odmernom valci. Pokúste sa vysvetliť, čím môžu byť pozorované zmeny spôsobené. Na obrázkoch je priebeh tohto pokusu. na začiatku asi po 3 sekundách asi po 6 sekundách asi po 5 minútach Otázky a úlohy 1. Doplňte text a napíšte si ho do zošita. a)... je chemická reakcia, pri ktorej z jedného zložitejšieho reaktantu vznikajú dva alebo viac jednoduchších produktov. Napr.:.... b)... je chemická reakcia, pri ktorej z dvoch alebo viacerých jednoduchších reaktantov vzniká jeden zložitejší produkt. Napr.: Zahrievaním uhličitanu meďnatého vznikol oxid uhličitý a oxid meďnatý. A B + C Podľa opisu reakcie namiesto písmen A, B, C doplňte do schémy správne názvy látok. Uveďte, či je táto chemická reakcia chemické zlučovanie alebo chemický rozklad. 3. Reakcia horčíka so vzdušným kyslíkom, ktorú ste už pozorovali, je chemické zlučovanie alebo chemický rozklad? Zdôvodnite.
7 1 Spoznávame chemické reakcie v našom okolí Pozorne si prezrite obrázky a pomocou nich opíšte danú chemickú reakciu. Do tabuľky zaznačte reaktanty, produkty a ich vlastnosti, ktoré môžete z obrázkov zistiť. Spomeňte si, či ste sa na vyučovacej hodine chémie s niektorou z látok už stretli, a využite aj tieto informácie. Uveďte, či reakcia je chemické zlučovanie alebo chemický rozklad, a svoje tvrdenie zdôvodnite. práškový zinok prášková síra zmes práškového zinku a práškovej síry horenie zmesi zinku a síry produkt vzniknutý horením zinku a síry 5. Sóda bikarbóna je biela tuhá látka. Používa sa napr. pri žalúdočných ťažkostiach, v kypriacom prášku do pečiva, na čistenie kovových predmetov, čistenie škvŕn, do pracích prostriedkov na zmäkčovanie vody. a) Zistite, aký je jej chemický názov. b) Pri pečení pridávame do cesta kypriaci prášok. Jeho pôsobením cesto zväčší svoj objem, stáva sa ľahkým, vláčnym a čo je najdôležitejšie chutným. Pri pečení dochádza k tepelnému rozkladu sódy bikarbóny. Zdvihnutie cesta spôsobuje plyn, ktorý je jedným z produktov rozkladu. Zistite názov tohto plynu. c) Prezrite si etikety kypriacich práškov a zistite, ktoré zložky obsahujú.
8 32 1 Spoznávame chemické reakcie v našom okolí 1.4 Horenie Čo je horenie? Jánsky oheň V slovanskej kultúre je známy zvyk spojený s posvätnosťou ohňa jánske ohne. Na oslavu letného slnovratu sa rozkladali 4 vatry na všetky svetové strany. Ten, koho oheň nepopálil pri preskakovaní, bol duchovne čistý. Slovania využívali oheň na liečenie, veštenie a čarovanie. Téma ohňa nechýba ani v ľudových rozprávkach, povestiach a piesňach. Napríklad v rozprávke O dvanástich mesiačikoch sedia dvanásti mesiačikovia okolo vatry a pozerajú do ohňa. Väčšina pracovných postupov chemikov v minulosti závisela od účinku ohňa. Pred vyše 300 rokmi nemecký lekár a chemik G. E. Stahl vyslovil predstavu, že látka, ktorá je schopná horieť, obsahuje flogiston. Ten pri horení vyprchá a zostane iba popol. Tento názor pretrvával v chémii takmer celé jedno storočie. Oheň ľudí odpradávna priťahoval. Jeho pôvod a príčinu si však dlho nevedeli vysvetliť. Podľa starej gréckej báje ukradol oheň bohom z Olympu Prometeus a dal ho ľuďom. Už v praveku ľudia vedeli pomocou ohňa pripravovať jedlo. Oheň získavali z horiacich stromov, ktoré zapálil blesk. Niektoré látky začnú horieť hneď po vložení do plameňa. Napríklad papier sa v plameni ihneď zapáli a zostane po ňom sivobiely popol. Ďalším produktom je bezfarebný plyn oxid uhličitý. Ak priblížime horiacu zápalku k porcelánovej miske, v ktorej je malé množstvo etanolu, etanol začne horieť už v okamihu, keď sa ešte horiaca zápalka nedotkla hladiny etanolu. Nezostane po ňom tuhý zvyšok, lebo vzniknuté produkty vodná para a oxid uhličitý sú plynné látky. Na obrázku vidieť, ako horí zemný plyn, ktorý používame v domácnostiach na varenie. Spaľuje sa bez vzniku sadzí, vzniknuté produkty sú oxid uhličitý a vodná para. Pokusom sme zistili, že horčík sa krátko po vložení do plameňa zapálil a zhorel. Produktom tejto reakcie je oxid horečnatý biela tuhá látka (s. 20). G. E. Stahl Túto predstavu vyvrátil v druhej polovici 18. storočia významný francúzsky vedec A. L. Lavoisier. Vysvetlil podstatu horenia ako prudké zlučovanie látok s kyslíkom a potvrdil, že kyslík je zložkou vzduchu. Je nevyhnutný na dýchanie organizmov. Lavoisier pokusmi zistil, že po spálení kovu vznikla látka, ktorá mala väčšiu hmotnosť o zlúčený kyslík. Požiar ropných vrtov môže spôsobiť ekologickú katastrofu. Okrem oxidu uhličitého a vody vzniká pri tomto horení ešte množstvo škodlivých produktov. Pri horení papiera, etanolu, zemného plynu, horčíka a ropy bol druhým reaktantom kyslík zo vzduchu. Látky sa zmenili na iné látky horenie je chemická reakcia.
9 1 Spoznávame chemické reakcie v našom okolí 33 Horľavá látka začne horieť teda reagovať so vzdušným kyslíkom, ak sa zahreje na určitú teplotu. Táto teplota sa nazýva zápalná teplota. Značka horľaviny Na horenie musia byť splnené tri podmienky: 1. Prítomnosť horľavej látky Horľavá látka je látka, ktorá reaguje s kyslíkom, pričom vzniká plameň. Plameň je stĺpec horiacich, väčšinou plynných látok. 2. Prítomnosť kyslíka Kyslík reaguje s horľavými látkami, pričom vzniká svetlo a teplo. Látka horí vtedy, ak má k nej prístup kyslík. Zvyčajne je to kyslík zo vzduchu. 3. Zahriatie látky na zápalnú teplotu Zápalná teplota je teplota, pri ktorej sa látka zapáli. Pri dosiahnutí zápalnej teploty sa látka môže rozkladať na plynné produkty alebo vyparovať. Možno ju dosiahnuť napr. plameňom, iskrou, teplom vzniknutým pri chemickej reakcii alebo pri trení. Čím je zápalná teplota nižšia, tým je látka nebezpečnejšia z hľadiska vzniku požiaru. Pre skladovanie a prácu s horľavinami platia zvláštne bezpečnostné predpisy. Horľaviny musia byť výrazne označené. Aj pary horľavín sú ľahko zápalné a horľavé, so vzduchom tvoria výbušnú zmes. Benzín, etanol a iné horľavé kvapaliny možno v uzavretých miestnostiach skladovať iba v malých množstvách a v dobre uzavretých nádobách. Miestnosti musia byť dobre vetrané. V blízkosti horľavín sa nesmie pracovať s otvoreným ohňom (stačí iskra z cigarety, zapaľovača alebo zlého elektrického vypínača). Napríklad na benzínových čerpacích staniciach je prísny zákaz fajčiť. Na mieste uskladnenia horľavín musí byť vždy umiestnený hasiaci prístroj. Veľmi nebezpečné sú horľavé plyny, ktoré vytvárajú so vzduchom výbušné plynné zmesi, napr. vodík, metán, acetylén. Medzi horľavé látky patria aj plasty. Látky môžu horieť aj vtedy, ak namiesto kyslíka je prítomná iná látka podporujúca horenie. Napríklad rozžeravený sodík prudko zhorí po vložení do plynného chlóru. Produktom reakcie je chlorid sodný. Sú aj horľaviny, ktoré sa samovoľne vznietia so vzdušným kyslíkom už pri nízkych teplotách (napr. biely fosfor). Zápalná teplota niektorých hor ľavín: Horľavá látka Zápalná teplota ( C) hlavička zápalky 60 benzín 220 suché drevo etanol 425 papier 440 uhlie zemný plyn 650 koks Horenie je chemická reakcia, pri ktorej sa uvoľňuje svetlo a teplo. Látky sa pri horení zlučujú so vzdušným kyslíkom. Horenie niektorých látok pozorujeme ako výbuch
10 34 1 Spoznávame chemické reakcie v našom okolí Skúmanie horenia Čo budeme skúmať? Horenie etanolu I. Pomôcky a chemikálie: 1. porcelánová miska 2. nehorľavá podložka (môžeme použiť aj kovovú sieťku s keramickou vložkou) 3. etanol (ďalšie pomôcky: zápalky) Čo budeme potrebovať? Ako budeme postupovať? 1. Porcelánovú misku položíme na nehorľavú podložku a nalejeme do nej trochu etanolu. 2. Opatrne priložíme horiacu zápalku, sfúkneme zápalku a pozorujeme. Čo sme pozorovali? Etanol sa po priložení horiacej zápalky zapálil. Začal horieť už v okamihu, keď sme sa ešte horiacou zápalkou nedotkli jeho hladiny. Vysvetlenie: Pary etanolu v zmesi so vzdušným kyslíkom začali horieť, lebo sme etanol zahriali horiacou zápalkou na zápalnú teplotu.
11 1 Spoznávame chemické reakcie v našom okolí 35 Čo budeme skúmať? Horenie etanolu II. Čo budeme potrebovať? Pomôcky a chemikálie: 1. porcelánová miska 2. laboratórna lyžička 3. 2 pipety 4. nehorľavá podložka (môžeme použiť aj kovovú sieťku s keramickou vložkou) 5. hypermangán 6. kyselina sírová (koncentrovaná) 7. etanol Poznámka: Pokus robí učiteľ v digestore. 6 7 Ako budeme postupovať? 1. Lyžičku hypermangánu premiešame v porcelánovej miske s niekoľkými kvapkami kyseliny sírovej. 2. Opatrne pipetou pridáme 3 5 kvapiek etanolu a pozorujeme. Čo sme pozorovali? Zmes hypermangánu a kyseliny sírovej sa pridaním etanolu zapálila a prudko zhorela. Vysvetlenie: Pri pokuse boli reaktantmi etanol, hypermangán a kyselina sírová. Po zapálení etanolu sa stal reaktantom aj vzdušný kyslík. Etanol sa zahrial na zápalnú teplotu teplom, ktoré sa uvoľnilo pri chemickej reakcii.
12 36 1 Spoznávame chemické reakcie v našom okolí Priebeh požiaru môžeme rozdeliť na štyri fázy: Prvá fáza: je od vzniku požiaru do začiatku intenzívneho horenia. Trvá 3 až 10 minút. V tejto fáze je najväčšia šanca uhasiť požiar. Z časového intervalu prvej fázy vyplýva, aké dôležité je rýchle nahlásenie požiaru. Druhá fáza: je od začiatku intenzívneho horenia až do okamihu, keď požiar zachváti všetky horľavé materiály. Požiar je v maximálnej intenzite, jeho hasenie je veľmi náročné. Tretia fáza: nastáva, keď intenzita požiaru sa začína znižovať. Štvrtá fáza: dochádza k prerušeniu procesu horenia. Ako zavčasu spozorovať požiar, keď ľudia spia? Od včasného spozorovania požiaru závisí záchrana ľudí a možnosť zahasiť požiar. Požiar zvyčajne spozorujú ľudia, ktorí sú v budove pri jeho vzniku. Požiar však môže vzniknúť aj v čase, keď v budove nikto nie je, alebo v noci, keď ľudia spia. Niektoré budovy sú preto vybavené elektrickou požiarnou signalizáciou so samočinnými hlásičmi požiaru, ktoré reagujú na dym, teplo a žiarenie ohňa. Z hlásiča sa signál dostane do ústredne, ktorá odošle impulz na vyhlásenie poplachu, môže ho odoslať priamo hasičskému útvaru a pod. Sú aj také hasiace zariadenia, ktoré reagujú na teplo a samočinne začnú hasiť vzniknutý požiar. Nazývajú sa stabilné hasiace zariadenia. Automatický detektor ohňa Požiar a jeho hasenie Požiar je každé nežiaduce horenie, pri ktorom môže dôjsť k zraneniu osôb alebo zvierat, prípadne až k usmrteniu alebo materiálnym škodám. Za požiar sa považuje aj nežiaduce horenie, pri ktorom sú osoby, zvieratá, majetok alebo životné prostredie priamo ohrozené. Hasenie požiaru: 1. Odstránenie horľavej látky Tento spôsob sa využíva najmä pri rozsiahlych lesných požiaroch. Pri ich hasení sa robia široké prieseky, na ktorých oheň zhasne, čím sa zabráni ďalšiemu šíreniu ohňa. 2. Zabránenie prístupu vzdušného kyslíka Prístupu vzdušného kyslíka účinne zabraňuje oxid uhličitý, ktorým sú naplnené snehové hasiace prístroje. Keďže má väčšiu hustotu ako vzduch, vytvorí nad ohniskom vrstvu, ktorá bráni prístupu vzdušného kyslíka. Sneh je tvorený tuhým oxidom uhličitým, ktorý má veľmi nízku teplotu (približne 70 C). Horiaca látka sa teda hasí nielen zabránením prístupu vzdušného kyslíka, ale aj jej ochladením. Na zabránenie prístupu kyslíka sa používajú aj penové alebo práškové hasiace prístroje, ale ak ich nemáme, povrch horiacej látky zasypeme pieskom, hlinou, prikryjeme dekou a pod. 3. Ochladenie látky pod zápalnú teplotu Najbežnejším hasiacim prostriedkom je voda. Ochladí horiaci predmet pod jeho zápalnú teplotu. Okrem toho voda a vodná para zabraňujú aj prístupu vzduchu. Voda sa nesmie použiť na hasenie zariadení pod elektrickým napätím, lebo voda vedie elektrický prúd a tým by bol ohrozený život hasičov. Vodou sa nesmie hasiť ani horiaci benzín, nafta, oleje a náterové látky. Všetky tieto látky majú menšiu hustotu ako voda. Keďže pri horení sú horúce, pri poliatí vodou by došlo k ich prudkému prskaniu.
13 1 Spoznávame chemické reakcie v našom okolí Čo treba robiť v prípade požiaru? Nepodľahnúť panike, zachovať pokoj! V prípade, že je požiar veľký a jeho hasenie nezvládneme vlastnými silami, ihneď zavoláme hasičov. 112 Dospelý človek rýchlo, ale rozvážne vyhodnotí vzniknutú situáciu: kde je ohnisko požiaru kde a čo horí, ktorým smerom a na čo sa môže oheň rozšíriť, aký veľký je požiar a či ho dokáže uhasiť prostriedkami, ktoré má k dispozícii hasiace prístroje, voda, lopata, piesok a pod., kto je v ohrozenom priestore okrem neho. Deti sa majú usilovať čím skôr opustiť horiaci priestor a hneď hlásiť požiar dospelej osobe alebo zavolať hasičom. Nikdy sa nesmú schovávať do inej miestnosti, odkiaľ nie je východ von! Jedovatý dym sa po krátkom čase rozšíri všade. Čo je hlavnou príčinou vzniku požiarov? Zakladanie ohnísk v blízkosti lesa alebo priamo v lese. Vypaľovanie suchej trávy na jar. Hry detí so zápalkami doma, v pivniciach, v lese, v stohoch slamy alebo sena. Fajčenie v priestoroch, kde sa vyskytujú horľaviny. Poruchy na elektrických zariadeniach. Porušovanie zásad bezpečnosti pri práci a nedbalosť vo výrobných prevádzkach s veľkou prašnosťou, prípadne v takých prevádzkach, kde je veľa odpadov z dreva, papiera, textilu a iných horľavých látok. Úder blesku alebo elektrický výboj, napr. pri plastoch. evakuácia osôb Ak sa nachádzame v horiacej budove, z ktorej nemôžeme uniknúť, nikdy neotvárame dvere, ak sú kľučky horúce (na druhej strane dverí je otvorený oheň), a v žiadnom prípade nepoužívame výťah. Otvoríme okno a upozorňujeme na svoju prítomnosť volaním: Horí! alebo Pomoc! a mávaním dostatočne veľkým kusom bielej látky (aby nás ľahšie našli). Ukladanie horľavých látok v blízkosti komínov, vykurovacích telies alebo sušenie na nich. Žiaľ, niekedy aj úmyselné zapálenie. Požiar však tak či onak spôsobí väčšinou človek. Požiar je nežiaduce horenie. Pri jeho hasení treba odstrániť aspoň jednu z podmienok horenia: odstrániť horľavú látku, zabrániť prístupu vzdušného kyslíka alebo ochladiť horľavú látku pod zápalnú teplotu. Telefónne číslo, ktoré združuje hasičov, záchrannú zdravotnícku službu a políciu, je 112.
14 38 1 Spoznávame chemické reakcie v našom okolí Voda sa používala na hasenie požiaru už veľmi dávno. Vodu ľudia nosili vo vedrách a vylievali na oheň. S rozvojom spoločnosti sa ľudia organizovali do hasičských spolkov. V súčasnosti používajú hasiči cisternové hasičské striekačky s čerpadlami, hadicami a rôznymi prúdnicami. V roku 2009 uskutočnili hasiči na Slovensku vyše výjazdov. Čo robia hasiči, keď nehorí? Hasiči musia byť psychicky silní, telesne zdatní, odborne pripravení a v stálej pohotovosti vo dne aj v noci. Keď nehorí, zdokonaľujú svoje vedomosti, robia preventívne akcie, telesnú prípravu a cvičenia, kontrolnú činnosť, údržbu hasičskej techniky a pod. Hasiči zasahujú aj v iných nepredvídaných udalostiach, najmä pri dopravných nehodách, povodniach, pri úniku nebezpečných látok do pôdy, do vody alebo na iných miestach, kde by takéto látky spôsobili nebezpečenstvo požiaru, výbuchu, ohrozenie človeka a prírody. Pomôžu aj vtedy, keď treba zachrániť človeka vo veľkých výškach alebo aj pod vodou Hasiace látky Okrem najbežnejšej hasiacej látky vody, sa na hasenie používa aj piesok a rôzne typy hasiacich prístrojov. Druh hasiacej látky Čo hasiť? Čo nehasiť? voda najmä tuhé látky, ktoré s vodou nereagujú elektrické zariadenia pod napätím, benzín, oleje piesok menšie požiare, kde nemožno použiť jemnú mechaniku, elektroniku vodu vodný hasiaci prístroj voda najmä tuhé látky, ktoré s vodou nereagujú elektrické zariadenia pod napätím, benzín, oleje snehový hasiaci prístroj tuhé, kvapalné a plynné látky, elektrické práškové látky oxid uhličitý zariadenia pod napätím penový hasiaci prístroj tuhé a kvapalné látky elektrické zariadenia pod napätím oxid uhličitý, voda práškový hasiaci prístroj napr. oxid hlinitý tuhé, kvapalné a plynné látky, elektrické zariadenia pod napätím jemnú mechaniku, elektroniku, práškové látky Premýšľame a objavujeme Aký oheň hltajú hltači ohňa? Prečo sa nepopália? Prečo sa nepopáli kúzelník na obrázku?
15 1 Spoznávame chemické reakcie v našom okolí 39 Čo budeme skúmať? Model penového hasiaceho prístroja. Čo budeme potrebovať? Pomôcky a chemikálie: 1. odsávacia banka s dobre tesniacou zátkou 2. skúmavka 3. odmerný valec 4. saponát 5. sóda bikarbóna (nasýtený roztok) 6. kyselina sírová (zriedená 1 : 3) 1 2 H 2 SO 4 1 : 3 Poznámka: Pokus robí učiteľ nad umývadlom. 6 Ako budeme postupovať? 1. Do odsávacej banky nalejeme asi do tretiny objemu nasýtený roztok sódy bikarbóny. 2. Pridáme asi 2 ml saponátu. 3. Do banky vložíme skúmavku, do ktorej sme naliali asi 15 ml roztoku kyseliny sírovej. 4. Banku uzavrieme zátkou a nakloníme tak, aby sa oba roztoky premiešali. kyselina sírová sóda bikarbóna saponát premiešanie roztokov Čo sme pozorovali? Po zmiešaní roztokov v banke a v skúmavke sme pozorovali vznik peny, ktorá vystrekovala bočným otvorom banky. Vysvetlenie: Spenený obsah banky vytlačil bočným otvorom plyn, ktorý vznikol chemickou reakciou sódy bikarbóny a kyseliny sírovej. Týmto plynom bol oxid uhličitý.
16 40 1 Spoznávame chemické reakcie v našom okolí Otázky a úlohy 1. Charakterizujte, čo je horenie. 2. Vysvetlite, ktoré látky nazývame horľaviny. Uveďte aspoň dva príklady. 3. Z týchto látok vyberte horľaviny: a) papier, b) etanol, c) slama, d) sklo, e) nafta, f) voda, g) oxid uhličitý. 4. Ktorá z výstražných značiek označuje horľavinu? a) b) c) d) e) 5. Na horenie látky musia byť splnené tri podmienky. Uveďte, ktoré. 6. Uveďte, čo je požiar. 7. Pri hasení požiaru treba odstrániť horľavú látku, zabrániť prístupu vzdušného kyslíka k nej alebo ju ochladiť pod zápalnú teplotu. Rozhodnite, ktoré z týchto podmienok pri hasení požiaru spĺňa: a) voda, b) piesok, c) oxid uhličitý. 8. Opíšte, čo budete robiť, keď niekomu začnú horieť šaty. 9. V kuchyni pri vyprážaní vám začne horieť olej na panvici. Vysvetlite, ako by ste ho zahasili. 10. Voda vedie elektrický prúd. Uveďte, čo by sa stalo, keby sme hasili vodou elektrické zariadenia pod napätím. 11. Ktoré hasiace látky sa nemajú používať na hasenie jemnej mechaniky a elektroniky? 12. Vysvetlite, prečo ohrozuje svoj život človek, ktorý v uzavretej garáži nechá naštartovaný motor automobilu na benzínové palivo. 13. Zdôvodnite, prečo sa nesmú používať propán-butánové (a iné plynové) spotrebiče v uzavretom priestore. 14. Z poškodenej propán-butánovej fľaše unikal do miestnosti plyn, ktorý sa zmiešal so vzduchom. Vysvetlite, prečo nastal výbuch tejto zmesi až po zapálení zápalky v miestnosti. 15. Zistite, či je vo vašom okolí miesto, kde je zvýšené nebezpečenstvo vzniku požiaru. Je toto miesto označené? Ako?
17 1 Spoznávame chemické reakcie v našom okolí Prečítajte si správu z tlače. Vedeli by ste, ako sa správať, keby sa vo vašej škole stalo niečo podobné, ako opisuje správa z tlače? Vyriešte s ňou súvisiace otázky. V pondelok predpoludním vypukol v Nových Zámkoch požiar v budove bývalej elektrotechnickej školy. Mesto na niekoľko hodín zahalil hustý čierny dym. Plamene boli miestami vysoké až 5 metrov a z miesta požiaru sa valil hustý čierny dym. Pri zásahu boli ľahko zranení dvaja hasiči. (správa z tlače) a) Vymenujte látky v školskej triede, ktoré sú horľavé. b) Pri všeobecnom ohrození sa spúšťa varovný signál všeobecné ohrozenie, ktorý varuje pri ohrození alebo vzniku mimoriadnej udalosti, ako aj pri možnosti rozšírenia následkov mimoriadnej udalosti. Z možností vyberte správny tón sirén: b1) 2-minútový kolísavý tón sirén, b2) 6-minútový stály tón sirén, b3) 2-minútový stály tón sirén. c) Vysvetlite, čo je evakuácia. d) Opíšte spôsob evakuácie vo vašej škole. e) Spoločne prejdite po trase, ktorou pôjdete celá trieda zo školského chemického laboratória po vyhlásení signálu pre všeobecné ohrozenie v prípade požiaru. f) Zistite, kde máte v škole umiestnené hasiace prístroje a hasiace zariadenia, ktoré hasiace prístroje sú to a ako sú označené. g) V školskom chemickom laboratóriu začal horieť práškový horčík. Na stránke prípadne na inej stránke, vyhľadajte typ hasiaceho prístroja, ktorým horiaci práškový horčík môžeme hasiť. Ktorý hasiaci prístroj sa nesmie použiť na hasenie práškového horčíka? 17. Z látok uvedených v tabuľke vyberte látku, ktorá predstavuje najväčšie nebezpečenstvo z hľadiska vzniku požiaru. Svoj výber zdôvodnite. Horľavá látka Zápalná teplota ( C ) nafta 40 parafín 160 petrolej 38 asfalt 205 Tvoríme projekt Vypracujte projekt na tému Oheň dobrý sluha, ale zlý pán. Využite aj poznatky z úlohy 16.
Učebné osnovy CHÉMIA
 Názov predmetu CHÉMIA Vzdelávacia oblasť Človek a príroda Stupeň vzdelania ISCED 2 Dátum poslednej zmeny 5. 9. 2017 UO vypracovala Učebné osnovy CHÉMIA Ing. Jarmila Bohovicová Časová dotácia Ročník piaty
Názov predmetu CHÉMIA Vzdelávacia oblasť Človek a príroda Stupeň vzdelania ISCED 2 Dátum poslednej zmeny 5. 9. 2017 UO vypracovala Učebné osnovy CHÉMIA Ing. Jarmila Bohovicová Časová dotácia Ročník piaty
Informačný list 1. Čo je energia? Všetci potrebujeme energiu! Energia doma
 Informačný list 1 Čo je energia? Ľudia potrebujú energiu, aby sa mohli hrať a hýbať. Energiu získajú z jedla. Potrebuješ energiu, aby si mohol rásť. Dokonca aj keď spíš, potrebuješ energiu. Aj zvieratá
Informačný list 1 Čo je energia? Ľudia potrebujú energiu, aby sa mohli hrať a hýbať. Energiu získajú z jedla. Potrebuješ energiu, aby si mohol rásť. Dokonca aj keď spíš, potrebuješ energiu. Aj zvieratá
1.5 Spoločné a rozdielne vlastnosti kvapalín a plynov PL KEGA 130UK/2013
 Pokus (Lapitková et al., 2010, s. 30) Úloha: Zisti a porovnaj správanie vzduchu a vody v injekčných striekačkách, ak v nich zväčšíme priestor. Pomôcky: 2 injekčné striekačky s objemom 200 ml, hadička na
Pokus (Lapitková et al., 2010, s. 30) Úloha: Zisti a porovnaj správanie vzduchu a vody v injekčných striekačkách, ak v nich zväčšíme priestor. Pomôcky: 2 injekčné striekačky s objemom 200 ml, hadička na
Sú ažné úlohy Chemickej olympiády v kategórii C. Krajské kolo Zadanie teoretických úloh 2007/2008
 Sú ažné úlohy Chemickej olympiády v kategórii C Pre prvé ročníky stredných škôl Krajské kolo Zadanie teoretických úloh 2007/2008 Vydala IUVENTA v spolupráci so Slovenskou komisiou Chemickej olympiády v
Sú ažné úlohy Chemickej olympiády v kategórii C Pre prvé ročníky stredných škôl Krajské kolo Zadanie teoretických úloh 2007/2008 Vydala IUVENTA v spolupráci so Slovenskou komisiou Chemickej olympiády v
SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY
 SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 53. ročník, školský rok 2016/2017 Kategória C Krajské kolo TEORETICKÉ ÚLOHY ÚLOHY Z ANORGANICKEJ, VŠEOBECNEJ A ORGANICKEJ CHÉMIE Chemická olympiáda
SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 53. ročník, školský rok 2016/2017 Kategória C Krajské kolo TEORETICKÉ ÚLOHY ÚLOHY Z ANORGANICKEJ, VŠEOBECNEJ A ORGANICKEJ CHÉMIE Chemická olympiáda
Aktivizujúce úlohy k téme sacharidy
 Aktivizujúce úlohy k téme sacharidy Poznámky pre učiteľa Téma: Sacharidy Ciele: - charakterizovať vlastnosti, štruktúru, zloženie, využitie a výskyt sacharidov - popísať základné vlastnosti D-glukózy a
Aktivizujúce úlohy k téme sacharidy Poznámky pre učiteľa Téma: Sacharidy Ciele: - charakterizovať vlastnosti, štruktúru, zloženie, využitie a výskyt sacharidov - popísať základné vlastnosti D-glukózy a
Aktivizujúce úlohy k téme tuky
 Aktivizujúce úlohy k téme tuky Poznámky pre učiteľa Téma: Tuky Ciele: - charakterizovať lipidy z hľadiska výskytu, štruktúry, vlastností, významu a zastúpenia vo výžive človeka - charakterizovať výskyt
Aktivizujúce úlohy k téme tuky Poznámky pre učiteľa Téma: Tuky Ciele: - charakterizovať lipidy z hľadiska výskytu, štruktúry, vlastností, významu a zastúpenia vo výžive človeka - charakterizovať výskyt
Tematický výchovno-vzdelávací plán z predmetu chémia pre 7. ročník
 Tematický výchovno-vzdelávací plán z predmetu chémia pre 7. ročník Stupeň vzdelania: ISCED 2 nižšie sekundárne vzdelávanie Vzdelávacia oblasť: Človek a príroda Predmet: Chémia Ročník: siedmy Počet hodín:
Tematický výchovno-vzdelávací plán z predmetu chémia pre 7. ročník Stupeň vzdelania: ISCED 2 nižšie sekundárne vzdelávanie Vzdelávacia oblasť: Človek a príroda Predmet: Chémia Ročník: siedmy Počet hodín:
Tematický výchovno-vzdelávací plán z chémie pre 7. ročník
 Tematický výchovno-vzdelávací plán z chémie pre 7. ročník Vypracované podľa učebných osnov školského vzdelávacieho programu schválených radou školy dňa 28.8.2008 s platnosťou od 1.9.2008 inovovaných k
Tematický výchovno-vzdelávací plán z chémie pre 7. ročník Vypracované podľa učebných osnov školského vzdelávacieho programu schválených radou školy dňa 28.8.2008 s platnosťou od 1.9.2008 inovovaných k
Nebezpečné látky a ich rozdelenie
 ADR delenie tovarov Nebezpečné látky sú všetky látky alebo substancie, ktoré môžu nebezpečne pôsobiť alebo ohrozovať zdravie alebo život ľudí, ich majetok a v neposlednom rade životné prostredie. Nebezpečné
ADR delenie tovarov Nebezpečné látky sú všetky látky alebo substancie, ktoré môžu nebezpečne pôsobiť alebo ohrozovať zdravie alebo život ľudí, ich majetok a v neposlednom rade životné prostredie. Nebezpečné
SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY
 SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 50. ročník, školský rok 2013/2014 Kategória C Školské kolo TEORETICKÉ ÚLOHY ÚLOHY ŠKOLSKÉHO KOLA Chemická olympiáda kategória C 50. ročník školský
SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 50. ročník, školský rok 2013/2014 Kategória C Školské kolo TEORETICKÉ ÚLOHY ÚLOHY ŠKOLSKÉHO KOLA Chemická olympiáda kategória C 50. ročník školský
Globálny chemický experiment IYC Solárny destilátor
 Globálny chemický experiment IYC 2011 Solárny destilátor Tento dokument obsahuje popis pre aktivitu Solárny destilátor, ktorá je časťou Globálneho chemického experimentu pri príležitosti Medzinárodného
Globálny chemický experiment IYC 2011 Solárny destilátor Tento dokument obsahuje popis pre aktivitu Solárny destilátor, ktorá je časťou Globálneho chemického experimentu pri príležitosti Medzinárodného
Všeobecne záväzné nariadenie Mesta Trenčianske Teplice č. x/2016 o používaní pyrotechnických výrobkov na území mesta Trenčianske Teplice
 Dôvodová správa S účinnosťou k 2.12.2015 došlo k zmene zákona č. 58/2014 Z. z. o výbušninách, výbušných predmetoch a munícii a o zmene a doplnení niektorých zákonov v znení neskorších predpisov, ktorý
Dôvodová správa S účinnosťou k 2.12.2015 došlo k zmene zákona č. 58/2014 Z. z. o výbušninách, výbušných predmetoch a munícii a o zmene a doplnení niektorých zákonov v znení neskorších predpisov, ktorý
Laboratórne cvičenie č. 6
 Laboratórne cvičenie č. 6 Dátum: 24.04.2015 Meno: Katarína Zdráhalová Téma: Bielkoviny Spolupracovníci: Filip Kubus Úlohy: 1. Dôkaz bielkovín vo vaječnom bielku Pomôcky: kadička, lyžička, skúmavky, držiak
Laboratórne cvičenie č. 6 Dátum: 24.04.2015 Meno: Katarína Zdráhalová Téma: Bielkoviny Spolupracovníci: Filip Kubus Úlohy: 1. Dôkaz bielkovín vo vaječnom bielku Pomôcky: kadička, lyžička, skúmavky, držiak
LÁBORATÓRNE POMÔCKY. Anorganická a organická chémia ZS
 Materiálovotechnologická fakulta STU v Bratislave so sídlom v Trnave Ústav bezpečnostného a environmentálneho inžinierstva Katedra environmentálneho inžinierstva LÁBORATÓRNE POMÔCKY Anorganická a organická
Materiálovotechnologická fakulta STU v Bratislave so sídlom v Trnave Ústav bezpečnostného a environmentálneho inžinierstva Katedra environmentálneho inžinierstva LÁBORATÓRNE POMÔCKY Anorganická a organická
POZNÁMKY K PRÍPRAVE PRAKTICKEJ ČASTI
 POZNÁMKY K PRÍPRAVE PRAKTICKEJ ČASTI Chemická olympiáda kategória C 51. ročník šk. rok 2014/2015 Domáce kolo Mária Linkešová Maximálne 40 bodov (b), resp. 143 pomocných bodov (pb) Pri prepočte pomocných
POZNÁMKY K PRÍPRAVE PRAKTICKEJ ČASTI Chemická olympiáda kategória C 51. ročník šk. rok 2014/2015 Domáce kolo Mária Linkešová Maximálne 40 bodov (b), resp. 143 pomocných bodov (pb) Pri prepočte pomocných
Človek a príroda. Chémia. Počet voliteľných hodín 0
 Chémia ŠkVP pre žiaka s ľahkým stupňom mentálneho postihnutia-variant A,ISCED 1 -Primárne vzdelávanie Vzdelávacia oblasť Názov predmetu Človek a príroda Chémia Ročník 9. Časový rozvrh výučby ŠkVP 1 hodina
Chémia ŠkVP pre žiaka s ľahkým stupňom mentálneho postihnutia-variant A,ISCED 1 -Primárne vzdelávanie Vzdelávacia oblasť Názov predmetu Človek a príroda Chémia Ročník 9. Časový rozvrh výučby ŠkVP 1 hodina
INDIVIDUÁLNA OCHRANA
 INDIVIDUÁLNA OCHRANA Ochrana obyvateľstva a jeho bezpečnosť v najširšom význame slov patrí k prioritám každej vyspelej spoločnosti či štátu. Realizuje sa najrôznejšími spôsobmi v každodennom živote obyvateľstva.
INDIVIDUÁLNA OCHRANA Ochrana obyvateľstva a jeho bezpečnosť v najširšom význame slov patrí k prioritám každej vyspelej spoločnosti či štátu. Realizuje sa najrôznejšími spôsobmi v každodennom živote obyvateľstva.
Zisti, ktoré farby sa zobrazia na bielom povrchu, ak svetlo prechádza hranolom.
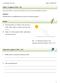 Úloha 1 (Lapitková, 2012, s. 18) Zisti, ktoré farby sa zobrazia na bielom povrchu, ak svetlo prechádza hranolom. Pomôcky: trojboký hranol z priehľadného skla, biely povrch (hárok papiera) Postup: a) Nasmeruj
Úloha 1 (Lapitková, 2012, s. 18) Zisti, ktoré farby sa zobrazia na bielom povrchu, ak svetlo prechádza hranolom. Pomôcky: trojboký hranol z priehľadného skla, biely povrch (hárok papiera) Postup: a) Nasmeruj
PROTENG - samohasiaci systém
 PROTENG - samohasiaci systém Revolučná novinka automatické plynové hasiace systémy - Princíp fungovania je postavený na jednej polyamidovej detekčnej hadici, ktorá je natlakovaná účinným hasiacim plynom
PROTENG - samohasiaci systém Revolučná novinka automatické plynové hasiace systémy - Princíp fungovania je postavený na jednej polyamidovej detekčnej hadici, ktorá je natlakovaná účinným hasiacim plynom
Úvod. Vážení učitelia, milí žiaci,
 Úvod 1 Vážení učitelia, milí žiaci, v cvičebnici pracovnej učebnici pre žiaka sú spracované prvé dva celky Štátneho vzdelávacieho programu (ISCED 2) Chémia okolo nás a Premeny látok. Témy sú rozvrhnuté
Úvod 1 Vážení učitelia, milí žiaci, v cvičebnici pracovnej učebnici pre žiaka sú spracované prvé dva celky Štátneho vzdelávacieho programu (ISCED 2) Chémia okolo nás a Premeny látok. Témy sú rozvrhnuté
Je na vás, kde prespíte dnes v noci
 Je na vás, kde prespíte dnes v noci VSE - letak DL CO Alarm 23022015 0950.indd 1 23.2.2015 9:59:46 ODHAĽTE TICHÉHO ZABIJAKA A OCHRÁŇTE SVOJU RODINU VSE - letak DL CO Alarm 23022015 0950.indd 2 Pri spaľovaní
Je na vás, kde prespíte dnes v noci VSE - letak DL CO Alarm 23022015 0950.indd 1 23.2.2015 9:59:46 ODHAĽTE TICHÉHO ZABIJAKA A OCHRÁŇTE SVOJU RODINU VSE - letak DL CO Alarm 23022015 0950.indd 2 Pri spaľovaní
Fyzika 9. ročník 3. Laboratórna úloha
 Základná škola s materskou školou Chlebnice Fyzika 9. ročník 3. Laboratórna úloha Úloha: Urč pevnú látku, z ktorej je zhotovené teleso, pomocou mernej tepelnej kapacity Príprava: Medzi telesami, ktorých
Základná škola s materskou školou Chlebnice Fyzika 9. ročník 3. Laboratórna úloha Úloha: Urč pevnú látku, z ktorej je zhotovené teleso, pomocou mernej tepelnej kapacity Príprava: Medzi telesami, ktorých
1. Látkové množstvo a molárna hmotnosť
 1. Látkové množstvo a molárna hmotnosť jeden mól plynnej látky jeden mól kvapalnej látky jeden mól tuhej látky Naučíme sa Čo je látkové množstvo Čo predstavuje 1 mól látky Čo je molárna hmotnosť L á t
1. Látkové množstvo a molárna hmotnosť jeden mól plynnej látky jeden mól kvapalnej látky jeden mól tuhej látky Naučíme sa Čo je látkové množstvo Čo predstavuje 1 mól látky Čo je molárna hmotnosť L á t
pre 7. roèník základných škôl a 2. roèník gymnázií s osemroèným štúdiom
 2 pre 7. roèník základných škôl a 2. roèník gymnázií s osemroèným štúdiom Chémia pre 7. ročník základných škôl a 2. ročník gymnázií s osemročným štúdiom Helena Vicenová Veronika Zvončeková Emil Adamkovič
2 pre 7. roèník základných škôl a 2. roèník gymnázií s osemroèným štúdiom Chémia pre 7. ročník základných škôl a 2. ročník gymnázií s osemročným štúdiom Helena Vicenová Veronika Zvončeková Emil Adamkovič
2. Do pripravenej schémy (do sivo pofarbených polí) vpíšte prvky podľa stúpajúceho protónového čísla v smere zľava doprava.
 1. Na obrázku sú zašifrované značky piatich chemických prvkov. Dokážete ich nájsť? Uveďte ich slovenský názov, latinský názov, značku a protónové číslo. 2. Do pripravenej schémy (do sivo pofarbených polí)
1. Na obrázku sú zašifrované značky piatich chemických prvkov. Dokážete ich nájsť? Uveďte ich slovenský názov, latinský názov, značku a protónové číslo. 2. Do pripravenej schémy (do sivo pofarbených polí)
Nebezpečnosť vyplývajúca z fyzikálnych a chemických
 Nebezpečnosť vyplývajúca z fyzikálnych a chemických vlastností látok výbušniny horľavé plyny horľavé aerosóly oxidujúce plyny stlačené plyny horľavé kvapaliny horľavé tuhé látky reaktívne látky, zmesi
Nebezpečnosť vyplývajúca z fyzikálnych a chemických vlastností látok výbušniny horľavé plyny horľavé aerosóly oxidujúce plyny stlačené plyny horľavé kvapaliny horľavé tuhé látky reaktívne látky, zmesi
Názov: Osmóza. Vek žiakov: Témy a kľúčové slová: osmóza, koncentrácia, zber dát a grafické znázornenie. Čas na realizáciu: 120 minút.
 Názov: Osmóza Témy a kľúčové slová: osmóza, koncentrácia, zber dát a grafické znázornenie. Čas na realizáciu: 120 minút Vek žiakov: 14 16 rokov Úrovne práce s materiálom: Úlohy majú rôznu úroveň náročnosti.
Názov: Osmóza Témy a kľúčové slová: osmóza, koncentrácia, zber dát a grafické znázornenie. Čas na realizáciu: 120 minút Vek žiakov: 14 16 rokov Úrovne práce s materiálom: Úlohy majú rôznu úroveň náročnosti.
1.9 Meranie hmotnosti kvapalín a plynov PL KEGA 130UK/2013
 Úloha (Lapitková et al., 2010, s. 49) Úloha: Porovnaj hodnotu objemu vody s hodnotou jej hmotnosti. Pomôcky: odmerný valec, váhy, voda, pipeta. Postup: 1. Odváž odmerný valec a zaznamenaj si jeho hodnotu
Úloha (Lapitková et al., 2010, s. 49) Úloha: Porovnaj hodnotu objemu vody s hodnotou jej hmotnosti. Pomôcky: odmerný valec, váhy, voda, pipeta. Postup: 1. Odváž odmerný valec a zaznamenaj si jeho hodnotu
Základy optických systémov
 Základy optických systémov Norbert Tarjányi, Katedra fyziky, EF ŽU tarjanyi@fyzika.uniza.sk 1 Vlastnosti svetla - koherencia Koherencia časová, priestorová Časová koherencia: charakterizuje koreláciu optického
Základy optických systémov Norbert Tarjányi, Katedra fyziky, EF ŽU tarjanyi@fyzika.uniza.sk 1 Vlastnosti svetla - koherencia Koherencia časová, priestorová Časová koherencia: charakterizuje koreláciu optického
Návod k laboratornímu cvičení. Efektní pokusy
 Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
Návod k laboratornímu cvičení Efektní pokusy Úkol č. 1: Chemikova zahrádka Pomůcky: skleněná vana, lžička na chemikálie. Chemikálie: vodní sklo, síran zinečnatý ZnSO 4 (X i ), síran železnatý FeSO 4, chlorid
Tematický výchovno-vzdelávací plán z predmetu chémia pre 7. ročník
 SEPTEMBER Tematický výchovno-vzdelávací plán z predmetu chémia pre 7. ročník Stupeň vzdelania: ISCED 2 nižšie sekundárne vzdelávanie Vzdelávacia oblasť: Človek a príroda Predmet: Chémia Ročník: siedmy
SEPTEMBER Tematický výchovno-vzdelávací plán z predmetu chémia pre 7. ročník Stupeň vzdelania: ISCED 2 nižšie sekundárne vzdelávanie Vzdelávacia oblasť: Človek a príroda Predmet: Chémia Ročník: siedmy
Diplomový projekt. Detská univerzita Žilinská univerzita v Žiline Matilda Drozdová
 Diplomový projekt Detská univerzita Žilinská univerzita v Žiline 1.7.2014 Matilda Drozdová Pojem projekt Projekt je určitá časovo dlhšia práca, ktorej výsledkom je vyriešenie nejakej úlohy Kto rieši projekt?
Diplomový projekt Detská univerzita Žilinská univerzita v Žiline 1.7.2014 Matilda Drozdová Pojem projekt Projekt je určitá časovo dlhšia práca, ktorej výsledkom je vyriešenie nejakej úlohy Kto rieši projekt?
Tematický výchovno-vzdelávací plán z chémie pre 7. ročník ZŠ (spracovaný v súlade so ŠVP Chémia ISCED 2 príloha)
 Tematický výchovno-vzdelávací plán z chémie pre 7. ročník ZŠ (spracovaný v súlade so ŠVP Chémia ISCED 2 príloha) Spracovaný v rámci projektu: E-learning vo výchovno-vzdelávacom procese Dopytovo-orientovaný
Tematický výchovno-vzdelávací plán z chémie pre 7. ročník ZŠ (spracovaný v súlade so ŠVP Chémia ISCED 2 príloha) Spracovaný v rámci projektu: E-learning vo výchovno-vzdelávacom procese Dopytovo-orientovaný
TEMATICKÝ OKRUH VEK DETÍ TÉMA
 Aktivita: CESTUJEME OD PRAVEKU Autor: Mgr. Drahomíra Koledová, MŠ Skalka 17, Lietavská Lúčka Cesta na kurikulum: Ja som Kultúra Ľudia Príroda TEMATICKÝ OKRUH VEK DETÍ TÉMA Minutáž: 30 minút 4 5 rokov 4
Aktivita: CESTUJEME OD PRAVEKU Autor: Mgr. Drahomíra Koledová, MŠ Skalka 17, Lietavská Lúčka Cesta na kurikulum: Ja som Kultúra Ľudia Príroda TEMATICKÝ OKRUH VEK DETÍ TÉMA Minutáž: 30 minút 4 5 rokov 4
Flashover kontejnery (FOK) podpora pro instruktory v oblasti hašení požárů v uzavřených prostorech
 Minulý týždeň (24.-25.11) sa v Školní a výcvikové zařízení Hasičského záchranného sboru České republiky středisko Brno konal odborný seminár Flashover kontejnery (FOK) 2016 - podpora pro instruktory v
Minulý týždeň (24.-25.11) sa v Školní a výcvikové zařízení Hasičského záchranného sboru České republiky středisko Brno konal odborný seminár Flashover kontejnery (FOK) 2016 - podpora pro instruktory v
Ročník 3. Predmet SLOVENSKÝ JAZYK Environmentálna výchova Školský rok 2014/2015 Tvorca materiálu PaedDr. Paulína Krivosudská
 Financované Prijímateľ: Názov projektu: Kód projektu: Aktivita, resp. názov seminára z Finančného mechanizmu EHP a ŠR SR Základná škola s materskou školou kráľa Svätopluka Šintava Revitalizuj a zachráň
Financované Prijímateľ: Názov projektu: Kód projektu: Aktivita, resp. názov seminára z Finančného mechanizmu EHP a ŠR SR Základná škola s materskou školou kráľa Svätopluka Šintava Revitalizuj a zachráň
NEVLASTNÁ VODIVOSŤ POLOVODIČOVÉHO MATERIÁLU TYPU P
 NEVLASTNÁ VODIVOSŤ POLOVODIČOVÉHO MATERIÁLU TYPU P 1. VLASTNÉ POLOVODIČE Vlastnými polovodičmi nazývame polovodiče chemicky čisté, bez prímesí iných prvkov. V súčasnosti je najpoužívanejším polovodičovým
NEVLASTNÁ VODIVOSŤ POLOVODIČOVÉHO MATERIÁLU TYPU P 1. VLASTNÉ POLOVODIČE Vlastnými polovodičmi nazývame polovodiče chemicky čisté, bez prímesí iných prvkov. V súčasnosti je najpoužívanejším polovodičovým
Ročník 7. ročník Predmet Biológia Školský rok 2014/2015 Tvorca materiálu Mgr. Milada Rajterová
 Financované Prijímateľ: Názov projektu: Kód projektu: Aktivita, resp. názov seminára z Finančného mechanizmu EHP a ŠR SR Základná škola s materskou školou kráľa Svätopluka Šintava Revitalizuj a zachráň
Financované Prijímateľ: Názov projektu: Kód projektu: Aktivita, resp. názov seminára z Finančného mechanizmu EHP a ŠR SR Základná škola s materskou školou kráľa Svätopluka Šintava Revitalizuj a zachráň
Ing. Motešický POLOVODIČE
 Ing. Motešický POLOVODIČE Zopakujme si: Látky z hľadiska vedenia elektrického prúdu delíme na: 1. vodiče - kladú prechádzajúcemu el. I nízky R, majú vysokú el. vodivosť G, látka má veľké množstvo voľných
Ing. Motešický POLOVODIČE Zopakujme si: Látky z hľadiska vedenia elektrického prúdu delíme na: 1. vodiče - kladú prechádzajúcemu el. I nízky R, majú vysokú el. vodivosť G, látka má veľké množstvo voľných
7) Uveď příklad chemické reakce, při níž se sloučí dva prvky za vzniku sloučeniny. (3) hoření vodíku s kyslíkem a vzniká voda
 Chemické reakce a děje Chemické reakce 1) Jak se chemické reakce odlišují od fyzikálních dějů? (2) změna vlastností látek, změna vazeb mezi atomy 2) Co označujeme v chemických reakcích jako reaktanty a
Chemické reakce a děje Chemické reakce 1) Jak se chemické reakce odlišují od fyzikálních dějů? (2) změna vlastností látek, změna vazeb mezi atomy 2) Co označujeme v chemických reakcích jako reaktanty a
Napíšte do zošita minimálne tri chemické reakcie.
 Chemické reakcie Napíšte do zošita minimálne tri chemické reakcie. Fotosyntéza Trávenie potravy Dýchanie hnitie jablka hrdzavenie Pečenie chleba varenie karamelu Výroba železa zo železnej rudy odstraňovanie
Chemické reakcie Napíšte do zošita minimálne tri chemické reakcie. Fotosyntéza Trávenie potravy Dýchanie hnitie jablka hrdzavenie Pečenie chleba varenie karamelu Výroba železa zo železnej rudy odstraňovanie
Starogrécky filozof Demokritos ( pred n.l) Látky sú zložené z veľmi malých, ďalej nerozdeliteľných častíc - atómov
 STAVBA ATÓMU Starogrécky filozof Demokritos (450-420 pred n.l) Látky sú zložené z veľmi malých, ďalej nerozdeliteľných častíc - atómov Starogrécky filozof Aristoteles (384-322 pred n.l) Látky možno neobmedzene
STAVBA ATÓMU Starogrécky filozof Demokritos (450-420 pred n.l) Látky sú zložené z veľmi malých, ďalej nerozdeliteľných častíc - atómov Starogrécky filozof Aristoteles (384-322 pred n.l) Látky možno neobmedzene
SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY
 SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 54. ročník, školský rok 2017/2018 Kategória D Okresné kolo TEORETICKÉ A PRAKTICKÉ ÚLOHY TEORETICKÉ ÚLOHY Chemická olympiáda kategória D 54. ročník
SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 54. ročník, školský rok 2017/2018 Kategória D Okresné kolo TEORETICKÉ A PRAKTICKÉ ÚLOHY TEORETICKÉ ÚLOHY Chemická olympiáda kategória D 54. ročník
Provokačná myšlienka: Vieme ovplyvniť využitie zdrojov v našom živote?
 Aktivita: OD ZDROJA K TEPLU Autor: Mgr. Hana Chlebanová, Gymnázium, Varšavská cesta 1, Žilina Cesta na kurikulum: Biológia PREDMET ROČNÍK TEMATICKÝ CELOK 4. ročník SŠ Usadené horniny Organické usadené
Aktivita: OD ZDROJA K TEPLU Autor: Mgr. Hana Chlebanová, Gymnázium, Varšavská cesta 1, Žilina Cesta na kurikulum: Biológia PREDMET ROČNÍK TEMATICKÝ CELOK 4. ročník SŠ Usadené horniny Organické usadené
Metodický list k pracovnému listu Oheň- dobrý sluha a zlý pán.
 Názov projektu: Čítaj viac a dvere k poznaniu sa samy otvoria Kód projektu: 26110130437 ZŠ s MŠ Centrum I 32, Dubnica nad Váhom Metodický list k pracovnému listu Oheň- dobrý sluha a zlý pán. Mgr. Jana
Názov projektu: Čítaj viac a dvere k poznaniu sa samy otvoria Kód projektu: 26110130437 ZŠ s MŠ Centrum I 32, Dubnica nad Váhom Metodický list k pracovnému listu Oheň- dobrý sluha a zlý pán. Mgr. Jana
POWLI Fig. A Copyright 2014 VARO
 POWLI421 1 7 6 2 3 4 5 Fig. A Copyright 2014 VARO www.varo.com POWLI421 Fig 1 Copyright 2014 VARO www.varo.com LED BATERKA 1,5 W POWLI421 POWLI421 SK 1 POPIS (OBR. A) 1. Otočná hlava 2. Hlavný vypínač
POWLI421 1 7 6 2 3 4 5 Fig. A Copyright 2014 VARO www.varo.com POWLI421 Fig 1 Copyright 2014 VARO www.varo.com LED BATERKA 1,5 W POWLI421 POWLI421 SK 1 POPIS (OBR. A) 1. Otočná hlava 2. Hlavný vypínač
Bezdrôtová nabíjačka K7
 Bezdrôtová nabíjačka K7 kompatibilné UŽÍVATEĽSKÝ MANUÁL 1 Úvod Ďakujeme Vám za zakúpenie nášho produktu. Pred prvým použitím si pre Vašu pozornosť, prosím pozorne prečítajte tento manuál. Prosíme Vás o
Bezdrôtová nabíjačka K7 kompatibilné UŽÍVATEĽSKÝ MANUÁL 1 Úvod Ďakujeme Vám za zakúpenie nášho produktu. Pred prvým použitím si pre Vašu pozornosť, prosím pozorne prečítajte tento manuál. Prosíme Vás o
HODNOTENIE SPOKOJNOSTI ŽIAKA
 HODNOTENIE SPOKOJNOSTI ŽIAKA TRIEDA: V súčasnosti sa zaoberáme sebahodnotením a veľmi by sme privítali vaše názory na našu školu. Prečítajte si uvedené tvrdenia a vyznačte odpoveď, ktorá najlepšie vystihuje
HODNOTENIE SPOKOJNOSTI ŽIAKA TRIEDA: V súčasnosti sa zaoberáme sebahodnotením a veľmi by sme privítali vaše názory na našu školu. Prečítajte si uvedené tvrdenia a vyznačte odpoveď, ktorá najlepšie vystihuje
Akreditované skúšky horľavosti kvapalín
 Akreditované horľavosti kvapalín 1. STN EN 14522:2006 Stanovenie teploty vznietenia plynov a pár. 2. STN EN ISO 2592:2003 Určovanie bodu vzplanutia a horenia. Clevelandova metóda v otvorenom tégliku. 3.
Akreditované horľavosti kvapalín 1. STN EN 14522:2006 Stanovenie teploty vznietenia plynov a pár. 2. STN EN ISO 2592:2003 Určovanie bodu vzplanutia a horenia. Clevelandova metóda v otvorenom tégliku. 3.
PRAKTICKÉ ÚLOHY Z ANALYTICKEJ CHÉMIE
 1. postup PRAKTICKÉ ÚLOHY Z ANALYTICKEJ CHÉMIE Chemická olympiáda kategória A 53. ročník školský rok 2016/17 Celoštátne kolo Odpoveďový hárok Štartovné číslo:... Úloha 1 Stanovenie presnej koncentrácie
1. postup PRAKTICKÉ ÚLOHY Z ANALYTICKEJ CHÉMIE Chemická olympiáda kategória A 53. ročník školský rok 2016/17 Celoštátne kolo Odpoveďový hárok Štartovné číslo:... Úloha 1 Stanovenie presnej koncentrácie
Úloha: Prezri si podkapitoly 1.6 a 1.11 a vypíš z nich vlastnosti tuhých látok a telies do tabuľky Vlastnosti tuhých látok a telies
 Úloha (Lapitková et al., 2010, s. 63) Úloha: Prezri si podkapitoly 1.6 a 1.11 a vypíš z nich vlastnosti tuhých látok a telies do tabuľky 1.12.1. Tabuľka 1.12.1 Vlastnosti tuhých látok a telies Vlastnosti
Úloha (Lapitková et al., 2010, s. 63) Úloha: Prezri si podkapitoly 1.6 a 1.11 a vypíš z nich vlastnosti tuhých látok a telies do tabuľky 1.12.1. Tabuľka 1.12.1 Vlastnosti tuhých látok a telies Vlastnosti
Téma : Špecifiká marketingu finančných služieb
 Téma : Špecifiká marketingu finančných služieb Marketing predstavuje komplex činností, ktorý zahrňuje všetky činnosti od nápadu až po uvedenie produktu na trh. Cieľom marketingu je potom predať: správny
Téma : Špecifiká marketingu finančných služieb Marketing predstavuje komplex činností, ktorý zahrňuje všetky činnosti od nápadu až po uvedenie produktu na trh. Cieľom marketingu je potom predať: správny
Vodík, kyslík a jejich sloučeniny
 I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í TENTO PROJEKT JE SPOLUFINANCOVÁN EVROPSKÝM SOCIÁLNÍM FONDEM A STÁTNÍM ROZPOČTEM ČESKÉ REPUBLIKY Laboratorní práce č. 8 Vodík, kyslík a jejich sloučeniny
PPC brief. Zadanie pre tvorbu PPC reklamnej kampane
 PPC brief Zadanie pre tvorbu PPC reklamnej kampane Tento dokument slúži ako východiskový bod projektu pre tvorbu PPC reklamnej kampane. Vďaka nemu si môžeme ujasniť základné informácie potrebné na začatie
PPC brief Zadanie pre tvorbu PPC reklamnej kampane Tento dokument slúži ako východiskový bod projektu pre tvorbu PPC reklamnej kampane. Vďaka nemu si môžeme ujasniť základné informácie potrebné na začatie
Podlimitná zákazka Verejný obstarávateľ
 Finančné limity platné a účinné po 1. marci 2015 Podlimitná zákazka Verejný obstarávateľ BEŽNE DOSTUPNÉ NA TRHU 1 000 eur < 134 000 eur b) bod 3. alebo c)] Stavebné práce 1 000 eur < 5 186 000 eur b) bod.
Finančné limity platné a účinné po 1. marci 2015 Podlimitná zákazka Verejný obstarávateľ BEŽNE DOSTUPNÉ NA TRHU 1 000 eur < 134 000 eur b) bod 3. alebo c)] Stavebné práce 1 000 eur < 5 186 000 eur b) bod.
Cieľ: správne vysvetlenie významu slova migrovanie, priblížiť prečo ľudia migrujú, zapájať do odpovedí účastníkov,
 Práca v Európe Seminár- modul 5 Počas tohto seminára sa účastníci naučia: Čo je migrovanie Aké sú dôvody migrovania v Európe Aké sú výhody a nevýhody práce v zahraničí Ako správne písať žiadosť a životopis
Práca v Európe Seminár- modul 5 Počas tohto seminára sa účastníci naučia: Čo je migrovanie Aké sú dôvody migrovania v Európe Aké sú výhody a nevýhody práce v zahraničí Ako správne písať žiadosť a životopis
RNDr. Daniela Kravecová, PhD. Premonštrátske gymnázium, Kováčska 28, Košice
 Redoxné reakcie RNDr. Daniela Kravecová, PhD. Premonštrátske gymnázium, Kováčska 28, Košice Redoxné reakcie Redoxné reakcie sú chemické reakcie, pri ktorých dochádza k zmene oxidačného čísla atómov alebo
Redoxné reakcie RNDr. Daniela Kravecová, PhD. Premonštrátske gymnázium, Kováčska 28, Košice Redoxné reakcie Redoxné reakcie sú chemické reakcie, pri ktorých dochádza k zmene oxidačného čísla atómov alebo
Zmena skupenstva látok
 1. Keď má sústava v rovnovážnom stave vo vrtkých častiach rovnaké fyzikálne a chemické vlastnosti, napr. rovnakú hustotu, štruktúru, rovnaké chemické zloženie, nazýva sa fáza. Prechod látky z jednej fázy
1. Keď má sústava v rovnovážnom stave vo vrtkých častiach rovnaké fyzikálne a chemické vlastnosti, napr. rovnakú hustotu, štruktúru, rovnaké chemické zloženie, nazýva sa fáza. Prechod látky z jednej fázy
To bolo ľahké. Dokážete nakresliť kúsok od prvého stromčeka rovnaký? Asi áno, veď môžete použiť tie isté príkazy.
 Opakuj a pomenuj Nakreslime si ovocný sad Príklad 1 Pomocou príkazového riadku skúste s korytnačkou nakresliť ovocný stromček. Vaša postupnosť príkazov sa možno podobá na nasledujúcu:? nechfp "hnedá? nechhp
Opakuj a pomenuj Nakreslime si ovocný sad Príklad 1 Pomocou príkazového riadku skúste s korytnačkou nakresliť ovocný stromček. Vaša postupnosť príkazov sa možno podobá na nasledujúcu:? nechfp "hnedá? nechhp
TomTom Referenčná príručka
 TomTom Referenčná príručka Obsah Rizikové zóny 3 Rizikové zóny vo Francúzsku... 3 Upozornenia na rizikové zóny... 3 Zmena spôsobu upozornenia... 4 tlačidlo Ohlásiť... 4 Nahlásenie novej rizikovej zóny
TomTom Referenčná príručka Obsah Rizikové zóny 3 Rizikové zóny vo Francúzsku... 3 Upozornenia na rizikové zóny... 3 Zmena spôsobu upozornenia... 4 tlačidlo Ohlásiť... 4 Nahlásenie novej rizikovej zóny
Vyhláš. áška MV SR č.. 523/2006 Z. z. O podrobnostiach na zabezpečenie záchranných prác a organizovania Jednotiek civilnej ochrany
 Záchranné práce Vyhláš áška MV SR č.. 523/2006 Z. z. O podrobnostiach na zabezpečenie záchranných prác a organizovania Jednotiek civilnej ochrany Definícia záchranných prác (ZP) Zákon NR SR č. 42/1994
Záchranné práce Vyhláš áška MV SR č.. 523/2006 Z. z. O podrobnostiach na zabezpečenie záchranných prác a organizovania Jednotiek civilnej ochrany Definícia záchranných prác (ZP) Zákon NR SR č. 42/1994
5. Vysušte a pozorujte mikroskopom preparáty oboch modelových B ako i preparát Vašej izolovanej B.
 NÁZOV PRÁCE: CIEĽ PRÁCE: PRÁCA 3 NEGATÍVNE ZOBRAZENIE MIKROORGANIZMOV. FIXÁCIA A DIAGNOSTICKÉ FARBENIE BAKTÉRIÍ. A) Naučiť sa negatívne zobrazenie mikroorganizmov (MO). B) Naučiť sa prípravu fixovaného
NÁZOV PRÁCE: CIEĽ PRÁCE: PRÁCA 3 NEGATÍVNE ZOBRAZENIE MIKROORGANIZMOV. FIXÁCIA A DIAGNOSTICKÉ FARBENIE BAKTÉRIÍ. A) Naučiť sa negatívne zobrazenie mikroorganizmov (MO). B) Naučiť sa prípravu fixovaného
Piezo hořák UTPZ225 Piezo horák UTPZ225 NÁVOD K POUŽITÍ
 Piezo hořák UTPZ225 Piezo horák UTPZ225 NÁVOD K POUŽITÍ Pečlivě si prosím přečtěte tento návod a seznamte se s tímto zařízením. Dodržujte pokyny pro použití a dávejte pozor na omezení a možná rizika související
Piezo hořák UTPZ225 Piezo horák UTPZ225 NÁVOD K POUŽITÍ Pečlivě si prosím přečtěte tento návod a seznamte se s tímto zařízením. Dodržujte pokyny pro použití a dávejte pozor na omezení a možná rizika související
2. Spaľovanie tuhých palív, kvapalných palív a plynných palív okrem spaľovania v plynových turbínach a stacionárnych piestových spaľovacích motoroch
 IV. VÄČŠIE STREDNÉ SPAĽOVACIE ZARIADENIA 1. Členenie väčších stredných spaľovacích zariadení vo vzťahu k uplatňovaniu emisných limitov Podľa dátumu vydaného povolenia sa väčšie stredné spaľovacie zariadenia
IV. VÄČŠIE STREDNÉ SPAĽOVACIE ZARIADENIA 1. Členenie väčších stredných spaľovacích zariadení vo vzťahu k uplatňovaniu emisných limitov Podľa dátumu vydaného povolenia sa väčšie stredné spaľovacie zariadenia
VZOR OZNÁMENIE O ZARADENÍ PODNIKU PODĽA 5 ZÁKONA
 VZOR OZNÁMENIE O ZARADENÍ PODNIKU PODĽA 5 ZÁKONA 1. Dôvod vypracovania oznámenia Označiť dôvod/zmenu x Nové oznámenie Nový podnik 3 ods. 5 písm. a) zákona Aktualizácia oznámenia Možnosť výberu z viacerých
VZOR OZNÁMENIE O ZARADENÍ PODNIKU PODĽA 5 ZÁKONA 1. Dôvod vypracovania oznámenia Označiť dôvod/zmenu x Nové oznámenie Nový podnik 3 ods. 5 písm. a) zákona Aktualizácia oznámenia Možnosť výberu z viacerých
Pracovný list pre žiaka
 Pracovný list pre žiaka Pokus 1 (Lapitková, et al., 2010a, s. 33) Úloha č.1 Zistite akú teplotu má povrch banky, aby sa na ňom začala tvoriť rosa. Pomôcky: sklenená nádoba (banka), teplomer, kocky ľadu,
Pracovný list pre žiaka Pokus 1 (Lapitková, et al., 2010a, s. 33) Úloha č.1 Zistite akú teplotu má povrch banky, aby sa na ňom začala tvoriť rosa. Pomôcky: sklenená nádoba (banka), teplomer, kocky ľadu,
PRÍLOHY: Príloha 1 Organizačná štruktúra firmy
 PRÍLOHY: Príloha 1 Organizačná štruktúra firmy Príloha 2 Dotazník pre zamestnancov MPC CESSI, a. s., Spišská Nová Ves Vážený respondent, som študentka Materiálovotechnologickej fakulty Slovenskej technickej
PRÍLOHY: Príloha 1 Organizačná štruktúra firmy Príloha 2 Dotazník pre zamestnancov MPC CESSI, a. s., Spišská Nová Ves Vážený respondent, som študentka Materiálovotechnologickej fakulty Slovenskej technickej
PRÍLOHY. k návrhu SMERNICE EURÓPSKEHO PARLAMENTU A RADY
 EURÓPSKA KOMISIA V Bruseli 18.12.2013 COM(2013) 919 final ANNEXES 1 to 4 PRÍLOHY k návrhu SMERNICE EURÓPSKEHO PARLAMENTU A RADY o obmedzení emisií určitých znečisťujúcich látok do ovzdušia zo stredne veľkých
EURÓPSKA KOMISIA V Bruseli 18.12.2013 COM(2013) 919 final ANNEXES 1 to 4 PRÍLOHY k návrhu SMERNICE EURÓPSKEHO PARLAMENTU A RADY o obmedzení emisií určitých znečisťujúcich látok do ovzdušia zo stredne veľkých
Ako zamedziť tvorbe plesní v byte?
 Ako zamedziť tvorbe plesní v byte? Obvodové steny mnohých bytových domov postavených pred rokom 1991 (najmä panelových) majú nedostatočné tepelnoizolačné vlastnosti a nízku priepustnosť vodných pár. V
Ako zamedziť tvorbe plesní v byte? Obvodové steny mnohých bytových domov postavených pred rokom 1991 (najmä panelových) majú nedostatočné tepelnoizolačné vlastnosti a nízku priepustnosť vodných pár. V
OBCHOD MARKETING PSYCHOLÓGIA A ETIKA PREDAJA
 MAAG MAAG - Program na zvýšenie adaptability žiakov stredných škôl pri vstupe na trh práce Projekt je spolufinancovaný Európskou úniou Kód projektu 13120120211 maag.euba.sk maag@euba.sk OBCHOD MARKETING
MAAG MAAG - Program na zvýšenie adaptability žiakov stredných škôl pri vstupe na trh práce Projekt je spolufinancovaný Európskou úniou Kód projektu 13120120211 maag.euba.sk maag@euba.sk OBCHOD MARKETING
Programy vzdelávania: Vzdelávanie s interaktívnou tabuľou
 Pri tvorbe edukačných materiálov, nielen digitálnej povahy je mnohokrát potrebné dodatočne upraviť vybraný obrazový materiál. Najjednoduchším spôsobom je pouţiť program Microsoft Office Picture Manager.
Pri tvorbe edukačných materiálov, nielen digitálnej povahy je mnohokrát potrebné dodatočne upraviť vybraný obrazový materiál. Najjednoduchším spôsobom je pouţiť program Microsoft Office Picture Manager.
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH ROVNIC VY_32_INOVACE_03_3_18_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH ROVNIC VY_32_INOVACE_03_3_18_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou VÝPOČTY Z CHEMICKÝCH
Porovnanie výsledkov IQ (test SON- R 2 1/2-7) a GHS (Göppingen - hrubé skóre) vo vzťahu k subjektívnym faktorom správania
 Porovnanie výsledkov IQ (test SON- R 2 1/2-7) a GHS (Göppingen - hrubé skóre) vo vzťahu k subjektívnym faktorom správania Dagmar Kopčanová VÚDPaP Bratislava kopcanova@vudpap.sk V prvej polovici roka 2008
Porovnanie výsledkov IQ (test SON- R 2 1/2-7) a GHS (Göppingen - hrubé skóre) vo vzťahu k subjektívnym faktorom správania Dagmar Kopčanová VÚDPaP Bratislava kopcanova@vudpap.sk V prvej polovici roka 2008
Kombinatorická pravdepodobnosť (opakovanie)
 Kombinatorická pravdepodobnosť (opakovanie) Metódy riešenia úloh z pravdepodobnosti a štatistiky Cvičenie 1 Beáta Stehlíková, FMFI UK Bratislava www.iam.fmph.uniba.sk/institute/stehlikova Príklad 1: Zhody
Kombinatorická pravdepodobnosť (opakovanie) Metódy riešenia úloh z pravdepodobnosti a štatistiky Cvičenie 1 Beáta Stehlíková, FMFI UK Bratislava www.iam.fmph.uniba.sk/institute/stehlikova Príklad 1: Zhody
Základná škola s materskou školou Rabča
 Základná škola s materskou školou Rabča Motto: SLUŠNOSŤ A MÚDROSŤ NECH TI OTVORIA BRÁNU DO ŽIVOTA naše motto predstavuje zámer školy postupnými zmenami v ponímaní výchovy a vzdelávania vytvoriť novú modernú
Základná škola s materskou školou Rabča Motto: SLUŠNOSŤ A MÚDROSŤ NECH TI OTVORIA BRÁNU DO ŽIVOTA naše motto predstavuje zámer školy postupnými zmenami v ponímaní výchovy a vzdelávania vytvoriť novú modernú
FYZIKA - 6. ročník. šk. r / Časovo tematický plán vyučovania. Základná škola, Holubyho 15, Piešťany, / ISCED2 /
 Základná škola, Holubyho 15, Piešťany, 921 01 šk. r. 2010 / 2011 Časovo tematický plán vyučovania FYZIKA - 6. ročník / ISCED2 / Časová dotácia: 1 týždenne / 33 hodín ročne Vyučujúci: Schválil: Mgr. Jana
Základná škola, Holubyho 15, Piešťany, 921 01 šk. r. 2010 / 2011 Časovo tematický plán vyučovania FYZIKA - 6. ročník / ISCED2 / Časová dotácia: 1 týždenne / 33 hodín ročne Vyučujúci: Schválil: Mgr. Jana
Smartfóny ako spotrebiče so zabudovanými snímačmi
 3 Smartfóny ako spotrebiče so zabudovanými snímačmi Karl Heller, Bernhard Horlacher Odporúčaný ročník 10. 12. Časový rámec Názov tematického celku 2 4 min. Elektrické spotrebiče Cieľ a rozvoj kompetencií
3 Smartfóny ako spotrebiče so zabudovanými snímačmi Karl Heller, Bernhard Horlacher Odporúčaný ročník 10. 12. Časový rámec Názov tematického celku 2 4 min. Elektrické spotrebiče Cieľ a rozvoj kompetencií
Laboratorní cvičení z kinetiky chemických reakcí
 Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
Laboratorní cvičení z kinetiky chemických reakcí LABORATORNÍ CVIČENÍ 1. Téma: Ovlivňování průběhu reakce změnou koncentrace látek. podmínek průběhu reakce. Jednou z nich je změna koncentrace výchozích
2.4 Hustota kvapalín PL KEGA 130UK/2013
 Úloha (Lapitková et al., 2010, s. 85) Úloha: Urč hustoty kvapalín v poradí voda, med, olej. Pomôcky: voda, med, jedlý olej, digitálne váhy (s presnosťou na 0,1 g), kadička so stupnicou v mililitroch (odmerný
Úloha (Lapitková et al., 2010, s. 85) Úloha: Urč hustoty kvapalín v poradí voda, med, olej. Pomôcky: voda, med, jedlý olej, digitálne váhy (s presnosťou na 0,1 g), kadička so stupnicou v mililitroch (odmerný
DANE A DAŇOVÝ SYSTÉM V SR
 DANE A DAŇOVÝ SYSTÉM V SR Na tomto svete nie je nič isté, iba dane a smrť. Benjamin Franklin, 1789 DAŇ Povinná, zákonom stanovená platba, ktorú odvádza daňový subjekt, t.j. fyzická alebo právnická osoba,
DANE A DAŇOVÝ SYSTÉM V SR Na tomto svete nie je nič isté, iba dane a smrť. Benjamin Franklin, 1789 DAŇ Povinná, zákonom stanovená platba, ktorú odvádza daňový subjekt, t.j. fyzická alebo právnická osoba,
VECIT 2006 Tento materiál vznikol v rámci projektu, ktorý je spolufinancovaný Európskou úniou. 1/4
 Príklad 1 Naučte korytnačku príkaz čelenka. Porozmýšľajte nad využitím príkazu plnytrojuhol60: viem plnytrojuhol60 opakuj 3 [do 60 vp 120 Riešenie: definujeme ďalšie príkazy na kreslenie trojuholníka líšiace
Príklad 1 Naučte korytnačku príkaz čelenka. Porozmýšľajte nad využitím príkazu plnytrojuhol60: viem plnytrojuhol60 opakuj 3 [do 60 vp 120 Riešenie: definujeme ďalšie príkazy na kreslenie trojuholníka líšiace
NEINTERAKTÍVNA KOMUNIKÁCIA
 NEINTERAKTÍVNA KOMUNIKÁCIA ICSED3 informatika Gymnázium Kráľovnej pokoja, Žilina Mgr. Miroslav Malacha Komunikácia prostredníctvom IKT Komunikácia: vyvinulo sa z lat. communicare= deliť sa, zverovať, všeobecnosti
NEINTERAKTÍVNA KOMUNIKÁCIA ICSED3 informatika Gymnázium Kráľovnej pokoja, Žilina Mgr. Miroslav Malacha Komunikácia prostredníctvom IKT Komunikácia: vyvinulo sa z lat. communicare= deliť sa, zverovať, všeobecnosti
Co je chemie a proč se ji máme učit?
 ÚVOD Co je chemie a proč se ji máme učit? ➊ Spoj některé následující vynálezy s místem, kde byly objeveny. Dále zakroužkuj látky, které se snažili vyrobit dávní alchymisté. střelný prach papír oheň papyrus
ÚVOD Co je chemie a proč se ji máme učit? ➊ Spoj některé následující vynálezy s místem, kde byly objeveny. Dále zakroužkuj látky, které se snažili vyrobit dávní alchymisté. střelný prach papír oheň papyrus
Analýza dopravnej situácie v SR
 Analýza dopravnej situácie v SR Príloha č. 4 Nehodovosť Dopravná nehodovosť na pozemných komunikáciách predstavuje dôležitý ukazovateľ úrovne cestných podmienok (stavebno-technického stavu) a premávkových
Analýza dopravnej situácie v SR Príloha č. 4 Nehodovosť Dopravná nehodovosť na pozemných komunikáciách predstavuje dôležitý ukazovateľ úrovne cestných podmienok (stavebno-technického stavu) a premávkových
Kombinatorická pravdepodobnosť (opakovanie)
 Kombinatorická pravdepodobnosť (opakovanie) Metódy riešenia úloh z pravdepodobnosti a štatistiky Beáta Stehlíková, FMFI UK Bratislava www.iam.fmph.uniba.sk/institute/stehlikova Príklad 1: Zhody kariet
Kombinatorická pravdepodobnosť (opakovanie) Metódy riešenia úloh z pravdepodobnosti a štatistiky Beáta Stehlíková, FMFI UK Bratislava www.iam.fmph.uniba.sk/institute/stehlikova Príklad 1: Zhody kariet
(Nelegislatívne akty) NARIADENIA
 18.4.2013 Úradný vestník Európskej únie L 108/1 II (Nelegislatívne akty) NARIADENIA NARIADENIE KOMISIE (EÚ) č. 348/2013 zo 17. apríla 2013, ktorým sa mení a dopĺňa príloha XIV k nariadeniu Európskeho parlamentu
18.4.2013 Úradný vestník Európskej únie L 108/1 II (Nelegislatívne akty) NARIADENIA NARIADENIE KOMISIE (EÚ) č. 348/2013 zo 17. apríla 2013, ktorým sa mení a dopĺňa príloha XIV k nariadeniu Európskeho parlamentu
1. LABORATÓRNE CVIČENIE
 MENO: ROČNÍK A TRIEDA: 1. LABORATÓRNE CVIČENIE ROVNOMERNÝ POHYB - ZÁVISLOSŤ POLOHY OD ČASU Cieľ: Naučiť sa pracovať so senzorom polohy a ako sú rôzne druhy pohybu prezentované na grafe závislosti polohy
MENO: ROČNÍK A TRIEDA: 1. LABORATÓRNE CVIČENIE ROVNOMERNÝ POHYB - ZÁVISLOSŤ POLOHY OD ČASU Cieľ: Naučiť sa pracovať so senzorom polohy a ako sú rôzne druhy pohybu prezentované na grafe závislosti polohy
Osoba podľa 8 zákona finančné limity, pravidlá a postupy platné od
 A. Právny rámec Osoba podľa 8 zákona finančné limity, pravidlá a postupy platné od 18. 4. 2016 Podľa 8 ods. 1 zákona č. 343/2015 Z. z. o verejnom obstarávaní a o zmene a doplnení niektorých zákonov v znení
A. Právny rámec Osoba podľa 8 zákona finančné limity, pravidlá a postupy platné od 18. 4. 2016 Podľa 8 ods. 1 zákona č. 343/2015 Z. z. o verejnom obstarávaní a o zmene a doplnení niektorých zákonov v znení
INFORMÁCIE ENERGII-ELEKTRÁRNE
 INFORMÁCIE O ENERGII-ELEKTRÁRNE ENERGIA? ČO JE Energia je schopnosť konať prácu. Energia je všade v slnečnom svetle ako teplo i svetlo, v magnetofóne ako energia zvuku, dokonca aj v hrude uhlia ako skrytá
INFORMÁCIE O ENERGII-ELEKTRÁRNE ENERGIA? ČO JE Energia je schopnosť konať prácu. Energia je všade v slnečnom svetle ako teplo i svetlo, v magnetofóne ako energia zvuku, dokonca aj v hrude uhlia ako skrytá
CHL a P Novinky v legislatíve. VOC, aerosóly, harmonizovaná klasifikácia
 CHL a P Novinky v legislatíve VOC, aerosóly, harmonizovaná klasifikácia Chemické látky a prípravky Chemická legislatíva EÚ uvedenie na trh + harmonizovaná klasifikácia REACH výroba a dovoz GHS nový systém
CHL a P Novinky v legislatíve VOC, aerosóly, harmonizovaná klasifikácia Chemické látky a prípravky Chemická legislatíva EÚ uvedenie na trh + harmonizovaná klasifikácia REACH výroba a dovoz GHS nový systém
Potrebujem: pracovný list uvedený v prílohe, staré noviny, časopisy, nožnice, lepidlo, hárok papiera (formát A3), farbičky/pastelky
 Aktivita: DOPRAVNÉ PROSTRIEDKY Cesta na kurikulum: TEMATICKÝ OKRUH STUPEŇ OBSAHOVÉ ŠTANDARDY Ja som Ľudia Príroda Zhotoviť výtvory z rozmanitého materiálu, vrátane odpadového, rôznymi technikami (strihať,
Aktivita: DOPRAVNÉ PROSTRIEDKY Cesta na kurikulum: TEMATICKÝ OKRUH STUPEŇ OBSAHOVÉ ŠTANDARDY Ja som Ľudia Príroda Zhotoviť výtvory z rozmanitého materiálu, vrátane odpadového, rôznymi technikami (strihať,
MATURITA 2016 ZÁKLADNÉ INFORMÁCIE
 MATURITA 2016 ZÁKLADNÉ INFORMÁCIE Organizáciu MS upravuje zákon č. 245/2008 Z. z. o výchove a vzdelávaní (školský zákon) a o zmene a doplnení niektorých zákonov v znení neskorších predpisov a vyhláška
MATURITA 2016 ZÁKLADNÉ INFORMÁCIE Organizáciu MS upravuje zákon č. 245/2008 Z. z. o výchove a vzdelávaní (školský zákon) a o zmene a doplnení niektorých zákonov v znení neskorších predpisov a vyhláška
Ministerstvo školstva Slovenskej republiky
 Ministerstvo školstva Slovenskej republiky Metodické usmernenie č. 4/2009-R z 11. februára 2009 k zavedeniu jednotného postupu škôl, školských zariadení a vysokých škôl pri vzniku registrovaného školského
Ministerstvo školstva Slovenskej republiky Metodické usmernenie č. 4/2009-R z 11. februára 2009 k zavedeniu jednotného postupu škôl, školských zariadení a vysokých škôl pri vzniku registrovaného školského
Demonštračné a žiacke pokusy v chémii
 Moderné vzdelávanie pre vedomostnú spoločnosť / Projekt je spolufinancovaný zo zdrojov EÚ RNDr. Helena Vicenová Demonštračné a žiacke pokusy v chémii Osvedčená pedagogická skúsenosť edukačnej praxe Osvedčená
Moderné vzdelávanie pre vedomostnú spoločnosť / Projekt je spolufinancovaný zo zdrojov EÚ RNDr. Helena Vicenová Demonštračné a žiacke pokusy v chémii Osvedčená pedagogická skúsenosť edukačnej praxe Osvedčená
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY
 LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
LABORATORNÍ PRÁCE Č. 6 PRÁCE S PLYNY Mezi nejrozšířenější práce s plyny v laboratoři patří příprava a důkazy oxidu uhličitého CO 2, kyslíku O 2, vodíku H 2, oxidu siřičitého SO 2 a amoniaku NH 3. Reakcí
Návod na používanie súboru na vyhodnotenie testov všeobecnej pohybovej výkonnosti
 Návod na používanie súboru na vyhodnotenie testov všeobecnej pohybovej výkonnosti Na overenie trénovanosti hráčov sa o.i. vykonávajú testy všeobecnej pohybovej výkonnosti. Z hľadiska vyhodnotenia je potrebné
Návod na používanie súboru na vyhodnotenie testov všeobecnej pohybovej výkonnosti Na overenie trénovanosti hráčov sa o.i. vykonávajú testy všeobecnej pohybovej výkonnosti. Z hľadiska vyhodnotenia je potrebné
KARTA BEZPEČNOSTNÝCH ÚDAJOV. Armaflex/Armaduct
 Strana 1 z 5 1 IDENTIFIKÁCIA LÁTKY (PRÍPRAVKU) A SPOLOČNOSTI (PODNIKU) 1.1 Identifikácia prípravku (obchodný názov): 1.1.1 Popis prípravku: pena založená na báze syntetického kaučuku (elastomér) ; v tvare
Strana 1 z 5 1 IDENTIFIKÁCIA LÁTKY (PRÍPRAVKU) A SPOLOČNOSTI (PODNIKU) 1.1 Identifikácia prípravku (obchodný názov): 1.1.1 Popis prípravku: pena založená na báze syntetického kaučuku (elastomér) ; v tvare
LINKA TIESŇOVÉHO VOLANIA
 LINKA TIESŇOVÉHO VOLANIA Koordinačné stredisko integrovaného záchranného systému v Košiciach Ing. Adriana Bobková Európska únia a linka tiesňového volania 112 Rozhodnutie Rady Európskej únie 91/399EEC
LINKA TIESŇOVÉHO VOLANIA Koordinačné stredisko integrovaného záchranného systému v Košiciach Ing. Adriana Bobková Európska únia a linka tiesňového volania 112 Rozhodnutie Rady Európskej únie 91/399EEC
RAKOVICE SYSTÉM DOMÁCEHO KOMPOSTOVANIA
 RAKOVICE SYSTÉM DOMÁCEHO KOMPOSTOVANIA ZÁKLADNÉ ÚDA JE Rakovice sú malá obec v okrese Piešťany. Na jar 2016 sa vedenie obce rozhodlo zefektívniť svoje odpadové hospodárstvo, a to prechodom na model domáceho
RAKOVICE SYSTÉM DOMÁCEHO KOMPOSTOVANIA ZÁKLADNÉ ÚDA JE Rakovice sú malá obec v okrese Piešťany. Na jar 2016 sa vedenie obce rozhodlo zefektívniť svoje odpadové hospodárstvo, a to prechodom na model domáceho
