KONESTAT ALFA, RUCONEST : IMUNOLOGICKÉ ANALÝZY EDUKAČNÍ MATERIÁL PRO ZDRAVOTNICKÉ PRACOVNÍKY/PŘEDEPISUJÍCÍ LÉKAŘE
|
|
|
- Ladislav Holub
- před 8 lety
- Počet zobrazení:
Transkript
1 Edukační materiály KONESTAT ALFA, RUCONEST : IMUNOLOGICKÉ ANALÝZY EDUKAČNÍ MATERIÁL PRO ZDRAVOTNICKÉ PRACOVNÍKY/PŘEDEPISUJÍCÍ LÉKAŘE Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Strana 1 z 13
2 Před předepsáním a podáním přípravku RUCONEST je nutné prostudovat Souhrn údajů o přípravku. Ruconest (konestat alfa), rekombinantní lidský inhibitor C1 esterázy (rhc1inh), pochází z mléka transgenních králíků exprimujících gen kódující lidský C1INH. Jako u jiných intravenózně podávaných bílkovinných přípravků nelze vyloučit hypersenzitivní reakce a před zahájením léčby přípravkem Ruconest nebo v případě, že jsou po podání přípravku Ruconest pozorovány alergické reakce či nedostatečná klinická odpověď, je nutné provést několik opatření. Jedná se o následující opatření: I) Před zahájením léčby přípravkem Ruconest musí anamnéza všech pacientů obsahovat zhodnocení, zda pacient nevykazuje známky a příznaky alergie na králíky. Je možné, že na alergii v rané fázi života si pacient nevzpomene nebo si své alergie na králičí srst není vědom. Lékař musí položit náležité otázky, aby zjistil, zda pacient nemůže alergii na králičí srst mít. Takové otázky mohou zahrnovat: a. Byl/a jste v minulosti v kontaktu s králíky? b. Zaznamenal/a jste při kontaktu s králíky svědění, vyrážku, kýchání, svědění nosu nebo rýmu, červené nebo svědící oči, kašel, dušnost nebo sípání nebo vám jiným způsobem nebylo dobře? Pokud je odpověď na druhou otázku kladná, je nutné zvážit alternativní léčbu nekráličího původu. II) Je důležité, aby ošetřující lékař pacienty důkladně obeznámil s příznaky hypersenzitivity nebo alergie (kopřivka, generalizovaná kopřivka, pocit tíže na hrudi, sípání, hypotenze a anafylaxe) a ujistil se, že si pacienti uvědomují závažnost těchto příznaků a v případě jejich objevení lékaře okamžitě kontaktují. III) Upozornění na to, že je nutné okamžitě hlásit jakékoli alergické reakce na králíky, je nutné pacientům pravidelně opakovat. IV) Pokud je pacientům přípravek Ruconest předepsán, je potřeba jim dát Kartu pacienta a příbalovou informaci přípravku. V případě vážné hypersenzitivity/nežádoucích imunologických reakcí po podání přípravku Ruconest musí tuto skutečnost lékaři hlásit prostřednictvím národního systému hlášení nežádoucích účinků a také místnímu zástupci pro Ruconest nebo firmě Pharming prostřednictvím u. Podrobnosti uvádí tabulka níže: Strana 2 z 13
3 Národní systém pro hlášení nežádoucích účinků Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí být hlášeno Státnímu ústavu pro kontrolu léčiv. Podrobnosti o hlášení najdete na: Lokální zástupce: Phone: E mail: pharmacovigilance@pharmin.sk safety@pharming.com Adresa pro zasílání je: Státní ústav pro kontrolu léčiv, oddělení farmakovigilance, Šrobárova 48, Praha 10, , farmakovigilance@sukl.cz Ruconest je biologický léčivý přípravek, na hlášení je třeba doplnit i přesný obchodní název a číslo šarže. Úvod Léčivou látkou v přípravku Ruconest je rekombinantní lidský C1 inhibitor (rhc1inh) (konestat alfa). Sekvence aminokyselin rekombinantní formy je identická se sekvencí endogenního lidského C1INH. Ruconest je vytvářen v králičích buňkách prsních žláz a purifikován z mléka transgenních králíků exprimujících gen kódující C1INH. Ačkoli byl proces purifikace navržen tak, aby v maximální možné míře eliminoval nečistoty pocházející z hostitelského organismu (HRI) s původem v králičím mléku, přípravek Ruconest obsahuje stopy králičích bílkovin. Rekombinantní bílkovinné přípravky jako Ruconest mohou vyvolat protilátky proti rekombinantní bílkovině a jejímu endogennímu protějšku i proti nečistotám pocházejícím z hostitelského organismu (HRI). Jako u jiných intravenózně podávaných bílkovinných přípravků nelze vyloučit hypersenzitivní reakce. Před zahájením léčby přípravkem Ruconest je nutné u pacientů zjistit, zda netrpí prokázanou alergií na králíky nebo podezřením na ni. V takovém případě je nutné zvážit alternativní léčbu nekráličího původu. Pacienti musí být důkladně monitorováni a pečlivě sledováni, zda nevykazují příznaky hypersenzitivity během a ihned po podávání přípravku. V případě anafylaktických reakcí nebo šoku je nutné poskytnout rychlou lékařskou pomoc. Strana 3 z 13
4 Léčbu přípravkem Ruconest je nutné zahájit pod dohledem lékaře, který má s diagnózou a léčbou vrozeného angioedému zkušenosti, a musí být podávána zdravotnickým pracovníkem. Možným imunologickým reakcím souvisejícím s přípravkem Ruconest se věnují tři kapitoly: 1. Hypersenzitivita typu I (okamžitá nebo anafylaktická reakce), 2. Neutralizující protilátky (způsobí snížení účinnosti), 3. Hypersenzitivita typu III (hypersenzitivita způsobená imunokomplexy). Každá z těchto kapitol se věnuje: mechanizmům zapojeným v těchto reakcích, faktům a poznatkům dokládajícím riziko, testům, kterých lze využít k prevenci takovýchto reakcí, nebo testům, které jsou k dispozici pro vyšetření příhod, u nichž existuje podezření na imunologický základ, léčbě a jejím důsledkům. 1 HYPERSENZITIVITA TYPU I (okamžitá nebo anafylaktická reakce) Mechanizmus: Hypersenzitivita typu I se může projevovat jako kopřivka, zánět spojivek, rinitida, dušnost nebo šok a je zprostředkována IgE protilátkami. Hypersenzitivitu typu I může být obtížné odlišit od vrozeného angioedému. IgE protilátky jsou indukovány předchozím vystavením se antigenům stejným nebo podobným těm, které reakci spustily. Například: Pacienti alergičtí na králíky mohou mít preexistující IgE protilátky, které mohou reagovat na stopy nečistot králičí bílkoviny v přípravku Ruconest. Fakta: V rámci programu klinické studie přípravku Ruconest bylo 180 subjektům podáno více než 500 dávek přípravku Ruconest. U jednoho zdravého dobrovolníka se po prvním podání přípravku Ruconest projevila hypersenzitivní reakce typu I. U tohoto subjektu nebyla odhalena preexistující alergie na králíky. Mezitím bylo v klinických studiích s přípravkem Ruconest podáno více než dávek bez dalších hlášení vážné hypersenzitivity/anafylaktických reakcí. Anamnéza: Z důvodu rizika možných alergických reakcí je přípravek Ruconest kontraindikován u pacientů se známou nebo předpokládanou alergií na králíky nebo s pozitivními sérovými IgE protilátkami proti králičí srsti a proto: Strana 4 z 13
5 Před zahájením léčby přípravkem Ruconest je nutné vyhodnotit minulost a aktuální anamnézu všech pacientů a zaměřit se na známou alergii na králíky nebo podezření na ni. Před zahájením léčby přípravkem Ruconest musí být všichni pacienti vyšetřeni na přítomnost IgE protilátek proti králičímu epitelu (srsti). Přípravkem Ruconest mohou být léčeni pouze pacienti, u nichž byly výsledky takového testu negativní. Pacienti musí obdržet pacientskou kartu dokládající negativní výsledek. Informace o vhodné metodice pro laboratorní vyšetření sérových IgE protilátek proti králičímu epitelu (srsti)jsou uvedeny v Souhrnu údajů standartního operačního postupu kožního testu (Skin Prick Test). Vyšetření IgE protilátek je třeba opakovat jednou ročně nebo po 10 podáních, podle toho, co nastane dříve. Dále je třeba vyšetření IgE protilátek zopakovat, pokud se objeví příznaky alergie na králíky. Pacienti s klinicky prokázanou alergií na kravské mléko mohou mít protilátky zkříženě reagující s nečistotami králičího mléka v přípravku Ruconest. Léčba: U pacientů léčených přípravkem Ruconest je potřeba sledovat, zda během a ihned po podávání přípravku nevykazují klinické známky a příznaky hypersenzitivity. V případě anafylaktických reakcí nebo šoku je nutné poskytnout rychlou lékařskou pomoc. Je důležité pacienty obeznámit s časnými známkami hypersenzitivních reakcí, mezi které patří kopřivka, generalizovaná kopřivka, pocit tíže na hrudi, dušnost, hypotenze a anafylaxe, a poučit je, že pokud se některý z těchto příznaků objeví, musí okamžitě upozornit svého lékaře. Pacientům je nutné opakovaně připomínat, aby hlásili jakékoli alergické reakce na králíky (např. při nejbližší návštěvě ošetřujícího lékaře). Je také důležité vysvětlit pacientovi rozdíl mezi záchvatem vrozeného angioedému a hypersenzitivní reakcí. Pokud existuje podezření na hypersenzitivitu typu I na přípravek Ruconest nebo se objeví příznaky alergie, pacienti musí okamžitě ukončit léčbu přípravkem Ruconest. Je nutné zvážit jiné možnosti léčby nekráličího původu. 2 NEUTRALIZUJÍCÍ PROTILÁTKY (ZPŮSOBÍ SNÍŽENÍ ÚČINNOSTI) Mechanizmus: Vznik neutralizujících protilátek proti C1INH může snížit hladiny funkčního C1INH a způsobit nízkou klinickou odpověď (níže jsou uvedena kritéria, která mohou vést k imunologickému testování). Pokud by se protilátky vázaly na endogenní C1INH, byl by klinický stav srovnatelný se stavem získaného angioedému (AAE), což je vzácné onemocnění obvykle Strana 5 z 13
6 způsobené přítomností neutralizujících protilátek proti endogennímu C1INH, vytvořených lymfomem nebo spojených s autoimunitním onemocněním. Fakta: Během klinické studie byly odebrány vzorky plazmy před i po podání přípravku. Přítomnost protilátek proti C1INH ve vzorcích plazmy byla prověřena použitím 6 různých analýz ELISA (Enzyme Linked Immuno Sorbent Assays imunoanalýza s vázaným enzymem na imunosorbent), s jejichž pomocí byly zjištěny IgM, IgG a IgA protilátky proti pdc1inh a proti rhc1inh (výsledky IgG protilátek jsou uvedeny na obrázku níže). Výsledek analýzy Na obrázku jsou uvedeny počty IgG protilátek proti rhc1inh u pacientů s vrozeným angioedémem před 1. podáním rhc1inh a po podání rhc1inh. Vodorovná červená čára představuje hraniční úroveň analýzy ELISA. Poslední sloupec je souhrnem všech poexpozičních vzorků od subjektů, kteří dostali mezi 6 až 26 podáními přípravku. Vzorky plazmy s hodnotami přesahujícími hraniční úroveň byly testovány na neutralizující protilátky proti C1INH. Výsledky jsou shrnuty následovně: Nebyly pozorovány žádné trvalé protilátkové odpovědi na pdc1inh ani na rhc1inh. Nebyly nalezeny žádné neutralizující protilátky proti C1INH. Testy: Klinické podezření na neutralizující protilátky může mít počátek v nízké klinické odpovědi: Strana 6 z 13
7 (a) A/NEBO (b) V případě dvou po sobě jdoucích akutních záchvatů angioedému u pacientů s vrozeným angioedémem, kteří dříve reagovali na léčbu přípravkem Ruconest o velikosti dávky 50 j./kg; nutnost dvou dávek přípravku Ruconest, aby byl záchvat léčen. V případě dvou po sobě jdoucích akutních záchvatů angioedému u pacientů s vrozeným angioedémem, kteří dříve reagovali na léčbu přípravkem Ruconest o velikosti dávky 50 j./kg; žádná reakce na léčbu přípravkem Ruconest během 4 hodin navzdory adekvátnímu dávkování 50 j./kg. Prvním doporučovaným diagnostickým krokem je změření aktivity funkčního C1INH 15 minut po infuzi dávky o velikosti 50 j./kg přípravku Ruconest. Koncentrace >0,7 j./ml vylučuje přítomnost klinicky významných neutralizujících protilátek. Společnost Pharming Technologies B.V. poskytuje přístup k programu imunologických laboratorních vyšetření pro sledování vzniku podezřelých neutralizujících protilátek. Tato vyšetření budou poskytnuta zdarma. Tento program by měl být zvážen u pacientů s vrozeným angioedémem, kteří splňují kritéria (a) nebo (b) uvedená výše a u kterých funkční C1INH 15 minut po infuzi dávky o velikosti 50 j./kg přípravku Ruconest nedosáhl hodnoty >0,7 j./ml (viz výše): O testovací soupravu můžete požádat odesláním u na adresu medicalinfo@pharming.com. Odběr vzorku plazmy a postupy expedice jsou podrobně popsány v DODATKU A. Vzorky budou testovány podle následujícího algoritmu: Testy ELISA odhalují přítomnost IgG a IgM protilátek proti rhc1inh. Tyto testy jsou založeny na vázání těchto protilátek na imobilizovaný rhc1inh. Pokud budou výsledné hodnoty některého z testů na protilátky proti rhc1inh přesahovat hraniční úroveň, bude proveden potvrzující test odchylky, aby bylo možné rozlišit specifické a nespecifické odpovědi. Pokud budou specifické protilátky potvrzeny, bude prostřednictvím analýzy neutralizačních protilátek testována schopnost těchto protilátek neutralizovat funkční pdc1inh. Úplná strategie testování podezřelých neutralizačních protilátek je shrnuta v rozpisu níže. Strana 7 z 13
8 Léčba: Klinický obraz a možnosti léčby pacientů s neutralizujícími protilátkami by byly jako u pacientů se získaným angioedémem (AAE). Akutní záchvaty získaného angioedému obvykle vyžadují vyšší dávky C1INH než záchvaty vrozeného angioedému. Podání C1INH je možnou léčbou v případě život ohrožujícího záchvatu získaného angioedému. Kromě podpůrné léčby, jakou je například intubace v případě život ohrožujících záchvatů, lze také zvážit léčbu icatibantem. 3 HYPERSENZITIVITA TYPU III (hypersenzitivita způsobená imunokomplexy) Mechanizmus: Tvorba protilátek proti C1INH nebo proti nečistotám pocházejícím z hostitelského organismu (HRI) může vyústit v hypersenzitivitu typu III. Reakce zprostředkovaná imunokomplexy může být generalizována nebo se může týkat jednotlivých orgánů (příznaky transfuzní reakce nebo sérová nemoc). Fakta: Během klinické studie byly odebrány vzorky plazmy před i po podání přípravku. Kromě screeningu protilátek proti C1INH popsanému výše byla analýza ELISA použita také ke zjištění přítomnosti IgM, IgG i IgA protilátek proti nečistotám pocházejícím z hostitelského organismu (HRI) (výsledky jsou uvedeny na obrázku níže). Strana 8 z 13
9 Na obrázku je uvedena analýza protilátek proti nečistotám pocházejícím z hostitelského organismu (HRI) u symptomatických pacientů s vrozeným angioedémem po opakovaném podání rhc1inh. Červená čára představuje hraniční úroveň analýzy ELISA. Poslední sloupec je souhrnem všech poexpozičních vzorků od subjektů, kteří dostali mezi 6 až 26 podáními přípravku. Vzorky plazmy označené při screeningu analýzou ELISA jako pozitivní byly testovány v potvrzující analýze odchylky. Výsledky jsou shrnuty následovně: Nebyly pozorovány žádné trvalé protilátkové odpovědi na C1INH. U některých pacientů byly zjištěny hodnoty protilátek proti nečistotám pocházejícím z hostitelského organismu (HRI) přesahující hraniční úroveň, ale nebyly spojeny s žádnými klinickými příznaky imunologické reakce. Testy: Společnost Pharming Technologies B.V. poskytuje přístup k programu imunologických laboratorních vyšetření, která dále zkoumají podezřelé hypersenzitivní reakce. Tato vyšetření budou poskytnuta zdarma. Tento program by měl být zvážen u pacientů s vrozeným angioedémem, kteří splňují kritéria (c) nebo (d) uvedená níže: (c) (d) Hypersenzitivní reakce typu III (příznaky s projevy na kůži, kloubech nebo ledvinách) vzniklá během dní nebo týdnů následujících po podání přípravku Ruconest, která nemůže být po prošetření dalších příčin zcela vysvětlena expozicí dalším antigenům a reakcí na ně. Hypersenzitivní reakce typu III ve dvou po sobě jdoucích projevech během dní nebo týdnů následujících po podání přípravku Ruconest. O testovací soupravu můžete požádat odesláním u na adresu medicalinfo@pharming.com. Odběr vzorku plazmy a postupy expedice jsou podrobně popsány v Dodatku A Strana 9 z 13
10 Vzorky budou testovány podle následujícího algoritmu: Testy ELISA odhalují přítomnost IgG a IgM protilátek proti rhc1inh. Tyto testy jsou založeny na vázání těchto protilátek na imobilizovaný rhc1inh. Pokud budou výsledné hodnoty některého z testů na protilátky proti rhc1inh přesahovat hraniční úroveň, bude proveden potvrzující test odchylky, aby bylo možné rozlišit specifické a nespecifické odpovědi. Další analýza ELISA odhalí přítomnost celkového množství imunoglobulinu proti nečistotám pocházejícím z hostitelského organismu (HRI). Tato analýza ELISA anti-hri eluát SP měří vázání protilátek na antigeny získané v prvním kroku purifikace výrobního postupu (eluát SP). Proto je tato analýza velmi specifická a citlivá na nečistoty pocházející z hostitelského organismu (HRI) v přípravku Ruconest. Pokud jsou při vyšetření anti-hri eluát SP pozorovány hodnoty přesahující hraniční úroveň, bude na vzorku proveden potvrzující test odchylky, aby bylo možné rozlišit specifické a nespecifické odpovědi. Úplná strategie testování suspektní hypersenzitivity typu III na přípravek Ruconest je shrnuta v rozpisu níže. Léčba: Pozitivní výsledky vyšetření protilátek by měly zamezit veškeré další léčbě přípravkem Ruconest. Akutní symptomatická léčba senzitivity typu III zahrnuje protizánětlivé látky. Strana 10 z 13
11 4 DODATEK A ODBĚR VZORKU PLAZMY A POSTUPY EXPEDICE. Pro pacienty s podezřením na výskyt neutralizujících protilátek nebo hypersenzitivitu typu III na přípravek Ruconest a splňující kritéria specifikovaná ve vzdělávacích materiálech bude testovací souprava k imunologické analýze přípravku Ruconest odeslána na požádání a bude obsahovat: 8 štítků, 2 zkumavky s citrátem, 4 kryozkumavky, instrukce k odběru vzorků plazmy (uvedeny níže), ové upozornění na odběr vzorků. INSTRUKCE K ODBĚRU VZORKŮ PLAZMY: Před odběrem vzorků krve vyplňte údaje o pacientovi a datum, které je potřeba uvést na štítek. Naberte 4,5 ml krve do zkumavky s citrátem za použití standardní venepunkce. Tuto zkumavku s citrátem označte identifikačním štítkem pacienta ve vodorovném směru, nikoli podélném. Vzorek centrifugujte při pokojové teplotě rychlostí 1000 x g (přibližně 2000 ot./m) po dobu minut, aby se plazma oddělila od červených krvinek. Označte kryozkumavky identifikačním štítkem pacienta ve vodorovném směru. Odeberte plazmu (supernatant) a přeneste 2 x 0,75 ml plazmy do označených kryozkumavek. Vzorky plazmy (2 kryozkumavky x 0,75 ml) co nejdříve zmrazte a uskladněte ve svislé poloze při teplotě rovné nebo nižší než -70 C Podle standardních místních postupů zlikvidujte zbývající plazmu. EXPEDICE VZORKŮ PLAZMY: Po odeslání ového upozornění na odběr vzorků vás kontaktuje kurýrní služba, aby se s vámi domluvila na vyzvednutí vzorků. Strana 11 z 13
12 Souhrn údajů standardního operačního postupu kožního testu (Skin Prick Test) ÚVOD Tento souhrn popisuje postup provedení kožního testu (Skin Prick test - SPT). SPT je prováděn buď na volární straně předloktí, nebo na vnější straně paže. Plná koncentrace (150 U/ml) a ředění 1:10 přípravku Ruconest se připravuje se sterilní vodou na injekci. SPT se zředěným roztokem přípravku Ruconest 1:10, extraktem kravského mléka, králičí srsti, pozitivní kontrolou (histamin 10 mg/ ml) a negativní kontrolou (fyziologický roztok), vše ALK- ABELLO, Nieuwegein, Nizozemí, je odečítán minut po aplikaci. Pozitivní kožní reakce je definována v porovnání s negativní kontrolou jako otok o velikosti 3 mm a větší. Pokud je výsledek SPT se zředěným roztokem přípravku Ruconest 1:10 negativní, provede se SPT s plnou koncentrací přípravku, a po se odečte výsledek. U pacientů s anamnézou anafylaktoidní reakce na králíky nebo kravské mléko (králičí srst nebo extrakt kravského mléka) musí být provedeno ředění dle standardní praxe (nejprve 1:100, pokud je negativní, následuje 1:10, při opětovném negativním výsledku standardní roztok). Kožní reakce bude považována za pozitivní, pokud je otok stejný nebo větší než pozitivní kontrola. Rozměry pozitivních reakcí budou zaznamenány. POPIS POSTUPU Pacient musí být v pohodlné pozici, s předloktím ve vhodné výšce pro provedení testu. Po přípravě vybrané oblasti, buď na volární straně předloktí, nebo na vnější straně paže jsou aplikovány kapky alergenů (extrakt kravského mléka a králičí srst) a rhc1inh ve vzestupném ředění a pozitivní/negativní kontrola ve 2 cm rozestupech od sebe (a od pásky), aby nedošlo ke smíchání alergenů. Pro identifikaci alergenů se použije lepicí páska s čísly a bodnutí musí být provedeno v blízkosti číslic, aby nedošlo k záměně alergenů. Pro každý alergen se použije nová epikutánní lanceta, aby se zabránilo kontaminaci. Přebytečná tekutina se vysaje. Lanceta propíchne kapku, epidermis a vrchní škáru směrem kolmo ke kůži, ale nepronikne příliš hluboko. ZÁZNAM KOŽNÍCH REAKCÍ Obvod otoku se vyznačí fixem a obtiskne na pásku, aby byl výsledek uchován nastálo. Pásku je třeba přitlačit prstem, aby byly otisky fixem viditelné. Páska se založí do dokumentace pacienta, měření může být provedeno průhledným pravítkem označeným mm. Průměr otoku musí být zaznamenán číselně, ne kvalitativními značkami (např. +, ++), jelikož takové značení může být vysoce variabilní. Pokud je otok kulatý, stačí zaznamenat průměr (v mm), pokud je otok nepravidelný, je třeba změřit nejdelší a nejkratší osu, čísla sečíst a vydělit 2 (střední průměr). Strana 12 z 13
13 VÝSLEDKY Jelikož je reakce na histamin rychlejší než na alergenové extrakty a lokální reakce se ke konci sledování vytrácejí, optimální čas pro odečet kožních reakcí je v době, kdy se kožní reakce každého alergenu projevuje nejvýrazněji. Pozitivní reakce SPT je střední průměr (střední v horizontálním a vertikálním průměru), který přesahuje negativní kontrolu o nejméně 3 mm. Strana 13 z 13
Ruconest : imunologické analýzy září 2010
 RUCONEST : IMUNOLOGICKÉ ANALÝZY, NEPROPAGAČNÍ VZDĚLÁVACÍ MATERIÁLY PRO PŘEDEPISUJÍCÍ LÉKAŘE Poznámka: Tyto informace budou poskytnuty předepisujícím lékařům. Shrnutí Ruconest (konestat alfa), rekombinantní
RUCONEST : IMUNOLOGICKÉ ANALÝZY, NEPROPAGAČNÍ VZDĚLÁVACÍ MATERIÁLY PRO PŘEDEPISUJÍCÍ LÉKAŘE Poznámka: Tyto informace budou poskytnuty předepisujícím lékařům. Shrnutí Ruconest (konestat alfa), rekombinantní
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE
 EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ruconest 2100 j. prášek pro přípravu injekčního roztoku. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje 2100 jednotek conestatum
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ruconest 2100 j. prášek pro přípravu injekčního roztoku. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje 2100 jednotek conestatum
PRŮKAZ PACIENTA. užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019
 PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
EDUKAČNÍ MATERIÁL - Pioglitazone Accord
 Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ruconest 2100 j. prášek pro injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje conestatum alfa 2100 jednotek,
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ruconest 2100 j. prášek pro injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje conestatum alfa 2100 jednotek,
PRŮKAZ PACIENTA. užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1
 PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
INFLECTRA SCREENINGOVÝ LIST. a výběru pacientů pro všechny schválené indikace. Obsahuje pokyny ke správnému screeningu
 Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Edukační materiály. KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře
 Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Pioneer in Rare Diseases. Pozvánka na satelitní sympozium společnosti SOBI. Co přináší Fc technologie do léčby dětských pacientů s hemofilií A i B?
 Pioneer in Rare Diseases Pozvánka na satelitní sympozium společnosti SOBI Co přináší Fc technologie do léčby dětských pacientů s hemofilií A i B? Vážená paní doktorko, vážený pane doktore, dovolte, abychom
Pioneer in Rare Diseases Pozvánka na satelitní sympozium společnosti SOBI Co přináší Fc technologie do léčby dětských pacientů s hemofilií A i B? Vážená paní doktorko, vážený pane doktore, dovolte, abychom
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin. Informace pro lékaře EU
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
Jakou změnu přináší přípravky s prodlouženým účinkem v profylaxi pacientů s hemofilií A/B?
 pozvánka na satelitní sympozium společnosti Sobi Jakou změnu přináší přípravky s prodlouženým účinkem v profylaxi pacientů s hemofilií A/B? Vážená paní doktorko, vážený pane doktore, dovolte, abychom Vás
pozvánka na satelitní sympozium společnosti Sobi Jakou změnu přináší přípravky s prodlouženým účinkem v profylaxi pacientů s hemofilií A/B? Vážená paní doktorko, vážený pane doktore, dovolte, abychom Vás
Rozměr zavřeného průkazu mm
 Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Poznámka: Tyto úpravy souhrnu údajů o přípravku a
 PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
Návod pro pacienta / pečovatele
 Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
EDUKAČNÍ MATERIÁLY. Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce
 EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
Hemlibra (emicizumab) Subkutánní injekce. Návod pro zdravotnické pracovníky
 EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Nebido EDUKAČNÍ MATERIÁL. Jak úspěšně aplikovat přípravek. (testosterone undecanoate)
 EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Edukační materiál. Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera
 Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Zvažte oddálení podání regadenosonu u pacientů s nekontrolovanou hypertenzí.
 CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
EDUKAČNÍ MATERIÁLY. KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1
![Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1 Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1](/thumbs/102/154291766.jpg) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ruconest 2100 j. prášek pro injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje conestatum alfa 2100 jednotek,
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Ruconest 2100 j. prášek pro injekční roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje conestatum alfa 2100 jednotek,
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH)
 Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
alergie na složky potravy SVOBODA Petr Ambulance estetické dermatologie, Pekařská 3, Brno
 alergie na složky potravy SVOBODA Petr Ambulance estetické dermatologie, Pekařská 3, 602 00 Brno alergie na potraviny - definice Imunologicky zprostředkovaný vedlejší účinek po požití potravy. alergie
alergie na složky potravy SVOBODA Petr Ambulance estetické dermatologie, Pekařská 3, 602 00 Brno alergie na potraviny - definice Imunologicky zprostředkovaný vedlejší účinek po požití potravy. alergie
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Edukační materiál. Yervoy (ipilimumab) Časté otázky Brožura pro. zdravotníky
 Edukační materiál Yervoy (ipilimumab) Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Tento léčivý
Edukační materiál Yervoy (ipilimumab) Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Tento léčivý
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
PŘÍLOHA VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ ZAMÍTNUTÍ ŽÁDOSTI O ROZHODNUTÍ O REGISTRACI PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY
 PŘÍLOHA VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ ZAMÍTNUTÍ ŽÁDOSTI O ROZHODNUTÍ O REGISTRACI PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY VĚDECKÉ ZÁVĚRY Dne 20. července 2006 předložila společnost Pharming
PŘÍLOHA VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ ZAMÍTNUTÍ ŽÁDOSTI O ROZHODNUTÍ O REGISTRACI PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY VĚDECKÉ ZÁVĚRY Dne 20. července 2006 předložila společnost Pharming
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
Praxbind doporučení pro podávání (SPC)
 Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
BAVENCIO (avelumab) Váš průvodce informacemi pro pacienta
 Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Použití komponent v diagnostice alergií
 Použití komponent v diagnostice alergií RNDr. Petr Šotkovský, Ph.D. Tel.: +420 724 756 980 Email: petr.sotkovsky@thermofisher.com ImmunoCAP Směsi 80 Extrakty přes 600 Komponenty přes 100 Značení komponent
Použití komponent v diagnostice alergií RNDr. Petr Šotkovský, Ph.D. Tel.: +420 724 756 980 Email: petr.sotkovsky@thermofisher.com ImmunoCAP Směsi 80 Extrakty přes 600 Komponenty přes 100 Značení komponent
Jedna předplněná injekční stříkačka obsahuje immunoglobulinum humanum anti-d 1500 IU (300 mikrogramů).
 sp. zn. sukls262204/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Igamad 1500 IU, injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
sp. zn. sukls262204/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Igamad 1500 IU, injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
Familiární středomořská (Mediterranean) horečka (Fever)
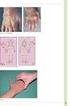 www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
NeuroBloc. botulinový toxin typu B injekční roztok, U/ml
 NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
MUDr Zdeněk Pospíšil
 MUDr Zdeněk Pospíšil Imunita Charakteristika-soubor buněk,molekul a humorálních faktorů majících schopnost rozlišit cizorodé látky a odstranit je /rozeznává vlastní od cizích/ Zajišťuje-homeostazu,obranyschopnost
MUDr Zdeněk Pospíšil Imunita Charakteristika-soubor buněk,molekul a humorálních faktorů majících schopnost rozlišit cizorodé látky a odstranit je /rozeznává vlastní od cizích/ Zajišťuje-homeostazu,obranyschopnost
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls12350/2006 a příloha k sp zn. sukls41484/2007, sukls49174/2008
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls12350/2006 a příloha k sp zn. sukls41484/2007, sukls49174/2008 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Rhesonativ 625 IU/ml, injekční
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls12350/2006 a příloha k sp zn. sukls41484/2007, sukls49174/2008 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV PŘÍPRAVKU Rhesonativ 625 IU/ml, injekční
EXELON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY
 XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
XLON NÁPLASTI NÁVOD K POUŽITÍ & ZÁZNAMOVÁ KARTA VAŠÍ LÉČBY Než se začnete léčit přípravkem xelon náplasti, přečtěte si pozorně celou příbalovou informaci požádejte někoho, aby Vám ji celou přečetl. Případné
Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel)
 EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
Alergie na bílkovinu kravského mléka (ABKM) 6
 Doporučení Pracovní skupiny dětské gastroenterologie a výživy ČPS pro výživu kojenců a batolat Alergie na bílkovinu kravského mléka (ABKM) 6 1 2 3 4 ABKM je nejčastější potravinová alergie u dětí do 3
Doporučení Pracovní skupiny dětské gastroenterologie a výživy ČPS pro výživu kojenců a batolat Alergie na bílkovinu kravského mléka (ABKM) 6 1 2 3 4 ABKM je nejčastější potravinová alergie u dětí do 3
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
sp.zn. sukls221052/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1 g očních kapek Pomocná
Důležité informace pro pacienty
 MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
dnavou artritidou (GA)
 EDUKAČNÍ MATERIÁLY ILARIS (kanakinumab) Průvodce pro lékaře k používání přípravku Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
EDUKAČNÍ MATERIÁLY ILARIS (kanakinumab) Průvodce pro lékaře k používání přípravku Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
Příbalová informace: informace pro uživatele
 sp.zn. sukls55434/2017 Příbalová informace: informace pro uživatele Kybernin P 500 IU prášek a rozpouštědlo pro injekční/infuzní roztok Kybernin P 1000 IU prášek a rozpouštědlo pro injekční/infuzní roztok
sp.zn. sukls55434/2017 Příbalová informace: informace pro uživatele Kybernin P 500 IU prášek a rozpouštědlo pro injekční/infuzní roztok Kybernin P 1000 IU prášek a rozpouštědlo pro injekční/infuzní roztok
Odběry vzorků u pacientů s podezřením na infekci krevního řečiště
 Odběry vzorků u pacientů s podezřením na infekci krevního řečiště Eva Krejčí Centrum klinických laboratoří, Zdravotní ústav se sídlem v Ostravě Lékařská fakulta Ostravské univerzity Infekce krevního řečiště
Odběry vzorků u pacientů s podezřením na infekci krevního řečiště Eva Krejčí Centrum klinických laboratoří, Zdravotní ústav se sídlem v Ostravě Lékařská fakulta Ostravské univerzity Infekce krevního řečiště
* Přípravek MabThera s.c. je indikován pouze k léčbě dospělých pacientů s non-hodgkinským lymfomem (NHL):
 Tyto edukační materiály týkající se bezpečného a účinného používání přípravku MabThera 1 400 mg roztoku pro subkutánní injekci (dále jen MabThera s.c.) je příručkou pro lékaře, zdravotní sestry a lékárníky.
Tyto edukační materiály týkající se bezpečného a účinného používání přípravku MabThera 1 400 mg roztoku pro subkutánní injekci (dále jen MabThera s.c.) je příručkou pro lékaře, zdravotní sestry a lékárníky.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
sp.zn. sukls171995/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte
Veronika Janů Šárka Kopelentová Petr Kučera. Oddělení alergologie a klinické imunologie FNKV Praha
 Veronika Janů Šárka Kopelentová Petr Kučera Oddělení alergologie a klinické imunologie FNKV Praha interakce antigenu s protilátkou probíhá pouze v místech epitopů Jeden antigen může na svém povrchu nést
Veronika Janů Šárka Kopelentová Petr Kučera Oddělení alergologie a klinické imunologie FNKV Praha interakce antigenu s protilátkou probíhá pouze v místech epitopů Jeden antigen může na svém povrchu nést
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
sp.zn.sukls78453/2015
 sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls78453/2015 Příbalová informace: informace pro uživatele Viru-Merz, 10 mg/g, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Zdravotní deník pro sledování léčby
 Zdravotní deník pro sledování léčby Péče o muže s rakovinou prostaty Proč bych měl být sledován pravidelně? Lékaři mi nedávno zjistili rakovinu prostaty, se kterou se budu dlouhodobě léčit. Můj lékař zvolil
Zdravotní deník pro sledování léčby Péče o muže s rakovinou prostaty Proč bych měl být sledován pravidelně? Lékaři mi nedávno zjistili rakovinu prostaty, se kterou se budu dlouhodobě léčit. Můj lékař zvolil
Příbalová informace: informace pro uživatele. VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa
 Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Příbalová informace: informace pro uživatele VPRIV 400 jednotek prášek pro infuzní roztok velaglucerasum alfa Přečtěte si pozorně celou příbalovou informaci před použitím tohoto přípravku, protože obsahuje
Souhrn údajů o přípravku
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls19325/2006 Souhrn údajů o přípravku 1. NÁZEV PŘÍPRAVKU TYPHERIX 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna dávka vakcíny (0,5 ml) obsahuje 25
Indikační kritéria pro imunoterapii hmyzími jedy. M. Vachová, P. Panzner a kol. ÚIA FN Plzeň
 Indikační kritéria pro imunoterapii hmyzími jedy M. Vachová, P. Panzner a kol. ÚIA FN Plzeň 1. Alergie na jed blanokřídlého hmyzu. 2. Imunoterapie hmyzím jedem. 3. Indikační kritéria imunoterapie. Doporučený
Indikační kritéria pro imunoterapii hmyzími jedy M. Vachová, P. Panzner a kol. ÚIA FN Plzeň 1. Alergie na jed blanokřídlého hmyzu. 2. Imunoterapie hmyzím jedem. 3. Indikační kritéria imunoterapie. Doporučený
Složení vakcíny odpovídá doporučení SZO (pro severní polokouli) a EU rozhodnutí pro sezónu2007/2008
 Příbalová informace - RP Informace pro použití, čtěte pozorně! Begrivac (vakcína proti chřipce) Injekční suspenze Sezóna 2007/2008 Držitel rozhodnutí o registraci a výrobce Novartis Vaccines and Diagnostics
Příbalová informace - RP Informace pro použití, čtěte pozorně! Begrivac (vakcína proti chřipce) Injekční suspenze Sezóna 2007/2008 Držitel rozhodnutí o registraci a výrobce Novartis Vaccines and Diagnostics
s energií 172 kev (91 %) a 246 kev (94 %). Vnitřní konverzí vzniká záření rentgenové s energií 23 kev a 26 kev.
 sp.zn. sukls101319/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Indium (In111) Chloride 370 MBq/ml, radionuklidový prekurzor, roztok 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Obsah lahvičky k datu a
sp.zn. sukls101319/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Indium (In111) Chloride 370 MBq/ml, radionuklidový prekurzor, roztok 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Obsah lahvičky k datu a
EDUKAČNÍ MATERIÁLY. TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM)
 EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
Ferrum. Opakovaná léčba Diafer 50 mg/ml injekčním roztokem je používána k doplnění a udržení zásob železa v těle.
 sp.zn. sukls57833/2014 Příbalová informace: informace pro pacienta 50 mg/ml injekční roztok Ferrum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete
sp.zn. sukls57833/2014 Příbalová informace: informace pro pacienta 50 mg/ml injekční roztok Ferrum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete
Obsah. Několik slov úvodem... 19 Vít Petrů
 Několik slov úvodem...................... 19 Vít Petrů OBECNÁ ČÁST 1 Prevalence astmatu a alergie u dětí a mladistvých.... 25 Jiřina Chládková 1.1 Prevalence průduškového astmatu............ 26 1.2 Prevalence
Několik slov úvodem...................... 19 Vít Petrů OBECNÁ ČÁST 1 Prevalence astmatu a alergie u dětí a mladistvých.... 25 Jiřina Chládková 1.1 Prevalence průduškového astmatu............ 26 1.2 Prevalence
Zkušenosti s laboratorní diagnostikou infekcí virem Zika. Hana Zelená NRL pro arboviry Zdravotní ústav se sídlem v Ostravě
 Zkušenosti s laboratorní diagnostikou infekcí virem Zika Hana Zelená NRL pro arboviry Zdravotní ústav se sídlem v Ostravě Základní charakteristika viru Zika Čeleď Flaviviridae, rod Flavivirus obalený RNA
Zkušenosti s laboratorní diagnostikou infekcí virem Zika Hana Zelená NRL pro arboviry Zdravotní ústav se sídlem v Ostravě Základní charakteristika viru Zika Čeleď Flaviviridae, rod Flavivirus obalený RNA
Příloha IV. Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci
 Příloha IV Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 132 Vědecké závěry Výbor CHMP zvážil níže uvedené doporučení výboru PRAC ze dne 5. prosince 2013 s ohledem na postup podle
Příloha IV Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 132 Vědecké závěry Výbor CHMP zvážil níže uvedené doporučení výboru PRAC ze dne 5. prosince 2013 s ohledem na postup podle
Rozdělení imunologických laboratorních metod
 Rozdělení imunologických laboratorních metod Aglutinace Mgr. Petr Bejdák Ústav klinické imunologie a alergologie Fakultní nemocnice u sv. Anny a Lékařská fakulta MU Rozdělení imunologických laboratorních
Rozdělení imunologických laboratorních metod Aglutinace Mgr. Petr Bejdák Ústav klinické imunologie a alergologie Fakultní nemocnice u sv. Anny a Lékařská fakulta MU Rozdělení imunologických laboratorních
Rekurentní horečka spojená s NRLP21
 www.printo.it/pediatric-rheumatology/cz/intro Rekurentní horečka spojená s NRLP21 Verze č 2016 1. CO JE TO REKURENTNÍ HOREČKA SPOJENÁ S NRLP12 1.1 Co je to? Rekurentní horečka spojená s NRLP12 patří mezi
www.printo.it/pediatric-rheumatology/cz/intro Rekurentní horečka spojená s NRLP21 Verze č 2016 1. CO JE TO REKURENTNÍ HOREČKA SPOJENÁ S NRLP12 1.1 Co je to? Rekurentní horečka spojená s NRLP12 patří mezi
Příbalová informace: informace pro uživatele. ANTITHROMBIN III BAXALTA Prášek a rozpouštědlo pro infuzní roztok Antithrombinum III
 Příbalová informace: informace pro uživatele ANTITHROMBIN III BAXALTA Prášek a rozpouštědlo pro infuzní roztok Antithrombinum III Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele ANTITHROMBIN III BAXALTA Prášek a rozpouštědlo pro infuzní roztok Antithrombinum III Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Mgr. Dagmar Chátalova
 Mgr. Dagmar Chátalova Transfuze - převod lidské krve nebo krevních přípravků od jednoho člověka ( dárce ) do krevního oběhu druhého člověka ( příjemce ) Indikace při ztrátě krve úraz, operace,těžký porod,
Mgr. Dagmar Chátalova Transfuze - převod lidské krve nebo krevních přípravků od jednoho člověka ( dárce ) do krevního oběhu druhého člověka ( příjemce ) Indikace při ztrátě krve úraz, operace,těžký porod,
98/2012 Sb. VYHLÁŠKA. ze dne 22. března 2012
 98/2012 Sb. VYHLÁŠKA ze dne 22. března 2012 o zdravotnické dokumentaci Změna: 236/2013 Sb. Změna: 364/2015 Sb. Změna: XXX/2017 Sb. Ministerstvo zdravotnictví stanoví podle 120 zákona č. 372/2011 Sb., o
98/2012 Sb. VYHLÁŠKA ze dne 22. března 2012 o zdravotnické dokumentaci Změna: 236/2013 Sb. Změna: 364/2015 Sb. Změna: XXX/2017 Sb. Ministerstvo zdravotnictví stanoví podle 120 zákona č. 372/2011 Sb., o
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
Základní informace o interferenci daratumumabu s testy krevní kompatibility
 EDUKAČNÍ MATERÁLY Daratumumab Základní informace o interferenci daratumumabu s testy krevní kompatibility Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERÁLY Daratumumab Základní informace o interferenci daratumumabu s testy krevní kompatibility Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Kelapril 5mg 7x14tbl.
 Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
Organizace transfuzní služby. I.Sulovská
 Organizace transfuzní služby I.Sulovská Transfuzní oddělení Výroba transfuzních přípravků (TP) řízena zákony, vyhláškami a metodickými pokyny 2 druhy TO: výrobci TP odběrová střediska Výrobci TP mají uděleno
Organizace transfuzní služby I.Sulovská Transfuzní oddělení Výroba transfuzních přípravků (TP) řízena zákony, vyhláškami a metodickými pokyny 2 druhy TO: výrobci TP odběrová střediska Výrobci TP mají uděleno
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls158867/2010. Allergena purificita adsorpta (purifikované adsorbované alergeny)
 Příloha č. k rozhodnutí o změně registrace sp.zn. sukls58867/00 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Alutard SQ Allergena purificita adsorpta (purifikované adsorbované alergeny) injekční suspenze
Příloha č. k rozhodnutí o změně registrace sp.zn. sukls58867/00 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE Alutard SQ Allergena purificita adsorpta (purifikované adsorbované alergeny) injekční suspenze
CAVE! Informační dopis pro zdravotnické pracovníky
 CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
ANTITHROMBIN III NF BAXTER Prášek pro přípravu infuzního roztoku s rozpouštědlem Antithrombinum humanum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE ANTITHROMBIN III NF BAXTER Prášek pro přípravu infuzního roztoku s rozpouštědlem Antithrombinum humanum Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE ANTITHROMBIN III NF BAXTER Prášek pro přípravu infuzního roztoku s rozpouštědlem Antithrombinum humanum Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele. Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas
 Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Bricanyl 0,5 mg/ml injekční roztok terbutalini sulfas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
(alemtuzumab 12 mg i.v.)
 EDUKAČNÍ MATERIÁL Pomůcka pro podání přípravku Tento text je pouze doporučením a pomůckou pro podávání léčivého přípravku Lemtrada. Nenahrazuje edukační materiály, které jsou k dispozici pro předepisující
EDUKAČNÍ MATERIÁL Pomůcka pro podání přípravku Tento text je pouze doporučením a pomůckou pro podávání léčivého přípravku Lemtrada. Nenahrazuje edukační materiály, které jsou k dispozici pro předepisující
Jeden ml obsahuje: Proteinum plasmatis humani... 200 mg (čistota minimálně 98% IgG)
 1. NÁZEV PŘÍPRAVKU Hizentra 200 mg/ml injekční roztok k subkutánnímu podání 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale (SCIg) Jeden ml obsahuje: Proteinum plasmatis humani...
1. NÁZEV PŘÍPRAVKU Hizentra 200 mg/ml injekční roztok k subkutánnímu podání 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Immunoglobulinum humanum normale (SCIg) Jeden ml obsahuje: Proteinum plasmatis humani...
2012 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 2 Jak sledovat bezpečnost léčivých přípravků v ČR problémy a výzvy MUDr. Jana Mladá Státní ústav pro kontrolu léčiv 3 O čem dnes? Monitorování bezpečnosti léčivých přípravků Farmakovigilanční systém Chyby
2 Jak sledovat bezpečnost léčivých přípravků v ČR problémy a výzvy MUDr. Jana Mladá Státní ústav pro kontrolu léčiv 3 O čem dnes? Monitorování bezpečnosti léčivých přípravků Farmakovigilanční systém Chyby
DIAQUICK Mononukleóza kazeta z plné krve, séra nebo plazmy
 DIAQUICK Mononukleóza kazeta z plné krve, séra nebo plazmy REF CONT Z06620CE 30 testů individuálně balených 30 jednorázových pipet 1 lahvička s pufrem (pro 30 testů) 2 kontroly (pozitivní a negativní)
DIAQUICK Mononukleóza kazeta z plné krve, séra nebo plazmy REF CONT Z06620CE 30 testů individuálně balených 30 jednorázových pipet 1 lahvička s pufrem (pro 30 testů) 2 kontroly (pozitivní a negativní)
Příloha III. Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Feligen CRP Lyofilizát pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizovaná složka Léčivé
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Feligen CRP Lyofilizát pro přípravu injekční suspenze s rozpouštědlem 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Lyofilizovaná složka Léčivé
ODMÍTAVÉ REAKCE NA POTRAVINY
 ODMÍTAVÉ REAKCE NA POTRAVINY Pavel Rauch Ústav biochemie a mikrobiologie, VŠCHT Praha Týden bezpečnosti potravin, VŠCHT Praha, květen 2006 ALERGIE JAKO MÓDA SOUČASNOSTI 20% POPULACE VĚŘÍ, ŽE MÁ INTOLERANCI
ODMÍTAVÉ REAKCE NA POTRAVINY Pavel Rauch Ústav biochemie a mikrobiologie, VŠCHT Praha Týden bezpečnosti potravin, VŠCHT Praha, květen 2006 ALERGIE JAKO MÓDA SOUČASNOSTI 20% POPULACE VĚŘÍ, ŽE MÁ INTOLERANCI
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA
 sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
sp.zn.sukls49563/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA Kaloba Perorální kapky, roztok Pelargonii sidoidis extractum fluidum (1 : 8 10) (EPs 7630) extrahováno 11% ethanolem (m/m) Přečtěte si
Co je Voltaren Ophtha CD Léčivou látkou přípravku Voltaren Ophtha CD je diklofenak sodný (diclofenacum natricum).
 Příloha č.1 ke sdělení sp.zn.sukls23896/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VOLTAREN OPHTHA CD oční kapky, roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou informaci dříve,
Příloha č.1 ke sdělení sp.zn.sukls23896/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE VOLTAREN OPHTHA CD oční kapky, roztok (diclofenacum natricum) Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro pacienta. Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky
 sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
sp.zn. sukls227576/2009 Příbalová informace: informace pro pacienta Neo-angin bez cukru 1,2 mg/0,6 mg/5,72 mg pastilky alcohol dichlorobenzylicus, amylmetacresolum, levomentholum Přečtěte si pozorně tuto
[ 1 ] MUDr. Jana Mladá. VIII. Vakcinologické dny, Hradec Králové, 6.10.2012 2012 Státní ústav kontrolu léčiv
![[ 1 ] MUDr. Jana Mladá. VIII. Vakcinologické dny, Hradec Králové, 6.10.2012 2012 Státní ústav kontrolu léčiv [ 1 ] MUDr. Jana Mladá. VIII. Vakcinologické dny, Hradec Králové, 6.10.2012 2012 Státní ústav kontrolu léčiv](/thumbs/26/8097174.jpg) [ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Role SÚKL v oblasti regulace vakcín MUDr. Jana Mladá Oddělení farmakovigilance [ 3 ] O čem dnes? Registrace vakcín před uvedením na trh Po uvedení na trh Laboratorní
[ 1 ] Státní ústav pro kontrolu léčiv [ 2 ] Role SÚKL v oblasti regulace vakcín MUDr. Jana Mladá Oddělení farmakovigilance [ 3 ] O čem dnes? Registrace vakcín před uvedením na trh Po uvedení na trh Laboratorní
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
