POKYNY PRO ZDRAVOTNICKÉ PRACOVNÍKY, JAK OMEZIT ZÁVAŽNÁ RIZIKA PŘÍPRAVKU LEMTRADA
|
|
|
- Michaela Havlová
- před 6 lety
- Počet zobrazení:
Transkript
1 EDUKAČNÍ MATERIÁL LEMTRADA POKYNY PRO ZDRAVOTNICKÉ PRACOVNÍKY, JAK OMEZIT ZÁVAŽNÁ RIZIKA PŘÍPRAVKU LEMTRADA Použití přípravku LEMTRADA (alemtuzumab) u pacientů s relabující-remitující roztroušenou sklerózou (RRRS) Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí být hlášeno Státnímu ústavu pro kontrolu léčiv. Podrobnosti o hlášení najdete na: Adresa pro zasílání je Státní ústav pro kontrolu léčiv, oddělení farmakovigilance, Šrobárova 48, Praha 10, , farmakovigilance@sukl.cz. Je třeba doplnit i přesný obchodní název a číslo šarže. Tato informace může být také hlášena společnosti sanofi-aventis, s.r.o.
2 OBSAH 1. Úvod 3 2. Jaká rizika jsou spojena s použitím přípravku LEMTRADA? 5 3. Přehled doporučeného monitorování pacientů 8 4. Péče o pacienty léčené přípravkem Lemtrada 9 5. Další informace 9 6. Nejčastější otázky 10 Přehled informací o přípravku Lemtrada Přípravek LEMTRADA je indikován k léčbě dospělých pacientů s relabující-remitující roztroušenou sklerózou (RRRS) v aktivním stadiu onemocnění definovaném klinickými příznaky nebo nálezem daným zobrazovacími metodami. Tyto pokyny byly vypracovány v rámci plánu řízení rizik (RMP) pro předepisující lékaře a zdravotnické pracovníky (HCP) podílející se na péči o pacienty léčené přípravkem LEMTRADA k zajištění dalších informací ohledně potenciálních závažných rizik spojených s použitím přípravku LEMTRADA. Tyto pokyny obsahují popis okamžitých a pozdních rizik souvisejících s léčbou přípravkem LEMTRADA, které se mohou vyskytnout i mnoho let po léčbě a mohou být závažné nebo život ohrožující, včetně: závažných infekcí autoimunitních stavů, včetně: > poruch štítné žlázy, > imunitní trombocytopenické purpury (ITP), > nefropatií, včetně onemocnění s tvorbou protilátek proti glomerulární bazální membráně (anti-gbm), a doporučené postupy ke zmírnění rizik. Upozorňujeme, že tyto pokyny nezahrnují všechna rizika spojená s použitím přípravku LEMTRADA a nenahrazují Souhrn údajů o přípravku (SPC). Aktuálně platné SmPC lze vyhledat na webových stránkách Státního ústavu pro kontrolu léčiv v databázi léků medication/search.php Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakékoli podezření na nežádoucí účinky. 1. Úvod Přípravek LEMTRADA je indikován k léčbě dospělých pacientů s relabující-remitující roztroušenou sklerózou (RRRS) v aktivním stadiu onemocnění definovaném klinickými příznaky nebo nálezem daným zobrazovacími metodami. LEMTRADA je monoklonální protilátka podávaná nitrožilně. Váže se na CD52, povrchový antigen přítomný ve vysokých hladinách na povrchu T a B lymfocytů, a v menší míře na NK buňkách, monocytech a makrofázích. Mechanismus, jakým přípravek LEMTRADA uplatňuje svůj účinek u RS, není zcela vysvětlen. Výzkumy však ukazují na imunomodulační účinky prostřednictvím deplece a repopulace lymfocytů, včetně: > alterací v počtu, proporcích a vlastnostech některých podskupin lymfocytů po léčbě, > zvýšeného zastoupení podskupin regulačních T buněk, > zvýšeného zastoupení paměťových T a B lymfocytů, > přechodných účinků na složky vrozené imunity (tj. neutrofily, makrofágy, NK buňky). Za terapeutický účinek může odpovídat snížení hladin cirkulujících B a T buněk přípravkem LEMTRADA a jejich následná repopulace. Použití alemtuzumabu je spojeno s rizikem závažných infekcí a autoimunitních stavů. Autoimunitní stavy se mohou objevit i mnoho let po léčbě a z hlediska závažnosti mohou být závažné až život ohrožující. Léčba přípravkem LEMTRADA má být zahájena a sledována neurologem se zkušenostmi v léčbě pacientů s RS. Pro minimalizaci potenciálních rizik a nežádoucích účinků přípravku LEMTRADA je nutné sledování pacienta po dobu 48 měsíců přípravku. Je důležité, aby pacienti vzali na vědomí, že je třeba pokračovat v monitorování, i když se cítí dobře a jejich RS je pod kontrolou. Navození spolupráce mezi Vámi, Vaším pacientem a Vaším zdravotním týmem a pečlivé zvážení, jak používat edukační nástroje pro pacienty, umožní pacientům, aby: Další informace > dodržovali docházku na předepsané periodické vyšetření, > včas identifikovali a hlásili symptomy, > získali včasnou a správnou léčbu v případě potřeby. Kontrolní seznam by měl být použit při zahájení léčby a během následného sledování. Pokyny pro pacienty a Kartu pacienta byste měl/měla předat pacientům před zahájením léčby přípravkem LEMTRADA. Pokyny pro pacienta byste měli spolu s pacientem pečlivě projít před zahájením léčby a také pravidelně během následného sledování. Cílem Karty pacienta je poučit pacienta o příznacích autoimunitních stavů a závažných infekcí a vytvořit pacientovo povědomí o tom, že je třeba 2 LEMTRADA Pokyny pro zdravotnické pracovníky LEMTRADA Pokyny pro zdravotnické pracovníky 3
3 podstupovat pravidelné kontroly, sledovat případně vzniklé symptomy a v případě jejich výskytu neprodleně vyhledat lékařskou pomoc. Karta pacienta je pomůcka informující zdravotnické pracovníky starající se o pacienty léčené přípravkem LEMTRADA. Pacient (nebo jeho opatrovník, pokud potřeba) by měl mít tuto kartu vždy při sobě a vždy ji předložit zdravotnickému pracovníkovi. Pro ilustraci délky účinků léčby a délky požadovaného následného sledování si prosím prostudujte níže uvedené schéma s názvem Přehled léčby přípravkem LEMTRADA a tabulku: Přehled monitorování při léčbě přípravkem LEMTRADA Přehled léčby přípravkem LEMTRADA Tabulka č. 1 Začněte s testováním krve a moči před léčbou *POZNÁMKA: Studie sledující pacienty po dobu 6 let po podání první infuze (cyklus 1) prokázala, že většina pacientů nepotřebuje další léčbu po 2 úvodních léčebných cyklech. Přehled monitorování při léčbě přípravkem LEMTRADA Stav Vyšetření Načasování Imunitní trombocytopenická purpura (ITP) Nefropatie, včetně onemocnění anti- GBM Nefropatie, včetně onemocnění anti- GBM Onemocnění štítné žlázy ÚVODNÍ LÉČBA SE 2 LÉČEBNÝMI CYKLY Cyklus 12 měsíců Cyklus 1 po léčebném 5denní léčba cyklu 1 3denní léčba Nepřetržité sledování po dobu 4 let od ukončení poslední léčby Kompletní krevní obraz a diferenciál 1 měsíčně, Sérový kreatinin 1 měsíčně, Analýza a mikroskopické vyšetření moči Funkční testy štítné žlázy (např. TSH) 2 Nejméně 12 měsíců po léčebném cyklu 2 DALŠÍ LÉČEBNÉ CYKLY PODLE POTŘEBY* Cyklus 3denní léčba Cyklus Nejméně měsíců po léčebném cyklu 3 3denní léčba 1 měsíčně, Každé 3 měsíce, 2. Jaká rizika jsou spojena s použitím přípravku LEMTRADA? Upozorňujeme, že tyto pokyny nezahrnují všechna rizika spojená s použitím přípravku LEMTRADA a nenahrazují Souhrn údajů o přípravku (SPC). Závažné infekce Léčba přípravkem LEMTRADA je spojena s rizikem závažných infekcí. Pro snížení tohoto rizika je důležité: > odložit léčbu, pokud je přítomna aktivní infekce a dokud není vyléčena, > testovat na přítomnost HIV, vyhodnotit riziko aktivní i latentní tuberkulózy dle aktuálních doporučení, testovat výskyt HBV a HCV, > testovat na přítomnost HPV infekce a test každoročně opakovat; zvážit očkování před zahájením léčby, > dokončit plánovaná očkování nejméně 6 týdnů před zahájením léčby, > doporučit dietu, omezující riziko listeriové nákazy 2 týdny před léčbou, během infuze a 1 měsíc po podání infuze, > antiherpetická profylaxe by měla být zahájena první den podání infuze a pokračovat nejméně 1 měsíc po ukončení každého infuzního cyklu, > vyloučit souběžnou léčbu ostatnímu imunomodulačními látkami. Autoimunitní stavy Použití alemtuzumabu je spojeno s rizikem autoimunitních stavů, včetně (seřazeno dle frekvence výskytu): > poruch štítné žlázy, > imunitní trombocytopenické purpury (ITP), > nefropatií, včetně onemocnění s tvorbou protilátek proti glomerulární bazální membráně (anti-gbm). Tyto stavy mohou být závažné povahy, mohou vést k morbiditě a/nebo mortalitě, a mohou se objevit i mnoho let po léčbě. Časná detekce může zlepšit výsledky u pacientů, u nichž se tyto stavy vyskytnou. Je důležité pečlivě monitorovat laboratorní hodnoty a bedlivě sledovat příznaky a projevy. Prosím prostudujte si následující části pro lepší porozumění těmto rizikům. a) Poruchy štítné žlázy Během klinických hodnocení byly hlášeny autoimunitní poruchy štítné žlázy, včetně hypertyreózy a hypotyreózy. Poruchy štítné žlázy byly velmi časté v klinických hodnoceních a většina těchto poruch byla mírné až střední závažnosti a vyskytla se do 48 měsíců po první expozici organismu účinkům přípravku LEMTRADA. Některé poruchy byly přechodné a nevyžadovaly léčbu. Většinu poruch štítné žlázy se podařilo zvládnout pomocí konvenční terapie; u některých pacientů byla zapotřebí chirurgická intervence. U pacientek lidský papilomavir (HPV) Screeningové vyšetření HPV 1 ročně 4 LEMTRADA Pokyny pro zdravotnické pracovníky LEMTRADA Pokyny pro zdravotnické pracovníky 5
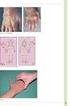
4 Je důležité informovat pacienty, že v závislosti na stavu štítné žlázy u nich může být zapotřebí celoživotní léčba (např. při hypotyreóze). > Funkční vyšetření štítné žlázy, např. stanovení TSH, je třeba provést před zahájením léčby, a následně opakovat každé 3 měsíce po dobu 48 měsíců. Po uplynutí této periody je třeba provádět testování na základě klinických nálezů signalizujících onemocnění štítné žlázy. Jestliže není hladina TSH v normě, doporučuje se stanovit hodnotu volného T3 a T4. > Sledujte i nadále příznaky a projevy poruch štítné žlázy. > Onemocnění štítné žlázy představují zvláštní riziko u těhotných žen. Neléčené onemocnění štítné žlázy může vést k poškození nenarozeného plodu nebo dítěte po narození. Obzvláštní pozornost je zapotřebí věnovat těhotným ženám s Basedowovou chorobou (označovanou též jako Gravesova nemoc), protože protilátky proti receptorům tyreostimulačního hormonu matky se mohou přenášet do vyvíjejícího se plodu a způsobit přechodnou novorozeneckou Basedowovu nemoc. Zdravotničtí pracovníci zodpovědní za péči o těhotné pacientky musí být obeznámeni se zvýšeným rizikem onemocnění štítné žlázy v důsledku léčby přípravkem Lemtrada a s potřebou náležité léčby těchto onemocnění. b) Imunitní trombocytopenická purpura (ITP) Imunitní trombocytopenická purpura je autoimunitní onemocnění, zpravidla spojené s tvorbou protilátek proti krevním destičkám. Jedná se o klinický syndrom, kdy se snížený počet cirkulujících trombocytů (trombocytopenie) manifestuje sklonem ke krvácení, snadnou tvorbou modřin (purpura) nebo extravazací krve z kapilár do kůže a sliznic (petechie). Symptomy ITP mohou zahrnovat (mimo jiné) snadnou tvorbu modřin a krevních výronů, petechie, spontánní mukokutánní krvácení (např. epistaxe, hemoptýza), silnější menstruační krvácení v porovnání s normálním stavem nebo nepravidelné menstruační krvácení. Tyto klinické příznaky ITP se mohou objevit ještě před vznikem závažného krvácení. ITP může být závažným stavem vedoucím k morbiditě a mortalitě a může se vyskytnout i několik let po podání léčby. V klinických hodnoceních byli pacienti s ITP diagnostikováni a léčeni včas a ve většině případů odpovídali na terapii první linie. Proto je nezbytné monitorovat všechny pacienty na ITP následujícím způsobem: > Kompletní krevní obraz a diferenciál je třeba provést před zahájením léčby a dále v měsíčních intervalech po dobu 48 měsíců. > Kontrola pacientů na klinické symptomy ITP. > Poučení pacientů o významu dodržování měsíčního monitorování krve a o potřebě pokračovat v tomto monitorování po dobu 48 měsíců. > Vzdělávání pacientů na téma, jak rozpoznat symptomy související s ITP, a zdůraznění, že je zapotřebí zachovávat ostražitost. > Při podezření na ITP je třeba urychleně zahájit vhodné léčebné intervence, včetně okamžitého odeslání ke specialistovi. Potenciální rizika spojená s opakovanou léčbou přípravkem LEMTRADA po výskytu ITP nejsou známa. Na podporu spolupráce/compliance pacientů byly vyvinuty speciální edukační nástroje pro pacienty. Podrobný popis těchto nástrojů je uveden v části Péče o pacienty léčené přípravkem LEMTRADA. Zde je znázorněn příklad petechií na dolní končetině. Petechie jsou drobné, difuzně rozptýlené skvrnky pod kůží, které nabývají červené, fialové nebo purpurové barvy. Petechie se mohou vyskytnout kdekoli na těle pacienta, nemusí být omezeny pouze na oblast nohou. Příklady ITP Zde je znázorněn příklad nadměrné tvorby modřin. Modřiny se mohou vyskytnout kdekoli na těle pacienta. Zde je znázorněn příklad purpury pod jazykem. Purpura se může objevit na každé sliznici, včetně sliznic v ústní dutině (pod jazykem, na patře, na vnitřní části tváří, jazyku nebo dásních). Poznámka: Následující snímky mají pouze informační charakter a slouží jako příklad krevních výronů a petechií při ITP. Pacient může mít ITP i tehdy, pokud se u něho vyskytuje méně závažný typ krevního výronu nebo petechií, než je uvedeno na obrázku. c) Nefropatie včetně anti-gbm onemocnění Nefropatie, včetně onemocnění anti-gbm, jsou vzácně hlášeny u pacientů s roztroušenou sklerózou po léčbě přípravkem LEMTRADA v klinických hodnoceních a obecně se vyskytly do 39 měsíců po posledním podání přípravku LEMTRADA. Klinické manifestace nefropatie mohou zahrnovat zvýšení hladin sérového kreatininu, hematurii a/nebo proteinurii. Častým projevem anti-gbm onemocnění (Goodpasturův syndrom) je alveolární krvácení, které se manifestuje hemoptýzou, ačkoli nebylo dosud pozorováno v klinických hodnoceních. Vzhledem k tomu, že pacienti mohou zůstat asymptomatičtí, je důležité provádět periodické laboratorní testy. > Hladiny sérového kreatininu je třeba měřit před zahájením léčby a následně v měsíčních intervalech po dobu 48 měsíců. 6 LEMTRADA Pokyny pro zdravotnické pracovníky LEMTRADA Pokyny pro zdravotnické pracovníky 7
5 > Analýza moči včetně mikroskopického vyšetření se má provádět před zahájením léčby a dále v měsíčních intervalech po dobu 48 měsíců. Po uplynutí této periody je třeba provádět testování na základě klinických nálezů signalizujících nefropatii. > V případě pozorování klinicky významných změn hladin sérového kreatininu oproti výchozímu stavu, nevysvětlitelné hematurie a/nebo proteinurie je zapotřebí další posouzení nefropatie, včetně odeslání ke specialistovi. Časná detekce a léčba nefropatie může snížit riziko špatného výsledku léčby. Anti-GBM onemocnění, pokud není léčeno, je život ohrožující stav, který vyžaduje okamžitou péči. Bez urychleného zahájení léčby se u pacienta může rychle vyvinout selhání ledvin vyžadující dialýzu a/nebo transplantaci a onemocnění může vést k úmrtí pacienta. 3. Přehled doporučeného monitorování pacientů V následující tabulce je uveden přehled milníků doporučených při monitorování. Pro každého pacienta, kterému předepíšete přípravek LEMTRADA, navíc máte k dispozici soubor předtištěných kontrolních přehledů. nezapomeňte ověřit bod Kontraindikace v přiloženém souhrnu údajů o přípravku (SPC). Stav Vyšetření Načasování Imunitní trombocytopenická purpura (ITP) Nefropatie, včetně onemocnění anti- GBM Nefropatie, včetně onemocnění anti- GBM Onemocnění štítné žlázy U pacientek lidský papilomavir (HPV) Kompletní krevní obraz a diferenciál 1 měsíčně, Sérový kreatinin 1 měsíčně, Analýza a mikroskopické vyšetření moči Funkční testy štítné žlázy (např. TSH) Screeningové vyšetření HPV 1 měsíčně, Každé 3 měsíce, 1 ročně 4. Péče o pacienty léčené přípravkem Lemtrada > Je mimořádně důležité, aby vaši pacienti vzali na vědomí, že musí absolvovat periodická vyšetření (po dobu 48 měsíců ), a to i tehdy, pokud budou asymptomatičtí a jejich onemocnění (RS) bude pod kontrolou. > Je zapotřebí naplánovat a vést periodické monitorování ve spolupráci s pacienty. > U nespolupracujících pacientů může být zapotřebí další poučení, při kterém se zdůrazní rizika vyplývající z vynechání plánovaných vyšetření a testů v rámci monitorování. > Je třeba monitorovat výsledky testů a pečlivě sledovat symptomy nežádoucích vedlejších účinků. > Prodiskutujte se svým pacientem pokyny pro pacienta a příbalovou informaci k přípravku LEMTRADA. Připomeňte pacientovi, aby pečlivě sledoval symptomy týkající se autoimunitních stavů a aby v případě obav vyhledal pomoc lékaře. > Požádejte pacienty, aby vždy nosili s sebou Kartu pacienta. Pacienti by měli ukázat tuto kartu všem zdravotnickým pracovníkům, kteří jim budou z jakéhokoli důvodu poskytovat péči, nebo v případě návštěvy pohotovostního oddělení. > Je třeba zajistit dostupnost odborníků a vybavení pro včasnou diagnózu a léčbu nejčastějších nežádoucích účinků, zejména autoimunitních stavů a infekcí. 5. Další informace Vakcinace > Pacientům se doporučuje, aby splnili požadavky na vakcinaci (podle národních předpisů) minimálně 6 týdnů před zahájením léčby přípravkem LEMTRADA. > Bezpečnost imunizace živými vakcínami po léčbě přípravkem LEMTRADA nebyla dosud hodnocena, a živé vakcíny se proto nemají podávat pacientům, kteří v nedávné době absolvovali cyklus léčby přípravkem LEMTRADA. > přípravkem LEMTRADA zvažte vakcinaci proti VZV u pacientů negativních na protilátky. Fertilita, antikoncepce, těhotenství a kojení > Ženy v reprodukčním věku by měly používat účinnou antikoncepci během podání léčby přípravkem LEMTRADA a po dobu 4 měsíců po podání léčby přípravkem LEMTRADA. > Nejsou prováděny žádné adekvátní a dobře kontrolované studie s přípravkem LEMTRADA u těhotných žen. Přípravek LEMTRADA by se měl podávat během těhotenství pouze tehdy, pokud potenciální přínos ospravedlňuje potenciální riziko pro plod. > Onemocnění štítné žlázy představují zvláštní riziko u těhotných žen (viz část 2, Poruchy štítné žlázy). U těhotných s Basedowovou chorobou (označovanou též jako Gravesova nemoc) se protilátky proti receptorům tyreostimulačního hormonu matky mohou přenášet do vyvíjejícího se plodu a způsobit přechodnou novorozeneckou Basedowovu nemoc. 8 LEMTRADA Pokyny pro zdravotnické pracovníky LEMTRADA Pokyny pro zdravotnické pracovníky 9
6 > Není známo, zda je alemtuzumab vylučován do lidského mateřského mléka. Riziko pro kojené dítě nelze vyloučit. Proto by během každého léčebného cyklu přípravkem LEMTRADA a také po dobu 4 měsíců po podání poslední infuze každého léčebného cyklu mělo být kojení přerušeno. Přínos imunity získané z mateřského mléka však může u kojeného dítěte převážit riziko z potenciální expozice přípravku Lemtrada. > Nejsou k dispozici žádné adekvátní klinické bezpečnostní údaje o vlivu přípravku LEMTRADA na fertilitu. V podstudii u 13 pacientů (mužů) léčených alemtuzumabem (léčených buď 12 mg, nebo 24 mg) nebyly zjištěny žádné známky aspermie, azoospermie, konzistentně sníženého počtu spermií, poruch motility ani zvýšení počtu morfologických abnormalit spermií. Je známo, že CD52 je přítomný v reprodukčních tkáních lidí a hlodavců. Údaje získané ve studiích na zvířatech ukazovaly účinky na fertilitu humanizovaných myší (viz bod 5.3 souhrnu údajů o přípravku), nicméně potenciální vliv na lidskou fertilitu během období expozice není na základě dostupných údajů znám. 6. Nejčastější otázky Prosím, před předepsáním přípravku LEMTRADA zvažte následující skutečnosti: Jaké laboratorní testy je třeba provést před zahájením léčby přípravkem LEMTRADA? Je třeba provést následující testy: > kompletní krevní obraz a diferenciál, > sérový kreatinin, > funkční vyšetření štítné žlázy, např. stanovení TSH, > vyšetření moči, včetně mikroskopického vyšetření. Další informace jsou uvedeny v Tabulce č. 1. Mohu předepsat přípravek LEMTRADA pacientům užívajícím jiný lék na RS? Přípravek LEMTRADA dosud nebyl podáván k léčbě RS souběžně s jinými antineoplastickými nebo imunosupresivními léky. Stejně jako u všech ostatních imunomodulačních léků je třeba při zvažování léčby přípravkem LEMTRADA vzít do úvahy potenciální kombinované účinky na imunitní systém pacienta. Souběžné použití přípravku LEMTRADA s jakýmkoli z těchto léků by mohlo zvýšit riziko imunosuprese. Postupné podání přípravku LEMTRADA po jiné, chorobu modifikující léčbě roztroušené sklerózy musí být provedeno dle příslušných souhrnů údajů o přípravku (SPC) přípravku LEMTRADA a použitých přípravků. Budu pokračovat v laboratorních testech během léčby přípravkem LEMTRADA a po jejím ukončení? Jak dlouho? Ano, testování začíná před léčbou (vstupní testy) a mělo by pokračovat po dobu 48 měsíců od poslední infuze. Podrobné informace včetně údajů o tom, jaké konkrétní testy provádět, kdy a jak dlouhou dobu, jsou uvedeny v části 1. Jak mám postupovat, pokud se u mého pacienta objeví infekce v době, kdy chci zahájit léčebný cyklus s přípravkem LEMTRADA? U pacientů s aktivní infekcí je třeba zvážit odložení zahájení léčby přípravkem LEMTRADA na dobu, kdy se infekce dostane pod plnou kontrolu. HIV infekce a jiné závažné aktivní infekce jsou kontraindikací podání přípravku LEMTRADA. Léčba Jak se přípravek LEMTRADA podává a jak dlouho infuze trvá? Přípravek LEMTRADA se podává nitrožilní infuzí ve dvou cyklech s ročním odstupem. Úvodní cyklus léčby zahrnuje denní infuze po dobu 5 po sobě jdoucích dnů. Druhý cyklus léčby se podává o 12 měsíců později a zahrnuje každodenní infuze po dobu 3 po sobě jdoucích dnů. Třetí nebo čtvrtý léčebný cyklus, zahrnující každodenní infuze po dobu 3 po sobě jdoucích dnů, podané nejméně 12 měsíců po předchozím léčebném cyklu, lze zvážit u pacientů s aktivní RS definovanou klinickými nebo zobrazovacími metodami. V případě výskytu infuzní reakce (IAR) zajistěte náležitou symptomatickou léčbu dle potřeby. Není-li infuze dobře tolerována, lze prodloužit dobu trvání infuze. V případě výskytu závažných infuzních reakcí je třeba zvážit okamžité ukončení nitrožilní infuze. V rámci klinických hodnocení byl výskyt anafylaktických nebo jiných závažných reakcí vyžadujících přerušení léčby velmi vzácný. Je třeba mít k dispozici připravené prostředky pro zvládnutí anafylaktických nebo jiných závažných reakcí. Lékaři by se měli obeznámit s kardiologickou anamnézou pacienta, protože infuzní reakce mohou zahrnovat srdeční symptomy, např. tachykardii. Je třeba mít k dispozici připravené prostředky pro zvládnutí anafylaktických nebo jiných závažných reakcí. Je třeba použít profylaktickou léčbu? Těsně před zahájením infuze přípravku LEMTRADA je třeba pacienty premedikovat kortikosteroidy (1 000 mg methylprednisolonu nebo ekvivalent) po dobu prvních 3 dnů každého léčebného cyklu. Před podáním přípravku LEMTRADA lze dále zvážit předléčení antihistaminiky a/nebo antipyretiky. Všem pacientům je třeba podávat perorální přípravky k profylaxi herpetických infekcí během léčby a po dobu minimálně 1 měsíce po léčbě. V klinických hodnoceních byl pacientům podáván acyclovir v dávce 200 mg (nebo ekvivalent) 2 denně. 10 LEMTRADA Pokyny pro zdravotnické pracovníky LEMTRADA Pokyny pro zdravotnické pracovníky 11
7 Monitorování nežádoucích účinků Jaké jsou příznaky a projevy ITP? Symptomy ITP mohou zahrnovat (mimo jiné) snadnou tvorbu modřin, petechie, spontánní mukokutánní krvácení (např. epistaxe, hemoptýza), silné nebo nepravidelné menstruační krvácení. Tyto klinické příznaky ITP se mohou objevit před rozvojem závažného krvácení. Mezi příznaky ITP patří rovněž nízký počet destiček nebo významné změny kompletního krevního obrazu a diferenciálu oproti výchozímu stavu. Jak bych měl/a léčit pacienta s podezřením na ITP? Je důležité monitorovat všechny pacienty na ITP, aby bylo možné u každého pacienta stanovit včas diagnózu a nasadit odpovídající léčbu. Proto je nezbytné stanovit kompletní krevní obraz a diferenciál před zahájením léčby a dále v pravidelných měsíčních intervalech po dobu 48 měsíců. V případě podezření na ITP je třeba neprodleně zahájit léčebnou intervenci, včetně okamžitého odeslání ke specializovanému lékaři. Závažné nebo rozsáhlé krvácení je život ohrožujícím stavem a vyžaduje okamžitou péči. Jaké symptomy mohou být spojeny s nefropatiemi, jako je například onemocnění anti-gbm? Manifestace nefropatií mohou zahrnovat zvýšení sérového kreatininu, hematurii a/nebo proteinurii. Častým projevem anti-gbm onemocnění je alveolární krvácení, které se manifestuje hemoptýzou, ačkoli nebylo dosud pozorováno v klinických hodnoceních. Vzhledem k tomu, že pacienti mohou zůstat asymptomatičtí, je důležité provádět periodické laboratorní testy (sérový kreatinin a analýza moči včetně mikroskopického vyšetření). Jak bych měl/a léčit pacienta s podezřením na nefropatii? V případě klinicky významných změn sérového kreatininu oproti výchozímu stavu, nevysvětlitelné hematurie a/nebo proteinurie je nezbytné další vyšetření na nefropatii, včetně okamžitého odeslání ke specialistovi. Časná detekce a léčba nefropatií může snížit riziko špatného výsledku. Informace týkající se těhotenství, antikoncepce a kojení Mají pacientky ženského pohlaví užívat antikoncepci? Alfa poločas alemtuzumabu se blížil 4 5 dnům a byl srovnatelný mezi jednotlivými cykly vedoucími k nízkým nebo nedetekovatelným sérovým koncentracím během cca 30 dnů po každém léčebném cyklu. Ženy v reprodukčním věku by proto měly používat účinnou antikoncepci během podávání léčby a po dobu 4 měsíců po každé sérii léčby přípravkem LEMTRADA. Je třeba vzít v úvahu, že léčba přípravkem LEMTRADA sestává ze dvou léčebných cyklů s odstupem 12 měsíců. Ženy, které mohou otěhotnět, by na toto měly být upozorněny a odrazovány od otěhotnění během tohoto léčebného intervalu. Je možné podat přípravek LEMTRADA během těhotenství? Přípravek LEMTRADA lze podávat během těhotenství pouze v případě, že potenciální přínos odůvodní možné riziko pro plod. Je známo, že lidský IgG prostupuje placentární bariérou; alemtuzumab může placentární bariérou prostupovat také, a tím představovat potenciální riziko pro plod. Studie na zvířatech prokázaly reprodukční toxicitu. Není známo, zda LEMTRADA může způsobit poškození plodu, je-li podávána těhotným ženám, nebo zda může ovlivnit schopnost reprodukce. Onemocnění štítné žlázy představuje u těhotných žen zvláštní riziko. Bez léčby hypotyreózy existuje v těhotenství zvýšené riziko spontánního potratu a účinků na plod ve smyslu mentální retardace a nanismu. U matek s Gravesovou nemocí se protilátky proti receptorům tyreostimulačního hormonu matky mohou přenášet do vyvíjejícího se plodu a způsobit přechodnou novorozeneckou Gravesovu nemoc. Pokud chce žena otěhotnět, jak dlouho má vyčkat po ukončení léčby přípravkem LEMTRADA? Protože ženy, které mohou otěhotnět, by měly během léčby a 4 měsíce po léčebném cyklu přípravkem LEMTRADA používat účinná antikoncepční opatření, měly by s plánovaným otěhotněním vyčkat alespoň 4 měsíce. Je třeba vzít v úvahu, že léčba přípravkem LEMTRADA sestává ze dvou léčebných cyklů s odstupem 12 měsíců. Ženy, které mohou otěhotnět, by na toto měly být upozorněny a odrazovány od otěhotnění během tohoto léčebného intervalu. Bude mít LEMTRADA dopad na budoucí fertilitu u žen nebo mužů? Nejsou k dispozici žádné adekvátní klinické bezpečnostní údaje o vlivu přípravku LEMTRADA na fertilitu. V kohortě 13 pacientů (mužů) léčených přípravkem LEMTRADA (léčených buď 12 mg, nebo 24 mg) nebyly zjištěny žádné známky aspermie, azoospermie, konzistentně sníženého počtu spermií, poruch motility ani zvýšení počtu morfologických abnormalit spermií. Je známo, že CD52 je přítomný v reprodukčních tkáních lidí a hlodavců. Údaje získané ve studiích na zvířatech ukazovaly účinky na fertilitu humanizovaných myší (viz bod 5.3 SPC), nicméně potenciální vliv na lidskou fertilitu během období expozice není na základě dostupných údajů znám. Měly by kojící pacientky absolvovat cyklus léčby přípravkem LEMTRADA? Není známo, zda je alemtuzumab vylučován do lidského mateřského mléka. Riziko pro kojené dítě nelze vyloučit. Proto by během každého léčebného cyklu přípravkem LEMTRADA a také po dobu 4 měsíců po podání poslední infuze každého léčebného cyklu mělo být kojení přerušeno. Přínos imunity získané z mateřského mléka však může u kojeného dítěte převážit riziko z potenciální expozice přípravku LEMTRADA. 12 LEMTRADA Pokyny pro zdravotnické pracovníky LEMTRADA Pokyny pro zdravotnické pracovníky 13
8 Očkování Co je třeba zohlednit z hlediska vakcinace při zvažování léčby přípravkem LEMTRADA? Bezpečnost imunizace živými vakcínami po léčbě přípravkem LEMTRADA nebyla dosud hodnocena a živé vakcíny se proto nemají podávat pacientům, kteří v nedávně době absolvovali cyklus léčby přípravkem LEMTRADA. Pacientům se doporučuje, aby splnili požadavky na vakcinaci (podle národních předpisů) minimálně 6 týdnů před zahájením léčby přípravkem LEMTRADA. přípravkem LEMTRADA zvažte možnost vakcinace proti VZV u pacientů negativních na protilátky. Poznámky Poznámky 14 LEMTRADA Pokyny pro zdravotnické pracovníky LEMTRADA Pokyny pro zdravotnické pracovníky 15
9 Sanofi-aventis, s.r.o. Evropská 846/176a, Praha 6 Tel , fax Datum přípravy materiálu: Srpen 2018 GZCS.LEMT (1) Verze 2.1
Pokyny pro zdravotnické pracovníky
 Edukační materiál Pokyny pro zdravotnické pracovníky Použití přípravku (alemtuzumab) u pacientů s relabující-remitující roztroušenou sklerózou (RRRS) Tento léčivý přípravek podléhá dalšímu sledování. To
Edukační materiál Pokyny pro zdravotnické pracovníky Použití přípravku (alemtuzumab) u pacientů s relabující-remitující roztroušenou sklerózou (RRRS) Tento léčivý přípravek podléhá dalšímu sledování. To
LEMTRADA alemtuzumab 12 mg i.v.
 POKYNY PRO PACIENTY Důležité informace pro pacienty začínající léčbu přípravkem LEMTRADA Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte
POKYNY PRO PACIENTY Důležité informace pro pacienty začínající léčbu přípravkem LEMTRADA Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte
LEMTRADA. Pokyny pro pacienty. Důležité informace pro pacienty začínající léčbu přípravkem LEMTRADA. alemtuzumab 12mg i.v.
 Pokyny pro pacienty Důležité informace pro pacienty začínající léčbu přípravkem Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Pokyny pro pacienty Důležité informace pro pacienty začínající léčbu přípravkem Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE
 EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL - Pioglitazone Accord
 Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Informovaný souhlas pacienta(tky) s výkonem. Nitrožilní aplikace monoklonální protilátky alemtuzumab (LEMTRADA)
 Informovaný souhlas pacienta(tky) s výkonem Nitrožilní aplikace monoklonální protilátky alemtuzumab (LEMTRADA) Vážená paní, Vážený pane, vzhledem k tomu, že jako svéprávný jedinec se podílíte významným
Informovaný souhlas pacienta(tky) s výkonem Nitrožilní aplikace monoklonální protilátky alemtuzumab (LEMTRADA) Vážená paní, Vážený pane, vzhledem k tomu, že jako svéprávný jedinec se podílíte významným
Důležité bezpečnostní informace pro zdravotnické pracovníky
 Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
Edukační materiály BAVENCIO (avelumab) 20 mg/ml koncentrát pro infuzní roztok Důležité bezpečnostní informace pro zdravotnické pracovníky Tento dokument obsahuje důležité informace o bezpečnosti, s nimiž
PRŮKAZ PACIENTA. užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019
 PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
INFLECTRA SCREENINGOVÝ LIST. a výběru pacientů pro všechny schválené indikace. Obsahuje pokyny ke správnému screeningu
 Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Důležité informace pro pacienty
 MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
MAVENCLAD (cladribinum) Důležité informace pro pacienty OBSAH Seznámení s přípravkem MAVENCLAD Jak se přípravek MAVENCLAD podává? Nežádoucí účinky a možná rizika Lymfopenie Herpes zoster (pásový opar)
Edukační materiál. Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera
 Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Návod pro pacienta / pečovatele
 Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
PRŮKAZ PACIENTA. užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1
 PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise
 PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
PŘÍLOHA III ÚPRAVY SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Tyto změny k SPC a příbalové informace jsou platné v den Rozhodnutí Komise Po Rozhodnutí Komise aktualizuje národní kompetentní autorita
EDUKAČNÍ MATERIÁLY. TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM)
 EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Program prevence
Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti.
 Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti. I V A N A K O V Á Ř O V Á C E N T R U M P R O D E M Y E L I N I Z A Č N Í O N E M O C N Ě N Í N E U R O L O G I C
Perorální kladribin: bezpečnostní profil, monitorování pacientů a praktické zkušenosti. I V A N A K O V Á Ř O V Á C E N T R U M P R O D E M Y E L I N I Z A Č N Í O N E M O C N Ě N Í N E U R O L O G I C
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
BAVENCIO (avelumab) Váš průvodce informacemi pro pacienta
 Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Váš průvodce informacemi pro pacienta BAVENCIO (avelumab) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli
Rozměr zavřeného průkazu mm
 Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Příloha IV. Vědecké závěry
 Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
(alemtuzumab 12 mg i.v.)
 EDUKAČNÍ MATERIÁL Pomůcka pro podání přípravku Tento text je pouze doporučením a pomůckou pro podávání léčivého přípravku Lemtrada. Nenahrazuje edukační materiály, které jsou k dispozici pro předepisující
EDUKAČNÍ MATERIÁL Pomůcka pro podání přípravku Tento text je pouze doporučením a pomůckou pro podávání léčivého přípravku Lemtrada. Nenahrazuje edukační materiály, které jsou k dispozici pro předepisující
Příloha II. Vědecké závěry
 Příloha II Vědecké závěry 74 Vědecké závěry Dne 7. července 2016 zahájila Velká Británie na základě farmakovigilančních údajů postup podle článku 31 směrnice 2001/83/ES a požádalo výbor PRAC, aby přezkoumal
Příloha II Vědecké závěry 74 Vědecké závěry Dne 7. července 2016 zahájila Velká Británie na základě farmakovigilančních údajů postup podle článku 31 směrnice 2001/83/ES a požádalo výbor PRAC, aby přezkoumal
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
EDUKAČNÍ MATERIÁL. Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid)
 EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge
 Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge Erivedge může způsobit závažné vrozené vady Může vést
Program prevence početí při léčbě přípravkem Erivedge: Důležité informace o prevenci početí a antikoncepci pro pacienta užívajícího přípravek Erivedge Erivedge může způsobit závažné vrozené vady Může vést
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH)
 Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
Zvažte oddálení podání regadenosonu u pacientů s nekontrolovanou hypertenzí.
 CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
EDUKAČNÍ MATERIÁLY. Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce
 EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
TOCTINO (ALITRETINOIN)
 EDUKAČNÍ MATERIÁLY TOCTINO (ALITRETINOIN) PROGRAM PREVENCE TĚHOTENSTVÍ POKYNY PRO LÉKAŘE A LÉKÁRNÍKY Pokyny pro lékaře předepisující TOCTINO Prosíme, abyste si tyto pokyny pečlivě přečetli před tím, než
EDUKAČNÍ MATERIÁLY TOCTINO (ALITRETINOIN) PROGRAM PREVENCE TĚHOTENSTVÍ POKYNY PRO LÉKAŘE A LÉKÁRNÍKY Pokyny pro lékaře předepisující TOCTINO Prosíme, abyste si tyto pokyny pečlivě přečetli před tím, než
Hemlibra (emicizumab) Subkutánní injekce. Návod pro zdravotnické pracovníky
 EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Rekurentní horečka spojená s NRLP21
 www.printo.it/pediatric-rheumatology/cz/intro Rekurentní horečka spojená s NRLP21 Verze č 2016 1. CO JE TO REKURENTNÍ HOREČKA SPOJENÁ S NRLP12 1.1 Co je to? Rekurentní horečka spojená s NRLP12 patří mezi
www.printo.it/pediatric-rheumatology/cz/intro Rekurentní horečka spojená s NRLP21 Verze č 2016 1. CO JE TO REKURENTNÍ HOREČKA SPOJENÁ S NRLP12 1.1 Co je to? Rekurentní horečka spojená s NRLP12 patří mezi
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
Co byste měl(a) vědět o léčivém přípravku
 Co byste měl(a) vědět o léčivém přípravku Důležité bezpečnostní informace pro pacienty léčené přípravkem MabThera 1 Co byste měl(a) vědět o přípravku MabThera Pokud máte revmatoidní artritidu (RA), granulomatózu
Co byste měl(a) vědět o léčivém přípravku Důležité bezpečnostní informace pro pacienty léčené přípravkem MabThera 1 Co byste měl(a) vědět o přípravku MabThera Pokud máte revmatoidní artritidu (RA), granulomatózu
Příloha II. Vědecké závěry a zdůvodnění změny v registraci
 Příloha II Vědecké závěry a zdůvodnění změny v registraci 6 Vědecké závěry Celkové shrnutí vědeckého hodnocení přípravku Cymevene i.v. a souvisejících názvů (viz příloha I) Evropská komise jménem všech
Příloha II Vědecké závěry a zdůvodnění změny v registraci 6 Vědecké závěry Celkové shrnutí vědeckého hodnocení přípravku Cymevene i.v. a souvisejících názvů (viz příloha I) Evropská komise jménem všech
Familiární středomořská (Mediterranean) horečka (Fever)
 www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření
Edukační materiál. Yervoy (ipilimumab) Časté otázky Brožura pro. zdravotníky
 Edukační materiál Yervoy (ipilimumab) Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Tento léčivý
Edukační materiál Yervoy (ipilimumab) Časté otázky Brožura pro zdravotníky Přípravek YERVOY je indikován k léčbě pokročilého melanomu (neresekovatelného nebo metastazujícího) u dospělých. 1 Tento léčivý
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU LEMTRADA 12 mg koncentrát pro infuzní roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje alemtuzumabum 12 mg v 1,2
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU LEMTRADA 12 mg koncentrát pro infuzní roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje alemtuzumabum 12 mg v 1,2
Příloha III. Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha III Doplnění do příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tyto dodatky příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referral
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Edukační materiály. KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře
 Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Edukační materiály KADCYLA (trastuzumab emtansin): Edukační materiál pro lékaře Informace pro lékaře EU Listopad 2013 Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE
 LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE Léčba by měla být zahájena a sledována specialistou se zkušenostmi v léčbě revmatoidní artritidy a psoriatické artritidy. Lékař by měl poučit pacienty
LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE Léčba by měla být zahájena a sledována specialistou se zkušenostmi v léčbě revmatoidní artritidy a psoriatické artritidy. Lékař by měl poučit pacienty
Brožura s informacemi pro pacienta a rodiče pacienta s ahus
 Brožura s informacemi pro pacienta a rodiče pacienta s ahus Schválena SÚKL dne 18. března 2019 SLOVNÍK POJMŮ Atypický hemolytickouremický syndrom (ahus) Vzácná porucha způsobená chronickou a nadměrnou
Brožura s informacemi pro pacienta a rodiče pacienta s ahus Schválena SÚKL dne 18. března 2019 SLOVNÍK POJMŮ Atypický hemolytickouremický syndrom (ahus) Vzácná porucha způsobená chronickou a nadměrnou
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU LEMTRADA 12 mg koncentrát pro infuzní roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje alemtuzumabum 12 mg v 1,2
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU LEMTRADA 12 mg koncentrát pro infuzní roztok. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna injekční lahvička obsahuje alemtuzumabum 12 mg v 1,2
NeuroBloc. botulinový toxin typu B injekční roztok, U/ml
 NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
NeuroBloc botulinový toxin typu B injekční roztok, 5 000 U/ml Důležité bezpečnostní informace určené lékařům Účelem této příručky je poskytnout lékařům, kteří jsou oprávněni předepisovat a aplikovat přípravek
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příručka k přípravku KEYTRUDA. (pembrolizumab) Informace pro pacienty. Informace pro pacienty
 Příručka k přípravku KEYTRUDA (pembrolizumab) Informace pro pacienty Informace pro pacienty Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příručka k přípravku KEYTRUDA (pembrolizumab) Informace pro pacienty Informace pro pacienty Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět
Příloha I Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Edukační materiály. Imnovid (pomalidomid) Informace pro zdravotnické pracovníky. Brožura pokyny pro bezpečné použití přípravku
 Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pokyny pro bezpečné použití přípravku Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Brožura pokyny
Imnovid Edukační materiály, verze 3.0; schváleno SUKL 30/JAN/2017 Brožura pokyny pro bezpečné použití přípravku Edukační materiály Imnovid (pomalidomid) Informace pro zdravotnické pracovníky Brožura pokyny
RADA A POUČENÍ LÉKAŘE
 RADA A POUČENÍ LÉKAŘE Obsah: Uživatelky kombinované hormonální antikoncepce Léčebné účinky kombinované hormonální antikoncepce Kontraindikace kombinované hormonální antikoncepce Vysvětlivky: COC = z anglického
RADA A POUČENÍ LÉKAŘE Obsah: Uživatelky kombinované hormonální antikoncepce Léčebné účinky kombinované hormonální antikoncepce Kontraindikace kombinované hormonální antikoncepce Vysvětlivky: COC = z anglického
Praxbind doporučení pro podávání (SPC)
 Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
Praxbind doporučení pro podávání (SPC) Idarucizumab je indikován pro použití v případech, kde je zapotřebí rychlá antagonizace antagonizačních účinků dabigatranu Idarucizumab je specifický přípravek pro
Očkování v těhotenství. T. Binder, B. Vavřinková Výbor SPaFMM ČGPS Revize R. Prymula, P. Kosina, ČVS JEP
 Očkování v těhotenství T. Binder, B. Vavřinková Výbor SPaFMM ČGPS Revize R. Prymula, P. Kosina, ČVS JEP Obecná pravidla 1) K očkování těhotné ženy je třeba přistupovat individuálně. 2) Vždy je třeba zvážit
Očkování v těhotenství T. Binder, B. Vavřinková Výbor SPaFMM ČGPS Revize R. Prymula, P. Kosina, ČVS JEP Obecná pravidla 1) K očkování těhotné ženy je třeba přistupovat individuálně. 2) Vždy je třeba zvážit
CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití)
 CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
CAPRELSA (vandetanibum) Pokyny pro pacienty a pečovatele ohledně dávkování a monitorování (pediatrické použití) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
Zvláštní bezpečnostní informace
 Zvláštní bezpečnostní informace Edukační materiál pro lékaře Součást Plánu řízení rizik léčivého přípravku Arava Schváleno Státním ústavem pro kontrolu léčiv Zvláštní bezpečnostní informace Arava (leflunomid),
Zvláštní bezpečnostní informace Edukační materiál pro lékaře Součást Plánu řízení rizik léčivého přípravku Arava Schváleno Státním ústavem pro kontrolu léčiv Zvláštní bezpečnostní informace Arava (leflunomid),
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy (PSUR) pro bendamustin-hydrochlorid byly
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy (PSUR) pro bendamustin-hydrochlorid byly
KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin. Informace pro lékaře EU
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Listopad 2016 Informace pro lékaře EU Tento léčivý přípravek podléhá dalšímu
Vývoj nových léčiv. Preklinický výzkum Klinický výzkum
 Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
Kelapril 5mg 7x14tbl.
 Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
Kelapril 5mg 7x14tbl. Popis zboží: PŘÍBALOVÁ INFORMACE KELAPRIL 5 mg, potahované tablety pro psy kočky 1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ
ANAMNÉZA DÁRKYNĚ PUPEČNÍKOVÉ KRVE
 ANAMNÉZA DÁRKYNĚ PUPEČNÍKOVÉ KRVE JMÉNO A PŘÍJMENÍ DÁRKYNÉ DATUM NAROZENÍ RODNÉ ČÍSLO ZAMĚSTNÁNÍ TELEFON ULICE A ČÍSLO POPISNÉ MĚSTO PSČ PORODNÍK MINULÉ TĚHOTENSTVÍ počet předchozích porodů počet spontánních
ANAMNÉZA DÁRKYNĚ PUPEČNÍKOVÉ KRVE JMÉNO A PŘÍJMENÍ DÁRKYNÉ DATUM NAROZENÍ RODNÉ ČÍSLO ZAMĚSTNÁNÍ TELEFON ULICE A ČÍSLO POPISNÉ MĚSTO PSČ PORODNÍK MINULÉ TĚHOTENSTVÍ počet předchozích porodů počet spontánních
CZ PAR. QUETIAPINI FUMARAS Seroquel. UK/W/0004/pdWS/001 NL/W/0004/pdWS/001
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
1. NÁZEV PŘÍPRAVKU TETAVAX Injekční suspenze Vakcína proti tetanu (adsorbovaná) SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: 1 dávka (0,5 ml) obsahuje Tetani anatoxinum
EDUKAČNÍ MATERIÁLY. GILENYA (fingolimod)
 EDUKAČNÍ MATERIÁLY GILENYA (fingolimod) Souhrn doporučení pro předepisující lékaře Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
EDUKAČNÍ MATERIÁLY GILENYA (fingolimod) Souhrn doporučení pro předepisující lékaře Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
Souhrn doporučení pro předepisujícího lékaře
 G Souhrn doporučení pro předepisujícího lékaře Kritéria výběru pacientů pro léčbu přípravkem GILENYA (fingolimod) Přípravek GILENYA je vhodný pro dospělé pacienty k léčbě vysoce aktivní relabující-remitentní
G Souhrn doporučení pro předepisujícího lékaře Kritéria výběru pacientů pro léčbu přípravkem GILENYA (fingolimod) Přípravek GILENYA je vhodný pro dospělé pacienty k léčbě vysoce aktivní relabující-remitentní
HIV (z klinického pohledu)
 HIV (z klinického pohledu) David Jilich HIV centrum, Nemocnice Na Bulovce, Praha 11.12. 2014 Vývoj situace ve světě Changes in incidance rate 2001 to 2009 zdroj: UNAIDS Zákadní charakteristika virová infekce
HIV (z klinického pohledu) David Jilich HIV centrum, Nemocnice Na Bulovce, Praha 11.12. 2014 Vývoj situace ve světě Changes in incidance rate 2001 to 2009 zdroj: UNAIDS Zákadní charakteristika virová infekce
dnavou artritidou (GA)
 EDUKAČNÍ MATERIÁLY ILARIS (kanakinumab) Průvodce pro lékaře k používání přípravku Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
EDUKAČNÍ MATERIÁLY ILARIS (kanakinumab) Průvodce pro lékaře k používání přípravku Jakékoli podezření na závažný nebo neočekávaný nežádoucí účinek a jiné skutečnosti závažné pro zdraví léčených osob musí
PNEUMOKOKOVÉ INFEKCE A MOŽNOSTI PREVENCE aneb CO MŮŽE ZPŮSOBIT PNEUMOKOK
 PNEUMOKOKOVÉ INFEKCE A MOŽNOSTI PREVENCE aneb CO MŮŽE ZPŮSOBIT PNEUMOKOK Očkování! Nejvýznamnější možnost prevence infekčních chorob! Lepší infekční chorobě předcházet než ji léčit! Významný objev v medicíně,
PNEUMOKOKOVÉ INFEKCE A MOŽNOSTI PREVENCE aneb CO MŮŽE ZPŮSOBIT PNEUMOKOK Očkování! Nejvýznamnější možnost prevence infekčních chorob! Lepší infekční chorobě předcházet než ji léčit! Významný objev v medicíně,
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Příloha III Pozměňovací návrh příslušných bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Tento souhrn údajů o přípravku a příbalová informace mohou být následně dle potřeby aktualizovány
Důležité informace k užívání přípravku Tasigna
 Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
Důležité informace k užívání přípravku Tasigna Co je důležité vědět o přípravku Tasigna... Přípravek Tasigna je lék vydávaný pouze na lékařský předpis. Tasigna se používá k léčbě leukemie nazývané chronická
Důležité informace o užívání přípravku TASIGNA
 Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Důležité informace o užívání přípravku TASIGNA Důležité informace o užívání přípravku TASIGNA Co je důležité vědět o přípravku TASIGNA Přípravek TASIGNA je lék vydávaný pouze na lékařský předpis. TASIGNA
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
von Willebrandova choroba Mgr. Jaroslava Machálková
 von Willebrandova choroba Mgr. Jaroslava Machálková von Willebrandova choroba -je dědičná krvácivá choroba způsobená vrozeným kvantitativním či kvalitativním defektem von Willebrandova faktoru postihuje
von Willebrandova choroba Mgr. Jaroslava Machálková von Willebrandova choroba -je dědičná krvácivá choroba způsobená vrozeným kvantitativním či kvalitativním defektem von Willebrandova faktoru postihuje
EDUKAČNÍ MATERIÁLY. KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin
 EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
EDUKAČNÍ MATERIÁLY KADCYLA (Trastuzumab emtansin): Edukační materiál pro lékaře o riziku záměny mezi přípravky Kadcyla a Herceptin Informace pro lékaře EU UPOZORNĚNÍ Riziko záměny mezi přípravky Kadcyla
Klinické hodnocení u bolestí spojených s endometriózou. Bolest, kterou cítíte, je skutečná... i když to ostatní nevidí. A822523
 Klinické hodnocení u bolestí spojených s endometriózou Bolest, kterou cítíte, je skutečná... i když to ostatní nevidí. A822523 Studie SOLSTICE se provádí v přibližně 200 výzkumných centrech na celém světě.
Klinické hodnocení u bolestí spojených s endometriózou Bolest, kterou cítíte, je skutečná... i když to ostatní nevidí. A822523 Studie SOLSTICE se provádí v přibližně 200 výzkumných centrech na celém světě.
Průvodce použitím přípravku YERVOY (ipilimumab)
 Průvodce použitím přípravku YERVOY (ipilimumab) Informační brožura pro pacienty Yervoy podléhá dalšímu sledování, které umožní rychlé získávání nových informací o bezpečnosti. Pokud se u Vás vyskytne jakýkoli
Průvodce použitím přípravku YERVOY (ipilimumab) Informační brožura pro pacienty Yervoy podléhá dalšímu sledování, které umožní rychlé získávání nových informací o bezpečnosti. Pokud se u Vás vyskytne jakýkoli
Nebido EDUKAČNÍ MATERIÁL. Jak úspěšně aplikovat přípravek. (testosterone undecanoate)
 EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
EDUKAČNÍ MATERIÁL Jak úspěšně aplikovat přípravek Nebido (testosterone undecanoate) Tento edukační materiál Vám poskytne informace o některých aspektech aplikace přípravku Nebido za účelem rozšíření Vašich
SOUHRN ÚDAJŮ O PŘÍPRAVKU. PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová
 sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
sp.zn.sukls44523/2015 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU PNEUMO 23, injekční roztok v předplněné injekční stříkačce Vakcína proti pneumokokům polysacharidová 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha III. Změny příslušných bodů informace o přípravku
 Příloha III Změny příslušných bodů informace o přípravku Poznámka: Tyto změny v příslušných bodech souhrnu údajů a přípravku a příbalové informace jsou výsledkem postupu přezkoumání. Informace o přípravku
Příloha III Změny příslušných bodů informace o přípravku Poznámka: Tyto změny v příslušných bodech souhrnu údajů a přípravku a příbalové informace jsou výsledkem postupu přezkoumání. Informace o přípravku
INFORMACE PRO ZDRAVOTNÍKY O PŘÍPRAVKU BOSENTAN ACCORD
 EDUKAČNÍ MATERIÁLY INFORMACE PRO ZDRAVOTNÍKY O PŘÍPRAVKU BOSENTAN ACCORD Předtím, než předepíšete přípravek Bosentan Accord jakémukoli pacientovi, přečtěte si prosím pečlivě příslušný Souhrn údajů o přípravku.
EDUKAČNÍ MATERIÁLY INFORMACE PRO ZDRAVOTNÍKY O PŘÍPRAVKU BOSENTAN ACCORD Předtím, než předepíšete přípravek Bosentan Accord jakémukoli pacientovi, přečtěte si prosím pečlivě příslušný Souhrn údajů o přípravku.
CZ PAR QUETIAPINUM. Seroquel. UK/W/0004/pdWS/001. NL/W/0004/pdWS/001
 CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
CZ PAR Název (léčivá látka/ přípravek) Číslo procedury QUETIAPINUM Seroquel UK/W/0004/pdWS/001 NL/W/0004/pdWS/001 ART. NÁZVY PŘÍPRAVKŮ KLINICKÝCH STUDIÍ INN DRŽITELÉ PŘÍPRAVKŮ KLINICKÝCH STUDIÍ SCHVÁLENÉ
CAVE! Informační dopis pro zdravotnické pracovníky
 CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
Infekční hepatitidy u těhotných
 Infekční hepatitidy u těhotných Rožnovský Luděk 6. konference Sekce infekčních nemocí v gynekologii a porodnictví Virové hepatitidy v graviditě Neobvyklá dvojice matka a plod (dítě) snaha ochránit matku
Infekční hepatitidy u těhotných Rožnovský Luděk 6. konference Sekce infekčních nemocí v gynekologii a porodnictví Virové hepatitidy v graviditě Neobvyklá dvojice matka a plod (dítě) snaha ochránit matku
Příbalová informace: informace pro uživatele
 sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
sp.zn. sukls120097/2014 Příbalová informace: informace pro uživatele TYPHIM Vi Injekční roztok v předplněné injekční stříkačce Typhoidi capsulae Vi polysaccharidum purificatum (stripe Ty2) - (polysacharidová
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím
 Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Soňa Fraňková Klinika hepatogastroenterologie, Transplantcentrum IKEM
 Soňa Fraňková Klinika hepatogastroenterologie, Transplantcentrum IKEM 1971 Combes poprvé popsal membranózní glomerulonefritidu asociovanou s HBV infekcí (depozita imunokomplexů) Různé typy glomerulární
Soňa Fraňková Klinika hepatogastroenterologie, Transplantcentrum IKEM 1971 Combes poprvé popsal membranózní glomerulonefritidu asociovanou s HBV infekcí (depozita imunokomplexů) Různé typy glomerulární
Trombocytopenie v těhotenství
 Trombocytopenie v těhotenství doc. MUDr. Antonín Pařízek, CSc. Gynekologicko-porodnická klinika 1. LF UK a VFN v Praze Definice normální počet trombocytů u netěhotných žen 150-400 x 10 9 /l v těhotenství
Trombocytopenie v těhotenství doc. MUDr. Antonín Pařízek, CSc. Gynekologicko-porodnická klinika 1. LF UK a VFN v Praze Definice normální počet trombocytů u netěhotných žen 150-400 x 10 9 /l v těhotenství
Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel)
 EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
EDUKAČNÍ MATERIÁLY Rozdíly mezi přípravky Mirena (levonorgestrel) Jaydess (levonorgestrel) Kyleena (levonorgestrel) Léčivý přípravek Jaydess podléhá dalšímu sledování. To umožní rychlé získání nových informací
Deficit antagonisty IL-1 receptoru (DIRA)
 www.printo.it/pediatric-rheumatology/cz/intro Deficit antagonisty IL-1 receptoru (DIRA) Verze č 2016 1. CO JE DIRA? 1.1 O co se jedná? Deficit antagonisty IL-1Receptoru (DIRA) je vzácné vrozené onemocnění.
www.printo.it/pediatric-rheumatology/cz/intro Deficit antagonisty IL-1 receptoru (DIRA) Verze č 2016 1. CO JE DIRA? 1.1 O co se jedná? Deficit antagonisty IL-1Receptoru (DIRA) je vzácné vrozené onemocnění.
Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1
![Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1 Alofisel. Edukační materiály. (darvadstrocel) Pokyny pro příjem a uchovávání léku. [PŘÍRUČKA pro LEKÁRNÍKY] Verze: 1](/thumbs/102/154291766.jpg) Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Edukační materiály
CZ PAR. QUETIAPINI FUMARAS Seroquel. NL/W/0004/pdWS/002
 Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Název (léčivá látka/přípravek) CZ PAR QUETIAPINI FUMARAS Seroquel Číslo procedury NL/W/0004/pdWS/002 ART. NÁZEV INN DRŽITEL SCHVÁLENÉ INDIKACE ATC KÓD LÉKOVÁ FORMA, SÍLA INDIKAČNÍ SKUPINA ZMĚNA V SmPC
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ přijetí hlášení společností Roche (den-měsíc-rok): Lokální číslo: AER: OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení:
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ přijetí hlášení společností Roche (den-měsíc-rok): Lokální číslo: AER: OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení:
Viru-Merz je účinný při léčbě infekce způsobené virem herpes simplex, ale pouze do fáze vzniku puchýřků.
 sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp.zn.: sukls106117/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Viru-Merz, gel tromantadini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příloha IV. Vědecké závěry
 Příloha IV Vědecké závěry 37 Vědecké závěry Rychle narůstá počet vědeckých důkazů o progresivní multifokální leukoencefalopatii (PML) u pacientů léčených přípravkem Tysabri. Jsou k dispozici nové informace
Příloha IV Vědecké závěry 37 Vědecké závěry Rychle narůstá počet vědeckých důkazů o progresivní multifokální leukoencefalopatii (PML) u pacientů léčených přípravkem Tysabri. Jsou k dispozici nové informace
Kapitola III. Poruchy mechanizmů imunity. buňka imunitního systému a infekce
 Kapitola III Poruchy mechanizmů imunity buňka imunitního systému a infekce Imunitní systém Zásadně nutný pro přežití Nezastupitelná úloha v obraně proti infekcím Poruchy imunitního systému při rozvoji
Kapitola III Poruchy mechanizmů imunity buňka imunitního systému a infekce Imunitní systém Zásadně nutný pro přežití Nezastupitelná úloha v obraně proti infekcím Poruchy imunitního systému při rozvoji
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Glucosum monohydricum
 sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
sp.zn.sukls126426/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Glukóza 5 Braun infuzní roztok Glucosum monohydricum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám tento přípravek bude
