Gymnázium Vysoké Mýto nám. Vaňorného 163, Vysoké Mýto
|
|
|
- Iveta Procházková
- před 9 lety
- Počet zobrazení:
Transkript
1 Gymnázium Vysoké Mýto nám. Vaňorného 163, Vysoké Mýto
2 Periodická soustava prvků
3 Chemické prvky V současné době známe 104 chemických prvků. Většina z nich se vyskytuje v přírodě. Jen malá část byla připravena uměle. Ze 104 prvků je 82 kovů, 5 polokovů a 17 nekovů. Při normální teplotě je většina prvků tuhých 91, dva kapalné a 11 plynných. Kapalný je nekov bróm a kov rtuť. Plynné jsou vodík, kyslík, dusík, fluór, chlór, helium, neon, argon, krypton, xenon a radon. 20 prvků je tzv. čistých, monoizotopických. Jsou tvořeny pouze jediným izotopem. Jsou to např. Be, F, Na, Al, P, Mn, Co, As, I a další. Ostatní jsou tvořeny více izotopy. Například vodík je tvořen třemi izotopy lišícími se počtem neutronů v jádře atomu. H 1 2 H H
4 Periodický zákon Snahy o klasifikaci chemických prvků vyvrcholily prací Dimitrije Ivanoviče Mendělejeva v roce Mendělejev sestavil všech tehdy 62 známých prvků v pořadí vzrůstajících atomových hmotností v tzv. přirozenou řadu prvků. Při uspořádání do tabulky řadu přerušil tak, aby pod sebe přišly prvky s podobnými vlastnostmi a mocenstvím. Vznikla přirozená soustava prvků kterou Mendělejev nazval periodickou. Periodickou závislost chemických a fyzikálních vlastností prvků na atomové hmotnosti formuloval jako periodický zákon. Protože se později zjistilo, že jediná veličina, která charakterizuje prvek je atomové číslo používáme nyní zákon ve znění. Chemické a mnohé fyzikální vlastnosti prvků jsou periodickou funkcí jejich atomového čísla.
5 Dlouhá periodická tabulka I.a II.a III.b IV.b V.b VI.b VII.b VIII.b VIII.b VIII.b I.b II.b III.a IV.a V.a VI.a VII.a VIII.a 1. H He 2. Li Be B C N O F Ne 3. Na Mg Al Si P S Cl Ar 4. K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5. Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6. CS Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 7. Fr Ra Ac Lanthanoidy Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Aktinoidy Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lw
6 Prvky jsou v periodické tabulce uspořádány do sedmi vodorovných řad, zvaných periody. V první periodě jsou dva prvky, vodík a helium. Druhá a třetí perioda má po osmi prvcích. Čtvrtá a pátá perioda má po 18 prvcích. Šestá perioda obsahuje 32 prvků. Poslední sedmá perioda, dosud neúplná má dosud devatenáct prvků. Z šesté periody je v dlouhé tabulce vyloučeno 14 prvků- lanthanoidy. Ze sedmé periody 14 prvků- aktinoidy. Periody se značí arabskými číslicemi 1 až 7. Číslice odpovídá elektronovým vrstvám (slupkám) K, L, M, N, O, P, Q. Počet elektronů ve slupkách je 2, 8, 8, 16, 16, 32, 32. Úplně zaplněnou slupku mají vzácné plyny He, Ne, Ar, Kr, Xe, Rn. Jejich atomová čísla jsou 2, 10, 18, 36, 54 a 86. Svisle jsou prvky uspořádány do osmi skupin. Každá skupina je dvojnásobná, hlavní, označená a. Vedlejší, označená b. V hlavních podskupinách jsou nepřechodné prvky s valenčními elektrony v orbitalu s a p. Ve vedlejších podskupinách jsou prvky přechodné s valenčními elektrony v orbitalu d. Lanthanoidy a aktinoidy s valenčními elektrony v orbitalu f se označují jako vnitřně přechodné. Skupiny se označují římskými číslicemi I. až VIII. Skupina VIII.b je trojnásobná. Obsahuje trojice železných, lehkých a těžkých platinových kovů.
7 Některé skupiny prvků mají své zažité názvy. I.a alkalické kovy Li, Na, K, Rb, Cs, Fr II.a kovy alkalických zemin Ca, Sr, Ba, Ra III.a triely B, Al, Ga, In, Tl IV.a tetrely C, Si, Ge, Sn, Pb V.a pentely N, P, As, Sb, Bi VI.a chalkogeny O, S, Se, Te, Po VII.a halogeny F, Cl, Br, I, At VIII.a vzácné plyny He, Ne, Ar, Kr, Xe, Rn
8 Vlastnosti prvků. Vlastnosti prvků A r, kovový a nekovový charakter, ionizační potenciál, elektronová afinita, elektronegativita, oxidačně redukční vlastnosti, kyselinotvornost a zásadotvornost souvisí s postavením prvku v periodické tabulce. Uděláme-li tabulkou myšlenou čáru od bóru po astat. Leží kovy pod touto čárou. Nad čárou leží nekovy. Relativní atomová hmotnost roste v periodách zleva doprava a ve skupinách shora dolů. Ostatní vlastnosti se mění po úhlopříčce zleva dole doprava nahoru. Nejnižší elektronegativitu má francium, největší fluor. Prvky vlevo v tabulce elektrony snadno uvolňují, tvoří kationty a chovají se jako redukční činidla. Prvky vpravo v tabulce se stabilizují přijetím elektronů, tvoří anionty a chovají se jako oxidační činidla. Vlevo v tabulce leží prvky zásadotvorné. Vpravo kyselinotvorné.
9 Oxidační čísla Také oxidační čísla prvků ve sloučeninách souvisí s postavením prvků v periodické tabulce. Platí, že nejvyšší kladné oxidační číslo, kterého může prvek dosáhnout se rovná číslu skupiny, v níž leží. To platí s výjimkou kyslíku, který může nabývat maximálního oxidačního čísla +II a fluóru, který se ve sloučeninách s kladným oxidačním číslem vůbec nevyskytuje. Takže prvky I.a i b skupiny mají maximální oxidační číslo +I, prvky II.a i b skupiny +II, III.a i b +III atd. Také nejnižší záporná oxidační čísla prvků můžeme dostat odečteme-li od čísla 8 číslo skupiny v níž prvek leží. Takže prvky skupiny VII.a, halogeny mají nejnižší záporné oxidační číslo I. Prvky VI.a skupiny mají nejnižší oxidační číslo II. Prvky V.a III, IV.a IV.
10 Test Jestlipak dokážete vybrat pětici prvků které v periodické tabulce chybí. a) Sc, V, Pt, Os, Pb b) K, Ba, Mn, Al, Br c) K, Ba, Mn, Hg, Br I.a II.a III.b IV.b V.b VI.b VII.b VIII.b VIII.b VIII.b I.b II.b III.a IV.a V.a VI.a VII.a VIII.a 1. H He 2. Li Be B C N O F Ne 3. Na Mg Al Si P S Cl Ar 4. Ca Sc Ti V Cr Fe Co Ni Cu Zn Ga Ge As Se Kr 5. Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6. Cs La Hf Ta W Re Os Ir Pt Au Tl Pb Bi Po At Rn 7. Fr Ra Ac Konec prezentace
11 Výborně. D.I. Mendělejev
12 Chyba! Ještě se musíš hodně učit.
13 Použitá literatura MAREČEK, Aleš a Jaroslav HONZA. Chemie pro čtyřletá gymnázia. 3., přeprac. vyd. Olomouc: Nakladatelství Olomouc, 2005, 240 s. ISBN ŠRÁMEK, Vratislav a Ludvík KOSINA. Obecná a anorganická chemie. 2. vyd. Olomouc: Nakladatelství Olomouc, 2000, 262 s. ISBN
14 Registrační číslo projektu Šablona Autor Název materiálu CZ.1.07/1.5.00/ III/2 INOVACE A ZKVALITNĚNÍ VÝUKY PROSTŘEDNICTVÍM ICT Ing. František Paseka 20. Periodická soustava prvků Ověřeno ve výuce dne Předmět Ročník Klíčová slova Anotace Metodický pokyn Chemie První Periodický zákon, dlouhá periodická tabulka, periody, skupiny, prvky nepřechodné, přechodné, vnitřně přechodné, kovy, nekovy, vlastnosti prvků, oxidační čísla. Úvodní snímek věnovaný chemickým prvkům. Uvádí se rozdělení podle kovového charakteru, skupenství a počtu izotopů. Na následném snímku je vysvětlen a zapsán periodický zákon. Dále se ukazuje a diskutuje dlouhá periodická tabulka. Část snímků je věnována vztahu mezi postavením prvků v PSP a jejich vlastnostmi. Na závěr je test ze znalosti postavení prvků v dlouhé tabulce. Prezentace je určena jako výklad do hodiny i jako materiál určený k samostudiu Počet stran 14 Pokud není uvedeno jinak, použitý materiál je z vlastních zdrojů autora.
DIGITÁLNÍ UČEBNÍ MATERIÁL. Ing. Alena Musilová ŠVP cukrář-cukrovinkář; ZPV chemie, 1. ročník ŠVP kuchař-číšník;zpv chemie, 1.
 DIGITÁLNÍ UČEBNÍ MATERIÁL Číslo projektu CZ.1.07/1.5.00/34.0763 Název školy SOUpotravinářské, Jílové u Prahy, Šenflukova 220 Název materiálu INOVACE_32_ZPV-CH 1/04/02/1 Autor Obor; předmět, ročník Tematická
DIGITÁLNÍ UČEBNÍ MATERIÁL Číslo projektu CZ.1.07/1.5.00/34.0763 Název školy SOUpotravinářské, Jílové u Prahy, Šenflukova 220 Název materiálu INOVACE_32_ZPV-CH 1/04/02/1 Autor Obor; předmět, ročník Tematická
Chemie = přírodní věda zkoumající složení a strukturu látek a jejich přeměny v látky jiné
 Otázka: Obecná chemie Předmět: Chemie Přidal(a): ZuzilQa Základní pojmy v chemii, periodická soustava prvků Chemie = přírodní věda zkoumající složení a strukturu látek a jejich přeměny v látky jiné -setkáváme
Otázka: Obecná chemie Předmět: Chemie Přidal(a): ZuzilQa Základní pojmy v chemii, periodická soustava prvků Chemie = přírodní věda zkoumající složení a strukturu látek a jejich přeměny v látky jiné -setkáváme
ACH 02 VZÁCNÉPLYNY. Katedra chemie FP TUL www.kch.tul.cz VZÁCNÉ PLYNY
 VZÁCNÉPLYNY ACH 02 Katedra chemie FP TUL www.kch.tul.cz VZÁCNÉ PLYNY 1 VZÁCNÉ PLYNY 2 Vzácné plyny 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 I II III IV V VI VII VIII I II III IV V VI VII VIII s 2 p
VZÁCNÉPLYNY ACH 02 Katedra chemie FP TUL www.kch.tul.cz VZÁCNÉ PLYNY 1 VZÁCNÉ PLYNY 2 Vzácné plyny 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 I II III IV V VI VII VIII I II III IV V VI VII VIII s 2 p
www.zlinskedumy.cz Inovace výuky prostřednictvím šablon pro SŠ
 Název projektu Číslo projektu Název školy Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Tematický okruh Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748
Název projektu Číslo projektu Název školy Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Tematický okruh Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748
VY_52_INOVACE_08_II.1.23_TABULKA, PERIODICKÁ SOUSTAVA PRVKŮ TABULKA PERIODICKÁ SOUSTAVA PRVKŮ
 VY_52_INOVACE_08_II.1.23_TABULKA, PERIODICKÁ SOUSTAVA PRVKŮ TABULKA PERIODICKÁ SOUSTAVA PRVKŮ PERIODICKÁ SOUSTAVA PRVKŮ 8. TŘÍDA PERIODICKÝ ZÁKON FYZIKÁLNÍ A CHEMICKÉ VLASTNOSTI PRVKŮ JSOU PERIODICKOU
VY_52_INOVACE_08_II.1.23_TABULKA, PERIODICKÁ SOUSTAVA PRVKŮ TABULKA PERIODICKÁ SOUSTAVA PRVKŮ PERIODICKÁ SOUSTAVA PRVKŮ 8. TŘÍDA PERIODICKÝ ZÁKON FYZIKÁLNÍ A CHEMICKÉ VLASTNOSTI PRVKŮ JSOU PERIODICKOU
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 08.04.2013 Číslo DUMu: VY_32_INOVACE_01_Ch_ACH
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 08.04.2013 Číslo DUMu: VY_32_INOVACE_01_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 08.04.2013 Číslo DUMu: VY_32_INOVACE_01_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 09.04.2013 Číslo DUMu: VY_32_INOVACE_02_Ch_ACH
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 09.04.2013 Číslo DUMu: VY_32_INOVACE_02_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 09.04.2013 Číslo DUMu: VY_32_INOVACE_02_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Šablona III/2 číslo materiálu 393
 Šablona III/2 číslo materiálu 393 Jméno autora Mgr. Alena Krejčíková Třída/ ročník 1. ročník Datum vytvoření 20.10.2013 Vzdělávací oblast: Tematická oblast: Předmět: Anotace: Klíčová slova: Druh učebního
Šablona III/2 číslo materiálu 393 Jméno autora Mgr. Alena Krejčíková Třída/ ročník 1. ročník Datum vytvoření 20.10.2013 Vzdělávací oblast: Tematická oblast: Předmět: Anotace: Klíčová slova: Druh učebního
VZÁCNÉ PLYNY ACH 02. Katedra chemie FP TUL
 VZÁCNÉ PLYNY ACH 02 Katedra chemie FP TUL www.kch.tul.cz VZÁCNÉ PLYNY VZÁCNÉ PLYNY Xenon Radon Vzácné plyny 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 I II III IV V VI VII VIII I II III IV V VI VII
VZÁCNÉ PLYNY ACH 02 Katedra chemie FP TUL www.kch.tul.cz VZÁCNÉ PLYNY VZÁCNÉ PLYNY Xenon Radon Vzácné plyny 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 I II III IV V VI VII VIII I II III IV V VI VII
Ch - Periodický zákon, periodická tabulka prvků
 Ch - Periodický zákon, periodická tabulka prvků Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento
Ch - Periodický zákon, periodická tabulka prvků Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento
Ch - Stavba atomu, chemická vazba
 Ch - Stavba atomu, chemická vazba Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl
Ch - Stavba atomu, chemická vazba Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl
Orbitaly ve víceelektronových atomech
 Orbitaly ve víceelektronových atomech Elektrony jsou přitahovány k jádru ale také se navzájem odpuzují. Repulzní síly způsobené dalšími elektrony stíní přitažlivý účinek atomového jádra. Efektivní náboj
Orbitaly ve víceelektronových atomech Elektrony jsou přitahovány k jádru ale také se navzájem odpuzují. Repulzní síly způsobené dalšími elektrony stíní přitažlivý účinek atomového jádra. Efektivní náboj
Elektrické vlastnosti látek
 Elektrické vlastnosti látek Druhy elektrického náboje elektrické vlastnosti souvisí nějak s elektrony? částice v atomu jsme značili takto: elekron, proton, neutron znaménka +, - v kolečku značí vlastnost
Elektrické vlastnosti látek Druhy elektrického náboje elektrické vlastnosti souvisí nějak s elektrony? částice v atomu jsme značili takto: elekron, proton, neutron znaménka +, - v kolečku značí vlastnost
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 20.04.2013 Číslo DUMu: VY_32_INOVACE_15_Ch_ACH
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 20.04.2013 Číslo DUMu: VY_32_INOVACE_15_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 20.04.2013 Číslo DUMu: VY_32_INOVACE_15_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Geochemie endogenních procesů 1. část
 Geochemie endogenních procesů 1. část geochemie = použití chemických nástrojů na studium Země a dalších planet Sluneční soustavy počátky v 15. století spjaté zejména s kvalitou vody a půdy rozmach a první
Geochemie endogenních procesů 1. část geochemie = použití chemických nástrojů na studium Země a dalších planet Sluneční soustavy počátky v 15. století spjaté zejména s kvalitou vody a půdy rozmach a první
VLASTNOSTI KOVŮ. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 12. 10. 2012. Ročník: osmý
 Autor: Mgr. Stanislava Bubíková VLASTNOSTI KOVŮ Datum (období) tvorby: 12. 10. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Částicové složení látek a chemické prvky 1 Anotace: Žáci
Autor: Mgr. Stanislava Bubíková VLASTNOSTI KOVŮ Datum (období) tvorby: 12. 10. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Částicové složení látek a chemické prvky 1 Anotace: Žáci
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto Výjimky z pravidelné elektronové konfigurace atomů, aneb snaha o dosažení stability. Stabilita vzácných plynů Vzácné plyny mají velmi stabilní
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto Výjimky z pravidelné elektronové konfigurace atomů, aneb snaha o dosažení stability. Stabilita vzácných plynů Vzácné plyny mají velmi stabilní
Periodická soustava prvků
 Periodická soustava prvků Historie: 1789 Lavoisier kovy a nekovy 1818 Berzelius podle reaktivity 1817 Döbereiner triády 1863 Newlands oktávy 1864 Mayer grafická závislost vlastností prvků na atomovém čísle,
Periodická soustava prvků Historie: 1789 Lavoisier kovy a nekovy 1818 Berzelius podle reaktivity 1817 Döbereiner triády 1863 Newlands oktávy 1864 Mayer grafická závislost vlastností prvků na atomovém čísle,
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou PERIODICKÁ TABULKA PRVKŮ PERIODICKÝ ZÁKON VY_32_INOVACE_03_3_06_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou Dmitrij
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou PERIODICKÁ TABULKA PRVKŮ PERIODICKÝ ZÁKON VY_32_INOVACE_03_3_06_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou Dmitrij
Základní stavební částice
 Základní stavební částice ATOMY Au O H Elektroneutrální 2 H 2 atomy vodíku 8 Fe Ř atom železa IONTY Na + Cl - H 3 O + P idávat nebo odebírat se mohou jenom elektrony Kationty Kladn nabité Odevzdání elektron
Základní stavební částice ATOMY Au O H Elektroneutrální 2 H 2 atomy vodíku 8 Fe Ř atom železa IONTY Na + Cl - H 3 O + P idávat nebo odebírat se mohou jenom elektrony Kationty Kladn nabité Odevzdání elektron
KONTROLNÍ TEST ŠKOLNÍHO KOLA
 Ústřední komise Chemické olympiády 50. ročník 2013/2014 ŠKOLNÍ KOLO kategorie D KONTROLNÍ TEST ŠKOLNÍHO KOLA časová náročnost: 90 minut 1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16 17
Ústřední komise Chemické olympiády 50. ročník 2013/2014 ŠKOLNÍ KOLO kategorie D KONTROLNÍ TEST ŠKOLNÍHO KOLA časová náročnost: 90 minut 1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16 17
Fyzika (učitelství) Zkouška - teoretická fyzika. Čas k řešení je 120 minut (6 minut na úlohu): snažte se nejprve rychle vyřešit ty nejsnazší úlohy,
 Státní bakalářská zkouška. 9. 05 Fyzika (učitelství) Zkouška - teoretická fyzika (test s řešením) Jméno: Pokyny k řešení testu: Ke každé úloze je správně pouze jedna odpověď. Čas k řešení je 0 minut (6
Státní bakalářská zkouška. 9. 05 Fyzika (učitelství) Zkouška - teoretická fyzika (test s řešením) Jméno: Pokyny k řešení testu: Ke každé úloze je správně pouze jedna odpověď. Čas k řešení je 0 minut (6
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 05.04.2013 Číslo DUMu: VY_32_INOVACE_07_Ch_ACH
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 05.04.2013 Číslo DUMu: VY_32_INOVACE_07_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 05.04.2013 Číslo DUMu: VY_32_INOVACE_07_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Periodická soustava prvků
 Periodická soustava prvků 1829 Döbereiner Triády: Li, Na, K; Ca, Sr, Ba; S, Se, Te; Cl, Br, I; 1870 Meyer - atomové objemy 1869, 1871 Mendelejev předpověď vlastností chybějících prvků (Sc, Ga, Ge, Tc,
Periodická soustava prvků 1829 Döbereiner Triády: Li, Na, K; Ca, Sr, Ba; S, Se, Te; Cl, Br, I; 1870 Meyer - atomové objemy 1869, 1871 Mendelejev předpověď vlastností chybějících prvků (Sc, Ga, Ge, Tc,
1 18 I. A VIII. A 1,00794 4,003. relativní atomová hmotnost. 3Li 4Be 9F 5B 6C 7N 8O 9F 10Ne 0,97 1,50 4,10 2,00 2,50 3,10 3,50 4,10.
 1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16 17 2He 2,20 II. A III. A IV. A V. A VI. A VII. A Vodík relativní atomová hmotnost Helium 6,941 9,012 18,998 10,811 12,011 14,007 15,999 18,998
1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16 17 2He 2,20 II. A III. A IV. A V. A VI. A VII. A Vodík relativní atomová hmotnost Helium 6,941 9,012 18,998 10,811 12,011 14,007 15,999 18,998
KONTROLNÍ TEST ŠKOLNÍHO KOLA
 Ústřední komise Chemické olympiády 51. ročník 2014/2015 ŠKOLNÍ KOLO kategorie D KONTROLNÍ TEST ŠKOLNÍHO KOLA časová náročnost: 90 minut 1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16 17
Ústřední komise Chemické olympiády 51. ročník 2014/2015 ŠKOLNÍ KOLO kategorie D KONTROLNÍ TEST ŠKOLNÍHO KOLA časová náročnost: 90 minut 1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16 17
Složení látek a chemická vazba Číslo variace: 1
 Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Složení látek a chemická vazba Číslo variace: 1 Zkoušecí kartičku si PODEPIŠ a zapiš na ni ČÍSLO VARIACE TESTU (číslo v pravém horním rohu). Odpovědi zapiš na zkoušecí kartičku, do testu prosím nepiš.
Průvodka. CZ.1.07/1.5.00/ Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 13.04.2013 Číslo DUMu: VY_32_INOVACE_09_Ch_ACH
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 13.04.2013 Číslo DUMu: VY_32_INOVACE_09_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 13.04.2013 Číslo DUMu: VY_32_INOVACE_09_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
PERIODICKÁ TABULKA PRVKŮ. www.egmont.cz
 PERIODICKÁ TABULKA PRVKŮ www.egmont.cz 1 PERIODICKÁ H VODÍK 3 4 TABULKA PRVKŮ Be BERYLLIUM Li LITHIUM 11 12 CHEMICKÉ PRVKY, KTERÉ MAJÍ STYL! Mg Na SODÍK HOŘČÍK 20 19 Ca K DRASLÍK Sr Cs BARYUM Ra Fr RADIUM
PERIODICKÁ TABULKA PRVKŮ www.egmont.cz 1 PERIODICKÁ H VODÍK 3 4 TABULKA PRVKŮ Be BERYLLIUM Li LITHIUM 11 12 CHEMICKÉ PRVKY, KTERÉ MAJÍ STYL! Mg Na SODÍK HOŘČÍK 20 19 Ca K DRASLÍK Sr Cs BARYUM Ra Fr RADIUM
ELEKTROTECHNICKÉ MATERIÁLY
 ELEKTROTECHNICKÉ MATERIÁLY PŘEDNÁŠÍ: Prof. Ing. Jaromír r Drápala, CSc. VEDOUCÍ CVIČEN ENÍ : Ing. Kateřina Skotnicová, Ph.D. (A622) Čt 7.15-8.45; 9.00-10.30 Ing. Ivo Szurman, Ph.D. (J304) Čt 12.30-14.00;
ELEKTROTECHNICKÉ MATERIÁLY PŘEDNÁŠÍ: Prof. Ing. Jaromír r Drápala, CSc. VEDOUCÍ CVIČEN ENÍ : Ing. Kateřina Skotnicová, Ph.D. (A622) Čt 7.15-8.45; 9.00-10.30 Ing. Ivo Szurman, Ph.D. (J304) Čt 12.30-14.00;
Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan. Datum tvorby
 Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie ATOM 1. ročník Datum tvorby 31.10.2013 Anotace a) určeno pro
Číslo projektu CZ.1.07/1.5.00/34.0743 Název školy Autor Tematická oblast Ročník Moravské gymnázium Brno s.r.o. RNDr. Miroslav Štefan Chemie ATOM 1. ročník Datum tvorby 31.10.2013 Anotace a) určeno pro
Chemické výpočty. výpočty ze sloučenin
 Cheické výpočty výpočty ze sloučenin Cheické výpočty látkové nožství n, 1 ol obsahuje stejný počet stavebních částic, kolik je atoů ve 1 g uhlíku 1 C počet částic v 1 olu stanovuje Avogadrova konstanta
Cheické výpočty výpočty ze sloučenin Cheické výpočty látkové nožství n, 1 ol obsahuje stejný počet stavebních částic, kolik je atoů ve 1 g uhlíku 1 C počet částic v 1 olu stanovuje Avogadrova konstanta
Elektronová mikroskopie a mikroanalýza-2
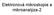 Elektronová mikroskopie a mikroanalýza-2 elektronové dělo elektronové dělo je zařízení, které produkuje elektrony uspořádané do svazku (paprsku) elektrony opustí svůj zdroj katodu- po dodání určité množství
Elektronová mikroskopie a mikroanalýza-2 elektronové dělo elektronové dělo je zařízení, které produkuje elektrony uspořádané do svazku (paprsku) elektrony opustí svůj zdroj katodu- po dodání určité množství
SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI
 Ústřední komise Chemické olympiády 51. ročník 2014/2015 ŠKOLNÍ KOLO kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Školní kolo ChO kat. D 2014/2015 V souladu se zásadami pro organizování soutěží je pro vedení
Ústřední komise Chemické olympiády 51. ročník 2014/2015 ŠKOLNÍ KOLO kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI Školní kolo ChO kat. D 2014/2015 V souladu se zásadami pro organizování soutěží je pro vedení
PERIODICKÁ SOUSTAVA PRVKŮ
 PERIODICKÁ SOUSTAVA PRVKŮ Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 13. 9. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Částicové složení látek a chemické prvky 1 Anotace:
PERIODICKÁ SOUSTAVA PRVKŮ Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 13. 9. 2012 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Částicové složení látek a chemické prvky 1 Anotace:
Klasifikace struktur
 Klasifikace struktur typ vazby iontové, kovové, kovalentní, molekulové homodesmické x heterodesmické stechiometrie prvky, binární: X, X, m X n, ternární: m B k X n,... Title page symetrie prostorové grupy
Klasifikace struktur typ vazby iontové, kovové, kovalentní, molekulové homodesmické x heterodesmické stechiometrie prvky, binární: X, X, m X n, ternární: m B k X n,... Title page symetrie prostorové grupy
Periodická soustava prvků Prvky známé od nepaměti: Au, Ag, Fe, S, C, Zn, Cu, Sn, Pb, Hg, Bi P první objevený prvek, Hennig Brand (1669) Lavoisier
 Periodická soustava prvků Prvky známé od nepaměti: Au, Ag, Fe, S, C, Zn, Cu, Sn, Pb, Hg, Bi P první objevený prvek, Hennig Brand (1669) Lavoisier 1789 33 (21) prvků Traité Élémentaire de Chimie (1789)
Periodická soustava prvků Prvky známé od nepaměti: Au, Ag, Fe, S, C, Zn, Cu, Sn, Pb, Hg, Bi P první objevený prvek, Hennig Brand (1669) Lavoisier 1789 33 (21) prvků Traité Élémentaire de Chimie (1789)
Metodický postup stanovení kovů v půdách volných hracích ploch metodou RTG.
 Strana : 1 1) Význam a použití: Metoda je používána pro stanovení prvků v půdách volných hracích ploch. 2) Princip: Vzorek je po odběru homogenizován, je stanovena sušina, ztráta žíháním. Suchý vzorek
Strana : 1 1) Význam a použití: Metoda je používána pro stanovení prvků v půdách volných hracích ploch. 2) Princip: Vzorek je po odběru homogenizován, je stanovena sušina, ztráta žíháním. Suchý vzorek
Periodická soustava prvků
 Periodická soustava prvků Lavoisier 1789 33(21) prvků Traité Élémentaire de Chimie (1789) první moderní učebnice chemie Dalton 1808-36 prvků Berzelius 1813-14 - 47 prvků Mendělejev 1869-63 prvků Poslední
Periodická soustava prvků Lavoisier 1789 33(21) prvků Traité Élémentaire de Chimie (1789) první moderní učebnice chemie Dalton 1808-36 prvků Berzelius 1813-14 - 47 prvků Mendělejev 1869-63 prvků Poslední
Vyučující po spuštění prezentace může provádět výklad a zároveň vytvářet zápis. Výklad je doprovázen cvičeními k osvojení probírané tématiky.
 Projekt: Příjemce: Tvořivá škola, registrační číslo projektu CZ.1.07/1.4.00/21.3505 Základní škola Ruda nad Moravou, okres Šumperk, Sportovní 300, 789 63 Ruda nad Moravou Zařazení materiálu: Šablona: Sada:
Projekt: Příjemce: Tvořivá škola, registrační číslo projektu CZ.1.07/1.4.00/21.3505 Základní škola Ruda nad Moravou, okres Šumperk, Sportovní 300, 789 63 Ruda nad Moravou Zařazení materiálu: Šablona: Sada:
Chemické názvosloví anorganika Nápověda
 Chemické názvosloví anorganika Nápověda Jan Hrnčíř janhrncir@seznam.cz Gymnázium F. X. Šaldy Liberec 2006 Obsah 0 Úvod...2 1 Základní rozvržení...3 2 Testování...4 3 Sloučeniny...8 4 Prvky... 11 5 Pro
Chemické názvosloví anorganika Nápověda Jan Hrnčíř janhrncir@seznam.cz Gymnázium F. X. Šaldy Liberec 2006 Obsah 0 Úvod...2 1 Základní rozvržení...3 2 Testování...4 3 Sloučeniny...8 4 Prvky... 11 5 Pro
ACH 03 ALKALICKÉ KOVY. Katedra chemie FP TUL
 ACH 03 ALKALICKÉ KOVY Katedra chemie FP TUL www.kch.tul.cz ALKALICKÉ KOVY s 1 Li I II III IV V VI VII VIII I II III IV V VI VII VIII 1 H n s n p He 2 Li Be B C N O F Ne 3 Na Mg (n-1) d Al Si P S Cl Ar
ACH 03 ALKALICKÉ KOVY Katedra chemie FP TUL www.kch.tul.cz ALKALICKÉ KOVY s 1 Li I II III IV V VI VII VIII I II III IV V VI VII VIII 1 H n s n p He 2 Li Be B C N O F Ne 3 Na Mg (n-1) d Al Si P S Cl Ar
Zařazení materiálu: Šablona: Sada: Inovace a zkvalitnění výuky v oblasti přírodních věd (V/2) Název materiálu: Autor materiálu: Pavel Polák
 Projekt: Příjemce: Tvořivá škola, registrační číslo projektu CZ.1.07/1.4.00/21.3505 Základní škola Ruda nad Moravou, okres Šumperk, Sportovní 300, 789 63 Ruda nad Moravou Zařazení materiálu: Šablona: Sada:
Projekt: Příjemce: Tvořivá škola, registrační číslo projektu CZ.1.07/1.4.00/21.3505 Základní škola Ruda nad Moravou, okres Šumperk, Sportovní 300, 789 63 Ruda nad Moravou Zařazení materiálu: Šablona: Sada:
Ceník. Platný od 01. 07. 2014. Laboratorní standardy a chemikálie. Ceny uvedené v tomto ceníku nezahrnují 21% DPH, balné a dopravné
 Ceník Platný od 01. 07. 2014 Laboratorní standardy a chemikálie Ceny uvedené v tomto ceníku nezahrnují 21% DPH, balné a dopravné Změna cen vyhrazena bez předchozího upozornění K objednávkám v ceně zboží
Ceník Platný od 01. 07. 2014 Laboratorní standardy a chemikálie Ceny uvedené v tomto ceníku nezahrnují 21% DPH, balné a dopravné Změna cen vyhrazena bez předchozího upozornění K objednávkám v ceně zboží
PERIODICKÁ SÚSTAVA PRVKOV
 PERIODICKÁ SÚSTAVA PRVKOV PERIODICKÝ ZÁKON Mendelejev (1869) zoradil 68 známych prvkov do sústavy na základe periodického zákona: Vlastnosti prvkov a ich zlúčenín sú periodickou funkciou ich atómových
PERIODICKÁ SÚSTAVA PRVKOV PERIODICKÝ ZÁKON Mendelejev (1869) zoradil 68 známych prvkov do sústavy na základe periodického zákona: Vlastnosti prvkov a ich zlúčenín sú periodickou funkciou ich atómových
Střední odborná škola a Střední odborné učiliště, Hradec Králové, Vocelova 1338, příspěvková organizace
 Střední odborná škola a Střední odborné učiliště, Hradec Králové, Vocelova 1338, příspěvková organizace Registrační číslo projektu: Číslo DUM: Tematická oblast: Téma: Autor: CZ.1.07/1.5.00/34.0245 VY_32_INOVACE_08_A_07
Střední odborná škola a Střední odborné učiliště, Hradec Králové, Vocelova 1338, příspěvková organizace Registrační číslo projektu: Číslo DUM: Tematická oblast: Téma: Autor: CZ.1.07/1.5.00/34.0245 VY_32_INOVACE_08_A_07
??????? Záporně nabitá částice... ANION. Těžký, toxický, červenohnědý, kapalný halogen... VY_32_INOVACE_193 6. 6. 2013
 VY_32_INVACE_193 6. 6. 2013 Popis a použití výukového materiálu Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.4.00/21.3707 Šablona: III/2 Č. materiálu:
VY_32_INVACE_193 6. 6. 2013 Popis a použití výukového materiálu Výukový materiál zpracován v rámci projektu EU peníze školám Registrační číslo projektu: CZ.1.07/1.4.00/21.3707 Šablona: III/2 Č. materiálu:
SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI
 Ústřední komise Chemické olympiády 51. ročník 2014/2015 OKRESNÍ KOLO kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI časová náročnost: 90 minut 1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16
Ústřední komise Chemické olympiády 51. ročník 2014/2015 OKRESNÍ KOLO kategorie D SOUTĚŽNÍ ÚLOHY TEORETICKÉ ČÁSTI časová náročnost: 90 minut 1 18 I. A VIII. A 1 2 3 4 5 6 7 1,00794 4,003 1H 2 13 14 15 16
212 a. 5. Vyzáří-li radioaktivní nuklid aktinia částici α, přemění se na atom: a) radia b) thoria c) francia d) protaktinia e) zůstane aktinium
 Pracovní list - Jaderné reakce 1. Vydává-li radionuklid záření alfa: a) protonové číslo se zmenšuje o 4 a nukleonové číslo se nemění b) nukleonové číslo se změní o 4 a protonové se nemění c) protonové
Pracovní list - Jaderné reakce 1. Vydává-li radionuklid záření alfa: a) protonové číslo se zmenšuje o 4 a nukleonové číslo se nemění b) nukleonové číslo se změní o 4 a protonové se nemění c) protonové
Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností
 Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností obrázky molekul a Lewisovy vzorce molekul v této přednášce čerpány z:
Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností obrázky molekul a Lewisovy vzorce molekul v této přednášce čerpány z:
Vzdělávací oblast: Člověk a příroda. Vyučovací předmět: Chemie. Třída: tercie. Očekávané výstupy. Poznámky. Přesahy. Žák: Průřezová témata
 Vzdělávací oblast: Člověk a příroda Vyučovací předmět: Chemie Třída: tercie Očekávané výstupy Uvede příklady chemického děje a čím se zabývá chemie Rozliší tělesa a látky Rozpozná na příkladech fyzikální
Vzdělávací oblast: Člověk a příroda Vyučovací předmět: Chemie Třída: tercie Očekávané výstupy Uvede příklady chemického děje a čím se zabývá chemie Rozliší tělesa a látky Rozpozná na příkladech fyzikální
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 16.04.2013 Číslo DUMu: VY_32_INOVACE_12_Ch_ACH
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 16.04.2013 Číslo DUMu: VY_32_INOVACE_12_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 16.04.2013 Číslo DUMu: VY_32_INOVACE_12_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto H 2 + Cl 2 2HCl Jak si představit rychlost chemické reakce? Obecný zápis chemické reakce A B C D Kde α, β, γ, δ jsou stechiometrické koeficienty,
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto H 2 + Cl 2 2HCl Jak si představit rychlost chemické reakce? Obecný zápis chemické reakce A B C D Kde α, β, γ, δ jsou stechiometrické koeficienty,
NITON XL3t GOLDD+ Nový analyzátor
 Nový analyzátor NITON XL3t GOLDD+ Ruční rentgenový analyzátor NITON XL3t GOLDD+ je nejnovější model od Thermo Fisher Scientific. Navazuje na úspěšný model NITON XL3t GOLDD. Díky špičkovým technologiím
Nový analyzátor NITON XL3t GOLDD+ Ruční rentgenový analyzátor NITON XL3t GOLDD+ je nejnovější model od Thermo Fisher Scientific. Navazuje na úspěšný model NITON XL3t GOLDD. Díky špičkovým technologiím
Název školy: Číslo a název sady: klíčové aktivity: VY_32_INOVACE_131_Elektrochemická řada napětí kovů_pwp
 Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: Předmět, ročník, obor: Číslo a název sady: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ
Název školy: Číslo a název projektu: Číslo a název šablony klíčové aktivity: Označení materiálu: Typ materiálu: Předmět, ročník, obor: Číslo a název sady: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ
Úvod Vlastnosti materiálů a pojmy, které byste měli znát
 Úvod Vlastnosti materiálů a pojmy, které byste měli znát Co je to materiál? Definice hmota, která splňuje svými vlastnostmi nároky na spolehlivou funkci a požadovanou životnost. Jaké znáte příklady? Ve
Úvod Vlastnosti materiálů a pojmy, které byste měli znát Co je to materiál? Definice hmota, která splňuje svými vlastnostmi nároky na spolehlivou funkci a požadovanou životnost. Jaké znáte příklady? Ve
Otázka: Periodická soustava prvků. Předmět: Chemie. Přidal(a): Claire Rye
 Otázka: Periodická soustava prvků Předmět: Chemie Přidal(a): Claire Rye Periodický zákon: Vlastnosti prvků jsou periodickou funkcí jejich protonového čísla. (vyplývá z pravidel, jimiž se řídí výstavba
Otázka: Periodická soustava prvků Předmět: Chemie Přidal(a): Claire Rye Periodický zákon: Vlastnosti prvků jsou periodickou funkcí jejich protonového čísla. (vyplývá z pravidel, jimiž se řídí výstavba
Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností
 Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností obrázky molekul a Lewisovy vzorce molekul v této přednášce čerpány z:
Periodický systém víceelektronové systémy elektronová konfigurace periodický systém periodicita fyzikálních a chemických vlastností obrázky molekul a Lewisovy vzorce molekul v této přednášce čerpány z:
Test pro 8. třídy A. 3) Vypočítej kolik potřebuješ gramů soli na přípravu 600 g 5 % roztoku.
 Test pro 8. třídy A 1) Rozhodni, zda je správné tvrzení: Vzduch je homogenní směs. a) ano b) ne 2) Přiřaď k sobě: a) voda-olej A) suspenze b) křída ve vodě B) emulze c) vzduch C) aerosol 3) Vypočítej kolik
Test pro 8. třídy A 1) Rozhodni, zda je správné tvrzení: Vzduch je homogenní směs. a) ano b) ne 2) Přiřaď k sobě: a) voda-olej A) suspenze b) křída ve vodě B) emulze c) vzduch C) aerosol 3) Vypočítej kolik
Přílohy. Příloha 1. Mapa s výskytem dolů a pramenů s hladinami vod po r (Čadek et al. 1968) [Zadejte text.]
![Přílohy. Příloha 1. Mapa s výskytem dolů a pramenů s hladinami vod po r (Čadek et al. 1968) [Zadejte text.] Přílohy. Příloha 1. Mapa s výskytem dolů a pramenů s hladinami vod po r (Čadek et al. 1968) [Zadejte text.]](/thumbs/81/83251433.jpg) Přílohy Příloha 1 Mapa s výskytem dolů a pramenů s hladinami vod po r. 1895 (Čadek et al. 1968) Příloha 2 Komplexní rozbor vody z pramene Pravřídlo 2002 (Lázně Teplice) Chemické složení Kationty mg/l mmol/l
Přílohy Příloha 1 Mapa s výskytem dolů a pramenů s hladinami vod po r. 1895 (Čadek et al. 1968) Příloha 2 Komplexní rozbor vody z pramene Pravřídlo 2002 (Lázně Teplice) Chemické složení Kationty mg/l mmol/l
Chemické repetitorium. Václav Pelouch
 ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Chemické repetitorium Václav Pelouch kapitola ve skriptech - 1 Anorganická a obecná chemie Stavba atomu Atom je nejmenší částice hmoty, která obsahuje jádro (složené
ZÁKLADY OBECNÉ A KLINICKÉ BIOCHEMIE 2004 Chemické repetitorium Václav Pelouch kapitola ve skriptech - 1 Anorganická a obecná chemie Stavba atomu Atom je nejmenší částice hmoty, která obsahuje jádro (složené
1. Periodický zákon formuloval: a) John Dalton b) D.I.Mendělejev c) Bohuslav Brauner
 Pracovní list periodická tabulka prvků 1. Periodický zákon formuloval: a) John Dalton b) D.I.Mendělejev c) Bohuslav Brauner 2. Trochu z historie chemie: Čím se zasloužili (přiřaďte): ATOMISTÉ objevy v
Pracovní list periodická tabulka prvků 1. Periodický zákon formuloval: a) John Dalton b) D.I.Mendělejev c) Bohuslav Brauner 2. Trochu z historie chemie: Čím se zasloužili (přiřaďte): ATOMISTÉ objevy v
TEST 2. Anotace: Očekávaný výstup: Klíčová slova Organizace řízení učební činnosti: Nutné pomůcky:
 Anotace: Jazyk Autor Očekávaný výstup: Klíčová slova Organizace řízení učební činnosti: Nutné pomůcky: TEST 2 Test je zaměřen na zopakování kapitol - chemické prvky, kovy, polokovy, nekovy, TPSP. Test
Anotace: Jazyk Autor Očekávaný výstup: Klíčová slova Organizace řízení učební činnosti: Nutné pomůcky: TEST 2 Test je zaměřen na zopakování kapitol - chemické prvky, kovy, polokovy, nekovy, TPSP. Test
Galvanický článek. Li Rb K Na Be Sr Ca Mg Al Be Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi As CU Hg Ag Pt Au
 Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
Řada elektrochemických potenciálů (Beketova řada) v níž je napětí mezi dvojicí kovů tím větší, čím větší je jejich vzdálenost v této řadě. Prvek více vlevo vytěsní z roztoku kov nacházející se vpravo od
VYSOKÁ ŠKOLA BÁŇSKÁ TECHNICKÁ UNIVERZITA OSTRAVA FAKULTA METALURGIE A MATERIÁLOVÉHO INŽENÝRSTVÍ STUDIJNÍ OPORA. Doc. RNDr. Hana KULVEITOVÁ, Ph.D.
 Chemie prvků VYSOKÁ ŠKOLA BÁŇSKÁ TECHNICKÁ UNIVERZITA OSTRAVA FAKULTA METALURGIE A MATERIÁLOVÉHO INŽENÝRSTVÍ STUDIJNÍ OPORA Název opory/předmětu: CHEMIE II. Číslo předmětu: 617403/01 Autor/Autoři: Doc.
Chemie prvků VYSOKÁ ŠKOLA BÁŇSKÁ TECHNICKÁ UNIVERZITA OSTRAVA FAKULTA METALURGIE A MATERIÁLOVÉHO INŽENÝRSTVÍ STUDIJNÍ OPORA Název opory/předmětu: CHEMIE II. Číslo předmětu: 617403/01 Autor/Autoři: Doc.
Kovy a jejich vlastnosti. Kovy dělíme na: a) nepřechodné (s- a p-prvky) b) přechodné (d- a f- prvky)
 Kovy a jejich vlastnosti Kovy dělíme na: a) nepřechodné (s- a p-prvky) b) přechodné (d- a f- prvky) Nepřechodné kovy mají konfiguraci valenční slupky: ns 1 ns 2 ns 2 p 1 ns 2 p 2 ns 2 p 3 ns 2 p 4 ns 2
Kovy a jejich vlastnosti Kovy dělíme na: a) nepřechodné (s- a p-prvky) b) přechodné (d- a f- prvky) Nepřechodné kovy mají konfiguraci valenční slupky: ns 1 ns 2 ns 2 p 1 ns 2 p 2 ns 2 p 3 ns 2 p 4 ns 2
OBSAH. 1) Směsi. 2) Voda, vzduch. 3) Chemické prvky (názvy, značky) atomy prvků, molekuly. 4) Chemické prvky (vlastnosti, použití)
 OBSAH 1) Směsi 2) Voda, vzduch 3) Chemické prvky (názvy, značky) atomy prvků, molekuly 4) Chemické prvky (vlastnosti, použití) 5) Názvosloví halogenidy 6) Názvosloví oxidy, sulfidy 7) Názvosloví kyseliny,
OBSAH 1) Směsi 2) Voda, vzduch 3) Chemické prvky (názvy, značky) atomy prvků, molekuly 4) Chemické prvky (vlastnosti, použití) 5) Názvosloví halogenidy 6) Názvosloví oxidy, sulfidy 7) Názvosloví kyseliny,
Zařazení nekovů v periodické tabulce
 Nekovy Zařazení nekovů v periodické tabulce pouze 17 nekovů [1] špatné vodiče tepla a elektřiny ochotně přijímají valenční elektrony jiných prvků Obecné vlastnosti nekovů izolanty oxidy nekovů jsou kyselinotvorné
Nekovy Zařazení nekovů v periodické tabulce pouze 17 nekovů [1] špatné vodiče tepla a elektřiny ochotně přijímají valenční elektrony jiných prvků Obecné vlastnosti nekovů izolanty oxidy nekovů jsou kyselinotvorné
Kovy II. hlavní skupiny (alkalických zemin + Be,, Mg)
 Kovy II. hlavní skupiny (alkalických zemin + Be,, Mg) I II III IV V VI VII VIII I II III IV V VI VII VIII 1 H n s n p He 2 Li Be B C N O F Ne 3 Na Mg (n-1) d Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co
Kovy II. hlavní skupiny (alkalických zemin + Be,, Mg) I II III IV V VI VII VIII I II III IV V VI VII VIII 1 H n s n p He 2 Li Be B C N O F Ne 3 Na Mg (n-1) d Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co
ISO Guide 34 ISO ISO 9001
 ISO Guide 34 ISO 17025 ISO 9001 OBSAH OBSAH OBSAH 2 O NÁS 4 SYSTÉMY KVALITY 5 REFERENČNÍ MATERIÁLY DLE POŽADAVKŮ ZÁKAZNÍKA 6 DOKUMENTACE 7 TECHNICKÁ PODPORA 9 VODNÉ CERTIFIKOVANÉ REFERENČNÍ MATERIÁLY
ISO Guide 34 ISO 17025 ISO 9001 OBSAH OBSAH OBSAH 2 O NÁS 4 SYSTÉMY KVALITY 5 REFERENČNÍ MATERIÁLY DLE POŽADAVKŮ ZÁKAZNÍKA 6 DOKUMENTACE 7 TECHNICKÁ PODPORA 9 VODNÉ CERTIFIKOVANÉ REFERENČNÍ MATERIÁLY
Potenciální zdroje kritických surovin v ČR RNDr. Petr Rambousek RNDr. Jaromír Starý. Cínovec - odkaliště
 Potenciální zdroje kritických surovin v ČR RNDr. Petr Rambousek RNDr. Jaromír Starý Cínovec - odkaliště 1 Nerostné suroviny provázejí téměř každou lidskou činnost od počátku existence lidstva. Samotné
Potenciální zdroje kritických surovin v ČR RNDr. Petr Rambousek RNDr. Jaromír Starý Cínovec - odkaliště 1 Nerostné suroviny provázejí téměř každou lidskou činnost od počátku existence lidstva. Samotné
Periodický zákon, periodická tabulka, periodicita chemických a fyzikálních vlastností prvků
 Periodický zákon, periodická tabulka, periodicita chemických a fyzikálních vlastností prvků Periodický zákon, periodická tabulka, periodicita chemických a fyzikálních vlastností prvků 2 Vlnově mechanický
Periodický zákon, periodická tabulka, periodicita chemických a fyzikálních vlastností prvků Periodický zákon, periodická tabulka, periodicita chemických a fyzikálních vlastností prvků 2 Vlnově mechanický
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 20.04.2013 Číslo DUMu: VY_32_INOVACE_17_Ch_ACH
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 20.04.2013 Číslo DUMu: VY_32_INOVACE_17_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 20.04.2013 Číslo DUMu: VY_32_INOVACE_17_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Analytické metody využívané ke stanovení chemického složení kovů. Ing.Viktorie Weiss, Ph.D.
 Analytické metody využívané ke stanovení chemického složení kovů. Ing.Viktorie Weiss, Ph.D. Rentgenová fluorescenční spektrometrie ergiově disperzní (ED-XRF) elé spektrum je analyzováno najednou polovodičovým
Analytické metody využívané ke stanovení chemického složení kovů. Ing.Viktorie Weiss, Ph.D. Rentgenová fluorescenční spektrometrie ergiově disperzní (ED-XRF) elé spektrum je analyzováno najednou polovodičovým
Základy analýzy potravin Přednáška 1
 ANALÝZA POTRAVIN Význam a využití kontrola jakosti surovin, výrobků jakost výživová jakost technologická jakost hygienická autenticita, identita potravinářských materiálů hodnocení stravy (diety) Analytické
ANALÝZA POTRAVIN Význam a využití kontrola jakosti surovin, výrobků jakost výživová jakost technologická jakost hygienická autenticita, identita potravinářských materiálů hodnocení stravy (diety) Analytické
Alkalické kovy. Gymnázium a Jazyková škola s právem státní jazykové zkoušky Zlín
 Alkalické kovy Temacká oblast : Chemie anorganická chemie Datum vytvoření: 23. 8. 2012 Ročník: 2. ročník čtyřletého gymnázia (sexta osmiletého gymnázia) Stručný obsah: Alkalické kovy vlastnos a výroba
Alkalické kovy Temacká oblast : Chemie anorganická chemie Datum vytvoření: 23. 8. 2012 Ročník: 2. ročník čtyřletého gymnázia (sexta osmiletého gymnázia) Stručný obsah: Alkalické kovy vlastnos a výroba
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/
 Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT-PZC_2_6 Test obecná chemie Střední
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT-PZC_2_6 Test obecná chemie Střední
Přirovnání. Elektrony = obyvatelé panelového domu Kde bydlí paní Kostková? Musíme udat patro a číslo bytu.
 Kvantová čísla Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. Přirovnání Elektrony = obyvatelé
Kvantová čísla Dostupné z Metodického portálu www.rvp.cz, ISSN: 1802-4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze. Přirovnání Elektrony = obyvatelé
Skupenské stavy. Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
 Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
BINÁRNÍ SYSTÉMY HORCÍK PRÍMES A ROZDELOVACÍ KOEFICIENTY PRÍMESÍ V HORCÍKOVÝCH SLITINÁCH. Lumír Kuchar, Jaromír Drápala, Kamil Krybus
 BINÁRNÍ SYSTÉMY HORCÍK PRÍMES A ROZDELOVACÍ KOEFICIENTY PRÍMESÍ V HORCÍKOVÝCH SLITINÁCH Lumír Kuchar, Jaromír Drápala, Kamil Krybus Vysoká škola bánská - Technická Univerzita, katedra neželezných kovu,
BINÁRNÍ SYSTÉMY HORCÍK PRÍMES A ROZDELOVACÍ KOEFICIENTY PRÍMESÍ V HORCÍKOVÝCH SLITINÁCH Lumír Kuchar, Jaromír Drápala, Kamil Krybus Vysoká škola bánská - Technická Univerzita, katedra neželezných kovu,
REDOXNÍ REAKCE. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: 27. 2. 2012. Ročník: devátý
 Autor: Mgr. Stanislava Bubíková REDOXNÍ REAKCE Datum (období) tvorby: 27. 2. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s redoxními reakcemi.
Autor: Mgr. Stanislava Bubíková REDOXNÍ REAKCE Datum (období) tvorby: 27. 2. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemické reakce 1 Anotace: Žáci se seznámí s redoxními reakcemi.
STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ UČILIŠTĚ, Česká Lípa, 28. října 2707, příspěvková organizace. Digitální učební materiály www.skolalipa.
 Název školy Číslo projektu Název projektu Klíčová aktivita Označení materiálu: Typ materiálu: Předmět, ročník, obor: Tematická oblast: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ
Název školy Číslo projektu Název projektu Klíčová aktivita Označení materiálu: Typ materiálu: Předmět, ročník, obor: Tematická oblast: Téma: Jméno a příjmení autora: STŘEDNÍ ODBORNÁ ŠKOLA a STŘEDNÍ ODBORNÉ
Elektrochemie. Koroze kovových materiálů. Kovy. Kovy. Kovy. Kovy, mechanismy koroze, ochrana před korozí 1. Kovy Polokovy Nekovy
 Koroze kovových materiálů Polokovy Nekovy, mechanismy koroze, ochrana před korozí 1 2 Vysoká elektrická a tepelná vodivost Lesklé Kujné a tažné V přírodě se vyskytují převážně ve formě sloučenin, výjimku
Koroze kovových materiálů Polokovy Nekovy, mechanismy koroze, ochrana před korozí 1 2 Vysoká elektrická a tepelná vodivost Lesklé Kujné a tažné V přírodě se vyskytují převážně ve formě sloučenin, výjimku
Koroze kovových materiálů. Kovy, mechanismy koroze, ochrana před korozí
 Koroze kovových materiálů Kovy, mechanismy koroze, ochrana před korozí 1 Kovy Kovy Polokovy Nekovy 2 Kovy Vysoká elektrická a tepelná vodivost Lesklé Kujné a tažné V přírodě se vyskytují převážně ve formě
Koroze kovových materiálů Kovy, mechanismy koroze, ochrana před korozí 1 Kovy Kovy Polokovy Nekovy 2 Kovy Vysoká elektrická a tepelná vodivost Lesklé Kujné a tažné V přírodě se vyskytují převážně ve formě
Kvantová teorie atomů
 Kvantová teorie atomů Kdo otevřel Pandořinu skříňku? l při studiu záření abs. černého tělesa (hvězda) použil Max von Planck (1900, NP 1918) předpoklad, že oscilátor má diskrétní spektrum, s velikostí kvanta
Kvantová teorie atomů Kdo otevřel Pandořinu skříňku? l při studiu záření abs. černého tělesa (hvězda) použil Max von Planck (1900, NP 1918) předpoklad, že oscilátor má diskrétní spektrum, s velikostí kvanta
Anotace Metodický list
 ZÁKLADNÍ ŠKOLA a MATEŘSKÁ ŠKOLA STRUPČICE, okres Chomutov Autor výukového Materiálu Datum (období) vytvoření materiálu Ročník, pro který je materiál určen Vzdělávací obor tématický okruh Název materiálu,
ZÁKLADNÍ ŠKOLA a MATEŘSKÁ ŠKOLA STRUPČICE, okres Chomutov Autor výukového Materiálu Datum (období) vytvoření materiálu Ročník, pro který je materiál určen Vzdělávací obor tématický okruh Název materiálu,
ATOM VÝVOJ PŘEDSTAV O SLOŽENÍ A STRUKTUŘE ATOMU
 Předmět: Ročník: Vytvořil: Datum: CHEMIE PRVNÍ Mgr. Tomáš MAŇÁK 20. říjen 202 Název zpracovaného celku: ATOM VÝVOJ PŘEDSTAV O SLOŽENÍ A STRUKTUŘE ATOMU Leukippos, Démokritos (5. st. př. n. l.; Řecko).
Předmět: Ročník: Vytvořil: Datum: CHEMIE PRVNÍ Mgr. Tomáš MAŇÁK 20. říjen 202 Název zpracovaného celku: ATOM VÝVOJ PŘEDSTAV O SLOŽENÍ A STRUKTUŘE ATOMU Leukippos, Démokritos (5. st. př. n. l.; Řecko).
JADERNÁ CHEMIE včera, dnes a zítra
 JADERNÁ CHEMIE včera, dnes a zítra J. John (john@fjfi.cvut.cz) U3V 11.4.2013 1 Obsah Část 1 Pravěk Objev radioaktivity Starověk Objevy radioaktivních prvků v přírodě Výroba radia v Jáchymově Vsuvka: Pojmy
JADERNÁ CHEMIE včera, dnes a zítra J. John (john@fjfi.cvut.cz) U3V 11.4.2013 1 Obsah Část 1 Pravěk Objev radioaktivity Starověk Objevy radioaktivních prvků v přírodě Výroba radia v Jáchymově Vsuvka: Pojmy
Průvodka. CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Pořadí DUMu v sadě 07
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Gymnázium, Brno, Elgartova 3
 Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Základy názvosloví Autor: Název: Mgr. Petra Holzbecherová Procvičování
Gymnázium, Brno, Elgartova 3 GE - Vyšší kvalita výuky CZ.1.07/1.5.00/34.0925 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Téma: Základy názvosloví Autor: Název: Mgr. Petra Holzbecherová Procvičování
Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9.
 Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9. Školní rok 0/03, 03/04 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup) Počet hodin pro kapitolu Úvod
Učební osnovy Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemický kroužek ročník 6.-9. Školní rok 0/03, 03/04 Kapitola Téma (Učivo) Znalosti a dovednosti (výstup) Počet hodin pro kapitolu Úvod
 ď ř ř ř é ř ř ů ř ř é ř řú é ň é ř ň ř ů ň řú ů é ň ř ů ň ř ů é ň ř ú ň ř ů ň ř ů ž ž ň ř é ž ů é ň ů ž ř é ř ů ř š é ů ř é ř ů é ň ř ň é ř ž ů ů ř ž é ž ž ž ž ř é ř ř ů ř ř ů ř ú ů Ú ů ů ř é ř é ř ř é
ď ř ř ř é ř ř ů ř ř é ř řú é ň é ř ň ř ů ň řú ů é ň ř ů ň ř ů é ň ř ú ň ř ů ň ř ů ž ž ň ř é ž ů é ň ů ž ř é ř ů ř š é ů ř é ř ů é ň ř ň é ř ž ů ů ř ž é ž ž ž ž ř é ř ř ů ř ř ů ř ú ů Ú ů ů ř é ř é ř ř é
Atomové jádro, elektronový obal
 Atomové jádro, elektronový obal 1 / 9 Atomové jádro Atomové jádro je tvořeno protony a neutrony Prvek je látka skládající se z atomů se stejným počtem protonů Nuklid je systém tvořený prvky se stejným
Atomové jádro, elektronový obal 1 / 9 Atomové jádro Atomové jádro je tvořeno protony a neutrony Prvek je látka skládající se z atomů se stejným počtem protonů Nuklid je systém tvořený prvky se stejným
(a) (a) de hydratovan ze olitu (b) silikage l. Aktivní uhlí. (c)
 Hydrotermální syntéza Molekulová síta Molekulově sítový effekt - rozdělení molekul dle jejich velikosti ve vztahu k velikosti porů - distribuce velikosti porů Rozdělení IUPAC Zeolity Mikroporézní látky
Hydrotermální syntéza Molekulová síta Molekulově sítový effekt - rozdělení molekul dle jejich velikosti ve vztahu k velikosti porů - distribuce velikosti porů Rozdělení IUPAC Zeolity Mikroporézní látky
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: Číslo DUMu: VY_32_INOVACE_20_Ch_ACH
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 26.04.2013 Číslo DUMu: VY_32_INOVACE_20_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 26.04.2013 Číslo DUMu: VY_32_INOVACE_20_Ch_ACH Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Anorganická
Stavba atomu. Created with novapdf Printer (www.novapdf.com). Please register to remove this message.
 Stavba atomu Atom je v chemii základní stavební částice, jeho průměr je přibližně 10-10 m. Je složen z jádra a obalu. Atomové jádro obsahuje protony p + (kladný náboj) a neutrony n 0 (neutrální částice).
Stavba atomu Atom je v chemii základní stavební částice, jeho průměr je přibližně 10-10 m. Je složen z jádra a obalu. Atomové jádro obsahuje protony p + (kladný náboj) a neutrony n 0 (neutrální částice).
Kateřina Fišerová - Seminární práce k předmětu Didaktika fyziky
 Kateřina Fišerová - Seminární práce k předmětu Didaktika fyziky Problémová situace První jaderný reaktor spustil 2. prosince 942 na univerzitě v Chicagu italský fyzik Enrico Fermi se svými spolupracovníky.
Kateřina Fišerová - Seminární práce k předmětu Didaktika fyziky Problémová situace První jaderný reaktor spustil 2. prosince 942 na univerzitě v Chicagu italský fyzik Enrico Fermi se svými spolupracovníky.
Přechodné prvky, jejich vlastnosti a sloučeniny
 Přechodné prvky, jejich vlastnosti a sloučeniny - jsou to d-prvky, nazývají se také přechodné prvky - v PSP jsou umístěny mezi s a p prvky - nacházejí se ve 4. 7. periodě - atomy přechodných prvků mají
Přechodné prvky, jejich vlastnosti a sloučeniny - jsou to d-prvky, nazývají se také přechodné prvky - v PSP jsou umístěny mezi s a p prvky - nacházejí se ve 4. 7. periodě - atomy přechodných prvků mají
