FARMACEUTICKÁ FAKULTA V HRADCI KRÁLOVÉ
|
|
|
- Vratislav Kříž
- před 6 lety
- Počet zobrazení:
Transkript
1 FARMACEUTICKÁ FAKULTA V HRADCI KRÁLOVÉ KATEDRA ANORGANICKÉ A ORGANICKÉ CHEMIE DIPLOMOVÁ PRÁCE VYUŽITÍ NMR PŘI STRUKTURNÍ ANALÝZE PŘÍRODNÍCH LÁTEK Hradec Králové, 2010 Hana Dohnalová
2 Prohlašuji, že tato práce je mým původním autorským dílem, které jsem vypracovala samostatně. Veškerá literatura a další zdroje, z nichž jsem při zpracování čerpala, jsou uvedeny v seznamu použité literatury a v práci řádně citovány. 2
3 Za všestrannou a obětavou pomoc, cenné rady a připomínky při vypracovávání diplomové práce děkuji doc.pharmdr. Jiřímu Kunešovi, CSc. a Ing.Lucii Cahlíkové, Ph.D. 3
4 OBSAH 1. Abstrakt 5 2. Úvod Eschscholtzia californica Obsahové látky E.californica Využití E.californica Cíl práce Výsledky s komentářem Použité experimentální postupy LC LC LC Závěr Literatura Přílohy NMR spektra sloučeniny LC NMR spektra sloučeniny LC NMR spektra sloučeniny LC
5 Abstrakt 1. Abstrakt Diplomová práce je věnována určení struktury neznámých látek. Na Katedře farmaceutické botaniky a ekologie Farmaceutické fakulty v Hradci Králové byla z rostliny Eschscholtzia californica z čeledi Papaveraceae izolována celá řada alkaloidů. Některé z nich byly předány do Laboratoře struktury a interakcí biologicky aktivních molekul s žádostí o určení jejich struktury. Cílem diplomové práce byla identifikace tří neznámých vzorků pomocí NMR analýzy. U neznámých sloučenin byla na základě provedených NMR experimentů ( 1 H-NMR, 13 C-NMR, DEPT, ghmqc, ghsqc, ghmqfcops a dpfgnoe) určena jejich struktura. Ta byla potvrzena na základě srovnání s údaji uvedenými v literatuře. Identifikované sloučeniny patří mezi isochinolinové alkaloidy. Jedná se o skulerin a retikulin, třetí sloučenina nebyla v literatuře pojmenována. 5
6 Abstrakt Abstract This Diploma work is dedicated to the determination of the structure of unknown substances. A large number of alkaloids was isolated from an Eschscholtzia Californica plant (Papaveraceae) at the Department of Pharmaceutical Botanic and Ecology of the Pharmaceutical Faculty in Hradec Králové. Some of them were passed to the Laboratory of the structure and interaction of the biological aktive molecules along with the request for the structure analysis.the main object of this Diploma work was the identification of three of unknown subjects by the help of NMR analysis. The structures of unknown substances were identified on the basis of the NMR experiments ( 1 H-NMR, 13 C-NMR, DEPT, ghmqc, ghsqc, ghmqfcops a dpfgnoe). These structures were confirmed based on the comparison with the data provided in the subject publications. Now identified substances belong to isochinoline alkaloids. Namely, it is scoulerine and retikuline. The third substance was not specified in the subject publication. 6
7 Úvod 2. ÚVOD 2.1. Eschscholtzia californica Eschscholtzia californica sluncovka kalifornská z čeledi Papaveraceae je tradiční léčivá rostlina indiánů užívaná pro své sedativní a analgetické účinky 1. Divoce roste po celé Kalifornii (obvykle pod hranicí metrů), v některých částech Oregonu a ve Washingtonu 2. V 19. století byla dovezena do Evropy jako dekorativní zahradní rostlina 3. Eschscholtzia patří do čeledi Papaveraceae a pojmenoval ji Albert von Chamisso podle svého přítele, profesora Johanna Friedricha Eschscholtze, německého fyzika a přírodovědce, který se účastnil ruské expedice do Kalifornie 4. Eschscholtzia californica je jednoletá bylina, má cm vysokou, řídce větvenou lodyhu s jemně zpeřenými šedozelenými listy. Kvete žlutě až oranžově. Květy velikosti 5-6 cm vyrůstají jednotlivě, mají nálevkovitý nebo miskovitý tvar. Dva kališní lístky jsou kápovitě srostlé a při rozkvětu odpadávají. Korunní lístky jsou čtyři. Kvete od května do září, květ se však rozevře pouze za svitu slunce 4,5,6. 7
8 Úvod 2.2. Obsahové látky E.californica Obsahové látky Eschscholtzia californica jsou poměrně dobře známy. Bylina obsahuje asi % alkaloidů. Byla izolována komplexní směs asi třiceti terciálních a kvarterních isochinolinových alkaloidů, náležících do 6 strukturních typů 3. Hlavním alkaloidem Eschscholtzia californica je kvartení báze californidin (N-methylescholzinium hydroxid) 7, který se v rostlině vyskytuje v množství % 6. Obsah terciálních alkaloidů v rostlině je %. Hlavními složkami terciálních nefenolických bází jsou escholtzin, allocryptopin a protopin (každý asi %) 7. Escholtzin je typickou složkou nadzemní části rostliny, v kořenech obsažen není. Hlavním zástupcem fenolických terciálních bazí je aporfin, N- metyllaurotetanin (lauroscholzin), který se však v rostlině vyskytuje v nepatrných množstvích, stejně jako další aporfiny korydin, isokorydin a pavinany karyachin, isokaryachin, isonorargemonin, norargemonin a bisnorargemonin. Z kvarterních isochinolinových alkaloidů jsou v rostlině ve stopách obsaženy protoberberinové alkaloidy berberin, koptsin a korysamin, benzylisochinoliny escholamidin a escholamin, aporfin magnoflorin a ve velmi nepatrném množství se vyskytují benzofenantridiny sanqinarin a chelerytrin, doprovázené chelirubinem, makarpinem a chelilutinem 6,7. 8
9 Úvod H 2 C O O O N OR 1 H 3 CO HO HO N + CH 3 CH 3 OR 2 H 3 CO protopin R 1 +R 2 =CH 2 allokryptopin R 1 =R 2 =CH 3 magnof lorin H 2 C O O N + H 2 C O O N + O CH 3 OR 1 O CH 3 OR 2 berberin escholamin R 1 +R 2 =CH 2 escholamidin R 1 =CH 3,R 2 =H Kromě alkaloidů obsahuje Eschscholtzia californica také flavonoidy, které se vyskytují hlavně jako glykosidy kvercetinu a isorhamnetinu 2. Jsou to například flavonolové glykosidy rutin a kvercetin a isoflavony 2 -metoxyformononetin a 7-metoxy-2,4 - dihydroxyisoflavony 1. 9
10 Úvod 2.3. Využití E.californica V lidové medicíně se nadzemní část rostliny využívá pro analgetické, diaforetické, diuretické, sedativní a spasmolytické účinky. Různé farmakologické studie potvrdily sedativní a anxiolytickou aktivitu a nepřítomnost nežádoucích účinků extraktu z rostliny 3. Mechanismus sedativní a anxiolytické aktivity zatím není objasněn. Uvažuje se o zapojení benzodizepinových receptorů. Navíc by aktivita mohla být spojena s inhibicí rozkladu katecholaminů inhibicí enzymů dopamin-β-hydroxylázy a monoaminooxidázy 2. Obecně se soudí, že na aktivitě extraktu z Eschscholtzia californica se podílí isochinolinové alkaloidy, zatím to však nebylo potvrzeno žádnou studií s izolovanými sloučeninami 3. V Americe a v Evropě se rostlina používá jako mírné sedativum. V Americe jsou přípravky z drogy předepisovány při poruchách spánku, především v pediatrii a ve Francii při léčbě nervozity. Výjimečně je Eschscholtzia využívána jako náhradní droga za marihuanu. Po požití nebo vykouření navozuje mírnou euforii trvající minut. Pravidelné a dlouhodobé užívání nevyvolává návyk 6. 10
11 Cíl práce 3. CÍL PRÁCE Cílem mé práce byla identifikace 3 neznámých látek s kódovým označením LC-004, LC-006 a LC10-4, které byly, ing. Lucií Cahlíkovou z Katedry farmaceutické botaniky a ekologie, izolovány z rostliny Eschscholtzia californica z čeledi Papaveraceae. 11
12 Výsledky s komentářem 4. VÝSLEDKY S KOMENTÁŘEM 4.1. Použité experimentální postupy Nadzemní část a kořen rostliny Eschscholtzia californica byly získány od prodejce rostlin Planta Naturalis (Markvartice u Sobotky). Doklad vzorku je uložen v herbáři Farmaceutické fakulty v Hradci Králové. Extrakt alkaloidů byl připraven perkolací suché rostliny s kořeny (36.54 kg) pomocí 95% etanolu (328 l). Extrakt alkaloidů byl zahuštěn za sníženého tlaku na 4 litry a následně 3x digerován při 50 C několika litry 1% H 2 SO 4 ; vodná vrstva byla vždy slita. Byl získán hnědý roztok o ph 2. Tento spojený hnědý digerát byl zfiltrován nejprve přes viskózový filtr, posléze přes vrstvu křemeliny. Jeho celkový objem byl 17.2 litrů. Další zpracování primárního extraktu a izolace alkaloidů bylo provedeno na Katedře farmaceutické botaniky a ekologie v rámci diplomových a rigorózních prací (J. Doležal) 8. Některé alkaloidy byly předány do Laboratoře struktury a interakcí biologicky aktivních molekul s žádostí o určení jejich struktury. Měření hmotnostních spekter všech látek bylo provedeno na hmotnostním spektrometru Thermo Finningan LCQ Duo (ionizace elektrosprejem, analyzátor iontová past). NMR spektra ( 1 H, 13 C, DEPT, ghmqc, ghsqc, ghmqfcops a dpfgnoe) všech látek byla měřena v roztocích CDCl 3 nebo CD 3 OD při laboratorní teplotě na přístroji VARIAN Mercury Vx BB 300 MHz pracujícím při 300 MHz pro 1 H a při 75 MHz pro 13 C. Chemické posuny byly změřeny jako hodnoty δ v pars per milion (ppm) a byly nepřímo vztaženy k tetramethylsilanu (TMS) jako standardu pomocí zbytkového signálu rozpouštědla (7.26 pro 1 H a 77.0 pro 13 C pro CDCl 3 resp pro 1 H a 49.0 pro 13 C pro CD 3 OD). Data jsou prezentována v následujícím pořadí: chemický posun (δ), integrovaná intenzita (v protonovaných spektrech), multiplicita (s: singlet, d: dublet, t: triplet, q: kvartet, qd: kvartet dubletů, bs: široký singlet, dd: dublet dubletů, m: multiplet), interakční konstanta (Hz) a přiřazení (v některých produktech). 12
13 Výsledky s komentářem 4.2. LC-004 Neznámá sloučenina s kódovým označením LC-004 byla získána izolací z rostliny Eschscholtzia californica z čeledi Papaveraceae. V klasickém 1 H spektru jsem si podle integrálu určila, kolik atomů vodíku odpovídá jednotlivým signálům. Podle chemického posunu je zřejmé, že neznámá sloučenina obsahuje 4 atomy vodíku navázané na aromatickém jádře. Podle štěpení se jedná o dublet δ=6.84 ppm, singlet δ=6.76 ppm a v oblasti δ= ppm dublet a singlet. Singlety odpovídají dvěma atomům vodíku ležící na aromatickém jádře v poloze para (aromatické jádro je substituováno v polohách 1, 2, 4 a 5), viz obr.1, nebo izolovaným atomům vodíku vázaným na dvou různých aromatických jádrech. Dublety s interakční konstantou J=8.5 Hz náleží dvěma sousedním aromatickým atomům vodíku (viz obr.2). Neznámá sloučenina obsahuje minimálně 2 aromatická jádra. Signál s chemickým posunem δ=4.36 ppm náleží jednomu atomu vodíku a je štepen na dublet. Chemický posun δ=4.36 ppm napovídá, že se tento atom vodíku nachází v blízkosti elektronegativního atomu, nebo skupiny atomů, které způsobí jeho odstínění. Signál s chemickým posunem δ= ppm odpovídá podle integrálu osmi atomům vodíku a je složen z několika signálů, které se vzájemně překrývají. Této skupině dominují výrazné singlety při chemickém posunu δ=3.82 ppm, typické pro methoxy skupiny navázané na aromatickém jádře. Dalším výrazným signálem je dublet při chemickém posunu δ=3.71 ppm. Podle integrálu odpovídá signál s chemickým posunem δ= ppm osmi atomům vodíku. Musí tedy náležet kromě dvěma methoxy skupinám a jednomu atomu vodíku s chemickým posunem δ=3.71 ppm ještě jednomu atomu vodíku. Signály s chemickým posunem δ= ppm náleží dalším šesti alifatickým atomům vodíku. V klasickém 13 C spektru je patrné, že se v neznámé sloučenině nachází 12 aromatických atomů uhlíku. Sloučenina tedy pravděpodobně obsahuje 2 aromatická jádra, což odpovídá rozvržení atomů vodíku vázaných na aromatických jádrech podle obr.1 a obr.2. 13
14 Výsledky s komentářem Chemický posun atomů uhlíku 143.7, 146.6, a ppm je typický pro atomy uhlíku aromatického jádra, na které je vázán atom kyslíku. Neznámá sloučenina tedy obsahuje 4 atomy kyslíku. V oblasti chemického posunu ppm leží celkem 7 alifatickým atomů uhlíku. Z MS spektra vyplývá, že neznámá sloučenina má molekulovou hmotnost 327. V 13 C- NMR spektru je patrné, že sloučenina obsahuje 19 atomů uhlíku a 4 atomy kyslíku viz úvaha výše. Z 1 H spektra jsem určila, že neznámá sloučenina obsahuje pouze 2 methoxy skupiny, na další 2 atomy kyslíku tedy musí být navázány atomy vodíku. Zatím jsem tedy určila, že sloučenina obsahuje 19 atomů uhlíku, 21 atomů vodíku a 4 atomy kyslíku. Součtem jejich molárních hmotností jsem získala číslo 313 a do celkové molekulové hmotnosti mi chybí 14, což je přesně molární hmotnost atomu dusíku. Neznámá sloučenina tedy ve své molekule obsahuje ještě atom dusíku. Sumární vzorec neznámé sloučeniny bude C 19 H 21 NO 4. Pomocí experimentu DEPT jsem určila počet methylových, methylenových a methinových skupin. Atomy uhlíku při chemickém posunu δ=119.8, 125.1, 127.1, 128.7, 143.7, 146.6, a ppm odpovídají kvarterním uhlíkovým atomům. Methinové jsou atomy uhlíku při chemickém posunu δ=120.1, 113.1, 112.5, a 60.8 ppm, methylenovým skupinám odpovídají atomy uhlíku při chemickém posunu δ=54.1, 52.6, 35.6 a 28.3 ppm. Metylovou skupinu tvoří atomy uhlíku s chemickým posunem δ=56.5 a 56.3 ppm. Experiment ghsqc mi umožnil určit konkrétní atomy vodíku, které jsou navázané na jednotlivé atomy uhlíku. C (120.1)..H(6.70) C(113.1)..H(6.76) C(112.5)..H(6.69) C(111.7)..H(6.84) C(60.8)....H( ) C(56.5).H(3.82) C(56.3)...H(3.82) C(54.1)...H(3.71, 4.36) C(52.6)...H( , ) C(35.6)...H( , ) C(28.3)...H( ; ) Neznámá sloučenina obsahuje 2 aromatická jádra a tedy 6 atomů uhlíku na každé jádro. Na každé aromatické jádro jsou navázány dva atomy vodíku. Pomocí experimentu ghsqc jsem již určila, na které atomy uhlíku jsou tyto atomy vodíku navázány. Z toho vyplývá, že je třeba ještě určit umístění zbývajících čtyř kvarterních atomů uhlíku na každém aromatickém jádře. Podle experimentu ghmqc je patrné, že atom vodíku δ=6.70 ppm má korelaci na atomy uhlíku a Tyto atomy uhlíku musí ležet ve vzdálenosti tří vazeb od atomu vodíku δ=6.70 ppm, musí tedy ležet v polohách 2 a 4 aromatického jádra, tedy blíže k atomu vodíku δ=6.76 ppm. Atom vodíku δ=6.76 ppm má korelaci na atomy uhlíku a 14
15 Výsledky s komentářem Obdobnou úvahou jako v předchozím případě jsem určila, že tyto atomy uhlíku musí ležet v polohách 1 a 5 aromatického jádra (viz obr.3). Atom vodíku δ=6.84 ppm má korelaci na atomy uhlíku δ=143.7, a Výrazné korelace na atomy uhlíku a napovídají, že se jedná o korelace přes tři vazby a tyto atomy uhlíku se budou nacházet v polohách 2 a 4 aromatického jádra, tedy ve vzdálenosti tří vazeb od atomu vodíku δ=6.84 ppm. Korelace atomu vodíku δ=6.84 ppm na atom uhlíku je výrazně menší, jedná se tedy o korelaci přes dvě vazby a tento atom uhlíku se bude nacházet v poloze 1 aromatického jádra. Atom vodíku δ=6.69 ppm má korelaci na atom uhlíku Tento atom uhlíku se tedy bude nacházet v poloze 3 aromatického jádra (viz obr.4) H H 6.69 H 6.76 obr.3 Dalším mým krokem bylo určení napojení alifatických atomů uhlíku na aromatická jádra. Atom vodíku δ=6.70 ppm má korelaci na atom uhlíku Tento atom uhlíku musí být vůči atomu vodíku δ=6.70 ppm ve vzdálenosti tří vazeb, musí tedy být na aromatické jádro vázán v poloze 1 nebo 5. V této poloze leží buď atom uhlíku 125.1, nebo atom uhlíku Atom uhlíku 28.3 musí být vázán na atom uhlíku 125.1, protože na atom uhlíku je navázán atom kyslíku. Atom vodíku δ=6.76 ppm má korelaci na atom uhlíku Tento atom uhlíku musí být na aromatické jádro vázán v poloze 2, nebo 4, tedy v polohách, ve kterých leží atomy uhlíku a Na atom je vázán atom kyslíku, atom uhlíku 60.8 musí být tedy na aromatické jádro navázán přes atom uhlíku Podle chemického posunu atomu uhlíku 60.8 jsem usoudila, že tento atom uhlíku nemůže být vázán na další atom uhlíku, ale musí se nacházet v sousedství elektronegativního atomu. Z chemického posunu vyplývá, že atom uhlíku 60.8 musí ležet v sousedství atomu dusíku, který způsobí jeho odstínění (viz obr.5). Korelace atomu vodíku δ= ppm (navázán na atomu uhlíku 28.3) na atom uhlíku mi umožnila určit, že atomy uhlíku a leží na aromatickém jádře vedle sebe a atomy uhlíku 60.8 a 28.3, které toto aromatické jádro substituují, leží na stejné straně vůči atomům vodíku δ=6.70 ppm a δ=6.76 ppm (viz obr.5). Atom vodíku δ=6.69 ppm druhého aromatického jádra má v experimentu ghmqc korelaci na alifatický atom uhlíku Aby byla dodržená vzdálenost tří vazeb, musí být tento alifatický atom uhlíku vázán na aromatické jádro přes atom uhlíku vedle atomu uhlíku 15 H 6.84 obr.4
16 Výsledky s komentářem 112.5, který nese navázaný atom vodíku δ =6.69 ppm. Vedle atomu uhlíku je navázán atom uhlíku 111.7, který nese navázaný atom vodíku δ=6.84 ppm. Z druhé strany vůči atomu uhlíku je navázán buď atom uhlíku 127.1, nebo atom uhlíku Na atom uhlíku je navázán atom kyslíku. Alifatický atom uhlíku 35.6 tedy musí být na aromatické jádro vázán přes atom uhlíku 127.1, který se musí nacházet v poloze 4 aromatického jádra, tedy vedle atomu uhlíku (viz obr.6). O O H H R H R 1 N 60.8 R 2 R 3 H H obr H H R 1 R O H O H 6.84 obr.6 Z chemického posunu atomu uhlíku 28.3 je patrné, že tento atom uhlíku nemůže být vázán na elektronegativní atom, který by způsobil jeho odstínění. Na atom uhlíku 28.3 musí tedy být vázán další atom uhlíku. Atom vodíku δ= ppm (leží na atomu uhlíku 28.3) má korelaci na atom uhlíku Tato korelace je velmi slabá, jedná se tedy pravděpodobně o korelaci přes dvě vazby. Atom uhlíku 52.6 bude ležet v těsném sousedství atomu uhlíku Slabou korelaci přes dvě vazby na atom uhlíku 28.3 má i atom vodíku δ= ppm, který je navázán na atomu uhlíku Z chemického posunu atomu uhlíku 52.6 je patrné, že musí být vázán na elektronegativní atom, který způsobí jeho odstínění. Tento atom uhlíku tedy musí ležet v sousedství atomu dusíku, a tím dojde k uzavření cyklu s alifatickým uhlíkem Přítomnost tohoto cyklu ve struktuře neznámé sloučeniny potvrzuje korelace atomu vodíku δ= ppm (navázaný na atomu uhlíku 28.3) na atom uhlíku 60.8 a korelace atomu vodíku δ= ppm (navázaný na atom uhlíku 52.6) na tentýž atom uhlíku 60.8 (viz obr.7). 16
17 Výsledky s komentářem Atom uhlíku 60.8 má korelaci na atom vodíku δ=4.36 ppm, který je navázán na atom uhlíku Z důvodu této korelace a z výrazného chemického posunu atomu uhlíku 54.1 jsem určila, že atom uhlíku 54.1 bude třetím atomem uhlíku navázaným na atom dusíku. Tento předpoklad jsem si potvrdila také korelací atomu vodíku δ=3.71 ppm (je navázán na atomu uhlíku 54.1) na atom uhlíku 52.6 (viz obr.8). Atom vodíku δ= ppm, který je navázán na atom uhlíku 35.6, má slabou korelaci (přes dvě vazby) na atom uhlíku Atom uhlíku 35.6 bude tedy ležet v těsném sousedství atomu uhlíku Z výše uvedeného rozboru vyplynulo, že atom uhlíku 35.6 je vázán na druhé aromatické jádro (korelace atomu vodíku δ= ppm na aromatický atom uhlíku 119.8). Vazbou atomu uhlíku 60.8 na atom uhlíku 35.6 jsem tedy spojila obě aromatická jádra do jednoho skeletu (viz obr.9). Na druhé aromatické jádro bude napojen i atom uhlíku Toto tvrzení dokazuje korelace atomu vodíku δ=4.36 ppm i δ=3.71 ppm (oba jsou navázány na atom uhlíku 54.1) na atom uhlíku a korelace atomu vodíku δ=4.36 ppm na atom uhlíku i na atom uhlíku Atom uhlíku 54.1 bude na druhé aromatické jádro vázán v poloze 3, tedy přes atom uhlíku (viz obr.9). 17
18 Výsledky s komentářem Ještě mi zbývalo rozhodnout, na kterém atomu kyslíku je navázaná methylová skupina a který atom kyslíku nese atom vodíku a tvoří fenolickou skupinu. Podle experimentu ghmqc má jedna metylová skupina s chemickým posunem δ=3.82 ppm korelaci na atom uhlíku a druhá na uhlík Methoxy skupiny budou navázané na atomy uhlíku a (viz obr.10). Tím jsem určila strukturu celé sloučeniny se sumárním vzorcem: C 19 H 21 NO 4. 1 H NMR: (300 MHz, CD 3 OD) δ 6.84 (1H, d, J=8.5 Hz, H10); 6.76 (1H, s, H1); 6.70 (1H, s, H4); 6.69 (1H, d, J=8.5 Hz, H11); 4.36 (1H, d, J=15.7 Hz, H7); (1H, m, NCH); 3.82 (3H, s, OCH 3 ); 3.82 (3H, s, OCH 3 ); 3.71 (1H, d, J=15.7 Hz, H7); (2H, m, H6, H12); (1H, m, H5); (3H, m, H5, H6, H12). 13 C NMR: (75 MHz, CD 3 OD) δ 148.4, 146.8, 146.6, 143.7, 128.7, 127.1, 125.1, 120.1, 119.8, 113.1, 112.5, 111.7, 60.8, 56.5, 56.3, 54.1, 52.6, 35.6, ESI-MS m/z 328 [M+H] + 18
19 19 Výsledky s komentářem
20 Výsledky s komentářem 4.3. LC-006 Neznámá sloučenina s kódovým označením LC10-4 byla získána izolací z rostliny Eschscholtzia californica z čeledi Papaveraceae. V klasickém 1 H-NMR spektru jsem si podle poměru integrálů určila, kolik atomů vodíku připadá jednotlivým signálům. V aromatické oblasti bylo zřetelně pozorováno 5 signálů při chemickém posunu δ=6.40 ppm, δ=6.53 ppm, δ=6.59 ppm, δ=6.73 ppm, δ=6.77 ppm, které náleží pěti atomům vodíku navázaným na aromatickém jádře. Signály s chemickým posunem δ=6.40 ppm a δ= 6.53 ppm nejsou štěpené, což je v aromatickém systému typické pro atomy vodíku navázané na jednom aromatickém jádře substituovaném v polohách 1, 2, 4 a 5 (viz obr.1), nebo pro izolované atomy vodíku na dvou různých aromatických jadrech. Signály s chemickým posunem δ=6.59 ppm, δ=6.73 ppm a δ=6.77 ppm jsou štěpené na dublet dubletů (interakční konstanta J=1.9 Hz, J=8.2 Hz), dublet s interakční konstantou J=8.2 Hz (δ=6.73 ppm) a dublet s interakční konstantou J=1.9 Hz (δ=6.77 ppm), což je štěpení typické pro atomy vodíku na aromatickém jádře substituovaném v polohách 1,2 a 4 (viz obr.2). H 6.53 H H H 6.40 H 6.73 obr.1 obr.2 Singlety s chemickými posuny δ=3.85 ppm a δ=3.84 ppm odpovídají podle integrálu šesti atomům vodíku. Chemický posun δ=3.85 ppm a δ=3.84 ppm je typický pro methoxy skupinu na aromatickém jádře. Neznámá chemická látka tedy ve své struktuře obsahuje dvě methoxy skupiny na aromatickém jádře. Dále jsem určila, že singletu s chemickým posunem δ=2.45 ppm odpovídají 3 atomy vodíku. Z chemického posunu, který je větší než chemický posun odpovídající methylové skupině vázané na kvarterní atom uhlíku, jsem určila, že se jedná o methylovou skupinu navázanou na heteroatom, který způsobí odstínění. Z 1 H-NMR spektra je patrné, že signál s chemickým posunem δ=3.66 ppm, odpovídající jednomu atomu vodíku, je štěpen na triplet. Musí být tedy v sousedství CH 2 skupiny. Chemický posun také napovídá, že v sousedství CH skupiny bude elektronegativní atom způsobující odstínění. Ve spektru je také vidět široký singlet s chemickým posunem δ=5.63 ppm, který náleží atomu nebo atomům vodíku na heteroatomu. 20
21 Výsledky s komentářem Signály s chemickým posunem δ= ppm náleží dalším 9 alifatickým atomům vodíku. V 13 C-NMR spektru se nachází 19 signálů, které náleží atomům uhlíku neznámé chemické sloučeniny, 12 z nich leží v aromatické oblasti. Neznámá sloučenina obsahuje 2 aromatická jádra a atomy vodíku s chemickým posunem δ=6.40 ppm a δ=6.53 ppm musí tedy ležet na jednom aromatickém jádře. 4 signály se nachází v oblasti okolo 145 ppm, což je chemický posun typický pro atomy uhlíku aromatického jádra, na které je navázaný atom kyslíku. Pomocí ghsqc experimentu jsem určila, příslušnost atomů vodíku k jednotlivým atomům uhlíku: C (120.8)..H(6.59) C(115.5)..H(6.77) C(113.6)..H(6.40) C(110.5)..H(6.53) C(110.4)..H(6.73) C(64.5)....H(3.66) C(55.9)...H(3.85) C(55.8)...H(3.84) C(46.8)...H( ; ) C(42.5)...H(2.45) C(41.0)...H( ; 3.01) C(25.1)...H( ; ) Správnost přiřazení atomů vodíku k jednotlivým atomům uhlíku jsem si zkontrolovala pomocí experimentu DEPT. Z tohoto experimentu jsem určila, že atomy uhlíku s chemickým posunem 145.2, 145.0, 144.9, 143.3, a jsou kvarterní, což odpovídá tomu, že v experimentu ghsqc jim nebyl přiřazen žádný atom vodíku. Methinové jsou atomy uhlíku 120.8, 115.5, 113.6, 110.5, a Methylenovým skupinám náleží atomy uhlíku při chemických posunech 46.8, 41.0 a Atomy uhlíku 55.9, 55.8 a 42.5 jsou methylové. Rozmístění atomů vodíku na aromatickém jádře jsem si zkontrolovala pomocí experimentu gmqfcops. Atomy vodíku s chemickým posunem δ=6.59 ppm a δ=6.73 ppm mají v tomto experimentu vzájemnou korelaci, což je v souladu s mým předpokladem, že leží na aromatickém jádře vedle sebe. Ostatní aromatické atomy vodíku v gmqfcops žádnou korelaci nemají, leží tedy izolovaně. V alifatické části je výrazná korelace atomu vodíku δ=3.66 ppm (na atomu uhlíku 64.5) a atomů vodíku δ=3.01 ppm a δ= ppm (oba na atomu uhlíku 41.0). Tyto atomy vodíku musí být v neznámé sloučenině umístěny vedle sebe (viz obr.3). Umístění CH 2 skupiny vedle atomu uhlíku, na kterém je navázaný atom vodíku δ=3.66 ppm odpovídá štěpení signálu atomu vodíku δ=3.66 ppm na triplet. 21
22 Výsledky s komentářem Pomocí ghmqc experimentu jsem určila, které kvarterní atomy uhlíku leží na jednotlivých aromatických jádrech. Atom vodíku s chemickým posunem δ=6.40 ppm má z kvarteních atomů uhlíku korelaci na atomy uhlíku 125.4, a Korelace na uhlík je výrazně menší, jedná se pravděpodobně o méně výraznou korelaci přes dvě vazby. Tento atom uhlíku je tedy pravděpodobně umístěn v poloze 2 nebo 4 na aromatickém jádře podle číslování na obr.1. Korelace na atomy uhlíku a jsou korelace přes 3 vazby, tyto uhlíky se tedy nachází v polohách 1 nebo 5 na aromatickém jádře (viz obr.4). Atom vodíku δ=6.53 ppm má korelace na atomy uhlíku 130.5, a Korelace na atom uhlíku je slabší, jedná se tedy o korelaci přes dvě vazby, což neodporuje umístění uhlíku v poloze 1 nebo 5 na aromatickém jádře podle jeho korelace na atom vodíku δ=6.40 ppm. Korelace atomu vodíku δ=6.53 ppm přes tři vazby na atomy uhlíku a je důvodem jejich umístění v polohách 2 a 4 na aromatickém jádře (viz obr.4). Atomy uhlíku, které nesou navázané atomy vodíku, jsem už určila pomocí experimentu ghsqc. Atom vodíku δ=6.77 ppm má korelace na atomy uhlíku a Atom uhlíku na sobě nese navázaný atom vodíku δ=6.59 ppm a již jsem ho umístila do polohy 5 na druhém aromatickém jádře, podle štěpení signálu jeho atomu vodíku (viz obr.2). Další poloha, která je ve vzdálenosti tří vazeb od atomu vodíku δ=6.77 ppm, je poloha 1. Zde je tedy umístěn atom uhlíku Tomu odpovídá i jeho korelace přes tři vazby na atom vodíku δ=6.59 ppm. Atom vodíku δ=6.73 ppm má korelace na atomy uhlíku a Tyto atomy uhlíku jsou tedy umístěny v polohách 2 nebo 4 na druhém aromatickém jádře (viz obr.5). Zbývající 3 atomy uhlíku druhého aromatického jádra, na které jsou navázány atomy vodíku, jsem již určila pomocí experimentu ghsqc. 22
23 Výsledky s komentářem V dalším kroku jsem řešila napojení alifatických atomů uhlíku na aromatická jádra, což mi umožnil 2D experiment ghmqc. Atom vodíku s chemickým posunem δ=6.40 ppm má korelaci na atom uhlíku Aby atom uhlíku ležel ve vzdálenosti tří vazeb od atomu vodíku δ=6.40 ppm, musí být na aromatické jádro navázán v poloze 2, nebo 4. Již jsem určila, že v poloze 2 tohoto aromatického jádra se nachází buď atom uhlíku 130.5, nebo atom uhlíku Podle chemických posunů těchto uhlíkových atomů jsem rozhodla, že atom uhlíku 64.5 bude na aromatické jádro vázám přes atom uhlíku 130.5, protože z chemického posunu atomu uhlíku vyplývá, že na něho bude navázán atom kyslíku (viz obr.6). Atom vodíku δ=6.53 ppm má korelaci na alifatický atom uhlíku Tento atom uhlíku musí ležet ve vzdálenosti tří vazeb od atomu vodíku δ=6.53 ppm, bude tedy vázán v polohách 1, nebo 5. V těchto polohách leží buď atom uhlíku 125.4, a nebo atom uhlíku Obdobnou úvahou jako v předchozím případě jsem rozhodla, že atom uhlíku 25.1 bude na aromatické jádro vázán přes atom uhlíku (viz obr.6). Pomocí ghmqc experimentu jsem také určila vzájemnou polohu atomů uhlíku a Atom vodíku δ=3.66 ppm (na atomu uhlíku 64.5) má korelaci na atom uhlíku a atom vodíku δ= ppm (na uhlíku 25.1) má korelaci na atom uhlíku Atomy uhlíku a musí ležet na aromatickém jádře vedle sebe (viz obr.6). Atomy vodíku δ=6.59 ppm a δ=6.77 ppm mají korelaci na atom uhlíku Aby byla splněna podmínka, že tento atom uhlíku musí ležet ve vzdálenosti tří vazeb od obou atomů vodíku, musí být na aromatické jádro navázán v poloze 4. V této poloze leží buď atom uhlíku 133.3, nebo atom uhlíku Obdobně jako v předchozích případech jsem určila, že atom uhlíku 41.0 bude navázán na atom uhlíku (viz obr.7). Podle experimentu gmqfcops jsem určila, že atomy uhlíku 64.5 a 41.0 leží vedle sebe (obr.3). To znamená, že tento alifatický řetězec spojuje obě aromatická jádra. Tento předpoklad jsem si potvrdila podle korelací atomu vodíku δ=3.66 ppm (je navázán na atomu uhlíku 64.5) na atom uhlíku a atomu vodíku δ=3.01 ppm (náleží atomu uhlíku 41.0) na atom uhlíku (viz obr.8). 23
24 Výsledky s komentářem V dalším kroku jsem určila atom, nebo skupinu, která je navázaná na atom uhlíku 25.1, který substituuje aromatické jádro. Chemický posun 25.1 ppm je příliš malý, aby byl tento uhlík vázán na heteroatom. Musí být tedy navázán na uhlíkový atom. Pokud by tento uhlíkový atom nesl navázané atomy vodíku, projevilo by se to korelacemi v experimentech gmqfcops a ghmqc. V experimentu ghmqfcops má atom vodíku δ= ppm korelaci na atom vodíku δ= ppm. Tento atom vodíku je podle ghsqc navázán na atom uhlíku Atom vodíku δ= ppm má v ghmqc korelaci na atom uhlíku Tato korelace potvrzuje můj předpoklad, že atom uhlíku 46.8 je navázán na atom uhlíku 25.1 (viz obr.9). Od neznámé sloučeniny byla naměřena MS spektra. Molekulový pík této látky byl 330. Podle 13 C-NMR spektra je patrné, že sloučenina obsahuje 19 atomů uhlíku a podle 24
25 Výsledky s komentářem chemických posunů 4 atomů uhlíku δ=143.3 ppm, δ=144.9 ppm, δ=145.0 ppm a δ=145.2 ppm je zřejmé, že se ve sloučenině nachází 4 atomy kyslíku. Z 1 H-NMR spektra jsem určila, že sloučenina obsahuje pouze 2 methoxy skupiny na aromatickém jádře, na další 2 atomy kyslíku musí tedy být navázán atom vodíku tvořící fenolickou skupinu. Široký singlet s chemickým posunem δ=5.63 ppm musí odpovídat dvěma atomům vodíku a celá sloučenina tedy obsahuje 23 atomů vodíku. Pokud sečtu molární hmotnosti 19 atomů uhlíku, 23 atomů vodíku a 4 atomů kyslíku, dostanu číslo 315. Celková molární hmotnost neznámé sloučeniny je 329, zbývá mi tedy 14, což je přesně molární hmotnost jednoho atomu dusíku. Atom dusíku nemůže být vázán na aromatické jádro, protože substituenty obou aromatických jader jsou již přiřazeny. Musí být tedy vázán v alifatické oblasti. V alifatické části jsem ještě neurčila substituenty na atomech uhlíku 64.5 a 46.8 a umístění methylové skupiny atomu uhlíku Z chemického posunu těchto atomů je patrné, že jsou odstíněné, jedinou možností je tedy jejich vazba na atom dusíku. Cyklizaci alifatického řetězce uhlíků 25.1 a 46.8 pomocí atomu dusíku s atomem uhlíku 64.5 jsem si ověřila v ghmqc experimentu. Tuto teorii dokazují korelace atomu vodíku δ=3.66 ppm (na atomu uhlíku 64.5) s atomem uhlíku 46.8 a korelace atomu vodíku δ= ppm (na atomu uhlíku 46.8) s atomem uhlíku 64.5 (viz obr.10). Umístění methylové skupiny na atom dusíku potvrzují kromě chemického posunu také korelace jejího atomu uhlíku (42.5) s atomy vodíku δ=3.66 ppm (na atomu uhlíku 64.5) a δ= ppm (na atomu uhlíku 46.8), stejně tak jako korelace jejích atomů vodíku δ=2.45 ppm na atomy uhlíku 64.5 i 46.8 (viz obr.10). Výše uvedenou úvahou jsem určila skelet neznámé sloučeniny a ještě mi zbývalo rozhodnout o umístění fenolických a methoxy skupin na aromatických jádrech. Pomocí experimentu ghmqc však přiřazení není možné, protože v 1 H-NMR spektru mají methoxy skupiny signály, které se překrývají, nelze tedy rozlišit, které methoxy skupině náleží jednotlivé korelace na atomy uhlíku. V této situaci bylo třeba použít experimenty na prostorovou blízkost, pomocí kterých lze určit vzájemné ovlivnění substituentů v prostoru. Pro toto zjištění se využívají NOE-experimenty. Pomocí experimentu dpfgnoe jsem zjistila, 25
26 Výsledky s komentářem že atomy vodíku methoxy skupiny (δ=3.85 ppm, δ=3.84 ppm) jsou v prostorové blízkosti atomů vodíku δ=6.53 ppm a δ=6.73 ppm. Atomy vodíku δ=6.53 ppm a δ=6.73 ppm jsou každý na jiném aromatickém jádře, methoxy skupiny tedy budou ležet na různých jádrech a umístěny tak, aby byly v prostorové blízkosti těchto atomů vodíku. První methoxy skupina je v prostorové blízkosti atomu vodíku δ=6.53 ppm, musí být tedy navázaná na atom uhlíku ppm (viz obr.11). Toto umístění jsem si zkontrolovala pomocí experimentu dpfgnoe zjištěním, které atomy vodíku leží v prostorové blízkosti atomu vodíku δ=6.40 ppm. Methoxy skupina v prostorové blízkosti atomu vodíku δ=6.40 ppm neleží, což odpovídá mému předpokladu. V prostorové blízkosti atomu vodíku δ=6.40 ppm leží pouze alifatický atom vodíku δ=3.66 ppm (viz obr.11). Druhá methoxy skupina se musí nacházet v prostorové blízkosti atomu vodíku δ=6.73 ppm. Musí být tedy vázána na atom uhlíku (viz obr.11). Tím jsem dokončila určení struktury neznámé sloučeniny se sumárním vzorcem C 19 H 23 NO 4. 1 H NMR: (300 MHz, CDCl 3 ) δ 6.77 (1H, d, J=1.9 Hz, H2 ); 6.73 (1H, d, J=8.2 Hz, H5 ); 6.59 (1H, dd, J=1.9 Hz, J=8.2 Hz, H6 ); 6.53 (1H, s, H5); 6.40 (1H, s, H8); 5.63 (2H, bs, OH), 3.85 (3H, s, OCH 3 ); 3.84 (3H, s, OCH 3 ); 3.66 (1H, t, J=6.0 Hz, H1); (1H, m, H3); 3.01 (1H, dd, J=14.0 Hz, J=6.3 Hz, CH 2 ); (3H, m, H3, H4, CH 2 ); (1H, m, H4); 2.45 (3H, s, NCH 3 ). 13 C NMR: (75 MHz, CDCl 3 ) δ 145.2, 145.0, 144.9, 143.3, 133.3, 130.5, 125.4, 120.8, 115.5, 113.6, 110.5, 110.4, 64.5, 55.9, 55.8, 46.8, 42.5, 41.0, ESI-MS m/z 330 [M+H] + 26
27 Výsledky s komentářem O HO N OH O
28 Výsledky s komentářem 4.4. LC10-4 Neznámá sloučenina s kódovým označením LC10-4 byla získána izolací z rostliny Eschscholtzia californica z čeledi Papaveraceae. Základní informace o struktuře neznámé sloučeniny jsem získala prostudováním 1 H- NMR spektra. Z poměru integrálů jednotlivých píků, jsem určila počet atomů vodíku, které náleží k jednotlivým signálům. Podle chemických posunů jsem určila, že sloučenina obsahuje 5 atomů vodíků navázaných na aromatickém jádře. Jde o atomy vodíku s chemickým posunem δ=6.25 ppm, δ=6.53 ppm; δ=6.59 ppm; δ=6.74 ppm a δ=6.77 ppm. Na základě štěpení je velmi pravděpodobné, že sloučenina obsahuje nejméně 2 aromatická jádra. Po expandování této oblasti spektra je patrné štěpení jednotlivých signálů. Signály s chemickým posunem δ=6.25 ppm a δ=6.53 ppm jsou singlety, jde tedy o atomy vodíku navázané na jednom aromatickém jádře vzájemně v poloze para (aromatické jádro je substituováno v polohách 1, 2, 4 a 5), viz obr.1, nebo by se mohlo jednat o izolované atomy vodíku na dvou různých aromatických jádrech. Zbývající 3 atomy vodíku v aromatické oblasti mají štěpení: dublet dubletů δ=6.59 ppm s interakční konstantou J=1.9 Hz, J=8.2 Hz, dublet δ=6.74 ppm s interakční konstantou J=8.2 Hz a dublet δ=6.77 ppm s interakční konstantou J=1.9 Hz. Toto štěpení je typické pro atomy vodíku na aromatickém jádře substituovaném v polohách 1, 2 a 4 (viz obr.2). Signály s chemickým posunem δ=5.87 ppm a δ=5.85 ppm podle integrálu odpovídají každý jednomu atomu vodíku. Podle chemického posunu by se mohlo jednat o dva aromatické atomy vodíku, o dvě silně odstíněné CH skupiny nebo o CH 2 skupinu, která je navázaná na silně elektronegativní atom, nebo atomy. Rozhodnutí mezi těmito možnostmi mi umožní až přiřazení atomů vodíku k jednotlivým atomům uhlíku pomocí experimentu ghsqc. Singlet s chemickým posunem δ=3.86 ppm odpovídá třem atomům vodíku. Chemický posun 3.86 je typický pro methoxy skupinu navázanou na aromatickém jádře. Obdobně singlet s chemickým posunem δ=2.46 ppm odpovídá třem atomům vodíku, jde tedy o CH 3 skupinu. Chemický posun δ=2.46 ppm je příliš velký na to, aby se dalo 28
29 Výsledky s komentářem uvažovat o skupině navázané na kvarterním atomu uhlíku. Jde tedy o CH 3 skupinu, která je navázaná na elektronegativní atom. Z chemického posunu vyplývá, že by se mohlo jednat buď o atom dusíku, nebo atom síry. Signál s chemickým posunem δ=3.67 ppm je štěpený na triplet, z čehož jsem usoudila, že musí mít v těsném sousedství 2 atomy vodíku, pravděpodobně CH 2 skupinu. Chemický posun svědčí o odstínění. V sousedství musí být buď atom, nebo skupina způsobující výrazné odstínění. Ostatní signály ve spektru (δ= ppm) odpovídají dalším 6 alifatickým vodíkovým atomům. Z 13 C-NMR spektra jsem zjistila, že 12 atomů uhlíku má chemický posun větší než 100 ppm. Sloučenina tedy obsahuje 2 aromatická jádra. Chemický posun okolo 145 ppm je typický pro uhlíkové atomy aromatického jádra, na které je navázaný atom kyslíku. Dalších 6 atomů uhlíku má chemický posun menší než 70 ppm. Jedná se o alifatické uhlíky. Pomocí 2D experimentu ghsqc jsem mohla přiřadit jednotlivé vodíky příslušným uhlíkům: C (120.9)..H(6.59) C(115.5)..H(6.77) C(110.4)..H(6.74) C(108.3)..H(6.53) C(107.8)..H(6.25) C(100.5)..H(5.85; 5.87) C(65.1)....H(3.67) C(55.9) H(3.86) C(46.5)...H( ; ) C(42.5)....H(2.46) C(41.0)....H( ; 3.02) C(25.6)....H( ; ) Atomy uhlíku s chemickým posunem 145.7; 145.3, 144.9; 133.2; a jsou kvarterní. Atomy vodíku s chemickým posunem δ=5.87 ppm a δ=5.85 ppm náleží jednomu atomu uhlíku. Jedná se tedy o silně odstíněnou CH 2 skupinu. V důsledku toho je ve spektru pouze 11 uhlíkových atomů náležících aromatického systému. Je pravděpodobné, že 2 atomy uhlíku budou mít velice podobné chemické posuny, jedná se o atomy uhlíku s chemickým posunem ppm, což vyplývá z integrálu tohoto signálu. V 2D experimentu gmqfcops je patrné rozložení atomů vodíků na aromatických jádrech. Vodíkový atom s chemickým posunem δ=6.59 ppm má korelaci na atom s chemickým posunem δ=6.74 ppm, což mému rozvržení odpovídá, protože tyto atomy leží na aromatickém jádře vedle sebe. Ostatní vodíkové atomy aromatického systému na sebe korelaci nemají, nejsou tedy na aromatickém jádře vázány vedle sebe. 29
30 Výsledky s komentářem V alifatické oblasti je výrazná korelace tripletu δ=3.67 ppm na dva vodíkové atomy CH 2 skupiny (δ= ppm; δ=3.02 ppm), což odpovídá rozštěpení signálu na triplet (viz obr.3). Pomocí 2D experimentu ghmqc jsem nejdříve určila, které kvarterní atomy uhlíku patří jednotlivým aromatickým jádrům. Aromatické jádro s dvěma atomy vodíku v para poloze vůči sobě musí obsahovat další 4 kvarterní atomy uhlíku. Jsou to atomy uhlíku s chemickým posunem 127.1, (díky korelaci na atom vodíku s chemickým posunem δ=6.25 ppm) a atomy uhlíku s chemickým posunem 130.8, (díky korelaci na atom vodíku s chemickým posunem δ=6.53 ppm), viz obr.4. Na druhé aromatické jádro jsou navázány 3 atomy vodíku, musela jsem tedy přiřadit další 3 kvarterní atomy uhlíky. Prvním z přiřazených atomů je atom uhlíku s chemickým posunem z důvodu jeho korelace s atomem vodíku s chemickým posunem δ=6.59 ppm. Díky této korelaci jsem mohla přesně určit jeho umístění v poloze 1 aromatického jádra substituovaného v polohách 1, 2 a 4. Další pozorovatelná korelace atomu vodíku δ=6.59 ppm je na atom uhlíku 115.5, který nese atom vodíku δ=6.77 ppm jehož umístění jsem už určila z 1 H spektra. Správnost umístění atomu uhlíku jsem si potvrdila jeho korelací přes tři vazby s atomem vodíku δ=6.77 ppm. Z korelací s atomem vodíku δ=6.74 ppm jsem určila zbývající kvarterní atomy uhlíku: a (viz obr.5). Dalším mým krokem bylo určení napojení alifatických řetězců na aromatická jádra. Určení jsem prováděla pomocí korelací atomů vodíku na aromatickém systému s alifatickými atomy uhlíku. Atom vodíku δ=6.25 ppm má korelaci na atom uhlíku Protože jde o 30
31 Výsledky s komentářem korelaci přes tři vazby, je tento atom uhlíku (65.1) vázán na aromatické jádro v poloze ortho vůči atomu vodíku δ=6.25 ppm. Už jsem určila, že vedle atomu uhlíku jsou atomy uhlíku s chemickým posunem a Chemický posun odpovídá vazbě na atom kyslíku. Alifatický atom uhlíku 65.1 bude tedy na aromatické jádro připojen přes atom uhlíku (viz obr.6). Tuto úvahu jsem si zkontrolovala pomocí korelace atomu vodíku δ=3.67 ppm navázaném na uhlíku 65.1, který má korelaci na atom uhlíku a nemá korelaci na atom uhlíku Atom vodíku δ=6.53 ppm má korelaci na atom uhlíku Obdobným postupem jako v případě atomu uhlíku 65.1 jsem dospěla k závěru, že atom uhlíku 25.6 je na aromatické jádro vázán přes atom uhlíku (viz obr.6). Díky korelacím atomu uhlíku s atomem vodíku δ= ppm (navázaným na uhlík 25.6) a atomu uhlíku s atomem vodíku δ=3.67 ppm (vázáným na uhlík 65.1) jsem určila, že atomy uhlíku a jsou na aromatickém jádře vedle sebe a alifatické uhlíky 65.1 a 25.6 leží na stejné straně vůči atomům vodíku δ=6.25 ppm a δ=6.53 ppm. Atom uhlíku 41.0 má korelaci na atomy vodíku δ=6.59 ppm a δ=6.77 ppm, z čehož vyplývá, že musí být vázán na aromatické jádro v poloze 4. V této poloze je buď atom uhlíku 133.2, nebo atom uhlíku Obdobně jako v minulém případě bude na atom uhlíku vázán atom kyslíku a atom uhlíku 41.0 bude vázán na aromatické jádro přes atom uhlíku (viz obr.7). Z gmqfcops experimentu jsem už určila, že CH skupina uhlíku 65.1 se nachází v sousedství CH 2 skupiny uhlíku CH skupina uhlíku 65.1 je vázána na jedno jádro a CH 2 skupina uhlíku 41.0 na jádro druhé. Z toho plyne, že obě aromatická jádra jsou spojena alifatickým fragmentem CH(65.1)-CH 2 (41.0), viz obr.8. Tuto úvahu jsem zkontrolovala pomocí korelace atomu vodíku δ=3.67 ppm (na uhlíku 65.1) s uhlíkem (náleží vzdálenějšímu jádru) a korelace atomu vodíku δ=3.02 ppm (na uhlíku 41.0) s uhlíkem
32 Výsledky s komentářem Dalším mým krokem v určování struktury neznámé látky bylo určení druhého substituentu CH 2 skupiny uhlíku 25.6 (jednou vazbou je vázána na aromatické jádro). Chemický posun atomu uhlíku je 25.6 ppm, což je v oblasti vyššího pole. Tento chemický posun vylučuje vazbu na elektronegativní atom typu např. kyslíku nebo dusíku. CH 2 skupina tedy musí být vázaná na atom uhlíku. Z gmqfcops experimentu není jasné, zda korelace atomu vodíku δ= ppm s atomem vodíku δ= ppm je korelací mezi diastereotopickými atomy vodíku téhož atomu uhlíku, nebo mezi dvěma sousedními atomy vodíku náležící dvěma různým atomům uhlíku. Pokud by šlo o korelaci dvou sousedních atomů vodíku, sousedil by s atomem uhlíku 25.6 atom uhlíku 46.5 nebo Atom uhlíku 41.0 to být nemůže, protože je jasně potvrzeno, že leží vedle atomu uhlíku 65.1 a vedle druhého aromatického jádra. Z ghmqc experimentu vyplývá korelace atomu vodíku δ= ppm s atomem uhlíku Z toho vyplývá, že v sousedství atomu uhlíku 25.6 je CH 2 skupina atomu uhlíku 46.5 (viz obr.9). H H 2 C 25.6 H H H C R 1 R 2 H H H 2 C H H obr.9 32
33 Výsledky s komentářem V alifatické části mi zůstaly nevyřešené volné vazby z atomů uhlíku 65.1 a 46.5 a také methylová skupina atomu uhlíku Všechny tyto atomy uhlíku jsou odstíněny, musí tedy být vázané na elektronegativní atom. V případě dvojvazného kyslíku by mi zbyla neumístěná methylová skupina a atomy uhlíku by byly mnohem více odstíněné. Jediným řešením je vazba těchto tří atomů uhlíku přes trojvazný atom dusíku. Tuto úvahu jsem si zkontrolovala součtem molárních hmotností všech atomů ve sloučenině. Z údajů získaných z hmotnostního spektra vím, že neznámá sloučenina má molekulový pík M = 328 (M = M R +1) a tedy molární hmotnost 327. Zatím jsem při tvorbě struktury sloučeniny použila 19 atomů uhlíku, 21 atomů vodíku a 4 atomy kyslíku. Sečtením jejich molárních hmotností jsem dostala číslo 313. Když jsem ho odečetla od celkové molární hmotnosti neznámé sloučeniny, dostala jsem číslo 14, což je přesně molární hmotnost jednoho atomu dusíku. Uzavření alifatických řetězců do kruhu potvrzují korelace atomu uhlíku 65.1 s atomem vodíku δ= ppm (vázán na atomu uhlíku 46.5) a korelace atomu uhlíku 46.5 s atomem vodíku δ= ppm (vázán na atomu uhlíku 65.1). Umístění methylové skupiny potvrzují korelace jejích atomů vodíku (δ=2.46 ppm) na oba atomy uhlíku, 65.1 i 46.5 (viz obr.10). Umístění methoxy skupiny jsem určila pomocí experimentu ghmqc. Atomy vodíku methoxy skupiny (δ=3.86 ppm) mají korelaci na atom uhlíku Methoxy skupina je tedy navázaná na atom uhlíku a atom uhlíku na témže aromatickém jádře nese hydroxylovou skupinu (viz obr.11). Dalším problémem bylo umístění atomu uhlíku s chemickým posunem 100.5, na který jsou navázané 2 atomy vodíku s chemickým posunem δ=5.87 ppm a δ=5.85 ppm. Chemický posun napovídá silnému odstínění. Jedinou korelací atomů vodíku této skupiny je korelace s atomem uhlíku Tato skupina bude tedy navázaná přes atom kyslíku na atom uhlíku a vytvoří můstek na vedlejší atom kyslíku navázaný na sousedním atomu uhlíku 33
34 Výsledky s komentářem aromatického jádra (145.7), viz obr.11. Chemický posun atomu uhlíku (100.5) i atomů vodíku (δ=5.87 ppm a δ=5.85 ppm) této CH 2 skupiny odpovídá jejímu umístění mezi dvěma atomy kyslíku, které jsou silně elektronegativní a způsobí silné odstínění. Tím jsem dokončila určení struktury neznámé látky. Sloučenina má sumární vzorec C 19 H 21 NO 4 a tedy molární hmotnost H NMR: (300 MHz, CDCl 3 ) δ 6.77 (1H, d, J=1.9 Hz, H2 ); 6.74 (1H, d, J=8.2 Hz, H5 ); 6.59 (1H, dd, J=1.9 Hz, J=8.2 Hz, H6 ); 6.53 (1H, s, H5); 6.25 (1H, s, H8); 5.87 (1H, d, J=1.5 Hz, OCH 2 ), 5.85 (1H, d, J=1.5 Hz, OCH 2 ); 3.86 (3H, s, OCH 3 ); 3.67 (1H, t, J=6.2 Hz, H1); (1H, m, H3); 3.02 (1H, dd, J=14.0 Hz, J=6.1 Hz, CH 2 ); (3H, m, H3, H4, CH 2 ); (1H, m, H4); 2.46 (3H, s, NCH 3 ). 13 C NMR: (75 MHz, CDCl 3 ) δ 145.7, 145.3, 145.3, 144.9, 133.2, 130.8, 127.1, 120.9, 115.5, 110.4, 108.3, 107.8, 100.5, 65.1, 55.9, 46.5, 42.5, 41.0, ESI-MS m/z 328 [M+H] + 34
35 35 Výsledky s komentářem
36 Závěr 5. ZÁVĚR V rámci této diplomové práce byla určena struktura 3 neznámých sloučenin získaných izolací z rostliny Eschscholtzia californica (sluncovka kalifornská) z čeledi Papaveracea provedenou na katedře farmaceutické botaniky a ekologie Farmaceutické fakulty v Hradci Králové. Neznámá látka s kódovým označením LC-004 byla identifikována jako skulerin a její struktura byla ověřena na základě porovnání naměřeného 13 C-NMR spektra se spektry v literatuře 9. Neznámá látka s kódovým označením LC-006 je retikulin a porovnáním naměřeného 13 C-NMR spektra se spektry v literatuře 10 byla jeho identita potvrzena. Struktura látky s kódovým označením LC10-4 byla ověřena porovnáním naměřeného 1 H-NMR se spektrem v literatuře
37 Literatura 6. LITERATURA 1. Beck M. A., Häberlein H., Phytochemistry, 1999, 50, Gafner S. et al., J. Nat. Prod. 2002, 69, Fabre N. et al., J.Chromatogr. A, 2000, 904, Větvička V., Letničky a dvouletky, 1.vydání, Praha, Aventinum, 1999, 223 s., ISBN , Simon H., Letničky, 1.vydání, Čestlice, Rebo Productions, 2006, 95 s., ISBN , Blaschek, W. et al.: HagerROM Hagers Handbuch der Drogen und Arzneistoffe. CD-Realisierung: Informatik II, Universität Würzburg, [Programmversion 6.1], Springer Medizin Verlag Heidelberg Slavík J., Slavíková L. Coll. Czech. Chem. Commun. 1986, 51, Doležal J., Biologická aktivita obsahových látek VIII. Vliv alkaloidů z různých rostlinných taxonů na acetylcholinesterázu. (Diplomová práce) Hradec Králové, Univerzita Karlova, Farmaceutická fakulta, Eisenreich W.J., Isolierung, Identifizierung und Partialsynthese von Pflanzeninhaltsstoffen aus Croton Flavens L. (disertační práce) München, Ludwig- Maximilians-Universität München, Fakultät für Chemie und Pharmazie, 2002, str Tosce S.G., Cooper S.D., Morello D.R., Hays P.A., Casale J.F., Casale E., J.Forensic Sci, 2006, 51, Pinna G.A., Cignarella G., Scolastico S., Porceddu S.C., Eur. J. Med. Chem., 1994, 29,
38 Přílohy 7. PŘÍLOHY 7.1. NMR spektra sloučeniny LC
39 Přílohy 1 H-NMR 39
40 Přílohy 13 C-NMR 40
41 Přílohy DEPT 41
42 Přílohy ghsqc 42
43 Přílohy ghmqc 43
44 Přílohy 7.2. NMR spektra sloučeniny LC
45 Přílohy 1 H-NMR 45
46 Přílohy 13 C-NMR 46
47 Přílohy DEPT 47
48 Přílohy gmqfcops 48
49 Přílohy ghsqc 49
50 Přílohy ghmqc 50
51 Přílohy NMR spektra sloučeniny LC
52 Přílohy 1 H-NMR 52
53 Přílohy 13 C-NMR 53
54 Přílohy gmqfcops 54
55 Přílohy ghsqc 55
56 Přílohy ghmqc 56
Využití NMR při strukturní analýze látek izolovaných z Corydalis cava (Fumariaceae) a Eschscholtzia californica (Papaveraceae)
 FARMACEUTICKÁ FAKULTA V HRADCI KRÁLOVÉ KATEDRA ANORGANICKÉ A ORGANICKÉ CHEMIE RIGORÓZNÍ PRÁCE Využití NMR při strukturní analýze látek izolovaných z Corydalis cava (Fumariaceae) a Eschscholtzia californica
FARMACEUTICKÁ FAKULTA V HRADCI KRÁLOVÉ KATEDRA ANORGANICKÉ A ORGANICKÉ CHEMIE RIGORÓZNÍ PRÁCE Využití NMR při strukturní analýze látek izolovaných z Corydalis cava (Fumariaceae) a Eschscholtzia californica
O Minimální počet valencí potřebných ke spojení vícevazných atomů = (24 C + 3 O + 7 N 1) * 2 = 66 valencí
 Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Jméno a příjmení:_bohumil_dolenský_ Datum:_10.12.2010_ Fakulta:_FCHI_ Kruh:_ÚACh_ 1. Sepište seznam signálů 1 H dle klesajícího chemického posunu (včetně nečistot), uveďte chemický posun, multiplicitu
Postup při interpretaci NMR spekter neznámého vzorku
 Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
Postup při interpretaci NMR spekter neznámého vzorku VŠCT 2017, Bohumil Dolenský, dolenskb@vscht.cz Tento text byl vypracován pro projekt Inovace předmětu Semestrální práce oboru analytická chemie I. Slouží
Univerzita Karlova v Praze. Farmaceutická fakulta v Hradci Králové
 Univerzita Karlova v Praze Farmaceutická fakulta v radci Králové VYUŽITÍ NMR SPEKTRSKPIE PŘI STRUKTURNÍ ANALÝZE SEKUNDÁRNÍC METABLITŮ IZLVANÝC Z BERBERIS VULGARIS L. (diplomová práce) radec Králové, 2014
Univerzita Karlova v Praze Farmaceutická fakulta v radci Králové VYUŽITÍ NMR SPEKTRSKPIE PŘI STRUKTURNÍ ANALÝZE SEKUNDÁRNÍC METABLITŮ IZLVANÝC Z BERBERIS VULGARIS L. (diplomová práce) radec Králové, 2014
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE
 SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
SPEKTROSKOPIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Obecné základy nedestruktivní metoda strukturní analýzy zabývá se rezonancí atomových jader nutná podmínka pro měření spekter: nenulový spin atomového jádra
Základní parametry 1 H NMR spekter
 LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
Měření a interpretace NMR spekter
 Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Řešení
Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Řešení
LEKCE 1b. Základní parametry 1 H NMR spekter. Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)*
 Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Spektra 1 H NMR. Velmi zjednodušeně! Bohumil Dolenský
 Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními prin
 Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Autoři: Pavel Zachař, David Sýkora Ukázky spekter k procvičování na semináři: Tento soubor je pouze prvním ilustrativním seznámením se základními principy hmotnostní spektrometrie a v žádném případě nezahrnuje
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance II. Příprava předmětu byla podpořena
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance II. Příprava předmětu byla podpořena
Středoškolská odborná činnost 2005/2006
 Středoškolská odborná činnost 2005/2006 Obor 3 - chemie Autor: Martin Hejda MSŠCH, Křemencova 12 116 28 Praha 1, 3. ročník Zadavatel a vedoucí práce: Mgr. Miroslav Kašpar CSc. Fyzikální ústav AVČR Na Slovance
Středoškolská odborná činnost 2005/2006 Obor 3 - chemie Autor: Martin Hejda MSŠCH, Křemencova 12 116 28 Praha 1, 3. ročník Zadavatel a vedoucí práce: Mgr. Miroslav Kašpar CSc. Fyzikální ústav AVČR Na Slovance
Měření a interpretace NMR spekter
 Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 4110 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
Univerzita Karlova v Praze. Farmaceutická fakulta v Hradci Králové
 Univerzita Karlova v Praze Farmaceutická fakulta v radci Králové VYUŽITÍ MR SPEKTRSKPIE PŘI STRUKTURÍ AALÝZE LÁTEK IZLVAÝC Z BERBERIS VULGARIS L. A ARCISSUS PETICUS CV. PIK PARASL (rigorózní práce) radec
Univerzita Karlova v Praze Farmaceutická fakulta v radci Králové VYUŽITÍ MR SPEKTRSKPIE PŘI STRUKTURÍ AALÝZE LÁTEK IZLVAÝC Z BERBERIS VULGARIS L. A ARCISSUS PETICUS CV. PIK PARASL (rigorózní práce) radec
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie
 Jména: Datum: Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie Cílem laboratorního cvičení je prozkoumat interakce léčiva diclofenac s -cyklodextrinem v D 2 O při tvorbě komplexu
Jména: Datum: Studium komplexace -cyklodextrinu s diclofenacem s využitím NMR spektroskopie Cílem laboratorního cvičení je prozkoumat interakce léčiva diclofenac s -cyklodextrinem v D 2 O při tvorbě komplexu
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 4110, dolenskb@vscht.cz Hmotnostní spektrometrie II. Příprava předmětu byla podpořena projektem
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 4110, dolenskb@vscht.cz Hmotnostní spektrometrie II. Příprava předmětu byla podpořena projektem
LEKCE 3b. Využití 2D experimentů k přiřazení složitější molekuly. Zpracování, výpočet a databáze NMR spekter (ACD/Labs, Topspin, Mnova) ppm
 LEKCE 3b Využití D experimentů k přiřazení složitější molekuly ppm ppm 10 1.0 1.5 15.0 130.5 3.0 135 3.5 140 4.0 4.5 145 5.0 150 5.5 155 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0.5.0 1.5 1.0 ppm 160.6.4..0
LEKCE 3b Využití D experimentů k přiřazení složitější molekuly ppm ppm 10 1.0 1.5 15.0 130.5 3.0 135 3.5 140 4.0 4.5 145 5.0 150 5.5 155 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0.5.0 1.5 1.0 ppm 160.6.4..0
LEKCE 7. Interpretace 13 C NMR spekter. Využití 2D experimentů. Zpracování, výpočet a databáze NMR spekter (ACD/Labs, Topspin, Mnova) ppm
 LEKCE 7 Interpretace 13 C MR spekter Využití 2D experimentů ppm 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0 2.5 2.0 1.5 1.0 ppm Zpracování, výpočet a databáze MR spekter
LEKCE 7 Interpretace 13 C MR spekter Využití 2D experimentů ppm 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 6.5 6.5 6.0 5.5 5.0 4.5 4.0 3.5 3.0 2.5 2.0 1.5 1.0 ppm Zpracování, výpočet a databáze MR spekter
Měření a interpretace NMR spekter
 Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 40 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
Měření a interpretace NMR spekter Bohumil Dolenský E-mail : Telefon : Místnost : www : dolenskb@vscht.cz (+420) 220 44 40 budova A, místnost 28 http://www.vscht.cz/anl/dolensky/technmr/index.html Struktura
POROVNÁNÍ ÚČINNOSTI SRÁŽENÍ REAKTIVNÍCH AZOBARVIV POUŽITÍM IONTOVÉ KAPALINY A NÁSLEDNÁ FLOKULACE AZOBARVIV S Al 2 (SO 4 ) 3.18H 2 O S ÚPRAVOU ph
 POROVNÁNÍ ÚČINNOSTI SRÁŽENÍ REAKTIVNÍCH AZOBARVIV POUŽITÍM IONTOVÉ KAPALINY A NÁSLEDNÁ FLOKULACE AZOBARVIV S Al 2 (SO 4 ) 3.18H 2 O S ÚPRAVOU ph Ing. Jana Martinková Ing. Tomáš Weidlich, Ph.D. prof. Ing.
POROVNÁNÍ ÚČINNOSTI SRÁŽENÍ REAKTIVNÍCH AZOBARVIV POUŽITÍM IONTOVÉ KAPALINY A NÁSLEDNÁ FLOKULACE AZOBARVIV S Al 2 (SO 4 ) 3.18H 2 O S ÚPRAVOU ph Ing. Jana Martinková Ing. Tomáš Weidlich, Ph.D. prof. Ing.
Typy vzorců v organické chemii
 Typy vzorců v organické chemii Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Březen 2010 Mgr. Alena Jirčáková Typy vzorců v organické chemii Zápis
Typy vzorců v organické chemii Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Březen 2010 Mgr. Alena Jirčáková Typy vzorců v organické chemii Zápis
Význam interakční konstanty, Karplusova rovnice. konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TOCSY
 Význam interakční konstanty, Karplusova rovnice konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TOCSY Karplusova rovnice ve strukturní analýze J(H,H) = A + B cos f
Význam interakční konstanty, Karplusova rovnice konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TOCSY Karplusova rovnice ve strukturní analýze J(H,H) = A + B cos f
Univerzita Karlova v Praze Farmaceutická fakulta v Hradci Králové Využití NMR při strukturní analýze
 Univerzita Karlova v Praze Farmaceutická fakulta v radci Králové Využití MR při strukturní analýze (diplomová práce) radec Králové, 2011 Zdeněk ovák Prohlášení Prohlašuji, že tato práce je mým původním
Univerzita Karlova v Praze Farmaceutická fakulta v radci Králové Využití MR při strukturní analýze (diplomová práce) radec Králové, 2011 Zdeněk ovák Prohlášení Prohlašuji, že tato práce je mým původním
COSY + - podmínky měření a zpracování dat ztráta rozlišení ve spektru. inphase dublet, disperzní. antiphase dublet, absorpční
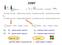 y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
Laboratoř NMR Strukturní analýza a 2D NMR spektra
 Laboratoř NMR Strukturní analýza a 2D NMR spektra Místo: Laboratoř NMR, místnost A28, Kontakt: doc. Ing. Bohumil DOLENSKÝ, Ph.D., Ústav analytické chemie, Vysoká škola chemicko-technologická, Technická
Laboratoř NMR Strukturní analýza a 2D NMR spektra Místo: Laboratoř NMR, místnost A28, Kontakt: doc. Ing. Bohumil DOLENSKÝ, Ph.D., Ústav analytické chemie, Vysoká škola chemicko-technologická, Technická
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance I. Příprava předmětu byla podpořena projektem
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: doc. Ing. Bohumil Dolenský, Ph.D. A28, linka 40, dolenskb@vscht.cz Nukleární Magnetická Rezonance I. Příprava předmětu byla podpořena projektem
LEKCE 2b. NMR a chiralita, posunová činidla. Interpretace 13 C NMR spekter
 LEKCE 2b NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Stanovení optické čistoty Enantiomery jsou nerozlišitelné v NMR spektroskopii není možné rozlišit enantiomer od racemátu!!! Enantiotopické
LEKCE 2b NMR a chiralita, posunová činidla Interpretace 13 C NMR spekter Stanovení optické čistoty Enantiomery jsou nerozlišitelné v NMR spektroskopii není možné rozlišit enantiomer od racemátu!!! Enantiotopické
HYDROXYDERIVÁTY. Alkoholy Fenoly Bc. Miroslava Wilczková
 HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
CHEMIE - Úvod do organické chemie
 Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
Název školy Číslo projektu Autor Název šablony Název DUMu Stupeň a typ vzdělávání Vzdělávací oblast Vzdělávací obor Vzdělávací okruh Druh učebního materiálu Cílová skupina Anotace SŠHS Kroměříž CZ.1.07/1.5.00/34.0911
NMR spektroskopie. Úvod
 NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
INTERPRETACE HMOTNOSTNÍCH SPEKTER
 INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
NMR spektroskopie Instrumentální a strukturní analýza
 NMR spektroskopie Instrumentální a strukturní analýza prof. RNDr. Zdeněk Friedl, CSc. Použitá a doporučená literatura Solomons T.W.G., Fryhle C.B.: Organic Chemistry, 8th Ed., Wiley 2004. Günther H.: NMR
NMR spektroskopie Instrumentální a strukturní analýza prof. RNDr. Zdeněk Friedl, CSc. Použitá a doporučená literatura Solomons T.W.G., Fryhle C.B.: Organic Chemistry, 8th Ed., Wiley 2004. Günther H.: NMR
Naše NMR spektrometry
 Naše NMR spektrometry Varian NMR System 300 MHz Varian INOVA 400 MHz Bruker Avance III 600 MHz NMR spektrometr magnet průřez supravodičem NMR spektrometr sonda Tvar spektra reálná část imaginární část
Naše NMR spektrometry Varian NMR System 300 MHz Varian INOVA 400 MHz Bruker Avance III 600 MHz NMR spektrometr magnet průřez supravodičem NMR spektrometr sonda Tvar spektra reálná část imaginární část
Chemický posun v uhlíkových NMR spektrech
 13 -NMR spektrometrie rezonance jader 13 nastává ve srovnání s 1 při cca čtvrtinové frekvenci, tj. pracovní frekvenci 100 Mz (v 1 ) odpovídá 25,15 Mz ( 13 ) a frekvenci 600 Mz (v 1 ) odpovídá 150,9 Mz
13 -NMR spektrometrie rezonance jader 13 nastává ve srovnání s 1 při cca čtvrtinové frekvenci, tj. pracovní frekvenci 100 Mz (v 1 ) odpovídá 25,15 Mz ( 13 ) a frekvenci 600 Mz (v 1 ) odpovídá 150,9 Mz
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1. Jan Sýkora
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1 Jan Sýkora LC/NMR Jan Sýkora (ÚCHP AV ČR) LC - NMR 1 H NMR (500 MHz) mez detekce ~ 1 mg/ml (5 µmol látky) NMR parametry doba
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti LC-NMR 1 Jan Sýkora LC/NMR Jan Sýkora (ÚCHP AV ČR) LC - NMR 1 H NMR (500 MHz) mez detekce ~ 1 mg/ml (5 µmol látky) NMR parametry doba
MIKROVLNNÁ SPEKTROSKOPIE RADIKÁLU FCO 2. Lucie Kolesniková
 MIKROVLÁ SPEKTROSKOPIE RADIKÁLU FCO 2 Lucie Kolesniková Ústav analytické chemie, Fakulta chemicko-inženýrská, Vysoká škola chemicko-technologická v Praze, Technická 5, 166 28 Praha 6 E-mail: lucie.kolesnikova@vscht.cz
MIKROVLÁ SPEKTROSKOPIE RADIKÁLU FCO 2 Lucie Kolesniková Ústav analytické chemie, Fakulta chemicko-inženýrská, Vysoká škola chemicko-technologická v Praze, Technická 5, 166 28 Praha 6 E-mail: lucie.kolesnikova@vscht.cz
Vysoká škola chemicko-technologická v Praze. Ústav organické technologie. Václav Matoušek
 Vysoká škola chemicko-technologická v Praze Ústav organické technologie VŠCHT PRAHA SVOČ 2005 Václav Matoušek Školitel : Ing. Petr Kačer, PhD. Prof. Ing. Libor Červený, DrSc. Proč asymetrická hydrogenace?
Vysoká škola chemicko-technologická v Praze Ústav organické technologie VŠCHT PRAHA SVOČ 2005 Václav Matoušek Školitel : Ing. Petr Kačer, PhD. Prof. Ing. Libor Červený, DrSc. Proč asymetrická hydrogenace?
OBECNÁ CHEMIE. Kurz chemie pro fyziky MFF-UK přednášející: Jaroslav Burda, KChFO.
 OBECNÁ CHEMIE Kurz chemie pro fyziky MFF-UK přednášející: Jaroslav Burda, KChFO burda@karlov.mff.cuni.cz HMOTA, JEJÍ VLASTNOSTI A FORMY Definice: Každý hmotný objekt je charakterizován dvěmi vlastnostmi
OBECNÁ CHEMIE Kurz chemie pro fyziky MFF-UK přednášející: Jaroslav Burda, KChFO burda@karlov.mff.cuni.cz HMOTA, JEJÍ VLASTNOSTI A FORMY Definice: Každý hmotný objekt je charakterizován dvěmi vlastnostmi
Dolenský, VŠCHT Praha, pracovní verze 1
 1. Multiplicita_INDA Interpretujte multiplety všech signálů spektra. Všechny multiplety jsou důsledkem interakce výhradně s jádry s magnetickým jaderným spinem 1/2, a nejsou významně komplikovány přítomností
1. Multiplicita_INDA Interpretujte multiplety všech signálů spektra. Všechny multiplety jsou důsledkem interakce výhradně s jádry s magnetickým jaderným spinem 1/2, a nejsou významně komplikovány přítomností
Diskutujte, jak široký bude pás spojený s fosforescencí versus fluorescencí. Udělejte odhad v cm -1.
 S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
S použitím modelu volného elektronu (=částice v krabici) spočtěte vlnovou délku a vlnočet nejdlouhovlnějšího elektronového přechodu u molekuly dekapentaenu a oktatetraenu. Diskutujte polohu absorpčního
Dynamické procesy & Pokročilé aplikace NMR. chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů
 Dynamické procesy & Pokročilé aplikace NMR chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů Chemická výměna jakýkoli proces při kterém dané jádro mění svůj stav
Dynamické procesy & Pokročilé aplikace NMR chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů Chemická výměna jakýkoli proces při kterém dané jádro mění svůj stav
spinový rotační moment (moment hybnosti) kvantové číslo jaderného spinu I pro NMR - jádra s I 0
 Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla energetické stavy jádra v magnetickém poli rezonanční podmínka - instrumentace pulsní metody, pulsní sekvence relaxační
Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla energetické stavy jádra v magnetickém poli rezonanční podmínka - instrumentace pulsní metody, pulsní sekvence relaxační
Nukleární magnetická rezonance (NMR)
 Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) Použití GC-MS spektrometrie
 LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) C Použití GC-MS spektrometrie Vedoucí práce: Doc. Ing. Petr Kačer, Ph.D., Ing. Kamila Syslová Umístění práce: laboratoř 79 Použití GC-MS spektrometrie
LABORATOŘ OBORU I ÚSTAV ORGANICKÉ TECHNOLOGIE (111) C Použití GC-MS spektrometrie Vedoucí práce: Doc. Ing. Petr Kačer, Ph.D., Ing. Kamila Syslová Umístění práce: laboratoř 79 Použití GC-MS spektrometrie
ALKOHOLY, FENOLY A ETHERY. b. Jaké zdroje cukru znáte a jak se nazývají produkty jejich kvašení?
 ALKOLY, FENOLY A ETHERY Kvašení 1. S použitím literatury nebo internetu odpovězte na následující otázky: a. Jakým způsobem v přírodě vzniká etanol? Napište rovnici. b. Jaké zdroje cukru znáte a jak se
ALKOLY, FENOLY A ETHERY Kvašení 1. S použitím literatury nebo internetu odpovězte na následující otázky: a. Jakým způsobem v přírodě vzniká etanol? Napište rovnici. b. Jaké zdroje cukru znáte a jak se
Význam interakční konstanty, Karplusova rovnice
 LEKCE 9 Význam interakční konstanty, Karplusova rovnice konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TCSY T E E 1 E 1 T 0 6 T E 1 T 0 88 7 0 T E 0 0 E T 0 5 108
LEKCE 9 Význam interakční konstanty, Karplusova rovnice konfigurace na dvojné vazbě a na šestičlenných kruzích konformace furanosového kruhu TCSY T E E 1 E 1 T 0 6 T E 1 T 0 88 7 0 T E 0 0 E T 0 5 108
Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch
 Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch Atom, složení a struktura Chemické prvky-názvosloví, slučivost Chemické sloučeniny, molekuly Chemická vazba
Sekunda (2 hodiny týdně) Chemické látky a jejich vlastnosti Směsi a jejich dělení Voda, vzduch Atom, složení a struktura Chemické prvky-názvosloví, slučivost Chemické sloučeniny, molekuly Chemická vazba
Metody spektrální. Metody molekulové spektroskopie NMR. Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti
 Metody spektrální Metody molekulové spektroskopie NMR Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla
Metody spektrální Metody molekulové spektroskopie NMR Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla
Základní parametry 1 H NMR spekter
 LEKCE 6 Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 6 Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)*
 Základní parametry 1 NMR spekter NMR a chiralita, posunová činidla Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR
Základní parametry 1 NMR spekter NMR a chiralita, posunová činidla Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR
NUKLEÁRNÍ MAGNETICKÁ REZONANČNÍ SPEKTROMETRIE
 NUKLEÁRNÍ MAGNETIKÁ REZNANČNÍ SPEKTRMETRIE Teoretický úvod Pracovní technika NMR 1 -NMR organických sloučenin 13 -NMR Aplikace NMR Nukleární (jaderná) magnetická rezonanční spektrometrie je založena na
NUKLEÁRNÍ MAGNETIKÁ REZNANČNÍ SPEKTRMETRIE Teoretický úvod Pracovní technika NMR 1 -NMR organických sloučenin 13 -NMR Aplikace NMR Nukleární (jaderná) magnetická rezonanční spektrometrie je založena na
Program. Materiály ke studiu NMR. Data, Soubory. Seminář z Analytické chemie B. \\PYR\SCRATCH\
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Seminář z Analytické chemie B Tento materiál vznikl za podpory projektu CHEMnote PPA CZ..7/../48 Inovace bakalářského studijního programu
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti Seminář z Analytické chemie B Tento materiál vznikl za podpory projektu CHEMnote PPA CZ..7/../48 Inovace bakalářského studijního programu
Univerzita Karlova v Praze
 Univerzita Karlova v Praze Farmaceutická fakulta v Hradci Králové Katedra anorganické a organické chemie Mgr. Eva Lepičová Darzens Reaction of 2-Bromo-4,6-dimethoxy-3(2H)-benzofuranone with Aromatic Aldehydes
Univerzita Karlova v Praze Farmaceutická fakulta v Hradci Králové Katedra anorganické a organické chemie Mgr. Eva Lepičová Darzens Reaction of 2-Bromo-4,6-dimethoxy-3(2H)-benzofuranone with Aromatic Aldehydes
Chemické veličiny, vztahy mezi nimi a chemické výpočty
 SBÍRKA ŘEŠENÝCH PŘÍKLADŮ PRO PROJEKT PŘÍRODNÍ VĚDY AKTIVNĚ A INTERAKTIVNĚ CZ.1.07/1.1.24/01.0040 Chemické veličiny, vztahy mezi nimi a chemické výpočty Mgr. Jana Žůrková, 2013, 20 stran Obsah 1. Veličiny
SBÍRKA ŘEŠENÝCH PŘÍKLADŮ PRO PROJEKT PŘÍRODNÍ VĚDY AKTIVNĚ A INTERAKTIVNĚ CZ.1.07/1.1.24/01.0040 Chemické veličiny, vztahy mezi nimi a chemické výpočty Mgr. Jana Žůrková, 2013, 20 stran Obsah 1. Veličiny
Tabulace učebního plánu. Obecná chemie. Vzdělávací obsah pro vyučovací předmět : Ročník: 1.ročník a kvinta
 Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
Tabulace učebního plánu Vzdělávací obsah pro vyučovací předmět : CHEMIE Ročník: 1.ročník a kvinta Obecná Bezpečnost práce Názvosloví anorganických sloučenin Zná pravidla bezpečnosti práce a dodržuje je.
Vlastnosti. Pozor! H 3 C CH 3 H CH 3
 Alkeny Vlastnosti C n 2n obsahují dvojné vazby uhlíky v sp 2 hybridizaci násobná vazba vzniká překryvem 2p orbitalů obou atomů uhlíku nad a pod prostorem obsazeným vazbou aby k překryvu mohlo dojít, musí
Alkeny Vlastnosti C n 2n obsahují dvojné vazby uhlíky v sp 2 hybridizaci násobná vazba vzniká překryvem 2p orbitalů obou atomů uhlíku nad a pod prostorem obsazeným vazbou aby k překryvu mohlo dojít, musí
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL.
 CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
CHEMICKÉ VÝPOČTY I. ČÁST LÁTKOVÉ MNOŽSTVÍ. HMOTNOSTI ATOMŮ A MOLEKUL. Látkové množství Značka: n Jednotka: mol Definice: Jeden mol je množina, která má stejný počet prvků, jako je atomů ve 12 g nuklidu
ZÁKLADNÍ EXPERIMENTÁLNÍ
 Kurz praktické NMR spektroskopie 10. - 12. říjen 2011, Praha ZÁKLADNÍ EXPERIMENTÁLNÍ POSTUPY NMR ROZTOKŮ A KAPALIN Jana Svobodová Ústav Makromolekulární chemie AV ČR, v.v.i. Bruker 600 Avance III PŘÍSTROJOVÉ
Kurz praktické NMR spektroskopie 10. - 12. říjen 2011, Praha ZÁKLADNÍ EXPERIMENTÁLNÍ POSTUPY NMR ROZTOKŮ A KAPALIN Jana Svobodová Ústav Makromolekulární chemie AV ČR, v.v.i. Bruker 600 Avance III PŘÍSTROJOVÉ
Spektrální metody NMR I. opakování
 Spektrální metody NMR I opakování Využití NMR určování chemické struktury přírodní látky, organická syntéza konstituce, konformace, konfigurace ověření čistoty studium dynamických procesů reakční kinetika
Spektrální metody NMR I opakování Využití NMR určování chemické struktury přírodní látky, organická syntéza konstituce, konformace, konfigurace ověření čistoty studium dynamických procesů reakční kinetika
NMR spektroskopie rádiové frekvence jádra spinovou rezonancí jader spinový moment lichý počet
 NMR spektroskopie NMR spektroskopie Nukleární Magnetická Resonance - spektroskopická metoda založená na měření absorpce elektromagnetického záření (rádiové frekvence asi od 4 do 900 MHz). Na rozdíl od
NMR spektroskopie NMR spektroskopie Nukleární Magnetická Resonance - spektroskopická metoda založená na měření absorpce elektromagnetického záření (rádiové frekvence asi od 4 do 900 MHz). Na rozdíl od
KOMPLEXY EUROPIA(III) LUMINISCENČNÍ VLASTNOSTI A VYUŽITÍ V ANALYTICKÉ CHEMII. Pavla Pekárková
 KOMPLEXY EUROPIA(III) LUMINISCENČNÍ VLASTNOSTI A VYUŽITÍ V ANALYTICKÉ CHEMII Pavla Pekárková Katedra analytické chemie, Přírodovědecká fakulta, Masarykova univerzita, Kotlářská 2, 611 37 Brno E-mail: 78145@mail.muni.cz
KOMPLEXY EUROPIA(III) LUMINISCENČNÍ VLASTNOSTI A VYUŽITÍ V ANALYTICKÉ CHEMII Pavla Pekárková Katedra analytické chemie, Přírodovědecká fakulta, Masarykova univerzita, Kotlářská 2, 611 37 Brno E-mail: 78145@mail.muni.cz
Strukturní analýza. NMR spektroskopie
 Strukturní analýza NMR spektroskopie RNDr. Zdeněk Tošner, Ph.D. lavova 8, místnost 020 tel. 22195 1323 tosner@natur.cuni.cz www.natur.cuni.cz/nmr/vyuka.html Literatura Böhm, Smrčková-Voltrová: Strukturní
Strukturní analýza NMR spektroskopie RNDr. Zdeněk Tošner, Ph.D. lavova 8, místnost 020 tel. 22195 1323 tosner@natur.cuni.cz www.natur.cuni.cz/nmr/vyuka.html Literatura Böhm, Smrčková-Voltrová: Strukturní
Struktura proteinů. - testík na procvičení. Vladimíra Kvasnicová
 Struktura proteinů - testík na procvičení Vladimíra Kvasnicová Mezi proteinogenní aminokyseliny patří a) kyselina asparagová b) kyselina glutarová c) kyselina acetoctová d) kyselina glutamová Mezi proteinogenní
Struktura proteinů - testík na procvičení Vladimíra Kvasnicová Mezi proteinogenní aminokyseliny patří a) kyselina asparagová b) kyselina glutarová c) kyselina acetoctová d) kyselina glutamová Mezi proteinogenní
Obor: Zemědělské biotechnologie Specializace: Rostlinné biotechnologie Katedra agroekologie. Bakalářská práce
 JIHOČESKÁ UNIVERZITA V ČESKÝCH BUDĚJOVICÍCH ZEMĚDĚLSKÁ FAKULTA Obor: Zemědělské biotechnologie Specializace: Rostlinné biotechnologie Katedra agroekologie Bakalářská práce Vliv genotypu na obsah rutinu
JIHOČESKÁ UNIVERZITA V ČESKÝCH BUDĚJOVICÍCH ZEMĚDĚLSKÁ FAKULTA Obor: Zemědělské biotechnologie Specializace: Rostlinné biotechnologie Katedra agroekologie Bakalářská práce Vliv genotypu na obsah rutinu
ORGANICKÉ SLOUČENINY
 ORGANICKÉ SLOUČENINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 7. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci se seznámí se
ORGANICKÉ SLOUČENINY Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 12. 7. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci se seznámí se
Studijní program: Analytická a forenzní chemie
 Studijní program: Analytická a forenzní chemie Studijní program: Analytická a forenzní chemie První rok je studium společné a dělí se až od druhého roku na specializace Specializace 1: Analytická chemie,
Studijní program: Analytická a forenzní chemie Studijní program: Analytická a forenzní chemie První rok je studium společné a dělí se až od druhého roku na specializace Specializace 1: Analytická chemie,
Stereochemie. Přednáška 6
 Stereochemie Přednáška 6 Stereoheterotopické ligandy a NMR spektroskopie Stereoheterotopické ligandy a NMR spektroskopie NMR může rozlišit atomy v odlišném okolí stíněny jinou měrou rozdíl v chemických
Stereochemie Přednáška 6 Stereoheterotopické ligandy a NMR spektroskopie Stereoheterotopické ligandy a NMR spektroskopie NMR může rozlišit atomy v odlišném okolí stíněny jinou měrou rozdíl v chemických
OPVK CZ.1.07/2.2.00/
 18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
Laboratorní práce č. 1: Přibližné určení průměru molekuly kyseliny olejové
 Přírodní vědy moderně a interaktivně FYZIKA 4. ročník šestiletého a 2. ročník čtyřletého studia Laboratorní práce č. 1: Přibližné určení průměru molekuly kyseliny olejové ymnázium Přírodní vědy moderně
Přírodní vědy moderně a interaktivně FYZIKA 4. ročník šestiletého a 2. ročník čtyřletého studia Laboratorní práce č. 1: Přibližné určení průměru molekuly kyseliny olejové ymnázium Přírodní vědy moderně
N A = 6,023 10 23 mol -1
 Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
Pro vyjadřování množství látky se v chemii zavádí veličina látkové množství. Značí se n, jednotkou je 1 mol. Látkové množství je jednou ze základních veličin soustavy SI. Jeden mol je takové množství látky,
Indentifikace molekul a kvantitativní analýza pomocí MS
 Indentifikace molekul a kvantitativní analýza pomocí MS Identifikace molekul snaha určit molekulovou hmotnost, sumární složení, strukturní části molekuly (funkční skupiny, aromatická jádra, alifatické
Indentifikace molekul a kvantitativní analýza pomocí MS Identifikace molekul snaha určit molekulovou hmotnost, sumární složení, strukturní části molekuly (funkční skupiny, aromatická jádra, alifatické
Třídění látek. Chemie 1.KŠPA
 Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
NMR spektrometr. Interpretace NMR spektra
 N (R)--propylpiperidin C N (S)--propylpiperidin C ( bod) Pon vadž se jedná o chirální organickou bázi, bylo by možné ji rozšt pit na izomery krystalizací vínan, pop ípad kafr-0-sulfonát. C C (7,7-dimethylbicyklo[..]hept--yl)methansulfonová
N (R)--propylpiperidin C N (S)--propylpiperidin C ( bod) Pon vadž se jedná o chirální organickou bázi, bylo by možné ji rozšt pit na izomery krystalizací vínan, pop ípad kafr-0-sulfonát. C C (7,7-dimethylbicyklo[..]hept--yl)methansulfonová
12.NMR spektrometrie při analýze roztoků
 Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 12.NMR spektrometrie při analýze roztoků Pavel Matějka pavel.matejka@vscht.cz pavel.matejka@gmail.com 12.NMR spektrometrie při analýze
Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti 12.NMR spektrometrie při analýze roztoků Pavel Matějka pavel.matejka@vscht.cz pavel.matejka@gmail.com 12.NMR spektrometrie při analýze
Pokročilé cvičení z fyzikální chemie KFC/POK2 Vibrační spektroskopie
 Pokročilé cvičení z fyzikální chemie KFC/POK2 Vibrační spektroskopie Vibrace molekul mohou být měřeny buď pomocí absorpce infračerveného záření, nebo pomocí neelastického rozptylu záření, tzn. Ramanova
Pokročilé cvičení z fyzikální chemie KFC/POK2 Vibrační spektroskopie Vibrace molekul mohou být měřeny buď pomocí absorpce infračerveného záření, nebo pomocí neelastického rozptylu záření, tzn. Ramanova
Aminy a další dusíkaté deriváty
 Aminy a další dusíkaté deriváty Aminy jsou sloučeniny příbuzné amoniaku, u kterých jsou nahrazeny jeden, dva nebo všechny tři atomy vodíku alkylovými nebo arylovými skupinami. Aminy mají stejně jako amoniak,
Aminy a další dusíkaté deriváty Aminy jsou sloučeniny příbuzné amoniaku, u kterých jsou nahrazeny jeden, dva nebo všechny tři atomy vodíku alkylovými nebo arylovými skupinami. Aminy mají stejně jako amoniak,
Nukleární Overhauserův efekt (NOE)
 Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
ZÁKLADY SPEKTROMETRIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE
 ZÁKLADY SPEKTROMETRIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Co to je NMR? nedestruktivní spektroskopická metoda využívající magnetických vlastností atomových jader ke studiu struktury molekul metoda č.1 pro určování
ZÁKLADY SPEKTROMETRIE NUKLEÁRNÍ MAGNETICKÉ REZONANCE Co to je NMR? nedestruktivní spektroskopická metoda využívající magnetických vlastností atomových jader ke studiu struktury molekul metoda č.1 pro určování
Základy NMR 2D spektroskopie
 Základy NMR 2D spektroskopie Jaroslav Kříž Ústav makromolekulární chemie AV ČR v.v.i. puls 1D : d 1 Fourierova transformace časového rozvoje odezvy dá 1D spektrum 2D: d 1 d 1 d 1 d 0 d 0 + in 0 d 0 + 2in
Základy NMR 2D spektroskopie Jaroslav Kříž Ústav makromolekulární chemie AV ČR v.v.i. puls 1D : d 1 Fourierova transformace časového rozvoje odezvy dá 1D spektrum 2D: d 1 d 1 d 1 d 0 d 0 + in 0 d 0 + 2in
Molekulární krystal vazebné poměry. Bohumil Kratochvíl
 Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
OPVK CZ.1.07/2.2.00/
 OPVK CZ.1.07/2.2.00/28.0184 Základní principy vývoje nových léčiv OCH/ZPVNL Mgr. Radim Nencka, Ph.D. ZS 2012/2013 Molekulární interakce SAR Možné interakce jednotlivých funkčních skupin 1. Interakce alkoholů
OPVK CZ.1.07/2.2.00/28.0184 Základní principy vývoje nových léčiv OCH/ZPVNL Mgr. Radim Nencka, Ph.D. ZS 2012/2013 Molekulární interakce SAR Možné interakce jednotlivých funkčních skupin 1. Interakce alkoholů
Opakování učiva organické chemie Smart Board
 Opakování učiva organické chemie Smart Board VY_52_INOVACE_200 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie ročník: 9 Projekt EU peníze školám Operačního programu Vzdělávání pro konkurenceschopnost
Opakování učiva organické chemie Smart Board VY_52_INOVACE_200 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie ročník: 9 Projekt EU peníze školám Operačního programu Vzdělávání pro konkurenceschopnost
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Sešit pro laboratorní práci z chemie téma: Příprava roztoků a měření ph autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie a chemie registrační
Analýza směsí, kvantitativní NMR spektroskopie a využití NMR spektroskopie ve forenzní analýze
 Analýza směsí, kvantitativní NMR spektroskopie a využití NMR spektroskopie ve forenzní analýze Analýza směsí a kvantitativní NMR NMR spektrum čisté látky je lineární kombinací spekter jejích jednotlivých
Analýza směsí, kvantitativní NMR spektroskopie a využití NMR spektroskopie ve forenzní analýze Analýza směsí a kvantitativní NMR NMR spektrum čisté látky je lineární kombinací spekter jejích jednotlivých
Organická chemie 3.ročník studijního oboru - kosmetické služby.
 Organická chemie 3.ročník studijního oboru - kosmetické služby. T-6 ALKANY Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu: CZ.1.07/1.5.00/34.0639 ŠABLONA III / 2
Organická chemie 3.ročník studijního oboru - kosmetické služby. T-6 ALKANY Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu: CZ.1.07/1.5.00/34.0639 ŠABLONA III / 2
Klinická a farmaceutická analýza. Petr Kozlík Katedra analytické chemie
 Klinická a farmaceutická analýza Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz http://web.natur.cuni.cz/~kozlik/ 1 Spojení separačních technik s hmotnostní spektrometrem Separační
Klinická a farmaceutická analýza Petr Kozlík Katedra analytické chemie e-mail: kozlik@natur.cuni.cz http://web.natur.cuni.cz/~kozlik/ 1 Spojení separačních technik s hmotnostní spektrometrem Separační
Škola: Gymnázium, Brno, Slovanské náměstí 7 III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT Inovace výuky na GSN prostřednictvím ICT
 Škola: Gymnázium, Brno, Slovanské náměstí 7 Šablona: Název projektu: Číslo projektu: Autor: Tematická oblast: Název DUMu: Kód: III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT Inovace výuky na GSN
Škola: Gymnázium, Brno, Slovanské náměstí 7 Šablona: Název projektu: Číslo projektu: Autor: Tematická oblast: Název DUMu: Kód: III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT Inovace výuky na GSN
Látkové množství. 6,022 10 23 atomů C. Přípravný kurz Chemie 07. n = N. Doporučená literatura. Látkové množství n. Avogadrova konstanta N A
 Doporučená literatura Přípravný kurz Chemie 2006/07 07 RNDr. Josef Tomandl, Ph.D. Mailto: tomandl@med.muni.cz Předmět: Přípravný kurz chemie J. Vacík a kol.: Přehled středoškolské chemie. SPN, Praha 1990,
Doporučená literatura Přípravný kurz Chemie 2006/07 07 RNDr. Josef Tomandl, Ph.D. Mailto: tomandl@med.muni.cz Předmět: Přípravný kurz chemie J. Vacík a kol.: Přehled středoškolské chemie. SPN, Praha 1990,
Charakteristika Teorie kyselin a zásad. Příprava kyselin Vlastnosti + typické reakce. Významné kyseliny. Arrheniova teorie Teorie Brönsted-Lowryho
 Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
KARBOXYLOVÉ KYSELINY
 LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
LABORATORNÍ PRÁCE Č. 28 KARBOXYLOVÉ KYSELINY PRINCIP Karboxylové kyseliny jsou látky, které ve své molekule obsahují jednu nebo více karboxylových skupin. Odvozují se od nich dva typy derivátů, substituční
Ověření možnosti zpracování rašeliny pomocí termické depolymerizace
 Ověření možnosti zpracování rašeliny pomocí termické depolymerizace Ing. Libor Baraňák Ph.D., ENRESS s.r.o Praha, doc. RNDr. Miloslav Bačiak Ph.D., ENRESS s.r.o Praha, Jaroslav Pátek ENRESS s.r.o Praha
Ověření možnosti zpracování rašeliny pomocí termické depolymerizace Ing. Libor Baraňák Ph.D., ENRESS s.r.o Praha, doc. RNDr. Miloslav Bačiak Ph.D., ENRESS s.r.o Praha, Jaroslav Pátek ENRESS s.r.o Praha
EU peníze středním školám digitální učební materiál
 EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
Hmotnostní spektrometrie. Historie MS. Schéma MS
 Hmotnostní spektrometrie MS mass spectrometry MS je analytická technika, která se používá k měření poměru hmotnosti ku náboji (m/z) u iontů původně studium izotopového složení dnes dynamicky se vyvíjející
Hmotnostní spektrometrie MS mass spectrometry MS je analytická technika, která se používá k měření poměru hmotnosti ku náboji (m/z) u iontů původně studium izotopového složení dnes dynamicky se vyvíjející
1. ročník Počet hodin
 SOUSTAVY LÁTEK A JEJICH SLOŽENÍ rozdělení přírodních látek a vlastnosti chemických látek soustavy látek a jejich složení STAVBA ATOMU historie pohledu na atom složení a struktura atomu stavba atomu VELIČINY
SOUSTAVY LÁTEK A JEJICH SLOŽENÍ rozdělení přírodních látek a vlastnosti chemických látek soustavy látek a jejich složení STAVBA ATOMU historie pohledu na atom složení a struktura atomu stavba atomu VELIČINY
Organická chemie 3.ročník studijního oboru - kosmetické služby.
 Organická chemie 3.ročník studijního oboru - kosmetické služby. T-7 Funkční a substituční deriváty karboxylových kyselin Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu:
Organická chemie 3.ročník studijního oboru - kosmetické služby. T-7 Funkční a substituční deriváty karboxylových kyselin Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu:
Sešit pro laboratorní práci z chemie
 Sešit pro laboratorní práci z chemie téma: Důkaz C, H, N a halogenů v organických sloučeninách autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie
Sešit pro laboratorní práci z chemie téma: Důkaz C, H, N a halogenů v organických sloučeninách autor: ing. Alena Dvořáková vytvořeno při realizaci projektu: Inovace školního vzdělávacího programu biologie
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
HMOTNOSTNÍ SPEKTROMETRIE - kvalitativní i kvantitativní detekce v GC a LC - pyrolýzní hmotnostní spektrometrie - analýza polutantů v životním
 HMOTNOSTNÍ SPEKTROMETRIE - kvalitativní i kvantitativní detekce v GC a LC - pyrolýzní hmotnostní spektrometrie - analýza polutantů v životním prostředí - farmakokinetické studie - kvantifikace proteinů
HMOTNOSTNÍ SPEKTROMETRIE - kvalitativní i kvantitativní detekce v GC a LC - pyrolýzní hmotnostní spektrometrie - analýza polutantů v životním prostředí - farmakokinetické studie - kvantifikace proteinů
