VÁŠ PRŮVODCE PRO PŘÍPRAVEK
|
|
|
- Lucie Staňková
- před 9 lety
- Počet zobrazení:
Transkript
1 VÁŠ PRŮVODCE PRO PŘÍPRAVEK EYLEA se používá k léčbě poruchy zraku způsobené makulárním edémem v důsledku okluze centrální retinální žíly (CRVO) Tento léčivý přípravek podléhá dalšímu sledování. Další informace a podrobnosti o přípravku EYLEA jsou uvedeny v příbalové informaci.
2 Vaše klinika/nemocnice:... Kontakt:... Telefon:... Adresa:
3 Vítá Vás průvodce přípravkem EYLEA. Lékař Vám předepsal přípravek EYLEA, protože u Vás byla diagnostikována okluze centrální retinální žíly neboli CRVO. Jedná se o onemocnění, které způsobuje zhoršení zraku. Léčba přípravkem EYLEA může pomoci zastavit zhoršování zraku a může zlepšit některé z příznaků, kterými trpíte. Tato brožura obsahuje také zvukové CD se všemi informacemi uvedenými v brožuře. Ať už si tuto příručku přečtete nebo se rozhodnete poslechnout CD, informace Vám mají pomoci zodpovědět jakékoli otázky, které můžete mít, abyste získali maximum z léčby. 3
4 V TÉTO BROŽUŘE NALEZNETE: Informace, které Vám pomohou porozumět onemocnění CRVO Co je CRVO? Co můžete očekávat od léčby přípravkem EYLEA Co je přípravek EYLEA? Kdo může být přípravkem EYLEA léčen? Jak se mám připravit na podání přípravku EYLEA? Co mohu očekávat na návštěvě spojené s podáním přípravku EYLEA? Pokud mám obavy nebo otázky? Jak pečovat o oči po aplikaci přípravku EYLEA Co mohu očekávat po podání přípravku EYLEA? Kdy mám přijít na další návštěvu? Možné nežádoucí účinky Také zde naleznete užitečné připomenutí návštěv, které Vám pomůže udržovat přehled o léčbě přípravkem EYLEA. 4
5 CO JE CRVO? Okluze centrální retinální žíly je onemocnění, které poškozuje zrak v důsledku bránění toku krve k sítnici v zadní části oka a zpět. Sítnice je místo, kde se vytváří všechny obrazy, které vidíte. Sítnice pracuje podobně jako film v kameře. Blokáda zamezuje toku krve do sítnice a zpět, což může poškodit zrak a případně vést ke slepotě a bolestem oka. U mnoha lidí s CRVO není možné zjistit jednoznačnou příčinu, ale často vzniká jako důsledek jiných onemocnění, jako je glaukom (zelený zákal), hypertenze (vysoký krevní tlak) nebo diabetes (cukrovka). Nejlepší, co můžete dělat pro ochranu zraku, je řídit se radami svého očního lékaře a ujistit se, že dodržujete všechny plánované návštěvy. CO JE PŘÍPRAVEK EYLEA? EYLEA je léčivý přípravek patřící do skupiny tzv. anti- VEGF přípravků, tj. přípravků blokujících účinek vaskulárního endoteliálního růstového faktoru, což je protein nutný pro tvorbu nových cév v oku. EYLEA brání tvorbě slabých krevních cév, což může pomoci zlepšit zrak nebo zastavit jeho zhoršování. 5
6 Přípravek EYLEA je roztok (tekutina), který se podává injekčně do oka. Je pochopitelné mít obavy z podání injekce. Nicméně většina lidí, kteří podstoupili léčbu přípravkem EYLEA, uvádí, že injekce je bezbolestná a představa o injekci je horší, než jaká injekce ve skutečnosti je. KDO MŮŽE BÝT PŘÍPRAVKEM EYLEA LÉČEN? Přípravek EYLEA je určen pro pacienty s onemocněním CRVO. Před léčbou přípravkem EYLEA se ujistěte, že jste informoval/a lékaře nebo zdravotní sestru, pokud: máte infekci v oku nebo v jeho okolí máte v současné době zarudnutí oka nebo cítíte jakoukoli bolest v oku domníváte se, že můžete být alergický/á na jód, jakékoli léky proti bolesti nebo jakoukoli složku přípravku EYLEA měl/a jste v minulosti jakékoli potíže v souvislosti s podáním injekce do oka máte glaukom (zelený zákal) nebo jste měl/a v minulosti vysoký nitrooční tlak vidíte nebo jste v minulosti viděl/a záblesky světla nebo vločky v zorném poli užíváte jakékoli léky, na lékařský předpis nebo bez něj 6
7 jste těhotná, plánujete otěhotnět nebo kojíte. Nejsou žádné zkušenosti s používáním přípravku EYLEA u těhotných žen. EYLEA se nemá užívat během těhotenství. Před léčbou přípravkem EYLEA se poraďte se svým lékařem. Ženy v plodném věku musí užívat účinnou antikoncepci v průběhu léčby a minimálně tři měsíce po poslední injekci přípravku EYLEA. podstoupil/a jste nebo plánujete podstoupit chirurgický zákrok na oku v období 4 týdny před nebo po léčbě přípravkem EYLEA Přípravek EYLEA by neměl být podáván, pokud: máte aktivní závažnou infekci v oku nebo v jeho okolí jste alergický/á na aflibercept nebo jakoukoli pomocnou složku přípravku EYLEA JAK SE MÁM PŘIPRAVIT NA PODÁNÍ PŘÍPRAVKU EYLEA? Lékař Vás může požádat, abyste několik dnů před podáním injekce používal/a oční kapky. Po podání injekce můžete vidět rozmazaně a tak byste neměl/a cestou domů řídit. Požádejte o doprovod přítele nebo rodinného příslušníka nebo si zajistěte jiný způsob, jak se dostavit na podání injekce a zpátky domů. V den léčby nepoužívejte žádný make-up. 7
8 CO MOHU OČEKÁVAT NA NÁVŠTĚVĚ SPOJENÉ S PODÁNÍM PŘÍPRAVKU EYLEA? Lékař nebo sestra Vás připraví na podání přípravku EYLEA. Tyto osoby jsou vysoce kvalifikovaní odborníci se zkušeností s léčbou CRVO. Chápou, že způsob léčby může vyvolat obavy a zajistí, abyste byl/a relaxovaná/ý a cítil/a se pohodlně. Budou Vám podány oční kapky, které působí jako lokální anestetikum a oko s jeho okolím bude vyčištěno. Obličej bude překrytý speciální rouškou a oko bude přidržené otevřené. Kapky lokálního anestetika mohou kromě znecitlivění způsobit i rozostření zraku a může se stát, že neuvidíte injekční jehlu. Zkušený lékař aplikuje injekci do bělimy (bílá část) oka. Většina lidí říká, že injekce je bezbolestná a někteří říkají, že cítí mírný tlak. Celý postup je trochu nepříjemný, ale trvá jen několik minut. POKUD MÁM OBAVY NEBO OTÁZKY? Pokud máte jakékoli obavy nebo otázky, je nejlepší obrátit se na svého lékaře nebo zdravotní sestru. Jsou velmi zkušení a znají Vaši osobní situaci a tak Vám mohou zodpovědět všechny Vaše dotazy. 8
9 Pamatujte si, že lékař nebo zdravotní sestra jsou ty nejvhodnější osoby, které Vám poskytnou informace o léčbě. Neobávejte se klást otázky nebo vyjádřit jakékoli obavy. Lékař nebo zdravotní sestra Vám poskytnou odpovědi a ujištění. CO MOHU OČEKÁVAT PO PODÁNÍ PŘÍPRAVKU EYLEA? Po aplikaci injekce může lékař provést některá oční vyšetření. Ta mohou zahrnovat fouknutí vzduchu do oka, kterým se měří tlak uvnitř oka. Po podání injekce budete vidět rozmazaně a proto byste neměl/a plánovat řízení, dokud nedojde k úpravě vidění. V několika následujících dnech může dojít k zarudnutí oka nebo budete vidět pohybující se skvrny v zorném poli. Oba z těchto příznaků by se měly upravit během několika dní. Pokud nedojde k úpravě anebo dojde ke zhoršení, kontaktujte lékaře. Někteří lidé mohou po podání injekce cítit mírnou bolest nebo nepříjemný pocit v oku. Pokud bolest nebo jiné obtíže neodezní nebo dojde ke zhoršení, kontaktujte lékaře. 9
10 KDY MÁM PŘIJÍT NA DALŠÍ NÁVŠTĚVU? Lékař s Vámi naplánuje další návštěvu. Před ukončením léčby přípravkem EYLEA si promluvte se svým lékařem. Když se objednáte na další návštěvu, nezapomeňte si ji pro připomenutí zaznamenat na zadní stranu obálky. MOŽNÉ NEŽÁDOUCÍ ÚČINKY Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Při podávání přípravku EYLEA se mohou projevit některé nežádoucí účinky, které jsou spojovány s injekčním podáním. Některé mohou být závažné a zahrnují: infekci uvnitř oka (endoftalmitida) zakalení čočky (šedý zákal) odloučení gelové hmoty uvnitř oka od sítnice (odloučení sklivce) Tyto závažné nežádoucí účinky mohou postihnout až 1 ze 100 pacientů. Pokud se u Vás objeví infekce uvnitř oka nebo další komplikace, můžete zaznamenat: 10
11 bolest oka nebo nepříjemný pocit, zhoršení zarudnutí oka, rozmazané nebo snížené vidění, zvýšení citlivosti na světlo, méně jasné linie a tvary, stíny a změny barevného vidění, náhlé záblesky světla a výskyt nebo zvýšení počtu sklivcových vloček, zastření části zorného pole, nevolnost a zvracení. Je důležité, aby byly příznaky diagnostikovány a léčeny co možná nejdříve. Pokud se u Vás vyskytne jakýkoli náznak těchto příznaků, kontaktujte, prosím, okamžitě svého lékaře. Nejčastějšími nežádoucími účinky jsou: překrvení oka způsobené krvácením z drobných cév ve vnějších vrstvách oka (krvácení do spojivek), bolest oka, odloučení gelovité látky uvnitř oka od sítnice (odloučení sklivce), zakalení čočky (katarakta), pohybující se skvrny v zorném poli (sklivcové vločky), zvýšení nitroočního tlaku. 11
12 Dále je uveden seznam dalších nežádoucích účinků, které byly zaznamenány a u kterých je možné předpokládat, že souvisely s injekcí nebo lékem. Pokud se u Vás vyskytne jakýkoli náznak těchto příznaků, kontaktujte, prosím, okamžitě svého lékaře. Časté (mohou postihnout až 1 z 10 osob): snížení ostrosti zraku (trhlina v pigmentovém epitelu sítnice, odchlípení pigmentového epitelu sítnice)* porucha zraku (degenerace sítnice) krvácení v oku (krvácení do sklivce) určitá forma zakalení čočky (katarakta, katarakta nukleární, katarakta subkapsulární) poškození povrchu oční koule (eroze rohovky, poškrábání rohovky) zvýšení tlaku v oku (zvýšení nitroočního tlaku) rozmazané vidění pohybující se skvrny v zorném poli (sklivcové vločky) otok povrchu oční koule (otok rohovky) odchlípení gelovité hmoty uvnitř oka od sítnice (odchlípení sklivce) bolest v místě aplikace injekce pocit něčeho v oku (pocit cizího tělesa v oku) zvýšená tvorba slz (zvýšené slzení) *) Onemocnění, o kterých je známo, že souvisí s VPMD; pozorované pouze u pacientů s vlhkou formou VPMD. 12
13 otok očního víčka (edém očního víčka) krvácení v místě vpichu injekce (hemorrhagie v místě vpichu injekce) zarudnutí oka (konjunktivální hyperemie, okulární hyperemie) Méně časté (mohou postihnout až 1 ze 100 osob): alergické reakce (hypersenzitivita) zánět uvnitř oka (endoftalmitida) snížení zrakové ostrosti (odchlípení sítnice, trhlina v sítnici) zánět duhovky oka (iritida) zánět určitých částí oka (iridocyklitida, zarudnutí přední komory) určité formy zakalení čočky (kortikální katarakta, lentikulární opacity) poškození vrchní vrstvy oční koule (defekt korneálního epitelu) podráždění v místě aplikace injekce neobvyklé pocity v oku (podráždění očního víčka) Vzácné (mohou postihnout až 1 z osob): zánět uvnitř oka (endoftalmitida) zánět určitých částí oka (vitritida, uveitida) hnis v oku (hypopyon) 13
14 V klinických studiích byl u pacientů, kteří užívali přípravky na ředění krve, zaznamenán zvýšený výskyt krvácení z malých krevních cév ve vnější vrstvě oka (krvácení do spojivek). Frekvence výskytu těchto příhod byla mezi pacienty, kteří byli léčeni ranibizumabem, a pacienty, kteří byli léčeni přípravkem EYLEA srovnatelná. Používání systémových inhibitorů VEGF, látek podobných látce v přípravku EYLEA, může souviset s rizikem arteriálních tromboembolických příhod (krevní sraženiny blokující krevní cévy), které mohou vést k srdečnímu infarktu nebo cévní mozkové příhodě. Existuje teoretické riziko takových příhod po podání injekce přípravku EYLEA do oka. Kontaktujte co nejdříve svého lékaře, pokud cítíte zvětšující se bolest oka, dojde ke zhoršení zarudnutí, vidíte rozmazaně nebo hůř anebo jste více citlivý/á na světlo. Kontaktujte okamžitě svého lékaře, pokud se u Vás vyskytne jakýkoli náznak těchto příznaků: bolest na hrudníku, dušnost, pocení, nevolnost, bolest hlavy, zvracení, slabost nebo ochabnutí svalů (obzvláště na jedné straně), setřelá řeč nebo poruchy vidění. Úplný seznam nežádoucích účinků naleznete v příbalové informaci pro pacienta, která je přiložena k této brožuře. Pokud si myslíte, že můžete mít nežádoucí účinky v souvislosti s Vaší léčbou, řekněte to lékaři. 14
15 PŘÍSLUŠNÉ MÍSTNÍ BEZPEČNOSTNÍ INFORMACE Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Hlášení nežádoucích účinků Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v tomto edukačním materiálu. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48, Praha 10 Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku. Nežádoucí účinky mohou být hlášeny také na: Tel : Fax : pharmacovigilance.czech@bayer.com BAYER s. r. o., Siemensova 2717/4, Praha
16 BAYER s. r. o. Siemensova 2717/ Praha 5 CZ/1.0/
VÁŠ PRŮVODCE PRO PŘÍPRAVEK. (aflibercept solution for injection)
 VÁŠ PRŮVODCE PRO PŘÍPRAVEK Před zahájením léčby přípravkem EYLEA si, prosím, pečlivě přečtěte celý tento informační materiál, včetně přiložené příbalové informace pro pacienta a poslechněte si zvukové
VÁŠ PRŮVODCE PRO PŘÍPRAVEK Před zahájením léčby přípravkem EYLEA si, prosím, pečlivě přečtěte celý tento informační materiál, včetně přiložené příbalové informace pro pacienta a poslechněte si zvukové
VÁŠ PRŮVODCE PRO PŘÍPRAVEK EYLEA. EYLEA se používá k léčbě poruchy zraku způsobené diabetickým makulárním edémem (DME)
 VÁŠ PRŮVODCE PRO PŘÍPRAVEK EYLEA EYLEA se používá k léčbě poruchy zraku způsobené diabetickým makulárním edémem (DME) Tento léčivý přípravek podléhá dalšímu sledování. Další informace a podrobnosti o přípravku
VÁŠ PRŮVODCE PRO PŘÍPRAVEK EYLEA EYLEA se používá k léčbě poruchy zraku způsobené diabetickým makulárním edémem (DME) Tento léčivý přípravek podléhá dalšímu sledování. Další informace a podrobnosti o přípravku
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Eylea 40 mg/ml injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 mililitr injekčního roztoku obsahuje 40
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Eylea 40 mg/ml injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 mililitr injekčního roztoku obsahuje 40
Eylea. afliberceptum. Co je Eylea? K čemu se přípravek Eylea používá? Souhrn zprávy EPAR určený pro veřejnost
 EMA/677928/2015 EMEA/H/C/002392 Souhrn zprávy EPAR určený pro veřejnost afliberceptum Tento dokument je souhrnem Evropské veřejné zprávy o hodnocení (European public assessment report, EPAR) pro přípravek.
EMA/677928/2015 EMEA/H/C/002392 Souhrn zprávy EPAR určený pro veřejnost afliberceptum Tento dokument je souhrnem Evropské veřejné zprávy o hodnocení (European public assessment report, EPAR) pro přípravek.
Příbalová informace: informace pro pacienta. Latalux 50 mikrogramů/ml oční kapky, roztok Latanoprostum
 Sp. zn. sukls136408/2014 Příbalová informace: informace pro pacienta Latalux 50 mikrogramů/ml oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp. zn. sukls136408/2014 Příbalová informace: informace pro pacienta Latalux 50 mikrogramů/ml oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Adriblastina CS injekční roztok 2 mg/ml doxorubicini hydrochloridum
 Příbalová informace: informace pro uživatele Adriblastina CS injekční roztok 2 mg/ml doxorubicini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro uživatele Adriblastina CS injekční roztok 2 mg/ml doxorubicini hydrochloridum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Příbalová informace: informace pro pacienta. Fredomat 40 mikrogramů/ml oční kapky, roztok. travoprostum
 sp.zn.sukls190238/2015 Příbalová informace: informace pro pacienta Fredomat 40 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls190238/2015 Příbalová informace: informace pro pacienta Fredomat 40 mikrogramů/ml oční kapky, roztok travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Xaloptic 0,005% (0,05 mg/ml), oční kapky, roztok. Latanoprostum
 Sp.zn. sukls116684/2014 Příbalová informace: informace pro uživatele Xaloptic 0,005% (0,05 mg/ml), oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete užívat
Sp.zn. sukls116684/2014 Příbalová informace: informace pro uživatele Xaloptic 0,005% (0,05 mg/ml), oční kapky, roztok Latanoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete užívat
DESFERAL prášek pro přípravu injekčního roztoku (deferoxamini mesilas)
 Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls19458/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DESFERAL prášek pro přípravu injekčního roztoku (deferoxamini mesilas) Přečtěte si pozorně
Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls19458/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DESFERAL prášek pro přípravu injekčního roztoku (deferoxamini mesilas) Přečtěte si pozorně
PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA. FOTIL FOTIL FORTE oční kapky, roztok pilocarpinum hydrochloridum, timololi maleas
 sp.zn. sukls154707/2012 sukls154712/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA FOTIL FOTIL FORTE oční kapky, roztok pilocarpinum hydrochloridum, timololi maleas Přečtěte si pozorně celou příbalovou
sp.zn. sukls154707/2012 sukls154712/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA FOTIL FOTIL FORTE oční kapky, roztok pilocarpinum hydrochloridum, timololi maleas Přečtěte si pozorně celou příbalovou
Váš průvodce léčbou poškození zraku způsobeného makulárním edémem v důsledku okluze retinální žíly (RVO) přípravkem Lucentis (ranibizumab)
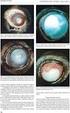 Váš průvodce léčbou poškození zraku způsobeného makulárním edémem v důsledku okluze retinální žíly (RVO) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit
Váš průvodce léčbou poškození zraku způsobeného makulárním edémem v důsledku okluze retinální žíly (RVO) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit
sp.zn.sukls192314/2011
 sp.zn.sukls192314/2011 Příbalová informace: Informace pro uživatele Optipres 20 mg/ml oční kapky, roztok dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
sp.zn.sukls192314/2011 Příbalová informace: Informace pro uživatele Optipres 20 mg/ml oční kapky, roztok dorzolamidum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
ECRITEN 100 mg potahované tablety. Sildenafilum
 Příbalová informace: Informace pro uživatele ECRITEN 100 mg potahované tablety Sildenafilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
Příbalová informace: Informace pro uživatele ECRITEN 100 mg potahované tablety Sildenafilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro
sp.zn.: sukls59875/2012 a k sp.zn.: sukls58444/2012
 sp.zn.: sukls59875/2012 a k sp.zn.: sukls58444/2012 Příbalová informace: informace pro pacienta BETALMIC 0,5% Oční kapky, roztok Betaxololi hydrochloridum Přečtěte si pozorně celou příbalovou informaci
sp.zn.: sukls59875/2012 a k sp.zn.: sukls58444/2012 Příbalová informace: informace pro pacienta BETALMIC 0,5% Oční kapky, roztok Betaxololi hydrochloridum Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele. Ofloxacin-POS 3 mg/ml oční kapky, roztok. Ofloxacinum
 Sp. zn. sukls201848/2013 Příbalová informace: informace pro uživatele Ofloxacin-POS 3 mg/ml oční kapky, roztok Ofloxacinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp. zn. sukls201848/2013 Příbalová informace: informace pro uživatele Ofloxacin-POS 3 mg/ml oční kapky, roztok Ofloxacinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. TEARS NATURALE II oční kapky, roztok dextranum 70, hypromelosum
 sp.zn.sukls29736/2015 Příbalová informace: informace pro uživatele TEARS NATURALE II oční kapky, roztok dextranum 70, hypromelosum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.sukls29736/2015 Příbalová informace: informace pro uživatele TEARS NATURALE II oční kapky, roztok dextranum 70, hypromelosum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro uživatele Engerix-B 20 µg. antigenum tegiminis hepatitidis B injekční suspenze
 sp.zn. sukls204563/2014 Příbalová informace: informace pro uživatele Engerix-B 10 µg Engerix-B 20 µg antigenum tegiminis hepatitidis B injekční suspenze Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls204563/2014 Příbalová informace: informace pro uživatele Engerix-B 10 µg Engerix-B 20 µg antigenum tegiminis hepatitidis B injekční suspenze Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Eylea 40 mg/ml injekční roztok v injekční lahvičce Afliberceptum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Příbalová informace: informace pro uživatele Eylea 40 mg/ml injekční roztok v injekční lahvičce Afliberceptum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Váš průvodce léčbou vlhké (neovaskulární) formy věkem podmíněné makulární degenerace (AMD) přípravkem Lucentis (ranibizumab)
 Váš průvodce léčbou vlhké (neovaskulární) formy věkem podmíněné makulární degenerace (AMD) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu vlhké
Váš průvodce léčbou vlhké (neovaskulární) formy věkem podmíněné makulární degenerace (AMD) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu vlhké
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele XGEVA 120 mg injekční roztok denosumabum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Akistan 50 mikrogramů/ml oční kapky, roztok (latanoprostum)
 Sp. zn. sukls79185/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Akistan 50 mikrogramů/ml oční kapky, roztok (latanoprostum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete používat
Sp. zn. sukls79185/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Akistan 50 mikrogramů/ml oční kapky, roztok (latanoprostum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete používat
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Imlygic 10 6 jednotek tvořících plaky (PFU)/ml injekční roztok Imlygic 10 8 jednotek tvořících plaky (PFU)/ml injekční roztok talimogenum
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Imlygic 10 6 jednotek tvořících plaky (PFU)/ml injekční roztok Imlygic 10 8 jednotek tvořících plaky (PFU)/ml injekční roztok talimogenum
Příbalová informace: informace pro uživatele. Cardilopin 2,5 mg Cardilopin 5 mg Cardilopin 10 mg tablety amlodipinum
 sp.zn. sukls180582/2014 Příbalová informace: informace pro uživatele Cardilopin 2,5 mg Cardilopin 5 mg Cardilopin 10 mg tablety amlodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls180582/2014 Příbalová informace: informace pro uživatele Cardilopin 2,5 mg Cardilopin 5 mg Cardilopin 10 mg tablety amlodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Ebrantil i.v. 25, injekční roztok Ebrantil i.v. 50, injekční roztok urapidilum
 sp.zn. sukls144430/2014 Příbalová informace: informace pro pacienta Ebrantil i.v. 25, injekční roztok Ebrantil i.v. 50, injekční roztok urapidilum Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls144430/2014 Příbalová informace: informace pro pacienta Ebrantil i.v. 25, injekční roztok Ebrantil i.v. 50, injekční roztok urapidilum Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro pacienta. Dermovate 0,5 mg/g krém. Clobetasoli propionas
 Příbalová informace: informace pro pacienta Dermovate 0,5 mg/g krém Clobetasoli propionas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro
Příbalová informace: informace pro pacienta Dermovate 0,5 mg/g krém Clobetasoli propionas Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro
KATORA 25 mg žvýkací tablety KATORA 50 mg žvýkací tablety KATORA 100 mg žvýkací tablety
 Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls103376/2011, sukls103377/2011 a sukls103378/2011 Příbalová informace: informace pro uživatele KATORA 25 mg žvýkací tablety KATORA 50 mg žvýkací tablety
Příloha č. 1 k rozhodnutí o registraci sp.zn. sukls103376/2011, sukls103377/2011 a sukls103378/2011 Příbalová informace: informace pro uživatele KATORA 25 mg žvýkací tablety KATORA 50 mg žvýkací tablety
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls154079/2012
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls154079/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OPTODROP COMBI 2% + 0,5% oční kapky, roztok (dorzolamidi hydrochloridum, timololi maleas)
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.: sukls154079/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OPTODROP COMBI 2% + 0,5% oční kapky, roztok (dorzolamidi hydrochloridum, timololi maleas)
1. Co je přípravek Lipanthyl NT 145 mg a k čemu se používá
 sp.zn.sukls50259/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE LIPANTHYL NT 145 mg potahované tablety fenofibratum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls50259/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE LIPANTHYL NT 145 mg potahované tablety fenofibratum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.: sukls32991/2012 a sp.zn.: sukls148548/2014
 sp.zn.: sukls32991/2012 a sp.zn.: sukls148548/2014 Příbalová informace: Informace pro uživatele TRUSOPT 20 mg/ml, oční kapky, roztok dorzolamidi hydrochloridum Přečtěte si pozorně celou příbalovou informaci
sp.zn.: sukls32991/2012 a sp.zn.: sukls148548/2014 Příbalová informace: Informace pro uživatele TRUSOPT 20 mg/ml, oční kapky, roztok dorzolamidi hydrochloridum Přečtěte si pozorně celou příbalovou informaci
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Voltaren ActiGo Extra
 sp. zn. sukls96703/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Voltaren ActiGo Extra obalené tablety diclofenacum kalicum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
sp. zn. sukls96703/2016 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Voltaren ActiGo Extra obalené tablety diclofenacum kalicum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek
AMFIDOR 50 mg AMFIDOR 100 mg potahované tablety. sildenafilum (ve formě sildenafili citras)
 Sp.zn.sukls206980/2013 Sp.zn.sukls206981/2013 Příbalová informace: informace pro pacienta AMFIDOR 50 mg AMFIDOR 100 mg potahované tablety sildenafilum (ve formě sildenafili citras) Přečtěte si pozorně
Sp.zn.sukls206980/2013 Sp.zn.sukls206981/2013 Příbalová informace: informace pro pacienta AMFIDOR 50 mg AMFIDOR 100 mg potahované tablety sildenafilum (ve formě sildenafili citras) Přečtěte si pozorně
Váš průvodce léčbou poškození zraku v důsledku diabetického makulárního edému (DME) přípravkem Lucentis (ranibizumab)
 Váš průvodce léčbou poškození zraku v důsledku diabetického makulárního edému (DME) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu poškození
Váš průvodce léčbou poškození zraku v důsledku diabetického makulárního edému (DME) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu poškození
Příbalová informace: informace pro uživatele. Clexane forte injekční roztok v předplněné injekční stříkačce enoxaparinum natricum
 sp.zn. sukls78333/2014 Příbalová informace: informace pro uživatele Clexane forte injekční roztok v předplněné injekční stříkačce enoxaparinum natricum Přečtěte si pozorně celou příbalovou informaci dříve,
sp.zn. sukls78333/2014 Příbalová informace: informace pro uživatele Clexane forte injekční roztok v předplněné injekční stříkačce enoxaparinum natricum Přečtěte si pozorně celou příbalovou informaci dříve,
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Kyprolis 60 mg prášek pro infuzní roztok carfilzomibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro pacienta Kyprolis 60 mg prášek pro infuzní roztok carfilzomibum Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Omidria 10 mg/ml + 3 mg/ml, koncentrát pro roztok k nitroočnímu výplachu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čtyři ml roztoku v injekční lahvičce
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Omidria 10 mg/ml + 3 mg/ml, koncentrát pro roztok k nitroočnímu výplachu 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čtyři ml roztoku v injekční lahvičce
Příbalová informace: informace pro uživatele. Micropaque 1 g/ml, gastroenterálni suspenze (pro perorální nebo rektální podáni) Barii sulfas
 sp.zn. sukls218636/2011 Příbalová informace: informace pro uživatele Micropaque 1 g/ml, gastroenterálni suspenze (pro perorální nebo rektální podáni) Barii sulfas Přečtěte si pozorně celou příbalovou informaci
sp.zn. sukls218636/2011 Příbalová informace: informace pro uživatele Micropaque 1 g/ml, gastroenterálni suspenze (pro perorální nebo rektální podáni) Barii sulfas Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro uživatele
 sp. zn. sukls167840/2014 Příbalová informace: informace pro uživatele Priorix inj.stříkačka, prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce Živá atenuovaná vakcína proti spalničkám,
sp. zn. sukls167840/2014 Příbalová informace: informace pro uživatele Priorix inj.stříkačka, prášek a rozpouštědlo pro injekční roztok v předplněné injekční stříkačce Živá atenuovaná vakcína proti spalničkám,
Příbalová informace: informace pro uživatele. Dilatrend 25 tablety Carvedilolum
 sp. zn.: sukls144781/2012 a sp. zn.: sukls88569/2014 Příbalová informace: informace pro uživatele Dilatrend 25 tablety Carvedilolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp. zn.: sukls144781/2012 a sp. zn.: sukls88569/2014 Příbalová informace: informace pro uživatele Dilatrend 25 tablety Carvedilolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls79449/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte
sp.zn. sukls79449/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte
Příbalová informace: informace pro uživatele. Prostavasin prášek pro infuzní roztok Alprostadilum
 Příbalová informace: informace pro uživatele Prostavasin prášek pro infuzní roztok Alprostadilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele Prostavasin prášek pro infuzní roztok Alprostadilum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje
Příbalová informace: informace pro uživatele. GUTTALAX 7,5 mg, perorální kapky, roztok natrii picosulfas
 sp.zn. sukls115768/2009 a sp.zn. sukls226721/2015 Příbalová informace: informace pro uživatele GUTTALAX 7,5 mg, perorální kapky, roztok natrii picosulfas Přečtěte si pozorně tuto příbalovou informaci dříve,
sp.zn. sukls115768/2009 a sp.zn. sukls226721/2015 Příbalová informace: informace pro uživatele GUTTALAX 7,5 mg, perorální kapky, roztok natrii picosulfas Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele
 sp.zn.: sukls236606/2012 Příbalová informace: informace pro uživatele MENJUGATE, prášek a rozpouštědlo pro injekční suspenzi Konjugovaná oligosacharidová vakcína proti meningitidě C Přečtěte si pozorně
sp.zn.: sukls236606/2012 Příbalová informace: informace pro uživatele MENJUGATE, prášek a rozpouštědlo pro injekční suspenzi Konjugovaná oligosacharidová vakcína proti meningitidě C Přečtěte si pozorně
Příbalová informace: informace pro pacienta. Eylea 40 mg/ml injekční roztok v předplněné injekční stříkačce Afliberceptum
 Příbalová informace: informace pro pacienta Eylea 40 mg/ml injekční roztok v předplněné injekční stříkačce Afliberceptum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám bude tento přípravek
Příbalová informace: informace pro pacienta Eylea 40 mg/ml injekční roztok v předplněné injekční stříkačce Afliberceptum Přečtěte si pozorně celou příbalovou informaci dříve, než Vám bude tento přípravek
Příbalová informace: informace pro uživatele. Bisogamma 5 potahované tablety Bisoprololi fumaras
 sp.zn.sukls112700/2015 Příbalová informace: informace pro uživatele Bisogamma 5 potahované tablety Bisoprololi fumaras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn.sukls112700/2015 Příbalová informace: informace pro uživatele Bisogamma 5 potahované tablety Bisoprololi fumaras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro pacienta. ZOXON 2 ZOXON 4 tablety doxazosinum
 sp.zn. sukls97553/2015 Příbalová informace: informace pro pacienta ZOXON 2 ZOXON 4 tablety doxazosinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
sp.zn. sukls97553/2015 Příbalová informace: informace pro pacienta ZOXON 2 ZOXON 4 tablety doxazosinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Váš průvodce léčbou poškození zraku způsobeného makulárním edémem v důsledku okluze retinální žíly (RVO) přípravkem Lucentis (ranibizumab)
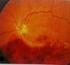 Váš průvodce léčbou poškození zraku způsobeného makulárním edémem v důsledku okluze retinální žíly (RVO) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit
Váš průvodce léčbou poškození zraku způsobeného makulárním edémem v důsledku okluze retinální žíly (RVO) přípravkem Lucentis (ranibizumab) Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit
*Ranibizumab je fragment humanizované monoklonální protilátky produkovaný buňkami Escherichia coli rekombinantní DNA technologií.
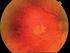 1. NÁZEV PŘÍPRAVKU Lucentis 10 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje 10 mg ranibizumabum*. Jedna injekční lahvička obsahuje 2,3 mg ranibizumabum v 0,23 ml roztoku.
1. NÁZEV PŘÍPRAVKU Lucentis 10 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml obsahuje 10 mg ranibizumabum*. Jedna injekční lahvička obsahuje 2,3 mg ranibizumabum v 0,23 ml roztoku.
Sp. zn. sukls119329/2014, sukls119332/2014, sukls119337/2014, sukls119338/2014, sukls119341/2014, sukls119342/2014, sukls119343/2014, sukls119344/2014
 Sp. zn. sukls119329/2014, sukls119332/2014, sukls119337/2014, sukls119338/2014, sukls119341/2014, sukls119342/2014, sukls119343/2014, sukls119344/2014 Příbalová informace: informace pro uživatele Pregabalin
Sp. zn. sukls119329/2014, sukls119332/2014, sukls119337/2014, sukls119338/2014, sukls119341/2014, sukls119342/2014, sukls119343/2014, sukls119344/2014 Příbalová informace: informace pro uživatele Pregabalin
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Meloxicam Mylan 15 mg tablety meloxicamum
 sp.zn.sukls151971/2012 a k sp.zn.sukls69213/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Meloxicam Mylan 15 mg tablety meloxicamum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn.sukls151971/2012 a k sp.zn.sukls69213/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Meloxicam Mylan 15 mg tablety meloxicamum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
 sp.zn. sukls88228/2014 Příbalová informace: Informace pro uživatele BONEFOS koncentrát pro infuzní roztok (Dinatrii clodronas) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
sp.zn. sukls88228/2014 Příbalová informace: Informace pro uživatele BONEFOS koncentrát pro infuzní roztok (Dinatrii clodronas) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE 22
 PŘÍBALOVÁ INFORMACE 22 Příbalová informace: Informace pro uživatele VELETRI 0,5 mg prášek pro infuzní roztok VELETRI 1,5 mg prášek pro infuzní roztok Epoprostenolum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE 22 Příbalová informace: Informace pro uživatele VELETRI 0,5 mg prášek pro infuzní roztok VELETRI 1,5 mg prášek pro infuzní roztok Epoprostenolum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls115134/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Voltaren ActiGo 12,5 mg potahované tablety diclofenacum kalicum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
sp.zn. sukls115134/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Voltaren ActiGo 12,5 mg potahované tablety diclofenacum kalicum Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 sp.zn. sukls79449/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte
sp.zn. sukls79449/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn. sukls73712/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Bimican 0,3 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje bimatoprostum 0,3 mg. Jedna kapka
Sp.zn. sukls73712/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Bimican 0,3 mg/ml oční kapky, roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml roztoku obsahuje bimatoprostum 0,3 mg. Jedna kapka
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE. TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum
 PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
PŘÍBALOVÁ INFORMACE-INFORMACE PRO UŽIVATELE TRAVATAN 40 mikrogramů/ml oční kapky, roztok Travoprostum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat. Ponechte
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Temomedac 5 mg tvrdé tobolky Temomedac 20 mg tvrdé tobolky Temomedac 100 mg tvrdé tobolky Temomedac 140 mg tvrdé tobolky Temomedac 180 mg tvrdé tobolky Temomedac
Příbalová informace: informace pro uživatele Temomedac 5 mg tvrdé tobolky Temomedac 20 mg tvrdé tobolky Temomedac 100 mg tvrdé tobolky Temomedac 140 mg tvrdé tobolky Temomedac 180 mg tvrdé tobolky Temomedac
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls194490/2009
 Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls194490/2009 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE AMFIDOR 50 mg potahované tablety sildenafilum (ve formě sildenafili citras) Přečtěte si pozorně
Příloha č. 2 k rozhodnutí o registraci sp.zn. sukls194490/2009 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE AMFIDOR 50 mg potahované tablety sildenafilum (ve formě sildenafili citras) Přečtěte si pozorně
INFORMACE PRO PŘEDEPISUJÍCÍHO LÉKAŘE
 Injekce do sklivce Doporučení pro léčbu přípravkem INFORMACE PRO PŘEDEPISUJÍCÍHO LÉKAŘE Tento léčivý přípravek podléhá dalšímu sledování. Další informace a podrobnosti o přípravku EYLEA jsou uvedeny v
Injekce do sklivce Doporučení pro léčbu přípravkem INFORMACE PRO PŘEDEPISUJÍCÍHO LÉKAŘE Tento léčivý přípravek podléhá dalšímu sledování. Další informace a podrobnosti o přípravku EYLEA jsou uvedeny v
160330_v17.0_Vidaza_PI_CS_PRINT B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 27 Příbalová informace: informace pro uživatele Vidaza 25 mg/ml prášek pro injekční suspenzi Azacitidinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
B. PŘÍBALOVÁ INFORMACE 27 Příbalová informace: informace pro uživatele Vidaza 25 mg/ml prášek pro injekční suspenzi Azacitidinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Amiptic 20mg/ml + 5mg/ml oční kapky, roztok dorzolamidum/timololum
 sp.zn.sukls55072/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Amiptic 20mg/ml + 5mg/ml oční kapky, roztok dorzolamidum/timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.sukls55072/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Amiptic 20mg/ml + 5mg/ml oční kapky, roztok dorzolamidum/timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cosopt FREE bez konzervačních přísad 20 mg/ml + 5 mg/ml oční kapky, roztok, jednodávkový obal (dorzolamidum / timololum) Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Cosopt FREE bez konzervačních přísad 20 mg/ml + 5 mg/ml oční kapky, roztok, jednodávkový obal (dorzolamidum / timololum) Přečtěte si pozorně celou příbalovou
sp.zn. sukls66229/2015 Příbalová informace: informace pro uživatele
 sp.zn. sukls66229/2015 Příbalová informace: informace pro uživatele Iomeron 150, injekční roztok Iomeron 200, injekční roztok Iomeron 250, injekční roztok Iomeron 300, injekční roztok Iomeron 350, injekční
sp.zn. sukls66229/2015 Příbalová informace: informace pro uživatele Iomeron 150, injekční roztok Iomeron 200, injekční roztok Iomeron 250, injekční roztok Iomeron 300, injekční roztok Iomeron 350, injekční
Příbalová informace: informace pro pacienta. Milurit 100 Milurit 300 tablety allopurinolum
 sp. zn. sukls107451/2015 a sukls107472/2015 Příbalová informace: informace pro pacienta Milurit 100 Milurit 300 tablety allopurinolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp. zn. sukls107451/2015 a sukls107472/2015 Příbalová informace: informace pro pacienta Milurit 100 Milurit 300 tablety allopurinolum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Vyrůstat s důvěrou Informace o nedostatku IGF-1 a jak může pomoci Increlex
 Vyrůstat s důvěrou Informace o nedostatku IGF-1 a jak může pomoci Increlex Úvod Rodiče, pacienti, ošetřovatelé odpovědi na Vaše otázky Pro Vás jako rodiče (nebo pečovatele) je dobro Vašich dětí tou největší
Vyrůstat s důvěrou Informace o nedostatku IGF-1 a jak může pomoci Increlex Úvod Rodiče, pacienti, ošetřovatelé odpovědi na Vaše otázky Pro Vás jako rodiče (nebo pečovatele) je dobro Vašich dětí tou největší
TOCTINO 30 mg měkké tobolky. Alitretinoinum
 Příbalová informace: Informace pro uživatele TOCTINO 10 mg měkké tobolky TOCTINO 30 mg měkké tobolky Alitretinoinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: Informace pro uživatele TOCTINO 10 mg měkké tobolky TOCTINO 30 mg měkké tobolky Alitretinoinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
Příbalová informace: informace pro uživatele. Normodipine 5 mg, tablety Normodipine 10 mg, tablety Amlodipinum
 Příbalová informace: informace pro uživatele Normodipine 5 mg, tablety Normodipine 10 mg, tablety Amlodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro uživatele Normodipine 5 mg, tablety Normodipine 10 mg, tablety Amlodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE. NEOFOLLIN Injekční roztok Estradioli valeras
 sp. zn. sukls75049/2013 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE NEOFOLLIN Injekční roztok Estradioli valeras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
sp. zn. sukls75049/2013 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE NEOFOLLIN Injekční roztok Estradioli valeras Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
Váš průvodce léčbou poškození zraku způsobeného choroidální neovaskularizací (CNV) sekundární k patologické myopii (PM) přípravkem Lucentis
 Váš průvodce léčbou poškození zraku způsobeného choroidální neovaskularizací (CNV) sekundární k patologické myopii (PM) přípravkem Lucentis (ranibizumab). Oddíl 1 O přípravku Lucentis Tato brožura Vám
Váš průvodce léčbou poškození zraku způsobeného choroidální neovaskularizací (CNV) sekundární k patologické myopii (PM) přípravkem Lucentis (ranibizumab). Oddíl 1 O přípravku Lucentis Tato brožura Vám
Příbalová informace: Informace pro uživatele Coltowan 10 mg tablety
 Příbalová informace: Informace pro uživatele 10 mg tablety Ezetimibum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
Příbalová informace: Informace pro uživatele 10 mg tablety Ezetimibum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
Příbalová informace: informace pro uživatele
 Sp.zn. sukls20326/2014 Příbalová informace: informace pro uživatele Solifenacin G.L.Pharma 5 mg, potahované tablety Solifenacin G.L.Pharma 10 mg, potahované tablety solifenacini succinas Přečtěte si pozorně
Sp.zn. sukls20326/2014 Příbalová informace: informace pro uživatele Solifenacin G.L.Pharma 5 mg, potahované tablety Solifenacin G.L.Pharma 10 mg, potahované tablety solifenacini succinas Přečtěte si pozorně
CNV. Váš průvodce léčbou poškození zraku způsobeného choroidální neovaskularizací (CNV) přípravkem Lucentis (ranibizumab)
 CNV Váš průvodce léčbou poškození zraku způsobeného choroidální neovaskularizací (CNV) přípravkem Lucentis (ranibizumab) 2 Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu poškození
CNV Váš průvodce léčbou poškození zraku způsobeného choroidální neovaskularizací (CNV) přípravkem Lucentis (ranibizumab) 2 Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit léčbu poškození
Zvláštní opatrnosti při použití přípravku Dozotima je zapotřebí Použití u dětí Použití u starších pacientů
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DOZOTIMA 20 mg/ml + 5 mg/ml Oční kapky, roztok Dorzolamidum/timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DOZOTIMA 20 mg/ml + 5 mg/ml Oční kapky, roztok Dorzolamidum/timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat.
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE. SonoVue, 8 mikrolitrů/ml, prášek pro přípravu injekční disperze s rozpouštědlem sulfuris hexafluoridum
 PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE SonoVue, 8 mikrolitrů/ml, prášek pro přípravu injekční disperze s rozpouštědlem sulfuris hexafluoridum Přečtěte si pozorně celou příbalovou informaci dříve,
PŘÍBALOVÁ INFORMACE INFORMACE PRO UŽIVATELE SonoVue, 8 mikrolitrů/ml, prášek pro přípravu injekční disperze s rozpouštědlem sulfuris hexafluoridum Přečtěte si pozorně celou příbalovou informaci dříve,
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Menveo prášek a roztok pro injekční roztok Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: informace pro uživatele Menveo prášek a roztok pro injekční roztok Konjugovaná vakcína proti meningokokové skupině A, C, W135 a Y Přečtěte si pozorně tuto příbalovou informaci dříve,
Příbalová informace: Informace pro uživatele. Zarelle 75 mikrogramů potahované tablety. desogestrelum
 Sp.zn.sukls59895/2013 Příbalová informace: Informace pro uživatele Zarelle 75 mikrogramů potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Sp.zn.sukls59895/2013 Příbalová informace: Informace pro uživatele Zarelle 75 mikrogramů potahované tablety desogestrelum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: Informace pro uživatele. Viazet 20 mg/10 mg. tvrdé tobolky. rosuvastatinum a ezetimibum
 Sp.zn.sukls121904/2013, sukls121905/2013 Příbalová informace: Informace pro uživatele Viazet 10 mg/10 mg Viazet 20 mg/10 mg tvrdé tobolky rosuvastatinum a ezetimibum Přečtěte si pozorně celou příbalovou
Sp.zn.sukls121904/2013, sukls121905/2013 Příbalová informace: Informace pro uživatele Viazet 10 mg/10 mg Viazet 20 mg/10 mg tvrdé tobolky rosuvastatinum a ezetimibum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. Dracenax 2,5 mg Letrozolum potahované tablety
 Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls172883/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dracenax 2,5 mg Letrozolum potahované tablety Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls172883/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Dracenax 2,5 mg Letrozolum potahované tablety Přečtěte si pozorně celou příbalovou informaci
Příbalová informace: informace pro pacienta. ISOTREXIN gel. Erythromycinum/isotretinoinum
 sp.zn. sukls241539/2012 a sp.zn. sukls58476/2013 Příbalová informace: informace pro pacienta ISOTREXIN gel Erythromycinum/isotretinoinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls241539/2012 a sp.zn. sukls58476/2013 Příbalová informace: informace pro pacienta ISOTREXIN gel Erythromycinum/isotretinoinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele Bexsero injekční suspenze v předplněné injekční stříkačce Vakcína proti meningokokům skupiny B (rdna, komponentní, adsorbovaná) Tento přípravek podléhá dalšímu
Příbalová informace: informace pro uživatele Bexsero injekční suspenze v předplněné injekční stříkačce Vakcína proti meningokokům skupiny B (rdna, komponentní, adsorbovaná) Tento přípravek podléhá dalšímu
Příbalová informace: Informace pro uživatele. Oxaliplatinum medac 5 mg/ml prášek pro přípravu infuzního roztoku oxaliplatinum
 Příbalová informace: Informace pro uživatele Oxaliplatinum medac 5 mg/ml prášek pro přípravu infuzního roztoku oxaliplatinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: Informace pro uživatele Oxaliplatinum medac 5 mg/ml prášek pro přípravu infuzního roztoku oxaliplatinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro uživatele. Enap i.v. 1,25 mg/1 ml injekční roztok enalaprilatum dihydricum
 sp.zn. sukls184192/2014 Příbalová informace: informace pro uživatele Enap i.v. 1,25 mg/1 ml injekční roztok enalaprilatum dihydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn. sukls184192/2014 Příbalová informace: informace pro uživatele Enap i.v. 1,25 mg/1 ml injekční roztok enalaprilatum dihydricum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Timlatan 50 mikrogramů/ml + 5 mg/ml oční kapky, roztok Latanoprostum /timololum
 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Timlatan 50 mikrogramů/ml + 5 mg/ml oční kapky, roztok Latanoprostum /timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Timlatan 50 mikrogramů/ml + 5 mg/ml oční kapky, roztok Latanoprostum /timololum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. DICLOIN 75 mg/ml injekční roztok. diclofenacum natricum
 Sp.zn.sukls126468/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DICLOIN 25 mg/ml injekční roztok DICLOIN 50 mg/ml injekční roztok DICLOIN 75 mg/ml injekční roztok diclofenacum natricum Přečtěte si
Sp.zn.sukls126468/2015 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE DICLOIN 25 mg/ml injekční roztok DICLOIN 50 mg/ml injekční roztok DICLOIN 75 mg/ml injekční roztok diclofenacum natricum Přečtěte si
sp. zn. sukls189078/2015
 sp. zn. sukls189078/2015 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE COLDREX MAXGRIP CITRON prášek pro perorální roztok v sáčku paracetamolum, phenylephrini hydrochloridum, acidum ascorbicum Přečtěte
sp. zn. sukls189078/2015 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE COLDREX MAXGRIP CITRON prášek pro perorální roztok v sáčku paracetamolum, phenylephrini hydrochloridum, acidum ascorbicum Přečtěte
sp.zn.sukls187300/2013
 sp.zn.sukls187300/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE TRAMAL kapky 100 mg/1 ml, Perorální kapky, roztok (Tramadoli hydrochloridum) v lahvičce s dávkovací pumpou Přečtěte si pozorně celou
sp.zn.sukls187300/2013 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE TRAMAL kapky 100 mg/1 ml, Perorální kapky, roztok (Tramadoli hydrochloridum) v lahvičce s dávkovací pumpou Přečtěte si pozorně celou
Doporučení pro léčbu přípravkem EYLEA (afliberceptum) Injekce do sklivce. Informace pro předepisujícího lékaře
 EDUKAČNÍ MATERIÁLY Doporučení pro léčbu přípravkem EYLEA (afliberceptum) Injekce do sklivce Informace pro předepisujícího lékaře Tento léčivý přípravek podléhá dalšímu sledování. BAYER-EYLEA_PrecriberBooklet_A4_CZ2015_04.indd
EDUKAČNÍ MATERIÁLY Doporučení pro léčbu přípravkem EYLEA (afliberceptum) Injekce do sklivce Informace pro předepisujícího lékaře Tento léčivý přípravek podléhá dalšímu sledování. BAYER-EYLEA_PrecriberBooklet_A4_CZ2015_04.indd
Tato brožura Vám pomůže lépe pochopit léčbu vlhké (neovaskulární) formy věkem podmíněné makulární degenerace (AMD) přípravkem Lucentis
 Tato brožura Vám pomůže lépe pochopit léčbu vlhké (neovaskulární) formy věkem podmíněné makulární degenerace (AMD) přípravkem Lucentis Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit
Tato brožura Vám pomůže lépe pochopit léčbu vlhké (neovaskulární) formy věkem podmíněné makulární degenerace (AMD) přípravkem Lucentis Oddíl 1 O přípravku Lucentis Tato brožura Vám pomůže lépe pochopit
Gadovist 1,0 mmol/ml injekční roztok Gadobutrolum Gadovist 1,0 mmol/ml injekční roztok v předplněné injekční stříkačce Gadobutrolum
 Sp.z. sukls177880/2014 a k sp.zn. sukls129971/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gadovist 1,0 mmol/ml injekční roztok Gadobutrolum Gadovist 1,0 mmol/ml injekční roztok v předplněné injekční
Sp.z. sukls177880/2014 a k sp.zn. sukls129971/2014 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Gadovist 1,0 mmol/ml injekční roztok Gadobutrolum Gadovist 1,0 mmol/ml injekční roztok v předplněné injekční
Příbalová informace: informace pro uživatele. CORSIM 10 CORSIM 20 CORSIM 40 potahované tablety (simvastatinum)
 sp.zn.sukls30566/2015 Příbalová informace: informace pro uživatele CORSIM 10 CORSIM 20 CORSIM 40 potahované tablety (simvastatinum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
sp.zn.sukls30566/2015 Příbalová informace: informace pro uživatele CORSIM 10 CORSIM 20 CORSIM 40 potahované tablety (simvastatinum) Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento
Příbalová informace: informace pro pacienta. Ezen 10 mg tablety Ezetimibum
 Sp.zn.sukls4582/2015 Příbalová informace: informace pro pacienta tablety Ezetimibum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité
Sp.zn.sukls4582/2015 Příbalová informace: informace pro pacienta tablety Ezetimibum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité
B. PŘÍBALOVÁ INFORMACE
 B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele CELVAPAN injekční suspenze Vakcína proti chřipce (H1N1)v (celý virion, namnožená na buňkách Vero, inaktivovaná) Přečtěte si pozorně
B. PŘÍBALOVÁ INFORMACE 1 Příbalová informace: informace pro uživatele CELVAPAN injekční suspenze Vakcína proti chřipce (H1N1)v (celý virion, namnožená na buňkách Vero, inaktivovaná) Přečtěte si pozorně
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. APO-COMBILOS 50/12,5 mg potahované tablety (losartanum kalicum / hydrochlorothiazidum)
 Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls237572/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-COMBILOS 50/12,5 mg potahované tablety (losartanum kalicum / hydrochlorothiazidum)
Příloha č. 1 k rozhodnutí o změně registrace sp. zn. sukls237572/2011 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-COMBILOS 50/12,5 mg potahované tablety (losartanum kalicum / hydrochlorothiazidum)
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls9651/2011, sukls9654/2011
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls9651/2011, sukls9654/2011 PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Celebrex 100 mg, tvrdé tobolky Celebrex 200 mg, tvrdé tobolky (Celecoxibum)
Příloha č. 1 k rozhodnutí o změně registrace sp.zn.sukls9651/2011, sukls9654/2011 PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE Celebrex 100 mg, tvrdé tobolky Celebrex 200 mg, tvrdé tobolky (Celecoxibum)
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU OZURDEX 700 mikrogramů intravitreální implantát v aplikátoru. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden implantát obsahuje dexamethasonum 700
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU OZURDEX 700 mikrogramů intravitreální implantát v aplikátoru. 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden implantát obsahuje dexamethasonum 700
Příbalová informace: informace pro uživatele
 Příbalová informace: informace pro uživatele VAQTA Adult 50 U/ml injekční suspenze v předplněné injekční stříkačce Očkovací látka proti hepatitidě typu A, inaktivovaná, adsorbovaná Pro dospělé Přečtěte
Příbalová informace: informace pro uživatele VAQTA Adult 50 U/ml injekční suspenze v předplněné injekční stříkačce Očkovací látka proti hepatitidě typu A, inaktivovaná, adsorbovaná Pro dospělé Přečtěte
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. OXALIPLATINA MYLAN 5 mg/ml prášek pro přípravu infuzního roztoku oxaliplatinum
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp. zn. sukls128291/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OXALIPLATINA MYLAN 5 mg/ml prášek pro přípravu infuzního roztoku oxaliplatinum Přečtěte
Příloha č. 2 k rozhodnutí o prodloužení registrace sp. zn. sukls128291/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE OXALIPLATINA MYLAN 5 mg/ml prášek pro přípravu infuzního roztoku oxaliplatinum Přečtěte
Příbalová informace: informace pro uživatele. Bosentan Sandoz 62,5 mg Bosentan Sandoz 125 mg potahované tablety. Bosentanum
 Sp.zn. sukls165516/2015 Příbalová informace: informace pro uživatele Bosentan Sandoz 62,5 mg Bosentan Sandoz 125 mg potahované tablety Bosentanum Přečtěte si pozorně celou příbalovou informaci dříve, než
Sp.zn. sukls165516/2015 Příbalová informace: informace pro uživatele Bosentan Sandoz 62,5 mg Bosentan Sandoz 125 mg potahované tablety Bosentanum Přečtěte si pozorně celou příbalovou informaci dříve, než
PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE. ARICEPT 5 mg ARICEPT 10 mg donepezilum potahované tablety
 PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE ARICEPT 5 mg ARICEPT 10 mg donepezilum potahované tablety Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
PŘÍBALOVÁ INFORMACE- INFORMACE PRO UŽIVATELE ARICEPT 5 mg ARICEPT 10 mg donepezilum potahované tablety Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro uživatele
 Sp. zn. sukls 20364/2013, sukls20365/2013, sukls20366/2013 Příbalová informace: informace pro uživatele Rosuvastatin Tchaikapharma 10 mg potahované tablety Rosuvastatin Tchaikapharma 20 mg potahované tablety
Sp. zn. sukls 20364/2013, sukls20365/2013, sukls20366/2013 Příbalová informace: informace pro uživatele Rosuvastatin Tchaikapharma 10 mg potahované tablety Rosuvastatin Tchaikapharma 20 mg potahované tablety
Příbalová informace: informace pro pacienta Plendil ER 5 mg Plendil ER 10 mg tablety s prodlouženým uvolňováním felodipinum
 Příbalová informace: informace pro pacienta Plendil ER 5 mg Plendil ER 10 mg tablety s prodlouženým uvolňováním felodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
Příbalová informace: informace pro pacienta Plendil ER 5 mg Plendil ER 10 mg tablety s prodlouženým uvolňováním felodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
