Petrochemie. zemní plyn) a zpracovává je na uhlovodíkové, kyslíkaté, výroba surovin pro organické a anorganické syntézy.
|
|
|
- Hynek Slavík
- před 8 lety
- Počet zobrazení:
Transkript
1 Petro zpracování uhlovodíků vzniklých při technologickém zpracování ropy a zemního plynu definice: odvětví chemické technologie, které vychází z uhlovodíkových surovin (ropa, zemní plyn) a zpracovává je na uhlovodíkové, kyslíkaté, halogenné, dusíkaté a sirné látky. výroba surovin pro organické a anorganické syntézy Výchozí suroviny Postupy zemní plyn parní reforming (konverze s vodní parou) parciální oxidace pyrolýza rafinérské plyny dělení plynů nízkooktanový benzín motorová nafta, oleje pyrolýza benzín z reformování dělení aromatických uhlovodíků 1
2 Hlavní produkty 1. Alifatické uhlovodíky a jejich deriváty (alkeny, dieny, acetylen, ethylenoxid) 2. Aromatické uhlovodíky a některé jejich deriváty (benzen, toluen, xylen, naftalen, fenol, styren) 3. Syntézní plyny (amoniak, metanol) 1. Alifatické uhlovodíky a jejich deriváty 1.1 Alkeny (eten, propen, buten, isobuten, penten) 1.2 Dieny (1,3 butadien, isopren, chloropren) 1.3 Acetylen 1.4 Etylenoxid 2. Aromatické uhlovodíky a některé jejich deriváty 2.1 Benzen 2.2 Toluen 2.3 Xyleny 2.4 Naftalen 2
3 1. Alifatické uhlovodíky 1.1 Alkeny (jedna dvojná vazba C = C ) význam v pořadí: eten propen buten isobuten penten Suroviny pro výrobu primární benzíny (benzíny z primární destilace ropy) zemní plyn rafinérské plyny (plyny z krakovacích procesů rafinérií) Metody A. Pyrolýza plynných a kapalných ropných frakcí B. Krakování kapalných ropných frakcí (C C, nevratná reakce) C. Katalytická dehydrogenace plynných alkanů (C H, vratná reakce) Příklad: pyrolýza propanu Krakování: CH3 CH2 CH3 CH2 = CH2 + CH4 eten Hr 0 = + 67,4 kj/mol Dehydrogenace: CH3 CH2 CH3 == CH3 CH = CH2 + H2 propen Hr 0 = + 125,5 kj/mol 3
4 A. Pyrolýza plynných a kapalných ropných frakcí destrukce vazeb působením tepla Pyrolýza Podmínky Produkt Nízkoteplotní pyrolýza C alkeny ; % etenu Středoteplotní pyrolýza C topný plyn (svítiplyn) Vysokoteplotní pyrolýza C acetylen Plazmová pyrolýza C acetylen Maximalizace výtěžku alkenů při pyrolýze nutno odvádět plynné produkty z oblasti sekundárním reakcím alkenů vysokých teplot, aby se zabránilo Dělení plynných produktů pyrolýzy Absorpce, selektivní adsorpce + frakční destilace zkapalněné směsi plynů 4
5 1.1.1 Etén (ethylen) CH2 = CH2 bezbarvý, hořlavý plyn nasládlé vůně, se vzduchem tvoří výbušnou směs výchozí látka pro 30 % všech petrochemikálií (etylenovod Böhlen Záluží Neratovice) Použití katalytická oxidace etylenoxid (oxiran) polyetylenoxid adice HClO etylenchlorhydrin etylenoxid chlorace 1,2 dichloretan ethylfluorid vinylchlorid PVC thiokol katalytická polymerace AlCl3 syntetické mazací oleje nízkotlaká polymerace (Zieglerův katalyzátor) polyetylen nízkotlaký středotlaká polymerace (Ziegler-Nattův katalyzátor) polyetylen středotlaký vysokotlaká polymerace (stopy O2) polyetylen vysokotlaký alkylace benzenem etylbenzen styren polystyren, kopolymer s butadienem alkylace isobutanem isohexan hydratace etenu etanol hydroformylace propanal propionová kyselina, propanol katalytická oxidace (O2, PdCl2) acetaldehyd kyselina octová adice HCl etylchlorid 2O propionová kyselina adice CO + H 5
6 1.1.2 Propén (propylen) CH3 CH = CH2 hořlavý plyn Použití katalytická oxidace propylenoxid polypropylenglykol polyuretany propylenglykol nemrznoucí směsi, PES pryskyřice katalytická oxidace PdCl2 aceton polymerace polypropylen katalytická hydratace + adice vody isopropylalkohol katalytická oxidace akrylaldehyd (akrolein) glycerol methionin (esenciální aminokyselina) katalytická oxidace kyselina akrylová + estery (akryláty) homopolymery, kopolymery katalytická amoxidace akrylonitril syntetická vlákna, pryskyřice, termoplasty elastomery (syn.kaučuk BUNA kopolymer s butadienem) 6
7 Ostré parní štěpení primárních benzínů + recirkulace etenu a propenu Produkty: etylen 35 % mol. propylen 15 % mol. frakce C4 8,5 % mol. frakce C5 a vyšší (pyrolýzní benzín) 25,5 % mol. zbytkový plyn (CH4, H2) 16 % mol. 7
8 1.2 Dieny (dvě(di) dvojné vazby C = C v molekule) technicky významné: dvojné vazby v poloze ,3 butadien CH2 = CH CH = CH Isopren (2-methyl 1,3 butadien) Chloropren (2 chlorbutadien) 8
9 ,3 butadien CH2 = CH CH = CH2 Metody A. Výroba z acetylenu, acetaldehydu B. Lebeděvův proces výroba z etanolu dehydrogenační dimerizace etanolu na kat. MgO SiO2 ; 400 C 2 C2H5OH CH2 = CH CH = CH2 + 2 H2O + H2 C. Reppeho syntéza z acetylenu a formaldehydu D. Petrochemický způsob Pozn. A, B, C historické metody 9
10 D. Petrochemický způsob výroby butadienu Metody: 1. Separace z pyrolýzních plynů pyrolýza (parní štěpení) primárních benzínů nebo výše vroucích podílů ropy při výrobě etylenu př.: ostré krakování primárních benzínů: 9 % štěpných produktů obsahuje % hm. butadienu 2. Dehydrogenace, oxyhydrogenace alkanů nebo alkanů C4 (butan, buten) 10
11 Ad 1 Separace pyrolýzních plynů izolace butadienu ze směsi uhlovodíku frakce C4 blízké body varu frakce C4 tvorba azeotropu přímá izolace destilací není možná Příklady bodu varu látka tvaru ( C) látka tvaru ( C) isobutylen 6,9 trans 2 buten + 0,88 1 buten 6,26 cis 2 buten + 3,72 1,3 - butadien 4,41 vinylacetylen + 5,1 Metody: A. Protiproudá extrakce plynné frakce C4 s částečnou recyklací butadienu B. Extrakční destilace 11
12 A. Protiproudá extrakce plynné frakce C4 s částečnou recyklací butadienu extrakční činidlo: dimetylformamid, N metylpyrrolidon postup roztok extrakčního činidla se nasycuje rozpustnějším butadienem a malým množstvím butenu pro zmenšení podílu butenů v roztoku se zvyšuje parciální tlak butadienu ve směsi tím, že se do kolony vede část již izolovaného čistého butadienu plynné buteny odcházejí z hlavy kolony regenerace: uvolnění butadienu vyvařením, následně kondenzace a destilace čistota butadienu: 95,8 % mol. výtěžek: 96 % mol. z původního obsahu ve frakci C4 12
13 B. Extrakční destilace extrakční činidlo: aceton, 2 furaldehyd, acetonitril, dimetylacetamid, dimetylformamid, N metylpyrrolidon princip změna relativní těkavosti některé ze složek dělené směsi (v tomto případě butadienu) přídavkem vhodného rozpouštědla (většinou selektivní organické) roztok požadované komponenty zůstane při destilaci ve vařáku, ostatní složky se oddestilují 13
14 Ad 2. Dehydrogenace, oxyhydrogenace alkanů nebo alkanů C4 (butan, buten) A. Dehydrogenace endotermická reakce ; teplota C podpora dehydrogenace snížením parciálního tlaku uhlovodíků vodní parou Proces Dow Chemical teplota C, tlak p = 0,1 MPa, katalyzátor: fosforečnan nikelnato-vápenatý přídavek vodní páry, poměr H2O: buteny = 20 : 1 teplo do reakce se přivádí přehřátou vodní párou konverze butenu: 50 %, selektivita pro butadien: 90 % katalyzátor nutno po 15 min regenerovat po dobu 11 minut izolace butadienu z reakční směsi: extrakční destilace 14
15 B. Oxydehydrogenace endotermická reakce ; teplo spalováním vodíku podpora dehydrogenace přídavkem kyslíku pro posun rovnováhy mezi buteny a butadieny regenerace katalyzátoru spalování koksu kyslík způsobuje: dodatečné spalování vodíku vlastní dehydrogenaci tím, že napomáhá odtržení protonu z vnitřních uhlíků řetězce množství kyslíku: a) právě tolik, aby exo spalování = endo reakce odstranění H2 při kyslíkem b) přebytek vzduchu pak řízení teploty přídavkem páry dehydrogenaci: reakce s halogeny: C4H I2 = C4H6 + 4 HI oxidace HI a regenerace halogenů 15
16 1.2.2 Isopren (2-methyl 1,3 butadien) základní složka přírodního kaučuku základní složka pro výrobu syntetického kaučuku Výroba: podobně jako 1,3 butadien A. Separace z frakce C5 při krakování extrakce frakční destilace B. Dehydrogenace parafínů a olefínů (např. isopentan, 2 metylbuten) C. Syntézní výroba z nižších stavebních jednotek příklad: propen: katalytická dimerizace izomerace pyrolýza 16
17 1.2.3 Chloropren (2 chlorbutadien) Výroba: z acetylenu klesající význam z butadienu Použití: výroba kaučuku odolnějšího ke slunečnímu záření a olejům (př. neopren) 17
18 2. Aromatické uhlovodíky a některé jejich deriváty Pořadí: benzen, toluen, xyleny, etylbenzen, naftalen, antracen (podle velikosti produkce) Základní výrobní postupy Tepelné nebo katalytické procesy výroby z uhlí nebo ropy s následnou separací Suroviny 1. Produkty z koksování černého uhlí černouhelný dehet, koksárenský plyn, koksárenské vody koksování = vysokoteplotní pyrolýza převážně aromatických vysokomolekulárních sloučenin za vzniku koksu a nízkomolekulárních uhlovodíků a koksu 2. Benzín získaný reformováním benzínových frakcí (tzv. reformátový benzín) 3. Pyrolýzní benzín z výroby etylenu a propylenu 18
19 Aromatické uhlovodíky a jejich deriváty benzen (C6H6) CH3 CH2CH3 CH=CH2 toluen (C7H8) styrén (C8H8) metylbenzen etylbenzen (C8H10) vinylbenzen CH3 CH3 CH3 CH3 CH3 CH3 o-xylen m-xylen p-xylen 1,2-dimetylbenzen 1,3-dimetylbenzen 1,4-dimetylbenzen 19
20 2.1. Suroviny Ad 1. Produkty z koksování černého uhlí Izolace BTX A. Černouhelný dehet 1. Frakční destilace rozdělení na frakce 2. Zpracování frakcí krystalizace, extrakce Typické složení destilátu z černouhelného dehtu (hlavní složky) lehký olej (3%) aromatické uhlovodíky BTX, pyridin karbolový olej (3%) fenoly naftalenový olej (10 12)% naftalen prací olej (7 8) % metylnaftaleny, acenafteny antracenový olej (20 28) % antracen, fenantren, karbazol smola 20
21 B. Koksárenský plyn 1. Izolace 1a) Vypírka pomocí výševroucích uhlovodíků Vypírka: např. antracenový olej Odstranění BTX z pracího oleje: destilace 1b) Adsorpce na aktivním uhlí Desorbce BTX : vodní parou 2. Rafinace Odstranění dusíkatých a sirných sloučenin a nenasycených uhlovodíků 2a) reakce s kyselinou sírovou 2b) katalytická hydrogenace Produkt: tzv. surový benzen 21
22 Typické složení extraktu z koksárenského plynu Složka % obj. přední těkavá frakce 2 benzen 65 toluen 18 xyleny 6 etylbenzen 2 vyšší aromatické uhlovodíky 7 22
23 C. Koksárenské vody složení: 0,3 % hm. fenolu a jeho homologů (kresol, xylenol) postup: izolace z vodní fáze extrakcí extrakční činidlo: např. benzen produkt: 52 % hm. fenol, krezol, xylenol, aj. 23
24 Ad 2+3 Reformátový benzín a pyrolýzní benzín Reformátové benzíny produkt katalytického krakování obsahuje frakce bohaté na aromatické uhlovodíky (zejména toluen, xylen) BTX lze získávat přímo bez předchozí úpravy Pyrolýzní benzín produkt parního krakování ropných frakcí při výrobě etylenu a propylenu obsahuje poměrně velký obsah benzenu nutná předchozí úprava nutno vyčistit od polymerujících olefinů a diolefinů pomocí hydrogenace (odstranění dvojných vazeb a látek obsahujících S, N, O) 24
25 Typické složení reformátových a pyrolýzních benzínů Složení (% mol.) Složka B. reformátový B. pyrolýzní benzen 3 40 toluen xyleny etylbenzen vyšší aromatické uhlovodíky 16 3 nearomáty
26 2.2 Izolace aromatických uhlovodíků Obecný postup: 1. Oddělení nearomatických uhlovodíků 2. Dělení jednotlivých aromatických složek Metody pro získávání aromatických uhlovodíků Proces Účel Podmínky použitelnosti Azeotropická destilace Extrakční destilace Extrakce kapalina kapalina Krystalizace vymražováním Adsorpce na tuhých sorbentech separace BTX z pyrolýzního benzínu separace BTX z pyrolýzního benzínu separace BTX z reformátového benzínu izolace p-xylenu ze směsi p/m xylenu izolace p-xylenu z aroatické frakce C8 velký obsah aromátů (> 90 % mol.) střední obsah aromátů (65 90 % mol.) malý obsah aromátů (20 65 % mol.) předběžné destilační oddělení o- xylenu a ETB z arom. frakce C8 kontinuální, reverzibilní, selektivní 26
27 Proč NE frakční destilace? vznik azeotropických směsí aromátů a nearomátů cyklohexan, heptan + další alkany + benzen nebo toluen = azeotropické směsi málo rozdílné teploty varu složek aromatické frakce C8 příklad: etylbenzen 136,2 C p xylen 138,3 C m xylen 139,1 C o xylen 144,4 C Příklad: Získání 98 % o-xylenu = teoretických pater kolony + refluxní poměr (5 8):1 27
28 2.2.1 Azeotropická destilace oddělení nearomátů (alkanů, cykloalkanů) s přidanou třetí látkou v důsledku zvýšení těkavosti nearomátů princip: přidání silně polární pomocné látky (aminy, alkoholy, ketony, voda) pro zvýšení rozdílů bodů varu aromátů a nearomátů v důsledku vzniku níževroucích azeotropických směsí nearomátů s pomocnými látkami přidání látky vznik níževroucích azeotropických směsí nearomátů s pomocnými látkami zvýšení těkavosti nearomátů hlava kolony: nearomáty, spodek kolony: aromáty Frakce Pomocná látka Benzenová aceton Toluenová metanol Xylenová metanol nevýhoda: nutno zajistit velmi úzké frakce výhoda: je-li obsah aromátů velký, nemusí se hlavní podíl dělené směsi vypařovat energeticky výhodné ( požadavek min. 90 %) regenerace pomocné látky z destilátu: extrakce acetonu nebo metanolu vodou, destilační oddělení acetonu a metanolu 28
29 2.2.2 Extrakční destilace oddělení nearomátů s přidanou třetí látkou v důsledku zvýšení těkavosti nearomátů princip: přidání pomocné látky pro zvýšení rozdílů bodů varu aromátů a nearomátů v důsledku vzniku výševroucích směsí aromátů s pomocnými látkami přidání látky vznik výševroucích směsí aromátů s pomocnými látkami zvýšení těkavosti nearomátů hlava kolony: nearomáty, spodek kolony: aromáty Pomocné látky: rozpouštědla selektivní pro aromáty (tepelně stabilní nekorozívní) dichlorbenzen, trichlorbenzen, benzylalkohol, polyglykol, fenol, aminy, nitrily, N-metylpyrrolidon (proces Distapex), N-formylmorfolin (proces Morphylane), metylformamid, sulfolan regenerace pomocné látky: destilační oddělení na aromáty a pomocnou látku hlava kolony: většinou aromáty, spodek: většinou rozpoštědlo 29
30 2.2.3 Extrakce kapalina kapalina selektivní extrakce aromátů směsí polárních rozpouštědel, tj. oddělení aromátů přídavkem třetí látky v důsledku vzniku nemísitelných fází princip: vytvoření dvou nemísitelných fází pomocí silně polárních rozpoštědel selektivních pro aromáty rafinát: nearomáty extrakt: aromáty + rozpouštědlo zpracování extraktu: tj. rozdělení aromátů a rozpouštědla a) přímá destilace (např. destilace vodní párou) b) reextrakce Reextrakce reextrakce levnými nízkovroucími rozpouštědly (např. pentan) oddělení selektivních extrakčních rozpouštědel oddělení aromátů od nového extrakčního rozpouštědla destilací výhody: úspora drahých extrakčních činidel energetická výhodnost (nenákladné destilační oddělení lehkých uhlovodíků) 30
31 Technická řešení extrakce Extrakční kolona Kaskáda extraktorů typu mísič usazovák Extrakční kolona se zpětným tokem aromátů pro zvýšení dělícího účinku rozpouštědlo nearomáty směs k dělení čistý aromát (pro zvýšení dělícího účinku, tj. úplné vytěsnění nearomátů) rozpouštědlo + aromáty 31
32 Příklady Postup Firma Rozpouštědlo Podmínky extrakce UDEX UOP Dow mono-, di-, tri-, tetraetylenglykol/h2o nebo směsi C 0,5 0,7 MPa SULFOLAN Shell UOP tetrahydrothiofendioxid (sulfolan) 50 C AROSOLVAN Lurgi N metylpyrrolidon/h2o C 0,1 MPa IFP IFP dimetylsulfoxid/h 2O C SSSR propylenkarbonát C DuoSol Milwhite Co. propan/kresol nebo fenol n/a FORMEX SNAM Progeti N formylmorfolin/h2o 40 C ; 0,1 MPa AROMEX Koppers N formylmorfolin/h2o 80 C ; 0,2 MPa MOFEX Leuna Werke monometylformamid/h2o C kpa AREX Leuna Werke N metyl ε kaprolaktam C 32
33 IFP proces extrakční činidlo: dimetylsulfoxid/ H2O surovina: 10 % mol. benzen, 27 % mol. toluen, 18 % mol. xylen výtěžky: benzen 99,9 %, toluen 98,5 %, xyleny 95 % Výhody extrakce použitelné i při velmi proměnlivých koncentračních poměrech nevyžaduje úzké frakce možno směs aromátů, tj. společná extrakce všech aromátů 33
34 Postup UDEX rozpouštědlo: glykol + voda (8 10 % vody) Dow Chemical UOP (Universal Oil Products Co.) rafinát rafinát vodní pračka aromáty k extrakční odháněcí aromáty destilaci frakce s kolona kolona voda aromáty usazovák glykolový roztok zpětný tok extrakt aromátu vodní pračka: vyprání zbytků glykolu z rafinátu 34
35 Extrakční destilace s fenolem nearomáty extrakční odháněcí frakce s destilační kolona aromáty kolona fenolový roztok aromáty na kyselou rafinaci fenolový extrakt čerstvý fenol Benzenová frakce (min. 10 % benzenu): 90 % výtěžek % benzenu 35
36 2.2.4 Krystalizace nízkoteplotní frakční krystalizace použití: dělení xylenů princip: využití vyšších rozdílů v bodu tání ve srovnání s nepatrnými rozdíly v bodech varu Složka Bod varu ( C) Bod tání ( C) p xylen 138,3 + 13,3 o xylen 144,4 25,2 m xylen 139,1 47,9 etylbenzen 136,2 95 benzen 80,1 5,53 toluen 110,6 95 Pozn. oddělení m xylenu a p xylenu oddělení destilací by vyžadovalo kolonu o 800 teoretických patrech s velkým refluxním poměrem 36
37 Zpracování aromatické frakce C8 (xylenová frakce (xyleny + ETB)) 1. Předběžné destilační dělení na níževroucí směs a výše vroucí o-xylen 60 patrová kolona, refluxní poměr = 10:1, destilační zbytek = 97 % o-xylenu 2. Nákladné destilační oddělení nízkovroucího etylbenzenu ze střední frakce destilační zbytek = 2/3 m-xylen, 1/3 p-xylen 3. Předsušení střední frakce na Al2O3 nebo SiO2 na 10 ppm H2O (jinak dochází k ucpávání armatur) 4. Mnohastupňová krystalizace se separací, promytím a opětovným tavením 37
38 Ad 4. Mnohastupňová krystalizace se separací, promytím a opětovným tavením 1. stupeň předchlazení na 32 C začátek krystalizace zchlazení na 70 C odstředění nebo filtrace vzniklé kaše tuhý produkt (krystalický podíl): 70 % p xylen filtrát: 80 % m xylen 2. stupeň roztavení krystalického podílu v nádrži ohřátím na 24 C opětovná krystalizace předchlazení na + 7 C odstřeďování při 18 C tuhý produkt (krystalický podíl): 90 % p xylen filtrát: 85 % m xylen : : p xylen : 99,5 % čistota Pozn. Eutektikum 12 % p-xylen, 88 % m-xylen izolace p-xylenu je možná pouze do obsahu 85% m-xylenu, jinak se vylučuje eutektikum 38
39 2.2.5 Adsorpce na tuhých adsorbentech princip: využití adsorpční specifičnosti povrchu a pórovité struktury adsorbentu pro určité typy molekul k selektivnímu dělení směsi historické procesy 1. izolace benzenu z koksárenského plynu pomocí aktivního uhlí 2. izolace benzenu a toluenu ze směsi s nearomáty pomocí silikagelu (proces AROSORB) desorpce pomocí aromátů s vyšší molekulovou hmotností (např. benzen, toluen pomocí xylenu) současnost izolace p-xylenu ze směsi izomerních xylenů nebo z frakce C8 proces AROMAX (Aromatics Maximum Recovery) Toray proces PAREX (Paraxylene Extraction) UOP 39
40 Proces AROMAX selektivní adsorpce p-xylenu ze směsi izomerních xylenů desorpce: rozpouštědlo 200 C ; 1,5 MPa ; p-xylen 99,5% Proces PAREX adsorpce na molekulových sítech extrakce p-xylenu z C8 frakce nebo ze směsi izomerních xylenů postup: adsorpce v kapalné fázi C desorpce: promytí nízkovroucím uhlovodíkem destilační oddělení p-xylenu z desorbentu produkt: p-xylen 99,5 % mol. výtěžek: 95 % 40
41 2.3 Vzájemná přeměna aromatických uhlovodíků Důvody: různé objemy výroby výchozích surovin + různé složení aromátů nerovnováha množství jednotlivých aromátů nutnost vzájemné přeměny Metody: 1. Hydrodealkylace toluenu (toluen benzen) 2. Izomerace m xylenu (m-xylen o-, p- xylen) 3. Disproporcionace toluenu (toluen benzen + xyleny) 41
42 2.3.1 Hydrodealkylace hydrogenační odštěpení alkylových postranních řetězců na aromatickém jádře toluen (C7H8) + H2 benzen (C6H6) + CH4 H 0 = 126 kj/mol CH3 + H 2 + CH4 toluen (metylbenzen) A. Tepelná hydrodealkylace B. Katalytická hydrodealkylace A. Tepelná hydrodealkylace proces: THD (Gulf), MHD (Mitsubishi), HDA podmínky: C, 3 10 MPa výsledky: konverze toluenu %, 95 % selektivita pro benzen 42
43 B. Katalytická hydrodealkylace toluenu proces: Detol, Pyrotol (Houdry), Hydeal (UOP), Bextol (Shell), BASF podmínky: C, 3 5 MPa katalyzátor: oxidy Cr, Mo, Co (Cr2O3, Mo2O3, CoO na nosiči) produkt: 99,9% benzenu, malý obsah síry benzen vhodný pro hydrogenaci na cyklohexan) Problém: vysoké pracovní teploty karbonizace (usazování uhlíku na katalyzátoru) systém dvou reaktorů s regenerací katalyzátoru vždy po h chodu 43
44 H recirkulující plyn 2 H2/CH4 toluen T + RP Reaktor K. d. NT.D. metan na parní refomin toluen + výše Destilace benzen vroucí podíly K.d. = kondenzační oddělení kondenzovatelných fází NT.D. oddělení metanu nízkoteplotní destilací ; (CH4 na parní reforming pro výrobu H2) T+RP = toluen + recirkulující plyn (smě s H 2 + CH 4 ) g 44
45 2.3.2 Izomerace m-xylenu princip: ustavení rovnováhy ve směsi aromátů ve frakci C8 s velkým podílem m- xylenu rovnovážné složení ETB 8 % C o-xylen 22 % m-xlen 48 % p-xylen 22 % CH3 CH3 CH3 CH3 CH3 CH3 o-xylen m-xylen p-xylen 1,2-dimetylbenzen 1,3-dimetylbenzen 1,4-dimetylbenzen 45
46 ICI, Manzen katalyzátor: Al2SiO3.SiO C, p = atmosférický výhody: levný katalyzátor nevýhody: vedlejší reakce (disproporcionace) deaktivace katalyzátoru usazováním uhlíku Hydrokatalytická izomerace OCTAFINING katalyzátor: Pt na Al 2 SiO 3.SiO 2 za přítomnost vodíku platina a vodík přítomny pro omezení dehydrogenace a usazování uhlíku (Pt/H2 hydrogenace) C, p = 1 2,5 MPa výhody: dlouhá životnost katalyzátoru malá ztráta aromátů C8 disproporcionací Friedelova Craftsova izomerace zeolity jako katalyzátor: C, p = 1,4 MPa HBF4 jako katalyzátor: izomerace v kapalné fázi s HBF4 ; 100 C, p = atmosférický výhody: nižší teploty snížení disproporcionace 46
47 2.3.3 Disproporcionace princip: přenos alkylových skupin za vzniku směsi níže alkylovaných a výše alkylovaných aromátů disproporcionace toluenu na benzen a xyleny 2 toluen (C7H8) + H2 benzen (C6H6) + xylen (C8H10) H 0 = 126 kj/mol CH3 2 CH3 + CH3 47
48 2.4 Aromáty Benzen C6H % spotřeby ETB, kumen, cyklohexan, zbytek ostatní katalytická alkylace etylbenzen styren polystyren + butadien buna S + izobuten polymer S kumen fenol (90 % výroby fenolu) kresol herbicidy, insekticidy desinfekční prostředky benzoová kyselina fenolické pryskyřice bisfenol epoxidové pryskyřice ε -kaprolaktam anilin cyklohexan adipová kyselina ε -kaprolaktam kyselina maleinová/maleinanhydrid barvení textilií, potiskování textilií umělé pryskyřice polyesterové pesticidy (Malathion) sulface, chlorace fenol (10 % výroby fenolu) ; Nevýhody: velké množství odpadních solí nitrobenzen a jeho deriváty anilin (> 95%) sulfonany syntetické prací prostředky 48
49 2.4.2 Toluen kyselina benzoová (konzervační prostředky, léčiva) fenol TNT sacharin, chloramin T Xyleny o-xylen kyselina ftalová plastické hmoty pryskyřice plastifikátory m-xylen kyselina izoftalová dtto p-xylen kyselina tereftalová chemická vlákna (tesil, terylen, dacron,..) 49
50 2.4.4 Etylbenzen C8H10 výroba: etylace benzenu etylenem (etylace benzenu) benzen (C6H6) + etylen (C2H4) ETB (C8H10) + H2 H 0 = 113 kj/mol + CH 2=CH2 CH2CH3 Metody: A. Etylace v kapalné fázi B. Etylace v plynné fázi 50
51 A. Etylace v kapalné fázi Nevýhody korozivní katalyzátor oddělování katalyzátoru z produktů (vypírka vodou a alkáliemi) odstraňování vody z recyklovaného benzenu (vysušení) Klasický postup protiproudé vedení dvoufázového systému katalyzátor/promotor a benzen/etylen za atmosférického/zvýšeného v problublávaném reaktoru teplota C, p = 0,1 0,7 MPa katalyzátor: AlCl3 (+ ETB HAlCl4. n C6H5C2H5) ; 1 kg AlCl3/100 kg ETB promotor: etylchlorid HCl(C2H5Cl) směs etylen : benzen = 0,6 : 1 vedlejší reakce: vznik dietylbenzenů, polyetylbenzenů optimalizace ETB selektivity omezení konverze benzenu (na %) nestechiometrický poměr etylen : benzen (0,6:1místo 1:1) problublávaná kolona (alkylační věž: spodem etylen + benzen, horem katalyzátor) 51
52 Postup Monsanto snížené množství AlCl3 homogenní jednofázový systém AlCl3/benzen/etylen snížení spotřeby AlCl3 na 0,25 kg AlCl3/100 kg ETB teplota C, p = 0,3 1 MPa omezení vedlejších reakcí ; selektivita pro ETB 99 % podmínka: řízené dávkování etylenu nikde nesmí být v přebytku 52
53 B. Etylace v plynné fázi (zejména USA) teplota 300 C, tlak 4 6,5 MPa kyselé katalyzátory na nosičích Al2O3.SiO2, H3PO4 na SiO2 katalyzátory inaktivní pro dealkylaci recyklovaných oligoetylbenzenů poměr etylen : benzen = 0,2 : 1 (mol) proces Mobil-Badger aluminosilikát ve formě molekulového síta ; nutno každé 2-4 týdny regenerovat teplota C ; tlak 1,4 2,8 MPa konverze 85 %, selektivita pro ETB 98 % (počítáno na benzen) proces Alkar (UOP) katalyzátor BF3/γ-Al2O3 katalyzátor aktivní pro transalkylace a dealkylace úplná konverze etylenu + velká selektivita pro ETB (98 99 %) teplota C ; tlak 1,4 2,8 MPa výhody: možno použít i zředěný etylen obsahující i kyslík a CO2 nedochází ke korozi 53
54 2.4.5 Styren (vinylbenzen) C8H8 Starší postupy 1. Chlorace do postranního řetězce a dehydrochlorace 2. Oxidace ETB na acetofenon, hydrogenace na 1-fenyletanol, dehydratace na styren Moderní postupy 1. Nepřímá oxidace propylenu (proces HALCON) oxidace propylenu propylenoxid 1-fenyletanol dehydratace na styren 1 kg propylenoxidu 2,5 kg styrenu 2. Katalytická dehydrogenace ETB ETB (C8H10) styren (C8H8) + H2 H 0 = kj/mol CH2CH3 CH=CH2 + H2 teplota C katalyzátor: oxidy železa + promotory Cr2O3, draselné sloučeniny (KOH, K2CO3) 54
55 Varianty přívodu tepla Nepřímý přívod (BASF) Přímý přívod (Dow) Trubkový reaktor trubky naplněné katalyzátorem teplo spalováním plynu (např. vodík vznikající při reakci) Šachtová pec katalyzátor: nepohyblivá vrstva v šachtové peci adiabatické provedení endotermické dehydrogenace přívod tepla ve formě přehřáté páry pro zajištění dostatečné teploty na konci katal. vrstvy nutno cca 2,5 3 kg páry na 1 kg ETB při teplotě 720 C Optimalizace selektivity pro styren (tj. omezení vedlejších reakcí) vedlejší produkty: toluen, benzen, dehtovité látky možnosti: 1. omezení teploty 2. přídavek vodní páry (snížení parciálního tlaku ETB posun rovnováhy ve prospěch styrenu) 55
56 Zpracování a čistění styrenu 1. Rychlé ochlazení na 100 C (zabránění polymeraci) 2. Frakční kondenzace: nejprve dehet styren ETB 3. Vakuová destilace styrenu (dočištění styrenu na polymerační čistotu 99,8 % mol.) Vakuová destilace styrenu (s přídavkem polymeračních inhibitorů, např. síry) problém: sklon k polymeraci blízké body varu (ETB 136 C, styren C) čistota 99,8 % mol. styrenu vyžaduje 4 kolony řešení: přídavek inhibitorů nízká teplota ve vakuových kolonách ( malý počet pater a velký malá tlaková ztráta refluxní poměr) Radek
EVROPSKÝ PARLAMENT C6-0267/2006. Společný postoj. Dokument ze zasedání 2003/0256(COD) 06/09/2006
 EVROPSKÝ PARLAMENT 2004 Dokument ze zasedání 2009 C6-0267/2006 2003/0256(COD) CS 06/09/2006 Společný postoj Společný postoj Rady k přijetí nařízení Evropského parlamentu a Rady o registraci, hodnocení,
EVROPSKÝ PARLAMENT 2004 Dokument ze zasedání 2009 C6-0267/2006 2003/0256(COD) CS 06/09/2006 Společný postoj Společný postoj Rady k přijetí nařízení Evropského parlamentu a Rady o registraci, hodnocení,
Ropa Kondenzované uhlovodíky
 Nejdůležitější surovina pro výrobu organických sloučenin Nejvýznamnější surovina světové ekonomiky Výroba energie Chemické zpracování - 15 % Cena a zásoby ropy (70-100 let) Ropné krize Nutnost hledání
Nejdůležitější surovina pro výrobu organických sloučenin Nejvýznamnější surovina světové ekonomiky Výroba energie Chemické zpracování - 15 % Cena a zásoby ropy (70-100 let) Ropné krize Nutnost hledání
UHLOVODÍKY ALKANY (...)
 UHLOVODÍKY ALKANY (...) alifatické nasycené uhlovodíky nerozvětvené i rozvětvené mezi atomy uhlíku pouze jednoduché vazby (σ vazby), mezi nimi úhel 109 28 název: kmen + an obecný vzorec C n H 2n + 2 tvoří
UHLOVODÍKY ALKANY (...) alifatické nasycené uhlovodíky nerozvětvené i rozvětvené mezi atomy uhlíku pouze jednoduché vazby (σ vazby), mezi nimi úhel 109 28 název: kmen + an obecný vzorec C n H 2n + 2 tvoří
Aromatické uhlovodíky z koksování černého uhlí Vysokoteplotní karbonizace ( C) Koksárenský plyn Koksárenská voda Dehet Extrakt koksárenského
 Klíčové produkty v petrochemii Benzen, toluen, xyleny, ethylbenzen >> naftalen, anthracen Základní pochody při výrobě aromatických uhlovodíků Syntéza aromatických uhlovodíků ekonomicky nepříliš výhodná
Klíčové produkty v petrochemii Benzen, toluen, xyleny, ethylbenzen >> naftalen, anthracen Základní pochody při výrobě aromatických uhlovodíků Syntéza aromatických uhlovodíků ekonomicky nepříliš výhodná
Zpracování ropy doc. Ing. Josef Blažek, CSc. 5. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 5. přednáška Reformování a izomerace benzinů, výroba benzinových složek
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 5. přednáška Reformování a izomerace benzinů, výroba benzinových složek
zpracování těžkých frakcí na motorová paliva (mazut i vakuový zbytek)
 Ropa štěpné procesy zpracování těžkých frakcí na motorová paliva (mazut i vakuový zbytek) typy štěpných procesů: - termické krakování - katalytické krakování - hydrogenační krakování (hydrokrakování) podmínky
Ropa štěpné procesy zpracování těžkých frakcí na motorová paliva (mazut i vakuový zbytek) typy štěpných procesů: - termické krakování - katalytické krakování - hydrogenační krakování (hydrokrakování) podmínky
Nerozvětvené (atomy C jsou spojeny maximálně s dvěma dalšími C) Rozvětvené (atomy C jsou spojeny s více než dvěma dalšími C)
 Otázka: Uhlovodíky Předmět: Chemie Přidal(a): Majdush Obsahují ve svých molekulách pouze atomy uhlíku a vodíku Nejjednodušší org. sloučeniny Uhlík je schopný řetězit se a vytvářet tak nejrůznější řetězce,
Otázka: Uhlovodíky Předmět: Chemie Přidal(a): Majdush Obsahují ve svých molekulách pouze atomy uhlíku a vodíku Nejjednodušší org. sloučeniny Uhlík je schopný řetězit se a vytvářet tak nejrůznější řetězce,
Gymnázium Vysoké Mýto nám. Vaňorného 163, Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto H 3 C Vymezení arenů V aromatickém cyklu dochází k průniku orbitalů kolmých k rovině cyklu. Vzniká tzv. delokalizovaná vazba π. Stabilita benzenu
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto H 3 C Vymezení arenů V aromatickém cyklu dochází k průniku orbitalů kolmých k rovině cyklu. Vzniká tzv. delokalizovaná vazba π. Stabilita benzenu
CHEMICKÉ TECHNOLOGIE PRO PROCESNÍ INŽENÝRSTVÍ N VÝROBA MTBE
 CHEMICKÉ TECHNOLOGIE PRO PROCESNÍ INŽENÝRSTVÍ N409059 VÝROBA MTBE Fyzikální a chemické vlastnosti Suroviny Reakce Technologie Dvoustupňová výroba Jednostupňová výroba Charakteristiky technologií Zdroje
CHEMICKÉ TECHNOLOGIE PRO PROCESNÍ INŽENÝRSTVÍ N409059 VÝROBA MTBE Fyzikální a chemické vlastnosti Suroviny Reakce Technologie Dvoustupňová výroba Jednostupňová výroba Charakteristiky technologií Zdroje
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: Číslo šablony: CZ.1.07/1.5.00/34.0410 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Název materiálu: Fosilní zdroje
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: Číslo šablony: CZ.1.07/1.5.00/34.0410 III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Název materiálu: Fosilní zdroje
Základní škola a mateřská škola Hutisko Solanec. žák uvede základní druhy uhlovodíků, jejich použití a zdroje. Chemie - 9. ročník
 Základní škola a mateřská škola Hutisko Solanec Digitální učební materiál Anotace: Autor: Jazyk: Očekávaný výstup: Speciální vzdělávací potřeby: Klíčová slova: Druh učebního materiálu: Druh interaktivity:
Základní škola a mateřská škola Hutisko Solanec Digitální učební materiál Anotace: Autor: Jazyk: Očekávaný výstup: Speciální vzdělávací potřeby: Klíčová slova: Druh učebního materiálu: Druh interaktivity:
1)uhlovodík musí být cyklický, všechny atomy musí být v jedné rovině
 Otázka: Areny Předmět: Chemie Přidal(a): I. Prokopová 3 podmínky: 1)uhlovodík musí být cyklický, všechny atomy musí být v jedné rovině 2) musí existovat minimálně dvě možnosti uspořádání π elektronů 3)
Otázka: Areny Předmět: Chemie Přidal(a): I. Prokopová 3 podmínky: 1)uhlovodík musí být cyklický, všechny atomy musí být v jedné rovině 2) musí existovat minimálně dvě možnosti uspořádání π elektronů 3)
spalné teplo h spal = kj/kg složení: % C, % H, 2 3 % O, N,S hustota ρ (20 C) = kg/m 3
 4. Zpracování ropy 4.1 Ropa směs uhlovodíků (parafíny, nafteny, aromáty) kapalina hnědé až černé barvy složení: 84 87 % C, 11 14 % H, 2 3 % O, N,S hustota ρ (20 C) = 800 1000 kg/m 3 spalné teplo h spal
4. Zpracování ropy 4.1 Ropa směs uhlovodíků (parafíny, nafteny, aromáty) kapalina hnědé až černé barvy složení: 84 87 % C, 11 14 % H, 2 3 % O, N,S hustota ρ (20 C) = 800 1000 kg/m 3 spalné teplo h spal
TVORBA UHLÍKATÝCH PRODUKTŮ PŘI I PYROLÝZE UHLOVODÍKŮ
 TVORBA UHLÍKATÝCH PRODUKTŮ PŘI I PYROLÝZE UHLOVODÍKŮ Martin Hrádel 5. ročník Školitel: Doc. Ing. Zdeněk Bělohlav, CSc. Obsah Úvod Mechanismus vzniku a vlastnosti uhlíkatých produktů Provozního sledování
TVORBA UHLÍKATÝCH PRODUKTŮ PŘI I PYROLÝZE UHLOVODÍKŮ Martin Hrádel 5. ročník Školitel: Doc. Ing. Zdeněk Bělohlav, CSc. Obsah Úvod Mechanismus vzniku a vlastnosti uhlíkatých produktů Provozního sledování
16.IZOMERIE a UHLOVODÍKY 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem liší?
 16.IZOMERIE a UHLOVODÍKY 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem liší? 4) Urči typy konstituční izomerie. 5) Co je tautomerie
16.IZOMERIE a UHLOVODÍKY 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem liší? 4) Urči typy konstituční izomerie. 5) Co je tautomerie
ANORGANICKÁ ORGANICKÁ
 EMIE ANORGANIKÁ ORGANIKÁ 1 EMIE ANORGANIKÁ Anorganické látky Oxidy: O, O 2.. V neživé přírodě.. alogenidy: Nal.. ydroxidy: NaO Uhličitany: ao 3... Kyseliny: l. ydrogenuhličitany: NaO 3. 2 EMIE ORGANIKÁ
EMIE ANORGANIKÁ ORGANIKÁ 1 EMIE ANORGANIKÁ Anorganické látky Oxidy: O, O 2.. V neživé přírodě.. alogenidy: Nal.. ydroxidy: NaO Uhličitany: ao 3... Kyseliny: l. ydrogenuhličitany: NaO 3. 2 EMIE ORGANIKÁ
Zpracování ropy doc. Ing. Josef Blažek, CSc. 6. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 6. přednáška Vlastnosti a výroba minerálních olejů ZÁKLADOVÉ OLEJE Oleje:
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 6. přednáška Vlastnosti a výroba minerálních olejů ZÁKLADOVÉ OLEJE Oleje:
H H C C C C C C H CH 3 H C C H H H H H H
 Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Zpracování ropy doc. Ing. Josef Blažek, CSc.
 ODBONÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PO VÝKON STÁTNÍ SPÁVY OCHANY OVZDUŠÍ V ČESKÉ EPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 2. přednáška Složení ropy, základní schémata zpracování ropy, odsolování a
ODBONÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PO VÝKON STÁTNÍ SPÁVY OCHANY OVZDUŠÍ V ČESKÉ EPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 2. přednáška Složení ropy, základní schémata zpracování ropy, odsolování a
TERMICKÉ PROCESY PŘI VYUŽITÍ ALTERNATIVNÍCH SUROVIN. Most, 13.6.2013 Autor: Doc. Ing. J.LEDERER, CSc.
 TERMICKÉ PROCESY PŘI VYUŽITÍ ALTERNATIVNÍCH SUROVIN Most, 13.6.2013 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH PRINCIPY POUŽÍVANÝCH TERMOCHEMICKÝCH PROCESŮ VELKOKAPACITNÍ REALIZACE TERMOCHEMICKÝCH PROCESŮ
TERMICKÉ PROCESY PŘI VYUŽITÍ ALTERNATIVNÍCH SUROVIN Most, 13.6.2013 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH PRINCIPY POUŽÍVANÝCH TERMOCHEMICKÝCH PROCESŮ VELKOKAPACITNÍ REALIZACE TERMOCHEMICKÝCH PROCESŮ
Rada Evropské unie Brusel 26. července 2017 (OR. en)
 Rada Evropské unie Brusel 26. července 2017 (OR. en) 11526/17 ADD 4 RŮVODNÍ OZNÁMKA Odesílatel: Evropská komise Datum přijetí: 24. července 2017 říjemce: Generální sekretariát Rady Č. dok. Komise: D050725/02
Rada Evropské unie Brusel 26. července 2017 (OR. en) 11526/17 ADD 4 RŮVODNÍ OZNÁMKA Odesílatel: Evropská komise Datum přijetí: 24. července 2017 říjemce: Generální sekretariát Rady Č. dok. Komise: D050725/02
Paliva. nejběžnějším zdrojem tepla musí splňovat tyto podmínky: co nejmenší náklady na těžbu a výrobu snadno uskutečnitelné spalování
 Paliva Paliva nejběžnějším zdrojem tepla musí splňovat tyto podmínky: co nejmenší náklady na těžbu a výrobu snadno uskutečnitelné spalování Dělení paliv podle skupenství pevná uhlí, dřevo kapalná benzín,
Paliva Paliva nejběžnějším zdrojem tepla musí splňovat tyto podmínky: co nejmenší náklady na těžbu a výrobu snadno uskutečnitelné spalování Dělení paliv podle skupenství pevná uhlí, dřevo kapalná benzín,
Masarykova střední škola zemědělská a Vyšší odborná škola, Opava, příspěvková organizace
 Číslo projektu Číslo materiálu Název školy Autor Průřezové téma Tematický celek Ročník 1. CZ.1.07/1.5.00/34.0565 VY_32_INOVACE_359_Uhlovodíky Masarykova střední škola zemědělská a Vyšší odborná škola,
Číslo projektu Číslo materiálu Název školy Autor Průřezové téma Tematický celek Ročník 1. CZ.1.07/1.5.00/34.0565 VY_32_INOVACE_359_Uhlovodíky Masarykova střední škola zemědělská a Vyšší odborná škola,
Kyslíkaté deriváty. 1) Hydroxyderiváty: a) Alkoholy b) Fenoly. řešení. Dle OH = hydroxylová skupina
 Kyslíkaté deriváty řešení 1) Hydroxyderiváty: a) Alkoholy b) Fenoly Dle = hydroxylová skupina 1 Hydroxyderiváty Alifatické alkoholy: náhrada 1 nebo více atomů H. hydroxylovou skupinou (na 1 atom C vázaná
Kyslíkaté deriváty řešení 1) Hydroxyderiváty: a) Alkoholy b) Fenoly Dle = hydroxylová skupina 1 Hydroxyderiváty Alifatické alkoholy: náhrada 1 nebo více atomů H. hydroxylovou skupinou (na 1 atom C vázaná
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/
 Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT- PZC 2/11 Zdroje uhlovodíků Střední
Využití ICT pro rozvoj klíčových kompetencí CZ.1.07/1.5.00/34.0448 Číslo projektu Číslo materiálu Název školy Autor Tematický celek Ročník CZ.1.07/1.5.00/34.0448 ICT- PZC 2/11 Zdroje uhlovodíků Střední
Přírodní zdroje uhlovodíků. a jejich zpracování
 Přírodní zdroje uhlovodíků a jejich zpracování 1 Rozdělení: Přírodní zdroje org. látek fosilní - zemní plyn, ropa, uhlí (vznikají geochemickými procesy miliony let) recentní (současné) - dřevo, rostlinné
Přírodní zdroje uhlovodíků a jejich zpracování 1 Rozdělení: Přírodní zdroje org. látek fosilní - zemní plyn, ropa, uhlí (vznikají geochemickými procesy miliony let) recentní (současné) - dřevo, rostlinné
Alkany a cykloalkany
 Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Září 2010 Mgr. Alena Jirčáková Charakteristika alkanů: Malá reaktivita, odolné chemickým činidlům Nasycené
Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Září 2010 Mgr. Alena Jirčáková Charakteristika alkanů: Malá reaktivita, odolné chemickým činidlům Nasycené
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115
 Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: III/2 Inovace a zkvalitněni výuky prostřednictvím ICT. Název materiálu: Zpracování ropy
Gymnázium a Střední odborná škola, Rokycany, Mládežníků 1115 Číslo projektu: CZ.1.07/1.5.00/34.0410 Číslo šablony: III/2 Inovace a zkvalitněni výuky prostřednictvím ICT. Název materiálu: Zpracování ropy
DEZA, a.s. Studijní materiál k předmětu Chemická exkurze C6950 Brno 2011
 Studijní materiál k předmětu Chemická exkurze C6950 Brno 2011 DEZA, a.s. Vypracovala: Bc. et Bc. Monika Janoušková Úpravy: Mgr. Zuzana Garguláková, doc. Ing. Vladimír Šindelář, Ph.D. Obecné informace DEZA,
Studijní materiál k předmětu Chemická exkurze C6950 Brno 2011 DEZA, a.s. Vypracovala: Bc. et Bc. Monika Janoušková Úpravy: Mgr. Zuzana Garguláková, doc. Ing. Vladimír Šindelář, Ph.D. Obecné informace DEZA,
4 frakce 4 5 UHLOVODÍKY Oddělení isobutenu z 4 frakce (4 rafinát) - rozdílná reaktivita - butany nereagují Hydratace isobutenu na terc. butyl alkohol
 4 5 UHLOVODÍKY 4 frakce - buteny, butadien, butany Starší výroby dehydratace butanolů disproporcionace propylenu (Shawinigan, Kanada) dimerizace acetylenu Současné způsoby krakování primárních benzínů
4 5 UHLOVODÍKY 4 frakce - buteny, butadien, butany Starší výroby dehydratace butanolů disproporcionace propylenu (Shawinigan, Kanada) dimerizace acetylenu Současné způsoby krakování primárních benzínů
www.zlinskedumy.cz Inovace výuky prostřednictvím šablon pro SŠ
 Název projektu Číslo projektu Název školy Autor Název šablony Název DUMu Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748 Gymnázium Jana Pivečky a Střední odborná škola Slavičín Mgr.
Název projektu Číslo projektu Název školy Autor Název šablony Název DUMu Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748 Gymnázium Jana Pivečky a Střední odborná škola Slavičín Mgr.
Bezpečnostní inženýrství - Chemické procesy -
 Bezpečnostní inženýrství - Chemické procesy - M. Jahoda Nebezpečí a prevence chemických procesů 2 Chemické reakce Tepelné efekty exotermní procesy (teplo se uvolňuje => nutnost chlazení) endotermní procesy
Bezpečnostní inženýrství - Chemické procesy - M. Jahoda Nebezpečí a prevence chemických procesů 2 Chemické reakce Tepelné efekty exotermní procesy (teplo se uvolňuje => nutnost chlazení) endotermní procesy
11. Zemní plyn jako energetická a chemická surovina. Ing. Tomáš Hlinčík, Ph.D.
 11. Zemní plyn jako energetická a chemická surovina Ing. Tomáš Hlinčík, Ph.D. Zpracování zemního plynu Nepřímá přeměna methanu syntézní plyn (chemikálie, paliva) - výroba vodíku pro syntézu amoniaku -
11. Zemní plyn jako energetická a chemická surovina Ing. Tomáš Hlinčík, Ph.D. Zpracování zemního plynu Nepřímá přeměna methanu syntézní plyn (chemikálie, paliva) - výroba vodíku pro syntézu amoniaku -
PROPEN - PŘEHLED VYUŽITÍ
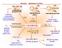 PRPEN - PŘEHLED VYUŽITÍ polymery propandioly propylenkarbonát isopropanolaminy C 4 aldehydy alkoholy kyseliny jejich estery CH methyloxiran (propylenoxid) hydroformylace hydrokarbonylace + 2 isopropylbenzen
PRPEN - PŘEHLED VYUŽITÍ polymery propandioly propylenkarbonát isopropanolaminy C 4 aldehydy alkoholy kyseliny jejich estery CH methyloxiran (propylenoxid) hydroformylace hydrokarbonylace + 2 isopropylbenzen
Ropa rafinérské výrobky
 Ropa rafinérské výrobky rafinérské výrobky - nelze použít přímo (koroze, zápach, vzhled výrobku) nežádoucí látky: sirné sloučeniny (korozivní, deaktivují katalyzátory, zhoršení životního prostředí) dusíkaté
Ropa rafinérské výrobky rafinérské výrobky - nelze použít přímo (koroze, zápach, vzhled výrobku) nežádoucí látky: sirné sloučeniny (korozivní, deaktivují katalyzátory, zhoršení životního prostředí) dusíkaté
HYDROXYDERIVÁTY. Alkoholy Fenoly Bc. Miroslava Wilczková
 HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
Destilace
 Výpočtový ý seminář z Procesního inženýrství podzim 2007 Destilace 18.9.2008 1 Tématické okruhy destilace - základní pojmy rovnováha kapalina - pára jednostupňová destilace rektifikace 18.9.2008 2 Destilace
Výpočtový ý seminář z Procesního inženýrství podzim 2007 Destilace 18.9.2008 1 Tématické okruhy destilace - základní pojmy rovnováha kapalina - pára jednostupňová destilace rektifikace 18.9.2008 2 Destilace
III/2 Inovace a zkvalitnění výuky prostřednictvím ICT. Test k ověření znalostí o ropě 2. verze
 Číslo projektu CZ.1.07/1.5.00/34.0514 Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast Suroviny organické technologie, vy_32_inovace_ma_09_32
Číslo projektu CZ.1.07/1.5.00/34.0514 Číslo a název šablony klíčové aktivity III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Tematická oblast Suroviny organické technologie, vy_32_inovace_ma_09_32
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace
 Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
ETHYLEN - PRŮMYSLOVÉ ZPRACOVÁNÍ
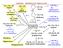 H ethanol CH= acetaldehyd CH octová kys. C CH= vinylacetát ETHYLE - PRŮMYSLVÉ ZPRACVÁÍ oxiran (ethylenoxid) ~ 10 % + 2 ~ 20 % -H 2 + KYS. KATAL. ETHE CH= styren (-CH- -) n Ph polystyren PS a jeho kopolymery
H ethanol CH= acetaldehyd CH octová kys. C CH= vinylacetát ETHYLE - PRŮMYSLVÉ ZPRACVÁÍ oxiran (ethylenoxid) ~ 10 % + 2 ~ 20 % -H 2 + KYS. KATAL. ETHE CH= styren (-CH- -) n Ph polystyren PS a jeho kopolymery
Zpracování ropy doc. Ing. Josef Blažek, CSc. 3. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 3. přednáška Termické a katalytické krakování a hydrokrakování těžkých
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 3. přednáška Termické a katalytické krakování a hydrokrakování těžkých
Hydroxysloučeniny Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Únor
 Hydroxysloučeniny Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Únor 2011 Mgr. Alena Jirčáková Hydroxysloučeniny Dělení hydroxysloučenin: Deriváty
Hydroxysloučeniny Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Únor 2011 Mgr. Alena Jirčáková Hydroxysloučeniny Dělení hydroxysloučenin: Deriváty
VÝROBA A VYUŽITÍ AROMÁTŮ
 VÝROBA A VYUŽITÍ AROMÁTŮ AROMÁTY OBECNÉ INFORMACE VÝROBA V ČR OPTIMÁLNÍ VÝROBA VARIANTY HLAVNÍ DERIVÁTY SITUACE V PRODUKCI AROMÁTŮ V ZÁPADNÍ EVROPĚ TRH AROMÁTŮ V ZÁPADNÍ EVROPĚ MIL. T/ROK MLD. US$ Spotřeba
VÝROBA A VYUŽITÍ AROMÁTŮ AROMÁTY OBECNÉ INFORMACE VÝROBA V ČR OPTIMÁLNÍ VÝROBA VARIANTY HLAVNÍ DERIVÁTY SITUACE V PRODUKCI AROMÁTŮ V ZÁPADNÍ EVROPĚ TRH AROMÁTŮ V ZÁPADNÍ EVROPĚ MIL. T/ROK MLD. US$ Spotřeba
Zplyňování biomasy. Sesuvný generátor. Autotermní zplyňování Autotermní a alotermní zplyňování
 Zplyňování = termochemická přeměna uhlíkatého materiálu v pevném či kapalném skupenství na výhřevný energetický plyn pomocí zplyňovacích médií a tepla. Produktem je plyn obsahující výhřevné složky (H 2,
Zplyňování = termochemická přeměna uhlíkatého materiálu v pevném či kapalném skupenství na výhřevný energetický plyn pomocí zplyňovacích médií a tepla. Produktem je plyn obsahující výhřevné složky (H 2,
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 16, 566 01 Vysoké Mýto Alkeny Vlastnosti dvojné vazby Hybridizace uhlíku vázaného dvojnou vazbou je sp. Valenční úhel který svírají vazby na uhlíkovém atomu je přibližně
Gymnázium Vysoké Mýto nám. Vaňorného 16, 566 01 Vysoké Mýto Alkeny Vlastnosti dvojné vazby Hybridizace uhlíku vázaného dvojnou vazbou je sp. Valenční úhel který svírají vazby na uhlíkovém atomu je přibližně
16.UHLOVODÍKY A IZOMERIE ORGANICKÝCH SLOUČENIN IZOMERIE:
 16.UHLOVODÍKY A IZOMERIE ORGANICKÝCH SLOUČENIN IZOMERIE: 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem se liší? 4) Vyber správné
16.UHLOVODÍKY A IZOMERIE ORGANICKÝCH SLOUČENIN IZOMERIE: 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem se liší? 4) Vyber správné
T E C H N I C K Á chemická odolnost membrána čistá polyurea TECNOCOAT P-2049
 TEKUTÁ OCHRANNÁ HYDROIZOLAČNÍ MEMBRÁNA T E C H N I C K Á S L O Ž K A chemická odolnost membrána čistá polyurea TECNOCOAT P-2049 t93 568 21 11 f93 568 02 11 e-mail: info@ Voda Solanka xxxxxx Odolná Chlorovaná
TEKUTÁ OCHRANNÁ HYDROIZOLAČNÍ MEMBRÁNA T E C H N I C K Á S L O Ž K A chemická odolnost membrána čistá polyurea TECNOCOAT P-2049 t93 568 21 11 f93 568 02 11 e-mail: info@ Voda Solanka xxxxxx Odolná Chlorovaná
POLYMERY PRINCIPY, STRUKTURA, VLASTNOSTI. Doc. ing. Jaromír LEDERER, CSc.
 POLYMERY PRINCIPY, STRUKTURA, VLASTNOSTI Doc. ing. Jaromír LEDERER, CSc. O čem budeme mluvit Úvod do chemie a technologie polymerů Makromolekulární řetězce Struktura, fázový stav a základní vlastnosti
POLYMERY PRINCIPY, STRUKTURA, VLASTNOSTI Doc. ing. Jaromír LEDERER, CSc. O čem budeme mluvit Úvod do chemie a technologie polymerů Makromolekulární řetězce Struktura, fázový stav a základní vlastnosti
Jednou z nejdůležitějších skupin derivátů uhlovodíků jsou sloučeniny obsahující jednovazné hydroxylové skupiny OH, proto hydroxyderiváty:
 ALKOHOLY, FENOLY A ANALOGICKÉ SIRNÉ SLOUČENINY Jednou z nejdůležitějších skupin derivátů uhlovodíků jsou sloučeniny obsahující jednovazné hydroxylové skupiny OH, proto hydroxyderiváty: Obecný vzorec hydroxysloučenin
ALKOHOLY, FENOLY A ANALOGICKÉ SIRNÉ SLOUČENINY Jednou z nejdůležitějších skupin derivátů uhlovodíků jsou sloučeniny obsahující jednovazné hydroxylové skupiny OH, proto hydroxyderiváty: Obecný vzorec hydroxysloučenin
Zpracování ropy doc. Ing. Josef Blažek, CSc. 4. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 4. přednáška Rafinace pohonných hmot, zpracování sulfanu, výroba vodíku
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 4. přednáška Rafinace pohonných hmot, zpracování sulfanu, výroba vodíku
Technické plyny. kapalný vzduch kyslík dusík vzácné plyny vodík (syntézní plyny)
 Technické plyny kapalný vzduch kyslík dusík vzácné plyny vodík (syntézní plyny) Kapalný vzduch složení vzduchu Před zkapalněním odstranění nežádoucích složek, např. vodní pára, CO 2, prach Zkapalňování
Technické plyny kapalný vzduch kyslík dusík vzácné plyny vodík (syntézní plyny) Kapalný vzduch složení vzduchu Před zkapalněním odstranění nežádoucích složek, např. vodní pára, CO 2, prach Zkapalňování
VLASTNOSTI ALKANŮ 2. RADIKÁLOVÁ SUBSTITUCE 3. ELIMINAČNÍ REAKCE VÝZNAMNÉ ALKANY. Substituční reakce. Sulfochlorace alkanů. Termolýza.
 Kromě CO 2 vznikají i saze roste svítivost Substituční reakce vazby: C C C H jsou nepolární => jsou radikálové S R...radikálová substituce 3 fáze... VLASTNOSTI ALKANŮ tady něco chybí... 2. RADIKÁLOVÁ SUBSTITUCE
Kromě CO 2 vznikají i saze roste svítivost Substituční reakce vazby: C C C H jsou nepolární => jsou radikálové S R...radikálová substituce 3 fáze... VLASTNOSTI ALKANŮ tady něco chybí... 2. RADIKÁLOVÁ SUBSTITUCE
NEKONVENČNÍ ZPŮSOBY VÝROBY TEPELNÉ A ELEKTRICKÉ ENERGIE. Ing. Stanislav HONUS
 NEKONVENČNÍ ZPŮSOBY VÝROBY TEPELNÉ A ELEKTRICKÉ ENERGIE Ing. Stanislav HONUS ORGANICKÝ MATERIÁL Spalování Chemické přeměny Chem. přeměny ve vodním prostředí Pyrolýza Zplyňování Chemické Biologické Teplo
NEKONVENČNÍ ZPŮSOBY VÝROBY TEPELNÉ A ELEKTRICKÉ ENERGIE Ing. Stanislav HONUS ORGANICKÝ MATERIÁL Spalování Chemické přeměny Chem. přeměny ve vodním prostředí Pyrolýza Zplyňování Chemické Biologické Teplo
V. Soustavy s chemickou reakcí
 V. Soustavy s chemickou reakcí 1 5. Soustavy s chemickou reakcí 5.1 Základní pojmy 5.2 Rozdělení reakcí 5.3 Reakční kinetika 5.3.1 Podmínky pro zreagování dvou molekul 5.3.2 Mechanismy reakce 5.3.3 Rychlost
V. Soustavy s chemickou reakcí 1 5. Soustavy s chemickou reakcí 5.1 Základní pojmy 5.2 Rozdělení reakcí 5.3 Reakční kinetika 5.3.1 Podmínky pro zreagování dvou molekul 5.3.2 Mechanismy reakce 5.3.3 Rychlost
Průmysl dusíku. amoniak - kyselina dusičná - dusičnan amonný - močovina - chloramin - hydrazin. NaClO NaOH CO(NH 2 ) 2.
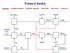 Průmysl dusíku amoniak - kyselina dusičná - dusičnan amonný - močovina - chloramin - hydrazin CO(NH 2 ) 2 NaClO NaOH NH 2 Cl N 2 H 4 methan CO 2 (uhlí, ropa) H 2 NH 3 NO 2 HNO 3 O 2 vzduch voda vzduch
Průmysl dusíku amoniak - kyselina dusičná - dusičnan amonný - močovina - chloramin - hydrazin CO(NH 2 ) 2 NaClO NaOH NH 2 Cl N 2 H 4 methan CO 2 (uhlí, ropa) H 2 NH 3 NO 2 HNO 3 O 2 vzduch voda vzduch
Autor: Tomáš Galbička Téma: Alkany a cykloalkany Ročník: 2.
 Alkany uhlovodíky s otevřeným řetězcem a pouze jednoduchými vazbami vazby sigma, největší výskyt elektronů na spojnici jader v názvu mají koncovku an Cykloalkany uhlovodíky s uzavřeným řetězcem a pouze
Alkany uhlovodíky s otevřeným řetězcem a pouze jednoduchými vazbami vazby sigma, největší výskyt elektronů na spojnici jader v názvu mají koncovku an Cykloalkany uhlovodíky s uzavřeným řetězcem a pouze
ALKOHOLY, FENOLY A ETHERY. b. Jaké zdroje cukru znáte a jak se nazývají produkty jejich kvašení?
 ALKOLY, FENOLY A ETHERY Kvašení 1. S použitím literatury nebo internetu odpovězte na následující otázky: a. Jakým způsobem v přírodě vzniká etanol? Napište rovnici. b. Jaké zdroje cukru znáte a jak se
ALKOLY, FENOLY A ETHERY Kvašení 1. S použitím literatury nebo internetu odpovězte na následující otázky: a. Jakým způsobem v přírodě vzniká etanol? Napište rovnici. b. Jaké zdroje cukru znáte a jak se
OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ. Seminář, Bratislava, 6.6.2013 Autor: J.LEDERER
 OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ Seminář, Bratislava, 6.6.2013 Autor: J.LEDERER OBSAH - CESTY K REDUKCI NOVOTVORBY CO 2 NEOBNOVITELNÉ SUROVINY OMEZENÍ UHLÍKOVÝCH
OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ Seminář, Bratislava, 6.6.2013 Autor: J.LEDERER OBSAH - CESTY K REDUKCI NOVOTVORBY CO 2 NEOBNOVITELNÉ SUROVINY OMEZENÍ UHLÍKOVÝCH
Herní otázky a jejich řešení:
 Herní otázky a jejich řešení: 1) Kde v přírodě můžeme najít methan? Methan je plyn, který je hlavní součástí zemního plynu, tvoří se také při přeměnách uhlí a dále vzniká mikrobiálním rozkladem celulosy
Herní otázky a jejich řešení: 1) Kde v přírodě můžeme najít methan? Methan je plyn, který je hlavní součástí zemního plynu, tvoří se také při přeměnách uhlí a dále vzniká mikrobiálním rozkladem celulosy
Zpracování ropy doc. Ing. Josef Blažek, CSc. 7. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 7. přednáška Spalování pohonných hmot, vlastnosti a použití plynných uhlovodíků
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 7. přednáška Spalování pohonných hmot, vlastnosti a použití plynných uhlovodíků
T E C H N I C K Á chemická odolnost membrána čistá polyurea TECNOCOAT P-2049
 TEKUTÁ OCHRANNÁ HYDROIZOLAČNÍ MEMBRÁNA T E C H N I C K Á S L O Ž K A chemická odolnost membrána čistá polyurea TECNOCOAT P-2049 Voda Solanka Odolná Chlorovaná Demineralizovaná voda voda H 2 O Destilovaná
TEKUTÁ OCHRANNÁ HYDROIZOLAČNÍ MEMBRÁNA T E C H N I C K Á S L O Ž K A chemická odolnost membrána čistá polyurea TECNOCOAT P-2049 Voda Solanka Odolná Chlorovaná Demineralizovaná voda voda H 2 O Destilovaná
Gymnázium Jana Pivečky a Střední odborná škola Slavičín Mgr. Veronika Prchlíková III/2 Inovace a zkvalitnění výuky prostřednictvím ITC
 Název projektu Číslo projektu Název školy Autor Název šablony Název DUMu Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748 Gymnázium Jana Pivečky a Střední odborná škola Slavičín Mgr.
Název projektu Číslo projektu Název školy Autor Název šablony Název DUMu Inovace výuky prostřednictvím šablon pro SŠ CZ.1.07/1.5.00/34.0748 Gymnázium Jana Pivečky a Střední odborná škola Slavičín Mgr.
Škola: Gymnázium, Brno, Slovanské náměstí 7 III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT Inovace výuky na GSN prostřednictvím ICT
 VY_32_INOVACE_C.3.01 Škola: Gymnázium, Brno, Slovanské náměstí 7 Šablona: Název projektu: Číslo projektu: Autor: Tematická oblast: Název DUMu: Kód: III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT
VY_32_INOVACE_C.3.01 Škola: Gymnázium, Brno, Slovanské náměstí 7 Šablona: Název projektu: Číslo projektu: Autor: Tematická oblast: Název DUMu: Kód: III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT
Ch - Uhlovodíky VARIACE
 Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukových materiálů je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE Tento dokument byl kompletně vytvořen, sestaven a vytištěn
Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukových materiálů je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE Tento dokument byl kompletně vytvořen, sestaven a vytištěn
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie Tercie 2 hodiny týdně Školní tabule, interaktivní tabule, Apple TV, tablety, tyčinkové a kalotové modely molekul,
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie Tercie 2 hodiny týdně Školní tabule, interaktivní tabule, Apple TV, tablety, tyčinkové a kalotové modely molekul,
Charakteristika Teorie kyselin a zásad. Příprava kyselin Vlastnosti + typické reakce. Významné kyseliny. Arrheniova teorie Teorie Brönsted-Lowryho
 Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
Petra Ustohalová 1 harakteristika Teorie kyselin a zásad Arrheniova teorie Teorie Brönsted-Lowryho Příprava kyselin Vlastnosti + typické reakce Fyzikální a chemické Významné kyseliny 2 Látky, které ve
CH 2 = CH 2 ethen systematický název propen CH 2 = CH CH 3 but-1-en CH 2 = CH CH 2 CH 3 but-2-en CH 3 CH = CH CH 3 buta-1,3-dien CH 2 = CH CH = CH 2
 Základní názvy organických látek alifatické nasycené alkany (příklady s nerozvětvenými řetězci) methan CH 4 ethan CH 3 CH 3 propan CH 3 CH 2 CH 3 butan CH 3 CH 2 CH 2 CH 3 pentan CH 3 CH 2 CH 2 CH 2 CH
Základní názvy organických látek alifatické nasycené alkany (příklady s nerozvětvenými řetězci) methan CH 4 ethan CH 3 CH 3 propan CH 3 CH 2 CH 3 butan CH 3 CH 2 CH 2 CH 3 pentan CH 3 CH 2 CH 2 CH 2 CH
(Text s významem pro EHP) (2012/C 387/06)
 CS 15.12.2012 Úřední věstník Evropské unie C 387/5 Sdělení Komise, kterým se mění sdělení Komise Pokyny k některým opatřením státní podpory v souvislosti se systémem obchodování s povolenkami na emise
CS 15.12.2012 Úřední věstník Evropské unie C 387/5 Sdělení Komise, kterým se mění sdělení Komise Pokyny k některým opatřením státní podpory v souvislosti se systémem obchodování s povolenkami na emise
Pyrolýzní technologie pro možnosti energetického a materiálového využití odpadů
 Pyrolýzní technologie pro možnosti energetického a materiálového využití odpadů Petr Pavlík a;b a VŠB Technická Univerzita Ostrava, Centrum ENET Energetické jednotky pro využití netradičních zdrojů energie
Pyrolýzní technologie pro možnosti energetického a materiálového využití odpadů Petr Pavlík a;b a VŠB Technická Univerzita Ostrava, Centrum ENET Energetické jednotky pro využití netradičních zdrojů energie
materiál č. šablony/č. sady/č. materiálu: Autor:
 Masarykova základní škola Klatovy, tř. Národních mučedníků 185, 339 01 Klatovy; 376312154, fax 376326089 E-mail: skola@maszskt.investtel.cz; internet: www.maszskt.investtel.cz Kód přílohy vzdělávací VY_32_INOVACE_CH8SA_01_03_14
Masarykova základní škola Klatovy, tř. Národních mučedníků 185, 339 01 Klatovy; 376312154, fax 376326089 E-mail: skola@maszskt.investtel.cz; internet: www.maszskt.investtel.cz Kód přílohy vzdělávací VY_32_INOVACE_CH8SA_01_03_14
ČESKÉ RAFINÉRSKÉ, a.s.
 Bilance vodíku v ČESKÉ RAFINÉRSKÉ, a.s. APROCHEM 2010 Kouty nad Desnou 19 21.4.2010 Ing.Hugo Kittel, CSc., MBA www.ceskarafinerska.cz 1 Obsah Úvod do problému Zdroje vodíku pro rafinérie Využití vodíku
Bilance vodíku v ČESKÉ RAFINÉRSKÉ, a.s. APROCHEM 2010 Kouty nad Desnou 19 21.4.2010 Ing.Hugo Kittel, CSc., MBA www.ceskarafinerska.cz 1 Obsah Úvod do problému Zdroje vodíku pro rafinérie Využití vodíku
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/
 Uhlovodíky Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Alkany jsou nasycené uhlovodíky s jednoduchými vazbami mezi atomy uhlíku (v uhlíkovém řetězci).
Uhlovodíky Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Alkany jsou nasycené uhlovodíky s jednoduchými vazbami mezi atomy uhlíku (v uhlíkovém řetězci).
Školní výstupy Učivo (pojmy) Poznámka
 Vyučovací předmět: Chemie (Ch) Ročník Předmět Průřezová témata Mezipředmět. vazby Školní výstupy Učivo (pojmy) Poznámka Období splnění Metodická poznámka Rozsah vyžadovaného učiva OSV 1 (praktické pokusy)
Vyučovací předmět: Chemie (Ch) Ročník Předmět Průřezová témata Mezipředmět. vazby Školní výstupy Učivo (pojmy) Poznámka Období splnění Metodická poznámka Rozsah vyžadovaného učiva OSV 1 (praktické pokusy)
DERIVÁTY - OPAKOVÁNÍ
 DERIVÁTY - OPAKOVÁNÍ Doplňte k názvu derivátu uhlovodíku charakteristickou skupinu: alkohol Název derivátu Charakteristická skupina nitroderivát karboxylová kyselina aldehyd halogenderivát keton Doplňte
DERIVÁTY - OPAKOVÁNÍ Doplňte k názvu derivátu uhlovodíku charakteristickou skupinu: alkohol Název derivátu Charakteristická skupina nitroderivát karboxylová kyselina aldehyd halogenderivát keton Doplňte
2.4 AROMATICKÉ UHLOVODÍKY
 2.4 AROMATICKÉ UHLOVODÍKY Označení aromatické uhlovodíky sice historicky souvisí s charakteristickým zápachem mnohých z nich (např. benzen páchne po dehtu, toluen zapáchá jako toluánský balzám či benzaldehyd
2.4 AROMATICKÉ UHLOVODÍKY Označení aromatické uhlovodíky sice historicky souvisí s charakteristickým zápachem mnohých z nich (např. benzen páchne po dehtu, toluen zapáchá jako toluánský balzám či benzaldehyd
Vodík jako alternativní ekologické palivo. palivové články a vodíkové hospodářství
 Vodík jako alternativní ekologické palivo palivové články a vodíkové hospodářství Charakteristika vodíku vodík je nejrozšířenějším prvkem ve vesmíru na Zemi je třetím nejrozšířenějším prvkem po kyslíku
Vodík jako alternativní ekologické palivo palivové články a vodíkové hospodářství Charakteristika vodíku vodík je nejrozšířenějším prvkem ve vesmíru na Zemi je třetím nejrozšířenějším prvkem po kyslíku
Škola: Gymnázium, Brno, Slovanské náměstí 7 III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT Inovace výuky na GSN prostřednictvím ICT
 Škola: Gymnázium, Brno, Slovanské náměstí 7 Šablona: Název projektu: Číslo projektu: Autor: Tematická oblast: Název DUMu: Kód: III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT Inovace výuky na GSN
Škola: Gymnázium, Brno, Slovanské náměstí 7 Šablona: Název projektu: Číslo projektu: Autor: Tematická oblast: Název DUMu: Kód: III/2 - Inovace a zkvalitnění výuky prostřednictvím ICT Inovace výuky na GSN
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
ARENY. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: Ročník: devátý
 Autor: Mgr. Stanislava Bubíková ARENY Datum (období) tvorby: 13. 9. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci se seznámí s areny. V rámci tohoto
Autor: Mgr. Stanislava Bubíková ARENY Datum (období) tvorby: 13. 9. 2012 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Organické sloučeniny 1 Anotace: Žáci se seznámí s areny. V rámci tohoto
OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ. Most, Autor: Doc. Ing. J.LEDERER, CSc.
 OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ Most, 29.11.2012 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH - CESTY K REDUKCI NOVOTVORBY CO 2 NEOBNOVITELNÉ SUROVINY OMEZENÍ
OMEZOVÁNÍ NEGATIVNÍCH ENVIRONMENTÁLNÍCH DOPADŮ PŘI VÝROBĚ PALIV A PETROCHEMIKÁLIÍ Most, 29.11.2012 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH - CESTY K REDUKCI NOVOTVORBY CO 2 NEOBNOVITELNÉ SUROVINY OMEZENÍ
Rozezná a vysvětlí význam označení různých nebezpečných látek. Vybrané dostupné látky pojmenuje a vysvětlí jejich nebezpečnost.
 Vyučovací předmět: Ročník Předmět Průřezová témata Mezipředmět. vazby F emie () Školní výstupy Učivo (pojmy) Poznámka OSV 1 (praktické pokusy) Na konkrétních příkladech rozliší látky a tělesa, pokusným
Vyučovací předmět: Ročník Předmět Průřezová témata Mezipředmět. vazby F emie () Školní výstupy Učivo (pojmy) Poznámka OSV 1 (praktické pokusy) Na konkrétních příkladech rozliší látky a tělesa, pokusným
(Nelegislativní akty) NAŘÍZENÍ
 10.2.2012 Úřední věstník Evropské unie L 37/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE (EU) č. 109/2012 ze dne 9. února 2012, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1907/2006
10.2.2012 Úřední věstník Evropské unie L 37/1 II (Nelegislativní akty) NAŘÍZENÍ NAŘÍZENÍ KOMISE (EU) č. 109/2012 ze dne 9. února 2012, kterým se mění nařízení Evropského parlamentu a Rady (ES) č. 1907/2006
Zpracování ropy - Pracovní list
 Číslo projektu Název školy Předmět CZ.107/1.5.00/34.0425 INTEGROVANÁ STŘEDNÍ ŠKOLA TECHNICKÁ BENEŠOV Černoleská 1997, 256 01 Benešov BIOLOGIE A EKOLOGIE Tematický okruh Téma Ročník 2. Autor Datum výroby
Číslo projektu Název školy Předmět CZ.107/1.5.00/34.0425 INTEGROVANÁ STŘEDNÍ ŠKOLA TECHNICKÁ BENEŠOV Černoleská 1997, 256 01 Benešov BIOLOGIE A EKOLOGIE Tematický okruh Téma Ročník 2. Autor Datum výroby
Gymnázium Jiřího Ortena, Kutná Hora
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie Tercie 2 hodiny týdně Školní tabule, interaktivní tabule, Apple TV, tablety, tyčinkové a kalotové modely molekul,
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Chemie (CHE) Obecná chemie, anorganická chemie Tercie 2 hodiny týdně Školní tabule, interaktivní tabule, Apple TV, tablety, tyčinkové a kalotové modely molekul,
Omezování plynných emisí. Ochrana ovzduší ZS 2012/2013
 Omezování plynných emisí Ochrana ovzduší ZS 2012/2013 1 Úvod Různé fyzikální a chemické principy + biotechnologie Principy: absorpce adsorpce oxidace a redukce katalytická oxidace a redukce kondenzační
Omezování plynných emisí Ochrana ovzduší ZS 2012/2013 1 Úvod Různé fyzikální a chemické principy + biotechnologie Principy: absorpce adsorpce oxidace a redukce katalytická oxidace a redukce kondenzační
Zpracování ropy doc. Ing. Josef Blažek, CSc. 9. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 9. přednáška Emise ze zpracování ropy, BREF, komplexita rafinérií Emise
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 9. přednáška Emise ze zpracování ropy, BREF, komplexita rafinérií Emise
Chemické principy průmyslových výrob
 Chemické principy průmyslových výrob Jiří Vohlídal Katedra fyzikální a makromolekulární chemie Přírodovědecká fakulta University Karlovy, Praha Jiří Čejka Ústav fyzikální chemie Jaroslava Heyrovského Akademie
Chemické principy průmyslových výrob Jiří Vohlídal Katedra fyzikální a makromolekulární chemie Přírodovědecká fakulta University Karlovy, Praha Jiří Čejka Ústav fyzikální chemie Jaroslava Heyrovského Akademie
KARBOXYLOVÉ KYSELINY C OH COOH. řešení. uhlovodíkový zbytek. KARBOXYLOVÝCH funkčních skupin. - obsahují 1 či více
 KARBXYLVÉ KYSELINY - obsahují 1 či více KARBXYLVÝCH funkčních skupin. - nejvyšší organické oxidační produkty uhlovodíků řešení R CH R C H R = uhlovodíkový zbytek 1 KARBXYLVÉ KYSELINY Dělení dle: a) typu
KARBXYLVÉ KYSELINY - obsahují 1 či více KARBXYLVÝCH funkčních skupin. - nejvyšší organické oxidační produkty uhlovodíků řešení R CH R C H R = uhlovodíkový zbytek 1 KARBXYLVÉ KYSELINY Dělení dle: a) typu
Přírodní zdroje uhlovodíků
 Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Říjen 2010 Mgr. Alena Jirčáková Zemní plyn - vznik: Výskyt často spolu s ropou (naftový zemní plyn) nebo
Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Říjen 2010 Mgr. Alena Jirčáková Zemní plyn - vznik: Výskyt často spolu s ropou (naftový zemní plyn) nebo
Opakování učiva organické chemie Smart Board
 Opakování učiva organické chemie Smart Board VY_52_INOVACE_200 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie ročník: 9 Projekt EU peníze školám Operačního programu Vzdělávání pro konkurenceschopnost
Opakování učiva organické chemie Smart Board VY_52_INOVACE_200 Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Chemie ročník: 9 Projekt EU peníze školám Operačního programu Vzdělávání pro konkurenceschopnost
Aromacké uhlovodíky reakce
 Aromacké uhlovodíky reakce Temacká oblast : Chemie organická chemie Datum vytvoření: 20. 7. 2012 Ročník: 2. ročník čtyřletého gymnázia (sexta osmiletého gymnázia) Stručný obsah: Reakce výroby nesubstuovaných
Aromacké uhlovodíky reakce Temacká oblast : Chemie organická chemie Datum vytvoření: 20. 7. 2012 Ročník: 2. ročník čtyřletého gymnázia (sexta osmiletého gymnázia) Stručný obsah: Reakce výroby nesubstuovaných
PARAMO Pardubice. Studijní materiál k předmětu Chemická exkurze C6950 Brno 2011
 Studijní materiál k předmětu Chemická exkurze C6950 Brno 2011 PARAMO Pardubice Vypracoval: Mgr. Radek Matuška Úpravy: Mgr. Zuzana Garguláková, doc. Ing. Vladimír Šindelář, Ph.D. Obecné informace PARAMO,
Studijní materiál k předmětu Chemická exkurze C6950 Brno 2011 PARAMO Pardubice Vypracoval: Mgr. Radek Matuška Úpravy: Mgr. Zuzana Garguláková, doc. Ing. Vladimír Šindelář, Ph.D. Obecné informace PARAMO,
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STROJNÍHO INŽENÝRSTVÍ - ENERGETICKÝ ÚSTAV ODBOR TERMOMECHANIKY A TECHNIKY
 VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STROJNÍHO INŽENÝRSTVÍ - ENERGETICKÝ ÚSTAV ODBOR TERMOMECHANIKY A TECHNIKY PROSTŘEDÍ doc. Ing. Josef ŠTETINA, Ph.D. Předmět 3. ročníku BS http://ottp.fme.vutbr.cz/sat/
VYSOKÉ UČENÍ TECHNICKÉ V BRNĚ FAKULTA STROJNÍHO INŽENÝRSTVÍ - ENERGETICKÝ ÚSTAV ODBOR TERMOMECHANIKY A TECHNIKY PROSTŘEDÍ doc. Ing. Josef ŠTETINA, Ph.D. Předmět 3. ročníku BS http://ottp.fme.vutbr.cz/sat/
Reaktory pro systém plyn kapalina
 FCHT Reaktory pro systém plyn kapalina Lubomír Krabáč 1 Probublávané reaktory: příklady procesů oxidace organických látek kyslíkem, resp. vzduchem chlorace hydrogenace org. látek s homogenním katal. vyšších
FCHT Reaktory pro systém plyn kapalina Lubomír Krabáč 1 Probublávané reaktory: příklady procesů oxidace organických látek kyslíkem, resp. vzduchem chlorace hydrogenace org. látek s homogenním katal. vyšších
Průmyslově vyráběná paliva
 Registrační číslo projektu: CZ.1.07/1.1.38/02.0025 Název projektu: Modernizace výuky na ZŠ Slušovice, Fryšták, Kašava a Velehrad Tento projekt je spolufinancován z Evropského sociálního fondu a státního
Registrační číslo projektu: CZ.1.07/1.1.38/02.0025 Název projektu: Modernizace výuky na ZŠ Slušovice, Fryšták, Kašava a Velehrad Tento projekt je spolufinancován z Evropského sociálního fondu a státního
Amoniak. 1913 průmyslová výroba syntetického amoniaku
 Amoniak 1913 průmyslová výroba syntetického amoniaku využití 20 % výroba dusíkatých hnojiv 80 % nejrůznější odvětví průmyslu (plasty, vlákna, výbušiny, hydrazin, aminy, amidy, nitrily a další organické
Amoniak 1913 průmyslová výroba syntetického amoniaku využití 20 % výroba dusíkatých hnojiv 80 % nejrůznější odvětví průmyslu (plasty, vlákna, výbušiny, hydrazin, aminy, amidy, nitrily a další organické
EU peníze středním školám digitální učební materiál
 EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
Reálné gymnázium a základní škola města Prostějova Školní vzdělávací program pro ZV Ruku v ruce
 6 ČLOVĚK A PŘÍRODA UČEBNÍ OSNOVY 6. 2 Chemie Časová dotace 8. ročník 2 hodiny 9. ročník 2 hodiny Celková dotace na 2. stupni je 4 hodiny. Charakteristika: Vyučovací předmět chemie vede k poznávání chemických
6 ČLOVĚK A PŘÍRODA UČEBNÍ OSNOVY 6. 2 Chemie Časová dotace 8. ročník 2 hodiny 9. ročník 2 hodiny Celková dotace na 2. stupni je 4 hodiny. Charakteristika: Vyučovací předmět chemie vede k poznávání chemických
CELIO a.s. CZU Linka na úpravu odpadů za účelem jejich dalšího energetického využití SLUDGE
 CELIO a.s. CZU00168 Linka na úpravu odpadů za účelem jejich dalšího energetického využití SLUDGE Kód Název odpadu Příjem Pro úpravu 01 05 04 O Vrtné kaly a odpady obsahující sladkou vodu 01 05 05 N Vrtné
CELIO a.s. CZU00168 Linka na úpravu odpadů za účelem jejich dalšího energetického využití SLUDGE Kód Název odpadu Příjem Pro úpravu 01 05 04 O Vrtné kaly a odpady obsahující sladkou vodu 01 05 05 N Vrtné
Názvosloví Konformace Isomerie. Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o )
 ALKANY 1 Názvosloví Konformace Isomerie Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o ) 2 Alkany (resp. cykloalkany) jsou nejzákladnější organické sloučeniny složené pouze z
ALKANY 1 Názvosloví Konformace Isomerie Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o ) 2 Alkany (resp. cykloalkany) jsou nejzákladnější organické sloučeniny složené pouze z
