Fyzika biopolymerů. Struktura a vlastnosti vody, vodíková vazba
|
|
|
- Jaromír Macháček
- před 9 lety
- Počet zobrazení:
Transkript
1 Fyzika biopolymerů Struktura a vlastnosti vody, vodíková vazba
2 Pět základních podmínek pro život na Zemi přítomnost uhlíku a dalších důležitých prvků tvořících biomolekuly voda v blízkosti povrchu vhodná atmosféra dlouhá perioda termální stability, zaručující tekutou vodu bohaté zdroje ostatních prvků
3 Obecné vlastnosti vody
4 Teplotní anomálie vody charakteristická vlastnost vody významná pro existenci života na Zemi hustotní maximum při 4 C led má menší hustotu než kapalná voda, a proto plave na hladině
5 Neobvyklé fyzikální vlastnosti měrná tepelná kapacita voda má silnou schopnost absorbovat teplo (teplota takového systému roste jen zvolna)
6 Neobvyklé fyzikální vlastnosti velká tepelná vodivost (~4x větší než jiné kapaliny)
7 Neobvyklé fyzikální vlastnosti fázové přechody - skupenské teplo je asi 3x větší než u ostatních kapalin
8 Neobvyklé fyzikální vlastnosti nízká viskozita
9 Neobvyklé fyzikální vlastnosti povrchové napětí voda má velké povrchové napětí znemožňuje vytečení malými otvory (důležité pro existenci buněk) poměr povrchového napětí a viskozity většina kapalin má při nízkém povrch. napětí i nízkou viskozitu voda má vysoké povrchové napětí a nízkou viskozitu
10 Neobvyklé fyzikální vlastnosti dielektrické vlastnosti ε dielektrická konstanta udává, jak efektivně médium zmenšuje elektrickou sílu mezi náboji voda má jednu z nejvyšších diel. konstant mezi kapalinami
11 Závislost dielektrické konstanty na teplotě Dielektrická konstanta vody roste až do -70 C, až potom klesá.
12
13 Voda fyzikálně chemické vlastnosti jsou rozdílné od chemicky podobných látek (jako H 2 Te, H 2 Se, H 2 S, atd.) při extrapolaci vlastností těchto látek na vodu by T tání ~ -100 C a T varu ~ -30 C podobně při extrapolaci obecné řady alkoholů C n H 2n+1 OH (1. člen řady pro n=1 je HOH) existence neobvykle silné interakce, která se nazývá vodíková vazba
14 Molekula vody každá voda se může podílet na 4 vodíkových vazbách (2x vodíky, 2x volnými elektronovými páry na kyslíku)
15 Vodíková vazba vazba mezi dvěma elektronegativními atomy zprostředkovaná vodíkem kromě vody tvoří vodíkové vazby další elektronegativní atomy (O, F, N) neexistuje jednoduchá rovnice pro vyjádření interakčního potenciálu energie je úměrná 1/r 2 tvorba H-vazeb je kooperativní proces (souvisí se změnou elektronové hustoty)
16
17 Definice vodíkové vazby podle IUPAC (2011) The hydrogen nond is an attractive interaction between a hydrogen atom from a molecule or a molecular fragment X-H in which X is more electronegative than H, and an atom or a group of atoms in the same or a different molecule, in which there is evidence of bond formation. Kritéria existence H-vazby X-H...Y-Z: -na vzniku H-vazby se podílejí interakce elektrostatického původu, interakce v důsledku přenosu náboje mezi donorem a akceptorem, které vedou k vytvoření částečné kovalentní vazby mezi H a Y, a disperzní interakce -atomy X a H jsou spojeny kovalentní vazbou, která je polarizovaná, s rostoucí elektronegativitou X roste i síla vazby H...Y -X-H...Y je obvykle planární, čím se úhel více blíží 180, tím je vazba silnější a vzdálenost H...Y menší
18 Definice vodíkové vazby podle IUPAC (2011) Kritéria existence H-vazby X-H...Y-Z: -při vzniku H-vazby obvykle dochází k nárůstu délky X-H vazby v IR spektroskopii pozorován červený posun -vykazuje charakteristické signatury v NMR spektroskopii Gibbsova energie H-vazby by měla být větší než termální energie Poznámky: -kritérium, že délka H-vazby je menší než součet vdw poloměrů, neplatí obecně, pouze pro silné H-vazby -existují i H-vazby, které způsobují modrý nebo žádný posun vibračních frekvencí
19 Počet H-vazeb, které může molekula tvořit: 2 tvorba 1D řetězců či cyklických útvarů (HF, alkoholy) podobně dvojvazné atomy Se a Te tvoří dlouhé řetězce kovalentně vázaných atomů 3 tvorba 2D vrstevnatých struktur, které drží pohromadě slabými VDW silami (uhlík v grafitu) 4 a více tvorba 3D struktur (C, Si) polymery, proteiny, DNA, uhlík v diamantu a) 3D struktura (led) b) 2D struktura (formamid) c) 1D struktura (alkohol, HF) d) dimer (mastné kys.) e) intramolekulární HB f) symetrická HB (sdílení H)
20 dominance vodíkových vazeb dokonce i ve velmi polárních molekulách (např. aceton) vzrůstající důležitost disperzních interakcí u velkých molekul
21 Směrovost a síla vodíkové vazby vodíkové vazby kj/mol (5-10 kt) VDW interakce ~1 kj/mol (~1 kt) kovalentní vazby ~500 kj/mol (~100 kt)
22 Vodíkové vazby v nukleových kyselinách
23 Vodíkové vazby v proteinech Podíl na stabilizaci α-helixu a β-sheetu
24 H-vazby pozorované pomocí AFM Zhang et al., Science, 2013
25 Struktura ledu tetrahedrální struktura na každou molekulu vody připadají 4 vodíkové vazby úhel mezi vazbami je (v kapalné vodě je to ) Vzdálenosti O-H: intramolekulární 0.10 nm intermolekulární nm součet vdw poloměrů je ale 0.26 nm vodíková vazba
26 Kapalná voda počet sousedů je 5, průměrný počet vodíkových vazeb na molekulu je ~3.5, úhel menší než v ledu v ledu je průměrný počet vodíkových vazeb 4, tetrahedrální uspořádání je částečně zachováno i po roztání ledu silné intermolekulární interakce vytvořené v ledu jsou částečně zachovány i v kapalině molekuly vody vyplňují mezery přítomné ve struktuře ledu v ledu je vyšší protonová vodivost a mobilita (protony přeskakují podél sítě vodíkových vazeb Grotthussův mechanismus)
27 Klastrování vody se vzrůstající teplotou ubývá molekul vod v klastrech T(tání) ~ vod v klastru T(varu) ~ molekul v klastru vliv na viskozitu a její teplotní závislost doba života H-vazby: s, klastru s
28 Modely vody realistické modely jsou nezbytné pro úspěšné simulace v explicitním solventu 3-atomový model nejrozšířenější (popis pomocí 8 parametrů) nejznámější 3-atomové modely TIP3P, SPC/E reprodukce experimentálních dat (struktura, hustota, měrné skupenské teplo varu, rychlost difúze, permitivita) TIP3P měrné teplo, permitivita dobře, hustota podceněna, difúze výrazně přeceněna SPC/E hustota, difúze dobře, měrné teplo přeceněno, permitivita podceněna problém s popisem vlastností v závislosti na teplotě
29 Modely vody vylepšené modely s nábojem mimo centrum O (TIP4P, TIP5P) modely s fixovanými náboji neumožňují změnu dipólového momentu (dipól. moment vody v plynné fázi 1.85 D, v kapalné 3 D) vývoj polarizačních modelů vody (TIP4P/FQ) vyšší výpočetní náročnost
30 Solvatace iontu primární hydratace v přímém kontaktu s iontem tvoří ji malá část molekul vody, které jsou silně orientované v elektrickém poli iontu (strukturovaná voda), omezen jejich pohyb sekundární hydratace voda v kontaktu s vodou z primární hydratační vrstvy elektrické pole iontu je již příliš slabé, aby zorientovalo molekuly vody, je však dost silné na narušení normální struktury vody efekt je mnohem slabší a ve většině případů lze zanedbat (výjimkou jsou malé multivalentní ionty Al +3, Cr +3 )
31 Parametry solvatace solvatační číslo počet vod ovlivněných iontem (lze zjistit pomocí NMR) relativní rezidenční časy vlastní difúze (difúze vody ve vodě) čas t i (voda v blízkosti iontu), t (voda v blízkosti jiné vody), t i /t určuje stupeň demobilizace vody v blízkosti iontu t i /t > 1 zvýšení strukturního stupně vody v blízkosti iontu t i /t < 1 narušení struktury vody (chaotropní ionty) Stokesův poloměr r H efektivní poloměr makroskopické sféry s hydrofilním povrchem, může být uplatněn Stokesův zákon r r F = 6πηrv
32 chaotropní ionty: r H < r krystal (např. K +, Cs + ) oblast sekundární hydratace je větší než primární kosmotropní ionty r H >> r krystal (např. Li +, Na +, Mg 2+, Ca 2+ ) větší oblast primární hydratace rozdíl Na + a K + : oba nesou stejný náboj, r krystal (efektivní poloměr vnější elektronové slupky je ale větší pro K+ díky dalšímu elektron. orbitalu větší vzdálenost od jádra vede k zeslabení el. pole a ovlivnění H- vazeb v přímém sousedství iontu
33 Hydrofobní efekt molekuly vody mají tendenci se vzájemně spojovat pomocí vodíkových vazeb v okolí nepolárních molekul (netvoří vodíkové vazby) existuje riziko ztráty vodíkové vazby (max. počet vodíkových vazeb je 4) nejlepší konfigurace = všechny vodíkové vazby zachovány, směřují do vodní fáze (lze zajistit jen pokud solut není příliš velký)
34 Hydrofobní efekt v kapalné vodě tvoří každá molekula průměrně ~ vodíkových vazeb pokud se kolem inertní molekuly vytvoří útvar se 4 vodíkovými vazbami na molekulu tyto molekuly mají díky vyšší koordinaci nižší energii (entalpii) než vody v okolním solventu entropicky je toto uspořádání velmi nevýhodné, protože ruší existující struktury vody a vytváří nové organizovanější struktury vody v okolí nepolární molekuly velké povrchy jiná situace (zde existují jen 3 vodíkové vazby), závislost na velikosti a povrchu solutu
35 Hydrofobní interakce neobvykle silná přitažlivá interakce mezi hydrofobními molekulami a povrchy ve vodě často je silnější než jejich přitahování ve vakuu VDW energie 2 molekul CH 4 : vakuum voda J J původ není v žádné specifické vazbě, je to entropický fenomén v důsledku přeskupení vodíkových vazeb dosud neexistuje žádná uspokojivá teorie pro výpočet této interakce (příliš komplexní, dalekodosahová, nutnost zahrnutí mnoha dalších molekul)
36 Hydrofilní interakce hydrofilní molekuly upřednostňují kontakt s vodou (více než vzájemný kontakt) často jsou gyroskopické hydrofilní polymery se mohou ve vodě zvětšit až 1000x = hydrogely jsou to silně hydratované ionty, zwitterionty, ale také některé nenabité či nepolární molekuly (požadavek správné geometrie a schopnosti tvořit vodíkové vazby s vodou) např. kyslíky v C=O, -OH, dusíky v aminech polární skupina nemusí být vždy hydrofilní a nepolární skupina nemusí být vždy hydrofobní!
37 Hydrofilní interakce
38 Experimentální metody studia solvatace rentgenová difrakce přímá evidence přítomnosti vody v interakci s biomolekulou elektron. hustota se průměruje přes čas a velké množství struktur dynamická povaha vody horší určení polohy vody kryogenetické podmínky ovlivnění struktury solventu (klastry) neutronová difrakce vidí vodíky, vhodná ke studiu vody SAXS, SANS NMR strukturní i dynamické informace o vodě v blízkosti biomolekuly NOE: sledování solventu v přímé interakci s danou biomolekulou, omezené časové rozlišení (přecenění rezidenčních časů)
39 Experimentální metody studia optická spektroskopie solvatace femtosekund. fluorescenční spektroskopie flurescenč. pík je citlivý na dipól. moment sondy, který závisí na polarizaci solventu kombinace vysokého časového rozlišení s prostorovým rozlišením infračervená spektroskopie spektra jsou zvlášť citlivá na tvorbu H-vazeb, umožňuje studovat specifické interakce solut-solvent, kvalitativní informace dielektrická disperze frekvenční závislost permitivity, omezené rozlišení
40 Solvatace biomolekul solvent je nezbytný pro funkci biologických systémů, které ovlivňuje: přímo (aktivní účast v biologických procesech) nepřímo (stabilizace biologicky aktivních konformací biomolekul) interakce solut-voda silně ovlivňuje konformace peptidů hydrofobní efekt u protein foldingu, sekundární strukturní preference u peptidů solvent hraje klíčovou roli při tvorbě komplexů, rozpoznávání ligandů, interakcí mezi DNA a proteiny voda se účastní řady biochemických procesů může působit jako báze či kyselina
41 Hydratace biopolymerů proteiny hydrofóbní efekt elektrostatický screening nukleové kyseliny oproti proteinům mají 2 rozdíly: každý nukleotid nese záporný náboj (proteiny jsou skoro neutrální) netvoří globulární struktury (RNA tvoří kompaktnější struktury, folding řízen jinak než u proteinů) interakce se solventem jsou silnější než u proteinů
42 spine of hydration
43 Vázaná voda biomolekuly mají vodu semipermanentně navázanou na povrchu nebo uvnitř, některé vody mají specifickou chemickou roli vázané molekuly vody mají často jiné vlastnosti než voda v okolním solventu
Mezimolekulové interakce
 Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
Mezimolekulové interakce Interakce molekul reaktivně vzniká či zaniká kovalentní vazba překryv elektronových oblaků, mění se vlastnosti nereaktivně vznikají molekulové komplexy slabá, nekovalentní, nechemická,
Opakování
 Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
Slabé vazebné interakce Opakování Co je to atom? Opakování Opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího protony a neutrony
02 Nevazebné interakce
 02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
02 Nevazebné interakce Nevazebné interakce Druh chemické vazby Určují 3D konfiguraci makromolekul, účastní se mnoha biologických procesů, zodpovědné za uspořádání molekul v krystalu Síla nevazebných interakcí
Skupenské stavy. Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
 Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Skupenské stavy Plyn Zcela neuspořádané Hodně volného prostoru Zcela volný pohyb částic Částice daleko od sebe Kapalina Částečně neuspořádané Volný pohyb částic nebo skupin částic Částice blíže u sebe
Typy molekul, látek a jejich vazeb v organismech
 Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Typy molekul, látek a jejich vazeb v organismech Typy molekul, látek a jejich vazeb v organismech Organismy se skládají z molekul rozličných látek Jednotlivé látky si organismus vytváří sám z jiných látek,
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 3. listopadu 2016 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 3. listopadu 2016 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii
Nekovalentní interakce
 Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Nekovalentní interakce Jan Řezáč UOCHB AV ČR 31. října 2017 Jan Řezáč (UOCHB AV ČR) Nekovalentní interakce 31. října 2017 1 / 28 Osnova 1 Teorie 2 Typy nekovalentních interakcí 3 Projevy v chemii 4 Výpočty
Chemická vazba. Příčinou nestability atomů a jejich ochoty tvořit vazbu je jejich elektronový obal.
 Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
Chemická vazba Volné atomy v přírodě jen zcela výjimečně (vzácné plyny). Atomy prvků mají snahu se navzájem slučovat a vytvářet molekuly prvků nebo sloučenin. Atomy jsou v molekulách k sobě poutány chemickou
 Chemická vazba Něco málo opakování Něco málo opakování Co je to atom? Něco málo opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího
Chemická vazba Něco málo opakování Něco málo opakování Co je to atom? Něco málo opakování Co je to atom? Atom je nejmenší částice hmoty, chemicky dále nedělitelná. Skládá se z atomového jádra obsahujícího
Chemie. Mgr. Petra Drápelová Mgr. Jaroslava Vrbková. Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou
 Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA VY_32_INOVACE_03_3_07_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA Volné atomy v přírodě
Chemie Mgr. Petra Drápelová Mgr. Jaroslava Vrbková Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA VY_32_INOVACE_03_3_07_CH Gymnázium, SOŠ a VOŠ Ledeč nad Sázavou CHEMICKÁ VAZBA Volné atomy v přírodě
Vazby v pevných látkách
 Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
Vazby v pevných látkách Hlavní body 1. Tvorba pevných látek 2. Van der Waalsova vazba elektrostatická interakce indukovaných dipólů 3. Iontová vazba elektrostatická interakce iontů 4. Kovalentní vazba
Molekulární krystal vazebné poměry. Bohumil Kratochvíl
 Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
Molekulární krystal vazebné poměry Bohumil Kratochvíl Předmět: Chemie a fyzika pevných léčiv, 2017 Složení farmaceutických substancí - API Z celkového portfolia API tvoří asi 90 % organické sloučeniny,
Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118
 Chemická vazba Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118 Chemická vazba Většina atomů má tendenci se spojovat do větších celků (molekul), v nichž jsou vzájemně vázané chemickou vazbou. Chemická vazba je
Chemická vazba Mgr. Jakub Janíček VY_32_INOVACE_Ch1r0118 Chemická vazba Většina atomů má tendenci se spojovat do větších celků (molekul), v nichž jsou vzájemně vázané chemickou vazbou. Chemická vazba je
Dynamické procesy & Pokročilé aplikace NMR. chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů
 Dynamické procesy & Pokročilé aplikace NMR chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů Chemická výměna jakýkoli proces při kterém dané jádro mění svůj stav
Dynamické procesy & Pokročilé aplikace NMR chemická výměna, translační difuze, gradientní pulsy, potlačení rozpouštědla, NMR proteinů Chemická výměna jakýkoli proces při kterém dané jádro mění svůj stav
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Orbitaly ve víceelektronových atomech
 Orbitaly ve víceelektronových atomech Elektrony jsou přitahovány k jádru ale také se navzájem odpuzují. Repulzní síly způsobené dalšími elektrony stíní přitažlivý účinek atomového jádra. Efektivní náboj
Orbitaly ve víceelektronových atomech Elektrony jsou přitahovány k jádru ale také se navzájem odpuzují. Repulzní síly způsobené dalšími elektrony stíní přitažlivý účinek atomového jádra. Efektivní náboj
Ch - Elektronegativita, chemická vazba
 Ch - Elektronegativita, chemická vazba Autor: Mgr. Jaromír Juřek Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s využitím odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument
Ch - Elektronegativita, chemická vazba Autor: Mgr. Jaromír Juřek Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s využitím odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument
Průvodka. CZ.1.07/1.5.00/ Zkvalitnění výuky prostřednictvím ICT. III/2 Inovace a zkvalitnění výuky prostřednictvím ICT
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Teorie chemické vazby a molekulární geometrie Molekulární geometrie VSEPR
 Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
Geometrie molekul Lewisovy vzorce poskytují informaci o tom které atomy jsou spojeny vazbou a o jakou vazbu se jedná (topologie molekuly). Geometrické uspořádání molekuly je charakterizováno: Délkou vazeb
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Test vlastnosti látek a periodická tabulka
 DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
DUM Základy přírodních věd DUM III/2-T3-2-08 Téma: Test vlastnosti látek a periodická tabulka Střední škola Rok: 2012 2013 Varianta: A Zpracoval: Mgr. Pavel Hrubý Mgr. Josef Kormaník TEST Test vlastnosti
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Chemická vazba. John Dalton Amadeo Avogadro
 Chemická vazba John Dalton 1766-1844 Amadeo Avogadro 1776-1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904-1981 Fritz W. London 1900-1954 Teorie molekulových orbitalů Friedrich und 1896-1997
Chemická vazba John Dalton 1766-1844 Amadeo Avogadro 1776-1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904-1981 Fritz W. London 1900-1954 Teorie molekulových orbitalů Friedrich und 1896-1997
CHEMICKÁ VAZBA. Autor: Mgr. Stanislava Bubíková. Datum (období) tvorby: Ročník: osmý
 Autor: Mgr. Stanislava Bubíková CHEMICKÁ VAZBA Datum (období) tvorby: 13. 11. 01 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Částicové složení látek a chemické prvky; chemické reakce 1
Autor: Mgr. Stanislava Bubíková CHEMICKÁ VAZBA Datum (období) tvorby: 13. 11. 01 Ročník: osmý Vzdělávací oblast: Člověk a příroda / Chemie / Částicové složení látek a chemické prvky; chemické reakce 1
Valenční elektrony a chemická vazba
 Valenční elektrony a chemická vazba Ve vnější energetické hladině se nacházejí valenční elektrony, které se mohou podílet na tvorbě chemické vazby. Valenční elektrony často znázorňujeme pomocí teček kolem
Valenční elektrony a chemická vazba Ve vnější energetické hladině se nacházejí valenční elektrony, které se mohou podílet na tvorbě chemické vazby. Valenční elektrony často znázorňujeme pomocí teček kolem
Chemická vazba. Molekula vodíku. Elektronová teorie. Oktetové pravidlo (Kossel, Lewis, 1916) Pevnost vazby vazebná energie.
 Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Elektronová teorie ktetové pravidlo (Kossel, Lewis, 1916) Chemická vazba sdílení 2 valenčních e - opačného spinu 2 atomy za vzniku stabilní elektronové konfigurace vzácného plynu Spojení atomů prvků v
Částicové složení látek atom,molekula, nuklid a izotop
 Částicové složení látek atom,molekula, nuklid a izotop ATOM základní stavební částice všech hmotných těles jádro 100 000x menší než atom působí jaderné síly p + n 0 [1] e - stejný počet protonů a elektronů
Částicové složení látek atom,molekula, nuklid a izotop ATOM základní stavební částice všech hmotných těles jádro 100 000x menší než atom působí jaderné síly p + n 0 [1] e - stejný počet protonů a elektronů
DUSÍK NITROGENIUM 14,0067 3,1. Doplňte:
 Doplňte: Protonové číslo: Relativní atomová hmotnost: Elektronegativita: Značka prvku: Latinský název prvku: Český název prvku: Nukleonové číslo: Prvek je chemická látka tvořena z atomů o stejném... čísle.
Doplňte: Protonové číslo: Relativní atomová hmotnost: Elektronegativita: Značka prvku: Latinský název prvku: Český název prvku: Nukleonové číslo: Prvek je chemická látka tvořena z atomů o stejném... čísle.
Molekulová spektroskopie 1. Chemická vazba, UV/VIS
 Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
Molekulová spektroskopie 1 Chemická vazba, UV/VIS 1 Chemická vazba Silová interakce mezi dvěma atomy. Chemické vazby jsou soudržné síly působící mezi jednotlivými atomy nebo ionty v molekulách. Chemická
6.3.2 Periodická soustava prvků, chemické vazby
 6.3. Periodická soustava prvků, chemické vazby Předpoklady: 060301 Nejjednodušší atom: vodík s jediným elektronem v obalu. Ostatní prvky mají více protonů v jádře i více elektronů v obalu změny oproti
6.3. Periodická soustava prvků, chemické vazby Předpoklady: 060301 Nejjednodušší atom: vodík s jediným elektronem v obalu. Ostatní prvky mají více protonů v jádře i více elektronů v obalu změny oproti
2. Atomové jádro a jeho stabilita
 2. Atomové jádro a jeho stabilita Atom je nejmenší hmotnou a chemicky nedělitelnou částicí. Je tvořen jádrem, které obsahuje protony a neutrony, a elektronovým obalem. Elementární částice proton neutron
2. Atomové jádro a jeho stabilita Atom je nejmenší hmotnou a chemicky nedělitelnou částicí. Je tvořen jádrem, které obsahuje protony a neutrony, a elektronovým obalem. Elementární částice proton neutron
Genomické databáze. Shlukování proteinových sekvencí. Ivana Rudolfová. školitel: doc. Ing. Jaroslav Zendulka, CSc.
 Genomické databáze Shlukování proteinových sekvencí Ivana Rudolfová školitel: doc. Ing. Jaroslav Zendulka, CSc. Obsah Proteiny Zdroje dat Predikce struktury proteinů Cíle disertační práce Vstupní data
Genomické databáze Shlukování proteinových sekvencí Ivana Rudolfová školitel: doc. Ing. Jaroslav Zendulka, CSc. Obsah Proteiny Zdroje dat Predikce struktury proteinů Cíle disertační práce Vstupní data
COSY + - podmínky měření a zpracování dat ztráta rozlišení ve spektru. inphase dublet, disperzní. antiphase dublet, absorpční
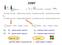 y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
y x COSY 90 y chem. posuv J vazba 90 x : : inphase dublet, disperzní inphase dublet, disperzní antiphase dublet, absorpční antiphase dublet, absorpční diagonální pík krospík + - - + podmínky měření a zpracování
Periodická tabulka prvků
 Periodická tabulka prvků 17. století s objevem dalších a dalších prvků nutnost systematizace J. W. Döberreiner (1829) teorie o triádách prvků triáda kovů (lithium, sodík, draslík reagují podobným způsobem)
Periodická tabulka prvků 17. století s objevem dalších a dalších prvků nutnost systematizace J. W. Döberreiner (1829) teorie o triádách prvků triáda kovů (lithium, sodík, draslík reagují podobným způsobem)
Mezimolekulové interakce
 Mezimolekulové interakce, od teorie po interakce biomolekul s grafenem Pavel Banáš Mezimolekulové interakce slabé mezimolekulové interakce fyzikální původ mezimolekulárních interakcí poruchová teorie mezimolekulárních
Mezimolekulové interakce, od teorie po interakce biomolekul s grafenem Pavel Banáš Mezimolekulové interakce slabé mezimolekulové interakce fyzikální původ mezimolekulárních interakcí poruchová teorie mezimolekulárních
3. Stavba hmoty Nadmolekulární uspořádání
 mezimolekulové interakce supramolekulární chemie sebeskladba molekulární zařízení Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti mezimolekulové interakce (nekovalentní) seskupování
mezimolekulové interakce supramolekulární chemie sebeskladba molekulární zařízení Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti mezimolekulové interakce (nekovalentní) seskupování
Univerzita Tomáše Bati ve Zlíně
 Univerzita Tomáše Bati ve Zlíně Ústav elektrotechniky a měření Základní pojmy elektroniky Přednáška č. 1 Milan Adámek adamek@ft.utb.cz U5 A711 +420576035251 Základní pojmy elektroniky 1 Model atomu průměr
Univerzita Tomáše Bati ve Zlíně Ústav elektrotechniky a měření Základní pojmy elektroniky Přednáška č. 1 Milan Adámek adamek@ft.utb.cz U5 A711 +420576035251 Základní pojmy elektroniky 1 Model atomu průměr
Optické spektroskopie 1 LS 2014/15
 Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
Optické spektroskopie 1 LS 2014/15 Martin Kubala 585634179 mkubala@prfnw.upol.cz 1.Úvod Velikosti objektů v přírodě Dítě ~ 1 m (10 0 m) Prst ~ 2 cm (10-2 m) Vlas ~ 0.1 mm (10-4 m) Buňka ~ 20 m (10-5 m)
Atom vodíku. Nejjednodušší soustava: p + e Řešitelná exaktně. Kulová symetrie. Potenciální energie mezi p + e. e =
 Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Atom vodíku Nejjednodušší soustava: p + e Řešitelná exaktně Kulová symetrie Potenciální energie mezi p + e V 2 e = 4πε r 0 1 Polární souřadnice využití kulové symetrie atomu Ψ(x,y,z) Ψ(r,θ, φ) x =? y=?
Protonové číslo Z - udává počet protonů v jádře atomu, píše se jako index vlevo dole ke značce prvku
 Stavba jádra atomu Protonové Z - udává protonů v jádře atomu, píše se jako index vlevo dole ke značce prvku Neutronové N - udává neutronů v jádře atomu Nukleonové A = Z + N, udává nukleonů (protony + neutrony)
Stavba jádra atomu Protonové Z - udává protonů v jádře atomu, píše se jako index vlevo dole ke značce prvku Neutronové N - udává neutronů v jádře atomu Nukleonové A = Z + N, udává nukleonů (protony + neutrony)
Nauka o materiálu. Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny
 Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
ELEKTRICKÝ NÁBOJ A ELEKTRICKÉ POLE POJMY K ZOPAKOVÁNÍ. Testové úlohy varianta A
 Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D12_Z_OPAK_E_Elektricky_naboj_a_elektricke_ pole_t Člověk a příroda Fyzika Elektrický
Škola: Autor: DUM: Vzdělávací obor: Tematický okruh: Téma: Masarykovo gymnázium Vsetín Mgr. Jitka Novosadová MGV_F_SS_3S3_D12_Z_OPAK_E_Elektricky_naboj_a_elektricke_ pole_t Člověk a příroda Fyzika Elektrický
Základní parametry 1 H NMR spekter
 LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
LEKCE 1a Základní parametry 1 NMR spekter Počet signálů ve spektru (zjištění počtu skupin chemicky ekvivalentních jader) Integrální intenzita (intenzita pásů závisí na počtu jader) Chemický posun (polohy
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Elektrostatické pole. Vznik a zobrazení elektrostatického pole
 Elektrostatické pole Vznik a zobrazení elektrostatického pole Elektrostatické pole vzniká kolem nepohyblivých těles, které mají elektrický náboj. Tento náboj mohl vzniknout například přivedením elektrického
Elektrostatické pole Vznik a zobrazení elektrostatického pole Elektrostatické pole vzniká kolem nepohyblivých těles, které mají elektrický náboj. Tento náboj mohl vzniknout například přivedením elektrického
Úvod do studia organické chemie
 Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
Úvod do studia organické chemie 1828... Wöhler... uměle připravil močovinu Organická chemie - chemie sloučenin uhlíku a vodíku, případně dalších prvků (O, N, X, P, S) Příčiny stability uhlíkových řetězců:
Od kvantové mechaniky k chemii
 Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
Od kvantové mechaniky k chemii Jan Řezáč UOCHB AV ČR 19. září 2017 Jan Řezáč (UOCHB AV ČR) Od kvantové mechaniky k chemii 19. září 2017 1 / 33 Úvod Vztah mezi molekulovou strukturou a makroskopickými vlastnostmi
MOLEKULOVÉ MODELOVÁNÍ - STRUKTURA. Monika Pěntáková Katedra Farmaceutické chemie
 MOLEKULOVÉ MODELOVÁNÍ - STRUKTURA Monika Pěntáková Katedra Farmaceutické chemie Chemická struktura a geometrie KONFORMACE = můžeme změnit pouhým otočením kolem kovalentní vazby KONFIGURACE = při změně
MOLEKULOVÉ MODELOVÁNÍ - STRUKTURA Monika Pěntáková Katedra Farmaceutické chemie Chemická struktura a geometrie KONFORMACE = můžeme změnit pouhým otočením kolem kovalentní vazby KONFIGURACE = při změně
Plazmové metody. Základní vlastnosti a parametry plazmatu
 Plazmové metody Základní vlastnosti a parametry plazmatu Atom je základní částice běžné hmoty. Částice, kterou již chemickými prostředky dále nelze dělit a která definuje vlastnosti daného chemického prvku.
Plazmové metody Základní vlastnosti a parametry plazmatu Atom je základní částice běžné hmoty. Částice, kterou již chemickými prostředky dále nelze dělit a která definuje vlastnosti daného chemického prvku.
Nukleární Overhauserův efekt (NOE)
 Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
Nukleární Overhauserův efekt (NOE) NOE je důsledek dipolární interakce mezi dvěma jádry. Vzniká přímou interakcí volně přes prostor, tudíž není ovlivněn chemickými vazbami jako nepřímá spin-spinová interakce.
jádro a elektronový obal jádro nukleony obal elektrony, pro chemii významné valenční elektrony
 atom jádro a elektronový obal jádro nukleony obal elektrony, pro chemii významné valenční elektrony molekula Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti seskupení alespoň dvou atomů
atom jádro a elektronový obal jádro nukleony obal elektrony, pro chemii významné valenční elektrony molekula Evropský sociální fond Praha & EU: Investujeme do vaší budoucnosti seskupení alespoň dvou atomů
John Dalton Amadeo Avogadro
 Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Spojením atomů vznikají molekuly... John Dalton 1766 1844 Amadeo Avogadro 1776 1856 Výpočet molekuly 2, metoda valenční vazby Walter eitler 1904 1981 Fritz W. London 1900 1954 Teorie molekulových orbitalů
Struktura atomů a molekul
 Struktura atomů a molekul Obrazová příloha Michal Otyepka tento text byl vysázen systémem L A TEX2 ε ii Úvod Dokument obsahuje všechny obrázky tak, jak jsou uvedeny ve druhém vydání skript Struktura atomů
Struktura atomů a molekul Obrazová příloha Michal Otyepka tento text byl vysázen systémem L A TEX2 ε ii Úvod Dokument obsahuje všechny obrázky tak, jak jsou uvedeny ve druhém vydání skript Struktura atomů
České vysoké učení technické v Praze Fakulta jaderná a fyzikálně inženýrská. Příloha formuláře C OKRUHY
 Příloha formuláře C OKRUHY ke státním závěrečným zkouškám BAKALÁŘSKÉ STUDIUM Obor: Studijní program: Aplikace přírodních věd Základy fyziky kondenzovaných látek 1. Vazebné síly v kondenzovaných látkách
Příloha formuláře C OKRUHY ke státním závěrečným zkouškám BAKALÁŘSKÉ STUDIUM Obor: Studijní program: Aplikace přírodních věd Základy fyziky kondenzovaných látek 1. Vazebné síly v kondenzovaných látkách
Molekuly 1 12/4/2011. Molekula definice IUPAC. Molekuly. Proč existují molekuly? Kosselův model. Představy o molekulách
 1/4/011 Molekuly 1 Molekula definice IUPC elektricky neutrální entita sestávající z více nežli jednoho atomu. Přesně, molekula, v níž je počet atomů větší nežli jedna, musí odpovídat snížení na ploše potenciální
1/4/011 Molekuly 1 Molekula definice IUPC elektricky neutrální entita sestávající z více nežli jednoho atomu. Přesně, molekula, v níž je počet atomů větší nežli jedna, musí odpovídat snížení na ploše potenciální
Nukleární Overhauserův efekt (NOE)
 LEKCE 8 Nukleární verhauserův efekt (NE) určení prostorové struktury molekul využití REY spektroskopie projevy NE a chemické výměny v jednom systému Nukleární verhauserův efekt (NE) důsledek dipolární
LEKCE 8 Nukleární verhauserův efekt (NE) určení prostorové struktury molekul využití REY spektroskopie projevy NE a chemické výměny v jednom systému Nukleární verhauserův efekt (NE) důsledek dipolární
INTERPRETACE HMOTNOSTNÍCH SPEKTER
 INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
INTERPRETACE HMOTNOSTNÍCH SPEKTER Hmotnostní spektrometrie hmotnostní spektrometrie = fyzikálně chemická metoda založená na rozdělení hmotnosti iontů v plynné fázi podle jejich poměru hmotnosti a náboje
ATOMOVÉ JÁDRO. Nucleus Složení: Proton. Neutron 1 0 n částice bez náboje Proton + neutron = NUKLEON PROTONOVÉ číslo: celkový počet nukleonů v jádře
 ATOM 1 ATOM Hmotná částice Dělit lze: Fyzikálně ANO Chemicky Je z nich složena každá látka Složení: Atomové jádro (protony, neutrony) Elektronový obal (elektrony) NE Elektroneutrální částice: počet protonů
ATOM 1 ATOM Hmotná částice Dělit lze: Fyzikálně ANO Chemicky Je z nich složena každá látka Složení: Atomové jádro (protony, neutrony) Elektronový obal (elektrony) NE Elektroneutrální částice: počet protonů
Počítačová chemie. výpočetně náročné simulace chemických a biomolekulárních systémů. Zora Střelcová
 Počítačová chemie výpočetně náročné simulace chemických a biomolekulárních systémů Zora Střelcová Národní centrum pro výzkum biomolekul, Masarykova univerzita, Kotlářská 2, 611 37 Brno, Česká Republika
Počítačová chemie výpočetně náročné simulace chemických a biomolekulárních systémů Zora Střelcová Národní centrum pro výzkum biomolekul, Masarykova univerzita, Kotlářská 2, 611 37 Brno, Česká Republika
5. Lipidy a biomembrány
 5. Lipidy a biomembrány Obtížnost A Co je chybného na často slýchaném konstatování: Biologická membrána je tvořena dvojvrstvou fosfolipidů.? Jmenujte alespoň tři skupiny látek, které se podílejí na výstavbě
5. Lipidy a biomembrány Obtížnost A Co je chybného na často slýchaném konstatování: Biologická membrána je tvořena dvojvrstvou fosfolipidů.? Jmenujte alespoň tři skupiny látek, které se podílejí na výstavbě
Základy NMR 2D spektroskopie
 Základy NMR 2D spektroskopie Jaroslav Kříž Ústav makromolekulární chemie AV ČR v.v.i. puls 1D : d 1 Fourierova transformace časového rozvoje odezvy dá 1D spektrum 2D: d 1 d 1 d 1 d 0 d 0 + in 0 d 0 + 2in
Základy NMR 2D spektroskopie Jaroslav Kříž Ústav makromolekulární chemie AV ČR v.v.i. puls 1D : d 1 Fourierova transformace časového rozvoje odezvy dá 1D spektrum 2D: d 1 d 1 d 1 d 0 d 0 + in 0 d 0 + 2in
Přednáška IX: Elektronová spektroskopie II.
 Přednáška IX: Elektronová spektroskopie II. 1 Försterův resonanční přenos energie Pravděpodobnost (rychlost) přenosu je určená jako: k ret 1 = τ 0 D R r 0 6 0 τ D R 0 r Doba života donoru v excitovaném
Přednáška IX: Elektronová spektroskopie II. 1 Försterův resonanční přenos energie Pravděpodobnost (rychlost) přenosu je určená jako: k ret 1 = τ 0 D R r 0 6 0 τ D R 0 r Doba života donoru v excitovaném
2.3 CHEMICKÁ VAZBA. Molekula bílého fosforu P 4 a kyseliny sírové H 2 SO 4. Předpona piko p je dílčí jednotkou a udává velikost m.
 2.3 CHEMICKÁ VAZBA Spojováním dvou a více atomů vznikají molekuly. Jestliže dochází ke spojování výhradně atomů téhož chemického prvku, pak se jedná o molekuly daného prvku (vodíku H 2, dusíku N 2, ozonu
2.3 CHEMICKÁ VAZBA Spojováním dvou a více atomů vznikají molekuly. Jestliže dochází ke spojování výhradně atomů téhož chemického prvku, pak se jedná o molekuly daného prvku (vodíku H 2, dusíku N 2, ozonu
OPVK CZ.1.07/2.2.00/
 OPVK CZ.1.07/2.2.00/28.0184 Základní principy vývoje nových léčiv OCH/ZPVNL Mgr. Radim Nencka, Ph.D. ZS 2012/2013 Molekulární interakce SAR Možné interakce jednotlivých funkčních skupin 1. Interakce alkoholů
OPVK CZ.1.07/2.2.00/28.0184 Základní principy vývoje nových léčiv OCH/ZPVNL Mgr. Radim Nencka, Ph.D. ZS 2012/2013 Molekulární interakce SAR Možné interakce jednotlivých funkčních skupin 1. Interakce alkoholů
Chemická reaktivita NK.
 Chemické vlastnosti, struktura a interakce nukleových kyselin Bi7015 Chemická reaktivita NK. Hydrolýza NK, redukce, oxidace, nukleofily, elektrofily, alkylační činidla. Mutageny, karcinogeny, protinádorově
Chemické vlastnosti, struktura a interakce nukleových kyselin Bi7015 Chemická reaktivita NK. Hydrolýza NK, redukce, oxidace, nukleofily, elektrofily, alkylační činidla. Mutageny, karcinogeny, protinádorově
LEKCE 1b. Základní parametry 1 H NMR spekter. Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)*
 Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Základní parametry 1 NMR spekter LEKCE 1b Symetrie v NMR spektrech: homotopické, enantiotopické, diastereotopické protony (skupiny)* 3.5 3.0 2.5 2.0 1.5 Základní parametry 1 NMR spekter Počet signálů ve
Organická chemie 3.ročník studijního oboru - kosmetické služby.
 Organická chemie 3.ročník studijního oboru - kosmetické služby. T-7 Funkční a substituční deriváty karboxylových kyselin Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu:
Organická chemie 3.ročník studijního oboru - kosmetické služby. T-7 Funkční a substituční deriváty karboxylových kyselin Zpracováno v rámci projektu Zlepšení podmínek ke vzdělávání Registrační číslo projektu:
spinový rotační moment (moment hybnosti) kvantové číslo jaderného spinu I pro NMR - jádra s I 0
 Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla energetické stavy jádra v magnetickém poli rezonanční podmínka - instrumentace pulsní metody, pulsní sekvence relaxační
Spektroskopie NMR - teoretické základy spin nukleonů, spin jádra, kvantová čísla energetické stavy jádra v magnetickém poli rezonanční podmínka - instrumentace pulsní metody, pulsní sekvence relaxační
Spektra 1 H NMR. Velmi zjednodušeně! Bohumil Dolenský
 Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
Spektra 1 MR Velmi zjednodušeně! Bohumil Dolenský Spektra 1 MR... Počet signálů C 17 18 2 O 2 MeO Počet signálů = počet neekvivalentních skupin OMe = informace o symetrii molekuly Spektrum 1 MR... Počet
NMR spektroskopie. Úvod
 NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
NMR spektroskopie Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem umístěným v silném magnetickém poli poskytuje
Jádro se skládá z kladně nabitých protonů a neutrálních neutronů -> nukleony
 Otázka: Atom a molekula Předmět: Chemie Přidal(a): Dituse Atom = základní stavební částice všech látek Skládá se ze 2 částí: o Kladně nabité jádro o Záporně nabitý elektronový obal Jádro se skládá z kladně
Otázka: Atom a molekula Předmět: Chemie Přidal(a): Dituse Atom = základní stavební částice všech látek Skládá se ze 2 částí: o Kladně nabité jádro o Záporně nabitý elektronový obal Jádro se skládá z kladně
Základy Mössbauerovy spektroskopie. Libor Machala
 Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
Základy Mössbauerovy spektroskopie Libor Machala Rudolf L. Mössbauer 1958: jev bezodrazové rezonanční absorpce záření gama atomovým jádrem 1961: Nobelova cena Analogie s rezonanční absorpcí akustických
Nukleární magnetická rezonance (NMR)
 Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
Nukleární magnetická rezonance (NMR) Mgr. Zdeněk Moravec, Ph.D. Úvod Zkratka NMR znamená Nukleární Magnetická Rezonance. Jde o analytickou metodu, která na základě absorpce radiofrekvenčního záření vzorkem
Látkové množství. 6,022 10 23 atomů C. Přípravný kurz Chemie 07. n = N. Doporučená literatura. Látkové množství n. Avogadrova konstanta N A
 Doporučená literatura Přípravný kurz Chemie 2006/07 07 RNDr. Josef Tomandl, Ph.D. Mailto: tomandl@med.muni.cz Předmět: Přípravný kurz chemie J. Vacík a kol.: Přehled středoškolské chemie. SPN, Praha 1990,
Doporučená literatura Přípravný kurz Chemie 2006/07 07 RNDr. Josef Tomandl, Ph.D. Mailto: tomandl@med.muni.cz Předmět: Přípravný kurz chemie J. Vacík a kol.: Přehled středoškolské chemie. SPN, Praha 1990,
Úvod do strukturní analýzy farmaceutických látek
 Úvod do strukturní analýzy farmaceutických látek Garant předmětu: Vyučující: doc. Ing. Bohumil Dolenský, Ph.D. prof. RNDr. Pavel Matějka, Ph.D., A136, linka 3687, matejkap@vscht.cz doc. Ing. Bohumil Dolenský,
Úvod do strukturní analýzy farmaceutických látek Garant předmětu: Vyučující: doc. Ing. Bohumil Dolenský, Ph.D. prof. RNDr. Pavel Matějka, Ph.D., A136, linka 3687, matejkap@vscht.cz doc. Ing. Bohumil Dolenský,
Třídění látek. Chemie 1.KŠPA
 Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Třídění látek Chemie 1.KŠPA Systém (soustava) Vymezím si kus prostoru, látky v něm obsažené nazýváme systém soustava okolí svět Stěny soustavy Soustava může být: Izolovaná = stěny nedovolí výměnu částic
Molekulová fyzika a termika. Přehled základních pojmů
 Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Molekulová fyzika a termika Přehled základních pojmů Kinetická teorie látek Vychází ze tří experimentálně ověřených poznatků: 1) Látky se skládají z částic - molekul, atomů nebo iontů, mezi nimiž jsou
Vazebné interakce protein s DNA
 Vazebné interakce protein s DNA Vazebné možnosti vn jší vazba atmosféra + iont kolem nabité DNA vazba ve žlábku van der Waalsovský kontakt s lé ivem ve žlábku interkalace vmeze ení planárního aromat.
Vazebné interakce protein s DNA Vazebné možnosti vn jší vazba atmosféra + iont kolem nabité DNA vazba ve žlábku van der Waalsovský kontakt s lé ivem ve žlábku interkalace vmeze ení planárního aromat.
Oddělení fyziky vrstev a povrchů makromolekulárních struktur
 Oddělení fyziky vrstev a povrchů makromolekulárních struktur Témata diplomových prací 2014/2015 Studium změn elektrické vodivosti emeraldinových solí vystavených pokojovým a mírně zvýšeným teplotám klíčová
Oddělení fyziky vrstev a povrchů makromolekulárních struktur Témata diplomových prací 2014/2015 Studium změn elektrické vodivosti emeraldinových solí vystavených pokojovým a mírně zvýšeným teplotám klíčová
OPVK CZ.1.07/2.2.00/
 18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
18.2.2013 OPVK CZ.1.07/2.2.00/28.0184 Cvičení z NMR OCH/NMR Mgr. Tomáš Pospíšil, Ph.D. LS 2012/2013 18.2.2013 NMR základní principy NMR Nukleární Magnetická Resonance N - nukleární (studujeme vlastnosti
Opakování: shrnutí základních poznatků o struktuře atomu
 11. Polovodiče Polovodiče jsou krystalické nebo amorfní látky, jejichž elektrická vodivost leží mezi elektrickou vodivostí kovů a izolantů a závisí na teplotě nebo dopadajícím optickém záření. Elektrické
11. Polovodiče Polovodiče jsou krystalické nebo amorfní látky, jejichž elektrická vodivost leží mezi elektrickou vodivostí kovů a izolantů a závisí na teplotě nebo dopadajícím optickém záření. Elektrické
Fyzika je přírodní věda, která zkoumá a popisuje zákonitosti přírodních jevů.
 Fyzika je přírodní věda, která zkoumá a popisuje zákonitosti přírodních jevů. Násobky jednotek název značka hodnota kilo k 1000 mega M 1000000 giga G 1000000000 tera T 1000000000000 Tělesa a látky Tělesa
Fyzika je přírodní věda, která zkoumá a popisuje zákonitosti přírodních jevů. Násobky jednotek název značka hodnota kilo k 1000 mega M 1000000 giga G 1000000000 tera T 1000000000000 Tělesa a látky Tělesa
Základy molekulové fyziky a termodynamiky
 Základy molekulové fyziky a termodynamiky Molekulová fyzika je částí fyziky, která zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného silového působení částic, z nichž jsou
Základy molekulové fyziky a termodynamiky Molekulová fyzika je částí fyziky, která zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného silového působení částic, z nichž jsou
3. Vlastnosti skla za normální teploty (mechanické, tepelné, optické, chemické, elektrické).
 PŘEDMĚTY KE STÁTNÍM ZÁVĚREČNÝM ZKOUŠKÁM V BAKALÁŘSKÉM STUDIU SP: CHEMIE A TECHNOLOGIE MATERIÁLŮ SO: MATERIÁLOVÉ INŽENÝRSTVÍ POVINNÝ PŘEDMĚT: NAUKA O MATERIÁLECH Ing. Alena Macháčková, CSc. 1. Souvislost
PŘEDMĚTY KE STÁTNÍM ZÁVĚREČNÝM ZKOUŠKÁM V BAKALÁŘSKÉM STUDIU SP: CHEMIE A TECHNOLOGIE MATERIÁLŮ SO: MATERIÁLOVÉ INŽENÝRSTVÍ POVINNÝ PŘEDMĚT: NAUKA O MATERIÁLECH Ing. Alena Macháčková, CSc. 1. Souvislost
Teorie hybridizace. Vysvětluje vznik energeticky rovnocenných kovalentních vazeb a umožňuje předpovědět prostorový tvar molekul.
 Chemická vazba co je chemická vazba charakteristiky chemické vazby jak vzniká vazba znázornění chemické vazby kovalentní a koordinační vazba vazba σ a π jednoduchá, dvojná a trojná vazba polarita vazby
Chemická vazba co je chemická vazba charakteristiky chemické vazby jak vzniká vazba znázornění chemické vazby kovalentní a koordinační vazba vazba σ a π jednoduchá, dvojná a trojná vazba polarita vazby
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Vlastnosti kapalin. Povrchová vrstva kapaliny
 Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
Struktura a vlastnosti kapalin Vlastnosti kapalin, Povrchová vrstva kapaliny Jevy na rozhraní pevného tělesa a kapaliny Kapilární jevy, Teplotní objemová roztažnost Vlastnosti kapalin Kapalina - tvoří
Vysoká škola technická a ekonomická v Českých Budějovicích. Institute of Technology And Business In České Budějovice
 KAPITOLA 2: PRVEK Vysoká škola technická a ekonomická v Českých Budějovicích Institute of Technology And Business In České Budějovice Tento učební materiál vznikl v rámci projektu "Integrace a podpora
KAPITOLA 2: PRVEK Vysoká škola technická a ekonomická v Českých Budějovicích Institute of Technology And Business In České Budějovice Tento učební materiál vznikl v rámci projektu "Integrace a podpora
