POLYMERY I. Doc.ing.Jaromír LEDERER, CSc.
|
|
|
- Richard Bednář
- před 9 lety
- Počet zobrazení:
Transkript
1 POLYMERY I Doc.ing.Jaromír LEDERER, CSc.
2 O čem budeme mluvit Úvod do chemie a technologie polymerů Makromolekulární řetězce Struktura, fázový stav a základní vlastnosti polymerů Mechanismy vzniku Principy průmyslových syntéz lavní typy polymerů
3 Obecné vlastnosti polymerů pevné nebo elastické transparentní, průsvitné nebo neprůsvitné tvrdé nebo měkké odolné vůči povětrnostním vlivům nebo degradabilní odolné vůči vysoké nebo nízké teplotě.
4 Použití polymerů Plasty obalová technika stavebnictví strojírenství elektrotechnika, elektronika nábytkářství Nátěrové hmoty (filmotvorné polymery + pigmenty + plniva + ředidla) Lepidla a tmely lepidla termoplastická a reaktivní Vlákna přírodní, chemická Kaučuky
5 Oblast aplikace polymerů
6 Spotřeba polymerů v Evropě
7 Použití polymerů Plasty obalová technika stavebnictví strojírenství elektrotechnika, elektronika nábytkářství Nátěrové hmoty (filmotvorné polymery + pigmenty + plniva + ředidla) Lepidla a tmely lepidla termoplastická a reaktivní Vlákna přírodní, chemická Kaučuky
8 Použití PUR v automobilech
9 Úvod do chemie a technologie polymerů POLYMERY Elastomery Plasty Termoplasty Reaktoplasty (Termosety) Pryskyřice
10 Trochu historie Indiáni v Jižní Americe. plačící dřevo..přírodní kaučuk Goodyear vulkanizace Dr.Dunlop.. Pneu (1888) Igelit (1925) PVC Celuloid (1873) J.yatt Bakelit (1909) L.Beakland Nylon (1935) W.Carothers Ziegler Natta koordinační katalyzátory
11 lavní typy polymerů ABS (AKRYLONITRIL, BUTADIEN A STYREN) ASA (AKRYLONITRIL, STYREN A AKRYLÁTY) SBR (BUTADIEN STYRENOVÝ KAUČUK) CA (ACETÁT CELULOSY) EP (EPOXIDOVÉ PRYSKYŘICE) E/P (KOPOLYMER ETYLENUA PROPYLENU) EPDM (ETYLEN-PROPYLENOVÝ KAUČUK S DIENEM) EVA (KOPOLYMEN ETYLEN- VINYLACETÁT) SI (SILIKON) UF (MOČOVINOFORMALDEYDOVÁ PRYSKYŘICE) MF (MELAMINOFORMALDEYDOVÁ PRYSKŘICE) DPE (POLYETYLEN O VYSOKÉ USTOTĚ) LDPE (POLYETYLEN O NÍZKÉ USTOTĚ) LLDPE(POLYETYLEN O NÍZKÉ USTOTĚ S LINEÁRNÍ STRUKTUROU) PA (POLYAMIDY) PAN (POLYAKRYLONITRIL) PC (POLYKARBONÁTY) PET (POLYETYLENTEREFTALÁT) PF (FENOLFORMALDEYDOVÁ PRYSKYŘICE) POP (POLYFENYLENOXID) PP (POLYPROPYLEN) PS (POLYSTYREN) PUR (POLYURETAN) PVC (POLYVINYLCLORID) UP (NENASYCENÁ POLYESTEROVÁ PRYSKYŘICE)
12 Co jsou polymery a co je charakterizuje? Složení Velikost molekul Tvar molekul polymeru Organizovanost molekul polymeru Vliv na vlastnosti
13 lavní monomery ethylen (g) b.v. 101 C propylen (g) b.v. 44 C buteny (g) b.v. 9 C styren (l), b.v. 145 C divinylbenzen (l), b.v. 184 C alfa-methylstyren (l), b.v. 172 C vinylchlorid (g), b.v. 14 C kyselina akrylová (l) b.v. 141 C k.methakrylová (l) b.v. 163 C akrylonitril (l) b.v. 77 C vinylacetát (l) b.v. 73 C 1,3 butadien (g) isopren (l) b.v. 34 C anilin (s) b.t. 89 C fenol (s) b.t. 41 C bisfenol A chloropren (l) b.v. 60 C formaldehyd (g) b.v. 19 C acetaldehyd (l) b.v. 20 C epsilon kaprolaktam (s) b.t. 64 C dimethyldichlorsilan tolylendiisokyanát bis(4-isokyanátofenyl)methan kyselina adipová (s) b.t. 153 C maleinanhydrid (s) b.t. 53 C ftalanhydrid (s) b.t. 131 C kyselina tereftalová (s) b.t. 427 C ethylenglykol (l) b.v. 198 C glycerol (l) b.v. 290 C hexamethylendiamin (s) b.t. 42 C močovina(s) b.t. 132 C melamín (s) b.t. 354 C
14 Základní struktura polymerů OObrázek : Základní struktura polymerů AA) BB) CC) lineární polymer rozvětvený polymer prostorově zesíťovaný polymer
15 Chemické složení AB kopolymerů A) homopolymer B) nepravidelný kopolymer C) blokový kopolymer D) alternující kopolymer
16 Chemické složení polymerů AA) BB) CC) homopolymer nepravidelný kopolymer blokový kopolymer DD) alternující kopolymer /směsné polymery = směsi polymerů/
17 Molární hmotnost polymeru Molární hmotnost syntetických polymerů může nabývat hodnot od několika g/mol až do několika g/mol. Obrázek ukazuje jako příklad distribuční křivky molární hmotnosti (MMD) několika různých polymerních standardů.
18 Plasty a polymery
19 Co je polymer?
20 Rozdělení polymerů, krystalizace
21 Co rozhoduje o vlastnostech polymeru?
22 Složení polymerů
23 Vznik polymeru adiční a kondenzační polymerace NÁSOBNÁ VAZBA 2 A VÍCE FUNKČNÍ SKUPINY POLYADIČNÍ POLYMERACE POLYURETANY
24 Velikost molekuly polymeru
25 Distribuce velikostí molekul polymeru
26 Vyjádření rozsahu velikostí molekul polymeru
27 Polydisperzita
28 Význam polydisperzity
29 Co je krystalinita polymeru?
30 O čem rozhoduje hustota? Tuhost Bod tání Smrštivost Tvrdost Odolnost k otěru Zakalenost Chemická odolnost
31 Vnitřní organizace molekul
32 Organizovanost molekul polymeru amorfní a semikrystalické Čirost zákal Propletenostorganizovanost molekul Bod tání Smrštivost při chlazení taveniny Isotropie- Anisoptropie Chemická odolnost
33 Struktury makromolekulárních řetězců lineární rozvětvená zesíťovaná
34 Zpracování plastů
35 Zpracovatelské technologie vytlačování pro trubky, profily, desky a izolace kabelů vstřikování pro výrobky růz ných, často velmi složitých tvarů jako jsou strojní části, elektrické svíčky a lékařské vybavení (např. stříkačky); termoplasty a termosety vyfukování pro láhve, nádoby a fólie kalandrování pro fólie a desky rotační tvarování pro velké formáty taže ní pro tyče, potrubí atd. natírání pro tenké vrstvy na různých podkladech stlačování pro pryskyřice spřádání pro vlákna protlačování pro termosety tvarování tlakem pro termosety vulkanizace pro kaučuky směšování obecně použitelná tech nika.
36 Zpracování polymerů a plastů Výrobek Roztavení Tok a tváření Chlazení a Zpevnění
37 Roztavení Tok a tváření taveniny Chlazení a tuhnutí polymeru Zpracování polymerů a plastů
38 Tavení polymeru Roztavení amorfních nebo Semikrystalických polymerů
39 Tavení amorfních polymerů Tuhá látka=skelný stav kaučukovitý stav..tavenina
40 Termomechanická křivka T(g)-teplota zeskelnění T(m) t.tání T(f) t.toku 1.amorfní polymer 2,3..krystalický polymer
41 Tavení semikrystalického polymeru Skelný stav..kaučukovitý stav teplota tání
42 Tečení a formování polymeru Molekuly zapletené navzájem
43 Pomalá deformace Při pomalé deformaci se spletené molekuly převalují a pohybuje se celá masa polymeru odpor k pohybu je vysoký
44 Rychlá deformace Při rychlé deformaci se molekuly protahují a orientují se ve směru toku odpor k pohybu klesá
45 Tok taveniny skrze vstřikovací tryskou Molekuly se převalují protahují..vysoké protažení vratný pochod
46 odnocení tokových vlastností polymerů Tok : nevratná deformace způsobená smykovým napětím Napětí: síla působící na jednotkovou plochu Smykové napětí: napětí působící ve směru tečny k namáhanému tělesu Smyková deformace: charakterizuje změnu tvaru polymeru při působení smykového napětí
47 Model toku
48 Viskozita Smykové napětí smyková rychlost
49 Viskozita..odpor k toku
50 Vliv struktury na viskozitu polymerů
51 Chlazení taveniny amorfního polymeru
52 Chlazení taveniny semikrystalického polymeru
53 SUMMARY
54 POLYMERY II Doc.ing.Jaromír LEDERER, CSc.
55 O čem budeme mluvit Typy polymeračních reakcí mechanismy Základní způsoby výroby polymerů
56 POLYMERAČNÍ REAKCE ADIČNÍ KONDENZAČNÍ ŘETĚZOVÉ POSTUPNÉ KOORDINAČNÍ (ZIEGLER-NATTA)
57 ADIČNÍ POLYMERACE Adiční polymerace: Celá molekula monomeru, všechny její atomy, přejdou do polymeru ethylen polyethylen C C [ ] C C n 2 x C 4 x 2 x C 4 x
58 Cl O KONDENZAČNÍ POLYMERACE Kondenzační polymerace - některé atomy monomeru neskončí v polymeru - vzniklý polymer je vzhledem k monomeru kondenzován - atomy, které neskončí v polymeru, odcházejí jako vedlejší nízkomolekulární produkt - kondenzát C C 2 adipoylchlorid C 2 hexamethylen diamin O C 2 C 2 C Cl + N C 2 C 2 C 2 C 2 C 2 C 2 N Tento chlor a tento vodík neskončí v polymeru [ O C C 2 C 2 O C 2 C 2 C N C 2 C 2 C 2 C 2 C 2 C 2 N + Cl nylon 6,6 ] n
59 Řetězová polymerace ŘETĚZOVÁ POLYMERACE - k rostoucímu řetězci se připojuje vždy jedna molekula monomeru - rostoucí řetězce se navzájem nemohou spojit - reakční směs obsahuje řetězce stejné délky, na začátku pouze monomery, na konci pouze hotové makromolekuly Aniontová polymerace styrenu A : + C 2 C A C 2 C : A C 2 C : + C 2 C A C 2 C C 2 C :
60 Postupná polymerace POSTUPNÁ POLYMERACE - k rostoucímu řetězci se může připojit mono -, di -, tri -,... mer. - rostoucí řetězce se navzájem mohou spojit - reakční směs obsahuje řetězc e různých délek, od monomeru až po hotové makromolekuly PET Dva monomery se spojí za vzniku dimeru. O O Cl C C Cl + O C 2 C 2 O tereftoylchlorid ethylenglykol O O - Cl Cl C C o C 2 dimer C 2 O
61 POSTUPNÁ POLYMERACE Vzniklý dimer má teď několik možností. Může reagovat s dalším monomerem za vzniku trimeru. Buď s tereftoylchloridem: O O O O Cl C C C 2 C 2 O + Cl C C Cl - Cl Cl O C O C C 2 C 2 O C O C Cl Nebo s ethylenglykolem: O O Cl C C C 2 C 2 O + O C 2 C 2 O O O - Cl O C 2 C 2 C C C 2 C 2 O
62 POLYMERACE - SRNUTÍ ADIČNÍ nevzniká vedlejší produkt KONDENZAČNÍ vzniká vedlejší produkt POLYMERACE ŘETĚZOVÁ rostoucí řetězec reaguje pouze s monomerem POSTUPNÁ rostoucí řetězce mohou reagovat navzájem
63 RADIKÁLOVÁ POLYMERACE Radikálová polymerace vinylových monomerů - jedna z nejrozšířenějších reakcí při výrobě polymerů - vinylové monomery obsahují dvojnou vazbu mezi dvěma uhlíky - vyrábí se tak polystyren, polymethylmetakrylát, polybutadien (syntetický kaučuk) polyvinylacetát a rozvětvený polyethylen
64 Celá reakce začíná u molekuly zvané iniciátor. Iniciátory mohou být např.: C 3 C 3 3 C C N N C C 3 O O CN CN 2,2'-azo-bis-izobutyronitril C O O C dibenzoylperoxid Tyto molekuly mají dosti neobvyklý způsob rozpadu, při kterém se dva elektrony jedné z va rozdělí mezi vznikající fragmenty jako tzv. nepárové elektrony. Molekuly obsahující nepárové elektrony se nazývají volné radikály. zeb C 3 C 3 C 3 C 3 3 C C N N C C 3 3 C C + N N + C C 3 CN CN CN CN O O O O C O O C C O + O C O C O O + C O
65 C C C C ybnou silou této reakce je skutečnost, že vazba σ je pevnější než vazba π. Rozpad iniciátoru na volné radikály a reakce těchto radikálů s monomerem se nazývá INICIACE. Při iniciaci vzniklé volné radikály opět napadají dvojné vazby dalších monomerů. Řetězce postupně rostou připojováním dalších a dalších monomerů. Této fázi reakce se říká PROPAGACE. C C C C C C C C C C [ ] n
66 Volné radikály zanikají ve fázi TERMINACE. Zánik volných radikálů může probíhat jedním ze dvou způsobů: Spárování - spojení dvou volných radikálů za vzniku jednoduché vazby mezi nimi C C C C C C C C C C C C Disproporcionace C C C C C C C C C C C C C C C C C C
67 Aniontová polymerace vinylových monomerů Reakce opět začíná u molekuly zvané iniciátor. C 3 C 2 C 2 C 2 Li butyllithium Butyllithium a podobné sloučeniny mohou disociovat za vzniku kovového kationtu a uhlíkatého aniontu, tzv. karbaniontu : C 3 C 2 C 2 C 2 Li C 3 C 2 C 2 C : + Li + Volný elektronový pár v karbaniontu se může "nacpat" k uhlíku s dvojnou vazbou v monomeru. Napadený uhlík ovšem nemůže zůstat pětivazný, a tak se zbaví té nejslabší vazby, tj. vazby π. Vznikne tak nový karbaniont. C 3 C 2 C 2 C : Li + C C C 3 C 2 C 2 C 2 C C : Li +
68 Podobně jako u radikálové polymerace se tato fáze reakce nazývá INICIACE. Po ní následuje PROPAGACE. Karbaniont reaguje s dalším a dalším monomerem. Řetězec se neustále prodlužuje. C 3 C 2 C 2 C 2 C C : Li + C C C 3 C 2 C 2 C 2 C C C C : Li + C 3 C 2 C 2 C 2 C C [ ] n Li + C C : Propagace řetězce může probíhat nekonečně dlouho. Karbanionty v podstatě nezanikají, TERMINACE chybí!
69 Reakce se zastaví až po vyčerpání monomeru. Ovšem i pak je již hotový polymer v aktivním stavu a přidáním monomeru se reakce obnoví a pokračuje dále. Takovéto systémy se označují jako "ŽIVÉ POLYMERY". Živé polymery se dají usmrtit přídavkem látek likvidujících karbanionty, např. 2 O. Řízená syntéza blokových kopolymerů : [ ] n A C 2 C C 2 C : + C 3 C C C 2 živý polystyren butadien [ ] [ C ] 2 n n A C 2 C C 2 C C C C : C C živý polystyren-butadienový blokový kopolymer
70 Kationtová polymerace vinylových monomerů Iniciátorem kationtové polymerace jsou obvykle tzv. Lewisovy kyseliny, tj. látky, jejichž atomy mají volný vazebný orbital a mohou tedy přijmout elektronový pár. Příkladem takové sloučeniny je chlorid hlinitý, který s vodou tvoří komplex : Cl Cl Al Cl O Cl Cl Al Cl O Při INICIACI reaguje tento komplex s molekulou monomeru za vzniku karbokationtu : Cl Cl Al Cl O C 3 C 3 C 3 C + + Cl Cl Al - O C 2 C C 3 Cl C 3
71 Karbokationtu chybí elektrony, snaží si je doplnit odkudkoliv. Vhodné místo na získání elektronů je dvojná vazba monomeru. C 3 C 3 C 3 C 3 C 2 C + + C 2 C C 2 C C 2 C + C 3 C 3 C 3 C 3 C 3 C 3 [ ] C 2 C n C 2 C + C 3 C 3 Makromolekulární řetězec se neustále prodlužuje. Dochází k PROPAGACI. Karbokanionty se neustále obnovují.
72 Iniciační činidla pro CR kationtová polymerace Iniciační systém Iniciátor Koiniciátor Iniciující kationt Aniont SO 2 4 SO SO - 4 O/BF 2 3 O 2 BF 3 + BF O - 3 t - BuCl/Et AlCl 2 t - BuCl Et AlCl 2 t - Bu + Et AlCl Cl /BCl 2 3 Cl 2 BCl 3 Cl + BCl - 4
73 Polymerace vinylových monomerů s katalyzátory Ziegler-Natta - umožňuje připravit polymer s požadovanou takticitou - umožňuje přípravu nevětveného PE a PP - mechanismus ještě zdaleka není jasný Ziegler-Nattovy katalyzátory - skládají ze soli přechodného kovu (vlastní katalyzátor) a organokovové sloučeniny prvku III. hlavní skupiny (kokatalyzátor). TiCl 3 Al(C 2 5 ) 2 Cl TiCl 4 Al(C 2 5 ) 3 Cl Cl Ti Cl + Cl Al Cl Cl Ti Cl + Al Cl
74 Takovéto povrchové atomy titanu mají tendeci podlehnou reakci s kokatalyzátorem. Ve vzniklém útvaru je hliník vázán sice pouze koordinačními vazbami, přesto je toto spojení velice stálé. Titanu zůstal ještě jeden volný d-orbital. Ten může využít na tvorbu koordinační vazby s dvojnou vazbou alkenu.
75 Výsledkem je, že se propylen stane součástí rostoucího řetězce, přičemž se obnoví prázdný d-orbital titanu. Může vzniknout komplex s novým propylenem, atd. Řetězec roste a roste. Methylové skupiny jsou v izotaktickém uspořádání.
76 Polymerace vinylových monomerů s metalocenovými katalyzátory Metaloceny - sloučeniny, ve kterých je kovový kationt uzavřen mezi dva cyklopentadienylové anionty - sendvičové sloučeniny Cyklopentadienyl vystupuje jako běžný aniont a s kovovými kationty tvoří vlastně soli.
77 Pokud má kov vyšší náboj, pak se váže s více anionty. Z prostorových důvodů se však cyklopentadienyly vlezou pouze dva, ostatní náboje kationtu se vysytí menšími anionty. Např. pro Zr 4+ se dá připravit sendvičová sloučenina: bis-chlorozirkonocen
78 Polymerační reaktory Vsádkový reaktor (batch reactor) Trubkový reaktor (continuous plug-flow reactor) Vsádkový míchaný kontinuální reaktor CSTR (continuous stirred tank reactor
79 Typy polymeračních reaktorů
80 Možnosti odstranění zbytkového monomeru A) Strand degasser ; B) Tubular evaporator ; C) Degassing extruder ; D) Thin-film evaporator
81 Polymerace výrobní postupy Reakce monomerů na polymery může obecně probíhat diskontinuálně nebo kontinuálně jedním z následujících postupů: polymerace v suspenzi polymerace v bloku polymerace v emulzi polymerace v plynné fázi polymerace v roztoku.
82 Schematické znázornění suspenzní polymerace
83 Schematické znázornění adsorpce na povrchu - disperzanty
84 Polymerace v suspenzi Polymerace v suspenzi je chemickou reakcí, která se uskutečňuje v kapénkách, které jsou v suspenzi rozpouštědla. Polymerace v suspenzi je charakteristická dobrým přenosem reakčního tepla, nízkou disperzní viskozitou a nízkými náklady na separaci na straně jedné, ale také skutečností, že se jedná o diskontinuální proces, a vzniká relativně velké množství odpadních vod, významné množství nálepů na stěnách reaktoru a ve finálním výrobku a odpadech zůstávají suspenzní činidla.
85 Polymerace v suspenzi Typickými produkty vyráběnými procesy v suspenzi jsou: polyvinylchlorid polymethylmethakrylát polystyrén (IPS a EPS) polytetrafluorethylén polyolefiny jako suspenze ve frakcích minerálních olejů.
86 Polymerace v suspenzi Polymerací v suspenzi se tvoří částice latexů o velikosti od 1 až 1000 μm. Výroby se účastní monomer + iniciační činidlo + rozpouštědlo(obvykle voda) + povrchově aktivní látka. Monomer a iniciační činidlo jsou nerozpustné (ve vodě), např. styrén, benzoylperoxid. Monomer je dispergován ve formě kapek (jako při polymerizaci v emulzi), avšak iniciační činidlo je přítomno v kapkách (nikoliv však ve vodné fázi). Úkolem povrchově aktivní látky je stabilizace kapek. Ve vodné fázi se netvoří žádné micely.polymerace je nyní zcela soustředěna uvnitř kapek monomeru. Polymerace se tak podobá polymeraci v mikrobloku, ale omezuje se na každou kapku monomeru. Problémy s přestupem tepla se snižují v porovnání se skutečnou polymerací v bloku, protože vodná fáze může odvádět většinu vytvořeného tepla. Distribuce velikosti finálních částic by měla odpovídat počátečním kapkám emulze monomeru (za předpokladu, že je zabráněno koalescenci).
87 Polymerace v bloku Při polymeraci v bloku se polymer vyrábí v reaktoru, kde je přítomen pouze monomer a malé množství iniciátoru. Polymerace v bloku jsou charakterizovány vysokou čistotou výrobku, vysokými výkony reaktoru a nízkými náklady na separaci, ale také vysokou viskozitou v reaktorech. Procesy v bloku způsobují zanášení reaktoru a v případě polykondenzačních produktů je vyžadováno vysoké vakuum.
88 Polymerace v bloku Typickými produkty vyráběnými procesy v bloku jsou: polyolefiny polystyrén polyvinylchlorid polymethylmethakrylát polyamidy polyestery.
89 Polymerace v emulzi Při emulzní polymeraci se chemická reakce uskutečňuje v kapičkách, které jsou v suspenzi s rozpouštědlem, jako v případě polymerace v suspenzi, ale také v emulzních strukturách, zvaných micely, a v rozpouštědle. Emulzní procesy vykazují nízkou disperzní viskozitu, dobrý přenos tepla, vysokou rychlost konverze a jsou vhodné pro výrobu polymerů s vysokou molární hmotností. Jsou také charakteristické vysokými náklady na separaci, usazováním na stěnách reaktoru a tím, že ve výrobku a odpadech zůstávají emulzní činidla.
90 Emulzní polymerace Schematic representation of an emulsion polymerization A) Particle nucleation stage ; B) Particle growth stage ; C) Monomer finishing stage a) Monomer droplet ; b) Micelle ; c) Emulsifier molecule ; d) Latex particle ; e) Water ; f) Radical ; g) Monomer molecule
91 Polymerace v emulzi Polymerací v emulzi se tvoří částice latexu o velikosti 0,03 až 0,1 μm. Výroby se účastní monomer + iniciátor + rozpouštědlo (obvykle voda) + povrchově aktivní látka (obvykle anionické povahy, např. dodecylsíran sodný). Monomer má pouze velmi omezenou (konečnou) rozpustnost v rozpouštědle (např. styrén ve vodě). Většina monomeru je zpočátku přítomna ve formě dispergovaných kapek (odtud název polymerace v suspenzi ). Úlohou povrchově (anionických) aktivních látek je napomoci stabilizaci těchto kapek adsorpcí na rozhraní kapka/voda. Některé monomery jsou však přítomny ve vodné fázi. Většina povrchově aktivních látek je přítomna ve formě micel, opět ve vodné fázi, a některé monomery jsou rozpuštěny v těchto micelách.
92 Polymerace v emulzi Monomer je tak ve skutečnosti distribuován na tři místa: kapky, vodný roztok (malé množství) a micely. Iniciátor je rozpustný (a tudíž přítomný) ve vodné fázi. Počáteční místo polymerace je opět ve vodném roztoku (jako polymerace v disperzi). Rostoucí oligomerní řetězec bez volných radikálů bude vytvářet micely s existujícími micelami přidané anionické povrchově aktivní látky. Primární místo polymerace se nyní přesouvá na micely, ve kterých rozpuštěný polymer začíná polymerizovat. S pokračující polymerací (v micelách) se začínají tvořit částice jako při polymeraci v disperzi a distribuce monomeru se postupně posouvá doprava. Polymerace pokračuje růstem částic tak dlouho, až veškerý monomer v kapkách a roztoku není spotřebován. Velikost finálních částic je řízena počtem přítomných micel (tj. počáteční koncentrací povrchově aktivní látky).
93 Polymerace v plynné fázi Při polymeraci v plynné fázi je monomer přiváděn v plynné fázi a přichází do kontaktu s katalyzátorem, naneseným na pevném loži. Procesy v plynné fázi umožňují snadný odvod reakčního tepla, jsou zde nízké emise a odpady, a nejsou vyžadována žádná dodatečná rozpouštědla. Procesy v plynné fázi nejsou použitelné pro všechny finální výrobky a investiční náklady jsou relativně vysoké, což je částečně způsobeno tím, že v zařízení je pro většinu výrobních postupů nutný vysoký tlak.
94 POLYMERY II Doc.ing.Jaromír LEDERER, CSc.
95 O ČEM BUDEME MLUVIT ZPRACOVÁNÍ POLYMERŮ REOLOGIE POLYMERŮ
96 Zpracování plastů proč je důležité zkoumat reologické vlastnosti?
97 Zpracovatelské technologie vytlačování pro trubky, profily, desky a izolace kabelů vstřikování pro výrobky růz ných, často velmi složitých tvarů jako jsou strojní části, elektrické svíčky a lékařské vybavení (např. stříkačky); termoplasty a termosety vyfukování pro láhve, nádoby a fólie kalandrování pro fólie a desky rotační tvarování pro velké formáty taže ní pro tyče, potrubí atd. natírání pro tenké vrstvy na různých podkladech stlačování pro pryskyřice spřádání pro vlákna protlačování pro termosety tvarování tlakem pro termosety vulkanizace pro kaučuky směšování obecně použitelná tech nika.
98 Zpracování polymerů a plastů Výrobek Roztavení Tok a tváření Chlazení a Zpevnění
99 Roztavení Tok a tváření taveniny Chlazení a tuhnutí polymeru Zpracování polymerů a plastů
100 Tavení polymeru Roztavení amorfních nebo Semikrystalických polymerů
101 Tavení amorfních polymerů Tuhá látka=skelný stav kaučukovitý stav..tavenina
102 Termomechanická křivka T(g)-teplota zeskelnění T(m) t.tání T(f) t.toku 1.amorfní polymer 2,3..krystalický polymer
103 Tavení semikrystalického polymeru Skelný stav..kaučukovitý stav teplota tání
104 Tečení a formování polymeru Molekuly zapletené navzájem
105 Pomalá deformace Při pomalé deformaci se spletené molekuly převalují a pohybuje se celá masa polymeru odpor k pohybu je vysoký
106 Rychlá deformace Při rychlé deformaci se molekuly protahují a orientují se ve směru toku odpor k pohybu klesá
107 Tok taveniny skrze vstřikovací tryskou Molekuly se převalují protahují..vysoké protažení vratný pochod
108 odnocení tokových vlastností polymerů Tok : nevratná deformace způsobená smykovým napětím Napětí: síla působící na jednotkovou plochu Smykové napětí: napětí působící ve směru tečny k namáhanému tělesu Smyková deformace: charakterizuje změnu tvaru polymeru při působení smykového napětí
109 Model toku
110 Viskozita Smykové napětí smyková rychlost
111 Viskozita..odpor k toku
112 Vliv struktury na viskozitu polymerů
113 Vliv mol. hmotnosti, její distribuce a struktury polymeru na viskozitu
114 Rychlosti toku při různých způsobech zpracování polymerní taveniny tváření, extruze, vstřikování
115 Viskozitní křivka
116 Měření rychlosti toku a viskozity
117 Přístroj pro měření rychlosti toku taveniny Množství vyteklé taveniny
118 Tavný index motnost materiálu, který je vytlačen za časovou jednotku a předepsané teplotě
119 Kapilární rheometr
120 Měření na kapilárním rheometru Konstantní smykové napětí Konstantní smyková rychlost Výpočet viskozity
121 Teplotní stabilita omezení teploty při zpracování polymeru
122 Chlazení taveniny
123 Chlazení taveniny amorfního polymeru
124 Chlazení taveniny semikrystalického polymeru
125 Deformace tahem ookův zákon: Sigma = E * epsilon Sigma.napětí epsilon.deformace E Youngův modul pružnosti
126 SUMMARY
127 Mechanické vlastnosti polymerů
128 Mechanické vlastnosti polymerů
129
130
131
132 Výroba hlavních monomerů J.Lederer
133 Průměrná celosvětová produkce některých monomerů (miliony tun/rok) ethylen 100 propylen 50 vinylchlorid 26 styren 18 akrylonitril 5 kyselina akrylová 2 methylmetakrylát 2 1,3-butadien 8 isopren 1 chloropren 0,5 ethylenoxid 10 propylenoxid 4 epsilon-kaprolaktam 4 kyselina adipová 3 hexamethylendiamin 1 maleinanhydrid 1 ftalanhydrid 4 kyselina tereftalová 16 fenol 6 bisfenol A 2 formaldehyd 17 močovina 95 ethylenglykol 9 vinylacetát 3,5
134 Nejdůležitější jedenáctka ethylen 100 propylen 50 vinylchlorid 26 styren 18 formaldehyd 17 kyselina tereftalová 16 ethylenoxid 10 ethylenglykol 9 1,3-butadien 8 fenol 6 akrylonitril 5 Pozn.: Močovina používána jako monomer jen minoritně
135 Základy výroby ethylenu a propylenu
136 Světové výrobní kapacity a podíl výroby z pyrolýzy Mil.t / rok Podíl výroby( %) Ethylen Propylen ,3-Butadien 9 91 Benzen (Evropa)
137 lavní principy pyrolýzy uhlovodíků nekatalytický proces vysoce endotermní radikálový mechanismus proces řízený kinetikou proces s vysokým nárůstem objemu
138 lavní procesní parametry Vysoká teplota C Nízký tlak max. 0,16 MPa Ředění vodou % hmot. Doba zdržení ms
139
140
141 Tvorba ethylenu a dalších produktů pyrolýzy Primární reakce (Δ > 0, reakce 1.řádu) Iniciace: C 2 6 C 3 + C 3 Propagace: C 3 + C 2 6 C 4 + C 2 5 C 2 5 C C C 2 5 [(β štěpení) R- C 2 C 2 C 2 RC 2 + C 2 = C 2 ] Terminace: + 2 C 3 + C 4 C C 2 6 C C 3 C 3 8 C C 2 5 C 4 10 Sekundární reakce (reakce 2.řádu) C 2 = C 2 + C 2 = C 2 C 2 = C - C = C 2 C 2 = C - C = C 2 + C 2 = C oleje + koks
142 ETYLENOVÁ JEDNOTKA CEMOPETROLU
143 Geometrie reaktorů Lummus SRT III Gradient Kinetics GK6
144 Dělení komplexního produktu pyrolýzy
145
146 Princip výroby hlavních monomerů z ethylenu
147
148 Syntéza vinylchloridu C 2 = C 2 + Cl 2 ClC 2 C 2 Cl ClC 2 C 2 Cl C 2 = CCl + Cl 2 C 2 = C Cl + O 2 2 ClC 2 C 2 Cl O Chlorace ethylenu: Teplota 65 C Katalyzátor FeCl 3 Termolýza DCE: Teplota 500 C Oxichlorace ethylenu: Teplota 220 C Katalyzátor CuCl 2 / Al 2 O 3
149 Výroba vinylchloridu Cl VC DCE, 2 O, Cl Odpad. voda Roztok NaO 500 C Cl 2 DCE Ethylen DCE DCE VC+DCE Cl 95% DCE Lehké podily na spálení Cl 2 Odplyn Vzduch DCE, 2 O, Cl DCE
150 Syntéza ethylenoxidu C2 = C2 + 1/2 O2 Teplota 260 C Tlak MPa Katalyzátory na bázi Ag/SiO2 O EXO CO 2 EXO
151 40 % mol 7 % mol ETYLENOXID ETYLCLORID VINYLCLORID Trubky 1000, 12 m, mm, reakce: x= 7 až 15%
152 Výroba ethylenoxidu s použitím kyslíku Methan CO 2 Odplyn Lehké podily Desorber ethylenoxidu Ethylenoxid Skruber ethylenoxidu Inhibitor Destilační kolona Kyslík Ethylen Stripovací kolona Glykol Ethylenoxid + voda (k výrobě glykolu)
153 Výroba ethylenglykolu hydrolýzou ethylenoxidu 200 C, 2 MPa O + 2 O O-C 2 -C 2 -O Současný vznik oligomerů diethylenglykol, triethylenglykol Vakuová rektifikace na jednotlivé složky. Vliv na selektivitu má velikost přebytku vody nebo přítomnost kyselých katalyzátorů.
154 Syntéza vinylacetátu C 2 = C 2 + C 3 CO 2 + PdCl 2 C 3 CO 2 C = C Cl + Pd Pd + 2 CuCl 2 PdCl CuCl 2 CuCl + 2 Cl + 1/2 O 2 2 CuCl O Teplota C Tlak 1.6 MPa
155 Výroba vinylacetatu Odplyn Kyslík Separační kolona Odparka Kys. octová Voda Ethylen Kyselina octová Trubkový reaktor: C MPa Separátor fází Voda Surový vinylacetat k destilaci
156 Výroba ethylenoxidu s použitím kyslíku Methan CO 2 Odplyn Lehké podily Desorber ethylenoxidu Ethylenoxid Skruber ethylenoxidu Inhibitor Destilační kolona Kyslík Ethylen Stripovací kolona Glykol Ethylenoxid + voda (k výrobě glykolu)
157 Výroba 1,3-butadienu
158 Zpracování a použití C4-frakce
159 Depropanizer d=2500 mm h=26300 mm Vodík z PSA Zbytek deetanizeru Zbytek strip. kolony Inhibitor polymerace 14 C 0.85 MPa DA C 0.88 MPa Depropanizer, debutanizer a propylenová kolona FA C 0.7 MPa FA 406 DC 451 ydrogenační reaktory FA MPa DC C 1.71 MPa DA C 1.8 MPa Propylenová kolona d=6000 mm h=90300 mm Na polní hořák DA FA C 1.63 MPa Debutanizer d=2200 mm h=24300 mm 40 FA C 0.47 MPa Propylen Do pyrolýzy Pyrobenzin C 4 frakce - produkt Pyrobenzin
160 Složení C4-frakcí (% hmot.) Látky C 4 -frakce C 4 -rafinat 1 C 4 -rafinat 2 C ,7 n-butan 2,0 3,9 6,9 isobutan 1,0 2,0 3,4 isobuten 22, ,0 1-buten 14, ,3 2-buten 11, ,9 1,3-butadien 49,0 0,0 0,0 C ,7 Suma
161 Zpracování C 4 frakce C 4 -rafinat 1 DMF Butadieny Druhý extraktor DMF Acetylenový odplyn na spálení První extraktor Stripovací kolona Stripovací kolona Regenerace DMF Kapalná C 4 - frakce C 3 odplyny do topného plynu 1, 3- butadien Destilační kolony 1,3 - butadienu C 5 - zbytky
162 Princip výroby kyseliny akrylové
163 Výroba kyseliny akrylové dvoustupňovou oxidací propylenu multitubes exion - Sokolov Cca 50 kt /rok 400 C 300 C OXIDY Co-Mo-V Oxidation Catalysts. Research on catalysts for propene oxidation to acrylic acid began in the latter half of the 1950 s. The two methods for the heterogeneously catalyzed gas-phase oxidation of propene are single-step and two-step processes: Single-step process: C 2 =CC 3 + 3/2 O 2 C 2 =CCOO + 2 O = kj/mol Two-step process: C 2 =CC 3 + O 2 C=C 2 CO + 2 O = kj/mol C 2 =CCO + 1/2 O 2 C 2 =CCOO = kj/mol
164 Princip výroby akrylonitrilu
165 Výroba akrylonitrilu Sohio Process In the Sohio process propene, oxygen (as air), and ammonia are catalytically converted directly to acrylonitrile using a fluidized-bed reactor operated at temperatures of C pressures of kpa (0.3 2 bar) 2 C 2 =C-C N O 2 2 C 2 =C-C N O Sohio introduced Catalyst 21 (antimony uranium) in 1967, Catalyst 41 (ferrobismuth phosphomolybdate) in 1972, and Catalyst 49 (undisclosed)
166 Syntéza akrylonitrylu 2 C 2 = C-C N O 2 2 C 2 = C-CN O Teplota C Tlak bar Katalyzátory na bázi Bi a Mo
167 Výroba akrylonitrylu Absorber Odplyn Voda Surový akrylonitryl Surový CN Akrylonitryl - produkt Pára Fluidní reaktor C bar Kolona extraktivní destilace Voda Surový acetonitryl Vzduch Amoniak Propylen Destilační kolony Destilační zbytek Stripovací kolona Voda
168 VÝROBA AKRYLONITRILU Simplified diagram of the Sohio acrylonitrile process a) Fluidized-bed reactor; b) Absorber column; c) Extractive distillation column; d) Acetonitrile stripping column; e) Lights fractionation column; f) Product column
169 VÝROBA A VYUŽITÍ AROMÁTŮ BENZENU A PARA-XYLENU
170 VÝROBA AROMÁTŮ DLE ZDROJŮ Jiné zdroje 3% Pyrolyzní benzín 27% Reformát 70%
171 VZNIK AROMÁTŮ REFORMING PYROLÝZA
172 CCR
173 Reforming výroba aromátů
174 Prací kolona a výroba technologické páry Pyroplyn do FA 201 Destilat do FA C 1 Prací kolona d 1 =6300 mm d 2 =8000 mm h=18000 mm 1 NaO 1 DA C Pyroplyn z DA DA DA 104 WQ 80 C FA 121 WP PyBi FD 102 FA 122 Prací voda Technol. voda Těžký PyBi Reflux DA 101
175 Depropanizer d=2500 mm h=26300 mm Vodík z PSA Zbytek deetanizeru Zbytek strip. kolony Inhibitor polymerace 14 C 0.85 MPa DA C 0.88 MPa Depropanizer, debutanizer a propylenová kolona FA C 0.7 MPa FA 406 DC 451 ydrogenační reaktory FA MPa DC C 1.71 MPa DA C 1.8 MPa Propylenová kolona d=6000 mm h=90300 mm Na polní hořák DA FA C 1.63 MPa Debutanizer d=2200 mm h=24300 mm 40 FA C 0.47 MPa Propylen Do pyrolýzy Pyrobenzin C 4 frakce - produkt Pyrobenzin
176 SITUACE V ČR BENZEN Z PYROBENZINU DEALKYLACÍ-LITVÍNOV (200 kt) ETYLBENZEN ALKYLACÍ BENZENU ETYLENEM- LITVÍNOV (180 kt) STYREN DEYDROGENACÍ EB KRALUPY (170 kt) NAFTALEN Z PYROOLEJE LITVÍNOV (15 kt) ANILÍN BC-MCZ OSTRAVA (150 kt) VYŠŠÍ AROMÁTY DEZA (DETOCEMIE) FTALANYDRID DEZA (25 kt)
177 VÝROBA BENZENU KAT. YDRODEALKYLACÍ 200 KT/ROK 600 C, 5 MPa, přebytek vodíku, kat. oxid chromitý na alumině
178 DPG hydrogenace pyrolýzního benzinu Teplota C Tlak 4 MPa LSV = 15 Katalyzátor 0.3% Pd /Al 2 O 3
179 Proces katalytické hydrodealkylace proces Pyrotol nearomáty methan ethan propan dealkylační reakce
180 VÝROBA ETYLBENZENU UNIPETROL: TECNOLOGIE Lummus/UOP (EB ONE) kapalná fáze KAPACITA 300 kt/rok VÝROBA 180 kt/rok
181 Výroba ethylbenzenu alkylační reakce
182 Výroba ethylbenzenu - transalkylace
183 ETYLBENZEN - Schéma technologie T = C, P = 2,8 MPa, velký přebytek benzenu
184 Výroba styrenu - Kaučuk Kralupy (železitý katalyzátor, platinový kat., podtlak, oxidace vodíku, radiální tok, vakuové destilace) Pára ze sítě 40 t/h Kyslík benzen + toluen Vodík 580 C 40% styrenu 750 C 400 C 65-70% styrenu Parní kondenzát Polymery Kapalný etylbenzen 30 t/h Etylbenzen do dehydrogenace Voda Zásobník styrenu ETYLBENZEN STYREN + VODÍK (ENDO)
185 Syntéza fenolu C 3 - C = C O 2 O - O Více reaktorů, t= 4 hod probublávaný reaktor + 2 SO C MPa p 7-8 / C O O - O + (C 3 ) 2 C = O kumen kumenhydroperoxid homogenní heterogenní přebytek acetonu; % 2 SO 4 ; T = 56 C % 2 SO 4 ; C : 2 SO 4 = 1 : 5; T = C
186 Výroba kumenu Benzen z recyklu Kumen Benzen Alkylační reaktory Depropanizer Propan DIPB Propylen Propylen Transalkylační reaktor
187 Výroba fenolu Aceton Fenol katalyzátor Vzduch Štěpení CP Kumen Regenerace uhlovodíku Regenerace fenolu Zpracování odpadních vod Topný olej Odpadní voda α-methylstyren
188 VÝROBA P-XYLENU C 3 3 C
189 lavní fyzikální vlastnosti (princip separace) hustota b.varu b.tání BENZEN 0,88 88,1 +5,5 TOLUEN 0,86 110,6-95 STYREN 0,9 145,2-31 ETYLBENZEN 0,87 136,2-95 o-xylen 0,88 144,4-25 m-xylen 0,86 139,1-48 p-xylen 0,86 138,3 +32
190 KOMPLEXNÍ ZPRACOVÁNÍ REFORMÁTU NA AROMÁTY
191 Adsorpční separace p-xylenu
192 Parex process a) Adsorbent chamber ; b) Rotary valve ; c) Extract column ; d) Raffinate column
193 Isomar process a) eater ; b) Reaction column ; c) ydrogen separation ; d) Recycle compressor ; e) Deheptanizer column
194 OXIDACE P-XYLENU C 3 COO C 3 + O 2 COO NEČISTOTOU JE K. FORMYLBENZOOVÁ ČISTŠÍ PRODUKT: OXIDACE NA DIMETYLTEREFTALÁT P-X + O2 PMB + C30 METESTER PMB+O2 +C3O.. DMTF Oxiace p-xylenu v kapalné fázi. Směs p-xylenu, vzduchu, k. octové a katalyzátoru (soli kobaltu a manganu) je dávkován do reaktoru při teplotě 175 až 230 C a tlaku 2 až 3 MPa, kde se zdrží 0,5 a 3 hodiny. Vzniklá suspenze je ochlazena, kyselina tereftalová se odstředí (krystalická látka), promyje a vysuší.
195 Princip výroby formaldehydu
196 Methanol CO C 3 O DELTA = - 92 /mol Varianty výroby: 1. Vysokotlaký proces BASF: 34 MPa, 320 až 380 C, ZnO + Cr2O3 2. Nízkotlaké procesy ICI: 10 MPa, 240 až 260 C, CuO + ZnO 3. Nízkotlaké procesy Lurgi: 5 MPa, 250 až 260 C, CuO + ZnO (trubkový reaktor) 4. Středotlaké postupy
197 Použití methanolu APLIKACE PODÍL (%) Formaldehyd 40 MTBE 20 Dimethyltereftalát K.octová/acetáty 10 MTO?
198 Princip výroby formaldehydu C 3 O CO + 2 ENDO 2 + ½ O 2 2 O EXO
199 Výroba formaldehydu
200 VÝROBA BISFENOLU A a) Storage tank ; b) Reactor ; c) Column ; d) Crystallizer ; e) Separator ; f ) Melt ; g) Desorber ; h) Flaking off
201 VÝROBA BISFENOLU A FENOL + ACETON BISFENOL A PRINCIP REAKCE Sulfonated cross-linked polystyrenes [372], [377][378][379] are used as the catalyst which are usually arranged as a fixed bed over which the reaction mixture is passed. The reaction of phenol with acetone takes place at C, the molar ratio phenol acetone is up to 15 :1.
202 VÝROBA K.TEREFTALOVÉ A feed mixture of p-xylene, acetic acid, and catalyst is continuously fed to the oxidation reactor (Fig. (1)). The feed mixture also contains water, which is a byproduct of the reaction. The reactor is operated at C and kpa. Compressed air is added to the reactor in excess of stoichiometric requirements to provide measurable oxygen partial pressure and to achieve high p-xylene conversion.
203 VÝROBA K.TEREFTALOVÉ Catalytic, liquid-phase oxidation of p-xylene to terephthalic acid by the Amoco process a) Oxidation reactor ; b) Surge vessel ; c) Filter ; d) Dryer ; e) Residue still ; f ) Dehydration column
204 VÝROBA K.TEREFTALOVÉ Purification of terephthalic acid by the Amoco process a) Slurry drum ; b) ydrogenation reactor ; c) Crystallizers ; d) Centrifuge ; e) Dryer
205 VÝROBA DIMETYLTEREFTALÁTU Production of dimethyl terephthalate by the Dynamit Nobel process a) Oxidation reactor ; b) Esterifier ; c) Expansion vessel ; d) Methanol recovery column ; e, f ) Methyl p-toluate and dimethyl terephthalate columns ; g, j) Dissolvers ; h, k) Crystallizers ; i, l) Centrifuges
206 VÝROBA DIMETYLTEREFTALÁTU
207 Fresh and recovered p-xylene, along with catalyst (mostly cobalt with some manganese) are combined with methyl p-toluate and fed to the liquid-phase oxidation reactor. Because bromine and acetic acid are not used, vessels lined with titanium or other expensive metals are not necessary. Oxygen supplied by compressed air is added at the bottom. Oxidation conditions are C and kpa. The heat generated by oxidation is removed by vapors of unreacted p-xylene and the water of reaction. Cooling coils in the reactor are used to generate steam. The steam and reactor vapors are condensed and combined to recover p-xylene for recycle.
208 The oxidation effluent is then heated and sent to the esterification reactor, operated at 250 C and 2500 kpa. Excess vaporized methanol is sparged into the esterifier, where the p- toluic acid and monomethyl terephthalate are converted noncatalytically to methyl p-toluate and dimethyl terephthalate, respectively. Overhead vapors from the esterification reactor are condensed and fed to a distillation system, where the water from the esterification is separated from methanol, which is recycled. The remainder of the process separates the dimethyl terephthalate from methanol and methyl p-toluate, which are recycled, and residue and wastewater, which go to waste treatment.
209 The product from the esterifier goes to an expansion vessel. Vapor from this vessel feeds a methanol recovery column, where the methanol overhead goes to methanol recovery, and the methyl p- toluate bottoms are recycled to the oxidation reactor. Liquid from the expansion vessel feeds two vacuum distillation columns in series, which yield crude dimethyl terephthalate. The first column recovers more methyl p-toluate overhead for recycle to oxidation, and the bottoms feeds the crude dimethyl terephthalate column, where the product is taken overhead. The bottoms from the dimethyl terephthalate column, containing heavy byproducts and catalyst metals, can be mixed with water from the oxidation, which dissolves the catalyst. The resulting slurry is centrifuged ; the catalyst solution is recycled, and the cake is sent to disposal.
210 Výroba dalších významných monomerů isokyanáty, epsilon-kaprolaktam, bisfenol A, epichlorhydrin, PET
211 POLYURETANY (PUR)
212 Vznik isokyanátu
213 Vznik uretanu R-N 2 + COCl 2 R-N=C=O isokyanát alkohol R-N=C=O + O-R R-N-CO-O-R URETANY = ESTERY KYSELINY KARBAMOVÉ -O-C-N 2 O
214 Reakce uretanů látky s aktivním vodíkem R-NCO + 2 N-R* R N-CO-N-R* ALKYLOVANÉ MOČOVINY R-NCO + 2 O R-N 2 + CO 2 REAKCÍ S VODOU SE UVOLŇUJE OXID ULIČITÝ
215 Základní reakce isokyanátů
216 Technicky důležité polyisokyanáty examethylendiisokyanát OCN-(C 2 )6-NCO { } rozmanitost diizokyanáto dicyklohexylmethan 2,4 toluen diisokyanát 4,4 -diisokyanatodifenylmethan (kondenzace anilinu a formaldehydu)
217 Vznik polyolů polyetheralkoholy, polyesteralkoholy (propylenoxid, ethylenoxid + voda, alkoholy, dioly) C 2 C 2 + O-C 2 -C 2 -O O O-C 2 -C 2 -O-C 2 -C 2 -O dikarboxylová kyselina + přebytek diolu
218 Polyesteralkoholy C 3 O O C O C O C 3 + O C 2 C 2 O -2 C 3 O O C 2 C 2 O O C O C O C 2 C 2 O
219 Tolylendiizokyanát hlavní monomer pro výrobu polyuretanů 1. Nitrace toluenu na dinitrotoluen 2. ydrogenace dinitrotoluenu na toluendiamin 3. Fosgenace na tolylendiisokyanát Fosgen vzniká slučováním oxidu uhelnatého s chlorem při trplotě od 130 C do 150 C z přítomnosti katlyzátoru, kterým je aktivní uhlí nebo houbovitá platina CO + Cl 2 COCl 2
220 Výroba TDI a MDI
221 Výroba TDI a MDI
222 Fosgenace 1. krok: studená fosgenace Reakce primárních aminů s fosgenem v rozpouštědle (dichlorbenzen) při 0 až 50 C za tvorby karbamidchloridu a hydrochloriduaminů 2. krok: horká fosgenace 170 C až 180 C reakce s dalším fosgenem..diisokyanát
223 Výroba TDI a MDI
224 Výroba TDI
225 Výroba 4,4 - difenylmethandiisokyanátu MDI 1. krok: kondenzace anilinu s formaldehydem 2. krok: fosgenace 4,4 - diaminodifenylmethanu
226 Variantní méně rozšířené technologie bez fosgenu
227 Světové výrobní kapacity TDI
228 Světové výrobní kapacity MDI
229 MDI 4,4 -difenylmethandiisokyanát 1. Kondenzace anilinu s formaldehydem 2. Fosgenace na MDI
230 Další významné diisikyanáty
231 ydrogenovaný MDI
232 Kaprolaktam
233
234
235
236
237
238
239
240 Monomery pro výrobu epoxidů
241 Reakce dianu (bisfenolu A) s epichlorhydrinem
242 VÝROBA BISFENOLU A FENOL + ACETON BISFENOL A PRINCIP REAKCE Sulfonated cross-linked polystyrenes [372], [377][378][379] are used as the catalyst which are usually arranged as a fixed bed over which the reaction mixture is passed. The reaction of phenol with acetone takes place at C, the molar ratio phenol acetone is up to 15 :1.
243 Epichlorhydrin 1. Vysokoteplotní radikálová substituce 2. Adice k.chlorné 3. Eliminace chlorovodíku (vápenné mléko)
244 Kyselina tereftalová, dimethyltereftalát
245 OXIDACE P-XYLENU C 3 COO C 3 + O 2 COO NEČISTOTOU JE K. FORMYLBENZOOVÁ ČISTŠÍ PRODUKT: OXIDACE NA DIMETYLTEREFTALÁT P-X + O2 PMB + C30 METESTER PMB+O2 +C3O.. DMTF Oxiace p-xylenu v kapalné fázi. Směs p-xylenu, vzduchu, k. octové a katalyzátoru (soli kobaltu a manganu) je dávkován do reaktoru při teplotě 175 až 230 C a tlaku 2 až 3 MPa, kde se zdrží 0,5 a 3 hodiny. Vzniklá suspenze je ochlazena, kyselina tereftalová se odstředí (krystalická látka), promyje a vysuší.
246 VÝROBA K.TEREFTALOVÉ A feed mixture of p-xylene, acetic acid, and catalyst is continuously fed to the oxidation reactor (Fig. (1)). The feed mixture also contains water, which is a byproduct of the reaction. The reactor is operated at C and kpa. Compressed air is added to the reactor in excess of stoichiometric requirements to provide measurable oxygen partial pressure and to achieve high p-xylene conversion.
247 VÝROBA K.TEREFTALOVÉ Catalytic, liquid-phase oxidation of p-xylene to terephthalic acid by the Amoco process a) Oxidation reactor ; b) Surge vessel ; c) Filter ; d) Dryer ; e) Residue still ; f ) Dehydration column
248 VÝROBA K.TEREFTALOVÉ Purification of terephthalic acid by the Amoco process a) Slurry drum ; b) ydrogenation reactor ; c) Crystallizers ; d) Centrifuge ; e) Dryer
249 VÝROBA DIMETYLTEREFTALÁTU
250 Fresh and recovered p-xylene, along with catalyst (mostly cobalt with some manganese) are combined with methyl p-toluate and fed to the liquid-phase oxidation reactor. Because bromine and acetic acid are not used, vessels lined with titanium or other expensive metals are not necessary. Oxygen supplied by compressed air is added at the bottom. Oxidation conditions are C and kpa. The heat generated by oxidation is removed by vapors of unreacted p-xylene and the water of reaction. Cooling coils in the reactor are used to generate steam. The steam and reactor vapors are condensed and combined to recover p-xylene for recycle.
251 The oxidation effluent is then heated and sent to the esterification reactor, operated at 250 C and 2500 kpa. Excess vaporized methanol is sparged into the esterifier, where the p- toluic acid and monomethyl terephthalate are converted noncatalytically to methyl p-toluate and dimethyl terephthalate, respectively. Overhead vapors from the esterification reactor are condensed and fed to a distillation system, where the water from the esterification is separated from methanol, which is recycled. The remainder of the process separates the dimethyl terephthalate from methanol and methyl p-toluate, which are recycled, and residue and wastewater, which go to waste treatment.
252 The product from the esterifier goes to an expansion vessel. Vapor from this vessel feeds a methanol recovery column, where the methanol overhead goes to methanol recovery, and the methyl p- toluate bottoms are recycled to the oxidation reactor. Liquid from the expansion vessel feeds two vacuum distillation columns in series, which yield crude dimethyl terephthalate. The first column recovers more methyl p-toluate overhead for recycle to oxidation, and the bottoms feeds the crude dimethyl terephthalate column, where the product is taken overhead. The bottoms from the dimethyl terephthalate column, containing heavy byproducts and catalyst metals, can be mixed with water from the oxidation, which dissolves the catalyst. The resulting slurry is centrifuged ; the catalyst solution is recycled, and the cake is sent to disposal.
POLYMERY PRINCIPY, STRUKTURA, VLASTNOSTI. Doc. ing. Jaromír LEDERER, CSc.
 POLYMERY PRINCIPY, STRUKTURA, VLASTNOSTI Doc. ing. Jaromír LEDERER, CSc. O čem budeme mluvit Úvod do chemie a technologie polymerů Makromolekulární řetězce Struktura, fázový stav a základní vlastnosti
POLYMERY PRINCIPY, STRUKTURA, VLASTNOSTI Doc. ing. Jaromír LEDERER, CSc. O čem budeme mluvit Úvod do chemie a technologie polymerů Makromolekulární řetězce Struktura, fázový stav a základní vlastnosti
POLYMERY II MECHANISMY VZNIKU VÝROBNÍ POSTUPY
 PLYMERY II MEANISMY VZNIKU VÝRBNÍ PSTUPY čem budeme mluvit Typy polymeračních reakcí mechanismy Základní způsoby výroby polymerů PLYMERAČNÍ REAKE ADIČNÍ KNDENZAČNÍ ŘETĚZVÉ PSTUPNÉ KRDINAČNÍ (ZIEGLER-NATTA)
PLYMERY II MEANISMY VZNIKU VÝRBNÍ PSTUPY čem budeme mluvit Typy polymeračních reakcí mechanismy Základní způsoby výroby polymerů PLYMERAČNÍ REAKE ADIČNÍ KNDENZAČNÍ ŘETĚZVÉ PSTUPNÉ KRDINAČNÍ (ZIEGLER-NATTA)
Výroba dalších významných monomerů. isokyanáty, k.benzoová, epsilonkaprolaktam, trinitrotoluen, bisfenol A, epichlorhydrin, monomery PET
 Výroba dalších významných monomerů isokyanáty, k.benzoová, epsilonkaprolaktam, trinitrotoluen, bisfenol A, epichlorhydrin, monomery PET POLYURETANY (PUR) Vznik isokyanátu Vznik uretanu R-NH 2 + COCl 2
Výroba dalších významných monomerů isokyanáty, k.benzoová, epsilonkaprolaktam, trinitrotoluen, bisfenol A, epichlorhydrin, monomery PET POLYURETANY (PUR) Vznik isokyanátu Vznik uretanu R-NH 2 + COCl 2
VÝROBA A VYUŽITÍ AROMÁTŮ
 VÝROBA A VYUŽITÍ AROMÁTŮ AROMÁTY OBECNÉ INFORMACE VÝROBA V ČR OPTIMÁLNÍ VÝROBA VARIANTY HLAVNÍ DERIVÁTY SITUACE V PRODUKCI AROMÁTŮ V ZÁPADNÍ EVROPĚ TRH AROMÁTŮ V ZÁPADNÍ EVROPĚ MIL. T/ROK MLD. US$ Spotřeba
VÝROBA A VYUŽITÍ AROMÁTŮ AROMÁTY OBECNÉ INFORMACE VÝROBA V ČR OPTIMÁLNÍ VÝROBA VARIANTY HLAVNÍ DERIVÁTY SITUACE V PRODUKCI AROMÁTŮ V ZÁPADNÍ EVROPĚ TRH AROMÁTŮ V ZÁPADNÍ EVROPĚ MIL. T/ROK MLD. US$ Spotřeba
MAKROMOLEKULÁRNÍ LÁTKY
 MAKROMOLEKULÁRNÍ LÁTKY 1. Základní pojmy - makromolekulární látky = molekulové systémy složené z velkého počtu atomů, které jsou vázány chemickou vazbou do dlouhých řetězců - řetězce jsou tvořeny stavebními
MAKROMOLEKULÁRNÍ LÁTKY 1. Základní pojmy - makromolekulární látky = molekulové systémy složené z velkého počtu atomů, které jsou vázány chemickou vazbou do dlouhých řetězců - řetězce jsou tvořeny stavebními
Celosvětová produkce plastů
 PRODUKCE PLASTŮ Zpracování plastů cvičení 1 TU v Liberci, FS Celosvětová produkce plastů Mil. tun Asie (bez Japonska) 16 % Střední a západní Evropa 21 % Společenství nezávislých států 3 % 235 mil. tun
PRODUKCE PLASTŮ Zpracování plastů cvičení 1 TU v Liberci, FS Celosvětová produkce plastů Mil. tun Asie (bez Japonska) 16 % Střední a západní Evropa 21 % Společenství nezávislých států 3 % 235 mil. tun
(-NH-CO-) Typy polyamidů
 POLYAMIDY (NYLONY) Typy polyamidů (-NH-CO-) AB typ Ty jsou vyráběny polymerací laktamů nebo ω- aminokyselin, kde A označuje aminovou skupinu a B karboxylovou skupinu a obě jsou částí stejné monomerní molekuly.
POLYAMIDY (NYLONY) Typy polyamidů (-NH-CO-) AB typ Ty jsou vyráběny polymerací laktamů nebo ω- aminokyselin, kde A označuje aminovou skupinu a B karboxylovou skupinu a obě jsou částí stejné monomerní molekuly.
Kopolymerace polymerace dvou a více monomerů
 Kopolymerace polymerace dvou a více monomerů ( 1 monomer homopolymer; 2 monomery kopolymer; 3 monomery ternární kopolymer [ př ABS]) mezní případy kopolymerace: n A n B A A n B B n A B n Struktury vznikajících
Kopolymerace polymerace dvou a více monomerů ( 1 monomer homopolymer; 2 monomery kopolymer; 3 monomery ternární kopolymer [ př ABS]) mezní případy kopolymerace: n A n B A A n B B n A B n Struktury vznikajících
18MTY 9. přenáška polymery 2
 18MTY 9. přenáška polymery 2 Zkouškové okruhy Důležité vazby v polymerech Nejvýznamnější a nejvíce vyráběné polymery Co rozumíme pod pojmem konfigurace? Je konfigurace z chemického hlediska trvalá? Vysvětlete
18MTY 9. přenáška polymery 2 Zkouškové okruhy Důležité vazby v polymerech Nejvýznamnější a nejvíce vyráběné polymery Co rozumíme pod pojmem konfigurace? Je konfigurace z chemického hlediska trvalá? Vysvětlete
Struktura polymerů. Příprava (výroba).struktura vlastnosti. Materiálové inženýrství (Nauka o materiálu) Základní představy: přírodní vs.
 Struktura polymerů Základní představy: přírodní vs. syntetické V.Švorčík, vaclav.svorcik@vscht.cz celulóza přírodní kaučuk Příprava (výroba).struktura vlastnosti Materiálové inženýrství (Nauka o materiálu)
Struktura polymerů Základní představy: přírodní vs. syntetické V.Švorčík, vaclav.svorcik@vscht.cz celulóza přírodní kaučuk Příprava (výroba).struktura vlastnosti Materiálové inženýrství (Nauka o materiálu)
Polymery lze rozdělit podle několika kritérií. Podle původu rozlišujeme polymery přírodní a syntetické. Přírodní polymery jsou:
 MAKROMOLEKULÁRNÍ LÁTKY (POLYMERY) Makromolekuly jsou molekulové systémy složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců. Tyto řetězce tvoří pravidelně se opakující části,
MAKROMOLEKULÁRNÍ LÁTKY (POLYMERY) Makromolekuly jsou molekulové systémy složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců. Tyto řetězce tvoří pravidelně se opakující části,
TVORBA UHLÍKATÝCH PRODUKTŮ PŘI I PYROLÝZE UHLOVODÍKŮ
 TVORBA UHLÍKATÝCH PRODUKTŮ PŘI I PYROLÝZE UHLOVODÍKŮ Martin Hrádel 5. ročník Školitel: Doc. Ing. Zdeněk Bělohlav, CSc. Obsah Úvod Mechanismus vzniku a vlastnosti uhlíkatých produktů Provozního sledování
TVORBA UHLÍKATÝCH PRODUKTŮ PŘI I PYROLÝZE UHLOVODÍKŮ Martin Hrádel 5. ročník Školitel: Doc. Ing. Zdeněk Bělohlav, CSc. Obsah Úvod Mechanismus vzniku a vlastnosti uhlíkatých produktů Provozního sledování
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009
 Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Plasty Plasty, známé také pod názvem plastické hmoty nebo pod ne zcela přesným (obecnějším) názvem umělé hmoty,
Projekt: Inovace oboru Mechatronik pro Zlínský kraj Registrační číslo: CZ.1.07/1.1.08/03.0009 Plasty Plasty, známé také pod názvem plastické hmoty nebo pod ne zcela přesným (obecnějším) názvem umělé hmoty,
kopolymerace kopolymery
 kopolymerace kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické
kopolymerace kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické
Makromolekulární látky
 Makromolekulární látky Učební texty k výuce chemie školní rok 2016/2017 Makromolekuly látky složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců látky s velkou relativní molekulovou
Makromolekulární látky Učební texty k výuce chemie školní rok 2016/2017 Makromolekuly látky složené z velkého počtu atomů vázaných chemickými vazbami do dlouhých řetězců látky s velkou relativní molekulovou
Přírodní proteiny, nukleové kyseliny (NA)
 kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické akrylonitril-butadien-styrenový
kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické akrylonitril-butadien-styrenový
Plasty. Základy materiálového inženýrství. Katedra materiálu Strojní fakulty Technická univerzita v Liberci Doc. Ing. Karel Daďourek, 2010
 Plasty Základy materiálového inženýrství Katedra materiálu Strojní fakulty Technická univerzita v Liberci Doc. Ing. Karel Daďourek, 2010 Základní vlastnosti plastů Výroba z levných surovin. Jsou to sloučeniny
Plasty Základy materiálového inženýrství Katedra materiálu Strojní fakulty Technická univerzita v Liberci Doc. Ing. Karel Daďourek, 2010 Základní vlastnosti plastů Výroba z levných surovin. Jsou to sloučeniny
Základní formy využití polymerů. Aditivy do polymerních látek Plasty Nátěrové hmoty Vlákna
 Základní formy využití polymerů Aditivy do polymerních látek Plasty Nátěrové hmoty Vlákna ADITIVY DO POLYMERŮ POLMER + ADITIVUM = PLAST. PŘÍDAVNÉ LÁTKY DO HDPE/PP ZBYTKY KATALYTICKÉHO SYSTÉMU (SiO2, chromocen,
Základní formy využití polymerů Aditivy do polymerních látek Plasty Nátěrové hmoty Vlákna ADITIVY DO POLYMERŮ POLMER + ADITIVUM = PLAST. PŘÍDAVNÉ LÁTKY DO HDPE/PP ZBYTKY KATALYTICKÉHO SYSTÉMU (SiO2, chromocen,
PLASTY A SYNTETICKÁ VLÁKNA
 PLASTY A SYNTETICKÁ VLÁKNA Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 15. 1. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemie a společnost 1 Anotace: Žáci se seznámí
PLASTY A SYNTETICKÁ VLÁKNA Autor: Mgr. Stanislava Bubíková Datum (období) tvorby: 15. 1. 2013 Ročník: devátý Vzdělávací oblast: Člověk a příroda / Chemie / Chemie a společnost 1 Anotace: Žáci se seznámí
Titanic Costa Concordia
 18MTY-polymery Titanic 15. 4. 1912 Costa Concordia 13. 1. 2012 Pro dlouhou historii nesprávného užití jsou plasty vysmívány Pelíšky (1999) Definice polymerů/plastů Organické látky založené na opakující
18MTY-polymery Titanic 15. 4. 1912 Costa Concordia 13. 1. 2012 Pro dlouhou historii nesprávného užití jsou plasty vysmívány Pelíšky (1999) Definice polymerů/plastů Organické látky založené na opakující
H H C C C C C C H CH 3 H C C H H H H H H
 Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Alkany a cykloalkany sexta Martin Dojiva uhlovodíky obsahující pouze jednoduché vazby obecný vzorec alkanů: C n 2n+2 cykloalkanů: C n 2n homologický přírůstek C 2 Dělení alkanů přímé větvené u větvených
Přírodní proteiny, nukleové kyseliny (NA)
 kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické akrylonitril-butadien-styrenový
kopolymery 1 kopolymery - homopolymer - kopolymer - vzniklé ze dvou či více druhů monomerů - Kopolymerizace (řetězová, stupňovitá) - pseudokopolymer (PVA) - PA, PES není kopolymer Syntetické akrylonitril-butadien-styrenový
Prof. Ing. Václav Švorčík, DrSc.
 Prof. Ing. Václav Švorčík, DrSc. Ústav inženýrství pevných látek Fakulta chemické technologie Vysoká škola chemicko-technologická v Praze tel.: 220445149, 220445150 e-mail: vaclav.svorcik@vscht.cz Sylabus
Prof. Ing. Václav Švorčík, DrSc. Ústav inženýrství pevných látek Fakulta chemické technologie Vysoká škola chemicko-technologická v Praze tel.: 220445149, 220445150 e-mail: vaclav.svorcik@vscht.cz Sylabus
PETROCHEMIE J.LEDERER
 PETROCHEMIE J.LEDERER PILÍŘE PETROCHEMIE ALKENY ETHYLEN, PROPYLEN BUTADIEN AROMÁTY BENZEN TOLUEN XYLENY VODÍK, SYNTÉZNÍ PLYNY OSTATNÍ PETROCHEMIE AMONIAK, METHANOL, GTL PRODUKTY PLASTY SYNTETICKÁ VLÁKNA
PETROCHEMIE J.LEDERER PILÍŘE PETROCHEMIE ALKENY ETHYLEN, PROPYLEN BUTADIEN AROMÁTY BENZEN TOLUEN XYLENY VODÍK, SYNTÉZNÍ PLYNY OSTATNÍ PETROCHEMIE AMONIAK, METHANOL, GTL PRODUKTY PLASTY SYNTETICKÁ VLÁKNA
Polymery a plasty v praxi POLYSTYREN & KOPOLYMERY STYRÉMU
 Polymery a plasty v praxi POLYSTYREN & KOPOLYMERY STYRÉMU RNDr. Ladislav Pospíšil, CSc. pospisil@gascontrolplast.cz 29716@mail.muni.cz 21. 3.2016 POLYMERY A PLASTY V PRAXI 1 POLYSTYREN & KOPOLYMERY STYRÉNU
Polymery a plasty v praxi POLYSTYREN & KOPOLYMERY STYRÉMU RNDr. Ladislav Pospíšil, CSc. pospisil@gascontrolplast.cz 29716@mail.muni.cz 21. 3.2016 POLYMERY A PLASTY V PRAXI 1 POLYSTYREN & KOPOLYMERY STYRÉNU
MAKROMOLEKULÁRNÍ CHEMIE
 MAKROMOLEKULÁRNÍ Doporučená literatura: CHEMIE OCH/MMC/MMCH doc.rndr. Jakub Stýskala, Ph.D. 1. Nálepa K.: Stručné základy chemie a fyziky polymerů, UPOL, 1990 2. Vollmert B: Základy makromolekulární chemie,
MAKROMOLEKULÁRNÍ Doporučená literatura: CHEMIE OCH/MMC/MMCH doc.rndr. Jakub Stýskala, Ph.D. 1. Nálepa K.: Stručné základy chemie a fyziky polymerů, UPOL, 1990 2. Vollmert B: Základy makromolekulární chemie,
Podstata plastů [1] Polymery
![Podstata plastů [1] Polymery Podstata plastů [1] Polymery](/thumbs/33/15817342.jpg) PLASTY Podstata plastů [1] Materiály, jejichž podstatnou část tvoří organické makromolekulami látky (polymery). Kromě látek polymerní povahy obsahují plasty ještě přísady (aditiva) jejichž účelem je specifická
PLASTY Podstata plastů [1] Materiály, jejichž podstatnou část tvoří organické makromolekulami látky (polymery). Kromě látek polymerní povahy obsahují plasty ještě přísady (aditiva) jejichž účelem je specifická
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 16, 566 01 Vysoké Mýto Alkeny Vlastnosti dvojné vazby Hybridizace uhlíku vázaného dvojnou vazbou je sp. Valenční úhel který svírají vazby na uhlíkovém atomu je přibližně
Gymnázium Vysoké Mýto nám. Vaňorného 16, 566 01 Vysoké Mýto Alkeny Vlastnosti dvojné vazby Hybridizace uhlíku vázaného dvojnou vazbou je sp. Valenční úhel který svírají vazby na uhlíkovém atomu je přibližně
Gymnázium Vysoké Mýto nám. Vaňorného 163, Vysoké Mýto
 Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto H 3 C Vymezení arenů V aromatickém cyklu dochází k průniku orbitalů kolmých k rovině cyklu. Vzniká tzv. delokalizovaná vazba π. Stabilita benzenu
Gymnázium Vysoké Mýto nám. Vaňorného 163, 566 01 Vysoké Mýto H 3 C Vymezení arenů V aromatickém cyklu dochází k průniku orbitalů kolmých k rovině cyklu. Vzniká tzv. delokalizovaná vazba π. Stabilita benzenu
ALKENY NENASYCENÉ UHLOVODÍKY
 ALKENY NENASYCENÉ ULOVODÍKY 1 ALKENY - mají ve svých molekulách alespoň jednu dvojnou vazbu- C=C homologický vzorec : C n 2n názvy od alkanů zakončeny koncovkou en CYKLOALKENY - homologický vzorec : C
ALKENY NENASYCENÉ ULOVODÍKY 1 ALKENY - mají ve svých molekulách alespoň jednu dvojnou vazbu- C=C homologický vzorec : C n 2n názvy od alkanů zakončeny koncovkou en CYKLOALKENY - homologický vzorec : C
zpracování těžkých frakcí na motorová paliva (mazut i vakuový zbytek)
 Ropa štěpné procesy zpracování těžkých frakcí na motorová paliva (mazut i vakuový zbytek) typy štěpných procesů: - termické krakování - katalytické krakování - hydrogenační krakování (hydrokrakování) podmínky
Ropa štěpné procesy zpracování těžkých frakcí na motorová paliva (mazut i vakuový zbytek) typy štěpných procesů: - termické krakování - katalytické krakování - hydrogenační krakování (hydrokrakování) podmínky
Prof. Ing. Václav Švorčík, DrSc.
 Prof. Ing. Václav Švorčík, DrSc. Ústav inženýrství pevných látek Fakulta chemické technologie Vysoká škola chemicko-technologická v Praze tel.: 220445149, 220445150 e-mail: vaclav.svorcik@vscht.cz tkáňové
Prof. Ing. Václav Švorčík, DrSc. Ústav inženýrství pevných látek Fakulta chemické technologie Vysoká škola chemicko-technologická v Praze tel.: 220445149, 220445150 e-mail: vaclav.svorcik@vscht.cz tkáňové
TERMICKÉ PROCESY PŘI VYUŽITÍ ALTERNATIVNÍCH SUROVIN. Most, 13.6.2013 Autor: Doc. Ing. J.LEDERER, CSc.
 TERMICKÉ PROCESY PŘI VYUŽITÍ ALTERNATIVNÍCH SUROVIN Most, 13.6.2013 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH PRINCIPY POUŽÍVANÝCH TERMOCHEMICKÝCH PROCESŮ VELKOKAPACITNÍ REALIZACE TERMOCHEMICKÝCH PROCESŮ
TERMICKÉ PROCESY PŘI VYUŽITÍ ALTERNATIVNÍCH SUROVIN Most, 13.6.2013 Autor: Doc. Ing. J.LEDERER, CSc. OBSAH PRINCIPY POUŽÍVANÝCH TERMOCHEMICKÝCH PROCESŮ VELKOKAPACITNÍ REALIZACE TERMOCHEMICKÝCH PROCESŮ
Jaromír Literák. Zelená chemie Problematika odpadů, recyklace
 Zelená chemie Problematika odpadů, recyklace Problematika odpadů Vznik odpadů a odpadní energie ve všech fázích životního cyklu. dpadem se může stát samotný výrobek na konci životního cyklu. Vznik odpadů
Zelená chemie Problematika odpadů, recyklace Problematika odpadů Vznik odpadů a odpadní energie ve všech fázích životního cyklu. dpadem se může stát samotný výrobek na konci životního cyklu. Vznik odpadů
Nauka o materiálu. Přednáška č.13 Polymery
 Nauka o materiálu Přednáška č.13 Polymery Úvod Technické materiály, které jsou určeny k dalšímu technologickému zpracování zahrnují širokou škálu možného chemického složení, různou vnitřní stavbu a různé
Nauka o materiálu Přednáška č.13 Polymery Úvod Technické materiály, které jsou určeny k dalšímu technologickému zpracování zahrnují širokou škálu možného chemického složení, různou vnitřní stavbu a různé
Polymerační způsoby. Bloková polymerace: monomer + iniciátor (0,1%) + (event. regulátor)
 Polymerační způsoby Technika provedení radikálové polymerace: Polymerace homogenní: a) bloková b) roztoková Polymerace heterogenní: a) srážecí b) suspenzní c) emulzní d) ostatní polymerace Bloková polymerace:
Polymerační způsoby Technika provedení radikálové polymerace: Polymerace homogenní: a) bloková b) roztoková Polymerace heterogenní: a) srážecí b) suspenzní c) emulzní d) ostatní polymerace Bloková polymerace:
Průmysl dusíku. amoniak - kyselina dusičná - dusičnan amonný - močovina - chloramin - hydrazin. NaClO NaOH CO(NH 2 ) 2.
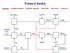 Průmysl dusíku amoniak - kyselina dusičná - dusičnan amonný - močovina - chloramin - hydrazin CO(NH 2 ) 2 NaClO NaOH NH 2 Cl N 2 H 4 methan CO 2 (uhlí, ropa) H 2 NH 3 NO 2 HNO 3 O 2 vzduch voda vzduch
Průmysl dusíku amoniak - kyselina dusičná - dusičnan amonný - močovina - chloramin - hydrazin CO(NH 2 ) 2 NaClO NaOH NH 2 Cl N 2 H 4 methan CO 2 (uhlí, ropa) H 2 NH 3 NO 2 HNO 3 O 2 vzduch voda vzduch
Amoniak. 1913 průmyslová výroba syntetického amoniaku
 Amoniak 1913 průmyslová výroba syntetického amoniaku využití 20 % výroba dusíkatých hnojiv 80 % nejrůznější odvětví průmyslu (plasty, vlákna, výbušiny, hydrazin, aminy, amidy, nitrily a další organické
Amoniak 1913 průmyslová výroba syntetického amoniaku využití 20 % výroba dusíkatých hnojiv 80 % nejrůznější odvětví průmyslu (plasty, vlákna, výbušiny, hydrazin, aminy, amidy, nitrily a další organické
POLYAMIDY (NYLONY) Doc.ing.Jaromír LEDERER, CSc.
 POLYAMIDY (NYLONY) Doc.ing.Jaromír LEDERER, CSc. Typy polyamidů (-NH-CO-) AB typ Ty jsou vyráběny polymerací laktamů nebo ω- aminokyselin, kde A označuje aminovou skupinu a B karboxylovou skupinu a obě
POLYAMIDY (NYLONY) Doc.ing.Jaromír LEDERER, CSc. Typy polyamidů (-NH-CO-) AB typ Ty jsou vyráběny polymerací laktamů nebo ω- aminokyselin, kde A označuje aminovou skupinu a B karboxylovou skupinu a obě
Ropa Kondenzované uhlovodíky
 Nejdůležitější surovina pro výrobu organických sloučenin Nejvýznamnější surovina světové ekonomiky Výroba energie Chemické zpracování - 15 % Cena a zásoby ropy (70-100 let) Ropné krize Nutnost hledání
Nejdůležitější surovina pro výrobu organických sloučenin Nejvýznamnější surovina světové ekonomiky Výroba energie Chemické zpracování - 15 % Cena a zásoby ropy (70-100 let) Ropné krize Nutnost hledání
Alkeny. Alkeny. Největšíprůmyslový význam majíethen (ethylen) a propen (propylen) jako suroviny pro další přeměny nebo pro polymerace
 Alkeny Dvojná vazba je tvořena jednou vazbou sigma a jednou vazbou pí. Dvojná vazba je kratší než vazba jednoduchá a všechny čtyři atomy vázané na dvojnou vazbu leží v jedné rovině. Fyzikální vlastnosti
Alkeny Dvojná vazba je tvořena jednou vazbou sigma a jednou vazbou pí. Dvojná vazba je kratší než vazba jednoduchá a všechny čtyři atomy vázané na dvojnou vazbu leží v jedné rovině. Fyzikální vlastnosti
Plasty A syntetická vlákna
 Plasty A syntetická vlákna Plasty Nesprávně umělé hmoty Makromolekulární látky Makromolekuly vzniknou spojením velkého množství atomů (miliony) Syntetické či přírodní Známé od druhé pol. 19 století Počátky
Plasty A syntetická vlákna Plasty Nesprávně umělé hmoty Makromolekulární látky Makromolekuly vzniknou spojením velkého množství atomů (miliony) Syntetické či přírodní Známé od druhé pol. 19 století Počátky
VII.6.4 Polykondenzace Lineární polymery. H. Schejbalová & I. Stibor, str I. Prokopová, str D. Lukáš 2013
 VII.6.4 Polykondenzace Lineární polymery H. Schejbalová & I. Stibor, str. 172. I. Prokopová, str. 157. D. Lukáš 2013 1 Vzdělávací záměr 1. Polykondenzace uvést obecný průběh stupňovité reakce 2. Příklady
VII.6.4 Polykondenzace Lineární polymery H. Schejbalová & I. Stibor, str. 172. I. Prokopová, str. 157. D. Lukáš 2013 1 Vzdělávací záměr 1. Polykondenzace uvést obecný průběh stupňovité reakce 2. Příklady
CHEMICKÉ TECHNOLOGIE PRO PROCESNÍ INŽENÝRSTVÍ N VÝROBA MTBE
 CHEMICKÉ TECHNOLOGIE PRO PROCESNÍ INŽENÝRSTVÍ N409059 VÝROBA MTBE Fyzikální a chemické vlastnosti Suroviny Reakce Technologie Dvoustupňová výroba Jednostupňová výroba Charakteristiky technologií Zdroje
CHEMICKÉ TECHNOLOGIE PRO PROCESNÍ INŽENÝRSTVÍ N409059 VÝROBA MTBE Fyzikální a chemické vlastnosti Suroviny Reakce Technologie Dvoustupňová výroba Jednostupňová výroba Charakteristiky technologií Zdroje
VIII. 6.5 Polyadice. H. Schejbalová & I. Stibor, str. 179. I. Prokopová, str. 181. D. Lukáš 2013
 VIII. 6.5 Polyadice H. Schejbalová & I. Stibor, str. 179. I. Prokopová, str. 181. D. Lukáš 2013 1 Vzdělávací záměr 1. Polyadice obecný průběh polyadice, odlišnosti od polykondenzace. 2. Syntéza polyuretanů
VIII. 6.5 Polyadice H. Schejbalová & I. Stibor, str. 179. I. Prokopová, str. 181. D. Lukáš 2013 1 Vzdělávací záměr 1. Polyadice obecný průběh polyadice, odlišnosti od polykondenzace. 2. Syntéza polyuretanů
Netkané textilie. Materiály 2
 Materiály 2 1 Pojiva pro výrobu netkaných textilií Pojivo je jednou ze dvou základních složek pojených textilií. Forma pojiva a jeho vlastnosti předurčují technologii a podmínky procesu pojení způsob rozmístění
Materiály 2 1 Pojiva pro výrobu netkaných textilií Pojivo je jednou ze dvou základních složek pojených textilií. Forma pojiva a jeho vlastnosti předurčují technologii a podmínky procesu pojení způsob rozmístění
Ing. Hana Zmrhalová. Název školy: Autor: Název: VY_32_INOVACE_20_CH 9. Číslo projektu: Téma: Anotace: Datum: Základní škola Městec Králové
 Název školy: Autor: Základní škola Městec Králové Ing. Hana Zmrhalová Název: VY_32_INOVACE_20_CH 9 Číslo projektu: Téma: Anotace: CZ.1.07/1.4.00/21.2313 ORGANICKÁ CHEMIE PLASTY A SYNTETICKÁ VLÁKNA Prezentace,
Název školy: Autor: Základní škola Městec Králové Ing. Hana Zmrhalová Název: VY_32_INOVACE_20_CH 9 Číslo projektu: Téma: Anotace: CZ.1.07/1.4.00/21.2313 ORGANICKÁ CHEMIE PLASTY A SYNTETICKÁ VLÁKNA Prezentace,
Životní prostředí. Plasty v životním prostředí
 Životní prostředí Plasty v životním prostředí 1868 John Wesley Hyatt inzerát 1856 Alexander Parkes nitrát celulosy 1870 John Wesley Hyatt celuloid 1872 The Celluloid Manufacturing Co. & J. W. Hyatt
Životní prostředí Plasty v životním prostředí 1868 John Wesley Hyatt inzerát 1856 Alexander Parkes nitrát celulosy 1870 John Wesley Hyatt celuloid 1872 The Celluloid Manufacturing Co. & J. W. Hyatt
CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT. Základy chemie makromolekulárních látek VY_32_INOVACE_18_11
 Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
Průvodka Číslo projektu Název projektu Číslo a název šablony klíčové aktivity CZ.1.07/1.5.00/34.0802 Zkvalitnění výuky prostřednictvím ICT III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Příjemce
UHLOVODÍKY ALKANY (...)
 UHLOVODÍKY ALKANY (...) alifatické nasycené uhlovodíky nerozvětvené i rozvětvené mezi atomy uhlíku pouze jednoduché vazby (σ vazby), mezi nimi úhel 109 28 název: kmen + an obecný vzorec C n H 2n + 2 tvoří
UHLOVODÍKY ALKANY (...) alifatické nasycené uhlovodíky nerozvětvené i rozvětvené mezi atomy uhlíku pouze jednoduché vazby (σ vazby), mezi nimi úhel 109 28 název: kmen + an obecný vzorec C n H 2n + 2 tvoří
Polymery a plasty v praxi POLYSTYREN & KOPOLYMERY STYRÉMU
 Polymery a plasty v praxi POLYSTYREN & KOPOLYMERY STYRÉMU RNDr. Ladislav Pospíšil, CSc. pospisil@gascontrolplast.cz 29716@mail.muni.cz 16. 3.2015 POLYMERY A PLASTY V PRAXI 1 POLYSTYREN & KOPOLYMERY STYRÉNU
Polymery a plasty v praxi POLYSTYREN & KOPOLYMERY STYRÉMU RNDr. Ladislav Pospíšil, CSc. pospisil@gascontrolplast.cz 29716@mail.muni.cz 16. 3.2015 POLYMERY A PLASTY V PRAXI 1 POLYSTYREN & KOPOLYMERY STYRÉNU
Bezpečnostní inženýrství - Chemické procesy -
 Bezpečnostní inženýrství - Chemické procesy - M. Jahoda Nebezpečí a prevence chemických procesů 2 Chemické reakce Tepelné efekty exotermní procesy (teplo se uvolňuje => nutnost chlazení) endotermní procesy
Bezpečnostní inženýrství - Chemické procesy - M. Jahoda Nebezpečí a prevence chemických procesů 2 Chemické reakce Tepelné efekty exotermní procesy (teplo se uvolňuje => nutnost chlazení) endotermní procesy
Autor: Tomáš Galbička Téma: Alkany a cykloalkany Ročník: 2.
 Alkany uhlovodíky s otevřeným řetězcem a pouze jednoduchými vazbami vazby sigma, největší výskyt elektronů na spojnici jader v názvu mají koncovku an Cykloalkany uhlovodíky s uzavřeným řetězcem a pouze
Alkany uhlovodíky s otevřeným řetězcem a pouze jednoduchými vazbami vazby sigma, největší výskyt elektronů na spojnici jader v názvu mají koncovku an Cykloalkany uhlovodíky s uzavřeným řetězcem a pouze
Základní požadavky: mechanické a fyzikální vlastnosti materiálu
 Materiály Základní požadavky: mechanické a fyzikální vlastnosti materiálu nesmí se měnit při provozních podmínkách mechanické vlastnosti jsou funkcí teploty vliv zpracování u kovových materiálů (např.
Materiály Základní požadavky: mechanické a fyzikální vlastnosti materiálu nesmí se měnit při provozních podmínkách mechanické vlastnosti jsou funkcí teploty vliv zpracování u kovových materiálů (např.
MATERIÁLY A TECHNOLOGIE 1 PAVEL ČERNÝ
 MATERIÁLY A TECHNOLOGIE 1 PAVEL ČERNÝ Co vás napadne, když se řekne plast? Proč právě plasty? skupina syntetických materiálů slovo plast ze slova plastický, tvárný, formovatelný název plyne z chemické
MATERIÁLY A TECHNOLOGIE 1 PAVEL ČERNÝ Co vás napadne, když se řekne plast? Proč právě plasty? skupina syntetických materiálů slovo plast ze slova plastický, tvárný, formovatelný název plyne z chemické
VLASTNOSTI VLÁKEN. 3. Tepelné vlastnosti vláken
 VLASNOSI VLÁKEN 3. epelné vlastnosti vláken 3.. Úvod epelné vlastnosti vláken jsou velice důležité, neboť jsou rozhodující pro volbu vhodných parametrů zpracování i použití vláken. Závisí na chemickém
VLASNOSI VLÁKEN 3. epelné vlastnosti vláken 3.. Úvod epelné vlastnosti vláken jsou velice důležité, neboť jsou rozhodující pro volbu vhodných parametrů zpracování i použití vláken. Závisí na chemickém
COBRAPEX TRUBKA S KYSLÍKOVOU BARIÉROU
 COBRAPEX TRUBKA S KYSLÍKOVOU BARIÉROU COBRAPEX TRUBKA S KYSLÍK. BARIÉROU 2.1. COBRATEX TRUBKA COBRAPEX trubka s EVOH (ethylen vinyl alkohol) kyslíkovou bariérou z vysokohustotního polyethylenu síťovaného
COBRAPEX TRUBKA S KYSLÍKOVOU BARIÉROU COBRAPEX TRUBKA S KYSLÍK. BARIÉROU 2.1. COBRATEX TRUBKA COBRAPEX trubka s EVOH (ethylen vinyl alkohol) kyslíkovou bariérou z vysokohustotního polyethylenu síťovaného
Polymerizace. Polytransformace
 vznik makromolekuly Polymerizace Polytransformace Podmínky vzniku makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce
vznik makromolekuly Polymerizace Polytransformace Podmínky vzniku makromolekuly Podmínky vzniku makromolekuly 1) chemická podmínka Výchozí nízkomolekulární látka(y) musí být z pohledu polymerní reakce
MATERIÁLOVÁ PROBLEMATIKA PŘI SEPARACI PLYNŮ A PAR
 MATERIÁLOVÁ PROBLEMATIKA PŘI SEPARACI PLYNŮ A PAR Ing. Miroslav Bleha, CSc. Ústav makromolekulární chemie AV ČR, v.v.i. bleha@imc.cas.cz Membrány - separační medium i chemický reaktor Membránové materiály
MATERIÁLOVÁ PROBLEMATIKA PŘI SEPARACI PLYNŮ A PAR Ing. Miroslav Bleha, CSc. Ústav makromolekulární chemie AV ČR, v.v.i. bleha@imc.cas.cz Membrány - separační medium i chemický reaktor Membránové materiály
KAPITOLA 12: PLASTICKÉ HMOTY Vysoká škola technická a ekonomická v Českých Budějovicích. Institute of Technology And Business In České Budějovice
 KAPITOLA 12: PLASTICKÉ HMOTY Vysoká škola technická a ekonomická v Českých Budějovicích Institute of Technology And Business In České Budějovice Tento učební materiál vznikl v rámci projektu "Integrace
KAPITOLA 12: PLASTICKÉ HMOTY Vysoká škola technická a ekonomická v Českých Budějovicích Institute of Technology And Business In České Budějovice Tento učební materiál vznikl v rámci projektu "Integrace
Nauka o materiálu. Přednáška č.14 Kompozity
 Nauka o materiálu Úvod Technické materiály, které jsou určeny k dalšímu technologickému zpracování zahrnují širokou škálu možného chemického složení, různou vnitřní stavbu a různé vlastnosti. Je nutno
Nauka o materiálu Úvod Technické materiály, které jsou určeny k dalšímu technologickému zpracování zahrnují širokou škálu možného chemického složení, různou vnitřní stavbu a různé vlastnosti. Je nutno
- Kromě pneumatik se syntetické kaučuky využívají i při výrobě obuvi, hraček, lékařských pomůcek, lepidel či nátěrových hmot.
 Příklady látek vzniklých polyinsercí - Syntetické kaučuky - zvýšení odolnosti - proces zvaný vulkanizace -> provázání polymerních řetězců, čímž vzrůstá pružnost, na druhou stranu již není možné hmotu tvarovat
Příklady látek vzniklých polyinsercí - Syntetické kaučuky - zvýšení odolnosti - proces zvaný vulkanizace -> provázání polymerních řetězců, čímž vzrůstá pružnost, na druhou stranu již není možné hmotu tvarovat
ETHYLEN - PRŮMYSLOVÉ ZPRACOVÁNÍ
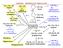 H ethanol CH= acetaldehyd CH octová kys. C CH= vinylacetát ETHYLE - PRŮMYSLVÉ ZPRACVÁÍ oxiran (ethylenoxid) ~ 10 % + 2 ~ 20 % -H 2 + KYS. KATAL. ETHE CH= styren (-CH- -) n Ph polystyren PS a jeho kopolymery
H ethanol CH= acetaldehyd CH octová kys. C CH= vinylacetát ETHYLE - PRŮMYSLVÉ ZPRACVÁÍ oxiran (ethylenoxid) ~ 10 % + 2 ~ 20 % -H 2 + KYS. KATAL. ETHE CH= styren (-CH- -) n Ph polystyren PS a jeho kopolymery
Ţijeme v době plastové
 České vysoké učení technické v Praze Fakulta strojní Ústav materiálového inţenýrství Karlovo nám. 13 121 35 Praha 2 Ţijeme v době plastové Zdeňka Jeníková ISTORIE 12. století Anglie, cech zpracovatelů
České vysoké učení technické v Praze Fakulta strojní Ústav materiálového inţenýrství Karlovo nám. 13 121 35 Praha 2 Ţijeme v době plastové Zdeňka Jeníková ISTORIE 12. století Anglie, cech zpracovatelů
Polymery: minimum, které bychom si měli pamatovat. Lukáš Horný
 Polymery: minimum, které bychom si měli pamatovat ČVUT v Praze, fakulta strojní, ústav mechaniky, biomechaniky a mechatroniky Obor: Biomechanika a lékařské přístroje Lukáš Horný Lukas.horny@fs.cvut.cz
Polymery: minimum, které bychom si měli pamatovat ČVUT v Praze, fakulta strojní, ústav mechaniky, biomechaniky a mechatroniky Obor: Biomechanika a lékařské přístroje Lukáš Horný Lukas.horny@fs.cvut.cz
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Animovaná chemie Top-Hit Analytická chemie Analýza anorganických látek Důkaz aniontů Důkaz kationtů Důkaz kyslíku Důkaz vody Gravimetrická analýza Hmotnostní spektroskopie Chemická analýza Nukleární magnetická
Zplyňování biomasy. Sesuvný generátor. Autotermní zplyňování Autotermní a alotermní zplyňování
 Zplyňování = termochemická přeměna uhlíkatého materiálu v pevném či kapalném skupenství na výhřevný energetický plyn pomocí zplyňovacích médií a tepla. Produktem je plyn obsahující výhřevné složky (H 2,
Zplyňování = termochemická přeměna uhlíkatého materiálu v pevném či kapalném skupenství na výhřevný energetický plyn pomocí zplyňovacích médií a tepla. Produktem je plyn obsahující výhřevné složky (H 2,
ANORGANICKÁ ORGANICKÁ
 EMIE ANORGANIKÁ ORGANIKÁ 1 EMIE ANORGANIKÁ Anorganické látky Oxidy: O, O 2.. V neživé přírodě.. alogenidy: Nal.. ydroxidy: NaO Uhličitany: ao 3... Kyseliny: l. ydrogenuhličitany: NaO 3. 2 EMIE ORGANIKÁ
EMIE ANORGANIKÁ ORGANIKÁ 1 EMIE ANORGANIKÁ Anorganické látky Oxidy: O, O 2.. V neživé přírodě.. alogenidy: Nal.. ydroxidy: NaO Uhličitany: ao 3... Kyseliny: l. ydrogenuhličitany: NaO 3. 2 EMIE ORGANIKÁ
VY_32_INOVACE_CHK4_5460 ŠAL
 VY_32_INOVACE_CHK4_5460 ŠAL Výukový materiál v rámci projektu OPVK 1.5 Peníze středním školám Číslo projektu: CZ.1.07/1.5.00/34.0883 Název projektu: Rozvoj vzdělanosti Číslo šablony: III/2 Datum vytvoření:
VY_32_INOVACE_CHK4_5460 ŠAL Výukový materiál v rámci projektu OPVK 1.5 Peníze středním školám Číslo projektu: CZ.1.07/1.5.00/34.0883 Název projektu: Rozvoj vzdělanosti Číslo šablony: III/2 Datum vytvoření:
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: Číslo DUMu: VY_32_INOVACE_10_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné
 Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 12.02.2013 Číslo DUMu: VY_32_INOVACE_10_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Jméno autora: Mgr. Ladislav Kažimír Datum vytvoření: 12.02.2013 Číslo DUMu: VY_32_INOVACE_10_Ch_OB Ročník: I. Vzdělávací oblast: Přírodovědné vzdělávání Vzdělávací obor: Chemie Tematický okruh: Obecná
Zpracování ropy doc. Ing. Josef Blažek, CSc. 5. přednáška
 ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 5. přednáška Reformování a izomerace benzinů, výroba benzinových složek
ODBORNÉ VZDĚLÁVÁNÍ ÚŘEDNÍKŮ PRO VÝKON STÁTNÍ SPRÁVY OCHRANY OVZDUŠÍ V ČESKÉ REPUBLICE Zpracování ropy doc. Ing. Josef Blažek, CSc. 5. přednáška Reformování a izomerace benzinů, výroba benzinových složek
PROPEN - PŘEHLED VYUŽITÍ
 PRPEN - PŘEHLED VYUŽITÍ polymery propandioly propylenkarbonát isopropanolaminy C 4 aldehydy alkoholy kyseliny jejich estery CH methyloxiran (propylenoxid) hydroformylace hydrokarbonylace + 2 isopropylbenzen
PRPEN - PŘEHLED VYUŽITÍ polymery propandioly propylenkarbonát isopropanolaminy C 4 aldehydy alkoholy kyseliny jejich estery CH methyloxiran (propylenoxid) hydroformylace hydrokarbonylace + 2 isopropylbenzen
EU peníze středním školám digitální učební materiál
 EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
EU peníze středním školám digitální učební materiál Číslo projektu: Číslo a název šablony klíčové aktivity: Tematická oblast, název DUMu: Autor: CZ.1.07/1.5.00/34.0515 III/2 Inovace a zkvalitnění výuky
Úvod technologie hot melt
 Technologie hotmelt Úvod technologie hot melt Průmyslové technologie hot melt jsou v současné době velice dobře konkurenceschopné klasických postupům tepelného pojení. Důvodem jejich použití je zejména
Technologie hotmelt Úvod technologie hot melt Průmyslové technologie hot melt jsou v současné době velice dobře konkurenceschopné klasických postupům tepelného pojení. Důvodem jejich použití je zejména
Kolik energie by se uvolnilo, kdyby spalování ethanolu probíhalo při teplotě o 20 vyšší? Je tato energie menší nebo větší než při teplotě 37 C?
 TERMOCHEMIE Reakční entalpie při izotermním průběhu reakce, rozsah reakce 1 Kolik tepla se uvolní (nebo spotřebuje) při výrobě 2,2 kg acetaldehydu C 2 H 5 OH(g) = CH 3 CHO(g) + H 2 (g) (a) při teplotě
TERMOCHEMIE Reakční entalpie při izotermním průběhu reakce, rozsah reakce 1 Kolik tepla se uvolní (nebo spotřebuje) při výrobě 2,2 kg acetaldehydu C 2 H 5 OH(g) = CH 3 CHO(g) + H 2 (g) (a) při teplotě
6. Plasty a pryže. surovina. Vztahy mezi petrochemií a výrobou polymerů. Výroba polymerů. Petrochemická surovina. cyklohexan 100 etylenoxid 50 60
 6. Plasty a pryže Vztahy mezi petrochemií a výrobou polymerů Petrochemická surovina Výroba polymerů uplatnění (%) Petrochemická surovina Výroba polymerů uplatnění (%) etylen 80 k. octová 70 propylen 50
6. Plasty a pryže Vztahy mezi petrochemií a výrobou polymerů Petrochemická surovina Výroba polymerů uplatnění (%) Petrochemická surovina Výroba polymerů uplatnění (%) etylen 80 k. octová 70 propylen 50
16.IZOMERIE a UHLOVODÍKY 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem liší?
 16.IZOMERIE a UHLOVODÍKY 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem liší? 4) Urči typy konstituční izomerie. 5) Co je tautomerie
16.IZOMERIE a UHLOVODÍKY 1) Co je to izomerie a jak se dělí? 2) Co je konstituce, konfigurace a konformace? 3) V čem se izomery shodují a v čem liší? 4) Urči typy konstituční izomerie. 5) Co je tautomerie
VLASTNOSTI ALKANŮ 2. RADIKÁLOVÁ SUBSTITUCE 3. ELIMINAČNÍ REAKCE VÝZNAMNÉ ALKANY. Substituční reakce. Sulfochlorace alkanů. Termolýza.
 Kromě CO 2 vznikají i saze roste svítivost Substituční reakce vazby: C C C H jsou nepolární => jsou radikálové S R...radikálová substituce 3 fáze... VLASTNOSTI ALKANŮ tady něco chybí... 2. RADIKÁLOVÁ SUBSTITUCE
Kromě CO 2 vznikají i saze roste svítivost Substituční reakce vazby: C C C H jsou nepolární => jsou radikálové S R...radikálová substituce 3 fáze... VLASTNOSTI ALKANŮ tady něco chybí... 2. RADIKÁLOVÁ SUBSTITUCE
ÚPRAVA VODY V ENERGETICE. Ing. Jiří Tomčala
 ÚPRAVA VODY V ENERGETICE Ing. Jiří Tomčala Úvod Voda je v elektrárnách po palivu nejdůležitější surovinou Její množství v provozních systémech elektráren je mnohonásobně větší než množství spotřebovaného
ÚPRAVA VODY V ENERGETICE Ing. Jiří Tomčala Úvod Voda je v elektrárnách po palivu nejdůležitější surovinou Její množství v provozních systémech elektráren je mnohonásobně větší než množství spotřebovaného
Alkyny. C n H 2n-2 (obsahuje jednu trojnou vazbu) uhlíky v sp hybridizaci
 Alkyny C n H 2n-2 (obsahuje jednu trojnou vazbu) uhlíky v sp hybridizaci 1 Klasifikace 2 Alkyny - dvě π vazby; lineární uspořádání Pozor! 3 Vlastnosti -π elektrony jsou méně mobilní než u alkenů H CH 3
Alkyny C n H 2n-2 (obsahuje jednu trojnou vazbu) uhlíky v sp hybridizaci 1 Klasifikace 2 Alkyny - dvě π vazby; lineární uspořádání Pozor! 3 Vlastnosti -π elektrony jsou méně mobilní než u alkenů H CH 3
Názvosloví Konformace Isomerie. Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o )
 ALKANY 1 Názvosloví Konformace Isomerie Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o ) 2 Alkany (resp. cykloalkany) jsou nejzákladnější organické sloučeniny složené pouze z
ALKANY 1 Názvosloví Konformace Isomerie Uhlíky: primární (1 o ) sekundární (2 o ) terciární (3 o ) kvartérní (4 o ) 2 Alkany (resp. cykloalkany) jsou nejzákladnější organické sloučeniny složené pouze z
LEPIDLA POUŽÍVANÁ V MUZEJNÍ PRAXI A PRO KONZERVOVÁNÍ A RESTAUROVÁNÍ
 LEPIDLA POUŽÍVANÁ V MUZEJNÍ PRAXI A PRO KONZERVOVÁNÍ A RESTAUROVÁNÍ Lepení se jako účinná technika spojování materiálů, pouţívá jiţ více neţ 6000 let. Zpočátku se pouţívaly pouze přírodní látky, zejména
LEPIDLA POUŽÍVANÁ V MUZEJNÍ PRAXI A PRO KONZERVOVÁNÍ A RESTAUROVÁNÍ Lepení se jako účinná technika spojování materiálů, pouţívá jiţ více neţ 6000 let. Zpočátku se pouţívaly pouze přírodní látky, zejména
ZÁKLADNÍ BILANCE A ZPŮSOB NAKLÁDÁNÍ S ODPADNÍMI PLASTY Z KOMUNÁLNÍHO SBĚRU
 RECYKLACE PLASTŮ ZÁKLADNÍ BILANCE A ZPŮSOB NAKLÁDÁNÍ S ODPADNÍMI PLASTY Z KOMUNÁLNÍHO SBĚRU 14,3 % 5,9 % Zdroj: ČSÚ, březen 2009 Komunální odpad v ČR - cca 3 mil. tun / rok (cca 300 kg /obyv.) Vzrůstající
RECYKLACE PLASTŮ ZÁKLADNÍ BILANCE A ZPŮSOB NAKLÁDÁNÍ S ODPADNÍMI PLASTY Z KOMUNÁLNÍHO SBĚRU 14,3 % 5,9 % Zdroj: ČSÚ, březen 2009 Komunální odpad v ČR - cca 3 mil. tun / rok (cca 300 kg /obyv.) Vzrůstající
Herní otázky a jejich řešení:
 Herní otázky a jejich řešení: 1) Kde v přírodě můžeme najít methan? Methan je plyn, který je hlavní součástí zemního plynu, tvoří se také při přeměnách uhlí a dále vzniká mikrobiálním rozkladem celulosy
Herní otázky a jejich řešení: 1) Kde v přírodě můžeme najít methan? Methan je plyn, který je hlavní součástí zemního plynu, tvoří se také při přeměnách uhlí a dále vzniká mikrobiálním rozkladem celulosy
Základní škola a mateřská škola Hutisko Solanec. žák uvede základní druhy uhlovodíků, jejich použití a zdroje. Chemie - 9. ročník
 Základní škola a mateřská škola Hutisko Solanec Digitální učební materiál Anotace: Autor: Jazyk: Očekávaný výstup: Speciální vzdělávací potřeby: Klíčová slova: Druh učebního materiálu: Druh interaktivity:
Základní škola a mateřská škola Hutisko Solanec Digitální učební materiál Anotace: Autor: Jazyk: Očekávaný výstup: Speciální vzdělávací potřeby: Klíčová slova: Druh učebního materiálu: Druh interaktivity:
2. KINETICKÁ ANALÝZA HOMOGENNÍCH REAKCÍ
 2. KINETICKÁ ANALÝZA HOMOGENNÍCH REAKCÍ Úloha 2-1 Řád reakce a rychlostní konstanta integrální metodou stupeň přeměny... 2 Úloha 2-2 Řád reakce a rychlostní konstanta integrální metodou... 2 Úloha 2-3
2. KINETICKÁ ANALÝZA HOMOGENNÍCH REAKCÍ Úloha 2-1 Řád reakce a rychlostní konstanta integrální metodou stupeň přeměny... 2 Úloha 2-2 Řád reakce a rychlostní konstanta integrální metodou... 2 Úloha 2-3
Paliva. nejběžnějším zdrojem tepla musí splňovat tyto podmínky: co nejmenší náklady na těžbu a výrobu snadno uskutečnitelné spalování
 Paliva Paliva nejběžnějším zdrojem tepla musí splňovat tyto podmínky: co nejmenší náklady na těžbu a výrobu snadno uskutečnitelné spalování Dělení paliv podle skupenství pevná uhlí, dřevo kapalná benzín,
Paliva Paliva nejběžnějším zdrojem tepla musí splňovat tyto podmínky: co nejmenší náklady na těžbu a výrobu snadno uskutečnitelné spalování Dělení paliv podle skupenství pevná uhlí, dřevo kapalná benzín,
Reakce alkanů 75. mechanismem), iniciované světlem nebo radikálovými iniciátory: Oxidace kyslíkem, hoření, tvorba hydroperoxidů.
 eakce alkanů 75 5. eakce alkanů Alkany poskytují především radikálové reakce (často probíhající řetězovým mechanismem), iniciované světlem nebo radikálovými iniciátory: alogenace pomocí X 2 ; bromaci lze
eakce alkanů 75 5. eakce alkanů Alkany poskytují především radikálové reakce (často probíhající řetězovým mechanismem), iniciované světlem nebo radikálovými iniciátory: alogenace pomocí X 2 ; bromaci lze
Plasty v automobilovém průmyslu
 Plasty v automobilovém průmyslu Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je Ing. Iveta Konvičná Dostupné z Metodického portálu www.rvp.cz; ISSN 1802-4785, financovaného z ESF a státního
Plasty v automobilovém průmyslu Autorem materiálu a všech jeho částí, není-li uvedeno jinak, je Ing. Iveta Konvičná Dostupné z Metodického portálu www.rvp.cz; ISSN 1802-4785, financovaného z ESF a státního
1)uhlovodík musí být cyklický, všechny atomy musí být v jedné rovině
 Otázka: Areny Předmět: Chemie Přidal(a): I. Prokopová 3 podmínky: 1)uhlovodík musí být cyklický, všechny atomy musí být v jedné rovině 2) musí existovat minimálně dvě možnosti uspořádání π elektronů 3)
Otázka: Areny Předmět: Chemie Přidal(a): I. Prokopová 3 podmínky: 1)uhlovodík musí být cyklický, všechny atomy musí být v jedné rovině 2) musí existovat minimálně dvě možnosti uspořádání π elektronů 3)
HYDROXYDERIVÁTY. Alkoholy Fenoly Bc. Miroslava Wilczková
 HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
HYDROXYDERIVÁTY Alkoholy Fenoly Bc. Miroslava Wilczková HYDROXYDERIVÁTY Alkoholy -OH skupina vázána na uhlíkový atom alifatického řetězce Fenoly -OH skupina vázána na uhlíku, který je součástí aromatického
Alkany a cykloalkany
 Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Září 2010 Mgr. Alena Jirčáková Charakteristika alkanů: Malá reaktivita, odolné chemickým činidlům Nasycené
Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje Září 2010 Mgr. Alena Jirčáková Charakteristika alkanů: Malá reaktivita, odolné chemickým činidlům Nasycené
2 VLIV STRUKTURY NA VLASTNOSTI A ZPRACOVATELNOST PLASTŮ
 2 VLIV STRUKTURY NA VLASTNOSTI A ZPRACOVATELNOST PLASTŮ 2.1 Řetězová stavba makromolekul organických polymerů Tvar makromolekul je jedním z hlavních činitelů ovlivňujících chování a vlastnosti plastů.
2 VLIV STRUKTURY NA VLASTNOSTI A ZPRACOVATELNOST PLASTŮ 2.1 Řetězová stavba makromolekul organických polymerů Tvar makromolekul je jedním z hlavních činitelů ovlivňujících chování a vlastnosti plastů.
I N V E S T I C E D O R O Z V O J E V Z D Ě L Á V Á N Í
 Historie: 1. Materiály vyrobené chemickou úpravou přírodních polymerů: EBONIT (Ch. Goodyear, 1851) = tvrdá pryž vyrobena... (působením síry) přírodního kaučuku, původně elektrický izolant Dnešní použití:
Historie: 1. Materiály vyrobené chemickou úpravou přírodních polymerů: EBONIT (Ch. Goodyear, 1851) = tvrdá pryž vyrobena... (působením síry) přírodního kaučuku, původně elektrický izolant Dnešní použití:
Organická chemie pro biochemiky II část 14 14-1
 rganická chemie pro biochemiky II část 14 14-1 oxidace a redukce mají v organické chemii trochu jiný charakter než v chemii anorganické obvykle u jde o adici na systém s dvojnou vazbou či štěpení vazby
rganická chemie pro biochemiky II část 14 14-1 oxidace a redukce mají v organické chemii trochu jiný charakter než v chemii anorganické obvykle u jde o adici na systém s dvojnou vazbou či štěpení vazby
Plastové obaly v potravinářství
 Středoškolská technika 2014 Setkání a prezentace prací středoškolských studentů na ČVUT Plastové obaly v potravinářství Diana Koytyuk SOŠ Stříbro Benešova 508, e-mail: skola@sosstribro.cz SOŠ Stříbro Předmět:
Středoškolská technika 2014 Setkání a prezentace prací středoškolských studentů na ČVUT Plastové obaly v potravinářství Diana Koytyuk SOŠ Stříbro Benešova 508, e-mail: skola@sosstribro.cz SOŠ Stříbro Předmět:
Karbonylové sloučeniny
 Karbonylové sloučeniny více než 120 o 120 o C O C C d + d - C O C sp 2 C sp 2 R C O H R 1 C O R 2 1.aldehydy, ketony Nu E R C O R C O 2. karboxylové kyseliny a funkční deriváty O H 3. deriváty kys. uhličité
Karbonylové sloučeniny více než 120 o 120 o C O C C d + d - C O C sp 2 C sp 2 R C O H R 1 C O R 2 1.aldehydy, ketony Nu E R C O R C O 2. karboxylové kyseliny a funkční deriváty O H 3. deriváty kys. uhličité
Nerozvětvené (atomy C jsou spojeny maximálně s dvěma dalšími C) Rozvětvené (atomy C jsou spojeny s více než dvěma dalšími C)
 Otázka: Uhlovodíky Předmět: Chemie Přidal(a): Majdush Obsahují ve svých molekulách pouze atomy uhlíku a vodíku Nejjednodušší org. sloučeniny Uhlík je schopný řetězit se a vytvářet tak nejrůznější řetězce,
Otázka: Uhlovodíky Předmět: Chemie Přidal(a): Majdush Obsahují ve svých molekulách pouze atomy uhlíku a vodíku Nejjednodušší org. sloučeniny Uhlík je schopný řetězit se a vytvářet tak nejrůznější řetězce,
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace
 Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
Sada 7 Název souboru Ročník Předmět Formát Název výukového materiálu Anotace VY_52_INOVACE_737 8. Chemie notebook Směsi Materiál slouží k vyvození a objasnění pojmů (klíčová slova - chemická látka, směs,
