Příloha pro metrologii teploty
|
|
|
- Jiřina Blažková
- před 9 lety
- Počet zobrazení:
Transkript
1 Příloha pro metrologii teploty Historie měření teploty a teplotních stupnic První teploměr sestrojil Galileo Galilei r. 1603, byl to vzduchový teploměr, který ukazoval změnu teploty nasáváním barevné kapaliny, avšak číselně ji nekvantifikoval. Dnes bychom toto zařízení nazvali detektor teploty. První lihový teploměr sestrojil r velkovévoda toskánský Ferdinand II. Teploměry založené na roztažnosti kapalin mezi dvěma pevnými kalibračními body vytvořili Fahrenheit, Réaumur a Celsius. Huygens navrhl pevné teplotní body bod tání ledu a bod varu vody. Návrh na rozdělení Celsiovy stupnice na sto stupňů podal Christin. Roku 1848 navrhl Kelvin termodynamickou stupnici teploty, založenou na Carnotově cyklu. Dodnes se používají teplotní stupnice tehdy navržené. Snahy sjednotit měření teploty v širším rozsahu se datují od konce 19. století. Rozsáhlá mezinárodní spolupráce předních metrologických laboratoří přispěla k vypracování podrobných pokynů, jak měřit teplotu v širokém rozsahu. V roce 1887 vydal CIPM první dohodu o způsobu měření teplot. Vyšel ze stodílkového vodíkového teploměru se dvěma pevnými teplotami. Byla to teplota tání ledu (0 C a teplota varu destilované vody (100 C při normálním atmosférickém tlaku (760 Torr. Počáteční tlak vodíku v plynovém teploměru byl torrů. Mezinárodní teplotní stupnice 197 (ITS-7: Byla přijata jako náhrada vzhledem k přímé realizaci měření termodynamické teploty plynovým teploměrem. Mezi bodem varu kyslíku a bodem tuhnutí zlata bylo realizováno množství reprodukovatelných teplot nebo pevných bodů, jejichž číselné hodnoty byly určené plynovým teploměrem. Byly realizovány dva interpolační přístroje, každý z nich byl kalibrovaný v několika pevných bodech pro určení konstant v interpolačním vztahu. Pro nižší teploty byl použitý platinový odporový teploměr a pro teploty nad 660 C termoelektrický článek PtRh-Pt. Pro oblast nad bod tuhnutí zlata byla teplota definována Wienovým vyzařovacím zákonem s použitím optického pyrometru. Mezinárodní teplotní stupnice 1948 (ITS-48: Spodní hranice rozsahu platinového odporového teploměru byla změněna z -190 C na definiční bod varu kyslíku -18,97 C a bodem spojení rozsahu platinového odporového teploměru a termoelektrického článku s stal bod tuhnutí antimonu 630 C místo původního 660 C. Bod tuhnutí stříbra byl definovaný jako 960,8 C místo 960,5 C. Bod tuhnutí zlata nahradil bod tání zlata 1063 C. Wienův vyzařovací zákon byl nahrazen Planckovým vyzařovacím zákonem. Mezinárodní praktická teplotní stupnice 1948, doplněné vydání 1960 (IPTS-48: Trojný bod vody byl přijat jako jediný bod definující kelvin (K, jako jednotka termodynamické teploty. Trojný bod vody 0,01 C nahradil bod tání ledu jako kalibrační bod v této oblasti. Bod tuhnutí zinku byl definovaný jako 419,505 C a upřednostňoval se před bodem varu síry. Dovolené rozsahy pro konstanty interpolačních vzorců pro etalonový odporový teploměr a termoelektrický článek byly upravené, odstranilo se omezení optického pyrometru pro viditelné záření. Číselné hodnoty IPTS-48 a ITS-48 byly stejné, stupnice nebyla revidovaná, pouze doplněná. 1
2 Mezinárodní praktická teplotní stupnice 1968 (IPTS-68: Tato stupnice přinesla rozsáhlé změny s cílem zabezpečit větší shodu s termodynamickou teplotou. Dolní hranice stupnice byla rozšířená na 13,81 K, pro nižší teploty (0,5 K až 5, K bylo doporučené používat stupnici tlaku par helia. Bylo zavedeno šest nových definičních bodů: trojný bod vodíku (13,81 K, bod varu normálního rovnovážného vodíku za určitého podtlaku (17,04 K, bod varu normálního rovnovážného vodíku (0,8 K, bod varu neonu (7,10 K, trojný bod kyslíku (54,361 K a bod tuhnutí cínu (31,9681 C, který se stal alternativním k bodu varu vody. Hodnoty pro další pevné body byly změněné: bod varu kyslíku (90,188 K, bod tuhnutí zinku (419,58 C, bod tuhnutí stříbra (961,93 C a bod tuhnutí zlata (1064,43 C. Byly změněny interpolační vzorce pro odporový teploměr a změnila se hodnota radiační konstanty pro radiační teploměr. Dovolené rozsahy konstant pro odporový teploměr a pro termoelektrický článek byly znovu upravené. Mezinárodní praktická teplotní stupnice 1968, doplněné vydání 1975 (IPTS-68(75: Největší změny byly v textu pro vyjasnění a zjednodušení použití. Bod kyslíku byl definovaný jako bod kondenzace přednostně před bodem varu. Trojný bod argonu (83,768 K byl zavedený jako dovolená alternativa k bodu kondenzace kyslíku, u neonu byly přijaty nové hodnoty přirozeného izotopového složení. Prozatímní teplotní stupnice 0,5 K až 30 K z r (EPT-76: Tato stupnice byla zavedena pro redukci chyby pod 7 K v IPTS-68 a pro přemostění mezery mezi 5, K až 13,81 K, kde dosud nebyla provizorní stupnice. Tato stupnice byla termodynamicky hladká a shodná s IPTS-68 při 7,1 K. Byla definovaná jedenácti pevnými teplotami, z nichž dolních pět je vázáno na teploty přechodu z normálního do supravodivého stavu: kadmium, zinek, hliník, indium a olovo. Soubor kovů byl konstrukčně řešen jako svazek pěti tyčinek tvořící jádro dvou souosých válcových cívek, jejichž vzájemná indukčnost závisí na magnetické susceptibilitě těchto kovů a ta opět na jejich normálním či supravodivém stavu. Takto upravený supravodivý soubor pěti standardních referenčních materiálů dodával NBS pod označením SRM-767. Současná teplotní stupnice - Mezinárodní teplotní stupnice 1990 (ITS-90: Pokroky v polovodičové a počítačové technice umožnily zvýšení přesnosti měření teploty. Zásluhou zlepšení čistících technik, metodou zonálního tavení, se zlepšila čistota látek používaných při výrobě polovodičů. Byly připraveny materiály dříve nepoužívané galium a indium v čistotách na hranicích možností. Také rtuť se dnes používá v čistotě 7,85, tedy se znečištěním 15 ppb, tj Při takových čistotách již souhlasí teploty tání s teplotami tuhnutí. Důsledkem toho je, že v posledních desetiletích vzrostla přesnost měření teploty o jeden řád. Počítačová technika umožnila aplikaci interpolačních polynomů vysokých stupňů, což bylo bez počítačů značně obtížné. Poznámka: Udávání čistoty materiálů se skládá z čísla s desetinnou čárkou. Číslo před desetinou čárkou udává počet devítek, číslo za desetinnou čárkou udává další číslice za poslední devítkou. Např. údaj čistoty 7,85 znamená 99, %Hg ve vzorku. Údaj ppb (pars per bilion - "částí na bilion" znamená ovšem jedna ku miliardě. Miliarda v evropských zvyklostech znamená 10 9, v anglosaských zemích je to bilion. U nás je bilion 10 1, což je v anglosaských zemích trilion.
3 Rozdíly mezi teplotami stupnic T 90 a T 68 jsou uvedeny v následujícím grafu. U publikovaných přesných měření teplot určitých fyzikálních vlastností je nutno tento rozdíl vzít v úvahu, viz obr.p-1. Obr. P-1: Teplotní rozdíly definicí stupnic (T 90 - T 68 v závislosti na teplotě Doplňky z fyziky a fyzikální chemie pro etalonáž a měření teploty Gibbsovo fázové pravidlo: popisuje vztah mezi složkami a fázemi. kde je: v = k f +, (P-1 v počet stupňů volnosti, k počet složek, f počet fází. Rovnice Clapeyronova: popisuje směrnici křivky v diagramu p,t při fázových přeměnách. dp dt Δ H p = T ΔV m (P- 3
4 Rovnice Clausius-Clapeyronova: popisuje závislost mezi tlakem par a teplotou při fázové přeměně z kapaliny na páru nebo naopak. kde je: d lnp Δ H výp = (P-3 dt R T p (Pa tlak, T (K termodynamická teplota, ΔH P (J/mol molární skupenské teplo fázové přeměny, ΔV m (m 3 /mol změna molárního objemu látky fázové přeměny, ΔH výp (J/mol molární výparné teplo. Wienův vyzařovací zákon: popisoval vyzařování černého tělesa, odpovídal tehdejší úrovni poznání, později byl nahrazen přesnějším Plackovým zákonem. c1 1 H = (P-4 0λ 5 λ exp( c ( λ T Planckův vyzařovací zákon: popisuje vyzařování černého tělesa pro různé vlnové délky při různých teplotách. c1 1 H = 0 5 exp( c ( T λ λ λ 1 (P-5 kde je: H 0λ (W/m -3 spektrální hustota intenzity vyzařování, λ (m vlnová délka záření, T (K termodynamická teplota, c 1 = 3, W m, c = 1, m K. Rovnovážné stavy vodíku Atom vodíku, isotop 1 H, se skládá z jednoho protonu a jednoho elektronu. Molekula vodíku 1 H má dva atomy. Obě částice, proton i elektron mají kvantovou vlastnost - spin. V molekule vodíku mohou být oba jaderné spiny (spiny protonů vzájemně stejnosměrné nebo protisměrné. V případě stejnosměrných spinů v molekule vodíku se jedná o orthovodík o-h, protisměrné spiny má pak paravodík p-h. Chemicky se chovají stejně, ale mají různé fyzikální vlastnosti. Rovnovážný vodík e-h, označovaný také jako normální vodík n-h, za obvyklých teplot se skládá ze tří dílů orthovodíku a jednoho dílu paravodíku. Za hlubokých teplot a vyšších tlaků je při rovnováze více paravodíku, avšak rovnováha nastává velmi pomalu. Chování vody při teplotách v blízkosti trojného bodu Kapalná voda tuhne na led. Led má více krystalických modifikací. Za normálního tlaku je to led I, který krystalizuje v šesterečné soustavě, základní krystalickou jednotkou je osmičlenný agregát (H O 8. Při tání ledu se uvolňují shluky molekul vody opět o složení (H O 8. Tyto 4
5 molekuly vody jsou vzájemně vázány vodíkovými můstky. Při zvyšující se teplotě se zmenšuje počet základních molekul vody v těchto agregátech a při teplotách blížících se bodu varu a v parní fázi se vyskytuje voda jen jako monomer H O. Viz obr. P-. Obr. P-: Krystalová mřížka ledu a struktura molekuly (H O 8, elementární jednotka je vytažena silněji, kuličkami jsou znázorněny jen atomy kyslíku. Chování helia za nízkých teplot Přírodní helium je složeno ze dvou izotopů 3 He a 4 He. Lehčí izotop je k izotopu těžšímu zastoupen v přírodě v poměru 1 : Oba izotopy mají význam v metrologii nízkých teplot. Helium je jediný prvek, který nelze za normálního tlaku převést na pevnou fázi, to je možné jen za vyšších tlaků. Kapalné helium se vyskytuje za normálního tlaku při teplotách 4, K. Helium vykazuje za nízkých teplot supratekutost. To je vlastnost, kdy se jeho viskozita blíží k nule. Tato změna nastává u 4 He kolem teploty, K. Tomuto bodu se říká λ bod, podle charakteristického tvaru křivky. Při vyšších teplotách se vyskytuje kapalná fáze helia označovaná jako He-I, při nižších teplotách se vyskytuje kapalná fáze označovaná jako He-II, což je směs normálního (He-I a supratekutého helia. Z tohoto důvodu interpolační přístroj založený na tlaku par 4 He vykazuje v tomto bodě diskontinuitu. Pro tuto fázovou přeměnu neplatí Gibbsův zákon fází! Tento jev se nevyskytuje u 3 He. Viz obr. P-3 a P-4. 5
6 Obr. P-3: Fázový diagram 4 He. Helium nemá trojný bod, v grafu je vidět křivka λ. Obr. P-4: Znázornění diskontinuity C V kapalného 4 He na křivce λ. 6
7 Vývoj výpočetních vztahů pro Pt odporový teploměr 1. První vztah: použitelný dosud jen v úzkém teplotním rozsahu: R = R ( 1+ α t (P-6 0. Callendarova rovnice (1886: pro teploty (0 až 600 C: odvozená z komparace odporového a plynového teploměru R R ( a t b t 0 kde je a = + 0,003 9 C-1, (P-7 b = 0, C Callendar - van Düsenova rovnice: pro teploty (-190 až 600 C: R = R ( 1+ a t + b t + c ( t 100 t (P Výpočetní vztahy podle ITS-48 platily do konce roku 1968 vztahy upravené podle předchozích rovnic (norma ČSN : pro teploty (0 až 850 C: pro Pt100, kde R 0 = 100 Ω, a R 100 /R 0 = 1,385: R t = R ( 1+ A t + B t (P kde konstanty byly: R 0 = 100 Ω, A 1 = 0, K -1, - BB1 = 0, K. pro Pt98,47, kde R 0 = 98,4655 Ω, a R 100 /R 0 = 1,391: R t = R ( 1+ A t + B t (P kde konstanty byly: R 0 = 98,4655 Ω, A 1 = 0, K -1, - BB1 = 0, K. 5. Výpočetní vztahy podle IPTS-68: pro teploty (0 až 630 C: t t t t t = t + 0, (P ,58 630,74 kde pro pomocnou hodnotu teploty t (to není derivace! platí: R t = R ( 1 + A t + B t (P kde konstanty jsou: pro Pt100: R 0 = 100 Ω, A = 0, K -1, - BB = 0, K. pro Pt98,47: R 0 = 98,4655 Ω, A = 0, K -1, - BB = 0, K. 7
8 Někdy je výhodnější počítat hodnoty R t68 měřicího odporu přímo z teplot t 68. Pak se dá použít s postačující přesností následující vztah (P-13. Opačný výpočet je pak klasické řešení nelineární rovnice R t = R ( 1+ A t + B t + C t + D t + E t (P hodnoty konstant jsou: pro Pt100: R 0 = 100 Ω, A 3 = 0, K -1, -6 - BB3 = 0, K, C 3 = 0, K -3, D = 0, K -4, E = 0, K -5. pro Pt98,47: R 0 = 98,4655 Ω, A 3 = 0, K -1, -6 - BB3 = 0, K, C 3 = 0, K -3, D = 0, K -4, E = 0, K -5. Hodnoty podle vztahů v této části (5 je možno extrapolovat až do teploty t 68 = 850 C. 6. Výpočetní vztah podle ITS-90: pro rozsah teplot (0 až 660 C: Výpočet pomocí poměru odporů naměřeného na skutečném teploměru W t90 a referenčního podle ideálního odporového teploměru W r : W W t 90 = R R, kde R je odpor naměřený při teplotě trojného bodu H t90 01 O. t90 01 r ( 1 3 W b ( W 1 c ( 1 t90 t90 t 90 = W a W (P-14 t 90 hodnoty konstant a, b a c se určí z kalibrace ve třech bodech, např. bodech tání cínu, zinku a hliníku. = D 0 + i 9 W,64 r D (P-15 i = 1 1, 64 i kde je: D 0 = 439,93 854, D 1 = 47,418 00, D = 37, , D 3 = 7,47 018, D 4 =,90 88, D 5 = 0, , D 6 = 0, , D 7 = 0,188 73, D 8 = 0,191 03, D 9 = 0,
Metrologie teploty. Mezinárodní teplotní stupnice 1990 (ITS-90)
 Metrologie teploty Již dávno si lidé všimli zvláštního stavu látek, nazývali jej podle svých pocitů studený nebo teplý. Teplota vyjadřuje stav hmoty, je to míra vnitřní energie látek. Teplota je mírou
Metrologie teploty Již dávno si lidé všimli zvláštního stavu látek, nazývali jej podle svých pocitů studený nebo teplý. Teplota vyjadřuje stav hmoty, je to míra vnitřní energie látek. Teplota je mírou
TEPLOTA (termodynamické a statistické pojetí)
 TEPLOTA (termodynamické a statistické pojetí) TEPELNÁ ROVNOVÁHA TEPLOTA, TEPLOTNÍ STUPNICE Teplota jako statistická veličina Prof. RNDr. Emanuel Svoboda, CSc. Původ slova Podnět a příčina určitého druhu
TEPLOTA (termodynamické a statistické pojetí) TEPELNÁ ROVNOVÁHA TEPLOTA, TEPLOTNÍ STUPNICE Teplota jako statistická veličina Prof. RNDr. Emanuel Svoboda, CSc. Původ slova Podnět a příčina určitého druhu
1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu:
 1 Pracovní úkol 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: (a) platinovýodporovýteploměr(určetekonstanty R 0, A, B). (b) termočlánek měď-konstantan(určete konstanty a, b,
1 Pracovní úkol 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: (a) platinovýodporovýteploměr(určetekonstanty R 0, A, B). (b) termočlánek měď-konstantan(určete konstanty a, b,
Tepelná vodivost. střední rychlost. T 1 > T 2 z. teplo přenesené za čas dt: T 1 T 2. tepelný tok střední volná dráha. součinitel tepelné vodivosti
 Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Tepelná vodivost teplo přenesené za čas dt: T 1 > T z T 1 S tepelný tok střední volná dráha T součinitel tepelné vodivosti střední rychlost Tepelná vodivost součinitel tepelné vodivosti při T = 300 K součinitel
Mol. fyz. a termodynamika
 Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Molekulová fyzika pracuje na základě kinetické teorie látek a statistiky Termodynamika zkoumání tepelných jevů a strojů nezajímají nás jednotlivé částice Molekulová fyzika základem jsou: Látka kteréhokoli
Měření teploty v budovách
 Měření teploty v budovách Zadání 1. Seznamte se s fyzikálními principy a funkčností předložených senzorů: odporový teploměr Pt100, termistor NCT, termočlánek typu K a bezdotykový úhrnný pyrometr 2. Proveďte
Měření teploty v budovách Zadání 1. Seznamte se s fyzikálními principy a funkčností předložených senzorů: odporový teploměr Pt100, termistor NCT, termočlánek typu K a bezdotykový úhrnný pyrometr 2. Proveďte
c) vysvětlení jednotlivých veličin ve vztahu pro okamžitou výchylku, jejich jednotky
 Harmonický kmitavý pohyb a) vysvětlení harmonického kmitavého pohybu b) zápis vztahu pro okamžitou výchylku c) vysvětlení jednotlivých veličin ve vztahu pro okamžitou výchylku, jejich jednotky d) perioda
Harmonický kmitavý pohyb a) vysvětlení harmonického kmitavého pohybu b) zápis vztahu pro okamžitou výchylku c) vysvětlení jednotlivých veličin ve vztahu pro okamžitou výchylku, jejich jednotky d) perioda
Rovnováha Tepelná - T všude stejná
 Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fyzika, maturitní okruhy (profilová část), školní rok 2014/2015 Gymnázium INTEGRA BRNO
 1. Jednotky a veličiny soustava SI odvozené jednotky násobky a díly jednotek skalární a vektorové fyzikální veličiny rozměrová analýza 2. Kinematika hmotného bodu základní pojmy kinematiky hmotného bodu
1. Jednotky a veličiny soustava SI odvozené jednotky násobky a díly jednotek skalární a vektorové fyzikální veličiny rozměrová analýza 2. Kinematika hmotného bodu základní pojmy kinematiky hmotného bodu
Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické
![Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické Termodynamika. T [K ]=t [ 0 C] 273,15 T [ K ]= t [ 0 C] termodynamická teplota: Stavy hmoty. jednotka: 1 K (kelvin) = 1/273,16 část termodynamické](/thumbs/24/2778201.jpg) Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
Termodynamika termodynamická teplota: Stavy hmoty jednotka: 1 K (kelvin) = 1/273,16 část termodynamické teploty trojného bodu vody (273,16 K = 0,01 o C). 0 o C = 273,15 K T [K ]=t [ 0 C] 273,15 T [ K ]=
17. Celá čísla.notebook. December 11, 2015 CELÁ ČÍSLA
 CELÁ ČÍSLA 1 Teploměr na obrázku ukazuje teplotu 15 C Říkáme: je mínus 15 stupňů Celsia je 15 stupňů pod nulou je 15 stupňů mrazu Ukaž na teploměru: 10 C, 8 C, +3 C, 6 C, 25 C, +36 C 2 Teploměr Teploměr
CELÁ ČÍSLA 1 Teploměr na obrázku ukazuje teplotu 15 C Říkáme: je mínus 15 stupňů Celsia je 15 stupňů pod nulou je 15 stupňů mrazu Ukaž na teploměru: 10 C, 8 C, +3 C, 6 C, 25 C, +36 C 2 Teploměr Teploměr
5.7 Vlhkost vzduchu 5.7.5 Absolutní vlhkost 5.7.6 Poměrná vlhkost 5.7.7 Rosný bod 5.7.8 Složení vzduchu 5.7.9 Měření vlhkosti vzduchu
 Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Fázové přechody 5.6.5 Fáze Fázové rozhraní 5.6.6 Gibbsovo pravidlo fází 5.6.7 Fázový přechod Fázový přechod prvního druhu Fázový přechod druhého druhu 5.6.7.1 Clausiova-Clapeyronova rovnice 5.6.8 Skupenství
Metrologie v geodézii (154MEGE) Ing. Lenka Línková, Ph.D. Katedra speciální geodézie B
 Metrologie v geodézii (154MEGE) Ing. Lenka Línková, Ph.D. Katedra speciální geodézie B 902 http://k154.fsv.cvut.cz/~linkova linkova@fsv.cvut.cz 1 Metrologie definice z TNI 01 0115: věda zabývající se měřením
Metrologie v geodézii (154MEGE) Ing. Lenka Línková, Ph.D. Katedra speciální geodézie B 902 http://k154.fsv.cvut.cz/~linkova linkova@fsv.cvut.cz 1 Metrologie definice z TNI 01 0115: věda zabývající se měřením
Maturitní témata fyzika
 Maturitní témata fyzika 1. Kinematika pohybů hmotného bodu - mechanický pohyb a jeho sledování, trajektorie, dráha - rychlost hmotného bodu - rovnoměrný pohyb - zrychlení hmotného bodu - rovnoměrně zrychlený
Maturitní témata fyzika 1. Kinematika pohybů hmotného bodu - mechanický pohyb a jeho sledování, trajektorie, dráha - rychlost hmotného bodu - rovnoměrný pohyb - zrychlení hmotného bodu - rovnoměrně zrychlený
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA
 MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 2 metody zkoumání látek na základě vnějších projevů: I. KINETICKÁ TEORIE LÁTEK -studium vlastností látek na základě vnitřní struktury, pohybu a vzájemného působení jednotlivých
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem
 Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Fázové heterogenní rovnováhy Fáze = homogenní část soustavy, oddělná fyzickým rozhraním, na rozhraní se vlastnosti mění skokem Rovnováha Tepelná - T všude stejná Mechanická - p všude stejný Chemická -
Skupenské stavy látek. Mezimolekulární síly
 Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Skupenské stavy látek Mezimolekulární síly 1 Interakce iont-dipól Např. hydratační (solvatační) interakce mezi Na + (iont) a molekulou vody (dipól). Jde o nejsilnější mezimolekulární (nevazebnou) interakci.
Fyzika - Sexta, 2. ročník
 - Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
- Sexta, 2. ročník Fyzika Výchovné a vzdělávací strategie Kompetence komunikativní Kompetence k řešení problémů Kompetence sociální a personální Kompetence občanská Kompetence k podnikavosti Kompetence
MĚŘENÍ RELATIVNÍ VLHKOSTI. - pro měření relativní vlhkosti se používají metody měření
 MĚŘENÍ RELATIVNÍ VLHKOSTI - pro měření relativní vlhkosti se používají metody měření obsahu vlhkosti vplynech Psychrometrické metody Měření rosného bodu Sorpční metody Rovnovážné elektrolytické metody
MĚŘENÍ RELATIVNÍ VLHKOSTI - pro měření relativní vlhkosti se používají metody měření obsahu vlhkosti vplynech Psychrometrické metody Měření rosného bodu Sorpční metody Rovnovážné elektrolytické metody
Základem molekulové fyziky je kinetická teorie látek. Vychází ze tří pouček:
 Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Molekulová fyzika zkoumá vlastnosti látek na základě jejich vnitřní struktury, pohybu a vzájemného působení částic, ze kterých se látky skládají. Termodynamika se zabývá zákony přeměny různých forem energie
Fázové rovnováhy I. Phase change cooling vest $ with Free Shipping. PCM phase change materials
 Fázové rovnováhy I PCM phase change materials akumulace tepla pomocí fázové změny (tání-tuhnutí) parafin, mastné kyseliny tání endotermní tuhnutí - exotermní Phase change cooling vest $149.95 with Free
Fázové rovnováhy I PCM phase change materials akumulace tepla pomocí fázové změny (tání-tuhnutí) parafin, mastné kyseliny tání endotermní tuhnutí - exotermní Phase change cooling vest $149.95 with Free
Cvičení: APLIKOVANÁ BIOKLIMATOLOGIE. Ing. Petr Hlavinka, Ph.D. Dveře č. N5068 (tel.: 3090) phlavinka@centrum.cz
 Cvičení: APLIKOVANÁ BIOKLIMATOLOGIE Ing. Petr Hlavinka, Ph.D. Dveře č. N5068 (tel.: 3090) phlavinka@centrum.cz Zápočet: -Docházka na cvičení (max. 2 absence) -Vyřešit 3 samostatné úkoly Meteorologická
Cvičení: APLIKOVANÁ BIOKLIMATOLOGIE Ing. Petr Hlavinka, Ph.D. Dveře č. N5068 (tel.: 3090) phlavinka@centrum.cz Zápočet: -Docházka na cvičení (max. 2 absence) -Vyřešit 3 samostatné úkoly Meteorologická
1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu:
 1 Pracovní úkoly 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: a. platinový odporový teploměr (určete konstanty R 0, A, B) b. termočlánek měď-konstantan (určete konstanty a,
1 Pracovní úkoly 1. Okalibrujte pomocí bodu tání ledu, bodu varu vody a bodu tuhnutí cínu: a. platinový odporový teploměr (určete konstanty R 0, A, B) b. termočlánek měď-konstantan (určete konstanty a,
Maturitní témata profilová část
 SEZNAM TÉMAT: Kinematika hmotného bodu mechanický pohyb, relativnost pohybu a klidu, vztažná soustava hmotný bod, trajektorie, dráha klasifikace pohybů průměrná a okamžitá rychlost rovnoměrný a rovnoměrně
SEZNAM TÉMAT: Kinematika hmotného bodu mechanický pohyb, relativnost pohybu a klidu, vztažná soustava hmotný bod, trajektorie, dráha klasifikace pohybů průměrná a okamžitá rychlost rovnoměrný a rovnoměrně
PRAKTIKUM I. Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM I. Úloha č. VIII. Název: Kalibrace odporového teploměru a termočlánku - fázové přechody Pracoval: Lukáš Vejmelka stud. skup.
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM I. Úloha č. VIII. Název: Kalibrace odporového teploměru a termočlánku - fázové přechody Pracoval: Lukáš Vejmelka stud. skup.
Molekulová fyzika a termika:
 Molekulová fyzika a termika: 1. Měření teploty: 2. Délková roztažnost a Objemová roztažnost látek 3. Bimetal 4. Anomálie vody 5. Částicová stavba látek, vlastnosti látek 6. Atomová hmotnostní konstanta
Molekulová fyzika a termika: 1. Měření teploty: 2. Délková roztažnost a Objemová roztažnost látek 3. Bimetal 4. Anomálie vody 5. Částicová stavba látek, vlastnosti látek 6. Atomová hmotnostní konstanta
Do známky zkoušky rovnocenným podílem započítávají získané body ze zápočtového testu.
 Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
Podmínky pro získání zápočtu a zkoušky z předmětu Chemicko-inženýrská termodynamika pro zpracování ropy Zápočet je udělen, pokud student splní zápočtový test alespoň na 50 %. Zápočtový test obsahuje 3
LOGO. Molekulová fyzika
 Molekulová fyzika Molekulová fyzika Molekulová fyzika vysvětluje fyzikální jevy na základě znalosti jejich částicové struktury. Jejím základem je kinetická teorie látek (KTL). KTL obsahuje tři tvrzení:
Molekulová fyzika Molekulová fyzika Molekulová fyzika vysvětluje fyzikální jevy na základě znalosti jejich částicové struktury. Jejím základem je kinetická teorie látek (KTL). KTL obsahuje tři tvrzení:
2.4 Stavové chování směsí plynů Ideální směs Ideální směs reálných plynů Stavové rovnice pro plynné směsi
 1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
1. ZÁKLADNÍ POJMY 1.1 Systém a okolí 1.2 Vlastnosti systému 1.3 Vybrané základní veličiny 1.3.1 Množství 1.3.2 Délka 1.3.2 Délka 1.4 Vybrané odvozené veličiny 1.4.1 Objem 1.4.2 Hustota 1.4.3 Tlak 1.4.4
Nauka o materiálu. Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny
 Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
Nauka o materiálu Přednáška č.10 Difuze v tuhých látkách, fáze a fázové přeměny Difuze v tuhých látkách Difuzí nazýváme přesun atomů nebo iontů na vzdálenost větší než je meziatomová vzdálenost. Hnací
T0 Teplo a jeho měření
 Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
Teplo a jeho měření 1 Teplo 2 Kalorimetrie Kalorimetr 3 Tepelná kapacita 3.1 Měrná tepelná kapacita Měrná tepelná kapacita při stálém objemu a stálém tlaku Poměr měrných tepelných kapacit 3.2 Molární tepelná
PRINCIP MĚŘENÍ TEPLOTY spočívá v porovnání teploty daného tělesa s definovanou stupnicí.
 1 SENZORY TEPLOTY TEPLOTA je jednou z nejdůležitějších veličin ovlivňujících téměř všechny stavy a procesy v přírodě Ke stanovení teploty se využívá závislosti určitých fyzikálních veličin na teplotě (A
1 SENZORY TEPLOTY TEPLOTA je jednou z nejdůležitějších veličin ovlivňujících téměř všechny stavy a procesy v přírodě Ke stanovení teploty se využívá závislosti určitých fyzikálních veličin na teplotě (A
Termodynamika materiálů. Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn
 Termodynamika materiálů Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn Důležité konstanty Standartní podmínky Avogadrovo číslo N A = 6,023.10
Termodynamika materiálů Vztahy a přeměny různých druhů energie při termodynamických dějích podmínky nutné pro uskutečnění fázových přeměn Důležité konstanty Standartní podmínky Avogadrovo číslo N A = 6,023.10
Okruhy k maturitní zkoušce z fyziky
 Okruhy k maturitní zkoušce z fyziky 1. Fyzikální obraz světa - metody zkoumaní fyzikální reality, pojem vztažné soustavy ve fyzice, soustava jednotek SI, skalární a vektorové fyzikální veličiny, fyzikální
Okruhy k maturitní zkoušce z fyziky 1. Fyzikální obraz světa - metody zkoumaní fyzikální reality, pojem vztažné soustavy ve fyzice, soustava jednotek SI, skalární a vektorové fyzikální veličiny, fyzikální
IV. Fázové rovnováhy. 4. Fázové rovnováhy Ústav procesní a zpracovatelské techniky FS ČVUT v Praze
 IV. Fázové rovnováhy 1 4. Fázové rovnováhy 4.1 Základní pojmy 4.2 Fázové rovnováhy jednosložkové soustavy 4.3 Fázové rovnováhy dvousložkových soustav 4.3.1 Soustava tuhá složka tuhá složka 4.3.2 Soustava
IV. Fázové rovnováhy 1 4. Fázové rovnováhy 4.1 Základní pojmy 4.2 Fázové rovnováhy jednosložkové soustavy 4.3 Fázové rovnováhy dvousložkových soustav 4.3.1 Soustava tuhá složka tuhá složka 4.3.2 Soustava
Profilová část maturitní zkoušky 2017/2018
 Střední průmyslová škola, Přerov, Havlíčkova 2 751 52 Přerov Profilová část maturitní zkoušky 2017/2018 TEMATICKÉ OKRUHY A HODNOTÍCÍ KRITÉRIA Studijní obor: 78-42-M/01 Technické lyceum Předmět: FYZIKA
Střední průmyslová škola, Přerov, Havlíčkova 2 751 52 Přerov Profilová část maturitní zkoušky 2017/2018 TEMATICKÉ OKRUHY A HODNOTÍCÍ KRITÉRIA Studijní obor: 78-42-M/01 Technické lyceum Předmět: FYZIKA
Termodynamika. Děj, který není kvazistatický, se nazývá nestatický.
 Termodynamika Zabývá se ději, při nichž se mění tepelná energie v jiné druhy energie (zejména mechanické). Studuje vlastnosti látek bez přihlédnutí k jejich mikrostruktuře. Je vystavěna na axiomech (0.,
Termodynamika Zabývá se ději, při nichž se mění tepelná energie v jiné druhy energie (zejména mechanické). Studuje vlastnosti látek bez přihlédnutí k jejich mikrostruktuře. Je vystavěna na axiomech (0.,
PRAKTIKUM I. Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK. Pracoval: Pavel Ševeček stud. skup.: F/F1X/11 dne:
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM I. Úloha č. VIII Název: Kalibrace odporového teploměru a termočlánku fázové přechody Pracoval: Pavel Ševeček stud. skup.:
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM I. Úloha č. VIII Název: Kalibrace odporového teploměru a termočlánku fázové přechody Pracoval: Pavel Ševeček stud. skup.:
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
d p o r o v t e p l o m ě r, t e r m o č l á n k
 d p o r o v t e p l o m ě r, t e r m o č l á n k Ú k o l : a) Proveďte kalibraci odporového teploměru, termočlánku a termistoru b) Určete teplotní koeficienty odporového teploměru, konstanty charakterizující
d p o r o v t e p l o m ě r, t e r m o č l á n k Ú k o l : a) Proveďte kalibraci odporového teploměru, termočlánku a termistoru b) Určete teplotní koeficienty odporového teploměru, konstanty charakterizující
Molekulová fyzika a termodynamika
 Molekulová fyzika a termodynamika Molekulová fyzika a termodynamika Úvod, vnitřní energie soustavy, teplo, teplota, stavová rovnice ideálního plynu Termodynamické zákony, termodynamické děje Teplotní a
Molekulová fyzika a termodynamika Molekulová fyzika a termodynamika Úvod, vnitřní energie soustavy, teplo, teplota, stavová rovnice ideálního plynu Termodynamické zákony, termodynamické děje Teplotní a
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny
 Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
Transportní jevy v plynech Reálné plyny Fázové přechody Kapaliny Hustota toku Zatím jsme studovali pouze soustavy, které byly v rovnovážném stavu není-li soustava v silovém poli, je hustota částic stejná
FYZIKA 6. ročník 2. část
 FYZIKA 6. ročník 2. část 23_Hmotnost tělesa... 2 24_Rovnoramenné váhy.... 3 25_Hustota... 4 26_Výpočet hustoty látky... 4 27_Výpočet hustoty látky příklady... 6 28_Výpočet hmotnosti tělesa příklady...
FYZIKA 6. ročník 2. část 23_Hmotnost tělesa... 2 24_Rovnoramenné váhy.... 3 25_Hustota... 4 26_Výpočet hustoty látky... 4 27_Výpočet hustoty látky příklady... 6 28_Výpočet hmotnosti tělesa příklady...
Číslo projektu: CZ.1.07/1.4.00/21.3811 Název DUM: Teplota Číslo DUM: III/2/FY/2/1/13 Vzdělávací předmět: Fyzika Tematická oblast: Fyzikální veličiny
 Číslo projektu: CZ.1.07/1.4.00/21.3811 Název DUM: Teplota Číslo DUM: III/2/FY/2/1/13 Vzdělávací předmět: Fyzika Tematická oblast: Fyzikální veličiny a jejich měření Autor: Mgr. Petra Kejkrtová Anotace:
Číslo projektu: CZ.1.07/1.4.00/21.3811 Název DUM: Teplota Číslo DUM: III/2/FY/2/1/13 Vzdělávací předmět: Fyzika Tematická oblast: Fyzikální veličiny a jejich měření Autor: Mgr. Petra Kejkrtová Anotace:
Základy elektrotechniky - úvod
 Elektrotechnika se zabývá výrobou, rozvodem a spotřebou elektrické energie včetně zařízení k těmto účelům používaným, dále sdělovacími a informačními technologiemi. Elektrotechnika je úzce spjata s matematikou
Elektrotechnika se zabývá výrobou, rozvodem a spotřebou elektrické energie včetně zařízení k těmto účelům používaným, dále sdělovacími a informačními technologiemi. Elektrotechnika je úzce spjata s matematikou
Fyzikální chemie. Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302. 14. února 2013
 Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Fyzikální chemie Magda Škvorová KFCH CN463 magda.skvorova@ujep.cz, tel. 3302 14. února 2013 Co je fyzikální chemie? Co je fyzikální chemie? makroskopický přístup: (klasická) termodynamika nerovnovážná
Integrovaná střední škola, Hlaváčkovo nám. 673, Slaný
 Označení materiálu: VY_32_INOVACE_STEIV_FYZIKA1_11 Název materiálu: Teplo a teplota. Tematická oblast: Fyzika 1.ročník Anotace: Prezentace slouží k vysvětlení základních fyzikálních veličin tepla a teploty.
Označení materiálu: VY_32_INOVACE_STEIV_FYZIKA1_11 Název materiálu: Teplo a teplota. Tematická oblast: Fyzika 1.ročník Anotace: Prezentace slouží k vysvětlení základních fyzikálních veličin tepla a teploty.
2.1 Empirická teplota
 Přednáška 2 Teplota a její měření Termika zkoumá tepelné vlastnosti látek a soustav těles, jevy spojené s tepelnou výměnou, chování soustav při tepelné výměně, změny skupenství látek, atd. 2.1 Empirická
Přednáška 2 Teplota a její měření Termika zkoumá tepelné vlastnosti látek a soustav těles, jevy spojené s tepelnou výměnou, chování soustav při tepelné výměně, změny skupenství látek, atd. 2.1 Empirická
PROCESY V TECHNICE BUDOV 8
 UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
UNIVERZITA TOMÁŠE BATI VE ZLÍNĚ FAKULTA APLIKOVANÉ INFORMATIKY PROCESY V TECHNICE BUDOV 8 Dagmar Janáčová, Hana Charvátová Zlín 2013 Tento studijní materiál vznikl za finanční podpory Evropského sociálního
bak-06=1/1 http://www.vscht.cz/fch/cz/pomucky/kolafa/n403011p.html
 bak-06=1/1 pst=101325 = 1.013e+05 Pa R=8.314 = 8.314JK 1 mol 1 Gibbsovo fázové pravidlo v = k f + 2 C počet stupnů volnosti počet složek počet fází počet vazných podmínek 1. Gibbsovo fázové pravidlo Určete
bak-06=1/1 pst=101325 = 1.013e+05 Pa R=8.314 = 8.314JK 1 mol 1 Gibbsovo fázové pravidlo v = k f + 2 C počet stupnů volnosti počet složek počet fází počet vazných podmínek 1. Gibbsovo fázové pravidlo Určete
Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4.
 Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Vyučovací předmět - Chemie Vzdělávací obor - Člověk a příroda Gymnázium, Milevsko, Masarykova 183 Školní vzdělávací program (ŠVP) pro vyšší stupeň osmiletého studia a čtyřleté studium 4. ročník - seminář
Gymnázium, Havířov - Město, Komenského 2 MATURITNÍ OTÁZKY Z FYZIKY Školní rok: 2012/2013
 1. a) Kinematika hmotného bodu klasifikace pohybů poloha, okamžitá a průměrná rychlost, zrychlení hmotného bodu grafické znázornění dráhy, rychlosti a zrychlení na čase kinematika volného pádu a rovnoměrného
1. a) Kinematika hmotného bodu klasifikace pohybů poloha, okamžitá a průměrná rychlost, zrychlení hmotného bodu grafické znázornění dráhy, rychlosti a zrychlení na čase kinematika volného pádu a rovnoměrného
11. Odporový snímač teploty, měřicí systém a bezkontaktní teploměr
 11. Odporový snímač teploty, měřicí systém a bezkontaktní teploměr Otázky k úloze (domácí příprava): Pro jakou teplotu je U = 0 v případě použití převodníku s posunutou nulou dle obr. 1 (senzor Pt 100,
11. Odporový snímač teploty, měřicí systém a bezkontaktní teploměr Otázky k úloze (domácí příprava): Pro jakou teplotu je U = 0 v případě použití převodníku s posunutou nulou dle obr. 1 (senzor Pt 100,
Základní poznatky. Teplota Vnitřní energie soustavy Teplo
 Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
Molekulová fyzika a termika Základní poznatky Základní poznatky Teplota Vnitřní energie soustavy Teplo Termika = část fyziky zabývající se studiem vlastností látek a jejich změn souvisejících s teplotou
Digitální učební materiál
 Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
Evidenční číslo materiálu: 516 Digitální učební materiál Autor: Mgr. Pavel Kleibl Datum: 22. 1. 2013 Ročník: 8. Vzdělávací oblast: Člověk a příroda Vzdělávací obor: Fyzika Tematický okruh: Energie Téma:
Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Molekulová fyzika, termika 2. ročník, sexta 2 hodiny týdně Fyzikální učebna vybavená audiovizuální technikou, interaktivní tabule, fyzikální pomůcky
Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika v učebně fyziky, interaktivní tabule a i-učebnice
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA
 MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 5. TEPLOTNÍ STUPNICE Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. TEPLOTNÍ STUPNICE Teplotních stupnic existuje více: - Kelvinova stupnice - Fahrenheitova stupnice
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 5. TEPLOTNÍ STUPNICE Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. TEPLOTNÍ STUPNICE Teplotních stupnic existuje více: - Kelvinova stupnice - Fahrenheitova stupnice
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA
 MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 4. TEPLO, TEPLOTA, TEPELNÁ VÝMĚNA Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. TEPLO Teplo je míra změny vnitřní energie, kterou systém vymění při styku s jiným
MOLEKULOVÁ FYZIKA A TERMODYNAMIKA 4. TEPLO, TEPLOTA, TEPELNÁ VÝMĚNA Autor: Ing. Eva Jančová DESS SOŠ a SOU spol. s r. o. TEPLO Teplo je míra změny vnitřní energie, kterou systém vymění při styku s jiným
Maturitní temata z fyziky pro 4.B, OkB ve školním roce 2011/2012
 Maturitní temata z fyziky pro 4.B, OkB ve školním roce 2011/2012 1. Kinematika pohybu hmotného bodu pojem hmotný bod, vztažná soustava, určení polohy, polohový vektor trajektorie, dráha, rychlost (okamžitá,
Maturitní temata z fyziky pro 4.B, OkB ve školním roce 2011/2012 1. Kinematika pohybu hmotného bodu pojem hmotný bod, vztažná soustava, určení polohy, polohový vektor trajektorie, dráha, rychlost (okamžitá,
ZŠ ÚnO, Bratří Čapků 1332
 Animovaná fyzika Top-Hit Atomy a molekuly Atom Brownův pohyb Difúze Elektron Elementární náboj Jádro atomu Kladný iont Model atomu Molekula Neutron Nukleonové číslo Pevná látka Plyn Proton Protonové číslo
Animovaná fyzika Top-Hit Atomy a molekuly Atom Brownův pohyb Difúze Elektron Elementární náboj Jádro atomu Kladný iont Model atomu Molekula Neutron Nukleonové číslo Pevná látka Plyn Proton Protonové číslo
Teplota. fyzikální veličina značka t
 Teplota fyzikální veličina značka t Je to vlastnost předmětů a okolí, kterou je člověk schopen vnímat a přiřadit jí pocity studeného, teplého či horkého. Jak se tato vlastnost jmenuje? Teplota Naše pocity
Teplota fyzikální veličina značka t Je to vlastnost předmětů a okolí, kterou je člověk schopen vnímat a přiřadit jí pocity studeného, teplého či horkého. Jak se tato vlastnost jmenuje? Teplota Naše pocity
1. Látkové soustavy, složení soustav
 , složení soustav 1 , složení soustav 1. Základní pojmy 1.1 Hmota 1.2 Látky 1.3 Pole 1.4 Soustava 1.5 Fáze a fázové přeměny 1.6 Stavové veličiny 1.7 Složka 2. Hmotnost a látkové množství 3. Složení látkových
, složení soustav 1 , složení soustav 1. Základní pojmy 1.1 Hmota 1.2 Látky 1.3 Pole 1.4 Soustava 1.5 Fáze a fázové přeměny 1.6 Stavové veličiny 1.7 Složka 2. Hmotnost a látkové množství 3. Složení látkových
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kalibrace odporového teploměru a termočlánku
 Kalibrace odporového teploměru a termočlánku Jakub Michálek 10. dubna 2009 Teorie Pro označení veličin viz text [1] s výjimkou, že teplotní rozdíl značím T, protože značku t už mám vyhrazenu pro čas. Ze
Kalibrace odporového teploměru a termočlánku Jakub Michálek 10. dubna 2009 Teorie Pro označení veličin viz text [1] s výjimkou, že teplotní rozdíl značím T, protože značku t už mám vyhrazenu pro čas. Ze
Kapaliny Molekulové vdw síly, vodíkové můstky
 Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Kapaliny Molekulové vdw síly, vodíkové můstky Metalické roztavené kovy, ionty + elektrony, elektrostatické síly Iontové roztavené soli, FLINAK (LiF + NaF + KF), volně pohyblivé anionty a kationty, iontová
Měření měrného skupenského tepla tání ledu
 KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
KATEDRA EXPERIMENTÁLNÍ FYZIKY PŘÍRODOVĚDECKÁ FAKULTA UNIVERZITY PALACKÉHO V OLOMOUCI FYZIKÁLNÍ PRAKTIKUM Z MOLEKULOVÉ FYZIKY A TERMODYNAMIKY Měření měrného skupenského tepla tání ledu Úvod Tání, měrné
EXPERIMENTÁLNÍ METODY I 3. Měření teplot
 FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí prof. Ing. Milan Pavelek, CSc. EXPERIMENTÁLNÍ METODY I 3. Měření teplot OSNOVA 3. KAPITOLY Úvod do problematiky měření teplot
FSI VUT v Brně, Energetický ústav Odbor termomechaniky a techniky prostředí prof. Ing. Milan Pavelek, CSc. EXPERIMENTÁLNÍ METODY I 3. Měření teplot OSNOVA 3. KAPITOLY Úvod do problematiky měření teplot
Základní pojmy a jednotky
 Základní pojmy a jednotky Tlak: p = F S [N. m 2 ] [kg. m. s 2. m 2 ] [kg. m 1. s 2 ] [Pa] (1) Hydrostatický tlak: p = h. ρ. g [m. kg. m 3. m. s 2 ] [kg. m 1. s 2 ] [Pa] (2) Převody jednotek tlaku: Bar
Základní pojmy a jednotky Tlak: p = F S [N. m 2 ] [kg. m. s 2. m 2 ] [kg. m 1. s 2 ] [Pa] (1) Hydrostatický tlak: p = h. ρ. g [m. kg. m 3. m. s 2 ] [kg. m 1. s 2 ] [Pa] (2) Převody jednotek tlaku: Bar
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno
 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno 1 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno Struktura
Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno 1 Přednášky z lékařské biofyziky Biofyzikální ústav Lékařské fakulty Masarykovy univerzity, Brno Struktura
Základní pojmy. T = ϑ + 273,15 [K], [ C] Definice teploty:
![Základní pojmy. T = ϑ + 273,15 [K], [ C] Definice teploty: Základní pojmy. T = ϑ + 273,15 [K], [ C] Definice teploty:](/thumbs/30/14603809.jpg) Definice teploty: Základní pojmy Fyzikální veličina vyjadřující míru tepelného stavu tělesa Teplotní stupnice Termodynamická (Kelvinova) stupnice je určena dvěma pevnými body: absolutní nula (ustává termický
Definice teploty: Základní pojmy Fyzikální veličina vyjadřující míru tepelného stavu tělesa Teplotní stupnice Termodynamická (Kelvinova) stupnice je určena dvěma pevnými body: absolutní nula (ustává termický
metoda je základem fenomenologické vědy termodynamiky, statistická metoda je základem kinetické teorie plynů, na níž si princip této metody ukážeme.
 Přednáška 1 Úvod Při studiu tepelných vlastností látek a jevů probíhajících při tepelné výměně budeme používat dvě různé metody zkoumání: termodynamickou a statistickou. Termodynamická metoda je základem
Přednáška 1 Úvod Při studiu tepelných vlastností látek a jevů probíhajících při tepelné výměně budeme používat dvě různé metody zkoumání: termodynamickou a statistickou. Termodynamická metoda je základem
10. Energie a její transformace
 10. Energie a její transformace Energie je nejdůležitější vlastností hmoty a záření. Je obsažena v každém kousku hmoty i ve světelném paprsku. Je ve vesmíru a všude kolem nás. S energií se setkáváme na
10. Energie a její transformace Energie je nejdůležitější vlastností hmoty a záření. Je obsažena v každém kousku hmoty i ve světelném paprsku. Je ve vesmíru a všude kolem nás. S energií se setkáváme na
ZMĚNY SKUPENSTVÍ LÁTEK
 ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
ZMĚNY SKUPENSTVÍ LÁTEK TÁNÍ A TUHNUTÍ - OSNOVA Kapilární jevy příklad Skupenské přeměny látek Tání a tuhnutí Teorie s video experimentem Příklad KAPILÁRNÍ JEVY - OPAKOVÁNÍ KAPILÁRNÍ JEVY - PŘÍKLAD Jak
TEMATICKÝ PLÁN 6. ročník
 TEMATICKÝ PLÁN 6. ročník Týdenní dotace: 1,5h/týden Vyučující: Mgr. Tomáš Mlejnek Ročník: 6. (6. A, 6. B) Školní rok 2018/2019 FYZIKA pro 6. ročník ZŠ PROMETHEUS, doc. RNDr. Růžena Kolářová, CSc., PaeDr.
TEMATICKÝ PLÁN 6. ročník Týdenní dotace: 1,5h/týden Vyučující: Mgr. Tomáš Mlejnek Ročník: 6. (6. A, 6. B) Školní rok 2018/2019 FYZIKA pro 6. ročník ZŠ PROMETHEUS, doc. RNDr. Růžena Kolářová, CSc., PaeDr.
Soustava SI FYZIKÁLNÍ VELIČINY A JEDNOTKY
 Soustava SI FYZIKÁLNÍ VELIČINY A JEDNOTKY Mezinárodní soustava jednotek SI Systéme Internationald Unités (Mezinárodní soustava jednotek) zavedena dohodou v roce 1960 Rozdělení Základní jednotky Odvozené
Soustava SI FYZIKÁLNÍ VELIČINY A JEDNOTKY Mezinárodní soustava jednotek SI Systéme Internationald Unités (Mezinárodní soustava jednotek) zavedena dohodou v roce 1960 Rozdělení Základní jednotky Odvozené
Historie bezdotykového měření teplot
 Historie bezdotykového měření teplot Jana Kuklová, 3 70 2008/2009 FD ČVUT v Praze Ústav aplikované matematiky K611 Softwarové nástroje pro zpracování obrazu z termovizních měření Osnova prezentace Úvod
Historie bezdotykového měření teplot Jana Kuklová, 3 70 2008/2009 FD ČVUT v Praze Ústav aplikované matematiky K611 Softwarové nástroje pro zpracování obrazu z termovizních měření Osnova prezentace Úvod
Ch - Rozlišování látek
 Ch - Rozlišování látek Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl kompletně
Ch - Rozlišování látek Autor: Mgr. Jaromír JUŘEK Kopírování a jakékoliv další využití výukového materiálu je povoleno pouze s uvedením odkazu na www.jarjurek.cz. VARIACE 1 Tento dokument byl kompletně
PRAKTIKUM IV Jaderná a subjaderná fyzika
 Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM IV Jaderná a subjaderná fyzika Úloha č. A15 Název: Studium atomových emisních spekter Pracoval: Radim Pechal dne 19. listopadu
Oddělení fyzikálních praktik při Kabinetu výuky obecné fyziky MFF UK PRAKTIKUM IV Jaderná a subjaderná fyzika Úloha č. A15 Název: Studium atomových emisních spekter Pracoval: Radim Pechal dne 19. listopadu
Zákony ideálního plynu
 5.2Zákony ideálního plynu 5.1.1 Ideální plyn 5.1.2 Avogadrův zákon 5.1.3 Normální podmínky 5.1.4 Boyleův-Mariottův zákon Izoterma 5.1.5 Gay-Lussacův zákon 5.1.6 Charlesův zákon 5.1.7 Poissonův zákon 5.1.8
5.2Zákony ideálního plynu 5.1.1 Ideální plyn 5.1.2 Avogadrův zákon 5.1.3 Normální podmínky 5.1.4 Boyleův-Mariottův zákon Izoterma 5.1.5 Gay-Lussacův zákon 5.1.6 Charlesův zákon 5.1.7 Poissonův zákon 5.1.8
Číslo materiálu Předmět ročník Téma hodiny Ověřený materiál Program
 Číslo materiálu Předmět ročník Téma hodiny Ověřený materiál Program 1 VY_32_INOVACE_01_13 fyzika 6. Elektrické vlastnosti těles Výklad učiva PowerPoint 6 4 2 VY_32_INOVACE_01_14 fyzika 6. Atom Výklad učiva
Číslo materiálu Předmět ročník Téma hodiny Ověřený materiál Program 1 VY_32_INOVACE_01_13 fyzika 6. Elektrické vlastnosti těles Výklad učiva PowerPoint 6 4 2 VY_32_INOVACE_01_14 fyzika 6. Atom Výklad učiva
3.2 Látka a její skupenství
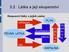 3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
3.2 Látka a její skupenství Skupenství látky a jejich změny sublimace PEVNÁ LÁTKA tání desublimace tuhnutí PLYN vy pa řo vá ní KAPALINA zka pal ňo vá ní Látka a změna vnitřní energie Změna vnitřní energie
A:Měření odporových teploměrů v ultratermostatu B:Měření teploty totálním pyrometrem KET/MNV (8. cvičení)
 A:Měření odporových teploměrů v ultratermostatu B:Měření teploty totálním pyrometrem KET/MNV (8. cvičení) Vypracoval : Martin Dlouhý Osobní číslo : A8B268P A:Měření odporových teploměrů v ultratermostatu
A:Měření odporových teploměrů v ultratermostatu B:Měření teploty totálním pyrometrem KET/MNV (8. cvičení) Vypracoval : Martin Dlouhý Osobní číslo : A8B268P A:Měření odporových teploměrů v ultratermostatu
Hmotnost atomů a molekul 6 Látkové množství 11. Rozdělení směsí 16 Separační metody 20. Hustota, hmotnostní a objemový zlomek 25.
 Obsah Obecná chemie II. 1. Látkové množství Hmotnost atomů a molekul 6 Látkové množství 11 2. Směsi Rozdělení směsí 16 Separační metody 20 3. Chemické výpočty Hustota, hmotnostní a objemový zlomek 25 Koncentrace
Obsah Obecná chemie II. 1. Látkové množství Hmotnost atomů a molekul 6 Látkové množství 11 2. Směsi Rozdělení směsí 16 Separační metody 20 3. Chemické výpočty Hustota, hmotnostní a objemový zlomek 25 Koncentrace
Teplota jedna ze základních jednotek soustavy SI, vyjadřována je v Kelvinech (značka K) další používané stupnice: Celsiova, Fahrenheitova
 1 Rozložení, distribuce tepla Teplota je charakteristika tepelného stavu hmoty je to stavová veličina, charakterizující termodynamickou rovnováhu systému. Teplo vyjadřuje kinetickou energii částic. Teplota
1 Rozložení, distribuce tepla Teplota je charakteristika tepelného stavu hmoty je to stavová veličina, charakterizující termodynamickou rovnováhu systému. Teplo vyjadřuje kinetickou energii částic. Teplota
Termomechanika cvičení
 KATEDRA ENERGETICKÝCH STROJŮ A ZAŘÍZENÍ Termomechanika cvičení 1. cvičení Ing. Michal Volf / 18.02.2019 Informace o cvičení Ing. Michal Volf Email: volfm@kke.zcu.cz Konzultace: po vzájemné dohodě prezentace
KATEDRA ENERGETICKÝCH STROJŮ A ZAŘÍZENÍ Termomechanika cvičení 1. cvičení Ing. Michal Volf / 18.02.2019 Informace o cvičení Ing. Michal Volf Email: volfm@kke.zcu.cz Konzultace: po vzájemné dohodě prezentace
Příprava pro lektora
 Příprava pro lektora stanoviště aktivita pomůcky 1 typy oblačnosti podle manuálu Globe stanov typy mraků na obrázcích pokryvnost oblohy vytvoř model oblohy s 25% oblačností, použij modrý papír (obloha)
Příprava pro lektora stanoviště aktivita pomůcky 1 typy oblačnosti podle manuálu Globe stanov typy mraků na obrázcích pokryvnost oblohy vytvoř model oblohy s 25% oblačností, použij modrý papír (obloha)
Konstrukce a interpretace fázových diagramů
 Konstrukce a interpretace fázových diagramů http://www.atilim.edu.tr/~ktur/ktur/images/chocolate%20phase%20diagram.gif J. Leitner Ústav inženýrství pevných látek VŠCHT Praha 1 O čem to bude? Co jsou FD
Konstrukce a interpretace fázových diagramů http://www.atilim.edu.tr/~ktur/ktur/images/chocolate%20phase%20diagram.gif J. Leitner Ústav inženýrství pevných látek VŠCHT Praha 1 O čem to bude? Co jsou FD
Nultá věta termodynamická
 TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
TERMODYNAMIKA Nultá věta termodynamická 2 Práce 3 Práce - příklady 4 1. věta termodynamická 5 Entalpie 6 Tepelné kapacity 7 Vnitřní energie a entalpie ideálního plynu 8 Výpočet tepla a práce 9 Adiabatický
UČIVO. Termodynamická teplota. První termodynamický zákon Přenos vnitřní energie
 PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
PŘEDMĚT: FYZIKA ROČNÍK: SEXTA VÝSTUP UČIVO MEZIPŘEDM. VZTAHY, PRŮŘEZOVÁ TÉMATA, PROJEKTY, KURZY POZNÁMKY Zná 3 základní poznatky kinetické teorie látek a vysvětlí jejich praktický význam Vysvětlí pojmy
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH
 SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
SBÍRKA ŘEŠENÝCH FYZIKÁLNÍCH ÚLOH MECHANIKA MOLEKULOVÁ FYZIKA A TERMIKA ELEKTŘINA A MAGNETISMUS KMITÁNÍ A VLNĚNÍ OPTIKA FYZIKA MIKROSVĚTA TERMODYNAMICKÁ TEPLOTNÍ STUPNICE, TEPLOTA 1) Převeďte hodnoty v
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů
 ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Mgr. Vladimír Hradecký Číslo materiálu 8_F_1_02 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
ZÁKLADNÍ ŠKOLA KOLÍN II., KMOCHOVA 943 škola s rozšířenou výukou matematiky a přírodovědných předmětů Autor Mgr. Vladimír Hradecký Číslo materiálu 8_F_1_02 Datum vytvoření 2. 11. 2011 Druh učebního materiálu
Maturitní otázky z předmětu FYZIKA
 Wichterlovo gymnázium, Ostrava-Poruba, příspěvková organizace Maturitní otázky z předmětu FYZIKA 1. Pohyby z hlediska kinematiky a jejich zákony Klasifikace pohybů z hlediska trajektorie a závislosti rychlosti
Wichterlovo gymnázium, Ostrava-Poruba, příspěvková organizace Maturitní otázky z předmětu FYZIKA 1. Pohyby z hlediska kinematiky a jejich zákony Klasifikace pohybů z hlediska trajektorie a závislosti rychlosti
Krása fázových diagramů jak je sestrojit a číst Silvie Mašková
 Krása fázových diagramů jak je sestrojit a číst Silvie Mašková Katedra fyziky kondenzovaných látek Matematicko-fyzikální fakulta Univerzita Karlova Praha Pár základích pojmů na začátek Co jsou fázové diagramy?
Krása fázových diagramů jak je sestrojit a číst Silvie Mašková Katedra fyziky kondenzovaných látek Matematicko-fyzikální fakulta Univerzita Karlova Praha Pár základích pojmů na začátek Co jsou fázové diagramy?
Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika v učebně fyziky, interaktivní tabule
 Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Předmět: Náplň: Třída: Počet hodin: Pomůcky: Fyzika (FYZ) Práce a energie, tepelné jevy, elektrický proud, zvukové jevy Tercie 1+1 hodina týdně Pomůcky, které poskytuje sbírka fyziky, a audiovizuální technika
Plyn. 11 plynných prvků. Vzácné plyny. He, Ne, Ar, Kr, Xe, Rn Diatomické plynné prvky H 2, N 2, O 2, F 2, Cl 2
 Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
Plyny Plyn T v, K Vzácné plyny 11 plynných prvků He, Ne, Ar, Kr, Xe, Rn 165 Rn 211 N 2 O 2 77 F 2 90 85 Diatomické plynné prvky Cl 2 238 H 2, N 2, O 2, F 2, Cl 2 H 2 He Ne Ar Kr Xe 20 4.4 27 87 120 1 Plyn
VLASTNOSTI VLÁKEN. 3. Tepelné vlastnosti vláken
 VLASNOSI VLÁKEN 3. epelné vlastnosti vláken 3.. Úvod epelné vlastnosti vláken jsou velice důležité, neboť jsou rozhodující pro volbu vhodných parametrů zpracování i použití vláken. Závisí na chemickém
VLASNOSI VLÁKEN 3. epelné vlastnosti vláken 3.. Úvod epelné vlastnosti vláken jsou velice důležité, neboť jsou rozhodující pro volbu vhodných parametrů zpracování i použití vláken. Závisí na chemickém
TEMATICKÝ PLÁN. Literatura: FYZIKA pro 6. ročník ZŠ PROMETHEUS, doc. RNDr. Růžena Kolářová, CSc., PaeDr. Jiří Bohuněk,
 TEMATICKÝ PLÁN Předmět: FYZIKA Týdenní dotace: 2h/týden Vyučující: Mgr. Jan Souček Vzdělávací program: ŠVP Umím, chápu, rozumím Ročník: 6. (6. A, 6. B) Školní rok 2016/2017 Literatura: FYZIKA pro 6. ročník
TEMATICKÝ PLÁN Předmět: FYZIKA Týdenní dotace: 2h/týden Vyučující: Mgr. Jan Souček Vzdělávací program: ŠVP Umím, chápu, rozumím Ročník: 6. (6. A, 6. B) Školní rok 2016/2017 Literatura: FYZIKA pro 6. ročník
Hydrochemie koncentrace látek (výpočty)
 Atomová hmotnostní konstanta/jednotka m u Relativní atomová hmotnost Relativní molekulová hmotnost Látkové množství (mol) mol je takové množství látky, které obsahuje tolik částic, kolik je atomů ve 2
Atomová hmotnostní konstanta/jednotka m u Relativní atomová hmotnost Relativní molekulová hmotnost Látkové množství (mol) mol je takové množství látky, které obsahuje tolik částic, kolik je atomů ve 2
PŘEVODY JEDNOTEK. jednotky " 1. základní
 PŘEVODY JEDNOTEK jednotky 1. základní Fyzikální veličina Jednotka Značka Délka l metr m Hmotnost m kilogram kg Čas t sekunda s Termodynamická teplota T kelvin K Látkové množství n mol mol Elektrický proud
PŘEVODY JEDNOTEK jednotky 1. základní Fyzikální veličina Jednotka Značka Délka l metr m Hmotnost m kilogram kg Čas t sekunda s Termodynamická teplota T kelvin K Látkové množství n mol mol Elektrický proud
