SOUHRN ÚDAJŮ O PŘÍPRAVKU. AMILOSTAD 5 mg AMILOSTAD 10 mg tablety
|
|
|
- Alžběta Havlíčková
- před 6 lety
- Počet zobrazení:
Transkript
1 Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls / NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU AMILOSTAD 5 mg AMILOSTAD 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amilostad 5 mg: jedna tableta obsahuje amlodipinum 5 mg (jako amlodipini besilas) Amilostad 10 mg: jedna tableta obsahuje amlodipinum 10 mg (jako amlodipini besilas) Úplný seznam pomocných látek viz bod LÉKOVÁ FORMA Tablety Popis přípravku: Amilostad 5 mg: bílé kulaté tablety Amilostad 10 mg: bílé kulaté tablety s půlící rýhou na jedné straně. Tablety lze dělit na dvě stejné poloviny. 4. KLINICKÉ ÚDAJE 4.1 Terapeutické indikace Esenciální hypertenze. Chronická stabilní a vasospastická angina pectoris. 4.2 Dávkování a způsob podání Dospělí V léčbě jak hypertenze, tak anginy pectoris je obvyklá počáteční dávka 5 mg amlodipinu 1krát denně. Pokud není cíleného terapeutického efektu dosaženo během 2 až 4 týdnů, může být tato dávka v závislosti na individuální odpovědi pacienta zvýšena až na maximální denní dávku 10 mg (jako jedna dávka). Amlodipin může být užíván buď v monoterapii nebo v kombinaci s jinými léky na anginu pectoris. Děti s hypertenzí ve věku od 6 do 17 let Doporučená antihypertenzivní perorální zahajovací dávka u pediatrických pacientů ve věku 6 až 17 let je 2,5 mg užívaných jednou denně. Pokud není cíleného terapeutického účinku dosaženo po 4 týdnech léčby, může být tato dávka zvýšena až na 5 mg. Denní dávky vyšší než 5 mg nebyly u pediatrických pacientů studovány (viz body 5.1. a 5.2.). Účinek amlodipinu na krevní tlak u pacientů do 6 let není známý. Dávky 2,5 mg není možné s přípravkem Amilostad 5 mg dosáhnout, jelikož tyto tablety nejsou vyráběny s půlící rýhou, která by umožnila rozdělení tablety na dvě stejné poloviny. Starší pacienti U starších nemocných se doporučuje užít obvyklé dávkování, ale je potřeba opatrnosti při zvyšování dávek (viz bod 5.2). 1/7
2 Pacienti s renálním poškozením U těchto pacientů lze užít amlodipin v normálním dávkování (viz bod 5.2). U pacientů podrobujících se dialýze musí být podáván se zvláštní opatrností. Amlodipin není dialyzovatelný. Pacienti s jaterním poškozením Dávkovací schéma pro pacienty s jaterním poškozením nebylo stanoveno a proto je potřeba při podávání amlodipinu těmto pacientům zvýšené opatrnosti (viz bod 4.4). Tablety musí být zapity sklenicí vody, mohou být užívány nezávisle na příjmu potravy. 4.3 Kontraindikace Amlodipin je kontraindikován u pacientů: - s přecitlivělostí na deriváty dihydropyridinu, amlodipin, nebo na jakoukoli pomocnou látku - se závažnou hypotenzí - v šoku, včetně kardiogenního šoku - s obstrukcí levokomorového odtoku (např. aortální stenóza vysokého stupně) - s hemodynamicky nestabilním srdečním selháním po akutním infarktu myokardu 4.4 Zvláštní upozornění a opatření pro použití Bezpečnost a účinnost amlodipinu u hypertenzních krizí nebyla prokázána. Pacienti se srdečním selháním Tito pacienti musí být léčeni s opatrností. V dlouhodobé placebem kontrolované studii s amlodipinem u nemocných se závažným srdečním selháním (NYHA stupeň III a IV) byl u pacientů léčených amlodipinem hlášen vyšší výskyt plicního edému než u skupiny užívající placebo, ale nebyla zjištěna žádná souvislost se zhoršením srdečního selhání (viz bod 5.1). Užití u pacientů se zhoršenou funkcí jater Plazmatický poločas vylučování amlodipinu je u nemocných se sníženou funkcí jater prodloužen. Dávkovací schéma u těchto pacientů nebylo stanoveno. V těchto případech je třeba podávat amlodipin s mimořádnou opatrností. Užití u starších pacientů U těchto pacientů je třeba opatrnosti při zvyšování dávek (viz bod 5.2). Užití u pacientů s ledvinovým selháním Amlodipin může být u těchto pacientů v normálních dávkách použit. Změny koncentrací amlodipinu v plazmě nekorelují se stupněm renálního poškození. Amlodipin není dialyzovatelný. 4.5 Interakce s jinými léčivými přípravky a jiné formy interakce Účinky jiných léků na amlodipin Inhibitory CYP3A4: Při současném užívání s inhibitorem CYP3A erytromycinem u mladých pacientů a diltiazemem u starších pacientů se zvýšila plazmatická koncentrace amlodipinu o 22% a 50%. Přesto, klinický význam těchto zjištění není jasný. Není vyloučeno, že silné inhibitory CYP3A4 (např. ketokonazol, itrakonazol, ritonavir) mohou zvýšit plazmatickou koncentraci amlodipinu ve větším rozsahu než diltiazem. Proto je nutná při kombinaci amlodipinu s CYP3A4 inhibitory opatrnost. Žádné nežádoucí účinky odpovídající této interakci nebyly hlášeny. Induktory CYP3A4: Účinek CYP3A4 induktorů na amlodipin není znám. Současné užívání induktorů CYP3A4 (např. rifampicin, třezalka) může vést ke snížené plazmatické koncentraci amlodipinu. Proto při kombinaci amlodipinu s CYP3A4 induktory je nutná opatrnost. 2/7
3 V klinických interakčních studiích grapefruitová šťáva, cimetidin, antacida s hliníkem a hořčíkem a sildenafil neměly vliv na farmakokinetiku amlodipinu. Účinek amlodipinu na jiné léky Amlodipin může zesílit účinek jiných antihypertenziv. V klinických interakčních studiích amlodipin neovlivnil farmakokinetiku atorvastatinu, digoxinu, etanolu (alkoholu), warfarinu a cyklosporinu. Amlodipin neměl vliv na laboratorní testy. 4.6 Fertilita, těhotenství a kojení Těhotenství Bezpečnost amlodipinu u těhotných žen nebyla ověřena. Reprodukční studie u potkanů neprokázaly toxicitu, s výjimkou opožděného a prodlouženého porodu v dávkách 50x vyšších než je maximální doporučená dávka pro člověka. Užití v těhotenství je doporučeno pouze tehdy, kdy není k dispozici bezpečnější alternativa a kdy onemocnění samo znamená větší riziko pro matku a plod než léčba. Kojení Není známo, zda amlodipin přechází do mateřského mléka. Rozhodnutí zda pokračovat/přerušit kojení nebo pokračovat/přerušit léčbu amlodipinem záleží na posouzení přínosu kojení pro dítě a léčby pro matku. 4.7 Účinky na schopnost řídit a obsluhovat stroje Amlodipin má zanedbatelný nebo malý vliv na schopnost řídit a ovládat stroje. Pokud se u pacienta užívajícího amlodipin objeví závratě, bolest hlavy, únava nebo nevolnost, může být poškozena schopnost rychlé reakce. 4.8 Nežádoucí účinky Následující nežádoucí účinky byly pozorovány a hlášeny při léčbě amlodipinem s následující frekvencí: Velmi časté ( 1/10); časté ( 1/100 až < 1/10); méně časté ( 1/1 000 až < 1/100); vzácné ( 1/ až < 1/1 000); velmi vzácné (< 1/10 000). Orgánový systém Frekvence Nežádoucí účinek Poruchy krve a lymfatického Velmi vzácné Leukocytopénie, trombocytopénie systému Poruchy imunitního systému Velmi vzácné Alergické reakce Poruchy metabolismu a Velmi vzácné Hyperglykémie výživy Psychiatrické poruchy Insomnie, změny nálady (včetně úzkosti), deprese Vzácné Zmatenost Poruchy nervového systému Časté Velmi vzácné Somnolence, závratě, bolest hlavy (zejména na počátku léčby) Třes, dysgeuzie, synkopa, hypestézie, parestézie Hypertonie, 3/7
4 Periferní neuropatie Poruchy oka Poruchy vidění (včetně diplopie) Poruchy ucha a labyrintu Tinitus Srdeční poruchy Palpitace Velmi vzácné Infarkt myokardu, arytmie (včetně bradykardie, ventrikulární tachykardie a atriální fibrilace) Cévní poruchy Časté Zčervenání Hypotenze Velmi vzácné Vaskulitida Respirační, hrudní a Dyspnoe, rinitida mediastinální poruchy Velmi vzácné Kašel Gastrointestinální poruchy Časté Bolest břicha, nevolnost, Zvracení, dyspepsie, změna činnosti střev (včetně průjmu a zácpy), sucho v ústech Velmi vzácné Pankreatitida, gastritida, hypeplazie dásní Poruchy jater a žlučových cest Velmi vzácné Hepatitida, žloutenka, zvýšená hladina jaterních enzymů* Poruchy kůže a podkožní tkáně Alopecie, purpura, změna barvy pokožky, hyperhydróza, svědění, vyrážka Velmi vzácné Angioedém, erythema multiforme, kopřivka, exfoliativní dermatitida, Stevens-Johnsonův syndrom, Quinckeho edém Velmi vzácné Fotosensitivita Poruchy svalové a kosterní Časté Otok kotníků soustavy a pojivové tkáně Artralgie, myalgie, svalové křeče, bolest zad Poruchy ledvin a močových cest Poruchy reprodukčního systému a prsu Celkové poruchy a reakce v místě aplikace Časté Poruchy močení, nokturie, častější močení Impotence, gynekomastie Edémy, únava Bolest na hrudi, asténie, bolest, slabost Vícenásobná vyšetření Zvýšení nebo snížení tělesné hmotnosti *většinou souvisí s cholestázou 4.9 Předávkování U lidí jsou zkušenosti se záměrným předávkováním omezené. Příznaky: Dostupná data ukazují, že předávkování může způsobit rozsáhlou periferní vasodilataci a možnou reflexní tachykardii. Byla hlášena výrazná a pravděpodobně prolongovaná systémová hypotenze, až šok s fatálním koncem. Léčba Klinicky významná hypotenze v důsledku předávkování amlodipinu vyžaduje aktivní podporu kardiovaskulárních funkcí, včetně monitorování srdeční a respirační funkce, elevace dolních končetin a pozorného sledování cirkulujícího objemu tekutin a objemu vyloučené moči. Při obnově vaskulárního tonu a krevního tlaku mohou být užitečné vasokonstrikční látky, pokud ovšem jejich aplikace není kontraindikována. K potlačení účinku blokátorů kalciových kanálů je užitečné podat intravenózně monohydrát glukonanu vápenatého. 4/7
5 V některých případech je užitečné provést výplach žaludku. Bylo prokázáno, že podání aktivního uhlí zdravým dobrovolníkům během 2 hodin po požití amlodipinu 10 mg významně snižuje absorpci amlodipinu. Vzhledem k tomu, že amlodipin se ve značné míře váže na bílkoviny v plazmě, dialýza nemá při předávkování větší význam. 5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti Farmakoterapeutická skupina: deriváty dihydropyridinu ATC kód: C08CA01 Amlodipin je kalciový antagonista a inhibuje transport kalciových iontů do srdečních buněk a buněk hladkého svalstva. Mechanismus antihypertenzního působení amlodipinu vyplývá z jeho přímého relaxačního účinku na hladké svalstvo cévní stěny. Přesný mechanismus, jímž amlodipin vede k ústupu anginózních bolestí, nebyl dosud zcela poznán, avšak je známo, že amlodipin působí dvěma mechanismy: 1. Amlodipin dilatuje periferní arterioly a tak redukuje celkovou periferní rezistenci (afterload), proti níž musí srdce pracovat. To vede k odlehčení práce srdce a snížení spotřeby energie a kyslíkových nároků v myokardu. 2. Mechanismus účinku amlodipinu zahrnuje pravděpodobně také dilataci hlavních větví koronárních tepen a koronárních arteriol. Důsledkem této dilatace je zlepšená dodávka kyslíku k myokardu u pacientů s Prinzmetalovou anginou pectoris. U nemocných s hypertenzí amlodipin při dávkování 1krát denně klinicky významně snižuje krevní tlak vleže i vestoje po celých 24 hodin. U nemocných s anginou pectoris zvyšuje jedna denní dávka amlodipinu celkovou dobu tolerance fyzické zátěže, oddaluje nástup anginózních bolestí a dobu do vzniku 1 mm depresí úseku ST na EKG a snižuje jak frekvenci agninózních atak, tak spotřebu nitroglycerinu. U nemocných se srdečním selháním Hemodynamické studie a kontrolované klinické studie, při nichž pacienti se srdečním selháním třídy II - IV podle NYHA podstoupili zátěžový test ukázaly, že amlodipin nevede ke zhoršení klinického stavu, hodnoceného pomocí tolerance fyzické zátěže, ejekční frakce levé komory a klinické symptomatologie. Z placebem kontrolované studie (PRAISE) vyplynulo, že u pacientů s chronickým srdečním selháním stupně III-IV dle NYHA léčených digoxinem, diuretiky a inhibitory angiotensin konvertujícího enzymu (ACE) po podání amlodipinu nedošlo ke vzestupu rizika mortality nebo rizika kombinované mortality a morbidity u pacientů se srdečním selháním. Doplňující dlouhodobá, placebem kontrolovaná studie (PRAISE 2) u pacientů se srdečním selháním NYHA III a IV bez klinických příznaků nebo objektivních nálezů ischemického onemocnění, léčených stabilizovanými dávkami ACE inhibitorů, digitalisem a diuretiky ukázala, že amlodipin nemá vliv na celkovou nebo kardiovaskulární úmrtnost pacientů. V této studii bylo užívání amlodipinu spojeno se zvýšeným výskytem plicního edému, i když zhoršení srdečního selhání nebylo při srovnání s placebem zjištěno. Děti Ve studii s 268 dětmi ve věku 6 17 let s převážně sekundární hypertenzí bylo provedeno srovnání dávky 2,5 mg a 5 mg amlodipinu s placebem. Bylo prokázáno, že obě dávky snižují systolický krevní tlak významně více než placebo. Rozdíl mezi dávkami amlodipinu nebyl statisticky významný. 5/7
6 Dlouhodobé účinky amlodipinu na růst, dospívání a celkový vývoj nebyly studovány. Dlouhodobá účinnost léčby amlodipinem u dětí na snížení kardiovaskulární morbidity a mortality v dospělosti také nebyla stanovena. 5.2 Farmakokinetické vlastnosti Absorbce / Distribuce Po perorálním podání v terapeutických dávkách je amlodipin pomalu vstřebáván z gastrointestinálního traktu. Absorpce amlodipinu není ovlivněna současným příjmem potravy. Absolutní biologická dostupnost nezměněné sloučeniny se pohybuje v rozmezí 64-80%. Maximální hladiny v plazmě je dosaženo za 6 až 12 hodin po podání. Distribuční objem je přibližně 20 l/kg, pka amlodipinu je 8,6. Vazba na plazmatické bílkoviny in vitro je přibližně 98%. Metabolizmus /Eliminace Plazmatický eliminační poločas se pohybuje v rozmezí 35 až 50 hodin. Ustálených plazmatických hladin se dosahuje po 7-8 dnech nepřetržitého podávání. Amlodipin je ve značné míře metabolizován na neaktivní metabolity. Močí se vylučuje cca 60% podané dávky, přibližně 10% ve formě nezměněného amlodipinu. Použití u starších osob Doba potřebná k dosažení vrcholových plazmatických koncentrací amlodipinu je u starších a mladších osob obdobná. Clearance amlodipinu může být u starších pacientů snížena spolu se zvýšením AUC a eliminačního poločasu. Zvýšení AUC a eliminačního poločasu u pacientů s kongestivním srdečním selháním bylo u této skupiny pacientů očekáváno (viz bod 4.4.). Použití u dětí a dospívajících Farmakokinetická studie byla provedena u 74 hypertenzních dětí ve věku od 12 měsíců do 17 let (34 pacientů ve věku 6 až 12 let a 28 pacientů 13 až 17 let). Bylo podávána dávka mezi 1,25 a 20 mg buď jednou nebo dvakrát denně. U dětí ve věku 6 až 12 let a u dospívajících 13 až 17 let byla typická perorální clearance (CL/F) 22,5 a 27,4 l/hod, u chlapců 16,4 l/hod a 21,3 l/hod u dívek. U jednotlivců byla sledována velká variabilita expozice. Údaje o dětech do 6 let jsou omezené. Použití u pacientů s porušenou renální funkcí Amlodipin je rozsáhle metabolizován na neaktivní metabolity. 10% aktivní látky je vyloučeno nezměněno močí. Změny v plazmatických koncentracích amlodipinu nesouvisejí se stupněm renálního postižení. Těmto pacientům může být amlodipin podáván v normálních dávkách. Amlodipin není dialyzovatelný. Použití u pacientů s porušenou jaterní funkcí Poločas amlodipinu je u pacientů s porušenou jaterní funkcí prodloužen. 5.3 Předklinické údaje vztahující se k bezpečnosti Předklinické údaje založené na konvenčních studiích bezpečnosti, toxicity po opakovaném podání, genotoxicity a karcinogenního potenciálu neukazují žádná zvláštní rizika pro člověka. Ve studiích reprodukční toxicity u potkanů bylo pozorováno při vysokých dávkách zpoždění porodu, ztížený porod a snížení přežití plodů a mláďat. 6. FARMACEUTICKÉ ÚDAJE 6.1 Seznam pomocných látek Mikrokrystalická celulosa, hydrogenfosforečnan vápenatý, sodná sůl karboxymethylšrobu, magnesium-stearát 6/7
7 6.2 Inkompatibility Neuplatňuje se. 6.3 Doba použitelnosti 5 let 6.4 Zvláštní opatření pro uchovávání Uchovávat v původním obalu, aby byl přípravek chráněn před světlem. 6.5 Druh obalu a velikost balení AMILOSTAD 5 mg PVC/PE/PVDC/ Al blistr: Velikost balení: 7, 10, 14, 15, 20, 28, 30, 50, 56, 60, 98, 100, 200 tablet AMILOSTAD 10 MG PVC/PE/PVDC/ Al blistr Velikost balení: 7, 10, 14, 15, 20, 28, 30, 50, 56, 60, 98, 100 tablet Ne všechny velikosti balení musí být obchodovány. 6.6 Zvláštní opatření pro likvidaci přípravku Žádné zvláštní požadavky. 7. DRŽITEL ROZHODNUTÍ O REGISTRACI STADA Arzneimittel AG Stadastrasse Bad Vilbel Německo 8. REGISTRAČNÍ ČÍSLA Amilostad 5 mg: 83/166/07-C Amilostad 10 mg: 83/167/07-C 9. DATUM PRVNÍ REGISTRACE / PRODLOUŽENÍ REGISTRACE / DATUM REVIZE TEXTU /7
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls84143/2011, sukls84154/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls84143/2011, sukls84154/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RECOTENS 5 mg RECOTENS 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls84143/2011, sukls84154/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RECOTENS 5 mg RECOTENS 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls123718/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlodipin Mylan 5 mg tablety Amlodipin Mylan 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls123718/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlodipin Mylan 5 mg tablety Amlodipin Mylan 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls178202/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AFITEN 5 mg AFITEN 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ AFITEN 5 mg: Jedna tableta obsahuje amlodipinum 5 mg (ve formě
sp.zn.sukls178202/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AFITEN 5 mg AFITEN 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ AFITEN 5 mg: Jedna tableta obsahuje amlodipinum 5 mg (ve formě
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sukls243257-58/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU APO-AMLO 5 APO-AMLO 10 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ APO-AMLO 5: jedna tableta
Příloha č. 2 k rozhodnutí o změně registrace sukls243257-58/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU APO-AMLO 5 APO-AMLO 10 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ APO-AMLO 5: jedna tableta
Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls80342/2012
 Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls80342/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AMLODIPIN ACCORD 5 mg tablety AMLODIPIN ACCORD 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 3 k rozhodnutí o změně registrace sp.zn. sukls80342/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AMLODIPIN ACCORD 5 mg tablety AMLODIPIN ACCORD 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls148009-10/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Orcal Neo 5 mg, tablety Orcal Neo 10 mg, tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn. sukls148009-10/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Orcal Neo 5 mg, tablety Orcal Neo 10 mg, tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls173202/2010 1. NÁZEV PŘÍPRAVKU GENAM 5 mg GENAM 10 mg Tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Genam 5 mg: jedna
Příloha č. 2 k rozhodnutí o změně registrace sp. zn. sukls173202/2010 1. NÁZEV PŘÍPRAVKU GENAM 5 mg GENAM 10 mg Tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Genam 5 mg: jedna
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls231660/2010, sukls231662/2010 Příloha k sp.zn. sukls91955/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AGEN 5 AGEN 10 tablety 2. KVALITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls231660/2010, sukls231662/2010 Příloha k sp.zn. sukls91955/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AGEN 5 AGEN 10 tablety 2. KVALITATIVNÍ
Pomocná látka se známým účinkem: Jedna tableta obsahuje 75 mg monohydrátu laktosy. Úplný seznam pomocných látek viz bod 6.1.
 sp.zn.: sukls81995/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Loratadin-ratiopharm 10 mg Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se
sp.zn.: sukls81995/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Loratadin-ratiopharm 10 mg Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls179122/2011, sukls179170/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls179122/2011, sukls179170/2011 1. NÁZEV PŘÍPRAVKU Nitresan 10 mg Nitresan 20 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls179122/2011, sukls179170/2011 1. NÁZEV PŘÍPRAVKU Nitresan 10 mg Nitresan 20 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č.3 k rozhodnutí o změně registrace sp.zn.sukls98466/2010 a příloha k sp.zn.sukls164928/2009, sukls164929/2009
 Příloha č.3 k rozhodnutí o změně registrace sp.zn.sukls98466/2010 a příloha k sp.zn.sukls164928/2009, sukls164929/2009 1. NÁZEV PŘÍPRAVKU Kapidin 10 mg Kapidin 20 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU
Příloha č.3 k rozhodnutí o změně registrace sp.zn.sukls98466/2010 a příloha k sp.zn.sukls164928/2009, sukls164929/2009 1. NÁZEV PŘÍPRAVKU Kapidin 10 mg Kapidin 20 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp. zn. sukls211402/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alfuzostad 10 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje alfuzosini hydrochloridum10
sp. zn. sukls211402/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alfuzostad 10 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje alfuzosini hydrochloridum10
SOUHRN ÚDAJŮ O PŘÍPRAVKU. AMILOSTAD 5 mg AMILOSTAD 10 mg tablety
 Příloha č.2 k rozhodnutí o změnu registrace sp. zn. sukls42236/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU AMILOSTAD 5 mg AMILOSTAD 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amilostad
Příloha č.2 k rozhodnutí o změnu registrace sp. zn. sukls42236/2012 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU AMILOSTAD 5 mg AMILOSTAD 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amilostad
Tableta s prodlouženým uvolňováním. Popis přípravku : bílé, kulaté, nepotahované tablety se zkosenými hranami.
 Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls37077/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alfuzostad 10 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č.2 k rozhodnutí o změně registrace sp. zn. sukls37077/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Alfuzostad 10 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls42776/2010 a sukls62504/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlozek 5 Amlozek 10 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls42776/2010 a sukls62504/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlozek 5 Amlozek 10 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls229853/2012, sukls229854/2012 1. NÁZEV PŘÍPRAVKU Amlozek 5 tablety Amlozek 10 tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipini besilas
sp.zn. sukls229853/2012, sukls229854/2012 1. NÁZEV PŘÍPRAVKU Amlozek 5 tablety Amlozek 10 tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipini besilas
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn.:sukls32256/2007, sukls32257/2007
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn.:sukls32256/2007, sukls32257/2007 1. NÁZEV PŘÍPRAVKU UNIPRES 10 UNIPRES 20 tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn.:sukls32256/2007, sukls32257/2007 1. NÁZEV PŘÍPRAVKU UNIPRES 10 UNIPRES 20 tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
3 LÉKOVÁ FORMA Tableta s prodlouženým uvolňováním. Růžové, kulaté bikonvexní tablety s vyraženým '35' na jedné straně, na druhé straně hladké.
 Příloha č. 3 k rozhodnutí o registraci sp.zn.sukls200469/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV LÉČIVÉHO PŘÍPRAVKU Portora 35 mg tablety s prodlouženým uvolňováním 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č. 3 k rozhodnutí o registraci sp.zn.sukls200469/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 NÁZEV LÉČIVÉHO PŘÍPRAVKU Portora 35 mg tablety s prodlouženým uvolňováním 2 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
AGEN 5 AGEN 10 Tablety (Amlodipinum)
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls231660/2010, sukls231662/2010 Příloha k sp.zn. sukls91955/2011, sukls85224/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE AGEN 5 AGEN
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls231660/2010, sukls231662/2010 Příloha k sp.zn. sukls91955/2011, sukls85224/2011 PŘÍBALOVÁ INFORMACE - INFORMACE PRO UŽIVATELE AGEN 5 AGEN
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Normodipine 5 mg, tablety Normodipine 10 mg, tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Normodipine 5 mg, tablety: Jedna tableta obsahuje amlodipini besilas
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Normodipine 5 mg, tablety Normodipine 10 mg, tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Normodipine 5 mg, tablety: Jedna tableta obsahuje amlodipini besilas
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ZOREM 5 mg ZOREM 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipini besilas odpovídající amlodipinum 5 mg. Jedna tableta
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ZOREM 5 mg ZOREM 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipini besilas odpovídající amlodipinum 5 mg. Jedna tableta
Jedna tableta obsahuje amlodipini besilas odpovídající amlodipinum 5 mg. Jedna tableta obsahuje amlodipini besilas odpovídající amlodipinum 10 mg.
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls86953/2012 a příloha k sp. zn.sukls82184/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ZOREM 5 mg ZOREM 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls86953/2012 a příloha k sp. zn.sukls82184/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ZOREM 5 mg ZOREM 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
Příloha č. 3 k rozhodnutí o převodu registrace sp.zn. sukls62363/2011 a sukls62355/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Procto-Glyvenol 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky:Tribenosidum
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jedna tableta obsahuje amlodipinum 5 mg nebo 10 mg (ve formě amlodipini besilas)
 sp.zn.sukls79714/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlodipin Vitabalans 5 mg Amlodipin Vitabalans 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipinum
sp.zn.sukls79714/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlodipin Vitabalans 5 mg Amlodipin Vitabalans 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls120670/2012, sukls120664/2012 a sukls42302/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU HIPRES 5 HIPRES 10 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Hipres 5: Amlodipini maleas 6,42
sp.zn. sukls120670/2012, sukls120664/2012 a sukls42302/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU HIPRES 5 HIPRES 10 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Hipres 5: Amlodipini maleas 6,42
Jedna tableta s prodlouženým uvolňováním obsahuje 0,4 mg tamsulosini hydrochloridum, což odpovídá 0,367 mg tamsulosinum.
 sp.zn.sukls48957/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Tamsulosin HCl Teva 0,4 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním
sp.zn.sukls48957/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Tamsulosin HCl Teva 0,4 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta s prodlouženým uvolňováním
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Agen 5: Jedna tableta obsahuje amlodipini besilas 6,935 mg, což odpovídá 5 mg amlodipinum.
 Sp.zn. sukls40780/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AGEN 5 AGEN 10 5mg 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Agen 5: Jedna tableta obsahuje amlodipini besilas 6,935 mg, což
Sp.zn. sukls40780/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AGEN 5 AGEN 10 5mg 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Agen 5: Jedna tableta obsahuje amlodipini besilas 6,935 mg, což
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 400 mg + 40 mg. čípky PROCTO-GLYVENOL. 50 mg/g + 20 mg/g. rektální krém
 sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
sp.zn. sukls74884/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PROCTO-GLYVENOL 400 mg + 40 mg čípky PROCTO-GLYVENOL 50 mg/g + 20 mg/g rektální krém 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Čípky: Jeden
AMLOZEK 5 mg tablety AMLOZEK 10 mg tablety
 Sp.zn. sukls202938/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AMLOZEK 5 mg tablety AMLOZEK 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipinum 5 mg odpovídající
Sp.zn. sukls202938/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AMLOZEK 5 mg tablety AMLOZEK 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipinum 5 mg odpovídající
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn. sukls93011/2018, sukls93051/2018 a sukls47865/2018 1. NÁZEV PŘÍPRAVKU Amlodipin Aurovitas 5 mg tablety Amlodipin Aurovitas 10 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ
Sp.zn. sukls93011/2018, sukls93051/2018 a sukls47865/2018 1. NÁZEV PŘÍPRAVKU Amlodipin Aurovitas 5 mg tablety Amlodipin Aurovitas 10 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Příloha č. 2 k rozhodnutí o prodloužení registrace sp.zn. sukls17735/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GUAJACURAN 5% injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Guaifenesinum
Torella 5 mg, tablety Torella 10 mg, tablety
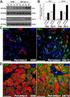 Příloha č. 2 ke sdělení sp.zn. sukls161411, sukls161423 PŘÍBALOVÁ INFORMACE Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci pro
Příloha č. 2 ke sdělení sp.zn. sukls161411, sukls161423 PŘÍBALOVÁ INFORMACE Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat. Ponechte si příbalovou informaci pro
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls42776/2010 a sukls62504/2010. Příbalová informace : informace pro uživatele
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls42776/2010 a sukls62504/2010 Příbalová informace : informace pro uživatele Amlozek 5 Amlozek 10 Tablety Amlodipinum Přečtěte si pozorně celou příbalovou
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls42776/2010 a sukls62504/2010 Příbalová informace : informace pro uživatele Amlozek 5 Amlozek 10 Tablety Amlodipinum Přečtěte si pozorně celou příbalovou
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Pomocné látky se známým účinkem: Jedna tableta obsahuje 28 mg laktosy a 5 mg glyceromakrogol-hydroxystearátu.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PLENDIL ER 5 mg PLENDIL ER 10 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje felodipinum 5,0 mg. Pomocné látky se známým účinkem: Jedna tableta
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PLENDIL ER 5 mg PLENDIL ER 10 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje felodipinum 5,0 mg. Pomocné látky se známým účinkem: Jedna tableta
sp. zn. sukls178963/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FAMOSAN 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
 sp. zn. sukls178963/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FAMOSAN 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje famotidinum 10 mg. Pomocné
sp. zn. sukls178963/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU FAMOSAN 10 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje famotidinum 10 mg. Pomocné
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ZOREM 5 mg tablety ZOREM 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipini besilas odpovídající amlodipinum 5 mg. Jedna
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ZOREM 5 mg tablety ZOREM 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipini besilas odpovídající amlodipinum 5 mg. Jedna
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp. zn. sukls32844/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU APO-AMLO 5 APO-AMLO 10 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ APO-AMLO 5: jedna tableta obsahuje amlodipini besilas odpovídající
Sp. zn. sukls32844/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU APO-AMLO 5 APO-AMLO 10 tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ APO-AMLO 5: jedna tableta obsahuje amlodipini besilas odpovídající
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jedna tableta obsahuje amlodipinum 5 mg nebo 10 mg (ve formě amlodipini besilas).
 sp.zn.sukls22819/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlodipin Vitabalans 5 mg Amlodipin Vitabalans 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipinum
sp.zn.sukls22819/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlodipin Vitabalans 5 mg Amlodipin Vitabalans 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls102162/2012 1. NÁZEV PŘÍPRAVKU AGEN 5 AGEN 10 tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipini
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls102162/2012 1. NÁZEV PŘÍPRAVKU AGEN 5 AGEN 10 tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipini
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn. sukls176492/2012 a sukls176495/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Amlodipin Bluefish 5 mg tablety Amlodipin Bluefish 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Sp.zn. sukls176492/2012 a sukls176495/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU Amlodipin Bluefish 5 mg tablety Amlodipin Bluefish 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Jedna tableta obsahuje 10 mg loratadinum. Jedna 10 mg tableta loratadinu obsahuje 71,3 mg monohydrátu laktosy.
 sp.zn. sukls138016/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 10 mg loratadinum. Jedna 10 mg tableta loratadinu obsahuje
sp.zn. sukls138016/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE Tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje 10 mg loratadinum. Jedna 10 mg tableta loratadinu obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls144430/2014 1. Název přípravku Ebrantil 30 retard Ebrantil 60 retard Tvrdé tobolky s prodlouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. Kvalitativní a kvantitativní složení Jedna tobolka
sp.zn. sukls144430/2014 1. Název přípravku Ebrantil 30 retard Ebrantil 60 retard Tvrdé tobolky s prodlouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. Kvalitativní a kvantitativní složení Jedna tobolka
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin +pharma 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin +pharma 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum v množství 5 mg. Úplný seznam pomocných
1/11. Sp. zn. sukls126328/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU. AMLORATIO 5 mg AMLORATIO 10 mg. tablety
 Sp. zn. sukls126328/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AMLORATIO 5 mg AMLORATIO 10 mg tablety 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Amlodipini besilas Amloratio 5 mg 1 tableta
Sp. zn. sukls126328/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AMLORATIO 5 mg AMLORATIO 10 mg tablety 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Amlodipini besilas Amloratio 5 mg 1 tableta
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
Příloha č. 3 k rozhodnutí o registraci sp.zn. sukls187009/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU ARTAXIN 625 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje glucosaminum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls63588/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Claritine 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se známým účinkem:
sp.zn.sukls63588/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Claritine 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje loratadinum 10 mg. Pomocná látka se známým účinkem:
Sp.zn. sukls288358/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU. Amlodipin Mylan 5 mg tablety Amlodipin Mylan 10 mg tablety
 Sp.zn. sukls288358/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlodipin Mylan 5 mg tablety Amlodipin Mylan 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipinum
Sp.zn. sukls288358/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Amlodipin Mylan 5 mg tablety Amlodipin Mylan 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje amlodipinum
sp.zn.: sukls132182/2010 a sp.zn.: sukls82396/2014
 sp.zn.: sukls132182/2010 a sp.zn.: sukls82396/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MYTELASE tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ambenonii chloridum 10 mg v 1 tabletě. Pomocné látky
sp.zn.: sukls132182/2010 a sp.zn.: sukls82396/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MYTELASE tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Ambenonii chloridum 10 mg v 1 tabletě. Pomocné látky
Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls198549/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls198549/2010 1. NÁZEV PŘÍPRAVKU LANBICA 50 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 potahovaná
Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls198549/2010 1. NÁZEV PŘÍPRAVKU LANBICA 50 mg Potahované tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 potahovaná
SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ. Trimetazidini dihydrochloridum 35 mg v jedné tabletě s řízeným uvolňováním.
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Angizidine 35 mg, tablety s řízeným uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Trimetazidini dihydrochloridum 35 mg v jedné tabletě s řízeným uvolňováním.
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Angizidine 35 mg, tablety s řízeným uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Trimetazidini dihydrochloridum 35 mg v jedné tabletě s řízeným uvolňováním.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU XATRAL UNO tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Alfuzosini hydrochloridum 10 mg v jedné tabletě. Úplný seznam
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU XATRAL UNO tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: Alfuzosini hydrochloridum 10 mg v jedné tabletě. Úplný seznam
Desloratadin STADA 5 mg jsou modré, kulaté, bikonvexní potahované tablety o průměru přibližně 6,5 mm.
 Sp.zn.sukls74932/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin STADA 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje desloratadinum 5 mg.
Sp.zn.sukls74932/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Desloratadin STADA 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje desloratadinum 5 mg.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU DOXIUM 500 500 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 tvrdá tobolka obsahuje calcii dobesilas monohydricus 500 mg. Úplný seznam pomocných
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU DOXIUM 500 500 mg, tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 tvrdá tobolka obsahuje calcii dobesilas monohydricus 500 mg. Úplný seznam pomocných
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn.sukls10638/2011 a příloha k sp.zn. sukls246529/2010, sukls242130/2011, sukls46873/2012
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn.sukls10638/2011 a příloha k sp.zn. sukls246529/2010, sukls242130/2011, sukls46873/2012 1. NÁZEV PŘÍPRAVKU Ewofex 120 mg potahované tablety SOUHRN
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn.sukls10638/2011 a příloha k sp.zn. sukls246529/2010, sukls242130/2011, sukls46873/2012 1. NÁZEV PŘÍPRAVKU Ewofex 120 mg potahované tablety SOUHRN
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls40472/2007
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls40472/2007 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU D I A C O R D I N 60 tablety 2. SLOŽENÍ KVALITATIVNÍ I KVANTITATIVNÍ Léčivá látka:
Příloha č. 3 k rozhodnutí o prodloužení registrace sp. zn.:sukls40472/2007 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU D I A C O R D I N 60 tablety 2. SLOŽENÍ KVALITATIVNÍ I KVANTITATIVNÍ Léčivá látka:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn.sukls40560/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Claritine 1mg/ml sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml sirupu obsahuje loratadinum 1 mg. Pomocná látka se známým účinkem:
sp.zn.sukls40560/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Claritine 1mg/ml sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml sirupu obsahuje loratadinum 1 mg. Pomocná látka se známým účinkem:
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Normodipine 5 mg tablety Normodipine 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Normodipine 5 mg: Jedna tableta obsahuje amlodipinum 5 mg ve formě
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Normodipine 5 mg tablety Normodipine 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Normodipine 5 mg: Jedna tableta obsahuje amlodipinum 5 mg ve formě
Bezpečnost a účinnost přípravku Neoclarityn 5 mg potahované tablety u dětí mladších 12 let nebyla dosud stanovena. Nejsou dostupné žádné údaje.
 1. NÁZEV PŘÍPRAVKU Neoclarityn 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum 5 mg. Pomocná látka se známým účinkem: Tento přípravek obsahuje laktózu.
1. NÁZEV PŘÍPRAVKU Neoclarityn 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje desloratadinum 5 mg. Pomocná látka se známým účinkem: Tento přípravek obsahuje laktózu.
Příloha č. 2 k rozhodnutí o prodloužení registrace sp. zn. sukls38977-78/2011 a příloha k sp. zn. sukls30132/2012
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp. zn. sukls38977-78/2011 a příloha k sp. zn. sukls30132/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA AMLORATIO 5 mg AMLORATIO 10 mg tablety (Amlodipini
Příloha č. 2 k rozhodnutí o prodloužení registrace sp. zn. sukls38977-78/2011 a příloha k sp. zn. sukls30132/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO PACIENTA AMLORATIO 5 mg AMLORATIO 10 mg tablety (Amlodipini
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls193313/2014 1. NÁZEV PŘÍPRAVKU TAMALIS 10 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje: rupatadinum 10 mg (ve formě fumarátu) Pomocné látky
Sp.zn.sukls193313/2014 1. NÁZEV PŘÍPRAVKU TAMALIS 10 mg tablety SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje: rupatadinum 10 mg (ve formě fumarátu) Pomocné látky
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AFITEN 5 mg AFITEN 10 mg tablety amlodipinum
 Příloha č. 2 k rozhodnutí o prodloužení registrace sp. zn. sukls234496-7/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AFITEN 5 mg AFITEN 10 mg tablety amlodipinum Přečtěte si pozorně celou příbalovou
Příloha č. 2 k rozhodnutí o prodloužení registrace sp. zn. sukls234496-7/2010 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE AFITEN 5 mg AFITEN 10 mg tablety amlodipinum Přečtěte si pozorně celou příbalovou
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE. APO-AMLO 5 APO-AMLO 10 tablety (amlodipinum)
 Příloha č. 1 k rozhodnutí o změně registrace sukls243257-58/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-AMLO 5 APO-AMLO 10 tablety (amlodipinum) Přečtěte si pozorně celou příbalovou informaci
Příloha č. 1 k rozhodnutí o změně registrace sukls243257-58/2009 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE APO-AMLO 5 APO-AMLO 10 tablety (amlodipinum) Přečtěte si pozorně celou příbalovou informaci
Vesicare 5 mg potahované tablety
 Sp. zn. sukls74933/2013 SOUHR ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vesicare 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vesicare 5 mg, potahované tablety: Jedna tableta obsahuje 5 mg
Sp. zn. sukls74933/2013 SOUHR ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Vesicare 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Vesicare 5 mg, potahované tablety: Jedna tableta obsahuje 5 mg
Celkové shrnutí vědeckého hodnocení přípravku Norvasc a přípravků souvisejících názvů (viz příloha I)
 PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV V SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÉ INFORMACI PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY Vědecké závěry Celkové
PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV V SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÉ INFORMACI PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY Vědecké závěry Celkové
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls30063/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU. Chondrostad 1500 mg
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls30063/2010 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Chondrostad 1500 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje 1884,0 mg
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls30063/2010 1. NÁZEV PŘÍPRAVKU SOUHRN ÚDAJŮ O PŘÍPRAVKU Chondrostad 1500 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden sáček obsahuje 1884,0 mg
Příbalová informace: informace pro uživatele. Cardilopin 2,5 mg Cardilopin 5 mg Cardilopin 10 mg tablety amlodipinum
 sp.zn. sukls180582/2014 Příbalová informace: informace pro uživatele Cardilopin 2,5 mg Cardilopin 5 mg Cardilopin 10 mg tablety amlodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
sp.zn. sukls180582/2014 Příbalová informace: informace pro uživatele Cardilopin 2,5 mg Cardilopin 5 mg Cardilopin 10 mg tablety amlodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn. sukls8496/2013 a sukls8497/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AMLODIPIN ACCORD 5 mg tablety AMLODIPIN ACCORD 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amlodipin Accord
Sp.zn. sukls8496/2013 a sukls8497/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU AMLODIPIN ACCORD 5 mg tablety AMLODIPIN ACCORD 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Amlodipin Accord
Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls74848/2010
 Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls74848/2010 1. NÁZEV PŘÍPRAVKU MONO MACK DEPOT MONO MACK 50 D tablety s proslouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 3 k rozhodnutí o převodu registrace sp. zn. sukls74848/2010 1. NÁZEV PŘÍPRAVKU MONO MACK DEPOT MONO MACK 50 D tablety s proslouženým uvolňováním SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ
Příloha č. 3 ke sdělení sp.zn.sukls58816/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 ke sdělení sp.zn.sukls58816/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREDUCTAL MR tablety s řízeným uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Trimetazidini dihydrochloridum
Příloha č. 3 ke sdělení sp.zn.sukls58816/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREDUCTAL MR tablety s řízeným uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Trimetazidini dihydrochloridum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls243280/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Dorsiflex 200 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje mephenoxalonum 200 mg. Úplný seznam pomocných
sp.zn. sukls243280/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Dorsiflex 200 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje mephenoxalonum 200 mg. Úplný seznam pomocných
Příbalová informace: informace pro uživatele. Normodipine 5 mg, tablety Normodipine 10 mg, tablety Amlodipinum
 Příbalová informace: informace pro uživatele Normodipine 5 mg, tablety Normodipine 10 mg, tablety Amlodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příbalová informace: informace pro uživatele Normodipine 5 mg, tablety Normodipine 10 mg, tablety Amlodipinum Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls122181/2011 a příloha k sp. zn. sukls91704/2011
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls122181/2011 a příloha k sp. zn. sukls91704/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SANDOMIGRAN 0,5 mg obalené tablety 2. KVALITATIVNÍ
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls122181/2011 a příloha k sp. zn. sukls91704/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU SANDOMIGRAN 0,5 mg obalené tablety 2. KVALITATIVNÍ
SOUHRN ÚDAJŮ O PŘÍPRAVKU. 100 ml roztoku obsahuje Hederae helicis folii extractum siccum (4 8 : 1), extrahováno ethanolem 30 % (m/m).
 Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Sp.zn.sukls15900/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Mucoplant břečťanový sirup proti kašli sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 100 ml roztoku obsahuje Hederae helicis folii extractum
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls174437/2011 a příloha ke sp.zn.sukls49144/2012
 Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls174437/2011 a příloha ke sp.zn.sukls49144/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Concor Combi 5 mg/5 mg, tablety Concor Combi 5 mg/10
Příloha č. 1 k rozhodnutí o změně registrace sp.zn. sukls174437/2011 a příloha ke sp.zn.sukls49144/2012 PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE Concor Combi 5 mg/5 mg, tablety Concor Combi 5 mg/10
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn.sukls52362/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Orcal Neo 5 mg Orcal Neo 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Orcal Neo 5 mg Jedna tableta obsahuje amlodipinum 5 mg (ve
Sp.zn.sukls52362/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Orcal Neo 5 mg Orcal Neo 10 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Orcal Neo 5 mg Jedna tableta obsahuje amlodipinum 5 mg (ve
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 sp.zn. sukls197050/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RANISAN 75 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje ranitidini hydrochloridum
sp.zn. sukls197050/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU RANISAN 75 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje ranitidini hydrochloridum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls4008/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LIVOSTIN nosní sprej, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 2.1. Obecný popis sterilní
Příloha č. 2 k rozhodnutí o změně registrace sp.zn.sukls4008/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LIVOSTIN nosní sprej, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 2.1. Obecný popis sterilní
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Sp.zn. sukls79692/2011 1. NÁZEV PŘÍPRAVKU Flonidan 10 mg DISTAB SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Každá dispergovatelná tableta obsahuje loratadinum 10 mg. Pomocné látky:
Sp.zn. sukls79692/2011 1. NÁZEV PŘÍPRAVKU Flonidan 10 mg DISTAB SOUHRN ÚDAJŮ O PŘÍPRAVKU 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Každá dispergovatelná tableta obsahuje loratadinum 10 mg. Pomocné látky:
Sp. zn. sukls6920/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU. 1. NÁZEV PŘÍPRAVKU BETAHISTIN ACTAVIS 16 mg
 Sp. zn. sukls6920/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU BETAHISTIN ACTAVIS 16 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje betahistini dihydrochloridum 16 mg. Pomocná látka
Sp. zn. sukls6920/2013 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU BETAHISTIN ACTAVIS 16 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje betahistini dihydrochloridum 16 mg. Pomocná látka
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Felodipinum 5,0 mg; resp.10,0 mg v jedné tabletě s prodlouženým uvolňováním.
 sp.zn.sukls262139/2012, sukls262138/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PLENDIL ER 5 mg PLENDIL ER 10 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Felodipinum 5,0 mg; resp.10,0 mg v jedné tabletě
sp.zn.sukls262139/2012, sukls262138/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PLENDIL ER 5 mg PLENDIL ER 10 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Felodipinum 5,0 mg; resp.10,0 mg v jedné tabletě
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls115710/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLYPRESSIN 1 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna ampule s 8,5 ml
Příloha č. 3 k rozhodnutí o registraci sp. zn. sukls115710/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLYPRESSIN 1 mg injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna ampule s 8,5 ml
Jedna potahovaná tableta obsahuje levocetirizini dihydrochloridum 5 mg (což odpovídá 4,2 mg levocetirizinum).
 Sp.zn.sukls82355/2012 SOUHRN ÚDAJU O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Levocetirizin Actavis 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje levocetirizini
Sp.zn.sukls82355/2012 SOUHRN ÚDAJU O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Levocetirizin Actavis 5 mg potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná tableta obsahuje levocetirizini
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE Sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml sirupu obsahuje 1 mg loratadinum. Jeden ml loratadinového sirupu obsahuje 600 mg sacharosy.
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE Sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jeden ml sirupu obsahuje 1 mg loratadinum. Jeden ml loratadinového sirupu obsahuje 600 mg sacharosy.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU Borgal 200/40 mg/ml injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ 1 ml obsahuje: Léčivé látky: Sulfadoxinum 200 mg Trimethoprimum
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls52815/2009
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls52815/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LEVOPRONT sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: levodropropizinum
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls52815/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU LEVOPRONT sirup 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivá látka: levodropropizinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Tablety: Jedna tableta obsahuje 10 mg loratadinum. Sirup: Jeden ml sirupu obsahuje 1 mg loratadinum. Pomocné
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CLARITINE 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Tablety: Jedna tableta obsahuje 10 mg loratadinum. Sirup: Jeden ml sirupu obsahuje 1 mg loratadinum. Pomocné
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls106353/2011
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls106353/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRVKU Lopacut 2 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls106353/2011 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRVKU Lopacut 2 mg, potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje
Příloha č.3 k rozhodnutí o prodloužení registrace sp.zn. sukls131383/2009 a příloha ke sp.zn. sukls85044/2008, sukls33584/2011
 Příloha č.3 k rozhodnutí o prodloužení registrace sp.zn. sukls131383/2009 a příloha ke sp.zn. sukls85044/2008, sukls33584/2011 1. NÁZEV PŘÍPRAVKU XATRAL 5-SR tablety s prodlouženým uvolňováním SOUHRN ÚDAJŮ
Příloha č.3 k rozhodnutí o prodloužení registrace sp.zn. sukls131383/2009 a příloha ke sp.zn. sukls85044/2008, sukls33584/2011 1. NÁZEV PŘÍPRAVKU XATRAL 5-SR tablety s prodlouženým uvolňováním SOUHRN ÚDAJŮ
Dospělí: Jeden čípek ráno, večer a po každém vyprázdnění střev. Zavést do rekta zaobleným koncem.
 sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
sp.zn. sukls186765/2014 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PREPARATION H čípky 23 mg / 69 mg 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Léčivé látky: Faecis extractum fluidum 1,00 % hmot., t.j. 23
Sp.zn.sukls133113/2016 a sp.zn.sukls133117/2016
 Sp.zn.sukls133113/2016 a sp.zn.sukls133117/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NITRESAN 10 mg NITRESAN 20 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Nitresan 10 mg: jedna tableta obsahuje
Sp.zn.sukls133113/2016 a sp.zn.sukls133117/2016 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU NITRESAN 10 mg NITRESAN 20 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Nitresan 10 mg: jedna tableta obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 1 ke sdělení sp.zn. sukls238164/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORVATON retard tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: molsidominum
Příloha č. 1 ke sdělení sp.zn. sukls238164/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU CORVATON retard tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ I KVANTITATIVNÍ SLOŽENÍ Léčivá látka: molsidominum
Gynekologie: Metroragie, primární menoragie nebo menoragie související s nitroděložním tělískem bez prokazatelné organické příčiny.
 Sp.zn.sukls81671/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Cyclonamine 500 mg Tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje etamsylatum 500 mg. Léčivý přípravek obsahuje
Sp.zn.sukls81671/2015 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Cyclonamine 500 mg Tvrdé tobolky 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje etamsylatum 500 mg. Léčivý přípravek obsahuje
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
Příloha č.3 ke sdělení sp.zn.sukls44100/2012 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Fucithalmic oční kapky, suspenze 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Acidum fusidicum hemihydricum 10 mg v 1
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls2006/2007 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PANADOL Rapide potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná
Příloha č. 3 k rozhodnutí o prodloužení registrace sp.zn. sukls2006/2007 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU PANADOL Rapide potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna potahovaná
Jedna tableta obsahuje bisulepini hydrochloridum 2,25 mg (bisulepinum 2 mg).
 sp. zn. sukls298106/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Dithiaden 2 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje bisulepini hydrochloridum 2,25 mg (bisulepinum
sp. zn. sukls298106/2018 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Dithiaden 2 mg tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta obsahuje bisulepini hydrochloridum 2,25 mg (bisulepinum
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU. MOXOSTAD 0,2 mg MOXOSTAD 0,3 mg MOXOSTAD 0,4 mg Potahované tablety
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MOXOSTAD 0,2 mg MOXOSTAD 0,3 mg MOXOSTAD 0,4 mg Potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Moxonidinum 0,2, 0,3 nebo 0,4 mg v 1 potahované tabletě.
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU MOXOSTAD 0,2 mg MOXOSTAD 0,3 mg MOXOSTAD 0,4 mg Potahované tablety 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Moxonidinum 0,2, 0,3 nebo 0,4 mg v 1 potahované tabletě.
SOUHRN ÚDAJŮ O PŘÍPRAVKU
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU XATRAL 5-SR tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Alfuzosini hydrochloridum 5 mg v jedné tabletě Úplný seznam pomocných
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU XATRAL 5-SR tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Alfuzosini hydrochloridum 5 mg v jedné tabletě Úplný seznam pomocných
Světle červené, ploché, kulaté, skvrnité tablety, na jedné straně označené písmenem K.
 1. NÁZEV PŘÍPRAVKU Aerius 2,5 mg tablety dispergovatelné v ústech 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta dispergovatelná v ústech obsahuje desloratadinum 2,5 mg. Pomocné látky se známým
1. NÁZEV PŘÍPRAVKU Aerius 2,5 mg tablety dispergovatelné v ústech 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tableta dispergovatelná v ústech obsahuje desloratadinum 2,5 mg. Pomocné látky se známým
Příloha č.3 k rozhodnutí o registraci sp.zn. sukls48796/2009
 Příloha č.3 k rozhodnutí o registraci sp.zn. sukls48796/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLUCOPHAGE XR 750 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Příloha č.3 k rozhodnutí o registraci sp.zn. sukls48796/2009 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU GLUCOPHAGE XR 750 mg tablety s prodlouženým uvolňováním 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Oranžová tobolka č. 2 (tvrdá želatinová), která obsahuje bílé nebo nažloutlé granule.
 Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls151812/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TAMIPRO 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje 0,4 mg tamsulosini
Příloha č. 2 k rozhodnutí o změně registrace sp.zn. sukls151812/2010 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU TAMIPRO 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna tobolka obsahuje 0,4 mg tamsulosini
