Edukační program o AEAB způsobené PRCA V2. Edukační progam k léčivému přípravku MIRCERA (metoxy-polyetylenglykol-epoetin beta) Příručka lékaře
|
|
|
- Matěj Šmíd
- před 10 lety
- Počet zobrazení:
Transkript
1 Edukační program o AEAB způsobené PRCA V2 Edukační progam k léčivému přípravku MIRCERA (metoxy-polyetylenglykol-epoetin beta) Příručka lékaře Diagnostika a hlášení nežádoucích účinků v souvislosti s užíváním léčivého přípravku MIRCERA Čistá aplazie buněk červené řady způsobená antierytropoetinovými protilátkami v souvislosti s podáváním látek stimulujících erytropoézu
2 Edukační program o AEAB způsobené PRCA V2 OBSAH 1. Přípravek MIRCERA a čistá aplazie buněk červené řady způsobená antierytropoetinovými protilátkami v souvislosti s podáváním látek stimulujících erytropoézu (AEAB způsobená PRCA) 1 2. Co je cílem tohoto edukačního programu? 1 3. Ztráta účinku léčby ESA Pokud ESA ztratí svoji účinnost po předchozím prokázaném účinku léčby u pacienta, co mám udělat? 3.2 Jaké jsou nejčastější příčiny? 4. K čemu dochází při AEAB způsobené PRCA? Nálezy v krvi a kostní dřeni 4.2 Načasování nástupu onemocnění 4.3 Ukončení léčby ESA 5. Diagnostika PRCA Pokles hladiny hemoglobinu 5.2 Vyšetření protilátek 5.3 Vyšetření kostní dřeně 6. Sledování po stanovení diagnózy PRCA 3 7. Hlášení nežádoucích účinků 3 8. Dotazník 3 9. Jak získat další informace 4 Důležité informace 4 1. Přípravek MIRCERA a čistá aplazie buněk červené řady způsobená antierytropoetinovými protilátkami v souvislosti s podáváním látek stimulujících erytropoézu (AEAB způsobená PRCA) Přípravek MIRCERA je látka stimulující erytropoézu neboli ESA. Velmi vzácným nežádoucím účinkem ESA je čistá aplazie buněk červené řady zprostředkovaná protilátkami proti erytropoetinu neboli AEAB zprostředkovaná PRCA. Nežádoucí účinky jsou důležitým rozpoznaným rizikem v plánu řízení rizik (RMP) EU pro přípravek MIRCERA. 2. Co je cílem tohoto edukačního programu? Cílem této brožurky a edukačního programu je: zvýšení povědomí a znalostí o AEAB zprostředkované PRCA v souvislosti s ESA; podpora plnění profesní povinnosti lékařů hlásit výskyt nežádoucích účinků přípravku MIRCERA, zejména s ohledem na AEAB zprostředkovanou PRCA; porozumění důležitosti sběru podrobných informací o AEAB zprostředkované PRCA jednotným přístupem prostřednictvím dotazníku vyplněného lékařem; informování o nabídce společnosti Roche na bezplatné vyšetření protilátek po obdržení hlášení podezření na AEAB zprostředkovanou PRCA. To se týká i případů ztráty účinku neznámé etiologie v souvislosti s léčbou přípravkem MIRCERA. Pro komplexní informaci o tomto tématu odkazujeme na Souhrn údajů o přípravku léčivého přípravku MIRCERA, zejména na část: Zvláštní upozornění a opatření pro použití týkající se důležitých údajů o látkách stimulujících erytropoézu, přípravku MIRCERA a AEAB zprostředkované PRCA. 3. Ztráta účinku léčby ESA 3.1 Pokud ESA ztrácí svoji účinnost po předchozím prokázaném účinku léčby u pacienta, co mám udělat? Vyšetřit hlavní možné příčiny: hemolýza malnutrice deficit železa aluminiová intoxikace chronická ztráta krve neadekvátní dialýza zánětlivá onemocnění mnohočetný myelom, myelofibróza ostatní malignity hyperparatyreóza/fibrózní osteitida hypovitaminóza (například deficit kyseliny listové nebo vitamínu B12 ) hemoglobinopatie (například alfa- a beta-talasemie nebo srpkovitá anémie) nežádoucí účinky souběžně podávaných léků (například cytotoxických a imunosupresivních látek a ACE inhibitorů) Pokud nebyly diagnostikovány žádné z uvedených stavů, měla by být anémie plně vyšetřena (viz bod 7). 3.2 Jaké jsou nejčastější příčiny? Nejčastější příčiny získané PRCA jsou následující: lymfoproliferativní onemocnění infekce (například parvovirus B19) systémové autoimunitní onemocnění (například systémový lupus, revmatoidní artritida) léky (například azathioprin, isoniazid, fenytoin) thymom (okolo 5 % případů PRCA) idiopatická (okolo 50 % případů) 1
3 Edukační program k léčivému přípravku MIRCERA Edukační program o AEAB způsobené PRCA V2 4. K čemu dochází při AEAB způsobené PRCA? Epoetin umožňuje terminální dozrávání prekurzorů erytroidních buněk a tím i léčbu anémie způsobené chronickým onemocněním ledvin. AEAB zprostředkovaná PRCA je získané imunitní onemocnění, při kterém dochází k inhibici erytropoézy specifickými protilátkami proti erytropoetinu. 4.1 Nálezy v krvi a kostní dřeni Současná diagnostická kritéria pro PRCA byla definována následovně: pokles hemoglobinu přibližně o 0,1 g/dl/den; počet retikulocytů nižší než 10 nebo 20 x 10 9 /l; žádné významnější změny v počtu bílých krvinek, krevních destiček či diferenciálním počtu leukocytů; normální buněčnost kostní dřeně, méně než 1 % erytroblastů (příležitostně až do 5 % proerytroblastů nebo bazofilních erytroblastů), normální myeloidní buňky a megakaryocyty. 4.2 Načasování nástupu onemocnění Nejkratší hlášený interval nástupu PRCA od začátku léčby byl hlášený v průběhu 2 měsíců a nejdelší 90 měsíců. 4.3 Ukončení léčby ESA Panuje shoda, že u všech pacientů s potvrzenou AEAB zprostředkovanou PRCA má být podávání ESA ukončeno. Měl(a) byste: vyšetřit přítomnost protilátek proti erytropoetinu; provést vyšetření kostní dřeně. Pacienti nesmí být převedeni na jinou rekombinantní ESA, a to z důvodu zkřížené reaktivity protilátek s endogenním erytropoetinem a všemi ostatními rekombinantními molekulami ESA. 5. Diagnostika PRCA 5.1 Pokles hladiny hemoglobinu Evropská Best Practice Guidelines doporučuje mít silné podezření na rozvoj PRCA, pokud pacient léčený ESA: má náhlý, rychlý pokles koncentrace hemoglobinu přibližně o 0,5 1 g/dl/týden navzdory pokračující léčbě ESA nebo vyžaduje k udržení hladiny hemoglobinu transfuzi 1 2 jednotek buněk červené krevní řady týdně. V takovýchto případech musí být provedeno vyšetření kompletního krevního obrazu společně s vyšetřením krevního nátěru a vyšetřením počtu retikulocytů. Počet retikulocytů nižší než 10 nebo 20 x 10 9 /l svědčí silně pro PRCA. 5.2 Vyšetření protilátek Pro případy podezření či případy potvrzené AEAB zprostředkované PRCA nebo nevysvětlitelné ztráty účinnosti (zaznamenané v hlášení nežádoucího účinku či dotazníku) společnost Roche zajistí na vyžádání lékaře bezplatné vyšetření či opětovné vyšetření vzorků séra v referenční laboratoři. Instrukce týkající se vzorků budou lékařům zaslány, podrobnější informace naleznete v bodě 9 Jak získat další informace. 5.3 Vyšetření kostní dřeně Impulsem k vyšetření kostní dřeně je rychlý a setrvalý pokles počtu retikulocytů. Pro PRCA je charakteristická: normální buněčnost; < 1 % erytroblastů; příležitostně erytroblasty do 5 % s přítomností blokády dozrávání prekurzorů buněk červené krevní řady; buňky myeloidní a megakaryocytární řady v normě. Nálezy z vyšetření kostní dřeně pomohou odlišit PRCA od aplastické anémie a myelodysplastického syndromu. Pokud není vyšetření kostní dřeně možné, může být suspektní diagnóza dostačující, ale stupeň jistoty takové diagnózy může být nižší. 6. Sledování po stanovení diagnózy PRCA V průběhu sledování je třeba počet retikulocytů pravidelně kontrolovat. Počet retikulocytů je nejlepší laboratorní ukazatel produkce buněk červené krevní řady. Počet retikulocytů je měřítkem stupně aktivity kostní dřeně s ohledem na denní tvorbu červených krvinek. Poklesu hladiny hemoglobinu bude předcházet změna rychlosti produkce buněk červené krevní řady. Nezměněný počet retikulocytů svědčí o účinnosti léčby. Každý pokles počtu retikulocytů musí být vyšetřen. Jako jedno z diagnostických kritérií pro AEAB zprostředkovanou PRCA byl navržen absolutní počet retikulocytů nižší než 10 nebo 20 x 10 9 /l. 7. Hlášení nežádoucích účinků Potřebujeme znát co nejvíce podrobností o hlášení podezření na případy AEAB zprostředkované PRCA související potenciálně s léčbou přípravkem MIRCERA. Nahlášení nežádoucích účinků je třeba zvážit při následujících skutečnostech: potvrzené hlášení AEAB zprostředkované PRCA (například pozitivní nález AEAB, vyšetření kostní dřeně ukazující na PRCA); podezření na AEAB zprostředkovanou PRCA s nedostatečnými či nejednoznačnými výsledky, včetně následných výsledků doplňujících vyšetření a aktualizovaných výsledků pokračujícího sledování těchto pacientů; hlášení nevysvětlitelné ztráty účinnosti, zejména: - po vyloučení alternativních příčin PRCA (viz bod 5); - pokud měl pacient dříve stabilní koncentrace hemogobinu po ustálení dávkování přípravku MIRCERA (nikoli během titrace). Ztráta účinnosti se může odrážet ve zjištěních jako refrakterní anémie, masivní zvýšení dávky v již stanoveném dávkovacím schématu přípravku MIRCERA či snížení účinku léku. Podezření na AEAB zprostředkovanou PRCA nebo nevysvětlitelnou ztrátu léčebného účinku musí být dále prošetřeno prostřednictvím vyšetření protilátek proti erytropoetinu a hematologickým vyšetřením. Hlášení nežádoucích účinků Kontaktní údaje pro hlášení nežádoucích účinků společnosti Roche s.r.o.: Lékařské oddělení/farmakovigilance, Dukelských hrdinů 52, Praha 7, mobil: , lucie.otcenaskova@roche.com Připomínáme zdravotnickým pracovníkům povinnost hlásit Státnímu ústavu pro kontrolu léčiv (SÚKL) jakékoli podezření na závažné a/nebo neočekávané nežádoucí účinky a jiné skutečnosti významné pro zdraví léčených osob spojené s užíváním léčivého přípravku MIRCERA. Informace o hlášení podezření na nežádoucí účinky je na kde je možno vyplnit elektronický formulář. 8. Dotazník Společnost Roche po obdržení hlášení nežádoucích účinků (AEAB zprostředkovaná PRCA nebo ztráta účinku) zašle hlásícímu lékaři doprovodný dotazník. Tento dotazník se nazývá: Dotazník k látkám stimulujícím erytropoézu (ESA) týkající se nežádoucího účinku čisté aplazie buněk červené řady zprostředkované protilátkami proti erytropoetinu, nedostatečné odpovědi na léčbu ESA, anémie refrakterní na léčbu ESA a nevysvětlitelné ztráty účinku léčby ESA Dotazník bude doplněn o již obdržené informace. V případě potřeby budou tato sebraná data tvořit podklad pro komunikaci významných změn, například cestou aktualizace údajů o přípravku. Dotazník bude shromažďovat data, jako jsou například: diagnostické výsledky potvrzující diagnózu nebo klinické podezření na ni; relevantní souběžná onemocnění či konkomitantní léčba; alternativní stavy vysvětlující náhlý pokles hladiny hemoglobinu; expozice typům erytropoetinu s ohledem na objevení se prvních známek/příznaků svědčících pro AEAB zprostředkovanou PRCA. Tento strukturovaný dotazník je určený pouze pro případy, kdy je přípravek MIRCERA používán mimo klinické studie. V klinických studiích vás navede studijní protokol, jak pokračovat při hlášení možné AEAB zprostředkované PRCA nebo ztráty účinku. 2 3
4 Edukační program k léčivému přípravku MIRCERA Edukační program o AEAB způsobené PRCA V2 9. Jak získat další informace Pro získání dalších informací o hlášení nežádoucích účinků včetně informací o Dotazníku a informací týkajících se testování protilátek kontaktujte prosím místní zastoupení společnosti Roche, Lékařské oddělení/farmakovigilance, Dukelských hrdinů 52, Praha 7, mobil: , lucie.otcenaskova@roche.com Pro získání dalších informací o přípravku MIRCERA včetně literatury kontaktujte prosím místní zastoupení společnosti Roche, Dukelských hrdinů 52, Praha 7, tel: , prague.info@roche.com Důležité informace POTŘEBA A KLINICKÝ VÝZNAM HLÁŠENÍ NEŽÁDOUCÍCH ÚČINKŮ Účelem farmakovigilance je detekce, hodnocení a prevence výskytu nežádoucích účinků. Pro stanovení signálu je potřeba určitý počet hlášení. Záchyt vzácného nežádoucího účinku se zvýší a urychlí, pokud se do systému hlášení nežádoucích účinků zapojí více lékařů [Meyboom 1999]. Podle autorů Wallera a Evanse [2003] může být systém spontánního hlášení nežádoucích účinků definován jako sběr jednotlivých hlášení podezření na nežádoucí účinky, s hlavním cílem zachytit potenciální neznámou závažnou toxicitu léku. Primární úloha systému spontánního hlášení z postmarketingu je generace signálu pro účinky typu A (farmakologický účinek léku závislý na dávce) a účinky typu B (například alergické či idiosynkratické reakce, AEAB zprostředkovaná PRCA) [Meyboom 1999]. Systém spontánního hlášení nežádoucích účinků léčivých přípravků uváděných nově na trh není pouze o identifikaci a kvantifikaci neočekávaných nežádoucích účinků. Jde rovněž o identifikaci podskupin rizikových pacientů, například souvislostí s jiným současně probíhajícím onemocněním, věkem, pohlavím a dávkou. Bezpečnost přípravku je po jeho uvedení na trh průběžně sledována s cílem zajistit zachování akceptovatelného hodnocení poměru rizika a prospěchu a s cílem předávat příslušné informace lékařské veřejnosti [Talbot 2004]. Systém spontánního hlášení nežádoucích účinků je chápán jako pilíř farmakovigilance [Waller 2003]. Důležité údaje o AEAB způsobené PRCA a ESA Všechny exogenní proteiny mohou být potenciálně imunogenní. U terapeutických proteinů se hlášená incidence výskytu tvorby protilátek značně liší, například v závislosti na genetické výbavě pacienta, typu onemocnění, typu proteinu, cestě podání, frekvenci dávkování a délce léčby. Během výroby, zacházení s přípravkem a uchovávání může navíc docházet ke kontaminaci nebo ovlivnění trojrozměrné struktury proteinu prostřednictvím oxidace či tvorby agregátů [Schellekens 2002]. V průběhu prvních 10 let ( ) léčby epoetiny byly publikovány tři případy AEAB zprostředkované PRCA [Bergrem 1993, Peces 1996, Prabhakar 1997] v souvislosti s léčbou několika miliónů pacientů. Od roku 1998 se objevil náhlý vzestup počtu hlášení AEAB zprostředkované PRCA u pacientů s chronickým onemocněním ledvin. Většina jich byla hlášena u pacientů léčených subkutánně podávanými preparáty epoetinu alfa humánního séra neobsahujícího albumin, obchodovanými mimo území USA, s maximem počtu hlášení v letech 2001 a 2002 [Rossert 2004]. Testování V průběhu vývojového programu pro přípravek MIRCERA byly použity dva testovací přístupy. Tyto přístupy budou aplikovány rovněž při zkoumání poznatků z postmarketingu. Prvním testem je přemosťující ELISA test, což je metoda kvantifikace anti-epo a anti-metoxy-polyetylenglykol-epoetin beta (anti-mircera) protilátek. Druhý typ testování je neutralizační test na protilátky, což je funkční test založený na použití standardní in vitro metody pro detekci aktivity EPO či metoxy-polyetylenglykol-epoetinu beta. Tento test měří EPO či metoxy-polyetylenglykol-epoetinem beta stimulovanou proliferaci buněčné linie exprimující EPO receptory jak v přítomnosti, tak i v nepřítomnosti séra pacienta. Přítomnost neutralizačních anti-epo či anti-metoxy-polyetylenglykol-epoetin beta protilátek snižuje nebo potlačuje buněčnou proliferaci. Tento test může být dle uvážení použit na vzorky s rozporem mezi titrem protilátek zjištěným prostřednictvím testu na protilátky ELISA a klinickou diagnózou. Vzhledem k tomu, že test na protilátky ELISA má několikanásobně vyšší senzitivitu v porovnání s neutralizačním testem na protilátky, neočekává se, že tento test poskytne doplňující klinicky relevantní informace pro vzorky s nízkými titry protilátek nebo s potvrzenou PRCA. Literatura Stručný obsah naznačuje hlavní aspekty publikací seřazených s ohledem na praktická a základní doporučení týkající se hodnocení pacienta a dále s ohledem na podrobné aspekty jednotlivých témat, jak je stručně uvedeno ve shrnutí každé publikace. Praktické a základní doporučení týkající se hodnocení pacienta Revised European Best Practice Guidelines on Anaemia Management (Section I. Anaemia evaluation) Nephrol Dial Transplant, 2004; 19(Suppl 2): ii2-ii5 - Kteří pacienti by měli být hodnoceni a kdy by mělo být zahájeno laboratorní vyšetření - Výzkum vhodných laboratorních vyšetření anémie u chronického onemocnění ledvin - Diagnóza renální anémie Revised European Best Practice Guidelines on Anaemia Management (Section IV. Failure to respond to treatment) Nephrol Dial Transplant, 2004; 19(Suppl 2): ii32-ii36 - Selhání dosažení či udržení cílové hladiny hemoglobinu - Kritéria vedoucí k podezření na AEAB zprostředkovanou PRCA - Kritéria potvrzující AEAB zprostředkovanou PRCA Casadevall N., Cournoyer D. et al. Recommendations on haematological criteria for the diagnosis of epoetin-induced pure red cell aplasia. Eur J Haematol 2004: 73: Doporučení pro diagnostický přístup včetně diskuse o potenciálních zjištěních Další literatura / Tyto publikace jsou dostupné na vyžádání Bennett C.L., Luminari S. et al. Pure Red-Cell Aplasia and Epoetin Therapy. N Engl J Med, September 30, 2004; 351(14): Popis celosvětového sběru hlášení AEAB-zprostředkované PRCA, zdůrazňující potřebu spontánního hlášení lékařů pro dokumentování změny v míře výskytu Bennett C.L., Cournoyer D., et al. Long-term outcome of individuals with pure red cell aplasia and antierythropoietin antibodies in patients treated with recombinant epoetin: a follow-up report from the Research on Adverse Drug Events and Reports (RADAR) Project. Blood. 2005; 106: Informace o léčbě a dlouhodobém následném sledování 191 pacientů s AEAB zprostředkovanou PRCA Casadevall N., Nataf J., et al. Pure Red-Cell Aplasia and Antierythropoietin Antibodies in Patients Treated with Recombinant Erythropoietin. N Engl J Med 2002; 346(7): Klinická charakteristika 13 pacientů s AEAB-zprostředkovanou PRCA Eckardt K. U. and Casadevall N. Pure red-cell aplasia due to anti-erythropoietin antibodies. Nephrol Dial Transplant 2003; 18: Diagnóza, příčiny AEAB zprostředkované PRCA Rossert J. et al. Anti-Erythropoietin Antibodies and Pure Red Cell Aplasia. J Am Soc Nephrol 2004; 15: Diagnóza, testy, epidemiologie, rizikové faktory Schellekens H. Factors influencing the immunogenicity of therapeutic proteins. Nephrol Dial Transplant. 2005; 20 (Suppl 6):vi3-9 - Následky tvorby protilátek Schellekens H. Immunogenicity of Therapeutic Proteins: Clinical Implications and Future Prospects. Clin Ther 2002; 24: Účinky protilátek na produkci endogenních bílkovin, klinické účinky protilátek, faktory ovlivňující imunogenitu Další odkazy zmíněné v textu Bergrem H. et al. A Case of Antierythropoietin Antibodies Following Recombinant Human Erythropoietin Treatment. In: Bauer C., Koch K.M., Scigalla P., Wieczorek L, eds. Erythropoietin: Molecular physiology and clinical applications. New York: Marcel Dekker. 1993; Cavill I. and Williams J.D. Benefits of recombinant human erythropoietin. Lancet 2002; 360 Nov 16: Meyboom RHB, Egberts AC, et al. Pharmacovigilance in Perspective. Drug Safety, December 1999, 21(6): Peces R., Alcazar R. Antibodies against recombinant human erythropoietin in a patient with erythropoietin-resistant anemia. N Engl J Med. 1996; 335: Prabhakar S.S., Muhlfelder T. Antibodies to recombinant human erythropoietin causing pure red cell aplasia. Clin Nephrol. 1997; 47: Talbot J., Waller P. Steven s Detection of New Adverse Drug Reactions, Chapter 1 Introduction, pp1-2, 5th ed Waller P.C., Evans S.J.W. A model for the future conduct of pharmacovigilance. Pharmacoepidemiol Drug Safety 2003; 12: Weber G. et al. Allergic Skin and Systemic Reactions in a Patient with Pure Red Cell Aplasia and Anti-Erythropoietin Antibodies Challenged with Different Epoetins. J Am Soc Nephrol 2002; 13:
5
Klinický pohled na biosimilars. Prof. MUDr Vladimír Tesař, Klinika nefrologie 1.LF UK a VFN
 Klinický pohled na biosimilars Prof. MUDr Vladimír Tesař, Klinika nefrologie 1.LF UK a VFN Komu z pacientů biosimilars mohou pomoci? Je možné pacienta převést z biologického léku, který dosud užíval na
Klinický pohled na biosimilars Prof. MUDr Vladimír Tesař, Klinika nefrologie 1.LF UK a VFN Komu z pacientů biosimilars mohou pomoci? Je možné pacienta převést z biologického léku, který dosud užíval na
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH)
 Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
Přímé sdělení pro zdravotnické pracovníky týkající se spojitosti mezi léčbou Sprycelem (dasatinibem) a plicní arteriální hypertenzí (PAH) Se souhlasem Evropské lékové agentury (EMA) a její
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE
 EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
EDUKAČNÍ MATERIÁL PŘÍRUČKA PRO PŘEDEPISUJÍCÍHO LÉKAŘE Příručka pro předepisujícího lékaře Pokyny pro zdravotnické pracovníky ohledně předepisování přípravku Cerdelga (eliglustat) Tento léčivý přípravek
Návod pro pacienta / pečovatele
 Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Návod pro pacienta / pečovatele Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že
Parvovirus B 19. Renata Procházková
 Renata Procházková Parvovirus B 19 - Běžný lidský patogen - Objeven 1975 Yvonne Cossart - Neobalený DNA virus (18-22 nm) - Odolný vůči prostředí - Parvoviridae rod Erythrovirus - 3 genotypy: * klasická
Renata Procházková Parvovirus B 19 - Běžný lidský patogen - Objeven 1975 Yvonne Cossart - Neobalený DNA virus (18-22 nm) - Odolný vůči prostředí - Parvoviridae rod Erythrovirus - 3 genotypy: * klasická
Jaké máme leukémie? Akutní myeloidní leukémie (AML) Akutní lymfoblastická leukémie (ALL) Chronické leukémie, myelodysplastický syndrom,
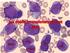 Akutní myeloidní leukémie (AML) Jaké máme leukémie? Akutní lymfoblastická leukémie (ALL) Chronické leukémie, myelodysplastický syndrom, Chronické leukémie, mnohočetný myelom, Někdy to není tak jednoznačné
Akutní myeloidní leukémie (AML) Jaké máme leukémie? Akutní lymfoblastická leukémie (ALL) Chronické leukémie, myelodysplastický syndrom, Chronické leukémie, mnohočetný myelom, Někdy to není tak jednoznačné
ESA - erytropoézu stimulující agens a jejich použití v klinické praxi
 ESA - erytropoézu stimulující agens a jejich použití v klinické praxi T. Kotulák Klinika anestezie a resuscitace, IKEM, Praha a 1. LF UK a VFN, Praha etiologie ICU anémie anémie kritických stavů je častý
ESA - erytropoézu stimulující agens a jejich použití v klinické praxi T. Kotulák Klinika anestezie a resuscitace, IKEM, Praha a 1. LF UK a VFN, Praha etiologie ICU anémie anémie kritických stavů je častý
Příloha IV. Vědecké závěry
 Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
Příloha IV Vědecké závěry 57 Vědecké závěry Dne 7. června 2017 byla Evropská komise (EK) informována o případu úmrtí v důsledku fulminantního selhání jater u pacienta léčeného daklizumabem v rámci průběžné
Informace pro zdravotnické odborníky
 EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
EDUKAČNÍ MATERIÁL Agomelatin k léčbě depresivních epizod u dospělých Informace pro zdravotnické odborníky Doporučení ohledně: Monitorování jaterních funkcí Interakce se silnými inhibitory CYP1A2 Souhrnné
MZ A POHLED NA LÉKOVÉ INTERAKCE. PharmDr. Alena Tomášková 24. únor 2015
 MZ A POHLED NA LÉKOVÉ INTERAKCE PharmDr. Alena Tomášková 24. únor 2015 Lékové interakce O lékové interakci mluvíme tehdy, když při současném podávání dvou nebo více léčivých přípravků dojde ke změně účinku
MZ A POHLED NA LÉKOVÉ INTERAKCE PharmDr. Alena Tomášková 24. únor 2015 Lékové interakce O lékové interakci mluvíme tehdy, když při současném podávání dvou nebo více léčivých přípravků dojde ke změně účinku
EDUKAČNÍ MATERIÁL - Pioglitazone Accord
 Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
Pioglitazon preskripční informace pro lékaře Výběr pacienta a zvládání rizik Evropská léková agentura přezkoumala možnou spojitost mezi podáním léčivých přípravků s obsahem pioglitazonu a zvýšeným rizikem
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU MIRCERA 50 mikrogramů/0,3 ml injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU MIRCERA 50 mikrogramů/0,3 ml injekční roztok v předplněné injekční stříkačce 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Jedna předplněná injekční stříkačka
EDUKAČNÍ MATERIÁLY. Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce
 EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Návod pro zdravotnické pracovníky Hemlibra (emicizumab) Subkutánní injekce Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Hemlibra (emicizumab) Subkutánní injekce. Návod pro zdravotnické pracovníky
 EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERIÁLY Hemlibra (emicizumab) Subkutánní injekce Návod pro zdravotnické pracovníky Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Edukační materiál. Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera
 Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Edukační materiál Strattera (atomoxetin) Informace pro lékaře týkající se posouzení a monitorování kardiovaskulárních rizik u přípravku Strattera Přípravek Strattera je indikován k léčbě hyperkinetické
Srovnání hematologického analyzátoru Heska Element HT5 a veterinárního hematologického analyzátoru IDEXX ProCyte DX v klinickém prostředí
 Srovnání hematologického analyzátoru Heska Element HT5 a veterinárního hematologického analyzátoru IDEXX ProCyte DX v klinickém prostředí Úvod Hematologický analyzátor od společnosti Heska a veterinární
Srovnání hematologického analyzátoru Heska Element HT5 a veterinárního hematologického analyzátoru IDEXX ProCyte DX v klinickém prostředí Úvod Hematologický analyzátor od společnosti Heska a veterinární
LÉKAŘSKÁ VYŠETŘENÍ A LABORATORNÍ TESTY
 LÉKAŘSKÁ VYŠETŘENÍ A LABORATORNÍ TESTY Pokud čtete tento text, pravděpodobně jste v kontaktu s odborníkem na léčbu mnohočetného myelomu. Diagnóza mnohočetného myelomu je stanovena pomocí četných laboratorních
LÉKAŘSKÁ VYŠETŘENÍ A LABORATORNÍ TESTY Pokud čtete tento text, pravděpodobně jste v kontaktu s odborníkem na léčbu mnohočetného myelomu. Diagnóza mnohočetného myelomu je stanovena pomocí četných laboratorních
Diagnostika a příznaky mnohočetného myelomu
 Diagnostika a příznaky mnohočetného myelomu J.Minařík, V.Ščudla Mnohočetný myelom Nekontrolované zmnožení nádorově změněných plasmatických buněk v kostní dřeni Mnohočetný = obvykle více oblastí kostní
Diagnostika a příznaky mnohočetného myelomu J.Minařík, V.Ščudla Mnohočetný myelom Nekontrolované zmnožení nádorově změněných plasmatických buněk v kostní dřeni Mnohočetný = obvykle více oblastí kostní
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) dexamethasonu (kromě
ANÉMIE CHRONICKÝCH CHOROB
 ANÉMIE CHRONICKÝCH CHOROB (ACD anemia of chronic disease) seminář Martin Vokurka 2007 neoficiální verze pro studenty 2007 1 Proč se jí zabýváme? VELMI ČASTÁ!!! U hospitalizovaných pacientů je po sideropenii
ANÉMIE CHRONICKÝCH CHOROB (ACD anemia of chronic disease) seminář Martin Vokurka 2007 neoficiální verze pro studenty 2007 1 Proč se jí zabýváme? VELMI ČASTÁ!!! U hospitalizovaných pacientů je po sideropenii
Farmakovigilance v KH změny a novinky
 Státní ústav pro kontrolu léčiv [ 1 ] Farmakovigilance v KH změny a novinky MUDr. Tomáš Boráň Oddělení klinického hodnocení Farmakovigilance v KH [ 2 ] Obsah CT-3 Aktualizace pokynu KLH-21 DSUR Chyby v
Státní ústav pro kontrolu léčiv [ 1 ] Farmakovigilance v KH změny a novinky MUDr. Tomáš Boráň Oddělení klinického hodnocení Farmakovigilance v KH [ 2 ] Obsah CT-3 Aktualizace pokynu KLH-21 DSUR Chyby v
Základní informace o interferenci daratumumabu s testy krevní kompatibility
 EDUKAČNÍ MATERÁLY Daratumumab Základní informace o interferenci daratumumabu s testy krevní kompatibility Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
EDUKAČNÍ MATERÁLY Daratumumab Základní informace o interferenci daratumumabu s testy krevní kompatibility Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti.
Thomas Plot Olga Bálková, Roche s.r.o., Diagnostics Division SWA pracovní dny, Praha, 24. února 2010
 Thomas Plot Olga BálkovB lková,, Roche s.r.o., Diagnostics Division SWA pracovní dny, Praha, 24. února 2010 Příčiny anémie Anémie je většinou následkem mnoha jiných základních onemocnění. Nedostatek EPO
Thomas Plot Olga BálkovB lková,, Roche s.r.o., Diagnostics Division SWA pracovní dny, Praha, 24. února 2010 Příčiny anémie Anémie je většinou následkem mnoha jiných základních onemocnění. Nedostatek EPO
LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE
 LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE Léčba by měla být zahájena a sledována specialistou se zkušenostmi v léčbě revmatoidní artritidy a psoriatické artritidy. Lékař by měl poučit pacienty
LEFLUNOMID SANDOZ 20 MG INFORMAČNÍ LETÁK PRO LÉKAŘE Léčba by měla být zahájena a sledována specialistou se zkušenostmi v léčbě revmatoidní artritidy a psoriatické artritidy. Lékař by měl poučit pacienty
Celkové shrnutí vědeckého hodnocení přípravku Atacand Plus a související názvy (viz Příloha I)
 PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÝCH INFORMACÍ PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 14 Vědecké závěry Celkové
PŘÍLOHA II VĚDECKÉ ZÁVĚRY A ZDŮVODNĚNÍ POTŘEBNÝCH ÚPRAV SOUHRNU ÚDAJŮ O PŘÍPRAVKU, OZNAČENÍ NA OBALU A PŘÍBALOVÝCH INFORMACÍ PŘEDKLÁDANÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY 14 Vědecké závěry Celkové
Zvažte oddálení podání regadenosonu u pacientů s nekontrolovanou hypertenzí.
 CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
CAVE! Informační dopis pro zdravotníky Rapiscan (regadenoson) - Nové důležité doporučení pro minimalizaci rizika cévní mozkové příhody a prodloužení křečí vyvolaných přípravkem Rapiscan po podání aminofylinu.
Hlášení těhotenství (formulář)
 Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Hlášení těhotenství (formulář) OSOBA PODÁVAJÍCÍ HLÁŠENÍ Počáteční Následné sledování Jméno a příjmení: Upřesnění: Lékař (specializace) Lékárník pacient ostatní (upřesněte) Kontaktní adresa: Telefonní číslo:
Příloha III. Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace
 Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Příloha III Úpravy příslušných částí Souhrnu údajů o přípravku a Příbalové informace Poznámka: Tento Souhrn údajů o přípravku, Označení na obalu a Příbalová informace jsou výsledkem posuzovacího řízení.
Režimy s nízkým rizikem FN riziko do 10 % Režimy se středním rizikem FN riziko 10 19% Režimy s vysokým rizikem FN riziko 20 a více procent
 Portál DIOS verze II Druhá verze portálu DIOS a jeho elektronické knihovny chemorežimů přináší nové informace a nové nástroje týkající se problematiky toxicity chemoterapie. Jde především o problematiku
Portál DIOS verze II Druhá verze portálu DIOS a jeho elektronické knihovny chemorežimů přináší nové informace a nové nástroje týkající se problematiky toxicity chemoterapie. Jde především o problematiku
Časné fáze klinických studií
 Časné fáze klinických studií Mikulov, 13.4.2012 Regina Demlová, FÚ LF MU a MOÚ Stávající situace v klinickém výzkumu Počet nových látek v klinickém výzkumu (NMEs) v posledních 15-20-ti letech narůstá Počet
Časné fáze klinických studií Mikulov, 13.4.2012 Regina Demlová, FÚ LF MU a MOÚ Stávající situace v klinickém výzkumu Počet nových látek v klinickém výzkumu (NMEs) v posledních 15-20-ti letech narůstá Počet
PRŮKAZ PACIENTA. užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019
 PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
PRŮKAZ PACIENTA užívajícího přípravek Amgevita (určeno dospělým i dětským pacientům) Verze 2 Shváleno SÚKL březen 2019 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě
CEBO: (Center for Evidence Based Oncology) Incidence Kostních příhod u nádorů prsu PROJEKT IKARUS. Neintervenční epidemiologická studie
 CEBO: (Center for Evidence Based Oncology) Incidence Kostních příhod u nádorů prsu PROJEKT Neintervenční epidemiologická studie PROTOKOL PROJEKTU Verze: 4.0 Datum: 26.09.2006 Strana 2 PROTOKOL PROJEKTU
CEBO: (Center for Evidence Based Oncology) Incidence Kostních příhod u nádorů prsu PROJEKT Neintervenční epidemiologická studie PROTOKOL PROJEKTU Verze: 4.0 Datum: 26.09.2006 Strana 2 PROTOKOL PROJEKTU
DOKUMENTACE K ŽÁDOSTI
 1 KAPITOLA IV + PŘÍLOHA I DOKUMENTACE K ŽÁDOSTI MUDr. Alena Trunečková Oddělení klinického hodnocení 2 Článek 25 Údaje předložené v dokumentaci k žádosti Článek 26 Jazykové požadavky Příloha I Dokumentace
1 KAPITOLA IV + PŘÍLOHA I DOKUMENTACE K ŽÁDOSTI MUDr. Alena Trunečková Oddělení klinického hodnocení 2 Článek 25 Údaje předložené v dokumentaci k žádosti Článek 26 Jazykové požadavky Příloha I Dokumentace
Prohlášení o ochraně osobních údajů pro farmakovigilanci
 Prohlášení o ochraně osobních údajů pro farmakovigilanci Společnost Bayer bere bezpečnost výrobků a vaše soukromí vážně Společnost Bayer AG, se sídlem 51368 Leverkusen, Německo (dále jen Bayer, nás, naše
Prohlášení o ochraně osobních údajů pro farmakovigilanci Společnost Bayer bere bezpečnost výrobků a vaše soukromí vážně Společnost Bayer AG, se sídlem 51368 Leverkusen, Německo (dále jen Bayer, nás, naše
B.Stibor. Landesklinikum Baden bei Wien, Austria
 B.Stibor Landesklinikum Baden bei Wien, Austria Transfúzní strategie na ICU Transfúzní strategie na ICU anémie na ICU etiologie transfúzní trigger erytropoézu stimulující látky (ESA) možnosti bezkrevní
B.Stibor Landesklinikum Baden bei Wien, Austria Transfúzní strategie na ICU Transfúzní strategie na ICU anémie na ICU etiologie transfúzní trigger erytropoézu stimulující látky (ESA) možnosti bezkrevní
Jedna předplněná injekční stříkačka obsahuje 20 mikrogramů darbepoetinu alfa (darbepoetin alfa)
 1. NÁZEV PŘÍPRAVKU Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 20 mikrogramů injekční roztok v
1. NÁZEV PŘÍPRAVKU Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 20 mikrogramů injekční roztok v
Hlášení těhotenství (formulář) RO-GNE: HLÁŠENÍ TĚHOTENSTVÍ
 Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Zároveň žádáme
Česká Myelomová Skupina na poli mnohočetného myelomu
 Česká Myelomová Skupina na poli mnohočetného myelomu Vladimír Maisnar IV. interní hematologická klinika LF UK a FN Hradec Králové Lázně Bělohrad, 10. září 2016 Epidemiologická data: MM 1% všech malignit,
Česká Myelomová Skupina na poli mnohočetného myelomu Vladimír Maisnar IV. interní hematologická klinika LF UK a FN Hradec Králové Lázně Bělohrad, 10. září 2016 Epidemiologická data: MM 1% všech malignit,
Syfilis přehledně. MUDr.Hana Zákoucká Odd. STI, NRL pro syfilis, Státní zdravotní ústav ROCHE 6-2014
 Syfilis přehledně MUDr.Hana Zákoucká Odd. STI, NRL pro syfilis, Státní zdravotní ústav ROCHE 6-214 LEGISLATIVA Zákon č. 258/2 Sb., o ochraně veřejného zdraví Vyhláška MZ ČR č. 36/212 Sb., podmínky předcházení
Syfilis přehledně MUDr.Hana Zákoucká Odd. STI, NRL pro syfilis, Státní zdravotní ústav ROCHE 6-214 LEGISLATIVA Zákon č. 258/2 Sb., o ochraně veřejného zdraví Vyhláška MZ ČR č. 36/212 Sb., podmínky předcházení
Zkušební otázky z oboru hematologie 2. ročník bakalářského studia LF MU obor Zdravotní laborant
 Zkušební otázky z oboru hematologie 2. ročník bakalářského studia LF MU obor Zdravotní laborant I. Praktická zkouška z laboratorní hematologie IA) Část morfologická 1. Hematopoéza - vývojové krevní řady
Zkušební otázky z oboru hematologie 2. ročník bakalářského studia LF MU obor Zdravotní laborant I. Praktická zkouška z laboratorní hematologie IA) Část morfologická 1. Hematopoéza - vývojové krevní řady
Familiární středomořská (Mediterranean) horečka (Fever)
 www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
www.printo.it/pediatric-rheumatology/cz/intro Familiární středomořská (Mediterranean) horečka (Fever) Verze č 2016 2. DIAGNÓZA A LÉČBA 2.1 Jak se nemoc diagnostikuje? Obecně se uplatňuje následující postup:
EDUKAČNÍ MATERIÁL. Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid)
 EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
EDUKAČNÍ MATERIÁL Informace pro zdravotnické pracovníky k bezpečnému užívání léčivého přípravku Leflunopharm (leflunomid) Leflunopharm (leflunomid), jako chorobu modifikující antirevmatikum (Disease-Modifying
PRŮKAZ PACIENTA. užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1
 PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
PRŮKAZ PACIENTA užívajícího přípravek Imraldi (určeno dospělým i dětským pacientům) verze 1 Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi při každé návštěvě zdravotnického zařízení.
Časnou diagnostikou k lepší kvalitě života. Projekt CRAB
 Časnou diagnostikou k lepší kvalitě života Projekt CRAB Prim. MUDr. Jan Straub I. Interní klinika hematoonkologie 1. LF-UK a VFN - Praha Lednice 8.9.2007 Stanovením m diagnózy mnohočetn etného myelomu
Časnou diagnostikou k lepší kvalitě života Projekt CRAB Prim. MUDr. Jan Straub I. Interní klinika hematoonkologie 1. LF-UK a VFN - Praha Lednice 8.9.2007 Stanovením m diagnózy mnohočetn etného myelomu
Léčba anemie. Prim. MUDr. Jan Straub I. Interní klinika VFN Praha
 Léčba anemie Prim. MUDr. Jan Straub I. Interní klinika VFN Praha Anemie Nedostatek červených krvinek - erytrocytů resp. krevního barviva - hemoglobinu Stupně anemie normální KO hgb 120-175 g/l lehká anemie
Léčba anemie Prim. MUDr. Jan Straub I. Interní klinika VFN Praha Anemie Nedostatek červených krvinek - erytrocytů resp. krevního barviva - hemoglobinu Stupně anemie normální KO hgb 120-175 g/l lehká anemie
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha III. Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace
 Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Příloha III Úpravy odpovídajících bodů souhrnu údajů o přípravku a příbalové informace Poznámka: Úpravy v souhrnu údajů o přípravku a příbalové informaci mohou být dále aktualizovány příslušnými vnitrostátními
Kapitola III. Poruchy mechanizmů imunity. buňka imunitního systému a infekce
 Kapitola III Poruchy mechanizmů imunity buňka imunitního systému a infekce Imunitní systém Zásadně nutný pro přežití Nezastupitelná úloha v obraně proti infekcím Poruchy imunitního systému při rozvoji
Kapitola III Poruchy mechanizmů imunity buňka imunitního systému a infekce Imunitní systém Zásadně nutný pro přežití Nezastupitelná úloha v obraně proti infekcím Poruchy imunitního systému při rozvoji
Anémie u chronických onemocnění
 Projekt sponzorován z fondů FRVŠ 2334/2010 G3 Anémie u chronických onemocnění Dagmar Pospíšilová Barbora Ludíková Dětská klinika Fakultní nemocnice Olomouc Lékařská fakulta Univerzita Palackého v Olomouci
Projekt sponzorován z fondů FRVŠ 2334/2010 G3 Anémie u chronických onemocnění Dagmar Pospíšilová Barbora Ludíková Dětská klinika Fakultní nemocnice Olomouc Lékařská fakulta Univerzita Palackého v Olomouci
PRVKY BEZPEČNOSTI Č VE VÝROBĚ TRANSFUZNÍCH PŘÍPRAVKŮ
 PRVKY BEZPEČNOSTI Č FAKULTNÍ NEMOCNICE BRNO VE VÝROBĚ TRANSFUZNÍCH PŘÍPRAVKŮ EVA TESAŘOVÁ 6. STŘEŠOVICKÝ TRANSFUZNÍ DEN, PRAHA, 22.11.2012 1 BEZPEČNÁ HEMOTERAPIE Bezpečné postupy Bezpečné produkty Implementaci
PRVKY BEZPEČNOSTI Č FAKULTNÍ NEMOCNICE BRNO VE VÝROBĚ TRANSFUZNÍCH PŘÍPRAVKŮ EVA TESAŘOVÁ 6. STŘEŠOVICKÝ TRANSFUZNÍ DEN, PRAHA, 22.11.2012 1 BEZPEČNÁ HEMOTERAPIE Bezpečné postupy Bezpečné produkty Implementaci
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU MIRCERA 30 mikrogramů/0,3 ml injekční roztok v předplněné injekční stříkačce MIRCERA 40 mikrogramů/0,3 ml injekční roztok v předplněné injekční stříkačce
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1 1. NÁZEV PŘÍPRAVKU MIRCERA 30 mikrogramů/0,3 ml injekční roztok v předplněné injekční stříkačce MIRCERA 40 mikrogramů/0,3 ml injekční roztok v předplněné injekční stříkačce
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace
 Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
Odběr krvetvorných buněk z periferní krve: příprava, průběh a komplikace Helena Švábová, Andrea Žmijáková Interní hematologická a onkologická klinika FN Brno Separační středisko je součástí Interní hematologické
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Vývoj nových léčiv. Preklinický výzkum Klinický výzkum
 Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
Vývoj nových léčiv Preklinický výzkum Klinický výzkum Úvod Léčivo = nejprověřenější potravina vstupující do organismu Ideální léčivo kvalitní, účinné, bezpečné a dostupné Financování výzkumu léčiv souvislost
Rozměr zavřeného průkazu mm
 Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přední strana Str. 1 PRŮKAZ PACIENTA užívajícího přípravek Humira (určeno dospělým i dětským pacientům) Rozměr zavřeného průkazu 105 73 mm Je nutné předložit tuto kartičku každému lékaři či zdravotníkovi
Přínos farmakokinetického monitorování pro optimalizaci biologické léčby ISZ. T. Vaňásek (Hradec Králové)
 Přínos farmakokinetického monitorování pro optimalizaci biologické léčby ISZ T. Vaňásek (Hradec Králové) Farmakokinetické monitorování BL Biologická léčba Cílená modifikace imunitní reakce spojené s patogenezí
Přínos farmakokinetického monitorování pro optimalizaci biologické léčby ISZ T. Vaňásek (Hradec Králové) Farmakokinetické monitorování BL Biologická léčba Cílená modifikace imunitní reakce spojené s patogenezí
Základní informace o interferenci daratumumabu s testy krevní kompatibility a metody mitigace interference
 EDUKAČNÍ MATERÁLY Daratumumab Základní informace o interferenci daratumumabu s testy krevní kompatibility a metody mitigace interference Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé
EDUKAČNÍ MATERÁLY Daratumumab Základní informace o interferenci daratumumabu s testy krevní kompatibility a metody mitigace interference Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé
INFLECTRA SCREENINGOVÝ LIST. a výběru pacientů pro všechny schválené indikace. Obsahuje pokyny ke správnému screeningu
 Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Demyelinizační poruchy U pacientů s preexistujícími nebo nedávno vzniklými demyelinizačními poruchami, je nutné pečlivě zvážit prospěch a riziko anti-tnf terapie před zahájením léčby přípravkem INFLECTRA
Sledování bezpečnosti v registeru. MUDr. Tomáš Moravec
 Sledování bezpečnosti v registeru MUDr. Tomáš Moravec Jaký je náš cíl v sledování bezpečnosti? naší snahou a cílem je ověření bezpečnostního profilu daného léčivého přípravku a získání nových informací
Sledování bezpečnosti v registeru MUDr. Tomáš Moravec Jaký je náš cíl v sledování bezpečnosti? naší snahou a cílem je ověření bezpečnostního profilu daného léčivého přípravku a získání nových informací
Trombocytopenie v těhotenství
 Trombocytopenie v těhotenství doc. MUDr. Antonín Pařízek, CSc. Gynekologicko-porodnická klinika 1. LF UK a VFN v Praze Definice normální počet trombocytů u netěhotných žen 150-400 x 10 9 /l v těhotenství
Trombocytopenie v těhotenství doc. MUDr. Antonín Pařízek, CSc. Gynekologicko-porodnická klinika 1. LF UK a VFN v Praze Definice normální počet trombocytů u netěhotných žen 150-400 x 10 9 /l v těhotenství
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím
 Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
Příloha III Dodatky k odpovídajícím částem souhrnu údajů o přípravku a příbalovým informacím Poznámka: Tyto změny příslušných bodů souhrnu údajů o přípravku a příbalové informace jsou výsledkem referralové
EDUKAČNÍ MATERIÁLY. TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM)
 EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
EDUKAČNÍ MATERIÁLY TRUVADA 200 mg / 245 mg POTAHOVANÉ TABLETY (EMTRICITABINUM/ TENOFOVIRUM DISOPROXILUM) DŮLEŽITÉ BEZPEČNOSTNÍ INFORMACE PRO PŘEDEPISUJÍCÍ LÉKAŘE týkající se užívání přípravku Truvada k
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizovaných zpráv o bezpečnosti (PSUR) jodidu-( 131 I) sodného
SOUHRN ÚDAJŮ O PŘÍPRAVKU. Předplněné injekční stříkačky o objemu 0,5 ml obsahují 20 000 IU (168,0 mikrogramů) epoetinu alfa
 SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU EPREX 40 000 IU/ml, injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Epoetinum alfa *..40 000 IU (336,0 mikrogramů v 1 ml) * produkovaný v ovariálních
SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU EPREX 40 000 IU/ml, injekční roztok 2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ Epoetinum alfa *..40 000 IU (336,0 mikrogramů v 1 ml) * produkovaný v ovariálních
Vývoj VZV vakcín. Chlíbek Roman Katedra epidemiologie Fakulta vojenského zdravotnictví UO Hradec Králové
 Vývoj VZV vakcín Ticháčkovy dny vojenských epidemiologů, 17.5. 2012 Chlíbek Roman Katedra epidemiologie Fakulta vojenského zdravotnictví UO Hradec Králové Herpes zoster (HZ) 1953 první izolace viru (Thomas
Vývoj VZV vakcín Ticháčkovy dny vojenských epidemiologů, 17.5. 2012 Chlíbek Roman Katedra epidemiologie Fakulta vojenského zdravotnictví UO Hradec Králové Herpes zoster (HZ) 1953 první izolace viru (Thomas
R A P I D EARLY ADMINISTRATION OF ACTIVATED FACTOR VII IN PATIENTS WITH SEVERE BLEEDING ZÁZNAM SUBJEKTU HODNOCENÍ (CRF) Číslo centra.
 R A P I D EARLY ADMINISTRATION OF ACTIVATED FACTOR VII IN PATIENTS WITH SEVERE BLEEDING ZÁZNAM SUBJEKTU HODNOCENÍ (CRF) Číslo centra Číslo pacienta Iniciály pacienta VÝBĚR A VYŘAZENÍ PACIENTŮ Kritéria
R A P I D EARLY ADMINISTRATION OF ACTIVATED FACTOR VII IN PATIENTS WITH SEVERE BLEEDING ZÁZNAM SUBJEKTU HODNOCENÍ (CRF) Číslo centra Číslo pacienta Iniciály pacienta VÝBĚR A VYŘAZENÍ PACIENTŮ Kritéria
Požadavky SÚKL k vytváření, obsahu a distribuci edukačních materiálů určených pro zdravotnické pracovníky a pacienty
 PHV-7 Požadavky SÚKL k vytváření, obsahu a distribuci edukačních materiálů určených pro zdravotnické pracovníky a pacienty Platnost od: 25.4.2014 Pokyn blíže vymezuje pojmy a upravuje podmínky poskytování
PHV-7 Požadavky SÚKL k vytváření, obsahu a distribuci edukačních materiálů určených pro zdravotnické pracovníky a pacienty Platnost od: 25.4.2014 Pokyn blíže vymezuje pojmy a upravuje podmínky poskytování
Pimobendan Randomized Occult DCM Trial to Evaluate
 Randomizovaná studie léčby okultní DCM pimobendanem s cílem vyhodnotit klinické příznaky a dobu do nástupu srdečního selhání Pimobendan Randomized Occult DCM Trial to Evaluate Clinical symptoms and Time
Randomizovaná studie léčby okultní DCM pimobendanem s cílem vyhodnotit klinické příznaky a dobu do nástupu srdečního selhání Pimobendan Randomized Occult DCM Trial to Evaluate Clinical symptoms and Time
Nemocniční výjimka pokyn UST-37
 1 Nemocniční výjimka pokyn UST-37 2 Právní rámec Zákon č. 378/2007 Sb., o léčivech a změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Vyhláška č. 228/2008 Sb., o
1 Nemocniční výjimka pokyn UST-37 2 Právní rámec Zákon č. 378/2007 Sb., o léčivech a změnách některých souvisejících zákonů (zákon o léčivech), ve znění pozdějších předpisů Vyhláška č. 228/2008 Sb., o
v kombinaci s dexamethasonem u dospělých, jejichž onemocnění bylo alespoň jednou v minulosti léčeno.
 EMA/113870/2017 EMEA/H/C/000717 Souhrn zprávy EPAR určený pro veřejnost lenalidomidum Tento dokument je souhrnem Evropské veřejné zprávy o hodnocení (European Public Assessment Report, EPAR) pro přípravek.
EMA/113870/2017 EMEA/H/C/000717 Souhrn zprávy EPAR určený pro veřejnost lenalidomidum Tento dokument je souhrnem Evropské veřejné zprávy o hodnocení (European Public Assessment Report, EPAR) pro přípravek.
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU
 PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp
PŘÍLOHA I SOUHRN ÚDAJŮ O PŘÍPRAVKU 1. NÁZEV PŘÍPRAVKU Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp
Pokyny k interpretaci spontánně hlášených případů podezření na nežádoucí účinky léčivých přípravků
 30. ledna 2017 Inspekce, farmakovigilance humánních a výbory EMA/749446/2016 Revize 1* Pokyny k interpretaci spontánně hlášených případů podezření na nežádoucí účinky Schválil Farmakovigilanční tým listopad
30. ledna 2017 Inspekce, farmakovigilance humánních a výbory EMA/749446/2016 Revize 1* Pokyny k interpretaci spontánně hlášených případů podezření na nežádoucí účinky Schválil Farmakovigilanční tým listopad
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy / aktualizovaných zpráv o bezpečnosti (PSUR)
CAVE! Informační dopis pro zdravotnické pracovníky
 CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
CAVE! Informační dopis pro zdravotnické pracovníky říjen 2017 Výpadek léčivého přípravku Trisenox (oxid arzenitý, koncentrát pro infuzní roztok 1 mg/ml): nahrazení léčivým přípravkem Phenasen (injekční
Rozdělení imunologických laboratorních metod
 Rozdělení imunologických laboratorních metod Aglutinace Mgr. Petr Bejdák Ústav klinické imunologie a alergologie Fakultní nemocnice u sv. Anny a Lékařská fakulta MU Rozdělení imunologických laboratorních
Rozdělení imunologických laboratorních metod Aglutinace Mgr. Petr Bejdák Ústav klinické imunologie a alergologie Fakultní nemocnice u sv. Anny a Lékařská fakulta MU Rozdělení imunologických laboratorních
ANÉMIE Emanuel Nečas 2014
 ANÉMIE Emanuel Nečas 2014 necas@cesnet.cz Sylabus přednášky Anémie 1 1. Co je anémie 2. Co způsobuje anémii 3. Anemický syndrom 4. Klasifikace anémií 4. Shrnutí podstatných informací 1. Co je anémie? Anémie
ANÉMIE Emanuel Nečas 2014 necas@cesnet.cz Sylabus přednášky Anémie 1 1. Co je anémie 2. Co způsobuje anémii 3. Anemický syndrom 4. Klasifikace anémií 4. Shrnutí podstatných informací 1. Co je anémie? Anémie
von Willebrandova choroba Mgr. Jaroslava Machálková
 von Willebrandova choroba Mgr. Jaroslava Machálková von Willebrandova choroba -je dědičná krvácivá choroba způsobená vrozeným kvantitativním či kvalitativním defektem von Willebrandova faktoru postihuje
von Willebrandova choroba Mgr. Jaroslava Machálková von Willebrandova choroba -je dědičná krvácivá choroba způsobená vrozeným kvantitativním či kvalitativním defektem von Willebrandova faktoru postihuje
Příloha IV. Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci
 Příloha IV Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 132 Vědecké závěry Výbor CHMP zvážil níže uvedené doporučení výboru PRAC ze dne 5. prosince 2013 s ohledem na postup podle
Příloha IV Vědecké závěry a zdůvodnění změny podmínek rozhodnutí o registraci 132 Vědecké závěry Výbor CHMP zvážil níže uvedené doporučení výboru PRAC ze dne 5. prosince 2013 s ohledem na postup podle
Program na podporu zdravotnického aplikovaného výzkumu na léta 2015 2022
 Program na podporu zdravotnického aplikovaného výzkumu na léta 2015 2022 Ukončení příjmů projektů: 30. 6. 2015 Délka trvání řešení projektů: 45 měsíců Místo realizace: Celá ČR Oblast působení: Výzkum a
Program na podporu zdravotnického aplikovaného výzkumu na léta 2015 2022 Ukončení příjmů projektů: 30. 6. 2015 Délka trvání řešení projektů: 45 měsíců Místo realizace: Celá ČR Oblast působení: Výzkum a
Edukační materiály DHPC
 Edukační materiály/dhpc Edukační materiály DHPC STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Seminář oddělení farmakovigilance červen 2014 Lucie Skálová MVDr. Edukační materiály -úvod 2 EDUKAČNÍ MATERIÁLY Požadavky
Edukační materiály/dhpc Edukační materiály DHPC STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV Seminář oddělení farmakovigilance červen 2014 Lucie Skálová MVDr. Edukační materiály -úvod 2 EDUKAČNÍ MATERIÁLY Požadavky
BJA Eur J Anaesthesiol 2013
 BJA 2012 Eur J Anaesthesiol 2013 Lze snížit množství podaných trf? Optimalizace zdravotního stavu před výkonem Chirurgické a anesteziologické postupy vedoucí ke snížení krevní ztráty peroperačně Snížení
BJA 2012 Eur J Anaesthesiol 2013 Lze snížit množství podaných trf? Optimalizace zdravotního stavu před výkonem Chirurgické a anesteziologické postupy vedoucí ke snížení krevní ztráty peroperačně Snížení
Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům
 15 September 2016 EMA/PRAC/603546/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům Přijato na zasedání výboru PRAC konaném
15 September 2016 EMA/PRAC/603546/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nové znění informací o přípravku výňatky z doporučení výboru PRAC k signálům Přijato na zasedání výboru PRAC konaném
2016 STÁTNÍ ÚSTAV PRO KONTROLU LÉČIV
 1 2 NEINTERVENČNÍ POREGISTRAČNÍ STUDIE MONITOROVÁNÍ, POSUZOVACÍ PRAXE Mgr. Natália Svršková Velký sál SÚKL 3 Obsah Neintervenční poregistrační studie definice, monitorování Neintervenční poregistrační
1 2 NEINTERVENČNÍ POREGISTRAČNÍ STUDIE MONITOROVÁNÍ, POSUZOVACÍ PRAXE Mgr. Natália Svršková Velký sál SÚKL 3 Obsah Neintervenční poregistrační studie definice, monitorování Neintervenční poregistrační
Erytrocyty. Hemoglobin. Krevní skupiny a Rh faktor. Krevní transfúze. Somatologie Mgr. Naděžda Procházková
 Erytrocyty. Hemoglobin. Krevní skupiny a Rh faktor. Krevní transfúze. Somatologie Mgr. Naděžda Procházková Formované krevní elementy: Buněčné erytrocyty, leukocyty Nebuněčné trombocyty Tvorba krevních
Erytrocyty. Hemoglobin. Krevní skupiny a Rh faktor. Krevní transfúze. Somatologie Mgr. Naděžda Procházková Formované krevní elementy: Buněčné erytrocyty, leukocyty Nebuněčné trombocyty Tvorba krevních
Nové léčebné možnosti v léčbě mnohočetného myelomu GROUP. Roman Hájek 3.9.2005. Lednice
 Nové léčebné možnosti v léčbě mnohočetného myelomu CZECH CMG M Y E L O M A GROUP ČESKÁ MYELOMOVÁ SKUPINA ČESKÁ MYELOMOVÁ SKUPINA CZECH CMG M Y E L O M A NADAČNÍ FOND GROUP Roman Hájek 3.9.2005 Lednice
Nové léčebné možnosti v léčbě mnohočetného myelomu CZECH CMG M Y E L O M A GROUP ČESKÁ MYELOMOVÁ SKUPINA ČESKÁ MYELOMOVÁ SKUPINA CZECH CMG M Y E L O M A NADAČNÍ FOND GROUP Roman Hájek 3.9.2005 Lednice
Aglutinace Mgr. Jana Nechvátalová
 Aglutinace Mgr. Jana Nechvátalová Ústav klinické imunologie a alergologie FN u sv. Anny v Brně Aglutinace x precipitace Aglutinace Ag + Ab Ag-Ab aglutinogen aglutinin aglutinát makromolekulární korpuskulární
Aglutinace Mgr. Jana Nechvátalová Ústav klinické imunologie a alergologie FN u sv. Anny v Brně Aglutinace x precipitace Aglutinace Ag + Ab Ag-Ab aglutinogen aglutinin aglutinát makromolekulární korpuskulární
ŽIVOTNÍ CYKLUS LÉKŮ KLINICKÉ HODNOCENÍ STUDIE. Kateřina Kopečková FN Motol, Praha
 ŽIVOTNÍ CYKLUS LÉKŮ KLINICKÉ HODNOCENÍ STUDIE Kateřina Kopečková FN Motol, Praha Klinická hodnocení LP Nedílnou součásti vývoje léčiva Navazují na preklinický výzkum Pacienti jsou subjekty hodnocení V
ŽIVOTNÍ CYKLUS LÉKŮ KLINICKÉ HODNOCENÍ STUDIE Kateřina Kopečková FN Motol, Praha Klinická hodnocení LP Nedílnou součásti vývoje léčiva Navazují na preklinický výzkum Pacienti jsou subjekty hodnocení V
Výsledky vyšetření krve. Vítejte na našem dialyzačním středisku
 Výsledky vyšetření krve Vítejte na našem dialyzačním středisku Proč tak často kontrolujete mou krev? Každý měsíc Vám odebíráme vzorky krve, abychom zjistili, zda je pravidelná dialýza dostatečně účinná.
Výsledky vyšetření krve Vítejte na našem dialyzačním středisku Proč tak často kontrolujete mou krev? Každý měsíc Vám odebíráme vzorky krve, abychom zjistili, zda je pravidelná dialýza dostatečně účinná.
Edukační materiály VICTRELIS. boceprevir EDUKAČNÍ KARTA PRO LÉKAŘE
 Edukační materiály VICTRELIS boceprevir EDUKAČNÍ KARTA PRO LÉKAŘE Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky,
Edukační materiály VICTRELIS boceprevir EDUKAČNÍ KARTA PRO LÉKAŘE Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky,
NEINTERVENČNÍ POREGISTRAČNÍ STUDIE BEZPEČNOSTI
 1 NEINTERVENČNÍ POREGISTRAČNÍ STUDIE BEZPEČNOSTI Radim Tobolka 2 Obsah prezentace Typy studií Registry studií Hlášení nežádoucích účinků Studijní a návazná dokumentace Etika neintervenčního výzkumu Seznam
1 NEINTERVENČNÍ POREGISTRAČNÍ STUDIE BEZPEČNOSTI Radim Tobolka 2 Obsah prezentace Typy studií Registry studií Hlášení nežádoucích účinků Studijní a návazná dokumentace Etika neintervenčního výzkumu Seznam
AKUTNÍM SELHÁNÍM LEDVIN
 Co by měl mladý intenzivista vědět při péči o pacienta s AKUTNÍM SELHÁNÍM LEDVIN Jan Horák I. interní klinika FN Plzeň Biomedicínské Centrum LF v Plzni Definice AKI soubor syndromů, pro které je typický
Co by měl mladý intenzivista vědět při péči o pacienta s AKUTNÍM SELHÁNÍM LEDVIN Jan Horák I. interní klinika FN Plzeň Biomedicínské Centrum LF v Plzni Definice AKI soubor syndromů, pro které je typický
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE. Poznámka: Tyto úpravy souhrnu údajů o přípravku a
 PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
PŘÍLOHA III RELEVANTNÍ ČÁSTI SOUHRNU ÚDAJŮ O PŘÍPRAVKU A PŘÍBALOVÉ INFORMACE Poznámka: Tyto úpravy souhrnu údajů o přípravku a příbalové informace jsou platné v okamžiku přijetí rozhodnutí Komisí. Poté,
Urychlení úpravy krvetvorby poškozené cytostatickou terapií (5-fluorouracil a cisplatina) p.o. aplikací IMUNORu
 Urychlení úpravy krvetvorby poškozené cytostatickou terapií (5-fluorouracil a cisplatina) p.o. aplikací IMUNORu Úvod Myelosuprese (poškození krvetvorby) patří mezi nejčastější vedlejší účinky chemoterapie.
Urychlení úpravy krvetvorby poškozené cytostatickou terapií (5-fluorouracil a cisplatina) p.o. aplikací IMUNORu Úvod Myelosuprese (poškození krvetvorby) patří mezi nejčastější vedlejší účinky chemoterapie.
Chronická myeloproliferativní onemocnění. L. Bourková, OKH FN Brno
 Chronická myeloproliferativní onemocnění L. Bourková, OKH FN Brno Chronická myeloproliferativní onemocnění Chronická myeloidní leukémie (CML) s t(9;22), gen BCR/ABL pozitivní (Chronická granulocytární
Chronická myeloproliferativní onemocnění L. Bourková, OKH FN Brno Chronická myeloproliferativní onemocnění Chronická myeloidní leukémie (CML) s t(9;22), gen BCR/ABL pozitivní (Chronická granulocytární
3. Výdaje zdravotních pojišťoven
 3. Výdaje zdravotních pojišťoven Náklady sedmi zdravotních pojišťoven, které působí v současné době v České republice, tvořily v roce 2013 více než tři čtvrtiny všech výdajů na zdravotní péči. Z pohledu
3. Výdaje zdravotních pojišťoven Náklady sedmi zdravotních pojišťoven, které působí v současné době v České republice, tvořily v roce 2013 více než tři čtvrtiny všech výdajů na zdravotní péči. Z pohledu
Doporučení Farmakovigilančního výboru pro posuzování rizik léčiv (PRAC) k signálům pro aktualizaci informací o přípravku
 22. ledna 2015 EMA/PRAC/63322/2015 Farmakovigilanční výbor pro posuzování rizik léčiv Doporučení Farmakovigilančního výboru pro posuzování rizik léčiv (PRAC) k signálům pro aktualizaci informací o přípravku
22. ledna 2015 EMA/PRAC/63322/2015 Farmakovigilanční výbor pro posuzování rizik léčiv Doporučení Farmakovigilančního výboru pro posuzování rizik léčiv (PRAC) k signálům pro aktualizaci informací o přípravku
Příloha I. Vědecké závěry a zdůvodnění změny v registraci
 Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
Příloha I Vědecké závěry a zdůvodnění změny v registraci 1 Vědecké závěry S ohledem na hodnotící zprávu výboru PRAC týkající se pravidelně aktualizované zprávy/aktualizovaných zpráv o bezpečnosti (PSUR)
